FORMULACIÓN QUÍMICA INORGÁNICA
|
|
|
- María Villalobos Carrizo
- hace 7 años
- Vistas:
Transcripción
1 FORMULACIÓN QUÍMICA INORGÁNICA INTRODUCCIÓN. Las fórmulas representan a los compuestos químicos y constan de una agrupación de símbolos afectados de unos subíndices que nos indican la proporción en que combinan los elementos que constituyen el compuesto. La capacidad de los elementos para combinarse entre sí y formar compuestos se expresa mediante un número denominado valencia. Al hidrógeno se le asigna una valencia igual a 1. Los símbolos y las valencias de los elementos más importantes aparecen en tabla adjunta. Al formular un compuesto se coloca en primer lugar el símbolo del elemento con más carácter metálico y a continuación el elemento o grupo de elementos con menor carácter metálico. Para indicar el número de elementos o grupo de elementos, que forman parte del compuesto, en la fórmula, se utilizan números que se escriben como subíndices en la parte derecha del elemento o del grupo. Si se trata de un grupo de elementos que aparece en número superior a uno, debe encerrarse a todo el grupo entre paréntesis. Ejemplos: MgCl 2 CuSO 4 Ca(OH) 2 La nomenclatura, es la forma de nombrarlos. Es especial en cada clase de sustancia, por lo que estudiaremos caso por caso. Las nomenclaturas más utilizadas son tres: La nomenclatura sistemática, la nomenclatura de Stock y la tradicional. COMPUESTOS BINARIOS. Los compuestos binarios resultan de la combinación de dos elementos distintos. Existen varios tipos de compuestos binarios, los más importantes: Óxidos básicos. Son combinaciones binarias de un metal con el oxígeno, en las que el oxígeno actúa con valencia 2. Formulación: Se formulan colocando en primer lugar el metal y a continuación el oxígeno, colocando los subíndices que indican los prefijos (nomenclatura sistemática). En el caso de la nomenclatura de Stock y clásica, se intercambian las valencias y se simplifica siempre que sea posible. Nomenclatura: Para nombrar estos compuestos según el tipo de nomenclatura. 1
2 1.- Nomenclatura sistemática Esta nomenclatura nos indica la proporción en la que se encuentran los elementos en el compuesto mediante prefijos griegos: mono-: uno; di-: dos; tri-: tres; tetra-, cuatro; penta-, cinco; hexa-, seis y hepta-, siete. 2.- Nomenclatura de Stock En esta nomenclatura nos indica la valencia del elemento en números romanos y entre paréntesis inmediatamente después del nombre. Para los óxidos se antepone la palabra óxido y a continuación la partícula de, seguida del nombre del metal y su valencia. Si el metal tienen una única valencia no es preciso indicarla en números romanos. 3.- Nomenclatura tradicional En la tradicional, coloca sufijos oso e ico al nombre del metal, cuando tiene dos valencias, indicando oso la menor de ellas; ico la mayor. Si el metal tiene una única valencia se nombra como óxido seguido del nombre del metal en genitivo. Ejemplos: N. sistemática N.Stock N.tradicional FeO monóxido de hierro óxido de hierro (II) óxido ferroso Fe 2 O 3 trióxido de dihierro óxido de hierro (III) óxido férrico. Cu 2 O...monóxido de dicobre óxido de cobre (I) óxido cuproso CuO monóxido de monocobre óxido de cobre (II) óxido cúprico ÓXIDOS ÁCIDOS ó ANHÍDRIDOS. Son combinaciones binarias de un no metal con el oxígeno, en las que el oxígeno actúa con su valencia 2 y el no metal con su valencia correspondiente. Formulación: Se siguen las mismas reglas que en los óxidos básicos, en cada una de las nomenclaturas. Nomenclaturas: En las nomenclaturas sistemáticas y de Stock se siguen las mismas normas que para los óxidos básicos. En la tradicional se siguen también las mismas normas que en los básicos, salvo que no se nombrarían como óxidos sino como anhídridos. Además en estos compuestos el no metal puede tener 4, 3 ó 2 valencias. -Cuando el no metal tiene 4 valencias: Se usan los siguientes prefijos y sufijos: -hipo...oso, cuando el no metal actúa con la menor de las valencias. -...oso, cuando actúa con la siguiente valencia menor. -...ico, para la tercera. -per...ico, para la mayor de todas las valencias. 2
3 -Cuando el no metal tiene 3 valencias, salvo algunas excepciones, se empieza por hipo...oso, para la menor de las valencias, e...ico para la mayor, utilizándose...oso, para la valencia intermedia. -Cuando el no metal tiene 2 valencias, se usa...ico, para la mayor y...oso para la menor. -Cuando sólo tiene una valencia, se nombra como anhídrido del no metal correspondiente, o la terminación...ico. Ejemplos: N. sistemática N. Stock N. Tradicional N 2 O 5 pentaóxido de dinitrógeno...óxido de nitrógeno(v) anhídrido nítrico SO 2 dióxido de azufre.óxido de azufre(iv) anhídrido sulfuroso SO monóxido de azufre óxido de azufre (II) anhídrido hiposulfuroso. PERÓXIDOS. Resultan de la combinación de un metal con el grupo peroxi O 2. En estos compuestos el metal sólo puede tener valencia 1 o 2. Formulación: Se coloca en primer lugar el metal y a continuación el grupo peroxi. Si el metal (M) tiene valencia 1, el peróxido formado es del tipo M 2 O 2, y no se simplifica. Si tiene valencia 2 el peróxido formado es MO 2 Nomenclatura: Se antepone la palabra peróxido seguida del nombre del metal en genitivo, en las nomenclaturas de Stock y tradicional. En la sistemática se siguen las misma reglas que en los óxidos. Ejemplo: Na 2 O 2 peróxido de sódio, también peróxido sódico ó dióxido de disodio. BaO 2 peróxido de bario, peróxido de bario (II), dióxido de bario. HIDRUROS Resultan de la combinación del hidrógeno con otro elemento. HIDRUROS METÁLICOS. Combinación de un metal con el hidrógeno. Formulación: Se coloca el símbolo del metal y a continuación el del hidrógeno, colocándole como subíndice la valencia del metal. Nomenclatura: Se nombra con la palabra hidruro seguida del nombre del metal, utilizando las normas específicas de cada una de las tres nomenclaturas. Ejemplos: LiH N. sistemática: monohidruro de Litio; hidruro de Litio. N. Stock: hidruro de Litio (I); hidruro de Litio. N. tradicional: hidruro de Litio. 3
4 FeH 3 N. sistemática: trihidruro de hierro N. stock: hidruro de hierro (III) N.tradicional: hidruro férrico. HIDRUROS NO METÁLICOS. Combinación de un no metal con el hidrógeno. Formulación y Nomenclatura: Distinguiremos entre los hidruros formados por los elementos no metálicos de los grupos 14, 15 y 16, 17. En los hidruros no metálicos, los no metales actúan con las siguientes valencias: Los elementos del grupo 14 (C, Si, Ge), valencia 4; los del 15(N, P, As y Sb), valencia 3; los del 16(S, Se y Te), valencia 2 y los del 17 (F,Cl, Br, y I) valencia 1 Para los elementos de los grupos 14 y 15, se siguen las mismas normas que en los metálicos, si bien hay que hacer notar que la mayor parte de estos compuestos tienen nombre propio. CH 4 metano; SiH 4 silano; NH 3 amoniaco PH 3 fosfina. AsH 3 arsina; SbH 3 estibina. Para los elementos de los grupos 16 y 17 del sistema periódico, el hidrógeno ocupa el lugar más a la izquierda, escribiendo el elemento no metálico a su derecha. Se nombran terminando en uro, el nombre del no metal añadiendo a continuación la palabra de hidrógeno. Otra terminología de estos compuestos se nombran como ácidos, seguidos del nombre del no metal terminado en hídrico. Ejemplos: Grupo 16 H 2 S sulfuro de hidrógeno; ácido sulfhídrico. H 2 Se seleniuro de hidrógeno; ácido selenhídrico. H 2 Te telururo de hidrógeno, ácido telurhídrico. Grupo 17 HF fluoruro de hidrógeno; ácido fluorhídrico. HCl cloruro de hidrógeno; ácido clorhídrico. HBr bromuro de hidrógeno; ácido bromhídrico. HI yoduro de hidrógeno; ácido yodhídrico. SALES BINARIAS. SALES NEUTRAS. Son combinaciones de no metales y metales, el no metal se coloca a la derecha nombrándose con sufijo uro, según indicamos a continuación. En estos compuestos se recomienda la nomenclatura de stock Fórmula N. sistemática N. de stock Nomenclatura tradicional LiF Fluoruro de Litio Fluoruro de litio Fluoruro de litio CaF 2 Difluoruro de calcio fluoruro de calcio(ii) fluoruro de calcio FeCl 3 tricloruro de hierro cloruro de hierro(iii) cloruro férrico Al 2 S 3 trisulfuro de dialuminio sulfuro de aluminio(iii) sulfuro alumínico Mn 2 S 3 trisulfuro de dimanganeso sulfuro de manganeso(iii) sulfuro mangánico MnS monosulfuro de manganeso sulfuro de manganeso(ii) sulfuro manganoso CuBr 2 dibromuro de monocobre bromuro de cobre (II) bromuro cúprico 4
5 Las valencias del no metal son las mismas que las indicadas en los hidruros no metálicos. SALES VOLÁTILES: Son combinaciones de no metales con no metales. Se coloca en primer lugar el elemento que tiene más carácter metálico y a continuación el menos metálico terminado en uro. Sólo se utilizan las nomenclaturas sistemática y de stock. Ejemplos: BrF 3 Trifluoruro de bromo fluoruro de bromo(iii). CCl 4 tetracloruro de carbono cloruro de carbono (IV) CS 2 disulfuro de carbono sulfuro de carbono(iv) PCl 5 pentacloruro de fósforo cloruro de fósforo(v) PCl 3 tricloruro de fósforo cloruro de fósforo(iii) IF 7 heptafluoruro de yodo fluoruro de yodo (VII) COMPUESTOS TERNARIOS: Los compuestos ternarios son aquellos que constan de tres elementos distintos. HIDRÓXIDOS O BASES: Resultan de la combinación de un metal con su valencia y el grupo hidroxilo (OH - ). Formulación: se coloca en primer lugar el metal y a continuación tantos grupos OH encerrados entre paréntesis como sea la valencia del metal. Si la valencia es 1, no se utilizan los paréntesis. Nomenclatura: se nombra con la palabra genérica hidróxido, siguiendo las normas de las tres nomenclaturas. Fórmula Nomenclatura sistemática N. de stock N. tradicional Fe(OH) 2 dihidróxido de hierro hidróxido de hierro(ii) hidróxido ferroso Pb(OH) 4 tetrahidróxido de plomo hidróxido de plomo(iv) hidróxido plúmbico NaOH hidróxido de sodio hidróxido de sodio sosa ÁCIDOS OXÁCIDOS U OXOÁCIDOS. Los oxoácidos son compuestos formados por oxígeno, hidrógeno y no metales, la fórmula genérica es: H x A y O z ; donde A representa, en general, un no metal. También puede ser un metal de transición que actúa con valencia elevada, como el cromo, manganeso, molibdeno, vanadio, etc. Formulación: La formulación se hace a partir de los correspondientes aniones (especies químicas con un exceso de cargas negativas). Para nombrar los aniones se utilizan las terminaciones ito y ato para la menor y mayor valencia del no metal y los prefijos hipo y per en el caso de no metales con cuatro valencias. La valencia del no metal se considera positiva y el oxígeno actúa con valencia 2. Se conocen tres tipos de aniones: 5
6 -Aniones meta : Resultan de añadir al no metal el número mínimo de oxígenos necesarios para que el conjunto resulte negativo. Ejemplos: Ion hipoclorito Cl + O ClO - Ion sulfito S 4+ O 3 SO 3 Ion permanganato Mn 7+ - O 4 MnO 4 -Aniones di, tri, tetra, etc.: El prefijo nos indica el número de átomos del no metal que debe contener el ion y en lo demás se sigue la regla de los iones meta. Ion disulfato S 6+ 2 O 7 S 2 O 7 Ion trisilicato Si 4+ 3 O 7 Si 3 O 7 Ion dicromato Cr 6+ 2 O 7 Cr 2 O 7 -Aniones orto : Resultan de añadir al no metal un oxígeno más de los necesarios en los aniones meta En el caso del P, As y Sb, si no se especifica ningún prefijo el anión se supone orto, en vez de meta. Los aniones meta de estos tres elementos hay que añadir el prefijo meta al nombre del anion. Ion ortosilicato Si 4+ O 3+1 Ion fosfato P 5+ O SiO 4 3- PO 4 -Aniones piro : Son ortodi Ion pirofosfato o ortodifosfato o difosfato P 2 5+ O 7 P 2 O Una vez formulado el anión, el ácido resulta de sustituir la carga negativa del anión con hidrógeno. La nomenclatura utiliza los prefijos y sufijos hipo...oso ;... oso,... ico y per...ico. En la fórmula, el hidrógeno se escribe en primer lugar. HClO ácido hipocloroso H 2 SO 3 ácido sulfuroso H 2 S 2 O 7 ácido disulfúrico H 2 Si 3 O 7 ácido trisilícico HMnO 4 ácido permangánico H 4 SiO 4 ácido ortosilícico. SALES NEUTRAS U OXISALES Son compuestos formados por metal, no metal y oxígeno. B x A y O z ; B es un metal y A un no metal. Formulación: Se formula en primer lugar el correspondiente anión. El metal actúa con su valencia e intercambian sus valencias, simplificando siempre que sea posible. Se coloca siempre en primer lugar el metal. Nomenclatura: Se nombra el anion seguido del nombre del metal terminado en oso o ico, o bien se usa la nomenclatura de stock. Fe 2 (CO 3 ) 3 carbonato férrico; carbonato de hierro (III). 6
7 KMnO 4 permanganato potásico; permanganato de potasio. Ni 4 (P 2 O 7 ) 3 pirofosfato niquélico; difosfato de níquel (III); ortodifosfato de níquel (III). SALES ÁCIDAS: Resultan de la sustitución parcial de hidrógenos por metales en oxácido, o en un ácido hidrácido. Formulación: Se formula el anión correspondiente, a continuación el o los hidrógenos que se indican y se enfrenta al metal con su valencia, intercambiando y simplificando siempre que sea posible. CO 3 HCO 3 - KHCO 3 (sal ácida). Nomenclatura: Se antepone al nombre de la sal neutra la palabra hidrógeno, con un prefijo numérico que nos indique los hidrógenos que posee la sal. También se sigue al nombre de la sal la palabra ácido, con un prefijo numérico que nos indique los hidrógenos que posee la sal. NaHSO 4 hidrógenosulfato sódico; hidrógenosulfato de sodio; sulfato ácido de sodio. Fe(HSO 4 ) 2 hidrógeno sulfato de hierro (II); sulfato ácido ferroso. KH 2 PO 4 dihidrógeno fosfato de potasio; fosfato diácido de potasio. KHS hidrógenosulfuro de potasio; sulfuro ácido de potasio. 7
FORMULACIÓN Y NOMENCLATURA
 FORMULACIÓN Y NOMENCLATURA 0. Introducción. Existen tres tipos de nomenclaturas que nos permiten nombrar los compuestos químicos inorgánicos: A. Nomenclatura Sistemática (normas propuestas por la Unión
FORMULACIÓN Y NOMENCLATURA 0. Introducción. Existen tres tipos de nomenclaturas que nos permiten nombrar los compuestos químicos inorgánicos: A. Nomenclatura Sistemática (normas propuestas por la Unión
Trióxido de dihierro
 OXIDOS = Elemento - Oxígeno No metal (1) + Oxígeno = Óxido no metálico CO 2 ; SO 3 ; N 2 O 5 ; CO ; SO 2 ; NO 2 (1) excepto halógenos X no m Metal + Oxígeno = Óxido metálico Fe 2 O 3 ; Li 2 O ; CaO ; Ag
OXIDOS = Elemento - Oxígeno No metal (1) + Oxígeno = Óxido no metálico CO 2 ; SO 3 ; N 2 O 5 ; CO ; SO 2 ; NO 2 (1) excepto halógenos X no m Metal + Oxígeno = Óxido metálico Fe 2 O 3 ; Li 2 O ; CaO ; Ag
NOMENCLATURA y FORMULACIÓN en QUÍMICA INORGÁNICA. Nivel: Educación Secundaria Obligatoria
 NOMENCLATURA y FORMULACIÓN en QUÍMICA INORGÁNICA Nivel: Educación Secundaria Obligatoria Conceptos básicos Los elementos químicos se representan mediante símbolos, que consisten en una o dos letras que
NOMENCLATURA y FORMULACIÓN en QUÍMICA INORGÁNICA Nivel: Educación Secundaria Obligatoria Conceptos básicos Los elementos químicos se representan mediante símbolos, que consisten en una o dos letras que
Son compuestos binarios, resultan de la combinación de un metal más el oxígeno. Metal + Oxígeno =
 FUNCIÓN ÓXIDO BASICO U ÓXIDO Son compuestos binarios, resultan de la combinación de un metal más el oxígeno. Metal + Oxígeno = óxido NOMENCLATURA CLASICA.-Se nombra de acuerdo a: Primer caso: El no metal
FUNCIÓN ÓXIDO BASICO U ÓXIDO Son compuestos binarios, resultan de la combinación de un metal más el oxígeno. Metal + Oxígeno = óxido NOMENCLATURA CLASICA.-Se nombra de acuerdo a: Primer caso: El no metal
Indique el número de óxidos básicos y óxidos ácidos respectivamente en la siguiente tabla:
 EJERCICIO RESUELTO Ejercicio 1: Indique el número de óxidos básicos y óxidos ácidos respectivamente en la siguiente tabla: a) Fe 2 O 3 b) CO c) SO 3 d) CuO e) NO 2 f) Na 2 O g) MgO Solución: Comenzaremos
EJERCICIO RESUELTO Ejercicio 1: Indique el número de óxidos básicos y óxidos ácidos respectivamente en la siguiente tabla: a) Fe 2 O 3 b) CO c) SO 3 d) CuO e) NO 2 f) Na 2 O g) MgO Solución: Comenzaremos
TABLA PERIÓDICA Y FORMULACIÓN 4º ESO
 HIDRUROS Son combinaciones binarias de H con otro elemento (no metal o metal). La valencia del H es siempre 1. Hidruros no metálicos Hay que tener en cuenta la tabla de electronegatividad: B < Si < C
HIDRUROS Son combinaciones binarias de H con otro elemento (no metal o metal). La valencia del H es siempre 1. Hidruros no metálicos Hay que tener en cuenta la tabla de electronegatividad: B < Si < C
EJERCICIOS DE FORMULACIÓN Y NOMENCLATURA DE QUÍMICA INORGÁNICA 3º ESO
 EJERCICIOS DE FORMULACIÓN Y NOMENCLATURA DE QUÍMICA INORGÁNICA 3º ESO 1 COMPUESTOS BINARIOS 1.1 CON OXÍGENO 1.1.1 Y UN METAL (ÓXIDOS METÁLICOS) 1 BaO Monóxido de bario Óxido de bario 2 Na 2 O Monóxido
EJERCICIOS DE FORMULACIÓN Y NOMENCLATURA DE QUÍMICA INORGÁNICA 3º ESO 1 COMPUESTOS BINARIOS 1.1 CON OXÍGENO 1.1.1 Y UN METAL (ÓXIDOS METÁLICOS) 1 BaO Monóxido de bario Óxido de bario 2 Na 2 O Monóxido
- Nomenclatura tradicional. Hoy está totalmente en desuso, pero es necesario conocerla para poder formular oxiácidos. La posibilidad de que un mismo
 NORMAS BÁSICAS SOBRE FORMULACIÓN - Se escribe siempre en primer lugar el símbolo del elemento (o grupo) que actúa con número de oxidación positivo, generalmente un metal y a continuación el símbolo del
NORMAS BÁSICAS SOBRE FORMULACIÓN - Se escribe siempre en primer lugar el símbolo del elemento (o grupo) que actúa con número de oxidación positivo, generalmente un metal y a continuación el símbolo del
1.- CONCEPTOS PREVIOS
 TEMA 4: FORMULACIÓN 1.- CONCEPTOS PREVIOS Compuesto químico: es la unión de varios átomos que no pueden separarse por procedimientos físicos pero sí mediante procedimientos químicos. Ejemplo: dos átomos
TEMA 4: FORMULACIÓN 1.- CONCEPTOS PREVIOS Compuesto químico: es la unión de varios átomos que no pueden separarse por procedimientos físicos pero sí mediante procedimientos químicos. Ejemplo: dos átomos
H, Li, Na, K, Rb, Cs, Fr 1. Be, Mg, Ca, Sr, Ba, Ra, Zn, Cd 2. B, Al 3. N, P, As, Sb 1, 3, 5. F, Cl, Br, I 1, 3, 5, 7. C, Si, Ge, Sn, Pb 2, 4 O 2
 H, Li, Na, K, Rb, Cs, Fr 1 Be, Mg, Ca, Sr, Ba, Ra, Zn, Cd 2 B, Al 3 N, P, As, Sb 1, 3, 5 F, Cl, Br, I 1, 3, 5, 7 C, Si, Ge, Sn, Pb 2, 4 O 2 S, Se, Te 2, 4, 6 Cr 2, 3, 3, 6 Mn 2, 3, 4, 6, 7 Fe, Co, Ni 2,
H, Li, Na, K, Rb, Cs, Fr 1 Be, Mg, Ca, Sr, Ba, Ra, Zn, Cd 2 B, Al 3 N, P, As, Sb 1, 3, 5 F, Cl, Br, I 1, 3, 5, 7 C, Si, Ge, Sn, Pb 2, 4 O 2 S, Se, Te 2, 4, 6 Cr 2, 3, 3, 6 Mn 2, 3, 4, 6, 7 Fe, Co, Ni 2,
EJERCICIOS DE FORMULACIÓN QUÍMICA INORGÁNICA
 EJERCICIOS DE FORMULACIÓN QUÍMICA INORGÁNICA COMPUESTOS BINARIOS DEL OXÍGENO 1.- Cl 2 O 7 2.- FeO 3.- N 2 O 4.- SO 3 1.- NOMBRA LOS SIGUIENTES COMPUESTOS: 6.- Br 2 O 7.- P 2 O 5 8.- CO 2 9.- I 2 O 5 5.-
EJERCICIOS DE FORMULACIÓN QUÍMICA INORGÁNICA COMPUESTOS BINARIOS DEL OXÍGENO 1.- Cl 2 O 7 2.- FeO 3.- N 2 O 4.- SO 3 1.- NOMBRA LOS SIGUIENTES COMPUESTOS: 6.- Br 2 O 7.- P 2 O 5 8.- CO 2 9.- I 2 O 5 5.-
REPASO DE FORMULACIÓN INORGÁNICA
 REPASO DE FORMULACIÓN INORGÁNICA 1. Cl 2 O 7 2. FeO 3. N 2 O 4. SO 3 5. Cr 2 O 3 6. Br 2 O 7. P 2 O 5 8. CO 2 9. I 2 O 5 10. MnO 2 11. Trióxido de dicromo 12. Óxido de nitrógeno (V) 13. Heptaóxido de dicloro
REPASO DE FORMULACIÓN INORGÁNICA 1. Cl 2 O 7 2. FeO 3. N 2 O 4. SO 3 5. Cr 2 O 3 6. Br 2 O 7. P 2 O 5 8. CO 2 9. I 2 O 5 10. MnO 2 11. Trióxido de dicromo 12. Óxido de nitrógeno (V) 13. Heptaóxido de dicloro
NOMENCLATURA Y FORMULACIÓN DE QUÍMICA INORGÁNICA. Física y Química 3º de E.S.O. IES Isidra de Guzmán
 NOMENCLATURA Y FORMULACIÓN DE QUÍMICA INORGÁNICA Física y Química 3º de E.S.O. IES Isidra de Guzmán INTRODUCCIÓN La IUPAC ( Unión Internacional de Química Pura y Aplicada) es el organismo que coordina
NOMENCLATURA Y FORMULACIÓN DE QUÍMICA INORGÁNICA Física y Química 3º de E.S.O. IES Isidra de Guzmán INTRODUCCIÓN La IUPAC ( Unión Internacional de Química Pura y Aplicada) es el organismo que coordina
Óxido de hierro(iii)
 ÓXIDOS Los óxidos son combinaciones de los elementos con el oxígeno. El nombre de estos compuestos siempre incluye la palabra óxido que puede estar precedida de prefijos numerales indicadores del número
ÓXIDOS Los óxidos son combinaciones de los elementos con el oxígeno. El nombre de estos compuestos siempre incluye la palabra óxido que puede estar precedida de prefijos numerales indicadores del número
1 FORMULACIÓN Y NOMENCLATURA QUÍMICA INORGÁNICA
 1 FRMULACIÓN Y NMENCLATURA QUÍMICA INRGÁNICA I 1 ELEMENTS Un elemento químico es la clase de átomos que tienen el mismo número atómico. Existen hasta 109 elementos químicos con los que se forma toda la
1 FRMULACIÓN Y NMENCLATURA QUÍMICA INRGÁNICA I 1 ELEMENTS Un elemento químico es la clase de átomos que tienen el mismo número atómico. Existen hasta 109 elementos químicos con los que se forma toda la
FORMULACIÓN INORGÁNICA
 FORMULACIÓN INORGÁNICA 1. Elementos Químicos. 2. Valencia. 3. Combinaciones binarias del Oxígeno: Óxidos 4. Combinaciones binarias del Hidrógeno: Hidruros e Hidrácidos 5. Ácidos Oxácidos 6. Hidróxidos,
FORMULACIÓN INORGÁNICA 1. Elementos Químicos. 2. Valencia. 3. Combinaciones binarias del Oxígeno: Óxidos 4. Combinaciones binarias del Hidrógeno: Hidruros e Hidrácidos 5. Ácidos Oxácidos 6. Hidróxidos,
FORMULACIÓN QUÍMICA INORGÁNICA FORMULACIÓN QUÍMICA INORGÁNICA. Son aquellas sustancias que están formadas por átomos de la misma clase.
 FORMULACIÓN QUÍMICA INORGÁNICA FORMULACIÓN QUÍMICA INORGÁNICA Elementos químicos Son aquellas sustancias que están formadas por átomos de la misma clase. Símbolos Dalton se inventó una serie de símbolos
FORMULACIÓN QUÍMICA INORGÁNICA FORMULACIÓN QUÍMICA INORGÁNICA Elementos químicos Son aquellas sustancias que están formadas por átomos de la misma clase. Símbolos Dalton se inventó una serie de símbolos
SESIÓN 1 CÁLCULOS QUÍMICOS
 SESIÓN 1 CÁLCULOS QUÍMICOS I. CONTENIDOS: 1. Nomenclatura química. 2. atómica. 3. molecular. 4. Concepto mol. 5. El número de Avogadro. II. OBJETIVOS: Al término de la Sesión, el alumno: Recordará las
SESIÓN 1 CÁLCULOS QUÍMICOS I. CONTENIDOS: 1. Nomenclatura química. 2. atómica. 3. molecular. 4. Concepto mol. 5. El número de Avogadro. II. OBJETIVOS: Al término de la Sesión, el alumno: Recordará las
Formulación química inorgánica Compuestos binarios
 1/9 Los compuestos binarios son aquellos formados por dos elementos. A continuación se muestran las distintas combinaciones de dos elementos. Normas generales de formulación. Óxidos: Óxidos básicos y óxidos
1/9 Los compuestos binarios son aquellos formados por dos elementos. A continuación se muestran las distintas combinaciones de dos elementos. Normas generales de formulación. Óxidos: Óxidos básicos y óxidos
Trióxido de dihierro
 FORMULACIÓN QUÍMICA INORGÁNICA Combinaciones binarias (Combinaciones de dos elementos) OXIDOS = Elemento - Oxígeno No metal (1) + Oxígeno = Óxido no metálico CO 2 ; SO 3 ; N 2 O 5 ; CO ; SO 2 ; NO 2 (1)
FORMULACIÓN QUÍMICA INORGÁNICA Combinaciones binarias (Combinaciones de dos elementos) OXIDOS = Elemento - Oxígeno No metal (1) + Oxígeno = Óxido no metálico CO 2 ; SO 3 ; N 2 O 5 ; CO ; SO 2 ; NO 2 (1)
ion hidrógeno Li + ion litio Mg 2+ ion cloruro F - ion fluoruro S 2- ion sulfuro H - ion hidruro P 3-
 I. IONES Conformados por uno o más átomos del mismo elemento, presentan carga positiva o MONOATÓMICOS: negativa. I.1 CATIONES: Presentan carga positiva. H + ion hidrógeno Li + ion litio Mg 2+ ion magnesio
I. IONES Conformados por uno o más átomos del mismo elemento, presentan carga positiva o MONOATÓMICOS: negativa. I.1 CATIONES: Presentan carga positiva. H + ion hidrógeno Li + ion litio Mg 2+ ion magnesio
EJERCICIOS DE FORMULACIÓN Y NOMENCLATURA
 EJERCICIOS DE FORMULACIÓN Y NOMENCLATURA 1. Determina el número de oxidación del manganeso en los compuestos: MnO 2 Mn 2 O 3 2. Determina el número de oxidación del Cl en los compuestos: Cl 2 O 7 Cl 2
EJERCICIOS DE FORMULACIÓN Y NOMENCLATURA 1. Determina el número de oxidación del manganeso en los compuestos: MnO 2 Mn 2 O 3 2. Determina el número de oxidación del Cl en los compuestos: Cl 2 O 7 Cl 2
La fórmula química expresa la composición de moléculas y compuestos mediante símbolos químicos. 13 millones!!!
 La fórmula química expresa la composición de moléculas y compuestos mediante símbolos químicos El Nº de compuestos químicos conocidos es superior a 13 millones!!! Método sistemático de nombrar los compuestos:
La fórmula química expresa la composición de moléculas y compuestos mediante símbolos químicos El Nº de compuestos químicos conocidos es superior a 13 millones!!! Método sistemático de nombrar los compuestos:
NOMENCLATURA y FORMULACIÓN en QUÍMICA INORGÁNICA
 NOMENCLATURA y FORMULACIÓN en QUÍMICA INORGÁNICA I. Sustancias Simples Aquéllas constituidas por átomos de un mismo elemento. Los gases nobles son monoatómicos: He, Ne, Ar, Kr, Xe, Rn Las moléculas de
NOMENCLATURA y FORMULACIÓN en QUÍMICA INORGÁNICA I. Sustancias Simples Aquéllas constituidas por átomos de un mismo elemento. Los gases nobles son monoatómicos: He, Ne, Ar, Kr, Xe, Rn Las moléculas de
Para nombrar compuestos químicos según esta nomenclatura se utilizan los prefijos: MONO_, DI_, TRI_, TETRA_, PENTA_, HEXA_, HEPTA_...
 3. NOMENCLATURAS. Para nombrar los compuestos químicos inorgánicos se siguen las normas de la IUPAC (unión internacional de química pura y aplicada). Se aceptan tres tipos de nomenclaturas para los compuestos
3. NOMENCLATURAS. Para nombrar los compuestos químicos inorgánicos se siguen las normas de la IUPAC (unión internacional de química pura y aplicada). Se aceptan tres tipos de nomenclaturas para los compuestos
Formulación de Química Inorgánica
 Formulación de Química Inorgánica Conceptos básicos: Elemento químico: sustancia que no puede descomponerse en otra más sencilla por procedimientos químicos ordinarios. Cobre, plata, oro, sodio, azufre
Formulación de Química Inorgánica Conceptos básicos: Elemento químico: sustancia que no puede descomponerse en otra más sencilla por procedimientos químicos ordinarios. Cobre, plata, oro, sodio, azufre
M m+ + X n- M n X m. Qué es formular un compuesto binario?
 Qué es formular un compuesto binario? Cuando tenemos dos elementos, uno menos electronegativo que otro, es decir uno con tendencia a ceder electrones M m+ (m es número de oxidación o valencia) y otro con
Qué es formular un compuesto binario? Cuando tenemos dos elementos, uno menos electronegativo que otro, es decir uno con tendencia a ceder electrones M m+ (m es número de oxidación o valencia) y otro con
NOMENCLATURA y FORMULACIÓN en QUÍMICA INORGÁNICA. Nivel: Educación Secundaria Obligatoria
 NOMENCLATURA y FORMULACIÓN en QUÍMICA INORGÁNICA Nivel: Educación Secundaria Obligatoria Conceptos básicos Los elementos químicos se representan mediante símbolos, que consisten en una o dos letras que
NOMENCLATURA y FORMULACIÓN en QUÍMICA INORGÁNICA Nivel: Educación Secundaria Obligatoria Conceptos básicos Los elementos químicos se representan mediante símbolos, que consisten en una o dos letras que
FORMULACIÓN Y NOMENCLATURA
 1. SUSTANCIAS SIMPLES. FORMULACIÓN Y NOMENCLATURA Están constituidas por átomos de un solo elemento. En ellas las moléculas están formadas por átomos idénticos. Su fórmula indica el número de átomos de
1. SUSTANCIAS SIMPLES. FORMULACIÓN Y NOMENCLATURA Están constituidas por átomos de un solo elemento. En ellas las moléculas están formadas por átomos idénticos. Su fórmula indica el número de átomos de
Lo primero que hay que conocer para formular y nombrar los compuestos químicos es el número de oxidación de cada elemento.
 Tema 5. NOMENCLATURA Y FORMULACIÓN DE QUÍMICA INORGÁNICA Introducción La IUPAC (Unión Internacional de Química Pura y Aplicada) es el organismo que coordina y actualiza las normas que permiten formular
Tema 5. NOMENCLATURA Y FORMULACIÓN DE QUÍMICA INORGÁNICA Introducción La IUPAC (Unión Internacional de Química Pura y Aplicada) es el organismo que coordina y actualiza las normas que permiten formular
FORMULACIÓN DE QUÍMICA INORGÁNICA.
 FORMULACIÓN DE QUÍMICA INORGÁNICA. 1. VALENCIA. Es la capacidad que tiene un átomo de un elemento para combinarse con los átomos de otros elementos y formar compuestos. La valencia es un número, positivo
FORMULACIÓN DE QUÍMICA INORGÁNICA. 1. VALENCIA. Es la capacidad que tiene un átomo de un elemento para combinarse con los átomos de otros elementos y formar compuestos. La valencia es un número, positivo
1 HIDRUROS COMPUESTOS BINARIOS. Química Formulación y nomenclatura Adrián de la Torre Isidoro
 Química y nomenclatura Adrián de la Torre Isidoro Dependiendo del número de elementos que intervienen en un compuesto, estos se dividen en componentes binarios, sin tiene dos elementos; terciarios, si
Química y nomenclatura Adrián de la Torre Isidoro Dependiendo del número de elementos que intervienen en un compuesto, estos se dividen en componentes binarios, sin tiene dos elementos; terciarios, si
FORMULACIÓN INORGÁNICA. CURSO 2014-2015 COMPUESTOS BINARIOS.
 FORMULACIÓN INORGÁNICA. CURSO 2014-2015 COMPUESTOS BINARIOS. 1. ÓXIDOS. Son compuestos, formados por la unión del oxígeno y cualquier otro elemento de la tabla periódica (excepto los gases nobles que jamás
FORMULACIÓN INORGÁNICA. CURSO 2014-2015 COMPUESTOS BINARIOS. 1. ÓXIDOS. Son compuestos, formados por la unión del oxígeno y cualquier otro elemento de la tabla periódica (excepto los gases nobles que jamás
NOMENCLATURA. 2. Conocer los símbolos de los elementos y sus nombres.
 NOMENCLATURA La nomenclatura puede definirse como la terminología de los compuestos químicos. Representa el lenguaje básico de la química. Así como los estudiantes que estudian Francés deben aprenderse
NOMENCLATURA La nomenclatura puede definirse como la terminología de los compuestos químicos. Representa el lenguaje básico de la química. Así como los estudiantes que estudian Francés deben aprenderse
Formulación de Química Inorgánica
 Formulación de Química Inorgánica F. G. Calvo-Flores 1. VALENCIA. Es la capacidad que tiene un átomo de un elemento para combinarse con los átomos de otros elementos y formar compuestos. La valencia es
Formulación de Química Inorgánica F. G. Calvo-Flores 1. VALENCIA. Es la capacidad que tiene un átomo de un elemento para combinarse con los átomos de otros elementos y formar compuestos. La valencia es
FORMULACIÓN INORGÁNICA
 FORMULACIÓN INORGÁNICA 1. Valencia. 2. Combinaciones binarias del Oxígeno: Óxidos y peróxidos 3. Combinaciones binarias del Hidrógeno: Hidruros e Hidrácidos 4. Combinaciones binarias: sales haloideas y
FORMULACIÓN INORGÁNICA 1. Valencia. 2. Combinaciones binarias del Oxígeno: Óxidos y peróxidos 3. Combinaciones binarias del Hidrógeno: Hidruros e Hidrácidos 4. Combinaciones binarias: sales haloideas y
1 FORMULACIÓN Y NOMENCLATURA INORGÁNICA
 1 FORMULACIÓN Y NOMENCLATURA INORGÁNICA I.B. Alonso de Covarrubias En química utilizamos fórmulas para representar elementos y compuestos. La IUPAC (Unión Internacional de Química Pura y Aplicada) es el
1 FORMULACIÓN Y NOMENCLATURA INORGÁNICA I.B. Alonso de Covarrubias En química utilizamos fórmulas para representar elementos y compuestos. La IUPAC (Unión Internacional de Química Pura y Aplicada) es el
FORMULACIÓN QUÍMICA INORGÁNICA
 FORMULACIÓN QUÍMICA INORGÁNICA 1. VALENCIAS DE LOS ELEMENTOS QUÍMICOS MÁS CONOCIDOS Se entiende que las valencias con signo negativo se dan frente a elementos electropositivos y las valencias con signo
FORMULACIÓN QUÍMICA INORGÁNICA 1. VALENCIAS DE LOS ELEMENTOS QUÍMICOS MÁS CONOCIDOS Se entiende que las valencias con signo negativo se dan frente a elementos electropositivos y las valencias con signo
Formulación y Nomenclatura
 Formulación y más metal NÚMEROS DE OXIDACIÓN DE LOS ELEMENTOS MÁS FRECUENTES: Hidrógeno (-1/+1) Niquel (+2/+3) Fósforo (-3/+3/+5) Litio (+1) Platino (+2/+4) Arsénico (-3/+3/+5) Sodio (+1) Cobre (+1/+2)
Formulación y más metal NÚMEROS DE OXIDACIÓN DE LOS ELEMENTOS MÁS FRECUENTES: Hidrógeno (-1/+1) Niquel (+2/+3) Fósforo (-3/+3/+5) Litio (+1) Platino (+2/+4) Arsénico (-3/+3/+5) Sodio (+1) Cobre (+1/+2)
FORMULACIÓN DE QUÍMICA INORGÁNICA
 www.matyfyq.com 1/10 1. VALENCIA. Es la capacidad que tiene un átomo de un elemento para combinarse con los átomos de otros elementos y formar compuestos. La valencia es un número, positivo o negativo,
www.matyfyq.com 1/10 1. VALENCIA. Es la capacidad que tiene un átomo de un elemento para combinarse con los átomos de otros elementos y formar compuestos. La valencia es un número, positivo o negativo,
NOMENCLATURA DE QUÍMICA INORGÁNICA COMPUESTOS BINARIOS (3.º ESO)
 NOMENCLATURA DE QUÍMICA INORGÁNICA COMPUESTOS BINARIOS Para qué la nomenclatura química? Cuando estudiamos química nos encontramos con multitud de sustancias a las que debemos de asignar un nombre y una
NOMENCLATURA DE QUÍMICA INORGÁNICA COMPUESTOS BINARIOS Para qué la nomenclatura química? Cuando estudiamos química nos encontramos con multitud de sustancias a las que debemos de asignar un nombre y una
FORMULACIÓN INORGÁNICA. Departamento de Física y Química 3º ESO
 FORMULACIÓN INORGÁNICA Departamento de Física y Química 3º ESO 1. Tabla periódica de los elementos -1 Valencia: capacidad que posee un elemento para combinarse con otro Número de oxidación: número de electrones
FORMULACIÓN INORGÁNICA Departamento de Física y Química 3º ESO 1. Tabla periódica de los elementos -1 Valencia: capacidad que posee un elemento para combinarse con otro Número de oxidación: número de electrones
Formulación Inorgánica
 Formulación Inorgánica 1.- Sustancias Simples Por sustancias simples entendemos aquellas sustancias formadas por un solo tipo de elementos, podemos encontrar casos: Sustancias simples metálicas: se formulan
Formulación Inorgánica 1.- Sustancias Simples Por sustancias simples entendemos aquellas sustancias formadas por un solo tipo de elementos, podemos encontrar casos: Sustancias simples metálicas: se formulan
FORMULACIÓN INORGÁNICA
 FORMULACIÓN INORGÁNICA Al escribir la fórmula de un compuesto se escriben los símbolos de los elementos que lo forman desde el menos electronegativo (a la izquierda, suele ser un Metal), hasta el más electronegativo
FORMULACIÓN INORGÁNICA Al escribir la fórmula de un compuesto se escriben los símbolos de los elementos que lo forman desde el menos electronegativo (a la izquierda, suele ser un Metal), hasta el más electronegativo
Fórmula: primero se escribe el elemento menos electronegativo (orden decreciente: F, O, Cl, Br, I, S, Se, Te, H, N, P, As, Sb, C, Si, B )
 FORMULACIÓN INORGÁNICA Regla general para todos los compuestos: Fórmula: primero se escribe el elemento menos electronegativo (orden decreciente: F, O, Cl, Br, I, S, Se, Te, H, N, P, As, Sb, C, Si, B )
FORMULACIÓN INORGÁNICA Regla general para todos los compuestos: Fórmula: primero se escribe el elemento menos electronegativo (orden decreciente: F, O, Cl, Br, I, S, Se, Te, H, N, P, As, Sb, C, Si, B )
TEMA 4: FORMULACIÓN 1.- CONCEPTOS PREVIOS
 TEMA 4: FORMULACIÓN 1.- CONCEPTOS PREVIOS Compuesto químico: es la unión de varios átomos que no pueden separarse por procedimientos físicos pero sí mediante procedimientos químicos. Ejemplo: dos átomos
TEMA 4: FORMULACIÓN 1.- CONCEPTOS PREVIOS Compuesto químico: es la unión de varios átomos que no pueden separarse por procedimientos físicos pero sí mediante procedimientos químicos. Ejemplo: dos átomos
RÉSUMENES Y EJERCICIOS DE FORMULACIÓN QUÍMICA INORGÁNICA
 RÉSUMENES Y EJERCICIOS DE FORMULACIÓN QUÍMICA INORGÁNICA COMPUESTOS BINARIOS CON OXÍGENO El oxígeno se combina con todos los elementos excepto con los gases nobles. En estos compuestos el oxígeno actúa
RÉSUMENES Y EJERCICIOS DE FORMULACIÓN QUÍMICA INORGÁNICA COMPUESTOS BINARIOS CON OXÍGENO El oxígeno se combina con todos los elementos excepto con los gases nobles. En estos compuestos el oxígeno actúa
Tema 1 : Nomenclatura y formulación Química Inorgánica
 Tema 1 : Nomenclatura y formulación Química Inorgánica Esquema de trabajo: Introducción Compuestos Binarios 1. Combinaciones binarias del oxígeno 2. Combinaciones binarias del hidrógeno 3. Sales binarias
Tema 1 : Nomenclatura y formulación Química Inorgánica Esquema de trabajo: Introducción Compuestos Binarios 1. Combinaciones binarias del oxígeno 2. Combinaciones binarias del hidrógeno 3. Sales binarias
Nombre del no metal- uro de metal. Nombres de los aniones monoatómicos derivados de no metales
 NOMENCLATURA DE COMPUESTOS QUÍMICOS Compuestos binarios de un metal con un no metal Un compuesto binario está formado por átomos de dos elementos diferentes. Cuando uno es un metal y el otro un no metal,
NOMENCLATURA DE COMPUESTOS QUÍMICOS Compuestos binarios de un metal con un no metal Un compuesto binario está formado por átomos de dos elementos diferentes. Cuando uno es un metal y el otro un no metal,
Tema 6 : Nomenclatura y formulación Química Inorgánica
 Tema 6 : Nomenclatura y formulación Química Inorgánica Esquema de trabajo: Introducción Compuestos Binarios 1. Combinaciones binarias del oxígeno: A. Oxidos B. Anhídridos 2. Combinaciones binarias del
Tema 6 : Nomenclatura y formulación Química Inorgánica Esquema de trabajo: Introducción Compuestos Binarios 1. Combinaciones binarias del oxígeno: A. Oxidos B. Anhídridos 2. Combinaciones binarias del
EJERCICIOS DE FORMULACIÓN (QUÍMICA INORGÁNICA) EJERCICIOS POR GRUPOS DE COMPUESTOS. Óxidos metálicos
 EJERCICIOS DE FORMULACIÓN (QUÍMICA INORGÁNICA) EJERCICIOS POR GRUPOS DE COMPUESTOS Óxidos metálicos 1. Nombra los siguientes compuestos: 1. PbO 2 2. Ni 2 O 3 3. V 2 O 5 4. Cs 2 O 5. Bi 2 O 3 6. OsO 4 7.
EJERCICIOS DE FORMULACIÓN (QUÍMICA INORGÁNICA) EJERCICIOS POR GRUPOS DE COMPUESTOS Óxidos metálicos 1. Nombra los siguientes compuestos: 1. PbO 2 2. Ni 2 O 3 3. V 2 O 5 4. Cs 2 O 5. Bi 2 O 3 6. OsO 4 7.
La IUPAC recomienda lo siguiente para formular los hidrácidos: Para los hidrácidos la nomenclatura tradicional y la sistemática coinciden:
 ACIDOS HIDRÁCIDOS: Son compuestos formados por HIDRÓGENO y un NO METAL de los grupos 6A y 7A. El hidrógeno presenta un estado de oxidación 1+ por lo que el no metal tomará un estado de oxidación negativo,
ACIDOS HIDRÁCIDOS: Son compuestos formados por HIDRÓGENO y un NO METAL de los grupos 6A y 7A. El hidrógeno presenta un estado de oxidación 1+ por lo que el no metal tomará un estado de oxidación negativo,
En general para formular compuestos binarios los elementos se intercambian las valencias.
 1.- VALENCIAS Es de todos conocido que los elementos químicos se combinan entre si para formar compuestos, ahora bien estos compuestos no son fruto de combinaciones al azar, sino que son el resultado de
1.- VALENCIAS Es de todos conocido que los elementos químicos se combinan entre si para formar compuestos, ahora bien estos compuestos no son fruto de combinaciones al azar, sino que son el resultado de
Reglas generales. n Se nombra electronegativo de electropositivo. n Fórmula electropositivo electronegativo
 nomenclatura Reglas generales n Se nombra electronegativo de electropositivo n El electropositivo no se modifica n El electronegativo se modificará según las reglas de n compuestos binarios, n ternarios
nomenclatura Reglas generales n Se nombra electronegativo de electropositivo n El electropositivo no se modifica n El electronegativo se modificará según las reglas de n compuestos binarios, n ternarios
1.- CONCEPTOS PREVIOS
 TEMA 6: FORMULACIÓN 1.- CONCEPTOS PREVIOS Compuesto químico: es la unión de varios átomos que no pueden separarse por procedimientos físicos pero sí mediante procedimientos químicos. Ejemplo: dos átomos
TEMA 6: FORMULACIÓN 1.- CONCEPTOS PREVIOS Compuesto químico: es la unión de varios átomos que no pueden separarse por procedimientos físicos pero sí mediante procedimientos químicos. Ejemplo: dos átomos
FORMULACIÓN Y NOMENCLATURA DE QUÍMICA INORGÁNICA
 FORMULACIÓN Y NOMENCLATURA DE QUÍMICA INORGÁNICA Índice de contenido TABLAS DE NÚMEROS DE OXIDACIÓN MÁS COMUNES...2 MECANISMO DE FORMULACIÓN...2 NOMENCLATURAS EN QUÍMICA INORGÁNICA...2 NOMENCLATURA CON
FORMULACIÓN Y NOMENCLATURA DE QUÍMICA INORGÁNICA Índice de contenido TABLAS DE NÚMEROS DE OXIDACIÓN MÁS COMUNES...2 MECANISMO DE FORMULACIÓN...2 NOMENCLATURAS EN QUÍMICA INORGÁNICA...2 NOMENCLATURA CON
ACTIVIDAD I. Desarrollo. MATERIA: todo lo que posee masa, inercia y ocupa un lugar en el espacio.
 ACTIVIDAD I ELEMENTOS Y COMPUESTOS NUMERO DE OXIDACION ACTIVIDAD I TEMARIO: Materia - Atomo - Elemento - Sustancia: elementos y compuestos - Mezclas - Molécula - Atomicidad - Símbolo de los elementos químicos
ACTIVIDAD I ELEMENTOS Y COMPUESTOS NUMERO DE OXIDACION ACTIVIDAD I TEMARIO: Materia - Atomo - Elemento - Sustancia: elementos y compuestos - Mezclas - Molécula - Atomicidad - Símbolo de los elementos químicos
FORMULACIÓN Y NOMENCLATURA DE COMPUESTOS INORGÁNICOS 1º Bach.
 FORMULACIÓN Y NOMENCLATURA DE COMPUESTOS INORGÁNICOS Para poder formular y nombrar compuestos inorgánicos lo primero que tienes que aprender es: símbolos y nombres de los elementos grupo al que pertenecen
FORMULACIÓN Y NOMENCLATURA DE COMPUESTOS INORGÁNICOS Para poder formular y nombrar compuestos inorgánicos lo primero que tienes que aprender es: símbolos y nombres de los elementos grupo al que pertenecen
-Una valencia -Dos valencias oso -ico -Tres valencias hipo- -oso -oso -ico -Cuatro valencias hipo- -oso -oso -ico per- -ico
 Tema 5: Formulación inorgánica.valencias de algunos elementos químicos Es la capacidad que tiene un átomo de un elemento para combinarse con los átomos de otros elementos y formar compuestos. La valencia
Tema 5: Formulación inorgánica.valencias de algunos elementos químicos Es la capacidad que tiene un átomo de un elemento para combinarse con los átomos de otros elementos y formar compuestos. La valencia
TEMA 5.- Formulación y nomenclatura
 Tema 5.- Formulación y nomenclatura de compuestos binarios 0.- Introducción. 1.- Óxidos. 2.- Peróxidos. 3.- Combinaciones binarias del hidrógeno. 3.1.- Hidruros. 3.2.- Haluros. 3.3.- Hidruros volátiles.
Tema 5.- Formulación y nomenclatura de compuestos binarios 0.- Introducción. 1.- Óxidos. 2.- Peróxidos. 3.- Combinaciones binarias del hidrógeno. 3.1.- Hidruros. 3.2.- Haluros. 3.3.- Hidruros volátiles.
FORMULACIÓN Y NOMENCLATURA INORGÁNICA. FÍSICA Y QUÍMICA 3º y 4º E.S.O. COLEGIO ANTONIO MACHADO. Física y Química.
 FORMULACIÓN Y NOMENCLATURA INORGÁNICA FÍSICA Y QUÍMICA 3º y 4º E.S.O. COLEGIO ANTONIO MACHADO. Física y Química. NOTA DEL PROFESOR: El objetivo de estos apuntes no es sustituir a los apuntes y a los numerosos
FORMULACIÓN Y NOMENCLATURA INORGÁNICA FÍSICA Y QUÍMICA 3º y 4º E.S.O. COLEGIO ANTONIO MACHADO. Física y Química. NOTA DEL PROFESOR: El objetivo de estos apuntes no es sustituir a los apuntes y a los numerosos
UNIDAD I. TEMA II. NOMENCLATURA
 REPUBLICA BOLIVARIANA DE VENEZUELA UNIVERSIDAD EXPERIMENTAL SUR DEL LAGO Jesús María Semprúm PROGRAMA INGENIERÌA DE ALIMENTOS. UNIDAD CURRICULAR: QUIMICA GENERAL. UNIDAD I. TEMA II. NOMENCLATURA Prof.
REPUBLICA BOLIVARIANA DE VENEZUELA UNIVERSIDAD EXPERIMENTAL SUR DEL LAGO Jesús María Semprúm PROGRAMA INGENIERÌA DE ALIMENTOS. UNIDAD CURRICULAR: QUIMICA GENERAL. UNIDAD I. TEMA II. NOMENCLATURA Prof.
FORMULACIÓN Y NOMENCLATURA INORGÁNICA
 FORMULACIÓN Y NOMENCLATURA INORGÁNICA Número de oxidación (n.o.): es la carga real (si es un ion) o aparente (si no es un ion) que tienen los elementos que forman parte de un compuesto. (Ver la tabla de
FORMULACIÓN Y NOMENCLATURA INORGÁNICA Número de oxidación (n.o.): es la carga real (si es un ion) o aparente (si no es un ion) que tienen los elementos que forman parte de un compuesto. (Ver la tabla de
Formulación y nomenclatura de
 Formulación y nomenclatura de química inorgánica Luis Muñoz Fuente luis.munoz@hispalinux.es Junio de 2006 Índice 1. Licencia de este documento 2 2. Tabla de valencias 2 3. Nomenclaturas 3 4. Combinaciones
Formulación y nomenclatura de química inorgánica Luis Muñoz Fuente luis.munoz@hispalinux.es Junio de 2006 Índice 1. Licencia de este documento 2 2. Tabla de valencias 2 3. Nomenclaturas 3 4. Combinaciones
FORMULACIÓN Y NOMENCLATURA DE COMPUESTOS INORGÁNICOS
 FORMULACIÓN Y NOMENCLATURA DE COMPUESTOS INORGÁNICOS Este libro se presenta para exponer, analizar y aplicar las reglas de formulación y nomenclatura recomendadas por la IUPAC para los compuestos inorgánicos,
FORMULACIÓN Y NOMENCLATURA DE COMPUESTOS INORGÁNICOS Este libro se presenta para exponer, analizar y aplicar las reglas de formulación y nomenclatura recomendadas por la IUPAC para los compuestos inorgánicos,
Nombre: Curso 1. Formula las siguientes combinaciones binarias con el hidrógeno:
 Nombre: Curso 1. Formula las siguientes combinaciones binarias con el hidrógeno: 1) Ácido clorhídrico 2) Sulfuro de hidrógeno 3) Estibano 4) Agua u oxidano 5) Trihidruro de fósforo 6) Hidruro de estaño(iv)
Nombre: Curso 1. Formula las siguientes combinaciones binarias con el hidrógeno: 1) Ácido clorhídrico 2) Sulfuro de hidrógeno 3) Estibano 4) Agua u oxidano 5) Trihidruro de fósforo 6) Hidruro de estaño(iv)
FORMULACIÓN QUÍMICA INORGÁNICA. Combinaciones ternarias (combinaciones de tres elementos) Hidróxidos = Metal - (OH) El grupo (OH): - 1
 FORMULACIÓN QUÍMICA INORGÁNICA I.E.S. Juan.A. Suanzes Combinaciones ternarias (combinaciones de tres elementos) Hidróxidos = Metal - (OH) Ca(OH) 2 ; NaOH ; Al(OH) 3 X (OH) m AgOH ; Zn(OH) 2 ; Cr(OH) 3
FORMULACIÓN QUÍMICA INORGÁNICA I.E.S. Juan.A. Suanzes Combinaciones ternarias (combinaciones de tres elementos) Hidróxidos = Metal - (OH) Ca(OH) 2 ; NaOH ; Al(OH) 3 X (OH) m AgOH ; Zn(OH) 2 ; Cr(OH) 3
TECNICATURA SUPERIOR EN ALIMENTOS ESCUELA MEH Prof. Ing. Alex Fernando López Córdoba, Msc (c) FORMULA Y NOMENCLATURA DE COMPUESTOS INORGÁNICOS
 TECNICATURA SUPERIOR EN ALIMENTOS ESCUELA MEH Prof. Ing. Alex Fernando López Córdoba, Msc (c) FORMULA Y NOMENCLATURA DE COMPUESTOS INORGÁNICOS Se seguirán las reglas dictadas por la IUPAC (Unión Internacional
TECNICATURA SUPERIOR EN ALIMENTOS ESCUELA MEH Prof. Ing. Alex Fernando López Córdoba, Msc (c) FORMULA Y NOMENCLATURA DE COMPUESTOS INORGÁNICOS Se seguirán las reglas dictadas por la IUPAC (Unión Internacional
Química General Básica. Nomenclatura de Compuestos Inorgánicos
 Química General Básica Nomenclatura de Compuestos Inorgánicos Estelí, 11 de marzo de 2011 Formulación y Nomenclatura en Química Inorgánica La fórmula química expresa la composición de moléculas y compuestos
Química General Básica Nomenclatura de Compuestos Inorgánicos Estelí, 11 de marzo de 2011 Formulación y Nomenclatura en Química Inorgánica La fórmula química expresa la composición de moléculas y compuestos
BASE + ACIDO SAL + AGUA. NaOH + H Cl NaCl + H 2 O
 SALES Una sal es el producto de la reacción entre un ácido y una base: en esta reacción también se produce agua: en términos muy generales, este tipo de reacción se puede escribir como : BASE + ACIDO SAL
SALES Una sal es el producto de la reacción entre un ácido y una base: en esta reacción también se produce agua: en términos muy generales, este tipo de reacción se puede escribir como : BASE + ACIDO SAL
Ejercicios Nomenclatura Inorgánica
 Ejercicios Nomenclatura Inorgánica 1. De nombre a los siguientes compuestos: 1. Cl 2 O 7 2. FeO 3. N 2 O 4. SO 3 5. Cr 2 O 3 6. P 2 O 5 2. Indique la fórmula de los siguientes compuestos: 1. Trióxido de
Ejercicios Nomenclatura Inorgánica 1. De nombre a los siguientes compuestos: 1. Cl 2 O 7 2. FeO 3. N 2 O 4. SO 3 5. Cr 2 O 3 6. P 2 O 5 2. Indique la fórmula de los siguientes compuestos: 1. Trióxido de
ANIONES. Aniones monoatómicos: suelen corresponder a no metales que han ganado electrones completando su capa de valencia.
 ANIONES Son iones con carga negativa. Los hay monoatómicos y poliatómicos. Aniones monoatómicos: suelen corresponder a no metales que han ganado electrones completando su capa de valencia. Tradicional:
ANIONES Son iones con carga negativa. Los hay monoatómicos y poliatómicos. Aniones monoatómicos: suelen corresponder a no metales que han ganado electrones completando su capa de valencia. Tradicional:
FORMULACIÓN DE QUÍMICA INORGÁNICA
 FORMULACIÓN DE QUÍMICA INORGÁNICA 1. VALENCIA. Es la capacidad que tiene un átomo de un elemento para combinarse con los átomos de otros elementos y formar compuestos. La valencia es un número, positivo
FORMULACIÓN DE QUÍMICA INORGÁNICA 1. VALENCIA. Es la capacidad que tiene un átomo de un elemento para combinarse con los átomos de otros elementos y formar compuestos. La valencia es un número, positivo
FORMULACIÓN DE QUÍMICA INORGÁNICA
 DE QUÍMICA INORGÁNICA Del mismo modo que utilizamos las palabras para comunicarnos, en química recurrimos a las fórmulas para representar los compuestos. Estas fórmulas no son arbitrarias, sino que responden
DE QUÍMICA INORGÁNICA Del mismo modo que utilizamos las palabras para comunicarnos, en química recurrimos a las fórmulas para representar los compuestos. Estas fórmulas no son arbitrarias, sino que responden
TEMA 4: FORMULACIÓN 1.- CONCEPTOS PREVIOS
 TEMA 4: FORMULACIÓN 1.- CONCEPTOS PREVIOS Compuesto químico: es la unión de varios átomos que no pueden separarse por procedimientos físicos pero sí mediante procedimientos químicos. Ejemplo: dos átomos
TEMA 4: FORMULACIÓN 1.- CONCEPTOS PREVIOS Compuesto químico: es la unión de varios átomos que no pueden separarse por procedimientos físicos pero sí mediante procedimientos químicos. Ejemplo: dos átomos
Formulación: Introducción y compuesto binarios. Teoría. Compuestos binarios y ternarios
 Compuestos binarios y ternarios 1. Compuestos binarios son aquellos que están formados por dos elementos diferentes. Ejemplos: - NaH está formado por dos elementos el Na y el H - Cl 2 O está formado por
Compuestos binarios y ternarios 1. Compuestos binarios son aquellos que están formados por dos elementos diferentes. Ejemplos: - NaH está formado por dos elementos el Na y el H - Cl 2 O está formado por
PROGRAMA TOTAL FÓRMULAS QUÍMICAS Y SISTEMAS DE NOMENCLATURA CLASIFICACIÓN DE LOS COMPUESTOS QUÍMICOS INORGÁNICOS
 Departamento de Física y Química FÍSICA Y QUÍMICA ESO FORMULACIÓN Y NOMENCLATURA DE LOS COMPUESTOS QUÍMICOS INORGÁNICOS PROGRAMA TOTAL INTRODUCCIÓN FÓRMULAS QUÍMICAS Y SISTEMAS DE NOMENCLATURA CLASIFICACIÓN
Departamento de Física y Química FÍSICA Y QUÍMICA ESO FORMULACIÓN Y NOMENCLATURA DE LOS COMPUESTOS QUÍMICOS INORGÁNICOS PROGRAMA TOTAL INTRODUCCIÓN FÓRMULAS QUÍMICAS Y SISTEMAS DE NOMENCLATURA CLASIFICACIÓN
FORMULACIÓN -TEORIA ÓXIDOS. Son combinaciones binarias con oxígeno. Unidos con metales o no metales más.
 FORMULACIÓN -TEORIA ÓXIDOS Son combinaciones binarias con oxígeno. Unidos con metales o no metales más. Formulación: Se escribe el nombre del metal o no metal y luego se intercambian las valencias, se
FORMULACIÓN -TEORIA ÓXIDOS Son combinaciones binarias con oxígeno. Unidos con metales o no metales más. Formulación: Se escribe el nombre del metal o no metal y luego se intercambian las valencias, se
Nomenclatura de Compuestos Inorgánicos
 Nomenclatura de Compuestos Inorgánicos Química 105 Pontificia Universidad Católica de Puerto Rico Departamento de Química Dr. Ramón L. Hernández-Castillo Para estudiar Nomenclatura tenemos que conocer
Nomenclatura de Compuestos Inorgánicos Química 105 Pontificia Universidad Católica de Puerto Rico Departamento de Química Dr. Ramón L. Hernández-Castillo Para estudiar Nomenclatura tenemos que conocer
APUNTES DE FORMULACIÓN QUÍMICA INORGÁNICA 3º DE E.S.O
 APUNTES DE FORMULACIÓN QUÍMICA INORGÁNICA 3º DE E.S.O Colegio Cardenal Spínola Huelva FORMULACIÓN DE QUÍMICA INORGÁNICA. 1. VALENCIA. Es la capacidad que tiene un átomo de un elemento para combinarse con
APUNTES DE FORMULACIÓN QUÍMICA INORGÁNICA 3º DE E.S.O Colegio Cardenal Spínola Huelva FORMULACIÓN DE QUÍMICA INORGÁNICA. 1. VALENCIA. Es la capacidad que tiene un átomo de un elemento para combinarse con
3º ESO. FORMULACIÓN Y NOMENCLATURA DE QUÍMICA INORGÁNICA VOLVER A WEB
 3º ESO. FORMULACIÓN Y NOMENCLATURA DE QUÍMICA INORGÁNICA VOLVER A WEB 1.- IDEAS GENERALES La Química es una ciencia que posee un lenguaje propio, único e internacional. Para representar de forma abreviada
3º ESO. FORMULACIÓN Y NOMENCLATURA DE QUÍMICA INORGÁNICA VOLVER A WEB 1.- IDEAS GENERALES La Química es una ciencia que posee un lenguaje propio, único e internacional. Para representar de forma abreviada
Compuestos binarios (combinaciones de dos elementos) HIDRUROS METÁLICOS= Metal - Hidrógeno. X H m. H : - 1 Metales: el suyo. FeH 3
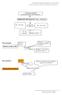 HIDRUROS METÁLICOS= Metal - Hidrógeno AlH 3 ; LiH; CuH 2 X H m KH ; FeH 3 ; ZnH 2 os N de H : - 1 Metales: el suyo Hidruro de hierro(iii) Metal a la izquierda FeH 3 Hidrógeno a la derecha (el mas electronegativo
HIDRUROS METÁLICOS= Metal - Hidrógeno AlH 3 ; LiH; CuH 2 X H m KH ; FeH 3 ; ZnH 2 os N de H : - 1 Metales: el suyo Hidruro de hierro(iii) Metal a la izquierda FeH 3 Hidrógeno a la derecha (el mas electronegativo
Como en los óxidos, pero cambiando la palabra óxido por peróxido. Ej: Cs 2 O 2 : peróxido de cesio
 Sustancias simples Formadas por átomos de un mismo elemento. Se nombran usando un prefijo indicando el número de átomos seguido del nombre del elemento. Sustancia Nombre sistemático Nombre común H Monohidrógeno
Sustancias simples Formadas por átomos de un mismo elemento. Se nombran usando un prefijo indicando el número de átomos seguido del nombre del elemento. Sustancia Nombre sistemático Nombre común H Monohidrógeno
NOMENCLATURA COMPUESTOS BINARIOS:
 NOMENCLATURA COMPUESTOS BINARIOS: ÓXIDOS: Existen tres nomenclaturas diferentes para nombrar estos compuestos. Nomenclatura de prefijos griegos: se antepone al nombre del elemento y a la palabra óxido
NOMENCLATURA COMPUESTOS BINARIOS: ÓXIDOS: Existen tres nomenclaturas diferentes para nombrar estos compuestos. Nomenclatura de prefijos griegos: se antepone al nombre del elemento y a la palabra óxido
FORMULACIÓN INORGÁNICA
 FORMULACIÓN INORGÁNICA SEMINARIO DE ACTUALIZACIÓN EN FÍSICA Y QUÍMICA C.P.R. ALCOBENDAS CURSO 1999-2000 ÍNDICE DEL CUADERNO DE FORMULACIÓN: PAG 1. Reglas para asignar el número de oxidación 1 2. Sistemas
FORMULACIÓN INORGÁNICA SEMINARIO DE ACTUALIZACIÓN EN FÍSICA Y QUÍMICA C.P.R. ALCOBENDAS CURSO 1999-2000 ÍNDICE DEL CUADERNO DE FORMULACIÓN: PAG 1. Reglas para asignar el número de oxidación 1 2. Sistemas
DEPARTAMENTO DE FÍSICA Y QUÍMICA
 Qué es formular un compuesto binario? Cuando tenemos dos elementos, uno menos electronegativo que otro, es decir uno con tendencia a ceder electrones Mm+ (m es número de oxidación o valencia) y otro con
Qué es formular un compuesto binario? Cuando tenemos dos elementos, uno menos electronegativo que otro, es decir uno con tendencia a ceder electrones Mm+ (m es número de oxidación o valencia) y otro con
Trióxido de dihierro
 ÓXIDOS Los óxidos son combinaciones de los elementos con el oxígeno. El nombre de estos compuestos siempre incluye la palabra óxido que puede estar precedida de prefijos numerales indicadores del número
ÓXIDOS Los óxidos son combinaciones de los elementos con el oxígeno. El nombre de estos compuestos siempre incluye la palabra óxido que puede estar precedida de prefijos numerales indicadores del número
Trióxido de dihierro
 COMBINACIONES BINARIAS (4ª ESO) ÓXIDOS Los óxidos son combinaciones de los elementos con el oxígeno. El nombre de estos compuestos siempre incluye la palabra óxido que puede estar precedida de prefijos
COMBINACIONES BINARIAS (4ª ESO) ÓXIDOS Los óxidos son combinaciones de los elementos con el oxígeno. El nombre de estos compuestos siempre incluye la palabra óxido que puede estar precedida de prefijos
Compuesto N. Stock N. tradicional N. sistemática. óxido de hierro (III) óxido férrico trióxido de dihierro
 Ejemplos de óxidos básicos FeO Fe 2 O 3 Cu 2 O CuO CaO PbO 2 óxido de hierro (II) óxido ferroso monóxido de hierro óxido de hierro (III) óxido férrico trióxido de dihierro óxido de cobre (I) óxido cuproso
Ejemplos de óxidos básicos FeO Fe 2 O 3 Cu 2 O CuO CaO PbO 2 óxido de hierro (II) óxido ferroso monóxido de hierro óxido de hierro (III) óxido férrico trióxido de dihierro óxido de cobre (I) óxido cuproso
Formulación y nomenclatura en Química Inorgánica. Adaptado a las normas de la IUPAC 2005 Repaso 2º bachillerato
 Formulación y nomenclatura en Química Inorgánica Adaptado a las normas de la IUPAC 2005 Repaso 2º bachillerato 2016 Conceptos básicos Valencia: nº entero que expresa la capacidad de combinación de un átomo
Formulación y nomenclatura en Química Inorgánica Adaptado a las normas de la IUPAC 2005 Repaso 2º bachillerato 2016 Conceptos básicos Valencia: nº entero que expresa la capacidad de combinación de un átomo
QUÍMICA INORGÁNICA REGLAS DE FORMULACIÓN
 QUÍMICA INORGÁNICA REGLAS DE FORMULACIÓN Rafael Jiménez Prieto FORMULACIÓN INORGÁNICA FORMULACIÓN INORGÁNICA VALENCIAS MÁS COMUNES DE LOS ELEMENTOS QUÍMICOS TIPOS DE COMPUESTOS Consideraciones generales
QUÍMICA INORGÁNICA REGLAS DE FORMULACIÓN Rafael Jiménez Prieto FORMULACIÓN INORGÁNICA FORMULACIÓN INORGÁNICA VALENCIAS MÁS COMUNES DE LOS ELEMENTOS QUÍMICOS TIPOS DE COMPUESTOS Consideraciones generales
Acuerdo 286. Química. Nomenclatura Inorgánica. Recopiló: M.C. Macaria Hernández Chávez
 Acuerdo 286 Química Nomenclatura Inorgánica Recopiló: M.C. Macaria Hernández Chávez Nomenclatura química inorgánica La Química tiene un lenguaje propio para nombrar las sustancias puras, ya sean simples
Acuerdo 286 Química Nomenclatura Inorgánica Recopiló: M.C. Macaria Hernández Chávez Nomenclatura química inorgánica La Química tiene un lenguaje propio para nombrar las sustancias puras, ya sean simples
Metal y no. metal. sodio. cloruro de COMPUESTOS IES RIBERA DE CASTILLA. Óxidos. Peróxidos. que los binarios) Pág 1
 FORMULACIÓN DE LOS COMPUESTOS QUÍMICOS BINARIOS Igual que todas las personas tenemos un nombre, también cada compuesto químico tiene el suyo. Es importante conocer la fórmula y el nombre de los compuestos
FORMULACIÓN DE LOS COMPUESTOS QUÍMICOS BINARIOS Igual que todas las personas tenemos un nombre, también cada compuesto químico tiene el suyo. Es importante conocer la fórmula y el nombre de los compuestos
NOMENCLATURA INORGÁNICA
 NOMENCLATURA INORGÁNICA Elemento: Se denomina elemento a toda sustancia que no puede descomponerse en otras más sencillas por métodos químicos. Nombre y símbolo de un elemento: Cada elemento se identifica
NOMENCLATURA INORGÁNICA Elemento: Se denomina elemento a toda sustancia que no puede descomponerse en otras más sencillas por métodos químicos. Nombre y símbolo de un elemento: Cada elemento se identifica
Formulación inorgánica
 Formulación inorgánica 1. Compuestos binarios con oxígeno (Óxidos) Combinaciones de cualquier elemento con el oxígeno. El elemento se coloca a la izquierda y el oxígeno a la derecha y se intercambian las
Formulación inorgánica 1. Compuestos binarios con oxígeno (Óxidos) Combinaciones de cualquier elemento con el oxígeno. El elemento se coloca a la izquierda y el oxígeno a la derecha y se intercambian las
FORMULACIÓN INORGÁNICA CURSO 2012-2013 DPTO. FÍSICA Y QUÍMICA IES. ALMINARES
 A) SUSTANCIAS SIMPLES - Los elementos gaseosos suelen encontrarse en forma de moléculas diatómicas. Ej: H 2, O 2, N 2, Cl 2,... Algunas excepciones son el ozono ( O 3 ), azufre ( S 8 )... - Los metales
A) SUSTANCIAS SIMPLES - Los elementos gaseosos suelen encontrarse en forma de moléculas diatómicas. Ej: H 2, O 2, N 2, Cl 2,... Algunas excepciones son el ozono ( O 3 ), azufre ( S 8 )... - Los metales
NOMENCLATURA y FORMULACIÓN en QUÍMICA INORGÁNICA
 NOMENCLATURA y FORMULACIÓN en QUÍMICA INORGÁNICA Adaptado a las normas de la IUPAC 1990 Nivel: 3º ESO 1 0. Introducción Valencia Es la capacidad que posee un elemento de combinarse con otro. Como el hidrógeno
NOMENCLATURA y FORMULACIÓN en QUÍMICA INORGÁNICA Adaptado a las normas de la IUPAC 1990 Nivel: 3º ESO 1 0. Introducción Valencia Es la capacidad que posee un elemento de combinarse con otro. Como el hidrógeno
Calcio(2+) Hierro(3+)
 CATIONES MONOATÓMICOS MONOATÓMICOS La carga se indica con un superíndice a la derecha del símbolo del elemento seguido del signo + Ca + Fe 3+ La carga se indica con un superíndice a la derecha seguido
CATIONES MONOATÓMICOS MONOATÓMICOS La carga se indica con un superíndice a la derecha del símbolo del elemento seguido del signo + Ca + Fe 3+ La carga se indica con un superíndice a la derecha seguido
GUIA Nº 1 LABORATORIO QUIMICA GENERAL NOMENCLATURA DE QUIMICA INORGÁNICA.
 1 GUIA Nº 1 LABORATORIO QUIMICA GENERAL NOMENCLATURA DE QUIMICA INORGÁNICA. 1. Estado de Oxidación Es la capacidad que tiene un átomo de un elemento para combinarse con los átomos de otros elementos y
1 GUIA Nº 1 LABORATORIO QUIMICA GENERAL NOMENCLATURA DE QUIMICA INORGÁNICA. 1. Estado de Oxidación Es la capacidad que tiene un átomo de un elemento para combinarse con los átomos de otros elementos y
