INFORME DE EVALUACIÓN COMITÉ DE EVALUACIÓN DE NUEVOS MEDICAMENTOS OXICODONA
|
|
|
- Julio Coronel Salinas
- hace 7 años
- Vistas:
Transcripción
1 INFORME DE EVALUACIÓN COMITÉ DE EVALUACIÓN DE NUEVOS MEDICAMENTOS Principio activo: Nombre Comercial y presentaciones: OXICODONA OXYCONTIN comprimidos de liberación prolongada (Mundipharma Pharmaceuticals) 10 mg 28 comp (15,92 ) 20 mg 28 comp (31,91 ) 40 mg 28 comp (64,29 ) 80 mg 28 comp (105,87 ) Condiciones de dispensación: Con receta de estupefacientes. Procedimiento de autorización: Reconocimiento mutuo Fecha de evaluación: Octubre 2004 Fecha de comercialización: Junio 2004 INDICACIONES APROBADAS 1 Tratamiento del dolor severo. MECANISMO DE ACCIÓN 1 Oxicodona es un analgésico opioide, con acción agonista pura sobre los receptores opioides del cerebro y de la médula espinal. El efecto terapéutico es principalmente analgésico, ansiolítico y sedante. FARMACOCINÉTICA 1 Oxicodona posee una biodisponibilidad de hasta el 87% tras administración oral. Tiene un tiempo de semivida de eliminación de 3 horas y se metaboliza principalmente a noroxicodona y oximorfona. La oximorfona posee cierta actividad analgésica pero está presente en el plasma a bajas concentraciones y no se considera que contribuya al efecto farmacológico de oxicodona. La liberación de oxicodona de los comprimidos de liberación controlada (LC) es bifásica, con una liberación inicial relativamente rápida, seguida de una liberación más controlada que determina las 12 horas de duración de su acción. El tiempo de semivida de eliminación de oxicodona LC es 4,5 horas lo que conduce a alcanzar un estado estacionario en aproximadamente 1 día. Oxicodona es metabolizada por el sistema enzimático citocromo P-450. POSOLOGÍA Y FORMA DE ADMINISTRACIÓN 1 Los comprimidos se deben tragar enteros; no se deben partir, masticar ni triturar, pues hacerlo conllevaría la rápida liberación y absorción de una dosis potencialmente fatal de oxicodona. La ingestión de alimentos no altera la absorción de oxicodona LC. Adultos y ancianos (más de 65 años): Oxicodona LC debe tomarse a intervalos de 12 horas. La dosificación depende de la intensidad del dolor, el historial previo, peso corporal y sexo del paciente (las mayores concentraciones en plasma se dan en la mujer). 1
2 En pacientes ancianos debilitados, pacientes que no han tomado opiáceos, o pacientes que presentan dolor severo no controlado con opiáceos más débiles, la dosis inicial usual es de 10 mg cada 12 horas. Se deberá titular la dosis cuidadosamente, diariamente si es necesario; se puede aumentar en incrementos del 25% - 50%. La ausencia de una presentación de 15 mg obliga a doblar la dosis cuando se inicia el tratamiento con 10 mg. La dosificación correcta para cualquier paciente individual es aquélla que controla el dolor y que es bien tolerada, durante un total de 12 horas. La necesidad de una medicación de rescate de más de dos veces al día indica que debe aumentarse la dosificación. Conversión de morfina oral: Los pacientes a los que se les administra morfina oral antes de la terapia con oxicodona LC deberán recibir su dosis diaria, según la siguiente proporción propuesta en la ficha técnica: 10 mg de oxicodona oral equivalen a 20 mg de morfina oral (1:2), si bien la variabilidad entre pacientes requiere que para cada uno sea titulada cuidadosamente la dosis. Sin embargo, en los ensayos clínicos evaluados la equivalencia es del orden de 1:1,4 a 1:1,8. Dolor no-maligno: El tratamiento deberá ser breve e intermitente a fin de minimizar el riesgo de dependencia. La necesidad de un tratamiento continuado deberá ser evaluada a intervalos regulares. Los pacientes no deberán precisar, en general, más de 160 mg por día. Dolor oncológico: Se evaluará la dosis hasta que se consiga suprimir el dolor en el paciente, salvo que lo impidan unas reacciones adversas al fármaco incontrolables. Pacientes con deterioro o insuficiencia renal o hepático: A diferencia de los preparados de morfina, la administración de oxicodona LC no causa niveles significativos de metabolitos activos. No obstante, la concentración de oxicodona en plasma en este grupo de pacientes puede verse aumentada en comparación con pacientes con una función renal o hepática normal. Por tanto, en estos pacientes la dosis inicial deberá seguir un planteamiento conservador, es decir, de un tercio a la mitad de la dosis habitual con una meticulosa evaluación de la dosis. En la insuficiencia hepática severa, puede que sea necesario reducir la frecuencia de la dosificación. No existen datos sobre el uso de oxicodona LC en pacientes sometidos a hemodiálisis. Adultos menores de 20 años y niños: No recomendado. EFICACIA CLÍNICA Se han publicado 5 ensayos clínicos aleatorizados (ECA) que evalúan oxicodona LC frente a un comparador activo (en 4 frente a morfina LC y en 1 frente a hidromorfona LC) en el tratamiento del dolor crónico oncológico (2-6). (VER TABLA DE ENSAYOS CLÍNICOS). En general, el número de pacientes que participaron en los ensayos es reducido. El interés de los mismos es la determinación de las dosis equianalgésicas. No se han encontrado ensayos comparativos que evalúen oxicodona en pacientes en los que hubiera fracasado el tratamiento con morfina o en los que los efectos adversos con morfina hubieran llevado al abandono del tratamiento (7). Los 4 ensayos comparativos doble ciego oxicodona LC vs morfina LC cada 12 horas, permiten considerar que en términos de eficacia analgésica, 1 dosis de 1 mg de oxicodona corresponde a 1,5 mg de morfina, con variaciones individuales importantes(2-5). Por otra parte, una dosis de 1 mg de oxicodona se corresponde con 0,25 mg de hidromorfona (no comercializada en España) (6). La variable principal de eficacia utilizada en estos estudios ha consistido en valoraciones subjetivas del dolor realizadas por los pacientes, entre ellas la escala visual-analógica (EVA) que utiliza una escala que va desde 0 (ausencia de dolor) a 10 ó 100 (dolor insoportable). También se determina la cantidad de medicación de rescate utilizada. Los ensayos clínicos en los que se compara oxicodona LC frente a morfina LC son todos aleatorizados, doble-ciego, 3 de ellos cruzados (2,4,5) y uno en paralelo (3), en los que se administran ambos fármacos cada 12 h. El ensayo clínico frente a hidromorfona es aleatorizado doble-ciego, cruzado y se administró oxicodona o hidromorfona cada 12 h(6). En cuatro de los ensayos (3-6), no se observaron diferencias significativas en el efecto analgésico de oxicodona LC frente a morfina LC e hidromorfona LC, mientras que en el ensayo restante (2) sí se observaron diferencias significativas, a favor de morfina LC. En cuanto al uso de analgésicos de rescate, en dos de los ensayos (3,6) no se observaron diferencias significativas. Por otra parte, en otros dos ensayos (2,4) se utilizaron más analgésicos de rescate en el grupo tratado con oxicodona LC 2
3 (diferencias significativas), y por el contrario, en el ensayo restante (5) el uso de analgésicos de rescate fue más frecuente en el grupo tratado con morfina LC. Por otra parte, en el dolor severo no oncológico: neuropatía diabética (8), neuralgia postherpética (9), artrosis (10,11), cirugía (12,13), los ensayos evalúan oxicodona frente a placebo, no habiéndose encontrado ninguno en el que se evalúe oxicodona LC frente a comparador activo. Es por ello que no se ha procedido a su evaluación. SEGURIDAD Reacciones adversas (RAM)(1,3-6) Las reacciones adversas son las típicas de los agonistas opioides, siendo las más comunes las náuseas y el estreñimiento, presentes en el 28% - 30% de los pacientes. También se describen como muy frecuentes (>10%): vómitos, somnolencia, vértigo, prurito. Como frecuentes (1-10%): edema, fiebre, dolor abdominal, astenia, cefaleas, vasodilatación, anorexia, diarrea, sequedad de boca, dispepsia, flatulencia, sueños anómalos, ansiedad, confusión, depresión, insomnio, alucinaciones, debilidad, disnea, broncoespasmo, rash, sudoración, trastornos urinarios. La incidencia global de efectos adversos en los ensayos clínicos con oxicodona no es diferente a la observada con morfina o hidromorfona. Aunque en algún ensayo se han observado diferencias en cuanto a mayor frecuencia de estreñimiento con oxicodona (2) y mayor frecuencia de vómitos con morfina (2,5), el reducido número de pacientes en ambos estudios, así como el elevado % de abandonos y la corta duración de uno de ellos (2), hacen que no se puedan establecer conclusiones fiables. Una supresión brusca del tratamiento o la administración de un antagonista de los opiáceos puede dar como resultado un síndrome de supresión, caracterizado por ansiedad, irritabilidad, escalofríos, sofocos, piloerección, dolor de las articulaciones, rinorrea, diaforesis, calambres abdominales y diarrea. Tratamiento de sobredosis por oxicodona: los signos de sobredosis son pupilas puntiformes y depresión respiratoria, la cual puede resultar en apnea, parada respiratoria, depresión circulatoria, hipotensión, coma o muerte. Se deberá prestar atención inmediata para el restablecimiento de las vías respiratorias del paciente e instalar ventilación asistida o controlada. En el caso de sobredosis masiva administrar por vía IV 0,8 mg de naloxona. Repetir a intervalos de 2-3 minutos según sea necesario o mediante infusión de 2 mg en 500 ml de solución salina normal o dextrosa al 5%. La infusión deberá administrarse en proporción a la dosis en bolo previamente administrada y deberá estar de acuerdo con la respuesta del paciente. Oxicodona LC continuará liberándose hasta 12 horas después de la administración, por lo que el control de la sobredosis deberá modificarse en concordancia. Para sobredosis menos severas, administrar por vía iv 0.2 mg de naloxona, seguido de incrementos de 0,1 mg cada 2 minutos si fuera necesario. Naloxona no deberá ser administrada en ausencia de una depresión respiratoria o circulatoria clínicamente significativa secundaria a la sobredosis por oxicodona. Se deberá administrar naloxona con precaución a aquellas personas que se sabe o se sospecha son físicamente dependientes de oxicodona. En tales casos una inversión drástica o completa de los efectos opioides puede precipitar dolor y síndrome de supresión agudo. Por tratarse de una formulación de liberación modificada puede ser necesario vaciar el contenido gástrico, para retirar el fármaco no absorbido. 3
4 Advertencias y precauciones 1 Al igual que con todos los narcóticos es aconsejable una reducción de la dosificación en caso de hipotiroidismo. Utilizar con precaución en pacientes opioide-dependientes, en pacientes con psicosis tóxica y en pacientes con elevada presión intracraneal, hipotensión, hipovolemia, y enfermedades del tracto biliar, pancreatitis, trastornos inflamatorios del intestino grueso, hipertrofia prostática, insuficiencia adrenocortical, alcoholismo agudo, enfermedad hepática y renal crónica y pacientes débiles. Al igual que con todas las preparaciones opioides, aquellos pacientes que se sometan a una cordot omía u otros procedimientos quirúrgicos que alivien el dolor, no deberán recibir oxicodona LC durante las 24 horas previas a la intervención. Si se indica un tratamiento posterior con oxicodona LC, la dosis deberá ajustarse a las nuevas necesidades post-operatorias. Oxicodona LC deberá administrarse con precaución tras una intervención abdominal, ya que los opiáceos causan disfunción de la motilidad intestinal. Puede producirse dependencia física en pacientes tratados con oxicodona. Una supresión drástica del fármaco o la administración de un opioide antagonista puede ser causa de síndrome de abstinencia. Cuando los pacientes ya no necesiten terapia con oxicodona LC los sometidos a dosis de mg/día pueden normalmente detener la terapia de forma drástica y sin consecuencias. Las dosis más elevadas deberán reducirse a lo largo de varios días, de forma que la dosis diaria se reduzca en aproximadamente el 50% durante los dos primeros días y en adelante un 25% cada dos días, hasta que el total de la dosis diaria sea de 10 mg cada 12 horas. En ese momento la terapia puede discontinuarse. Oxicodona puede modificar las reacciones del paciente en diversos grados, dependiendo de la dosis y de la susceptibilidad individual. Los pacientes afectados no deberán conducir o manejar máquinas. No se ha establecido la seguridad de oxicodona utilizada pre-operatoriamente y hasta 24 horas de post-operatorio, y no puede ser recomendada. Contraindicaciones 1 Depresión respiratoria, lesiones cerebrales, íleo paralítico, abdomen agudo, vaciamiento gástrico retardado, enfermedad obstructiva severa de las vías respiratorias, asma bronquial severa, hipercapnia, sensibilidad conocida a oxicodona, morfina u otros opiáceos, enfermedad hepática aguda, administración concomitante de inhibidores de la monoamino oxidasa o en las dos semanas siguientes a la discontinuación de su uso. Utilización en situaciones especiales 1,14 Embarazo: oxicodona LC tiene asignada la categoría B de la FDA, excepto si se utiliza en periodos prolongados o a altas dosis en embarazo a término, en cuyo caso tiene asignada la categoría D. Oxicodona se excreta a la leche materna y puede causar depresión respiratoria en el lactante. No está recomendado para adultos menores de 20 años ni niños. Interacciones 1 En pacientes que usen depresores del sistema nervioso central se reducirá la dosis de oxicodona LC ya que los opiáceos potencian los efectos de las fenotiacinas, antidepresivos tricíclicos, anestésicos, hipnóticos, sedantes, alcohol, miorrelajantes y antihipertensivos. Los inhibidores de la monoaminoxidasa pueden modificar la acción de los analgésicos narcóticos produciendo excitación del SNC o depresión con crisis hiper o hipotensiva. Su uso esta contraindicado. Oxicodona es metabolizada por el sistema enzimático citocromo P-450. La administración concomitante de quinidina, un inhibidor del citocromo P450-2D6, resultó en un aumento del nivel de oxicodona y noroxicodona, sin resultar alterados los efectos farmacodinámicos de oxicodona LC. Esta interacción puede observarse para otros inhibidores potentes del enzima citocromo P450-2D6. Cimetidina y los inhibidores o sustratos del citocromo P450-3A4, tales como ketoconazol y eritromicina pueden inhibir el metabolismo de oxicodona. 4
5 LUGAR EN TERAPÉUTICA En la escalera analgésica de la OMS, el tercer escalón lo ocupan los analgésicos opiáceos mayores, que son los fármacos utilizados para tratar el dolor severo. Dentro de este grupo, morfina es el fármaco de elección. En el tratamiento del dolor severo, la vía oral es la de elección. Si no es practicable, la alternativa es la vía subcutánea y después la rectal. Las formas de liberación controlada han supuesto la ventaja de poder administrar los opiáceos con una pauta más cómoda para el paciente. En este contexto, morfina LC es el tratamiento de elección del dolor crónico severo (15). En los ensayos clínicos realizados en pacientes con dolor oncológico crónico, oxicodona LC NO ha mostrado una eficacia ni un perfil de seguridad superiores a morfina LC. Por otra parte en el dolor severo no oncológico, únicamente se han publicado ensayos frente a placebo, no habiéndose realizado ECA frente a fármacos utilizados en esta indicación (morfina, gabapentina, amitriptilina...). La relación de dosis equianalgésicas oxicodona/morfina es del orden 1/1,5, con variaciones individuales importantes (7). Es una relación de dosis utilizable como primera aproximación, antes de adaptar la dosis a cada paciente. En la ficha técnica se propone una relación 1/2 (1). Morfina oral continúa siendo el tratamiento de referencia en el 3er escalón de la escalera analgésica de la OMS. En caso de no poder utilizar la vía oral, y una vez verificadas la ausencia de una nueva causa de dolor así como la correcta administración del tratamiento, existen alternativas terapéuticas: otra vía de administración de morfina o bien parches transdérmicos de fentanilo. RESUMEN ANÁLISIS COMPARATIVO Fármaco comparador: morfina de liberación controlada, administrada por vía oral. 1. Eficacia SIMILAR En los ensayos clínicos realizados en pacientes con dolor oncológico crónico, no se observan diferencias significativas entre oxicodona LC y morfina LC e hidromorfona LC en cuanto al efecto analgésico ni en cuanto al uso de analgésicos de rescate. En el dolor severo no oncológico, únicamente se han publicado ensayos frente a placebo, no habiéndose realizado ECA frente a fármacos utilizados en esta indicación (morfina, gabapentina, amitriptilina...). 2. Seguridad SIMILAR La incidencia global de efectos adversos en los ensayos clínicos con oxicodona no es diferente a la observada con morfina o hidromorfona. 3. Pauta IGUAL 4. Coste SUPERIOR El coste de oxicodona LC es 2,8 veces superior al de morfina LC. CONCLUSIÓN Oxicodona de liberación controlada (LC) es un analgésico opioide comercializado recientemente en España para el tratamiento del dolor severo. Los comprimidos de oxicodona LC permiten, al igual que los de morfina LC, una administración por vía oral cada 12 horas. En pacientes con dolor oncológico crónico, en los ensayos clínicos comparativos frente a morfina LC e hidromorfona LC (no comercializada en España) no ha presentado ventajas ni en eficacia, ni en seguridad, ni en pauta de administración con respecto a dichos fármacos. 5
6 Por otra parte, en el dolor severo no oncológico (neuropatía diabética, neuralgia postherpética, artrosis, cirugía), los ensayos evalúan oxicodona frente a placebo, no habiéndose realizado ningún ECA en el que se evalúe oxicodona LC frente a otros analgésicos. Con respecto a morfina LC, oxicodona LC presenta el inconveniente de que al inicio del tratamiento, cuando con un comprimido de 10 mg no se consigue suprimir el dolor, la inexistencia de comprimidos de 15 mg obliga a doblar la dosis. Además, debido a la inexistencia de formas de liberación inmediata de oxicodona en el mercado, en caso de necesitar medicación de rescate entre 2 tomas de oxicodona LC, habría que recurrir a especialidades farmacéuticas de morfina de liberación inmediata. El coste de oxicodona LC es 2,8 veces superior al de morfina LC. Morfina oral continúa siendo el tratamiento de referencia en el 3er escalón de la escalera analgésica de la OMS. En caso de no poder utilizar la vía oral, y una vez verificadas la ausencia de una nueva causa de dolor así como la correcta administración del tratamiento, existen alternativas terapéuticas: otra vía de administración de morfina (subcutánea) o bien parches transdérmicos de fentanilo. FRASE RESUMEN: Continuar utilizando el tratamiento de elección (morfina oral de liberación controlada) en el dolor crónico severo, ya que oxicodona LC no aporta ventajas en cuanto a eficacia, seguridad, pauta de administración ni coste. CALIFICACIÓN: NO APORTA NADA NUEVO Esta evaluación ha sido realizada de acuerdo con el Procedimiento Normalizado de Trabajo de los Comités de Evaluación de Nuevos Medicamentos de Andalucía, Cataluña y Euskadi. BIBLIOGRAFÍA 1. Ficha técnica de OXYCONTIN (Mundipharma Pharmaceuticals). 2. Heiskanen T, Kalso E. Controlled-release oxycodone and morphine in cancer related pain. Pain. 1997;73: Mucci-LoRusso P, Berman BS, Silberstein PT, Citron ML, Bressler L, Weinstein SM, et al. Controlled-release oxycodone compared with controlled-release morphine in the treatment of cancer pain: a randomized, double-blind, parallel-group study. Eur J Pain. 1998;2: Bruera E, Belzile M, Pituskin E, Fainsinger R, Darke A, Harsanyi Z, et al. Randomized, double-blind, cross-over trial comparing safety and efficay of oral controlled-release oxycodone with controlled-release morphine in patients with cancer pain. J Clin Oncol. 1998;16: Lauretti GR, Oliveira GM, Pereira NL. Comparison of sustained-release morphine with sustained-release oxycodone in advanced cancer patients. Br J Cancer. 2003; 89(11): Hagen NA, Babul N. Comparative clinical efficacy and safety of a novel controlled-release oxycodone formulation and controlled-release hydromorphone in the treatment of cancer pain. Cancer. 1997;79: Prescrire Rédaction. Oxycodone par voie orale (Oxycontin LPº). Pas d avantage sur la morphine orale. Rev Prescr. 2002;22(232): Gimbel JS, Richards P, Portenoy RK. Controlled-release oxycodone for pain in diabetic neuropathy. A randomized controlled trial. Neurology. 2003;60: Watson CP, Babul N. Efficacy of oxycodone in neuropathic pain: a randomized trial in postherpetic neuralgia. Neurology. 1998;50: Roth SH, Fleischmann RM, Burch FX, Dietz F, Bochow B, Rapoport R, et al. Around-the-clock, controlled-release oxycodone therapy for osteoarthritis-related pain. Placebo-controlled trial and long-term evaluation. Arch Intern Med. 2000;160: Caldwell JR, Hale ME, Boyd RE, Hague JM, Iwan T, et al. Treatment of osteoarthritis pain with controlled-release oxycodone or fixed combination oxycodone plus acetaminophen added to nonsteroidal antiinflammatory drugs: a double blind, randomized, multicenter, placebo controlled trial. J Rheumatol. 1999;26: Cheville A, Chen A, Oster G, McGarry L, Narcessian E. A randomized trial of controlled-release oxycodone during inpatient rehabilitation following unilateral total knee arthroplasty. J Bone Joint Surg. 2001;83(4): Reuben SS, Steinberg RB, Maciolek H. Preoperative administration of controlled-release oxycodone for the management of pain after ambulatory laparoscopic tubal ligation surgery. J Clin Anesth. 2002;14:
7 14. Briggs GG, Freeman RK, Yaffe SJ. Drugs in pregnancy and lactation. 6th edition. Philadelphia: Lippincott Williams and Wilkins; Control of pain in patients with cancer. A National Clinical Guideline. Scottish Intercollegiate Guidelines Network (SIGN). June AFSSPS. Commission de la Transparence Française. Avis de la Commission 9 mai Oxycontin LP. Disponible en URL: Fecha de acceso:
8 ANEXO 1. ESTUDIOS Referencia (Autor, publicación) Heiskanen T, Kalso, E (2) Pain. 1997;73: Financiado por The Purdue Frederick Company (oxicodona LC) Tipo de estudio EC aleatorizado, doble ciego, cruzado, con comparador activo. Objetivo: evaluar los perfiles farmacodinámicos de oxicodona LC vs morfina LC en pacientes con dolor oncológico crónico. Población (N, características) 45 pacientes adultos aleatorizados, medida de eficacia y seguridad de 27 pacientes. Datos basales: pacientes con dolor oncológico tratados con opiáceos, con dolor oncológico estable. Duración: - fase abierta aleatorizada de titulación hasta alcanzar control estable del dolor al menos 48 h (media: 6 días). - fase doble ciega cruzada en 2 periodos de 3-6 días cada uno. Resultados finales (end-point) Variable principal: eficacia: intensidad de dolor según ECVid. Variables secundarias: - dosis de medicación de rescate/día - Aceptabilidad de la terapia (dolor + efectos adversos ; escala verbal: 1-5). Tamaño del efecto Intervalos de confianza / valores p Media (DE) ECVid: oxicodona LC 0.99 (0.12) vs morfina LC 0.77 (0.07); p < Oxicodona LC 1.26 (0.22) vs morfina LC 0.79 (0.18) (p < 0.05). Oxicodona LC 3.19 (0.12) vs morfina LC 3.49 (0.11) (p < 0.05). Se describe mayor frecuencia de estreñimiento con oxicodona LC (p < 0.01) y mayor frecuencia de vómitos con morfina LC (p < 0.01). Comentarios No se hace análisis por intención de tratar. -% de abandonos: 40%. A pesar de mostrar diferencias significativas, se desconoce la relevancia clínica de diferencias de 0.22 ptos en la ECVid. La corta duración del estudio limita el alcance de estos resultados. Calidad del estudio (escala Jadad) Aleatorización: 1 Doble Ciego: 1 Pérdidas: 1 Aleatorización apropiada: 1 Ciego apropiado: 1 Total: 5 puntos 8
9 Referencia (Autor, publicación) Mucci-LoRusso P et al(3) Eur J Pain. 1998;2: Financiado por Purdue Pharma (oxicodona LC). Tipo de estudio EC multicéntrico aleatorizado, de grupos paralelos, doble ciego y controlado frente a comparador activo. Objetivo: evaluar la eficacia analgésica de oxicodona LC vs morfina LC en pacientes con dolor oncológico crónico. Población (N, características) 101 pacientes adultos aleatorizados, medida de eficacia de 79 y de seguridad de 100 pacientes. Datos basales: pacientes con dolor oncológico crónico tratados con opiáceos. Oxicodona LC (n=48) Morfina LC (n=52). Titulación de dosis hasta control estable del dolor al menos 48 h. Duración: 12 días Resultados finales (end-point) Variable principal: eficacia: intensidad de dolor según escala categórica de 0 a 3 y según EVA. Variables secundarias: - titulación de dosis - dosis de medicación de rescate/día - aceptabilidad de la terapia según escala categórica de 1 a 5. - efectos adversos ; somnolencia y náuseas. Tamaño del efecto Intervalos de confianza / valores p significativas. La relación de dosis equianalgésicas fue de 1:1,4. significativas. significativas. El perfil de efectos adversos fue similar. Comentarios -% de abandonos: 22%. Si antes del estudio estaban pautados analgésicos no opiáceos y/o medicación coadyuvante, se permitían durante el estudio. Calidad del estudio (escala Jadad) Aleatorización: 1 Doble Ciego: 1 Pérdidas: 0 Aleatorización apropiada: 1 Ciego apropiado: 1 Total: 4 puntos Bruera et al (4) J Clin Oncol. 1998;16: Financiado por Purdue Frederick (oxicodona LC). EC aleatorizado, doble ciego, cruzado, con comparador activo. Objetivo: evaluar la eficacia y seguridad de oxicodona LC vs morfina LC en pacientes con dolor oncológico. 32 pacientes adultos aleatorizados, medida de eficacia de 23 pacientes. Datos basales: pacientes con dolor oncológico tratados con opiáceos orales, con analgesia estable al menos 3 días. Relación inicial dosis oxicodona LC / morfina LC de 1:1,5. Variable principal: eficacia: intensidad de dolor según EVA (0-100) y CAT (0-4). Variables secundarias: - eficacia: dosis de medicación de rescate/día. significativas. (EVA: oxicodona LC 24,3 vs morfina LC 22,9 p=0.43; CAT: 1,3 vs 1,2 p=0.36) Relación dosis oxicodona LC / morfina LC: mediana de 1:1,5. Media (DE) : oxicodona LC 2.3 (2.3) vs morfina LC 1.7 (2.1); p= % de abandonos: 28%. Aleatorización: 1 Doble Ciego: 1 Pérdidas: 1 Aleatorización apropiada: 0 Ciego apropiado: 1 Total: 4 puntos Duración: 14 días en 2 periodos de 7 días cada uno. - seguridad: sedación, náuseas, otros efectos adversos. significativas. 9
10 Referencia (Autor, publicación) Lauretti GR et al (5). Br J Cancer. 2003; 89(11): Tipo de estudio EC multicéntrico aleatorizado, doble ciego, cruzado. Objetivo: evaluar la eficacia y seguridad de oxicodona LC vs morfina LC en pacientes con dolor oncológico, utilizando como rescate morfina de liberación rápida (MLR). Cálculo de dosis de opiáceos de liberación controlada:1:1,8 Población (nº, características) 26 pacientes aleatorizados, 22 pacientes f ueron evaluados. Datos basales: pacientes con dolor crónico oncológico en Tto con tramadol + AINE + amitriptilina con dolor en EVA de 4 (0-10). Todos los pacientes podían utilizar comprimidos de morfina de liberación rápida (MLR), para obtener un EVA<4. 1º fase abierta (7 días) tratados con morfina LR hasta control del dolor. Duración fase ciega: 28 días en 2 periodos de 14 días cada uno. Resultados finales (end-point) Consumo de MLR de rescate Reacciones adversas Analgesia (EVA) Tamaño del efecto Intervalos de confianza / valores p 38% más consumo en los pacientes con MLC; p<0,05. Menos náuseas y vómitos con oxicodona (1 evento) que con morfina (15 eventos ); p<0,05. No hubo diferencias significativas en el resto de las reacciones adversas. significativas. Comentarios -La muestra es muy pequeña (n=26). -% de abandonos: 16%. -No se dice cuál es el end-point principal. -ratio oxicodona morfina: 1:1,8 (este ratio varía en la literatura médica). Calidad del estudio (escala Jadad) Aleatorización:1 Doble Ciego:1 Pérdidas:1 Aleat apropiada:0 Ciego apropiado:0 Total: 3 puntos Hagen NA et al (6). Cancer. 1997;79: Financiado por Purdue Frederick (oxicodona LC e hidromorfona LC). EC aleatorizado, doble ciego, cruzado. Objetivo: estudiar la eficacia y seguridad de oxicodona LC vs hidromorfona LC. 44 pacientes aleatorizados, 31 pacientes fueron evaluados. Criterios inclusión: pacientes con dolor oncológico estable (necesitaban 2 o menos dosis de analgesia de rescate al día, durante 3 días) Variable principal: Analgesia escala EVA (0-100) y CAT (0-4). Variables secundarias: -Uso de opiáceos de rescate. -Sedación (EVA) -Náuseas (EVA) No hubo diferencias significativas en ninguna de las 2 escalas. significativas. Análisis por tratamiento -% de abandonos:30% Hidromorfona no está comercializada en España. Aleatorización:1 Doble Ciego:1 Pérdidas:1 Aleat apropiada:0 Ciego apropiado:1 Total: 4 puntos Duración: 14 días en 2 periodos de 7 días cada uno. -Efectos adversos significativas, excepto para la somnolencia, que fue más frecuente con OLC que con HLC (28 vs 19) (p=0,016). LC: liberación controlada. CAT: escala categórica de intensidad de dolor de 5 puntos, de 0 (ausencia de dolor) a 4 (dolor insoportable). EVA: escala visual-analógica que utiliza una línea que va desde 0 mm (ausencia de dolor) hasta 10 ó 100 mm (dolor insoportable). ECVid: escala de clasificación verbal de la intensidad de dolor, de 4 puntos: ausencia de dolor, suave, moderado, intenso. 10
INFORME A LA COMISIÓN DE FARMACIA Y TERAPÉUTICA (14/12/2009) OXICODONA
 Centro de Información de Medicamentos. Servicio de Farmacia. INFORME A LA COMISIÓN DE FARMACIA Y TERAPÉUTICA (14/12/2009) OXICODONA Datos del solicitante Dr. xxx del Servicio de Oncología solicita la inclusión
Centro de Información de Medicamentos. Servicio de Farmacia. INFORME A LA COMISIÓN DE FARMACIA Y TERAPÉUTICA (14/12/2009) OXICODONA Datos del solicitante Dr. xxx del Servicio de Oncología solicita la inclusión
Oxicodona Informe de la Comisión de Farmacia y Terapéutica
 Servicio Andaluz de Salud CONSEJERÍA DE SALUD Hospital Universitario Reina Sofía Oxicodona Informe de la Comisión de Farmacia y Terapéutica Hospital Universitario Reina Sofía 1.- Identificación del fármaco:
Servicio Andaluz de Salud CONSEJERÍA DE SALUD Hospital Universitario Reina Sofía Oxicodona Informe de la Comisión de Farmacia y Terapéutica Hospital Universitario Reina Sofía 1.- Identificación del fármaco:
OXICODONA. Informe para la Comisión de Farmacia y Terapéutica del CHUVI Febrero de 2010
 OXICODONA Informe para la Comisión de Farmacia y Terapéutica del CHUVI Febrero de 2010 1.- IDENTIFICACIÓN DEL FÁRMACO Y AUTORES DEL INFORME Fármaco: Oxicodona Indicación clínica solicitada: tratamiento
OXICODONA Informe para la Comisión de Farmacia y Terapéutica del CHUVI Febrero de 2010 1.- IDENTIFICACIÓN DEL FÁRMACO Y AUTORES DEL INFORME Fármaco: Oxicodona Indicación clínica solicitada: tratamiento
Oxicodona. . Agonista puro opioide de los receptores mu, Kappa y delta, con efecto analgésico, ansiolítico y sedante.
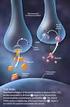 Oxicodona 1. Grupo Farmacoterapéutico:. Agonista puro opioide de los receptores mu, Kappa y delta, con efecto analgésico, ansiolítico y sedante. 2.- Formas farmacéuticas registradas:. Comprimidos de 10mg
Oxicodona 1. Grupo Farmacoterapéutico:. Agonista puro opioide de los receptores mu, Kappa y delta, con efecto analgésico, ansiolítico y sedante. 2.- Formas farmacéuticas registradas:. Comprimidos de 10mg
Tabla de equivalencia aproximada entre opioides
 Tabla de equivalencia aproximada entre opioides Documentos www.1aria.com DOSIS EQUIPOTENTES BUPRENORFINA PARCHE TRANSDÉRMICO 8,75 (0,2 17,5 (0,4 35 (0,8 52,5 (1,2 70 (1,6 105 (2,4 122,5 (2,8 140 (3,2 -
Tabla de equivalencia aproximada entre opioides Documentos www.1aria.com DOSIS EQUIPOTENTES BUPRENORFINA PARCHE TRANSDÉRMICO 8,75 (0,2 17,5 (0,4 35 (0,8 52,5 (1,2 70 (1,6 105 (2,4 122,5 (2,8 140 (3,2 -
INFORME TECNICO Nº 10 2010. Oxicodona 10mg tableta Oxicodona 20mg tableta
 INFORME TECNICO Nº 10 2010 Oxicodona 10mg tableta Oxicodona 20mg tableta 1. ANÁLISIS 1.1 EVALUACIÓN DE LA SOLICITUD Alternativas del PNME 1 Morfina 30mg tableta de liberación prolongada ATC/DCI: 2 N02AA05
INFORME TECNICO Nº 10 2010 Oxicodona 10mg tableta Oxicodona 20mg tableta 1. ANÁLISIS 1.1 EVALUACIÓN DE LA SOLICITUD Alternativas del PNME 1 Morfina 30mg tableta de liberación prolongada ATC/DCI: 2 N02AA05
INTERACCIONES ENTRE OPIOIDES
 ASPECTOS PRÁCTICOS EN EL USO DE OPIOIDES: INTERACCIÓN CON OTROS OPIOIDES: El desarrollo de nuevos agonistas opioides puros, permite en la actualidad su uso en combinación, estrategia que facilita reducir
ASPECTOS PRÁCTICOS EN EL USO DE OPIOIDES: INTERACCIÓN CON OTROS OPIOIDES: El desarrollo de nuevos agonistas opioides puros, permite en la actualidad su uso en combinación, estrategia que facilita reducir
OxyContin comprimidos 10 mg, 20 mg, 40 mg y 80 mg.
 1. NOMBRE DEL MEDICAMENTO OxyContin comprimidos 10 mg, 20 mg, 40 mg y 80 mg. 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Los comprimidos de 10 mg contienen 10 mg de clorhidrato de oxicodona equivalentes
1. NOMBRE DEL MEDICAMENTO OxyContin comprimidos 10 mg, 20 mg, 40 mg y 80 mg. 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Los comprimidos de 10 mg contienen 10 mg de clorhidrato de oxicodona equivalentes
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO. TOSEINA Solución oral 2. COMPOSICIÓN CUANTITATIVA Y CUALITATIVA
 FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO TOSEINA Solución oral 2. COMPOSICIÓN CUANTITATIVA Y CUALITATIVA Composición por 5 ml: Codeína Fosfato (Hemidrato) 10 mg 3. FORMA FARMACEUTICA Solución oral 4. DATOS
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO TOSEINA Solución oral 2. COMPOSICIÓN CUANTITATIVA Y CUALITATIVA Composición por 5 ml: Codeína Fosfato (Hemidrato) 10 mg 3. FORMA FARMACEUTICA Solución oral 4. DATOS
INFORMACION PARA PRESCRIBIR AMPLIA IPP-A K-ASMAL*
 INFORMACION PARA PRESCRIBIR AMPLIA IPP-A K-ASMAL* FORMA FARMACEUTICA Y FORMULACION Jarabe Cada 100 mi contienen: Fumarato ácido de Ketotifeno equivalente a... 20 mg de Ketotifeno vehículo, c.b.p... 100
INFORMACION PARA PRESCRIBIR AMPLIA IPP-A K-ASMAL* FORMA FARMACEUTICA Y FORMULACION Jarabe Cada 100 mi contienen: Fumarato ácido de Ketotifeno equivalente a... 20 mg de Ketotifeno vehículo, c.b.p... 100
TEMA XII: ANALGÉSICOS CENTRALES. OPIOIDES. Opio: látex que se obtiene de la cápsula de la adormidera (Papaver somniferum)
 TEMA XII: ANALGÉSICOS CENTRALES. OPIOIDES Opio: látex que se obtiene de la cápsula de la adormidera (Papaver somniferum) Los fármacos f opipoides inducen analgesia intensa Producen efectos subjetivos que
TEMA XII: ANALGÉSICOS CENTRALES. OPIOIDES Opio: látex que se obtiene de la cápsula de la adormidera (Papaver somniferum) Los fármacos f opipoides inducen analgesia intensa Producen efectos subjetivos que
Pacientes de edad avanzada: debe considerarse la conveniencia de ampliar el intervalo de dosificación (Ver Propiedades Famacocinéticas).
 FT290191-B+2 1. NOMBRE DEL MEDICAMENTO DARVON 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Dextropropoxifeno (D.C.I.) napsilato 100 mg. 3. FORMA FARMACÉUTICA Cápsulas para administración por vía oral. 4.
FT290191-B+2 1. NOMBRE DEL MEDICAMENTO DARVON 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Dextropropoxifeno (D.C.I.) napsilato 100 mg. 3. FORMA FARMACÉUTICA Cápsulas para administración por vía oral. 4.
Seminario Práctico Nº 3 INTERACCIÓNES Y METABOLISMO DE LOS FÁRMACOS: FARMACOGENÉTICA.-
 Facultad de Medicina Departamento de Farmacología y Terapéutica Seminario Práctico Nº 3 Objetivo.- INTERACCIÓNES Y METABOLISMO DE LOS FÁRMACOS: FARMACOGENÉTICA.- Se trata de adquirir conciencia sobre la
Facultad de Medicina Departamento de Farmacología y Terapéutica Seminario Práctico Nº 3 Objetivo.- INTERACCIÓNES Y METABOLISMO DE LOS FÁRMACOS: FARMACOGENÉTICA.- Se trata de adquirir conciencia sobre la
Laura March Ortí. Residente MFYC. Hospital Universitario de la Ribera. Noviembre 2014.
 Ketamina a dosis bajas asociada a morfina mejora el control del dolor en urgencias en el paciente con traumatismo Saeed Abbasi1, Mohsen Yosefzadeh2, Peyman Hafezimoghadam1, Mohammad Amin Zare1, Mahdi Rezai1,
Ketamina a dosis bajas asociada a morfina mejora el control del dolor en urgencias en el paciente con traumatismo Saeed Abbasi1, Mohsen Yosefzadeh2, Peyman Hafezimoghadam1, Mohammad Amin Zare1, Mahdi Rezai1,
Modo de administración Por vía oral. Administrar preferiblemente mañana, mediodía y noche.
 1. NOMBRE DEL MEDICAMENTO Cloperastina NORMON 3,54 mg/ml suspensión oral EFG. 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cloperastina NORMON 3,54 mg/ml suspensión oral: cada ml de suspensión oral contiene
1. NOMBRE DEL MEDICAMENTO Cloperastina NORMON 3,54 mg/ml suspensión oral EFG. 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cloperastina NORMON 3,54 mg/ml suspensión oral: cada ml de suspensión oral contiene
CINFATOS EXPECTORANTE JARABE FICHA TECNICA
 CINFATOS EXPECTORANTE JARABE FICHA TECNICA 1. NOMBRE DEL PRODUCTO CINFATOS Expectorante. 2. COMPOSICION CUALITATIVA Y CUANTITATIVA Composición por 5 ml: DEXTROMETORFANO HBr... 10 mg GUAIFENESINA... 100
CINFATOS EXPECTORANTE JARABE FICHA TECNICA 1. NOMBRE DEL PRODUCTO CINFATOS Expectorante. 2. COMPOSICION CUALITATIVA Y CUANTITATIVA Composición por 5 ml: DEXTROMETORFANO HBr... 10 mg GUAIFENESINA... 100
INFORME DE EVALUACIÓN HIDROMORFONA OROS. Comparador: MORFINA DE LIBERACIÓN CONTROLADA NO SUPONE UN AVANCE TERAPÉUTICO. Lactosa
 INFORME DE EVALUACIÓN HIDROMORFONA OROS Comparador: MORFINA DE LIBERACIÓN CONTROLADA NO SUPONE UN AVANCE TERAPÉUTICO Principio activo Nombre comercial y presentaciones: HIDROMORFINA OROS JURNISTA (Janssen-Cilag)
INFORME DE EVALUACIÓN HIDROMORFONA OROS Comparador: MORFINA DE LIBERACIÓN CONTROLADA NO SUPONE UN AVANCE TERAPÉUTICO Principio activo Nombre comercial y presentaciones: HIDROMORFINA OROS JURNISTA (Janssen-Cilag)
Lección 16. Anestésicos generales UNIDAD IV: DOLOR Y ANESTESIA. Ricardo Brage e Isabel Trapero - Farmacología Lección 16
 Ricardo Brage e Isabel Trapero - Lección 16 UNIDAD IV: DOLOR Y ANESTESIA Lección 16 Anestésicos generales Guión Ricardo Brage e Isabel Trapero - Lección 16 1. CONCEPTO ANESTESIA GENERAL. 2. EFECTOS DE
Ricardo Brage e Isabel Trapero - Lección 16 UNIDAD IV: DOLOR Y ANESTESIA Lección 16 Anestésicos generales Guión Ricardo Brage e Isabel Trapero - Lección 16 1. CONCEPTO ANESTESIA GENERAL. 2. EFECTOS DE
Guía para la toma de decisiones en la incorporación de medicamentos a la Guía Farmacoterapéutica
 Guía para la toma de decisiones en la incorporación de medicamentos a la Guía Farmacoterapéutica (GINF) VERSION: SSCC Documento Marco elaborado conjuntamente por la Comisión de Farmacia del Hospital universitario
Guía para la toma de decisiones en la incorporación de medicamentos a la Guía Farmacoterapéutica (GINF) VERSION: SSCC Documento Marco elaborado conjuntamente por la Comisión de Farmacia del Hospital universitario
Prospecto: información para el usuario Sekisan 3,54 mg/ml Jarabe Cloperastina fendizoato
 Prospecto: información para el usuario Sekisan 3,54 mg/ml Jarabe Cloperastina fendizoato Lea todo el prospecto detenidamente antes de empezar a tomar este medicamento, porque contiene información importante
Prospecto: información para el usuario Sekisan 3,54 mg/ml Jarabe Cloperastina fendizoato Lea todo el prospecto detenidamente antes de empezar a tomar este medicamento, porque contiene información importante
ANÁLISIS DE LAS NOTIFICACIONES ATENCIÓN PRIMARIA ERRORES DE MEDICACIÓN MARZO 2015
 ANÁLISIS DE LAS NOTIFICACIONES ATENCIÓN PRIMARIA ERRORES DE MEDICACIÓN MARZO 2015 Durante el mes de marzo de 2015 se han recibido en el Portal de Uso Seguro de Medicamentos un total de 252 notificaciones
ANÁLISIS DE LAS NOTIFICACIONES ATENCIÓN PRIMARIA ERRORES DE MEDICACIÓN MARZO 2015 Durante el mes de marzo de 2015 se han recibido en el Portal de Uso Seguro de Medicamentos un total de 252 notificaciones
Anexo 6. Dosificación de opioides en el dolor
 Anexo 6. Dosificación de opioides en el dolor Equivalencia aproximada entre opioides El factor de conversión se expresa como fracción con respecto a morfina oral o en mg respecto a una dosis de 30 mg de
Anexo 6. Dosificación de opioides en el dolor Equivalencia aproximada entre opioides El factor de conversión se expresa como fracción con respecto a morfina oral o en mg respecto a una dosis de 30 mg de
COMITÉ DE EVALUACIÓN DE NUEVOS MEDICAMENTOS DE EUSKADI INFORME DE EVALUACIÓN
 COMITÉ DE EVALUACIÓN DE NUEVOS MEDICAMENTOS DE EUSKADI INFORME DE EVALUACIÓN HIDROMORFONA OROS Comparador: MORFINA DE LIBERACIÓN CONTROLADA NO SUPONE UN AVANCE TERAPÉUTICO Nombre comercial y presentaciones:
COMITÉ DE EVALUACIÓN DE NUEVOS MEDICAMENTOS DE EUSKADI INFORME DE EVALUACIÓN HIDROMORFONA OROS Comparador: MORFINA DE LIBERACIÓN CONTROLADA NO SUPONE UN AVANCE TERAPÉUTICO Nombre comercial y presentaciones:
RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO Nombre del producto: Tableta entérica. 333 mg. 333,0 mg* 24 meses
 RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO Nombre del producto: ACAMPROSATO DE CALCIO Forma farmacéutica: Tableta entérica Fortaleza: Presentación: Titular del Registro Sanitario, país: Fabricante, país:
RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO Nombre del producto: ACAMPROSATO DE CALCIO Forma farmacéutica: Tableta entérica Fortaleza: Presentación: Titular del Registro Sanitario, país: Fabricante, país:
FICHA TÉCNICA. La dosis a utilizar dependerá de la evolución de los síntomas y deberá utilizarse siempre la menor dosis efectiva.
 FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Ultra-Levura 250 mg cápsulas duras 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada cápsula contiene: Saccharomyces boulardii 250 mg Excipientes con efecto conocido:
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Ultra-Levura 250 mg cápsulas duras 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada cápsula contiene: Saccharomyces boulardii 250 mg Excipientes con efecto conocido:
Uso clínico de la morfina en enfermos con dolor
 A. I. Menéndez Fernández a y M. E. Fernández Pérez b a Médico de Familia. Centro de Salud Valle Inclán. Área 7. Madrid. b Médico de Familia. Centro de Salud Las Águilas II. Área 7. Madrid. España. La morfina
A. I. Menéndez Fernández a y M. E. Fernández Pérez b a Médico de Familia. Centro de Salud Valle Inclán. Área 7. Madrid. b Médico de Familia. Centro de Salud Las Águilas II. Área 7. Madrid. España. La morfina
Mucosan jarabe pertenece a un grupo de medicamentos denominados mucolíticos-expectorantes.
 1. QUÉ ES MUCOSAN JARABE Y PARA QUÉ SE UTILIZA Mucosan jarabe pertenece a un grupo de medicamentos denominados mucolíticos-expectorantes. Mucosan jarabe se utiliza para tratar afecciones agudas y crónicas
1. QUÉ ES MUCOSAN JARABE Y PARA QUÉ SE UTILIZA Mucosan jarabe pertenece a un grupo de medicamentos denominados mucolíticos-expectorantes. Mucosan jarabe se utiliza para tratar afecciones agudas y crónicas
Resumen de las Características del Producto
 1. NOMBRE DEL MEDICAMENTO Resumen de las Características del Producto OxyNorm líquido 1 mg/ 1 ml, solución oral. 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada ml de OxyNorm líquido contiene 0,9 mg de
1. NOMBRE DEL MEDICAMENTO Resumen de las Características del Producto OxyNorm líquido 1 mg/ 1 ml, solución oral. 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada ml de OxyNorm líquido contiene 0,9 mg de
Oxycodone / Naloxone
 Oxycodone / Naloxone Centro Andaluz de Documentación e Información de Medicamentos (CADIME) Informes de Evaluación de Medicamentos Oxicodona / Naloxona INFORME (5) 2012 [Escribir el título del documento]
Oxycodone / Naloxone Centro Andaluz de Documentación e Información de Medicamentos (CADIME) Informes de Evaluación de Medicamentos Oxicodona / Naloxona INFORME (5) 2012 [Escribir el título del documento]
RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO
 RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1. NOMBRE DEL MEDICAMENTO PARACODINA 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Paracodina jarabe: Cada gramo de jarabe contiene 2 mg de dihidrocodeína bitartrato.
RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1. NOMBRE DEL MEDICAMENTO PARACODINA 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Paracodina jarabe: Cada gramo de jarabe contiene 2 mg de dihidrocodeína bitartrato.
FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO
 FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1. NOMBRE DEL MEDICAMENTO Lactulosa Level 667,5 mg/ml solución oral 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA 1 mililitro de solución oral contiene
FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1. NOMBRE DEL MEDICAMENTO Lactulosa Level 667,5 mg/ml solución oral 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA 1 mililitro de solución oral contiene
Nombre: Lincomicina Condición de venta: con receta médica Clasificación: antibiotico Disponible en: Nombres de marca:
 Nombre: Lincomicina Condición de venta: con receta médica Clasificación: antibiotico Disponible en: Nombres de marca: Lea cuidadosamente este folleto antes de la administración de este medicamento. Contiene
Nombre: Lincomicina Condición de venta: con receta médica Clasificación: antibiotico Disponible en: Nombres de marca: Lea cuidadosamente este folleto antes de la administración de este medicamento. Contiene
INTRODUCCIÓN. Mercedes Fernández Arévalo
 INTRODUCCIÓN Mercedes Fernández Arévalo FARMACIA GALÉNICA MEDICAMENTO SEGURO EFICAZ ESTABLE ORGANISMO VIVO RESPUESTA TERAPÉUTICA INICIO DURACIÓN INTENSIDAD MEDICAMENTO? TF (Sist. FQ) Proceso Tecnológico
INTRODUCCIÓN Mercedes Fernández Arévalo FARMACIA GALÉNICA MEDICAMENTO SEGURO EFICAZ ESTABLE ORGANISMO VIVO RESPUESTA TERAPÉUTICA INICIO DURACIÓN INTENSIDAD MEDICAMENTO? TF (Sist. FQ) Proceso Tecnológico
FICHA TÉCNICA. Los ingredientes activos en 1 ml de VITALIPID ADULTOS corresponden a:
 FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO VITALIPID ADULTOS 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA 1 ml de VITALIPID ADULTOS contiene: Principios activos: Retinolpalmitato (equivalente a Retinol 99 μg)
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO VITALIPID ADULTOS 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA 1 ml de VITALIPID ADULTOS contiene: Principios activos: Retinolpalmitato (equivalente a Retinol 99 μg)
Cada sobre contiene: Macrogol 3350 17.0 g. Cada frasco contiene: Macrogol 3350 255.00, 510.00 g
 Autorizado por Secretaría de Salud el 8-dic-2011 vigencia 09-nov-2015 INFORMACIÓN PARA PRESCRIBIR AMPLIA 1. Nombre Comercial: CONTUMAX 2. Nombre Genérico MACROGOL 3350 3. Forma Farmacéutica y Formulación:
Autorizado por Secretaría de Salud el 8-dic-2011 vigencia 09-nov-2015 INFORMACIÓN PARA PRESCRIBIR AMPLIA 1. Nombre Comercial: CONTUMAX 2. Nombre Genérico MACROGOL 3350 3. Forma Farmacéutica y Formulación:
HIDROMORFONA NAPP 4 mg, 8 mg, 16 mg, 24 mg, cápsulas de liberación modificada.
 1. DENOMINACIÓN DEL PRODUCTO HIDROMORFONA NAPP 4 mg, 8 mg, 16 mg, 24 mg, cápsulas de liberación modificada. 2. COMPOSICION CUALITATIVA Y CUANTITATIVA Las cápsulas contienen clorhidrato de hidromorfona
1. DENOMINACIÓN DEL PRODUCTO HIDROMORFONA NAPP 4 mg, 8 mg, 16 mg, 24 mg, cápsulas de liberación modificada. 2. COMPOSICION CUALITATIVA Y CUANTITATIVA Las cápsulas contienen clorhidrato de hidromorfona
PEDRO MESA RODRIGUEZ (Tutor: Dra Avellaneda) Dosis inicial 4-6h 30mg/ 6h v.o. Normal 5h Retard 14-24h
 ESCALERA ANALGÉSICA DE LA OMS 1º ESCALON 2º ESCALON 3º ESCALON Dolor leve Dolor moderado Dolor intenso Opioides potentes +/- coanalgésicos Opioides débiles +/- coanalgésicos ASCENSOR ANALGÉSICO Ascensor
ESCALERA ANALGÉSICA DE LA OMS 1º ESCALON 2º ESCALON 3º ESCALON Dolor leve Dolor moderado Dolor intenso Opioides potentes +/- coanalgésicos Opioides débiles +/- coanalgésicos ASCENSOR ANALGÉSICO Ascensor
LEXATUSSIN Dextrometorfano Bromhidrato 15 mg / 5 ml Jarabe
 LEXATUSSIN Dextrometorfano Bromhidrato 15 mg / 5 ml Jarabe LEXATUSSIN (Dextrometorfano Bromhidrato 15 mg/5 ml) Jarabe COMPOSICIÓN: Cada 100 ml de Jarabe contiene: Dextrometorfano Bromhidrato monohidrato...
LEXATUSSIN Dextrometorfano Bromhidrato 15 mg / 5 ml Jarabe LEXATUSSIN (Dextrometorfano Bromhidrato 15 mg/5 ml) Jarabe COMPOSICIÓN: Cada 100 ml de Jarabe contiene: Dextrometorfano Bromhidrato monohidrato...
FICHA TÉCNICA. Acetilcisteína NORMON 100 mg granulado para solución oral EFG. Acetilcisteína NORMON 200 mg granulado para solución oral EFG.
 FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Acetilcisteína NORMON 100 mg granulado para solución oral EFG. Acetilcisteína NORMON 200 mg granulado para solución oral EFG. 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Acetilcisteína NORMON 100 mg granulado para solución oral EFG. Acetilcisteína NORMON 200 mg granulado para solución oral EFG. 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA
Conciliación de medicación. Amparo Serrano Fabiá. 02/04/2008
 Conciliación de medicación Amparo Serrano Fabiá. 02/04/2008 Introducción El aumento de la esperanza de vida y la aparición de nuevos fármacos para el tratamiento de patologías crónicas ha hecho que aumente
Conciliación de medicación Amparo Serrano Fabiá. 02/04/2008 Introducción El aumento de la esperanza de vida y la aparición de nuevos fármacos para el tratamiento de patologías crónicas ha hecho que aumente
RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO. PRILBEN VET 20 mg COMPRIMIDO RECUBIERTO CON PELÍCULA PARA PERROS
 RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1. DENOMINACIÓN DEL MEDICAMENTO VETERINARIO PRILBEN VET 20 mg COMPRIMIDO RECUBIERTO CON PELÍCULA PARA PERROS 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada comprimido
RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1. DENOMINACIÓN DEL MEDICAMENTO VETERINARIO PRILBEN VET 20 mg COMPRIMIDO RECUBIERTO CON PELÍCULA PARA PERROS 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada comprimido
DOLOR POSTQUIRURGICO
 DOLOR POSTQUIRURGICO Por Qué tratar el Dolor? Porque es lo mas humano, la obligación moral del médico es aliviar el sufrimiento. Existen otras razones, disminuye la ansiedad del paciente y sus familiares,
DOLOR POSTQUIRURGICO Por Qué tratar el Dolor? Porque es lo mas humano, la obligación moral del médico es aliviar el sufrimiento. Existen otras razones, disminuye la ansiedad del paciente y sus familiares,
EBASTINA STADA 10 mg comprimidos recubiertos con película EFG EBASTINA STADA 20 mg comprimidos recubiertos con película EFG
 1. NOMBRE DEL MEDICAMENTO EBASTINA STADA 10 mg comprimidos recubiertos con película EFG EBASTINA STADA 20 mg comprimidos recubiertos con película EFG 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada comprimido
1. NOMBRE DEL MEDICAMENTO EBASTINA STADA 10 mg comprimidos recubiertos con película EFG EBASTINA STADA 20 mg comprimidos recubiertos con película EFG 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada comprimido
Centro Andaluz de Documentación e Información de Medicamentos (CADIME) Informes de Evaluación de Medicamentos. Tapentadol INFORME (8)
 Tapentadol Centro Andaluz de Documentación e Información de Medicamentos (CADIME) Informes de Evaluación de Medicamentos Tapentadol INFORME (8) 2012 [Escribir el título del documento] [Año] TAPENTADOL
Tapentadol Centro Andaluz de Documentación e Información de Medicamentos (CADIME) Informes de Evaluación de Medicamentos Tapentadol INFORME (8) 2012 [Escribir el título del documento] [Año] TAPENTADOL
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO. TRAMADOL ASTA Medica Gotas EFG. 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA
 FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO TRAMADOL ASTA Medica Gotas EFG. 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Composición cualitativa y cuantitativa Tramadol (DOE) clorhidrato, 100 mg 3. FORMA FARMACÉUTICA
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO TRAMADOL ASTA Medica Gotas EFG. 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Composición cualitativa y cuantitativa Tramadol (DOE) clorhidrato, 100 mg 3. FORMA FARMACÉUTICA
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO. DENUBIL 250 mg/180 mg solución oral. 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA
 FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO DENUBIL 250 mg/180 mg solución oral. 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Composición por ampolla (de 5 ml de solución oral): Pidolato de deanol 250 mg Heptaminol,
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO DENUBIL 250 mg/180 mg solución oral. 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Composición por ampolla (de 5 ml de solución oral): Pidolato de deanol 250 mg Heptaminol,
Tratamiento sintomático de la tos improductiva en adultos y niños mayores de 2 años.
 FLUDAN CODEINA 1. NOMBRE DEL MEDICAMENTO Fludan Codeina 10 mg/ 5 ml solución oral. 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada 5 ml de solución contienen 10 mg de fosfato de codeína. Excipientes con
FLUDAN CODEINA 1. NOMBRE DEL MEDICAMENTO Fludan Codeina 10 mg/ 5 ml solución oral. 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada 5 ml de solución contienen 10 mg de fosfato de codeína. Excipientes con
MINOXIDIL AL 2%, SOLUCIÓN DE. Excipientes: Propilenglicol Agua purificada Etanol 96 %
 FN/2006/PO/039 1. NOMBRE: Solución de minoxidil 2. SINÓNIMOS Minoxidil en solución hidroalcohólica MINOXIDIL AL 2%, SOLUCIÓN DE 3. COMPOSICIÓN 3.1. FÓRMULA PATRÓN ( 2 % ) Minoxidil Excipientes: Propilenglicol
FN/2006/PO/039 1. NOMBRE: Solución de minoxidil 2. SINÓNIMOS Minoxidil en solución hidroalcohólica MINOXIDIL AL 2%, SOLUCIÓN DE 3. COMPOSICIÓN 3.1. FÓRMULA PATRÓN ( 2 % ) Minoxidil Excipientes: Propilenglicol
Nuria Romero Laorden. Growing Up 14 de Febrero de 2012
 Nuria Romero Laorden R4 Oncología Médica HUFA Growing Up 14 de Febrero de 2012 1. Morfina 2. Oi Oxicodona 3. Fentanilo 4. Buprenorfina 5. Hidromorfona 6. Metadona OPIÁCEO: Sustancias que se extraen de
Nuria Romero Laorden R4 Oncología Médica HUFA Growing Up 14 de Febrero de 2012 1. Morfina 2. Oi Oxicodona 3. Fentanilo 4. Buprenorfina 5. Hidromorfona 6. Metadona OPIÁCEO: Sustancias que se extraen de
Niños entre 2 y 7 años: La posología media recomendada es de 300 mg de acetilcisteína al día por vía oral. En 3 tomas de 100 mg cada 8 horas.
 1. NOMBRE DEL MEDICAMENTO acetilcisteína cinfa 100 mg polvo para solución oral EFG acetilcisteína cinfa 200 mg polvo para solución oral EFG acetilcisteína cinfa 600 mg polvo para solución oral EFG 2. COMPOSICIÓN
1. NOMBRE DEL MEDICAMENTO acetilcisteína cinfa 100 mg polvo para solución oral EFG acetilcisteína cinfa 200 mg polvo para solución oral EFG acetilcisteína cinfa 600 mg polvo para solución oral EFG 2. COMPOSICIÓN
Losartán Potásico...50 mg. Excipientes...c.s.
 LOSARTÁN POTÁSICO 50 mg Comprimidos Recubiertos Vía de Administración: Oral FÓRMULA Cada comprimido recubierto de ACCORD contiene: Losartán Potásico...50 mg Excipientes...c.s. Justificación Accord comprimidos
LOSARTÁN POTÁSICO 50 mg Comprimidos Recubiertos Vía de Administración: Oral FÓRMULA Cada comprimido recubierto de ACCORD contiene: Losartán Potásico...50 mg Excipientes...c.s. Justificación Accord comprimidos
Para la lista completa de excipientes, véase la sección 6.1.
 1. DENOMINACIÓN DEL MEDICAMENTO VETERINARIO Metacam 1 mg comprimidos masticables para perros Metacam 2,5 mg comprimidos masticables para perros 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Un comprimido masticable
1. DENOMINACIÓN DEL MEDICAMENTO VETERINARIO Metacam 1 mg comprimidos masticables para perros Metacam 2,5 mg comprimidos masticables para perros 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Un comprimido masticable
FICHA TÉCNICA. Cada pastilla para chupar contiene 20 mg de ambroxol hidrocloruro.
 FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Bucoxon 20 mg pastillas para chupar sabor menta 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada pastilla para chupar contiene 20 mg de ambroxol hidrocloruro. Excipiente
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Bucoxon 20 mg pastillas para chupar sabor menta 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada pastilla para chupar contiene 20 mg de ambroxol hidrocloruro. Excipiente
FICHA DE INFORMACIÓN AL PACIENTE: DIHIDROCODEÍNA
 FICHA DE INFORMACIÓN AL PACIENTE: DIHIDROCODEÍNA 1.- QUÉ ES Y PARA QUE SE UTILIZA 1.1 Acción: Analgésico opiáceo narcótico. Antitusígeno. 1.2 Cómo actúa este fármaco: La dihidrocodeína se une a unos receptores
FICHA DE INFORMACIÓN AL PACIENTE: DIHIDROCODEÍNA 1.- QUÉ ES Y PARA QUE SE UTILIZA 1.1 Acción: Analgésico opiáceo narcótico. Antitusígeno. 1.2 Cómo actúa este fármaco: La dihidrocodeína se une a unos receptores
Prospecto: información para el paciente. Lomper 100 mg comprimidos Mebendazol
 Prospecto: información para el paciente Lomper 100 mg comprimidos Mebendazol Lea todo el prospecto detenidamente antes de empezar a tomar este medicamento, porque contiene información importante para usted.
Prospecto: información para el paciente Lomper 100 mg comprimidos Mebendazol Lea todo el prospecto detenidamente antes de empezar a tomar este medicamento, porque contiene información importante para usted.
Principios activos Eficacia Seguridad Conveniencia Niveles 1 Paracetamol +++ +++ +++ 1-2-3. 2 Ibuprofeno +++ ++ ++ 1-2-3
 Título: DOLOR Codificación CIE 10 R52.0 dolor agudo R52.1 dolor crónico intratable R52.9 dolor, no especificado Problema: El dolor es un signo y un síntoma, una experiencia anormal sensorial producida
Título: DOLOR Codificación CIE 10 R52.0 dolor agudo R52.1 dolor crónico intratable R52.9 dolor, no especificado Problema: El dolor es un signo y un síntoma, una experiencia anormal sensorial producida
THIPENTHAL. TIOPENTAL SÓDICO 1 g INYECTABLE. VENTA BAJO RECETA ARCHIVADA (Lista III) FÓRMULA CUALI Y CUANTITATIVA. Cada frasco ampolla contiene:
 THIPENTHAL TIOPENTALSÓDICO1g INYECTABLE VENTABAJORECETAARCHIVADA(ListaIII) FÓRMULACUALIYCUANTITATIVA Cadafrascoampollacontiene: Tiopentalsódicoestéril 1g ACCIÓNTERAPÉUTICA: Anestésicogeneral,barbitúrico.CódigoATC:N01AF03.
THIPENTHAL TIOPENTALSÓDICO1g INYECTABLE VENTABAJORECETAARCHIVADA(ListaIII) FÓRMULACUALIYCUANTITATIVA Cadafrascoampollacontiene: Tiopentalsódicoestéril 1g ACCIÓNTERAPÉUTICA: Anestésicogeneral,barbitúrico.CódigoATC:N01AF03.
ARIPIPRAZOL En adolescentes contrastorno Bipolar I
 ARIPIPRAZOL En adolescentes contrastorno Bipolar I Información para profesionales sanitarios Preguntas frecuentes Disponible en la web de la AEMPS www.aemps.gob.es Información sobre prevención de riesgos
ARIPIPRAZOL En adolescentes contrastorno Bipolar I Información para profesionales sanitarios Preguntas frecuentes Disponible en la web de la AEMPS www.aemps.gob.es Información sobre prevención de riesgos
Historia de los problemas de salud del paciente
 Colegio de Farmacéuticos de la Provincia de Buenos Aires Calle 5 Nº 966 - (1900) - La Plata - Telefax: (0221) 429-0900 (Líneas Rotativas) e-mail:farmaceuticos@colfarma.org.ar Historia de los problemas
Colegio de Farmacéuticos de la Provincia de Buenos Aires Calle 5 Nº 966 - (1900) - La Plata - Telefax: (0221) 429-0900 (Líneas Rotativas) e-mail:farmaceuticos@colfarma.org.ar Historia de los problemas
FICHA TÉCNICA O RESUMEN DE LAS CARACTERISTICAS DEL PRODUCTO
 FICHA TÉCNICA O RESUMEN DE LAS CARACTERISTICAS DEL PRODUCTO Hodernal 800 mg/ml solución oral Parafina líquida 1. NOMBRE DEL MEDICAMENTO Hodernal 800 mg/ml solución oral. 2. COMPOSICIÓN CUANTITATIVA Y CUALITATIVA
FICHA TÉCNICA O RESUMEN DE LAS CARACTERISTICAS DEL PRODUCTO Hodernal 800 mg/ml solución oral Parafina líquida 1. NOMBRE DEL MEDICAMENTO Hodernal 800 mg/ml solución oral. 2. COMPOSICIÓN CUANTITATIVA Y CUALITATIVA
1. NOMBRE DEL MEDICAMENTO DICLOFENACO RETARD JUVENTUS 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA. Composición por cápsula:
 1. NOMBRE DEL MEDICAMENTO DICLOFENACO RETARD JUVENTUS 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Composición por cápsula: Principio activo Diclofenaco (DCI) sódico Excipientes Sucrosa Almidón de maíz Ácido
1. NOMBRE DEL MEDICAMENTO DICLOFENACO RETARD JUVENTUS 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Composición por cápsula: Principio activo Diclofenaco (DCI) sódico Excipientes Sucrosa Almidón de maíz Ácido
TALLER VIA SUBCUTANEA. Elena Álvarez Alonso, DUE, Asistencial AP
 TALLER VIA SUBCUTANEA Elena Álvarez Alonso, DUE, Asistencial AP VIA SUBCUTANEA Vía de elección cuando la vía oral es impracticable. La administración subcutánea permite controlar la mayor parte de los
TALLER VIA SUBCUTANEA Elena Álvarez Alonso, DUE, Asistencial AP VIA SUBCUTANEA Vía de elección cuando la vía oral es impracticable. La administración subcutánea permite controlar la mayor parte de los
FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO
 FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1. NOMBRE DEL MEDICAMENTO Ginkokán 40 mg comprimidos Extracto de Ginkgo biloba EGb 761 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada comprimido
FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1. NOMBRE DEL MEDICAMENTO Ginkokán 40 mg comprimidos Extracto de Ginkgo biloba EGb 761 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada comprimido
RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO. Sustancia activa: Cabergolina... 50 µg. Excipiente, c.s.p... 1 ml
 RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1. DENOMINACIÓN DEL MEDICAMENTO VETERINARIO LACTOFIN, 50 mcg/ml solución oral para perros y gatos 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Sustancia activa:
RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1. DENOMINACIÓN DEL MEDICAMENTO VETERINARIO LACTOFIN, 50 mcg/ml solución oral para perros y gatos 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Sustancia activa:
ELABORACIÓN DE SOLUCION DE PROPANOLOL 1 mg/ml Fórmula Propanolol. 100 mg Agua conservans.20 ml Ácido cítrico 25 % 0,4 ml Jarabe simple c.s.
 ELABORACIÓN DE SOLUCION DE PROPANOLOL 1 mg/ml Fórmula Propanolol. 100 mg Agua conservans.20 ml Ácido cítrico 25 % 0,4 ml Jarabe simple c.s.p 100 ml Método específico 1.- Pesar (PN/L/OF/001/00) la cantidad
ELABORACIÓN DE SOLUCION DE PROPANOLOL 1 mg/ml Fórmula Propanolol. 100 mg Agua conservans.20 ml Ácido cítrico 25 % 0,4 ml Jarabe simple c.s.p 100 ml Método específico 1.- Pesar (PN/L/OF/001/00) la cantidad
MANEJO DE OPIOIDES INDICE
 MANEJO DE OPIOIDES INDICE A. INDICE... 1 B. INTRODUCCION... 2 OBJETIVO DEL TTO DEL DOLOR... 2 MÁS EMPLEO MÁS TOXICIDAD... 2 C. POSIBLES EFECTOS ADVERSOS DE LOS OPIOIDES... 2 1. NEUROTOXICIDAD INDUCIDA
MANEJO DE OPIOIDES INDICE A. INDICE... 1 B. INTRODUCCION... 2 OBJETIVO DEL TTO DEL DOLOR... 2 MÁS EMPLEO MÁS TOXICIDAD... 2 C. POSIBLES EFECTOS ADVERSOS DE LOS OPIOIDES... 2 1. NEUROTOXICIDAD INDUCIDA
PROSPECTO. NOVARTIS FARMACEUTICA, S.A. Ronda Santa Maria, 158. Barbera del Valles 08210 (Barcelona) España
 PROSPECTO Lea todo el prospecto detenidamente antes de que a usted o a su hijo le sea administrado Lioresal por vía intratecal, ya que contiene información importante. Conserve este prospecto. Puede tener
PROSPECTO Lea todo el prospecto detenidamente antes de que a usted o a su hijo le sea administrado Lioresal por vía intratecal, ya que contiene información importante. Conserve este prospecto. Puede tener
FICHA TECNICA LABORATORIO QUÍMICO FARMACÉUTICO INDUSTRIAL DELTA S.A. versión - 1.0. 2013
 FICHA TECNICA LABORATORIO QUÍMICO FARMACÉUTICO INDUSTRIAL DELTA S.A. versión - 1.0. 2013 DELTAGEL COMPRIMIDOS MASTICABLES ANTIÁCIDO Página 1 DELTAGEL Comprimidos Masticables Principio Activo Hidróxido
FICHA TECNICA LABORATORIO QUÍMICO FARMACÉUTICO INDUSTRIAL DELTA S.A. versión - 1.0. 2013 DELTAGEL COMPRIMIDOS MASTICABLES ANTIÁCIDO Página 1 DELTAGEL Comprimidos Masticables Principio Activo Hidróxido
RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO
 RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1. NOMBRE DEL MEDICAMENTO Mupirocina ISDIN 20 mg/g pomada 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada gramo de pomada contiene 20 mg de mupirocina. Para consultar
RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1. NOMBRE DEL MEDICAMENTO Mupirocina ISDIN 20 mg/g pomada 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada gramo de pomada contiene 20 mg de mupirocina. Para consultar
RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO SUPRALER. desloratadina. Jarabe
 Nombre del producto: RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO SUPRALER (desloratadina) Forma farmacéutica: Fortaleza: Jarabe 2,5mg/5 ml Presentación: Estuche por un frasco de vidrio ámbar con 50 ó 100
Nombre del producto: RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO SUPRALER (desloratadina) Forma farmacéutica: Fortaleza: Jarabe 2,5mg/5 ml Presentación: Estuche por un frasco de vidrio ámbar con 50 ó 100
Tratamiento del dolor neuropático e inflamatorio en neuralgias y dorsalgias
 Tratamiento del dolor neuropático e inflamatorio en neuralgias y dorsalgias Atención Farmacéutica Sistema Nervioso El dolor neuropático ocasiona un deterioro significativo de la calidad de vida de las
Tratamiento del dolor neuropático e inflamatorio en neuralgias y dorsalgias Atención Farmacéutica Sistema Nervioso El dolor neuropático ocasiona un deterioro significativo de la calidad de vida de las
PROSPECTO : INFORMACIÓN PARA EL USUARIO MOSEGOR 0,5 mg/10 ml solución oral Pizotifeno
 PROSPECTO PROSPECTO : INFORMACIÓN PARA EL USUARIO MOSEGOR 0,5 mg/10 ml solución oral Pizotifeno Lea todo el prospecto detenidamente antes de empezar a tomar este medicamento porque contiene información
PROSPECTO PROSPECTO : INFORMACIÓN PARA EL USUARIO MOSEGOR 0,5 mg/10 ml solución oral Pizotifeno Lea todo el prospecto detenidamente antes de empezar a tomar este medicamento porque contiene información
TODO SOBRE EL DOLOR. www.almirall.com. Soluciones pensando en ti
 TODO SOBRE EL DOLOR www.almirall.com Soluciones pensando en ti QUÉ ES? El dolor se describe como una experiencia sensorial y emocional desagradable asociada a un estímulo dañino. En las personas que sufren
TODO SOBRE EL DOLOR www.almirall.com Soluciones pensando en ti QUÉ ES? El dolor se describe como una experiencia sensorial y emocional desagradable asociada a un estímulo dañino. En las personas que sufren
FICHA TÉCNICA. Excipientes: Lactosa: 90,40 mg Carboximetilalmidón sódico (tipo A) de patata sin gluten: 3,80 mg
 FICHA TÉCNICA 1.NOMBRE DEL MEDICAMENTO DALPARAN 10 mg comprimidos recubiertos con película 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada comprimido recubierto con película contiene: zolpidem tartrato,
FICHA TÉCNICA 1.NOMBRE DEL MEDICAMENTO DALPARAN 10 mg comprimidos recubiertos con película 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada comprimido recubierto con película contiene: zolpidem tartrato,
COLERETICO INYECTABLE
 Reg. SAGARPA Q-784-41 D I G E S T I V O COLERETICO INYECTABLE mecanismo de acció n RESTABLECE LAS FUNCIONES DIGESTIVAS Aumenta las secreciones gástricas y pancreáticas Produce un efecto colerético y colagogo
Reg. SAGARPA Q-784-41 D I G E S T I V O COLERETICO INYECTABLE mecanismo de acció n RESTABLECE LAS FUNCIONES DIGESTIVAS Aumenta las secreciones gástricas y pancreáticas Produce un efecto colerético y colagogo
25/09/2015 ENFERMEDAD DE ALZHEIMER... ENFERMEDAD DE ALZHEIMER. DEFINICIÓN: Es un trastorno neurodegenerativo,
 ENFERMEDAD DE ALZHEIMER DEFINICIÓN: Es un trastorno neurodegenerativo, progresivo, que se asocia con una alteración global de las funciones mentales superiores y cuyo síntoma principal es la pérdida de
ENFERMEDAD DE ALZHEIMER DEFINICIÓN: Es un trastorno neurodegenerativo, progresivo, que se asocia con una alteración global de las funciones mentales superiores y cuyo síntoma principal es la pérdida de
BREAKYL PELÍCULA BUCAL (CITRATO DE FENTANILO)
 BREAKYL PELÍCULA BUCAL (CITRATO DE FENTANILO) Información importante sobre seguridad dirigida a profesionales sanitarios Información sobre prevención de riesgos autorizada por la Agencia Española de Medicamentos
BREAKYL PELÍCULA BUCAL (CITRATO DE FENTANILO) Información importante sobre seguridad dirigida a profesionales sanitarios Información sobre prevención de riesgos autorizada por la Agencia Española de Medicamentos
FICHA TÉCNICA. Cada comprimido contiene 28,7 mg de fosfato de codeína hemihidrato (28 mg de fosfato de codeína) equivalente a 21,4 mg de codeina
 FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Codeisan 28,7 mg comprimidos 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada comprimido contiene 28,7 mg de fosfato de codeína hemihidrato (28 mg de fosfato de codeína)
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Codeisan 28,7 mg comprimidos 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada comprimido contiene 28,7 mg de fosfato de codeína hemihidrato (28 mg de fosfato de codeína)
Causas, incidencia y factores de riesgo
 www.alcoholinformate.org.mx Estado de abstinencia alcohólica ESTADOS UNIDOS La abstinencia alcohólica se refiere a los síntomas que se pueden presentar cuando una persona suspende en forma repentina el
www.alcoholinformate.org.mx Estado de abstinencia alcohólica ESTADOS UNIDOS La abstinencia alcohólica se refiere a los síntomas que se pueden presentar cuando una persona suspende en forma repentina el
FICHA TÉCNICA. La utilización del carbón activado no exime de la utilización de tratamientos sintomáticos y específicos.
 FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO CARBOLIQ 200 mg/ml suspensión oral 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Contenido por cada ml de suspensión: Carbón activado.... 200 mg Excipientes con efecto
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO CARBOLIQ 200 mg/ml suspensión oral 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Contenido por cada ml de suspensión: Carbón activado.... 200 mg Excipientes con efecto
ITRASKIN Suspensión Oral
 ITRASKIN Suspensión Oral ANTIFÚNGICO. Itraskin, suspensión oral, está indicado para el tratamiento de infecciones fúngicas causadas por microorganismos susceptibles al Itraconazol, tales como dermatofitosis
ITRASKIN Suspensión Oral ANTIFÚNGICO. Itraskin, suspensión oral, está indicado para el tratamiento de infecciones fúngicas causadas por microorganismos susceptibles al Itraconazol, tales como dermatofitosis
Ranitidina (DCI) (hidrocloruro)... 75 mg
 1. NOMBRE DEL MEDICAMENTO ranitidina cinfa 75 mg 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Por cada comprimido recubierto: Ranitidina (DCI) (hidrocloruro)... 75 mg 3. FORMA FARMACÉUTICA Comprimidos recubiertos.
1. NOMBRE DEL MEDICAMENTO ranitidina cinfa 75 mg 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Por cada comprimido recubierto: Ranitidina (DCI) (hidrocloruro)... 75 mg 3. FORMA FARMACÉUTICA Comprimidos recubiertos.
PROSPECTO: INFORMACIÓN PARA EL USUARIO. Evacuol 7,5 mg/ml Gotas orales en solución Picosulfato de sodio
 PROSPECTO: INFORMACIÓN PARA EL USUARIO Evacuol 7,5 mg/ml Gotas orales en solución Picosulfato de sodio Lea todo el prospecto detenidamente porque contiene información importante para usted. - Este medicamento
PROSPECTO: INFORMACIÓN PARA EL USUARIO Evacuol 7,5 mg/ml Gotas orales en solución Picosulfato de sodio Lea todo el prospecto detenidamente porque contiene información importante para usted. - Este medicamento
FICHA TECNICA LABORATORIO QUÍMICO FARMACÉUTICO INDUSTRIAL DELTA S.A. versión - 1.0. 2013
 FICHA TECNICA LABORATORIO QUÍMICO FARMACÉUTICO INDUSTRIAL DELTA S.A. versión - 1.0. 2013 INDOMETACINA 25 mg COMPRIMIDOS RECUBIERTOS ANTIINFLAMATORIO ANTIRREUMÁTICO Página 1 INDOMETACINA 25 mg Comprimidos
FICHA TECNICA LABORATORIO QUÍMICO FARMACÉUTICO INDUSTRIAL DELTA S.A. versión - 1.0. 2013 INDOMETACINA 25 mg COMPRIMIDOS RECUBIERTOS ANTIINFLAMATORIO ANTIRREUMÁTICO Página 1 INDOMETACINA 25 mg Comprimidos
FICHA TÉCNICA O RESUMEN DE LAS CARACTERISTÍCAS DEL PRODUCTO
 FICHA TÉCNICA O RESUMEN DE LAS CARACTERISTÍCAS DEL PRODUCTO 1. NOMBRE DEL MEDICAMENTO AGUA DEL CARMEN solución oral 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Contenido por unidad de toma (cucharadita de
FICHA TÉCNICA O RESUMEN DE LAS CARACTERISTÍCAS DEL PRODUCTO 1. NOMBRE DEL MEDICAMENTO AGUA DEL CARMEN solución oral 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Contenido por unidad de toma (cucharadita de
PROSPECTO: INFORMACIÓN PARA EL USUARIO. Sulfato de Magnesio GENFARMA 150 mg/ml solución inyectable y para perfusión EFG
 PROSPECTO: INFORMACIÓN PARA EL USUARIO Sulfato de Magnesio GENFARMA 150 mg/ml solución inyectable y para perfusión EFG Lea todo el prospecto detenidamente antes de empezar a usar este medicamento, porque
PROSPECTO: INFORMACIÓN PARA EL USUARIO Sulfato de Magnesio GENFARMA 150 mg/ml solución inyectable y para perfusión EFG Lea todo el prospecto detenidamente antes de empezar a usar este medicamento, porque
Utilización de pregabalina en neuralgia postherpética refractaria a terapia convencional
 NOTA CLÍNICA 377 Rev. Soc. Esp. Dolor 6: 377-381; 2008 Utilización de pregabalina en neuralgia postherpética refractaria a terapia convencional M. Garví 1, V. L. Villanueva 2, J. M. Asensio 2, J. A. De
NOTA CLÍNICA 377 Rev. Soc. Esp. Dolor 6: 377-381; 2008 Utilización de pregabalina en neuralgia postherpética refractaria a terapia convencional M. Garví 1, V. L. Villanueva 2, J. M. Asensio 2, J. A. De
FICHA TÉCNICA. Cada sobre de Movicol Sabor Neutro contiene los siguientes principios activos:
 FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Movicol Sabor Neutro 13,7 g, polvo para solución oral en sobre 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA 2.2 Composición cualitativa y cuantitativa Cada sobre de
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Movicol Sabor Neutro 13,7 g, polvo para solución oral en sobre 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA 2.2 Composición cualitativa y cuantitativa Cada sobre de
Lección 34. Fármacos Antiasmáticos y Broncodilatadores UNIDAD VIII: ALTERACIONES RESPIRATORIAS
 UNIDAD VIII: ALTERACIONES RESPIRATORIAS Lección 34 Fármacos Antiasmáticos y Broncodilatadores Guión Ricardo Brage e Isabel Trapero - Lección 34 1. VÍA DE ADMINISTRACIÓN INHALATORIA 2. FÁRMACOS EMPLEADOS
UNIDAD VIII: ALTERACIONES RESPIRATORIAS Lección 34 Fármacos Antiasmáticos y Broncodilatadores Guión Ricardo Brage e Isabel Trapero - Lección 34 1. VÍA DE ADMINISTRACIÓN INHALATORIA 2. FÁRMACOS EMPLEADOS
Terapia sustitutiva con nicotina (TSN)
 Jornadas sobre Tabaquismo y entorno laboral Terapia sustitutiva con nicotina (TSN) Adriana Jiménez-Muro Franco Unidad de Tabaquismo Facultad de Medicina Universidad de Zaragoza Colegio Oficial de Médicos
Jornadas sobre Tabaquismo y entorno laboral Terapia sustitutiva con nicotina (TSN) Adriana Jiménez-Muro Franco Unidad de Tabaquismo Facultad de Medicina Universidad de Zaragoza Colegio Oficial de Médicos
1. NOMBRE DEL MEDICAMENTO Bicalutamida Bluefish 50 mg comprimidos recubiertos con película EFG
 1. NOMBRE DEL MEDICAMENTO Bicalutamida Bluefish 50 mg comprimidos recubiertos con película EFG 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada comprimido recubierto con película contiene 50 mg de bicalutamida.
1. NOMBRE DEL MEDICAMENTO Bicalutamida Bluefish 50 mg comprimidos recubiertos con película EFG 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada comprimido recubierto con película contiene 50 mg de bicalutamida.
Prospecto: información para el usuario. Toseina 2 mg/ml solución oral Codeína fosfato hemihidrato
 Prospecto: información para el usuario Toseina 2 mg/ml solución oral Codeína fosfato hemihidrato Lea todo el prospecto detenidamente antes de empezar a tomar este medicamento, porque contiene información
Prospecto: información para el usuario Toseina 2 mg/ml solución oral Codeína fosfato hemihidrato Lea todo el prospecto detenidamente antes de empezar a tomar este medicamento, porque contiene información
MOSEGOR. Solución clara o un poco opalescente, de color ligeramente amarillento.
 MOSEGOR 1. NOMBRE DEL MEDICAMENTO Mosegor 0,5 mg/10 ml solución oral 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA 2.1 Descripción general Solución clara o un poco opalescente, de color ligeramente amarillento.
MOSEGOR 1. NOMBRE DEL MEDICAMENTO Mosegor 0,5 mg/10 ml solución oral 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA 2.1 Descripción general Solución clara o un poco opalescente, de color ligeramente amarillento.
Tratamiento del dolor oncológico
 Miguel Angel Benítez-Rosario [Buscar autor en Medline] Tratamiento del dolor oncológico Ver resúmen y puntos clave Texto completo Ver texto completo Volver al sumario Aspectos Generales del Tratamiento
Miguel Angel Benítez-Rosario [Buscar autor en Medline] Tratamiento del dolor oncológico Ver resúmen y puntos clave Texto completo Ver texto completo Volver al sumario Aspectos Generales del Tratamiento
1. QUÉ ES loperamida cinfa 2 mg cápsulas duras Y PARA QUÉ SE UTILIZA
 Lea todo el prospecto detenidamente porque contiene información importante para usted. Este medicamento puede obtenerse sin receta, para el tratamiento de afecciones menores sin la intervención de un médico.
Lea todo el prospecto detenidamente porque contiene información importante para usted. Este medicamento puede obtenerse sin receta, para el tratamiento de afecciones menores sin la intervención de un médico.
Prospecto: información para el usuario. Morfina B. Braun 10 mg/ml solución inyectable Hidrocloruro de morfina
 Prospecto: información para el usuario Morfina B. Braun 10 mg/ml solución inyectable Hidrocloruro de morfina Lea todo el prospecto detenidamente antes de empezar a usar el medicamento, porque contiene
Prospecto: información para el usuario Morfina B. Braun 10 mg/ml solución inyectable Hidrocloruro de morfina Lea todo el prospecto detenidamente antes de empezar a usar el medicamento, porque contiene
INFORME DE EVALUACIÓN. RISEDRONATO (nueva presentación) 75 mg 2 comp consecutivos/mes
 COMITÉ DE EVALUACIÓN DE NUEVOS MEDICAMENTOS DE EUSKADI INFORME DE EVALUACIÓN Principio activo: Nombre Comercial y presentaciones: RISEDRONATO (nueva presentación) 75 mg 2 comp consecutivos/mes ACTONEL
COMITÉ DE EVALUACIÓN DE NUEVOS MEDICAMENTOS DE EUSKADI INFORME DE EVALUACIÓN Principio activo: Nombre Comercial y presentaciones: RISEDRONATO (nueva presentación) 75 mg 2 comp consecutivos/mes ACTONEL
Prospecto: Información para el usuario Loperan 2 mg cápsulas duras Loperamida, hidrocloruro
 Prospecto: Información para el usuario Loperan 2 mg cápsulas duras Loperamida, hidrocloruro Lea todo el prospecto detenidamente antes de empezar a tomar este medicamento, porque contiene información importante
Prospecto: Información para el usuario Loperan 2 mg cápsulas duras Loperamida, hidrocloruro Lea todo el prospecto detenidamente antes de empezar a tomar este medicamento, porque contiene información importante
FICHA TECNICA PROPUESTA 1.- NOMBRE DEL MEDICAMENTO GLUTAFERRO GOTAS
 FICHA TECNICA PROPUESTA 1.- NOMBRE DEL MEDICAMENTO GLUTAFERRO GOTAS 2.- COMPOSICION CUALITATIVA Y CUANTITATIVA Cada ml contiene: Ferroglicina sulfato.170 mg (equivalentes a 30 mg de Fe 2+ ). Excipientes,
FICHA TECNICA PROPUESTA 1.- NOMBRE DEL MEDICAMENTO GLUTAFERRO GOTAS 2.- COMPOSICION CUALITATIVA Y CUANTITATIVA Cada ml contiene: Ferroglicina sulfato.170 mg (equivalentes a 30 mg de Fe 2+ ). Excipientes,
