La estructura del átomo
|
|
|
- José Ignacio de la Cruz Moya
- hace 7 años
- Vistas:
Transcripción
1 SECCIÓN 3.2 La estructura del átomo La teoría atómica propuesta por John Dalton establecía que los átomos eran indivisibles. Hacia fines del siglo xix, se comprobó que esa idea era incorrecta. Se hizo evidente que los átomos en realidad están formados por varios tipos básicos de partículas. El número y la distribución de esas partículas determinan las propiedades del átomo. En la actualidad, el átomo se define como la partícula más pequeña de un elemento que conserva las propiedades químicas de ese elemento. Los átomos están formados por dos regiones. En cada región, hay diferentes tipos de partículas, denominadas partículas subatómicas. átomo Términos clave fuerzas nucleares El núcleo es una región muy pequeña ubicada en el centro del átomo. El núcleo contiene al menos una partícula con carga positiva denominada protón y normalmente una o más partículas neutras denominadas neutrones. Alrededor del núcleo se halla una región mucho más grande que contiene partículas con carga negativa denominadas electrones. 1. Dibuja un modelo que muestre las dos regiones de un átomo en el espacio de abajo. Rotula el núcleo y la región de los electrones. Los átomos contienen partículas positivas y negativas. El electrón fue la primera partícula subatómica que se descubrió. Hacia fines del siglo xix, se hicieron muchos experimentos en los que se hacía pasar corriente eléctrica a través de diversos gases. Los gases que tienen la misma presión que el aire de la superficie de la Tierra son malos conductores de la electricidad. Por esta razón, los científicos se aseguraron de que la presión de los gases de sus experimentos se mantuviera muy baja. Para realizar los experimentos, los científicos construyeron tubos de vidrio denominados tubos de rayos catódicos y los llenaron de gas a baja presión. En cada extremo del tubo se colocaron discos de metal, se dio carga positiva a un disco, el cátodo, y carga negativa al otro disco, el ánodo. 68 CAPÍTULO 3
2 Los rayos catódicos y los electrones Los científicos descubrieron que la superficie de un tubo de rayos catódicos resplandecía cuando se hacía pasar corriente eléctrica a través del tubo. Entonces plantearon la hipótesis de que el resplandor se producía debido a una corriente de partículas, denominada rayo catódico, que se desplazaba desde el cátodo hacia el ánodo. También descubrieron que los rayos catódicos podían desviarse por efecto de un imán o podían alejarse de un objeto con carga negativa. Esto dio origen a la hipótesis de que las partículas de un rayo catódico tienen carga negativa. Gas a baja presión - Cátodo (disco de metal) (a) Fuente de voltaje Rayo catódico + Ánodo (disco de metal) Los experimentos que realizó el físico inglés Joseph John Thomson en 1897 apoyaron esa hipótesis. Thomson logró calcular la razón entre la carga de las partículas y la masa de las partículas de un rayo catódico. Descubrió que esa razón era la misma, independientemente de los metales que se usaran en el cátodo y el ánodo. La razón también seguía siendo la misma si cambiaba el gas del tubo. Cátodo Ánodo Thomson llegó a la conclusión de que todos los rayos catódicos están formados por partículas idénticas con carga negativa denominadas electrones. Los átomos de los experimentos con rayos catódicos que se mencionan en esta página liberaban electrones. Eso demostró que los átomos son divisibles y que los electrones están presentes en diferentes tipos de átomos. (b) (a) Un tubo de rayos catódicos simple. (b) Un imán colocado encima del tubo de rayos catódicos desvía el rayo hacia abajo, lo que demuestra que las partículas del rayo tienen carga negativa. La carga y la masa de un electrón Los experimentos de Thomson también revelaron que el electrón presenta una razón de carga a masa muy alta. En 1909, el físico estadounidense Robert A. Millikan logró medir la carga del electrón. Los científicos usaron esa información para determinar la masa de un electrón. Descubrieron que la masa de un electrón representa aproximadamente dos milésimos de la masa del átomo más pequeño que se conozca. Thomson propuso un modelo de budín de pasas para explicar las propiedades del átomo que se conocían en esa época. Como los átomos son eléctricamente neutros, Thomson propuso la idea de que los electrones estaban equilibrados mediante un budín de carga positiva. Los electrones estaban metidos en ese material de carga positiva. También se creía que la región de carga positiva contenía la mayor parte de la masa del átomo, puesto que el electrón tiene muy poca masa. CONEXIÓN En la actualidad, los experimentos han determinado que el electrón tiene una masa de kg. Esto es 1/1837 de la masa del tipo más pequeño de átomo de hidrógeno. 2. Haz un dibujo del modelo de budín de pasas que propuso Thomson. Rotula los electrones y la región de carga positiva. ÁTOMOS: LOS COMPONENTES BÁSICOS DE LA MATERIA 69
3 Pantalla que detecta partículas desviadas Lámina de oro delgada (a) Caja de plomo que contiene una fuente radiactiva de partículas que se mueven rápidamente (b) Partículas desviadas por la lámina Los átomos tienen un núcleo pequeño, denso y con carga positiva. El neozelandés Ernest Rutherford y sus colaboradores Hans Geiger y Ernest Marsden descubrieron más detalles sobre la estructura de los átomos. Dispararon un rayo de partículas alfa sobre una lámina de oro. Las partículas alfa eran partículas que se movían a gran velocidad, tenían carga positiva y su masa era cuatro veces mayor que la de un átomo de hidrógeno. Rutherford y sus colaboradores esperaban que el rayo atravesara la lámina con una mínima desviación puesto que la masa y la carga estaban distribuidas equitativamente sobre la lámina de oro. Pero se sorprendieron cuando aproximadamente 1 de cada 8000 partículas se desvió en dirección opuesta, hacia la fuente. La hipótesis que planteó Rutherford fue que la desviación en dirección opuesta se debía a la presencia de pequeños y densos paquetes de materia con carga positiva. Esos paquetes debían de ser pequeños porque muy pocas partículas se desviaban en dirección opuesta. Rutherford usó el término núcleo para describir cada uno de esos paquetes de materia. Rutherford había descubierto que el volumen del núcleo era muy pequeño en comparación con el volumen total de un átomo. Se había descubierto la fuente de la carga positiva de un átomo. Tiempo después, Niels Bohr, un estudiante de Rutherford, descubrió la ubicación de los electrones en un átomo. Rayo de partículas positivas Desviación leve Núcleo Desviación mayor (a) Geiger y Marsden dispararon un rayo de partículas alfa sobre una lámina de oro delgada. (b) Algunas partículas se desviaron en dirección opuesta, hacia su fuente. Electrones que rodean el núcleo 3. Qué es el núcleo de un átomo? La mayoría de las partículas atravesaron la lámina de oro sin dificultades. Una pequeña cantidad se desvió debido al núcleo. 70 CAPÍTULO 3
4 Un núcleo contiene protones y neutrones. Con una excepción, todos los núcleos atómicos están formados por dos tipos de partículas: protones y neutrones. Un protón tiene una carga positiva de una magnitud igual a la de la carga negativa de un electrón. Los átomos son eléctricamente neutros porque contienen el mismo número de protones y de electrones. Un neutrón no tiene carga y, como sucede con el átomo, es eléctricamente neutro. El único núcleo atómico que carece de neutrón es el del átomo de hidrógeno más simple. Su núcleo es un solo protón con un solo electrón que se mueve alrededor. La masa de un protón, kg, es 1836 veces mayor que la masa de un electrón. Por lo tanto, un protón representa casi toda la masa del átomo de hidrógeno más simple. La masa de un neutrón, kg, es levemente mayor que la masa de un protón. DATO Muchas palabras del español y del inglés tienen su origen en el latín. Por ejemplo, la palabra núcleo proviene del latín nucleus, que significa centro y se usa para nombrar el centro de un átomo o de una célula. En inglés se usa el mismo término que en latín: nucleus. Otra palabra proveniente del latín es radio (radius), y en inglés también se usa el mismo término que en latín (radius). ÚTIL CONSEJOS El núcleo de los átomos de distintos elementos tiene diferentes números de protones. Por lo tanto, el número de protones determina la identidad de un átomo. Por cada protón que hay en el núcleo de un átomo, el mismo número de electrones rodea al núcleo. Los físicos han descubierto otras partículas subatómicas, pero esas partículas afectan muy poco a las propiedades químicas de la materia. Las propiedades de los electrones, los protones y los neutrones se resumen en la tabla de abajo. 4. Qué cantidad sirve para determinar la identidad de un átomo? Propiedades de las partículas subatómicas Partícula Símbolos Carga eléctrica relativa Número de masa Masa relativa (u*) Masa real (kg) Electrón e, 0 1 e Protón p +, 1 1 H Neutrón n, 1 0 n *1 u (unidad de masa atómica unificada) = k g ÁTOMOS: LOS COMPONENTES BÁSICOS DE LA MATERIA 71
5 Las fuerzas del núcleo Generalmente, las partículas que tienen la misma carga eléctrica se repelen. Por lo tanto, un núcleo que contenga más de un protón debería ser inestable. Sin embargo, existe una fuerza entre dos protones que supera a la fuerza eléctrica que intenta alejarlos. Esa fuerza solo actúa cuando dos protones están muy cerca uno del otro. Una fuerza similar actúa cuando dos neutrones están muy cerca uno del otro, o cuando un neutrón y un protón están muy cerca uno del otro. Juntas, las fuerzas de corto alcance que mantienen unidos a protones y protones, neutrones y neutrones, y protones y neutrones se denominan fuerzas nucleares. Esas fuerzas permiten que los átomos que tienen hasta 83 protones con carga positiva en el mismo núcleo sean estables. CONEXIÓN En física, se conocen cuatro fuerzas fundamentales que describen cómo interactúa la materia. Estas fuerzas son la fuerza electromagnética, la fuerza gravitatoria, la fuerza nuclear fuerte y la fuerza nuclear débil. El radio de los átomos se expresa en picómetros. Como el núcleo es tan pequeño, el tamaño de un átomo se determina por el tamaño de la región en la que se encuentran los electrones. Esa región suele describirse como una nube de electrones, es decir, una nube de carga negativa. El radio de un átomo es la distancia que existe desde el centro del núcleo hasta el límite exterior de la nube de electrones. Como los radios atómicos son tan pequeños, para expresarlos se usa una unidad más adecuada para el tamaño de los átomos, llamada picómetro. Otra unidad, llamada unidad de masa atómica unificada, o u, se usa para expresar la masa de los átomos. 1 pm = m = cm 1 u = kg Para tener una idea de lo pequeña que es la medida de un picómetro, piensa que 1 cm representa la misma parte fraccionaria con respecto a 1000 km (aproximadamente 600 mi) que 100 pm con respecto a 1 cm. Los radios atómicos miden entre 40 pm y 270 pm. Los núcleos atómicos tienen un radio mucho más pequeño, aproximadamente pm. Los núcleos atómicos también son increíblemente densos. Su densidad es aproximadamente g/cm 3. Razonamiento crítico 5. Calcular Verifica el valor de la densidad de un núcleo atómico dado en esta página para un átomo esférico que tiene una masa de 1 u. Recuerda que el volumen de una esfera se obtiene mediante la fórmula V = 3 4 π r CAPÍTULO 3
6 REPASO DE LA SECCIÓN 3.2 VOCABULARIO 1. Escribe la definición de los siguientes términos: a. átomo b. neutrón REPASO 2. Describe una conclusión sacada por cada científico que haya contribuido al desarrollo de la teoría atómica actual. a. Thomson b. Millikan c. Rutherford 3. Compara las tres partículas subatómicas según la ubicación en el átomo, la masa y la carga relativa. 4. Por qué el tubo de rayos catódicos que se muestra en esta sección está conectado a una bomba de vacío? Razonamiento crítico 5. EVALUAR IDEAS Se dice que las fuerzas nucleares mantienen unidos a los protones y a los neutrones. Qué característica de la composición del núcleo hace que sea necesario el concepto de fuerzas nucleares? ÁTOMOS: LOS COMPONENTES BÁSICOS DE LA MATERIA 73
Tema 9 Naturaleza eléctrica de la materia
 Tema 9 Naturaleza eléctrica de la materia 1.- El átomo Toda materia está formada por partículas como éstas llamadas átomos. Un átomo a su vez está compuesto por pequeños elementos, llamados partículas
Tema 9 Naturaleza eléctrica de la materia 1.- El átomo Toda materia está formada por partículas como éstas llamadas átomos. Un átomo a su vez está compuesto por pequeños elementos, llamados partículas
Estructura de los átomos.
 Estructura de los átomos. Teoría atomística de Demócrito: Átomo, del griego: que no se puede cortar. Demócrito, filósofo griego (s. IV a.c.): Si dividimos la materia de forma sucesiva llegará un momento
Estructura de los átomos. Teoría atomística de Demócrito: Átomo, del griego: que no se puede cortar. Demócrito, filósofo griego (s. IV a.c.): Si dividimos la materia de forma sucesiva llegará un momento
quimica2univia.wordpress.com www.youtube.com/watch?v=6-jfwqiv-q0
 quimica2univia.wordpress.com www.youtube.com/watch?v=6-jfwqiv-q0 Átomo definición 1 En física y química, átomo (del latín atomus, y éste del griego άτομος, indivisible) es la unidad más pequeña de un elemento
quimica2univia.wordpress.com www.youtube.com/watch?v=6-jfwqiv-q0 Átomo definición 1 En física y química, átomo (del latín atomus, y éste del griego άτομος, indivisible) es la unidad más pequeña de un elemento
EL INTERIOR DE LA MATERIA. De qué está hecha la materia?
 EL INTERIOR DE LA MATERIA De qué está hecha la materia? Esta cuestión ha preocupado a los seres humanos desde los tiempos más remotos. Algunas de las ideas propuestas a lo largo de la historia, más o menos
EL INTERIOR DE LA MATERIA De qué está hecha la materia? Esta cuestión ha preocupado a los seres humanos desde los tiempos más remotos. Algunas de las ideas propuestas a lo largo de la historia, más o menos
GUÍA DE TRABAJO: TEORÍA ATÓMICA. I_ Haciendo uso de tu libro y cuaderno responde las siguientes preguntas:
 GUÍA DE TRABAJO: TEORÍA ATÓMICA I_ Haciendo uso de tu libro y cuaderno responde las siguientes preguntas: 1_ Dibuja el modelo atómico de: _ Thomson _ Rutherford 2_ Nombra las diferencias que observas entre
GUÍA DE TRABAJO: TEORÍA ATÓMICA I_ Haciendo uso de tu libro y cuaderno responde las siguientes preguntas: 1_ Dibuja el modelo atómico de: _ Thomson _ Rutherford 2_ Nombra las diferencias que observas entre
TEORÍA ATÓMICA: Objetivos: -Describir los distintos modelos atómicos -Definir términos usados en la teoría atómica
 SUBSECTOR PROFESOR NIVEL AÑO UNIDAD SEMESTRE Química Paulina Gómez Octavo básico 2016 Teoría atómica, estructura del átomo Primero GUIA DE ESTUDIO N 1 MODELOS ATÓMICOS DALTON, THOMSON, RUTHERFORD Nombre
SUBSECTOR PROFESOR NIVEL AÑO UNIDAD SEMESTRE Química Paulina Gómez Octavo básico 2016 Teoría atómica, estructura del átomo Primero GUIA DE ESTUDIO N 1 MODELOS ATÓMICOS DALTON, THOMSON, RUTHERFORD Nombre
1. Cuál de los siguientes enunciados es uno de los postulados correspondientes al modelo atómico de Bohr?
 Programa Estándar Anual Nº Guía práctica: Teoría atómica I: modelos atómicos, estructura atómica y tipos de átomos Ejercicios PSU 1. Cuál de los siguientes enunciados es uno de los postulados correspondientes
Programa Estándar Anual Nº Guía práctica: Teoría atómica I: modelos atómicos, estructura atómica y tipos de átomos Ejercicios PSU 1. Cuál de los siguientes enunciados es uno de los postulados correspondientes
EL ÁTOMO. Se supuso que estas partículas deberían estar en todos los átomos. Thomson las llamó electrones.
 ANTECEDENTES HISTÓRICOS. () EL ÁTOMO Leucipo y Demócrito. Proponen la Discontinuidad de la materia. Dalton. Formula la primera Teoría atómica. Volta, Davy, Faraday, Berzelius, descubren la Naturaleza eléctrica
ANTECEDENTES HISTÓRICOS. () EL ÁTOMO Leucipo y Demócrito. Proponen la Discontinuidad de la materia. Dalton. Formula la primera Teoría atómica. Volta, Davy, Faraday, Berzelius, descubren la Naturaleza eléctrica
UNIDAD DIDÁCTICA 2: ESTRUCTURA DE LA MATERIA
 UNIDAD DIDÁCTICA 2: ESTRUCTURA DE LA MATERIA 1. Qué explica el modelo atómico de Dalton? a) La materia está constituida por átomos b) Los átomos tienen un núcleo muy pequeño donde se concentra casi toda
UNIDAD DIDÁCTICA 2: ESTRUCTURA DE LA MATERIA 1. Qué explica el modelo atómico de Dalton? a) La materia está constituida por átomos b) Los átomos tienen un núcleo muy pequeño donde se concentra casi toda
Mundo Atómico. Profesor: Robinson Pino H.
 Mundo Atómico Profesor: Robinson Pino H. 1 ÁTOMO En el siglo V a.c., el filósofo griego Demócrito expresó la idea de que toda la materia estaba formada por partículas muy pequeñas e indivisibles a las
Mundo Atómico Profesor: Robinson Pino H. 1 ÁTOMO En el siglo V a.c., el filósofo griego Demócrito expresó la idea de que toda la materia estaba formada por partículas muy pequeñas e indivisibles a las
QUÍMICA 3ºESO ACT TEMA 4. EL ÁTOMO. 1. UN ÁTOMO MUY ANTIGUO.
 TEMA 4. EL ÁTOMO. 1. UN ÁTOMO MUY ANTIGUO. En el siglo V a.c., Leucipo ya decía que había un solo tipo de materia. Pensaba, además que si dividíamos la materia en partes cada vez más pequeñas encontraríamos
TEMA 4. EL ÁTOMO. 1. UN ÁTOMO MUY ANTIGUO. En el siglo V a.c., Leucipo ya decía que había un solo tipo de materia. Pensaba, además que si dividíamos la materia en partes cada vez más pequeñas encontraríamos
ESTRUCTURA ATÓMICA I. MODELOS ATÓMICOS.
 ESTRUCTURA ATÓMICA I. MODELOS ATÓMICOS. 1. MODELOS ATÓMICOS. 2. PARTÍCULAS CONSTITUYENTES DEL ÁTOMO. 3. MODELO ATÓMICO DE BOHR. 4. ACTIVIDADES. 1. MODELOS ATÓMICOS. La idea de la existencia de los átomos
ESTRUCTURA ATÓMICA I. MODELOS ATÓMICOS. 1. MODELOS ATÓMICOS. 2. PARTÍCULAS CONSTITUYENTES DEL ÁTOMO. 3. MODELO ATÓMICO DE BOHR. 4. ACTIVIDADES. 1. MODELOS ATÓMICOS. La idea de la existencia de los átomos
EVOLUCIÓN HISTÓRICA DE LOS MODELOS ATÓMICOS.
 Mapa conceptual. EVOLUCIÓN HISTÓRICA DE LOS MODELOS ATÓMICOS. AUTOR DALTON (1808) THOMSON (1900) RUTHERFORD (1911) HECHOS EN LOS QUE SE BASÓ. Ley de conservación de la masa en las reacciones químicas (Lavoisier,
Mapa conceptual. EVOLUCIÓN HISTÓRICA DE LOS MODELOS ATÓMICOS. AUTOR DALTON (1808) THOMSON (1900) RUTHERFORD (1911) HECHOS EN LOS QUE SE BASÓ. Ley de conservación de la masa en las reacciones químicas (Lavoisier,
El átomo a través de la historia
 I.MUNICIPALIDAD DE PROVIDENCIA CORPORACIÓN DE DESARROLLO SOCIAL LICEO POLIVALENTE ARTURO ALESSANDRI PALMA DEPARTAMENTO DE QUÍMICA MARTA HERMOSILLA ARCE GUIA DE ESTUDIO OCTAVO BÁSICO QUÍMICA HISTORIA DEL
I.MUNICIPALIDAD DE PROVIDENCIA CORPORACIÓN DE DESARROLLO SOCIAL LICEO POLIVALENTE ARTURO ALESSANDRI PALMA DEPARTAMENTO DE QUÍMICA MARTA HERMOSILLA ARCE GUIA DE ESTUDIO OCTAVO BÁSICO QUÍMICA HISTORIA DEL
Ejercicios y respuestas del apartado: Teoría atómica. Z, A, isótopos, n, p, e-. Iones
 Ejercicios y respuestas del apartado: Teoría atómica. Z, A, isótopos, n, p, e-. Iones Teorías atómicas 1. Qué explica el modelo atómico de Dalton? a) La materia está constituida por átomos b) Los átomos
Ejercicios y respuestas del apartado: Teoría atómica. Z, A, isótopos, n, p, e-. Iones Teorías atómicas 1. Qué explica el modelo atómico de Dalton? a) La materia está constituida por átomos b) Los átomos
Átomos Repaso Química
 Átomos Repaso Química I. SELECCIÓN MÚLTIPLE. ESCOGE LA MEJOR CONTESTACIÓN. 1. La materia está compuesta de: (a) masa. (b) átomos. (c) volumen. 2. Parte más pequeña que retiene las características de un
Átomos Repaso Química I. SELECCIÓN MÚLTIPLE. ESCOGE LA MEJOR CONTESTACIÓN. 1. La materia está compuesta de: (a) masa. (b) átomos. (c) volumen. 2. Parte más pequeña que retiene las características de un
Modelos atómicos: Dalton, Thomson, Rutherford, Bohr y Mecánica Cuántica. Clasificación de los elementos y propiedades periódicas
 Modelos atómicos: Dalton, Thomson, Rutherford, Bohr y Mecánica Cuántica Clasificación de los elementos y propiedades periódicas Modelos atómicos: Átomo de Dalton NOMBRE EN QUÉ CONSISTE QUÉ EXPLICA QUÉ
Modelos atómicos: Dalton, Thomson, Rutherford, Bohr y Mecánica Cuántica Clasificación de los elementos y propiedades periódicas Modelos atómicos: Átomo de Dalton NOMBRE EN QUÉ CONSISTE QUÉ EXPLICA QUÉ
27. (b) 28. (a) 29. (b) 30. (c) 31. (a) 32. (c) 33. (d) 34. (d) 35. (b) 36. (a) 37. (b) 38. (d) 39. (c) TEMA 4
 grado de pulverización de la muestra 62. Se dice que dos líquidos son inmiscibles entre sí, cuando: a) se disuelven el uno en el otro b) no se disuelven el uno en el otro c) las partículas que forman los
grado de pulverización de la muestra 62. Se dice que dos líquidos son inmiscibles entre sí, cuando: a) se disuelven el uno en el otro b) no se disuelven el uno en el otro c) las partículas que forman los
RESUMEN DE LOS APORTES DE LOS CIENTÍFICOS AL MODELO ACTUAL
 Demócrito: El átomo es indivisible. DALTON Para Dalton los átomos eran esferas macizas. atómica: teoría se puede resumir en: Estableció la teoría 1.- Los elementos químicos están formados por partículas
Demócrito: El átomo es indivisible. DALTON Para Dalton los átomos eran esferas macizas. atómica: teoría se puede resumir en: Estableció la teoría 1.- Los elementos químicos están formados por partículas
Liceo 1 Javiera Carrera Dpto. Biología Prof. Danilo Parra l. Nivel Octavo Básico. Aprendizajes Esperados
 Liceo 1 Javiera Carrera Dpto. Biología Prof. Danilo Parra l. Nivel Octavo Básico INSTRUCCIONES: este tema no fue tratado en clases presenciales, por lo tanto, lean y desarrollen esta guía que será parte
Liceo 1 Javiera Carrera Dpto. Biología Prof. Danilo Parra l. Nivel Octavo Básico INSTRUCCIONES: este tema no fue tratado en clases presenciales, por lo tanto, lean y desarrollen esta guía que será parte
PROTONES Y ELECTRONES
 reflexiona Imagina que tienes un tazón de naranjas, plátanos, piñas, bayas, peras y sandía. Cómo identificas cada trozo de fruta? Es muy probable que estés familiarizado con las características de cada
reflexiona Imagina que tienes un tazón de naranjas, plátanos, piñas, bayas, peras y sandía. Cómo identificas cada trozo de fruta? Es muy probable que estés familiarizado con las características de cada
EL ÁTOMO. Contenidos (1)
 EL ÁTOMO 2 Contenidos (1) 1.- Antecedentes históricos. 2.- Partículas subatómicas. 3.- Modelo atómico de Thomsom. 4.- Los rayos X. 5.- La radiactividad. 6.- Modelo atómico de Rutherford. 1 3 Contenidos
EL ÁTOMO 2 Contenidos (1) 1.- Antecedentes históricos. 2.- Partículas subatómicas. 3.- Modelo atómico de Thomsom. 4.- Los rayos X. 5.- La radiactividad. 6.- Modelo atómico de Rutherford. 1 3 Contenidos
NOMBRE: CURSO: HOJAS DE ACTIVIDADES FÍSICA Y QUÍMICA 3º DE ESO
 NOMBRE: URSO: HOJAS DE ATIVIDADES FÍSIA Y QUÍMIA 3º DE ESO Tema 4 EL ÁTOMO Los trozos de una piedra partida en dos, incluso reducida a polvo, siguen siendo piedra, y cada uno de los fragmentos resultantes
NOMBRE: URSO: HOJAS DE ATIVIDADES FÍSIA Y QUÍMIA 3º DE ESO Tema 4 EL ÁTOMO Los trozos de una piedra partida en dos, incluso reducida a polvo, siguen siendo piedra, y cada uno de los fragmentos resultantes
Los números indican los niveles de energía. 2s 2p Las letras la forma del orbital. 3s 3p 3d 4s 4p 4d 4f 5s 5p 5d 5f 6s 6p 6d 7s 7p
 1s Los números indican los niveles de energía. 2s 2p Las letras la forma del orbital. 3s 3p 3d 4s 4p 4d 4f 5s 5p 5d 5f 6s 6p 6d 7s 7p Diagrama de orbitales: Consiste en dibujar los orbitales como cuadrados
1s Los números indican los niveles de energía. 2s 2p Las letras la forma del orbital. 3s 3p 3d 4s 4p 4d 4f 5s 5p 5d 5f 6s 6p 6d 7s 7p Diagrama de orbitales: Consiste en dibujar los orbitales como cuadrados
E L E C T R I C I D A D. Acción de un Campo Magnético sobre una Corriente. Acción de un Campo Magnético sobre una Corriente
 E L E C T R I C I D A D Acción de un Campo Magnético sobre una Corriente Acción de un Campo Magnético sobre una Corriente E L E C T R I C I D A D Una partícula cargada que se mueve en presencia de un campo
E L E C T R I C I D A D Acción de un Campo Magnético sobre una Corriente Acción de un Campo Magnético sobre una Corriente E L E C T R I C I D A D Una partícula cargada que se mueve en presencia de un campo
ISÓTOPOS, NÚMEROS ATÓMICOS Y NÚMEROS DE MASA
 El átomo nuclear Modelo del átomo de J.J. Thompson (antes de 1900) El átomo consiste de una esfera de carga positiva que tiene sepultados electrones con carga negativa. A este modelo se le conoce como
El átomo nuclear Modelo del átomo de J.J. Thompson (antes de 1900) El átomo consiste de una esfera de carga positiva que tiene sepultados electrones con carga negativa. A este modelo se le conoce como
INTRODUCCIÓN A RADIACTIVIDAD
 INTRODUCCIÓN A RADIACTIVIDAD Que es un átomo? Qué partículas se encuentran en el átomo? En que zonas? Es la unidad más pequeña de un elemento químico que no es posible dividir mediante procesos químicos.
INTRODUCCIÓN A RADIACTIVIDAD Que es un átomo? Qué partículas se encuentran en el átomo? En que zonas? Es la unidad más pequeña de un elemento químico que no es posible dividir mediante procesos químicos.
El átomo. Índice. 2. Modelos prenucleares. Contenidos. 1.1. Modelos atómicos. 2.1. Modelo atómico de Dalton
 5 El átomo Contenidos Índice 1 2 3 4 Estructura interna del átomo: modelos atómicos Modelos prenucleares Modelos nucleares Átomos y elementos 1. Estructura interna del átomo: modelos atómicos Los fenómenos
5 El átomo Contenidos Índice 1 2 3 4 Estructura interna del átomo: modelos atómicos Modelos prenucleares Modelos nucleares Átomos y elementos 1. Estructura interna del átomo: modelos atómicos Los fenómenos
NATURALEZA ELECTRICA DE LA MATERIA Y EL ATOMO
 NATURALEZA ELECTRICA DE LA MATERIA Y EL ATOMO PARTÍCULAS SUBATÓMICAS Y MODELOS ATÓMICOS MODELO ATÓMICO DE THOMSON Al final del s. XIX los experimentos realizados sobre la conducción de la electricidad
NATURALEZA ELECTRICA DE LA MATERIA Y EL ATOMO PARTÍCULAS SUBATÓMICAS Y MODELOS ATÓMICOS MODELO ATÓMICO DE THOMSON Al final del s. XIX los experimentos realizados sobre la conducción de la electricidad
Guía 2. Actividad 3 Trabajo extra clase. Determinar y comprender las partículas subatómicas mediante ejercicios prácticos.
 Guía 2 Actividad 3 Trabajo extra clase Objetivo: Docente: Javier Alexander Prada Comas Determinar y comprender las partículas subatómicas mediante ejercicios prácticos. Marco teórico Qué es átomo? Es la
Guía 2 Actividad 3 Trabajo extra clase Objetivo: Docente: Javier Alexander Prada Comas Determinar y comprender las partículas subatómicas mediante ejercicios prácticos. Marco teórico Qué es átomo? Es la
Todo lo que puedas imaginar está compuesto por átomos.
 Todo lo que puedas imaginar está compuesto por átomos. El átomo es la partícula más pequeña de un elemento químico (materia formada por átomos iguales) y posee las características del mismo. Cuando se
Todo lo que puedas imaginar está compuesto por átomos. El átomo es la partícula más pequeña de un elemento químico (materia formada por átomos iguales) y posee las características del mismo. Cuando se
Trataba de explicar las leyes de la época sobre la composición de las sustancias (leyes ponderales). La materia está constituida por unidades de
 EL ÁTOMO Configuración Cómo está formada la materia en su interior? Desde los tiempos de la antigua Grecia,los pensadores venían haciéndose esta pregunta, acerca de cómo estaba constituida id la materia
EL ÁTOMO Configuración Cómo está formada la materia en su interior? Desde los tiempos de la antigua Grecia,los pensadores venían haciéndose esta pregunta, acerca de cómo estaba constituida id la materia
TEMA 1: ORIGENES DE LA TEORIA CUANTICA DEL ATOMO
 TEMA 1: ORIGENES DE LA TEORIA CUANTICA DEL ATOMO Antecedentes Kanada, filosofo hindú ( V a.c.) materia discontinua, partículas eternas, muy pequeñas y en continuo movimiento. Leucipo, filosofo jónico (
TEMA 1: ORIGENES DE LA TEORIA CUANTICA DEL ATOMO Antecedentes Kanada, filosofo hindú ( V a.c.) materia discontinua, partículas eternas, muy pequeñas y en continuo movimiento. Leucipo, filosofo jónico (
Colegio Santa Gema Galgani
 Física: 4 Medio Guía de Estudio F4.6 Unidad 6: Modelos Atómicos Profesor: Juan Pedraza MODELOS ATOMICOS Desde la antigüedad se discutía sobre la composición de la materia y las partículas que la conforman.
Física: 4 Medio Guía de Estudio F4.6 Unidad 6: Modelos Atómicos Profesor: Juan Pedraza MODELOS ATOMICOS Desde la antigüedad se discutía sobre la composición de la materia y las partículas que la conforman.
IES Menéndez Tolosa Dpto. Física y Química 4º ESO - Modelos atómicos 1S
 IES Menéndez Tolosa Dpto. Física y Química 4º ESO - Modelos atómicos 1S 1 Escribe tres isótopos de oxígeno que tengan, y 10 neutrones. Cuál de ellos tendrá mayor Z? 16 17 1 O, O, O Todos ellos tienen el
IES Menéndez Tolosa Dpto. Física y Química 4º ESO - Modelos atómicos 1S 1 Escribe tres isótopos de oxígeno que tengan, y 10 neutrones. Cuál de ellos tendrá mayor Z? 16 17 1 O, O, O Todos ellos tienen el
1. Teoría atómica de Dalton
 1. Teoría atómica de Dalton Tipos de sustancias Las sustancias puras ( una única sustancia!) pueden ser simples o compuestas. Sustancia simple: a partir de ella no se pueden obtener otras más sencillas.
1. Teoría atómica de Dalton Tipos de sustancias Las sustancias puras ( una única sustancia!) pueden ser simples o compuestas. Sustancia simple: a partir de ella no se pueden obtener otras más sencillas.
ETIMOLOGÍA DEL ÁTOMO. A = Sin Tomo = División TEORÍAS Y MODELOS ATÓMICOS
 ETIMOLOGÍA DEL ÁTOMO A = Sin Tomo = División TEORÍAS Y MODELOS ATÓMICOS 1. TEORÍA GRIEGA: En Grecia los pensadores filósofos por año 460 a. C. fueron los primeros en hablar que todos los cuerpos estaban
ETIMOLOGÍA DEL ÁTOMO A = Sin Tomo = División TEORÍAS Y MODELOS ATÓMICOS 1. TEORÍA GRIEGA: En Grecia los pensadores filósofos por año 460 a. C. fueron los primeros en hablar que todos los cuerpos estaban
ESTRUCTURA DEL ÁTOMO SISTEMA PERIÓDICO. TEMA 2 Pág. 228 libro (Unidad 11)
 ESTRUCTURA DEL ÁTOMO SISTEMA PERIÓDICO TEMA 2 Pág. 228 libro (Unidad 11) PÁGS. 234-235 MAGNITUDES ATÓMICAS. REPASO MAGNITUDES ATÓMICAS. Conceptos clave - Repaso NÚMERO ATÓMICO (Z) Es el número de protones
ESTRUCTURA DEL ÁTOMO SISTEMA PERIÓDICO TEMA 2 Pág. 228 libro (Unidad 11) PÁGS. 234-235 MAGNITUDES ATÓMICAS. REPASO MAGNITUDES ATÓMICAS. Conceptos clave - Repaso NÚMERO ATÓMICO (Z) Es el número de protones
De qué se Compone la Materia?
 8vo Básico> Ciencias Naturales Composición de la materia De qué se Compone la Materia? Observa la siguiente situación y responde las preguntas propuestas: La profesora comienza su clase y pregunta: Profesora:
8vo Básico> Ciencias Naturales Composición de la materia De qué se Compone la Materia? Observa la siguiente situación y responde las preguntas propuestas: La profesora comienza su clase y pregunta: Profesora:
ESTRUCTURA DEL ATOMO
 ESTRUCTURA ATÓMICA ESTRUCTURA DEL ATOMO PROTONES NUCLEO NEUTRONES ELECTRONES Los electrones giran alrededor del núcleo en regiones del espacio denominadas órbitas. Los átomos grandes albergan a varias
ESTRUCTURA ATÓMICA ESTRUCTURA DEL ATOMO PROTONES NUCLEO NEUTRONES ELECTRONES Los electrones giran alrededor del núcleo en regiones del espacio denominadas órbitas. Los átomos grandes albergan a varias
INSTITUCION EDUCATIVA LA PRESENTACION
 INSTITUCION EDUCATIVA LA PRESENTACION NOMBRE ALUMNA: AREA : CIENCIAS NATURALES Y EDUCACION AMBIENTAL ASIGNATURA: QUIMICA DOCENTE: OSCAR GIRALDO HERNANDEZ TIPO DE GUIA: CONCEPTUAL - EJERCITACION PERIODO
INSTITUCION EDUCATIVA LA PRESENTACION NOMBRE ALUMNA: AREA : CIENCIAS NATURALES Y EDUCACION AMBIENTAL ASIGNATURA: QUIMICA DOCENTE: OSCAR GIRALDO HERNANDEZ TIPO DE GUIA: CONCEPTUAL - EJERCITACION PERIODO
(Demócrito, Siglo V a.c.) elementos
 El Átomo En la filosofía de la antigua Grecia la palabra átomo se empleaba para referirse a la parte más pequeña de materia que podía concebirse y era considerada indestructible. (Demócrito, Siglo V a.c.)
El Átomo En la filosofía de la antigua Grecia la palabra átomo se empleaba para referirse a la parte más pequeña de materia que podía concebirse y era considerada indestructible. (Demócrito, Siglo V a.c.)
Preguntas de Multiopción
 Física Nuclear & Reacciones Nucleares Problemas de Practica AP Física B de PSI 1. El núcleo atómico se compone de: (A) electrones (B) protones (C) protones y electrones (D) protones y neutrones (E) neutrones
Física Nuclear & Reacciones Nucleares Problemas de Practica AP Física B de PSI 1. El núcleo atómico se compone de: (A) electrones (B) protones (C) protones y electrones (D) protones y neutrones (E) neutrones
ACTIVIDADES 3º E.S.O. Tema 4.- La estructura de la materia. Agrupaciones de átomos
 ACTIVIDADES 3º E.S.O. Tema 4.- La estructura de la materia. Agrupaciones de átomos Pág. 74 3. Responde a las siguientes cuestiones basándote en la teoría atómica de Dalton: a) Pueden dos elementos distintos
ACTIVIDADES 3º E.S.O. Tema 4.- La estructura de la materia. Agrupaciones de átomos Pág. 74 3. Responde a las siguientes cuestiones basándote en la teoría atómica de Dalton: a) Pueden dos elementos distintos
El átomo. Aristóteles (384-322 a.c) Demócrito (460-370 a.c)
 El átomo Demócrito (460-370 a.c) En la antigua Grecia dos concepciones compitieron por dar una interpretación racional a cómo estaba formada la materia. Demócrito consideraba que la materia estaba formada
El átomo Demócrito (460-370 a.c) En la antigua Grecia dos concepciones compitieron por dar una interpretación racional a cómo estaba formada la materia. Demócrito consideraba que la materia estaba formada
FÍSICA Y QUÍMICA TEMA 4: LOS ÁTOMOS Y SU COMPLEJIDAD
 Física y Química 3º Curso Educación Secundaria Obligatoria Curso académico 2015/2016 1 FÍSICA Y QUÍMICA TEMA 4: LOS ÁTOMOS Y SU COMPLEJIDAD Física y Química 3º Curso Educación Secundaria Obligatoria Curso
Física y Química 3º Curso Educación Secundaria Obligatoria Curso académico 2015/2016 1 FÍSICA Y QUÍMICA TEMA 4: LOS ÁTOMOS Y SU COMPLEJIDAD Física y Química 3º Curso Educación Secundaria Obligatoria Curso
INSTITUCION EDUCATIVA LA PRESENTACION NOMBRE DE LA ALUMNA: CIENCIAS NATURALES Y EDUCACION AMBIENTAL ASIGNATURA: CIENCIAS NATURALES NOTA:
 INSTITUCION EDUCATIVA LA PRESENTACION NOMBRE DE LA ALUMNA: AREA : CIENCIAS NATURALES Y EDUCACION AMBIENTAL ASIGNATURA: CIENCIAS NATURALES NOTA: DOCENTE: JOSÉ ROMÁN TIPO DE GUIA: CONCEPTUAL - EJERCITACION.
INSTITUCION EDUCATIVA LA PRESENTACION NOMBRE DE LA ALUMNA: AREA : CIENCIAS NATURALES Y EDUCACION AMBIENTAL ASIGNATURA: CIENCIAS NATURALES NOTA: DOCENTE: JOSÉ ROMÁN TIPO DE GUIA: CONCEPTUAL - EJERCITACION.
UNIDAD 5: LOS ÁTOMOS Y LAS MOLÉCULAS
 UNIDAD 5: LOS ÁTOMOS Y LAS MOLÉCULAS Lee atentamente: 1. LA MISMA SUSTANCIA EN LOS TRES ESTADOS Todos los cuerpos están formados por sustancias: las personas, los coches, los muebles, el aire, etc. Todas
UNIDAD 5: LOS ÁTOMOS Y LAS MOLÉCULAS Lee atentamente: 1. LA MISMA SUSTANCIA EN LOS TRES ESTADOS Todos los cuerpos están formados por sustancias: las personas, los coches, los muebles, el aire, etc. Todas
B. Cuál es su número atómico y másico? Di cuántos protones y neutrones hay en el núcleo y electrones en la corteza.
 Problema nº 0 Los isótopos del boro se representan así: B 5 5 B. Cuál es su número atómico másico? Di cuántos protones neutrones ha en el núcleo electrones en la corteza. El número atómico es Z = 5, el
Problema nº 0 Los isótopos del boro se representan así: B 5 5 B. Cuál es su número atómico másico? Di cuántos protones neutrones ha en el núcleo electrones en la corteza. El número atómico es Z = 5, el
Módulo 1: Electrostática Fuerza eléctrica
 Módulo 1: Electrostática Fuerza eléctrica 1 Cargas eléctricas y fuerzas Hay dos tipos de cargas cargas positivas y cargas negativas REPELEN REPELEN ATRAEN Fuerzas del mismo signo se repelen, mientras que
Módulo 1: Electrostática Fuerza eléctrica 1 Cargas eléctricas y fuerzas Hay dos tipos de cargas cargas positivas y cargas negativas REPELEN REPELEN ATRAEN Fuerzas del mismo signo se repelen, mientras que
UNIDAD 4. ESTRUCTURA DE LA MATERIA.
 UNIDAD 4. ESTRUCTURA DE LA MATERIA. 1.- Resume las características principales de los distintos modelos atómicos que has estudiado y ordénalos cronológicamente. (Pág. 74 a 78) 2.- Indica si las siguientes
UNIDAD 4. ESTRUCTURA DE LA MATERIA. 1.- Resume las características principales de los distintos modelos atómicos que has estudiado y ordénalos cronológicamente. (Pág. 74 a 78) 2.- Indica si las siguientes
Enseñanza - Aprendizaje
 El modelo atómico de Bohr funcionaba muy bien para el átomo de hidrógeno, sin embargo, en los espectros realizados para átomos de otros elementos se observaba que electrones de un mismo nivel energético
El modelo atómico de Bohr funcionaba muy bien para el átomo de hidrógeno, sin embargo, en los espectros realizados para átomos de otros elementos se observaba que electrones de un mismo nivel energético
Colegio Superior de Señoritas Profesora: Noylen Vega Martínez Practica 8 avo año Química: - 1 -
 Profesora: Noylen Vega Martínez Practica 8 avo año Química: - 1 - Complete el siguiente cuadro calculando en cada caso los valores faltantes. Características de algunas especies químicas Especie química
Profesora: Noylen Vega Martínez Practica 8 avo año Química: - 1 - Complete el siguiente cuadro calculando en cada caso los valores faltantes. Características de algunas especies químicas Especie química
FÍSICA. 3- Un electrón y un protón están separados 10 cm cuál es la magnitud y la dirección de la fuerza sobre el electrón?
 ANEXO 1. FÍSICA. 1- Compara la fuerza eléctrica y la fuerza gravitacional entre: a- Dos electrones. b- Un protón y un electrón. Carga del electrón: e = 1,6x10-19 C Masa del protón: 1,67x10-27 Kg Masa del
ANEXO 1. FÍSICA. 1- Compara la fuerza eléctrica y la fuerza gravitacional entre: a- Dos electrones. b- Un protón y un electrón. Carga del electrón: e = 1,6x10-19 C Masa del protón: 1,67x10-27 Kg Masa del
qwertyuiopasdfghjklzxcvbnmqwerty uiopasdfghjklzxcvbnmqwertyuiopasd fghjklzxcvbnmqwertyuiopasdfghjklzx cvbnmqwertyuiopasdfghjklzxcvbnmq
 qwertyuiopasdfghjklzxcvbnmqwerty uiopasdfghjklzxcvbnmqwertyuiopasd fghjklzxcvbnmqwertyuiopasdfghjklzx cvbnmqwertyuiopasdfghjklzxcvbnmq Actividades de recuperación de 2º trimestre 3º ESO wertyuiopasdfghjklzxcvbnmqwertyui
qwertyuiopasdfghjklzxcvbnmqwerty uiopasdfghjklzxcvbnmqwertyuiopasd fghjklzxcvbnmqwertyuiopasdfghjklzx cvbnmqwertyuiopasdfghjklzxcvbnmq Actividades de recuperación de 2º trimestre 3º ESO wertyuiopasdfghjklzxcvbnmqwertyui
Ley de Coulomb. Introducción
 Ley de Coulomb Introducción En este tema comenzaremos el estudio de la electricidad con una pequeña discusión sobre el concepto de carga eléctrica, seguida de una breve introducción al concepto de conductores
Ley de Coulomb Introducción En este tema comenzaremos el estudio de la electricidad con una pequeña discusión sobre el concepto de carga eléctrica, seguida de una breve introducción al concepto de conductores
ESTRUCTURA ATOMICA. PARTICULAS FUNDAMENTALES. El átomo esta formado de partículas de muchos tipos:
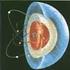 ESTRUCTURA ATOMICA. PARTICULAS FUNDAMENTALES. El átomo esta formado de partículas de muchos tipos: Protón (p, p, P) PARTICULAS ESTABLES Electrón (e, e, B) Neutrón (n, n, N) Electrón positivo o positrón
ESTRUCTURA ATOMICA. PARTICULAS FUNDAMENTALES. El átomo esta formado de partículas de muchos tipos: Protón (p, p, P) PARTICULAS ESTABLES Electrón (e, e, B) Neutrón (n, n, N) Electrón positivo o positrón
Los símbolos químicos son distintos signos abreviados que se utilizan para identificar los elementos y compuestos químicos en lugar de sus nombres
 Los símbolos químicos son distintos signos abreviados que se utilizan para identificar los elementos y compuestos químicos en lugar de sus nombres completos. La mayoría de los símbolos se derivan de las
Los símbolos químicos son distintos signos abreviados que se utilizan para identificar los elementos y compuestos químicos en lugar de sus nombres completos. La mayoría de los símbolos se derivan de las
ESTRUCTURA ATÓMICA TEORÍA ATÓMICA DE DALTON
 1 TEORÍA ATÓMICA DE DALTON John Dalton propuso, en 1803, una teoría sobre la constitución de la materia basada en los puntos que a continuación se indican. Aunque hoy sabemos que algunos de ellos son en
1 TEORÍA ATÓMICA DE DALTON John Dalton propuso, en 1803, una teoría sobre la constitución de la materia basada en los puntos que a continuación se indican. Aunque hoy sabemos que algunos de ellos son en
CLASE Nº 2 TEORÍA ATÓMICA DE LA MATERIA
 UNIVERSIDAD NACIONAL EXPERIMENTAL POLITECNICA ANTONIO JOSÉ DE SUCRE VICERRECTORADO BARQUISIMETO DEPARTAMENTO DE INGENIERÍA QUÍMICA QUÍMICA GENERAL CLASE Nº 2 TEORÍA ATÓMICA DE LA MATERIA 2012 1 Teorías
UNIVERSIDAD NACIONAL EXPERIMENTAL POLITECNICA ANTONIO JOSÉ DE SUCRE VICERRECTORADO BARQUISIMETO DEPARTAMENTO DE INGENIERÍA QUÍMICA QUÍMICA GENERAL CLASE Nº 2 TEORÍA ATÓMICA DE LA MATERIA 2012 1 Teorías
Observa la imagen de la derecha. Puedes identificar el núcleo y la nube de electrones? Qué crees que representan las esferas azules, rojas y grises?
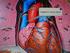 reflexiona Nuestro mundo está lleno de diversidad. Existe una variedad asombrosa en todos los materiales, sustancias y seres vivos que existen en la Tierra. Observa la imagen de la derecha. Incluso en
reflexiona Nuestro mundo está lleno de diversidad. Existe una variedad asombrosa en todos los materiales, sustancias y seres vivos que existen en la Tierra. Observa la imagen de la derecha. Incluso en
Qué información podemos obtener de ella?
 Qué información podemos obtener de ella? Dmitri Mendeleiev (1834-1907) Elementos enlistados según su masa atómica Propiedades periódicas de los elementos Predice existencia de elementos con determinadas
Qué información podemos obtener de ella? Dmitri Mendeleiev (1834-1907) Elementos enlistados según su masa atómica Propiedades periódicas de los elementos Predice existencia de elementos con determinadas
BLOQUE 2. EL ÁTOMO: MODELOS, TABLA PERIÓDICA Y ENLACE QUÍMICO.
 BLOQUE 2. EL ÁTOMO: MODELOS, TABLA PERIÓDICA Y ENLACE QUÍMICO. Modelos Atómicos. 1. Ordena cronológicamente los siguientes hechos. a) Descubrimiento del protón. b) Experimento de Millikan. c) Experimento
BLOQUE 2. EL ÁTOMO: MODELOS, TABLA PERIÓDICA Y ENLACE QUÍMICO. Modelos Atómicos. 1. Ordena cronológicamente los siguientes hechos. a) Descubrimiento del protón. b) Experimento de Millikan. c) Experimento
TEMA 3: La materia. Propiedades eléctricas y el átomo. 1.- En la siguiente sopa de letras puedes encontrar los nombres de 13 elementos químicos.
 Física y Química Curso 2012/13 3º E.S.O. TEMA 3: La materia. Propiedades eléctricas y el átomo. 1.- En la siguiente sopa de letras puedes encontrar los nombres de 13 elementos químicos. A O M O L P B A
Física y Química Curso 2012/13 3º E.S.O. TEMA 3: La materia. Propiedades eléctricas y el átomo. 1.- En la siguiente sopa de letras puedes encontrar los nombres de 13 elementos químicos. A O M O L P B A
Aplicaciones de la fuerza de Lorentz
 Aplicaciones de la fuerza de Lorentz Selector de velocidades La fuerza magnética sobre una partícula cargada que se mueve en el interior un campo magnético uniforme puede equilibrarse por una fuerza electrostática
Aplicaciones de la fuerza de Lorentz Selector de velocidades La fuerza magnética sobre una partícula cargada que se mueve en el interior un campo magnético uniforme puede equilibrarse por una fuerza electrostática
Demócrito (IV a.c.) afirmó: No hay mas que átomos (sin partes, indivisibles) y espacio vacío. Es la primera idea del concepto de átomo.
 TEORÍAS ATÓMICAS Demócrito (IV a.c.) afirmó: No hay mas que átomos (sin partes, indivisibles) y espacio vacío. Es la primera idea del concepto de átomo. Dalton (1808) propuso cinco hipótesis que podemos
TEORÍAS ATÓMICAS Demócrito (IV a.c.) afirmó: No hay mas que átomos (sin partes, indivisibles) y espacio vacío. Es la primera idea del concepto de átomo. Dalton (1808) propuso cinco hipótesis que podemos
Podemos definir la materia como todo aquello que ocupa un lugar en el espacio.
 Podemos definir la materia como todo aquello que ocupa un lugar en el espacio. MATERIA está formada por moléculas, las cuales son la parte más pequeña que poseen todas las propiedades físicas y químicas
Podemos definir la materia como todo aquello que ocupa un lugar en el espacio. MATERIA está formada por moléculas, las cuales son la parte más pequeña que poseen todas las propiedades físicas y químicas
A-1 - Indique cual de las siguientes afirmaciones es correcta:
 ESTRUCTURA ATÓMICA - PREGUNTAS DE TEST ))))))))))))))))))))))))))))))))))))))))))))))))))))))))))))))))))))))))))))))))))))))))))))))))))))))))Q Serie A: PARTICULAS SUBATOMICAS: Serie B- ESPECTROS: Serie
ESTRUCTURA ATÓMICA - PREGUNTAS DE TEST ))))))))))))))))))))))))))))))))))))))))))))))))))))))))))))))))))))))))))))))))))))))))))))))))))))))))Q Serie A: PARTICULAS SUBATOMICAS: Serie B- ESPECTROS: Serie
MODELO ATÓMICO DE DALTON 1808
 ESTRUCTURA ATÓMICA MODELO ATÓMICO DE DALTON 1808 Sienta las bases para la estequiometría de composición y la estequiometría de reacción. 1. Un elemento se compone de partículas extremadamente pequeñas,
ESTRUCTURA ATÓMICA MODELO ATÓMICO DE DALTON 1808 Sienta las bases para la estequiometría de composición y la estequiometría de reacción. 1. Un elemento se compone de partículas extremadamente pequeñas,
La electricidad se une con la química: Procesos de electrólisis
 docente La electricidad se une con la química: Procesos de electrólisis Tipo de actividad: Curso: Asignatura: Objetivos del currículum que aborda la actividad: Unidad: 1 y 3 Palabras claves: Materiales
docente La electricidad se une con la química: Procesos de electrólisis Tipo de actividad: Curso: Asignatura: Objetivos del currículum que aborda la actividad: Unidad: 1 y 3 Palabras claves: Materiales
Glosario. actividad. Número de desintegraciones que ocurren por segundo en un material que contiene elementos radioactivos.
 acelerador lineal (LINAC). Acelerador de electrones de uso médico que usualmente también tiene la posibilidad de generar rayos X de altas energías para radioterapia. actividad. Número de desintegraciones
acelerador lineal (LINAC). Acelerador de electrones de uso médico que usualmente también tiene la posibilidad de generar rayos X de altas energías para radioterapia. actividad. Número de desintegraciones
ESTRUCTURA ATÓMICA TABLA PERIÓDICA UNIÓN QUÍMICA
 ESTRUCTURA ATÓMICA TABLA PERIÓDICA UNIÓN QUÍMICA Teoría Atómica de DALTON 1- Los elementos químicos están constituidos por partículas denominadas átomos 2- Átomos de un mismo elemento, tienen las mismas
ESTRUCTURA ATÓMICA TABLA PERIÓDICA UNIÓN QUÍMICA Teoría Atómica de DALTON 1- Los elementos químicos están constituidos por partículas denominadas átomos 2- Átomos de un mismo elemento, tienen las mismas
LA TABLA PERIÓDICA. reflexiona
 reflexiona Imagina que quieres organizar tu casillero de la escuela. Cómo puedes separar y arreglar todo de una manera organizada? Puedes colocar los libros, los cuadernos y las carpetas en un estante,
reflexiona Imagina que quieres organizar tu casillero de la escuela. Cómo puedes separar y arreglar todo de una manera organizada? Puedes colocar los libros, los cuadernos y las carpetas en un estante,
Departamento de Física y Química Adaptaciones para 3º E.S.O.
 El átomo está formado por tres clases de partículas fundamentales: los protones, p +, que se encuentran en el núcleo o zona central del átomo y que tienen carga positiva y una masa apreciable. Los neutrones,
El átomo está formado por tres clases de partículas fundamentales: los protones, p +, que se encuentran en el núcleo o zona central del átomo y que tienen carga positiva y una masa apreciable. Los neutrones,
UNIDAD 1: ATOMOS Y MOLÉCULAS
 UNIDAD 1: ATOMOS Y MOLÉCULAS 1 Se define átomo como la menor porción de un elemento que se puede intercambiar por medio de una reacción química. Se define molécula como la menor porción de materia que
UNIDAD 1: ATOMOS Y MOLÉCULAS 1 Se define átomo como la menor porción de un elemento que se puede intercambiar por medio de una reacción química. Se define molécula como la menor porción de materia que
Tema 0. Conceptos Básicos en Química. Química Átomo: números másicos y atómicos Mol Fórmulas Reacciones químicas Gases Disoluciones
 Tema 0. Conceptos Básicos en Química Química Átomo: números másicos y atómicos Mol Fórmulas Reacciones químicas Gases Disoluciones Qué es la Química? Ciencia que trata de la composición y propiedades de
Tema 0. Conceptos Básicos en Química Química Átomo: números másicos y atómicos Mol Fórmulas Reacciones químicas Gases Disoluciones Qué es la Química? Ciencia que trata de la composición y propiedades de
EL ÁTOMO DIVISIBLE MODELOS ATÓMICOS
 EL ÁTOMO DIVISIBLE MODELOS ATÓMICOS TEORIA ATÓMICA DE DALTON 1808 TEORIA ATÓMICA DE DALTON 1. La materia está formada por minúsculas partículas indivisibles llamadas átomos. 2. Hay distintas clases de
EL ÁTOMO DIVISIBLE MODELOS ATÓMICOS TEORIA ATÓMICA DE DALTON 1808 TEORIA ATÓMICA DE DALTON 1. La materia está formada por minúsculas partículas indivisibles llamadas átomos. 2. Hay distintas clases de
PROBLEMAS FÍSICA MODERNA
 PROBLEMAS FÍSICA MODERNA 1.- (Jun 2014) Sobre un cierto metal cuya función de trabajo (trabajo de extracción) es 1,3eV incide un haz de luz cuya longitud de onda es 662nm. Calcule: a) La energía cinética
PROBLEMAS FÍSICA MODERNA 1.- (Jun 2014) Sobre un cierto metal cuya función de trabajo (trabajo de extracción) es 1,3eV incide un haz de luz cuya longitud de onda es 662nm. Calcule: a) La energía cinética
6.1. LAS CARACTERÍSTICAS DE LOS SERES VIVOS. Átomos y estructura atómica
 6.1. LAS CARACTERÍSTICAS DE LOS SERES VIVOS En este epígrafe se desarrollan las características que diferencian a los seres vivos. Una de ellas es la complejidad molecular, que se debe a la inmensa variedad
6.1. LAS CARACTERÍSTICAS DE LOS SERES VIVOS En este epígrafe se desarrollan las características que diferencian a los seres vivos. Una de ellas es la complejidad molecular, que se debe a la inmensa variedad
PROBLEMAS FÍSICA MODERNA
 PROBLEMAS FÍSICA MODERNA 1.- (Sept 2012) El periodo de semidesintegración de un isótopo radiactivo es de 1840 años. Si inicialmente se tiene una muestra de 30g de material radiactivo, a) Determine qué
PROBLEMAS FÍSICA MODERNA 1.- (Sept 2012) El periodo de semidesintegración de un isótopo radiactivo es de 1840 años. Si inicialmente se tiene una muestra de 30g de material radiactivo, a) Determine qué
LA ESTRUCTURA ATÓMICA
 LA ESTRUCTURA ATÓMICA Esta constituye una clave importante en la comprensión de la química moderna. El conocimiento de la estructura atómica nos proporciona una idea clara de cómo está constituida la materia
LA ESTRUCTURA ATÓMICA Esta constituye una clave importante en la comprensión de la química moderna. El conocimiento de la estructura atómica nos proporciona una idea clara de cómo está constituida la materia
LOS CUESTIONARIOS TIENEN RELACIÓN CON LOS CAPITULOS XX Y XXI DEL TEXTO GUÍA (FÍSCA PRINCIPIOS CON APLICACIONES SEXTA EDICIÓN DOUGLAS C.
 LOS CUESTIONARIOS TIENEN RELACIÓN CON LOS CAPITULOS XX Y XXI DEL TEXTO GUÍA (FÍSCA PRINCIPIOS CON APLICACIONES SEXTA EDICIÓN DOUGLAS C. Giancoli AL DESARROLLAR LOS CUESTIONARIOS, TENER EN CUENTA LOS PROCESOS
LOS CUESTIONARIOS TIENEN RELACIÓN CON LOS CAPITULOS XX Y XXI DEL TEXTO GUÍA (FÍSCA PRINCIPIOS CON APLICACIONES SEXTA EDICIÓN DOUGLAS C. Giancoli AL DESARROLLAR LOS CUESTIONARIOS, TENER EN CUENTA LOS PROCESOS
FÍSICA de 2º de BACHILLERATO FÍSICA NUCLEAR
 FÍSICA de 2º de BACHILLERATO FÍSICA NUCLEAR EJERCICIOS RESUELTOS QUE HAN SIDO PROPUESTOS EN LOS EXÁMENES DE LAS PRUEBAS DE ACCESO A ESTUDIOS UNIVERSITARIOS EN LA COMUNIDAD DE MADRID (1996 2013) DOMINGO
FÍSICA de 2º de BACHILLERATO FÍSICA NUCLEAR EJERCICIOS RESUELTOS QUE HAN SIDO PROPUESTOS EN LOS EXÁMENES DE LAS PRUEBAS DE ACCESO A ESTUDIOS UNIVERSITARIOS EN LA COMUNIDAD DE MADRID (1996 2013) DOMINGO
PRUEBA LIBRE PARA LA OBTENCIÓN DEL TÍTULO DE GRADUADO EN EDUCACIÓN SECUNDARIA OBLIGATORIA. MODELO 1 ÁMBITO CIENTÍFICO-TECNOLÓGICO (DOS HORAS)
 PRUEBA LIBRE PARA LA OBTENCIÓN DEL TÍTULO DE GRADUADO EN EDUCACIÓN SECUNDARIA OBLIGATORIA. DATOS PERSONALES Resolución de 17 de febrero de 2010. (D. O. E. nº 39, de 26 de febrero de 2010). MODELO 1 ÁMBITO
PRUEBA LIBRE PARA LA OBTENCIÓN DEL TÍTULO DE GRADUADO EN EDUCACIÓN SECUNDARIA OBLIGATORIA. DATOS PERSONALES Resolución de 17 de febrero de 2010. (D. O. E. nº 39, de 26 de febrero de 2010). MODELO 1 ÁMBITO
DEPARTAMENTO DE FÍSICA Y QUÍMICA FÍSICA Y QUÍMICA 4º DE ESO TEMA 7. ELEMENTOS Y COMPUESTOS
 DEPARTAMENTO DE FÍSICA Y QUÍMICA FÍSICA Y QUÍMICA 4º DE ESO Elementos y compuestos (Actividad 1) TEMA 7. ELEMENTOS Y COMPUESTOS El físico británico John Dalton dio a conocer entre los años 1803 y 1808
DEPARTAMENTO DE FÍSICA Y QUÍMICA FÍSICA Y QUÍMICA 4º DE ESO Elementos y compuestos (Actividad 1) TEMA 7. ELEMENTOS Y COMPUESTOS El físico británico John Dalton dio a conocer entre los años 1803 y 1808
Tema 4.-Teoría atómica de la materia
 Tema 4.-Teoría atómica de la materia Tema 4.-Teoría atómica de la materia 1.- Concepto de átomo 2.- Partículas que forman el átomo 3.- Estructura del átomo 4.- Átomos, isótopos e iones 5.- Configuración
Tema 4.-Teoría atómica de la materia Tema 4.-Teoría atómica de la materia 1.- Concepto de átomo 2.- Partículas que forman el átomo 3.- Estructura del átomo 4.- Átomos, isótopos e iones 5.- Configuración
Magnetismo e Inducción electromagnética. PAEG
 1. Por un hilo vertical indefinido circula una corriente eléctrica de intensidad I. Si dos espiras se mueven, una con velocidad paralela al hilo y otra con velocidad perpendicular respectivamente, se inducirá
1. Por un hilo vertical indefinido circula una corriente eléctrica de intensidad I. Si dos espiras se mueven, una con velocidad paralela al hilo y otra con velocidad perpendicular respectivamente, se inducirá
Universidad de Chile Preuniversitario Facultad de Medicina Subsector ciencias: Química Común. TALLER Nº1 Modelo Atómico de la Materia
 TALLER Nº1 Modelo Atómico de la Materia Escrito por: Juan Ceballo P. Editado por : Este taller tiene como finalidad ejercitar el primer eje temático de la PSU correspondiente al nivel de 2º medio: Modelo
TALLER Nº1 Modelo Atómico de la Materia Escrito por: Juan Ceballo P. Editado por : Este taller tiene como finalidad ejercitar el primer eje temático de la PSU correspondiente al nivel de 2º medio: Modelo
En una reacción química, los átomos se agrupan de forma diferente a como lo estaban inicialmente, pero ni aparecen ni desaparecen
 ESTRUCTURA DE LA MATERIA 1. Conceptos generales 2. Modelos atómicos. 3. Teoría cuántica. Fundamentos. 4. Números cuánticos. 5. Distribución de los electrones en el átomo: configuraciones electrónicas ÁTOMO:
ESTRUCTURA DE LA MATERIA 1. Conceptos generales 2. Modelos atómicos. 3. Teoría cuántica. Fundamentos. 4. Números cuánticos. 5. Distribución de los electrones en el átomo: configuraciones electrónicas ÁTOMO:
LA TEORÍA ATOMICA En el siglo y a.c., el filósofo griego Demócrito expresó la idea de que toda la materia estaba formada por partículas muy pequeñas
 LA TEORÍA ATOMICA En el siglo y a.c., el filósofo griego Demócrito expresó la idea de que toda la materia estaba formada por partículas muy pequeñas e indivisibles que llamó átomos (que significa indes..
LA TEORÍA ATOMICA En el siglo y a.c., el filósofo griego Demócrito expresó la idea de que toda la materia estaba formada por partículas muy pequeñas e indivisibles que llamó átomos (que significa indes..
ESTRUCTURA DEL ÁTOMO SISTEMA PERIÓDICO. TEMA 2 Pág. 228 libro (Unidad 11)
 ESTRUCTURA DEL ÁTOMO SISTEMA PERIÓDICO TEMA 2 Pág. 228 libro (Unidad 11) PÁGS. 234-235 MAGNITUDES ATÓMICAS. REPASO MAGNITUDES ATÓMICAS. Conceptos clave - Repaso NÚMERO ATÓMICO (Z) Es el número de protones
ESTRUCTURA DEL ÁTOMO SISTEMA PERIÓDICO TEMA 2 Pág. 228 libro (Unidad 11) PÁGS. 234-235 MAGNITUDES ATÓMICAS. REPASO MAGNITUDES ATÓMICAS. Conceptos clave - Repaso NÚMERO ATÓMICO (Z) Es el número de protones
qwertyuiopasdfghjklzxcvbnmqwerty uiopasdfghjklzxcvbnmqwertyuiopasd fghjklzxcvbnmqwertyuiopasdfghjklzx cvbnmqwertyuiopasdfghjklzxcvbnmq
 qwertyuiopasdfghjklzxcvbnmqwerty uiopasdfghjklzxcvbnmqwertyuiopasd fghjklzxcvbnmqwertyuiopasdfghjklzx cvbnmqwertyuiopasdfghjklzxcvbnmq ACTIVIDADES DE RECUPERACIÓN DE FÍSICA Y QUÍMICA 3º ESO 2º TRIMESTRE
qwertyuiopasdfghjklzxcvbnmqwerty uiopasdfghjklzxcvbnmqwertyuiopasd fghjklzxcvbnmqwertyuiopasdfghjklzx cvbnmqwertyuiopasdfghjklzxcvbnmq ACTIVIDADES DE RECUPERACIÓN DE FÍSICA Y QUÍMICA 3º ESO 2º TRIMESTRE
U N A M. Facultad de Ingeniería MODELO ATÓMICO DE J. J. THOMSON MODELO ATÓMICO DE ERNEST RUTHERFORD DESCUBRIMIENTO DEL PROTÓN Y DEL NEUTRON
 MODELO ATÓMICO DE J. J. THOMSON MODELO ATÓMICO DE ERNEST RUTHERFORD DESCUBRIMIENTO DEL PROTÓN Y DEL NEUTRON M. C. Q. Alfredo Velásquez Márquez Modelo Atómico de J. J. Thomson Electrones de Carga Negativa
MODELO ATÓMICO DE J. J. THOMSON MODELO ATÓMICO DE ERNEST RUTHERFORD DESCUBRIMIENTO DEL PROTÓN Y DEL NEUTRON M. C. Q. Alfredo Velásquez Márquez Modelo Atómico de J. J. Thomson Electrones de Carga Negativa
UD2. Estructura de la materia. 3º ESO. Dto. FyQ. IES Flavio Irnitano
 qwertyuiopasdfghjklzxcvbnmqwertyu iopasdfghjklzxcvbnmqwertyuiopasdfg hjklzxcvbnmqwertyuiopasdfghjklzxcv bnmqwertyuiopasdfghjklzxcvbnmqw ertyuiopasdfghjklzxcvbnmqwertyuiop asdfghjklzxcvbnmqwertyuiopasdfghjk
qwertyuiopasdfghjklzxcvbnmqwertyu iopasdfghjklzxcvbnmqwertyuiopasdfg hjklzxcvbnmqwertyuiopasdfghjklzxcv bnmqwertyuiopasdfghjklzxcvbnmqw ertyuiopasdfghjklzxcvbnmqwertyuiop asdfghjklzxcvbnmqwertyuiopasdfghjk
Importancia de las Interacciones Fundamentales de la Materia en Física Básica
 Importancia de las Interacciones Fundamentales de la Materia en Física Básica Nelson David González * 20031135028 Diana Patricia Santamaría** 20031135066 Universidad Distrital Francisco José de Caldas
Importancia de las Interacciones Fundamentales de la Materia en Física Básica Nelson David González * 20031135028 Diana Patricia Santamaría** 20031135066 Universidad Distrital Francisco José de Caldas
La materia. Clasificación de la materia
 27 de marzo de 2005 Contenidos 1 Introducción La materia 2 La materia Qué es la materia? Materia es todo aquello que tiene masa y posee volumen. La materia Qué es la materia? Materia es todo aquello que
27 de marzo de 2005 Contenidos 1 Introducción La materia 2 La materia Qué es la materia? Materia es todo aquello que tiene masa y posee volumen. La materia Qué es la materia? Materia es todo aquello que
Unidad didáctica 1. Naturaleza de la materia. El átomo
 Unidad didáctica 1 Naturaleza de la materia. El átomo 1.- Qué es la materia? Materia: es todo lo que tiene masa y ocupa un lugar en el espacio (tiene volumen). Sustancia: es el tipo de materia de que están
Unidad didáctica 1 Naturaleza de la materia. El átomo 1.- Qué es la materia? Materia: es todo lo que tiene masa y ocupa un lugar en el espacio (tiene volumen). Sustancia: es el tipo de materia de que están
Repaso Química: Compuestos
 Repaso Química: Compuestos Covalentes, formación, fórmulas I. Selección Múltiple. Escoge la mejor contestación para cada aseveración. 1 1. Los elementos en un compuesto covalente A. donan electrones. B.
Repaso Química: Compuestos Covalentes, formación, fórmulas I. Selección Múltiple. Escoge la mejor contestación para cada aseveración. 1 1. Los elementos en un compuesto covalente A. donan electrones. B.
FÍSICA Y QUÍMICA 1º Bachillerato PRESENTACIÓN DE ASIGNATURA
 FÍSICA Y QUÍMICA 1º Bachillerato PRESENTACIÓN DE ASIGNATURA TEMARIO CONTENIDOS FÍSICA Y QUÍMICA QUÍMICA 1. Estructura del átomo. Sistema periódico 2. Formulación y nomenclatura inorgánicas 3. Enlace químico
FÍSICA Y QUÍMICA 1º Bachillerato PRESENTACIÓN DE ASIGNATURA TEMARIO CONTENIDOS FÍSICA Y QUÍMICA QUÍMICA 1. Estructura del átomo. Sistema periódico 2. Formulación y nomenclatura inorgánicas 3. Enlace químico
SELECTIVIDAD: Física cuántica Física nuclear (Teoría)
 FÍSICA SELECTIVIDAD: Física cuántica Física nuclear (Teoría) Selectividad 2001 1. a) Qué significado tiene la expresión "longitud de onda asociada a una partícula"? b) Si la energía cinética de una partícula
FÍSICA SELECTIVIDAD: Física cuántica Física nuclear (Teoría) Selectividad 2001 1. a) Qué significado tiene la expresión "longitud de onda asociada a una partícula"? b) Si la energía cinética de una partícula
