TEMA 6: CINÉTICA HETEROGÉNEA FLUIDO - FLUIDO CQA-6/1
|
|
|
- Martín Aguirre Toledo
- hace 7 años
- Vistas:
Transcripción
1 TEMA 6: CINÉTICA HETEROGÉNEA FLUIDO - FLUIDO CQA-6/1
2 PLANTEAMIENTO DEL MODELO CINÉTICO Objetivos de las reacciones heterogéneas fluido-fluido:! Obtener productos valiosos mediante reacciones gas-líquido! Eliminar productos indeseados de corrientes gaseosas con disolventes líquidos! Llevar a cabo reacciones líquido-líquido en sistemas inmiscibles La velocidad depende del modo de contacto entre las fases:! Transporte de materia en cada una de las fases presentes! Equilibrio físico entre las fases (solubilidad, transporte en la interfase) Modelo cinético (Figura 6.1): 6.1 Esquema del modelo heterogéneo gas-líquido. CQA-6/2
3 " Reactivo A en una fase gaseosa " Reactivo B en una fase líquida " Reactivo A gaseoso es soluble en el líquido " Reactivo B no es soluble en el gas (no volátil, presión de vapor muy baja) " Reacción entre A y B se produce sólo en la fase líquida " Reacción irreversible y de segundo orden (-r A = k C A C B ): Interfase gas-líquido: a ambos lados se forma una película laminar en la que se produce el transporte de materia ( teoría de la película ). Reacción química provoca una modificación en los perfiles de concentración e incremento en la velocidad global respecto al proceso sólo físico. Perfiles de concentración (Figura 6.2): distinción de tres zonas [6.1] CQA-6/3
4 6.2 Perfiles de concentración en las reacciones gas-líquido.! Zona 1: sólo existe transporte de materia; velocidad global: [6.2] CQA-6/4
5 ! Zona 2: transporte de materia y reacción química simultáneos; velocidad global: [6.3] E: factor de aceleración química : factor de incremento de la absorción debido a la reacción química en la película líquida (cociente entre la velocidad de transporte de A con reacción química y la velocidad de transporte de A con sólo transporte de materia, para la misma fuerza impulsora): [6.4]! Zona 3: sólo reacción química; velocidad global: [6.5] $: retención líquida ( holdup ): volumen de líquido retenido por unidad de volumen de reactor. CQA-6/5
6 " Resistencias en serie de las tres zonas " Flujo continuo y estacionario " Ley de Henry (P A = H C A ) [6.6] sumando numeradores y denominadores: [6.7] Conclusión similar: aplicación de las ecuaciones de continuidad bajo las hipótesis de la teoría de la película para la cinética en estudio: [6.8] [6.9] condiciones límites: [6.10] [6.11] CQA-6/6
7 Análisis de la segunda condición límite (Figura 6.3): 6.3 Coordenadas espaciales de la fase líquida. En el seno de la fase líquida no existe difusión pero sí reacción química: Caudal de A a través de la interfase igual al que reacciona en el seno del líquido: [6.12] [6.13] [6.14] La ecuación [6.12] quedará de la forma: [6.15] que es la condición límite expresada por la ecuación [6.11]. CQA-6/7
8 REGÍMENES DE REACCIÓN: MÓDULO DE HATTA Varios regímenes de reacción (comportamientos del sistema) según la importancia relativa de los fenómenos en cada una de las zonas: diferentes perfiles de concentración. Perfiles de concentración expresados en función de un módulo adimensional: Módulo de Hatta, (Ha): relación entre la reacción química y el proceso difusivo [6.16] Para una cinética de segundo orden: [6.17] Teoría de la película: [6.18] Por tanto: [6.19] o bien: [6.20] Estudio de regímenes de reacción más representativos en reacciones heterogéneas gas-líquido: Obtención de la ecuación de velocidad CQA-6/8
9 REACCIONES RÁPIDAS (Ha > 3) El reactivo gaseoso A se agota en la película líquida (C Ao = 0): Ha > 3 Simplificación de la ecuación general [6.7]: [6.21] Necesario conocer el valor de E (función del régimen de reacción):! Estudio de casos límites: " Reacción instantánea " Reacción de pseudo-primer orden! Estudio de caso general CQA-6/9
10 CASO LÍMITE: REACCIÓN INSTANTÁNEA (Ha > 3; Ha > 5 E i ; E = E i ) A y B no coexistirán en ningún punto de la película líquida. Perfiles de concentración mostrados en la Figura Perfil de concentración de la reacción instantánea. d: distancia a la que está situado el llamado plano de reacción. CQA-6/10
11 Densidades de flujo, r' i (mol/m 2 As): [6.22] o bien: [6.23] de donde: [6.24] Velocidad global volumétrica (teoría de la película): [6.25] CQA-6/11
12 Si la resistencia ofrecida por la fase gaseosa fuese despreciable (P Ao = P Ai ), [6.21] queda: [6.26] Comparando con [6.25]: [6.27] E i : factor de aceleración (adimensional) factor de aceleración instantánea Cuando se opera a concentraciones altas del reactivo líquido y a presiones parciales muy bajas del reactivo gaseoso: y en la ecuación [6.24] se tendrá que d = 0: [6.28] CQA-6/12
13 Reacción instantánea interfacial : plano de reacción en la interfase (Figura 6.5): resistencia despreciable de la fase líquida frente a la de la fase gaseosa (cálculo del coeficiente k g a): [6.29] 6.5 Perfil de concentración de la reacción instantánea interfacial. CQA-6/13
14 CASO LÍMITE: REACCIÓN DE PSEUDO-PRIMER ORDEN (Ha > 3; Ha < E i /5; E = Ha Concentración de B mucho mayor que concentración de A (C B cte). Perfiles de concentración mostrados en la Figura Perfil de concentración de la reacción de pseudo-primer orden. CQA-6/14
15 Ecuación cinética (primer orden): [6.30] Sistema de ecuaciones diferenciales simplificado: [6.31] condiciones límites: [6.32] [6.33] CQA-6/15
16 Integración analítica de la ecuación diferencial: [6.34] Como además Ha > 3: [6.35] La ecuación [6.21] queda: [6.36] [6.37] o bien: [6.38] CQA-6/16
17 CASO GENERAL Reacciones rápidas, en general: [6.39] Perfiles de concentración mostrados en la Figura Perfil de concentración de la reacción rápida (en general). CQA-6/17
18 Factor de aceleración E no tiene una expresión analítica sencilla: Ecuación de Van Krevelen y Hoftijzer (1958) para reacción de segundo orden: [6.40] Valor de E implícito, por lo que elaboraron un gráfico para obtener E en función de Ha y E i (Figura 6.8). CQA-6/18
19 6.8 Diagrama de Van Krevelen y Hoftijzer. La Figura 6.8 permite distinguir tres regiones, correspondientes a los tres casos:! Región A, donde Ha > 5 E i y E = E i, independientemente del valor de Ha, es la correspondiente al caso límite de reacción instantánea.! Región B, donde E i > 5 Ha y E = Ha, es la correspondiente al caso límite de reacción de pseudo-primer orden.! Región C, corresponde al caso general de reacción rápida (Ha > 3), obteniéndose el valor de E por lectura sobre el eje de ordenadas a partir de los valores calculados de Ha y de E i. CQA-6/19
20 REACCIONES LENTAS (Ha < 0,02; E = 1) Reactivo gaseoso A no reacciona en la película líquida (sólo transporte difusivo de A) Perfiles de concentración mostrados en la Figura 6.9: 6.9 Perfil de concentración de la reacción lenta. La ecuación general, [6.7] queda (tres resistencias en serie): [6.41] La magnitud relativa de cada uno de los términos permitirá simplificaciones. CQA-6/20
21 Simplificación: la única resistencia importante es la debida a la reacción química en el seno del líquido: no existen resistencias difusionales en las películas gaseosa y líquida: P Ao = P Ai y C Ai = C Ao Perfiles de concentración mostrados en la Figura 6.10: La ecuación [6.41] queda: 6.10 Perfil de concentración de la reacción muy lenta. [6.42] Se produce cuando la reacción química puede considerarse infinitamente lenta. CQA-6/21
22 RÉGIMEN DE REACCIÓN INTERMEDIO (3 > Ha > 0,02; E > 1) Cierta cantidad del reactivo gaseoso A reacciona en el seno de la fase líquida y otra en la película líquida al mismo tiempo que se difunde en ella. Perfiles de concentración mostrados en la Figura 6.11: Ecuación general [6.7] no simplificable: 6.11 Perfil de concentración del régimen de reacción intermedio. [6.43] Caso más general de todos (el más complicado para el cálculo de E): Levenspiel propone una ecuación aproximada: [6.44] CQA-6/22
23 Análisis de la influencia relativa de cada una de las resistencias opuestas por la fase líquida (se considerará despreciable la resistencia opuesta por la fase gaseosa): Simplificación de la ecuación [6.43]: [6.45] Primer sumando (película líquida) dos resistencias: Extremo inferior: sólo resistencia difusiva (reacción lenta; E = 1; perfil plano; Ha < 0,02) Extremo superior: sólo resistencia a la reacción química (reacción rápida; C Ao = 0; Ha > 3) Entre ambos extremos, el perfil de concentración de A tendrá una cierta curvatura, que será un índice de la importancia relativa de la reacción química frente a la difusión, ambas en la película líquida, es decir, el valor de E (Figura 6.12) Límites del régimen de reacción intermedio. CQA-6/23
24 Curvatura del perfil de concentración de A (Figura 6.13) valores relativos de: Densidad de flujo del componente A en la interfase (pendiente i-i ) Densidad de flujo en el extremo de la película (pendiente j-j ) El cociente entre las pendientes i-i y j-j es, por definición, el factor E Curvatura del perfil de concentración del régimen de reacción intermedio. CQA-6/24
25 Para el régimen de reacción intermedio: siempre i-i $ j-j. Cuando Ha se aproxima a 0,02 (reacciones intermedias lentas ), y en el límite: [6.46] o bien: [6.47] entrándose en el régimen de las reacciones lentas. Cuando Ha se aproxima a 3, (reacciones intermedias rápidas ), y en el límite: [6.48] o bien: [6.49] entrándose en el régimen de las reacciones rápidas. CQA-6/25
26 UTILIZACIÓN DE LA ECUACIÓN GENERAL DE VELOCIDAD En la ecuación general de velocidad, [6.7], se conocen:! Condiciones del sistema (P Ao, C bo )! Datos hidrodinámicos ($, a, k g, k l, )! Datos difusivos (D A, D B )! Datos de equilibrio (H)! Datos cinéticos (k) Sólo será necesario determinar E para obtener la velocidad global, r A Como E depende, a su vez, del régimen de reacción (Ha y E i ), el primer paso ha de ser el cálculo de éstos mediante sus ecuaciones de definición: [6.50] [6.51] En la ecuación de E i interviene el valor de la presión interfacial, P Ai, que es desconocido: Suponer un valor inicial (considerar la resistencia en la fase gaseosa despreciable): P Ao = P Ai. Si se comprueba posteriormente que esta afirmación no es válida: P Ai < P Ai (comprobar siempre la validez del valor utilizado) Esquema del procedimiento a seguir para el cálculo de E para los diferentes regímenes de reacción. CQA-6/26
27 ! Cuando Ha > 3 (reacción rápida), el régimen de reacción depende, a su vez, de E i : " Si Ha < E i /5 (reacción de pseudo-primer orden), se tendrá: Aunque, en principio, E i sería supuesto, como P Ai está en el denominador de la ecuación [6.51], si la resistencia en fase gaseosa no fuese despreciable, esto es, P Ai < P Ao, E i sería aún mayor, por lo que se cumpliría con mayor razón el supuesto de la reacción de pseudo-primer orden siendo, en cualquier caso, válido el valor obtenido para E. " Si E i /5 < Ha < 5 E i (reacción rápida, en general), el valor de E se obtendrá de la gráfica de Van Krevelen y Hoftijzer (Figura 6.8). También en este caso, si la resistencia de la fase gaseosa no fuera despreciable, aumentaría el valor de E i, por lo que, o bien el supuesto de la reacción rápida en general se seguiría cumpliendo, o bien se estaría en el caso de reacción de pseudo-primer orden. En cualquiera de los casos sería válido el valor obtenido para E. " Si Ha > 5 E i (reacción instantánea), será necesario tener en cuenta la importancia relativa de la resistencia de la fase gaseosa, lo que obliga a llevar a cabo un tanteo para obtener el valor de E. Se comienza suponiendo P Ao = P Ai, esto es, E = E i, y se evalúan las resistencias opuestas por cada una de las fases: [6.52] [6.53] [6.54] CQA-6/27
28 Si R G no es despreciable frente a R L, la suposición no será correcta, siendo necesario, por tanto, suponer un nuevo valor de P ai, P Ai < P Ai. Este nuevo valor suele obtenerse definiendo la fracción de resistencia opuesta por la fase gaseosa respecto a la resistencia total, x g, como: [6.55] de tal forma que: Es decir, con el primer valor calculado para E se obtiene un nuevo valor de P Ai a partir de esta ecuación, lo que permitirá calcular un nuevo E i a partir de [6.51] y, en su caso, con ayuda de la gráfica de Van Krevelen y Hoftijzer (Figura 6.8), un nuevo E. Si éste coincide con el anterior, se habrá encontrado el E buscado y el último P Ai será el correcto. En caso contrario, se volvería a calcular un nuevo P Ai mediante la ecuación [6.56] y se repetiría el proceso. Obsérvese que puede darse el caso límite de que P Ai 0, es decir, reacción instantánea interfacial, en el que sólo existiría resistencia en la fase gaseosa y, por tanto, no tendría sentido la obtención de E.! Cuando Ha < 0,02 (reacción lenta), toda la reacción tiene lugar en el seno del líquido, y el la película líquida sólo existe transporte difusivo, por lo que:! Cuando 0,02 < Ha < 3 (régimen de reacción intermedio), la reacción tiene lugar tanto en el seno del líquido como en la película líquida, tomándose para el factor de aceleración el valor dado por la expresión aproximada propuesta por Levenspiel: [6.56] [6.57] [6.58] CQA-6/28
29 Regímenes de reacción para reacciones heterogéneas fluido-fluido Ha Régimen de reacción Zona de reacción Resistencias E R PG = 0 R PL = 0 Límites MUY LENTA < 0,02 LENTA SL PG + PL + SL 1 R PG = 0 R PL = 0 > 0,02 < 3 INTERMEDIA SL + PL PG + PL + SL E i Cinética en PL > 5 Ha PSEUDO OR- DEN Ha > 3 RÁPIDA PL PG + PL < 5 Ha > Ha/5 GENERAL Gráfica Van Krevelen INTERFACIAL < Ha/5 INSTANTÁNEA E i (tanteo P Ai ) R PL = 0 R SL = 0
Modelado de los procesos de tratamiento de aguas con ozono
 Modelado de los procesos de tratamiento de aguas con ozono Determinación de parámetros característicos Tratamiento de guas Residuales Industriales 5º Curso Ingeniero Químico - UGR Reacciones con ozono
Modelado de los procesos de tratamiento de aguas con ozono Determinación de parámetros característicos Tratamiento de guas Residuales Industriales 5º Curso Ingeniero Químico - UGR Reacciones con ozono
TEMA 4: BALANCES DE ENERGÍA. IngQui-4 [1]
![TEMA 4: BALANCES DE ENERGÍA. IngQui-4 [1] TEMA 4: BALANCES DE ENERGÍA. IngQui-4 [1]](/thumbs/40/22050892.jpg) TEMA 4: BALANCES DE ENERGÍA IngQui-4 [1] OBJETIVOS! Aplicar la ecuación de conservación al análisis de la energía involucrada en un sistema.! Recordar las componentes de la energía (cinética, potencial
TEMA 4: BALANCES DE ENERGÍA IngQui-4 [1] OBJETIVOS! Aplicar la ecuación de conservación al análisis de la energía involucrada en un sistema.! Recordar las componentes de la energía (cinética, potencial
Cinética química. Cinética Química Química 2º. Velocidad de reacción
 Cinética química Velocidad de reacción La velocidad de una reacción es la derivada de la concentración de un reactivo o producto con respecto al tiempo tomada siempre como valor positivo. Expresión de
Cinética química Velocidad de reacción La velocidad de una reacción es la derivada de la concentración de un reactivo o producto con respecto al tiempo tomada siempre como valor positivo. Expresión de
IV UNIDAD TRANSFERENCIA DE MASA
 IV UNIDAD TRANSFERENCIA DE MASA La transferencia de masa es la tendencia de uno o más componentes de una mezcla a transportarse desde una zona de alta concentración del o de los componentes a otra zona
IV UNIDAD TRANSFERENCIA DE MASA La transferencia de masa es la tendencia de uno o más componentes de una mezcla a transportarse desde una zona de alta concentración del o de los componentes a otra zona
ÁREA DE INGENIERÍA QUÍMICA Prof. Isidoro García García. Operaciones Básicas de Transferencia de Materia. Tema 1
 ÁREA DE INGENIERÍA QUÍMICA Operaciones Básicas de Transferencia de Materia Los procesos químicos modifican las condiciones de una determinada cantidad de materia: modificando su masa o composición modificando
ÁREA DE INGENIERÍA QUÍMICA Operaciones Básicas de Transferencia de Materia Los procesos químicos modifican las condiciones de una determinada cantidad de materia: modificando su masa o composición modificando
Qué son los diagramas Ternarios?
 Diagramas Ternarios Qué son los diagramas Ternarios? Diagramas que representan el equilibrio entre las distintas fases que se forman mediante tres componentes, como una función de la temperatura. Normalmente,
Diagramas Ternarios Qué son los diagramas Ternarios? Diagramas que representan el equilibrio entre las distintas fases que se forman mediante tres componentes, como una función de la temperatura. Normalmente,
Unidad 5- Cinética Química
 La termodinámica nos permite conocer la espontaneidad ó no espontaneidad de las reacciones, pero no nos informa de la rapidez con que tendrá lugar el proceso de transformación de los reactivos en productos:
La termodinámica nos permite conocer la espontaneidad ó no espontaneidad de las reacciones, pero no nos informa de la rapidez con que tendrá lugar el proceso de transformación de los reactivos en productos:
TEMA 6 EQUILIBRIO QUÍMICO
 TEMA 6 EQUILIBRIO QUÍMICO ÍNDICE 1. Equilibrio químico homogéneo y heterogéneo 2. Concentraciones en equilibrio 3. Constante de equilibrio K c 4. Constantes de equilibrio K p y K c 5. Cociente de reacción
TEMA 6 EQUILIBRIO QUÍMICO ÍNDICE 1. Equilibrio químico homogéneo y heterogéneo 2. Concentraciones en equilibrio 3. Constante de equilibrio K c 4. Constantes de equilibrio K p y K c 5. Cociente de reacción
IES Villalba Hervás Tecnología Industrial II Hidráulica 1
 IES Villalba Hervás Tecnología Industrial II Hidráulica 3. Hidráulica A. Propiedades de los fluidos hidráulicos a) Densidad Es la relación entre la masa de una determinada sustancia (en este caso líquida)
IES Villalba Hervás Tecnología Industrial II Hidráulica 3. Hidráulica A. Propiedades de los fluidos hidráulicos a) Densidad Es la relación entre la masa de una determinada sustancia (en este caso líquida)
TEMA 5: CINÉTICA HETEROGÉNEA. TRANSFERENCIA DE MATERIA CQA-5/1
 TEMA 5: CINÉTICA HETEROGÉNEA. TRANSFERENCIA DE MATERIA CQA-5/1 CARACTERÍSTICAS DE LAS REACCIONES HETEROGÉNEAS! Se requiere más de una fase para que la reacción transcurra del modo que lo hace.! Reacción
TEMA 5: CINÉTICA HETEROGÉNEA. TRANSFERENCIA DE MATERIA CQA-5/1 CARACTERÍSTICAS DE LAS REACCIONES HETEROGÉNEAS! Se requiere más de una fase para que la reacción transcurra del modo que lo hace.! Reacción
Absorción de Gases. Operaciones Unitarias II
 Absorción de Gases Operaciones Unitarias II Tipos de procesos y métodos de separación Muchos materiales de procesos químicos, así como sustancias biológicas, se presentan como mezclas de diferentes componentes
Absorción de Gases Operaciones Unitarias II Tipos de procesos y métodos de separación Muchos materiales de procesos químicos, así como sustancias biológicas, se presentan como mezclas de diferentes componentes
Universidad Tecnológica Nacional Facultad Regional Rosario Cátedra de Ing. De las Reacciones
 Universidad Tecnológica acional Facultad Regional Rosario Cátedra de Ing. e las Reacciones PRCTIC UI RECTORES IELES 01 Ing. Roque Masciarelli - Ing Silvia Stancich - Ing. Stoppani Fernando 1. Un reactor
Universidad Tecnológica acional Facultad Regional Rosario Cátedra de Ing. e las Reacciones PRCTIC UI RECTORES IELES 01 Ing. Roque Masciarelli - Ing Silvia Stancich - Ing. Stoppani Fernando 1. Un reactor
En todo momento se supone que el cambio de posición del interruptor es brusco; es decir, se produce en un intervalo nulo de tiempo.
 31 32 Se denomina expresión temporal o expresión instantánea a una expresión matemática en la que el tiempo es la variable independiente. Es decir, si se desea conocer el valor de la corriente (o el de
31 32 Se denomina expresión temporal o expresión instantánea a una expresión matemática en la que el tiempo es la variable independiente. Es decir, si se desea conocer el valor de la corriente (o el de
TEMA 7: CINÉTICA HETEROGÉNEA FLUIDO - SÓLIDO CQA-7/1
 TEMA 7: CINÉTICA HETEROGÉNEA FLUIDO - SÓLIDO CQA-7/1 PLANTEAMIENTO DEL MODELO CINÉTICO Reacciones heterogéneas fluido-sólido: numerosas y de gran importancia industrial: Se ponen en contacto un gas o un
TEMA 7: CINÉTICA HETEROGÉNEA FLUIDO - SÓLIDO CQA-7/1 PLANTEAMIENTO DEL MODELO CINÉTICO Reacciones heterogéneas fluido-sólido: numerosas y de gran importancia industrial: Se ponen en contacto un gas o un
Resolución de un problema básico de Cinética Química: hallar n y k
 Resolución de un problema básico de Cinética Química: hallar n y k Apellidos, nombre Departamento Centro Atarés Huerta, Lorena (loathue@tal.upv.es) Departamento de Tecnología de Alimentos ETSIA (Universidad
Resolución de un problema básico de Cinética Química: hallar n y k Apellidos, nombre Departamento Centro Atarés Huerta, Lorena (loathue@tal.upv.es) Departamento de Tecnología de Alimentos ETSIA (Universidad
TEMA 2: DERIVADA DE UNA FUNCIÓN
 TEMA : DERIVADA DE UNA FUNCIÓN Tasa de variación Dada una función y = f(x), se define la tasa de variación en el intervalo [a, a +h] como: f(a + h) f(a) f(a+h) f(a) y se define la tasa de variación media
TEMA : DERIVADA DE UNA FUNCIÓN Tasa de variación Dada una función y = f(x), se define la tasa de variación en el intervalo [a, a +h] como: f(a + h) f(a) f(a+h) f(a) y se define la tasa de variación media
Análisis esquemático simplificado de una torre de enfriamiento.
 Análisis esquemático simplificado de una torre de enfriamiento. En el diagrama el aire con una humedad Y 2 y temperatura t 2 entra por el fondo de la torre y la abandona por la parte superior con una humedad
Análisis esquemático simplificado de una torre de enfriamiento. En el diagrama el aire con una humedad Y 2 y temperatura t 2 entra por el fondo de la torre y la abandona por la parte superior con una humedad
CONSIDERACIONES GEOMETRICO CINETICAS SOBRE REACCIONES SOLIDO-FLUIDO
 CONSIDERACIONES GEOMETRICO CINETICAS SOBRE REACCIONES SOLIDO-FLUIDO Dr. Norberto 0. Lemcoff* Dr. Roberto E. Cunningham* SERIE II, n 207 x Departamento de Tecnología Química, Facultad de Ciencias Exactas,
CONSIDERACIONES GEOMETRICO CINETICAS SOBRE REACCIONES SOLIDO-FLUIDO Dr. Norberto 0. Lemcoff* Dr. Roberto E. Cunningham* SERIE II, n 207 x Departamento de Tecnología Química, Facultad de Ciencias Exactas,
Pese a las restricciones impuestas al estudio, los contenidos de este tema son lo suficientemente generales como para poder ser tenidos en cuenta
 En este tema se hará una referencia introductoria a los filtros. Un filtro es una agrupación de elementos activos y/o pasivos cuya presencia en un circuito modifica la respuesta en frecuencia del circuito.
En este tema se hará una referencia introductoria a los filtros. Un filtro es una agrupación de elementos activos y/o pasivos cuya presencia en un circuito modifica la respuesta en frecuencia del circuito.
TEMA 8: CINÉTICA HETEROGÉNEA CATALÍTICA CQA-8/1
 TEMA 8: CINÉTICA HETEROGÉNEA CATALÍTICA CQA-8/1 CARACTERÍSTICAS DE LAS REACCIONES HETEROGÉNEAS CATALÍTICAS FLUIDO-SÓLIDO Velocidad afectada por la presencia de sustancias ( catalizadores ): modifican la
TEMA 8: CINÉTICA HETEROGÉNEA CATALÍTICA CQA-8/1 CARACTERÍSTICAS DE LAS REACCIONES HETEROGÉNEAS CATALÍTICAS FLUIDO-SÓLIDO Velocidad afectada por la presencia de sustancias ( catalizadores ): modifican la
TEMA 5 CINÉTICA QUÍMICA
 TEMA 5 CINÉTICA QUÍMICA ÍNDICE 1. Cinética Química 2. Orden de reacción 3. Mecanismo de las reacciones químicas 4. Factores que influyen en la velocidad de reacción 5. Teoría de las reacciones químicas
TEMA 5 CINÉTICA QUÍMICA ÍNDICE 1. Cinética Química 2. Orden de reacción 3. Mecanismo de las reacciones químicas 4. Factores que influyen en la velocidad de reacción 5. Teoría de las reacciones químicas
EQUILIBRIO QUIMICO. Química General e Inorgánica Licenciatura en Ciencias Biológicas Profesorado en Biología Analista Biológico
 Química General e Inorgánica Licenciatura en Ciencias Biológicas rofesorado en Biología Analista Biológico EQUILIBRIO QUIMICO En general las reacciones químicas no se completan, es decir que no siempre
Química General e Inorgánica Licenciatura en Ciencias Biológicas rofesorado en Biología Analista Biológico EQUILIBRIO QUIMICO En general las reacciones químicas no se completan, es decir que no siempre
Anexo C. Introducción a las series de potencias. Series de potencias
 Anexo C Introducción a las series de potencias Este apéndice tiene como objetivo repasar los conceptos relativos a las series de potencias y al desarrollo de una función ne serie de potencias en torno
Anexo C Introducción a las series de potencias Este apéndice tiene como objetivo repasar los conceptos relativos a las series de potencias y al desarrollo de una función ne serie de potencias en torno
Autor: Antonio Rivero Cuesta, Tutor C.A. Palma de Mallorca
 Ejercicio: 4. 4. El intervalo abierto (,) es el conjunto de los números reales que verifican: a). b) < . - Intervalo abierto (a,b) al conjunto de los números reales, a < < b. 4. El intervalo
Ejercicio: 4. 4. El intervalo abierto (,) es el conjunto de los números reales que verifican: a). b) < . - Intervalo abierto (a,b) al conjunto de los números reales, a < < b. 4. El intervalo
LEY DE NEWTON DE LA VISCOSIDAD
 LEY DE NEWTON DE LA VISCOSIDAD Supongamos un fluido contenido entre dos grandes láminas planas y paralelas de área A separadas entre sí por una pequeña distancia Y. Fig. 1 Fluido contenido entre los láminas
LEY DE NEWTON DE LA VISCOSIDAD Supongamos un fluido contenido entre dos grandes láminas planas y paralelas de área A separadas entre sí por una pequeña distancia Y. Fig. 1 Fluido contenido entre los láminas
Fundamentos de Cinética Química: ecuación diferencial de velocidad
 Fundamentos de Cinética Química: ecuación diferencial de velocidad Apellidos, nombre Atarés Huerta, Lorena (loathue@tal.upv.es) Departamento Centro Departamento de Tecnología de Alimentos ETSIAMN (Universidad
Fundamentos de Cinética Química: ecuación diferencial de velocidad Apellidos, nombre Atarés Huerta, Lorena (loathue@tal.upv.es) Departamento Centro Departamento de Tecnología de Alimentos ETSIAMN (Universidad
2. Conservación de la masa
 2. Conservación de la masa La ecuación de conservación de la masa representa una previsión de la adición y sustracción de masa de una región concreta de un fluido. Pensemos en un volumen fijo e indeformable
2. Conservación de la masa La ecuación de conservación de la masa representa una previsión de la adición y sustracción de masa de una región concreta de un fluido. Pensemos en un volumen fijo e indeformable
Función lineal. Definición: f: R > R / f(x) = m.x+b donde m y b son números reales, es una función lineal.
 Función lineal Introducción: Recordemos que una función es una correspondencia entre los elementos de un conjunto de partida, llamado Dominio, y los elementos de un conjunto de llegada, llamado Codominio,
Función lineal Introducción: Recordemos que una función es una correspondencia entre los elementos de un conjunto de partida, llamado Dominio, y los elementos de un conjunto de llegada, llamado Codominio,
"OBSERVACIÓN DE LA CAÍDA DE UNA ESFERA A TRAVÉS DE UN MEDIO VISCOSO"
 EXPERIMENTO FA6 LABORATORIO DE FÍSICA AMBIENTAL "OBSERVACIÓN DE LA CAÍDA DE UNA ESFERA A TRAVÉS DE UN MEDIO VISCOSO" MATERIAL: () VISCOSÍMETRO ESFERAS DE ACERO 3 () MICROMETRO. ESCALA (O.00mm) (D x=0.0mm).
EXPERIMENTO FA6 LABORATORIO DE FÍSICA AMBIENTAL "OBSERVACIÓN DE LA CAÍDA DE UNA ESFERA A TRAVÉS DE UN MEDIO VISCOSO" MATERIAL: () VISCOSÍMETRO ESFERAS DE ACERO 3 () MICROMETRO. ESCALA (O.00mm) (D x=0.0mm).
JMLC - Chena IES Aguilar y Cano - Estepa
 Termodinámica es la parte de la física que estudia los intercambios de calor y trabajo que acompañan a los procesos fisicoquímicos. Si estos son reacciones químicas, la parte de ciencia que los estudia
Termodinámica es la parte de la física que estudia los intercambios de calor y trabajo que acompañan a los procesos fisicoquímicos. Si estos son reacciones químicas, la parte de ciencia que los estudia
Tema 5. Propiedades de transporte
 Tema 5 Propiedades de transporte 1 TEMA 5 PROPIEDADES DE TRANSPORTE 1. TEORÍA CINÉTICA DE LOS GASES POSTULADOS DE LA TEORÍA CINÉTICA DE LOS GASES INTERPRETACIÓN CINÉTICO MOLECULAR DE LA PRESIÓN Y LA TEMPERATURA
Tema 5 Propiedades de transporte 1 TEMA 5 PROPIEDADES DE TRANSPORTE 1. TEORÍA CINÉTICA DE LOS GASES POSTULADOS DE LA TEORÍA CINÉTICA DE LOS GASES INTERPRETACIÓN CINÉTICO MOLECULAR DE LA PRESIÓN Y LA TEMPERATURA
RESUMEN DE HIDROSTÁTICA E HIDRODINÁMICA
 Fluidos: RESUMEN DE HIDROSTÁTICA E HIDRODINÁMICA Materiales que fluyen, que no tienen forma propia, materiales que se comportan de manera diferente de los sólidos ya que estos tienen forma y volumen definido.
Fluidos: RESUMEN DE HIDROSTÁTICA E HIDRODINÁMICA Materiales que fluyen, que no tienen forma propia, materiales que se comportan de manera diferente de los sólidos ya que estos tienen forma y volumen definido.
DIFERENCIA ENTRE FLUIDOS Y SÓLIDOS
 DIFERENCIA ENTRE FLUIDOS Y SÓLIDOS Se le llama fluido a toda aquella sustancia continua que puede fluir. Los fluidos pueden ser gaseosos y líquidos. Esta es la diferencia fundamental entre un sólido, cuya
DIFERENCIA ENTRE FLUIDOS Y SÓLIDOS Se le llama fluido a toda aquella sustancia continua que puede fluir. Los fluidos pueden ser gaseosos y líquidos. Esta es la diferencia fundamental entre un sólido, cuya
PRÁCTICA No. 5 Estados del flujo en un canal
 PRÁCTICA No. 5 Estados del flujo en un canal Laboratorio de Hidráulica I OBJETIVO: Observar la generación y el comportamiento de diversos estados del flujo en un canal. INTRODUCCIÓN Para poder comprender
PRÁCTICA No. 5 Estados del flujo en un canal Laboratorio de Hidráulica I OBJETIVO: Observar la generación y el comportamiento de diversos estados del flujo en un canal. INTRODUCCIÓN Para poder comprender
Tema 3: Ecuaciones químicas y concentraciones
 Tema 3: Ecuaciones químicas y concentraciones Definición de disolución. Clases de disoluciones. Formas de expresar la concentración de una disolución. Proceso de dilución. Solubilidad. Diagramas de fases
Tema 3: Ecuaciones químicas y concentraciones Definición de disolución. Clases de disoluciones. Formas de expresar la concentración de una disolución. Proceso de dilución. Solubilidad. Diagramas de fases
CINÉTICA DE HIDRÓLISIS DEL ACETATO DE METILO Eva Mª Talavera Rodríguez y Francisco A. Ocaña Lara
 CINÉTICA DE HIDRÓLISIS DEL ACETATO DE METILO Eva Mª Talavera Rodríguez y Francisco A. Ocaña Lara OBJETIVOS 1.- Estudiar la cinética de la reacción de hidrólisis ácida del acetato de metilo en disolución
CINÉTICA DE HIDRÓLISIS DEL ACETATO DE METILO Eva Mª Talavera Rodríguez y Francisco A. Ocaña Lara OBJETIVOS 1.- Estudiar la cinética de la reacción de hidrólisis ácida del acetato de metilo en disolución
CAPITULO 5 LA DETERMINACIÓN DEL INGRESO DE EQUILIBRIO
 Documento elaborado por Jaime Aguilar Moreno Docente área económica Universidad del Valle Sede Buga CAPITULO 5 LA DETERMINACIÓN DEL INGRESO DE EQUILIBRIO OBJETIVO DEL CAPÍTULO Lograr que el estudiante
Documento elaborado por Jaime Aguilar Moreno Docente área económica Universidad del Valle Sede Buga CAPITULO 5 LA DETERMINACIÓN DEL INGRESO DE EQUILIBRIO OBJETIVO DEL CAPÍTULO Lograr que el estudiante
Estudio de funciones mediante límites y derivadas
 Estudio de funciones mediante límites y derivadas Observación: La mayoría de estos ejercicios se han propuesto en las pruebas de Selectividad, en los distintos distritos universitarios españoles El precio
Estudio de funciones mediante límites y derivadas Observación: La mayoría de estos ejercicios se han propuesto en las pruebas de Selectividad, en los distintos distritos universitarios españoles El precio
Balances de Masa. CI4102 Ingeniería Ambiental Profesor Marcelo Olivares A.
 Balances de Masa CI4102 Ingeniería Ambiental Profesor Marcelo Olivares A. Principio de Conservacion de Masa El concepto de continuidad o de conservación de masa es uno de los más fundamentales en ingeniería....la
Balances de Masa CI4102 Ingeniería Ambiental Profesor Marcelo Olivares A. Principio de Conservacion de Masa El concepto de continuidad o de conservación de masa es uno de los más fundamentales en ingeniería....la
DETERMINACIÓN DE LAS PÉRDIDAS DE CARGA
 DETERMINACIÓN DE LAS PÉRDIDAS DE CARGA I. PÉRDIDAS DE CARGA FRICCIONALES La pérdida de carga que tiene lugar en una conducción representa la pérdida de energía de un flujo hidráulico a lo largo de la misma
DETERMINACIÓN DE LAS PÉRDIDAS DE CARGA I. PÉRDIDAS DE CARGA FRICCIONALES La pérdida de carga que tiene lugar en una conducción representa la pérdida de energía de un flujo hidráulico a lo largo de la misma
Funciones de varias variables.
 Funciones de varias variables. Definición. Hasta ahora se han estudiado funciones de la forma y = f (x), f :D Estas funciones recibían el nombre de funciones reales de variable real ya que su valor y dependía
Funciones de varias variables. Definición. Hasta ahora se han estudiado funciones de la forma y = f (x), f :D Estas funciones recibían el nombre de funciones reales de variable real ya que su valor y dependía
9. MEDIDA DE LA DENSIDAD DE LÍQUIDOS
 9. MEDIDA DE LA DENSIDAD DE LÍQUIDOS OBJETIVO El objetivo de la practica es determinar la densidad de líquidos utilizando la balanza de Möhr y su aplicación a la determinación de la densidad de disoluciones
9. MEDIDA DE LA DENSIDAD DE LÍQUIDOS OBJETIVO El objetivo de la practica es determinar la densidad de líquidos utilizando la balanza de Möhr y su aplicación a la determinación de la densidad de disoluciones
PRÁCTICA 3: MEDIDAS DE LONGITUDES, PESOS Y TIEMPOS.
 PRÁCTICA : MEDIDAS DE LONGITUDES, PESOS Y TIEMPOS. MEDIDA DE DIMENSIONES GEOMÉTRICAS CON EL PALMER Y EL CALIRADOR. Con esta práctica se pretende que el alumno se familiarice con el manejo de distintos
PRÁCTICA : MEDIDAS DE LONGITUDES, PESOS Y TIEMPOS. MEDIDA DE DIMENSIONES GEOMÉTRICAS CON EL PALMER Y EL CALIRADOR. Con esta práctica se pretende que el alumno se familiarice con el manejo de distintos
PROBABILIDAD Y ESTADÍSTICA. Sesión 5 (En esta sesión abracamos hasta tema 5.8)
 PROBABILIDAD Y ESTADÍSTICA Sesión 5 (En esta sesión abracamos hasta tema 5.8) 5 DISTRIBUCIONES DE PROBABILIDAD CONTINUAS Y MUESTRALES 5.1 Distribución de probabilidades de una variable aleatoria continua
PROBABILIDAD Y ESTADÍSTICA Sesión 5 (En esta sesión abracamos hasta tema 5.8) 5 DISTRIBUCIONES DE PROBABILIDAD CONTINUAS Y MUESTRALES 5.1 Distribución de probabilidades de una variable aleatoria continua
Algunos conceptos microeconómicos. Tema: Elasticidad.
 UNIVERSIDAD DEL VALLE FACULTAD DE CIENCIAS DE LA ADMINISTRACIÓN MICROECONOMÍA rograma de Contaduría ública rofesor: Uvencer Alexander Gómez I. Marzo de 008. Algunos conceptos microeconómicos. Tema: Elasticidad.
UNIVERSIDAD DEL VALLE FACULTAD DE CIENCIAS DE LA ADMINISTRACIÓN MICROECONOMÍA rograma de Contaduría ública rofesor: Uvencer Alexander Gómez I. Marzo de 008. Algunos conceptos microeconómicos. Tema: Elasticidad.
Fluidos. Presión. Principio de Pascal.
 Fluidos. Presión. Principio de Pascal. CHOQUES ELASTICOS E INELASTICOS Se debe tener en cuenta que tanto la cantidad de movimiento como la energía cinética deben conservarse en los choques. Durante una
Fluidos. Presión. Principio de Pascal. CHOQUES ELASTICOS E INELASTICOS Se debe tener en cuenta que tanto la cantidad de movimiento como la energía cinética deben conservarse en los choques. Durante una
UNIVERSIDAD NACIONAL EXPERIMENTAL FRANCISCO DE MIRANDA AREA DE TECNOLOGÍA DEPARTAMENTO DE ENERGÉTICA UNIDAD CURRICULAR: TRANSFERENCIA DE CALOR
 UNIVERSIDAD NACIONAL EXPERIMENTAL FRANCISCO DE MIRANDA AREA DE TECNOLOGÍA DEPARTAMENTO DE ENERGÉTICA UNIDAD CURRICULAR: TRANSFERENCIA DE CALOR Convección Profesor: Ing. Isaac Hernández Isaachernandez89@gmail.com
UNIVERSIDAD NACIONAL EXPERIMENTAL FRANCISCO DE MIRANDA AREA DE TECNOLOGÍA DEPARTAMENTO DE ENERGÉTICA UNIDAD CURRICULAR: TRANSFERENCIA DE CALOR Convección Profesor: Ing. Isaac Hernández Isaachernandez89@gmail.com
UNIDAD EDUCATIVA COLEGIO SAN ANTONIO DEL TUY OCUMARE DEL TUY, ESTADO MIRANDA GUÍA N 3: CINÉTICA QUÍMICA
 UNIDAD EDUCATIVA COLEGIO SAN ANTONIO DEL TUY OCUMARE DEL TUY, ESTADO MIRANDA CURSO: 4 TO AÑO PROFESOR: CARLOS M. LANDAETA H. GUÍA N 3: CINÉTICA QUÍMICA 1.- Escriba las expresiones de las velocidades de
UNIDAD EDUCATIVA COLEGIO SAN ANTONIO DEL TUY OCUMARE DEL TUY, ESTADO MIRANDA CURSO: 4 TO AÑO PROFESOR: CARLOS M. LANDAETA H. GUÍA N 3: CINÉTICA QUÍMICA 1.- Escriba las expresiones de las velocidades de
Interacción aire - agua. Termómetro húmedo
 Interacción aire - agua. Termómetro húmedo Objetivos de la práctica! Obtener experimentalmente la denominada temperatura húmeda.! Estudiar las magnitudes psicrométricas de dos corrientes de aire húmedo,
Interacción aire - agua. Termómetro húmedo Objetivos de la práctica! Obtener experimentalmente la denominada temperatura húmeda.! Estudiar las magnitudes psicrométricas de dos corrientes de aire húmedo,
Principios de hidrodinámica
 Introducción Principios de hidrodinámica Adaptación: Prof. Hugo Chamorro HIDRODINÁMICA Mecánica y Fluidos Hidrodinámica Estudia los fluidos en movimientos, es decir, el flujo de los fluidos. Este estudio
Introducción Principios de hidrodinámica Adaptación: Prof. Hugo Chamorro HIDRODINÁMICA Mecánica y Fluidos Hidrodinámica Estudia los fluidos en movimientos, es decir, el flujo de los fluidos. Este estudio
Tema 6. Cinética de las Reacciones Químicas
 Tema 6 Cinética de las Reacciones Químicas 1 TEMA 6 CINÉTICA DE LAS REACCIONES QUÍMICAS 1. DEFINICIONES BÁSICAS CINÉTICA QUÍMICA VELOCIDAD DE REACCIÓN LEY DE VELOCIDADES Y ÓRDENES DE REACCIÓN ECUACIÓN
Tema 6 Cinética de las Reacciones Químicas 1 TEMA 6 CINÉTICA DE LAS REACCIONES QUÍMICAS 1. DEFINICIONES BÁSICAS CINÉTICA QUÍMICA VELOCIDAD DE REACCIÓN LEY DE VELOCIDADES Y ÓRDENES DE REACCIÓN ECUACIÓN
UNIVERSIDAD DE ANTIOQUIA FACULTAD DE QUÍMICA FARMACÉUTICA LABORATORIO DE QUÍMICA GENERAL Profesor: Jaime O. Pérez DEYMER GÓMEZ CORREA: 1 042 091 432
 UNIVERSIDAD DE ANTIOQUIA FACULTAD DE QUÍMICA FARMACÉUTICA LABORATORIO DE QUÍMICA GENERAL Profesor: Jaime O. Pérez Práctica: ESTEQUIOMETRÍA 2: RELACIÓN MASA- Fecha: 16/Febrero/2010 MASA. DEYMER GÓMEZ CORREA:
UNIVERSIDAD DE ANTIOQUIA FACULTAD DE QUÍMICA FARMACÉUTICA LABORATORIO DE QUÍMICA GENERAL Profesor: Jaime O. Pérez Práctica: ESTEQUIOMETRÍA 2: RELACIÓN MASA- Fecha: 16/Febrero/2010 MASA. DEYMER GÓMEZ CORREA:
Guía de Repaso 1: Introducción
 Guía de Repaso 1: Introducción 1- La distancia de la Tierra al Sol es casi 104 veces mayor que el diámetro de la Tierra. Al estudiar el movimiento de ésta alrededor del Sol, diría usted que la podemos
Guía de Repaso 1: Introducción 1- La distancia de la Tierra al Sol es casi 104 veces mayor que el diámetro de la Tierra. Al estudiar el movimiento de ésta alrededor del Sol, diría usted que la podemos
N = {1, 2, 3, 4, 5,...}
 Números y Funciones.. Números Los principales tipos de números son:. Los números naturales son aquellos que sirven para contar. N = {,,, 4, 5,...}. Los números enteros incluyen a los naturales y a sus
Números y Funciones.. Números Los principales tipos de números son:. Los números naturales son aquellos que sirven para contar. N = {,,, 4, 5,...}. Los números enteros incluyen a los naturales y a sus
Funciones y gráficas. 3º de ESO
 Funciones y gráficas 3º de ESO Funciones Una función es una correspondencia entre dos conjuntos numéricos que asocia a cada valor,, del primer conjunto un único valor, y, del segundo. La variable variable
Funciones y gráficas 3º de ESO Funciones Una función es una correspondencia entre dos conjuntos numéricos que asocia a cada valor,, del primer conjunto un único valor, y, del segundo. La variable variable
Universidad de La Laguna
 Universidad de La Laguna Departamento de Ingeniería Química y Tecnología Farmacéutica (Facultad de Química) Cinética Química Aplicada Manual Docente Ingeniero Químico 3 Curso Dr. Francisco Jarabo Friedrich
Universidad de La Laguna Departamento de Ingeniería Química y Tecnología Farmacéutica (Facultad de Química) Cinética Química Aplicada Manual Docente Ingeniero Químico 3 Curso Dr. Francisco Jarabo Friedrich
Unidad 1. Las fracciones.
 Unidad 1. Las fracciones. Ubicación Curricular en España: 4º, 5º y 6º Primaria, 1º, 2º y 3º ESO. Objetos de aprendizaje. 1.1. Concepto de fracción. Identificar los términos de una fracción. Escribir y
Unidad 1. Las fracciones. Ubicación Curricular en España: 4º, 5º y 6º Primaria, 1º, 2º y 3º ESO. Objetos de aprendizaje. 1.1. Concepto de fracción. Identificar los términos de una fracción. Escribir y
CURSO BÁSICO DE MATEMÁTICAS PARA ESTUDIANTES DE ECONÓMICAS Y EMPRESARIALES
 Unidad didáctica. Ecuaciones, inecuaciones y sistemas de ecuaciones e inecuaciones CONCEPTOS ECUACIONES Una ecuación es una igualdad entre dos epresiones en las que aparece una o varias incógnitas. En
Unidad didáctica. Ecuaciones, inecuaciones y sistemas de ecuaciones e inecuaciones CONCEPTOS ECUACIONES Una ecuación es una igualdad entre dos epresiones en las que aparece una o varias incógnitas. En
Estequiometría. En química, la estequiometría (del griego "στοιχειον"
 Estequiometría En química, la estequiometría (del griego "στοιχειον" = stoicheion (elemento) y "μετρον"=métron, (medida) es el cálculo de las relaciones cuantitativas entre reactivos y productos en el
Estequiometría En química, la estequiometría (del griego "στοιχειον" = stoicheion (elemento) y "μετρον"=métron, (medida) es el cálculo de las relaciones cuantitativas entre reactivos y productos en el
Tema 1. Cálculo diferencial
 Tema 1. Cálculo diferencial 1 / 57 Una función es una herramienta mediante la que expresamos la relación entre una causa (variable independiente) y un efecto (variable dependiente). Las funciones nos permiten
Tema 1. Cálculo diferencial 1 / 57 Una función es una herramienta mediante la que expresamos la relación entre una causa (variable independiente) y un efecto (variable dependiente). Las funciones nos permiten
Expresiones algebraicas
 Expresiones algebraicas Expresiones algebraicas Las expresiones algebraicas Elementos de una expresión algebraica Números de cualquier tipo Letras Signos de operación: sumas, restas, multiplicaciones y
Expresiones algebraicas Expresiones algebraicas Las expresiones algebraicas Elementos de una expresión algebraica Números de cualquier tipo Letras Signos de operación: sumas, restas, multiplicaciones y
INSTITUTO VALLADOLID PREPARATORIA Página 11 GEOMETRÍA ANALÍTICA
 INSTITUTO VALLADOLID PREPARATORIA Página 11 GEOMETRÍA ANALÍTICA Página 1 CONCEPTOS PRELIMINARES CONCEPTOS PRELIMINARES.1 GRÁFICAS Y TABULACIONES En Matemáticas, para toda operación existe su inversa, la
INSTITUTO VALLADOLID PREPARATORIA Página 11 GEOMETRÍA ANALÍTICA Página 1 CONCEPTOS PRELIMINARES CONCEPTOS PRELIMINARES.1 GRÁFICAS Y TABULACIONES En Matemáticas, para toda operación existe su inversa, la
Gráficas de las funciones racionales
 Gráficas de las funciones racionales Ahora vamos a estudiar de una manera geométrica las ideas de comportamiento de los valores que toma la función cuando los valores de crecen mucho. Es importante que
Gráficas de las funciones racionales Ahora vamos a estudiar de una manera geométrica las ideas de comportamiento de los valores que toma la función cuando los valores de crecen mucho. Es importante que
Pruebas de Acceso a Enseñanzas Universitarias Oficiales de Grado (PAEG) Matemáticas aplicadas a las Ciencias Sociales II - Junio 2011 - Propuesta B
 Pruebas de Acceso a Enseñanzas Universitarias Oficiales de Grado (PAEG) Matemáticas aplicadas a las Ciencias Sociales II - Junio 2011 - Propuesta B 1. Queremos invertir una cantidad de dinero en dos tipos
Pruebas de Acceso a Enseñanzas Universitarias Oficiales de Grado (PAEG) Matemáticas aplicadas a las Ciencias Sociales II - Junio 2011 - Propuesta B 1. Queremos invertir una cantidad de dinero en dos tipos
RESUMEN TEÓRICO DE CLASES
 Página 1 RESUMEN TEÓRICO DE CLASES Página 2 Tema 1. Inecuaciones Las inecuaciones son desigualdades algebraicas en la que sus dos miembros se relacionan por uno de estos signos: >; ;
Página 1 RESUMEN TEÓRICO DE CLASES Página 2 Tema 1. Inecuaciones Las inecuaciones son desigualdades algebraicas en la que sus dos miembros se relacionan por uno de estos signos: >; ;
DETERMINACION DE LA DENSIDAD Y HUMEDAD DE EQUILIBRIO I.N.V. E - 146
 E - 146-1 DETERMINACION DE LA DENSIDAD Y HUMEDAD DE EQUILIBRIO I.N.V. E - 146 1. OBJETO Existe dependencia del grado de compactación alcanzado por los suelos, con el contenido de humedad y la magnitud
E - 146-1 DETERMINACION DE LA DENSIDAD Y HUMEDAD DE EQUILIBRIO I.N.V. E - 146 1. OBJETO Existe dependencia del grado de compactación alcanzado por los suelos, con el contenido de humedad y la magnitud
18. DOMINIO FRECUENCIA CRITERIO DE NYQUIST
 18. DOMINIO FRECUENCIA CRITERIO DE NYQUIST 18.1. DIAGRAMAS POLARES En análisis dinámico de sistemas en el dominio de la frecuencia, además de emplearse los diagramas y el criterio de Bode, se utilizan
18. DOMINIO FRECUENCIA CRITERIO DE NYQUIST 18.1. DIAGRAMAS POLARES En análisis dinámico de sistemas en el dominio de la frecuencia, además de emplearse los diagramas y el criterio de Bode, se utilizan
ESCUELA TÉCNICA SUPERIOR DE INGENIEROS AERONÁUTICOS. Examen: Mecánica I (Probl. de Cinemática) Curso: 08/09 Fecha: 14.11.2008
 ESCUELA TÉCNICA SUPERIOR DE INGENIEROS AERONÁUTICOS APELLIDOS, NOMBRE: n o Examen: Mecánica I (Probl. de Cinemática) Curso: 08/09 Fecha: 14.11.008 Sea Oxyz un sistema de referencia ligado a un sólido S
ESCUELA TÉCNICA SUPERIOR DE INGENIEROS AERONÁUTICOS APELLIDOS, NOMBRE: n o Examen: Mecánica I (Probl. de Cinemática) Curso: 08/09 Fecha: 14.11.008 Sea Oxyz un sistema de referencia ligado a un sólido S
1. Las propiedades de los gases
 1. Las propiedades de los gases Para establecer por qué las diferentes sustancias tienen unas propiedades características de cada una de ellas (densidades, puntos de cambios de estado, solubilidad en agua,
1. Las propiedades de los gases Para establecer por qué las diferentes sustancias tienen unas propiedades características de cada una de ellas (densidades, puntos de cambios de estado, solubilidad en agua,
Conceptos fundamentales en Termodinámica
 Conceptos fundamentales en Termodinámica Física II Grado en Ingeniería de Organización Industrial Primer Curso Joaquín Bernal Méndez Curso 2011-2012 Departamento de Física Aplicada III Universidad de Sevilla
Conceptos fundamentales en Termodinámica Física II Grado en Ingeniería de Organización Industrial Primer Curso Joaquín Bernal Méndez Curso 2011-2012 Departamento de Física Aplicada III Universidad de Sevilla
Desorción (Stripping)
 INTRODUCCIÓN A LA ABSORCIÓN DE GASES Definición Operación unitaria de transferencia de materia que consiste en poner un gas en contacto con un líquido, a fin de disolver de manera selectiva uno o mas componentes
INTRODUCCIÓN A LA ABSORCIÓN DE GASES Definición Operación unitaria de transferencia de materia que consiste en poner un gas en contacto con un líquido, a fin de disolver de manera selectiva uno o mas componentes
UNIDAD 3: ANALICEMOS LA FUNCION EXPONENCIAL Y LOGARITMICA.
 UNIDAD 3: ANALICEMOS LA FUNCION EXPONENCIAL Y LOGARITMICA Históricamente, los exponentes fueron introducidos en matemáticas para dar un método corto que indicara el producto de varios factores semejantes,
UNIDAD 3: ANALICEMOS LA FUNCION EXPONENCIAL Y LOGARITMICA Históricamente, los exponentes fueron introducidos en matemáticas para dar un método corto que indicara el producto de varios factores semejantes,
TEMA 12 EL ESTADO GASEOSO
 TEMA 12 EL ESTADO GASEOSO Relación presión-volumen ley de Boyle A finales del siglo XVII boyle y Edme Mariotte, estudiaron independientemente la manera cómo cambia el volumen ocupado por un gas a una temperatura
TEMA 12 EL ESTADO GASEOSO Relación presión-volumen ley de Boyle A finales del siglo XVII boyle y Edme Mariotte, estudiaron independientemente la manera cómo cambia el volumen ocupado por un gas a una temperatura
TEMA 3: CINÉTICA HOMOGÉNEA. REACCIONES SIMPLES CQA-3/1
 TEMA 3: CINÉTICA HOMOGÉNEA. REACCIONES SIMPLES CQA-3/1 CARACTERÍSTICAS DE LAS REACCIONES HOMOGÉNEAS Todas las sustancias reaccionantes se encuentran en una sola fase Velocidad de reacción: Objetivo principal
TEMA 3: CINÉTICA HOMOGÉNEA. REACCIONES SIMPLES CQA-3/1 CARACTERÍSTICAS DE LAS REACCIONES HOMOGÉNEAS Todas las sustancias reaccionantes se encuentran en una sola fase Velocidad de reacción: Objetivo principal
F2 Bach. Movimiento armónico simple
 F Bach Movimiento armónico simple 1. Movimientos periódicos. Movimientos vibratorios 3. Movimiento armónico simple (MAS) 4. Cinemática del MAS 5. Dinámica del MAS 6. Energía de un oscilador armónico 7.
F Bach Movimiento armónico simple 1. Movimientos periódicos. Movimientos vibratorios 3. Movimiento armónico simple (MAS) 4. Cinemática del MAS 5. Dinámica del MAS 6. Energía de un oscilador armónico 7.
Aplicaciones de las integrales dobles
 Aplicaciones de las integrales dobles Las integrales dobles tienen multiples aplicaciones en física en geometría. A continuación damos una relación de alguna de ellas.. El área de una región plana R en
Aplicaciones de las integrales dobles Las integrales dobles tienen multiples aplicaciones en física en geometría. A continuación damos una relación de alguna de ellas.. El área de una región plana R en
PRÁCTICA 16 ESTEQUIOMETRÍA DE LAS REACCIONES QUÍMICAS 1.- FUNDAMENTO TEÓRICO.
 PRÁCTICA 16 ESTEQUIOMETRÍA DE LAS REACCIONES QUÍMICAS 1.- FUNDAMENTO TEÓRICO. En esta práctica se dirigirá la atención hacia el concepto de reacción química. Toda reacción es una transformación de la materia
PRÁCTICA 16 ESTEQUIOMETRÍA DE LAS REACCIONES QUÍMICAS 1.- FUNDAMENTO TEÓRICO. En esta práctica se dirigirá la atención hacia el concepto de reacción química. Toda reacción es una transformación de la materia
PARTE I TERMODINÁMICA QUÍMICA
 PARTE I TERMODINÁMICA QUÍMICA 01-Gonza lez.indd 1 5/6/06 19:26:43 01-Gonza lez.indd 2 5/6/06 19:26:49 Capítulo I Conceptos fundamentales Defi niciones 1,3,9 carácter macroscópico del sistema. Se determina
PARTE I TERMODINÁMICA QUÍMICA 01-Gonza lez.indd 1 5/6/06 19:26:43 01-Gonza lez.indd 2 5/6/06 19:26:49 Capítulo I Conceptos fundamentales Defi niciones 1,3,9 carácter macroscópico del sistema. Se determina
operaciones inversas Para unificar ambas operaciones, se define la potencia de exponente fraccionario:
 Potencias y raíces Potencias y raíces Potencia operaciones inversas Raíz exponente índice 7 = 7 7 7 = 4 4 = 7 base base Para unificar ambas operaciones, se define la potencia de exponente fraccionario:
Potencias y raíces Potencias y raíces Potencia operaciones inversas Raíz exponente índice 7 = 7 7 7 = 4 4 = 7 base base Para unificar ambas operaciones, se define la potencia de exponente fraccionario:
; En el caso de fuerzas conservativas, de donde:
 MECÁNICA DE FLUIDOS. PROBLEMAS RESUELTOS 1. Ecuación diferencial de la estática de fluidos en el caso particular de fuerzas conservativas. Analizar la relación entre las superficies equipotenciales y las
MECÁNICA DE FLUIDOS. PROBLEMAS RESUELTOS 1. Ecuación diferencial de la estática de fluidos en el caso particular de fuerzas conservativas. Analizar la relación entre las superficies equipotenciales y las
EL MOVIMIENTO Y SU DESCRIPCIÓN
 1. EL VECTOR VELOCIDAD EL MOVIMIENTO Y SU DESCRIPCIÓN Se van a tener dos tipos de magnitudes: Magnitudes escalares Magnitudes vectoriales Las magnitudes escalares son aquellas que quedan perfectamente
1. EL VECTOR VELOCIDAD EL MOVIMIENTO Y SU DESCRIPCIÓN Se van a tener dos tipos de magnitudes: Magnitudes escalares Magnitudes vectoriales Las magnitudes escalares son aquellas que quedan perfectamente
LEY DE NEWTON DE LA VISCOSIDAD. FLUIDOS NEWTONIANOS Y NO-NEWTONIANOS
 Fenómenos de Transporte.Licenciatura en Ciencia Tecnología de Alimentos Licenciatura en Ciencia Tecnología Ambiental Licenciatura en Biotecnología Biología Molecular LEY DE NEWTON DE LA VISCOSIDAD. FLUIDOS
Fenómenos de Transporte.Licenciatura en Ciencia Tecnología de Alimentos Licenciatura en Ciencia Tecnología Ambiental Licenciatura en Biotecnología Biología Molecular LEY DE NEWTON DE LA VISCOSIDAD. FLUIDOS
de una reacción n en la cual, tanto reactivos como productos están n en condiciones estándar (p = 1 atm; ; T = 298 K = 25 ºC;
 Entalpía a estándar de la reacción Es el incremento entálpico de una reacción n en la cual, tanto reactivos como productos están n en condiciones estándar (p = 1 atm; ; T = 298 K = 25 ºC; conc.. = 1 M).
Entalpía a estándar de la reacción Es el incremento entálpico de una reacción n en la cual, tanto reactivos como productos están n en condiciones estándar (p = 1 atm; ; T = 298 K = 25 ºC; conc.. = 1 M).
Profr. Efraín Soto Apolinar. La función racional
 La función racional Ahora estudiaremos una extensión de las funciones polinomiales. Las funciones racionales se definen a partir de las funciones polinomiales. Esta generalización es semejante a la que
La función racional Ahora estudiaremos una extensión de las funciones polinomiales. Las funciones racionales se definen a partir de las funciones polinomiales. Esta generalización es semejante a la que
TEMA 2: ECUACIONES DE CONSERVACIÓN. IngQui-2 [1]
![TEMA 2: ECUACIONES DE CONSERVACIÓN. IngQui-2 [1] TEMA 2: ECUACIONES DE CONSERVACIÓN. IngQui-2 [1]](/thumbs/89/98657449.jpg) TEMA 2: ECUACIONES DE CONSERVACIÓN IngQui-2 [1] 2.1 Ecuaciones de conservación: modelos Únicos cambios posibles que puede sufrir un sistema:! Materia (masa o composición).! Energía (cantidad o calidad).!
TEMA 2: ECUACIONES DE CONSERVACIÓN IngQui-2 [1] 2.1 Ecuaciones de conservación: modelos Únicos cambios posibles que puede sufrir un sistema:! Materia (masa o composición).! Energía (cantidad o calidad).!
Efecto de Resistencias Difusionales. El problema del Pellet
 CAPÍTULO 5 Efecto de Resistencias Difusionales. El problema del Pellet Gloria Lucia Orozco Cardona, Alan Didier Pérez Ávila. El segundo paso más importante en los procesos catalíticos es el paso de la
CAPÍTULO 5 Efecto de Resistencias Difusionales. El problema del Pellet Gloria Lucia Orozco Cardona, Alan Didier Pérez Ávila. El segundo paso más importante en los procesos catalíticos es el paso de la
EJERCICIOS RESUELTOS DE INECUACIONES. Juan Jesús Pascual. Inecuaciones
 MATEMÁTICAS EJERCICIOS RESUELTOS DE INECUACIONES Juan Jesús Pascual Inecuaciones Índice ejercicios resueltos A. Inecuaciones lineales con una incógnita B. Inecuaciones de segundo grado con una incógnita
MATEMÁTICAS EJERCICIOS RESUELTOS DE INECUACIONES Juan Jesús Pascual Inecuaciones Índice ejercicios resueltos A. Inecuaciones lineales con una incógnita B. Inecuaciones de segundo grado con una incógnita
La fotografía muestra una banda transportadora que se utiliza en un aeropuerto.
 M703: Banda transportadora A) Presentación del problema La fotografía muestra una banda transportadora que se utiliza en un aeropuerto. Para trasladarse de una sala a otra en el aeropuerto las personas
M703: Banda transportadora A) Presentación del problema La fotografía muestra una banda transportadora que se utiliza en un aeropuerto. Para trasladarse de una sala a otra en el aeropuerto las personas
Sobre La Mecánica Clásica de los Cuerpos Puntuales III
 Sobre La Mecánica Clásica de los Cuerpos Puntuales III Alejandro A. Torassa Buenos Aires, Argentina, E-mail: atorassa@gmail.com Licencia Creative Commons Atribución 3.0 (11 de febrero de 2008) Resumen.
Sobre La Mecánica Clásica de los Cuerpos Puntuales III Alejandro A. Torassa Buenos Aires, Argentina, E-mail: atorassa@gmail.com Licencia Creative Commons Atribución 3.0 (11 de febrero de 2008) Resumen.
TEMA N 2 RECTAS EN EL PLANO
 2.1 Distancia entre dos puntos1 TEMA N 2 RECTAS EN EL PLANO Sean P 1 (x 1, y 1 ) y P 2 (x 2, y 2 ) dos puntos en el plano. La distancia entre los puntos P 1 y P 2 denotada por d = esta dada por: (1) Demostración
2.1 Distancia entre dos puntos1 TEMA N 2 RECTAS EN EL PLANO Sean P 1 (x 1, y 1 ) y P 2 (x 2, y 2 ) dos puntos en el plano. La distancia entre los puntos P 1 y P 2 denotada por d = esta dada por: (1) Demostración
Química 2º Bacharelato
 Química 2º Bacharelato DEPARTAMENTO DE FÍSICA E QUÍMICA Termodinámica química 13/12/07 Nombre: Problemas 1. a) Calcula qué calor se desprende en la combustión de 20,0 cm 3 de etanol líquido a presión atmosférica
Química 2º Bacharelato DEPARTAMENTO DE FÍSICA E QUÍMICA Termodinámica química 13/12/07 Nombre: Problemas 1. a) Calcula qué calor se desprende en la combustión de 20,0 cm 3 de etanol líquido a presión atmosférica
Mezclas ( G, S, H) ) Equilibrio y energía libre de Gibbs. Química Física I QUIM 4041 6/17/2014. Ileana Nieves Martínez. 17 de Junio de 2014
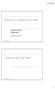 Equilibrio y energía libre de Gibbs Química Física I QUIM 441 Ileana Nieves Martínez 1 Mezclas (G, S, H) ) 2 1 Energía Libre molar parcial: i a T y constantes. dg dn dn 1 1 2 2... dg SdT Vd dn G total
Equilibrio y energía libre de Gibbs Química Física I QUIM 441 Ileana Nieves Martínez 1 Mezclas (G, S, H) ) 2 1 Energía Libre molar parcial: i a T y constantes. dg dn dn 1 1 2 2... dg SdT Vd dn G total
UNIDAD II FUNCIONES. Ing. Ronny Altuve Esp.
 República Bolivariana de Venezuela Universidad Alonso de Ojeda Administración Mención Gerencia y Mercadeo UNIDAD II FUNCIONES Ing. Ronny Altuve Esp. Ciudad Ojeda, Septiembre de 2015 Función Universidad
República Bolivariana de Venezuela Universidad Alonso de Ojeda Administración Mención Gerencia y Mercadeo UNIDAD II FUNCIONES Ing. Ronny Altuve Esp. Ciudad Ojeda, Septiembre de 2015 Función Universidad
5.1. Recta tangente, normal e intersección de curvas. Recta tangente
 5. Aplicaciones de la Derivada 5.1. Recta tangente, normal e intersección de curvas Recta tangente Desde la escuela primaria se sabe que la recta tangente en un punto de una circunferencia es aquella recta
5. Aplicaciones de la Derivada 5.1. Recta tangente, normal e intersección de curvas Recta tangente Desde la escuela primaria se sabe que la recta tangente en un punto de una circunferencia es aquella recta
Conceptos básicos de sistemas de ecuaciones diferenciales en la simulación de procesos ambientales y químicos
 Conceptos básicos de sistemas de ecuaciones diferenciales en la simulación de procesos ambientales y químicos Apellidos, nombre Departamento Centro Torregrosa López, Juan Ignacio (jitorreg@iqn.upv.es)
Conceptos básicos de sistemas de ecuaciones diferenciales en la simulación de procesos ambientales y químicos Apellidos, nombre Departamento Centro Torregrosa López, Juan Ignacio (jitorreg@iqn.upv.es)
Departamento de Matemáticas. Matemáticas. 2º Bachillerato
 Matemáticas 2º Bachillerato 1.- CONTENIDOS DE MATEMÁTICAS II QUE SERVIRÁN DE BASE PARA LA ELABORACIÓN DE LAS PROPUESTAS DE EXAMEN EN LAS PRUEBAS DE ACCESO A LA UNIVERSIDAD DE EXTREMADURA CURSO 2006-2007
Matemáticas 2º Bachillerato 1.- CONTENIDOS DE MATEMÁTICAS II QUE SERVIRÁN DE BASE PARA LA ELABORACIÓN DE LAS PROPUESTAS DE EXAMEN EN LAS PRUEBAS DE ACCESO A LA UNIVERSIDAD DE EXTREMADURA CURSO 2006-2007
Cálculo diferencial DERIVACIÓN
 DERIVACIÓN Definición de límite Entorno Definición. Se le llama entorno o vecindad de un punto a en R, al intervalo abierto (a - δ, a + δ ) = {a a - δ < x < a + δ }, en donde δ es semiamplitud a radio
DERIVACIÓN Definición de límite Entorno Definición. Se le llama entorno o vecindad de un punto a en R, al intervalo abierto (a - δ, a + δ ) = {a a - δ < x < a + δ }, en donde δ es semiamplitud a radio
Definición de vectores
 Definición de vectores Un vector es todo segmento de recta dirigido en el espacio. Cada vector posee unas características que son: Origen O también denominado Punto de aplicación. Es el punto exacto sobre
Definición de vectores Un vector es todo segmento de recta dirigido en el espacio. Cada vector posee unas características que son: Origen O también denominado Punto de aplicación. Es el punto exacto sobre
GUÍA DE PROBLEMAS. Cinética Química
 GUÍA DE PROBLEMAS 1) Deduzca las ecuaciones matemáticas que representan la cinética química para las reacciones de cero, primer y segundo orden. Asimismo, establezca la ecuación para cuando la concentración
GUÍA DE PROBLEMAS 1) Deduzca las ecuaciones matemáticas que representan la cinética química para las reacciones de cero, primer y segundo orden. Asimismo, establezca la ecuación para cuando la concentración
DERIVADA DE UNA FUNCIÓN
 www.fisicanet.com www.fisicaweb.com DERIVADA DE UNA FUNCIÓN fisicanet@interlap.com.ar Se abre aquí el estudio de uno de los conceptos fundamentales del cálculo diferencial: la derivada de una función.
www.fisicanet.com www.fisicaweb.com DERIVADA DE UNA FUNCIÓN fisicanet@interlap.com.ar Se abre aquí el estudio de uno de los conceptos fundamentales del cálculo diferencial: la derivada de una función.
