FORMULACIÓN Y NOMENCLATURA DE COMPUESTOS INORGÁNICOS 4ºESO
|
|
|
- Eugenio Quiroga Pereyra
- hace 7 años
- Vistas:
Transcripción
1 FORMULACIÓN Y NOMENCLATURA DE COMPUESTOS INORGÁNICOS Para poder formular y nombrar compuestos inorgánicos lo primero que tienes que aprender es: símbolos y nombres de los elementos grupo al que pertenecen en la tabla periódica distinguir entre elementos metálicos y no metálicos saber que siempre los metales forman cationes y los no metales, normalmente, aniones y por supuesto los estados de oxidación de los distintos elementos, además de una serie de reglas que veremos después. El estado de oxidación de un elemento es el número de electrones que se ponen en juego para formar un compuesto. Un elemento en estado fundamental tiene de número de oxidación 0, no tiene ningún tipo de carga y así es estable. Cuando se forma un compuesto es por que sus elementos, redistribuyen los electrones, dando lugar a una unión de tipo electrostático que se llama enlace y adquiere mayor estabilidad Se ha visto que los átomos más estables son los que tienen 8e -, en su última capa, igual que en los gases nobles, por ello los átomos buscan cediendo, ganando o compartiendo electrones de sus vecinos para obtener 8 e - Cómo sabemos los electrones que tiene un elemento?, pues viendo el grupo al que pertenecen, ya que el número de electrones de la capa de valencia coincide con el número de grupo. En el caso de los metales, que tienen pocos electrones en su última capa, pierden estos electrones para quedar con la capa anterior llena. Si pierden electrones forman cationes. En el grupo 1 y 2 son metales. En el grupo 1 tienen de capa de valencia ns 1, pierden un electrón y se quedan en forma de catión con la capa anterior llena, su estado de oxidación es +1, el grupo 2 tiene de capa de valencia ns 2, su estado de oxidación es Li Be Na Mg K Ca Rb Sr Cs Ba El H es un no metal y sus estados de oxidación son +1 y -1 En los siguientes grupos hay que tener en cuenta que hay elementos que son metales, no metales y semimetales, por lo tanto, tenemos que afinar más, ya que podrán tener estado de oxidación positivo o negativo IES ANTONIO CALVÍN 1
2 B C N O F Al Si P S Cl Ge Sn Pb As Se Br Sb Te I Los que quedan por debajo de la escalera, y están en azul, son metales, por tanto forman cationes y su estado de oxidación será positivo. Los que están por encima, naranjas, son no metales y tendrán nº de oxidación positivo y negativo, dependiendo del compuesto que formen. Para recordar los n os de oxidación en estos grupos y si son + o - : El número de oxidación -, sólo lo tienen los que están por encima de la escalera y sólo hay un estado de oxidación negativo, que coincide con el número que le falta al grupo para llegar a 18. Por ejemplo el O del grupo 16 tiene un estado de oxidación -2 El número de oxidación +, hay más de uno, el mayor coincide con el nº grupo menos 10. Para acordarnos vemos el grupo y si es par todos sus estados de oxidación + son pares siendo el mayor el del grupo menos 10 y descendiendo hasta 2 y si el grupo es impar desciende según los números impares siendo el mayor el que coincide con el nº del grupo menos 10. Por ejemplo, el S esta en el grupo 16, por tanto sus estados de oxidación positivos son: +6, +4 y +2. En el caso del Cl del grupo 17, sus estados de oxidación son: +7,+5,+3 y +1 En definitiva: B -3,+3, +1 C -4,+4,+2 N -3,+5,+3,+1 O -2 F -1,+1 Al +3 Si - 4,+4,+2 P -3,+5,+3,+1 S -2,+6,+4,+2 Cl -1,+1,+3,+5,+7 Sn +4,+2 As -3,+5,+3,+1 Se -2,+6,+4,+2 Br -1,+1,+3,+5,+7 Pb +4,+2 Sb -3,+5,+3,+1 Te -2,+6,+4,+2 I -1,+1,+3,+5,+7 Y también tenéis que saber algunos metales de transición como: Cr +2,+3,+4 y +6 Mn +2,+3,+4,+5,+6 y +7 Zn y Cd +2 Hg +1 y +2 Fe, Co y Ni +2 y +3 Pt y Pd +2 y +4 IES ANTONIO CALVÍN 2
3 Cu +1 y +2 Ag +1 Au +1 y NORMAS GENERALES. Para formular: Se escribe primero el símbolo del elemento con estado de oxidación positivo y a continuación el símbolo del elemento con valencia negativa, se intercambian las valencias que pasan a ser subíndices del contrario Para nombrar: Se nombra siempre primero el elemento escrito a la derecha, y se puede, según la IUPAC hacer de las siguientes maneras: Nomenclatura Sistemática. Se utilizan los prefijos griegos para expresar las proporciones de los elementos en la fórmula. Mono 1 ; di 2 ; tri 3 ; tetra 4 ; penta 5 ; hexa 6 ; hepta 7 ; El prefijo mono puede omitirse. Nomenclatura de Stock, se expresa la valencia del elemento en números romanos y entre paréntesis Nomenclatura tradicional, utiliza los sufijos ICO y OSO para especificar las valencias de los elementos. No se utiliza en compuestos binarios. 2. COMBINACIONES BINARIAS DEL HIDRÓGENO. 2.1 HIDRÁCIDOS Son las combinaciones del hidrógeno, que actúa con valencia +1, con: F, Cl, Br, I, S, Se y Te. En disolución acuosa presentan propiedades ácidas y de nombran como ácidos. Se formulan escribiendo primero el símbolo del H después el del otro elemento y se intercambian las valencias obteniéndose los subíndices adecuados. H +1 S -2 H 2 S 1 H 2 S Se nombran añadiendo la terminación URO al nombre del elemento que queda escrito a la derecha (es decir al que actúa con valencia negativa) Cuando se quiere hacer referencia a sus disoluciones acuosas se nombran Ácido...HÍDRICO. Ejemplos: IES ANTONIO CALVÍN 3
4 COMPUESTO NOMBRE SISTEMÁTICO EN SOLUCIÓN ACUOSA HF Fluoruro de hidrógeno Ácido fluorhídrico HCl Cloruro de hidrógeno Ácido clorhídrico H 2 S Sulfuro de hidrógeno Ácido sulfhídrico H 2 Te Telururo de hidrógeno Ácido telurhídrico ACTIVIDADES Nombrar: 1. HCl 2. H 2 S 3. HBr 4. H 2 Se 5. HI Formular: 1. Ácido clohídrico 2. Ácido sulfhídrico 3. Telururo de hidrógeno 4. Seleniuro de hidrógeno 5. Ácido selenhídrico 6. Ioduro de hidrógeno 7. Bromuro de hidrógeno 2.2. HIDRÓGENO CON OTROS NO METALES. Es la combinación del hidrógeno con el resto de no metales - Se formulan escribiendo primero el símbolo del no metal y a continuación el del hidrógeno y se intercambian las valencias dando los subíndices correspondientes. - Se nombran según las normas generales de los compuestos binarios, aunque la mayoría tiene nombres vulgares aceptados por la IUPAC. La nomenclatura de Stock no se suele utilizar en estos compuestos. COMPUESTO NOMBRE COMÚN NOMBRE SISTEMÁTICO NH 3 Amoniaco Trihidruro de nitrógeno PH 3 Fosfina Trihidruro de fósforo AsH 3 Arsina Trihidruro de arsénico SbH 3 Estibamina Trihidruro de antimonio IES ANTONIO CALVÍN 4
5 CH 4 Metano Tetrahidruro de carbono SiH 4 Silano Tetrahidruro de silicio. 2.3.HIDRUROS METÁLICOS Son las combinaciones del hidrógeno con los metales. El hidrógeno actúa con la valencia negativa ya que los metales la tienen positiva - Se formulan escribiendo primero el símbolo del metal y a continuación el del hidrógeno, intercambiando las valencias para obtener los subíndices adecuados - Se nombran diciendo la palabra HIDRURO DE (nombre del metal). Por la sistemática mediante los prefijos griegos y por la de Stock con la valencia del metal entre paréntesis y en números romanos. Ejemplos. COMPUESTO N. SISTEMÁTICA N. STOCK LiH Hidruro de litio Hidruro de litio KH Hidruro de potasio Hidruro de potasio MgH 2 Hidruro de magnesio Hidruro de magnesio Sn H 4 Tetrahidruro de estaño Hidruro de estaño (IV) Pb H 2 Dihidruro de plomo Hidruro de plomo (II) ACTIVIDADES Nombrar: NaH. FeH 3 AlH 3. ZnH 2 CuH PbH 4. Formular: Hidruro de litio Hidruro de plomo (II) IES ANTONIO CALVÍN 5
6 Hidruro de mercurio(ii) Dihidruro de cobre Trihidruro de cromo Hidruro de cobalto (III) Dihidruro de níquel Hidruro de estroncio Hidruro de potasio Tetrahidruro de platino 3. COMBINACIONES DE METALES CON NO METALES. En éstas combinaciones, lo no metales presentan las valencias negativas. Se formulan escribiendo primero el símbolo del metal y a continuación el del no metal y se intercambian las valencias. Se nombran dando la terminación- URO al nombre del elemento que queda escrito a la derecha, es decir al no metal. Se aplican las normas generales. COMPUESTO SISTEMÁTICA STOCK Ca F 2 Difluoruro de calcio Fluoruro de calcio (II) FeCl 2 Dicloruro de hierro Cloruro de hierro (II) K 2 S Sulfuro de dipotasio Sulfuro de potasio NiSe Monoseleniuro de niquel Seleniuro de niquel (II) ACTIVIDADES Nombrar: KCl. AgI AlBr 3 PbS Sn Se 2.. Formular Bromuro de potasio IES ANTONIO CALVÍN 6
7 Telururo de plomo(iv) Cloruro de aluminio Trisulfuro de dihierro Yoduro de plata 4. COMBINACIONES BINARIAS DEL OXÍGENO Reciben el nombre genérico de ÓXIDOS Se formulan escribiendo primero el símbolo del elemento y después el del oxígeno y se ajustan los subíndices correspondientes Se nombran diciendo ÓXIDO DE..., por la sistemática con los prefijos griegos correspondientes y por la de Stock con la valencia en del elemento en números romanos y entre paréntesis. COMPUESTO N. SISTEMÁTICO N. STOCK FeO monóxido de hierro óxido de hierro(ii) Fe 2 O 3 trióxido de dihierro óxido de hierro (III) NiO monóxido de nique óxido de niquel (II) Cu 2 O monóxido de dicobre óxido de cobre (I) l ACTIVIDADES Nombrar CaO Li 2 O Al 2 O 3 CoO SO 3 Cl 2 O 5 SeO 2 Ag 2 O MgO Formular IES ANTONIO CALVÍN 7
8 Dióxido de carbono Óxido de cobre (II) Trióxido de diniquel Óxido de platino (IV) Trióxido de dioro Óxido de cobalto (III) Heptaóxido de dibromo Óxido de estroncio Trióxido de dioro Óxido de plata Óxido de cesio Monóxido de selenio Monóxido de yodo 5. HIDRÓXIDOS Son compuestos formados por metales y el ión HIDRÓXIDO (OH) - Se formulan escribiendo primero el símbolo del metal y después tantos grupos OH como valencia tenga el metal Se nombran con los prefijos en la palabra HIDRÓXIDO y el nombre del metal o bien expresando la valencia variable entre paréntesis y número romanos. Ejemplos SISTEMÁTICA STOCK Li(OH) Hidróxido de litio Fe(OH) 2 Dihidróxido de hierro hidróxido de hierro(ii) Na(OH) Hidróxido de sodio (sosa caústica) Al(OH) 3 Hidróxido de aluminio ACTIVIDADES Nombrar: Ca(OH) 2 Fe(OH) 3 Pb(OH) 4 Sn(OH) 2 Al(OH) 3 IES ANTONIO CALVÍN 8
9 Formular: Hidróxido de cobalto(iii) Tetrahidróxido de plomo Hidróxido de bario Trihidróxido de oro Hidróxido de potasio Hidróxido de aluminio 6. ÁCIDOS OXOÁCIDOS Todos tienen la fórmula general: H a X b O c, donde X es un no metal excepto en el caso del Cr y Mn que forman ácidos con los estados de oxidación más altos. Cr con +6 y Mn con +6 y +7. POR LA TRADICIONAL Se nombran: Diciendo la palabrabra ácido y a continuación el nombre del elemento central con prefijos y sufijos que nos indica su estado de oxidación. - Si el elemento central tiene cuatro valencias como es el caso de Cl, Br y I: +1 Ácido hipo..oso ácido hipocloroso +3 Ácido..oso ácido cloroso +5 Ácido ico ácido clórico +7 Ácido per.ico ácido perclórico - Si el elemento central tiene tres valencias, solo se utilizan las tras primeras: +2 ácido hiposulfuroso + 4 ácido sulfuroso +6 ácido sulfúrico - Si el elemento central tiene dos valencias, solo se utilizan las terminaciones oso e - ico, para indicar el menor o mayor estado de oxidación, respectivamente - Si solo tiene una valencia se da la terminación ico Se formulan. Identificamos el estado de oxidación con el que actúa el elemento central (mediante los sufijos y prefijos), formulamos el óxido correspondiente y le añadimos H 2 O: ácido sulfúrico, la terminación -ico indica que el S está con estado de oxidación +6: S +6 O 2- S 2 O 6 SO 3 + H 2 O H 2 SO 4 Ácido permangánico Mn +7 O -2 Mn 2 O 7 + H 2 O H 2 Mn 2 O 8 HMnO 4 IES ANTONIO CALVÍN 9
10 Hay elementos como el P, As y Sb, entre otros, que con un mismo estado de oxidación dan lugar a distintos ácidos con distinto contenido de hidrógeno, son los ácidos, meta, piro y orto. - La forma meta se formula añadiendo al óxido una molécula de agua: P +5 O -2 P 2 O 5 + H 2 O H 2 P 2 O 6 HPO 3 ácido metafosfórico - La forma orto, a la forma meta se le añade una de agua: HPO 3 + H 2 O H 3 PO 4 ácido ortofofórico - La forma piro, se multiplica por dos la forma orto y se le quita una de agua: H 6 P 2 O 8 H 2 O H 4 P 2 O 7 ácido pirofosfórico Esta que os pongo es una de las muchas reglas nemotécnicas que hay para buscar las fórmulas de estos ácidos OXIDO + AGUA META META + AGUA ORTO 2ORTO AGUA PIRO Cómo nombrar estos ácidos si nos dan la fórmula? Primero determinamos el estado de oxidación y después nos fijamos en el número de átomos que hay del elemento central, si hay dos ya sabemos que es la forma piro, si solo hay un átomo no fijamos en el número de hidrógenos y cuando este es igual o menor de dos será la meta, ya que se hizo con una de agua, y si es superior a dos será la orto Por ejemplo: HAsO 2 como la molécula tiene que ser eléctricamente neutra, la suma de las cargas ha de ser cero, teniendo en cuenta que el O -2 y el H +. Al tener dos átomos de oxígeno 2 (-2) = -4 y un solo H +1, por tanto el arsénico tiene estado de oxidación +3 : 1+3-4=0 Ya sabemos que el As +3, acabará en oso. Ahora nos fijamos en los hidrógenos, como solo tiene uno se habrá formado con una molécula de agua, esto nos dice que es la forma meta, luego será el ácido metafosforoso POR LA SISTEMÁTICA Se nombran: Se lee la fórmula empezando por la derecha. Se indica el prefijo que indica el subíndice del oxígeno, a continuación el término oxo, después, el nombre del elemento central acabado en - ato y seguido de un número romano que indica su estado de oxidación y por último, la expresión de hidrógeno H 2 SO 4 HNO 3 Tetraoxosulfato(VI) de hidrógeno Trioxonitrato (V) de hidrógeno IES ANTONIO CALVÍN 10
11 H 2 CO 3 Trioxocarbonato (IV) de hidrógeno Se formulan: Puesto que con esta nomenclatura nos dicen el estado de oxidación del elemento central y el número de oxígenos calculamos los hidrógenos que son necesarios para que la suma de las cargas sea cero Para saber la fórmula del Trioxosulfato (IV) de hidrógeno escribimos el orden de los elementos H S O, sabemos que hay 3 oxígenos por tanto 3 (-2) = -6, que el S tiene estado de oxidación +4, luego el ácido tendrá que tener 2 hidrógenos 2 (+1) = +2, para que la suma de las cargas sea cero. La fórmula será H 2 SO 3 Dioxoyodato (III) de hidrógeno HIO 2 Monoxoclorato (I) de hidrógeno HClO Dioxoarseniato (III) de hidrógeno HAsO 2 POR STOCK Se nombran: Se dice la palabra ácido seguida del prefijo que indica el número de oxígenos a continuación el término oxo y por último el nombre del elemento central acabado en -ico y seguido de su estado de oxidación en números romanos y entre paréntesis H 2 SO 4 ácido tetraoxosulfúrico (VI) H 2 CO 3 ácido trioxocarbónico (IV) Se formulan Igual que en la sistemática. A modo de chuletilla : - Los oxoácidos de los halógenos (grupo 17) llevan todos un solo hidrógeno - Los oxoácidos de los elementos del grupo del nitrógeno llevan todos un solo hidrógeno - Los oxoácidos de los elementos del grupo del azufre y del carbono todos llevan dos hidrógenos - El subíndice del oxígeno multiplicado por 2 menos el estado de oxidación del elemento central indica el subíndice del hidrógeno 7. SALES OXISALES NEUTRAS. Las sales neutras son compuestos que resultan de la unión de un anión procedente de una oxoácido con un catión metálico. El anión tendrá una carga negativa igual al número de hidrógenos que tenía el ácido del que proviene H 2 SO 4 anión 2 SO 4 IES ANTONIO CALVÍN 11
12 HNO 3 anión NO 3 H 3 PO 4 anión 3 PO 4 POR LA TRADICIONAL Se nombran Se cambian las terminaciones del ácido del que proviene -ico y -oso por -ato e -ito respectivamente y a continuación se dice el metal indicando su valencia con números romanos NaClO 4 perclorato de sodio Cu(ClO 4 ) 2 perclorato de cobre (II) CdSO 4 sulfato de cadmio Para nombrarlas tenemos que sacar el estado de oxidación del no metal del anión, así sabemos el nombre del anión y después el estado de oxidación del metal Al 2 (SO 4 ) 3 Como se han intercambiado las valencias pasando a ser subíndices: Al 3+ y el 2 SO 4 La suma de las cargas del anión tiene que ser igual a -2, las cargas del oxígeno serán 4 (-2)= -8 el S tendrá que ser +6 para que +6 8 = -2, por lo tanto la sal se llamará sulfato de aluminio Se formulan Mediante la terminación sabemos el estado de oxidación del no metal del anión una vez sacado se intercambia con el del metal, pasando a ser subíndices Perbromato de plomo (II) El anión perbromato viene del ácido perbrómico, el Br +7 HBrO 4 BrO 4 Pb 2+ BrO 4 Pb (BrO 4 ) 2 POR LA SISTEMÁTICA Igual que los oxoácidos pero cambiando la coletilla de hidrógeno por el nombre del metal seguido de su estado de oxidación en números romanos Cu NO 3 Trioxonitrato (V) de cobre (I) IES ANTONIO CALVÍN 12
FORMULACIÓN Y NOMENCLATURA DE COMPUESTOS INORGÁNICOS 4ºESO
 FORMULACIÓN Y NOMENCLATURA DE COMPUESTOS INORGÁNICOS Para poder formular y nombrar compuestos inorgánicos lo primero que tienes que aprender es: símbolos y nombres de los elementos grupo al que pertenecen
FORMULACIÓN Y NOMENCLATURA DE COMPUESTOS INORGÁNICOS Para poder formular y nombrar compuestos inorgánicos lo primero que tienes que aprender es: símbolos y nombres de los elementos grupo al que pertenecen
TEMA 5. SISTEMA PERIÓDICO. FORMULACIÓN Y NOMENCLATURA DE COMPUESTOS INORGÁNICOS
 TEMA 5. SISTEMA PERIÓDICO. FORMULACIÓN Y NOMENCLATURA DE COMPUESTOS INORGÁNICOS SISTEMA PERIÓDICO El sistema periódico actual está formado por más de 100 elementos (114 en la actualidad), los cuales están
TEMA 5. SISTEMA PERIÓDICO. FORMULACIÓN Y NOMENCLATURA DE COMPUESTOS INORGÁNICOS SISTEMA PERIÓDICO El sistema periódico actual está formado por más de 100 elementos (114 en la actualidad), los cuales están
FORMULACIÓN DE QUÍMICA INORGÁNICA.
 FORMULACIÓN DE QUÍMICA INORGÁNICA. 1. VALENCIA. Es la capacidad que tiene un átomo de un elemento para combinarse con los átomos de otros elementos y formar compuestos. La valencia es un número, positivo
FORMULACIÓN DE QUÍMICA INORGÁNICA. 1. VALENCIA. Es la capacidad que tiene un átomo de un elemento para combinarse con los átomos de otros elementos y formar compuestos. La valencia es un número, positivo
NOMENCLATURA Y FORMULACIÓN DE QUÍMICA INORGÁNICA. Física y Química 3º de E.S.O. IES Isidra de Guzmán
 NOMENCLATURA Y FORMULACIÓN DE QUÍMICA INORGÁNICA Física y Química 3º de E.S.O. IES Isidra de Guzmán INTRODUCCIÓN La IUPAC ( Unión Internacional de Química Pura y Aplicada) es el organismo que coordina
NOMENCLATURA Y FORMULACIÓN DE QUÍMICA INORGÁNICA Física y Química 3º de E.S.O. IES Isidra de Guzmán INTRODUCCIÓN La IUPAC ( Unión Internacional de Química Pura y Aplicada) es el organismo que coordina
Para nombrar compuestos químicos según esta nomenclatura se utilizan los prefijos: MONO_, DI_, TRI_, TETRA_, PENTA_, HEXA_, HEPTA_...
 3. NOMENCLATURAS. Para nombrar los compuestos químicos inorgánicos se siguen las normas de la IUPAC (unión internacional de química pura y aplicada). Se aceptan tres tipos de nomenclaturas para los compuestos
3. NOMENCLATURAS. Para nombrar los compuestos químicos inorgánicos se siguen las normas de la IUPAC (unión internacional de química pura y aplicada). Se aceptan tres tipos de nomenclaturas para los compuestos
FORMULACIÓN Y NOMENCLATURA DE QUÍMICA INORGÁNICA
 FORMULACIÓN Y NOMENCLATURA DE QUÍMICA INORGÁNICA Índice de contenido TABLAS DE NÚMEROS DE OXIDACIÓN MÁS COMUNES...2 MECANISMO DE FORMULACIÓN...2 NOMENCLATURAS EN QUÍMICA INORGÁNICA...2 NOMENCLATURA CON
FORMULACIÓN Y NOMENCLATURA DE QUÍMICA INORGÁNICA Índice de contenido TABLAS DE NÚMEROS DE OXIDACIÓN MÁS COMUNES...2 MECANISMO DE FORMULACIÓN...2 NOMENCLATURAS EN QUÍMICA INORGÁNICA...2 NOMENCLATURA CON
Tema 6 : Nomenclatura y formulación Química Inorgánica
 Tema 6 : Nomenclatura y formulación Química Inorgánica Esquema de trabajo: Introducción Compuestos Binarios 1. Combinaciones binarias del oxígeno: A. Oxidos B. Anhídridos 2. Combinaciones binarias del
Tema 6 : Nomenclatura y formulación Química Inorgánica Esquema de trabajo: Introducción Compuestos Binarios 1. Combinaciones binarias del oxígeno: A. Oxidos B. Anhídridos 2. Combinaciones binarias del
Lo primero que hay que conocer para formular y nombrar los compuestos químicos es el número de oxidación de cada elemento.
 Tema 5. NOMENCLATURA Y FORMULACIÓN DE QUÍMICA INORGÁNICA Introducción La IUPAC (Unión Internacional de Química Pura y Aplicada) es el organismo que coordina y actualiza las normas que permiten formular
Tema 5. NOMENCLATURA Y FORMULACIÓN DE QUÍMICA INORGÁNICA Introducción La IUPAC (Unión Internacional de Química Pura y Aplicada) es el organismo que coordina y actualiza las normas que permiten formular
FORMULACIÓN QUÍMICA INORGÁNICA
 FORMULACIÓN QUÍMICA INORGÁNICA 1. VALENCIAS DE LOS ELEMENTOS QUÍMICOS MÁS CONOCIDOS Se entiende que las valencias con signo negativo se dan frente a elementos electropositivos y las valencias con signo
FORMULACIÓN QUÍMICA INORGÁNICA 1. VALENCIAS DE LOS ELEMENTOS QUÍMICOS MÁS CONOCIDOS Se entiende que las valencias con signo negativo se dan frente a elementos electropositivos y las valencias con signo
H, Li, Na, K, Rb, Cs, Fr 1. Be, Mg, Ca, Sr, Ba, Ra, Zn, Cd 2. B, Al 3. N, P, As, Sb 1, 3, 5. F, Cl, Br, I 1, 3, 5, 7. C, Si, Ge, Sn, Pb 2, 4 O 2
 H, Li, Na, K, Rb, Cs, Fr 1 Be, Mg, Ca, Sr, Ba, Ra, Zn, Cd 2 B, Al 3 N, P, As, Sb 1, 3, 5 F, Cl, Br, I 1, 3, 5, 7 C, Si, Ge, Sn, Pb 2, 4 O 2 S, Se, Te 2, 4, 6 Cr 2, 3, 3, 6 Mn 2, 3, 4, 6, 7 Fe, Co, Ni 2,
H, Li, Na, K, Rb, Cs, Fr 1 Be, Mg, Ca, Sr, Ba, Ra, Zn, Cd 2 B, Al 3 N, P, As, Sb 1, 3, 5 F, Cl, Br, I 1, 3, 5, 7 C, Si, Ge, Sn, Pb 2, 4 O 2 S, Se, Te 2, 4, 6 Cr 2, 3, 3, 6 Mn 2, 3, 4, 6, 7 Fe, Co, Ni 2,
Formulación Inorgánica
 Formulación Inorgánica 1.- Sustancias Simples Por sustancias simples entendemos aquellas sustancias formadas por un solo tipo de elementos, podemos encontrar casos: Sustancias simples metálicas: se formulan
Formulación Inorgánica 1.- Sustancias Simples Por sustancias simples entendemos aquellas sustancias formadas por un solo tipo de elementos, podemos encontrar casos: Sustancias simples metálicas: se formulan
Formulación inorgánica
 Formulación inorgánica 1. Compuestos binarios con oxígeno (Óxidos) Combinaciones de cualquier elemento con el oxígeno. El elemento se coloca a la izquierda y el oxígeno a la derecha y se intercambian las
Formulación inorgánica 1. Compuestos binarios con oxígeno (Óxidos) Combinaciones de cualquier elemento con el oxígeno. El elemento se coloca a la izquierda y el oxígeno a la derecha y se intercambian las
FORMULACIÓN Y NOMENCLATURA
 1. SUSTANCIAS SIMPLES. FORMULACIÓN Y NOMENCLATURA Están constituidas por átomos de un solo elemento. En ellas las moléculas están formadas por átomos idénticos. Su fórmula indica el número de átomos de
1. SUSTANCIAS SIMPLES. FORMULACIÓN Y NOMENCLATURA Están constituidas por átomos de un solo elemento. En ellas las moléculas están formadas por átomos idénticos. Su fórmula indica el número de átomos de
QUÍMICA INORGÁNICA. Elementos Símbolo Valencia Elemento Símbolo Valencia. Hidrógeno H Oxigeno O -2. Flúor F -1 Nitrógeno N
 QUÍMICA INORGÁNICA VALENCIAS NO METALES Elementos Símbolo Valencia Elemento Símbolo Valencia Hidrógeno H -1 +1 Oxigeno O -2 Flúor F -1 Nitrógeno N -3 +1+3+5 Cloro Cl -1 +1+3+5+7 Fósforo P -3 +1+3+5 Bromo
QUÍMICA INORGÁNICA VALENCIAS NO METALES Elementos Símbolo Valencia Elemento Símbolo Valencia Hidrógeno H -1 +1 Oxigeno O -2 Flúor F -1 Nitrógeno N -3 +1+3+5 Cloro Cl -1 +1+3+5+7 Fósforo P -3 +1+3+5 Bromo
FORMULACIÓN Y NOMENCLATURA
 FORMULACIÓN Y NOMENCLATURA.- Formulación: Es la representación escrita de una molécula que se rige por unas normas universales establecidas por acuerdo de la comunidad científica..- Nomenclatura: Es el
FORMULACIÓN Y NOMENCLATURA.- Formulación: Es la representación escrita de una molécula que se rige por unas normas universales establecidas por acuerdo de la comunidad científica..- Nomenclatura: Es el
NOMENCLATURA DE ÁCIDOS Y BASES
 COLEGIO SAN ESTEBAN DIÁCONO Departamento de Ciencias Química IVº Electivo Prof. Juan Pastrián Lisboa NOMENCLATURA DE ÁCIDOS Y BASES Objetivo: - Reconocer y aplicar reglas de nomenclatura tradicional y
COLEGIO SAN ESTEBAN DIÁCONO Departamento de Ciencias Química IVº Electivo Prof. Juan Pastrián Lisboa NOMENCLATURA DE ÁCIDOS Y BASES Objetivo: - Reconocer y aplicar reglas de nomenclatura tradicional y
TEMA 5.- Formulación y nomenclatura
 Tema 5.- Formulación y nomenclatura de compuestos binarios 0.- Introducción. 1.- Óxidos. 2.- Peróxidos. 3.- Combinaciones binarias del hidrógeno. 3.1.- Hidruros. 3.2.- Haluros. 3.3.- Hidruros volátiles.
Tema 5.- Formulación y nomenclatura de compuestos binarios 0.- Introducción. 1.- Óxidos. 2.- Peróxidos. 3.- Combinaciones binarias del hidrógeno. 3.1.- Hidruros. 3.2.- Haluros. 3.3.- Hidruros volátiles.
TEMA 4: FORMULACIÓN 1.- CONCEPTOS PREVIOS
 TEMA 4: FORMULACIÓN 1.- CONCEPTOS PREVIOS Compuesto químico: es la unión de varios átomos que no pueden separarse por procedimientos físicos pero sí mediante procedimientos químicos. Ejemplo: dos átomos
TEMA 4: FORMULACIÓN 1.- CONCEPTOS PREVIOS Compuesto químico: es la unión de varios átomos que no pueden separarse por procedimientos físicos pero sí mediante procedimientos químicos. Ejemplo: dos átomos
Tema 1 : Nomenclatura y formulación Química Inorgánica
 Tema 1 : Nomenclatura y formulación Química Inorgánica Esquema de trabajo: Introducción Compuestos Binarios 1. Combinaciones binarias del oxígeno 2. Combinaciones binarias del hidrógeno 3. Sales binarias
Tema 1 : Nomenclatura y formulación Química Inorgánica Esquema de trabajo: Introducción Compuestos Binarios 1. Combinaciones binarias del oxígeno 2. Combinaciones binarias del hidrógeno 3. Sales binarias
La fórmula química expresa la composición de moléculas y compuestos mediante símbolos químicos. 13 millones!!!
 La fórmula química expresa la composición de moléculas y compuestos mediante símbolos químicos El Nº de compuestos químicos conocidos es superior a 13 millones!!! Método sistemático de nombrar los compuestos:
La fórmula química expresa la composición de moléculas y compuestos mediante símbolos químicos El Nº de compuestos químicos conocidos es superior a 13 millones!!! Método sistemático de nombrar los compuestos:
1.- CONCEPTOS PREVIOS
 TEMA 6: FORMULACIÓN 1.- CONCEPTOS PREVIOS Compuesto químico: es la unión de varios átomos que no pueden separarse por procedimientos físicos pero sí mediante procedimientos químicos. Ejemplo: dos átomos
TEMA 6: FORMULACIÓN 1.- CONCEPTOS PREVIOS Compuesto químico: es la unión de varios átomos que no pueden separarse por procedimientos físicos pero sí mediante procedimientos químicos. Ejemplo: dos átomos
QUÍMICA INORGÁNICA REGLAS DE FORMULACIÓN
 QUÍMICA INORGÁNICA REGLAS DE FORMULACIÓN Rafael Jiménez Prieto FORMULACIÓN INORGÁNICA FORMULACIÓN INORGÁNICA VALENCIAS MÁS COMUNES DE LOS ELEMENTOS QUÍMICOS TIPOS DE COMPUESTOS Consideraciones generales
QUÍMICA INORGÁNICA REGLAS DE FORMULACIÓN Rafael Jiménez Prieto FORMULACIÓN INORGÁNICA FORMULACIÓN INORGÁNICA VALENCIAS MÁS COMUNES DE LOS ELEMENTOS QUÍMICOS TIPOS DE COMPUESTOS Consideraciones generales
TEMA 4: FORMULACIÓN 1.- CONCEPTOS PREVIOS
 TEMA 4: FORMULACIÓN 1.- CONCEPTOS PREVIOS Compuesto químico: es la unión de varios átomos que no pueden separarse por procedimientos físicos pero sí mediante procedimientos químicos. Ejemplo: dos átomos
TEMA 4: FORMULACIÓN 1.- CONCEPTOS PREVIOS Compuesto químico: es la unión de varios átomos que no pueden separarse por procedimientos físicos pero sí mediante procedimientos químicos. Ejemplo: dos átomos
Química General Básica. Nomenclatura de Compuestos Inorgánicos
 Química General Básica Nomenclatura de Compuestos Inorgánicos Estelí, 11 de marzo de 2011 Formulación y Nomenclatura en Química Inorgánica La fórmula química expresa la composición de moléculas y compuestos
Química General Básica Nomenclatura de Compuestos Inorgánicos Estelí, 11 de marzo de 2011 Formulación y Nomenclatura en Química Inorgánica La fórmula química expresa la composición de moléculas y compuestos
FORMULACIÓN Y NOMENCLATURA INORGÁNICA
 FORMULACIÓN Y NOMENCLATURA INORGÁNICA Número de oxidación (n.o.): es la carga real (si es un ion) o aparente (si no es un ion) que tienen los elementos que forman parte de un compuesto. (Ver la tabla de
FORMULACIÓN Y NOMENCLATURA INORGÁNICA Número de oxidación (n.o.): es la carga real (si es un ion) o aparente (si no es un ion) que tienen los elementos que forman parte de un compuesto. (Ver la tabla de
RÉSUMENES Y EJERCICIOS DE FORMULACIÓN QUÍMICA INORGÁNICA
 RÉSUMENES Y EJERCICIOS DE FORMULACIÓN QUÍMICA INORGÁNICA COMPUESTOS BINARIOS CON OXÍGENO El oxígeno se combina con todos los elementos excepto con los gases nobles. En estos compuestos el oxígeno actúa
RÉSUMENES Y EJERCICIOS DE FORMULACIÓN QUÍMICA INORGÁNICA COMPUESTOS BINARIOS CON OXÍGENO El oxígeno se combina con todos los elementos excepto con los gases nobles. En estos compuestos el oxígeno actúa
QUÍMICA INORGÁNICA: INTRODUCCIÓN A LA NOMENCLATURA Y FORMULACIÓN DE COMPUESTOS BINARIOS.
 QUÍMICA INORGÁNICA: INTRODUCCIÓN A LA NOMENCLATURA Y FORMULACIÓN DE COMPUESTOS BINARIOS. En el ámbito de la Química a cada sustancia le corresponde un nombre, que nos permite identificarla, y una fórmula,
QUÍMICA INORGÁNICA: INTRODUCCIÓN A LA NOMENCLATURA Y FORMULACIÓN DE COMPUESTOS BINARIOS. En el ámbito de la Química a cada sustancia le corresponde un nombre, que nos permite identificarla, y una fórmula,
FORMULACIÓN INORGÁNICA. Departamento de Física y Química 3º ESO
 FORMULACIÓN INORGÁNICA Departamento de Física y Química 3º ESO 1. Tabla periódica de los elementos -1 Valencia: capacidad que posee un elemento para combinarse con otro Número de oxidación: número de electrones
FORMULACIÓN INORGÁNICA Departamento de Física y Química 3º ESO 1. Tabla periódica de los elementos -1 Valencia: capacidad que posee un elemento para combinarse con otro Número de oxidación: número de electrones
PROGRAMA TOTAL FÓRMULAS QUÍMICAS Y SISTEMAS DE NOMENCLATURA CLASIFICACIÓN DE LOS COMPUESTOS QUÍMICOS INORGÁNICOS
 Departamento de Física y Química FÍSICA Y QUÍMICA ESO FORMULACIÓN Y NOMENCLATURA DE LOS COMPUESTOS QUÍMICOS INORGÁNICOS PROGRAMA TOTAL INTRODUCCIÓN FÓRMULAS QUÍMICAS Y SISTEMAS DE NOMENCLATURA CLASIFICACIÓN
Departamento de Física y Química FÍSICA Y QUÍMICA ESO FORMULACIÓN Y NOMENCLATURA DE LOS COMPUESTOS QUÍMICOS INORGÁNICOS PROGRAMA TOTAL INTRODUCCIÓN FÓRMULAS QUÍMICAS Y SISTEMAS DE NOMENCLATURA CLASIFICACIÓN
PLAN DE REFUERZO ÁREA PENDIENTE DE CIENCIAS NATURALES 3ºESO
 PLAN DE REFUERZO ÁREA PENDIENTE DE CIENCIAS NATURALES 3ºESO Para superar la materia, el alumno deberá realizar las actividades que se indican a continuación. Se realizarán en un cuaderno destinado únicamente
PLAN DE REFUERZO ÁREA PENDIENTE DE CIENCIAS NATURALES 3ºESO Para superar la materia, el alumno deberá realizar las actividades que se indican a continuación. Se realizarán en un cuaderno destinado únicamente
M m+ + X n- M n X m. Qué es formular un compuesto binario?
 Qué es formular un compuesto binario? Cuando tenemos dos elementos, uno menos electronegativo que otro, es decir uno con tendencia a ceder electrones M m+ (m es número de oxidación o valencia) y otro con
Qué es formular un compuesto binario? Cuando tenemos dos elementos, uno menos electronegativo que otro, es decir uno con tendencia a ceder electrones M m+ (m es número de oxidación o valencia) y otro con
REPASO: FORMULACIÓN INORGÁNICA
 COMPUESTOS BINARIOS REPASO: FORMULACIÓN INORGÁNICA OXÍGENO + METAL ÓXIDOS BÁSICOS COMPUESTOS BINARIOS CON OXÍGENO OXÍGENO + NO METAL ÓXIDOS ÁCIDOS El oxígeno se combina con todos los elementos excepto
COMPUESTOS BINARIOS REPASO: FORMULACIÓN INORGÁNICA OXÍGENO + METAL ÓXIDOS BÁSICOS COMPUESTOS BINARIOS CON OXÍGENO OXÍGENO + NO METAL ÓXIDOS ÁCIDOS El oxígeno se combina con todos los elementos excepto
FORMULACIÓN DE QUÍMICA INORGÁNICA
 DE QUÍMICA INORGÁNICA Del mismo modo que utilizamos las palabras para comunicarnos, en química recurrimos a las fórmulas para representar los compuestos. Estas fórmulas no son arbitrarias, sino que responden
DE QUÍMICA INORGÁNICA Del mismo modo que utilizamos las palabras para comunicarnos, en química recurrimos a las fórmulas para representar los compuestos. Estas fórmulas no son arbitrarias, sino que responden
UD 2 ENLACE QUÍMICO Y FUERZAS INTERMOLECULARES FORMULACIÓN Y NOMENCLATURA DE COMPUESTOS TERNARIOS
 FORMULACIÓN Y NOMENCLATURA DE COMPUESTOS TERNARIOS Ácidos oxoácidos o ternarios Se formulan añadiendo una molécula de agua a los óxidos no metálicos. Óxidos no metálicos Cl 2 O SO Cl 2 O 3 SO 2 N 2 O 3
FORMULACIÓN Y NOMENCLATURA DE COMPUESTOS TERNARIOS Ácidos oxoácidos o ternarios Se formulan añadiendo una molécula de agua a los óxidos no metálicos. Óxidos no metálicos Cl 2 O SO Cl 2 O 3 SO 2 N 2 O 3
NOMENCLATURA COMPUESTOS BINARIOS:
 NOMENCLATURA COMPUESTOS BINARIOS: ÓXIDOS: Existen tres nomenclaturas diferentes para nombrar estos compuestos. Nomenclatura de prefijos griegos: se antepone al nombre del elemento y a la palabra óxido
NOMENCLATURA COMPUESTOS BINARIOS: ÓXIDOS: Existen tres nomenclaturas diferentes para nombrar estos compuestos. Nomenclatura de prefijos griegos: se antepone al nombre del elemento y a la palabra óxido
FORMULACIÓN Y NOMENCLATURA INORGÁNICA
 FORMULACIÓN Y INORGÁNICA (IUPAC 2005) 0 COLEGIO COLÓN MARISTAS HUELVA CURSO ACADÉMICO 2015-2016 ÍNDICE 1. COMPUESTOS BINARIOS.. 2 1.1 ÓXIDOS 2 1.2 HALUROS DE OXÍGENO... 3 1.3 PERÓXIDOS...4 1.4 HIDRUROS..
FORMULACIÓN Y INORGÁNICA (IUPAC 2005) 0 COLEGIO COLÓN MARISTAS HUELVA CURSO ACADÉMICO 2015-2016 ÍNDICE 1. COMPUESTOS BINARIOS.. 2 1.1 ÓXIDOS 2 1.2 HALUROS DE OXÍGENO... 3 1.3 PERÓXIDOS...4 1.4 HIDRUROS..
Como en los óxidos, pero cambiando la palabra óxido por peróxido. Ej: Cs 2 O 2 : peróxido de cesio
 Sustancias simples Formadas por átomos de un mismo elemento. Se nombran usando un prefijo indicando el número de átomos seguido del nombre del elemento. Sustancia Nombre sistemático Nombre común H Monohidrógeno
Sustancias simples Formadas por átomos de un mismo elemento. Se nombran usando un prefijo indicando el número de átomos seguido del nombre del elemento. Sustancia Nombre sistemático Nombre común H Monohidrógeno
SUMARIO FÓRMULAS QUÍMICAS Y SISTEMAS DE NOMENCLATURA CLASIFICACIÓN DE LOS COMPUESTOS QUÍMICOS INORGÁNICOS INTRODUCCIÓN SUSTANCIAS SIMPLES
 Departamento de Ciencias Naturales IES Benalmádena FÍSICA Y QUÍMICA 3º ESO FORMULACIÓN Y NOMENCLATURA DE LOS COMPUESTOS QUÍMICOS INORGÁNICOS FORMULACIÓN Y NOMENCLATURA COMBINACIONES BINARIAS INTRODUCCIÓN
Departamento de Ciencias Naturales IES Benalmádena FÍSICA Y QUÍMICA 3º ESO FORMULACIÓN Y NOMENCLATURA DE LOS COMPUESTOS QUÍMICOS INORGÁNICOS FORMULACIÓN Y NOMENCLATURA COMBINACIONES BINARIAS INTRODUCCIÓN
Nomenclatura Inorgánica
 Nomenclatura Inorgánica Nomenclatura Química O Es el sistema de normas, comunes en todo el mundo, para denominar a los elementos y compuestos químicos. O El organismo encargado de dictar tales normas se
Nomenclatura Inorgánica Nomenclatura Química O Es el sistema de normas, comunes en todo el mundo, para denominar a los elementos y compuestos químicos. O El organismo encargado de dictar tales normas se
Colegio Superior de Señoritas Tema: Formación de Compuestos Químicos Septiembre 2010 Prof.: NVM 8vo Nivel Departamento de Ciencias
 COMPUESTOS QUÍMICOS Y SU CLASIFICACIÓN El número de oxidación: representa la cantidad de electrones que puede ganar o perder un elemento. El hidrógeno tiene número de oxidación +1 y puede perder un electrón;
COMPUESTOS QUÍMICOS Y SU CLASIFICACIÓN El número de oxidación: representa la cantidad de electrones que puede ganar o perder un elemento. El hidrógeno tiene número de oxidación +1 y puede perder un electrón;
FORMULACIÓN Compuestos inorgánicos
 Compuestos inorgánicos HSO 2 4 MgF 2 Na CO 2 3 I. Elementos. Valencias II. Sustancias simples III. Combinaciones binarias del hidrógeno A. Hidrácidos B. Hidrógeno con otros no metales C. Hidruros metálicos
Compuestos inorgánicos HSO 2 4 MgF 2 Na CO 2 3 I. Elementos. Valencias II. Sustancias simples III. Combinaciones binarias del hidrógeno A. Hidrácidos B. Hidrógeno con otros no metales C. Hidruros metálicos
FORMULACIÓN Y NOMENCLATURA (SISTEMÁTICA)
 FORMULACIÓN Y NOMENCLATURA (SISTEMÁTICA) FORMULACIÓN: el conjunto de reglas que se emplean para la representación simbólica de los compuestos químicos. NOMENCLATURA: la forma de nombrar los compuestos.
FORMULACIÓN Y NOMENCLATURA (SISTEMÁTICA) FORMULACIÓN: el conjunto de reglas que se emplean para la representación simbólica de los compuestos químicos. NOMENCLATURA: la forma de nombrar los compuestos.
Calcio(2+) Hierro(3+)
 CATIONES MONOATÓMICOS MONOATÓMICOS La carga se indica con un superíndice a la derecha del símbolo del elemento seguido del signo + Ca + Fe 3+ La carga se indica con un superíndice a la derecha seguido
CATIONES MONOATÓMICOS MONOATÓMICOS La carga se indica con un superíndice a la derecha del símbolo del elemento seguido del signo + Ca + Fe 3+ La carga se indica con un superíndice a la derecha seguido
FORMULACIÓN -TEORIA ÓXIDOS. Son combinaciones binarias con oxígeno. Unidos con metales o no metales más.
 FORMULACIÓN -TEORIA ÓXIDOS Son combinaciones binarias con oxígeno. Unidos con metales o no metales más. Formulación: Se escribe el nombre del metal o no metal y luego se intercambian las valencias, se
FORMULACIÓN -TEORIA ÓXIDOS Son combinaciones binarias con oxígeno. Unidos con metales o no metales más. Formulación: Se escribe el nombre del metal o no metal y luego se intercambian las valencias, se
Los elementos químicos se caracterizan por un nombre y un símbolo, acordados por la IUPAC (International Union of Pure and Applied Chemistry).
 4. FORMULACIÓN. 4.1. SÍMBOLOS E HIDRUROS. 4.1.1. SÍMBOLOS Y VALENCIAS. Los elementos químicos se caracterizan por un nombre y un símbolo, acordados por la IUPAC (International Union of Pure and Applied
4. FORMULACIÓN. 4.1. SÍMBOLOS E HIDRUROS. 4.1.1. SÍMBOLOS Y VALENCIAS. Los elementos químicos se caracterizan por un nombre y un símbolo, acordados por la IUPAC (International Union of Pure and Applied
FÍSICA Y QUÍMICA cuaderno de ejercicios
 FÍSICA Y QUÍMICA cuaderno de ejercicios FORMULACIÓN y nomenclatura 1.** Determinen si las siguientes afirmaciones se refieren a metales o a no metales. 1.1. Presentan un brillo característico. 1.2. Los
FÍSICA Y QUÍMICA cuaderno de ejercicios FORMULACIÓN y nomenclatura 1.** Determinen si las siguientes afirmaciones se refieren a metales o a no metales. 1.1. Presentan un brillo característico. 1.2. Los
REPASO FORMULACIÓN INORGÁNICA 1
 REPASO FORMULACIÓN INORGÁNICA 1 IES TURANIANA Nombre: Fecha: RELACIÓN 1: ÓXIDOS Trióxido de azufre Dióxido de azufre Oxido de cobalto (II) Oxido de magnesio Oxido de estaño (II) Oxido de potasio Oxido
REPASO FORMULACIÓN INORGÁNICA 1 IES TURANIANA Nombre: Fecha: RELACIÓN 1: ÓXIDOS Trióxido de azufre Dióxido de azufre Oxido de cobalto (II) Oxido de magnesio Oxido de estaño (II) Oxido de potasio Oxido
Trióxido de dihierro
 Curso 2012-13 FORMULACIÓN QUÍMICA INORGÁNICA COMBINACIONES BINARIAS CPI Conde de Fenosa Ares Los óxidos son combinaciones de los elementos con el oxígeno. El nombre de estos compuestos siempre incluye
Curso 2012-13 FORMULACIÓN QUÍMICA INORGÁNICA COMBINACIONES BINARIAS CPI Conde de Fenosa Ares Los óxidos son combinaciones de los elementos con el oxígeno. El nombre de estos compuestos siempre incluye
Nombrar Compuesto Sistemática Stok HI. Seleniuro de hidrógeno. Cloruro de hidrógeno. Fluoruro de hidrógeno. Sulfuro de hidrógeno
 Nombrar Compuesto Sistemática Stok HI Yoduro de hidrógeno H 2 Se HF H 2 S Seleniuro de hidrógeno Cloruro de hidrógeno Fluoruro de hidrógeno Sulfuro de hidrógeno Ácido yodhídrico Ácido selenhídrico Ácido
Nombrar Compuesto Sistemática Stok HI Yoduro de hidrógeno H 2 Se HF H 2 S Seleniuro de hidrógeno Cloruro de hidrógeno Fluoruro de hidrógeno Sulfuro de hidrógeno Ácido yodhídrico Ácido selenhídrico Ácido
EJRCICIOS de FORMULACIÓN DE FÍSICA Y QUÍMICA 3º ESO
 EJRCICIOS de FORMULACIÓN DE FÍSICA Y QUÍMICA 3º ESO Pablo Martín CURSO 2014-2015 1 EJERCICIOS DE FORMULACIÓN DE INORGÁNICA: Escribe el nombre de los siguientes compuestos 1. Cl 2 O 5 2. PbCl 4 3. HCl 4.
EJRCICIOS de FORMULACIÓN DE FÍSICA Y QUÍMICA 3º ESO Pablo Martín CURSO 2014-2015 1 EJERCICIOS DE FORMULACIÓN DE INORGÁNICA: Escribe el nombre de los siguientes compuestos 1. Cl 2 O 5 2. PbCl 4 3. HCl 4.
APUNTES DE FORMULACIÓN Y NOMENCLATURA DE QUÍMICA INORGÁNICA 3º ESO - CURSO METALES
 CONSEJERÍA DE EDUCACIÓN APUNTES DE FORMULACIÓN Y NOMENCLATURA DE QUÍMICA INORGÁNICA 3º ESO - CURSO 2012-2013 1. ELEMENTOS, SÍMBOLOS Y NÚMEROS DE OXIDACIÓN MÁS FRECUENTES EN LA FORMULACIÓN DE QUÍMICA INORGÁNICA
CONSEJERÍA DE EDUCACIÓN APUNTES DE FORMULACIÓN Y NOMENCLATURA DE QUÍMICA INORGÁNICA 3º ESO - CURSO 2012-2013 1. ELEMENTOS, SÍMBOLOS Y NÚMEROS DE OXIDACIÓN MÁS FRECUENTES EN LA FORMULACIÓN DE QUÍMICA INORGÁNICA
NOMENCLATURA y FORMULACIÓN en QUÍMICA INORGÁNICA. Nivel: Educación Secundaria Obligatoria
 NOMENCLATURA y FORMULACIÓN en QUÍMICA INORGÁNICA Nivel: Educación Secundaria Obligatoria Conceptos básicos Los elementos químicos se representan mediante símbolos, que consisten en una o dos letras que
NOMENCLATURA y FORMULACIÓN en QUÍMICA INORGÁNICA Nivel: Educación Secundaria Obligatoria Conceptos básicos Los elementos químicos se representan mediante símbolos, que consisten en una o dos letras que
Metal y no. metal. sodio. cloruro de COMPUESTOS IES RIBERA DE CASTILLA. Óxidos. Peróxidos. que los binarios) Pág 1
 FORMULACIÓN DE LOS COMPUESTOS QUÍMICOS BINARIOS Igual que todas las personas tenemos un nombre, también cada compuesto químico tiene el suyo. Es importante conocer la fórmula y el nombre de los compuestos
FORMULACIÓN DE LOS COMPUESTOS QUÍMICOS BINARIOS Igual que todas las personas tenemos un nombre, también cada compuesto químico tiene el suyo. Es importante conocer la fórmula y el nombre de los compuestos
Compuestos Binarios- Óxidos-Hidruros-Hidrácidos-Sales Binarias. ÓXIDOS ( Metal/No Metal + O )
 Alcalinos + O Alcalino-Térreos + O Metales de Transición + O Térreos + O Carbonoideos + O ÓXIDOS ( Metal/No Metal + O ) Li 2 O monóxido de dilitio óxido de litio (I) Na 2 O monóxido de disodio óxido de
Alcalinos + O Alcalino-Térreos + O Metales de Transición + O Térreos + O Carbonoideos + O ÓXIDOS ( Metal/No Metal + O ) Li 2 O monóxido de dilitio óxido de litio (I) Na 2 O monóxido de disodio óxido de
Nomenclatura de Compuestos Inorgánicos
 Repartido Nomenclatura Compuestos Inorgánicos Química 1 B.D. Prof. Javier Ponce Ecuaciones Químicas: Una ecuación química es la representación de una reacción química. En toda ecuación química se verifica
Repartido Nomenclatura Compuestos Inorgánicos Química 1 B.D. Prof. Javier Ponce Ecuaciones Químicas: Una ecuación química es la representación de una reacción química. En toda ecuación química se verifica
FORMULACIÓN QUÍMICA INORGÁNICA NÚMEROS DE OXIDACIÓN MÁS USUALES DE ALGUNOS ELEMENTOS METALES. Número de oxidación. + 1 Li, Na, K, Rb, Cs y Ag
 1 FORMULACIÓN QUÍMICA INORGÁNICA NÚMEROS DE OXIDACIÓN MÁS USUALES DE ALGUNOS ELEMENTOS METALES Número de oxidación Elementos + 1 Li, Na, K, Rb, Cs y Ag +2 Be, Mg, Ca, Sr, Ba ; Zn y Cd +3 B, Al +1, +2 Cu
1 FORMULACIÓN QUÍMICA INORGÁNICA NÚMEROS DE OXIDACIÓN MÁS USUALES DE ALGUNOS ELEMENTOS METALES Número de oxidación Elementos + 1 Li, Na, K, Rb, Cs y Ag +2 Be, Mg, Ca, Sr, Ba ; Zn y Cd +3 B, Al +1, +2 Cu
TEORÍA Y EJERCICIOS DE FORMULACIÓN QUÍMICA INORGÁNICA
 TEORÍA Y EJERCICIOS DE FORMULACIÓN QUÍMICA INORGÁNICA COMPUESTOS BINARIOS OXÍGENO + METAL-- ÓXIDOS BÁSICOS COMPUESTOS BINARIOS CON OXÍGENO OXÍGENO + NO METAL ÓXIDOS ÁCIDOS El oxígeno se combina con todos
TEORÍA Y EJERCICIOS DE FORMULACIÓN QUÍMICA INORGÁNICA COMPUESTOS BINARIOS OXÍGENO + METAL-- ÓXIDOS BÁSICOS COMPUESTOS BINARIOS CON OXÍGENO OXÍGENO + NO METAL ÓXIDOS ÁCIDOS El oxígeno se combina con todos
FORMULACIÓN DE QUÍMICA INORGÁNICA 3ºESO
 Euclides Enseñanza Sociedad Cooperativa Andaluza Colegio Privado Concertado Arboleda C/ Reina Victoria 2. 41020 Sevilla Telf. 954 408126 Fax 954 440186 www.colegioarboleda.es arboleda@aces-andalucia.org
Euclides Enseñanza Sociedad Cooperativa Andaluza Colegio Privado Concertado Arboleda C/ Reina Victoria 2. 41020 Sevilla Telf. 954 408126 Fax 954 440186 www.colegioarboleda.es arboleda@aces-andalucia.org
Compuesto N. Stock N. tradicional N. sistemática. óxido de hierro (III) óxido férrico trióxido de dihierro
 Ejemplos de óxidos básicos FeO Fe 2 O 3 Cu 2 O CuO CaO PbO 2 óxido de hierro (II) óxido ferroso monóxido de hierro óxido de hierro (III) óxido férrico trióxido de dihierro óxido de cobre (I) óxido cuproso
Ejemplos de óxidos básicos FeO Fe 2 O 3 Cu 2 O CuO CaO PbO 2 óxido de hierro (II) óxido ferroso monóxido de hierro óxido de hierro (III) óxido férrico trióxido de dihierro óxido de cobre (I) óxido cuproso
http://recursos-itaca.blogspot.com.es/ Formulación Inorgánica 1º) Nombra los compuestos siguientes por las tres nomenclaturas:
 1º) Nombra los compuestos siguientes por las tres nomenclaturas: COMPUESTOS BINARIOS CON OXÍGENO OXÍGENO + METAL-- ÓXIDOS BÁSICOS OXÍGENO + NO METAL ÓXIDOS ÁCIDOS El oxígeno se combina con todos los elementos
1º) Nombra los compuestos siguientes por las tres nomenclaturas: COMPUESTOS BINARIOS CON OXÍGENO OXÍGENO + METAL-- ÓXIDOS BÁSICOS OXÍGENO + NO METAL ÓXIDOS ÁCIDOS El oxígeno se combina con todos los elementos
TEMA 4: Formulación inorgánica
 TEMA 4: Formulación inorgánica Tema 4: Formulación Inorgánica 1 1.- CMPUESTS BINARIS Son sustancias formadas por la unión de dos elementos químicos, como por ejemplo NaH, Co 3, Li S y PCl 3 1.1.- los En
TEMA 4: Formulación inorgánica Tema 4: Formulación Inorgánica 1 1.- CMPUESTS BINARIS Son sustancias formadas por la unión de dos elementos químicos, como por ejemplo NaH, Co 3, Li S y PCl 3 1.1.- los En
ísica y uímica FORMULACIÓN Y NOMENCLATURA Nombre Óxido de bario Óxido de sodio Óxido de plata Fórmula
 Formula los siguientes compuestos: EJERCICIOS DE RECAPITULACIÓN Óxido de bario Óxido de sodio Óxido de plata BaO Na 2 O Ag 2 O Óxido de aluminio Al 2 O 3 Óxido de níquel (III) Ni 2 O 3 Óxido de cloro (VII)
Formula los siguientes compuestos: EJERCICIOS DE RECAPITULACIÓN Óxido de bario Óxido de sodio Óxido de plata BaO Na 2 O Ag 2 O Óxido de aluminio Al 2 O 3 Óxido de níquel (III) Ni 2 O 3 Óxido de cloro (VII)
Trióxido de dihierro
 ÓXIDOS Los óxidos son combinaciones de los elementos con el oxígeno. El nombre de estos compuestos siempre incluye la palabra óxido que puede estar precedida de prefijos numerales indicadores del número
ÓXIDOS Los óxidos son combinaciones de los elementos con el oxígeno. El nombre de estos compuestos siempre incluye la palabra óxido que puede estar precedida de prefijos numerales indicadores del número
Vamos a estudiar las sustancias a las que dan lugar los átomos. Pueden ser de dos tipos: ELEMENTOS. Sustancias formadas por un solo tipo de átomos.
 Vamos a estudiar las sustancias a las que dan lugar los átomos. Pueden ser de dos tipos: ELEMENTOS. Sustancias formadas por un solo tipo de átomos. COMPUESTOS. Sustancias que resultan de la agrupación
Vamos a estudiar las sustancias a las que dan lugar los átomos. Pueden ser de dos tipos: ELEMENTOS. Sustancias formadas por un solo tipo de átomos. COMPUESTOS. Sustancias que resultan de la agrupación
NOMENCLATURA y FORMULACIÓN en QUÍMICA INORGÁNICA
 NOMENCLATURA y FORMULACIÓN en QUÍMICA INORGÁNICA Adaptado a las normas de la IUPAC 1990 Nivel: 3º ESO 1 0. Introducción Valencia Es la capacidad que posee un elemento de combinarse con otro. Como el hidrógeno
NOMENCLATURA y FORMULACIÓN en QUÍMICA INORGÁNICA Adaptado a las normas de la IUPAC 1990 Nivel: 3º ESO 1 0. Introducción Valencia Es la capacidad que posee un elemento de combinarse con otro. Como el hidrógeno
INSTITUTO EDUCACIÓN SECUNDARIA POLITÉCNICO. CARTAGENA. 3º E.S.O.
 Cartagena-2012 1 FORMULACIÓN Y NOMENCLATURA INORGÁNICA 0. SÍMBOLOS Y VALENCIAS DE LOS ELEMENTOS Los símbolos y valencias de los elementos más comunes vienen recogidos en el ANEXO I. Por último, indicaremos
Cartagena-2012 1 FORMULACIÓN Y NOMENCLATURA INORGÁNICA 0. SÍMBOLOS Y VALENCIAS DE LOS ELEMENTOS Los símbolos y valencias de los elementos más comunes vienen recogidos en el ANEXO I. Por último, indicaremos
NOMENCLATURA DE QUÍMICA INORGÁNICA COMPUESTOS BINARIOS (3.º ESO)
 NOMENCLATURA DE QUÍMICA INORGÁNICA COMPUESTOS BINARIOS Para qué la nomenclatura química? Cuando estudiamos química nos encontramos con multitud de sustancias a las que debemos de asignar un nombre y una
NOMENCLATURA DE QUÍMICA INORGÁNICA COMPUESTOS BINARIOS Para qué la nomenclatura química? Cuando estudiamos química nos encontramos con multitud de sustancias a las que debemos de asignar un nombre y una
FORMULACIÓN INORGÁNICA
 1 FORMULACIÓN INORGÁNICA Hay tres métodos para poder nombrar cualquier compuesto, el tradicional, el de Stock y la sistemática. Para saber manejar los tres métodos lo mejor es empezar por el más complicado
1 FORMULACIÓN INORGÁNICA Hay tres métodos para poder nombrar cualquier compuesto, el tradicional, el de Stock y la sistemática. Para saber manejar los tres métodos lo mejor es empezar por el más complicado
FORMULACIÓN QUÍMICA (3 o ESO) Prof. Jorge Rojo Carrascosa
 FORMULACIÓN QUÍMICA (3 o ESO) QUÍMICA INORGÁNICA Prof. Jorge Rojo Carrascosa Índice general I FORMULACIÓN QUÍMICA INORGÁNICA 2 1. NÚMEROS DE OXIDACIÓN 4 2. COMBINACIONES CON EL OXÍGENO 5 2.1. ÓXIDOS METÁLICOS.........................
FORMULACIÓN QUÍMICA (3 o ESO) QUÍMICA INORGÁNICA Prof. Jorge Rojo Carrascosa Índice general I FORMULACIÓN QUÍMICA INORGÁNICA 2 1. NÚMEROS DE OXIDACIÓN 4 2. COMBINACIONES CON EL OXÍGENO 5 2.1. ÓXIDOS METÁLICOS.........................
LOS COMPUESTOS QUÍMICOS
 CONTENIDOS Definición de los compuestos químicos. Clasificación de los compuestos químicos. Escritura y Nomenclatura de los compuestos químicos. Los óxidos básicos o metálicos. Los óxidos ácidos o anhídridos.
CONTENIDOS Definición de los compuestos químicos. Clasificación de los compuestos químicos. Escritura y Nomenclatura de los compuestos químicos. Los óxidos básicos o metálicos. Los óxidos ácidos o anhídridos.
NOMENCLATURA INORGÁNICA
 NOMENCLATURA INORGÁNICA Elemento: Se denomina elemento a toda sustancia que no puede descomponerse en otras más sencillas por métodos químicos. Nombre y símbolo de un elemento: Cada elemento se identifica
NOMENCLATURA INORGÁNICA Elemento: Se denomina elemento a toda sustancia que no puede descomponerse en otras más sencillas por métodos químicos. Nombre y símbolo de un elemento: Cada elemento se identifica
FORMULACIÓN Y NOMENCLATURA INORGÁNICA
 FORMULACIÓN Y NOMENCLATURA INORGÁNICA 1º BACH 1. NORMAS BÁSICAS DE FORMULACIÓN Y NOMENCLATURA La fórmula química contiene los símbolos de los elementos que forman el compuesto, acompañados en muchos casos
FORMULACIÓN Y NOMENCLATURA INORGÁNICA 1º BACH 1. NORMAS BÁSICAS DE FORMULACIÓN Y NOMENCLATURA La fórmula química contiene los símbolos de los elementos que forman el compuesto, acompañados en muchos casos
Formulación de Química Inorgánica
 Formulación de Química Inorgánica F. G. Calvo-Flores 1. VALENCIA. Es la capacidad que tiene un átomo de un elemento para combinarse con los átomos de otros elementos y formar compuestos. La valencia es
Formulación de Química Inorgánica F. G. Calvo-Flores 1. VALENCIA. Es la capacidad que tiene un átomo de un elemento para combinarse con los átomos de otros elementos y formar compuestos. La valencia es
Trióxido de dihierro
 COMBINACIONES BINARIAS (4ª ESO) ÓXIDOS Los óxidos son combinaciones de los elementos con el oxígeno. El nombre de estos compuestos siempre incluye la palabra óxido que puede estar precedida de prefijos
COMBINACIONES BINARIAS (4ª ESO) ÓXIDOS Los óxidos son combinaciones de los elementos con el oxígeno. El nombre de estos compuestos siempre incluye la palabra óxido que puede estar precedida de prefijos
FORMULACIÓN DE QUÍMICA INORGÁNICA
 DE QUÍMICA INORGÁNICA Del mismo modo que utilizamos las palabras para comunicarnos, en química recurrimos a las fórmulas para representar los compuestos. Estas fórmulas no son arbitrarias, sino que responden
DE QUÍMICA INORGÁNICA Del mismo modo que utilizamos las palabras para comunicarnos, en química recurrimos a las fórmulas para representar los compuestos. Estas fórmulas no son arbitrarias, sino que responden
DEPARTAMENTO DE FÍSICA Y QUÍMICA
 Qué es formular un compuesto binario? Cuando tenemos dos elementos, uno menos electronegativo que otro, es decir uno con tendencia a ceder electrones Mm+ (m es número de oxidación o valencia) y otro con
Qué es formular un compuesto binario? Cuando tenemos dos elementos, uno menos electronegativo que otro, es decir uno con tendencia a ceder electrones Mm+ (m es número de oxidación o valencia) y otro con
FORMULACIÓN DE QUÍMICA INORGÁNICA.
 FORMULACIÓN DE QUÍMICA INORGÁNICA. A medida que fueron conociéndose los diferentes elementos químicos de la tabla periódica se vio que el número era relativamente pequeño si se compara con la gran variedad
FORMULACIÓN DE QUÍMICA INORGÁNICA. A medida que fueron conociéndose los diferentes elementos químicos de la tabla periódica se vio que el número era relativamente pequeño si se compara con la gran variedad
Reglas generales. n Se nombra electronegativo de electropositivo. n Fórmula electropositivo electronegativo
 nomenclatura Reglas generales n Se nombra electronegativo de electropositivo n El electropositivo no se modifica n El electronegativo se modificará según las reglas de n compuestos binarios, n ternarios
nomenclatura Reglas generales n Se nombra electronegativo de electropositivo n El electropositivo no se modifica n El electronegativo se modificará según las reglas de n compuestos binarios, n ternarios
TEMA 1 NOMENCLATURA Y FORMULACIÓN DE LOS COMPUESTOS QUÍMICOS INORGÁNICOS
 TEMA 1 NOMENCLATURA Y FORMULACIÓN DE LOS COMPUESTOS QUÍMICOS INORGÁNICOS ÍNDICE 1. Tipos de nomenclatura 2. Compuestos binarios 2.1. Combinaciones con hidrógeno 2.2. Combinaciones con oxígeno 2.3. Sales
TEMA 1 NOMENCLATURA Y FORMULACIÓN DE LOS COMPUESTOS QUÍMICOS INORGÁNICOS ÍNDICE 1. Tipos de nomenclatura 2. Compuestos binarios 2.1. Combinaciones con hidrógeno 2.2. Combinaciones con oxígeno 2.3. Sales
COLEGIO MILITAR GENERAL GUSTAVO MATAMOROS D CO "Formamos Hombres Nuevos Para Una Colombia Mejor"
 COLEGIO MILITAR GENERAL GUSTAVO MATAMOROS D CO "Formamos Hombres Nuevos Para Una Colombia Mejor" FECHA: TALLER # 1 AREA : CIENCIAS NATURALES Y MEDIO AMBIENTE HORAS DE CLASE GRADO 10:º ASIGNATURA: QUIMICA
COLEGIO MILITAR GENERAL GUSTAVO MATAMOROS D CO "Formamos Hombres Nuevos Para Una Colombia Mejor" FECHA: TALLER # 1 AREA : CIENCIAS NATURALES Y MEDIO AMBIENTE HORAS DE CLASE GRADO 10:º ASIGNATURA: QUIMICA
Compuestos ternarios (combinaciones de tres elementos) Hidróxidos = Metal - (OH) El grupo (OH): - 1. El metal: el suyo. Al(OH) 3
 Compuestos ternarios (combinaciones de tres elementos) Hidróxidos = Metal - (OH) Ca(OH) 2 ; NaOH ; Al(OH) 3 X (OH) m AgOH ; Zn(OH) 2 ; Cr(OH) 3 N os de oxidación El grupo (OH): - 1 El metal: el suyo Para
Compuestos ternarios (combinaciones de tres elementos) Hidróxidos = Metal - (OH) Ca(OH) 2 ; NaOH ; Al(OH) 3 X (OH) m AgOH ; Zn(OH) 2 ; Cr(OH) 3 N os de oxidación El grupo (OH): - 1 El metal: el suyo Para
Número de oxidación. Es un número que da la carga que presentaría un átomo si los electrones de cada enlace se asignaran al átomo más electronegativo
 FORMULACIÓN Número de oxidación Es un número que da la carga que presentaría un átomo si los electrones de cada enlace se asignaran al átomo más electronegativo Las reglas de asignación del número de oxidación
FORMULACIÓN Número de oxidación Es un número que da la carga que presentaría un átomo si los electrones de cada enlace se asignaran al átomo más electronegativo Las reglas de asignación del número de oxidación
M m+ + X n-! M n X m EJERCICIOS/ESTUDIO. Qué es formular un compuesto binario?
 EJERCICIOS/ESTUDIO Materia: Tema: Física y Química 3º ESO Curso: Qué es formular un compuesto binario? Cuando tenemos dos elementos, uno menos electronegativo que otro, es decir uno con tendencia a ceder
EJERCICIOS/ESTUDIO Materia: Tema: Física y Química 3º ESO Curso: Qué es formular un compuesto binario? Cuando tenemos dos elementos, uno menos electronegativo que otro, es decir uno con tendencia a ceder
Ejercicios de Formulación y Nomenclatura de Química y Inorgánica 1º Bach.
 Nombrar Compuesto Sistemática Stok HI Yoduro de hidrógeno Ácido yodhídrico H 2 Se Seleniuro de hidrógeno Ácido selenhídrico Cloruro de hidrógeno Ácido Clorhídrico HF Fluoruro de hidrógeno Ácido fluorhídrico
Nombrar Compuesto Sistemática Stok HI Yoduro de hidrógeno Ácido yodhídrico H 2 Se Seleniuro de hidrógeno Ácido selenhídrico Cloruro de hidrógeno Ácido Clorhídrico HF Fluoruro de hidrógeno Ácido fluorhídrico
OXIDOS METÁLICOS O BÁSICOS. Regla 1: se escribe la palabra óxido + nombre del metal (catión) + número de oxidación en números romanos
 OXIDOS METÁLICOS O BÁSICOS Nomenclatura Stock Regla 1: se escribe la palabra óxido + nombre del metal (catión) + número de oxidación en números romanos Hg +1 O -2 = Hg2O = óxido de mercurio (I) Hg +2 O
OXIDOS METÁLICOS O BÁSICOS Nomenclatura Stock Regla 1: se escribe la palabra óxido + nombre del metal (catión) + número de oxidación en números romanos Hg +1 O -2 = Hg2O = óxido de mercurio (I) Hg +2 O
Ti: +,+,+ en los hidruros no metálicos. +,+ en los óxidos, hidróxidos, hidruros metálicos. Cr: +,+ en las sales binarias. Mn:
 Número de oxidación de un átomo en un compuesto es un número teórico que indica el número de electrones que el átomo habría perdido o ganado, si el compuesto fuera completamente iónico. El número de oxidación,
Número de oxidación de un átomo en un compuesto es un número teórico que indica el número de electrones que el átomo habría perdido o ganado, si el compuesto fuera completamente iónico. El número de oxidación,
EJERCICIOS DE REPASO DE FORMULACIÓN Y NOMENCLATURA DE QUÍMICA INORGÁNICA COMPUESTOS BINARIOS
 EJERCICIOS DE REPASO DE FORMULACIÓN Y NOMENCLATURA DE QUÍMICA INORGÁNICA COMPUESTOS BINARIOS No hace falta hacerlos todos, ya os habréis dado cuenta de que si entendéis la lógica que hay detrás de la formulación
EJERCICIOS DE REPASO DE FORMULACIÓN Y NOMENCLATURA DE QUÍMICA INORGÁNICA COMPUESTOS BINARIOS No hace falta hacerlos todos, ya os habréis dado cuenta de que si entendéis la lógica que hay detrás de la formulación
11 Dióxido de carbono. 12 Trióxido de monoazufre. 13 Pentaóxido de difósforo. 14 Dióxido de monoselenio. 15 Dióxido de selenio. 16 Óxido de dimercurio
 1 FÍSICA Y QUÍMICA 3º ESO QUÍMICA - FORMULACIÓN Y SISTEMÁTICAMENTE LOS SIGUIENTES ÓXIDOS 1 Cu 2 O 2 Be O 3 I 2 O 5 4 CO 2 5 NiO 6 Ag 2 O 7 Li 2 O 8 N 2 O 3 9 CrO 10 Ni 2 O 3 11 Dióxido de carbono 12 Trióxido
1 FÍSICA Y QUÍMICA 3º ESO QUÍMICA - FORMULACIÓN Y SISTEMÁTICAMENTE LOS SIGUIENTES ÓXIDOS 1 Cu 2 O 2 Be O 3 I 2 O 5 4 CO 2 5 NiO 6 Ag 2 O 7 Li 2 O 8 N 2 O 3 9 CrO 10 Ni 2 O 3 11 Dióxido de carbono 12 Trióxido
Universidad Técnica Nacional
 Universidad Técnica Nacional Química I-CB005 Nomenclatura de Compuestos Inorgánicos Lic. Diego Orozco González Nomenclatura Clasificación de los compuestos Compuestos orgánicos Contienen carbono y otros
Universidad Técnica Nacional Química I-CB005 Nomenclatura de Compuestos Inorgánicos Lic. Diego Orozco González Nomenclatura Clasificación de los compuestos Compuestos orgánicos Contienen carbono y otros
Formulación Inorgánica Ejercicios (II)
 Ejercicios (II) EJERCICIOS DE FORMULACIÓN INORGÁNICA (II) COMPUESTOS BINARIOS DEL OXÍGENO 1.- Nombrar: Cl2O7 FeO N2O SO3 Cr2O3 Br2O P2O5 CO2 I2O5 2.- Formular: MnO2 Trióxido de dicromo Óxido de nitrógeno
Ejercicios (II) EJERCICIOS DE FORMULACIÓN INORGÁNICA (II) COMPUESTOS BINARIOS DEL OXÍGENO 1.- Nombrar: Cl2O7 FeO N2O SO3 Cr2O3 Br2O P2O5 CO2 I2O5 2.- Formular: MnO2 Trióxido de dicromo Óxido de nitrógeno
FORMULACIÓN Y NOMENCLATURA
 FORMULACIÓN Y NOMENCLATURA FORMULACIÓN Una fórmula química es la representación escrita de una molécula o compuesto iónico. Para expresar una fórmula química se utilizan los símbolos de los elementos que
FORMULACIÓN Y NOMENCLATURA FORMULACIÓN Una fórmula química es la representación escrita de una molécula o compuesto iónico. Para expresar una fórmula química se utilizan los símbolos de los elementos que
ÓXIDOS EJEMPLOS EJERCICICIOS. Br 2 O As 2 O 3 B 2 O 3 SnO 2 Cl 2 O 3 As 2 O 5 P 2 O 3. SeO 2 TeO 3 P 2 O 5. Óxido selenioso
 ÓXIDOS EJEMPLOS Fórmula N. Sistemática N. Stock N. tradicional CO Monóxido de carbono Óxido de carbono (I) Óxido carbonoso CO 2 Dióxido de carbono Óxido de carbono (II) Óxido carbónico SO Monóxido de azufre
ÓXIDOS EJEMPLOS Fórmula N. Sistemática N. Stock N. tradicional CO Monóxido de carbono Óxido de carbono (I) Óxido carbonoso CO 2 Dióxido de carbono Óxido de carbono (II) Óxido carbónico SO Monóxido de azufre
Óxido de hierro (III)
 COMPUESTOS BINARIOS: ÓXIDOS Los óxidos son combinaciones del oxígeno con otro elemento. El nombre de estos compuestos siempre incluye la palabra óxido que puede estar precedida de prefijos indicadores
COMPUESTOS BINARIOS: ÓXIDOS Los óxidos son combinaciones del oxígeno con otro elemento. El nombre de estos compuestos siempre incluye la palabra óxido que puede estar precedida de prefijos indicadores
Compuestos binarios (combinaciones de dos elementos) HIDRUROS METÁLICOS= Metal - Hidrógeno. X H m. H : - 1 Metales: el suyo. FeH 3
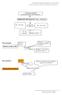 HIDRUROS METÁLICOS= Metal - Hidrógeno AlH 3 ; LiH; CuH 2 X H m KH ; FeH 3 ; ZnH 2 os N de H : - 1 Metales: el suyo Hidruro de hierro(iii) Metal a la izquierda FeH 3 Hidrógeno a la derecha (el mas electronegativo
HIDRUROS METÁLICOS= Metal - Hidrógeno AlH 3 ; LiH; CuH 2 X H m KH ; FeH 3 ; ZnH 2 os N de H : - 1 Metales: el suyo Hidruro de hierro(iii) Metal a la izquierda FeH 3 Hidrógeno a la derecha (el mas electronegativo
BASE + ACIDO SAL + AGUA. NaOH + H Cl NaCl + H 2 O
 SALES Una sal es el producto de la reacción entre un ácido y una base: en esta reacción también se produce agua: en términos muy generales, este tipo de reacción se puede escribir como : BASE + ACIDO SAL
SALES Una sal es el producto de la reacción entre un ácido y una base: en esta reacción también se produce agua: en términos muy generales, este tipo de reacción se puede escribir como : BASE + ACIDO SAL
FORMULACIÓN INORGÁNICA
 FORMULACIÓN INORGÁNICA La nomenclatura (lista de nombre de los compuestos químicos) y la formulación (fórmula de los compuestos químicos) constituyen el lenguaje químico. Número de oxidación. El número
FORMULACIÓN INORGÁNICA La nomenclatura (lista de nombre de los compuestos químicos) y la formulación (fórmula de los compuestos químicos) constituyen el lenguaje químico. Número de oxidación. El número
NOMENCLATURA INORGÁNICA
 NOMENCLATURA INORGÁNICA Símbolos y números de oxidación Reglas para conocer el número de oxidación de un elemento. a. El número de oxidación del hidrógeno en sus compuestos es +1, excepto en los hidruros
NOMENCLATURA INORGÁNICA Símbolos y números de oxidación Reglas para conocer el número de oxidación de un elemento. a. El número de oxidación del hidrógeno en sus compuestos es +1, excepto en los hidruros
