ESTUDIO DE UN SISTEMA DE MARCADORES MICROSATÉLITES PARA LA PROTECCIÓN Y DEFENSA LEGAL DE VARIEDADES DE VID (Vitis vinifera L.)
|
|
|
- Isabel Escobar Suárez
- hace 8 años
- Vistas:
Transcripción
1 UNIVERSIDAD DE ALCALÁ Departamento de Biología Celular y Genética ESTUDIO DE UN SISTEMA DE MARCADORES MICROSATÉLITES PARA LA PROTECCIÓN Y DEFENSA LEGAL DE VARIEDADES DE VID (Vitis vinifera L.) Mª Dolores Vélez Tébar Alcalá de Henares, 2007
2
3 Instituto Madrileño de Investigación y Desarrollo Rural, Agrario y Alimentario (IMIDRA) CONSEJERÍA DE ECONOMÍA Y CONSUMO Comunidad de Madrid D. JAVIER IBÁÑEZ MARCOS, Doctor en Ciencias Biológicas y Jefe de Sección de Conservación y Restauración Ambiental del Instituto Madrileño de Investigación y Desarrollo Rural, Agrario y Alimentario (IMIDRA) CERTIFICA Que la Tesis Doctoral titulada Estudio de un Sistema de Marcadores Microsatélites para la Protección y Defensa Legal de Variedades de Vid (Vitis vinifera L.), que presenta Dª. Mª DOLORES VÉLEZ TÉBAR en el Departamento de Biología Celular y Genética de la Universidad de Alcalá, para optar al grado de Doctor, ha sido realizada bajo su dirección en el Departamento de Investigación Agroalimentaria del I.M.I.D.R.A., y reúne los requisitos necesarios para ser defendida ante el Tribunal. Y para que así conste, expido el presente documento en Alcalá de Henares a 18 de Septiembre de dos mil siete. Fdo.: Javier Ibáñez Marcos V.ºB.º TUTORA, Fdo. Esther Ferrer Cebrián
4
5 Instituto Madrileño de Investigación y Desarrollo Rural, Agrario y Alimentario (IMIDRA) CONSEJERÍA DE ECONOMÍA Y CONSUMO Comunidad de Madrid TESIS DOCTORAL ESTUDIO DE UN SISTEMA DE MARCADORES MICROSATÉLITES PARA LA PROTECCIÓN Y DEFENSA LEGAL DE VARIEDADES DE VID (Vitis vinifera L.) Mª DOLORES VÉLEZ TÉBAR Alcalá de Henares, Septiembre de 2007
6
7 Agradecimientos Me gustaría comenzar esta tesis expresando mi gratitud a todas aquellas personas y entidades que de algún modo, han contribuido durante estos años a la realización de este trabajo. Al Instituto Madrileño de Investigación y Desarrollo Rural, Agrario y Alimentario (IMIDRA) de la Comunidad de Madrid, por la concesión de la Beca Predoctoral que me permitió llevar a cabo esta tesis doctoral, y al INIA (Instituto Nacional de Investigaciones Agrarias)-Ministerio de Ciencia y Tecnología, por financiar el Proyecto VIN C2-1 en su Programa Nacional de Alimentación, que permitió llevar a cabo el estudio de Homogeneidad y Estabilidad. Mi más sincero agradecimiento es sin duda para el Dr. Javier Ibáñez Marcos, por haber confiado en mí y brindarme la oportunidad de trabajar en su equipo, por su buena disposición y por la gran cantidad de tiempo y esfuerzo dedicado. A mi tutora en la Universidad de Alcalá, la Dra. Esther Ferrer Cebrián, por el interés y apoyo demostrado en la realización de este proyecto. Este trabajo ha sido posible gracias a la colaboración de numerosas personas e instituciones, tanto públicas como privadas, que han facilitado la recogida de material en las distintas áreas geográficas, tanto en territorio nacional como internacional. En concreto, el material vegetal de España correspondiente a variedades de uva de vinificación, se obtuvo esencialmente mediante la colaboración con numerosas Denominaciones de Origen: Almansa, Calatayud, Campo de Borja, Cariñena, Tarragona, Condado de Huelva, Costers del Segre, Jerez, Jumilla, La Mancha, Méntrida, Monterrei, Montilla-Moriles, Navarra, Penedés, Ribeira Sacra, Ribeiro, Ribera de Duero, Ribera del Guadiana, Rueda, Rioja, Málaga, Utiel-Requena, Valdeorras, Valdepeñas, Valencia, Vinos de Madrid y Yecla. Entre las personas que contribuyeron personalmente a la recogida de muestras, se encuentran: José María Hurtado (Superior Frutícola S.A., Murcia); Edit Hajdu (FVM Szölészeti és Borászati Kutató Intézete, Hungría); Patricio Hinrichsen (Centro experimental La Platina (INIA), Chile); Tim Sheehan (Sheehan Genetics,
8 USA); Jean Satterwhite (National Clonal Germoplasm Repository for Nut Crops, USA); Erika Dettweiler (Institute for Grapevine Breeding, Alemania); Jorge Cerolo (Agrovolcán, Tenerife); Nuria Cid (Estación de Viticultura y Enología de Galicia, Orense); Peter Allderman (Top Fruit, Sudáfrica); Thierry Lacombe (DGPC-Diversité et Génomes des Plantes Cultivées, Francia); Miguel Lara (CIFA-Centro de Investigación y Formación Agraria, Jerez de la Frontera); Javier Ibáñez, Joaquín Borrego, Paz Fernández, Maite de Andrés, Carlos González, Alba Osorio, Gregorio Muñoz, Cristina Rubio y Mariano Cabellos (IMIDRA). Una obligada y merecida mención es para mis compañeros del Laboratorio de Biología Molecular del Departamento de Agroalimentación del IMIDRA. Gracias por los buenos momentos que hemos compartido, por vuestra ayuda, apoyo, ánimo, comprensión Todos estos años, me han servido para darme cuenta de que a parte de ser unos estupendos compañeros, sois unos amigos inigualables. Gracias a Silvia, Paz, Alba, Carmen, Carlos, Maite, Javier y Joaquín. Tampoco puedo olvidarme de mis Compañeras Becarias : Alba, Visi, Maite y Loli, con las que tantas risas y agobios he compartido. Ánimo chicas, las siguientes sois vosotras! Quiero agradecer de forma muy especial a mis amigos el enorme apoyo y comprensión prestados durante este tiempo. Y por último, quiero dar las gracias a mi familia, en concreto a mis padres, ya que siempre confiaron en mí y estuvieron a mi lado en este largo camino. A todos y cada uno, GRACIAS
9 ABREVIATURAS ADN: Ácido desoxirribonucléico ADPIC: Aspectos de los Derechos de Propiedad Intelectual relacionados con el Comercio AFLP: Amplified Fragment Length Polymorphism AMOVA: Análisis Molecular de la Varianza BMT: Biochemical and Molecular Techniques and DNA-Profiling in particular CGIAR: Grupo Consultivo sobre Investigación Agrícola Internacional CIFA: Centro de Investigación y Formación Agraria CIOPORA: International Community of Breeders of Asexually Reproduced Ornamental and Fruit Varieties DHE: Distinción, Homogeneidad, Estabilidad DUS: Distinctness, Uniformity, Stability EDV: Variedades Esencialmente Derivadas EFV: Especies de la Familia Vitáceas no del género Vitis EGV: Especies del Género Vitis no vinifera EHW: Equilibrio de Hardy Weinberg EST: Expression Sequence Tag FAO: Organización de las Naciones Unidas para la Agricultura y la Alimentación Fst: Índice de Fijación HPD: Híbridos Productores Directos Ho: Heterocigosidad observada IMIDA: Instituto Murciano de Investigación y Desarrollo Agrario y Alimentario IMIDRA: Instituto Madrileño de Investigación y Desarrollo Rural, Agrario y Alimentario INIA: Instituto Nacional de Investigaciones Agrarias IPGRI: International Plant Genetic Resources Institute ISF: Federación Internacional de Semillas LR: Likelihood Ratio MAAP: Polimorfismo de Amplicones Múltiples Arbitrarios MAPA: Ministerio de Agricultura, Pesca y Alimentación MCMC: Cadena de Markov Monte Carlo NCBI: National Center of Biotechnology Information OCVV: Oficina Comunitaria de Variedades Vegetales OEVV: Oficina Española de Variedades Vegetales OIV: Organización Internacional de la Viña y el Vino OMC: Organización Mundial de Comercio PCR: Reacción en Cadena de la Polimerasa PI: Probabilidad Total de Identidad PTI: Portainjertos PVPP: Poli Vinil Poli Pirrolidona RAPD: Random Amplified Polymorphic DNA RFLP: Restriction Fragment Lenght Polymorphism SDL: seedless (sin semillas) SSR: Repeticiones de Secuencias Simples STMS: Sequence-Tagged Microsatellite Site STS: Sitios Marcados por Secuencia UPOV: Unión Internacional para la Protección de las Obtenciones Vegetales
10
11 ÍNDICE
12
13 1. INTRODUCCIÓN VITICULTURA Origen de la vid Encuadre taxonómico de la vid Clasificación de las variedades de vid por el destino de sus productos Cultivo de la vid en el mundo y en España Diversidad genética de la vid Variedad-población, sortogrupo, variedad y clon Homonimias y sinonimias Colecciones de variedades de vid CARACTERIZACIÓN DE VARIEDADES DE VID Ampelografía Métodos morfométricos Técnicas moleculares bioquímicas Técnicas moleculares basadas en el análisis de ADN Microsatélites Características de los microsatélites Uso de los STMS para caracterización de vid MARCO LEGAL Principios básicos sobre las variedades de vid Registro de Variedades Comerciales Protección legal de las obtenciones vegetales Normativa Protección y defensa legal Exámenes DHE Identificación, distinción y derivación esencial Posiciones frente al empleo de los marcadores moleculares en la protección y defensa legal de variedades vegetales En la protección legal (exámenes DHE) En la defensa legal (identificación y establecimiento de la derivación esencial) OBJETIVOS MATERIALES Y MÉTODOS MATERIALES...41
14 Material vegetal Estudio de Distinción Estudio de Identificación Estudio de Homogeneidad y Estabilidad Selección de variedades Toma de muestras Establecimiento de descriptores microsatélite MÉTODOS Extracción de ADN Estimación de la calidad y cantidad del ADN extraído Métodos de análisis de microsatélites (STMS) de genoma nuclear Amplificación de las secuencias STMS mediante PCR Determinación del tamaño de los alelos de los STMS Categorización de alelos para los estudios de Distinción e Identificación Análisis de microsatélites adicionales Diseño experimental Protección legal Estudio de Distinción Estudio de Homogeneidad y Estabilidad Defensa legal Estudio de Identificación Análisis matemático de la coincidencia Análisis de estructura Establecimiento de la derivación esencial Elaboración de descriptores microsatélite RESULTADOS Y DISCUSIÓN SISTEMA DE 9 MICROSATÉLITES EMPLEADO Extracción y cuantificación de ADN Selección de los microsatélites Diseño de la PCR múltiple para los 9 loci microsatélite Análisis en un analizador genético ESTUDIO DE DISTINCIÓN
15 Estudio de una colección para el cálculo de la distancia mínima Cálculo de la distancia mínima Utilidad del sistema de 9 loci microsatélite para el estudio de Distinción ESTUDIO DE IDENTIFICACIÓN Idoneidad de la colección utilizada Análisis de la estructura de la colección Análisis matemático de la coincidencia genotípica Utilidad del sistema de 9 loci microsatélite y de la colección de referencia, para el estudio de Identificación ESTUDIO DE HOMOGENEIDAD Y ESTABILIDAD Evaluación de la selección varietal Muestreo para el estudio de Homogeneidad y Estabilidad Errores de muestreo Evaluación de los datos microsatélite obtenidos Análisis de las diferencias superiores a 1 nucleótido Identificación de posibles quimeras en las variedades Merlot y Cardinal Consecuencias del quimerismo en los exámenes de Homogeneidad y Estabilidad Utilidad del sistema de 9 loci microsatélite para el estudio de Homogeneidad y Estabilidad PROPUESTA DE UTILIZACIÓN DEL SISTEMA Y TOMA DE DECISIONES Defensa legal Identificación de variedades de vid Establecimiento de la derivación esencial Protección legal Exámenes DHE Manejo de una colección de referencia Análisis crítico individualizado de los 9 loci microsatélite PROPUESTA DE 5 NUEVOS DESCRIPTORES MICROSATÉLITE CONCLUSIONES BIBLIOGRAFÍA
16 7. ANEXOS ANEXO I ANEXO II SUMMARY...229
17 1. INTRODUCCIÓN
18
19 Introducción 1. INTRODUCCIÓN 1.1. VITICULTURA Origen de la vid En la actualidad, la vid es uno de los mayores cultivos hortícolas del mundo, el cual ha estado estrechamente relacionado con el desarrollo de la cultura humana. Su principal producto, el vino, fue considerado como una bebida de los dioses, jugando también un papel muy importante en la cultura mediterránea. En This et al. (2006) se recoge una reciente revisión histórica acerca de este cultivo. La vid pertenece a la familia Vitaceae, la cual está compuesta por casi mil especies, agrupadas en 17 géneros. La mayoría de ellos se encuentran ubicados en regiones intertropicales, siendo muchas de sus plantas empleadas ornamentalmente. El único género de importancia agronómica lo constituye el género Vitis, formado aproximadamente por 60 especies interfértiles representadas casi todas ellas en el Hemisferio Norte. Entre ellas, Vitis vinifera es la única especie empleada en la producción mundial de vino. Es la única especie del género Vitis nativa de Eurasia, lo que parece indicar que su primera aparición data de hace aproximadamente 65 millones de años. Dos formas coexisten hoy en día en Eurasia y en el Norte de África: la forma cultivada, V. vinifera subespecie vinifera (o sativa) y la forma silvestre V. vinifera subespecie silvestris (o sylvestris). Esta separación histórica en subespecies pudo basarse en diferencias morfológicas debidas al aislamiento geográfico u ocurrir como resultado de la domesticación de la vid por los humanos a lo largo del tiempo. Hoy en día existen miles de variedades pertenecientes a las formas cultivadas de Vitis vinifera, clasificadas generalmente de acuerdo a sus productos finales: uvas para mesa, uvas para vinificación y uvas para pasificación. En contraste, las formas salvajes de Vitis vinifera son escasas, extendiéndose desde Portugal hasta Turkmenistán, y desde las riberas del Rin hasta los bosques del norte de Túnez. Se cree que estas formas salvajes son los antepasados de las variedades cultivadas en la actualidad. La domesticación de la vid parece estar muy ligada al descubrimiento del vino, no estando muy claro qué acto sucedió primero. Durante la domesticación de la vid, su biología sufrió cambios muy drásticos, dirigidos a asegurar un mayor contenido de azúcar en las uvas para una mejor fermentación, un mayor rendimiento y una producción más regular. En este proceso, los cambios sufridos en las bayas, en el tamaño de los racimos y el cambio de plantas dioicas (en las formas silvestres) a hermafroditas (en las formas 1
20 Introducción cultivadas) fueron cruciales. También ocurrieron cambios en la morfología de las semillas, y aunque su importancia biológica es desconocida, son de gran utilidad para el estudio de restos arqueológicos, pudiéndose diferenciar si las semillas proceden de vides silvestres o de vides cultivadas. Se desconoce si esos cambios ocurrieron lentamente mediante cruzamientos sexuales, naturales o artificiales (selección humana), o por el contrario ocurrieron rápidamente a través de mutaciones, llevándose a cabo posteriormente los procesos de selección y propagación mediante reproducción vegetativa. Todavía existe la incertidumbre de cuando y donde tuvo lugar la primera domesticación y si existieron también domesticaciones secundarias independientes. Aunque las especies silvestres estuvieron probablemente presentes en muchos lugares de Europa durante el Neolítico, pruebas arqueológicas e históricas sugieren que la primera domesticación ocurrió en Oriente Próximo. La primera evidencia de la producción de vino fue encontrada en Irán, exactamente en el yacimiento neolítico de Hajji Firuz Tepe, situado al norte de los Montes Zagros, hacia el a.c. Semillas de vides domésticas datadas del a.c., fueron encontradas en Georgia y Turquía. Sin embargo, restos de semillas halladas en el Neolítico, en Europa Occidental, sugieren la explotación de la vid en esta época. También se encontraron restos de semillas de vides silvestres en asentamientos franceses de la Edad de Bronce. Otros estudios que ponen de manifiesto posibles eventos de domesticación de la vid, son los llevados a cabo en Arroyo-Garcia et al. (2006), y en Imazio et al. (2006). En el primero, se estudió el ADN cloroplástico tanto de muestras pertenecientes a V. vinifera sativa como a V. vinifera sylvestris. Éstas correspondían a distintos lugares geográficos: Península Ibérica, Europa Central, Norte de África, Italia, Balcanes, Europa del Este, Oriente Próximo y Oriente Medio. Los resultados obtenidos en este estudio, apuntan a la existencia de al menos dos posibles eventos de domesticación, uno en Oriente Próximo y otro en la región del Mediterráneo Occidental, el cual dio lugar a muchas de las variedades presentes actualmente en Europa Occidental. En Imazio et al. (2006) también se estudió el ADN cloroplástico de 141 variedades de vid, éstas eran representativas de 4 regiones geográficas distribuidas entre Oriente Medio y Europa Occidental. Los resultados alcanzados en este estudio sugieren la existencia de un único y común centro de domesticación para todos los cultivares europeos, el cuál estaría localizado en la región de Oriente Medio. 2
21 Introducción Desde los primeros lugares donde se llevó a cabo la domesticación, Oriente Próximo, hubo una extensión gradual facilitada por la multiplicación vegetativa a regiones adyacentes tales como Egipto y la Baja Mesopotamia ( a.c.), y otra más dispersa alrededor del Mediterráneo siguiendo las principales civilizaciones (Asirios, Fenicios, Griegos, Romanos, Etruscos y Cartagineses), (This et al., 2006). El cultivo de la vid se extendió hasta China (Siglo II d.c.) y Japón (3.200 a.c.). Bajo la influencia de los romanos, Vitis vinifera se extendió a las islas y alcanzó muchas regiones templadas de Europa, llegando incluso hasta el norte de Alemania. Esta expansión a menudo seguía las principales rutas del comercio (ej. ríos tales como el Rin, el Ródano, el Danubio y el Garona). Al final del Imperio Romano, los lugares europeos donde se cultivaba la vid coinciden en su mayoría con los de hoy en día. Los romanos fueron los primeros en dar nombre a las variedades de vid, aunque es difícil relacionarlos con los nombres de las variedades actuales. En esa época, probablemente ya se distinguiría entre variedades de uva de mesa y de vino, así como los distintos colores que éstas pueden presentar. En la Edad Media, la iglesia Católica reemplazó a los romanos en la difusión del cultivo de la vid hacia nuevas regiones, y facilitaron el intercambio de material vegetal a través de las cruzadas y con la expansión de su religión hacia el Norte de Europa. La extensión del Islam al Norte de África, España y Oriente Medio también jugó un importante papel en el esparcimiento de la vid (principalmente variedades de uva de mesa). Durante la Edad Media aparecieron nombres de variedades que todavía se siguen utilizando en la actualidad. Siguiendo al Renacimiento (Siglo XVI), Vitis vinifera colonizó los países del Nuevo Mundo. Los misioneros la introdujeron en América, primero como semillas (fáciles de transportar) y después mediante esquejes desde sus países de origen (Francia, Alemania, España, Italia y Europa Oriental). Los esquejes también fueron introducidos en el siglo XIX en Sudáfrica, Australia y Nueva Zelanda, y un poco más tarde en el norte de África. Al final del siglo XIX, después de varios milenios de expansión geográfica de la vid, aparecieron nuevos agentes causantes de enfermedades, tales como los hongos o la filoxera. Se extendieron desde América hasta Europa, causando la destrucción de muchos viñedos europeos, cambiando radicalmente la diversidad de esta especie, tanto en vides cultivadas como en vides silvestres. La diversidad presente hoy en día podría ser un pálido reflejo de la que existía antes de la llegada 3
22 Introducción de la filoxera. La viticultura europea se libró de su extinción gracias a la introducción de varias especies no viníferas del género Vitis originarias de América, que fueron utilizadas como portainjertos y para la producción de híbridos ínterespecíficos resistentes a enfermedades. Esos híbridos productores directos fueron ampliamente utilizados hasta la mitad del Siglo XX, siendo hoy en día muy escasos. Desde finales de los años 50, el cultivo de la vid viene sufriendo otra drástica reducción de su diversidad, debido a la globalización del mercado del vino, favoreciendo la expansión de variedades mundialmente conocidas como Chardonnay, Cabernet sauvignon, Syrah y Merlot, y la desaparición de antiguas variedades locales. De este modo, la diversidad de las variedades de vid presente en la actualidad, ha estado estrechamente influenciada por el ser humano. Hoy en día existen varios miles de variedades, la mayoría se encuentran recogidas en colecciones de variedades de vid Encuadre taxonómico de la vid La familia Vitaceae pertenece al orden Rhamnales y jerárquicamente se clasifica en las siguientes categorías superiores: superorden Celastranae, subclase Rosidae (Rosiflorae), clase Magnoliatae (Dicotiledónea), subdivisión Magnoliophytina (Angio-spermae), división Spermatophyta. Las plantas de esta familia son generalmente arbustos trepadores, con tallo vivaz y leñoso, con zarcillos opuestos a las hojas. Estas últimas son alternas y con estipulas, las flores son pequeñas, regulares y en general hermafroditas. Los estambres son opuestos a los pétalos y el pistilo tiene dos carpelos casi bilobulados. Algunas variedades poseen flores femeninas con estambres no funcionales denominados estambres reflejos. El fruto es una baya y la semilla, si la hay, es de testa dura y gruesa. De acuerdo con Galet (1967), dentro del género Vitis hay dos subgéneros o secciones: Sección Muscadinia. Tienen zarcillos simples, 2n=40 cromosomas, corteza adherente, nudos sin diafragma, bayas poco azucaradas y con una maduración escalonada. Son vides situadas en zonas cálidas y templadas del sudeste de América del Norte: EEUU y México. Incluye tres especies V. rotundifolia Michx, V. munsoniana Simpson y V. popenoeii Fen. 4
23 Introducción Sección Euvitis. Presenta zarcillos bifurcados o compuestos, 2n=38 cromosomas, corteza exfoliable y nudos con diafragma. El grupo se divide en 11 series que, dependiendo de los autores, engloban entre 30 y 60 especies, incluyendo entre ellas V. vinifera. Hidalgo (1999) describe a la vid como un arbusto sarmentoso trepador, que se fija a tutores naturales o artificiales mediante órganos (zarcillos) de los que están provistos. Cuando faltan estos tutores se extiende sobre la superficie del terreno en una posición más o menos erguida ocupando extensiones de alguna consideración. En la planta se distingue una parte enterrada, formada por las raíces, cuyas extremidades se conocen con el nombre de cabellera, y una parte aérea en la que se reconocen el tronco, los brazos y los sarmientos, que duran varios años y en ellos se expanden las hojas, frutos y zarcillos, cuya duración normalmente no pasa de un año. La zona que une la parte subterránea y aérea se denomina cuello. Como ya se ha comentado, mientras que las variedades cultivadas de vid poseen en general flores hermafroditas, la subespecie silvestre es dioica, con plantas de flores masculinas y plantas de flores femeninas (Srinivasan y Mullins, 1976). Los frutos, bayas oligospermas agrupadas en racimos, están constituidos por una película exterior (el epicarpio) que se denomina hollejo, un mesocarpio (la pulpa) que rellena toda la uva, un máximo de cuatro pepitas situadas dentro del endocarpio, y el pincel (prolongación de los vasos conductores del pedicelo a través de los que se nutre la uva durante su formación) Clasificación de las variedades de vid por el destino de sus productos Las variedades de vid se pueden clasificar atendiendo a numerosos criterios: según su origen, su morfología, su distribución geográfica, etc., pero para los objetivos de este trabajo, resulta de mayor interés su clasificación de acuerdo al destino de sus productos. Así, se pueden distinguir tres tipos de variedades (Hidalgo, 1999): Uvas para mesa Corresponde a aquellas variedades que se aprecian más por las condiciones físicas y estructurales de sus frutos que por las características de sus mostos. En general son deseables los racimos grandes, bien conformados, de aspecto hermoso, con bayas sueltas de buen tamaño, pulpa crujiente, piel 5
24 Introducción resistente, difícil desgrane, no excesivamente dulces y sabor fresco. Habitualmente, las uvas de mesa tienen un gran desarrollo de las pepitas, en tamaño y número, factor que si bien es negativo en cuanto a la calidad, está íntimamente ligado al crecimiento de las mismas. Uvas para pasificación Generalmente se utilizan variedades apirenas, aunque no en exclusiva. La apirenia o ausencia de semillas surge como consecuencia de mutaciones de yema en las vides cultivadas. Esta ausencia de semillas puede ocurrir por dos mecanismos: partenocarpia y estenospermocarpia (Hidalgo, 1999). La pasificación es el único destino posible para las uvas sin semillas producidas por partenocarpia (tipo corinto), debido al pequeño tamaño de sus bayas. Este tipo de apirenia requiere que dos sucesos independientes se produzcan en el mismo individuo: el aborto de todos los óvulos y el desarrollo partenocárpico del fruto. Las variedades apirenas estenospermocárpicas (tipo sultanina) pueden en principio utilizarse tanto para mesa como para pasificación. La mayoría de las variedades de interés comercial son de este tipo, y no son estrictamente variedades sin semillas: en ellas se produce fecundación, aunque el posterior desarrollo del embrión y/o del endospermo es incompleto y se interrumpe unas semanas después de la floración [Barrit, 1970, citado por (Carreño et al., 1997)]. Las bayas poseen esbozos de semillas rudimentarias, de tamaño muy pequeño, no lignificadas y, por tanto, no perceptibles por el consumidor. Uvas para vino o mosto El interés de la variedad se centra fundamentalmente en las características y la calidad de su mosto y las del vino a que da lugar. En general son variedades con racimos de tamaño medio a pequeño, apretado, con bayas de dimensiones reducidas o pequeñas, piel fina, elevado contenido en azúcar y pepitas escasas en número y tamaño. La clasificación no puede ser rigurosa puesto que muchas variedades pueden servir para varios usos según las circunstancias. Por ejemplo, la variedad Moscatel de Málaga se utiliza para los tres fines citados. 6
25 Introducción El mercado de la uva de vino es mucho más importante económicamente, y estable, con respecto a las variedades usadas, porque en muchos casos los productores de vino de un determinado lugar tienen que usar ciertas variedades para conseguir una determinada etiqueta de calidad. Así, los esfuerzos de mejora genética están principalmente centralizados en la selección clonal. El mercado de la uva de mesa es mucho más dinámico, y la mayoría de las variedades que están siendo cultivadas en la actualidad, son diferentes con respecto a las cultivadas hace 30 años. El cruzamiento entre diferentes variedades está mucho más extendido en las uvas de mesa, y las nuevas obtenciones de interés son rápidamente distribuidas a otros países productores. Como consecuencia de ello, la protección legal de variedades de vid (similar a una patente o a una propiedad intelectual) afecta principalmente a estas variedades de uva de mesa Cultivo de la vid en el mundo y en España El cultivo de la vid se conoce en España desde la llegada de los fenicios, y se extendió con rapidez hasta llegar a ocupar más de dos millones de hectáreas a finales del siglo XIX. Las primeras referencias fehacientes del cultivo de la vid en tierras españolas, se remontan al año 520 a.c., aunque la expansión de este cultivo y la producción del vino no llegarían a completarse hasta la dominación romana, e incluso posterior a ella en Cantabria y Asturias. La superficie mundial de viñedo ha ido disminuyendo desde 1.986, con cerca de 9 millones de hectáreas, hasta llegar a una cierta estabilización en los últimos años, en cerca de los 8 millones de hectáreas (ha) (estadística de la Organización Internacional de la Viña y el Vino (OIV), datos hasta 2.004). Según las estadísticas de la OIV presentadas por su director general en el XXIX Congreso Mundial de la Viña y el Vino celebrado en Logroño en Junio del 2.006, el 59% de la superficie vitivinícola está en Europa, el 22% en Asia, el 12% en América, el 5% en África y el 2% en Oceanía. España, con 1,1 millones de hectáreas, representa el 14,86% de la superficie mundial; seguida de Francia, con (11,21%); Italia, (10,66%); Turquía, (7,18%); China, (6,13%); Estados Unidos, (5,02%); Irán, (3,73%); Portugal, (3,15%); Rumanía, (2,74%); y Argentina, (2,73%). El Ministerio de Agricultura, Pesca y Alimentación (MAPA), según su Anuario de Estadística Agroalimentaria de 2.004, correspondiente a datos del año 2.003, 7
26 Introducción indica que España con más de un millón de hectáreas ( ha), es el país del mundo con mayor superficie cultivada. De ellas, ha (1,9%) se dedican a la producción de uva de mesa, ha (97,4%) a la producción de uva para vinificación, ha (0,35%) a la producción de uva para pasificación y ha (0,30%) para viveros de viñedo. El total de la producción de uva en España está representado por Tm. De ellas, Tm (4,42%) pertenecen a uva de mesa, Tm (95%) a uva para vinificación y Tm (0,10%) a uva para pasificación. Como se puede observar el porcentaje de uva de mesa aumenta cuando se refiere a producción. Ello se debe al mayor rendimiento de la superficie en producción dedicada a la uva de mesa, por las condiciones de cultivo de cada tipo de explotación. Comparando con datos de de la OIV, se puede indicar que la producción total de uva en España contaba con casi 5 millones de Tm, mientras que en el presenta casi 7 millones, mostrando en estos dos años prácticamente las mismas hectáreas de superficie de cultivo (cerca de 1,2 millones de ha), como ya se ha indicado. En las hectáreas dedicadas en España a la producción de uva de mesa eran ha, mientras que en el el valor es de ha. Aún presentando menos hectáreas de cultivo, en el hay un mayor rendimiento en cuanto a la producción, debido principalmente, a la mejora de las condiciones de cultivo. En cuanto a la uva de vinificación, en 1.996, ha se dedicaron a su producción, prácticamente el mismo número que en el ( ha). Con respecto a la producción de uva destinada para pasificación, en 1.996, ha estaban dedicadas a este fin, siendo este valor muy parecido al presentado en el año (3.598 ha). Según datos del MAPA, correspondientes al año 2.003, las principales comunidades autónomas españolas destinadas a la producción de uva de mesa, vino y pasificación, respectivamente, serían las siguientes: Uva de mesa: Comunidad Valenciana con casi Tm (unas Tm son producidas en Alicante), Murcia con casi Tm y Andalucía con casi Tm (unas Tm son producidas en Sevilla). Uva de vino: Castilla La Mancha con más de Tm (las provincias más productivas son Ciudad Real con casi Tm y Toledo con un poco más de Tm), Extremadura con casi Tm (unas son producidas en 8
27 Introducción Badajoz) y Cataluña (siendo las provincias más productivas Tarragona con casi Tm y Barcelona con casi Tm). Uva para pasificación: Andalucía (Málaga) con Tm y Extremadura (Badajoz) con 132 Tm. Con respecto al comercio exterior de estos tres tipos de uvas en España, los datos del MAPA correspondientes al año fueron los siguientes: Uva de mesa: España exportó Tm de un total de Tm, lo que significa un 40% de toda la producción. Los países receptores de esta uva de mesa son, fundamentalmente, de la Unión Europea (94,5% del total): Alemania (unas Tm), Francia (unas Tm), seguidos de Reino Unido (unas Tm) y Portugal (unas Tm). Uva de vino: España exportó casi Tm de uva de vinificación de un total de Tm, lo que significa únicamente un 4% de toda la producción. Uva para pasificación: únicamente el 10% de la producción total de estas uvas (7.680 Tm) se exportó a países extranjeros Diversidad genética de la vid Variedad-población, sortogrupo, variedad y clon Hasta no hace mucho tiempo, atendiendo a su origen, se podían distinguir dos tipos de variedades: Variedades de origen policlonal: son aquellas que, aunque incluyen plantas que proceden de embriones diferentes, mantienen caracteres comunes, responsables de que sean reconocidas como pertenecientes a la misma variedad. Estas variedades, tradicionalmente se han denominado con el término de variedadpoblación. Según Cervera et al. (2001), el origen policlonal de una variedad probablemente corresponde a variedades pobremente caracterizadas, genética y morfológicamente y que, como consecuencia, incluyen distintas homonimias (variedades distintas designadas con el mismo nombre). En general, no se encuentran muchos ejemplos de variedades policlonales, aunque uno de ellos lo podría constituir el caso de las malvasías: se pueden encontrar diferentes tipos, como la riojana, la subirat parent o la de Sitges, entre otras. 9
28 Introducción Variedades de origen monoclonal: en la actualidad, todas las nuevas variedades de vid presentan un origen monoclonal. Están constituidas por individuos procedentes de un mismo embrión, con un genotipo original, y son por tanto genéticamente idénticos, salvo por las mutaciones somáticas, las cuales pueden ser estables en el tiempo y transmitirse a la descendencia a través de la reproducción vegetativa. Debido a estas mutaciones, no todos los individuos procedentes de un mismo embrión pertenecen a la misma variedad. En las mutaciones somáticas se basa la selección clonal dentro de estas variedades, monoclonales en su origen: la búsqueda de plantas con pequeñas diferencias genéticas, en un fondo esencialmente idéntico, que pueden provocar grandes diferencias agronómicas. A partir de esas plantas se establecen distintos clones de una variedad. En ocasiones, mutaciones somáticas evidentes, como las que afectan al color o tamaño de la baya, la forma del racimo, o al tiempo de maduración, dan lugar a clones que, por su importancia, se constituyen en nuevas variedades. Utilizando un término anglosajón, son los denominados sports, que son genéticamente idénticos a la variedad inicial excepto en uno o unos pocos caracteres. Este hecho es antiguo en viticultura, Negrul en 1946, citado por Bourquin et al. (1993) propuso el concepto de sortogrupo, donde se incluyen una variedad dada junto a todas las originadas a partir de un mismo embrión. Así, por ejemplo, pertenecen al mismo sortogrupo las variedades Pinot gris, Pinot noir, Pinot blanc y Pinot meunier (Regner et al., 2000a). Cuando los sports derivan de una variedad inicial protegida legalmente, se denominan variedades esencialmente derivadas (EDV). Este concepto se introdujo en el Convenio de la UPOV (Unión Internacional para la Protección de las Obtenciones Vegetales) por el Acta de 1991, para mantener un sólido sistema de protección, con el fin de promover la obtención de nuevas variedades vegetales. Aparte de la variabilidad intravarietal originada por el origen policlonal y por las mutaciones somáticas, puede existir variabilidad causada por una heterogeneidad en el estado sanitario de las plantas que constituyen la variedad. Desde el punto de vista estrictamente genético, esta es una variabilidad ficticia, pero puede dar lugar a problemas graves, tanto en la selección clonal como en la caracterización. Especialmente importantes son las virosis, debido a que no existen remedios curativos para ellas. Actualmente, en España, los virus que afectan más gravemente a los cultivos de vid son los siguientes: entrenudo corto, enrollado, 10
29 Introducción jaspeado y madera rizada (Ventura Padilla (Instituto Murciano de Investigación y Desarrollo Agrario y Alimentario-IMIDA), comunicación personal) Homonimias y sinonimias La extensión del cultivo de la vid en el espacio y en el tiempo también ha generado una gran confusión en las denominaciones de las variedades, resultando muy común la existencia de sinonimias y homonimias. La primera hace referencia a que una misma variedad, puede presentar diversos nombres o sinónimos según el lugar donde se cultive. La variedad en cuestión es denominada oficialmente con el nombre más extendido, llamándose al resto de los nombres, sinónimos de esa variedad. Así, los nombres de Tempranillo, Tinto fino, Cencibel, Tinta de Toro, Tinta del País y Ull de Llebre (ojo de liebre) corresponden a la misma variedad en distintas localizaciones geográficas españolas, como por ejemplo, Rioja y Alicante, Madrid, La Mancha, Zamora, Ribera de Duero y Penedés, respectivamente (Ibáñez et al., 2006a). En ocasiones, a variedades distintas se las conoce con el mismo nombre (homonimias), debido a errores o denominaciones populares. Así por ejemplo, en Guadalajara y en Madrid, a veces se denomina Malvar a la variedad Airén. También la variedad Marfal, cultivada en Extremadura, se ha confundido en ocasiones con Malvar, debido a la similitud ortográfica (Ibáñez et al., 2006b). Debido a la gran confusión existente en la denominación de las variedades de vid, tanto en el territorio nacional como en el internacional, resulta extremadamente difícil en la actualidad, conocer el número real de variedades diferentes de vid. Por este motivo, entre otros, resulta fundamental la existencia de colecciones de variedades de vid, donde se conserva y estudia el máximo de diversidad genética de las especies cultivadas y sus afines silvestres Colecciones de variedades de vid Según Alleweldt y Possingham (1988) existen aproximadamente unas variedades distintas, de las cuales, la mayoría se encuentran recogidas en colecciones de variedades de vid distribuidas por todo el mundo. En cambio, en This et al. (2006), basándose en resultados obtenidos mediante perfiles de ADN, se 11
30 Introducción especula que actualmente, el número más acertado de variedades diferentes de vid sería 5.000, estando muchas de ellas estrechamente relacionadas. Aunque todas las colecciones varietales pueden tener la misma aplicación: fuente de material genético para la obtención de nuevas variedades o colección de testigos varietales, cuando dicho material tiene que reunir unas determinadas características sanitarias y garantías de autenticidad varietal, se estaría hablando de colecciones de referencia. Las colecciones de referencia básicas en España son las de la OEVV (Oficina Española de Variedades Vegetales), ubicada en Aranjuez y, la de reserva, en la Escuela Técnica Superior de Ingenieros Agrónomos de Madrid. Actualmente se está preparando una nueva colección de referencia completa en Bullas (Murcia) por el Centro de Ensayos de Evaluación de Variedades del Instituto Nacional de Investigaciones Agrarias (INIA), en colaboración con el IMIDA y la OEVV. En España hay grandes colecciones varietales, pudiéndose decir que casi todas las Comunidades Autónomas disponen de ellas, pero debemos destacar las de la Finca de El Encín (Instituto Madrileño de Investigación y Desarrollo Rural, Agrario y Alimentario-IMIDRA), situada en Alcalá de Henares (Madrid), y El Rancho La Merced (Centro de Investigación y Formación Agraria-CIFA), en Jerez de la Frontera (Cádiz), por ser las más importantes, y ser fuente de otras muchas implantadas o en proceso de implantación. En dichas colecciones, se localiza posiblemente todo el panorama varietal español, además de un gran número de variedades extranjeras CARACTERIZACIÓN DE VARIEDADES DE VID Como se ha señalado anteriormente, la vid es uno de los cultivos más antiguos que se conocen, y existe una gran cantidad de variedades en todo el mundo. Muchas de estas variedades se cultivan desde hace siglos, y algunas son comunes a muchas localizaciones geográficas distintas. Es un hecho ancestralmente conocido por el hombre que distintas variedades de vid dan lugar a diferentes tipos de vino, lo que unido a los diferentes gustos existentes, dio lugar a una necesidad: la identificación, lo más precisa posible, de las distintas variedades disponibles en cada región vitícola. Esta necesidad se resolvió inicialmente, como en la totalidad de especies vegetales y animales, de la forma más natural e intuitiva 12
31 Introducción posible: mediante la descripción y comparación de determinados caracteres visibles. Con el tiempo, el estudio de la vid se hizo más sofisticado y alcanzó un rango elevado, pasando a constituirse en una ciencia propia: la Ampelografía (del griego ámpelos, vid) Ampelografía Tradicionalmente, se han utilizado métodos subjetivos de descripción de los caracteres morfológicos de los órganos de las vides. El International Plant Genetic Resources Institute (IPGRI), que es un centro del Grupo Consultivo sobre Investigación Agrícola Internacional (CGIAR) y que está vinculado a la FAO (Organización de las Naciones Unidas para la Agricultura y la Alimentación), editó los Descriptores para la vid (Vitis spp.) en 1.997, (IPGRI et al., 1997). En un intento de consenso, las listas de descriptores se realizaron en colaboración con la OIV y la UPOV. Los descriptores morfológicos seleccionados para la identificación de variedades de vid deben ser fácilmente detectados a simple vista y deben servir para hacer una discriminación fácil y rápida entre fenotipos. Generalmente son caracteres heredables, que se expresan igualmente en todos los ambientes. Actualmente estos tres organismos: IPGRI, OIV y UPOV presentan descriptores propios, disponen de una lista de caracteres que se refieren a aquellas características de la planta suficientemente estables para ser válidas a la hora de definir y diferenciar las distintas variedades. Estas listas de caracteres coinciden en una gran parte pero no llegan a ser completamente idénticas, pues reflejan los criterios y alternativas elegidos por los distintos grupos de expertos que han conformado cada uno de los organismos internacionales mencionados. Durante los años y 2.007, se han celebrado reuniones entre la UPOV y la OIV para tratar de unificar los descriptores morfológicos seleccionados para la identificación de variedades de vid. En cada descriptor, a cada carácter se le adjudica un código. Los niveles de expresión que pueden presentar cada uno de ellos se corresponden con dígitos enteros entre 1 y 9, y, con el fin de facilitar la determinación de estos niveles, se señalan variedades que sirven de referencia para cada uno. Tanto para la protección de variedades como para la realización de los Registros de Variedades Comerciales (referencia oficial en cuanto al panorama 13
32 Introducción varietal de la especie) en el ámbito de la Unión Europea, se ha fijado el descriptor UPOV como referencia obligada, si bien es frecuente, tener en cuenta el de la OIV, y para algunos cometidos de investigación el del IPGRI. La descripción ampelográfica mínima de una variedad de vid, de acuerdo con la OIV, puede efectuarse con 40 caracteres, mientras que para la descripción completa son necesarios 130. En cualquier caso se incluyen caracteres de todas las partes del ciclo vegetativo de la planta, así como algunos fenológicos. Los órganos de la planta sobre los que se estudian los diversos caracteres de los descriptores son los siguientes: sumidad o pámpano joven, hoja joven, hoja adulta, pámpano, sarmiento, inflorescencia y flor, racimo, baya y semilla. Entre los tratados clásicos de Ampelografía cabe destacar los desarrollados por Viala y Vermorel (1901) y Galet ( ). En el ámbito nacional, merece resaltarse el trabajo de Borrego et al. (1990) y Rodríguez Torres (2001). Pese a resultar indispensable, la Ampelografía adolece de unas características que limitan su utilidad frente a otras técnicas más recientes: Subjetividad: pese a la cuidadosa selección de los descriptores, sigue existiendo un cierto factor de subjetividad en la caracterización morfológica. Largo tiempo necesario para completar la descripción: desde que se inicia una plantación, pueden pasar 4 años hasta que las plantas estén listas para ser descritas. La descripción abarca un ciclo vegetativo completo de la planta, lo que implica un mínimo de cuatro visitas del ampelógrafo a la plantación a lo largo de unos seis meses. Además, debido a diferencias ambientales, el estudio debe realizarse durante varios años. El número de caracteres a estudiar es limitado, por lo que, dado el gran número de variedades de vid, no siempre es posible la identificación inequívoca. Ampliar la lista mínima a otros caracteres conlleva riesgos, pues muchos son susceptibles a las diferencias ambientales, lo que aumenta el riesgo de errores en la identificación. Los distintos tipos de poda afectan a los caracteres morfológicos de la planta, haciendo que los resultados no siempre sean comparables. 14
33 Introducción Métodos morfométricos Se han buscado una serie de caracteres susceptibles de cuantificación estricta y objetiva, con la finalidad de eliminar la subjetividad del operador. Así nació la Ampelometría, método que complementa los estudios ampelográficos. Está basado en la descripción cuantitativa y en el análisis e interpretación de la forma de las hojas mediante el uso de un digitalizador, que facilita tanto las mediciones de longitudes y ángulos presentes en las hojas, como el procesamiento de los datos. En resumen, se trata de un método de simple y rápida aplicación, que sustituye en parte al trabajo del operador en el campo con el fin de identificar una variedad (Cabello et al., 2000) Técnicas moleculares bioquímicas Hace algunos años, fueron bastante utilizadas técnicas moleculares con las que se obtenían estimaciones de la variabilidad de variedades de vid atendiendo a caracteres de tipo bioquímico, tales como isoenzimas de hoja y sarmiento, y proteínas de endospermo. Hoy en día, éstas técnicas prácticamente han sido reemplazadas por aquellas basadas en el estudio de los ácidos nucleicos Técnicas moleculares basadas en el análisis de ADN Las técnicas moleculares permiten estudiar polimorfismos en el ADN, origen de toda la variación genética, y constituyen por tanto una aproximación más fiable para determinar las diferencias entre variedades o especies. Además evitan problemas asociados con influencias medioambientales, factores fisiológicos y expresión específica de tejido y desarrollo. El genoma de la vid acaba de ser secuenciado a través de un proyecto franco-italiano y se encuentra libremente disponible para todo el mundo entre otras, en la página web: La vid posee un tamaño genómico de 475 Mpb organizado en 19 cromosomas (2n=38). Es aproximadamente tres veces mayor que el tamaño del genoma más pequeño conocido en plantas, perteneciente a Arabidopsis thaliana (145 Mpb), similar al del arroz [Oryza sativa ( Mpb)], y cinco veces más pequeño que el del maíz [Zea mays ( Mpb)] (Lodhi y Reisch, 1995). 15
34 Introducción El número de secuencias nucleotídicas totales presentes en el genoma de la vid, y publicadas en el NCBI-National Center of Biotechnology Information (USA) es de , la mayoría de estas secuencias ( ) son ESTs (Expression Sequence Tags-secuencias del genoma que se expresan como ARN). Dentro de estas secuencias nucleotídicas totales, son secuencias unigenes. La secuencia de ADN del genoma de una especie sufre a lo largo de su evolución mutaciones puntuales, deleciones y/o reorganización de fragmentos cromosómicos. Dada la dispersión de las secuencias codificantes en el genoma de los organismos superiores, la mayoría de estos cambios se acumulan en las regiones no codificantes. Los cambios ocurridos en el transcurso de la evolución en secuencias codificantes están sujetos a presión de selección, por lo que según para qué estudios, interesa trabajar con uno u otro tipo de secuencias, siendo las que afectan a regiones no codificantes de gran utilidad para análisis de identidad. A partir de los años 70, aparecieron los llamados marcadores moleculares, que consisten en sistemas polimórficos basados en la detección de pequeñas diferencias existentes en las secuencias del ADN. Se trata por tanto de polimorfismos moleculares relativos a diferencias de bases nucleotídicas que se pueden detectar por una gama diversa de técnicas y que se pueden utilizar como alelos moleculares. Normalmente, se analiza un pequeño fragmento del ADN, que puede o no contener genes. Los primeros marcadores utilizados fueron los RFLP (Restriction Fragment Lenght Polymorphism); una técnica laboriosa que inicialmente requería el empleo de materiales radiactivos, y no es fácilmente automatizable. En los últimos años ha sido ampliamente utilizada la reacción en cadena de la polimerasa (PCR). Esta técnica permite la amplificación de fragmentos específicos, hasta concentraciones muy elevadas, a partir de pequeñas cantidades de ADN molde. Para ello es necesario, además del ADN molde, una ADN polimerasa termoestable, nucleótidos y unos pequeños fragmentos monocatenarios de ADN que por complementariedad de bases se pueden unir al ADN molde y sirven de cebadores a la polimerasa. A partir de dos de estos cebadores que cumplan determinados requisitos, la polimerasa copia el fragmento contenido entre ellos. Este proceso se repite muchas veces, y en cada nuevo ciclo el fragmento recién sintetizado puede servir como molde; así el resultado es una amplificación exponencial de dicho fragmento. La especificidad del fragmento amplificado viene 16
35 Introducción dada por los cebadores, moléculas con secuencias complementarias a alguna zona del ADN molde. Dependiendo de la secuencia del ADN molde, un cebador concreto podrá o no unirse a él, dando lugar o no a la amplificación del fragmento determinado. Cuando no se analiza una secuencia determinada, se utilizan cebadores de secuencia arbitraria, lo que genera amplificación de múltiples regiones polimórficas, que se han denominado MAAP (Polimorfismo de Amplicones Múltiples Arbitrarios), entre ellas se encuentran los RAPD (Random Amplified Polymorphic DNA) (Williams et al., 1990), (Welsh y McClelland, 1990). El análisis de RAPD ha sido ampliamente utilizado en los últimos años debido a sus enormes ventajas en cuanto a su facilidad de uso, rapidez, mínimo requerimiento de muestra de ADN, economía y disponibilidad de un número ilimitado de cebadores útiles para detectar variabilidad. Sin embargo, presenta el inconveniente de la falta de codominancia, es decir, no es posible descifrar la heterocigosidad de los loci observados y adolece de falta de repetitividad cuando varían las condiciones experimentales. Esto hace plantear dudas, cuando de lo que se trata es de identificar variedades de vid con facilidad. Debido a ello, se han desarrollado técnicas alternativas que pueden paliar en parte este problema. Una de esas técnicas serían los AFLP (Amplified Fragment Length Polymorphism) (Vos et al., 1995). Se basa en la amplificación selectiva por PCR de fragmentos de restricción obtenidos en una digestión total de ADN genómico con enzimas de restricción. Presenta un grado de reproducibilidad mucho mayor que los RAPD. Aunque los AFLP, por su parte, también son unos marcadores de tipo dominante y su nivel de complejidad técnica es más alto que el de los RAPD, lo que representa una desventaja. Frente a ellos, los microsatélites presentan una serie de características, detalladas a continuación, que los convierten en unos marcadores moleculares idóneos para la caracterización de variedades de vid entre los disponibles en la actualidad Microsatélites En IPGRI et al. (1997), además de los Descriptores para la Caracterización, basada en el estudio de características morfológicas, estaban 17
36 Introducción reflejados los Descriptores para la Evaluación, de menor importancia, los cuales incluían a los microsatélites entre los marcadores moleculares. La situación hoy en día, diez años más tarde, ha cambiado considerablemente: muchos institutos de la vid utilizan los microsatélites como marcadores para identificar sus variedades, además de, o en vez de, las descripciones morfológicas. La OIV acaba de incorporarlos a su sistema como descriptores para la caracterización Características de los microsatélites Los microsatélites consisten en una pequeña unidad de repetición, generalmente de menos de 4 nucleótidos, que puede estar repetida un número variable de veces en distintos puntos del genoma, normalmente con longitudes menores de 100 pb cada locus. También se llaman por ello repeticiones de secuencias simples (SSR). Desde su descubrimiento se intuyó la utilidad que estas secuencias podían tener como marcadores polimórficos (Tautz, 1989). En Thomas y Scott (1993), se demostró que las secuencias repetidas presentes en el genoma de la vid (microsatélites, minisatélites, genes en tándem y secuencias altamente repetidas), son especialmente útiles para la identificación de cultivares de esta especie. Cabe destacar que, como otros eucariotas, el genoma de la vid es rico en secuencias microsatélites. En concreto observaron que las repeticiones de dinucleótidos (GA) y (GT) eran muy comunes y aparecían dispersas en el genoma, frente a repeticiones de tri o tetranucleótidos (CAC, GACA, GATA), que estaban en menor proporción. Los microsatélites son muy útiles como marcadores genéticos cuando se utilizan como Sitios Marcados por Secuencia o STS, denominados en este caso particular STMS Sequence-Tagged Microsatellite Site. Para su análisis, es necesario determinar previamente las secuencias que flanquean a la repetición. A partir de las mismas se pueden diseñar cebadores específicos para cada locus, y obtener así por amplificación mediante PCR los distintos alelos para cada locus microsatélite particular. Si hay variación de un individuo a otro en el número de veces que la unidad está repetida, se observará una diferencia entre ambos en el tamaño del fragmento amplificado. Dado que la vid es diploide, se obtienen normalmente dos fragmentos amplificados (dos alelos) para cada individuo por locus, excepto en los homocigotos. De esta manera se puede establecer, para cada STMS, la composición alélica de cada variedad. 18
37 Introducción El polimorfismo se genera por un mayor o menor número de repeticiones de la unidad básica. Se han propuesto dos mecanismos para explicar cómo se generan las diferencias en longitud de los distintos alelos: el deslizamiento de las hebras complementarias de ADN durante la replicación del mismo (Levinson y Gutman, 1987), y errores durante el sobrecruzamiento en la meiosis, ambos sucesos pueden co-existir en la misma variedad y en el mismo locus (Riaz et al., 2002). Probablemente ambos contribuyen a la creación de variabilidad en los microsatélites (Ortiz, 1998), aunque el primero parece ser predominante (Wolff et al., 1989). Además de estas mutaciones producidas por el aumento o disminución de repeticiones de la unidad básica, hay que tener en cuenta las mutaciones que producen alelos nulos (Regner et al., 2000b), (Crespan et al., 1999), (Bowers et al., 1996), (Sanchez-Escribano et al., 1999) etc. Los alelos nulos aparecen al producirse modificaciones en la secuencia diana de los cebadores, impidiendo la hibridación con el ADN molde. Por lo tanto, esas regiones no son amplificadas, con lo que no pueden ser observadas en el análisis. Este tipo de polimorfismo no es deseable, pues no es posible distinguir entre individuos heterocigóticos con un alelo nulo de los homocigóticos, y además, diferentes alelos nulos dan lugar al mismo fenotipo (ausencia de fragmento amplificado). Los STMS tienen numerosas ventajas frente a otros tipos de marcadores moleculares: Polimorfismo muy elevado Análisis rápido y escrutinio de alelos fácil y objetivo Reproducibilidad muy alta Resultados transferibles entre laboratorios Herencia mendeliana codominante y por ello permiten análisis de genealogías No están influidos por el ambiente Sin embargo, tienen el inconveniente de requerir el conocimiento previo de las secuencias flanqueantes de los loci microsatélite para poder diseñar los cebadores específicos. Naturalmente esto no es necesario si, como es el caso de la vid, ya se cuenta con un número suficiente de loci microsatélite descritos y libremente disponibles, además de estar su genoma ya secuenciado en la 19
38 Introducción actualidad. La altísima variabilidad de los STMS hace que sean necesarios muy pocos para estudios de identificación Uso de los STMS para caracterización de vid Para el análisis de la vid, los microsatélites fueron descritos por primera vez por Thomas y Scott (1993). Describieron 5 microsatélites y las secuencias necesarias para su amplificación mediante PCR (VVS1, VVS2, VVS3, VVS4 y VVS5). Estos cebadores, cuyas secuencias se obtuvieron de Vitis vinifera L. cv Sultana, amplificaban además de en esta especie en otras del mismo género, así como en híbridos interespecíficos. Con estos 5 STMS distinguieron 26 cultivares de vinífera y demostraron su utilidad para confirmar o rechazar genealogías en vid. En una publicación posterior, Thomas et al. (1994) incluyeron otros dos microsatélites más: VVS19 y VVS29, y una propuesta de metodología universal para la construcción de una base de datos global de vid. Esta metodología incorporaba un análisis semiautomático de los fragmentos amplificados, merced a su marcaje con un fluorocromo. La determinación del tamaño de los fragmentos se realizaría de forma automática con un programa informático GeneScan, de Perkin Elmer. De esta forma se empezaron a aplicar los STMS para analizar variedades de vid, (Cipriani et al., 1994), (Botta et al., 1995). Con posterioridad se desarrollaron nuevos marcadores STMS de Vitis vinifera: VVMD5, VVMD6, VVMD7 y VVMD8 (Bowers y Meredith, 1996), obtenidos de la variedad Pinot noir. Hasta la actualidad se han publicado un gran número de trabajos en los que se han utilizado los STMS para caracterizar variedades de vid (Meredith et al., 1996), (Ibáñez, 1998), (Sefc et al., 1999), (Ibáñez et al., 2003), (Merdinoglu et al., 2005). Actualmente, en el NCBI se cuenta con más de 360 loci microsatélite de libre disposición (This et al., 2006), además de otros que se han obtenido pero son de uso restringido para los miembros de un Consorcio Internacional de Vid. La utilidad de los STMS para distinguir variedades de vid es muy elevada, dada la cantidad de alelos existentes por loci y por ello, la improbabilidad de que dos variedades diferentes compartan los mismos alelos en todos sus loci. La técnica permite detectar las sinonimias y los problemas de identificación tan habituales en vides cultivadas. Los STMS también se han utilizado en estudios de similitud intervarietal en vid (Sefc et al., 1998), (Maletic et al., 1999), (Lopes et al., 1999), (Sefc et al., 2000). 20
39 Introducción Muchos grupos de investigación han desarrollado sus propios marcadores microsatélites, pero el principal intento internacional para armonizar un sistema basado en microsatélites para la identificación de variedades de vid fue llevado a cabo dentro de un proyecto de la Unión Europea (GENRES081). Los 10 laboratorios que colaboraron en el proyecto, entre los cuales se encontraba el laboratorio de Biología Molecular de la Finca El Encín (IMIDRA), representaban las mayores colecciones de vid europeas, persiguiendo como objetivo el desarrollo de una base de datos central europea que contuviera entre otros datos, alelos de referencia microsatélite para la identificación de accesiones de vid (This et al., 2004). Sin embargo, para que la base de datos resultara útil a diferentes laboratorios que emplearan diferentes equipos y métodos, los alelos debían ser estandarizados, como ya se había demostrado previamente para tomate (Bredemeijer et al., 2002) y para trigo (Röder et al., 2002). Seis microsatélites informativos fueron seleccionados: VVS2, VVMD5, VVMD7, VVMD27, ssrvrzag62 y ssrvrzag79. Todos los participantes analizaron idénticas muestras de DNA (ring test), pertenecientes, siempre que fue posible, a variedades de vid bien conocidas y ampliamente distribuidas geográficamente, con el fin de que el trabajo tuviera la mayor utilidad posible dentro de la comunidad científica. Para cada alelo de cada locus microsatélite, se seleccionó una variedad de las que lo presentaban, que serviría de referencia para todos los laboratorios implicados, y ello permitiría el desarrollo de una base de datos común e internacional. Con los resultados obtenidos, se elaboraron descriptores para los 6 loci microsatélite estudiados. Desafortunadamente, al comienzo de ese proyecto no había información de la posición en los mapas de los microsatélites, y entre los 6 microsatélites elegidos, cuatro de ellos estaban ligados genéticamente 2 a 2. Por esa razón, y porque no son capaces de discriminar todas las variedades diferentes (no sports ) (Martín et al., 2003), ese set de 6 microsatélites no supone una optima selección. Por ello se hace necesario proponer otro conjunto de microsatélites más adecuado para llevar a cabo la caracterización de variedades de vid. 21
40 Introducción 1.3. MARCO LEGAL Principios básicos sobre las variedades de vid La vid es una de las especies con una legislación más extensa, pues cubre tanto aspectos de cultivo y plantación como los de producción vinícola y de uva de mesa, el material de multiplicación y, por supuesto, el registro de variedades y protección de nuevas obtenciones (para revisión, Chomé et al. (2003). En cada ámbito existen referencias al tratamiento o regulación de las variedades, si bien, el único marco legal que define lo que es una variedad, su denominación y las distintas variedades presentes en el mercado es el relativo al Registro de Variedades Comerciales, que es la referencia oficial en cuanto al panorama varietal de la especie. Con referencia a las variedades de vid, se destacan los siguientes principios básicos legales: 1. Se define una variedad sólo cuando se conoce la expresión de su genotipo en unos caracteres morfológicos o fisiológicos que resultan estables y homogéneos y permiten distinguirla de cualquier otra variedad conocida. 2. Cada variedad tendrá una sola denominación que permita distinguirla de las demás. Se podrán admitir sinonimias locales cuando se haya confirmado que se refieren a la variedad. 3. Sólo podrá comercializarse material de multiplicación de las variedades de vid que se encuentren inscritas y reconocidas en el Registro de Variedades Comerciales de plantas. Este es el único marco legal que define lo que es una variedad, su denominación y las distintas variedades presentes en el mercado. Es la referencia oficial en cuanto al panorama varietal de la especie, como ya se ha mencionado. 4. El material de multiplicación se comercializará siempre etiquetado conforme a su categoría y con referencia a la variedad. 5. En cada región sólo podrán plantearse para constituir viñedos las variedades de vid, previamente registradas, que figuren en sus listas de autorizadas o recomendadas. 22
41 Introducción Registro de Variedades Comerciales La legislación española y la comunitaria, obligan a disponer de un Registro de Variedades Comerciales, llamado Catálogo de Variedades Comerciales, de las que están admitidas para su certificación o como material estándar, es decir, las autorizadas para ser producidas viverísticamente o importadas, (Chomé et al., 2003). Todos los países de la Comunidad tienen su Registro o Catálogo, y la suma de dichos catálogos formarán el Catálogo Común de la Unión Europea. Para poder incluir variedades en el catálogo, éstas deben reunir una serie de requisitos, entre ellos, el de ser variedades distintas a las ya incluidas, estables y homogéneas. La Lista de Variedades Comerciales incluida en el Registro, es fruto de estudios amplios y complejos, realizados en el panorama varietal español, por diferentes profesionales de prestigio de la administración central y de las administraciones autonómicas. Las variedades en las que no se han finalizado todos los estudios de comprobación, figuran en la inscripción provisional. Estas variedades están en proceso de caracterización porque, o bien son variedades de cultivo más local, o bien son nuevas obtenciones o variedades extranjeras que se quieren introducir en España como variedades mejorantes (Cabello, 2004). En la actualidad, la inscripción definitiva de variedades comerciales incluye 86 variedades, de las que 20 son de uva de mesa y el resto de vinificación. Por su parte, la inscripción provisional recoge 125 variedades de las cuales 38 son de mesa y el resto de vinificación Protección legal de las obtenciones vegetales Existen dos tipos de protecciones legales sobre la actividad creadora: propiedad industrial y propiedad intelectual. La protección jurídica de la propiedad industrial se remonta al siglo XV, mientras que la de la propiedad intelectual no se empezó a considerar hasta la aparición de la imprenta (Represa, 1998). Las obtenciones vegetales pertenecían en principio a la primera categoría, y así se han considerado en algunas legislaciones, regulando la protección de las mismas con patentes o modelos de utilidad. Sin embargo, en la aplicación de este tipo de normativa a las obtenciones vegetales han surgido dificultades graves, debido a las 23
42 Introducción peculiaridades de las mismas. Esto ha puesto de manifiesto la conveniencia de una normativa específica para la protección legal de las obtenciones vegetales Normativa En función del ámbito de cobertura de la protección legal de las obtenciones vegetales, se distinguen tres normativas: la Internacional, la de la Unión Europea y la de España. Normativa Internacional Antes del establecimiento del sistema UPOV, muchos países poseían sus propias reglas en lo que atañe al examen de variedades. Los criterios técnicos para la concesión de derechos eran diferentes de un país a otro, e incluso el concepto de variedad no era considerado de la misma forma en todos los países. Las normas técnicas y los procedimientos para el examen dependían en gran medida de los conocimientos especializados que poseía el examinador. Esa falta de armonización causaba problemas, en particular cuando un obtentor solicitaba protección para su variedad en varios países. Una variedad que había sido considerada distinta, homogénea y estable en un país, podía ser rechazada en otro, y viceversa. Se llegó a la conclusión de que era preciso introducir una armonización, y la UPOV asumió esa responsabilidad como resultado de la adopción del Convenio Internacional para la Protección de las Obtenciones Vegetales hecho en París en Este Convenio fue revisado en Ginebra el 10 de noviembre de 1.972, el 23 de octubre de y finalmente el 19 de marzo de donde sufrió una profunda revisión para adecuarlo a las nuevas necesidades. Este nuevo Convenio entró en vigor en abril de Este reconocimiento de derechos, armonizado a escala internacional gracias a la UPOV, cuyos principios han sido recogidos en las normativas nacionales de los países miembros de la organización, permite el fomento de las complejas y costosas actividades de investigación y mejora de las variedades, que son un factor clave para la productividad y rentabilidad de las economías agrarias de los países y por ello una razón del progreso de las poblaciones. Es el equivalente al régimen de las patentes para los inventos industriales, enfocado al mundo de las plantas vivas y la agricultura, con una particularidad: no sólo se registran las variedades, sino que antes ha sido necesario haber demostrado, mediante un examen técnico, que la variedad, es distinta de las demás, homogénea, estable y también es nueva. En las 24
43 Introducción directrices del Convenio de la UPOV de se definen estos cuatro conceptos de la siguiente manera: 1. Novedad: La variedad será considerada nueva, si en la fecha de presentación de la solicitud del título de obtención vegetal, el material de reproducción o de multiplicación vegetativa o un producto de cosecha de la variedad no ha sido vendido o entregado a terceros por el obtentor o con su consentimiento para la explotación de la variedad o, habiéndolo sido, no han transcurrido los siguientes plazos: ( ) 2. Distinción: Una variedad será considerada distinta si es posible diferenciarla claramente por la expresión de las características resultantes de un genotipo en particular o de una combinación de genotipos, de cualquier otra variedad cuya existencia, en la fecha de presentación de la solicitud, sea notoriamente conocida. En particular, se considerará que una variedad es notoriamente conocida, a partir de la fecha en que se haya presentado en cualquier país una solicitud: Bien de concesión de un derecho de obtentor, siempre que conduzca a la consecución de la protección solicitada. Bien de inscripción de la variedad en un registro oficial, siempre que resulte finalmente inscrita. Una variedad se considerará que se distingue claramente entre otras, si la diferencia en sus caracteres específicos es consistente y clara. 3. Homogeneidad: Se considerará homogénea la variedad si es suficientemente uniforme en sus caracteres específicos, a reserva de la variación previsible habida cuenta de las particularidades de su reproducción sexuada o de su multiplicación vegetativa. 4. Estabilidad: Se considerará estable la variedad si sus caracteres específicos se mantienen inalterados después de reproducciones o multiplicaciones sucesivas o, en caso de un ciclo particular de reproducciones o de multiplicaciones, al final de cada ciclo. Además del Convenio de la UPOV, la segunda normativa que influye de forma importante en el establecimiento de sistemas de protección de obtenciones vegetales es, el acuerdo sobre los Aspectos de los Derechos de Propiedad 25
44 Introducción Intelectual relacionados con el Comercio (ADPIC o TRIPS, en inglés), anexo incluido en la constitución de la Organización Mundial de Comercio (OMC) en abril de Este acuerdo en el párrafo 3 (b) de su artículo 27, obliga a todos los Estados miembros de la OMC a proporcionar algún sistema de protección a todas las obtenciones vegetales, ya sea mediante patentes, mediante un sistema eficaz sui generis, tal como el sistema de la UPOV, o mediante una combinación de ambos sistemas. Normativa en la Unión Europea En la Unión Europea se aprobó el Reglamento CE 2100/94 del Consejo, de 27 de julio de 1.994, relativo a la protección comunitaria de las obtenciones vegetales, con cobertura y efectos en todos los Estados miembros de la Unión Europea. Es de aplicación directa, y no necesita por ello transposición o desarrollo por parte de los Estados miembros, si bien reconoce el derecho de los mismos a conceder derechos de propiedad nacionales sobre las variedades vegetales. En cualquier caso, este reglamento prohíbe expresamente la doble titularidad de derechos, nacionales y comunitarios. El sistema ha seguido el marco del Convenio UPOV de 1.991, y se ha creado la Oficina Comunitaria de Variedades Vegetales (OCVV o CPVO, en inglés) para administrar y gestionar todo el sistema. Dentro de este contexto, el procedimiento de concesión del derecho sobre una variedad, se inicia con una solicitud única dirigida a la OCVV o a cualquiera de las oficinas nacionales. Tras el examen correspondiente, si procede, se concede un título de protección único y válido en toda la Unión Europea. Esta es la única forma de protección comunitaria de la propiedad industrial para las obtenciones vegetales, y es aplicable a todos los géneros y especies, y también a los híbridos intergenéricos e interespecíficos. Normativa en España Hasta hace pocos años, el sistema de protección de los obtentores en España se basaba en la Ley 12/1975 de 12 de marzo, inspirado en el Convenio UPOV de 1.961, que fue suscrito y ratificado por España. Ésta legislación permitía la protección de obtenciones vegetales mediante patentes y/o modelos de utilidad, cuando no existía Registro de Variedades Protegidas para la especie en cuestión. Con el fin de adaptar esa legislación al nuevo marco jurídico internacional, España estableció un sistema propio, aunque armonizado con la normativa europea 26
45 Introducción (concretado en la Ley 3/2000 de 7 de enero, modificada el 12 de marzo del 2.002), con el fin de reconocer a las Comunidades Autónomas la competencia para la tramitación de los procedimientos para la concesión de los títulos de obtención vegetal. Esta Ley sigue las directrices del Convenio UPOV de 1.991, y tiene como objetivos fundamentales la protección de los obtentores y mejorar el funcionamiento de la Administración pública en las gestiones correspondientes, con el fin de incentivar la investigación en este campo. A continuación se presentan algunos aspectos destacables de la Ley, en especial aquellos donde la aportación de expertos puede ser importante. A efectos de la ley, se define una variedad como un conjunto de plantas de un solo taxón botánico del rango más bajo conocido que, con independencia de si responde o no plenamente a las condiciones para la concesión de un derecho de obtentor, pueda: a) Definirse por la expresión de los caracteres resultantes de un cierto genotipo o de una cierta combinación de genotipos. b) Distinguirse de cualquier otro conjunto de plantas por la expresión de uno de dichos caracteres por lo menos. c) Considerarse como una unidad, habida cuenta de su aptitud a propagarse sin alteración. Los cuatro requisitos necesarios y suficientes para la concesión del título de obtención vegetal, son: Novedad, Distinción, Homogeneidad y Estabilidad (salvo problemas con la denominación). Para ello, debe pasar un examen técnico cuya finalidad es: a) Comprobar que la variedad pertenece al taxón botánico descrito. b) Determinar que es distinta, homogénea y estable. c) Establecer una descripción oficial de la variedad. El segundo punto se conoce como examen DHE (Distinción, Homogeneidad, Estabilidad) o test DUS (iniciales en inglés de Distinctness, Uniformity, Stability). La ley define de forma precisa los derechos de los obtentores, determinando con claridad las actuaciones de terceros relacionadas con su variedad que requieren su autorización. Merece destacarse que la protección alcanza a las variedades derivadas esencialmente de la variedad protegida (EDV). A estos 27
46 Introducción efectos, se considerará que una variedad es esencialmente derivada de otra variedad, denominada ésta última variedad inicial, si: a) Se deriva principalmente de la variedad inicial, o de una variedad que a su vez deriva principalmente de la variedad inicial, conservando al mismo tiempo las expresiones de los caracteres esenciales que resulten del genotipo o de la combinación de genotipos de la variedad inicial. b) Se distingue claramente de la variedad inicial, y c) Salvo por lo que respecta a las diferencias resultantes de la derivación, es conforme a la variedad inicial en la expresión de los caracteres esenciales que resulten del genotipo o de la combinación de genotipos de la variedad inicial. De esta forma, se crea un halo de protección alrededor de la variedad protegida, de manera que el obtentor de la variedad inicial tiene ciertos derechos sobre las variedades esencialmente derivadas (EDV). Ejemplos de métodos o eventos que pueden llevar a una EDV son: mutaciones inducidas o naturales, variantes somaclonales, selección de individuos dentro de una variedad inicial, retrocruzamiento múltiple o transformación genética. El examen técnico de las variedades se realiza por las autoridades oficiales nacionales, y, en el caso de España, son competencia actualmente de la Oficina Española de Variedades Vegetales como subdirección general del Ministerio de Agricultura, Pesca y Alimentación, que continúa los trabajos y la experiencia del anterior organismo autónomo responsable, el Instituto Nacional de Semillas y Plantas de Vivero, ampliamente conocido en los ámbitos nacional e internacional. Cuando las variedades sometidas a examen son nuevas, distintas, homogéneas y estables, se les adjudica un título de obtención vegetal que otorga a los obtentores derechos exclusivos de multiplicación y uso de dichas variedades. La inscripción de variedades en el Registro de Variedades Protegidas tiene el mismo procedimiento técnico de examen que el Registro de Variedades Comerciales, por lo que suelen realizarse en un solo acto, utilizando la misma colección de referencia y organizado por el mismo organismo oficial competente. La Figura I1 que se muestra a continuación, detalla cuales son los organismos oficiales que otorgan títulos de obtención vegetal tanto en España como en Europa. 28
47 Introducción Figura I1. Detalle de los organismos que otorgan títulos de obtención vegetal tanto en España como en el ámbito comunitario (Chomé et al., 2003). El pasado 18 de julio de 2.007, España ratificó oficialmente el Acta de del Convenio Internacional para la Protección de las Obtenciones Vegetales Protección y defensa legal Como ya se ha comentado, para conseguir un título de obtención vegetal es necesario que la variedad pase un examen técnico, realizado por los organismos oficiales competentes. Dentro de este examen, se encuentra el determinar si la variedad a proteger es distinta, homogénea y estable (exámenes DHE), además de nueva. Cuando el test de las variedades candidatas resulta positivo, es decir, si se cumplen los cuatro requisitos anteriores, a las nuevas variedades se les adjudica un título de obtención vegetal. La ley define los derechos de los obtentores, determinando las actuaciones de terceros relacionadas con su variedad que requieren su autorización. Ahora bien, una vez concedido el título, es competencia del obtentor la defensa de sus derechos, incluido llegado el caso, probar si una variedad es una EDV de una variedad suya, ante un tribunal de justicia. 29
48 Introducción Exámenes DHE Los exámenes DHE son un aspecto esencial de la protección. En la actualidad estos exámenes se basan casi exclusivamente en el estudio de características morfológicas, y se apoyan en ocasiones en análisis de proteínas (isoenzimas, proteínas totales, etc.). Estos marcadores son en ocasiones lentos, costosos, subjetivos y/o no concluyentes, lo que en algunos casos puede conducir a una deficiente protección de las nuevas obtenciones. Es por ello que existe un gran interés internacional por incorporar nuevos marcadores, que ha dado lugar a la creación, entre otros, de un grupo de trabajo en el seno de la UPOV sobre Técnicas Moleculares y Bioquímicas, en especial de perfiles de ADN, en inglés Biochemical and Molecular Techniques and DNA-Profiling in particular (BMT). Según la UPOV (documento TG/1/3), las condiciones básicas que una característica debería reunir para ser usada en los test DHE, serían las siguientes: 1. proceder de un genotipo determinado o de una combinación de genotipos. 2. ser suficientemente homogénea en un determinado ambiente. 3. presentar suficiente variación entre variedades para ser capaces de establecer la distinción. 4. ser capaz de definir y reconocer las variedades. 5. permitir que los requisitos de homogeneidad se cumplan. 6. permitir que los requisitos de estabilidad se cumplan, es decir, que produzca resultados consistentes y repetitivos después de repetidas multiplicaciones o, donde corresponda, al final de cada ciclo de multiplicación. La ISF (Federación Internacional de Semillas), que es una importante agrupación privada de obtentores, en ISF Position Papers (2003), apoya completamente lo estipulado por la UPOV en lo que respecta a las características para llevar a cabo el test DHE. Llama la atención a las autoridades competentes tanto nacionales como internacionales, para que concreten las características empleadas en los test DHE. Esto es necesario para asegurar la reproducibilidad de los resultados obtenidos y la consistencia de las observaciones realizadas por las diferentes autoridades competentes sobre la misma característica. La ISF propone la siguiente clasificación de las características usadas para llevar a cabo el test DHE: 30
49 Introducción 1. Características morfológicas estándar de la UPOV (incluidas en sus directrices individuales). 2. Características morfológicas adicionales. Estas deben satisfacer el criterio general de las características del punto anterior. Tienen que ser usadas por al menos un grupo de trabajo de la UPOV y presentadas a esta institución. Estas características son principalmente fisiológicas y pueden ser añadidas a la lista de características con el consentimiento del obtentor. Rendimiento Contenido en azúcar Resistencia a plagas o enfermedades Tolerancia a herbicidas Esta lista de características morfológicas adicionales no es exhaustiva y está sujeta a cambios en función del tipo de cultivo. 3. Pruebas convincentes adicionales. Generalmente, son características proteicas. Si fueran usadas, debería ser: Con el consentimiento del solicitante. Solo si todas las demás características fallan al establecer la clara distinción, a pesar de que se encuentre alguna evidencia de distinción con las características estándar de la UPOV. Solo si el procedimiento ha sido consentido por las autoridades competentes y los solicitantes de la protección. Si se usaran estas características, ellas solo podrían establecer la distinción en combinación con las características morfológicas citadas en las categorías 1 y Identificación, distinción y derivación esencial La diferencia entre distinción e identificación es que el test de Distinción establece que la variedad es única y constituye su descripción inicial, (Bould, 1996). Se basa fundamentalmente en caracteres morfológicos, y uno de ellos por sí solo puede ser suficiente para establecer que dos variedades son distintas. El proceso 31
50 Introducción consiste en esencia, en buscar las diferencias de la variedad analizada respecto a las demás, usando una colección de referencia apropiada, y en determinar si esas diferencias son superiores a una distancia mínima. Para Le Buanec (2000) la diferencia entre identificación y distinción radica precisamente en el concepto de distancia mínima, todavía en discusión en el seno de la UPOV. A pesar de los problemas que presenta, el sistema funciona más o menos satisfactoriamente, proporcionando un perímetro de protección suficiente a los obtentores. La UPOV divide los caracteres morfológicos en tres tipos: cualitativos, cuantitativos y pseudocualitativos. En teoría, para cada uno de estos caracteres, en el examen de Distinción, se establece la mínima diferencia que puede existir entre dos expresiones de un mismo carácter para considerarlas diferentes. Esta diferencia debe ser clara y consistente: Caracteres cualitativos: Aquellos que presentan estados de expresión distintos y discontinuos entre sí. Ej. los diferentes colores de un fruto o de una flor. Cada uno es diferente del otro y puede haber una gran cantidad de expresiones (colores): la diferencia es clara si los caracteres respectivos presentan expresiones correspondientes a dos estados diferentes. Caracteres cuantitativos: Aquellos que pueden medirse en una escala unidimensional y presentan una variación continua de un extremo al otro. A los efectos de la descripción se dividen en diversos estados de expresión. Ej. días de floración, altura de la planta, tamaño o peso del fruto: la diferencia deberá considerarse clara si puede establecerse con una probabilidad de error del 1%, por ejemplo, por el método de la mínima diferencia significativa. Las diferencias son coherentes si se producen en el mismo sentido en dos ciclos de cultivo o en dos de tres ciclos. Caracteres pseudocualitativos: Aquellos en los que los estados de expresión son, al menos parcialmente, continuos pero varían en más de una dimensión, y no pueden describirse adecuadamente definiendo únicamente los extremos de una gama lineal. Ej. la forma: oval, elíptica, redonda Un nivel diferente en las Directrices de Examen de la UPOV no es necesariamente suficiente para establecer la distinción. No obstante, en ciertas circunstancias, variedades descritas con el mismo nivel de expresión pueden distinguirse claramente. 32
51 Introducción La identificación consiste en verificar la conformidad de una variedad con respecto a los modelos establecidos en una colección de referencia. No es un sustituto de la distinción, y por ello la identificación de nuevas variedades que puedan ser iguales a una preexistente es responsabilidad del obtentor de la misma. El establecimiento de la derivación esencial también corresponde al obtentor. Dos variedades pueden ser diferentes en un carácter de suficiente importancia como para ser consideradas distintas por una oficina de protección. Si un obtentor considera que ha sido obtenida a partir de la suya en algunos de los supuestos contemplados en la derivación esencial, debe demostrarlo (prueba prima facie ). Para ello, al igual que en la identificación, se pueden emplear marcadores distintos a los morfológicos, ya que no se persigue la obtención del título de obtención vegetal. Si finalmente, el propietario de la variedad inicial muestra pruebas suficientes de que la otra variedad ha sido obtenida a partir de la suya, el segundo obtentor debería tener que probar que él no ha usado la variedad inicial, o una variedad esencialmente derivada de esa variedad inicial. La Figura I2 muestra gráficamente el alcance de la protección: a partir de una variedad inicial (variedad A, situada en el centro de los círculos), la protección abarca en principio a todas las variedades que queden dentro de un círculo delimitado por la distancia mínima (variedad C). Una EDV (variedad D), por definición, es distinta de la variedad inicial, y quedaría en un círculo externo al marcado por la distancia mínima, pero con la legislación vigente aún quedaría dentro de la protección. La variedad B, correspondería a una variedad distinta de A, estaría situada fuera del círculo de protección legal. 33
52 Introducción Figura I2. Descripción gráfica del alcance de la protección legal para una variedad A Posiciones frente al empleo de los marcadores moleculares en la protección y defensa legal de variedades vegetales En la protección legal (exámenes DHE) Los obtentores, en la sexta reunión del grupo de trabajo BMT, celebrada en Angers (Francia) 1-3 de marzo de 2.000, pusieron de manifiesto su temor ante el uso de los marcadores moleculares para los test DHE, por considerar que de momento traería consigo un debilitamiento de la protección de las nuevas (y antiguas) variedades. Consideran que una sola banda, alelo, etc., diferente podría llevar, según la definición de UPOV de distinción ( claramente distinguible ) a declarar una variedad distinta de otra, reduciendo el círculo interior de la Figura I2 a su mínima expresión. Ello obligaría a hacer uso en cada caso del concepto de derivación esencial, con lo que ello supone (demostrar judicialmente la derivación esencial, con el consiguiente retraso, gasto, etc). Hoy en día, los obtentores siguen con los mismos temores. 34
53 Introducción Debido a que en la actualidad los exámenes DHE se basan casi exclusivamente en marcadores morfológicos, y a sus problemas citados, la UPOV tiene un claro interés en incorporar los marcadores moleculares al sistema de protección cuando existan garantías suficientes. El grupo de trabajo BMT celebra reuniones periódicas aproximadamente cada año y medio para estudiar la manera de mejorar el sistema de protección incorporando los marcadores moleculares. La UPOV, también tiene intención de incorporar estos marcadores al manejo de colecciones de referencia, que cada vez se hace más difícil debido al crecimiento del número de países integrados en la UPOV, lo que hace incrementar el número de nuevas variedades en estas colecciones, haciendo más complejo el examen DHE. Los marcadores que se utilicen para describir estas colecciones de referencia deben ser los mismos que se usen para los exámenes DHE. Debido a que cada vez hay más países en el seno de la UPOV que podrían llegar a utilizar sistemas diferentes de protección, generando con ello una gran confusión y un aumento del coste para los solicitantes, la UPOV enfatiza sobre la necesidad de progresar en el grupo de trabajo BMT. No hay que olvidar además que uno de los objetivos de la UPOV precisamente es la armonización internacional de las descripciones y exámenes de las variedades entre los estados miembros. Para incorporar un nuevo marcador a los exámenes DHE, además de demostrar su utilidad para la distinción, debe ser también homogéneo y estable, dado que una variedad debe ser homogénea y estable para los caracteres usados en la distinción. De lo contrario, obligaría a los obtentores a un trabajo de selección adicional para mantener estas características estables. Como consecuencia, se propuso profundizar en los estudios de aplicabilidad de los marcadores moleculares a especies modelo concretas, insistiendo en el concepto de distancia mínima, o distancia más pequeña que puede existir entre dos variedades para considerarlas diferentes. En cualquier caso, hay que tener en cuenta que la distancia mínima depende de la variabilidad genética intra e intervarietal existente, y por ello su problemática es muy distinta en las especies en que las variedades se propagan por vía vegetativa y en las que lo hacen sexualmente, y dentro de éstas, también es muy diferente la variabilidad genética intravarietal e intervarietal presente. Al final se hace necesario establecer una distancia mínima para cada especie. 35
54 Introducción La Oficina Española de Variedades Vegetales realiza los exámenes DHE en base a los marcadores oficiales ampelográficos. Sin embargo, es consciente de la importancia que pueden tener los marcadores moleculares a la hora de complementar a los morfológicos, por lo que apoyan las iniciativas en el sentido de su posible inclusión futura en el sistema de protección, siempre que cumplan los requisitos planteados. La ISF, en ISF Position Papers (2000), no se opone al empleo de los marcadores moleculares de ADN para el test DHE. Sin embargo, la introducción de las nuevas tecnologías y de nuevos conceptos debe resolver más problemas que los que crea y, de momento, la ISF considera que las pruebas DHE deberían continuar efectuándose en base a las características fenotípicas. Afirma que los marcadores moleculares no deben ser los únicos empleados para establecer la distinción, sino sólo una evidencia adicional para esa distinción. Considera que esta posición es coherente con la definición de variedad incluida en el Acta de 1991 del Convenio de la UPOV, en la que una variedad está definida por la expresión de los caracteres resultantes de un cierto genotipo o de una cierta combinación de genotipos. Tanto en ISF Position Papers (2000), como en ISF Position Papers (2003), la ISF apoya la continuidad del trabajo del grupo BMT sobre el posible empleo de marcadores bioquímicos y moleculares para el examen DHE. En particular debería analizarse los siguientes aspectos: Definición de la distancia mínima para la distinción. Impacto sobre los conceptos de homogeneidad y estabilidad y evaluación de esos criterios. Diferencia práctica entre los conceptos de distinción y de derivación esencial cuando ambos son evaluados utilizando marcadores moleculares. Disponibilidad pública de los marcadores empleados, en ISF Position Papers (2006). Mientras no existan claras respuestas a los problemas suscitados por estos temas, la ISF considera que el uso de marcadores moleculares para el examen DHE podría reducir el ámbito de protección, cuando el objetivo es fortalecerlo. 36
55 Introducción Considera que la introducción de nuevos caracteres para el test DHE, se debería utilizar sin crear nuevas obligaciones a los obtentores de variedades ya protegidas. En la actualidad, la ISF sigue oponiéndose al empleo en solitario de los marcadores moleculares en el test DHE como características decisivas a la hora de conceder un título de obtención vegetal de acuerdo a la UPOV (ISF Position Papers, 2006). En resumen, obtentores, mejoradores y organismos oficiales encargados de conceder títulos de obtención vegetal, siguen oponiéndose actualmente al uso exclusivo de los marcadores moleculares en los exámenes DHE. Sin embargo, ninguno de ellos se opone a su empleo en estos exámenes junto con los marcadores morfológicos oficiales, siempre que no se usen en exclusiva para establecer la distinción. Para ello, previamente es necesario demostrar su utilidad en el sistema de protección de obtenciones vegetales En la defensa legal (identificación y establecimiento de la derivación esencial) En la décima reunión del grupo de trabajo BMT, celebrada en Seúl, del 21 al 23 de noviembre de 2.006, la UPOV manifestó su interés acerca del empleo de los marcadores moleculares en la identificación varietal. La Oficina Española de Variedades Vegetales, actualmente está utilizando el sistema de 9 loci microsatélite evaluados en esta tesis doctoral, para ayudar a caracterizar su colección de referencia de vid. La ISF, en ISF Position Papers (2003) e ISF Position Papers (2006) está de acuerdo con que los marcadores moleculares de ADN se empleen para la identificación de variedades ya protegidas, en caso de presunto mal uso de esa variedad o el mal uso de una línea parental original en el caso de una variedad híbrida. Los marcadores moleculares también pueden ser usados para definir una similitud genética que dispare un proceso legal en casos de derivación esencial afirmada, o para determinar la presencia o ausencia de un determinado gen o una mutación cuya expresión o falta de expresión es responsable de una característica esencial de la variedad. 37
56 Introducción Para esta demostración, en la ISF sería suficiente cumplir uno de los siguientes requisitos (ISF Position Papers, 2003): 1. Una fuerte similitud fenotípica 2. Sólo algunas pequeñas diferencias en algunos caracteres heredados 3. Una fuerte similitud genética En esta décima reunión del grupo BMT, el representante de CIOPORA (International Community of Breeders of Asexually Reproduced Ornamental and Fruit Varieties), informó que estaban trabajando en un Position Paper sobre variedades esencialmente derivadas. La base de éste sería establecer umbrales para semejanza basándose en herramientas moleculares, e indicó que se necesitaría información de un gran número de especies, por lo que en este aspecto, los estudios llevados a cabo por el grupo BMT serían de gran ayuda. En el laboratorio de Biología Molecular de la Finca El Encín (IMIDRA), se ha utilizado con frecuencia el sistema de 9 loci microsatélite evaluados en esta tesis para la identificación legal de variedades de vid. Se han llevado a cabo algunos trabajos como: la defensa de una variedad protegida por el supuesto infringimiento de los derechos del obtentor, la identificación de plantas vendidas en viveros, la determinación de si las plantas de una plantación pertenecen a una lista de variedades autorizadas en una Denominación de Origen o a la Lista de Variedades Comerciales. 38
57 2. OBJETIVOS
58
59 Objetivos 2. OBJETIVOS La concesión de protección legal a una variedad vegetal, es decir, de un título de obtención vegetal, requiere el cumplimiento de unas condiciones. Ese cumplimiento se evalúa mediante un examen en que se determina si la variedad, además de nueva, es distinta, homogénea y estable (DHE). En general, los exámenes DHE se basan exclusivamente en el estudio de marcadores morfológicos y, en algunos casos, bioquímicos. En el caso de la especie propuesta, Vitis vinifera L., existe una disciplina científica, la Ampelografía, que comprende la descripción morfológica de las plantas de vid, y que pese a resultar indispensable, adolece de unas características que limitan su utilidad frente a otras técnicas más recientes. Entre ellas, los marcadores moleculares de ADN presentan numerosas ventajas frente a los morfológicos y podrían complementarlos en numerosas ocasiones, con lo que los exámenes ganarían esencialmente tiempo y objetividad. Para poder incorporar cualquier nuevo marcador al sistema de protección es imperativo constatar su utilidad para estos propósitos tan específicos. Una vez obtenido el título de obtención vegetal, es necesario disponer de herramientas que permitan al obtentor la defensa de la misma, tanto del uso ilegal de plantas de su variedad como de variedades derivadas de la misma. En esta tesis doctoral se evaluará la utilidad de algunos marcadores moleculares microsatélites, tanto en la protección (incluyendo estudios de Distinción, Homogeneidad y Estabilidad), como en la defensa legal (incluyendo estudios de Identificación y establecimiento de la derivación esencial) de variedades pertenecientes a la especie Vitis vinifera L. Para ello, se definieron los siguientes objetivos: 1. Seleccionar un número adecuado de microsatélites. 2. Analizar una gran colección de accesiones de vid, genotipada con el conjunto de microsatélites elegido. Determinar en la citada colección las diferencias intra e intersortogrupo, y en base a ellas, establecer la distancia mínima (punto clave en el estudio de Distinción) en número de alelos. 39
60 Objetivos 3. Llevar a cabo un estudio de Homogeneidad y Estabilidad con el sistema de microsatélites seleccionado, recolectando y estudiando el material vegetal necesario para ello. 4. Establecer una colección de referencia que resulte útil para la identificación de variedades de vid y el establecimiento de la derivación esencial. 5. Elaborar una propuesta práctica de utilización del sistema y toma de decisiones, tanto para la defensa legal de variedades de vid, incluyendo en ella la identificación, y el establecimiento de la derivación esencial; como para la protección legal, incluyendo en ella los exámenes DHE. 6. Elaborar descriptores para la utilización sistemática en la vid de los marcadores STMS estudiados, empleando para ello la información derivada de los estudios anteriores. 40
61 3. MATERIALES Y MÉTODOS
62
63 Materiales y Métodos 3. MATERIALES Y MÉTODOS 3.1. MATERIALES Material vegetal Estudio de Distinción Se utilizaron un total de accesiones para llevar a cabo el estudio de Distinción. Dentro de este conjunto se encontraban 112 accesiones del proyecto que lleva por título: Detección de sinonimias entre las principales variedades de vid cultivadas en el mundo y las variedades españolas. Relación filogenética con las principales especies del Género Vitis, coordinado por D. Gregorio Muñoz Organero (IMIDRA-Finca El Encín). Este material vegetal se empleó para la realización del Museo de Briones en La Rioja, y procede de las Colecciones de variedades de vid de El Encín (España), Jerez de la Frontera (España), Geilweilerhof (Alemania), Montpellier (Francia) y San Michele (Italia). Incluye una amplia representación de las variedades más cultivadas en los países vitícolas del mundo, además de portainjertos, híbridos productores directos, especies del género Vitis no vinifera y géneros de la familia Vitáceas. Dicho material recibirá el nombre de Briones a lo largo de este trabajo. El material vegetal de Briones consistió en hojas jóvenes, que fueron introducidas de forma individual en sobres perfectamente identificados con el material que portaban y almacenadas en arcones a -80ºC en el momento de su llegada al laboratorio. Estas muestras llegaron en malas condiciones, lo que influyó negativamente en pasos posteriores. La Tabla M1, presenta cada una de las accesiones de Briones con algunas características relevantes. Además, se manejaron datos y ADN pertenecientes a accesiones de las parcelas 22, 25, y de la parcela de portainjertos de la Colección de variedades de vid de El Encín. Información de las accesiones correspondientes a dichas parcelas, se encuentra publicada en Cabello (1995). También se incluyeron datos correspondientes a una planta de cada una de las 19 variedades utilizadas en el estudio de Homogeneidad y Estabilidad (Tabla M2, página 45), y datos de 14 accesiones del estudio de establecimiento de descriptores microsatélite (Tabla M24, página 72). La gran cantidad de material utilizado en el estudio de Distinción, perseguía incluir las accesiones presentes en los diferentes estudios llevados a cabo en el laboratorio de Biología Molecular de la Finca el Encín (IMIDRA). 41
64 Materiales y Métodos Tabla M1. Datos correspondientes a las 112 muestras de Briones. VARIEDAD PAÍS DE ORIGEN DE LA CULTIVO MUESTRA COLOR OBSERVACIONES* Richter 110 Viveros Provedo (Logroño) PTI Paulsen 1103 Viveros Provedo (Logroño) PTI Ruggeri 140 Viveros Provedo (Logroño) PTI Couderc Viveros Provedo (Logroño PTI Couderc 1616 CIFA Rancho la Merced (Jerez) PTI Castel Viveros Provedo (Logroño) PTI Millardet et Grasset Finca del MAPA (Aranjuez) PTI Richter 31 CIFA Rancho la Merced (Jerez) PTI Couderc 3309 Finca del MAPA (Aranjuez) PTI 41 B M Viveros Provedo (Logroño) PTI Millardet et Grasset 420A Aranjuez PTI Aligoté Francia INRA-ENSA.Montpellier Blanca Arinto Portugal CIFA Rancho la Merced (Jerez) Blanca Arvine petite Suiza CIFA Rancho la Merced (Jerez) Blanca Babic Croacia I.R. Geilweilerhof Tinta Baga Portugal Finca El Encín Tinta Barbera Italia Finca El Encín Tinta Bicane Finca El Encín Bonarda Argentina INRA-ENSA.Montpellier Tinta Cabernet franc Francia Finca El Encín Tinta Cabernet sauvignon Francia Finca El Encín Tinta Chasselas blanc Francia Finca El Encín Blanca Chasselas Michel Tompa Finca El Encín Chenin Francia CIFA Rancho la Merced (Jerez) Blanca Cinsaut Francia Finca El Encín Tinta Colombard Francia Finca El Encín Blanca Dabouki Israel Finca El Encín Blanca Dimyat Bulgaria I.R. Geilweilerhof Blanca Dolcetto Italia Finca El Encín Tinta Emerald riesling USA Finca El Encín Blanca Fercal Viveros Provedo (Logroño) PTI Fernâo pires Portugal Finca El Encín Blanca Feteasca neagra Rumanía I.R. Geilweilerhof Tinta Feteasca regala Rumanía I.R. Geilweilerhof Blanca Furmint Hungría Finca El Encín Blanca Gamay Francia Finca El Encín Tinta Garganega Italia I.A. di San Michele Blanca Gewürztraminer Francia Finca El Encín Blanca Gibi Argentina I.A. di San Michele Blanca Isabella Brasil Finca El Encín Tinta Jacquez Finca El Encín HPD Kadarka Hungría Finca El Encín Tinta Kerner Alemania CIFA Rancho la Merced (Jerez) Blanca Koshu Japón I.R. Geilweilerhof Blanca Kratosija Macedonia CIFA Rancho la Merced (Jerez) Tinta Malbec Francia Finca del MAPA (Aranjuez) Tinta Malvasia di Candia Italia I.A. di San Michele Blanca Melon Francia Finca El Encín Blanca Merlot Francia Finca El Encín Tinta 42
65 Materiales y Métodos VARIEDAD PAÍS DE CULTIVO ORIGEN DE LA MUESTRA COLOR OBSERVACIONES* Mission USA Finca del MAPA (Aranjuez) Tinta Monbadon USA INRA-ENSA.Montpellier Blanca Montepulciano Italia CIFA Rancho la Merced (Jerez) Tinta Müller-Thurgau Alemania Finca El Encín Blanca Nebbiolo Italia I.A. di San Michele Tinta Negro amaro Italia CIFA Rancho la Merced (Jerez) Tinta Oberlin 595 Finca El Encín HPD Öküz gözü Turquía INRA-ENSA.Montpellier Tinta Olivette noire INRA-ENSA.Montpellier Pamid Bulgaria Finca El Encín Tinta Parthenocisus Viveros Sánchez (Cabanillas del Campo, Guadalajara) EFV Petit bouschet Finca El Encín Petit verdot Francia Finca El Encín Tinta Pinot blanc Francia Finca El Encín Blanca Pinot gris Francia INRA-ENSA.Montpellier Blanca Pinot meunier Francia Finca El Encín Tinta Pinot noir Francia Finca El Encín Tinta Pinotage Sudáfrica CIFA Rancho la Merced (Jerez) Tinta Plavac mali Croacia I.R. Geilweilerhof Tinta Portugais bleu Alemania Finca El Encín Tinta Primitivo Italia CIFA Rancho la Merced (Jerez) Tinta Prokupac Serbia Finca El Encín Tinta Prosecco Italia I.A. di San Michele Blanca Quebranta Perú INRA-ENSA.Montpellier Tinta Rabo de Ovella Portugal CIFA Rancho la Merced (Jerez) Blanca Riesling Alemania Finca El Encín Blanca Rkatsiteli Rusia I.A. di San Michele Blanca Ruby cabernet USA Finca del MAPA (Aranjuez) Tinta Rupestris de Lot Finca El Encín PTI Sangiovese Italia I.A. di San Michele Tinta Saperavi Rusia I.R. Geilweilerhof Tinta Sauvignon blanc Francia Finca El Encín Blanca Semillon Francia Finca El Encín Blanca Seyval Canadá Finca El Encín Tinta Silvaner Alemania Finca El Encín Blanca Smeredevka Serbia Finca El Encín Blanca SO4 Viveros Provedo (Logroño) PTI Syrah Francia Finca El Encín Tinta Tannat Francia INRA-ENSA.Montpellier Tinta Tinta barroca Portugal INRA-ENSA.Montpellier Tinta Tocai friulano Italia I.A. di San Michele Blanca Touriga nacional Portugal Finca El Encín Tinta Ugni blanc Francia Finca El Encín Blanca Veltliner gruen Austria I.R. Geilweilerhof Blanca Villard blanc Finca El Encín HPD Viognier Francia INRA-ENSA.Montpellier Blanca Vitis aestivalis CIFA Rancho la Merced (Jerez) EGV Vitis arizonica CIFA Rancho la Merced (Jerez) EGV Vitis californica INRA-ENSA.Montpellier EGV Vitis candicans CIFA Rancho la Merced (Jerez) EGV Vitis cinerea CIFA Rancho la Merced (Jerez) EGV 43
66 Materiales y Métodos VARIEDAD PAÍS DE CULTIVO ORIGEN DE LA MUESTRA COLOR OBSERVACIONES* Vitis cordifolia CIFA Rancho la Merced (Jerez) EGV Vitis labrusca I.R. Geilweilerhof EGV Vitis riparia Finca El Encín EGV Vitis rupestris Finca El Encín EGV Vitis silvestris (hembra) CIFA Rancho la Merced (Jerez) EGV Vitis silvestris (hembra) CIFA Rancho la Merced (Jerez) EGV Vitis silvestris (macho) CIFA Rancho la Merced (Jerez) EGV Vitis silvestris (macho) CIFA Rancho la Merced (Jerez) EGV Vranac Macedonia Finca El Encín Tinta Xynisteri Chipre Finca El Encín Blanca Xynomavro Grecia CIFA Rancho la Merced (Jerez) Tinta Zweigeltrebe blau Austria I.R. Geilweilerhof Tinta * EGV: Especies del Género Vitis no vinifera HPD: Híbridos Productores Directos EFV: Especies de la Familia Vitáceas no del género Vitis PTI: Portainjertos Estudio de Identificación Para llevar a cabo este estudio se utilizaron datos de una colección de 495 variedades obtenida durante el estudio de Distinción Estudio de Homogeneidad y Estabilidad Selección de variedades Para realizar este trabajo se utilizó como material vegetal hojas jóvenes de 19 variedades de vid. En la Tabla M2 se detalla para cada una de estas variedades, sus hectáreas mundiales de cultivo en (Hidalgo, 2002), el uso de sus productos (vino, mesa, vino-mesa), si presentan o no apirenia y el color de sus bayas. Se puede observar que para las variedades Crimson SDL, Flame SDL, Napoleón, Red globe y Sugraone, no aparecen datos de hectáreas mundiales de cultivo en ese año, pese a las consultas realizadas en distintas fuentes. Estas 19 variedades se seleccionaron cuidadosamente, buscando la mayor diversidad posible entre ellas. Se consideraron los siguientes aspectos: 44
67 Materiales y Métodos Empleo de las uvas (vino/mesa). Color de la piel de la baya (blancas/tintas) (recomendado por la UPOV para el agrupamiento de diferentes variedades de vid). Presencia o ausencia de semillas (característica muy importante para las variedades de uva de mesa). Origen en el tiempo (si son más antiguas o más recientes). Origen geográfico (variedades que tienen su origen en diferentes países/ continentes). En cultivo actualmente. Tabla M2. Material vegetal empleado para el estudio de Homogeneidad y Estabilidad. VARIEDAD HECTÁREAS CULTIVADAS USO APIRENA COLOR Airén Vino No Blanca Cabernet sauvignon Vino No Tinta Cardinal Mesa No Tinta Chardonnay Vino No Blanca Crimson SDL* Mesa Sí Tinta Flame SDL* Mesa Sí Tinta Garnacha Vino No Tinta Italia Mesa No Blanca Merlot Vino No Tinta Monastrell Vino No Tinta Moscatel de Málaga Ambas No Blanca Napoleón Mesa No Tinta Ohanes Mesa No Blanca Palomino fino Vino No Blanca Red globe Mesa No Tinta Sauvignon blanc Vino No Blanca Sugraone Mesa Sí Blanca Tempranillo Vino No Tinta Thompson SDL* Mesa Sí Blanca *SDL: seedless (sin semillas) 45
68 Materiales y Métodos Toma de muestras Los criterios seguidos para llevar a cabo el muestreo fueron los siguientes: Se tomó material vegetal de cada una de las 19 variedades en, al menos, 10 fincas diferentes (la Tabla M3 resume el muestreo para cada variedad). Tabla M3. Resumen del muestreo para el estudio de Homogeneidad y Estabilidad. VARIEDAD PAISES RECOGIDA DE Nº Nº PLANTAS MATERIAL PLANTACIONES MUESTREADAS Airén España Alemania, Chile, España, Cabernet Francia, Hungría, Sudáfrica, sauvignon USA Cardinal España, Francia, Hungría, USA Chardonnay Alemania, Chile, España, Francia, Hungría, Sudáfrica, USA Crimson Chile, España, Sudáfrica, SDL USA Flame SDL Chile, España, USA Garnacha España Italia Chile, España, Hungría, USA Merlot Alemania, Chile, España, Francia, Sudáfrica, USA Monastrell España Moscatel de Málaga España, Francia, USA Napoleón España Ohanes España, Francia Palomino fino España Red globe España Alemania, Chile, España, Sauvignon Francia, Hungría, Sudáfrica, blanc USA Sugraone Chile, España, Sudáfrica Tempranillo España Thompson Chile, España, Sudáfrica, SDL USA TOTAL En 7 Países, 3 Continentes Para el estudio de Homogeneidad se recolectaron muestras de 52 plantas en 3 fincas diferentes, de ellas se analizaron 50. Para el estudio de Estabilidad se recolectaron muestras de 7 plantas en 7 fincas diferentes, de ellas se analizaron 5 46
69 Materiales y Métodos plantas. Por tanto, para cada variedad se analizaron 185 plantas. El material vegetal recolectado en exceso, se tomó por si fuera necesario repetir algún análisis. Pese al cuidado tomado en el muestreo, efectivamente se detectaron errores: algunas o todas las plantas muestreadas de varias fincas no se correspondieron con la variedad esperada. En este caso, si el número de muestras erróneas era bastante grande y no se disponía de material de reserva en el laboratorio, hubo que realizar nuevos muestreos. En la recogida de material se procuró, siempre que fue posible, tomar muestras para cada variedad de lugares donde su cultivo es significativo. Por ejemplo, Airén en Castilla La Mancha. Se pretendió optimizar al máximo los viajes para la recogida de material. Así, en cada una de las regiones geográficas visitadas, se intentó recoger el máximo material de la zona necesario para la realización del trabajo. El material que se recogió, en general, estaba en cultivo comercial. La toma de muestras se enfocó de manera diferente dependiendo de si se trataba de variedades de uva de mesa o de vino: La uva de mesa en España se cultiva principalmente en el sur y sureste de la península. Por ello, la recogida de muestras de las variedades Cardinal, Crimson SDL, Flame SDL, Italia, Napoleón, Ohanes, Red globe, Sugraone y Thompson SDL, se centró principalmente en Alicante, Almería, Cádiz, Murcia y Huelva. La recolección de estas muestras en concreto, habría sido muy difícil sin la participación de José María Hurtado (Superior Frutícola S.A.), debido a la gran cantidad de contactos que posee en el sector productivo de uva de mesa. Dentro de este material también se incluyeron algunas muestras extranjeras procedentes de plantaciones de Chile, Estados Unidos de América, Francia, Hungría y Sudáfrica. La obtención de las mismas se llevó a cabo contactando en primer lugar con centros e investigadores de todo el mundo y, posteriormente solicitando permisos de importación para el material vegetal que se iba a recibir. En total, se dispuso de material de 25 plantaciones para el estudio de Homogeneidad y de 85 plantaciones adicionales para el estudio de Estabilidad. Con respecto a las 10 variedades de vinificación, incluyendo aquí a la variedad Moscatel de Málaga (apta para vino, mesa y pasificación), el material de España se obtuvo esencialmente a través de la colaboración con numerosas 47
70 Materiales y Métodos Denominaciones de Origen: Almansa, Calatayud, Campo de Borja, Cariñena, Tarragona, Condado de Huelva, Costers del Segre, Jerez, Jumilla, La Mancha, Méntrida, Monterrei, Montilla-Moriles, Navarra, Penedés, Ribeira Sacra, Ribeiro, Ribera de Duero, Ribera del Guadiana, Rueda, Rioja, Málaga, Utiel-Requena, Valdeorras, Valdepeñas, Valencia, Vinos de Madrid y Yecla (Tabla M4 y Figura M1, páginas 50 y 51). Dentro de este material también se incluyeron algunas muestras procedentes de fuera de España, siguiendo para su obtención el mismo procedimiento que para las variedades de uva de mesa. En total se dispuso de material de 35 plantaciones para el estudio de Homogeneidad y de 84 plantaciones adicionales para el estudio de Estabilidad. En cada plantación, se siguió siempre que era posible, el siguiente protocolo de toma de muestras: Recolección, en la mayoría de los casos, de hojas jóvenes, de unos 4 a 7 cm de longitud, localizadas en pámpanos verdes en pleno crecimiento de plantas seleccionadas al azar. Introducción de cada una de las muestras en sobres de papel individuales, perfectamente identificados. Mantenimiento de los sobres en frío hasta su llegada al laboratorio. Generalmente en neveras con acumuladores de frío. Una vez en el laboratorio, almacenamiento de las muestras en arcones a -80ºC, hasta su posterior utilización. Se recabó toda la información posible de las plantaciones en las cuales se recogió material vegetal; en concreto, se solicitó: Nombre de la finca y del propietario de la misma. Localización geográfica: población, provincia, país y siempre que fue posible, datos GPS para la mayoría de las fincas españolas. Conducción de las plantas (en vaso, en espaldera, en parral, en lira etc.). Año de plantación: se intentó cuando fue posible, recoger muestras con un amplio rango en cuanto al año de plantación para cada variedad. En algunos casos no fue posible obtener una fecha de plantación, ya que en el lugar de recogida no se disponía de estos datos. Procedencia de las plantas (viveros, injertos, etc.) 48
71 Materiales y Métodos Pertenencia a alguna Denominación de Origen. En total se muestrearon plantas de 7 países diferentes. Debido a la gran cantidad de información recogida, fue necesario crear una base de datos relacional en Microsoft Access, con el fin de optimizar la extracción de información útil a partir de la misma, y facilitar su análisis. Las Tablas M5 - M23, páginas 52-70, corresponden a cada una de las variedades estudiadas, donde se detalla exhaustivamente el muestreo para cada una de ellas. Se han omitido, por razones de confidencialidad, los nombres de las fincas y sus coordenadas GPS. 49
72 Materiales y Métodos Tabla M4. Denominaciones de Origen presentes en el estudio. Se citan las variedades que corresponden a cada una de ellas y el número de muestras recogidas de cada variedad. D.O VARIEDADES Nº DE MUESTRAS POR VARIEDAD TOTAL Almansa Monastrell 7 7 Calatayud Tempranillo 7 7 Campo de Borja Moscatel de Málaga-Tempranillo Cariñena Garnacha-Moscatel de Málaga Cataluña Chardonnay-Monastrell-Moscatel de Málaga-Sauvignon blanc Condado de Huelva Palomino fino Costers del Segre Garnacha-Merlot Jerez Monastrell-Moscatel de Málaga-Palomino fino Jumilla Airén-Monastrell La Mancha Airén-Cabernet sauvignon-garnacha Méntrida Garnacha Monterrei Palomino fino 7 7 Montilla-Moriles Airén-Moscatel de Málaga Navarra Cabernet sauvignon-chardonnay-garnacha-merlot Penedés Cabernet sauvignon-tempranillo Ribeira Sacra Palomino fino 7 7 Ribeiro Palomino fino 7 7 Ribera de Duero Cabernet sauvignon-garnacha-merlot-tempranillo Ribera del Guadiana Cabernet sauvignon-chardonnay-garnacha-merlot-monastrell-tempranillo Rioja Garnacha-Tempranillo Rueda Palomino fino-sauvignon blanc Sierra de Málaga Cabernet sauvignon-chardonnay-garnacha-merlot- Moscatel de Málaga-Sauvignon blanc-tempranillo Utiel-Requena Chardonnay-Garnacha-Merlot-Tempranillo Valdeorras Palomino fino 7 7 Valdepeñas Airén-Tempranillo Valencia Chardonnay-Monastrell Vinos de Madrid Airén-Garnacha-Merlot Yecla Monastrell
73 Materiales y Métodos Figura M1. Representación geográfica de las 28 Denominaciones de Origen que han participado en el estudio. Monterrey Ribeira Sacra Valdeorras Rioja Navarra Tarragona Ribeiro Costers del Segre Ribera del Duero Penedés Rueda Campo de Borja Cariñena Méntrida Ribera del Guadiana Calatayud Utiel-Requena La Mancha Almansa Valencia Vinos de Madrid Jumilla Yecla Condado de Huelva Montilla-Moriles Valdepeñas Jerez Málaga 51
74 Materiales y Métodos Tabla M5. Datos de la recogida de muestras de la variedad Airén. Nº LUGAR DE RECOGIDA FINCA PAÍS PROVINCIA POBLACIÓN 1 España Ciudad Real Alcázar de San Juan Nº PLANTAS RECOLECTADAS VARIEDAD AIRÉN AÑO RECOLECCIÓN AÑO PLANTACIÓN ORIGEN PLANTACIÓN DENOMINACIÓN DE ORIGEN OBSERVACIONES La Mancha La Mancha Vaso 2 España Murcia Jumilla Jumilla Jumilla Vaso. 8 plantas no eran Airén 3 España Córdoba Montilla Montilla Montilla- Vaso. 6 plantas Moriles no eran Airén 4 España Murcia Jumilla Jumilla Jumilla Vaso 5 España Ciudad Vivero de Montiel Real Valencia Valdepeñas Vaso 6 España Ciudad Vivero de Valdepeñas Real Valencia Valdepeñas Vaso 7 España Ciudad Alcázar de Autóctono Real San Juan Tradicional La Mancha Vaso 8 España Guadalajara Pioz Cuenca 9 España Madrid San Martín Vinos de de Madrid Valdeiglesias Vaso 10 España Madrid Arganda Vinos de Madrid Vaso 52
75 Materiales y Métodos Tabla M6. Datos de la recogida de muestras de la variedad Cabernet sauvignon. Nº LUGAR DE RECOGIDA FINCA PAÍS PROVINCIA POBLACIÓN 1 Chile 2 Sudáfrica Santiago de Chile Western Cape VARIEDAD CABERNET SAUVIGNON Nº PLANTAS RECOLECTADAS AÑO RECOLECCIÓN La Pintana AÑO PLANTACIÓN ORIGEN PLANTACIÓN Stellenbosch Sudáfrica 3 España Burgos La Horra Rioja DENOMINACIÓN DE ORIGEN Ribera de Duero OBSERVACIONES Espaldera 4 España Ciudad Alcázar de Vivero de Real San Juan Valencia La Mancha Vaso 5 Hungría Kecskemét España Barcelona Torrelavit Burdeos Penedés Espaldera 7 España Navarra Olite Viveros (clon certificado) Navarra Espaldera 8 Alemania Siebeldingen Vivero Freytag 9 España Badajoz Alanje Ribera del Guadiana Espaldera 10 España Málaga Antequera Francia Sierra de Málaga Espaldera 11 USA California Davis Francia Montpellier Francia Montpellier Fronsac, Gironde (Francia) Finca Macula, Santiago de Chile(Chile) 53
76 Materiales y Métodos Tabla M7. Datos de la recogida de muestras de la variedad Cardinal. Nº LUGAR DE RECOGIDA FINCA PAÍS PROVINCIA POBLACIÓN 1 España Sevilla Los Palacios y Villafranca Nº PLANTAS RECOLECTADAS VARIEDAD CARDINAL AÑO RECOLECCIÓN AÑO PLANTACIÓN ORIGEN PLANTACIÓN DENOMINACIÓN DE ORIGEN OBSERVACIONES Injerto Vaso 2 España Cádiz Jerez Espaldera Ninguna planta 3 Hungría Kecskemét era Cardinal 4 España Cádiz Jerez Injerto Espaldera 5 USA California España Cádiz Jerez Viveros "Vitis Jerez" 7 USA California Davis Francia Montpellier EEUU 9 España Madrid 10 España Madrid 11 España Sevilla 12 España Sevilla 13 España Madrid Alcalá de Henares Alcalá de Henares Dos Hermanas Los Palacios Alcalá de Henares Embajada de España en Roma (Italia) Espaldera Espaldera/Vaso Málaga Vaso Vivero Rauscedo(Italia) Autóctono Vaso Italia Espaldera Lira 54
77 Materiales y Métodos Tabla M8. Datos de la recogida de muestras de la variedad Chardonnay. Nº LUGAR DE RECOGIDA FINCA PAÍS PROVINCIA POBLACIÓN VARIEDAD CHARDONNAY Nº PLANTAS RECOLECTADAS AÑO RECOLECCIÓN AÑO PLANTACIÓN 1 España Badajoz Almendralejo España Navarra Olite Sudáfrica Western Cape ORIGEN PLANTACIÓN Viveros (clones comerciales) Stellenbosch Sudáfrica 4 Francia Montpellier Chile Santiago de Chile La Pintana Meursault, Cote d Or (Francia) DENOMINACIÓN DE ORIGEN Ribera del Guadiana Navarra OBSERVACIONES Espaldera 6 España Valencia Utiel Utiel- Requena Espaldera 7 España Tarragona Montblanc Cataluña Espaldera 8 España Málaga Antequera Francia Sierra de Málaga Espaldera 9 España Valencia Fontanars dels Alforins Alemania Siebeldingen Hungría Kecskemét USA California Davis Avignon (Francia) Vivero Freytag Valencia 55
78 Materiales y Métodos Tabla M9. Datos de la recogida de muestras de la variedad Crimson seedless. Nº LUGAR DE RECOGIDA FINCA PAÍS PROVINCIA POBLACIÓN VARIEDAD CRIMSON SEEDLESS Nº PLANTAS RECOLECTADAS AÑO RECOLECCIÓN AÑO PLANTACIÓN ORIGEN PLANTACIÓN DENOMINACIÓN DE ORIGEN OBSERVACIONES 1 España Murcia Alhama de Murcia España Murcia Alhama de Murcia España Cádiz Jerez Espaldera 4 España Murcia Abarán España Murcia Alhama de Murcia USA California España Murcia USA 8 USA California USA California España Murcia Cieza Chile V Región Llay Llay Sudáfrica 13 Sudáfrica 14 Sudáfrica Western Cape Western Cape Western Cape Saron Sudáfrica Saron Sudáfrica Saron Sudáfrica 15 España Cádiz Jerez Viveros Santa Margarita Parral 56
79 Materiales y Métodos Tabla M10. Datos de la recogida de muestras de la variedad Flame seedless. Nº LUGAR DE RECOGIDA FINCA PAÍS PROVINCIA POBLACIÓN VARIEDAD FLAME SEEDLESS Nº PLANTAS RECOLECTADAS AÑO RECOLECCIÓN 1 España Murcia AÑO PLANTACIÓN ORIGEN PLANTACIÓN Viveros Provedo (Logroño) DENOMINACIÓN DE ORIGEN OBSERVACIONES 2 España Cádiz Jerez España Cádiz Jerez Chile V Región Llay Llay USA California Davis España Murcia Águilas Viveros Valencia 7 USA California USA California España Murcia Abarán España Cádiz Jerez Injerto Espaldera 11 España Cádiz Jerez Viveros "Vitis Jerez" Espaldera 57
80 Materiales y Métodos Tabla M11. Datos de la recogida de muestras de la variedad Garnacha. Nº LUGAR DE RECOGIDA FINCA PAÍS PROVINCIA POBLACIÓN 1 España Ciudad Real Alcázar de San Juan VARIEDAD GARNACHA Nº PLANTAS RECOLECTADAS AÑO RECOLECCIÓN AÑO PLANTACIÓN España La Rioja Logroño ORIGEN PLANTACIÓN Vivero de Valencia Autóctono ( ) DENOMINACIÓN DE ORIGEN La Mancha Rioja OBSERVACIONES Vaso. Todas la plantas eran Garnacha Tintorera 3 España Lérida Balaguer Francia Costers del Segre Espaldera 4 España Badajoz Alanje Ribera del Guadiana Espaldera 5 España Málaga Antequera Francia Sierra de Málaga Espaldera 6 España Burgos La Horra Rioja Ribera de Duero Espaldera/Vaso 7 España Zaragoza Cariñena Cariñena Vaso 8 España Madrid San Martín de Vinos de Autóctono Valdeiglesias Madrid Espaldera 9 España Navarra Olite España Valencia El Rebollar Viveros (clones comerciales) Navarra Utiel- Requena 11 España Madrid España Madrid Alcalá de Henares Madrid Vaso 13 España Toledo La Torre de Esteban Hambrán Méntrida Vaso Vaso 58
81 Materiales y Métodos Tabla M12. Datos de la recogida de muestras de la variedad Italia. Nº LUGAR DE RECOGIDA FINCA PAÍS PROVINCIA POBLACIÓN Nº PLANTAS RECOLECTADAS VARIEDAD ITALIA AÑO RECOLECCIÓN AÑO PLANTACIÓN ORIGEN PLANTACIÓN DENOMINACIÓN DE ORIGEN OBSERVACIONES 1 España Alicante Monforte Valencia 2 España Murcia Alhama de Murcia España Murcia Alhama de Murcia USA California España Murcia Alhama de Murcia Hungría Kecskemét Chile Santiago de Chile La Pintana España Huelva Almonte Alicante Espaldera 9 España Murcia Abarán España Murcia Alhama de Murcia USA California Davis
82 Materiales y Métodos Tabla M13. Datos de la recogida de muestras de la variedad Merlot. Nº LUGAR DE RECOGIDA FINCA PAÍS PROVINCIA POBLACIÓN Nº PLANTAS RECOLECTADAS VARIEDAD MERLOT AÑO RECOLECCIÓN AÑO PLANTACIÓN ORIGEN PLANTACIÓN 1 España Burgos La Horra Rioja 2 España Navarra Olite España Valencia Utiel Chile 5 Sudáfrica Santiago de Chile Western Cape La Pintana Viveros (clones comerciales) Stellenbosch Sudáfrica 6 Alemania Siebeldingen Vivero Freytag 7 España Madrid Cenicientos Francia 8 España Badajoz Alanje Francia Montpellier Gauriac, Gironde (Francia) 10 España Málaga Antequera Francia 11 USA California Davis España Lérida Marcovau España Madrid Alcalá de Henares DENOMINACIÓN DE ORIGEN Ribera de Duero Navarra Utiel- Requena Vinos de Madrid Ribera del Guadiana Sierra de Málaga Costers del Segre OBSERVACIONES Espaldera/Vaso.Ninguna planta era Merlot Espaldera Vaso Espaldera Espaldera Espaldera Francia Vaso 60
83 Materiales y Métodos Tabla M14. Datos de la recogida de muestras de la variedad Monastrell. Nº LUGAR DE RECOGIDA FINCA PAÍS PROVINCIA POBLACIÓN 1 España Valencia Fontanars dels Alforins VARIEDAD MONASTRELL Nº PLANTAS RECOLECTADAS AÑO RECOLECCIÓN AÑO PLANTACIÓN ORIGEN PLANTACIÓN Viveros Soriano, Onteniente (Valencia) DENOMINACIÓN DE ORIGEN Valencia 2 España Cádiz Jerez Jerez 3 España Murcia Jumilla Villena (Valencia) Jumilla OBSERVACIONES Espaldera Espaldera. Sólo 5 plantas eran Monastrell 4 España Badajoz Alanje Ribera del Guadiana Vaso 5 España Albacete Almansa Almansa Almansa Vaso 6 España Tarragona Vimbodí Viveros Chauvin (Francia) Cataluña Espaldera 7 España Murcia Yecla Autóctono Yecla Vaso Vaso.1 planta no era Monastrell 8 España Madrid España Madrid Alcalá de Henares Albacete Vaso 10 España Madrid Alcalá de Henares Lérida Vaso 61
84 Materiales y Métodos Tabla M15. Datos de la recogida de muestras de la variedad Moscatel de Málaga. Nº LUGAR DE RECOGIDA FINCA PAÍS PROVINCIA POBLACIÓN VARIEDAD MOSCATEL DE MÁLAGA Nº PLANTAS RECOLECTADAS AÑO RECOLECCIÓN AÑO PLANTACIÓN 1 España Córdoba Montilla España Málaga Fuente de Piedra ORIGEN PLANTACIÓN Barcelona DENOMINACIÓN DE ORIGEN Montilla- Moriles Sierra de Málaga 3 España Tarragona Vila Rodona Cataluña OBSERVACIONES Espaldera. Ninguna planta era Moscatel de Málaga Espaldera. Ninguna planta era Moscatel de Málaga Espaldera.1 planta no era Moscatel de Málaga 4 España Cádiz Jerez Jerez Espaldera 5 España Cádiz Chipiona Chipiona Jerez Vaso 6 España Cádiz Chipiona Chipiona Jerez Vaso 7 España Zaragoza Ainzón Francia Montpellier Finca Pulenta, San Juan (Argentina) Campo de Borja Espaldera. Ninguna planta era Moscatel de Málaga 2 plantas no eran Moscatel de Málaga 9 España Tenerife Güímar España Tenerife La Orotava USA California Davis España Zaragoza Encina Corba Cariñena Vaso 13 España Madrid Alcalá de Torrox Henares (Málaga) Vaso 14 España Málaga El Borge Autóctono Vaso 15 España Madrid Alcalá de Henares Lanzarote Vaso 62
85 Materiales y Métodos Tabla M16. Datos de la recogida de muestras de la variedad Napoleón. Nº LUGAR DE RECOGIDA VARIEDAD NAPOLEÓN Nº PLANTAS RECOLECTADAS AÑO RECOLECCIÓN AÑO PLANTACIÓN ORIGEN PLANTACIÓN FINCA PAÍS PROVINCIA POBLACIÓN 1 España Almería Terque Almería 2 España Alicante Hondón de las Nieves España Murcia Alhama de Murcia España Almería Terque España Murcia Sotana España Cádiz Jerez España Murcia Abarán España Murcia Abarán España Murcia Alhama de Murcia España Murcia Cieza España Murcia Alhama de Murcia España Madrid Viveros "Vitis Jerez" DENOMINACIÓN DE ORIGEN OBSERVACIONES Espaldera. Experimental 63
86 Materiales y Métodos Tabla M17. Datos de la recogida de muestras de la variedad Ohanes. Nº LUGAR DE RECOGIDA FINCA PAÍS PROVINCIA POBLACIÓN Nº PLANTAS RECOLECTADAS VARIEDAD OHANES AÑO RECOLECCIÓN AÑO PLANTACIÓN ORIGEN PLANTACIÓN DENOMINACIÓN DE ORIGEN OBSERVACIONES 1 España Almería Terque Almería 2 España Almería Berja Yemas injertadas de la zona Parral 3 España Almería Terque Almería 4 España Almería Bentarique Almería 5 España Almería Terque Almería 6 España Almería Terque Almería 7 España Cádiz Jerez Espaldera 8 España Cádiz Jerez Espaldera 9 Francia Montpellier Rajonska Poljoprior (Yougoslavia) 10 España Madrid Alcalá de Henares Almería Vaso 11 España Almería Canjayar Autóctono Parral 64
87 Materiales y Métodos Tabla M18. Datos de la recogida de muestras de la variedad Palomino fino. Nº LUGAR DE RECOGIDA FINCA PAÍS PROVINCIA POBLACIÓN VARIEDAD PALOMINO FINO Nº PLANTAS RECOLECTADAS AÑO RECOLECCIÓN AÑO PLANTACIÓN ORIGEN PLANTACIÓN DENOMINACIÓN DE ORIGEN OBSERVACIONES 1 España Valladolid La Seca Rueda Vaso. Ninguna planta era Palomino fino 2 España Cádiz Jerez Jerez Espaldera 3 España Huelva Almonte España Cádiz Jerez España Ourense Barzamedelle- Leiro Colección Jerez 1943 Condado de Huelva Jerez Ribeiro 6 España Ourense Monterrei Monterrei 7 España Ourense A Rua España Lugo Concello de Sober Injertos propios Valdeorras Ribeira Sacra 9 España Cádiz Jerez Jerez Espaldera. 8 plantas no eran Palomino fino Espaldera Ninguna planta era Palomino fino Espaldera. 1 planta no era Palomino fino 10 España Cádiz Jerez Jerez 11 España Cádiz Jerez Jerez 12 España Madrid Alcalá de Henares Huelva Vaso 13 España Madrid Alcalá de Cigales Henares (Valladolid) Vaso 65
88 Materiales y Métodos Tabla M19. Datos de la recogida de muestras de la variedad Red globe. Nº LUGAR DE RECOGIDA FINCA PAÍS PROVINCIA POBLACIÓN Nº PLANTAS RECOLECTADAS VARIEDAD RED GLOBE AÑO RECOLECCIÓN AÑO PLANTACIÓN 1 España Almería Terque ORIGEN PLANTACIÓN Cooperativa Albentillas (Almería) 2 España Murcia Alhama de Murcia España Alicante Monforte Valencia 4 España Alicante Monforte Valencia 5 España Murcia Totana España Murcia Alhama de Murcia España Murcia El Paretón España Murcia Alhama de Murcia España Murcia Cieza España Murcia Águilas DENOMINACIÓN DE ORIGEN OBSERVACIONES 6 plantas no eran Red globe 66
89 Materiales y Métodos Tabla M20. Datos de la recogida de muestras de la variedad Sauvignon blanc. Nº LUGAR DE RECOGIDA FINCA PAÍS PROVINCIA POBLACIÓN VARIEDAD SAUVIGNON BLANC Nº PLANTAS RECOLECTADAS AÑO RECOLECCIÓN AÑO PLANTACIÓN ORIGEN PLANTACIÓN DENOMINACIÓN DE ORIGEN OBSERVACIONES 1 España Valladolid La Seca Rueda Rueda Espaldera 2 España Tarragona Montblanc Cataluña Espaldera 3 España Málaga Antequera Francia Sierra de Málaga Espaldera 4 Hungría Kecskemét Chile Santiago de Chile La Pintana Sudáfrica Western Cape Stellenbosch Sudáfrica 7 España Valladolid Rueda Francia Rueda Espaldera 8 Francia Montpellier Naujan et Postiac, Gironde (Francia) 9 Alemania Siebeldingen USA California Davis Vivero Freytag 67
90 Materiales y Métodos Tabla M21. Datos de la recogida de muestras de la variedad Sugraone. Nº LUGAR DE RECOGIDA FINCA PAÍS PROVINCIA POBLACIÓN Nº PLANTAS RECOLECTADAS VARIEDAD SUGRAONE AÑO RECOLECCIÓN 1 España Murcia AÑO PLANTACIÓN ORIGEN PLANTACIÓN Sunworld (USA) 2 Sudáfrica Western Cape Saron Sudáfrica 3 España Murcia Águilas Chile Santiago de Chile La Pintana España Murcia El Paretón España Almería Terque Murcia 7 España Murcia Águilas Viveros Valencia 8 España Alicante Monforte Valencia 9 España Murcia El Paretón España Murcia Archena Sudáfrica 12 Sudáfrica 13 Sudáfrica Western Cape Western Cape Western Cape Saron Sudáfrica Saron Sudáfrica Saron Sudáfrica DENOMINACIÓN DE ORIGEN OBSERVACIONES 68
91 Materiales y Métodos Tabla M22. Datos de la recogida de muestras de la variedad Tempranillo. Nº LUGAR DE RECOGIDA FINCA PAÍS PROVINCIA POBLACIÓN 1 España Ciudad Real VARIEDAD TEMPRANILLO Nº PLANTAS RECOLECTADAS AÑO RECOLECCIÓN AÑO PLANTACIÓN Montiel ORIGEN PLANTACIÓN Vivero de Valencia 2 España Burgos La Horra Rioja 3 España Barcelona El Pla del Penedés 4 España Badajoz Alanje DENOMINACIÓN DE ORIGEN Valdepeñas Ribera de Duero Autóctono Penedés 5 España La Rioja Logroño Bodegas Berrueco, Villabuena de Álava (Álava) Ribera del Guadiana Rioja OBSERVACIONES Espaldera Espaldera Espaldera. 2 plantas no eran Tempranillo Espaldera 6 España Málaga Antequera Francia Sierra de Málaga Espaldera 7 España Zaragoza Ainzón Rioja Campo de Borja Espaldera 8 España Zaragoza Alarba Calatayud Vaso 9 España Valencia Utiel Utiel- Requena Espaldera 10 España Guadalajara Pioz Autóctono. Tradicional 69
92 Materiales y Métodos Tabla M23. Datos de la recogida de muestras de la variedad Thompson seedless. Nº LUGAR DE RECOGIDA FINCA PAÍS PROVINCIA POBLACIÓN 1 Sudáfrica Western Cape VARIEDAD THOMPSON SEEDLESS Nº PLANTAS RECOLECTADAS AÑO RECOLECCIÓN AÑO PLANTACIÓN ORIGEN PLANTACIÓN Saron Sudáfrica DENOMINACIÓN DE ORIGEN OBSERVACIONES En Rancho la maceta.ninguna 2 España Almería Vicar Merced planta era (Jerez) Thompson SDL 3 España Cádiz Jerez Injerto Espaldera 4 Sudáfrica 5 Sudáfrica 6 Sudáfrica Western Cape Western Cape Western Cape Saron Sudáfrica Saron Sudáfrica Saron Sudáfrica 7 España Murcia Abarán USA California USA California USA California Davis Chile Santiago de Chile La Pintana España Madrid España Cádiz Jerez España Madrid Alcalá de Henares Viveros "Vitis Jerez" Ninguna planta era Thompson SDL Espaldera Grecia Espaldera 70
93 Materiales y Métodos Establecimiento de descriptores microsatélite El proyecto de la Unión Europea GENRES081 fue el principal intento internacional para armonizar un sistema basado en microsatélites para la identificación de variedades de vid. Se seleccionaron 6 microsatélites (VVS2, VVMD5, VVMD7, VVMD27, ssrvrzag62 y ssrvrzag79), y se analizaron por 10 laboratorios diferentes, idénticas muestras de DNA, pertenecientes siempre que fue posible, a variedades de vid bien conocidas y ampliamente distribuidas geográficamente (This et al., 2004). Para cada marcador, cada uno de sus alelos se designó mediante un código basado en el nombre del cultivar tomado como referencia que presentó ese alelo en particular. Con ello, se perseguía desarrollar una base de datos común e internacional que contuviera alelos de referencia microsatélite para la identificación de variedades de vid. Con los resultados obtenidos, se elaboraron descriptores para los 6 loci microsatélite estudiados. Estos descriptores fueron aprobados por la OIV en la reunión celebrada en Junio del en Budapest (Hungría). En este estudio se siguió esencialmente la metodología desarrollada en This et al. (2004), para la elaboración de descriptores microsatélite. El material utilizado para ello, estuvo compuesto en su mayoría, por ADN de plantas de la Colección de vides de El Encín. La Tabla M24 muestra aquellos cultivares utilizados en este estudio, pertenecientes a variedades empleadas en This et al. (2004), con algunas características relevantes. De todos ellos, 14 se tomaron del material con el que se llevó a cabo el estudio de This et al. (2004), ya que no estaban presentes en la Colección de vides de El Encín. Los cultivares Touriga nacional y Barbera, incluidos en el estudio anterior, no están presentes en este trabajo, ya que no se disponía de ellos. 71
94 Materiales y Métodos Tabla M24. Cultivares de vid empleados para la elaboración de descriptores microsatélite. Color de la baya (B-blanco, N-negro y RG-rojo); True to type (variedades que estudiadas en This et al. (2004) mediante ampelografía, correspondían o no a la descripción oficial de la misma); Cultivares de referencia (cultivares empleados como referencia de alelos). NOMBRE VARIEDAD COLOR BAYA CÓDIGO TRUE TO TYPE CULTIVARES DE REFERENCIA 1 Admirable de Courtiller B SI NO 2 Alvarelhao N AL SI SI 3 Argiogitiko N SI NO 4 Cabernet franc N CF SI SI 5 Cabernet sauvignon N CS SI SI 6 Carignan N SI NO 7 Castel 216-3* SI NO 8 Chardonnay B CH SI SI 9 Couderc 1616* 16C SI SI 10 Couderc 3309* 33C SI SI 11 Fercal* FE SI SI 12 Furmint B SI NO 13 Goethe 9* GO NO SI 14 Hans RG SI NO 15 Jacquez N JA NO SI 16 Kober 5 BB* 5BK SI SI 17 Madeleine royale B MAR SI SI 18 Malegue 44-53* 4MA SI SI 19 Mancin N MAN SI SI 20 Mauzac B MAU SI SI 21 Mavrodaphni N MAV SI SI 22 Merlot N ME SI SI 23 Millardet et Grasset * N 1MG SI SI 24 Millardet et Grasset 420A* 4MG SI SI 25 Mourvedre N SI NO 26 Muscat a petits grains blancs B MU SI SI 27 Muscat of Alexandria B SI NO 28 Paulsen 1103* SI NO 29 Pinot noir N PI SI SI 30 Portugieser blau N PO SI SI 31 Richter 110* 11R SI SI 32 Richter 99* 99R SI SI 33 Romorantin B RO SI SI 34 Rondinella N SI NO 35 Ruggeri 140* SI NO 36 Salvador ( = Seibel 128) SAL SI SI 37 Schwarzmann SCH SI SI 38 Silvaner B SI SI SI 39 Sultanina gigas B SU SI SI 40 Teleki 5 C* 5C SI SI 41 Traminer rot RG TR SI SI 42 Trebbiano toscano B NO NO 43 Veltliner rot RG VE SI SI 44 Vialla* N VIA SI SI 45 Vital B VI SI SI * portainjertos 72
95 Materiales y Métodos 3.2. MÉTODOS Extracción de ADN Para la extracción de ADN, inicialmente se empleó el kit comercial DNeasy Plant mini Kit de la empresa Qiagen, mediante el cuál se extraían un máximo de 50 muestras al día. Posteriormente, se empleó el kit DNeasy 96 Plant Kit de la misma empresa, el cuál permitió procesar 192 muestras a la vez. Los dos kits eran casi idénticos, la única diferencia que existía entre ellos, era el formato de columnas para la extracción; individuales para el DNeasy Plant mini Kit, y en placas de 96 columnas para el DNeasy 96 Plant Kit. El ADN perteneciente a las 112 muestras de Briones (Tabla M1, página 42), se extrajo en su totalidad con el DNeasy 96 Plant Kit. Para la extracción del ADN se utilizaron hojas jóvenes, obtenidas de los brotes tiernos que previamente habían sido congelados. Independientemente del kit empleado, se siguió esencialmente el protocolo del fabricante. Las muestras se trituraron en el molino Mixer Mill MM300 (1 minuto a 20Hz). Por cada muestra se introdujo en un tubo 50 mg de hoja conservada a - 80ºC, una bolita de tungsteno y una pequeña cantidad de PVPP (Poli Vinil Poli Pirrolidona) para mejorar el rendimiento de la extracción, debido a la cantidad de polifenoles que presenta la hoja de vid. En el proceso de triturado se utilizó Nitrógeno líquido para evitar la descongelación de las muestras y permitir así la destrucción de las paredes celulósicas de las células vegetales por acción de las bolitas de tungsteno. Posteriormente se añadió tampón de lisis para romper la membrana celular y proteger el ADN de la degradación. Asimismo, se incorporó una ARNasa para degradar el ARN, el cuál podría interferir en la cuantificación del ADN y/o en la posterior reacción de PCR. Sucesivas etapas de precipitación, filtración, unión selectiva a una matriz, lavados alcohólicos y elución sirvieron para la purificación de ese ADN, eliminando restos de membranas, proteínas, polisacáridos y otros componentes celulares Estimación de la calidad y cantidad del ADN extraído Para evaluar la calidad y la cantidad de los ADN, estos se sometieron a electroforesis en geles horizontales de agarosa al 0,8% y tampón TAE 1X (Trisacetato 40mM, EDTA ph 8 1mM). Tanto los geles como los tampones de 73
96 Materiales y Métodos electroforesis, contenían bromuro de etidio a una concentración de 0,5µg/ml, para poder visualizar el ADN al iluminarlo con luz UV. Las electroforesis se llevaron a cabo a temperatura ambiente y bajo una diferencia de potencial de unos 2 V/cm. La calidad se evaluó atendiendo a la presencia de una banda nítida de alto peso molecular, y observando el grado de rotura y/o degradación presente, visible como un rastro a partir de esa banda. Para estimar la cantidad, se incluyeron en el gel diferentes muestras de cantidades conocidas de ADN del fago lambda sin digerir junto a los ADN a cuantificar. Se obtuvieron distintas bandas con diferentes intensidades de fluorescencia, correspondientes a distintas cantidades de ADN. La comparación de la fluorescencia emitida por los ADN problema frente a los estándar permitió determinar la cantidad presente en los primeros. Las imágenes se obtuvieron con un equipo de análisis de imagen (UVP 5000 Imagestore) Métodos de análisis de microsatélites (STMS) de genoma nuclear Amplificación de las secuencias STMS mediante PCR En los 9 loci microsatélite seleccionados para realizar este trabajo, un cebador de cada pareja (cebador directo o upper ) incorporaba una molécula de fluorocromo de entre tres posibles: 6-FAM, TET y HEX, para permitir la posterior detección del fragmento amplificado. El diseño hacía posible la amplificación y análisis conjunto de los 9 microsatélites mediante PCR múltiple (o multiplex). Para ello se optimizó una mezcla de reacción y un programa de amplificación que se muestran en el apartado de Resultados y Discusión. Las reacciones de amplificación se llevaron a cabo en un termociclador PTC-100 de MJ Research Determinación del tamaño de los alelos de los STMS Se realizó esencialmente de acuerdo a Borrego et al. (2000). Tras la PCR se comprobó si se había producido la amplificación. Para ello se tomaron alícuotas de 7µl y se sometieron a electroforesis a temperatura ambiente en geles de agarosa al 2% (p/v) con tampón TAE 1X y bromuro de etidio (0,5µg/ml), aplicando una 74
97 Materiales y Métodos diferencia de potencial aproximada de 5V/cm. Además de las muestras, se incorporó en un pocillo de cada peine el marcador de peso molecular: 0,5µg de ADN del fago φx174 digerido con la enzima de restricción Hae III. El siguiente paso consistió en la separación y el análisis de fluorescencia de los microsatélites en el secuenciador ABI PRISM 310 con el software GeneScan (Applied Biosystems) empleado en este analizador genético. El ABI PRISM 310, es un secuenciador semiautomático. La electroforesis se lleva a cabo en el interior de un capilar donde las muestras se separan individualmente, a través de un polímero comercial ya preparado (POP4, de Applied Biosystems). Cada muestra procedente de la amplificación mediante PCR, se diluyó con agua entre diez y cien veces de acuerdo a la intensidad de fluorescencia observada en el gel de agarosa al 2%. A 1µl de la dilución se le añadieron 20 µl de formamida y 0,2 µl de un marcador de peso molecular: TAMRA 500 (Applied Biosystems). Esta mezcla se sometió a un tratamiento de calor (95ºC, 5 minutos) en el termociclador PTC-100 de MJ Research para desnaturalizar el ADN. Las muestras así preparadas se sometieron a electroforesis capilar en el ABI PRISM 310, a una diferencia de potencial de voltios y a 60ºC de temperatura. Próximo al extremo final, el capilar presenta una ventana transparente que, convenientemente alineada con el láser, permite excitar los fluorocromos que van pasando a través de la misma. Un lector del aparato detecta el paso de las moléculas de ADN a través de la fluorescencia emitida, cuya intensidad es almacenada. Tras la electroforesis, cada STMS se identificó por el color y el tamaño con el que aparecieron. Este color depende de dos factores: el fluorocromo que lleva incorporado el cebador en cada caso y el filtro utilizado para detectar la fluorescencia. El filtro adecuado para estos fluorocromos es el C, que da lugar a los siguientes colores: azul (para el fluorocromo 6-FAM), verde (para TET), amarillo (para HEX) y rojo (para TAMRA). Los datos brutos de intensidad de fluorescencia se recogieron en el programa informático ABI PRISM 310 Collection. Posteriormente, se analizaron con el software GeneScan. El análisis se realizó muestra a muestra, y comenzó por seleccionar manualmente los fragmentos o picos del marcador incorporado en cada una de ellas. En nuestro caso, TAMRA 500, se marcaron los picos correspondientes a los siguientes tamaños: 35, 50, 75, 100, 139, 150, 160, 200, 300, 350 y 400, de 75
98 Materiales y Métodos acuerdo a las instrucciones del fabricante y al rango de los tamaños de los fragmentos amplificados. El método recomendado y que se siguió para asignar el tamaño molecular del producto de amplificación se llama Local Southern. Los tamaños de los fragmentos amplificados, se calculan a partir de una recta de regresión entre los tamaños de los fragmentos del marcador de peso molecular y el tiempo de elución de los mismos (tiempo en el que pasan por el lector de la fluorescencia, menor cuanto menor es el tamaño). Como resultado de este proceso, no se obtienen valores enteros (que es lo esperable al medir el tamaño de los fragmentos de ADN, formados por un número determinado de nucleótidos) sino números reales con dos decimales. Estos valores expresados en números decimales, en el estudio de Homogeneidad y Estabilidad, se incorporaron a la base de datos de Access mencionada con anterioridad. En ocasiones se observó que uno o varios de los nueve microsatélites no amplificaron correctamente. Cuando esto ocurrió, se procedió a repetir la PCR para los mismos, de manera individual, o en conjunto. Si aún así no amplificaban correctamente, se procedió a la amplificación de la muestra diluyendo la solución de ADN, normalmente a una concentración de 1/10, para de este modo disminuir la concentración de posibles impurezas que pudieran estar interfiriendo negativamente en la reacción de PCR. Si después de esta dilución no se obtenía amplificación, lo que se hizo fue proceder a una nueva extracción del ADN de las muestras afectadas Categorización de alelos para los estudios de Distinción e Identificación Este proceso es necesario para construir una tabla de genotipos, que posteriormente sería de utilidad para llevar a cabo los estudios de Distinción e Identificación varietal. Debido a que los valores obtenidos para cada alelo de cada locus microsatélite analizado mediante el Software GeneScan, venían expresados con decimales, para ciertos estudios hubo que ajustarlos a los correspondientes números enteros (que corresponden idealmente a los pares de bases de los alelos). Para ello se usaron unas tablas de rangos previamente definidas en el laboratorio 76
99 Materiales y Métodos de Biología Molecular de la Finca El Encín, en las cuales se detalla una lista de valores enteros (alelos) para cada locus, y a la vez, para cada uno de ellos, dos valores GeneScan que corresponden a los valores máximo (rango inicio) y mínimo (rango fin) obtenidos para el mismo durante el análisis en el ABI PRISM 310 de un amplio número de ADN. En la Tabla M25 se muestra un ejemplo de los valores obtenidos para varios alelos del locus VVMD27, que es uno de los microsatélites empleados en este trabajo. Tabla M25. Rangos correspondientes a varios alelos del locus VVMD27. VALOR ENTERO (ALELO) RANGO INICIO RANGO FIN ,08 166, ,37 173, ,83 177, ,86 179, ,89 181, ,79 183, ,35 184, ,86 187, ,01 189, ,41 191, ,02 198,12 Estas tablas de rangos se obtuvieron realizando el proceso de categorización de alelos, en inglés allele binning o allele calling, que consiste en clasificar los valores obtenidos con GeneScan en diferentes categorías o bins, de manera que se incluyeran en la misma categoría aquellos valores que correspondieran al mismo alelo real. Para ello no se redondeó directamente el valor GeneScan al entero más próximo, sino que se llevó a cabo siguiendo esencialmente el algoritmo descrito por Ghosh et al. (1997). Dependiendo del microsatélite, el resultado obtenido como consecuencia de aplicar el algoritmo fue definitivo o no. En algunos casos fue necesario un ajuste manual, para el que se tuvieron en cuenta los valores de desviación estándar y el tipo de repetición de los diferentes loci empleados, así como otros elementos de interés. A veces, también fue necesario obtener nuevos valores GeneScan para tomar una decisión. Este proceso de allele binning se realizó durante el desarrollo del proyecto RF99-009, que llevaba por título Caracterización del Banco de Germoplasma de 77
100 Materiales y Métodos vid de El Encín mediante marcadores moleculares: microsatélites (STMS), desarrollándose la tabla de rangos inicial utilizada aquí para transformar valores GeneScan en números enteros asignándoles el valor de la categoría a la que corresponden. Durante el estudio para evaluar la Distinción, se tuvieron que crear nuevas categorías debido a que hubo muestras de Briones que presentaron valores de alelos que no encajaron en ninguna de las categorías ya existentes Análisis de microsatélites adicionales Durante el estudio de Distinción, fue necesario amplificar un determinado número de muestras con un número mayor de loci microsatélite. Se usaron 20 STMS: VVS2 (Thomas y Scott, 1993); VVMD5, VVMD7, VVMD21, VVMD24, VVMD25, VVMD27, VVMD28, VVMD32 (Bowers et al., 1996) y (Bowers et al., 1999b); VMC4F3 (Di Gaspero et al., 2000); VVIN73, VVIP31, VVIP60, VVIQ52, VVIV37, VVIV67, VVIN16, VVIB01 y VVIH54 (Merdinoglu et al., 2005) y VMC1B11 (Zyprian y Topfer, sin publicar 2005). Cuatro de ellos (VVMD5, VVS2, VVMD27 y VVMD28) se encuentran incluidos también en el conjunto de 9 microsatélites que ocupan este trabajo. La amplificación de algunas accesiones con los 20 loci microsatélite se hizo para aclarar dudas que surgieron acerca de su identidad cuando se analizaron con los 9 microsatélites iniciales. En estos 20 loci, un cebador de cada pareja (cebador directo o upper ) incorporaba una molécula de fluorocromo de entre cuatro posibles: FAM, NED, VIC y PET, para permitir la posterior detección del fragmento amplificado. La amplificación de estos 20 loci microsatélite se llevó a cabo mediante dos reacciones distintas de amplificación, una con 9 y otra con 11 loci, usando mezclas de reacción y programas de PCR previamente desarrollados en el laboratorio de Biología Molecular de la Finca El Encín (Vargas y col. en preparación). Estas reacciones de PCR se realizaron en el termociclador PTC-100 de MJ Research. Una vez concluido el proceso de amplificación, se comprobó su eficacia mediante electroforesis en geles de agarosa al 2% teñidos con bromuro de etidio. Posteriormente, estas muestras se sometieron a una electroforesis capilar en el analizador genético AB Tras la electroforesis, cada STMS se identificó, al 78
101 Materiales y Métodos igual que en el ABI PRISM 310, por el color y el tamaño con el que aparecieron. Este color depende del fluorocromo que lleva incorporado el cebador en cada caso y del filtro utilizado para detectar la fluorescencia. El filtro adecuado para estos fluorocromos es el G5, que da lugar a los siguientes colores: azul (para el fluorocromo FAM), rojo (para PET), amarillo (para NED), verde (para VIC) y naranja (para LIZ). LIZ corresponde al fluorocromo incorporado en el marcador de peso molecular utilizado en este análisis (LIZ Applied Biosystems). Los dos analizadores genéticos empleados en este estudio, ABI PRISM 310 y AB 3130, básicamente poseen el mismo mecanismo de electroforesis, presentando el ABI PRISM 310 un capilar, y el AB 3130 cuatro, por lo que este último puede analizar cuatro muestras a la vez. Las diferencias más relevantes que presentan entre sí, en este trabajo, son las siguientes: Marcador de peso molecular incorporado junto con las muestras a analizar. En el ABI PRISM 310 se usó el TAMRA 500 mientras que en el AB 3130 el LIZ 500, ambos de la casa comercial Applied Biosystems. Número de colores que aparecen en los electroforetogramas para identificar los fragmentos amplificados. Cuatro, incluido el marcador de peso molecular en el ABI PRISM 310 y cinco, incluido el marcador de peso molecular en el AB Software informático utilizado para analizar los resultados obtenidos. En el ABI PRISM 310 se empleó el software GeneScan, mientras que en el AB 3130 se empleó el GeneMapper 3.7. Los resultados son análogos, pero no idénticos: hay variaciones en el tamaño molecular obtenido para un mismo fragmento con los dos aparatos, aunque estas diferencias son consistentes para cada microsatélite, lo que permite identificar los distintos alelos sin ninguna duda Diseño experimental Protección legal Estudio de Distinción El estudio oficial de Distinción consiste fundamentalmente en buscar diferencias en caracteres morfológicos de la variedad analizada respecto a las demás, usando una colección de referencia apropiada, y en determinar si esas 79
102 Materiales y Métodos diferencias son superiores a una distancia mínima (distancia más pequeña que puede existir entre dos variedades para considerarlas diferentes). Por ello, el punto clave para establecer la distinción es determinar la distancia mínima que debería existir entre dos variedades de vid para que fueran consideradas distintas. En la actualidad, no existe un criterio definido utilizando marcadores moleculares. En este estudio, para establecer la distinción, se planteó el siguiente criterio: 1. Determinar el menor número de alelos diferentes entre plantas pertenecientes a sortogrupos diferentes. En términos generales se hablaría de establecer la menor diferencia intervarietal, excluyendo sports o mutantes somáticos. 2. Determinar el mayor número de alelos diferentes entre plantas pertenecientes a un mismo sortogrupo (incluye individuos procedentes de un mismo embrión original: clones, variedades sinónimas, EDV o sports). En términos generales se hablaría de determinar la mayor diferencia intravarietal. En función de la diferencia entre esos dos números, se podría o no determinar la distancia mínima con marcadores moleculares microsatélites. Para este estudio de Distinción, se partió de todo el material disponible en la Colección de variedades de vid de El Encín analizado previamente con los 9 loci microsatélite. A estos datos se le añadieron los de las muestras de Briones (Tabla M1, página 42), una vez se analizaron de igual manera; datos pertenecientes al estudio de Homogeneidad y Estabilidad; y datos correspondientes al estudio de establecimiento de descriptores microsatélite. Con ese conjunto de datos se obtuvo una colección que se estudió con el objetivo de establecer la distancia mínima (en número de alelos diferentes) requerida para declarar si una variedad es distinta de otra, o no. En esta colección, se llevaron a cabo comparaciones 2 a 2 entre todas las accesiones que la formaron, empleando para ello la aplicación de Excel Microsatellite Toolkit (Park, 2001). Este análisis permitió determinar en cuántos alelos de los 9 microsatélites coincidían las citadas accesiones. El análisis se centró en el estudio minucioso de las accesiones más próximas en cuanto a su genotipo para los 9 microsatélites. Se estudiaron las parejas de accesiones que coincidían en 18, 17 ó 16 alelos, de los 18 analizados (correspondientes a los 9 microsatélites), para estudiar si dentro de estos tres 80
103 Materiales y Métodos grupos, las accesiones pertenecen o no al mismo sortogrupo. En base a la experiencia previa, se consideró que las muestras que sólo coinciden en 15 alelos o menos, de los 18 analizados, pertenecen todas a sortogrupos diferentes. En el caso de coincidencia en 18, 17 o 16 alelos, se usaron dos importantes fuentes de información disponibles: Datos morfológicos de variedades de vinificación españolas [Félix Cabello, Inmaculada Rodríguez y Gregorio Muñoz (IMIDRA- Finca El Encín)]. Datos morfológicos y de microsatélites de un elevado número de variedades de vinificación y de mesa, procedentes tanto de España como del extranjero (Laboratorio de Biología Molecular de la Finca el Encín). En las accesiones que coincidieron en los 18 alelos, se comprobó si se habían considerado morfológicamente del mismo sortogrupo de acuerdo a los datos mencionados, y también a los datos encontrados en la siguiente bibliografía: (Borrego et al., 1990), (Galet, 2000) e (Ibáñez et al., 2003). Si era así, se procedió a seleccionar únicamente una accesión representativa para ese genotipo común que correspondería en principio a un determinado sortogrupo, y se eliminaron todas las demás de la tabla por considerarlas pertenecientes al mismo sortogrupo. Cuando no se encontraron datos que justificaran esa igualdad entre las muestras que coincidieron en los 18 alelos, se analizaron las accesiones implicadas con 20 loci microsatélite. Las accesiones que coincidieron en 17 y 16 alelos de los 18 analizados, también se amplificaron con 20 loci, debido a la proximidad existente entre ellas. Los resultados obtenidos con estos 20 microsatélites, se consideraron definitivos, independientemente de que hubiera datos bibliográficos o no, ya que es extremadamente improbable que con 25 loci microsatélite pudieran presentar el mismo genotipo, variedades procedentes de distintos embriones originales. Con estos datos, se determinó: 1. El menor número de alelos diferentes entre plantas pertenecientes a sortogrupos diferentes. 2. El mayor número de alelos diferentes entre plantas pertenecientes a un mismo sortogrupo (clones, variedades sinónimas, EDV o sports). 81
104 Materiales y Métodos En base a estos dos números, se estableció la distancia mínima con el sistema de 9 loci microsatélite seleccionado. Además, una vez eliminadas de la colección aquellas accesiones que presentaron entre sí el mismo genotipo con los 9 loci microsatélite y dejar únicamente una de ellas como representante, se obtuvo una colección formada por variedades de genotipos distintos, que se va a denominar a lo largo de este estudio Colección de genotipos únicos. Esta colección se tomó como referencia para realizar el estudio de Identificación varietal detallado más adelante Estudio de Homogeneidad y Estabilidad Este estudio de Homogeneidad y Estabilidad constituye por sí solo el proyecto VIN C2-1, subvencionado por la Dirección General del INIA, que llevaba por título: Evaluación de los marcadores moleculares STMS (microsatélites) para exámenes de Homogeneidad y Estabilidad en la protección legal de variedades de vid. Para evaluar la homogeneidad se estudiaron 50 plantas de cada variedad de 3 plantaciones distintas, y para evaluar la estabilidad se estudiaron 5 plantas de cada variedad de 7 plantaciones adicionales a las de homogeneidad. Por tanto, para realizar el proyecto se requería la recolección de al menos 185 muestras diferentes de hoja de vid, para cada una de las variedades seleccionadas (19), es decir, de un total de muestras. Para un estudio controlado de la estabilidad sería necesario multiplicar vegetativamente plantas de distintas variedades y comparar las descendencias con sus progenitores. Por ser la vid una planta leñosa de ciclo anual, llevar a cabo varias multiplicaciones sucesivas resultaría muy costoso en tiempo. Por ello se decidió aprovechar el hecho de que esa multiplicación se realiza de manera habitual para obtener las plantas que se utilizan al establecer los viñedos, bien por viveros, bien por los propios viticultores. El razonamiento seguido era que, al analizar plantas de la misma variedad de distintas procedencias lo que se haría en realidad sería precisamente estudiar la estabilidad, ya que con toda probabilidad procederían de distintos ciclos de multiplicación vegetativa respecto a la planta ancestral común originaria de la variedad. Por ello fue interesante comparar material antiguo con cepas más jóvenes de la misma variedad. En total, se 82
105 Materiales y Métodos analizaron al menos 10 plantaciones diferentes por variedad (incluidas las del estudio de Homogeneidad), y 5 plantas por plantación. Para el estudio de Homogeneidad hubo que estudiar un número elevado de plantas de cada variedad y plantación para constatar que los genotipos de los microsatélites se mantenían inalterables en todas ellas. Se asume que las plantas de cada plantación se encuentran aproximadamente en el mismo ciclo de reproducción vegetativa. Se analizaron las mismas variedades que para el estudio de Estabilidad, pero en este caso, un número mayor de plantas por plantación (50), y un total de 3 plantaciones diferentes por variedad. Una vez extraídos y amplificados los ADN de las plantas recolectadas, se sometieron a electroforesis en el analizador genético ABI PRISM 310. Seguidamente, se analizaron los datos obtenidos en GeneScan de los alelos microsatélites para cada una de las plantas analizadas. Estos datos vienen expresados en números reales con dos decimales, debido al método empleado por el software GeneScan para la asignación del tamaño molecular del producto de amplificación, que básicamente es una regresión lineal de los valores del estándar. Por ello, para un mismo alelo se pueden obtener valores GeneScan ligeramente distintos (por ejemplo 148,34 y 148,51). Es necesario determinar si dos valores corresponden al mismo alelo o no. Por ello se hizo un análisis de las diferencias que se produjeron entre los valores obtenidos para los alelos de distintas plantas de cada variedad. Para cada alelo de cada variedad se obtuvieron unos 185 valores GeneScan. Entre ellos, se determinaron los valores máximos y mínimos, y se estudió con más detalle cuando la diferencia entre esos valores fue superior a 1 nucleótido, lo que se consideró inicialmente como valor umbral para comprobar si existe cambio en el tamaño del alelo entre distintas plantas de la misma variedad. Debido a que los microsatélites utilizados tienen como unidad de repetición 2 nucleótidos, en principio, los alelos que esperamos se diferenciarían en 2 nucleótidos. En base a esto, y a la experiencia acumulada en el laboratorio de Biología Molecular de la Finca El Encín, durante el desarrollo de varios proyectos llevados a cabo con estos microsatélites, aceptamos que todos aquellos valores que se diferencien en menos de 1 nucleótido corresponden al mismo alelo. 83
106 Materiales y Métodos Cuando se detectaron diferencias superiores a 1 nucleótido, se procedió de la siguiente manera: 1. Se seleccionaron los ADN de las muestras a las que pertenecieron los valores máximos y mínimos de cada uno de los alelos correspondientes a los microsatélites que presentaron las diferencias. 2. Se repitieron las PCR de forma individual para cada uno de ellos con la misma polimerasa utilizada a lo largo del desarrollo del trabajo. Complementariamente, para mayor seguridad, en algunos casos se amplificaron también empleando otra polimerasa, la Pyrobest DNA polimerasa (Takara) utilizando un programa de PCR específico para ella. Dado que las variedades de vid son clónicas, si los microsatélites utilizados son homogéneos y estables en las variedades utilizadas, esperamos encontrar los mismos valores alélicos para cada microsatélite en cada una de las plantas que pertenezcan a la misma variedad, independientemente de su origen. En caso contrario, se tendrá que determinar dónde se ha producido la mutación, y la frecuencia con que tiene lugar ese suceso Defensa legal Estudio de Identificación El estudio de Identificación trata de buscar conformidad entre la planta analizada y alguna de las variedades que componen la colección de referencia. En este trabajo se llevó a cabo el estudio de Identificación utilizando microsatélites, para ello se tomó como colección de referencia, la Colección de genotipos únicos obtenida en el estudio de Distinción y que estaba formada por variedades de genotipos distintos para los 9 loci microsatélite que ocupan esta tesis. Esta colección se analizó con la versión 4 del software Identity (Wagner y Sefc, 1999) ( Con este análisis se determinó por un lado la Probabilidad Total de Identidad (PI) (probabilidad de que dos variedades distintas compartan el mismo genotipo al azar para los loci analizados); y por otro, la Heterocigosidad observada (Ho) de los 9 STMS elegidos, característica importante a la hora de determinar el poder de resolución del sistema en la identificación de las variedades que componen la colección. Para cada variedad se 84
107 Materiales y Métodos puede llevar a cabo un análisis matemático de la coincidencia, que se puede ver influenciado por la presencia de estructura en la colección Análisis matemático de la coincidencia Al analizar una planta, ésta puede presentar el mismo genotipo que una variedad determinada del conjunto estudiado. Esa coincidencia puede ser por azar, o porque realmente la planta pertenece a la variedad. En el ámbito legal, es conveniente acompañar el análisis molecular con un análisis matemático para conocer su fiabilidad. Para calcular la probabilidad de que por azar, una planta de vid presente el mismo genotipo para los 9 loci STMS que alguna de las variedades pertenecientes a las poblaciones tomadas como referencia, se calculó el cociente de probabilidades, de manera análoga al likelihood ratio (LR) o razón de verosimilitudes utilizado para casos forenses humanos (Carracedo y Barros, 1996). Se determina el cociente entre las probabilidades de que el resultado obtenido coincidente provenga de una o dos fuentes de ADN diferentes, es decir, de la misma o de distintas variedades (Ibáñez, 2000). En forma matemática: P(R/V) LR = P(R/NV) siendo P(R/V) la probabilidad de obtener el resultado coincidente si la muestra pertenece a la variedad y P(R/NV) la probabilidad de obtener el resultado coincidente cuando la muestra no pertenece a la variedad. Aquí, en principio, al no haber variabilidad intravarietal, P(R/V) sería igual a 1, y el problema reside en calcular P(R/NV), que en definitiva, es la probabilidad de obtener el resultado coincidente por azar en las poblaciones tomadas como referencia. La probabilidad de encontrar un genotipo concreto en una determinada población, depende de las frecuencias alélicas presentes en la citada población. El cálculo de las frecuencias genotípicas a partir de las alélicas requiere que los alelos de cada locus se combinen al azar para constituir los genotipos en la población (conjunto de variedades) utilizada, es decir que esté en Equilibrio de Hardy Weinberg (EHW). Asumiendo una combinación al azar de esas frecuencias alélicas, 85
108 Materiales y Métodos se calculó para cada muestra problema, la probabilidad de obtener al azar su genotipo en cada una de las poblaciones tomadas como referencia, es decir, p 2 para los homocigotos y 2pq para los heterocigotos, siendo p y q las frecuencias alélicas. Para calcular la probabilidad total de genotipo, P(R/NV), se utilizó la regla del producto, que asume independencia estadística entre los distintos loci. Los 9 loci microsatélite evaluados en este estudio, no están ligados genéticamente. En este trabajo, además de considerar como referencia a la Colección de genotipos únicos, también se utilizaron como referencia las poblaciones obtenidas al analizar esta colección con el software Structure 2.0 (Pritchard y Wen, 2003), detallado en el punto siguiente. Con ello se evaluó el efecto que tiene en el análisis matemático de la coincidencia, utilizar como referencia una población global o subpoblaciones de la misma. El uso de subpoblaciones es muy utilizado en genética forense de humanos cuando la población está estructurada. El hecho de que se utilice una colección de referencia más o menos adecuada a la muestra que se esté analizando, puede afectar considerablemente al resultado final. En general, cuanto más adecuada sea a la muestra a analizar, el resultado será más preciso. Se seleccionaron al azar varias variedades de la Colección de genotipos únicos, y se analizaron como si fueran muestras problema, en distintas poblaciones de referencia Análisis de estructura Con la Colección de genotipos únicos, obtenida durante el estudio de Distinción y formada por variedades de genotipos distintos para los 9 loci microsatélite, se realizaron test de estructuración genética utilizando los software Structure 2.0 (Pritchard y Wen, 2003) y Arlequín 3.11 (Excoffier et al., 2005). Esta colección incluía una amplia representación tanto de uva de mesa como de vinificación, además de portainjertos, híbridos productores directos, especies del género Vitis no vinifera y géneros de la familia Vitáceas. El software Structure, mediante un algoritmo Bayesiano, trata de agrupar probabilísticamente a un conjunto de individuos en distintas poblaciones. Para ello, utiliza datos genotípicos de marcadores moleculares no ligados o débilmente ligados, como pueden ser microsatélites, RFLP y SNP. Se asume además, que los marcadores estén en equilibrio de ligamiento dentro de estas poblaciones. 86
109 Materiales y Métodos Se asumió un modelo en el cuál las variedades que formaban la Colección de genotipos únicos analizadas con los 9 loci microsatélite, podían estar agrupadas en un número comprendido entre 1 y 15 poblaciones (K), cada una de las cuales se caracterizaría por presentar un determinado conjunto de frecuencias alélicas para los alelos de cada locus. Se usó una longitud de la carrera de la Cadena de Markov Monte Carlo (MCMC) de pasos, con pasos previos de desmemorización. Estos pasos previos se efectúan antes de empezar a comparar las probabilidades de las tablas alternativas con la de la observada, y son necesarios porque la cadena de Markov comienza precisamente en la tabla observada. Unos pocos miles de pasos son suficientes para alcanzar un punto de comienzo aleatorio que corresponda a una tabla independiente de la observada. Para cada K, se realizó un número máximo de 10 iteraciones aleatorias. Una vez finalizado el análisis, se observó en cuantas poblaciones, entre 1 y 15, estaban agrupadas las variedades de la Colección de genotipos únicos, en función de su genotipo. Se utilizó el modelo de mezcla, el cual permite la presencia en una determinada población, de individuos con cierto grado de mezcla genética procedente de grupos vecinos. Junto con el modelo de mezcla, se empleó el modelo de las frecuencias correlacionadas citado en Falush et al. (2003); que asume el total de poblaciones representadas en la colección de partida, como procedentes de una hipotética población ancestral, a partir de la cual han derivado las demás poblaciones, de modo que las frecuencias alélicas de las diferentes poblaciones presenten cierto parecido entre sí. Este modelo, cuando se emplea un número adecuado de marcadores, permite agrupar con exactitud a individuos procedentes de poblaciones estrechamente relacionadas. El criterio llevado a cabo en Pritchard et al. (2000) para detectar el verdadero número de poblaciones que hay en un conjunto de individuos, se basa en determinar el mayor valor logarítmico de la probabilidad de los datos obtenidos, lo cual puede no proporcionar una estimación correcta del número de poblaciones (K). Por ello, se empleó también la metodología descrita en Evanno et al. (2005) para determinar cuantas poblaciones se encontraban en la Colección de genotipos únicos. En este artículo se detallan diferentes cálculos estadísticos a los recomendados en Pritchard y Wen (2003), con los que se puede determinar de una forma gráfica y visiblemente más clara, cuántas poblaciones existen en una determinada colección. Concretamente, se determina cual es la tasa de cambio ( K) presente en los valores de la probabilidad en función de las poblaciones (K). 87
110 Materiales y Métodos Se visualiza, representando gráficamente la variable estadística ( K) frente a (K). Evanno et al. (2005) confirma que el software Structure alcanza resultados fiables en cuanto al número de poblaciones que se pueden encontrar en un determinado conjunto de variedades analizadas con marcadores moleculares AFLP y microsatélites. Una vez alcanzada la K más probable para la Colección de genotipos únicos con la metodología descrita en Evanno et al. (2005), se eligió aquella simulación de entre las 10 que se habían supuesto, que presentó la distribución más probable de genotipos para esa K. La exactitud de la asignación de individuos a una determinada población dependerá de los siguientes factores (Pritchard et al., 2000): Número de individuos que componen la población (afecta a la exactitud de las estimas de las frecuencias alélicas de las poblaciones). Número de loci empleados (afecta a la exactitud con que se estima el grado de mezcla que presenta cada individuo). La cantidad de mezcla que presenta cada individuo. La diferencia existente entre las frecuencias alélicas presentes en las diferentes poblaciones. Con el software Arlequin 3.11 (Excoffier et al., 2005), se estudió si en cada una de las poblaciones detectadas con el software Structure en la Colección de genotipos únicos, los distintos loci se encontraban en EHW. Se sigue esencialmente el procedimiento descrito por Guo y Thompson (1992) usando cadenas de Markov, éstas tenían una longitud de de pasos, con pasos previos de desmemorización. También se llevó a cabo un Análisis Molecular de la Varianza (AMOVA). A partir de los componentes de la varianza obtenidos se calcula el índice de fijación (F ST ). El programa calcula la varianza entre poblaciones permutando genotipos individuales entre las poblaciones. Además se llevaron a cabo test exactos de diferenciación entre las poblaciones detectadas con el software Structure, empleando cadenas de Markov con una longitud de de pasos y pasos previos de desmemorización. Se estimó la probabilidad de encontrar resultados con menor o 88
111 Materiales y Métodos igual probabilidad que el observado, bajo la hipótesis de que los individuos están distribuidos al azar en el conjunto de poblaciones estudiadas Establecimiento de la derivación esencial En general, las principales vías de obtención de EDV son a través de mutaciones somáticas (inducidas o naturales) y, en el futuro a través de transformaciones genéticas. Su obtención a través de un uso recurrente de la variedad inicial, no representa en esta especie una práctica común, ya que ello supondría un gran coste de tiempo por ser la vid una planta leñosa de ciclo anual. Por ello, generalmente en vid, una variedad esencialmente derivada (EDV), mostrará los mismos genotipos con microsatélites que la variedad inicial de la que procede. Es decir, la derivación esencial en vid se podría establecer en base a: 1. Distinción morfológica 2. Identidad con microsatélites Para el segundo punto se utilizó la información obtenida durante el estudio de Distinción, donde se analizaron minuciosamente las parejas de accesiones presentes en una colección formada por accesiones, que coincidían en 18, 17 o 16 alelos, de los 18 analizados. La bibliografía ayudó a determinar si variedades pertenecientes a un mismo sortogrupo eran EDV o no Elaboración de descriptores microsatélite Siguiendo esencialmente la metodología desarrollada en This et al. (2004), se elaboraron descriptores para 5 microsatélites (ssrvrzag29, ssrvrzag67, ssrvrzag83, ssrvrzag112 y VVMD28) de los 9 que ocupan esta tesis, ya que los otros 4 (ssrvrzag62, VVMD5, VVMD27 y VVS2), se encontraban incluidos en el estudio mencionado. El material utilizado fue mayoritariamente, el representado en la Tabla M24, página 72. Las reacciones de amplificación de este material se llevaron a cabo en un termociclador PTC-100 de MJ Research, analizándose posteriormente en el secuenciador ABI PRISM 310. Tras este análisis, en el que se determinaron todos 89
112 Materiales y Métodos los alelos obtenidos para los cultivares de la tabla anterior, se llevó a cabo un método de codificación de alelos, siguiendo básicamente el procedimiento descrito en This et al. (2004); codificando cada uno de los alelos en función de los códigos asignados a los cultivares que se tomaron como referencia. Cuando fue posible, para facilitar su uso, se emplearon los cultivares ya utilizados como referencia en los descriptores anteriores, mostrados en la Tabla M24, dando preferencia a aquellos cultivares más conocidos o más extendidos geográficamente. 90
113 4. RESULTADOS Y DISCUSIÓN
114
115 Resultados y Discusión 4. RESULTADOS Y DISCUSIÓN 4.1. SISTEMA DE 9 MICROSATÉLITES EMPLEADO Extracción y cuantificación de ADN El ADN se extrajo con los kits: DNeasy Plant mini Kit y DNeasy 96 Plant Kit de la empresa Qiagen. Con el primer kit se obtuvo un ADN de mayor calidad, pero el segundo permitió economizar una gran cantidad de tiempo obteniéndose además un ADN con la calidad suficiente como para llevar a cabo las posteriores amplificaciones. El rendimiento de la extracción se vio influenciado por fenómenos como la densidad de pelos que presentaron las hojas en su envés (muy alto en la variedad Cabernet sauvignon, por ejemplo), o que las hojas se encontraran en mejor o peor estado debido a las alteraciones que hubieran podido sufrir durante su transporte y almacenamiento. Concretamente, las 112 muestras de Briones (Tabla M1, página 42 de Materiales y Métodos), llegaron al laboratorio en malas condiciones; como consecuencia de ello, el rendimiento de la extracción fue menor, y el ADN obtenido resultó de inferior calidad, afectando negativamente a la posterior reacción de PCR. Estos métodos permitieron en general obtener una cantidad adecuada de ADN partiendo de poco material vegetal, unos 50 miligramos de hoja aproximadamente. En general, el rendimiento resultó ser más o menos constante en cada una de las muestras analizadas, entre 1,5 µg y 3 µg. Dado que se eluyó en un volumen final de 150 µl, las concentraciones obtenidas oscilaron entre 10 y 20 ng/µl. Se estimó la calidad y la cantidad de los ADN cargándolos en un gel de agarosa al 0,8%. Un ejemplo se muestra en la Figura R1. Figura R1. Ejemplo de cuantificación de ADN genómico. Fotografía obtenida tras una electroforesis en gel de agarosa (0,8%). Los tres últimos carriles corresponden a cantidades conocidas del estándar (fago λ: 10, 20 y 40 ng respectivamente). 91
116 Resultados y Discusión Selección de los microsatélites La selección de los microsatélites se llevó a cabo atendiendo a diferentes criterios: Número: se analizaron 9 microsatélites. En general, 6 serían suficientes para distinguir dos variedades cualesquiera de vid (This et al., 2004), pero en este caso se decidió seleccionar tres microsatélites más, por dos motivos: alguno de los microsatélites estudiados podría ser descartado como consecuencia de este estudio; además, dada la naturaleza legal y las implicaciones económicas que podrían generarse, también parecía interesante aumentar el número de loci microsatélite para incrementar así el grado de certeza de los análisis. Disponibilidad: en el momento de la selección existían más de un centenar de microsatélites cuyas secuencias habían sido publicadas (Bowers et al., 1996), (Bowers et al., 1999b), (Sefc et al., 1999), (Thomas y Scott, 1993) entre otras, y que podían usarse libremente, por lo que los nueve microsatélites a estudiar se eligieron entre ellos. Independencia: era fundamental elegir microsatélites no ligados genéticamente, por dos razones: por un lado para que la cobertura del genoma fuera mayor, al estar físicamente separados los distintos loci; por otra, para que se pudieran efectuar los análisis estadísticos que requieren independencia. En el momento de esta selección, había un mapa publicado de vid con datos de microsatélites, que se utilizó con este fin (Dalbó et al., 2000). Asimismo, había otros mapas en vías de publicación que también se emplearon para la selección de los microsatélites: Meredith, comunicación personal con referencia a Riaz et al. (2004), etc. Polimorfismo: era interesante elegir microsatélites polimórficos, pues son más discriminantes, y la certeza de la identidad sería mayor. Por ello se escogieron microsatélites con un alto grado de Heterocigosidad observada entre las variedades estudiadas por los autores que los habían descrito. En general, los microsatélites son bastante polimórficos en vid, por lo que, dentro de un orden, éste no fue un criterio limitante. Rango de amplificación: se buscaron rangos de amplificación compatibles con el desarrollo de una PCR múltiple. 92
117 Resultados y Discusión También se tuvo en consideración que los microsatélites no tuvieran alelos nulos conocidos ni alelos que se diferenciaran únicamente en 1pb. En base a estos criterios, se seleccionaron los siguientes 9 microsatélites: ssrvrzag29 (abreviado ZAG29), ssrvrzag62 (ZAG62), ssrvrzag67 (ZAG67), ssrvrzag83 (ZAG83) y ssrvrzag112 (ZAG112) (Sefc et al., 1999); VVMD5 (Bowers et al., 1996); VVMD27 y VVMD28 (Bowers et al., 1999b); VVS2 (Thomas y Scott, 1993), cuyas características se detallan en la Tabla R1. Los grupos de ligamiento presentes en la tabla están tomados de Riaz et al. (2004). Son loci que están en distintos grupos de ligamiento, las secuencias necesarias para su amplificación son públicas, son bastante o muy polimórficos (salvo uno, el ZAG29). Consisten en repeticiones de 2 nucleótidos, aunque en algunos casos estas repeticiones son imperfectas. Sus rangos de amplificación permitieron elegir los marcajes adecuados para su posterior análisis en un secuenciador genético, de manera que los 3 microsatélites marcados con el mismo fluorocromo amplificaran en distintos rangos y se pudieran diferenciar claramente. Los tres fluorocromos empleados fueron, como ya se ha comentado en Materiales y Métodos: 6-FAM, TET y HEX, que fluorescen en azul, verde y amarillo, respectivamente con el filtro C, y los microsatélites marcados con cada uno de ellos se distribuyeron de la siguiente forma: ZAG67, VVMD27 y VVMD5 estaban marcados con 6-FAM. ZAG29, ZAG62 y ZAG112 estaban marcados con TET. VVS2, ZAG83 y VVMD28 estaban marcados con HEX. 93
118 Resultados y Discusión Tabla R1. Características de los 9 loci microsatélite seleccionados. Se encuentran ordenados por marcaje y tamaño creciente. LOCUS GRUPO LIGAMIENTO ZAG RANGO (pb) SECUENCIA Tm FLUOROCROMO TIPO DE REPETICIÓN Cebador up Cebador lw 5 -ACCTGGCCCGACTCCTCTTGTATGC-3 5 -TCCTGCCGGCGATAACCAAGCTATG-3 62,4 ºC 60,8 ºC 6-FAM (Azul) Imperfecta (GA)5C(AG)2T(GA)3GG(GA)2T(AG)7 VVMD Cebador up Cebador lw 5 -GTACCAGATCTGAATACATCCGTAAGT-3 5 -ACGGGTATAGAGCAAACGGTGT-3 56,6 ºC 54,7 ºC 6-FAM (Azul) Imperfecta (GA)15(AA)(GA)5 VVMD Cebador up Cebador lw 5 -CTAGAGCTACGCCAATCCAA-3 5 -TATACCAAAAATCATATTCCTAAA-3 51,6 ºC 45,3 ºC 6-FAM (Azul) Imperfecta (CT)3AT(CT)11ATAG(AT)3 ZAG Cebador up Cebador lw 5 -ATAACCAGGACAAGTTATTCAAGCC-3 5 -ACCCAATTGACCATCTTTTATGCTG-3 54,2 ºC 54,2 ºC TET (Verde) Perfecta (GA)16 ZAG ZAG VVS ZAG VVMD Cebador up Cebador lw Cebador up Cebador lw Cebador up Cebador lw Cebador up Cebador lw Cebador up Cebador lw 5 -GGTGAAATGGGCACCGAACACACGC-3 5 -CCATGTCTCTCCTCAGCTTCTCAGC-3 5 -CGTTTAAAGCCAGCTGAATCTTGGG-3 5 -TGGCTCCATACTGCTTCACGTAGGC-3 5 -CAGCCCGTAAATGTATCCATC-3 5 -AAATTCAAAATTCTAATTCAACTGG-3 5 -GGCGGAGGCGGTAGATGAGAGGGCG-3 5 -ACGCAACGGCTAGTAAATACAACGG-3 5 -AACAATTCAATGAAAAGAGAGAGAGAGA-3 5 -TCATCAATTTCGTATCTCTATTTGCTG-3 62,4 ºC 60,8 ºC 57,5 ºC 60,8 ºC 52,2 ºC 47,7 ºC 67,4 ºC 57,5 ºC 53,9 ºC 53,5 ºC TET (Verde) TET (Verde) HEX (Amarillo) HEX (Amarillo) HEX (Amarillo) Perfecta (GA)19 Imperfecta (GA)18(TA)10 Perfecta (GA)22 Perfecta (GA)8 Perfecta (CT)14 94
119 Resultados y Discusión Diseño de la PCR múltiple para los 9 loci microsatélite Para optimizar la PCR múltiple se llevaron a cabo inicialmente amplificaciones individuales, y electroforesis en geles de agarosa al 2%, teñidos con bromuro de etidio para comprobar que todos los microsatélites empleados amplificaban correctamente con el mismo programa de PCR. Una vez ajustado el programa (Tabla R2), se tuvo en consideración la magnitud de la amplificación (en base a la intensidad de la fluorescencia del bromuro de etidio en el gel de agarosa) para calcular las concentraciones relativas de los distintos cebadores en la mezcla múltiple. Es decir, la concentración usada inicialmente para cada par de cebadores era inversamente proporcional a esa intensidad. Tabla R2. Programa de PCR para la amplificación conjunta de los 9 loci microsatélite. Nº CICLOS TEMPERATURA TIEMPO 1 95ºC 5 min 95ºC 45 seg 30 55ºC 1 min 72ºC 30 seg 1 72ºC 1 hora 1 4ºC ilimitado Esta mezcla múltiple que incluía los cebadores necesarios para amplificar los 9 loci microsatélite, se sometió a PCR y electroforesis en el Analizador Genético ABI PRISM 310. En función de la altura de los picos obtenidos para cada uno de ellos, se fueron ajustando las distintas concentraciones de los cebadores de cada microsatélite hasta encontrar una mezcla que amplificara más o menos por igual todos ellos (Tabla R3). Los ajustes mencionados se realizaron con un conjunto reducido de variedades y ADN, por lo que no siempre los resultados obtenidos fueron óptimos al analizar otras variedades/adn. Tras la PCR múltiple realizada con la mezcla de reacción final, se tomaron alícuotas de 7µl y se sometieron a electroforesis en geles de agarosa al 2%. Un ejemplo se recoge en la Figura R2. 95
120 Resultados y Discusión Tabla R3. Mezcla de reacción final (20,5 µl). (Up: cebador marcado con fluorocromo, Lw: cebador sin marcar). REACTIVO CONCENTRACIÓN FINAL Tampón Biotools 1 X Cl 2 Mg 2,0 mm dntps 0,25 mm VVS2 Up 0,30 µm VVS2 Lw 0,30 µm VVMD5 Up 0,50 µm VVMD5 Lw 0,50 µm VVMD27 Up 0,12 µm VVMD27 Lw 0,12 µm VVMD28 Up 0,20 µm VVMD28 Lw 0,20 µm ZAG29 Up 0,07 µm ZAG29 Lw 0,07 µm ZAG62 Up 0,06 µm ZAG62 Lw 0,06 µm ZAG67 Up 0,06 µm ZAG67 Lw 0,06 µm ZAG83 Up 0,10 µm ZAG83 Lw 0,10 µm ZAG112 Up 0,07 µm ZAG112 Lw 0,07 µm Polimerasa Biotools 0,075 U/µL ADN 1 µl Figura R2. Ejemplo de la reacción multiplex con 9 microsatélites tras una electroforesis en gel de agarosa (2%). El carril de la derecha corresponde al marcador de peso molecular (ADN del fago φx174 digerido con Hae III). La calidad del ADN se reflejó en el rendimiento de las reacciones de PCR. Aquellos ADN que no presentaron una calidad suficiente en la extracción, hubo que diluirlos a una concentración 1/10 para obtener amplificaciones adecuadas, como fue el caso de las muestras de Briones. Se puede suponer que ello se debe a que 96
121 Resultados y Discusión las impurezas presentes en la extracción eran un factor más limitante en este caso que la concentración de ADN, por lo que la dilución de las mismas posibilitaba la amplificación mediante PCR. De las casi PCR múltiples de 9 microsatélites realizadas en este estudio, en las que se amplificaron las muestras del estudio de Homogeneidad y Estabilidad así como las muestras de Briones, únicamente el 14% de estas PCR funcionaron bien, es decir, amplificaron los 9 loci microsatélite a la vez. En el resto hubo que recurrir a la amplificación individual o múltiple de los microsatélites no amplificados. A pesar de esto, hay que destacar que incluso en esas múltiples que no funcionaron bien del todo, se amplificaron conjuntamente entre 6 y 7 loci. Los microsatélites que presentaron más problema a la hora de la amplificación conjunta de los 9 loci, fueron el locus ZAG67 y el VVMD27, como se puede observar en la Tabla R4. En esta tabla se muestran los porcentajes de repetición para cada locus tras la amplificación conjunta de los 9 loci STMS en las casi muestras citadas anteriormente. Tabla R4. Porcentajes de repetición para cada locus tras la amplificación conjunta de los 9 loci STMS en casi ADN. LOCUS %REPETICIÓN ZAG67 52% VVMD27 65,7% VVMD5 19,4% ZAG29 9,7% ZAG62 6,8% ZAG112 2,6% VVS2 12,6% ZAG83 2,0% VVMD28 13,8% No se ha podido determinar la causa de la falta de robustez de la técnica. Posiblemente la irregular amplificación puede ser debida a la inestabilidad de algunos cebadores con el paso del tiempo, a cambios en la producción de la enzima, a modificaciones en la pureza de los cebadores, etc. 97
122 Resultados y Discusión En general, en vid no se han llevado a cabo muchos estudios en los que se amplifique conjuntamente en la misma reacción de PCR, un determinado set de loci microsatélite. Un estudio relacionado con la técnica de la PCR múltiple sería el llevado a cabo por Frei et al. (2004), donde utilizaron marcadores moleculares microsatélite para construir una base de datos que incluía 147 cultivares de Vitis vinifera y cultivares interespecíficos, variedades históricas y 4 especies pertenecientes a la familia Vitaceae. En un principio, para el análisis de estos marcadores emplearon el método tradicional de tinción de geles con nitrato de plata, para posteriormente emplear la técnica de la PCR múltiple y el consiguiente análisis en un analizador genético con 16 capilares. Los autores catalogaron esta técnica con respecto a la utilizada inicialmente, como más rápida, más reproducible, más fiable, y más barata. Otro estudio en vid concerniente a esta técnica sería el llevado a cabo por Merdinoglu et al. (2005), donde desarrollaron 169 loci fáciles de combinar entre ellos para llevar a cabo PCR múltiples. El hecho de marcar con distintos fluorocromos los loci que componen cada set, permite su fácil identificación al analizarlos en un analizador genético. Los autores afirman que empleando la técnica de la PCR múltiple frente a la individual, se reducen los costes de los reactivos empleados en la reacción de PCR en casi un 50%, y los de los reactivos empleados en la electroforesis llevada a cabo en un analizador genético, en más de un 85%. Aún con las dificultades encontradas en este estudio al emplear una PCR múltiple, esta técnica presenta un mayor número de ventajas que la de amplificar marcadores moleculares microsatélites de forma individual, como se ha detallado también en la bibliografía consultada. Entre ellas, cabe destacar: mayor información obtenida por análisis, reducción de tiempo en la realización de los análisis y disminución de gastos en material fungible Análisis en un analizador genético Cada una de las muestras amplificadas se sometió a electroforesis en el secuenciador ABI PRISM 310 para poder determinar su genotipo. 98
123 Resultados y Discusión Los picos obtenidos para los microsatélites presentaron diferentes alturas como se ha citado en el apartado anterior, ello era debido a que no todos los microsatélites eran amplificados con la misma eficacia ni todos los fluorocromos emitían luz con la misma intensidad. La altura de cada pico era proporcional a la cantidad de fluorescencia detectada, que, en cierto modo, reflejaba la cantidad del fragmento de ADN presente en la electroforesis. En ocasiones, la altura de los dos alelos de un mismo microsatélite podía ser diferente, incluso marcadamente distinta. Este fenómeno puede ser debido entre otras causas, a la naturaleza del propio alelo. Una vez obtenido el perfil electroforético había que identificar los picos que correspondían a los alelos. Para cada microsatélite analizado, normalmente aparecían 1 ó 2 picos principales que se interpretaban como genotipos homocigóticos o heterocigóticos, respectivamente. Para la interpretación se tuvo en cuenta la posible presencia de picos adicionales a los picos alélicos que podían complicar la identificación de éstos. Entre ellos estaban los llamados picos tartamudos ( stutter en inglés), picos de menor tamaño molecular y altura que los alelos en sí, y que normalmente tenían 2, 4, y hasta 6 nucleótidos menos que ellos, y además, su altura disminuía a medida que se alejaba del alelo verdadero. También hay que nombrar los denominados picos +A, que eran picos un nucleótido mayores que el alelo real, y que aparecían como un pico independiente o como un hombro del pico alélico bajo análisis. Podía presentarse con mayor o menor intensidad que el alelo verdadero. Estos fragmentos se deben a la adición por parte de la Taq polimerasa de un nucleótido con la base adenina al final del fragmento. Teniendo estos aspectos en consideración, así como los datos publicados y los producidos en el laboratorio de Biología Molecular de la Finca el Encín, se identificaron para cada microsatélite los picos correspondientes a los alelos. La Figura R3 muestra un ejemplo de una representación GeneScan típica para los 9 microsatélites. 99
124 Resultados y Discusión Figura R3. Representación en GeneScan de los nueve loci microsatélite para una de las muestras de la variedad Napoleón. La parte superior incluye los perfiles electroforéticos para los microsatélites ZAG67, VVMD27 y VVMD5 (azul), ZAG29, ZAG62 y ZAG112 (verde), VVS2, ZAG83 y VVMD28 (amarillo, representados en negro). La parte de abajo recoge la tabla de datos, siendo la tercera columna la de mayor interés: corresponde al tamaño aproximado en nucleótidos de los picos. 100
125 Resultados y Discusión 4.2. ESTUDIO DE DISTINCIÓN Estudio de una colección para el cálculo de la distancia mínima Para el estudio de Distinción, se partió de un total de accesiones, que pertenecían a 4 fuentes diferentes de material: Accesiones de tres parcelas de la Colección de variedades de vid de El Encín: 819 accesiones pertenecían a la parcela 22, 311 a la parcela 25 y 6 a la parcela de portainjertos. 112 muestras de Briones detalladas en la Tabla M1 de Materiales y Métodos, página accesiones de las utilizadas para el establecimiento de descriptores microsatélite, presentes en la Tabla M24 de Materiales y Métodos, página 72 (estas fueron cogidas del propio material con el que se llevó a cabo el estudio de This et al. (2004), ya que no estaban presentes en la Colección de variedades de vid de El Encín). 19 muestras pertenecientes a las 19 variedades de las empleadas para el estudio de Homogeneidad y Estabilidad. De todas las accesiones disponibles, se seleccionaron accesiones (Anexo I, página 211), que fueron las que presentaron datos completos para los 9 microsatélites que ocupan este estudio (597 accesiones pertenecían a la parcela 22, 307 a la parcela 25, 6 a la parcela de portainjertos, 80 a Briones, 14 a las del estudio para el establecimiento de descriptores y 19 a las del estudio de Homogeneidad y Estabilidad). Estas accesiones se utilizaron como una colección global de partida para el estudio de Distinción. Por ello era muy importante que esta colección incluyera muestras lo más variadas posible, y a la vez, variedades muy cercanas entre sí (padres, hijos, hermanos, etc.). Así, este material incluía una amplia representación tanto de uva de mesa como de vinificación, además de portainjertos, híbridos productores directos, especies del género Vitis no vinifera y géneros de la familia Vitáceas. Entre todas ellas se podían encontrar accesiones sinónimas, sports y accesiones homónimas. Algunas de ellas se encontraban perfectamente definidas como tal en la bibliografía consultada y otras no, como se detalla más adelante. 101
126 Resultados y Discusión El proceso del estudio de Distinción consiste, como ya se ha citado anteriormente, en buscar las diferencias de la variedad analizada respecto a las demás, usando una colección de referencia apropiada, y en determinar si esas diferencias son superiores a una distancia mínima (distancia más pequeña que puede existir entre dos variedades para considerarlas diferentes). Por ello, el punto clave para establecer la distinción es determinar la distancia mínima que debería existir entre dos variedades de vid para que fueran consideradas distintas. Usando marcadores moleculares microsatélites, y según el criterio seguido en este estudio, habría que determinar el menor número de alelos diferentes entre plantas pertenecientes a distintos sortogrupos y el mayor número de alelos diferentes entre plantas pertenecientes al mismo sortogrupo (clones, variedades sinónimas, EDV o sports). El procedimiento que se siguió fue el siguiente: una vez confeccionada la base de datos con 9 STMS de la colección formada por accesiones, se procedió al análisis de la misma. Se llevaron a cabo comparaciones 2 a 2 entre todas las accesiones que la formaban, empleando para ello la aplicación de Excel Microsatellite Toolkit (Park, 2001). El número total de parejas que se obtuvo fue El análisis se centró, como ya se ha comentado en Materiales y Métodos, en el estudio de las accesiones que coincidían en 18, 17 ó 16 alelos, de los 18 analizados (correspondientes a los 9 microsatélites). En cada uno de estos tres grupos, se comprobó si las accesiones que los formaban se habían considerado morfológicamente del mismo sortogrupo de acuerdo a los datos de Cabello y col. y a los de la bibliografía consultada. Cuando fue así, se procedió a seleccionar únicamente una accesión representativa para ese genotipo común que correspondía en principio a un determinado sortogrupo y se eliminaron todas las demás de la colección formada por accesiones. Cuando no se encontraron datos que justificaran esa igualdad, se analizaron las accesiones implicadas con 20 loci microsatélite, considerando estos resultados definitivos. Si las accesiones no pertenecían al mismo sortogrupo, estas se seguían manteniendo en la colección. Accesiones que coincidían en los 18 alelos Se encontró un total de parejas de accesiones con idéntico genotipo. Después de la primera comprobación morfológica y bibliográfica, fueron eliminadas 501 accesiones por considerar que pertenecían al mismo sortogrupo, quedando la 102
127 Resultados y Discusión colección representada por 522 accesiones. Entre éstas aún quedaban algunas que coincidían en los 18 alelos pero sus nombres no figuraban como pertenecientes al mismo sortogrupo en la bibliografía consultada (Tabla R5). Algunas variedades aparecen en la tabla con otro nombre entre paréntesis; este corresponde a su variedad sinónima, según estudios no publicados llevados a cabo en la Colección de variedades de vid de El Encín. (Inmaculada Rodríguez Torres-IMIDRA, comunicación personal). Tabla R5. En cada fila de la tabla se muestra el nombre de las accesiones que presentaron entre ellas el mismo genotipo para los 9 loci microsatélite, y no estaban reflejadas como pertenecientes al mismo sortogrupo en la bibliografía consultada. ACCESIÓN 1 ACCESIÓN 2 ACCESIÓN 3 ACCESIÓN 4 Agudelo Chenin - - Albarraz Blanco gordal (Corazón de Cabrito) (Corazón de Cabrito) - - Albillo blanco (Matza zuri) Slavjanka - - Aledo Cherta - - Apirena di Velletri Kischmisch Ali blanc - - Baga Diminitis - - Beba Blanca Superior para Valencí blanco Tchaoutc Parral (Beba) (Beba) Blanco de Mesa Jerónimo de Tudela Uva de Olaz - Bocalilla Negra rayada Rollales tinta - Caiño portugues Jaquez Yaqui - Corinto bianco Don Bueno Pedro Ximenez - De Rey Forastera blanca (Mantúo (Mantúo de Pilas) de Pilas) - - Escañavella Lanjarón claro - - Ferdinand de Lesseps Pansá blanca (Xarel.lo) - - Forcallat Luisa blanca - - Garganega Ugni blanc - - Japinkay Palomino Tempranillo de Granada - Moscatel (Moscatel de Romé (Moscatel de grano grano gordo) gordo) - - Pensal blanco (Rosetti) Professor Aberson
128 Resultados y Discusión Estas accesiones representadas en la Tabla R5, se analizaron con 20 loci microsatélite para comprobar si la identidad genotípica persistía. Los resultados obtenidos con estos 20 microsatélites (Tabla R6), determinaron que, efectivamente, las accesiones recogidas en cada fila de la Tabla R5 presentaron el mismo genotipo al analizarse con los 20 loci, confirmándose así los resultados de los 9 loci iniciales. Ya que es extremadamente improbable que variedades procedentes de distintos embriones originales pudieran salir iguales con 25 loci microsatélite, se concluye que estas accesiones pertenecen al mismo sortogrupo, aunque no estén recogidas como tal en la bibliografía consultada. No obstante, no se puede descartar que exista algún error en la colección. Al considerar las accesiones representadas en cada fila de la Tabla R5 como pertenecientes al mismo sortogrupo, el siguiente paso fue seleccionar una única accesión de cada fila, representativa para cada genotipo, y eliminar todas las demás de la lista de 522 accesiones. En este paso se eliminaron 26 accesiones, quedando la colección representada por 496 accesiones. 104
129 Resultados y Discusión Tabla R6. Genotipos obtenidos con 20 loci microsatélite, para las accesiones representadas en la Tabla R5 que coincidían en los 18 alelos. VARIEDADES VMC1B11 VVIB01 VVIH54 VVIP31 VVIP60 VVIQ52 VVMD7 VVS2 VVMD24 VVMD25 Agudelo Chenin 173: : : : :319 82:88 236: : : :247 VARIEDADES VVIN73 VMC4F3 VVIN16 VVIV67 VVMD21 VVMD32 VVMD27 VVMD28 VVMD5 VVIV37 Agudelo Chenin 263: : : : : : : : : :165 VARIEDADES VMC1B11 VVIB01 VVIH54 VVIP31 VVIP60 VVIQ52 VVMD7 VVS2 VVMD24 VVMD25 Albarraz Blanco gordal 185: : : : :321 84:86 236: : : :239 VARIEDADES VVIN73 VMC4F3 VVIN16 VVIV67 VVMD21 VVMD32 VVMD27 VVMD28 VVMD5 VVIV37 Albarraz Blanco gordal 263: : : : : : : : : :177 VARIEDADES VMC1B11 VVIB01 VVIH54 VVIP31 VVIP60 VVIQ52 VVMD7 VVS2 VVMD24 VVMD25 Albillo blanco Slavjanka 171: : : : :323 82:88 236: : : :247 VARIEDADES VVIN73 VMC4F3 VVIN16 VVIV67 VVMD21 VVMD32 VVMD27 VVMD28 VVMD5 VVIV37 Albillo blanco Slavjanka 263: : : : : : : : : :163 VARIEDADES VMC1B11 VVIB01 VVIH54 VVIP31 VVIP60 VVIQ52 VVMD7 VVS2 VVMD24 VVMD25 Aledo Cherta 167: : : : :321 84:88 236: : : :253 VARIEDADES VVIN73 VMC4F3 VVIN16 VVIV67 VVMD21 VVMD32 VVMD27 VVMD28 VVMD5 VVIV37 Aledo Cherta 263: : : : : : : : : :163 VARIEDADES VMC1B11 VVIB01 VVIH54 VVIP31 VVIP60 VVIQ52 VVMD7 VVS2 VVMD24 VVMD25 Apirena di Velletri Kischmisch Ali blanc 167: : : : :321 84:84 236: : : :247 VARIEDADES VVIN73 VMC4F3 VVIN16 VVIV67 VVMD21 VVMD32 VVMD27 VVMD28 VVMD5 VVIV37 Apirena di Velletri Kischmisch Ali blanc 263: : : : : : : : : :180 VARIEDADES VMC1B11 VVIB01 VVIH54 VVIP31 VVIP60 VVIQ52 VVMD7 VVS2 VVMD24 VVMD25 Baga Diminitis 171: : : : :331 84:88 236: : : :253 VARIEDADES VVIN73 VMC4F3 VVIN16 VVIV67 VVMD21 VVMD32 VVMD27 VVMD28 VVMD5 VVIV37 Baga Diminitis 256: : : : : : : : : :177 VARIEDADES VMC1B11 VVIB01 VVIH54 VVIP31 VVIP60 VVIQ52 VVMD7 VVS2 VVMD24 VVMD25 Beba Blanca Superior Parral Tchaoutc 185: : : : :321 82:84 240: : : :253 Valencí blanco VARIEDADES VVIN73 VMC4F3 VVIN16 VVIV67 VVMD21 VVMD32 VVMD27 VVMD28 VVMD5 VVIV37 Beba Blanca Superior Parral Tchaoutc Valencí blanco 256: : : : : : : : : :163 VARIEDADES VMC1B11 VVIB01 VVIH54 VVIP31 VVIP60 VVIQ52 VVMD7 VVS2 VVMD24 VVMD25 Blanco de Mesa Jerónimo de Tudela 185: : : : :327 84:88 240: : : :253 Uva de Olaz VARIEDADES VVIN73 VMC4F3 VVIN16 VVIV67 VVMD21 VVMD32 VVMD27 VVMD28 VVMD5 VVIV37 Blanco de Mesa Jerónimo de Tudela Uva de Olaz 263: : : : : : : : :161 VARIEDADES VMC1B11 VVIB01 VVIH54 VVIP31 VVIP60 VVIQ52 VVMD7 VVS2 VVMD24 VVMD25 Bocalilla Negra rayada 167: : : : :317 82:88 246: : : :253 Rollales Tinta VARIEDADES VVIN73 VMC4F3 VVIN16 VVIV67 VVMD21 VVMD32 VVMD27 VVMD28 VVMD5 VVIV37 Bocalilla Negra rayada Rollales Tinta 256: : : : : : : : : :163 VARIEDADES VMC1B11 VVIB01 VVIH54 VVIP31 VVIP60 VVIQ52 VVMD7 VVS2 VVMD24 VVMD25 Caiño portugues Jaquez 179: : : : :317 84:84 236: : : :253 Yaqui VARIEDADES VVIN73 VMC4F3 VVIN16 VVIV67 VVMD21 VVMD32 VVMD27 VVMD28 VVMD5 VVIV37 Caiño portugues Jaquez Yaqui 269: : : : :249 _ 179: : : :
130 Resultados y Discusión VARIEDADES VMC1B11 VVIB01 VVIH54 VVIP31 VVIP60 VVIQ52 VVMD7 VVS2 VVMD24 VVMD25 Corinto bianco Don Bueno 169: : : : :321 88:88 236: : : :247 Pedro Ximenez VARIEDADES VVIN73 VMC4F3 VVIN16 VVIV67 VVMD21 VVMD32 VVMD27 VVMD28 VVMD5 VVIV37 Corinto bianco Don Bueno Pedro Ximenez 263: : : : : : : : : :177 VARIEDADES VMC1B11 VVIB01 VVIH54 VVIP31 VVIP60 VVIQ52 VVMD7 VVS2 VVMD24 VVMD25 De Rey Forastera blanca 185: : : : :327 84:88 244: : : :253 VARIEDADES VVIN73 VMC4F3 VVIN16 VVIV67 VVMD21 VVMD32 VVMD27 VVMD28 VVMD5 VVIV37 De Rey Forastera blanca 263: : : : : : : : : :161 VARIEDADES VMC1B11 VVIB01 VVIH54 VVIP31 VVIP60 VVIQ52 VVMD7 VVS2 VVMD24 VVMD25 Escañavella Lanjarón claro 185: : : : :321 82:84 236: : : :253 VARIEDADES VVIN73 VMC4F3 VVIN16 VVIV67 VVMD21 VVMD32 VVMD27 VVMD28 VVMD5 VVIV37 Escañavella Lanjarón claro 263: : : : : : : : : :177 VARIEDADES VMC1B11 VVIB01 VVIH54 VVIP31 VVIP60 VVIQ52 VVMD7 VVS2 VVMD24 VVMD25 Ferdinand de Lesseps Pansá blanca 185: : : : :325 84:88 236: : : :253 VARIEDADES VVIN73 VMC4F3 VVIN16 VVIV67 VVMD21 VVMD32 VVMD27 VVMD28 VVMD5 VVIV37 Ferdinand de Lesseps Pansá blanca 263: : : : : : : : : :163 VARIEDADES VMC1B11 VVIB01 VVIH54 VVIP31 VVIP60 VVIQ52 VVMD7 VVS2 VVMD24 VVMD25 Forcallat Luisa blanca 173: : : : :327 84:88 231: : : :253 VARIEDADES VVIN73 VMC4F3 VVIN16 VVIV67 VVMD21 VVMD32 VVMD27 VVMD28 VVMD5 VVIV37 Forcallat Luisa blanca 263: : : : : : : : : :177 VARIEDADES VMC1B11 VVIB01 VVIH54 VVIP31 VVIP60 VVIQ52 VVMD7 VVS2 VVMD24 VVMD25 Garganega Ugni blanc 185: : : : :333 82:88 246: : : :253 VARIEDADES VVIN73 VMC4F3 VVIN16 VVIV67 VVMD21 VVMD32 VVMD27 VVMD28 VVMD5 VVIV37 Garganega Ugni blanc 256: : : : : : : : : :171 VARIEDADES VMC1B11 VVIB01 VVIH54 VVIP31 VVIP60 VVIQ52 VVMD7 VVS2 VVMD24 VVMD25 Japinkay Palomino 185: : : : :321 84:84 236: : : :239 Tempranillo de Granada VARIEDADES VVIN73 VMC4F3 VVIN16 VVIV67 VVMD21 VVMD32 VVMD27 VVMD28 VVMD5 VVIV37 Japinkay Palomino Tempranillo de Granada 256: : : : : : : : : :167 VARIEDADES VMC1B11 VVIB01 VVIH54 VVIP31 VVIP60 VVIQ52 VVMD7 VVS2 VVMD24 VVMD25 Moscatel Romé 167: : : : :321 82:82 246: : : :247 VARIEDADES VVIN73 VMC4F3 VVIN16 VVIV67 VVMD21 VVMD32 VVMD27 VVMD28 VVMD5 VVIV37 Moscatel Romé 263: : : : : : : : : :263 VARIEDADES VMC1B11 VVIB01 VVIH54 VVIP31 VVIP60 VVIQ52 VVMD7 VVS2 VVMD24 VVMD25 Pensal blanco Professor Aberson 185: : : : :317 82:84 236: : : :253 VARIEDADES VVIN73 VMC4F3 VVIN16 VVIV67 VVMD21 VVMD32 VVMD27 VVMD28 VVMD5 VVIV37 Pensal blanco Professor Aberson 263: : : : : : : : : :163 Accesiones que coincidían en 17 alelos de los 18 analizados Únicamente apareció 1 pareja con esa proporción, compuesta por las accesiones: Chasselas blanca y Chasselas Gros Coulard. Diferían entre sí en un alelo del locus ZAG83. Ambas accesiones no estaban descritas como pertenecientes al mismo sortogrupo en la bibliografía consultada, aunque su nombre indica una cierta relación entre ellas. Chasselas blanca presentó un 106
131 Resultados y Discusión genotipo heterocigótico para el citado locus ( ), mientras que Chasselas Gros Coulard presentó un genotipo homocigótico para el mismo (192). Para comprobar si existía entre ellas alguna otra diferencia en cuanto a su genotipo, se analizaron 20 loci microsatélite más. Los resultados, recogidos en la Tabla R7, mostraron que ambas accesiones presentaban el mismo genotipo para esos STMS. Tabla R7. Genotipos obtenidos con 20 loci microsatélite, para la pareja de muestras compuesta por Chasselas blanca y Chasselas Gros Coulard, que coincidían en 17 alelos de los 18 analizados. VARIEDADES VMC1B11 VVIB01 VVIH54 VVIP31 VVIP60 VVIQ52 VVMD7 VVS2 VVMD24 VVMD25 Chasselas blanca Chasselas Gros Coulard 173: : : : :321 84:88 236: : : :253 VARIEDADES VMC1B11 VVIB01 VVIH54 VVIP31 VVIP60 VVIQ52 VVMD7 VVS2 VVMD24 VVMD25 Chasselas blanca Chasselas Gros Coulard 263: : : : : : : : : :263 Con estos resultados se llegó a la conclusión de que Chasselas Gros Coulard es un sport de Chasselas blanca, que se habría originado por una mutación somática en un alelo del locus ZAG83, bien porque el alelo 201 hubiera mutado a 192 o bien a alelo nulo. Ambas accesiones procederían del mismo embrión original. Es decir, estamos en el caso de que las dos accesiones pertenecen al mismo sortogrupo, por lo que eliminamos la accesión Chasselas Gros Coulard de la colección formada por 496 accesiones, pasando a estar representada por 495 accesiones. Accesiones que coincidían en 16 alelos de los 18 analizados Aparecieron 2 parejas con esta proporción. Una de ellas correspondió a la compuesta por las accesiones denominadas Alfonso Lavalle y Princeps, ambas variedades estaban descritas en la bibliografía, pero no como pertenecientes al mismo sortogrupo. El segundo caso correspondió a la pareja de accesiones denominadas Pizzutelo Moscato Biondo y Galletta rosa. Estas variedades tampoco aparecían descritas como pertenecientes al mismo sortogrupo en la bibliografía consultada. En las dos parejas, los dos alelos que no coincidieron con los 18 totales correspondieron a microsatélites diferentes: en la primera pareja un alelo diferente correspondió al locus ZAG83 y el otro al VVS2, mientras que en la segunda, uno de los alelos diferentes perteneció al locus ZAG112 y el otro al VVMD5. Se 107
132 Resultados y Discusión amplificaron ambas parejas con 20 microsatélites más para observar si presentaban diferencias, obteniendo para cada una de ellas 9 alelos diferentes en un total de 7 loci (Tabla R8, remarcados en azul). En base a estos resultados, se concluyó que pertenecían a distintos sortogrupos, por lo que se mantuvieron en la colección formada por 495 accesiones. Tabla R8. Genotipos obtenidos con 20 loci microsatélite, para las dos parejas de muestras compuestas por Alfonso Lavalle-Princeps y Galletta rosa-pizzutelo Moscato Biondo, las cuales coincidían en 16 alelos de los 18 analizados. VARIEDADES VMC1B11 VVIB01 VVIH54 VVIP31 VVIP60 VVIQ52 VVMD7 VVS2 VVMD24 VVMD25 Alfonso Lavalle 167: : : : :327 82:84 246: : : :253 Princeps 173: : : : :317 84:86 246: : : :253 VARIEDADES VVIN73 VMC4F3 VVIN16 VVIV67 VVMD21 VVMD32 VVMD27 VVMD28 VVMD5 VVIV37 Alfonso Lavalle 256: : : : : : : : : :163 Princeps 256: : : : : : : : : :171 VARIEDADES VMC1B11 VVIB01 VVIH54 VVIP31 VVIP60 VVIQ52 VVMD7 VVS2 VVMD24 VVMD25 Galletta rosa 173: : : : :321 82:84 240: : : :253 Pizzutelo Moscato Biondo 173: : : : :321 88:88 240: : : :253 VARIEDADES VVIN73 VMC4F3 VVIN16 VVIV67 VVMD21 VVMD32 VVMD27 VVMD28 VVMD5 VVIV37 Galletta rosa 263: : : : : : : : : :163 Pizzutelo Moscato Biondo 263: : : : : : : : : :163 En definitiva, partiendo de una colección formada por accesiones, al analizar aquellas más próximas en cuanto a su genotipo para 9 microsatélites, se constituyó por eliminación una colección con 495 variedades, que aparecen marcadas con un asterisco en el Anexo I, página 211. Hubo 2 parejas compuestas por las accesiones Alfonso Lavalle-Princeps y Pizzutelo Moscato Biondo-Galletta rosa, que diferían entre sí en 2 alelos de los 18 analizados, y cuando se analizaron con 20 loci microsatélite, se confirmó que se trataba de variedades pertenecientes a diferentes sortogrupos. La colección final obtenida a lo largo del estudio de Distinción, estuvo formada por 495 variedades con genotipo diferente, considerándolas variedades pertenecientes a distintos sortogrupos. Esta colección se utilizó en varias ocasiones como colección de referencia y se denominó Colección de genotipos únicos Cálculo de la distancia mínima La distancia mínima debe ser estable y no estar sujeta a variaciones interlaboratorio, en la medida de lo posible. Por ello se tuvieron en cuenta y se analizaron con especial minuciosidad, tanto los resultados obtenidos durante el análisis de la colección de accesiones recién detallados, como datos bibliográficos acerca de los distintos tipos de variabilidad intrasortogrupo descritos 108
133 Resultados y Discusión en vid usando microsatélites. Se analizó por separado la variabilidad intrasortogrupo debida a mutaciones que producen alelos nulos, y la debida a mutaciones producidas por el aumento o disminución de repeticiones de la unidad básica. Variabilidad intrasortogrupo descrita en vid debida a mutaciones que producen alelos nulos: Los alelos nulos aparecen al producirse modificaciones en la secuencia diana de los cebadores, impidiendo la hibridación con el ADN molde. Cuando esto ocurre, no es posible distinguir entre individuos heterocigóticos con un alelo nulo e individuos homocigóticos, y además, diferentes alelos nulos dan lugar al mismo fenotipo (ausencia de fragmento amplificado). En la literatura se han descrito diferentes casos de mutaciones debidas a la presencia de alelos nulos: En el trabajo de Crespan et al. (1999), para el locus VVMD8, la variedad Sultanina presenta el genotipo (145:157), mientras que en el trabajo de Bowers et al. (1996), la variedad Thompson seedless (considerada en este estudio como sinónima de Sultanina) presentó para el citado locus el genotipo (145:-). La presencia de alelos nulos en el locus VVMD8 ya había sido detectada en variedades que fallaron en su amplificación, para las cuales se consideró que tenían genotipos homocigóticos nulos para ese locus. En el trabajo de Bowers et al. (1996), donde se analizaron 4 STMS, aparecieron alelos nulos en los loci VVMD6 y VVMD8, en 3 de los 31 cultivares de mesa estudiados. En los trabajos de Thomas et al. (1994) y Sanchez-Escribano et al. (1999), donde se amplificó el locus VVS3 en la variedad Marroo seedless, obtuvieron para este locus respectivamente, los siguientes genotipos: (216:-) y (216:222). En el estudio llevado a cabo analizando 47 loci microsatélite, en clones de White Riesling (Regner et al., 2000b), la mayoría de las mutaciones presentadas eran debidas a la aparición de alelos nulos en los loci VVMD6, ssrvrzag12, VRG1, VRG2 y VRG3. Excepto en el trabajo de Regner et al. (2000b), donde estaban incluidos los 9 loci microsatélites de esta tesis, todos los demás estudios citados incluían 1 ó 2 de ellos (VVS2 ó VVMD5). Lo que hay que remarcar, es que ninguno de estos loci STMS estuvo implicado en mutaciones debidas a la aparición de alelos nulos. 109
134 Resultados y Discusión Variabilidad intrasortogrupo descrita en vid debida a mutaciones producidas por el aumento o disminución de repeticiones de la unidad básica: Este tipo de variabilidad se ha descrito varias veces en vid, y se encuentra ampliamente representado en la bibliografía científica. Se describió por primera vez en el trabajo de Ibáñez et al. (2000), donde se encontró una diferencia de 2pb en un alelo del microsatélite VVMD7 entre dos variedades sinónimas de Corinto negro (Black currant y Mavri corinthiaki), 246pb en Black currant y 248pb en Mavri corinthiaki. Se hipotetizó que ese cambio era debido a un aumento o disminución de una repetición de la unidad básica. Un razonamiento similar se aplicó en el caso descrito por Lefort y Roubelakis-Angelakis (2001), donde fueron capaces de distinguir Kolokythas lefkos de su sinónima Roditis lefkos. La diferencia entre estas variedades se encontró en el locus microsatélite ssrvrzag64, en Kolokythas lefkos apareció un alelo con 139pb, y en Roditis lefkos para ese mismo locus aparecieron dos alelos con 137pb y 139 pb, respectivamente. Los mismos autores distinguieron Romeiko mavro de su sinónima Tsardana considerando los alelos del locus VVMD7, los cuales presentaban un valor de 236pb y 246 pb, y de 236pb y 244 pb, respectivamente. Más mutaciones de este tipo han sido encontradas en otras variedades como: Pinot (Regner et al., 2000a), y Refošk (Kozjak et al., 2001), (Kozjak et al., 2003) etc., e incluso algunos casos de quimerismo citados más adelante en este estudio. En el trabajo de Crespan (2004) se presentaron cuatro mutaciones de este tipo: tres de ellas mostraron un incremento en la secuencia del fragmento amplificado de una repetición del motivo básico para los loci VVMD32 (de 265pb a 267pb), VVS2 (de 155pb a 157 pb) y VVMD7 (de 249pb a 251 pb) en las variedades Muscat d Alsace, Greco di Tufo y Primitivo, respectivamente, mientras que una mutación en el locus ISV8 representó un incremento en tres repeticiones del motivo básico en la variedad Corvina veronese. En los datos de Franks et al. (2002) se mostraron dos mutaciones debidas al incremento de la longitud de los alelos, desde 186pb a 188 pb en el locus VVS19 para Primitivo de Gioia; y desde 121pb a 123 pb en el locus VVS5 para Pinot meunier. En ese estudio los resultados obtenidos en la secuenciación confirmaron la adición de una unidad de repetición. En el estudio de Riaz et al. (2002), inicialmente analizaron 25 clones de Pinot noir y 22 clones de Chardonnay con 100 loci microsatélite. Se mostraron datos para 15 loci en Pinot noir, y para 9 en Chardonnay. Estos loci fueron 110
135 Resultados y Discusión seleccionados de entre los 100 estudiados, por ser los más polimórficos en cada variedad y por aparecer en ellos distintos tipos de mutación. La mayoría presentaron dos genotipos posibles el genotipo esperado y el mutado- pero en 5 marcadores SSR de Pinot noir (VMCNg1b9, VMCNg1e8, VMCNg2b6, VMCNg1d12 y VMCNg2f12) y en uno de Chardonnay (VVC5g7) llegaron a presentarse entre 3 y 4 genotipos distintos para un mismo locus. Algunos de los alelos mutados diferían del esperado en una o dos repeticiones del motivo básico, mientras que otros diferían del esperado en un rango de 10pb a 20pb o más. En este último caso habitualmente aparece un tercer alelo (posible quimerismo), el cual presenta un tamaño intermedio entre los dos alelos esperados. En el trabajo de Moncada et al. (2006), empleando microsatélites, llevaron a cabo un estudio de diversidad genética y dispersión geográfica en clones de Cabernet sauvignon. En este estudio, analizaron 59 clones de esta variedad, procedentes de 7 países diferentes (Francia, Chile, España, Australia, Hungría, USA e Italia), con 84 marcadores microsatélites. Con 18 de ellos, los más polimórficos, detectaron 22 genotipos diferentes en Cabernet sauvignon, con un 97% de similitud genética entre ellos. De los 59 clones estudiados, sólo 2 mostraron el genotipo original. Los restantes 57 clones fueron distribuidos en 21 genotipos diferentes, que llegaron a mostrar para un mismo locus entre 2 y 4 genotipos distintos. El genotipo más frecuente, representado en 44 de los 59 clones, fue aquel en el que el locus VMC5g7 mostró un alelo adicional (198), presentando la combinación trialélica 194:196:198. De esos 44 clones, 29 presentaban únicamente ese polimorfismo, mientras que los 15 clones restantes presentaban polimorfismos adicionales basados en la aparición de nuevos alelos que diferían del esperado en un número determinado de repeticiones del motivo básico. La mayoría de los nuevos alelos diferían del alelo esperado en un rango de entre 1 y 4 repeticiones del motivo básico. En este caso, los autores sugirieron que el mecanismo de mutación implicado sería el slippage de la polimerasa. Mientras que los nuevos alelos detectados en los loci VVMD30 y VVMC8g9, diferían del alelo esperado en 16, 17 o 18 repeticiones del motivo básico. En este caso, los autores hipotetizaron que el polimorfismo sería debido a que hubiera ocurrido una mutación en la región flanqueante del microsatélite. Con los resultados obtenidos, concluyeron que la diversidad genética presente en los clones de la variedad Cabernet sauvignon es debida a una estructura quimérica similar a la obtenida en las variedades pertenecientes al sortogrupo Pinot (Hocquigny et al., 2004). Tanto Cabernet 111
136 Resultados y Discusión sauvignon como las variedades pertenecientes al sortogrupo Pinot presentan un origen muy antiguo, por lo que los resultados obtenidos en estos cultivares podrían explicar la diversidad genética existente en otras antiguas variedades de vid, no esperando encontrar esta variabilidad en clones o sports de variedades obtenidas recientemente en programas de mejora genética (Moncada et al., 2006). Únicamente en el trabajo de Crespan (2004), un microsatélite de los 9 evaluados en esta tesis (VVS2) estuvo implicado en una mutación debida al incremento de una repetición del motivo básico en la secuencia del fragmento amplificado. Teniendo en cuenta los resultados obtenidos en este estudio, y los descritos en la bibliografía, se puede establecer la distancia mínima para el sistema de 9 loci microsatélite según el criterio propuesto en este trabajo: a partir de la menor diferencia intersortogrupo y de la mayor diferencia intrasortogrupo. Ambas medidas en número de alelos diferentes. Los resultados obtenidos en este trabajo durante el análisis de la colección global formada por accesiones en base al estudio de aquellas más próximas en cuanto a su genotipo para los 9 loci microsatélite, se pueden resumir en: Todas las accesiones que coincidían en la totalidad de los alelos analizados, 18, se consideró que pertenecían al mismo sortogrupo y se seleccionó una sola accesión representativa de cada genotipo. Únicamente apareció una pareja de accesiones, Chasselas blanca y Chasselas Gros Coulard, que coincidía en 17 alelos de los 18 analizados. Dicha pareja difería entre sí en un alelo del locus ZAG83. Con el análisis de 20 loci microsatélite se concluyó que una de estas dos accesiones es un sport de la otra. La diferencia se consideró variabilidad intrasortogrupo. Alfonso Lavalle-Princeps y Pizzutelo Moscato Biondo-Galletta rosa fueron las dos parejas que coincidieron en 16 alelos de los 18 analizados. Con el análisis de 20 microsatélites se llegó a la conclusión de que pertenecían a sortogrupos diferentes. La diferencia se consideró variabilidad intersortogrupo. 112
137 Resultados y Discusión Con los resultados obtenidos al analizar los distintos tipos de variabilidad intrasortogrupo descrita en la literatura en vid para los 9 microsatélites empleados, se llega a la misma conclusión que con los obtenidos en este trabajo. Es decir, el mayor número de alelos diferentes entre plantas pertenecientes a un mismo sortogrupo, sería 1. Por lo tanto, con los resultados anteriores, la distancia más pequeña entre dos variedades para considerarlas pertenecientes a sortogrupos diferentes mediante el uso de los 9 loci estudiados, sería de 2 alelos. Resultados idénticos a los obtenidos en esta tesis, en cuanto al valor de la distancia mínima, se muestran en Ibáñez (2000). Se analizaron 53 accesiones apirenas con 6 loci microsatélite, entre los cuales se encuentran el VVS2 y VVMD5 presentes en este estudio. Se estimó la distancia mínima en 2 alelos. Es decir, dos variedades se considerarían pertenecientes a sortogrupos diferentes si se diferenciasen en más de un alelo de los 6 loci analizados. Hasta el momento, y en nuestro conocimiento, no se ha publicado ningún estudio en otras especies vegetales donde empleando microsatélites, se determine el valor de la distancia mínima en número de alelos. Es importante resaltar, como muestra la bibliografía, que la tasa de mutación en las secuencias microsatélites es superior a la de otras zonas del genoma, y la aparición de nuevos alelos por mutación somática en plantas de la misma variedad es un hecho infrecuente, pero posible, por lo que debe ser tenido en cuenta a la hora de establecer la distancia mínima. Cuando se considera que las plantas se están propagando vegetativamente, como ocurre en los viñedos, la probabilidad de encontrar mutaciones en regiones microsatélites está afectada por algunos factores: Edad de la variedad. Debido a que las mutaciones son acumulativas, la probabilidad de encontrar mutaciones es directamente proporcional a la edad de la variedad. Extensión de cultivo de la variedad (número de clones/variedad). 113
138 Resultados y Discusión Número de loci microsatélite analizados. Homogeneidad y estabilidad de los loci microsatélite analizados. En el estudio posterior se analizará la homogeneidad y estabilidad de los 9 loci microsatélite que ocupan esta tesis, pero los datos bibliográficos ya indican que el comportamiento de distintos microsatélites es diferente. En el trabajo de Crespan (2004), se estimó un ratio general de mutación por planta y microsatélite en vid de 8x10-5. Para calcularlo tomaron datos, tanto del trabajo citado como de la literatura, de 224 individuos analizados con 948 loci, entre los cuales se encontraron 35 mutaciones. Es muy improbable, pero se ha descrito (Riaz et al., 2002), (Moncada et al., 2006), encontrar en la misma planta dos mutaciones independientes en distintos microsatélites. Hay que destacar que este fenómeno tan infrecuente no ha aparecido representado en la bibliografía consultada con los 9 loci utilizados en este estudio, y dentro del propio trabajo, donde se ha manejado una colección de casi 500 genotipos, únicamente la pareja representada por Chasselas blanca y Chasselas Gros Coulard, mostró una diferencia entre sí en un alelo del locus ZAG83. Hay que tener en cuenta que el hecho de encontrar en una planta 1 o más mutaciones en un microsatélite, afectaría únicamente al microsatélite en cuestión. No es esperable que a raíz de esa mutación en el microsatélite aparezca una mutación morfológica en esa planta Utilidad del sistema de 9 loci microsatélite para el estudio de Distinción Los 9 loci microsatélite empleados en este estudio han demostrado ser una herramienta muy útil para el análisis de la colección formada por accesiones, siendo capaces de determinar en ella las diferencias intra e intersortogrupo. En base a estas diferencias se ha establecido la distancia mínima en 2 alelos. Con referencia al sistema de análisis con microsatélites, de toda la bibliografía citada en el apartado anterior más los resultados obtenidos en este trabajo, se puede destacar que: 114
139 Resultados y Discusión Las variedades que generalmente presentan alelos mutantes son muy antiguas (varios siglos), por lo que, en principio, este fenómeno no se espera que pueda llegar a ocurrir durante el periodo de tiempo que comprende la protección legal de una nueva variedad vegetal. Ninguno de los 9 microsatélites en estudio estuvo implicado en mutaciones que producen alelos nulos, y solamente uno, el VVS2, lo estuvo en mutaciones debidas a un incremento en la secuencia del fragmento amplificado (Crespan, 2004). En este trabajo, empleando una colección de casi 500 genotipos, únicamente apareció una pareja de accesiones, Chasselas blanca y Chasselas Gros Coulard, que difería entre sí en un alelo del locus ZAG83. Ambas pertenecían al mismo sortogrupo. En el análisis rutinario de variedades de vid, aquellas que morfológicamente no se distinguen, tampoco lo hacen al analizarlas con microsatélites. Sin embargo, variedades que con microsatélites muestran un mismo genotipo, al analizarlas morfológicamente pueden resultar distintas. Un ejemplo paradigmático de esto lo constituye el caso de Garnacha blanca y Garnacha tinta, siendo una de ellas un sport de la otra. Por lo tanto, los microsatélites, en base a la distancia mínima, permitirían establecer la distinción, aunque una identidad total en microsatélites no significaría que dos variedades no son distintas. Asimismo, en base a los resultados expuestos, al igual que en morfología puede no establecerse distinción con un carácter morfológico, en STMS tampoco debe establecerse la distinción con 1 alelo. Por lo que, en este sentido, los microsatélites podrían resultar aptos en el estudio de Distinción. Hay que recordar que en la actualidad, los marcadores de ADN no se admiten por la UPOV para realizar los test DHE, aunque se está trabajando en su seno (a través del grupo BMT) para estudiar su incorporación en varias especies. En la décima reunión del grupo de trabajo BMT, celebrada en Seúl, del 21 al 23 de noviembre de 2006, se expusieron otros trabajos, aparte del presentado por nuestro laboratorio ( Un sistema basado en microsatélites, útil para la identificación y protección legal de variedades de vid ), donde se manifestó que el empleo de marcadores moleculares microsatélites sería un complemento muy útil para los test 115
140 Resultados y Discusión DHE. Con referencia a cultivos propagados vegetativamente, donde se encuentra la vid, se presentaron estudios de interés; y dado que resulta difícil el acceso a los mismos, merece la pena describir alguno de ellos: - Expertos de Alemania, Holanda y Reino Unido, en el documento BMT/10/16, hacían referencia a un estudio basado en una colección de referencia de variedades de rosa. Debido al gran número de variedades de rosa existente en todo el mundo, se hace complicado llevar a cabo los test DHE en esta especie. Para intentar resolver este problema, en este estudio se construyó una base de datos que contenía datos administrativos, morfológicos, moleculares y fotos para un gran número de variedades de rosa tanto de invernadero como de jardín, que servirían como referencia para identificación de variedades. Todo ello conduciría a reforzar los derechos de los obtentores. Actualmente, los test DHE en rosa están basados en el análisis de caracteres morfológicos y, cuando es necesario, de fotografías, ambos pueden estar afectados por las condiciones medioambientales y por lo tanto la información requiere una cuidadosa interpretación por parte de los examinadores, al igual que ocurre en vid. En esta base de datos se recogen datos para 12 loci microsatélite en aproximadamente 380 variedades distintas de rosa. Estos 12 loci demostraron ser muy informativos para identificar variedades de rosa. Concluyeron que estos marcadores pueden apoyar e incluso mejorar la calidad de los test DHE y la calidad de la protección de variedades de esta especie. Usando los 12 loci de este estudio, la probabilidad de que dos variedades muestren el mismo perfil electroforético (PI), fue de 10-8 para rosas de invernadero y de 5x10-11, para rosas de jardín. Esto significa que, cuando dos muestras presentan perfiles genéticos idénticos, la probabilidad de que sean iguales o pertenezcan al mismo grupo mutante (que aquí denominamos sortogrupo) es de casi el 100%. Cuando combinaron los datos microsatélite obtenidos para las rosas de jardín y las de invernadero, observaron que todas ellas (excluyendo mutantes dentro de un determinado grupo de rosas de jardín o de invernadero) mostraron perfiles diferentes. A pesar de algunas dificultades, demostraron que los datos procedentes de dos laboratorios diferentes (ring test) eran sustancialmente equivalentes, y que los 116
141 Resultados y Discusión datos moleculares producidos eran una herramienta muy útil para el manejo de colecciones de referencia. - Expertos de Holanda, en el documento BMT/10/17, hacían referencia a un estudio basado en marcadores microsatélites para la identificación de variedades de claveles. Como muchas plantas ornamentales, los claveles presentan un gran número de variedades. Actualmente, el registro y la protección de variedades de claveles están basados en caracteres morfológicos. En este estudio muestran los resultados obtenidos en el empleo de marcadores microsatélites para caracterizar variedades de clavel, así como la construcción de una base de datos molecular. Se analizaron con 13 loci microsatélite 172 muestras que abarcaron una selección de variedades comunes de clavel así como algunos grupos de mutantes. Con el set de 13 microsatélites, todos los mutantes bien conocidos y las variedades de las que proceden fueron correctamente agrupados juntos. La probabilidad de que dos muestras presenten el mismo perfil electroforético (PI), fue de 16x10-7. El promedio de similitud entre muestras fue bajo (0,46), lo que indica un alto nivel de diversidad genética entre las muestras estudiadas. Así, el set de loci microsatélite descrito en este estudio puede ser usado para el genotipado de variedades de clavel y su consiguiente identificación. Aseguran que para supuestos prácticos, es recomendable analizar todas las muestras por duplicado y reanalizar todas aquellas que muestren diferencias en alelos antes de su incorporación a la base de datos. De esta forma, el valor umbral (valor usado para evitar que dos variedades sean consideradas diferentes debido a un error técnico) puede ser más bajo, consiguiendo un agrupamiento más preciso de las muestras. - Expertos de Reino Unido, en el documento BMT/10/5, hacían referencia a un estudio basado en la identificación de cultivares de patata del Catálogo Común de la Unión Europea mediante el uso de marcadores microsatélite. A principios del 2.006, la Oficina Comunitaria de Variedades Vegetales financió un proyecto para construir una base de datos que contuviera datos microsatélite y morfológicos para las variedades de patata presentes en el Catálogo Común de la Unión Europea. Los cuatro participantes de este proyecto eran los 117
142 Resultados y Discusión responsables del test DHE en Alemania, Holanda, Polonia y Reino Unido. La base de datos creada contiene información para 9 loci microsatélite en 579 variedades de patata. Exceptuando muy pocos casos (variantes somaclonales y variedades mal identificadas), todas las variedades se pudieron diferenciar usando esos 9 loci. En este estudio, se analizaron muestras pertenecientes a la misma variedad y procedentes de diferentes fuentes. Se demostró que existen errores en el etiquetado de variedades mantenidas en grandes colecciones de material. Concluyeron que, con esto, se manifiesta la importancia del empleo de los marcadores moleculares microsatélites como un complemento en el test DHE. Aunque en ninguno de estos estudios se ha analizado un número de muestras tan elevado como en esta tesis doctoral, ni se ha realizado un análisis específico sobre cómo los microsatélites empleados serían de útiles para su utilización en el test DHE, todos han llegado a la misma conclusión con los resultados obtenidos: que los marcadores moleculares microsatélite aparte de su ya conocida utilidad para la identificación de variedades vegetales, supondrían un complemento muy útil para el test DHE ESTUDIO DE IDENTIFICACIÓN Idoneidad de la colección utilizada La identificación mide la conformidad de una variedad con algún modelo establecido. Por ello, los aspectos más importantes en el estudio de Identificación son la elección de una colección de referencia adecuada, y el sistema con que se estudia esa colección. En este estudio, se tomó como colección de referencia, la Colección de genotipos únicos derivada del estudio de Distinción, analizada con 9 loci microsatélite. Esta colección estaba constituida por 495 variedades de genotipos distintos. Con ello se pretendía evitar información redundante, y que las frecuencias alélicas de la colección fueran más exactas. La Probabilidad Total de Identidad (PI) obtenida para el conjunto de los 9 loci microsatélite en esta colección mediante el software Identity, fue 6,87 x 10-12, lo que indica una muy baja probabilidad de que dos variedades distintas compartan el mismo genotipo al azar para los loci analizados. 118
143 Resultados y Discusión En general, los resultados obtenidos en este estudio son similares a otros trabajos publicados en los cuales se analizó un número considerable de muestras, como el de Ibáñez et al. (2003) (111 variedades y 13 microsatélites) en el que se obtuvo una PI total de 9,9 x y Sefc et al. (1999), donde analizando 120 variedades y 18 microsatélites, de los que solo presentaron la PI para 13 de ellos, obtuvieron un valor para PI total de 2,19 x Hay que resaltar el alto poder de resolución del sistema de 9 microsatélites utilizado, ya que únicamente fueron necesarios 5 de los 9 STMS para identificar inequívocamente las 495 variedades que formaban la Colección de genotipos únicos. Dichos loci fueron: VVMD27, VVMD5, VVS2, ZAG83 y VVMD28, que resultaron ser los que tenían el valor de Heterocigosidad observada más alto de los 9, excepto el locus ZAG83, como se puede observar en la Tabla R9. Concretamente, con los loci VVMD27, VVMD5, VVS2 y VVMD28 se identificaron inequívocamente 485 variedades. El resto se pudieron distinguir con el locus ZAG83. Este poder de resolución depende entre otros factores, de la heterocigosidad de los STMS elegidos para la identificación, y de la variabilidad de las muestras que formen la colección de referencia. Dentro de las 495 variedades que formaban la Colección de genotipos únicos, se encontraban variedades tanto de uva de mesa (52,72%) como de vinificación (40,61%), portainjertos (2,83%), híbridos productores directos (0,81%), especies del género Vitis no vinifera y géneros de la familia Vitáceas (3,03%). A su vez, como ya se ha comentado, dentro de esta diversidad, se encontraban variedades muy cercanas entre sí (padres, hijos, hermanos, etc.). Tabla R9. Valores de Heterocigosidad observada (Ho) en los 9 microsatélites del estudio. Destacados aparecen los 5 loci con los que se identificaron inequívocamente las 495 variedades de la Colección de genotipos únicos. LOCUS ZAG67 VVMD27 VVMD5 ZAG29 ZAG62 ZAG112 VVS2 ZAG83 VVMD28 Ho 0,78 0,82 0,87 0,33 0,81 0,80 0,88 0,78 0,87 Hay estudios en la bibliografía, por ejemplo el de Martín et al. (2003), donde partiendo de una colección de 176 variedades españolas de Vitis vinifera, analizadas con 6 loci microsatélite, no fueron capaces de identificar todas ellas 119
144 Resultados y Discusión inequívocamente. Se indicó que ello podía ser debido a que la colección estaba formada por variedades estrechamente relacionadas. En el trabajo de Ibáñez y Eeuwijk (2003), partiendo de una colección de 45 accesiones apirenas distintas, empleando 9 loci microsatélite, únicamente 3 fueron necesarios para identificar inequívocamente todos los cultivares presentes en la citada colección. En los dos trabajos anteriores, 3 de los microsatélites empleados coincidían con los 9 de este estudio: VVMD5, VVS2 y ZAG Análisis de la estructura de la colección Para estudiar si la Colección de genotipos únicos estaba estructurada en función de los genotipos que presentaba para los 9 loci evaluados, se utilizó el software Structure 2.0 (Pritchard y Wen, 2003). Siguiendo el criterio llevado a cabo en Pritchard et al. (2000), se detectaron 14 poblaciones en la colección compuesta por 495 variedades distintas. Como ya se ha comentado, este criterio puede no proporcionar una estimación correcta del número de poblaciones que podían existir en una determinada colección, por lo que se empleó la metodología descrita en Evanno et al. (2005). Se determinó K (tasa de cambio presente en los valores de la probabilidad en función de K), y se representó gráficamente este valor frente a K (Figura R4). Se visualizó un pico muy claro en K= 4, lo que pareció indicar que las 495 variedades que formaban la colección se agrupaban en cuatro poblaciones delta K K Figura R4. Representación gráfica de K frente a K. 120
145 Resultados y Discusión Una vez seleccionado el valor 4 para K, se eligió aquella simulación de entre las 10 realizadas en el análisis que presentó la combinación más probable de genotipos para esa K. De esta simulación, se obtuvieron los gráficos representados en las Figuras R5 y R6. Estas dos figuras muestran a las 495 variedades que forman la Colección de genotipos únicos, agrupadas por poblaciones, y concretamente, por el grado de mezcla genética que presentan de cada una de ellas. Así, cada variedad se encuentra representada por una barra vertical, pudiendo ésta mostrar un máximo de 4 fragmentos coloreados cuyo tamaño dependerá de la probabilidad que tenga cada variedad de pertenecer a una de las 4 poblaciones detectadas en el análisis. Estas se encuentran representadas por un color predominante: rojo, verde, azul y amarillo, respectivamente. La Figura R5 representa el gráfico de las 495 variedades, destacándose individualmente cada una de ellas. En la Figura R6 se ha variado la escala para una mejor visualización de las 4 poblaciones detectadas en la Colección de genotipos únicos. 121
146 Resultados y Discusión Figura R5. Representación gráfica de las 495 variedades que forman la Colección de genotipos únicos, destacando cada una de ellas individualmente. Se encuentran agrupadas en función del grado de mezcla genética que presentan de cada una de las 4 poblaciones detectadas en el análisis con el software Structure, y representadas cada una por un color diferente. Los números se corresponden con los de la Tabla R10, página
147 Resultados y Discusión Figura R6. Representación gráfica de la Figura R5 a diferente escala. La Tabla R10 presenta cada una de las 495 variedades que componen la Colección de genotipos únicos con algunas características relevantes. Las variedades utilizadas tanto para mesa como para vino, representadas en la Tabla R10 como MV, se consideraron en este análisis como variedades de uva de mesa. 123
148 Resultados y Discusión Tabla R10. Se recoge (de izquierda a derecha) la siguiente información para las 495 variedades que forman la Colección de genotipos únicos : Nº con el que aparecen representadas en la Figura R5; Nombre de la variedad; Código de parcela en la Colección de variedades de vid de El Encín (las muestras de Briones, las seleccionadas del estudio de establecimiento de descriptores microsatélite y las obtenidas del estudio de Homogeneidad y Estabilidad, no presentan código por no pertenecer la mayoría de ellas a la colección de El Encín ); Uso de las variedades [mesa (M); vino (V); Mesa/Vino (MV); especies del género Vitis no vinifera (EGV); híbridos productores directos (HPD) y portainjertos (PTI)]; y Origen [variedades españolas (ESP) y variedades extranjeras (EXT)]. Nº FIGURA R5 NOMBRE VARIEDAD CÓDIGO PARCELA USO ORIGEN Nº FIGURA R5 NOMBRE VARIEDAD CÓDIGO PARCELA USO ORIGEN Nº FIGURA R5 NOMBRE VARIEDAD CÓDIGO PARCELA 1 VITIS CALIFORNICA EGV EXT 26 MOLINERA 22B05 M ESP 51 PIROVANO I-A-13 M EXT 2 SO4 PTI EXT 27 DE CILINDRO 22B08 M ESP 52 REGINA DEI VIGNETI 25-I-A-14 M EXT 3 VITIS RIPARIA EGV EXT 28 IMPERIAL ROJA 22B09 M ESP 53 PRECOCE DE MALINGRE 25-I-A-15 M EXT 4 VITIS SILVESTRIS (MACHO) EGV ESP 29 FONDO DE ORZA 22B50 M ESP 54 PRECOCE DI ROMA 25-I-A-16 M EXT 5 MILLARDET EGV EXT 30 IMPERIAL 22C05 M ESP 55 JAOUMET 25-I-A-17 M EXT 6 COUDERC 1616 EGV EXT 31 MANTUA 22C25 M ESP 56 JULY MUSCAT 25-I-A-20 M EXT 7 MILLARDET 420A EGV EXT 32 CARDINAL 22C42 M EXT 57 EARLY MUSCAT 25-I-B-01 M EXT 8 VITIS SILVESTRIS (MACHO) EGV ESP 33 MOSCATEL 22D10 M ESP 58 MUSCAT SAINT LAURENT USO ORIGEN 25-I-B-04 M EXT 9 41 B M EGV ESP 34 GREG 22D11 M ESP 59 ANNA MARIA 25-I-B-05 M EXT 10 RUPESTRIS DE LOT EGV EXT 35 FUMAT 22H08 M ESP 60 PRIMIERA 25-I-B-06 M EXT 11 VITIS CINEREA EGV ESP 36 CARDINAL 22M23 M EXT 61 FERDINAND DE LESSEPS 25-I-B-07 M EXT 12 COUDERC EGV EXT 37 ALFONSO LAVALLE 22M25 M EXT 62 FONDO DE ORZA 25-I-B-10 M ESP 13 VITIS LABRUSCA EGV EXT 38 NÁPARO 22N10 M ESP 63 VILLARDIEL 25-I-B-11 M ESP 14 VITIS AESTIVALIS EGV ESP 39 CRUJILLÓN 22E04 M ESP 64 AUGUSTA 25-I-B-12 M EXT 15 VITIS ARIZONICA EGV ESP 40 MOSCATEL NEGRO 22E60 M ESP 65 CIRCA 25-I-B-13 M EXT 16 SALVADOR(=SEIBEL 128) 17 JACQUEZ HPD ESP 42 HPD EXT 41 PERLA DE CSABA 25-I-A-01 M EXT 66 BRUNI I-B-14 M EXT MADELEINE ANGEVINE 25-I-A-02 M EXT 67 EL GOUZ 25-I-B-15 M EXT 18 VILLARD BLANC HPD EXT 43 BRUNI I-A-03 M EXT 68 GRADISKA 25-I-B-17 M EXT 19 OBERLIN 595 HPD EXT 44 BRUNI I-A-04 M EXT 69 PROSPERI I-B-18 M EXT 20 NAPOLEÓN 22A47 M ESP DE CUERNO 22A48 M ESP 46 MADELEINE ROYALE LUGLIENGA BIANCA 25-I-A-05 M EXT 70 ATTILIO RAGGIONERI 25-I-B-19 M EXT 25-I-A-06 M EXT 71 BRUNI I-B-20 M EXT 22 DOMINGA 22A49 M ESP 47 GOLD 25-I-A-08 M EXT 72 PANSE PRECOCE 25-II-A-01 M EXT 23 OHANES 22A50 M ESP 48 PRIMUS 25-I-A-09 M EXT 73 ADMIRABLE DE COURTILLER 25-II-A-05 M EXT 24 NEGRA TARDÍA 22B01 M ESP 49 AGOSTENGA 25-I-A-11 M EXT 74 BRUNI II-A-06 M EXT 25 CIRUELA ROJA 22B03 M ESP 50 DONA MARIA 25-I-A-12 M EXT 75 ALBA MAGNA 25-II-A-07 M EXT 124
149 Resultados y Discusión Nº FIGURA R5 NOMBRE VARIEDAD CÓDIGO PARCELA USO ORIGEN Nº FIGURA R5 NOMBRE VARIEDAD CÓDIGO PARCELA USO ORIGEN Nº FIGURA R5 NOMBRE VARIEDAD CÓDIGO PARCELA 76 DELIZIA DI VAPRIO 25-II-A-08 M EXT 101 PIROVANO II-B-18 M EXT 126 UVA JIJONA 25-IV-A-01 M ESP 77 ANGIOLA BIANCA 25-II-A-10 M EXT SULIVAN 25-II-A-11 M EXT CHASSELAS MICHEL TOMPA MOSCATO GUSTAV SZAUTER FAVORITA DI CONEGLIANO USO ORIGEN 25-II-B-19 M EXT 127 VIVONA IV-A-02 M EXT 25-III-A-02 M EXT 128 PIROVANO IV-A-03 M EXT 25-II-A-12 M EXT 104 INZOLIA BIANCA 25-III-A-03 M EXT 129 DABOUKI 25-IV-A-05 M EXT 80 PALESTINA I 25-II-A-14 M EXT 105 WRATCHANSKI MISKET 25-III-A-04 M EXT 130 OLIVETTE BARTHELET 25-IV-A-07 M EXT 81 MATHIASZ JANOS DIADALA MUSKOTALY 25-II-A-15 M EXT 106 BICANE 25-III-A-05 M EXT PIROVANO II-A-16 M EXT 107 MOSCATO DI TERRACINA CORNIOLA DI MILAZZO 25-IV-A-09 M EXT 25-III-A-06 M EXT 132 AURATA 25-IV-A-10 M EXT 83 DALMASSO VI II-A-17 M EXT 108 MARENGO 25-III-A-08 M EXT 133 PERLONA 25-IV-A-11 M EXT 84 BOGNI II-A-18 M EXT 109 COARNA BIANCA 25-III-A-09 M EXT 134 LOCAL WHITE XYNISTERI 25-IV-A-12 M EXT 85 PRINCEPS 25-II-A-19 M EXT 110 SIDERITIS 25-III-A-11 M EXT 135 PIROVANO IV-A-13 M EXT 86 PROSPERI II-A-20 M EXT 111 AURORA 25-III-A-12 M EXT 136 ALEDO REAL 25-IV-A-17 M ESP 87 FOSTER'S WHITE SEEDLING 25-II-B-01 M EXT 112 ZARIZA NA LOSIATA X BOLGAR TRIESTE 25-II-B-02 M EXT 113 LACRIMA DI MARIA 25-III-A-14 M EXT III-A-13 M EXT 137 CIMINNITA 25-IV-A-19 M EXT PIZZUTELLO MOSCATO BIONDO 25-IV-B-03 M EXT 89 DORONA DI VENEZIA 25-II-B-03 M EXT 114 REGINA ELISABETTA 25-III-A-17 M EXT 139 AUSONIA 25-IV-B-04 M EXT 90 ALBERTA 25-II-B-05 M EXT 115 CICLÓPICA 25-III-A-18 M EXT 140 SERVANT 25-IV-B-05 M EXT 91 FORASTERA BLANCA 25-II-B-06 M ESP 116 IMPERO 25-III-B-02 M EXT 141 RODITIS 25-IV-B-06 M EXT 92 THALLOCZY LAJOS 25-II-B-07 M EXT 117 BARESANA 25-III-B-03 M EXT 142 PROSPERI IV-B-07 M EXT 93 CATALANESCA BIANCA 25-II-B-08 M EXT 118 ZIBIBBO 25-III-B-04 M EXT 143 TALISMANO 25-IV-B-08 M EXT 94 SCHIRADZOULI BIANCO 25-II-B-09 M EXT 119 ITALIA 25-III-B-07 M EXT 144 LATINA 25-IV-B-13 M EXT 95 GENERAL DE LA MARMORA 25-II-B-10 M EXT 120 VERDEA 25-III-B-08 M EXT 145 ALEDO 25-IV-B-15 M ESP 96 DUCHESS OF BUCCLEUGH 25-II-B-11 M EXT 121 ROSETI 25-III-B-09 M EXT 146 HIMONIATICO 25-IV-B-19 M EXT 97 MESLIER HÂTIF 25-II-B-12 M EXT 122 PROSPERI III-B-10 M EXT 147 CALMERIA 25-IV-B-20 M EXT 98 DIAMANT TRAUBE 25-II-B-13 M EXT 123 CLOTILDE PROSPERI 25-III-B-11 M EXT 148 VOLTA 25-V-A-01 M EXT 99 SUPERZIBIBBO 25-II-B-15 M EXT 124 NEHELESCOL 25-III-B-17 M EXT SAUVIGNON 25-II-B-17 M EXT 125 GALLURA ZENNI DE DAMASCO NOIR HÂTIF DE MARSEILLE 25-V-A-02 M EXT 25-III-B-18 M EXT 150 ROI DES PRECOCES 25-V-A-03 M EXT 125
150 Resultados y Discusión Nº FIGURA R5 NOMBRE VARIEDAD CÓDIGO PARCELA USO ORIGEN Nº FIGURA R5 151 CHAOUCH ROSE 25-V-A-04 M EXT PERLE DE CSABA ROUGE NOMBRE VARIEDAD MOSCATEL DE HAMBURGO CÓDIGO PARCELA USO ORIGEN Nº FIGURA R5 NOMBRE VARIEDAD CÓDIGO PARCELA USO ORIGEN 25-VI-A-05 M EXT 201 INZOLIA NERA 25-VI-B-17 M EXT 25-V-A-07 M EXT 177 TERESA PIROVANO 25-VI-A-08 M EXT 202 DARKAIA NERA 25-VI-B-18 M EXT 153 AGOSTENGA ROSA 25-V-A-08 M EXT 178 CILIEGUIOLO NERO 25-VI-A-10 M EXT 203 SUPERFRANKENTHAL 25-VII-A-01 M EXT 154 GATETA 25-V-A-09 M ESP 179 IGNEA 25-VI-A-12 M EXT 204 LASSINA 25-VII-A-04 M EXT 155 CHASSELAS ROUGE 25-V-A-12 M EXT 180 TRENTHAM BLACK 25-VI-A-13 M EXT 205 AHMEUR BOU AHMEUR 25-VII-A-05 M EXT 156 PORTUGUÉS AZUL 25-V-A-13 M EXT 181 SUPERBA 25-VI-A-14 M EXT PIROVANO 25-VII-A-06 M EXT 157 SCHIRAZ 25-V-A-14 M EXT 182 PIROVANO VI-A-15 M EXT 207 ROSAKI NOIR DES SEMIS 25-VII-A-07 M EXT 158 BRUNI V-A-16 M EXT 183 FUSCA 25-VI-A-16 M EXT 208 FRAULA KAKINI 25-VII-A-09 M EXT 159 COARNA NEAGRA 25-V-A-17 M EXT 184 VERNACCIA NERA 25-VI-A-17 M EXT 209 EL FARRYALI 25-VII-A-11 M EXT 160 SCARLET 25-V-A-19 M EXT 185 PERLA NERA 25-VI-A-18 M EXT 210 GROS MAROC 25-VII-A-12 M EXT 161 BRUNI V-A-20 M EXT 186 BRUNI VI-A-19 M EXT 211 DANUGUE 25-VII-A-13 M EXT 162 DUC DE MAGENTA 25-V-B-01 M EXT 187 ELETTRA 25-VI-A-20 M EXT 212 MISTRESS HALL 25-VII-A-14 M EXT 163 LOMBARDIA 25-V-B-02 M EXT 188 DALMASSO XI VI-B-01 M EXT 213 DALMASSO III VII-A-15 M EXT 164 BRUNI V-B-03 M EXT 189 GEMRE 25-VI-B-02 M EXT 214 BLACK ROSE 25-VII-A-16 M EXT 165 FRANKENTHAL 25-V-B-04 M EXT 190 BOGNI VI-B-03 M EXT 215 BLACK ALICANTE 25-VII-A-19 M EXT 166 CORNICHON VIOLET 25-V-B-06 M EXT 191 ARTURO MARESCALCHI 25-VI-B-04 M EXT 216 JERÓNIMO DE TUDELA 25-VII-A-20 M ESP 167 PRUNE DE CAZOULS 25-V-B-09 M EXT 192 PLANTA MULA 25-VI-B-06 M ESP 217 DATTIER NOIR 25-VII-B-01 M EXT 168 PIROVANO V-B-13 M EXT 193 BARBABLEU 25-VI-B-08 M EXT 218 LATTUARIO NERO 25-VII-B-02 M EXT 169 APESORGIA NERA 25-V-B-14 M EXT 194 NYMRANG 25-VI-B-09 M EXT 219 NORE 25-VII-B-03 M ESP 170 PIROVANO V-B-17 M EXT 195 DALMASSO XVIII VI-B-11 M EXT 220 OPHTALMO 25-VII-B-04 M EXT 171 CEREZA 25-V-B-18 M EXT 196 DALMASSO XI VI-B-12 M EXT 221 BARLINKA 25-VII-B-05 M EXT 172 MOSCATEL NEGRO 25-V-B-19 M ESP 197 GROS COLMAN 25-VI-B-13 M EXT 222 MARSIGLIANA 25-VII-B-06 M EXT 173 OILLADE NOIR 25-VI-A-01 M EXT 198 PIROVANO VI-B-14 M EXT 223 GLACIÈRE 25-VII-B-08 M EXT 174 NINCUSA 25-VI-A-03 M EXT 199 MARIA ROSA 25-VI-B-15 M EXT 224 PRUNESTA NERA 25-VII-B-09 M EXT 175 MOSCATO DEL ADDA 25-VI-A-04 M EXT 200 MAWRUD 25-VI-B-16 M EXT 225 COLGAR ROJA 25-VII-B-10 M EXT 126
151 Resultados y Discusión Nº FIGURA R5 NOMBRE VARIEDAD CÓDIGO PARCELA USO ORIGEN Nº FIGURA R5 226 PERGOLESE 25-VII-B-11 M EXT 251 NOMBRE VARIEDAD APIRENA DI VELLETRI CÓDIGO PARCELA USO ORIGEN Nº FIGURA R5 NOMBRE VARIEDAD CÓDIGO PARCELA USO ORIGEN 25-VIII-B-17 M EXT 276 SANTA MAGDALENA 25-IV-B-10 MV ESP 227 PIZZUTELLO NERO 25-VII-B-12 M EXT 252 SLAVJANKA 25-VIII-B-18 M EXT 277 PLOVDINA 25-V-B-16 MV EXT 228 ALMERIA NERA 25-VII-B-14 M ESP 253 BAYAD 25-VIII-B-19 M EXT 278 PIRIQUITA 25-VI-A-02 MV EXT 229 LOCAL BLACK 25-VII-B-17 M EXT 254 CRIMSON SEEDLESS M EXT 279 TORRALBA 25-VII-A-03 MV ESP 230 EMPEROR 25-VII-B-19 M EXT 255 FLAME SEEDLESS M EXT 280 RUBY CABERNET MV EXT 231 OLIVETTA NERA 25-VII-B-20 M EXT 256 RED GLOBE M EXT 281 COUDERC 3309 PTI EXT 232 DELIGHT 25-VIII-A-01 M EXT 257 SUGRAONE M EXT 282 FERCAL PTI EXT 233 LOOSE PERLETTE 25-VIII-A-03 M EXT 258 RAGOL 22B02 MV ESP 283 PAULSEN 1103 PTI EXT 234 GRAZIELLA I 25-VIII-A-06 M EXT 259 BEBA 22B13 MV ESP 284 RUGGERI 140 PTI EXT 235 SULTANINA 25-VIII-A-07 M EXT 260 FERRAL 22B14 MV ESP 285 CASTEL PTI EXT 236 MARIA PIROVANO 25-VIII-A-08 M EXT 261 MOSCATEL 22B22 MV ESP 286 COUDERC 1616 PTI EXT 237 PIROVANO 166A 25-VIII-A-09 M EXT 262 TORRONTÉS 22B32 MV ESP 287 GOETHE 9 PTI EXT 238 SULTANA MOSCATA 25-VIII-A-10 M EXT 263 ALBARRAZ 22C28 MV ESP 288 HANS V EXT 239 BASILE LOGOTHETIS 25-VIII-A-12 M EXT 264 MALAGUEÑA MOSCATEL 22C34 MV ESP 289 KOBER 5 BB PTI EXT 240 RODI 25-VIII-A-13 M EXT 265 COJONATA 22C43 MV ESP 290 MALEGUE PTI EXT 241 CANNER SEEDLESS 25-VIII-A-14 M EXT 266 MALVASÍA BLANCA 22F02 MV ESP 291 MILLARDET ET GRASSET BRUNI VIII-A-15 M EXT 267 ALBILLO 22I16 MV ESP 292 RICHTER 99 PTI EXT ITALIA X SULTANINA V-6 ITALIA X SULTANINA VI-4 25-VIII-A-16 M EXT 268 BOCALILLA 22J24 MV ESP 293 SCHWARZMANN PTI EXT 25-VIII-A-17 M EXT 269 MOSCATEL 22L53 MV ESP 294 TELEKI 5C PTI EXT 245 BRUNI VIII-A-19 M EXT 270 SEIBEL P22 MV EXT 295 VIALLA PTI EXT 246 SELECCION BRUNI 1 25-VIII-A-20 M EXT 271 FOGONEU FRANCÉS 22E16 MV ESP 296 VITAL V EXT 247 BEAUTY SEEDLESS 25-VIII-B-01 M EXT 272 CALOP NEGRO 22E18 MV ESP 297 GRACIANO 22A05 V ESP 248 BLACK CURRANT 25-VIII-B-03 M EXT 273 MALVASÍA BLANCA 22E54 MV ESP 298 MAZUELO 22A07 V ESP 249 BLACK MONUCCA 25-VIII-B-07 M EXT 274 CHASSELAS DORÉ 25-I-B-03 MV EXT EMERALD SEEDLESS 25-VIII-B-11 M EXT 275 MALVASÍA DE SITGES MOSCATEL GRANO MENUDO PTI EXT 22A18 V ESP 25-II-A-04 MV ESP 300 MORISCA 22A19 V ESP 127
152 Resultados y Discusión Nº FIGURA R5 NOMBRE VARIEDAD CÓDIGO PARCELA USO ORIGEN Nº FIGURA R5 NOMBRE VARIEDAD CÓDIGO PARCELA USO ORIGEN Nº FIGURA R5 NOMBRE VARIEDAD CÓDIGO PARCELA 301 TURRUNTÉS 22A20 V ESP 326 MOLLAR 22C17 V ESP 351 SEÑÁ TINTO 22F48 V ESP 302 MATURANA 22A21 V ESP 327 GARRIDO MACHO 22C18 V ESP 352 DE JOSÉ BLANCO 22F50 V ESP 303 VIURA 22A25 V ESP 328 PALOMINO 22C23 V ESP 353 MOSCATEL BLANCO 22F53 V ESP 304 CALAGRAÑO 22A26 V ESP 329 JAÉN EMPINADILLO 22C30 V ESP 354 VERDEJILLA TINTO 22F55 V ESP 305 MATURANA TINTA 22A27 V ESP 330 GARNACHA BASTA 22D07 V ESP 355 PANSA ROSA 22G19 V ESP 306 RIBOTE 22A31 V ESP 331 MORISTELL 22D08 V ESP 356 PARELLADA II 22G34 V ESP 307 VERUÉS DE HUARTE 22A32 V ESP 332 PANSERA 22D13 V ESP 357 SUMOLL NEGRA 22G50 V ESP 308 BENITILLO 22A33 V ESP 333 ALCAÑON BLANCO 22D15 V ESP 358 PANSA D'ALACANT 22G51 V ESP 309 MORATE 22A34 V ESP 334 SALCEÑO BLANCO 22D22 V ESP 359 ROYAL 22G54 V ESP 310 VERDEJO NEGRO 22A36 V ESP 335 PARREL 22D23 V ESP 360 CUATENDRÁ 22G55 V ESP 311 REDONDAL 22A38 V ESP 336 MIGUEL DE ARCO 22D29 V ESP 361 TROBAT 22H02 V ESP 312 TEMPRANILLO 22A40 V ESP 337 BENEDICTO 22D42 V ESP 362 MORAVIA 22H39 V ESP 313 JAÉN NEGRO 22A45 V ESP 338 MORENILLO 22D43 V ESP 363 GARNACHA TINTORERA USO ORIGEN 22H42 V ESP 314 LISTÁN 22B15 V ESP 339 GARNACHA FRANCESA 22D48 V ESP 364 ALBILLO 22H49 V ESP 315 GARRIDO FINO DE VILLANUEVA 22B16 V ESP 340 TINTORERA DE LONGARES 22D49 V ESP 365 ROJAL BLANCO 22H51 V ESP 316 GABRIELA 22B18 V ESP 341 NEGRA BLASCO 22D56 V ESP 366 FORCALLAT TINTO 22I04 V ESP 317 PALOMINO FINO 22B21 V ESP 342 GARRUT 22D61 V ESP 367 TARDANA 22I06 V ESP 318 PEDRO XIMENEZ 22B31 V ESP 343 NEGRA COMÚN 22F07 V ESP 368 COLORAILLO 22I07 V ESP 319 VIJIRIEGA COMÚN 22B35 V ESP 344 MOSCATEL NEGRA MENUDA 22F19 V ESP 369 MORAVIA AGRIA 22I10 V ESP 320 LAIRÉN 22B37 V ESP 345 ONDARRABI BELTZA 22F23 V ESP 370 LEGIRUELA 22I19 V ESP 321 PLATEADO 22B45 V ESP 346 ONDARRABI ZURI 22F24 V ESP 371 VERDONCHO 22I30 V ESP 322 PERRUNO 22B51 V ESP 347 CARRASQUÍN 22F27 V ESP 372 CHELVA 22I31 V ESP 323 MANTUO 22C09 V ESP 348 ALBARÍN NEGRO 22F29 V ESP 373 ROJAL 22I34 V ESP 324 ROCIA 22C14 V ESP 349 PARDUCA 22F45 V ESP 374 MALVAR 22I37 V ESP 325 PEDRO LUIS 22C15 V ESP 350 GASCÓN 22F47 V ESP 375 AIRÉN 22I42 V ESP 128
153 Resultados y Discusión Nº FIGURA R5 NOMBRE VARIEDAD CÓDIGO PARCELA USO ORIGEN Nº FIGURA R5 NOMBRE VARIEDAD CÓDIGO PARCELA USO ORIGEN Nº FIGURA R5 NOMBRE VARIEDAD CÓDIGO PARCELA 376 GARNACHA 22J17 V ESP 401 ALBILLO REAL 22M35 V ESP 426 VERDOSILLA 22O63 V ESP 377 RAYADA MELONERA 22J25 V ESP 402 MARFAL 22M38 V ESP 427 SEIBEL P11 V EXT 378 GARNACHA 22J34 V ESP 403 ROIBAL 22M39 V ESP BRUJIDERA 22J45 V ESP 404 AGUDELO 22M46 V ESP TINTO NAVALCARNERO 22J50 V ESP 405 MOSCATEL 22M47 V ESP PRIETO PICUDO 22K12 V ESP 406 TREIXADURA 22N02 V ESP PRIETO PICUDO BLANCO 22K13 V ESP 407 ALVARELLO 22N03 V ESP BLANQUILIÑA 22K15 V ESP 408 SOUSÓN 22N06 V ESP 433 SEYVE VILLARD SEYVE VILLARD SEYVE VILLARD SEYVE VILLARD SEYVE VILLARD SEYVE VILLARD USO ORIGEN 22P12 V EXT 22P13 V EXT 22P14 V EXT 22P15 V EXT 22P18 V EXT 22P20 V EXT 384 ALLARÉN 22K19 V ESP 409 FERRÓN 22N08 V ESP 434 BURDIN P21 V EXT 385 PRIETO PICUDO BLANCO 22K20 V ESP 410 DONA BLANCA 22N09 V ESP 435 LANDOT P23 V EXT 386 VERDEJO BLANCO 22K25 V ESP 411 TORRONTÉS 22N14 V ESP 436 MIGUEL DE ARCO 22E02 V ESP 387 BLANCO RECIO 22K36 V ESP 412 LOUREIRO BLANCO 22N15 V ESP 437 CABELIS 22E20 V ESP 388 TINTO ARAGONÉS 22K37 V ESP 413 GODELLO 22N23 V ESP 438 FERNANDELLA 22E22 V ESP 389 VERDEJO BLANCO 22K41 V ESP 414 TORRONTÉS 22N31 V ESP 439 BATISTA 22E23 V ESP 390 RUFETA 22K46 V ESP 415 CAIÑO 22N33 V ESP 440 GORGOLLASA 22E25 V ESP 391 MENCÍA 22K52 V ESP 416 ALBARIÑO 22N34 V ESP 441 CALLET 22E26 V ESP 392 CASTELLANA BLANCA 22K56 V ESP 417 CAGARRIZO 22N39 V ESP 442 EXCURSACH 22E27 V ESP 393 TINTO MADRID 22L18 V ESP 418 CATALÁN BLANCO 22N40 V ESP 443 SINSÓ 22E28 V ESP 394 CLAIRETO 22L28 V ESP 419 NEGRÓN DE ALDÁN 22N45 V ESP 444 MANSÉS DE TIBBUS 22E30 V ESP 395 GARNACHO 22L30 V ESP 420 MONDRAGÓN 22O22 V ESP 445 QUIGAT 22E33 V ESP 396 SALVADOR 22L43 V ESP 421 BOBAL 22O36 V ESP 446 SABATÉ 22E35 V ESP 397 VERDEJO NEGRO 22L52 V ESP 422 FORCALLAT 22O48 V ESP 447 GIRÓ 22E36 V ESP 398 FERNAN PIRIZ 22M12 V ESP 423 MORENILLO 22O52 V ESP 448 EPERÓ DE GALL 22E37 V ESP 399 BORBA 22M19 V ESP 424 PAMPOLAT DE SAGUNTO 22O53 V ESP 449 VINATÉ 22E45 V ESP 400 ALARIJE 22M34 V ESP 425 VERDIL 22O55 V ESP 450 PEDRO XIMENEZ 22E49 V ESP 129
154 Resultados y Discusión Nº FIGURA R5 NOMBRE VARIEDAD CÓDIGO PARCELA USO ORIGEN Nº FIGURA R5 NOMBRE VARIEDAD CÓDIGO PARCELA 451 AGIORGITIKO V EXT 476 PLAVAC MALI V EXT 452 BONARDA V EXT 477 ISABELLA V EXT 453 PINOTAGE V EXT 478 DIMYAT V EXT 454 TANNAT V EXT 479 TINTA BARROCA V EXT 455 KERNER V EXT 480 SILVANER V EXT 456 CABERNET SAUVIGNON USO ORIGEN V EXT 481 FURMINT V EXT 457 FETEASCA REGALA V EXT 482 SEMILLON V EXT 458 RIESLING V EXT 483 MÜLLER-THURGAU V EXT 459 BABIC V EXT 484 RABO DE OVELLA V EXT 460 SAPERAVI V EXT 485 MERLOT V EXT 461 VELTLINER GRUEN V EXT 486 SANGIOVESE V EXT 462 TOCAI FRIULANO V EXT 487 MONTEPULCIANO V EXT 463 UGNI BLANC V EXT 488 GEWÜRZTRAMINER V EXT 464 SAUVIGNON BLANC V EXT 489 CHARDONNAY V EXT 465 MELON V EXT 490 MANCIN V EXT 466 BAGA V EXT 491 MAUZAC V EXT 467 SEYVAL V EXT 492 MAVRODAPHNI V EXT 468 FETEASCA NEAGRA V EXT 493 ROMORANTIN V EXT 469 KRATOSIJA V EXT 494 RONDINELLA V EXT 470 ARVINE PETITE V EXT 495 VELTLINER ROT V EXT 471 MALBEC V EXT 472 PETIT VERDOT V EXT 473 PINOT BLANC V EXT 474 SYRAH V EXT 475 BARBERA V EXT 130
155 Resultados y Discusión Una vez obtenida la estructura de la colección, se estudió la información disponible acerca del uso y el origen de cada una de las variedades que formaban la Colección de genotipos únicos (Tabla R10), para así estudiar si estas características guardaban alguna relación con los agrupamientos detectados con el software Structure. Los resultados obtenidos se resumen en las Tablas R11 y R12. Tabla R11. Uso de las variedades que componen las 4 poblaciones detectadas con el software Structure. (Grupo EHP, corresponde a Especies del Género Vitis no vinifera, Híbridos productores directos y Portainjertos) POBLACIÓN 1 POBLACIÓN 2 POBLACIÓN 3 POBLACIÓN 4 TOTAL MESA 2,94% 39,01% 30,15% 98,69% 261 VINO 11,76% 60,44% 67,46% 1,31% 201 GRUPO EHP 85,30% 0,55% 2,39% 0 33 TOTAL VARIEDADES Tabla R12. Porcentaje de variedades de origen extranjero y español que se recogen en las 4 poblaciones detectadas con el software Structure. VARIEDADES ESPAÑOLAS VARIEDADES EXTRANJERAS POBLACIÓN 1 POBLACIÓN 2 POBLACIÓN 3 POBLACIÓN 4 TOTAL 26,47% 76,37% 31,75% 7,84% ,53% 23,63% 68,25% 92,16% 294 TOTAL VARIEDADES Estudiando en detalle los resultados mostrados en las Tablas R11 y R12 se puede destacar que en la población 1 (representada en rojo en las Figuras R5 y R6), la más pequeña de las 4, más del 85% de las variedades que la forman pertenecen al grupo EHP. En esta población predominan las variedades de origen extranjero alcanzando casi el 74% del total de individuos que la componen. La población 2 (representada en verde en las Figuras R5 y R6), es la que incluye mayor número de individuos, el 60% de las variedades que la componen son de vino y casi el 40% de mesa. Del total de variedades que forman esta población, el 77% de ellas presentan origen español. La siguiente población detectada, fue la denominada población 3 (representada en azul en las Figuras R5 y R6), en la que el 67% de las variedades que la forman son de vino y el 30% de mesa. En esta población, al contrario que en la población 2, el 68% de sus variedades presentan origen extranjero. Finalmente, la población 4 (representada en amarillo en las Figuras R5 y R6) está compuesta por 153 variedades, de las cuales casi el 99% son de mesa. En cuanto a su origen, más del 92% son extranjeras. 131
156 Resultados y Discusión Una vez analizados estos resultados, realmente se puede observar cierta relación en los cuatro agrupamientos con respecto al uso, de forma mayoritaria, y al origen de estas variedades, sobre todo para diferenciar las que componen las poblaciones 2 y 3, respectivamente. Resumiendo, prácticamente la totalidad de las variedades de la población 1 pertenecen al grupo EHP. Este agrupamiento es lógico, debido a que las variedades pertenecientes a este grupo son muy heterogéneas, y en general, presentan origen extranjero. En cuanto a las poblaciones 2 y 3 no existe mucha diferencia en cuanto a los porcentajes presentados en variedades de vino, mesa y grupo EHP, respectivamente, presentando ambas un mayor porcentaje en variedades de vino. Lo que resultó muy interesante fue determinar que del total de variedades que formaban estas 2 poblaciones, el 77 % de las correspondientes a la población 2 presentaban origen español, mientras que casi el 70% de las pertenecientes a la población 3 eran de origen extranjero. Una explicación a esto, podría ser la de que las variedades que componen estas dos poblaciones proceden de diferentes centros de domesticación. Finalmente, en cuanto a la población 4 no cabe duda que sus integrantes casi exclusivos, con un porcentaje casi del 99%, corresponden a variedades de uva de mesa extranjeras. Esto es esperable, debido a que la mayoría de las variedades de uva de mesa presentes en la actualidad son de origen extranjero. Con el fin de determinar el grado de divergencia entre las 4 poblaciones detectadas anteriormente con el software Structure, se realizó un Análisis Molecular de la Varianza (AMOVA) (Tabla R13), y un test de diferenciación con el software Arlequín
157 Resultados y Discusión Tabla R13. Diseño y resultados del Análisis Molecular de la Varianza llevado a cabo con los datos de los 9 loci microsatélite de las 4 poblaciones detectadas en la Colección de genotipos únicos con el software Structure. FUENTE DE VARIACIÓN GRADOS DE LIBERTAD SUMA DE CUADRADOS COMPONENTES DE LA VARIANZA PORCENTAJE DE VARIACIÓN Entre poblaciones 3 178,730 0, ,76 Dentro de poblaciones ,392 3, ,24 Total ,122 3, Índice de Fijación Fst : 0,06757 Se aprecia que el 93,24% de la variación proviene de la variabilidad intrínseca de las variedades dentro de las poblaciones, mientras que, solamente el 6,76% de la variación se debió a la variabilidad en las frecuencias alélicas encontrada entre las poblaciones. Con esto, se puede decir que la variabilidad encontrada entre las poblaciones establecidas con el software Structure no es muy elevada. Además, el valor medio del índice de fijación (Fst) es de 0,07, lo que indica una débil estructuración genética entre las 4 poblaciones. En el mismo sentido, el resultado obtenido con el test exacto de diferenciación realizado entre poblaciones con el software Arlequín, no fue significativo, por lo que se acepta la hipótesis de no diferenciación entre las poblaciones analizadas. Esto es debido a que el software Arlequín no tiene en cuenta la presencia de variedades con elevado grado de mezcla genética. A pesar de que el software Arlequín llega a la conclusión de que, si existe estructura entre las 4 poblaciones detectadas con el software Structure, su significación es muy pequeña, para los análisis posteriores se tendrá en cuenta este agrupamiento, ya que en principio presenta una estructura lógica Análisis matemático de la coincidencia genotípica Se llevó a cabo un análisis matemático en el que se calculó la probabilidad de que, por azar, una planta de vid presente el mismo genotipo para los 9 loci STMS que alguna de las variedades pertenecientes a las poblaciones tomadas como referencia en este estudio. Se calculó el cociente de probabilidades, de 133
158 Resultados y Discusión manera análoga al likelihood ratio (LR) o razón de verosimilitudes utilizado para casos forenses humanos (Carracedo y Barros, 1996). Para realizar el análisis matemático de la coincidencia, se eligieron de la Figura R5, página 122, dos variedades de cada una de las 4 poblaciones detectadas con el software Structure. Estas variedades se encuentran señaladas con una flecha en la citada figura. Una de las dos variedades seleccionadas de cada población presentaba un grado de mezcla genética muy alto, y la otra muy bajo. En total se seleccionaron 8 variedades: Variedades de la población 1 (roja): 12 (con 1,3% de mezcla) y 19 (con 32,5% de mezcla). Variedades de la población 2 (verde): 401 (con 1,7% de mezcla) y 94 (con 23,5% de mezcla). Variedades de la población 3 (azul): 471 (con 2,5% de mezcla) y 460 (con 41,8% de mezcla). Variedades de la población 4 (amarilla): 54 (con 1,4% de mezcla) y 110 (con 40,3% de mezcla). Para cada una de estas variedades, consideradas aquí como muestras problema, se calculó la probabilidad de obtener al azar sus genotipos para los distintos loci microsatélite a partir de sus frecuencias alélicas observadas en la colección global y en las distintas poblaciones detectadas [P(R/NV)], asumiendo que las mismas están en equilibrio de Hardy-Weinberg (EHW). Los test empleados para comprobar la existencia de EHW informan acerca de si la combinación de los distintos alelos para constituir los genotipos de los individuos es casual, pero no acerca de la realidad de la población. Es un hecho que la población de variedades utilizada aquí no es panmíctica, en el sentido de que muchas proceden de cruces diseñados o seleccionados por el hombre. Pero también es fácilmente aceptable que esos cruces no se han llevado a cabo teniendo en cuenta los genotipos de los progenitores para los distintos loci microsatélite, y en ese sentido, para estos loci, si existiría una panmixia. Por ello se puede aceptar en general que, a efectos de esos loci, neutros para la selección artificial, la población esté en EHW. 134
159 Resultados y Discusión En cualquier caso, utilizando el software Arlequín 3.11 (Excoffier et al., 2005), se evaluó el EHW en la Colección de genotipos únicos y en las 4 poblaciones detectadas en ella con el software Structure. Al evaluar el EHW en la Colección de genotipos únicos, se puede decir que la colección en su conjunto no cumple con el EHW en los 9 loci analizados. Este hecho no es de extrañar debido a la gran diversidad del material que compone esta colección, ya que incluye variedades de uva de mesa, de vinificación, portainjertos, híbridos productores directos, especies del género Vitis no vinifera y géneros de la familia Vitáceas. Ese origen diverso hace muy difícil que la composición genotípica se obtenga a partir de la composición alélica de acuerdo al EHW. Al evaluar el EHW en las cuatro poblaciones detectadas con el software Structure, se obtuvo que la población 1 para 5 loci (ZAG67, VVMD27, VVMD5, ZAG62 y ZAG83), y la población 3 para 4 loci (ZAG67, VVMD5, ZAG29 y ZAG62), no estaban en EHW, ya que estaban por debajo del nivel de significación (α = 0,05). Sin embargo, las poblaciones 2 y 4, estaban en EHW para todos los loci. No es de extrañar que en las poblaciones 1 y 3, donde la mayoría de sus variedades presentan origen extranjero, algunos loci no estén en EHW, ya que sobre todo en la población 1, el bajo número de individuos que la componen presentan un origen muy diverso. El hecho de que en la población 4, compuesta en un 99% por variedades de mesa extranjeras, todos sus loci se encuentren en EHW, podría deberse a que en muchos centros de mejora se han utilizado las mismas variedades de mesa para obtener nuevas variedades. Esta población, al estar en EHW para todos sus loci, indica que podría utilizarse como referencia en el análisis matemático para la identificación de variedades de uva de mesa, ya que en la actualidad la mayoría de las variedades que se protegen legalmente presentan este uso. Como se aprecia en los resultados, asumir que los microsatélites están en EHW puede ser erróneo. Es cierto que para algunos análisis, como los que se presentan a continuación, es necesario asumir que los microsatélites están en EHW en cada una de las poblaciones consideradas, pero hay que ser consciente de las limitaciones existentes y de que los valores obtenidos en esos cálculos pueden no ser muy reales. 135
160 Resultados y Discusión A partir de la probabilidad de coincidencia casual [P(R/NV)] de cada una de las muestras problema en las diferentes poblaciones, se calculó la razón de verosimilitud (LR) o poder de discriminar estas variedades seleccionadas, en las distintas poblaciones consideradas. Las Tablas R14 y R15 muestran para cada variedad seleccionada, la LR conjunta para los 9 loci STMS en estudio, en las 5 posibles poblaciones tenidas en cuenta (las cuatro detectadas al analizar la Colección de genotipos únicos con el software Structure y la citada colección sin considerar ningún tipo de estructura). En la Tabla R14 se recogen los resultados obtenidos para las variedades con menor grado de mezcla genética procedente de distintas poblaciones, mientras que la Tabla R15 muestra los resultados obtenidos para las variedades con mayor grado de mezcla genética proveniente de distintas poblaciones. Tabla R14. Razones de verosimilitudes (LR) obtenidas para las variedades con menor grado de mezcla para los 9 loci STMS, en las 5 poblaciones tenidas en cuenta. POBLACIÓN 1 POBLACIÓN 2 POBLACIÓN 3 POBLACIÓN 4 POBLACIÓN 495 ACCESIONES MENOR MEZCLA LR LR LR LR LR 12 4, , , , , , , , , Tabla R15. Razones de verosimilitudes (LR) obtenidas para las variedades con mayor grado de mezcla para los 9 loci STMS, en las 5 poblaciones tenidas en cuenta. POBLACIÓN 1 POBLACIÓN 2 POBLACIÓN 3 POBLACIÓN 4 POBLACIÓN 495 ACCESIONES MAYOR MEZCLA LR LR LR LR LR 19 8, , , , , , , , , , Los valores 0 que aparecen en las Tablas R14 y R15, se deben a que los individuos seleccionados presentan alelos exclusivos no representados en todas las poblaciones tomadas como referencia. 136
161 Resultados y Discusión Con los resultados obtenidos en la Tablas R14 y R15, se puede destacar lo siguiente: 1. Los valores (LR) para el poder de identificar cada una de las 8 variedades seleccionadas, tanto en la población a la que pertenece como en la global, son muy elevados, presentando el más pequeño un valor de 3, La influencia de estructura se manifiesta en que dependiendo de la colección que tomemos como referencia, cada una de ellas presentará unas determinadas frecuencias alélicas para los alelos de los 9 loci en estudio. Teniendo en cuenta esto, si se desconoce a priori a qué población de las 4 puede pertenecer el individuo que queremos identificar, y se compara con una población no adecuada, el valor que se obtendría para la LR sería mayor que si se compara con la población a la que pertenece, por lo que este valor sería erróneo. Por ejemplo, en la Tabla R15, cuando el individuo 94 de la población 2 se compara con esta población, el valor obtenido de LR es menor que si se compara este individuo con las demás poblaciones tomadas como referencia. Esto se debe a que las frecuencias alélicas del individuo 94 son más comunes en la población 2 que en las demás. Lo ideal sería conocer a priori a qué población pertenece la variedad que se quiere identificar, de este modo se estaría comparando con otras variedades con las que compartiría un mayor parentesco genético, y los resultados serían mucho más precisos. Esto en ocasiones puede resultar difícil de conocer, por lo que un análisis conservador sería calcular las LR de la variedad que se quiere identificar en las distintas poblaciones, y seleccionar el valor más bajo. Los resultados obtenidos en el análisis matemático llevado a cabo en este estudio utilizando los 9 loci microsatélites, proporcionan una buena base para la identificación legal, incluida la valoración de las infracciones sobre los derechos de los obtentores. En el trabajo de Ibáñez y Eeuwijk (2003), se partió de una colección de referencia formada por 45 accesiones apirenas distintas, analizadas con 9 loci microsatélite. Incluso eliminando 4 microsatélites del análisis, las probabilidades de 137
162 Resultados y Discusión coincidencia fueron tan bajas que se concluyó que el procedimiento forense utilizando microsatélites era óptimo para la identificación legal, incluida la valoración de las infracciones sobre los derechos de los obtentores. Con los resultados obtenidos tanto con el software Arlequín como con el software Structure, se abre la posibilidad de utilizar como colección de referencia para la identificación de variedades de uva de mesa, la población 4, formada por 153 individuos, de los cuales casi el 99% pertenecen a variedades de uva de mesa extranjeras. Sin embargo, dado que también hay variedades de uva de mesa en las otras poblaciones detectadas en el análisis, lo mejor sería bien utilizar como colección de referencia la Colección de genotipos únicos, o bien utilizarlas todas y elegir aquella donde la LR de la variedad que se quiere identificar presente un valor más bajo. La población 1, debido a que las variedades que la componen son muy heterogéneas, no se utilizaría como colección de referencia Utilidad del sistema de 9 loci microsatélite y de la colección de referencia, para el estudio de Identificación Los 9 loci microsatélite empleados en este estudio han demostrado ser una herramienta muy útil para la identificación molecular de variedades de vid: 1. Únicamente fueron necesarios 5 de los 9 STMS para identificar las 495 variedades que formaban la Colección de genotipos únicos. Al emplear cuatro microsatélites más en los análisis, se estaría incrementando el grado de certeza de la identificación. 2. Tanto la Colección de genotipos únicos, por la gran cantidad y diversidad de individuos que la componen, como las poblaciones de variedades 2, 3 y 4 detectadas al analizar la colección global con el software Structure, resultarían unas colecciones de referencia adecuadas. 3. Los elevados valores obtenidos de LR para poder discriminar las variedades seleccionadas en las distintas colecciones tomadas como referencia, indican que estos resultados se podrían considerar concluyentes en la identificación legal de variedades de vid, incluida la valoración de las infracciones sobre los derechos de los obtentores. 138
163 Resultados y Discusión 4.4. ESTUDIO DE HOMOGENEIDAD Y ESTABILIDAD Para el estudio de Homogeneidad y Estabilidad fueron analizadas aproximadamente plantas pertenecientes a 19 variedades distintas de vid (Tablas M5 - M23 en Materiales y Métodos, páginas 52-70). Para evaluar la homogeneidad se estudiaron 50 plantas de cada variedad de 3 plantaciones distintas. Y, para evaluar la estabilidad se estudiaron 5 plantas de cada variedad de 7 plantaciones adicionales. Se analizaron plantas de la misma variedad con distintos orígenes para estudiar principalmente la estabilidad (mantenimiento de las características esenciales de la variedad a lo largo de distintos ciclos de multiplicación vegetativa). Por ello se comparó material antiguo con cepas más jóvenes de la misma variedad. Además, se dispuso de material de plantaciones con distintas localizaciones, para así poder evaluar si un distinto emplazamiento (clima, suelo etc), influye en la estabilidad de los microsatélites en estudio. Por otro lado, la lejanía geográfica en la plantación probablemente refleja una lejanía temporal en cuanto al número de generaciones de reproducción vegetativa, que en definitiva es lo que se trata de comparar en este estudio. También se dispuso de material con distintas características agronómicas (blancas/tintas; mesa/vinificación, etc.). En el estudio de Homogeneidad (se considerará homogénea la variedad si es suficientemente uniforme en sus caracteres específicos), hubo que estudiar un número elevado de plantas de cada variedad en cuestión para constatar si los genotipos de los microsatélites se mantenían inalterables en todas ellas. Como en el caso de la estabilidad, se estudiaron distintas variedades comerciales con distintas localizaciones geográficas. Las 19 variedades de vid empleadas se encuentran incluidas en el Registro de Variedades Comerciales. De ellas, 14 han demostrado ser homogéneas y estables, ya que se recogen en la inscripción definitiva. Las 5 restantes (Crimson SDL, Napoleón, Ohanes, Red globe y Sugraone), se encuentran todavía en proceso de caracterización. Si los microsatélites utilizados son también homogéneos y estables en dichas variedades, se espera encontrar el mismo genotipo para cada microsatélite en cada una de las plantas que pertenezcan a la misma variedad, independientemente de su origen, lugar de plantación, etc. En caso contrario, habría que determinar dónde se ha producido la mutación, y la frecuencia con que tiene lugar el suceso. 139
164 Resultados y Discusión Evaluación de la selección varietal Hay que tener en cuenta que los resultados obtenidos con una variedad pueden no ser aplicables a otras, por lo que se hizo necesario extender el estudio en un cierto número de variedades (19 en este caso), de manera que resultara representativo de la variabilidad genética existente. Para determinar si la selección de las 19 variedades elegidas para este trabajo era representativa o no, se evaluó si en la Colección de genotipos únicos derivada del estudio de Distinción, los alelos más frecuentes para cada locus microsatélite estaban representados en estas 19 variedades. La Tabla R16 recoge el recuento en valores absolutos de cada uno de los alelos correspondientes a los 9 loci microsatélite que aparecieron en las 495 variedades de la Colección de genotipos únicos, y las frecuencias alélicas por locus para todas las variedades presentes en la misma. En esta tabla aparecen resaltados en amarillo los alelos representados en las 19 variedades de vid que ocupan el estudio de Homogeneidad y Estabilidad. Como se puede observar, los alelos más frecuentes para cada locus microsatélite en las 495 variedades (todos los alelos con frecuencia mayor o igual al 4%), estaban presentes en las 19 variedades elegidas. 140
165 Resultados y Discusión Tabla R16. Alelos detectados en la Colección de genotipos únicos (A), junto con sus frecuencias absolutas (B) y relativas (C). Se destacan en color amarillo los alelos representados en las 19 variedades del estudio de Homogeneidad y Estabilidad. Alelos ZAG67 VVMD27 VVMD5 ZAG29 ZAG62 ZAG112 VVS2 ZAG83 VVMD28 A B C A B C A B C A B C A B C A B C A B C A B C A B C , , , , , , , , , , , , , , , , , , , , , , , , , , , , , , , , , , , , , , , , , , , , , , , , , , , , , , , , , , , , , , , , , , , , , , , , , , , , , , , , , , , , , , , , , , , , , , , , , , , , , , , , , , , , , , , , , , , , , , , , , , , , , , , , , , , , , , , , , , , , , , , , , , , , , , , , , , , , , , , , , , , , , , , , ,10 141
166 Resultados y Discusión En la Tabla R17 se pueden observar las sumas de las frecuencias alélicas por locus que corresponden a los alelos representados en las 19 variedades de vid con respecto al total de alelos que aparecieron en la Colección de genotipos únicos. Tabla R17. Sumas de las frecuencias alélicas por locus que corresponden a los alelos representados en amarillo en la Tabla R16. ZAG67 VVMD27 VVMD5 ZAG29 ZAG62 ZAG112 VVS2 ZAG83 VVMD28 PROMEDIO 86,98% 95,26% 92,12% 94,95% 92,63% 93,04% 90,92% 94,34% 85,95% 91,80% En la Tabla R18 se detalla para cada locus, el porcentaje de alelos presentes en las 19 variedades con respecto al total de alelos presentes en la Colección de genotipos únicos. Tabla R18. Porcentaje de alelos presentes en las 19 variedades con respecto al total de alelos detectados en cada locus. ZAG67 VVMD27 VVMD5 ZAG29 ZAG62 ZAG112 VVS2 ZAG83 VVMD28 PROMEDIO 28,57% 36,36% 36,84% 20,00% 38,88% 43,75% 40,00% 26,66% 34,78% 33,98% Así por ejemplo, los 6 alelos encontrados en las 19 variedades para el locus ZAG67, suponen un 28,57% del total de alelos (21), y la suma de sus frecuencias en los 495 genotipos, es del 86,98%. Como se puede observar en la Tabla R18, el promedio del número de alelos encontrados en las 19 variedades de vid con respecto al total de alelos presentes en la Colección de genotipos únicos, es del 33,98%. Lo más importante, es que de los 169 alelos detectados en la Colección de genotipos únicos, 58 han aparecido representados en el estudio de Homogeneidad y Estabilidad con una frecuencia global casi del 92%. Es decir, que representan la mayoría de alelos existentes en la Colección de genotipos únicos. Aunque en un principio las 19 variedades seleccionadas para el estudio de Homogeneidad y Estabilidad se eligieron con otros criterios (Materiales y Métodos, página 44), este análisis demuestra que resultaron representativas en función de sus frecuencias alélicas, por lo que se puede concluir que la selección de las
167 Resultados y Discusión variedades de vid elegidas para llevar a cabo el estudio de Homogeneidad y Estabilidad ha sido adecuada Muestreo para el estudio de Homogeneidad y Estabilidad El proceso de muestreo se realizó durante los tres años de duración del proyecto VIN C2-1. La obtención de todo el material recolectado resultó complicada. Gran parte del material se recogió personalmente por diferentes miembros del laboratorio de Biología Molecular de la Finca El Encín. Además, se solicitó ayuda de un gran número de Consejos Reguladores de Denominaciones de Origen, así como Centros de Investigación y empresas tanto españolas como extranjeras, que ayudaron, e incluso recolectaron y enviaron material para su estudio. El número final de plantaciones en las cuales se recogió material vegetal fue 229, en 7 países diferentes, recolectándose un total de plantas. Los rangos que se manejaron en cuanto al año de plantación para cada una de las 19 variedades vienen representados en la Tabla R19. Son rangos aproximados porque en muchos casos, los propietarios o encargados de las fincas no conocían este dato con exactitud. Un caso especial lo constituyeron las muestras centenarias de las variedades Garnacha (14 plantas), Napoleón (2 plantas), Monastrell (1 planta) y Thompson SDL (1 planta), las cuales proceden del Real Jardín Botánico de Madrid y cuya fecha de plantación está en torno a
168 Resultados y Discusión Tabla R19. Rangos del año de plantación y los años que comprenden, para las 19 variedades del estudio de Homogeneidad y Estabilidad. VARIEDAD RANGO AÑO PLANTACIÓN AÑOS Airén Cabernet sauvignon Cardinal Chardonnay Crimson SDL Flame SDL Garnacha Italia Merlot Monastrell Moscatel de Málaga Napoleón Ohanes Palomino fino Red globe Sauvignon blanc Sugraone Tempranillo Thompson SDL En cuanto al origen geográfico que presentaron las muestras recogidas, la Tabla R20 presenta el total de fincas muestreadas y la cantidad de plantas recolectadas en cada una de ellas por cada uno de los 7 países donde se muestreó. La gran variabilidad de procedencia existente en cuanto al origen geográfico de las muestras, garantizaba de algún modo que se disponía de un material adecuado para evaluar la estabilidad de los marcadores microsatélites en estudio. Tabla R20. Plantas totales muestreadas por país. PAÍS TOTAL FINCAS PLANTAS MUESTREADAS MUESTREADAS Alemania 4 28 Chile España Francia 8 40 Hungría 5 34 Sudáfrica USA TOTAL
169 Resultados y Discusión Aunque la mayor cantidad de material muestreado procede de España, se trató de diversificar lo máximo posible las zonas de recogida de material dentro del país. Toda la información derivada del estudio de Homogeneidad y Estabilidad se recogió en la base de datos relacional creada en Microsoft Access, citada anteriormente. Las Figuras R7 y R8 recogen dos imágenes obtenidas de la citada base de datos. Concretamente, la Figura R7 muestra la pantalla a través de la cuál se puede acceder a diferentes puntos de interés de la base de datos. Y la Figura R8 muestra una de las 19 pantallas a las que se puede acceder marcando el icono, Ver Muestreo por Variedades de la Figura R7, concretamente se recoge el resumen del muestreo de la variedad Garnacha. En ella se observan los siguientes datos: número de fincas de las que se recogió material (el nombre de las fincas se ha ocultado para mantener su confidencialidad), número de plantas recolectadas en cada finca, recolector, fecha de recolección, año y origen de plantación, pertenencia de las fincas a alguna Denominación de Origen y posibles observaciones. Figura R7. Pantalla de acceso a los diferentes puntos de interés dentro de la base de datos de Access. 145
170 Resultados y Discusión Figura R8. Resumen del muestreo de la variedad Garnacha. 146
171 Resultados y Discusión Errores de muestreo Tras el análisis genético del material vegetal muestreado, se detectó que algunas o todas las plantas recolectadas en alguna finca no se correspondían con la variedad esperada (Tabla R21), ya que diferían en varios microsatélites. Estos errores pueden deberse a los siguientes motivos: Errores en el muestreo Errores en las plantaciones Existencia de homonimias, como es el caso de denominar Garnacha a la Garnacha tintorera, o el de denominar Moscatel, o Moscatel blanco tanto a la variedad Moscatel de Málaga (o de Alejandría) como a la Moscatel de grano menudo (Ibáñez et al., 2006b). En total no se correspondían con la variedad esperada 355 plantas de 4.137, pertenecientes a 20 plantaciones distintas. Representaron casi el 10% del material recolectado. El 95% de las plantas erróneas correspondía a variedades de vinificación, y el 5% restante a variedades de uva de mesa. Dentro de las plantas erróneas detectadas, la mayoría pertenecían a muestras recolectadas en plantaciones españolas. En las Tablas R22 y R23, página 149, se muestra el porcentaje de plantaciones y plantas erróneas de origen español respecto al total de errores, distinguiendo entre variedades de uva de mesa y de vino, así como entre variedades tintas y blancas. De la Tabla R22 se puede destacar que el 90% de las plantaciones que presentaron errores eran españolas. De ellas, el 75% correspondían a variedades de vinificación. Asimismo, en la Tabla R23 se observa que el 98,04% del total de plantas erróneas mostraban origen español. Dentro de ellas, casi el 94% pertenecían a variedades de vinificación. El hecho de que la mayoría de los errores se hayan detectado en variedades de vinificación, puede ser debido a que en general, algunas de las variedades de uva de mesa seleccionadas en este estudio llevan cultivándose durante mucho menos tiempo que las variedades de vinificación, y su cultivo está más controlado, por lo que prácticamente no se han encontrado errores en el material vegetal correspondiente a uva de mesa. 147
172 Resultados y Discusión En cualquier caso más del 90% del material recolectado era correcto y constituía una colección de gran interés para el presente estudio y para otros futuros. Tabla R21. Resumen del muestreo junto con los errores detectados para cada variedad (M: mesa, V: vino, B: blanca, T: tinta). VARIEDAD Nº PLANTACIONES MUESTREADAS Nº PLANTAS MUESTREADAS Nº PLANTACIONES ERRÓNEAS * H E Nº PLANTAS ERRÓNEAS Airén (V/B) (2) 14 Cabernet sauvignon (V/T) Cardinal (M/T) Chardonnay (V/B) Crimson SDL (M/T) Flame SDL (M/T) Garnacha (V/T) Italia (M/B) Merlot (V/T) Monastrell (V/T) (1) (1) 46 Moscatel de (1) 1+(1) 108 Málaga (M-V/B) Napoleón (M/T) Ohanes (M/B) Palomino fino (V/B) (2) Red globe (M/T) (1) 6 Sauvignon blanc (V/B) Sugraone (M/B) Tempranillo (V/T) (1) 2 Thompson SDL (M/B) TOTAL Fincas 355 *H: plantaciones para el estudio de Homogeneidad (muestreadas 52 plantas; analizadas 50) E: plantaciones para el estudio de Estabilidad (muestreadas 7 plantas; analizadas 5) (x) Error sólo en parte de las plantas muestreadas de x plantaciones 148
173 Resultados y Discusión Tabla R22. Errores detectados en plantaciones españolas respecto al total de errores. PLANTACIONES ESPAÑOLAS ERRÓNEAS VINO MESA TOTAL BLANCAS 50% 10% 60% TINTAS 25% 5% 30% TOTAL 75% 15% 90% Tabla R23. Errores detectados en plantas recolectadas en fincas españolas respecto al total de errores. PLANTAS ESPAÑOLAS ERRÓNEAS VINO MESA TOTAL BLANCAS 51,83% 2,82% 54,65% TINTAS 41,70% 1,69% 43,39% TOTAL 93,53% 4,51% 98,04% Evaluación de los datos microsatélite obtenidos Una vez obtenidos los datos microsatélite de las muestras en estudio, se incorporaron a la base de datos citada anteriormente. Así, en ella se recogieron todos los valores obtenidos para los 9 microsatélites en cada una de las variedades elegidas para este estudio. Un ejemplo se muestra en la Figura R9 para la variedad Napoleón. La Tabla R24, página 152, muestra un resumen de los datos microsatélite obtenidos. En ella se detalla para cada una de las 19 variedades en estudio, el número de fincas de las cuales se recolectó material, número de muestras extraídas, amplificadas e incorporadas a la base de datos, y el número de datos recogidos en cada uno de los 9 microsatélites. En esta tabla se puede observar que para todas las variedades se recogió material de al menos 10 plantaciones. Sin embargo, las variedades Flame seedless y Thompson seedless presentan un número de muestras recolectadas inferior al que se había planeado obtener para llevar a cabo el estudio de Homogeneidad y Estabilidad (185). Éstas fueron difíciles de conseguir, ya que su cultivo en España está muy limitado, y no se pudieron obtener más del exterior. Asimismo, se pueden apreciar diferencias entre el número de muestras extraídas, amplificadas e incorporadas a la base de datos, debido a los errores presentados en algunas o todas las plantas muestreadas de varias fincas y que se han detallado previamente en la Tabla R21, página
174 Resultados y Discusión Figura R9. Pantalla de la base de datos de Access, con una pequeña parte de los datos correspondientes a la variedad Napoleón. 150
175 Resultados y Discusión Pese a las limitaciones mencionadas, se consideró que se disponía de datos suficientes para llevar a cabo el estudio de Homogeneidad y Estabilidad. En las Tablas R25 - R43, páginas , se detallan los valores máximos, mínimos, la diferencia entre ellos, promedio y desviación estándar para cada uno de los 9 microsatélites, en cada una de las 19 variedades. Se incluye el análisis conjunto de todos los datos obtenidos para los ADN de todas las plantaciones, tanto para el estudio de Estabilidad como para el de Homogeneidad. Los fragmentos de ADN amplificados tienen, lógicamente, un número entero de nucleótidos. Sin embargo, los valores obtenidos con GeneScan son números reales con dos decimales (Figura R3, página 100, columna Size). Para un mismo alelo se obtiene un rango de valores ligeramente diferentes en GeneScan, que depende tanto del microsatélite como del alelo en cuestión. Así por ejemplo, en la Figura R9, página 150, para el alelo 1 del locus ZAG67 en la variedad Napoleón, se observan los siguientes los valores GeneScan: 129,65; 129,55; 129,68, 129,57, etc. Debido a que los microsatélites utilizados tienen como unidad de repetición 2 nucleótidos, para el análisis se consideró 1 nucleótido como valor umbral de comienzo para comprobar si existe cambio en el tamaño del alelo entre distintas plantas de la misma variedad. En definitiva, se aceptó que todos aquellos valores que diferían en menos de 1 nucleótido correspondían al mismo alelo. Lo más destacable en este estudio de Homogeneidad y Estabilidad es que, contando con un número elevado de datos (unas 185 plantas de cada una de las 19 variedades seleccionadas), casi el 98% de todos los valores alélicos GeneScan obtenidos para los 9 loci microsatélite en las 19 variedades estudiadas, presentaron unas diferencias menores o iguales a 1 nucleótido entre sus valores extremos. No obstante, se presentaron algunas excepciones que se analizaron con especial cuidado y se detallarán a continuación. 151
176 Resultados y Discusión Tabla R24. Resumen de datos de microsatélites. Se detalla el nº de fincas de las cuales se extrajo material, nº de muestras extraídas y amplificadas, nº de muestras incorporadas a la base de datos para cada una de las 19 variedades y nº de datos recogidos en cada uno de los nueve microsatélites para cada una de las variedades en estudio. VARIEDAD Nº FINCAS Nº MUESTRAS EXTRAÍDAS Y AMPLIFICADAS Nº MUESTRAS EN BASE DE DATOS ZAG67 VVMD27 VVMD5 ZAG29 ZAG62 ZAG112 VVS2 ZAG83 VVMD28 Airén Cabernet sauvignon Cardinal Chardonnay Crimson SDL Flame SDL Garnacha Italia Merlot Monastrell Moscatel de Málaga Napoleón Ohanes Palomino fino Red globe Sauvignon blanc Sugraone Tempranillo Thompson SDL TOTAL PROMEDIO 10,84 192,32 173,63 152
177 Resultados y Discusión Tabla R25. Resumen de los datos GeneScan obtenidos para 171 plantas de la variedad Airén. AIRÉN ZAG67 VVMD27 VVMD5 ZAG29 ZAG62 ZAG112 VVS2 ZAG83 VVMD28 VALOR MÁXIMO VALOR MÍNIMO 129,92 147,30 179,03 191,70 222,95 231,46 109, ,21 199,59 227,63 232,45 140,68 142,84 191,89 195,61 232,97 242,82 129,22 146,92 178,62 191,07 222,45 230,76 108, ,41 199,19 227, ,14 142,31 191,38 195,18 232,23 242,07 DIFERENCIA 0,70 0,38 0,41 0,63 0,50 0,70 0,91 0 0,80 0,40 0,47 0,45 0,54 0,53 0,51 0,43 0,74 0,75 PROMEDIO 129,55 147,13 178,84 191,33 222,72 231,01 109, ,88 199,36 227,44 232,24 140,38 142,63 191,67 195,43 232,58 242,41 DESVIACIÓN ESTANDAR 0,1171 0,0828 0,0822 0,0898 0,0905 0,1031 0, ,1096 0,0683 0,0754 0,0794 0,1002 0,0959 0,0730 0,0744 0,1385 0,1226 Tabla R26. Resumen de los datos GeneScan obtenidos para 185 plantas de la variedad Cabernet sauvignon. Se remarcan las diferencias entre los valores extremos de un mismo alelo, superiores a 1 nucleótido. CABERNET SAUVIGNON VALOR MÁXIMO VALOR MÍNIMO ZAG67 VVMD27 VVMD5 ZAG29 ZAG62 ZAG112 VVS2 ZAG83 VVMD28 123,70 137,01 173,15 186,77 228,90 237,15 109, ,16 193,85 227,61 232,47 136,53 149,76 201, ,98 234,96 123,05 136,53 172,16 185,92 227,28 235,41 108, ,24 193,05 227,05 231,91 135,47 148,57 201, ,00 234,03 DIFERENCIA 0,65 0,48 0,99 0,85 1,62 1,74 0,98 0 0,92 0,80 0,56 0,56 1,06 1,19 0,38 0 0,98 0,93 PROMEDIO 123,36 136,72 172,55 186,24 228,17 236,26 108, ,67 193,45 227,37 232,14 135,78 148,96 201, ,45 234,44 DESVIACIÓN ESTANDAR 0,1206 0,1074 0,2490 0,2057 0,4694 0,5282 0, ,2290 0,1753 0,0951 0,1082 0,2134 0,2470 0, ,2467 0,
178 Resultados y Discusión Tabla R27. Resumen de los datos GeneScan obtenidos para 191 plantas de la variedad Cardinal. CARDINAL ZAG67 VVMD27 VVMD5 ZAG29 ZAG62 ZAG112 VVS2 ZAG83 VVMD28 VALOR MÁXIMO VALOR MÍNIMO 123,75 136,97 177,20 183,37 223,16 233,59 109, , ,59 240,36 132, ,97 195,64 242,95 266,66 123,21 136,57 176,49 182,38 222,37 232,76 108, , ,89 239,69 131, ,50 195,14 241,97 265,67 DIFERENCIA 0,54 0,40 0,71 0,99 0,79 0,83 0,88 0 0,99 0 0,70 0,67 0,85 0 0,47 0,50 0,98 0,99 PROMEDIO 123,42 136,71 176,83 182,88 222,74 233,10 109, , ,19 240,06 132, ,70 195,41 242,46 266,15 DESVIACIÓN ESTANDAR 0,0842 0,0564 0,1985 0,2492 0,1983 0,2079 0, , ,1198 0,1161 0, ,1037 0,0830 0,2189 0,2225 Tabla R28. Resumen de los datos GeneScan obtenidos para 185 plantas de la variedad Chardonnay. CHARDONNAY ZAG67 VVMD27 VVMD5 ZAG29 ZAG62 ZAG112 VVS2 ZAG83 VVMD28 VALOR MÁXIMO VALOR MÍNIMO 136,92 150,74 178,94 186,70 231,32 235,26 109, ,12 195,63 238, ,25 140,55 189,85 201,67 216,78 226,83 136,36 150,12 178,37 186,13 230,64 234,68 108, ,49 195,05 237, ,62 139,88 189,49 201,16 216,10 226,06 DIFERENCIA 0,56 0,62 0,57 0,57 0,68 0,58 0,57 0 0,63 0,58 0,51 0 0,63 0,67 0,36 0,51 0,68 0,77 PROMEDIO 136,68 150,49 178,64 186,37 230,92 234,94 108, ,84 195,32 238, ,87 140,17 189,66 201,36 216,40 226,50 DESVIACIÓN ESTANDAR 0,0910 0,0945 0,1055 0,0969 0,1148 0,1152 0, ,1257 0,1051 0, ,1184 0,1180 0,0701 0,0612 0,1314 0,
179 Resultados y Discusión Tabla R29. Resumen de los datos GeneScan obtenidos para 200 plantas de la variedad Crimson SDL. CRIMSON SDL ZAG67 VVMD27 VVMD5 ZAG29 ZAG62 ZAG112 VVS2 ZAG83 VVMD28 VALOR MÁXIMO VALOR MÍNIMO 129,68 136,93 191, ,06 233,19 109, ,20 203,54 232,37 238,32 132,52 149,89 195, ,73 256,51 129,15 136,51 191, ,15 232,31 108, ,58 202,90 231,89 237,69 131,58 148,99 195, ,10 255,88 DIFERENCIA 0,53 0,42 0,77 0 0,91 0,88 0,89 0 0,62 0,64 0,48 0,63 0,94 0,90 0,47 0 0,63 0,63 PROMEDIO 129,38 136,69 191, ,64 232,80 109, ,86 203,19 232,16 238, ,36 195, ,46 256,22 DESVIACIÓN ESTANDAR 0,1025 0,0844 0, ,1306 0,1339 0, ,1191 0,1016 0,0795 0,0848 0,2007 0,2167 0, ,1129 0,1168 Tabla R30. Resumen de los datos GeneScan obtenidos para 112 plantas de la variedad Flame SDL. FLAME SDL ZAG67 VVMD27 VVMD5 ZAG29 ZAG62 ZAG112 VVS2 ZAG83 VVMD28 VALOR MÁXIMO VALOR MÍNIMO 123,63 136,82 179,33 183,24 231,36 233,57 109,48 111,39 188, , ,29 149,77 189, , ,21 136,39 178,57 182,45 230,47 232,70 108,68 110,60 187, , ,69 149,01 189, ,99 0 DIFERENCIA 0,42 0,43 0,76 0,79 0,89 0,87 0,80 0,79 0,71 0 0,55 0 0,60 0,76 0,42 0 0,99 0 PROMEDIO 123,43 136,69 178,98 182,88 231,06 233,23 109,15 111,10 188, , ,07 149,52 189, ,58 0 DESVIACIÓN ESTANDAR 0,0697 0,0686 0,2046 0,1972 0,2066 0,2123 0,1700 0,1776 0, , ,1599 0,2039 0, ,
180 Resultados y Discusión Tabla R31. Resumen de los datos GeneScan obtenidos para 197 plantas de la variedad Garnacha. GARNACHA ZAG67 VVMD27 VVMD5 ZAG29 ZAG62 ZAG112 VVS2 ZAG83 VVMD28 VALOR MÁXIMO VALOR MÍNIMO 129,62 147,23 191, ,28 237,46 109, , , ,46 143,03 189,98 191,97 242, ,06 146,66 190, ,34 236,50 108, , , ,72 142,26 189,28 191,25 242,08 0 DIFERENCIA 0,56 0,57 0,98 0 0,94 0,96 0,94 0 0,94 0 0,71 0 0,74 0,77 0,70 0,72 0,88 0 PROMEDIO 129,36 146,99 191, ,79 236,98 109, , , ,15 142,71 189,71 191,71 242,58 0 DESVIACIÓN ESTANDAR 0,1033 0,0975 0, ,1272 0,1351 0, , , ,1280 0,1331 0,1021 0,0934 0, Tabla R32. Resumen de los datos GeneScan obtenidos para 184 plantas de la variedad Italia. ITALIA ZAG67 VVMD27 VVMD5 ZAG29 ZAG62 ZAG112 VVS2 ZAG83 VVMD28 VALOR MÁXIMO VALOR MÍNIMO 136,98 153,02 177,02 191,84 229,06 235,38 109,56 111,56 192,05 203,71 227,95 245,85 130,28 147,51 190,07 195,97 232,95 242,98 136,46 152,06 176,17 190,88 228,16 234,54 108,64 110,66 191,28 202,89 227,17 244,86 129,42 146,53 189,46 194,99 232,01 242,01 DIFERENCIA 0,52 0,96 0,85 0,96 0,90 0,84 0,92 0,90 0,77 0,82 0,78 0,99 0,86 0,98 0,61 0,98 0,94 0,97 PROMEDIO 136,70 152,67 176,74 191,33 228,58 234,93 109,07 111,10 191,69 203,20 227,47 245,24 129,98 147,14 189,77 195,46 232,55 242,50 DESVIACIÓN ESTANDAR 0,0794 0,1226 0,1230 0,1496 0,2027 0,2062 0,1358 0,1406 0,1517 0,1291 0,1076 0,1313 0,1391 0,1770 0,1097 0,1102 0,1901 0,
181 Resultados y Discusión Tabla R33. Resumen de los datos GeneScan obtenidos para 189 plantas de la variedad Merlot. MERLOT ZAG67 VVMD27 VVMD5 ZAG29 ZAG62 ZAG112 VVS2 ZAG83 VVMD28 VALOR MÁXIMO VALOR MÍNIMO 129,48 136,83 186,81 188,69 222,97 233,34 109, , ,81 240,34 136,37 149,64 195,48 201,41 226,90 232,76 129,05 136,38 186,18 188,09 222,03 232,69 108, , ,12 239,58 135,88 148,97 195,20 201,19 226,12 231,96 DIFERENCIA 0,43 0,45 0,63 0,60 0,94 0,65 0,76 0 0,60 0 0,69 0,76 0,49 0,67 0,28 0,22 0,78 0,80 PROMEDIO 129,27 136,59 186,50 188,42 222,65 232,99 108, , ,39 240,03 136,07 149,29 195,36 201,30 226,52 232,37 DESVIACIÓN ESTANDAR 0,1054 0,1097 0,1280 0,1311 0,1405 0,1391 0, , ,1036 0,1036 0,1259 0,1525 0,0578 0,0510 0,1585 0,1675 Tabla R34. Resumen de los datos GeneScan obtenidos para 131 plantas de la variedad Monastrell. MONASTRELL ZAG67 VVMD27 VVMD5 ZAG29 ZAG62 ZAG112 VVS2 ZAG83 VVMD28 VALOR MÁXIMO VALOR MÍNIMO 136, ,86 186,76 223,05 237,30 109, ,25 203,55 227,67 232,45 130,29 149,77 191,83 201,62 242,90 256,78 136, ,20 186,17 222,31 236,49 108, ,58 202,85 227,17 231,97 129,64 148,97 191,49 201,25 242,04 255,95 DIFERENCIA 0,49 0 0,66 0,59 0,74 0,81 0,78 0 0,67 0,70 0,50 0,48 0,65 0,80 0,34 0,37 0,86 0,83 PROMEDIO 136, ,52 186,49 222,76 236,95 109, ,93 203,32 227,45 232,23 130,02 149,44 191,68 201,37 242,50 256,42 DESVIACIÓN ESTANDAR 0, ,1428 0,1438 0,1705 0,1985 0, ,1620 0,1147 0,1025 0,1089 0,1836 0,2031 0,0803 0,0673 0,2005 0,
182 Resultados y Discusión Tabla R35. Resumen de los datos GeneScan obtenidos para 135 plantas de la variedad Moscatel de Málaga. MOSCATEL DE MÁLAGA VALOR MÁXIMO VALOR MÍNIMO ZAG67 VVMD27 VVMD5 ZAG29 ZAG62 ZAG112 VVS2 ZAG83 VVMD28 123, ,99 191,66 224,92 228,92 109, ,14 203,33 232,32 245,44 130,33 147,33 188, ,61 266,30 123, ,31 190,89 224,24 228,29 108, ,26 202,77 231,91 244,91 129,35 146,59 189, ,97 265,59 DIFERENCIA 0,42 0 0,68 0,77 0,68 0,63 0,80 0 0,88 0,56 0,41 0,53 0,98 0,74 0,56 0 0,64 0,71 PROMEDIO 123, ,63 191,22 224,58 228,58 108, ,63 203,01 232,15 245,12 129,88 146,98 189, , DESVIACIÓN ESTANDAR 0, ,1620 0,1602 0,1455 0,1371 0, ,1982 0,0959 0,0783 0,0714 0,2083 0,2049 0, ,1701 0,1618 Tabla R36. Resumen de los datos GeneScan obtenidos para 192 plantas de la variedad Napoleón. NAPOLEÓN ZAG67 VVMD27 VVMD5 ZAG29 ZAG62 ZAG112 VVS2 ZAG83 VVMD28 VALOR MÁXIMO VALOR MÍNIMO 129,68 136,92 181,42 191,72 231,45 235,56 109, ,58 203,55 227,70 236,45 130,39 132,47 201, ,06 247,16 129,19 136,49 180,44 191,13 230,76 234,82 108, ,73 203,12 227,18 235,87 129,77 131,81 201, ,33 246,32 DIFERENCIA 0,49 0,43 0,98 0,59 0,69 0,74 0,99 0 0,85 0,43 0,52 0,58 0,62 0,66 0,32 0 0,73 0,84 PROMEDIO 129,45 136,73 180,68 191,36 231,11 235,16 109, ,01 203,30 227,46 236,18 130,05 132,09 201, ,69 246,70 DESVIACIÓN ESTANDAR 0,1227 0,1081 0,1208 0,1141 0,1289 0,1325 0, ,1272 0,0892 0,0836 0,0847 0,1404 0,1396 0, ,1421 0,
183 Resultados y Discusión Tabla R37. Resumen de los datos GeneScan obtenidos para 188 plantas de la variedad Ohanes. OHANES ZAG67 VVMD27 VVMD5 ZAG29 ZAG62 ZAG112 VVS2 ZAG83 VVMD28 VALOR MÁXIMO VALOR MÍNIMO 129,63 136,90 180,97 191,62 231,20 233,21 109, ,49 203,35 236,28 238,23 130,16 134,28 189,93 201,33 242,73 246,97 129,24 136,63 180,19 190,86 230,66 232,73 108, ,06 202,74 235,88 237,88 129,44 133,60 189,37 200,80 242,03 246,07 DIFERENCIA 0,39 0,27 0,78 0,76 0,54 0,48 0,73 0 0,43 0,61 0,40 0,35 0,72 0,68 0,56 0,53 0,70 0,90 PROMEDIO 129,44 136,75 180,64 191,30 230,92 232, ,31 203,04 236,10 238,05 129,94 134,03 189,60 201,12 242,44 246,48 DESVIACIÓN ESTANDAR 0,0822 0,0564 0,2082 0,2065 0,1125 0,1086 0, ,0843 0,0921 0,0726 0,0660 0,1366 0,1317 0,0967 0,0666 0,1254 0,1206 Tabla R38. Resumen de los datos GeneScan obtenidos para 176 plantas de la variedad Palomino fino. PALOMINO FINO VALOR MÁXIMO VALOR MÍNIMO ZAG67 VVMD27 VVMD5 ZAG29 ZAG62 ZAG112 VVS2 ZAG83 VVMD28 129,91 149,49 183,18 191,80 225,16 237,40 109, ,25 193,91 227,98 232,86 130,38 143,06 191,85 195,57 234, , ,31 190,94 224,32 236,44 108, ,62 193,38 227,22 231,98 129,56 142,27 191,47 195,26 234,18 246,01 DIFERENCIA 0,83 0,49 0,87 0,86 0,84 0,96 0,78 0 0,63 0,53 0,76 0,88 0,82 0,79 0,38 0,31 0,64 0,99 PROMEDIO 129,39 149,22 182,64 191,19 224,62 236,83 108, ,83 193,57 227,40 232,17 129,86 142,50 191,61 195,37 234,40 246,49 DESVIACIÓN ESTANDAR 0,1227 0,0990 0,1430 0,1391 0,1367 0,1503 0, ,1139 0,0936 0,1130 0,1199 0,1544 0,1571 0,0648 0,0628 0,1174 0,
184 Resultados y Discusión Tabla R39. Resumen de los datos GeneScan obtenidos para 181 plantas de la variedad Red globe. Se remarcan las diferencias entre los valores extremos de un mismo alelo, superiores a 1 nucleótido. RED GLOBE ZAG67 VVMD27 VVMD5 ZAG29 ZAG62 ZAG112 VVS2 ZAG83 VVMD28 VALOR MÁXIMO 136,90 149,56 179, ,87 236,20 109, ,47 188,56 228,10 232,89 132,62 150,19 192,01 201,46 257,42 0 VALOR MÍNIMO 136,12 149,12 178, ,62 234,80 108, ,50 187,61 227,28 232,06 131,74 149,12 191, ,07 0 DIFERENCIA 0,78 0,44 0,99 0 1,25 1,40 0,99 0 0,97 0,95 0,82 0,83 0,88 1,07 0,69 0,46 1,35 0 PROMEDIO 136,71 149,25 178, ,28 235,50 109, ,99 188,11 227,60 232,38 132,21 149,62 191,75 201,19 256,62 0 DESVIACIÓN ESTANDAR 0,0749 0,0603 0, ,2660 0,2897 0, ,2239 0,2131 0,1906 0,1918 0,1856 0,2562 0,1180 0,0947 0, Tabla R40. Resumen de los datos GeneScan obtenidos para 182 plantas de la variedad Sauvignon blanc. SAUVIGNON BLANC VALOR MÁXIMO VALOR MÍNIMO ZAG67 VVMD27 VVMD5 ZAG29 ZAG62 ZAG112 VVS2 ZAG83 VVMD28 123,61 147,27 173,17 186,76 225,16 229,19 109,60 113,39 188,26 193,96 232,55 238,45 130,45 149,89 191,86 201,49 233,03 235,16 123,07 146,86 172,43 186,12 224,33 228,39 108,62 112,64 187,63 193,38 231,99 237,84 129,64 148,98 191,45 201,17 232,15 234,20 DIFERENCIA 0,54 0,41 0,74 0,64 0,83 0,80 0,98 0,75 0,63 0,58 0,56 0,61 0,81 0,91 0,41 0,32 0,88 0,96 PROMEDIO 123,45 147,10 172,80 186,46 224,68 228,70 109,06 112,98 187,88 193,62 232,20 238, ,37 191,64 201,34 232,51 234,59 DESVIACIÓN ESTANDAR 0,0834 0,0681 0,1655 0,1275 0,1642 0,1638 0,1803 0,1763 0,1206 0,1122 0,1118 0,1225 0,1800 0,1853 0,0706 0,0536 0,1888 0,
185 Resultados y Discusión Tabla R41. Resumen de los datos GeneScan obtenidos para 185 plantas de la variedad Sugraone. SUGRAONE ZAG67 VVMD27 VVMD5 ZAG29 ZAG62 ZAG112 VVS2 ZAG83 VVMD28 VALOR MÁXIMO VALOR MÍNIMO 123,71 136,97 176,92 178,98 222,95 232,93 109,41 111,37 185,93 188,05 232, , ,80 195,48 246, ,41 136,67 176,45 178,47 222,48 232,03 108,74 110,76 185,45 187,55 232, , ,39 195,20 245,90 0 DIFERENCIA 0,30 0,30 0,47 0,51 0,47 0,90 0,67 0,61 0,48 0,50 0,82 0 0,46 0 0,41 0,28 0,96 0 PROMEDIO 123,55 136,81 176,69 178,77 222,68 232,74 109,09 111,04 185,69 187,81 232, , ,59 195,33 246,45 0 DESVIACIÓN ESTANDAR 0,0664 0,0632 0,0940 0,1154 0,0800 0,1813 0,1438 0,1369 0,1093 0,1149 0, , ,0720 0,0518 0, Tabla R42. Resumen de los datos GeneScan obtenidos para 183 plantas de la variedad Tempranillo. TEMPRANILLO ZAG67 VVMD27 VVMD5 ZAG29 ZAG62 ZAG112 VVS2 ZAG83 VVMD28 VALOR MÁXIMO VALOR MÍNIMO 123,73 147,29 180, , , ,52 199,48 227,55 236,40 140,69 142,84 195, , ,09 146,76 180, , , ,80 199,01 227,16 235,87 139,80 142,07 195, ,83 0 DIFERENCIA 0,64 0,53 0,59 0 0,84 0 0,98 0 0,72 0,47 0,39 0,53 0,89 0,77 0,33 0 0,75 0 PROMEDIO 123,42 147,02 180, , , ,18 199,26 227,38 236,12 140,19 142,41 195, ,14 0 DESVIACIÓN ESTANDAR 0,1235 0,0985 0, , , ,2117 0,1051 0,0745 0,0847 0,1997 0,1977 0, ,
186 Resultados y Discusión Tabla R43. Resumen de los datos GeneScan obtenidos para 132 plantas de la variedad Thompson SDL. Se remarca la diferencia entre los valores extremos del alelo 1 del locus VVMD28, el cual presentó un valor superior a 1 nucleótido. THOMPSON SDL VALOR MÁXIMO VALOR MÍNIMO ZAG67 VVMD27 VVMD5 ZAG29 ZAG62 ZAG112 VVS2 ZAG83 VVMD28 123,72 136,94 179,30 191,74 231, ,54 111,49 188, ,78 259,79 143, ,96 195,63 217,49 243,02 123,17 136,43 178,36 190,90 230, ,74 110,73 187, ,10 258,90 142, ,36 195,08 216,38 242,05 DIFERENCIA 0,55 0,51 0,94 0,84 0,98 0 0,80 0,76 0,98 0 0,68 0,89 0,89 1,00 0,60 0,55 1,11 0,97 PROMEDIO 123,48 136,76 178,86 191,32 231, ,15 111,10 187, ,47 259,26 142,76 149,50 189,71 195,42 216,95 242,55 DESVIACIÓN ESTANDAR 0,1638 0,1086 0,2606 0,2334 0, ,2292 0,2339 0, ,1647 0,1608 0,2624 0,2936 0,1462 0,1165 0,3084 0,
187 Resultados y Discusión Análisis de las diferencias superiores a 1 nucleótido En las muestras analizadas en este estudio con los 9 loci microsatélite, las únicas diferencias mayores de 1 nucleótido para un alelo, se detectaron en las variedades: Cabernet sauvignon, Red globe y Thompson SDL; Tablas R44, R45 y R46, respectivamente. Tabla R44. Diferencias superiores a 1 nucleótido detectadas en la variedad Cabernet sauvignon. CABERNET SAUVIGNON VVMD5 VVMD5 VVS2 VVS2 Alelo 1 Valor Diferencia Máximo 228,90 1,62 Mínimo 227,28 Alelo 2 Valor Diferencia Máximo 237,15 1,74 Mínimo 235,41 Alelo 1 Valor Diferencia Máximo 136,53 1,06 Mínimo 135,47 Alelo 2 Valor Diferencia Máximo 149,76 1,19 Mínimo 148,57 Tabla R45. Diferencias superiores a 1 nucleótido detectadas en la variedad Red globe. RED GLOBE VVMD5 VVMD5 VVS2 VVMD28 Alelo 1 Valor Diferencia Máximo 233,87 1,25 Mínimo 232,62 Alelo 2 Valor Diferencia Máximo 236,20 1,40 Mínimo 234,80 Alelo 2 Valor Diferencia Máximo 150,19 1,07 Mínimo 149,12 Alelo 1 Valor Diferencia Máximo 257,42 1,35 Mínimo 256,07 163
188 Resultados y Discusión Tabla R46. Diferencias superiores a 1 nucleótido detectadas en la variedad Thompson SDL. THOMPSON SDL VVMD5 Alelo 1 Valor Diferencia Máximo 217,49 1,11 Mínimo 216,38 Estas diferencias entre valores máximos y mínimos podrían deberse a diferentes motivos: 1. A una mutación, es decir, se trataría de nuevos alelos. 2. A un artefacto técnico: 2.1 A un artefacto producido durante la PCR. Por ejemplo, la aparición de picos +A citados anteriormente, y no resueltos convenientemente en el análisis. Estos picos se producen por la actividad Nucleotidil Terminal Transferasa que posee la Taq polimerasa utilizada, que añade al final del fragmento de ADN amplificado una Adenina. El programa de PCR utilizado se diseñó para favorecer esta actividad (ciclo final de una hora a 72ºC), con el fin de que todos los fragmentos detectados tuvieran el nucleótido añadido. Sin embargo, la actividad no siempre tiene un comportamiento reproducible y en ocasiones se presentaron problemas de este tipo. 2.2 A un artefacto producido durante la electroforesis, incluyendo falta de resolución del analizador genético. Normalmente, se obtienen valores ligeramente diferentes en un mismo alelo, pero podía ocurrir que las diferencias fueran algo mayores. En Grando y Frisinghelli (1998), se utilizó el secuenciador ABI PRISM 310 para el genotipado de variedades de vid con algunos microsatélites de los empleados en este estudio y los mismos fluorocromos. Observaron que para datos obtenidos con el mismo capilar las desviaciones estándar encontradas eran menores de 0,2 pb, mientras que algunas veces, utilizando distintos capilares, llegaron a apreciar diferencias de hasta 1 pb. 164
189 Resultados y Discusión En este contexto (homogeneidad y estabilidad) resultaba fundamental esclarecer si las diferencias encontradas eran debidas a una mutación o a un artefacto técnico, pues esto podía afectar a las conclusiones finales sobre homogeneidad y estabilidad de los microsatélites/variedades. Por ello, estas diferencias se estudiaron al detalle y de forma individual en cada una de las tres variedades citadas. Para ello, se seleccionaron los ADN de las muestras a las que pertenecían los valores extremos de cada uno de los alelos correspondientes a los loci representados en las Tablas R44, R45 y R46, y se repitieron las PCR de forma individual para cada uno de ellos. En todos los casos se repitieron las PCR utilizando la misma enzima con la que se llevó a cabo todo el estudio, empleando además en el caso de Cabernet sauvignon otra polimerasa distinta, Pyrobest DNA polimerasa (Takara), utilizando un programa de PCR específico para ella (Tabla R47). La enzima Pyrobest DNA polimerasa (Takara) posee actividad exonucleasa 3 5, es decir, correctora de pruebas, y no presenta la Nucleotidil Terminal Transferasa, por lo que su fidelidad es mayor y no añade +A. Tabla R47. Programa de PCR para la enzima Pyrobest DNA polimerasa. A continuación se detallan los resultados obtenidos tras el estudio minucioso de las diferencias superiores a 1 nucleótido encontradas en Cabernet sauvignon, Red globe y Thompson seedless. Cabernet sauvignon Nº CICLOS TEMPERATURA TIEMPO 1 94ºC 5 min 94ºC 10 seg 30 59ºC 30 seg 72ºC 1 min 1 4ºC ilimitado En esta variedad se detectaron las mayores diferencias entre los valores máximo y mínimo (Tabla R44, página 163), para los dos alelos correspondientes a los microsatélites VVMD5 y VVS2. Los perfiles electroforéticos y los resultados obtenidos al repetir la reacción de amplificación nuevamente con la Taq polimerasa y con la Pyrobest DNA polimerasa (Takara) se muestran, para el locus VVMD5, en la Figura R10 y en la Tabla R48, respectivamente; y para el locus VVS2, en la Figura R11 y en la Tabla R49, respectivamente. 165
190 Resultados y Discusión VVMD5- Cabernet sauvignon Figura R10. Gráficos GeneScan obtenidos para el locus VVMD5 amplificado con Taq polimerasa (1ª y 2ª amplificación, en las dos ventanas superiores), y Pyrobest DNA polimerasa (ventana inferior). Sombreados los valores correspondientes al alelo 1.. Tabla R48. Resultados obtenidos para el locus VVMD5 con las enzimas Taq polimerasa (1ª y 2ª amplificación), y Pyrobest DNA polimerasa. Los valores remarcados son los representados en la Figura R10. TAQ POLIMERASA TAQ POLIMERASA PYROBEST DNA VVMD5 1ª AMPLIFICACIÓN 2ª AMPLIFICACIÓN POLIMERASA Alelo 1 Valor Diferencia Valor Diferencia Valor Diferencia Máximo 228,90 228,56 227,61 1,62 0,01 0,02 Mínimo 227,28 228,57 227,63 Alelo 2 Valor Diferencia Valor Diferencia Valor Diferencia Máximo 237,15 236,78 235,85 1,74 0,04 0,03 Mínimo 235,41 236,82 235,88 166
191 Resultados y Discusión VVS2- Cabernet sauvignon Figura R11. Gráficos GeneScan obtenidos para el locus VVS2 amplificado con Taq polimerasa (1ª y 2ª amplificación, en las dos ventanas superiores), y Pyrobest DNA polimerasa (ventana inferior). Sombreados los valores correspondientes al alelo 2. Tabla R49. Resultados obtenidos para el locus VVS2 con las enzimas Taq polimerasa (1ª y 2ª amplificación), y Pyrobest DNA polimerasa. Los valores remarcados son los representados en la Figura R11. TAQ POLIMERASA TAQ POLIMERASA PYROBEST DNA VVS2 1ª AMPLIFICACIÓN 2ª AMPLIFICACIÓN POLIMERASA Alelo 1 Valor Diferencia Valor Diferencia Valor Diferencia Máximo 136,53 135,73 134,75 1,06 0,09 0,01 Mínimo 135,47 135,64 134,76 Alelo 2 Valor Diferencia Valor Diferencia Valor Diferencia Máximo 149,76 148,98 147,81 1,19 0,15 0,14 Mínimo 148,57 149,13 147,95 167
192 Resultados y Discusión Se puede observar que las diferencias apreciadas entre las muestras a las que pertenecían los valores extremos del alelo 1 del locus VVMD5 (Figura R10, y Tabla R48), y del alelo 2 del locus VVS2 (Figura R11 y Tabla R49), eran mucho menores, despreciables a los efectos de considerar si eran el mismo alelo o no. Los valores representados gráficamente han sido los correspondientes al alelo 1 del locus VVMD5, y al alelo 2 del locus VVS2; el alelo 2 del locus VVMD5, y el alelo 1 del locus VVS2 presentaron un perfil electroforético análogo. Los valores obtenidos tras la amplificación con la Pyrobest DNA polimerasa corresponden a alelos sin efecto +A, y los obtenidos tras la 2ª amplificación con la Taq polimerasa pertenecen a alelos con efecto +A, ya que entre estos valores se observa una diferencia de aproximadamente 1 nucleótido. Teniendo en cuenta esto, se puede obtener información acerca de la causa de las diferencias superiores a 1 nucleótido entre los valores máximos y mínimos detectadas en los loci VVMD5 y VVS2, en la 1ª amplificación con la Taq polimerasa. En la Tabla R48, para los dos alelos del locus VVMD5 obtenidos tras la 1ª amplificación con la Taq polimerasa, se observa que los valores máximos muestran un efecto +A, mientras que los valores mínimos no muestran ese efecto +A. Según estos datos, se puede intuir que las diferencias apreciadas en el locus VVMD5 se debían probablemente a la presencia/ausencia del efecto +A. En lo que respecta a la Tabla R49, para los dos alelos del locus VVS2 obtenidos tras la 1ª amplificación con la Taq polimerasa, se observa que los valores mínimos muestran un valor 1 nucleótido superior al obtenido con la Pyrobest DNA polimerasa, y coinciden con los valores obtenidos tras la 2ª amplificación con la Taq polimerasa. En cambio, los valores máximos presentan 1 nucleótido adicional a los valores obtenidos tras la 2ª amplificación con la Taq polimerasa. Con ello, se puede intuir que las diferencias apreciadas en el locus VVS2 podrían deberse a una falta de resolución durante la electroforesis en el ABI PRISM 310. Otra manera de analizarlo se muestra en la Figura R12, donde se representan gráficamente las frecuencias absolutas obtenidas para los valores detectados para el alelo 2 del locus VVMD5 y para el alelo 2 del locus VVS2. Los valores correspondientes a los alelos 1 de los loci VVMD5 y VVS2, no se han representado debido a que presentan un perfil muy similar al de sus respectivas parejas alélicas. Se observa que los distintos valores del alelo 2 del locus VVMD5 168
193 Resultados y Discusión obtenidos en el total de muestras analizadas, aparecen repartidos en dos distribuciones con forma de campana (o distribuciones normales), lo que indica que estos datos estarían agrupados en dos bloques diferentes. Los dos valores medios de cada distribución presentan prácticamente 1 nucleótido de diferencia entre ellos, lo que sugiere que un grupo de valores obtenidos para el alelo 2 del locus VVMD5 presentaron el efecto +A, mientras que otro grupo no lo presentó. En cambio, la representación gráfica obtenida para los valores del alelo 2 del locus VVS2 es totalmente distinta a la anterior, parece indicar que de haber ocurrido la presencia/ausencia del efecto +A, únicamente habría afectado a los valores extremos (149,8), aunque también falte resolución en esas electroforesis. VVMD ,4 235,5 235,6 235,7 235,8 235, ,1 236,2 236,3 236,4 236,5 236,6 236,7 236,8 236, ,1 237,2 VVS ,6 148,7 148,8 148, ,1 149,2 149,3 149,4 149,5 149,6 149,7 149,8 Figura R12. Representación gráfica de las frecuencias absolutas obtenidas para los valores observados para el alelo 2 del locus VVMD5 (ventana superior), y para el alelo 2 del locus VVS2 (ventana inferior). 169
194 Resultados y Discusión En base a los gráficos de la Figura R12, y a los resultados obtenidos después de amplificar individualmente los ADN de las muestras a las que pertenecían los valores extremos, se puede llegar a la conclusión de que las diferencias apreciadas en el locus VVMD5 se debían probablemente a la presencia/ausencia del efecto +A, mientras que las apreciadas en el locus VVS2 no nos permite diferenciar si realmente se debe a la presencia/ausencia del efecto +A o a un artefacto técnico originado durante la electroforesis en el ABI PRISM 310. Lo que sí parece claro es que no había ocurrido mutación alguna en los alelos de estos loci para estas muestras de Cabernet sauvignon. Obviamente, de aquí se podría deducir la conveniencia de utilizar una enzima como la Pyrobest DNA polimerasa para todo el proyecto. Sin embargo, ello lo hubiera encarecido notablemente, en tiempo y dinero, ya que su coste era mucho mayor, y resultaba muy complicado optimizar una PCR múltiple. Red globe En esta variedad se detectaron diferencias superiores a 1 nucleótido entre los valores máximo y mínimo, en tres loci: VVMD5 (en los 2 alelos), VVS2 (en 1 alelo) y VVMD28 (en 1 alelo), Tabla R45, página 163. Debido a que los resultados obtenidos en Cabernet sauvignon con la enzima Pyrobest DNA polimerasa (Takara) hicieron llegar a la misma conclusión que cuando se realizó una segunda amplificación con la Taq polimerasa utilizada durante todo el proyecto, no se consideró necesario en este caso la repetición de la amplificación con esta segunda enzima. Los resultados obtenidos con la enzima Taq polimerasa (1ª y 2ª amplificación), se muestran en Tabla R50. En ella se puede observar que aquellas diferencias apreciadas en la 1ª amplificación entre las muestras a las que pertenecían los valores extremos obtenidos para los alelos 1 y 2 del locus VVMD5, el alelo 2 del locus VVS2 y el alelo 1 del locus VVMD28, eran mucho menores en la repetición, despreciables a los efectos de considerar si eran el mismo alelo o no. Considerando que los valores obtenidos en la 2ª amplificación con la Taq polimerasa corresponderían a alelos con efecto +A (ver Cabernet sauvignon), se observa que los valores mínimos muestran ese efecto +A. Por el contrario, los valores máximos presentan 1 nucleótido adicional a los valores obtenidos tras la 2ª 170
195 Resultados y Discusión amplificación con la Taq polimerasa. Según estos datos se puede intuir que las diferencias apreciadas en los loci VVMD5, VVS2 y VVMD28, se debían probablemente a una falta de resolución durante la electroforesis en el ABI PRISM 310. Tabla R50. Resultados obtenidos para los loci VVMD5 (alelos 1 y 2), VVS2 (alelo 2) y VVMD28 (alelo 1) con la enzima Taq polimerasa (1ª y 2ª amplificación). LOCI VVMD5 VVMD5 VVS2 VVMD28 TAQ POLIMERASA TAQ POLIMERASA ALELOS 1ª AMPLIFICACIÓN 2ª AMPLIFICACIÓN Alelo 1 Valor Diferencia Valor Diferencia Máximo 233,87 232,75 1,25 0,15 Mínimo 232,62 232,60 Alelo 2 Valor Diferencia Valor Diferencia Máximo 236,20 234,89 1,40 0,08 Mínimo 234,80 234,81 Alelo 2 Valor Diferencia Valor Diferencia Máximo 150,19 149,12 1,07 0,17 Mínimo 149,12 148,95 Alelo 1 Valor Diferencia Valor Diferencia Máximo 257,42 256,19 1,35 0,13 Mínimo 256,07 256,06 En la Figura R13 se muestra una representación gráfica de las frecuencias absolutas obtenidas para los valores detectados para los alelos 1 y 2 del locus VVMD5, para el alelo 2 del locus VVS2 y, para el alelo 1 del locus VVMD28, respectivamente. Se observa que la distribución de los valores alélicos obtenidos en el total de muestras analizadas para esos loci, responde a una distribución prácticamente normal, aunque no nos permite diferenciar si realmente las diferencias superiores a 1 nucleótido entre los valores máximo y mínimo encontradas en estos tres loci se deben realmente a la presencia/ausencia del efecto +A o a un artefacto técnico originado durante la electroforesis en el ABI PRISM
196 Resultados y Discusión VVMD5-1 VVMD ,6 232,7 232,8 232, ,1 233,2 233,3 233,4 233,5 233,6 233,7 233,8 233, ,8 234, ,1 235,2 235,3 235,4 235,5 235,6 235,7 235,8 235, ,1 236,2 VVS2-2 VVMD ,1 149,2 149,3 149,4 149,5 149,6 149,7 149,8 149, ,1 150, ,1 256,2 256,3 256,4 256,5 256,6 256,7 256,8 256, ,1 257,2 257,3 257,4 Figura R13. Representación gráfica de las frecuencias absolutas obtenidas para los valores detectados para los alelos 1 y 2 del locus VVMD5 (2 ventanas superiores), para el alelo 2 del locus VVS2 (ventana inferior izquierda), y para el alelo 1 del locus VVMD28 (ventana inferior derecha). En base a los gráficos de la Figura R13, y a los resultados obtenidos después de amplificar individualmente los ADN de las muestras a las que pertenecían los valores extremos, se puede llegar a la conclusión de que las diferencias apreciadas en estos tres loci pueden deberse, bien a la presencia/ausencia del efecto +A, bien a un artefacto técnico originado durante la electroforesis en el ABI PRISM 310. Lo que si parece claro es que no había ocurrido mutación alguna en los alelos de estos loci para estas muestras de Red globe. Thompson seedless En esta variedad únicamente se detectaron diferencias superiores a 1 nucleótido entre los valores máximo y mínimo, en el alelo 1 del locus VVMD28. Tabla R46, página
197 Resultados y Discusión Para tratar de averiguar la causa de la variación, se procedió de igual forma que en los casos descritos anteriormente para las variedades Cabernet sauvignon y Red globe. Los resultados obtenidos para el locus VVMD28 con la enzima Taq polimerasa (1ª y 2ª amplificación) se resumen en la Tabla R51. Se observa que las diferencias, cuando se amplificaron nuevamente con la Taq polimerasa, eran despreciables a los efectos de considerar si eran el mismo alelo o no. Al igual que en Cabernet sauvignon para el locus VVS2, y en Red globe para los loci VVMD5, VVS2 y VVMD28, el valor mínimo presenta el efecto +A. Por el contrario, el valor máximo presenta un valor 1 nucleótido superior al valor obtenido tras la 2ª amplificación con la Taq polimerasa. Como en los casos anteriores, se puede intuir que las diferencias apreciadas en el alelo 1 del locus VVMD28, podrían ser debidas a una falta de resolución durante la electroforesis en el ABI PRISM 310. Tabla R51. Resultados obtenidos para el alelo 1 del locus VVMD28 con la enzima Taq polimerasa (1ª y 2ª amplificación). TAQ POLIMERASA TAQ POLIMERASA VVMD28 1ª AMPLIFICACIÓN 2ª AMPLIFICACIÓN Alelo 1 Valor Diferencia Valor Diferencia Máximo 217,49 216,45 1,11 0,12 Mínimo 216,38 216,33 En la Figura R14 se muestra una representación gráfica de las frecuencias absolutas obtenidas para los valores detectados para el alelo 1 del locus VVMD28. Se observa que la distribución de los valores alélicos obtenidos en el total de muestras analizadas para ese locus responde a una distribución distinta de la normal, que no permite diferenciar si realmente las diferencias superiores a 1 nucleótido entre los valores máximo y mínimo encontradas en este locus se deben realmente a la presencia/ausencia del efecto +A o a un artefacto técnico originado durante la electroforesis en el ABI PRISM
198 Resultados y Discusión VVMD ,4 216,5 216,6 216,7 216,8 216, ,1 217,2 217,3 217,4 217,5 Figura R14. Representación gráfica de las frecuencias absolutas obtenidas para los valores detectados para el alelo 1 del locus VVMD28. En base al gráfico de la Figura R14, y a los resultados obtenidos después de amplificar individualmente los ADN de las muestras a las que pertenecían los valores extremos, se puede llegar a la conclusión de que las diferencias apreciadas se debían a la presencia/ausencia del efecto +A, o a un artefacto técnico originado durante la electroforesis en el ABI PRISM 310, y no a que hubiera ocurrido alguna mutación en el alelo 1 del locus VVMD28 para estas muestras de Thompson seedless. En resumen, se ha podido demostrar que las diferencias por encima de 1 nucleótido que aparecieron entre valores GeneScan en las tres variedades detalladas anteriormente (Cabernet sauvignon, Red globe y Thompson seedless), no correspondían a diferencias en el genotipo causadas por alguna mutación en los alelos de estas muestras, sino que se debían a variaciones provocadas por un artefacto técnico producido durante la PCR o durante la electroforesis en el ABI PRISM
199 Resultados y Discusión De cualquier modo conviene puntualizar: 1. Las diferencias encontradas en la práctica totalidad de los casos están muy cerca de 1 nucleótido y no habrían ocasionado una categorización errónea de los genotipos en cuestión. 2. Dichas variaciones afectaron a muy pocas muestras. 3. Las dudas planteadas son fácilmente subsanables llevando a cabo una repetición del proceso completo de genotipado con la misma enzima. En el estudio mostrado se han analizado las diferencias entre valores para alelos dentro de cada variedad. Existían alelos coincidentes entre distintas variedades y se han estudiado las diferencias dentro de un alelo, considerando todos los valores disponibles, independientemente de la variedad. Se han encontrado diferencias superiores a las del estudio presentado (lógicamente, al incluir más datos), pero se ha podido comprobar, de manera análoga a la presentada, que las variaciones no correspondían a mutaciones genéticas, sino a artefactos técnicos Identificación de posibles quimeras en las variedades Merlot y Cardinal En el análisis de las muestras distintas que abarcan el estudio de Homogeneidad y Estabilidad, se encontraron 49 muestras de la variedad Merlot con tres alelos para el locus VVMD27, y 2 muestras de la variedad Cardinal con tres alelos para el locus VVMD5. En el análisis genético de vid mediante marcadores microsatélite se han observado ocasionalmente más de dos alelos en algún locus en determinados tejidos de la planta, entre ellos la hoja, el cual es el material vegetal con el que se trabajó en este estudio. Esto no es un fenómeno esperado en especies diploides, como es el caso de la vid, en el cual se esperan dos alelos para un determinado locus microsatélite. Se ha identificado como una fuente de tales anomalías el fenómeno que lleva por nombre quimerismo periclinal: tejidos distintos citoplasmática o genotípicamente, dispuestos en capas concéntricas. Este fenómeno puede afectar a la identificación varietal y a los análisis de pedigríes en vid. 175
200 Resultados y Discusión En la vid existen diferentes partes de la planta que presentan dos capas celulares denominadas L1 y L2 (Einset y Pratt, 1954), (Thompson y H.P., 1963), entre ellas podemos citar las anteras, las hojas etc. La interpretación más factible para la aparición de más de dos alelos por locus, es que uno de ellos ha mutado en una de las dos capas celulares citadas anteriormente y mediante reproducción vegetativa esta mutación se ha mantenido en el tiempo, mientras que el genotipo original se ha mantenido en la otra capa. Al extraer el ADN procedente de la hoja, el genotipo resultante es una mezcla de los genotipos de las dos capas, L1 y L2. Mientras uno de los alelos está presente en las dos capas, el alelo mutado sólo se encontrará en una de ellas, con lo que existirán efectivamente tres alelos del locus microsatélite mutado dentro del tejido foliar. El que la hoja presente este fenómeno no quiere decir que todos los órganos de la planta lo tengan ya que no todas las partes de la vid presentan las dos capas celulares. Esto se ha confirmado en estudios en los que mediante embriogénesis somática se han obtenido individuos procedentes de una sola célula, bien perteneciente a la capa celular L1 o a la L2, consiguiendo con ello estudiar el perfil genético correspondiente a cada una de ellas y su fenotipo (Franks et al., 2002); (Hocquigny et al., 2004); (Bertsch et al., 2005); (Moncada et al., 2006). Posibles quimeras en Merlot De las 189 muestras estudiadas de Merlot, 49 presentaron tres alelos para el locus VVMD27. Esas mismas plantas presentaron un genotipo igual al esperado para los otros ocho microsatélites. Una vez observado este posible fenómeno de quimerismo en el locus VVMD27, se procedió a la amplificación individual del citado locus, obteniendo exactamente el mismo perfil genético, tal y como se recoge en la Figura R15. Se comprobó que esta presencia de tres alelos no fuera debida a una posible contaminación de los cebadores, o a una contaminación del ADN genómico, ya que para este último caso, se extrajo nuevamente ADN de algunas muestras que presentaron tres alelos en el locus VVMD27. Además, se amplificaron algunas de las muestras que presentaron estos tres alelos con el locus microsatélite ssrvrzag47 (Sefc et al., 1999) (abreviado ZAG47). Los loci ZAG47 y VVMD27 amplifican la misma región microsatélite (Dalbó et al., 2000), pero debido al diferente diseño de los cebadores, los alelos del ZAG47 son aproximadamente
201 Resultados y Discusión nucleótidos más cortos que los correspondientes alelos del VVMD27. En la Tabla R52 se detallan las características del locus ZAG47. Tabla R52. Características del locus ssrvrzag47. RANGO (pb) SECUENCIA Tm FLUOROCROMO TIPO DE REPETICIÓN Cebador up Cebador lw 5 -GGTCTGAATACATCCGTAAGTATAT-3 5 -ACGGTGTGCTCTCATTGTCATTGAC-3 52,6ºC 57,5ºC 6-FAM (Azul) Imperfecta (GA)15(AA) (GA)5 Los resultados que se obtuvieron con la amplificación del locus ZAG47 se muestran en la Figura R16, página 178. Se puede observar que seguían apareciendo tres alelos para ese locus. Figura R15. En la figura se muestran tres ventanas pertenecientes a la amplificación del locus VVMD27 para tres muestras de la variedad Merlot. La ventana superior corresponde a una muestra que no presentó el posible fenómeno de quimerismo para el microsatélite VVMD27 (las flechas apuntan a los dos alelos esperados), mientras que las dos ventanas inferiores corresponden a dos muestras que presentaron tres alelos para este locus. 177
Identificación varietal en vid por técnicas de Biología Molecular. Lic. Luciana Garcia Lic. Carolina Chiconofri
 Identificación varietal en vid por técnicas de Biología Molecular. Lic. Luciana Garcia Lic. Carolina Chiconofri OBJETIVO Desarrollar un banco de datos a partir de plantas de origen indudable y del uso
Identificación varietal en vid por técnicas de Biología Molecular. Lic. Luciana Garcia Lic. Carolina Chiconofri OBJETIVO Desarrollar un banco de datos a partir de plantas de origen indudable y del uso
El impacto de la crisis en las ONG
 El impacto de la crisis en las ONG Estudio sobre la situación de las entidades sin ánimo de lucro en España Marzo de 2014 INTRODUCCIÓN En la Fundación Mutua Madrileña estamos firmemente comprometidos con
El impacto de la crisis en las ONG Estudio sobre la situación de las entidades sin ánimo de lucro en España Marzo de 2014 INTRODUCCIÓN En la Fundación Mutua Madrileña estamos firmemente comprometidos con
EVOLUCIÓN Y SITUACIÓN ACTUAL DE LA PRESENCIA DEL ALUMNADO EXTRANJERO EN EL SISTEMA EDUCATIVO ESPAÑOL (2000-2011)
 EVOLUCIÓN Y SITUACIÓN ACTUAL DE LA PRESENCIA DEL ALUMNADO EXTRANJERO EN EL SISTEMA EDUCATIVO ESPAÑOL (2000-2011) 1 ALUMNADO EXTRANJERO EN EL SISTEMA EDUCATIVO ESPAÑOL: EVOLUCIÓN Y SITUACIÓN ACTUAL (2000-2011)
EVOLUCIÓN Y SITUACIÓN ACTUAL DE LA PRESENCIA DEL ALUMNADO EXTRANJERO EN EL SISTEMA EDUCATIVO ESPAÑOL (2000-2011) 1 ALUMNADO EXTRANJERO EN EL SISTEMA EDUCATIVO ESPAÑOL: EVOLUCIÓN Y SITUACIÓN ACTUAL (2000-2011)
EVOLUCIÓN Y SITUACIÓN ACTUAL DE LA PRESENCIA DEL ALUMNADO EXTRANJERO EN EL SISTEMA EDUCATIVO ESPAÑOL (2001-2012)
 EVOLUCIÓN Y SITUACIÓN ACTUAL DE LA PRESENCIA DEL ALUMNADO EXTRANJERO EN EL SISTEMA EDUCATIVO ESPAÑOL (2001-2012) 1 RESUMEN EJECUTIVO En el año 2002 el entonces CIDE presentaba el primer informe sobre la
EVOLUCIÓN Y SITUACIÓN ACTUAL DE LA PRESENCIA DEL ALUMNADO EXTRANJERO EN EL SISTEMA EDUCATIVO ESPAÑOL (2001-2012) 1 RESUMEN EJECUTIVO En el año 2002 el entonces CIDE presentaba el primer informe sobre la
 GENÉTICA MENDELIANA EL GEN. El gen Mendeliano es una unidad de función, estructura, transmisión, mutación y evolución, que se distribuye ordenada y linealmente en los cromosomas. A nivel genético el gen
GENÉTICA MENDELIANA EL GEN. El gen Mendeliano es una unidad de función, estructura, transmisión, mutación y evolución, que se distribuye ordenada y linealmente en los cromosomas. A nivel genético el gen
Nuevos paneles de PCR Real Time: El diagnóstico molecular más rápido, fiable y eficaz
 IDEXX VetLab Suite IDEXX SNAP Tests Laboratorio de Referencia IDEXX Nuevos paneles de PCR Real Time: El diagnóstico molecular más rápido, fiable y eficaz Obtenga respuestas definitivas con la IDEXX RealPCR
IDEXX VetLab Suite IDEXX SNAP Tests Laboratorio de Referencia IDEXX Nuevos paneles de PCR Real Time: El diagnóstico molecular más rápido, fiable y eficaz Obtenga respuestas definitivas con la IDEXX RealPCR
Biotecnología. Historia y aplicaciones Su utilización en el INTA Alto Valle. investigación
 Alejandro Giayetto Técnico INTA agiayetto@correo.inta.gov.ar Mirta Rossini Técnico INTA mrossini@correo.inta.gov.ar Diana Vera Biotecnóloga labfitopatologia@correo.inta.gov.ar investigación 10 Biotecnología
Alejandro Giayetto Técnico INTA agiayetto@correo.inta.gov.ar Mirta Rossini Técnico INTA mrossini@correo.inta.gov.ar Diana Vera Biotecnóloga labfitopatologia@correo.inta.gov.ar investigación 10 Biotecnología
Principales resultados
 15 de julio de 2008 Encuesta sobre Recursos Humanos en Ciencia y Tecnología 2006 Resultados provisionales Principales resultados Los resultados de la Encuesta sobre Recursos Humanos en Ciencia y Tecnología
15 de julio de 2008 Encuesta sobre Recursos Humanos en Ciencia y Tecnología 2006 Resultados provisionales Principales resultados Los resultados de la Encuesta sobre Recursos Humanos en Ciencia y Tecnología
MEDICION DEL TRABAJO
 MEDICION DEL TRABAJO Habíamos dicho al comenzar el curso que habían 4 técnicas que permiten realizar una medición del trabajo 1 Técnicas Directas: - Estudio de tiempos con cronómetro - Muestreo del trabajo
MEDICION DEL TRABAJO Habíamos dicho al comenzar el curso que habían 4 técnicas que permiten realizar una medición del trabajo 1 Técnicas Directas: - Estudio de tiempos con cronómetro - Muestreo del trabajo
4.4.1 Servicio de Prevención Propio.
 1 Si se trata de una empresa entre 250 y 500 trabajadores que desarrolla actividades incluidas en el Anexo I del Reglamento de los Servicios de Prevención, o de una empresa de más de 500 trabajadores con
1 Si se trata de una empresa entre 250 y 500 trabajadores que desarrolla actividades incluidas en el Anexo I del Reglamento de los Servicios de Prevención, o de una empresa de más de 500 trabajadores con
Sistemas de Gestión de Calidad. Control documental
 4 Sistemas de Gestión de Calidad. Control documental ÍNDICE: 4.1 Requisitos Generales 4.2 Requisitos de la documentación 4.2.1 Generalidades 4.2.2 Manual de la Calidad 4.2.3 Control de los documentos 4.2.4
4 Sistemas de Gestión de Calidad. Control documental ÍNDICE: 4.1 Requisitos Generales 4.2 Requisitos de la documentación 4.2.1 Generalidades 4.2.2 Manual de la Calidad 4.2.3 Control de los documentos 4.2.4
Entender el funcionamiento de los relojes permitiría lidiar con ciertas patologías en humanos. 28 ACTUALIDAD EN I+D RIA / Vol. 41 / N.
 28 ACTUALIDAD EN I+D RIA / Vol. 41 / N.º 1 Entender el funcionamiento de los relojes permitiría lidiar con ciertas patologías en humanos Abril 2015, Argentina 29 Relojes biológicos en plantas Ajustar el
28 ACTUALIDAD EN I+D RIA / Vol. 41 / N.º 1 Entender el funcionamiento de los relojes permitiría lidiar con ciertas patologías en humanos Abril 2015, Argentina 29 Relojes biológicos en plantas Ajustar el
Superar las barreras
 Superar las barreras 6 La actuación de su empresa en el mercado elegido estará sujeta a las barreras que existan a su producto o a su actuación en el país. Las barreras pueden o no ser importantes. Pueden
Superar las barreras 6 La actuación de su empresa en el mercado elegido estará sujeta a las barreras que existan a su producto o a su actuación en el país. Las barreras pueden o no ser importantes. Pueden
EL AGUACATE EN AGRICULTURA ECOLÓGICA. PUNTOS DE CONTROL Y CERTIFICACIÓN SEGÚN EL REGLAMENTO EUROPEO 2092/91 Y SUS MODIFICACIONES
 Proceedings V World Avocado Congress (Actas V Congreso Mundial del Aguacate) 2003. pp. 701-705. EL AGUACATE EN AGRICULTURA ECOLÓGICA. PUNTOS DE CONTROL Y CERTIFICACIÓN SEGÚN EL REGLAMENTO EUROPEO 2092/91
Proceedings V World Avocado Congress (Actas V Congreso Mundial del Aguacate) 2003. pp. 701-705. EL AGUACATE EN AGRICULTURA ECOLÓGICA. PUNTOS DE CONTROL Y CERTIFICACIÓN SEGÚN EL REGLAMENTO EUROPEO 2092/91
ISO9001:2015. Todos los certificados emitidos en este periodo tienen una fecha de caducidad de 15 de septiembre de 2018.
 ISO9001:2015 PLAN DE TRANSICIÓN Tras la publicación de la nueva versión de la norma ISO9001 el pasado mes de septiembre se inicia un periodo de convivencia entre las dos versiones de la norma. Este periodo
ISO9001:2015 PLAN DE TRANSICIÓN Tras la publicación de la nueva versión de la norma ISO9001 el pasado mes de septiembre se inicia un periodo de convivencia entre las dos versiones de la norma. Este periodo
Criterio 2: Política y estrategia
 Criterio 2: Política y estrategia Definición. Cómo implanta el servicio su misión, y visión mediante una estrategia claramente centrada en todos los grupos de interés y apoyada por políticas, planes, objetivos,
Criterio 2: Política y estrategia Definición. Cómo implanta el servicio su misión, y visión mediante una estrategia claramente centrada en todos los grupos de interés y apoyada por políticas, planes, objetivos,
Como se mencionó en la parte de la teoría, no existe consenso en cuanto a la
 4. Metodología Definición de empleo informal Como se mencionó en la parte de la teoría, no existe consenso en cuanto a la definición de empleo informal y diferentes estudios han utilizado matices distintas
4. Metodología Definición de empleo informal Como se mencionó en la parte de la teoría, no existe consenso en cuanto a la definición de empleo informal y diferentes estudios han utilizado matices distintas
EL MATERIAL GENÉTICO:
 LA HUELLA GENÉTICA: PRUEBAS DE PATERNIDAD E IDENTIFICACIÓN INTRODUCCIÓN: En éstos últimos años, se ha popularizado a través de los medios de comunicación la expresión: identificación través de pruebas
LA HUELLA GENÉTICA: PRUEBAS DE PATERNIDAD E IDENTIFICACIÓN INTRODUCCIÓN: En éstos últimos años, se ha popularizado a través de los medios de comunicación la expresión: identificación través de pruebas
App para realizar consultas al Sistema de Información Estadística de Castilla y León
 App para realizar consultas al Sistema de Información Estadística de Castilla y León Jesús M. Rodríguez Rodríguez rodrodje@jcyl.es Dirección General de Presupuestos y Estadística Consejería de Hacienda
App para realizar consultas al Sistema de Información Estadística de Castilla y León Jesús M. Rodríguez Rodríguez rodrodje@jcyl.es Dirección General de Presupuestos y Estadística Consejería de Hacienda
Técnicas de valor presente para calcular el valor en uso
 Normas Internacionales de Información Financiera NIC - NIIF Guía NIC - NIIF NIC 36 Fundación NIC-NIIF Técnicas de valor presente para calcular el valor en uso Este documento proporciona una guía para utilizar
Normas Internacionales de Información Financiera NIC - NIIF Guía NIC - NIIF NIC 36 Fundación NIC-NIIF Técnicas de valor presente para calcular el valor en uso Este documento proporciona una guía para utilizar
Contenidos. INFORME ENCUESTA TELEFÓNICA. Curso 2009 10
 ENCUESTA DE OPINIÓN DEL ALUMNADO SOBRE LA ACTUACIÓN DOCENTE DEL PROFESORADO UNIVERSIDAD DE SEVILLA Curso 2009-2010 ENCUESTA TELEFÓNICA Contenidos Introducción.... 4 El Cuestionario... 5 El muestreo...
ENCUESTA DE OPINIÓN DEL ALUMNADO SOBRE LA ACTUACIÓN DOCENTE DEL PROFESORADO UNIVERSIDAD DE SEVILLA Curso 2009-2010 ENCUESTA TELEFÓNICA Contenidos Introducción.... 4 El Cuestionario... 5 El muestreo...
GUÍA PARA LA APLICACIÓN DEL SISTEMA DE TRAZABILIDAD EN LA EMPRESA AGROALIMENTARIA
 GUÍA PARA LA APLICACIÓN DEL SISTEMA DE TRAZABILIDAD EN LA EMPRESA AGROALIMENTARIA La idea de elaborar una Guía para la Aplicación del Sistema de Trazabilidad en la empresa Agroalimentaria por Parte de
GUÍA PARA LA APLICACIÓN DEL SISTEMA DE TRAZABILIDAD EN LA EMPRESA AGROALIMENTARIA La idea de elaborar una Guía para la Aplicación del Sistema de Trazabilidad en la empresa Agroalimentaria por Parte de
SÍNTESIS Y PERSPECTIVAS
 SÍNTESIS Y PERSPECTIVAS Los invitamos a observar, a identificar problemas, pero al mismo tiempo a buscar oportunidades de mejoras en sus empresas. REVISIÓN DE CONCEPTOS. Esta es la última clase del curso.
SÍNTESIS Y PERSPECTIVAS Los invitamos a observar, a identificar problemas, pero al mismo tiempo a buscar oportunidades de mejoras en sus empresas. REVISIÓN DE CONCEPTOS. Esta es la última clase del curso.
El proyecto Innova Cesal tiene como propósito llevar a cabo innovaciones en
 Reporte del cuestionario sobre formación de profesores Verdejo, P., Orta, M. Introducción El proyecto Innova Cesal tiene como propósito llevar a cabo innovaciones en los procesos de enseñanza aprendizaje
Reporte del cuestionario sobre formación de profesores Verdejo, P., Orta, M. Introducción El proyecto Innova Cesal tiene como propósito llevar a cabo innovaciones en los procesos de enseñanza aprendizaje
Normas y procedimientos para la clasificación de los documentos administrativos
 Normas y procedimientos para la clasificación de los documentos administrativos La Universidad de Lleida (UdL) necesita desarrollar el cuadro de clasificación de los documentos administrativos, para toda
Normas y procedimientos para la clasificación de los documentos administrativos La Universidad de Lleida (UdL) necesita desarrollar el cuadro de clasificación de los documentos administrativos, para toda
SISTEMAS Y MANUALES DE LA CALIDAD
 SISTEMAS Y MANUALES DE LA CALIDAD NORMATIVAS SOBRE SISTEMAS DE CALIDAD Introducción La experiencia de algunos sectores industriales que por las características particulares de sus productos tenían necesidad
SISTEMAS Y MANUALES DE LA CALIDAD NORMATIVAS SOBRE SISTEMAS DE CALIDAD Introducción La experiencia de algunos sectores industriales que por las características particulares de sus productos tenían necesidad
Una de cada cuatro empresas necesita el beneficio de diez años para devolver su deuda, casi el doble que la media europea
 www.fbbva.es DEPARTAMENTO DE COMUNICACIÓN NOTA DE PRENSA Estudio sobre endeudamiento y estructura financiera de las empresas de la Fundación BBVA y el Ivie Una de cada cuatro empresas necesita el beneficio
www.fbbva.es DEPARTAMENTO DE COMUNICACIÓN NOTA DE PRENSA Estudio sobre endeudamiento y estructura financiera de las empresas de la Fundación BBVA y el Ivie Una de cada cuatro empresas necesita el beneficio
SEGURIDAD DE LA INFORMACIÓN
 SEGURIDAD DE LA INFORMACIÓN La información es el principal activo de muchas organizaciones por lo que es necesario protegerla adecuadamente frente a amenazas que puedan poner en peligro la continuidad
SEGURIDAD DE LA INFORMACIÓN La información es el principal activo de muchas organizaciones por lo que es necesario protegerla adecuadamente frente a amenazas que puedan poner en peligro la continuidad
Modificación y parametrización del modulo de Solicitudes (Request) en el ERP/CRM Compiere.
 UNIVERSIDAD DE CARABOBO FACULTAD DE CIENCIA Y TECNOLOGÍA DIRECCION DE EXTENSION COORDINACION DE PASANTIAS Modificación y parametrización del modulo de Solicitudes (Request) en el ERP/CRM Compiere. Pasante:
UNIVERSIDAD DE CARABOBO FACULTAD DE CIENCIA Y TECNOLOGÍA DIRECCION DE EXTENSION COORDINACION DE PASANTIAS Modificación y parametrización del modulo de Solicitudes (Request) en el ERP/CRM Compiere. Pasante:
El número de empresas activas disminuyó un 1,6% durante 2011 y se situó en 3,2 millones
 7 de agosto de 2012 Estructura y Demografía Empresarial Directorio Central de Empresas (DIRCE) a 1 de enero de 2012 El número de empresas activas disminuyó un 1,6% durante 2011 y se situó en 3,2 millones
7 de agosto de 2012 Estructura y Demografía Empresarial Directorio Central de Empresas (DIRCE) a 1 de enero de 2012 El número de empresas activas disminuyó un 1,6% durante 2011 y se situó en 3,2 millones
La selección del mercado meta es esencialmente idéntica, sin importar si una firma vende un bien o servicio.
 4. SELECCIÓN Y EVALUACIÓN DE MERCADO META SELECCIÓN DE MERCADO META Un mercado meta se refiere a un grupo de personas u organizaciones a las cuales una organización dirige su programa de marketing. Es
4. SELECCIÓN Y EVALUACIÓN DE MERCADO META SELECCIÓN DE MERCADO META Un mercado meta se refiere a un grupo de personas u organizaciones a las cuales una organización dirige su programa de marketing. Es
ISO 9001:2000 DOCUMENTO INFORMATIVO DOCUMENTO ELABORADO POR CHRISTIAN NARBARTE PARA EL IVECE
 ISO 9001:2000 DOCUMENTO INFORMATIVO DOCUMENTO ELABORADO POR CHRISTIAN NARBARTE PARA EL IVECE MARZO 2007 Este documento contesta las preguntas más frecuentes que se plantean las organizaciones que quieren
ISO 9001:2000 DOCUMENTO INFORMATIVO DOCUMENTO ELABORADO POR CHRISTIAN NARBARTE PARA EL IVECE MARZO 2007 Este documento contesta las preguntas más frecuentes que se plantean las organizaciones que quieren
D 15/02. Dictamen sobre el Plan de Formación Profesional de Castilla y León. Fecha de aprobación: Pleno 31/10/02
 D 15/02 Dictamen sobre el Plan de Formación Profesional de Castilla y León Fecha de aprobación: Pleno 31/10/02 1 Dictamen 15/02 sobre el Plan de Formación Profesional en Castilla y León Se solicitó dictamen
D 15/02 Dictamen sobre el Plan de Formación Profesional de Castilla y León Fecha de aprobación: Pleno 31/10/02 1 Dictamen 15/02 sobre el Plan de Formación Profesional en Castilla y León Se solicitó dictamen
Elementos requeridos para crearlos (ejemplo: el compilador)
 Generalidades A lo largo del ciclo de vida del proceso de software, los productos de software evolucionan. Desde la concepción del producto y la captura de requisitos inicial hasta la puesta en producción
Generalidades A lo largo del ciclo de vida del proceso de software, los productos de software evolucionan. Desde la concepción del producto y la captura de requisitos inicial hasta la puesta en producción
ANÁLISIS DE CARGOS. 1. Nombre del cargo 2. Posición del cargo en el organigrama. 3. Contenido del cargo. 1. Requisitos intelectuales
 Análisis de CARGOS ANÁLISIS DE CARGOS Autor: Herman Bachenheimer Correo: herman@puj.edu.co Después de la descripción, sigue el análisis del cargo. Una vez identificado el contenido del cargo (aspectos
Análisis de CARGOS ANÁLISIS DE CARGOS Autor: Herman Bachenheimer Correo: herman@puj.edu.co Después de la descripción, sigue el análisis del cargo. Una vez identificado el contenido del cargo (aspectos
PLAN DE MEJORAS. Herramienta de trabajo. Agencia Nacional de Evaluación de la Calidad y Acreditación
 PLAN DE MEJORAS Herramienta de trabajo Agencia Nacional de Evaluación de la Calidad y Acreditación Índice 1 Introducción...3 2 Pasos a seguir para la elaboración del plan de mejoras...5 2.1 Identificar
PLAN DE MEJORAS Herramienta de trabajo Agencia Nacional de Evaluación de la Calidad y Acreditación Índice 1 Introducción...3 2 Pasos a seguir para la elaboración del plan de mejoras...5 2.1 Identificar
TEMA 3: MÉTODO CONTABLE. LAS CUENTAS
 TEMA 3: MÉTODO CONTABLE. LAS CUENTAS 1. HECHOS CONTABLES En el tema 1 se señalaba que, dentro de la función de elaboración de la información contable, la contabilidad se ocupaba, en una primera etapa,
TEMA 3: MÉTODO CONTABLE. LAS CUENTAS 1. HECHOS CONTABLES En el tema 1 se señalaba que, dentro de la función de elaboración de la información contable, la contabilidad se ocupaba, en una primera etapa,
PROTOCOLO DE EVALUACIÓN PARA LA VERIFICACIÓN DE TÍTULOS OFICIALES (GRADO Y MÁSTER)
 PROTOCOLO DE EVALUACIÓN PARA LA VERIFICACIÓN DE TÍTULOS OFICIALES (GRADO Y MÁSTER) V.01.02/12/10 Página 2 de 17 Para facilitar la labor que desarrollan los evaluadores, nombrados por AGAE, en el proceso
PROTOCOLO DE EVALUACIÓN PARA LA VERIFICACIÓN DE TÍTULOS OFICIALES (GRADO Y MÁSTER) V.01.02/12/10 Página 2 de 17 Para facilitar la labor que desarrollan los evaluadores, nombrados por AGAE, en el proceso
Mapa territorial de las entidades no lucrativas y de las cooperativas en España. Por Isabel Vidal CIES
 Mapa territorial de las entidades no lucrativas y de las cooperativas en España Por Isabel Vidal CIES 1. Introducción Las entidades no lucrativas y las cooperativas acostumbran a definirse como aquel conjunto
Mapa territorial de las entidades no lucrativas y de las cooperativas en España Por Isabel Vidal CIES 1. Introducción Las entidades no lucrativas y las cooperativas acostumbran a definirse como aquel conjunto
Metodología básica de gestión de proyectos. Octubre de 2003
 Metodología básica de gestión de proyectos Octubre de 2003 Dentro de la metodología utilizada en la gestión de proyectos el desarrollo de éstos se estructura en tres fases diferenciadas: Fase de Éjecución
Metodología básica de gestión de proyectos Octubre de 2003 Dentro de la metodología utilizada en la gestión de proyectos el desarrollo de éstos se estructura en tres fases diferenciadas: Fase de Éjecución
Gestión de la Configuración
 Gestión de la ÍNDICE DESCRIPCIÓN Y OBJETIVOS... 1 ESTUDIO DE VIABILIDAD DEL SISTEMA... 2 ACTIVIDAD EVS-GC 1: DEFINICIÓN DE LOS REQUISITOS DE GESTIÓN DE CONFIGURACIÓN... 2 Tarea EVS-GC 1.1: Definición de
Gestión de la ÍNDICE DESCRIPCIÓN Y OBJETIVOS... 1 ESTUDIO DE VIABILIDAD DEL SISTEMA... 2 ACTIVIDAD EVS-GC 1: DEFINICIÓN DE LOS REQUISITOS DE GESTIÓN DE CONFIGURACIÓN... 2 Tarea EVS-GC 1.1: Definición de
ISO14001:2015. - disponer de un certificado bajo la versión de 2008 en vigor - superar una auditoria bajo los requisitos de la nueva versión
 ISO14001:2015 PLAN DE TRANSICIÓN Tras la publicación de la nueva versión de la norma ISO14001 el pasado mes de septiembre se inicia un periodo de convivencia entre las dos versiones de la norma. Este periodo
ISO14001:2015 PLAN DE TRANSICIÓN Tras la publicación de la nueva versión de la norma ISO14001 el pasado mes de septiembre se inicia un periodo de convivencia entre las dos versiones de la norma. Este periodo
DESCRIPCIÓN DE POBLACIONES MENDELIANAS: EQUILIBRIO DE HARDY-WEINBERG
 DESCRIPCIÓN DE POBLACIONES MENDELIANAS: EQUILIBRIO DE HARDY-WEINBERG T. DOBZHANSKY G. H. HARDY CONCEPTO DE POBLACIÓN DESCRIPCIÓN ESTÁTICA DE POBLACIONES DESCRIPCIÓN DINÁMICA: EQUILIBRIO DE HARDY-WEINBERG
DESCRIPCIÓN DE POBLACIONES MENDELIANAS: EQUILIBRIO DE HARDY-WEINBERG T. DOBZHANSKY G. H. HARDY CONCEPTO DE POBLACIÓN DESCRIPCIÓN ESTÁTICA DE POBLACIONES DESCRIPCIÓN DINÁMICA: EQUILIBRIO DE HARDY-WEINBERG
7.012 Serie de ejercicios 5
 Nombre Grupo 7.012 Serie de ejercicios 5 Pregunta 1 Al estudiar los problemas de esterilidad, usted intenta aislar un hipotético gen de conejo que explique la prolífica reproducción de estos animales.
Nombre Grupo 7.012 Serie de ejercicios 5 Pregunta 1 Al estudiar los problemas de esterilidad, usted intenta aislar un hipotético gen de conejo que explique la prolífica reproducción de estos animales.
El comercio exterior en Asturias
 El comercio exterior en Asturias Mas información en: Página web de REGIOlab: http://www.uniovi.net/regiolab Página del Observatorio Regional REGIOlab: http://www.uniovi.net/regiolab/enlaces2/i1/ 1 1. Introducción
El comercio exterior en Asturias Mas información en: Página web de REGIOlab: http://www.uniovi.net/regiolab Página del Observatorio Regional REGIOlab: http://www.uniovi.net/regiolab/enlaces2/i1/ 1 1. Introducción
RESULTADOS CONSULTA CIUDADANA VIRTUAL. Consulta Laboral en Línea
 RESULTADOS CONSULTA CIUDADANA VIRTUAL Consulta Laboral en Línea Septiembre, 2015 1 Agradecimientos Ponemos a disposición de ustedes los resultados de la Consulta Ciudadana Virtual, efectuada en julio de
RESULTADOS CONSULTA CIUDADANA VIRTUAL Consulta Laboral en Línea Septiembre, 2015 1 Agradecimientos Ponemos a disposición de ustedes los resultados de la Consulta Ciudadana Virtual, efectuada en julio de
DATOS DE CONSUMO DE LOS GRANDES CONSUMIDORES: SERVICIOS DE CATERING, CENTROS EDUCATIVOS Y OTRAS ENTIDADES DE LANZAROTE OCTUBRE NOVIEMBRE 2011
 DATOS DE CONSUMO DE LOS GRANDES CONSUMIDORES: SERVICIOS DE CATERING, CENTROS EDUCATIVOS Y OTRAS ENTIDADES DE LANZAROTE OCTUBRE NOVIEMBRE 2011 PROYECTO MERCALANZAROTE Elaborado por el personal del Proyecto
DATOS DE CONSUMO DE LOS GRANDES CONSUMIDORES: SERVICIOS DE CATERING, CENTROS EDUCATIVOS Y OTRAS ENTIDADES DE LANZAROTE OCTUBRE NOVIEMBRE 2011 PROYECTO MERCALANZAROTE Elaborado por el personal del Proyecto
K2BIM Plan de Investigación - Comparación de herramientas para la parametrización asistida de ERP Versión 1.2
 K2BIM Plan de Investigación - Comparación de herramientas para la parametrización asistida de ERP Versión 1.2 Historia de revisiones Fecha VersiónDescripción Autor 08/10/2009 1.0 Creación del documento.
K2BIM Plan de Investigación - Comparación de herramientas para la parametrización asistida de ERP Versión 1.2 Historia de revisiones Fecha VersiónDescripción Autor 08/10/2009 1.0 Creación del documento.
Diciembre 2008. núm.96. El capital humano de los emprendedores en España
 Diciembre 2008 núm.96 El capital humano de los emprendedores en España En este número 2 El capital humano de los emprendedores Este cuaderno inicia una serie de números que detallan distintos aspectos
Diciembre 2008 núm.96 El capital humano de los emprendedores en España En este número 2 El capital humano de los emprendedores Este cuaderno inicia una serie de números que detallan distintos aspectos
Explotación de las variables educativas de la Encuesta de Población Activa: Nivel de Formación y Formación Permanente
 Explotación de las variables educativas de la Encuesta de Población Activa: Nivel de Formación y Formación Permanente 1. Introducción Notas metodológicas Se presenta información estadística sobre las variables
Explotación de las variables educativas de la Encuesta de Población Activa: Nivel de Formación y Formación Permanente 1. Introducción Notas metodológicas Se presenta información estadística sobre las variables
Integración de la prevención de riesgos laborales
 Carlos Muñoz Ruiz Técnico de Prevención. INSL Junio 2012 39 Integración de la prevención de riesgos laborales Base legal y conceptos básicos Ley 31/1995, de Prevención de Riesgos Laborales: Artículo 14.
Carlos Muñoz Ruiz Técnico de Prevención. INSL Junio 2012 39 Integración de la prevención de riesgos laborales Base legal y conceptos básicos Ley 31/1995, de Prevención de Riesgos Laborales: Artículo 14.
Act.7: Reconocimiento Unidad 2
 Act.7: Reconocimiento Unidad 2 Funciones del empaque Las funciones del empaque son varias y se dividen en dos: estructurales y modernas. Se llaman estructurales a todas aquellas que tienen que ver con
Act.7: Reconocimiento Unidad 2 Funciones del empaque Las funciones del empaque son varias y se dividen en dos: estructurales y modernas. Se llaman estructurales a todas aquellas que tienen que ver con
Nota de prensa RESULTADOS DE ESPAÑA EN PISA 2012
 RESULTADOS DE ESPAÑA EN PISA 2012 03-diciembre-2013.- La secretaria de Estado de Educación, Formación Profesional y Universidades, Montserrat Gomendio, ha presentado esta mañana los datos de España del
RESULTADOS DE ESPAÑA EN PISA 2012 03-diciembre-2013.- La secretaria de Estado de Educación, Formación Profesional y Universidades, Montserrat Gomendio, ha presentado esta mañana los datos de España del
Electrificación en zonas rurales mediante sistemas híbridos
 Electrificación en zonas rurales mediante sistemas híbridos Julio 2013 Pág. 1 de 6 Antecedentes y situación actual En los últimos años, el crecimiento y desarrollo del sector fotovoltaico ha sufrido un
Electrificación en zonas rurales mediante sistemas híbridos Julio 2013 Pág. 1 de 6 Antecedentes y situación actual En los últimos años, el crecimiento y desarrollo del sector fotovoltaico ha sufrido un
Situación Laboral de los Jóvenes Españoles
 Situación Laboral de los Jóvenes Españoles Área de Estudios Asempleo Marzo 2015 SITUACIÓN LABORAL DE LOS JÓVENES ESPAÑOLES Después de una treintena de trimestres acusando una de las peores crisis laborales
Situación Laboral de los Jóvenes Españoles Área de Estudios Asempleo Marzo 2015 SITUACIÓN LABORAL DE LOS JÓVENES ESPAÑOLES Después de una treintena de trimestres acusando una de las peores crisis laborales
Exceso del importe en libros del activo apto sobre el importe recuperable
 Norma Internacional de Contabilidad 23 Costos por Préstamos Principio básico 1 Los costos por préstamos que sean directamente atribuibles a la adquisición, construcción o producción de un activo apto forman
Norma Internacional de Contabilidad 23 Costos por Préstamos Principio básico 1 Los costos por préstamos que sean directamente atribuibles a la adquisición, construcción o producción de un activo apto forman
Análisis de paternidad y parentesco en alpacas (Vicugna pacos) mediante marcadores moleculares
 Análisis de paternidad y parentesco en alpacas (Vicugna pacos) mediante marcadores moleculares MSc. Juan Agapito Panta Laboratorio de Genómica y Biología Molecular Instituto Peruano de Energía Nuclear
Análisis de paternidad y parentesco en alpacas (Vicugna pacos) mediante marcadores moleculares MSc. Juan Agapito Panta Laboratorio de Genómica y Biología Molecular Instituto Peruano de Energía Nuclear
Curso de implantación 2010/2011
 Denominación del Título Universidad solicitante Rama de Conocimiento Grado en Comercio y Marketing Universidad de Oviedo Ciencias Sociales y Jurídicas Curso de implantación 2010/2011 ANECA, conforme a
Denominación del Título Universidad solicitante Rama de Conocimiento Grado en Comercio y Marketing Universidad de Oviedo Ciencias Sociales y Jurídicas Curso de implantación 2010/2011 ANECA, conforme a
1.1. Introducción y conceptos básicos
 Tema 1 Variables estadísticas Contenido 1.1. Introducción y conceptos básicos.................. 1 1.2. Tipos de variables estadísticas................... 2 1.3. Distribuciones de frecuencias....................
Tema 1 Variables estadísticas Contenido 1.1. Introducción y conceptos básicos.................. 1 1.2. Tipos de variables estadísticas................... 2 1.3. Distribuciones de frecuencias....................
Análisis de los datos
 Universidad Complutense de Madrid CURSOS DE FORMACIÓN EN INFORMÁTICA Análisis de los datos Hojas de cálculo Tema 6 Análisis de los datos Una de las capacidades más interesantes de Excel es la actualización
Universidad Complutense de Madrid CURSOS DE FORMACIÓN EN INFORMÁTICA Análisis de los datos Hojas de cálculo Tema 6 Análisis de los datos Una de las capacidades más interesantes de Excel es la actualización
La búsqueda, reconocimiento y posterior estudio del comportamiento
 Nuevas variedades de cítricos La búsqueda, reconocimiento y posterior estudio del comportamiento de nuevas variedades de cítricos, con el fin de adecuar el mapa varietal de recolección y comercialización
Nuevas variedades de cítricos La búsqueda, reconocimiento y posterior estudio del comportamiento de nuevas variedades de cítricos, con el fin de adecuar el mapa varietal de recolección y comercialización
1. Construcción de Planes de Acción Sectoriales (PAS)
 1. Construcción de Planes de Acción Sectoriales (PAS) La construcción de los PAS es la prioridad de trabajo de la ECDBC en el 2013. Los PAS estarán constituidos por diferentes medidas de mitigación (políticas,
1. Construcción de Planes de Acción Sectoriales (PAS) La construcción de los PAS es la prioridad de trabajo de la ECDBC en el 2013. Los PAS estarán constituidos por diferentes medidas de mitigación (políticas,
El sistema de franquicias mantiene su dinamismo frente a la crisis
 Nota de Prensa La Asociación Española de Franquiciadores presenta su estudio anual "Informe de la Franquicia en España 2014" El sistema de franquicias mantiene su dinamismo frente a la crisis La facturación
Nota de Prensa La Asociación Española de Franquiciadores presenta su estudio anual "Informe de la Franquicia en España 2014" El sistema de franquicias mantiene su dinamismo frente a la crisis La facturación
Diseño muestral de la Encuesta sobre integración social y necesidades sociales
 Diseño muestral la Encuesta sobre integración social y necesidas sociales Manuel Trujillo Carmona Instituto Estudios Sociales Avanzados l CSIC 1 1. Objetivos El objetivo la encuesta es cuantificar y analizar
Diseño muestral la Encuesta sobre integración social y necesidas sociales Manuel Trujillo Carmona Instituto Estudios Sociales Avanzados l CSIC 1 1. Objetivos El objetivo la encuesta es cuantificar y analizar
(Estudios in vivo y estudios in vitro)
 (Estudios in vivo y estudios in vitro) IN VIVO: es la experimentación con un todo, que viven organismos en comparación. Ensayos con animales y ensayos clínicos son dos formas de investigación in vivo.
(Estudios in vivo y estudios in vitro) IN VIVO: es la experimentación con un todo, que viven organismos en comparación. Ensayos con animales y ensayos clínicos son dos formas de investigación in vivo.
GUÍA METODOLÓGICA PARA LA FORMACIÓN CON E-LEARNING DIRIGIDA A COLECTIVOS SIN ALTA CUALIFICACIÓN CAPÍTULO 4. Dirección Técnica:
 LA FORMACIÓN EMPRESARIAL CON E-LEARNING GUÍA METODOLÓGICA PARA LA FORMACIÓN CON E-LEARNING DIRIGIDA A COLECTIVOS SIN ALTA CUALIFICACIÓN CAPÍTULO 4 Dirección Técnica: 4.- EL PLAN DE FORMACIÓN 33 Capítulo
LA FORMACIÓN EMPRESARIAL CON E-LEARNING GUÍA METODOLÓGICA PARA LA FORMACIÓN CON E-LEARNING DIRIGIDA A COLECTIVOS SIN ALTA CUALIFICACIÓN CAPÍTULO 4 Dirección Técnica: 4.- EL PLAN DE FORMACIÓN 33 Capítulo
Estas visiones de la información, denominadas vistas, se pueden identificar de varias formas.
 El primer paso en el diseño de una base de datos es la producción del esquema conceptual. Normalmente, se construyen varios esquemas conceptuales, cada uno para representar las distintas visiones que los
El primer paso en el diseño de una base de datos es la producción del esquema conceptual. Normalmente, se construyen varios esquemas conceptuales, cada uno para representar las distintas visiones que los
Generalidades. DOCUMENTOS DE PATENTES COMO FUENTE DE INFORMACION TECNOLOGICA
 DOCUMENTOS DE PATENTES COMO FUENTE DE INFORMACION TECNOLOGICA Generalidades. Cuando una persona ha realizado una invención lo más conveniente es protegerla obteniendo un derecho de Propiedad Industrial.
DOCUMENTOS DE PATENTES COMO FUENTE DE INFORMACION TECNOLOGICA Generalidades. Cuando una persona ha realizado una invención lo más conveniente es protegerla obteniendo un derecho de Propiedad Industrial.
SEPARACIONES Y DIVORCIOS TRAS LA LEY 15/2005
 Datos de Justicia SEPARACIONES Y DIVORCIOS TRAS LA LEY 15/2005 El 9 de julio de 2005 aparecía publicada en el BOE la Ley 15/2005 de 8 de julio por la que se modificó el Código Civil y la Ley de Enjuiciamiento
Datos de Justicia SEPARACIONES Y DIVORCIOS TRAS LA LEY 15/2005 El 9 de julio de 2005 aparecía publicada en el BOE la Ley 15/2005 de 8 de julio por la que se modificó el Código Civil y la Ley de Enjuiciamiento
NIFBdM C-7 OTRAS INVERSIONES PERMANENTES
 NIFBdM C-7 OTRAS INVERSIONES PERMANENTES OBJETIVO Establecer los criterios de valuación, presentación y revelación para el reconocimiento inicial y posterior de las otras inversiones permanentes del Banco.
NIFBdM C-7 OTRAS INVERSIONES PERMANENTES OBJETIVO Establecer los criterios de valuación, presentación y revelación para el reconocimiento inicial y posterior de las otras inversiones permanentes del Banco.
INTRODUCCION. La introducción del euro como moneda de pleno derecho en once países 1 de la Unión
 INTRODUCCION La introducción del euro como moneda de pleno derecho en once países 1 de la Unión Europea, nombrados en conjunto Zona Monetaria Europea o eurozona, ha implicado importantes cambios en las
INTRODUCCION La introducción del euro como moneda de pleno derecho en once países 1 de la Unión Europea, nombrados en conjunto Zona Monetaria Europea o eurozona, ha implicado importantes cambios en las
IAP 1005 - CONSIDERACIONES PARTICULARES SOBRE LA AUDITORÍA DE LAS EMPRESAS DE REDUCIDA DIMENSIÓN
 IAP 1005 - CONSIDERACIONES PARTICULARES SOBRE LA AUDITORÍA DE LAS EMPRESAS DE REDUCIDA DIMENSIÓN Introducción 1. Las Normas Internacionales de Auditoría (NIA) se aplican a la auditoría de la información
IAP 1005 - CONSIDERACIONES PARTICULARES SOBRE LA AUDITORÍA DE LAS EMPRESAS DE REDUCIDA DIMENSIÓN Introducción 1. Las Normas Internacionales de Auditoría (NIA) se aplican a la auditoría de la información
Mercados No tradicionales potencial para los alimentos y bebidas Argentinos-
 Mercados No tradicionales potencial para los alimentos y bebidas Argentinos- Agustín Gándara - COPAL Durante el 2012 la Industria de Alimentos y Bebidas Argentina (en adelante IAB) exportó a 188 destinos
Mercados No tradicionales potencial para los alimentos y bebidas Argentinos- Agustín Gándara - COPAL Durante el 2012 la Industria de Alimentos y Bebidas Argentina (en adelante IAB) exportó a 188 destinos
Los costes de la accidentalidad en la Red de Carreteras del Estado
 Los costes de la accidentalidad en la Red de Carreteras del Estado Un criterio objetivo para la política de mantenimiento de carreteras 17 de abril de 2013 índice Objetivos Introducción a la inversión
Los costes de la accidentalidad en la Red de Carreteras del Estado Un criterio objetivo para la política de mantenimiento de carreteras 17 de abril de 2013 índice Objetivos Introducción a la inversión
Covarianza y coeficiente de correlación
 Covarianza y coeficiente de correlación Cuando analizábamos las variables unidimensionales considerábamos, entre otras medidas importantes, la media y la varianza. Ahora hemos visto que estas medidas también
Covarianza y coeficiente de correlación Cuando analizábamos las variables unidimensionales considerábamos, entre otras medidas importantes, la media y la varianza. Ahora hemos visto que estas medidas también
PA 08 Gestión de los documentos y
 CÓDIGO VERSIÓN FECHA MOTIVO MODIFICACIÓN PA 08 Inicial 01/06/2010 ELABORADO POR: REVISADO POR: APROBADO POR: Equipo Directivo de la EUCC Unidad Técnica de Calidad de la Junta de Centro UAH Firma: José
CÓDIGO VERSIÓN FECHA MOTIVO MODIFICACIÓN PA 08 Inicial 01/06/2010 ELABORADO POR: REVISADO POR: APROBADO POR: Equipo Directivo de la EUCC Unidad Técnica de Calidad de la Junta de Centro UAH Firma: José
CAPÍTULO VI PREPARACIÓN DEL MODELO EN ALGOR. En este capítulo, se hablará acerca de los pasos a seguir para poder realizar el análisis de
 CAPÍTULO VI PREPARACIÓN DEL MODELO EN ALGOR. En este capítulo, se hablará acerca de los pasos a seguir para poder realizar el análisis de cualquier modelo en el software Algor. La preparación de un modelo,
CAPÍTULO VI PREPARACIÓN DEL MODELO EN ALGOR. En este capítulo, se hablará acerca de los pasos a seguir para poder realizar el análisis de cualquier modelo en el software Algor. La preparación de un modelo,
CAPÍTULO V. CONCLUSIONES Y RECOMENDACIONES. La franquicia es una figura jurídica regulada en la ley de propiedad industrial,
 CAPÍTULO V. CONCLUSIONES Y RECOMENDACIONES. La franquicia es una figura jurídica regulada en la ley de propiedad industrial, en donde de acuerdo a ésta ley, destacan ciertas características fundamentales,
CAPÍTULO V. CONCLUSIONES Y RECOMENDACIONES. La franquicia es una figura jurídica regulada en la ley de propiedad industrial, en donde de acuerdo a ésta ley, destacan ciertas características fundamentales,
ESTRATEGIA DE DINAMARCA: INFORME SOBRE EL FUTURO DEL ENTORNO LABORAL
 ESTRATEGIA DE DINAMARCA: INFORME SOBRE EL FUTURO DEL ENTORNO LABORAL NUEVAS PRIORIDADES PARA EL ENTORNO LABORAL ESTRATEGIA DE DINAMARCA: INFORME SOBRE EL FUTURO DEL ENTORNO LABORAL Página 1 ÍNDICE INTRODUCCIÓN
ESTRATEGIA DE DINAMARCA: INFORME SOBRE EL FUTURO DEL ENTORNO LABORAL NUEVAS PRIORIDADES PARA EL ENTORNO LABORAL ESTRATEGIA DE DINAMARCA: INFORME SOBRE EL FUTURO DEL ENTORNO LABORAL Página 1 ÍNDICE INTRODUCCIÓN
Caracterización de las OPFH de Tomate en Extremadura
 ACTAS DE HORTICULTURA N O 5 Caracterización de las OPFH de Tomate en Extremadura Montaño, A. 1 ; Llerena J.L. 1, ; Pérez, C. 1, Hernández, M. 1 1 Centro Tecnológico Agroalimentario Nacional Extremadura
ACTAS DE HORTICULTURA N O 5 Caracterización de las OPFH de Tomate en Extremadura Montaño, A. 1 ; Llerena J.L. 1, ; Pérez, C. 1, Hernández, M. 1 1 Centro Tecnológico Agroalimentario Nacional Extremadura
GESTIÓN DE LA CALIDAD
 Página: 1 de 5 DEFINICIÓN GESTIÓN DE LA CALIDAD Actividades coordinadas para dirigir y controlar una organización en lo relativo a la calidad, incluye el establecimiento de la política, los objetivos,
Página: 1 de 5 DEFINICIÓN GESTIÓN DE LA CALIDAD Actividades coordinadas para dirigir y controlar una organización en lo relativo a la calidad, incluye el establecimiento de la política, los objetivos,
También se relacionan los ratios superficie forestal por funcionario técnico en las mismas CCAA.
 PRIMER CONGRESO PROFESIONAL DE LOS INGENIEROS DE MONTES Sesión 5ª: El de Montes en las Administraciones Públicas y en Organismos Internacionales. Comunicación: Los puestos para s de Montes en la Administración
PRIMER CONGRESO PROFESIONAL DE LOS INGENIEROS DE MONTES Sesión 5ª: El de Montes en las Administraciones Públicas y en Organismos Internacionales. Comunicación: Los puestos para s de Montes en la Administración
PREGUNTAS DE RESPUESTA CORTA SELECTIVIDAD TEMA 4:
 PREGUNTAS DE RESPUESTA CORTA SELECTIVIDAD TEMA 4: 1. La organización formal e informal en la empresa. La organización formal se define como la estructura intencional definida e identificada en que la empresa
PREGUNTAS DE RESPUESTA CORTA SELECTIVIDAD TEMA 4: 1. La organización formal e informal en la empresa. La organización formal se define como la estructura intencional definida e identificada en que la empresa
REGLAMENTO DEL TRABAJO DE FIN DE GRADO
 REGLAMENTO DEL TRABAJO DE FIN DE GRADO Exposición de motivos El Real Decreto 1393/2007, de 29 de octubre, por el cual se establece la ordenación de las enseñanzas universitarias oficiales, modificado por
REGLAMENTO DEL TRABAJO DE FIN DE GRADO Exposición de motivos El Real Decreto 1393/2007, de 29 de octubre, por el cual se establece la ordenación de las enseñanzas universitarias oficiales, modificado por
Introducción. Ciclo de vida de los Sistemas de Información. Diseño Conceptual
 Introducción Algunas de las personas que trabajan con SGBD relacionales parecen preguntarse porqué deberían preocuparse del diseño de las bases de datos que utilizan. Después de todo, la mayoría de los
Introducción Algunas de las personas que trabajan con SGBD relacionales parecen preguntarse porqué deberían preocuparse del diseño de las bases de datos que utilizan. Después de todo, la mayoría de los
MUESTREO TIPOS DE MUESTREO
 MUESTREO En ocasiones en que no es posible o conveniente realizar un censo (analizar a todos los elementos de una población), se selecciona una muestra, entendiendo por tal una parte representativa de
MUESTREO En ocasiones en que no es posible o conveniente realizar un censo (analizar a todos los elementos de una población), se selecciona una muestra, entendiendo por tal una parte representativa de
Capítulo IV. Manejo de Problemas
 Manejo de Problemas Manejo de problemas Tabla de contenido 1.- En qué consiste el manejo de problemas?...57 1.1.- Ventajas...58 1.2.- Barreras...59 2.- Actividades...59 2.1.- Control de problemas...60
Manejo de Problemas Manejo de problemas Tabla de contenido 1.- En qué consiste el manejo de problemas?...57 1.1.- Ventajas...58 1.2.- Barreras...59 2.- Actividades...59 2.1.- Control de problemas...60
PARA COMERCIANTES Y AUTÓNOMOS. INFORMACIÓN SOBRE TARJETAS DE CRÉDITO.
 PARA COMERCIANTES Y AUTÓNOMOS. INFORMACIÓN SOBRE TARJETAS DE CRÉDITO. QUÉ DEBES SABER CUANDO ACEPTAS UNA TARJETA COMO FORMA DE PAGO EN TU ESTABLECIMIENTO? Hace ya muchos años que la mayoría de las microempresas
PARA COMERCIANTES Y AUTÓNOMOS. INFORMACIÓN SOBRE TARJETAS DE CRÉDITO. QUÉ DEBES SABER CUANDO ACEPTAS UNA TARJETA COMO FORMA DE PAGO EN TU ESTABLECIMIENTO? Hace ya muchos años que la mayoría de las microempresas
Capítulo 5: METODOLOGÍA APLICABLE A LAS NORMAS NE AI
 Capítulo 5: METODOLOGÍA APLICABLE A LAS NORMAS NE AI La segunda fase del NIPE corresponde con la adecuación de las intervenciones de enfermería del sistema de clasificación N.I.C. (Nursing Intervention
Capítulo 5: METODOLOGÍA APLICABLE A LAS NORMAS NE AI La segunda fase del NIPE corresponde con la adecuación de las intervenciones de enfermería del sistema de clasificación N.I.C. (Nursing Intervention
FORMULARIO DE DECLARACIÓN DE INVENCIÓN IIS-FJD Documentos adjuntos:
 1 FORMULARIO DE DECLARACIÓN DE INVENCIÓN IIS-FJD Documentos adjuntos: Memoria patente Figuras Lista de secuencias Resumen Cesión de derechos (si procede) Cotitularidad (si procede) Por favor, cumplimente
1 FORMULARIO DE DECLARACIÓN DE INVENCIÓN IIS-FJD Documentos adjuntos: Memoria patente Figuras Lista de secuencias Resumen Cesión de derechos (si procede) Cotitularidad (si procede) Por favor, cumplimente
Entrevista a: ESTHER LIÑÁN. Coordinadora TIC del IES Griñón y Sección de Torrejón de la Calzada.
 Entrevista a: ESTHER LIÑÁN. Coordinadora TIC del IES Griñón y Sección de Torrejón de la Calzada. P: Según he oído, el IES Griñón representa un buen ejemplo de uso e integración de TIC en la Educación.
Entrevista a: ESTHER LIÑÁN. Coordinadora TIC del IES Griñón y Sección de Torrejón de la Calzada. P: Según he oído, el IES Griñón representa un buen ejemplo de uso e integración de TIC en la Educación.
Los principales conceptos para mejorar la gestión de Marketing: preguntas clave
 Los principales conceptos para mejorar la gestión de Marketing: preguntas clave Luis Muñiz Economista y Consultor en sistemas de información y estrategia Nos puede describir que es la gestión de Marketing
Los principales conceptos para mejorar la gestión de Marketing: preguntas clave Luis Muñiz Economista y Consultor en sistemas de información y estrategia Nos puede describir que es la gestión de Marketing
ESTUDIO DEL IMPACTO ECONÓMICO DEL CONJUNTO MONUMENTAL DE LA ALHAMBRA Y GENERALIFE (CMAG) SOBRE LA CIUDAD DE GRANADA
 ESTUDIO DEL IMPACTO ECONÓMICO DEL CONJUNTO MONUMENTAL DE LA ALHAMBRA Y GENERALIFE (CMAG) SOBRE LA CIUDAD DE GRANADA Nota de Prensa Abril 2013 Grup d Anàlisi Quantitativa Regional Institut de Recerca en
ESTUDIO DEL IMPACTO ECONÓMICO DEL CONJUNTO MONUMENTAL DE LA ALHAMBRA Y GENERALIFE (CMAG) SOBRE LA CIUDAD DE GRANADA Nota de Prensa Abril 2013 Grup d Anàlisi Quantitativa Regional Institut de Recerca en
Gestión de la Prevención de Riesgos Laborales. 1
 UNIDAD Gestión de la Prevención de Riesgos Laborales. 1 FICHA 1. LA GESTIÓN DE LA PREVENCIÓN DE RIESGOS LABORALES. FICHA 2. EL SISTEMA DE GESTIÓN DE LA PREVENCIÓN DE RIESGOS LABORALES. FICHA 3. MODALIDAD
UNIDAD Gestión de la Prevención de Riesgos Laborales. 1 FICHA 1. LA GESTIÓN DE LA PREVENCIÓN DE RIESGOS LABORALES. FICHA 2. EL SISTEMA DE GESTIÓN DE LA PREVENCIÓN DE RIESGOS LABORALES. FICHA 3. MODALIDAD
REPRODUCCIÓN DE LAS TABLAS DE CRECIMENTO INFANTIL QUE UTILIZAN LOS PEDIATRAS CON LOS DATOS DE LOS NIÑOS DEL COLEGIO XX
 Página 1 de 12 REPRODUCCIÓN DE LAS TABLAS DE CRECIMENTO INFANTIL QUE UTILIZAN LOS PEDIATRAS CON LOS DATOS DE LOS NIÑOS DEL COLEGIO XX Autoras: Curso: 3º ESO Escuela: Tutora: Fecha: 08 Mayo 2015 Página
Página 1 de 12 REPRODUCCIÓN DE LAS TABLAS DE CRECIMENTO INFANTIL QUE UTILIZAN LOS PEDIATRAS CON LOS DATOS DE LOS NIÑOS DEL COLEGIO XX Autoras: Curso: 3º ESO Escuela: Tutora: Fecha: 08 Mayo 2015 Página
PROCEDIMIENTO DE AUDITORÍAS INTERNAS DEL SISTEMA DE GESTIÓN DE CALIDAD
 Página : 1 de 12 PROCEDIMIENTO DE DEL SISTEMA DE GESTIÓN DE CALIDAD Esta es una copia no controlada si carece de sello en el reverso de sus hojas, en cuyo caso se advierte al lector que su contenido puede
Página : 1 de 12 PROCEDIMIENTO DE DEL SISTEMA DE GESTIÓN DE CALIDAD Esta es una copia no controlada si carece de sello en el reverso de sus hojas, en cuyo caso se advierte al lector que su contenido puede
Modelo de fuerza deportiva NOTA TÉCNICA
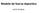 Modelo de fuerza deportiva NOTA TÉCNICA Contenido 1 Motivación 3 2 El modelo de fuerza deportiva 3 2.1 Supuestos del modelo 3 2.2 Críticas al modelo 4 2.3 Formulación 4 2.4 Estimación de los parámetros
Modelo de fuerza deportiva NOTA TÉCNICA Contenido 1 Motivación 3 2 El modelo de fuerza deportiva 3 2.1 Supuestos del modelo 3 2.2 Críticas al modelo 4 2.3 Formulación 4 2.4 Estimación de los parámetros
La prórroga del plazo se gestionará como una nueva solicitud.
 5 PRÉSTAMO DE DOCUMENTOS 5.1 OBJETO 5.1.1 El préstamo de documentos a las unidades productoras tiene como fin dar continuidad a la tramitación de los procedimientos administrativos de la Universidad que
5 PRÉSTAMO DE DOCUMENTOS 5.1 OBJETO 5.1.1 El préstamo de documentos a las unidades productoras tiene como fin dar continuidad a la tramitación de los procedimientos administrativos de la Universidad que
Criterios de Selección de Inversiones: El Valor Actual Neto y sus derivados *.
 Criterios de Selección de Inversiones: El Valor Actual Neto y sus derivados *. Uno de los criterios más válidos para la selección de inversiones alternativas es la determinación del Valor Actual Neto (VAN)
Criterios de Selección de Inversiones: El Valor Actual Neto y sus derivados *. Uno de los criterios más válidos para la selección de inversiones alternativas es la determinación del Valor Actual Neto (VAN)
Evaluación de la capacidad óptima de medida y alcance de la acreditación de un laboratorio de calibración
 Evaluación de la capacidad óptima de medida y alcance de la acreditación de un laboratorio de calibración Fernández Pareja, Mª Teresa te_fer@topografia.upm.es Departamento de Ingeniería Topográfica y Cartografía
Evaluación de la capacidad óptima de medida y alcance de la acreditación de un laboratorio de calibración Fernández Pareja, Mª Teresa te_fer@topografia.upm.es Departamento de Ingeniería Topográfica y Cartografía
