OBTENCIÓN DE UN PAPEL INDICADOR PARTIENDO DE PÉTALOS DE ROSAS, LOMBARDA Y CURRY
|
|
|
- Magdalena Rojas Jiménez
- hace 7 años
- Vistas:
Transcripción
1 OBTENCIÓN DE UN PAPEL INDICADOR PARTIENDO DE PÉTALOS DE ROSAS, LOMBARDA Y CURRY AUTOR JAVIER RUIZ HIDALGO TEMÁTICA QUÍMICA GENERAL ETAPA BACHILLERATO Resumen En el presente artículo vamos a intentar demostrar que podemos utilizar como indicador ácido-base, algunas sustancias cotidianas de origen vegetal, y que se suelen caracterizar por la presencia de pigmentos con colores muy vivos. En concreto trabajamos con pétalos de rosas rojas, hojas de lombarda y curry. Palabras clave Indicador, curcumina, antocianinas, viraje de un indicador, amarillo de alizarina, tornasol, rojo congo, violeta de metilo, azul de brotimol, rojo neutro, fenolftaleina, naranja de metilo, rojo de metilo, púrpura de cresol, nitramina, rojo de fenol, azul de timol, naranja de etilo, p-nitrofenol, púrpura de bromocresol, rojo de clorofenol, rojo de cresol, timolftaleina, tropeolina, verde de bromocresol y eritrosina disódica. 1. INTRODUCCIÓN En este trabajo pretendemos la obtención de un papel indicador, pero obtenido de forma artesanal. Pretendemos obtener dos papeles indicadores diferentes. Para la obtención de estos papeles indicadores tomaremos como base papel de filtro y sobre este colocaremos o el extracto de pétalos de rosas rojas, o el extracto de lombarda. Para poder ver los colores para los distintos valores de ph, de cada uno de los papeles indicadores, tomaremos una serie de disoluciones de ph conocidos y meteremos tiras de nuestros papeles indicadores, procediendo a un calibrado de nuestros papeles indicadores.
2 Para la preparación de las disoluciones de ph conocidas, emplearemos disoluciones de sosa cáustica y de ácido clorhídrico Indicadores ácido-base Un indicador ácido-base es una sustancia que puede ser una base o un ácido, de manera que esta sustancia y su par conjugado se caracterizan por presentar una coloración muy diferente, de forma que cuando el ph del medio cambia, y con el se produce el cambio de la sustancia en cuestión con su par conjugado se produce un cambio en la tonalidad del indicador, de forma que con este cambio de color del indicador (viraje del indicador) se pone de manifiesto, que ha cambiado el ph de la disolución. Entre los indicadores más frecuentes podemos encontrar los siguientes: Amarillo de alizarina, tornasol, rojo congo, violeta de metilo, azul de brotimol, rojo neutro, fenolftaleina, naranja de metilo, rojo de metilo, púrpura de cresol, nitramina, rojo de fenol, azul de timol, naranja de etilo, p-nitrofenol, púrpura de bromocresol, rojo de clorofenol, rojo de cresol, timolftaleina, tropeolina, verde de bromocresol y eritrosina disódica. En la siguiente tabla se especifican los colores del par tanto en medio ácido como en medio básico, así como en rango de viraje del indicador. Indicador Rango de viraje de ph Color ácido Color base Tornasol 4,5 8 Rojo Azul Fenolftaleína 8 10 Incoloro Violeta Naranja de metilo 3,1 4,4 Rojo Naranja-amarillo Rojo de metilo 4,2 6,2 Rojo Amarillo Podemos usar también como indicadores algunas sustancias naturales, que se caracterizan por presentar una pigmentación muy fuerte. Entre estas sustancias podemos destacar: cebolla morada, el curry, pétalos de rosas, lombarda y repollo morado. En el presenta artículo vamos a estudiar el comportamiento como indicador del curry, la lombarda y los pétalos de rosas rojas Antocianinas Las antocianinas son unos pigmentos solubles en agua, que pueden tener tonalidades muy variables, rojo, azul, violeta, etc. Suelen presentar coloración roja en medio ácido, una coloración más violeta en un ph neutro y una coloración más azulada en medio básico.
3 1.3. Curcuminas La curcumina es una sustancia que la podemos encontrar en el curry. La curcumina procede de una planta con el mismo nombre, la cual procede de la India. La sustancia que presenta el carácter ácido/base en la curcumina es el polifenol curcumina, esta es una sustancia que le da al curry su tonalidad tan característica entre amarillo y marrón Papel indicador El papel indicador es un papel que lleva una mezcla de indicadores, de manera que presenta una tonalidad diferente para cada unidad de ph. Por esa razón es muy útil en un laboratorio de química, para poder determinar el ph de una disolución sin más qué tomar una gotita de esta, echarla sobre el papel indicador, observar el color del indicador y compararlo con la escala de colores de ese indicador. Por lo general se suele emplear para la fabricación de papel indicador, papel de filtro y como indicador se emplea para impregnarlo en tornasol, de ahí que en diversas fuentes bibliográficas se le llame papel tornasol. 2. MATERIAL Para la realización del presente trabajo experimental vamos a utilizar el siguiente material: - Botella de plástico transparente de 2 litros con su tapón - Embudo - Anilla para embudo - Nuez fijadora - Soporte - Papel de filtro - Pipeta - Vaso de precipitados - Matraz aforado de un litro - Frasco lavador 3. REACTIVOS Para la realización del presente trabajo experimental vamos a utilizar los siguientes reactivos:
4 - Curry (50 g) - Hojas de lombarda (100 g) - Pétalos de rosas rojas (100 g) - Sosa cáustica - Ácido clorhídrico - Agua desionizada 4. PREPARACIÓN DE LAS DISOLUCIONES DE ph CONOCIDO Vamos a preparar 15 disoluciones de ph conocidos y que vayan de un en uno en la escala de ph. Para eso procedemos de la siguiente manera. - ph = 0 Preparamos una disolución 1M de HCl - ph = 1 Tomamos 100 ml de la disolución anterior con una pipeta y los echamos en un matraz - ph = 2 Tomamos 100 ml de la disolución anterior con una pipeta y los echamos en un matraz - ph = 3 Tomamos 100 ml de la disolución anterior con una pipeta y los echamos en un matraz - ph = 4 Tomamos 100 ml de la disolución anterior con una pipeta y los echamos en un matraz - ph = 5 Tomamos 100 ml de la disolución anterior con una pipeta y los echamos en un matraz - ph = 6 Tomamos 100 ml de la disolución anterior con una pipeta y los echamos en un matraz - ph = 7 Tomamos agua desionizada - ph = 14 Preparamos una disolución 1M de NaOH. - ph = 13 Tomamos 100 ml de la disolución anterior con una pipeta y los echamos en un matraz - ph = 12 Tomamos 100 ml de la disolución anterior con una pipeta y los echamos en un matraz - ph = 11 Tomamos 100 ml de la disolución anterior con una pipeta y los echamos en un matraz - ph = 10 Tomamos 100 ml de la disolución anterior con una pipeta y los echamos en un matraz
5 - ph = 9 Tomamos 100 ml de la disolución anterior con una pipeta y los echamos en un matraz - ph = 8 Tomamos 100 ml de la disolución anterior con una pipeta y los echamos en un matraz 5. PREPARACIÓN DEL PAPEL INDICADOR 3.1. Preparación del indicador Elaboramos tres indicadores uno con curry, otro con lombarda y el último con pétalos de rosas rojas. Debemos buscar una lombarda lo más morada posible, así como debemos buscar pétalos de rosas rojas lo más rojas posibles. Sí la lombarda es muy morada eso indica (el color muy acentuado) que tiene una gran cantidad de antocianina, de ahí que el indicador que pretendemos obtener será tanto mejor cuanto mayor sea la cantidad de esta sustancia presente en la lombarda. Sí los pétalos de rosa son muy rojos eso indica (el color muy acentuado) que tiene una gran cantidad de antocianina, de ahí que el indicador que pretendemos obtener será tanto mejor cuanto mayor sea la cantidad de esta sustancia presente en los pétalos de rosa. Tomamos 100 gramos de lombarda, los cortamos en trocitos muy pequeños. Tomamos una botella de refresco de 2 litros de volumen de plástico. En la botella metemos los trocitos de lombarda y le añadimos 100 mililitros de alcohol etílico. Tapamos la botella con su tapón. Colocamos la botella al sol y la dejamos durante unos 15 días. Así obtenemos un extracto alcohólico de antocianina, procedente de la lombarda. Transcurrido ese periodo, tomamos la mezcla y la vertimos en un embudo sobre el que previamente se ha colocado papel de filtro, bajo el embudo colocamos un vaso de precipitados, así nos quedará, los restos sólidos de la lombarda en el papel de filtro, y en el vaso de precipitados el extracto alcohólico de antocianina. Tomamos 100 gramos de pétalos de rosas rojas, los cortamos en trocitos muy pequeños. Tomamos una botella de refresco de 2 litros de volumen de plástico. En la botella metemos los trocitos de pétalos de rosas rojas y le añadimos 100 mililitros de alcohol etílico. Tapamos la botella con su tapón. Colocamos la botella al sol y la dejamos durante unos 15 días. Así obtenemos un extracto alcohólico de antocianina, procedente de los pétalos de rosas rojas. Transcurrido ese periodo, tomamos la mezcla y la vertimos en un embudo sobre el que previamente se ha colocado papel de filtro, bajo el embudo colocamos un vaso de precipitados, así nos quedará, los
6 restos sólidos de los pétalos de rosas rojas en el papel de filtro, y en el vaso de precipitados el extracto alcohólico de antocianina. Tomamos 50 gramos de curry en polvo, del que se utiliza en restauración como especia para condimentar comidas. Tomamos una botella de refresco de 2 litros de volumen de plástico. En la botella metemos el curry y le añadimos 100 mililitros de alcohol etílico. Tapamos la botella con su tapón. Colocamos la botella al sol y la dejamos durante unos 15 días. Así obtenemos un extracto alcohólico de curcumina, procedente del curry. Transcurrido ese periodo, tomamos la mezcla y la vertimos en un embudo sobre el que previamente se ha colocado papel de filtro, bajo el embudo colocamos un vaso de precipitados, así nos quedará, los restos sólidos del curry en el papel de filtro, y en el vaso de precipitados el extracto alcohólico de curcumina Obtención del papel indicador Una vez que tenemos los tres extractos alcohólico, uno de curcumina y dos de antocianina, tomamos tres grupos de 15 tiras de papel de filtro cada uno. Sumergimos completamente 15 tiras de papel de filtro en cada una de las tres disoluciones. Seguidamente dejamos secar a temperatura ambiente las 15 tiritas de papel de filtro de cada uno de los tres grupos indicados anteriormente. Seguidamente colocaremos cada una de las 15 tiras de papel (ya seco) de cada uno de los tres extractos, en 15 disoluciones de ph conocidos y de valores: 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13 y 14 Posteriormente vamos anotando los colores que corresponde a cada uno de los valores de ph, para ver si efectivamente podemos emplear estas sustancias como indicadores Resultados obtenidos Las antocianinas están presentes tanto en la lombarda como en los pétalos de rosas rojas. Los colores que presentan estas sustancias en función del ph se detallan en las siguientes tablas: Lombarda Color Rojo Violeta Azul Verde Amarillo ph Pétalos de rosas rojas
7 Color ISSN DEP. LEGAL: GR 2922/2007 Rojo y violeta claro Violeta a gris Amarillo Verde Marrón ph La curcumina está presente que está presente en el curry, presenta los siguientes colores en función del ph del medio. Curry Color ph Amarillo Naranja Marrón oscuro 6. CONCLUSIONES - El la curcumina procendente del curry está de color amarillo en medio ácido, naranja a ph neutro y marrón oscuro en medio básico. - Las antocianinas procedentes de los pétalos de rosas rojas, son de color rojo o violeta claro en medio ácido, violeta o gris a ph neutro y verde o amarillo en medio básico. - Las antocianinas procedentes de la lombarda, son de color rojo a violeta en medio ácido, a ph neutro azul y en medio básico de verde a amarillo. - Las antocianinas procedentes de la lombarda y los pétalos de rosas rojas pueden servir para la obtención de un papel indicador, como el tornasol, ya que presentan prácticamente un color diferente para cada unidad de ph. - La curcumina procendente del curry por el contrario no presenta la gradación cromática anterior, por lo que no es una sustancia adecuada para la obtención de un papel indicador. Sin embargo, si podemos utilizarlo para indicar si un determinado medio tiene carácter o bien ácido o bien básico. BIBLIOGRAFÍA - Adams, Jonson and Wilcox (1979). Laboratory Experiments in Organic Chemistry. 7ª ed.. Chicago: MacMillan.
8 - Bates, SChaefer (1977). Técnicas de Investigación en Química Orgánica Experimental. Madrid: Alambra. - Brewster, Vanderwerf y Mcewen (1974). Curso de Química Orgánica Experimental. Madrid: Alambra. - Campbell and McCarthy (1994). Organic Chemistry Experiments, microscale and semi-microscale. Boston: Brooks/Cole. - Fessenden R. J. and Fessenden J. S. (1993). Organic Laboratory Tecnhiques. Boston: Brooks/Cole. - Lozano, J.J: (1983). Fundamentos de Química General. Barcelona: Editorial Alambra. - Morcillo, Jesús (1976). Química General. Madrid: Editorial U.N.E.D. - Gutiérrez Ríos, Enrique (1998). Química Inorgánica. Madrid: Reverte - Lotear, Beyer (2000). Química Inorgánica. Barcelona: Editorial Ariel Autoría Nombre y Apellidos: Javier Ruiz Hidalgo Centro, localidad, provincia: IES Américo Castro, Huetor-Tajar, Granada javierruizh@hotmail.com
ESTUDIO SOBRE LA DESNATURALIZACIÓN DE PROTEÍNAS Y DETERMINACIÓN DE ALGUNAS PROPIEDADES DE LAS PROTEÍNAS CON SEGUNDO DE BACHILLERARO
 ESTUDIO SOBRE LA DESNATURALIZACIÓN DE PROTEÍNAS Y DETERMINACIÓN DE ALGUNAS PROPIEDADES DE LAS PROTEÍNAS CON SEGUNDO DE BACHILLERARO AUTOR JAVIER RUIZ HIDALGO TEMÁTICA PROTEINAS ETAPA BACHILLERATO Resumen
ESTUDIO SOBRE LA DESNATURALIZACIÓN DE PROTEÍNAS Y DETERMINACIÓN DE ALGUNAS PROPIEDADES DE LAS PROTEÍNAS CON SEGUNDO DE BACHILLERARO AUTOR JAVIER RUIZ HIDALGO TEMÁTICA PROTEINAS ETAPA BACHILLERATO Resumen
MATERIAL DIDÁCTICO DE LOS HIDROCARBUROS AROMÁTICOS
 MATERIAL DIDÁCTICO DE LOS HIDROCARBUROS AROMÁTICOS AUTOR JAVIER RUIZ HIDALGO TEMÁTICA QUÍMICA ORGÁNICA ETAPA BACHILLERATO Resumen En el presente artículo vamos a ver una serie de fotos de representaciones
MATERIAL DIDÁCTICO DE LOS HIDROCARBUROS AROMÁTICOS AUTOR JAVIER RUIZ HIDALGO TEMÁTICA QUÍMICA ORGÁNICA ETAPA BACHILLERATO Resumen En el presente artículo vamos a ver una serie de fotos de representaciones
DETERMINACIÓN EXPERIMENTAL DEL ORDEN DE UNA REACCIÓN QUÍMICA PARA SEGUNDO DE BACHILLERATO
 DETERMINACIÓN EXPERIMENTAL DEL ORDEN DE UNA REACCIÓN QUÍMICA PARA SEGUNDO DE BACHILLERATO AUTOR JAVIER RUIZ HIDALGO TEMÁTICA CINÉTICA QUÍMICA ETAPA BACHILLERATO Resumen En el presente artículo vamos a
DETERMINACIÓN EXPERIMENTAL DEL ORDEN DE UNA REACCIÓN QUÍMICA PARA SEGUNDO DE BACHILLERATO AUTOR JAVIER RUIZ HIDALGO TEMÁTICA CINÉTICA QUÍMICA ETAPA BACHILLERATO Resumen En el presente artículo vamos a
PROCEDIMIENTO DIDÁCTICO PARA LA REALIZACIÓN DE VALORACIONES ÁCIDO-BASE (CÁLCULO DE LA ACIDEZ DE UN ACEITE DE OLIVA)
 PROCEDIMIENTO DIDÁCTICO PARA LA REALIZACIÓN DE VALORACIONES ÁCIDO-BASE (CÁLCULO DE LA ACIDEZ DE UN ACEITE DE OLIVA) AUTOR JAVIER RUIZ HIDALGO TEMÁTICA REACCIONES DE TRANSFERENCIA DE PROTONES ETAPA BACHILLERATO
PROCEDIMIENTO DIDÁCTICO PARA LA REALIZACIÓN DE VALORACIONES ÁCIDO-BASE (CÁLCULO DE LA ACIDEZ DE UN ACEITE DE OLIVA) AUTOR JAVIER RUIZ HIDALGO TEMÁTICA REACCIONES DE TRANSFERENCIA DE PROTONES ETAPA BACHILLERATO
PREPARACIÓN DE MATERIALES DIDÁCTICOS PARA QUÍMICA POR PARTE DEL ALUMNADO DE LA EDUCACIÓN SECUNDARIA OBLIGATORIA
 PREPARACIÓN DE MATERIALES DIDÁCTICOS PARA QUÍMICA POR PARTE DEL ALUMNADO DE LA EDUCACIÓN SECUNDARIA OBLIGATORIA AUTOR JAVIER RUIZ HIDALGO TEMÁTICA DIDÁCIRTICA DE LA QUÍMICA ETAPA EDUCACIÓN SECUNDARIA OBLIGATORIA
PREPARACIÓN DE MATERIALES DIDÁCTICOS PARA QUÍMICA POR PARTE DEL ALUMNADO DE LA EDUCACIÓN SECUNDARIA OBLIGATORIA AUTOR JAVIER RUIZ HIDALGO TEMÁTICA DIDÁCIRTICA DE LA QUÍMICA ETAPA EDUCACIÓN SECUNDARIA OBLIGATORIA
Titulaciones ácido-base
 Titulaciones ácido-base Contenido de la clase: Introducción Curvas de titulación monofuncionales de ácidos y bases Curvas de titulación polifuncionales de ácidos y bases Comparación de curvas Elección
Titulaciones ácido-base Contenido de la clase: Introducción Curvas de titulación monofuncionales de ácidos y bases Curvas de titulación polifuncionales de ácidos y bases Comparación de curvas Elección
INTRODUCCIÓN DIDÁCTICA A LAS REACCIONES DE PRECIPITACIÓN Y A LAS DE FORMACIÓN DE COMPLEJOS
 INTRODUCCIÓN DIDÁCTICA A LAS REACCIONES DE PRECIPITACIÓN Y A LAS DE FORMACIÓN DE COMPLEJOS AUTOR JAVIER RUIZ HIDALGO TEMÁTICA REACCIONES QUÍMICAS DE PRECIPITACIÓN Y FORMACIÓN DE COMPLEJOS ETAPA BACHILLERATO
INTRODUCCIÓN DIDÁCTICA A LAS REACCIONES DE PRECIPITACIÓN Y A LAS DE FORMACIÓN DE COMPLEJOS AUTOR JAVIER RUIZ HIDALGO TEMÁTICA REACCIONES QUÍMICAS DE PRECIPITACIÓN Y FORMACIÓN DE COMPLEJOS ETAPA BACHILLERATO
DETERMINACIÓN EXPERIMENTAL DEL LAS PROPIEDADES FISICOQUÍMICAS DE UNA EMULSIÓN (ACONDICIONADOR DEL CABELLO) PARA FORMACIÓN PROFESIONAL
 DETERMINACIÓN EXPERIMENTAL DEL LAS PROPIEDADES FISICOQUÍMICAS DE UNA EMULSIÓN (ACONDICIONADOR DEL CABELLO) PARA FORMACIÓN PROFESIONAL AUTOR MANUELA CHAVES JIMÉNEZ TEMÁTICA COSMETOLOGÍA ETAPA CICLO DE FORMATIVO
DETERMINACIÓN EXPERIMENTAL DEL LAS PROPIEDADES FISICOQUÍMICAS DE UNA EMULSIÓN (ACONDICIONADOR DEL CABELLO) PARA FORMACIÓN PROFESIONAL AUTOR MANUELA CHAVES JIMÉNEZ TEMÁTICA COSMETOLOGÍA ETAPA CICLO DE FORMATIVO
DETERMINACIÓN EXPERIMENTAL DEL NÚMERO DE AVOGADRO CON PRIMERO DE BACHILLERATO
 DETERMINACIÓN EXPERIMENTAL DEL NÚMERO DE AVOGADRO CON PRIMERO DE BACHILLERATO AUTOR JAVIER RUIZ HIDALGO TEMÁTICA QUÍMICA GENERAL ETAPA BACHILLERATO Resumen En el presente trabajo, pretendemos determinar
DETERMINACIÓN EXPERIMENTAL DEL NÚMERO DE AVOGADRO CON PRIMERO DE BACHILLERATO AUTOR JAVIER RUIZ HIDALGO TEMÁTICA QUÍMICA GENERAL ETAPA BACHILLERATO Resumen En el presente trabajo, pretendemos determinar
DETERMINACIÓN DE LA ALCALINIDAD DE UN DESATASCADOR COMERCIAL
 DETERMINACIÓN DE LA ALCALINIDAD DE UN DESATASCADOR COMERCIAL AUTORÍA JOAQUÍN RUIZ MOLINA TEMÁTICA CIENCIAS EXPERIMENTALES, QUÍMICA ETAPA BACHILLERATO, FORMACIÓN PROFESIONAL Resumen En las asignaturas como
DETERMINACIÓN DE LA ALCALINIDAD DE UN DESATASCADOR COMERCIAL AUTORÍA JOAQUÍN RUIZ MOLINA TEMÁTICA CIENCIAS EXPERIMENTALES, QUÍMICA ETAPA BACHILLERATO, FORMACIÓN PROFESIONAL Resumen En las asignaturas como
REALIZACIÓN DE UNA DESTILACIÓN DE VINO PARA LA OBTENCIÓN DE ETANOL CON 2º DE BACHILLERATO
 REALIZACIÓN DE UNA DESTILACIÓN DE VINO PARA LA OBTENCIÓN DE ETANOL CON 2º DE BACHILLERATO AUTOR JAVIER RUIZ HIDALGO TEMÁTICA OPERACIONES FÍSICAS DE SEPARACIÓN DE MEZCLAS ETAPA BACHILLERATO Resumen En este
REALIZACIÓN DE UNA DESTILACIÓN DE VINO PARA LA OBTENCIÓN DE ETANOL CON 2º DE BACHILLERATO AUTOR JAVIER RUIZ HIDALGO TEMÁTICA OPERACIONES FÍSICAS DE SEPARACIÓN DE MEZCLAS ETAPA BACHILLERATO Resumen En este
PROYECTO DE INVESTIGACIÓN: DETERMINACIÓN DE AMONÍACO EN UN PRODUCTO COMERCIAL
 PROYECTO DE INVESTIGACIÓN: DETERMINACIÓN DE AMONÍACO EN UN PRODUCTO COMERCIAL AUTORÍA JOAQUÍN RUIZ MOLINA TEMÁTICA CIENCIAS EXPERIMENTALES, QUÍMICA ETAPA BACHILLERATO, FORMACIÓN PROFESIONAL Resumen En
PROYECTO DE INVESTIGACIÓN: DETERMINACIÓN DE AMONÍACO EN UN PRODUCTO COMERCIAL AUTORÍA JOAQUÍN RUIZ MOLINA TEMÁTICA CIENCIAS EXPERIMENTALES, QUÍMICA ETAPA BACHILLERATO, FORMACIÓN PROFESIONAL Resumen En
DETERMINACIÓN DE LA CANTIDAD DE ÁCIDO CLORHÍDRICO PRESENTE EN SALFUMÁN COMERCIAL
 DETERMINACIÓN DE LA CANTIDAD DE ÁCIDO CLORHÍDRICO PRESENTE EN SALFUMÁN COMERCIAL AUTORÍA JOAQUÍN RUIZ MOLINA TEMÁTICA CIENCIAS EXPERIMENTALES, QUÍMICA ETAPA BACHILLERATO, FORMACIÓN PROFESIONAL Resumen
DETERMINACIÓN DE LA CANTIDAD DE ÁCIDO CLORHÍDRICO PRESENTE EN SALFUMÁN COMERCIAL AUTORÍA JOAQUÍN RUIZ MOLINA TEMÁTICA CIENCIAS EXPERIMENTALES, QUÍMICA ETAPA BACHILLERATO, FORMACIÓN PROFESIONAL Resumen
DETERMINACIÓN EXPERIMENTAL DEL LAS PROPIEDADES FISICOQUÍMICAS DE UN ACONDICIONADOR DEL CABELLO (GEL) PARA FORMACIÓN PROFESIONAL
 DETERMINACIÓN EXPERIMENTAL DEL LAS PROPIEDADES FISICOQUÍMICAS DE UN ACONDICIONADOR DEL CABELLO (GEL) PARA FORMACIÓN PROFESIONAL AUTOR MANUELA CHAVES JIMÉNEZ TEMÁTICA COSMETOLOGÍA ETAPA CICLO FORMATIVO
DETERMINACIÓN EXPERIMENTAL DEL LAS PROPIEDADES FISICOQUÍMICAS DE UN ACONDICIONADOR DEL CABELLO (GEL) PARA FORMACIÓN PROFESIONAL AUTOR MANUELA CHAVES JIMÉNEZ TEMÁTICA COSMETOLOGÍA ETAPA CICLO FORMATIVO
OBTENCIÓN EXPERIMENTAL DEL NÚMERO DE AVOGADRO EMPLEANDO EL MÉTODO DE ELECTRODEPOSICIÓN CON PRIMERO DE BACHILLERATO
 OBTENCIÓN EXPERIMENTAL DEL NÚMERO DE AVOGADRO EMPLEANDO EL MÉTODO DE ELECTRODEPOSICIÓN CON PRIMERO DE BACHILLERATO AUTOR JAVIER RUIZ HIDALGO TEMÁTICA QUÍMICA GENERAL ETAPA BACHILLERATO Resumen En el presente
OBTENCIÓN EXPERIMENTAL DEL NÚMERO DE AVOGADRO EMPLEANDO EL MÉTODO DE ELECTRODEPOSICIÓN CON PRIMERO DE BACHILLERATO AUTOR JAVIER RUIZ HIDALGO TEMÁTICA QUÍMICA GENERAL ETAPA BACHILLERATO Resumen En el presente
Trabajo Práctico N 3. Reconocimiento de sustancias ácidas, básicas y neutras. mediante el empleo de indicadores químicos.
 Trabajo Práctico N 3 Reconocimiento de sustancias ácidas, básicas y neutras mediante el empleo de indicadores químicos. Objetivos: Diferenciar mediante el empleo de indicadores u el cambio de color de
Trabajo Práctico N 3 Reconocimiento de sustancias ácidas, básicas y neutras mediante el empleo de indicadores químicos. Objetivos: Diferenciar mediante el empleo de indicadores u el cambio de color de
Práctica de Laboratorio INDICADORES DE ACIDEZ Y BASICIDAD
 Práctica de Laboratorio INDICADORES DE ACIDEZ Y BASICIDAD Objetivo Identificar sustancias de uso cotidiano como ácidas o básicas según la determinación de su ph y de la escala del indicador utilizado.
Práctica de Laboratorio INDICADORES DE ACIDEZ Y BASICIDAD Objetivo Identificar sustancias de uso cotidiano como ácidas o básicas según la determinación de su ph y de la escala del indicador utilizado.
DETERMINACIÓN EXPERIMENTAL DEL CONTENIDO DE ÁCIDO ASCÓRBICO (VITAMINA C) EN UN ZUMO DE NARANJA
 DETERMINACIÓN EXPERIMENTAL DEL CONTENIDO DE ÁCIDO ASCÓRBICO (VITAMINA C) EN UN ZUMO DE NARANJA AUTOR JAVIER RUIZ HIDALGO TEMÁTICA REACCIONES DE OXIDACIÓN-REDUCCIÓN ETAPA BACHILLERATO Resumen En el presente
DETERMINACIÓN EXPERIMENTAL DEL CONTENIDO DE ÁCIDO ASCÓRBICO (VITAMINA C) EN UN ZUMO DE NARANJA AUTOR JAVIER RUIZ HIDALGO TEMÁTICA REACCIONES DE OXIDACIÓN-REDUCCIÓN ETAPA BACHILLERATO Resumen En el presente
PRÁCTICA 2 Determinación espectrofotométrica del pk de un indicador
 Laboratorio de Química Física 1 Grado en Química PRÁCTICA 2 Determinación espectrofotométrica del pk de un indicador Material 2 matraces aforados de 250 ml 1 varilla de vidrio/ 1 pesasustancias/ 1 cuentagotas/
Laboratorio de Química Física 1 Grado en Química PRÁCTICA 2 Determinación espectrofotométrica del pk de un indicador Material 2 matraces aforados de 250 ml 1 varilla de vidrio/ 1 pesasustancias/ 1 cuentagotas/
PRÁCTICAS DE QUÍMICA P-11: Preparación de una disolución 0,1M de Hidróxido de sodio (sosa)
 NOTA: PRÁCTICAS DE QUÍMICA P-11: Preparación de una disolución 0,1M de Hidróxido de sodio (sosa) Alumno: Fecha: Curso: 1. OBJETIVOS - Manejo del material básico de laboratorio. - Aprender a preparar disoluciones
NOTA: PRÁCTICAS DE QUÍMICA P-11: Preparación de una disolución 0,1M de Hidróxido de sodio (sosa) Alumno: Fecha: Curso: 1. OBJETIVOS - Manejo del material básico de laboratorio. - Aprender a preparar disoluciones
FABRICACIÓN ARTESANAL DE COSMÉTICOS PARA FORMACIÓN PROFESIONAL
 FABRICACIÓN ARTESANAL DE COSMÉTICOS PARA FORMACIÓN PROFESIONAL AUTOR MANUELA CHAVES JIMÉNEZ TEMÁTICA COSMETOLOGÍA ETAPA CICLO DE FORMACIÓN PROFESIONAL DE GRADO MEDIO DE IMAGEN PERSONAL Resumen En el presente
FABRICACIÓN ARTESANAL DE COSMÉTICOS PARA FORMACIÓN PROFESIONAL AUTOR MANUELA CHAVES JIMÉNEZ TEMÁTICA COSMETOLOGÍA ETAPA CICLO DE FORMACIÓN PROFESIONAL DE GRADO MEDIO DE IMAGEN PERSONAL Resumen En el presente
EJEMPLO DE ANÁLISIS POR RETROCESO: DETERMINACIÓN DEL SULFATO DE AMONIO PRESENTE EN UNA MUESTRA COMERCIAL
 ISSN 1988-607 DEP. EGA: GR 9/007 Nº 1 ENERO DE 008 EJEMPO DE ANÁISIS POR RETROCESO: DETERMINACIÓN DE SUFATO DE AMONIO PRESENTE EN UNA MUESTRA COMERCIA AUTORÍA JOAQUÍN RUIZ MOINA TEMÁTICA CIENCIAS EXPERIMENTAES,
ISSN 1988-607 DEP. EGA: GR 9/007 Nº 1 ENERO DE 008 EJEMPO DE ANÁISIS POR RETROCESO: DETERMINACIÓN DE SUFATO DE AMONIO PRESENTE EN UNA MUESTRA COMERCIA AUTORÍA JOAQUÍN RUIZ MOINA TEMÁTICA CIENCIAS EXPERIMENTAES,
UD 8. Aplicaciones de los equilibrios ácido-base
 UD 8. Aplicaciones de los equilibrios ácido-base 8.1 Efecto del ion común. 8.2 Disoluciones reguladoras del ph. 8.3 Sistemas reguladores biológicos. 8.4 Valoraciones ácido-base. 8.5 Indicadores ácido-base.
UD 8. Aplicaciones de los equilibrios ácido-base 8.1 Efecto del ion común. 8.2 Disoluciones reguladoras del ph. 8.3 Sistemas reguladores biológicos. 8.4 Valoraciones ácido-base. 8.5 Indicadores ácido-base.
Nombres de los integrantes: Práctica 12 Preparación de disoluciones
 Nombres de los integrantes: 1 Universidad Nacional Autónoma de México Facultad de Química Laboratorio de Química General I Grupo Equipo Práctica 12 Preparación de disoluciones Problemas: 1. Preparar 50mL
Nombres de los integrantes: 1 Universidad Nacional Autónoma de México Facultad de Química Laboratorio de Química General I Grupo Equipo Práctica 12 Preparación de disoluciones Problemas: 1. Preparar 50mL
Práctica 4: Termoquímica: Valoraciones
 Práctica 4: Termoquímica: Valoraciones Ingeniería agrónoma grado en hortofruticultura y jardinería Jorge Cerezo Martínez Objetivos Comprender el fundamento de las valoraciones químicas. Aplicar la metodología
Práctica 4: Termoquímica: Valoraciones Ingeniería agrónoma grado en hortofruticultura y jardinería Jorge Cerezo Martínez Objetivos Comprender el fundamento de las valoraciones químicas. Aplicar la metodología
Reacciones de transferencia de protones
 Reacciones de transferencia de protones 4. Aplicar la teoría de Brönsted para reconocer las sustancias que pueden actuar como ácidos o bases, saber determinar el ph de sus disoluciones, explicar las reacciones
Reacciones de transferencia de protones 4. Aplicar la teoría de Brönsted para reconocer las sustancias que pueden actuar como ácidos o bases, saber determinar el ph de sus disoluciones, explicar las reacciones
Química. Equilibrio ácido-base Nombre:
 Química DEPARTAMENTO DE FÍSICA E QUÍMICA Equilibrio ácido-base 25-02-08 Nombre: Cuestiones y problemas 1. a) Qué concentración tiene una disolución de amoníaco de ph =10,35? [1½ PUNTO] b) Qué es una disolución
Química DEPARTAMENTO DE FÍSICA E QUÍMICA Equilibrio ácido-base 25-02-08 Nombre: Cuestiones y problemas 1. a) Qué concentración tiene una disolución de amoníaco de ph =10,35? [1½ PUNTO] b) Qué es una disolución
PRÁCTICA Nº 7 SOLUCIONES AMORTIGUADORAS Y CURVAS DE TITULACIÓN
 PRÁCTICA Nº 7 SOLUCIONES AMORTIGUADORAS Y CURVAS DE TITULACIÓN OBJETIVOS Demostrar que el ph de una solución amortiguadora no depende de la concentración de sus componentes. Comprobar las propiedades de
PRÁCTICA Nº 7 SOLUCIONES AMORTIGUADORAS Y CURVAS DE TITULACIÓN OBJETIVOS Demostrar que el ph de una solución amortiguadora no depende de la concentración de sus componentes. Comprobar las propiedades de
Apéndice C. Formato de Pruebas
 Apéndice C Formato de Pruebas C.1 Alcalinidad Libre del Desengrase El método químico para determinar la alcalinidad libre es: 1. Tomar una muestra de 10 ml de la solución de CX y transferirlos a un matraz
Apéndice C Formato de Pruebas C.1 Alcalinidad Libre del Desengrase El método químico para determinar la alcalinidad libre es: 1. Tomar una muestra de 10 ml de la solución de CX y transferirlos a un matraz
3. Para preparar disoluciones de concentración molar específica, qué tipo de material de vidrio se recomienda usar?
 Equipo: Práctica 11: Preparación de disoluciones Preguntas a responder al final de la sesión En la preparación de disoluciones Para cuáles expresiones de concentración es fundamental conocer el volumen
Equipo: Práctica 11: Preparación de disoluciones Preguntas a responder al final de la sesión En la preparación de disoluciones Para cuáles expresiones de concentración es fundamental conocer el volumen
OBTENCIÓN DE UN CHAMPÚ NATURAL CON ALUMNOS/AS DE FORMACIÓN PROFESIONAL
 OBTENCIÓN DE UN CHAMPÚ NATURAL CON ALUMNOS/AS DE FORMACIÓN PROFESIONAL AUTOR MANUELA CHAVES JIMÉNEZ TEMÁTICA COSMOTOLOGÍA ETAPA CICLO FORMATIVO DE PELUQUERÍA Resumen En el presente trabajo, comenzamos
OBTENCIÓN DE UN CHAMPÚ NATURAL CON ALUMNOS/AS DE FORMACIÓN PROFESIONAL AUTOR MANUELA CHAVES JIMÉNEZ TEMÁTICA COSMOTOLOGÍA ETAPA CICLO FORMATIVO DE PELUQUERÍA Resumen En el presente trabajo, comenzamos
CONCURSO CRISTALIZACIÓN EN LA ESCUELA
 Realizado por: -Raquel Bolívar Soria -Sara Lastra Antón -David Machicado Fernández IES Victoria Kent Ampliación de Física y Química 4ºESO ESTANQUE Mayo-2016 CRISTALIZADO CONCURSO CRISTALIZACIÓN EN LA ESCUELA
Realizado por: -Raquel Bolívar Soria -Sara Lastra Antón -David Machicado Fernández IES Victoria Kent Ampliación de Física y Química 4ºESO ESTANQUE Mayo-2016 CRISTALIZADO CONCURSO CRISTALIZACIÓN EN LA ESCUELA
Práctica 9. Ácidos y bases fuertes y débiles
 Práctica 9. Ácidos y bases fuertes y débiles PREGUNTAS A RESPONDER AL FINAL DE LA PRÁCTICA Cómo es la acidez total de un ácido débil en relación con su acidez libre en disolución? Cómo es la basicidad
Práctica 9. Ácidos y bases fuertes y débiles PREGUNTAS A RESPONDER AL FINAL DE LA PRÁCTICA Cómo es la acidez total de un ácido débil en relación con su acidez libre en disolución? Cómo es la basicidad
Reactivos Química Meyer SOLUCIONES Presentación
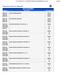 LISTA MEYER N.17 CORRECCIONES 08 NOVIEMBRE-2016.xlsx Página 1 Reactivos Química Meyer Catálogo SOLUCIONES Descripción Presentación 8000-125 ACETO CARMIN SOLUCIÓN 125 ml 8000-250 250 ml 8000-500 500 ml
LISTA MEYER N.17 CORRECCIONES 08 NOVIEMBRE-2016.xlsx Página 1 Reactivos Química Meyer Catálogo SOLUCIONES Descripción Presentación 8000-125 ACETO CARMIN SOLUCIÓN 125 ml 8000-250 250 ml 8000-500 500 ml
UNIVERSIDAD NACIONAL AUTÓNOMA DE MÉXICO FACULTAD DE QUÍMICA LABORATORIO DE QUÍMICA GENERAL II Grupo: Equipo: Nombre: Nombre: Nombre: Nombre: Nombre:
 UNIVERSIDAD NACIONAL AUTÓNOMA DE MÉXICO FACULTAD DE QUÍMICA LABORATORIO DE QUÍMICA GENERAL II Grupo: Equipo: 1 Práctica 9 fuertes y débiles Problemas Estimar comparativamente la acidez libre en una disolución
UNIVERSIDAD NACIONAL AUTÓNOMA DE MÉXICO FACULTAD DE QUÍMICA LABORATORIO DE QUÍMICA GENERAL II Grupo: Equipo: 1 Práctica 9 fuertes y débiles Problemas Estimar comparativamente la acidez libre en una disolución
Reactivos Química Meyer LISTA DE PRECIOS No.18
 LISTA MEYER No.18-2017 ultima modificacion 22 MAYO 2017 (1) Página 1 Reactivos Química Meyer LISTA DE PRECIOS No.18 Vigencia a partir del 02 de enero 2017 SOLUCIONES Catálogo Descripción Presentación precios
LISTA MEYER No.18-2017 ultima modificacion 22 MAYO 2017 (1) Página 1 Reactivos Química Meyer LISTA DE PRECIOS No.18 Vigencia a partir del 02 de enero 2017 SOLUCIONES Catálogo Descripción Presentación precios
Práctica 1. Preparación de disoluciones y determinación de la concentración de una disolución por medio de una valoración.
 1 Nombres Grupo Equipo Primera parte Práctica 1. Preparación de disoluciones y determinación de la concentración de una disolución por medio de una valoración. Problemas: - Preparar disoluciones aproximadamente
1 Nombres Grupo Equipo Primera parte Práctica 1. Preparación de disoluciones y determinación de la concentración de una disolución por medio de una valoración. Problemas: - Preparar disoluciones aproximadamente
COLEGIO DE BACHILLERES PLANTEL 5 SATÉLITE PRÁCTICAS DE LABORATORIO QUÍMICA II TERCER SEMESTRE
 COLEGIO DE BACHILLERES PLANTEL 5 SATÉLITE PRÁCTICAS DE LABORATORIO QUÍMICA II TERCER SEMESTRE 1 2 3 4 PRACTICA # 1 NOMENCLATURA QUÍMICA OBJETIVO DE LA PRÁCTICA: Identificar los aniones y cationes que forman
COLEGIO DE BACHILLERES PLANTEL 5 SATÉLITE PRÁCTICAS DE LABORATORIO QUÍMICA II TERCER SEMESTRE 1 2 3 4 PRACTICA # 1 NOMENCLATURA QUÍMICA OBJETIVO DE LA PRÁCTICA: Identificar los aniones y cationes que forman
OBTENCIÓN DE INDICADORES DEL TIPO DE LAS FTALEÍNAS FENOLFTALEÍNA Y FLUORESCEINA
 EXPERIMENT No. 8 BTENCIÓN DE INDICADRES DEL TIP DE LAS FTALEÍNAS FENLFTALEÍNA Y FLURESCEINA BJETIVS a) El alumno aprenda los métodos de síntesis de colorantes del tipo de las ftaleínas, por condensación
EXPERIMENT No. 8 BTENCIÓN DE INDICADRES DEL TIP DE LAS FTALEÍNAS FENLFTALEÍNA Y FLURESCEINA BJETIVS a) El alumno aprenda los métodos de síntesis de colorantes del tipo de las ftaleínas, por condensación
Problemas disoluciones
 Problemas disoluciones Determinar la concentración de una disolución expresada de diferentes formas: g/l, % en masa y en volumen, Molaridad y fracción molar Preparar disoluciones a partir de solutos sólidos
Problemas disoluciones Determinar la concentración de una disolución expresada de diferentes formas: g/l, % en masa y en volumen, Molaridad y fracción molar Preparar disoluciones a partir de solutos sólidos
= 10. TRABAJO PRÁCTICO: ph. TP ph 1/5
 TRABAJO PRÁCTICO: ph INTRODUCCIÓN: En el estudio de las reacciones ácido base en disolución acuosa, las magnitudes más importantes son las concentraciones de los iones hidrógeno (H +, también llamado protón
TRABAJO PRÁCTICO: ph INTRODUCCIÓN: En el estudio de las reacciones ácido base en disolución acuosa, las magnitudes más importantes son las concentraciones de los iones hidrógeno (H +, también llamado protón
C. Ntra. Sra. de Loreto Prácticas de laboratorio
 CARACTERÍSTICAS DE ÁCIDOS Y BASES. Ácidos: Son corrosivos para la piel. Disuelven sustancias Atacan a los metales desprendiendo H 2. Pierden sus propiedades al reaccionar con bases. Bases: Suaves al tacto
CARACTERÍSTICAS DE ÁCIDOS Y BASES. Ácidos: Son corrosivos para la piel. Disuelven sustancias Atacan a los metales desprendiendo H 2. Pierden sus propiedades al reaccionar con bases. Bases: Suaves al tacto
PRÁCTICA Nº 2 OPERACIONES COMUNES EN UN LABORATORIO
 PRÁCTICA Nº 2 OPERACIONES COMUNES EN UN LABORATORIO OBJETIVO Utilizar el material de laboratorio en las operaciones más comunes realizadas en un laboratorio de química. I. ASPECTOS TEÓRICOS Una vez conocido
PRÁCTICA Nº 2 OPERACIONES COMUNES EN UN LABORATORIO OBJETIVO Utilizar el material de laboratorio en las operaciones más comunes realizadas en un laboratorio de química. I. ASPECTOS TEÓRICOS Una vez conocido
DESTILACIÓN SIMPLE Y FRACCIONADA. a) Conocer una destilación simple, sus principales características y factores que en ella intervienen.
 DESTILACIÓN SIMPLE Y FRACCIONADA I. OBJETIVOS a) Conocer una destilación simple, sus principales características y factores que en ella intervienen. b) Conocer una destilación fraccionada, sus principales
DESTILACIÓN SIMPLE Y FRACCIONADA I. OBJETIVOS a) Conocer una destilación simple, sus principales características y factores que en ella intervienen. b) Conocer una destilación fraccionada, sus principales
Materiales Pipetas ;Tubos de ensayo ;Vaso de precipitado ;Sistema calentador (placa calefactora) ;Probeta
 PRÁCTICA 3: Lluvia de oro Parte cualitativa En primer lugar, de forma cualitativa, se demuestra que la lluvia de oro es una reacción iónica y por tanto muy rápida. Esta parte consta de la formación de
PRÁCTICA 3: Lluvia de oro Parte cualitativa En primer lugar, de forma cualitativa, se demuestra que la lluvia de oro es una reacción iónica y por tanto muy rápida. Esta parte consta de la formación de
TEMA 3. Preparación de disoluciones Concentración de disoluciones. Física y Química 3º ESO
 TEMA 3 Preparación de disoluciones Concentración de disoluciones Física y Química 3º ESO Cuando preparamos una disolución estamos mezclando al menos dos componentes o sustancias. Una de ellas es el disolvente,
TEMA 3 Preparación de disoluciones Concentración de disoluciones Física y Química 3º ESO Cuando preparamos una disolución estamos mezclando al menos dos componentes o sustancias. Una de ellas es el disolvente,
OBTENCIÓN DE COLORANTES AZOICOS ANARANJADO DE METILO Y NARANJA II
 EXPERIMENTO No. 5 OBTENCIÓN DE COLORANTES AZOICOS ANARANJADO DE METILO Y NARANJA II OBJETIVOS a) Enseñar al alumno la técnica de preparación de sales de diazonio, usadas para sintetizar los colorantes
EXPERIMENTO No. 5 OBTENCIÓN DE COLORANTES AZOICOS ANARANJADO DE METILO Y NARANJA II OBJETIVOS a) Enseñar al alumno la técnica de preparación de sales de diazonio, usadas para sintetizar los colorantes
Manual del usuario. Software de Química Valoraciones ácido-base para Windows. WinVal Versión 2.0.2
 Manual del usuario WinVal Versión 2.0.2 Software de Química Valoraciones ácido-base para Windows Windows XP - Windows Vista - Windows 7 - Windows 8 - Windows 10 S O F T W A R E Referencia: VABY www.vaxasoftware.com
Manual del usuario WinVal Versión 2.0.2 Software de Química Valoraciones ácido-base para Windows Windows XP - Windows Vista - Windows 7 - Windows 8 - Windows 10 S O F T W A R E Referencia: VABY www.vaxasoftware.com
OBJETIVO Aprender a preparar disoluciones de concentración dada, ya que la mayor parte de las reacciones químicas tienen lugar en forma de disolución.
 OBJETIVO Aprender a preparar disoluciones de concentración dada, ya que la mayor parte de las reacciones químicas tienen lugar en forma de disolución. FUNDAMENTO TEÓRICO Una disolución es una mezcla homogénea
OBJETIVO Aprender a preparar disoluciones de concentración dada, ya que la mayor parte de las reacciones químicas tienen lugar en forma de disolución. FUNDAMENTO TEÓRICO Una disolución es una mezcla homogénea
PRÁCTICA 5 VALORACIÓN ÁCIDO-BASE
 PRÁCTICA 5 VALORACIÓN ÁCIDO-BASE OBJETIVO Determinar concentraciones desconocidas de ácidos y bases. I. FUNDAMENTO TEÓRICO Las cantidades de reaccionantes y productos de una reacción, son investigados
PRÁCTICA 5 VALORACIÓN ÁCIDO-BASE OBJETIVO Determinar concentraciones desconocidas de ácidos y bases. I. FUNDAMENTO TEÓRICO Las cantidades de reaccionantes y productos de una reacción, son investigados
EXTRACCION ACIDO-BASE
 PRACTICA XI EXTRACCION ACIDO-BASE I. OBJETIVOS II MATERIAL a) Elegir los disolventes activos adecuados para un proceso de extracción aplicado a problemas específicos. b) Identificar la técnica de extracción
PRACTICA XI EXTRACCION ACIDO-BASE I. OBJETIVOS II MATERIAL a) Elegir los disolventes activos adecuados para un proceso de extracción aplicado a problemas específicos. b) Identificar la técnica de extracción
ACTIVIDAD Nº 5. NATURALEZA CORPUSCULAR DE LA MATERIA.
 ACTIVIDAD Nº 5. NATURALEZA CORPUSCULAR DE LA MATERIA. Como recursos didácticos tenemos multitud de Proyectos educativos como: 1.- Proyecto Ulloa de Química 2.- Proyecto Newton de Física 3.- Banco de pruebas
ACTIVIDAD Nº 5. NATURALEZA CORPUSCULAR DE LA MATERIA. Como recursos didácticos tenemos multitud de Proyectos educativos como: 1.- Proyecto Ulloa de Química 2.- Proyecto Newton de Física 3.- Banco de pruebas
Reactor discontinuo. Cálculos cinéticos para el diseño de reactores industriales
 Reactor discontinuo. Cálculos cinéticos para el diseño de reactores industriales Objetivos de la práctica! Realizar el seguimiento experimental de la conversión de una reacción química con el tiempo.!
Reactor discontinuo. Cálculos cinéticos para el diseño de reactores industriales Objetivos de la práctica! Realizar el seguimiento experimental de la conversión de una reacción química con el tiempo.!
SUSTANCIAS NATURALES CON ENLACE QUÍMICO IÓNICO
 SUSTANCIAS NATURALES CON ENLACE QUÍMICO IÓNICO AUTOR JAVIER RUIZ HIDALGO TEMÁTICA ENLACE QUÍMICO ETAPA BACHILLERATO Resumen En este trabajo he querido buscar imágenes de minerales, para poder utilizarlas
SUSTANCIAS NATURALES CON ENLACE QUÍMICO IÓNICO AUTOR JAVIER RUIZ HIDALGO TEMÁTICA ENLACE QUÍMICO ETAPA BACHILLERATO Resumen En este trabajo he querido buscar imágenes de minerales, para poder utilizarlas
Curso de Análisis Químico - Facultad de Ciencias Agrarias y Forestales UNLP
 SEMINARIO Nº 1 Volumetría ácido base Volumetría por formación de complejos Objetivo general: El objetivo general de este primer seminario es integrar los conocimientos adquiridos sobre los métodos volumétricos
SEMINARIO Nº 1 Volumetría ácido base Volumetría por formación de complejos Objetivo general: El objetivo general de este primer seminario es integrar los conocimientos adquiridos sobre los métodos volumétricos
PRÁCTICO 3: SOLUCIONES
 Curso de Laboratorio Página: 1/6 DEPARTAMENTO ESTRELLA CAMPOS PRÁCTICO 3: SOLUCIONES Bibliografía: Química, La Ciencia Central, T.L. Brown, H.E.LeMay, Jr., B.Bursten; Ed. Prentice-Hall Hispanoamericana,
Curso de Laboratorio Página: 1/6 DEPARTAMENTO ESTRELLA CAMPOS PRÁCTICO 3: SOLUCIONES Bibliografía: Química, La Ciencia Central, T.L. Brown, H.E.LeMay, Jr., B.Bursten; Ed. Prentice-Hall Hispanoamericana,
Ácidos y bases fuertes y débiles
 9. Ácidos y bases fuertes y débiles Problemas Estimar comparativamente la acidez libre en una disolución de un ácido fuerte con la acidez libre en una disolución de un ácido débil, ambas a la misma concentración.
9. Ácidos y bases fuertes y débiles Problemas Estimar comparativamente la acidez libre en una disolución de un ácido fuerte con la acidez libre en una disolución de un ácido débil, ambas a la misma concentración.
Ácido + Base -----> Sal + Agua
 - REACCIÓN DE NEUTRALIZACIÓN - Objetivos: A).- Realización de cálculos en la reacción de neutralización (o valoración) entre una base, la sosa cáustica NaOH, y un ácido, el ácido clorhídrico HCl. La ecuación
- REACCIÓN DE NEUTRALIZACIÓN - Objetivos: A).- Realización de cálculos en la reacción de neutralización (o valoración) entre una base, la sosa cáustica NaOH, y un ácido, el ácido clorhídrico HCl. La ecuación
ACETONA SOLUCION 80 % REACTIVO ACIDO ACETICO 1 NORMAL o MOLAR O FRACCIONAL ACIDO ACETICO 2 a 6 NORMAL o MOLAR
 1 8000-125 ACETO CARMIN SOLUCION 8005-125 ACETO ORCEINA SOLUCION 8010-500 ACETONA SOLUCION 80 % REACTIVO 8015-1000 ACIDO ACETICO 1 NORMAL o MOLAR O FRACCIONAL 8020-1000 ACIDO ACETICO 2 a 6 NORMAL o MOLAR
1 8000-125 ACETO CARMIN SOLUCION 8005-125 ACETO ORCEINA SOLUCION 8010-500 ACETONA SOLUCION 80 % REACTIVO 8015-1000 ACIDO ACETICO 1 NORMAL o MOLAR O FRACCIONAL 8020-1000 ACIDO ACETICO 2 a 6 NORMAL o MOLAR
PRÁCTICA 3 -De preparación de DISOLUCIONES
 1 Far X, Módulo Formulación Magistral De la UT1 PRÁCTICA 3 -De preparación de DISOLUCIONES acuosas, y de Interpretación de los Pictogramas de productos químicos comunes en un laboratorio 1ª Preparación
1 Far X, Módulo Formulación Magistral De la UT1 PRÁCTICA 3 -De preparación de DISOLUCIONES acuosas, y de Interpretación de los Pictogramas de productos químicos comunes en un laboratorio 1ª Preparación
UNIVERSIDAD NACIONAL AUTÓNOMA DE MÉXICO FACULTAD DE QUÍMICA LABORATORIO DE QUÍMICA GENERAL II Grupo: Equipo: Nombre: Nombre: Nombre: Nombre:
 UNIVERSIDAD NACIONAL AUTÓNOMA DE MÉXICO FACULTAD DE QUÍMICA LABORATORIO DE QUÍMICA GENERAL II Grupo: Equipo: 1 Práctica 9 Ácidos y bases fuertes y débiles PREGUNTAS A RESPONDER AL FINAL DE LA PRÁCTICA
UNIVERSIDAD NACIONAL AUTÓNOMA DE MÉXICO FACULTAD DE QUÍMICA LABORATORIO DE QUÍMICA GENERAL II Grupo: Equipo: 1 Práctica 9 Ácidos y bases fuertes y débiles PREGUNTAS A RESPONDER AL FINAL DE LA PRÁCTICA
Núcleo Temático 7. Titulaciones Ácido Base. opasdfghjklzxcvbnmqwertyuiopasdfg 30/06/2010
 qwertyuiopasdfghjklzxcvbnmqwerty uiopasdfghjklzxcvbnmqwertyuiopasd fghjklzxcvbnmqwertyuiopasdfghjklzx cvbnmqwertyuiopasdfghjklzxcvbnmq wertyuiopasdfghjklzxcvbnmqwertyui Núcleo Temático 7 Titulaciones Ácido
qwertyuiopasdfghjklzxcvbnmqwerty uiopasdfghjklzxcvbnmqwertyuiopasd fghjklzxcvbnmqwertyuiopasdfghjklzx cvbnmqwertyuiopasdfghjklzxcvbnmq wertyuiopasdfghjklzxcvbnmqwertyui Núcleo Temático 7 Titulaciones Ácido
2A Reacciones de Sustitución Nucleofílica Alifática. Obtención de Cloruro de ter-butilo.
 PRÁCTICA 2A Reacciones de Sustitución Nucleofílica Alifática. Obtención de Cloruro de ter-butilo. I. OBJETIVOS. a) Conocer la preparación de un haluro de alquilo terciario a partir del alcohol correspondiente,
PRÁCTICA 2A Reacciones de Sustitución Nucleofílica Alifática. Obtención de Cloruro de ter-butilo. I. OBJETIVOS. a) Conocer la preparación de un haluro de alquilo terciario a partir del alcohol correspondiente,
CUADERNO DE PRÁCTICAS QUÍMICA
 CUADERNO DE PRÁCTICAS QUÍMICA GRADO DE BIOTECNOLOGÍA ALUMNO: GRADO DE BIOTECNOLOGÍA- QUÍMICA PRACTICA 1ª PREPARACIÓN DE DISOLUCIONES y CÁLCULO DE CONCENTRACIÓN OBJETO: Preparación de una disoluciones
CUADERNO DE PRÁCTICAS QUÍMICA GRADO DE BIOTECNOLOGÍA ALUMNO: GRADO DE BIOTECNOLOGÍA- QUÍMICA PRACTICA 1ª PREPARACIÓN DE DISOLUCIONES y CÁLCULO DE CONCENTRACIÓN OBJETO: Preparación de una disoluciones
12 Reacción de Schotten-Baumann. Obtención de Benzoato de Fenilo.
 PRÁCTICA 12 Reacción de Schotten-Baumann. Obtención de Benzoato de Fenilo. I. OBJETIVO. Efectuar una esterificación del fenol como ejemplo de la reacción de Schotten-Baumann. REACCIÓN: OH O O + Cl NaOH
PRÁCTICA 12 Reacción de Schotten-Baumann. Obtención de Benzoato de Fenilo. I. OBJETIVO. Efectuar una esterificación del fenol como ejemplo de la reacción de Schotten-Baumann. REACCIÓN: OH O O + Cl NaOH
DETERMINACIÓN EXPERIMENTAL DEL LAS PROPIEDADES FISICOQUÍMICAS DE UN CHAMPÚ PARA FORMACIÓN PROFESIONAL
 DETERMINACIÓN EXPERIMENTAL DEL LAS PROPIEDADES FISICOQUÍMICAS DE UN CHAMPÚ PARA FORMACIÓN PROFESIONAL AUTORA MANUELA CHAVES JIMÉNEZ TEMÁTICA COSMETOLOGÍA ETAPA CICLO DE FORMACIÓN PROFESIONAL DE GRADO MEDIO
DETERMINACIÓN EXPERIMENTAL DEL LAS PROPIEDADES FISICOQUÍMICAS DE UN CHAMPÚ PARA FORMACIÓN PROFESIONAL AUTORA MANUELA CHAVES JIMÉNEZ TEMÁTICA COSMETOLOGÍA ETAPA CICLO DE FORMACIÓN PROFESIONAL DE GRADO MEDIO
GUÍA N 1 TERMOQUÍMICA 2018-I. Laboratorio N 1: Termoquímica LABORATORIO DE FISICOQUÍMICA - UNIVERSIDAD TECNOLÓGICA DEL PERÚ
 GUÍA N 1 TERMOQUÍMICA 2018-I Laboratorio N 1: Termoquímica LABORATORIO DE FISICOQUÍMICA - UNIVERSIDAD TECNOLÓGICA DEL PERÚ LABORATORIO N 1 I. OBJETIVOS TERMOQUÍMICA Conocer el funcionamiento de un calorímetro
GUÍA N 1 TERMOQUÍMICA 2018-I Laboratorio N 1: Termoquímica LABORATORIO DE FISICOQUÍMICA - UNIVERSIDAD TECNOLÓGICA DEL PERÚ LABORATORIO N 1 I. OBJETIVOS TERMOQUÍMICA Conocer el funcionamiento de un calorímetro
UNIVERSIDAD TECNOLÓGICA EQUINOCCIAL Laboratorio de Química. MEDICIÓN DEL ph DE ÁCIDOS, BASES Y SALES 2. INTRODUCCIÓN
 UNIVERSIDAD TECNOLÓGICA EQUINOCCIAL Laboratorio de Química 1 MEDICIÓN DEL ph DE ÁCIDOS, BASES Y SALES 1. OBJETIVOS. Reconocer la acidez o basicidad de una sustancia mediante el uso de indicadores. Relacionar
UNIVERSIDAD TECNOLÓGICA EQUINOCCIAL Laboratorio de Química 1 MEDICIÓN DEL ph DE ÁCIDOS, BASES Y SALES 1. OBJETIVOS. Reconocer la acidez o basicidad de una sustancia mediante el uso de indicadores. Relacionar
1. Preparación de disoluciones y determinación de la concentración de una disolución por medio de una valoración.
 1. Preparación de disoluciones y determinación de la concentración de una disolución por medio de una valoración. Primera parte Preparar una disolución de NaH 0.1M Preparar disoluciones 0.1M de ácido clorhídrico,
1. Preparación de disoluciones y determinación de la concentración de una disolución por medio de una valoración. Primera parte Preparar una disolución de NaH 0.1M Preparar disoluciones 0.1M de ácido clorhídrico,
Semana 7. A preparar soluciones. Semana Estudiando 8 las soluciones. Empecemos! Qué sabes de...? El reto es... Vamos al grano
 Semana Estudiando 8 las soluciones Semana 7 Empecemos! Seguiremos explorando esta semana el impacto de los desechos en nuestro ambiente, apreciando así el uso racional y mejorando el descarte de las sustancias
Semana Estudiando 8 las soluciones Semana 7 Empecemos! Seguiremos explorando esta semana el impacto de los desechos en nuestro ambiente, apreciando así el uso racional y mejorando el descarte de las sustancias
QUÍMICA LOCAL INVESTIGACIÓN EXPERIMENTAL OBTENCIÓN DE NARANJA DE METILO A PARTIR DE SUSTANCIAS EN DESUSO ÁGUILA
 ::. UNIVERSIDAD NACIONAL AUTÓNOMA DE MÉXICO.:: XX CONCURSO UNIVERSITARIO FERIA DE LAS CIENCIAS CARÁTULA DE TRABAJO QUÍMICA ÁREA LOCAL CATEGORÍA INVESTIGACIÓN EXPERIMENTAL MODALIDAD OBTENCIÓN DE NARANJA
::. UNIVERSIDAD NACIONAL AUTÓNOMA DE MÉXICO.:: XX CONCURSO UNIVERSITARIO FERIA DE LAS CIENCIAS CARÁTULA DE TRABAJO QUÍMICA ÁREA LOCAL CATEGORÍA INVESTIGACIÓN EXPERIMENTAL MODALIDAD OBTENCIÓN DE NARANJA
Práctica 10: Ácidos y bases fuertes y débiles
 Equipo: Nombre: Nombre: Nombre: Práctica 10: Ácidos y bases fuertes y débiles Preguntas a resolver: Cómo es la acidez total de un ácido débil en relación con su acidez libre en disolución? Cómo es la basicidad
Equipo: Nombre: Nombre: Nombre: Práctica 10: Ácidos y bases fuertes y débiles Preguntas a resolver: Cómo es la acidez total de un ácido débil en relación con su acidez libre en disolución? Cómo es la basicidad
Práctica 8: Ácidos y bases fuertes y débiles
 Equipo: Nombre: Nombre: Nombre: Práctica 8: Ácidos y bases fuertes y débiles Problemas Estimar comparativamente la acidez libre en una disolución de un ácido fuerte con la acidez libre en una disolución
Equipo: Nombre: Nombre: Nombre: Práctica 8: Ácidos y bases fuertes y débiles Problemas Estimar comparativamente la acidez libre en una disolución de un ácido fuerte con la acidez libre en una disolución
DETERMINACION DE ALCALINIDAD POR METODO SM 2320 B
 DETERMINACION DE ALCALINIDAD POR METODO SM 2320 B Proceso: LABORATORIO Versión: 01 Código: LB-PR-13 Página 1 de 5 Vigente desde: 26/04/2018 1. OBJETIVO Establecer un procedimiento que permita analizar
DETERMINACION DE ALCALINIDAD POR METODO SM 2320 B Proceso: LABORATORIO Versión: 01 Código: LB-PR-13 Página 1 de 5 Vigente desde: 26/04/2018 1. OBJETIVO Establecer un procedimiento que permita analizar
Volumetría ácido-base elemental y Aplicaciones al sector Lácteo
 Volumetría ácido-base elemental y Aplicaciones al sector Lácteo Este material ha sido generado como módulo de aplicación en el curso Química y Biología de los Lácteos organizado por CFIE Zamora Términos
Volumetría ácido-base elemental y Aplicaciones al sector Lácteo Este material ha sido generado como módulo de aplicación en el curso Química y Biología de los Lácteos organizado por CFIE Zamora Términos
VOLUMETRIA ACIDO-BASE ó DE NEUTRALIZACIÓN
 VOLUMETRIA ACIDO-BASE ó DE NEUTRALIZACIÓN Mediante la volumetría ácido-base se pueden valorar sustancias que actúen como ácidos o como bases y las reacciones que transcurren según los casos pueden formularse
VOLUMETRIA ACIDO-BASE ó DE NEUTRALIZACIÓN Mediante la volumetría ácido-base se pueden valorar sustancias que actúen como ácidos o como bases y las reacciones que transcurren según los casos pueden formularse
TÍTULO: Determinación colorimétrica de compuestos fenólicos en agua mediante el reactivo de Folin-Ciocalteu
 Página 1 de 6 1.- INTRODUCCIÓN El presente método colorimétrico permite el análisis de compuestos orgánicos que presenten anillos aromáticos hidroxilados (fenoles, ácido tánico, taninos, ligninas, ácidos
Página 1 de 6 1.- INTRODUCCIÓN El presente método colorimétrico permite el análisis de compuestos orgánicos que presenten anillos aromáticos hidroxilados (fenoles, ácido tánico, taninos, ligninas, ácidos
PRÁCTICA 6 CINÉTICA QUÍMICA DETERMINACIÓN DE LA CONSTANTE DE VELOCIDAD DE REACCIÓN EN LA HIDRÓLISIS DEL CLORURO DE TERBUTILO
 PRÁCTICA 6 CINÉTICA QUÍMICA DETERMINACIÓN DE LA CONSTANTE DE VELOCIDAD DE REACCIÓN EN LA HIDRÓLISIS DEL CLORURO DE TERBUTILO OBJETIVO. El alumno aprenderá a comprobar experimentalmente el mecanismo de
PRÁCTICA 6 CINÉTICA QUÍMICA DETERMINACIÓN DE LA CONSTANTE DE VELOCIDAD DE REACCIÓN EN LA HIDRÓLISIS DEL CLORURO DE TERBUTILO OBJETIVO. El alumno aprenderá a comprobar experimentalmente el mecanismo de
DETERMINACIÓN EXPERIMENTAL DEL LAS PROPIEDADES FISICOQUÍMICAS DE UN CHAMPÚ ANTICASPA (SOL) PARA FORMACIÓN PROFESIONAL
 DETERMINACIÓN EXPERIMENTAL DEL LAS PROPIEDADES FISICOQUÍMICAS DE UN CHAMPÚ ANTICASPA (SOL) PARA FORMACIÓN PROFESIONAL AUTOR MANUELA CHAVES JIMÉNEZ TEMÁTICA COSMETOLOGÍA ETAPA CICLO DE FORMATIVO DE PELUQUERÍA
DETERMINACIÓN EXPERIMENTAL DEL LAS PROPIEDADES FISICOQUÍMICAS DE UN CHAMPÚ ANTICASPA (SOL) PARA FORMACIÓN PROFESIONAL AUTOR MANUELA CHAVES JIMÉNEZ TEMÁTICA COSMETOLOGÍA ETAPA CICLO DE FORMATIVO DE PELUQUERÍA
DETERMINAR DE FORMA EXPERIMENTAL EL CALOR QUE SE ABSORBE O DESPRENDE EN UNA REACCIÓN DE NEUTRALIZACIÓN EN MEDIO ACUOSO (NAOH + HCl) QUE EVOLUCIONA A
 DETERMINAR DE FORMA EXPERIMENTAL EL CALOR QUE SE ABSORBE O DESPRENDE EN UNA REACCIÓN DE NEUTRALIZACIÓN EN MEDIO ACUOSO (NAOH + HCl) QUE EVOLUCIONA A PRESIÓN CONSTANTE, INTERPRETANDO LOS RESULTADOS OBTENIDOS
DETERMINAR DE FORMA EXPERIMENTAL EL CALOR QUE SE ABSORBE O DESPRENDE EN UNA REACCIÓN DE NEUTRALIZACIÓN EN MEDIO ACUOSO (NAOH + HCl) QUE EVOLUCIONA A PRESIÓN CONSTANTE, INTERPRETANDO LOS RESULTADOS OBTENIDOS
PROCEDIMIENTOS RECOMENDADOS PARA LA DETERMINACIÓN ANALÍTICA DE CIERTOS PARÁMETROS EN LAS AGUAS DESALADAS
 PROCEDIMIENTOS RECOMENDADOS PARA LA DETERMINACIÓN ANALÍTICA DE CIERTOS PARÁMETROS EN LAS AGUAS DESALADAS Introducción Cloruros Calcio Dureza Total Magnesio Alcalinidad Fundación Centro Canario del Agua
PROCEDIMIENTOS RECOMENDADOS PARA LA DETERMINACIÓN ANALÍTICA DE CIERTOS PARÁMETROS EN LAS AGUAS DESALADAS Introducción Cloruros Calcio Dureza Total Magnesio Alcalinidad Fundación Centro Canario del Agua
CARTILLA DE ARTICULACIÓN LABORATORIOS QUIMICA GRADO 11 DOCENTE FACULTAD DE CIENCIAS BÁSICAS PROGRAMA DE QUÍMICA ARMENIA, QUINDIO
 CARTILLA DE ARTICULACIÓN UNIVERSIDAD DEL QUINDÍO Y COLEGIOS CASD, RUFINO, INEM LABORATORIOS QUIMICA GRADO 11 DOCENTE FACULTAD DE CIENCIAS BÁSICAS PROGRAMA DE QUÍMICA ARMENIA, QUINDIO 2017 NOTA: TRAER LOS
CARTILLA DE ARTICULACIÓN UNIVERSIDAD DEL QUINDÍO Y COLEGIOS CASD, RUFINO, INEM LABORATORIOS QUIMICA GRADO 11 DOCENTE FACULTAD DE CIENCIAS BÁSICAS PROGRAMA DE QUÍMICA ARMENIA, QUINDIO 2017 NOTA: TRAER LOS
PRÁCTICA # 5 PREPARACIÓN DE DISOLUCIONES. 1. Preparar soluciones de diversas sustancias poniendo en práctica las
 PRÁCTICA # 5 PREPARACIÓN DE DISOLUCIONES OBJETIVOS 1. Preparar soluciones de diversas sustancias poniendo en práctica las técnicas más comunes. 2. Practicar cálculos que involucren cantidades de soluto,
PRÁCTICA # 5 PREPARACIÓN DE DISOLUCIONES OBJETIVOS 1. Preparar soluciones de diversas sustancias poniendo en práctica las técnicas más comunes. 2. Practicar cálculos que involucren cantidades de soluto,
9 Condensación de Claisen-Schmidt. Obtención de Dibenzalacetona.
 PRÁCTICA 9 Condensación de Claisen-Schmidt. Obtención de Dibenzalacetona. I. OBJETIVOS. a) Efectuar una condensación aldólica cruzada dirigida. b) Obtener un producto de uso comercial. REACCIÓN: H O O
PRÁCTICA 9 Condensación de Claisen-Schmidt. Obtención de Dibenzalacetona. I. OBJETIVOS. a) Efectuar una condensación aldólica cruzada dirigida. b) Obtener un producto de uso comercial. REACCIÓN: H O O
ALCALINIDAD TOTAL- REACCIONES ACIDO-BASE Página 1
 Práctica No. 3 REACCIONES ACIDO BASE ALCALINIDAD TOTAL AL CARBONATO, BICARBONATO E HIDROXIDO FENOFTALEINA 1. OBJETIVO Determinar mediante una relación estequiometrica los carbonatos, hidróxidos y bicarbonatos
Práctica No. 3 REACCIONES ACIDO BASE ALCALINIDAD TOTAL AL CARBONATO, BICARBONATO E HIDROXIDO FENOFTALEINA 1. OBJETIVO Determinar mediante una relación estequiometrica los carbonatos, hidróxidos y bicarbonatos
Semana 8. Valorando una solución. Semana A preparar 9soluciones. Empecemos! Qué sabes de...? El reto es...
 Semana A preparar 9soluciones Semana 8 Empecemos! Durante esta semana seguiremos explorando la marca que dejan los desechos químicos sobre nuestro ambiente, reforzando así el uso racional y destacando
Semana A preparar 9soluciones Semana 8 Empecemos! Durante esta semana seguiremos explorando la marca que dejan los desechos químicos sobre nuestro ambiente, reforzando así el uso racional y destacando
Universidad Autónoma Metropolitana. Unidad Xochimilco. Energía y consumo de sustancias fundamentales. Tronco Común Divisional de CBS
 Universidad Autónoma Metropolitana Unidad Xochimilco Energía y consumo de sustancias fundamentales Tronco Común Divisional de CBS Practica 1: Titulación de soluciones Integrantes Fuentes Romero Ivette.
Universidad Autónoma Metropolitana Unidad Xochimilco Energía y consumo de sustancias fundamentales Tronco Común Divisional de CBS Practica 1: Titulación de soluciones Integrantes Fuentes Romero Ivette.
PREPARACIÓN DE SOLUCIONES
 PRÁCTICA Nº 6 PREPARACIÓN DE SOLUCIONES OBJETIVOS: Determinar las concentraciones físicas y químicas de las disoluciones Preparar disoluciones a partir de reactivos sólidos y líquidos I. FUNDAMENTO TEÓRICO.
PRÁCTICA Nº 6 PREPARACIÓN DE SOLUCIONES OBJETIVOS: Determinar las concentraciones físicas y químicas de las disoluciones Preparar disoluciones a partir de reactivos sólidos y líquidos I. FUNDAMENTO TEÓRICO.
Tarea previa. Responde las siguientes preguntas usando únicamente el espacio asignado para ello, en caso de excederlo, tu respuesta será inválida.
 1 UNIVERSIDAD NACIONAL AUTÓNOMA DE MÉXICO FACULTAD DE QUÍMICA LABORATORIO DE QUÍMICA GENERAL II Nombre: Nombre: Nombre: Nombre: Nombre: Grupo: Equipo: Práctica 1. Preparación de disoluciones y determinación
1 UNIVERSIDAD NACIONAL AUTÓNOMA DE MÉXICO FACULTAD DE QUÍMICA LABORATORIO DE QUÍMICA GENERAL II Nombre: Nombre: Nombre: Nombre: Nombre: Grupo: Equipo: Práctica 1. Preparación de disoluciones y determinación
REACTIVOS QUIMICA MEYER
 CATÁLOGO DESCRIPCIÓN PRESENTACIÓN PRECIO 8000-125 ACETO CARMIN SOLUCION 125 ml $207.00 8000-250 250 ml $375.00 8000-500 500 ml $680.00 8005-125 ACETO ORCEINA SOLUCION 125 ml $561.00 8005-250 250 ml $1,019.00
CATÁLOGO DESCRIPCIÓN PRESENTACIÓN PRECIO 8000-125 ACETO CARMIN SOLUCION 125 ml $207.00 8000-250 250 ml $375.00 8000-500 500 ml $680.00 8005-125 ACETO ORCEINA SOLUCION 125 ml $561.00 8005-250 250 ml $1,019.00
RELACIÓN DE PROBLEMAS PROPUESTOS
 RELACIÓN DE PROBLEMAS PROPUESTOS 1) Una disolución con una concentración inicial 1 molar de ácido acético (ácido etanoico) tiene una concentración en equilibrio de ion hidronio, H 3 O +, 4,2.10 3 molar.
RELACIÓN DE PROBLEMAS PROPUESTOS 1) Una disolución con una concentración inicial 1 molar de ácido acético (ácido etanoico) tiene una concentración en equilibrio de ion hidronio, H 3 O +, 4,2.10 3 molar.
COLEGIO DE BACHILLERES PLANTEL 5 SATÉLITE PRÁCTICAS DE LABORATORIO QUÍMICA II TERCER SEMESTRE
 COLEGIO DE BACHILLERES PLANTEL 5 SATÉLITE PRÁCTICAS DE LABORATORIO QUÍMICA II TERCER SEMESTRE PRACTICA # 1 CAMBIOS QUÍMICOS OBJETIVO DE LA PRÁCTICA: Identificar que los cambios químicos están acompañados
COLEGIO DE BACHILLERES PLANTEL 5 SATÉLITE PRÁCTICAS DE LABORATORIO QUÍMICA II TERCER SEMESTRE PRACTICA # 1 CAMBIOS QUÍMICOS OBJETIVO DE LA PRÁCTICA: Identificar que los cambios químicos están acompañados
poh = - log [OH - ] ; poh = log 1/[OH - ] ph = poh = 7
![poh = - log [OH - ] ; poh = log 1/[OH - ] ph = poh = 7 poh = - log [OH - ] ; poh = log 1/[OH - ] ph = poh = 7](/thumbs/87/95365982.jpg) CONCEPTO DE ph Como es muy común en la práctica tratar valores muy pequeños de [H 3 O + ] y de [OH - ] resulta más conveniente el tratamiento de esos valores en términos logarítmicos. En 1909, Sörensen
CONCEPTO DE ph Como es muy común en la práctica tratar valores muy pequeños de [H 3 O + ] y de [OH - ] resulta más conveniente el tratamiento de esos valores en términos logarítmicos. En 1909, Sörensen
PRÁCTICA 15 CÁLCULO TEÓRICO Y EXPERIMENTAL DE ph DE DISOLUCIONES DE ÁCIDOS, BASES Y SALES. DISOLUCIONES REGULADORAS.
 PRÁCTICA 15 CÁLCULO TEÓRICO Y EXPERIMENTAL DE ph DE DISOLUCIONES DE ÁCIDOS, BASES Y SALES. DISOLUCIONES REGULADORAS. OBJETIVOS En esta práctica se tratarán aspectos de interés relacionados con los equilibrios
PRÁCTICA 15 CÁLCULO TEÓRICO Y EXPERIMENTAL DE ph DE DISOLUCIONES DE ÁCIDOS, BASES Y SALES. DISOLUCIONES REGULADORAS. OBJETIVOS En esta práctica se tratarán aspectos de interés relacionados con los equilibrios
HIDROLISIS DE CARBOHIDRATOS
 EXPERIMENTO No. 1 HIDROLISIS DE CARBOHIDRATOS OBJETIVOS a) Realizar la hidrólisis e inversión de la sacarosa y comprobar ésta mediante pruebas químicas y utilizando un polarímetro. b) Hidrolizar un almidón
EXPERIMENTO No. 1 HIDROLISIS DE CARBOHIDRATOS OBJETIVOS a) Realizar la hidrólisis e inversión de la sacarosa y comprobar ésta mediante pruebas químicas y utilizando un polarímetro. b) Hidrolizar un almidón
