DENSIDAD DE LÍQUIDOS CON DENSÍMETROS Y AREÓMETROS
|
|
|
- José Luis San Segundo Gómez
- hace 7 años
- Vistas:
Transcripción
1 DENSIDAD DE LÍQUIDOS CON DENSÍMETROS Y AREÓMETROS Para determinar la densidad y la concentración de líquidos y disoluciones existen en la industria los areómetros y los densímetros, que son unos flotadores de vidrio lastrados con perdigones de plomo en la parte inferior. En la parte superior, llevan una escala graduada y esta graduación es diferente según vaya a ser su uso. Se llaman alcohómetros a los densímetros destinados a medir riquezas alcohólicas por el valor de la densidad. Dan directamente el porcentaje de alcohol en volumen. Los oleómetros sirven para medir densidades de aceites. Su escala está graduada de 50º a 0º, correspondiendo a densidades desde 0,870 a 0,970 respectivamente. Los sacarómetros están destinados a medir riquezas de las soluciones acuosas de sacarosa. Existen varias escalas. Por ejemplo: Grados Brix que indican el 1% en peso de sacarosa disuelta a la temperatura dada en el momento de la medición. Grados Bates, graduados para medidas americanas, dan la concentración en libras por barril (32 galones). Hay una fórmula para pasar de grados Brix a Bates. Los salinómetros son utilizados para medir riquezas de soluciones acuosas de cloruro sódico. Los lactómetros se utilizan para medir la densidad de la leche. La escala de los areómetros Beaumé se basa en considerar el valor de 10º Bé a la densidad de una disolución de NaC1 en agua al 10% y el valor de 0º Bé al agua destilada. Existen unas fórmulas de conversión de ºBé en densidades que se citan más adelante. Procedimiento para medir la densidad de un líquido con densímetros 1. Se toma una probeta de 100 o 250 ml y se lava perfectamente. Se enjuaga interiormente con un poco del líquido problema. (El líquido de enjuagar se echa a la pileta con el grifo abierto.) 2. Se elige un densímetro y se introduce con cuidado en la probeta. 3. Si se observa que al soltarlo se va hacia el fondo, se coge, se limpia y se seca y se toma otro densímetro que mida densidades mayores. Así hasta dar con el adecuado. 4. Ya con el densímetro adecuado, se deja sobre la superficie del líquido dando una rotación con los dedos de forma que caiga girando. 5. De esta forma, cuando el densímetro se para, se puede medir en su escala sin que se quede adherido a la pared de la probeta. 6. Tomar la probeta con la mano y subirla hasta conseguir que el nivel del líquido quede a la altura de los ojos y hacer la lectura de la escala.
2 La densidad varía con la temperatura, es por lo que una vez se haya medido la densidad, hemos de medir también la temperatura a la que se ha hecho la medición y luego ver en las tablas la corrección que debemos hacer. Estas tablas vienen en la agenda del químico y otros libros de datos de uso frecuente en los laboratorios. El areómetro Beaumé Estos areómetros son de graduación arbitraria, sus escalas están divididas en grados Beaumé (ºBé). Existen tablas en las que se relacionan estos grados con la concentración de soluto disuelto en 100 ml de disolución. De este tipo se construyen dos modelos: Para líquidos o disoluciones menos densas que el agua. (En estos casos, el punto de enrase con el agua destilada se marca con el 10 de su escala.) Para líquidos o disoluciones más densas que el agua. (En éstos, el punto de enrase con el agua destilada se marca con el 0 de su escala.) Sabiendo los grados Bé de una disolución se puede deducir su densidad, y viceversa, para ello basta sólo con aplicar la fórmula correspondiente de las que se indican a continuación: Para líquidos menos densos que el agua: 146,3 d (con agua destilada n 10) 136,3 n Para líquidos más densos que el agua: 146,3 d (con agua destilada n 0) 136,3 n En estas fórmulas: d densidad y n número de grados Beaumé. En muchos casos, resulta de más comodidad el consultar las tablas de una buena agenda. Como ejercicio práctico, los alumnos pueden medir las densidades de diferentes líquidos con areómetros para más y para menos densos que el agua. Los líquidos propuestos son: Líquido problema Densidad con el areómetro Densidad según tablas ETANOL ACETONA TRICLOROETILENO
3 Determinación del grado alcohólico de un vino El objetivo de esta práctica es el de que los alumnos/as experimenten una aplicación directa de una destilación simple y al mismo tiempo se familiaricen con el manejo de alcohómetros y de tablas de densidades. Los componentes fundamentales de los vinos son el alcohol etílico y el agua. Cuando se destila un vino, su destilado será una mezcla de ambos, más enriquecida en alcohol que el vino del que procede y libre de los solutos no volátiles que el vino tenga. El punto de ebullición del alcohol etílico es de 78,5 ºC. El punto de ebullición del agua es de 100 ºC. Ambos a la presión atmosférica normal (760 mm de Hg). Se conoce como grado alcohólico de un vino al porcentaje en volumen (% en volumen) del alcohol etílico contenido por ese vino, es decir, los mililitros de alcohol etílico puro que continen 100 ml del vino que se analiza. Para su medida se utilizan unos densímetros que llevan la escala dividida en grados alcohólicos y que se conocen como alcohómetros. La densidad del destilado depende siempre de la cantidad de alcohol (concentración) y de la temperatura. Material necesario: Montaje para una destilación ordinaria. Un alcohómetro de 0 a 25 grados. Una probeta de 100 ml. Procedimiento: Hacer el montaje para una destilación simple teniendo en cuenta: Las pinzas metálicas que sujetan al matraz de destilación y al refrigerante conviene que estén recubiertas de material plástico o de tubo de goma para evitar la rotura del vidrio. Si se utilizan ajustes esmerilados, se debe procurar que ajusten perfectamente, dándoles un poco de vaselina por las uniones. El agua de refrigeración penetrará en el refrigerante por la parte inferior y saldrá por la parte superior; así, los vapores que están más fríos se pondrán en contacto con las paredes más frías y condensarán mejor. Introducir en el matraz 100 ml del vino que se vaya a destilar, medidos con una probeta y unos trozos de piedra pómez para ayudar a que la ebullición sea uniforme. Colocar la probeta como colector donde se recogerá el destilado. Comprobar que todas las uniones son correctas e iniciar la destilación, abriendo el agua de refrigeración y encendiendo el mechero. Cuando comience la destilación, regular la llama para que la ebullición sea tranquila. La destilación se da por finalizada cuando en la probeta se hayan recogido unos 60 ml del destilado (algo más de la mitad del vino puesto en el matraz). Añadir agua destilada en la probeta donde está el destilado hasta completar los 100 ml y homogeneizar por agitación.
4 Introducir el alcohómetro en la probeta con un giro de rotación para que no se adhiera a las paredes y leer el grado alcohólico. Para determinarlo con mayor precisión, utilizar un picnómetro para calcular la densidad del destilado y, con ayuda de las tablas que se adjuntan, establecer el grado alcohólico del vino analizado. Alcohometría (Alcohol etílico) a 20º C Densidad % Alcohol en volumen Densidad % Alcohol en volumen Tabla de densidades de los metales más corrientes a 15º C Metal Densidad Metal Densidad ALUMINIO 12,70 grs/ml COBRE 18,93 grs/ml CINC 17,10 grs/ml CROMO 17,10 grs/ml ESTAÑO 17,29 grs/ml HIERRO 17,87 grs/ml NÍQUEL 18,90 grs/ml PLATA 10,50 grs/ml PLOMO 11,30 grs/ml MERCURIO 13,50 grs/ml ORO 19,30 grs/ml PLATINO 21,50 grs/ml
5 Densidades de algunas tierras, piedras y materiales de construcción Material Densidad Material Densidad ALABASTRO 2,30 2,80 grs/ml BASALTO 2,70 3,20 grs/ml CALIZA 2,46 2,84 grs/ml CEMENTO 0,82 1,95 grs/ml CUARZO 2,50 2,80 grs/ml MÁRMOL ORDINARIO 2,52 2,85 grs/ml ARENA FINA SECA 1,40 1,65 grs/ml GRANITO 2,51 3,05 grs/ml Densidades de algunas aleaciones metálicas Aleación Densidad Aleación Densidad BRONCE 7,40 8,90 grs/ml LATÓN 8,40 8,70 grs/ml Densidades de algunas maderas (secadas al aire) Madera Densidad Madera Densidad CEDRO 0,57 grs/ml CEREZO 0,76 0,84 grs/ml ÉBANO 1,26 grs/ml ENCINA 0,69 1,03 grs/ml HAYA 0,66 0,83 grs/ml MANZANO 0,66 0,84 grs/ml NOGAL 0,60 0,81 grs/ml OLMO 0,56 0,82 grs/ml ROBLE 0,71 1,07 grs/ml PINO 0,31 0,76 grs/ml Densidades de algunos líquidos a 20º C Líquido Densidad Líquido Densidad ETANOL de 96º 0,810 grs/ml ACETONA 0,790 grs/ml METANOL 0,790 grs/ml AC. ACÉTICO GLACIAL grs/ml CLOROFORMO 1,475 grs/ml HEXANO 0,675 grs/ml TRICLOROETILENO 1,471 grs/ml AGUA DESTILADA (4ºC) grs/ml
Departamento Ciencias. Física y Química MATERIA. se clasifica en. SUSTANCIAS PURAS pueden ser. por métodos. físicos originan. Compuestos.
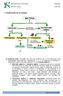 1. Clasificación de la materia MATERIA se clasifica en MEZCLAS pueden ser por métodos físicos originan SUSTANCIAS PURAS pueden ser Heterogéneas Homogéneas Compuestos como las Disoluciones formados por
1. Clasificación de la materia MATERIA se clasifica en MEZCLAS pueden ser por métodos físicos originan SUSTANCIAS PURAS pueden ser Heterogéneas Homogéneas Compuestos como las Disoluciones formados por
Densimetría, Termometría y Volumetría
 ALCOHOMETRO AREOMETRO DENSIMETRO PICNOMETRO TERMOMETROS BURETAS CONO SEDIMENTACION MATRACES AFORADOS MICROCAPILARES PIPETAS PROBETAS Densimetría ALCOHÓMETRO DE PRECISIÓN Sin termómetro. Calibrado a 20
ALCOHOMETRO AREOMETRO DENSIMETRO PICNOMETRO TERMOMETROS BURETAS CONO SEDIMENTACION MATRACES AFORADOS MICROCAPILARES PIPETAS PROBETAS Densimetría ALCOHÓMETRO DE PRECISIÓN Sin termómetro. Calibrado a 20
PALACORRE. TEMA 2: Los cambios de aspecto de la materia I.E.S. LA CORREDORIA OVIEDO 1º ESO GRUPO: ALUMNO: DPTO. CIENCIAS NATURALES
 PALACORRE I.E.S. LA CORREDORIA OVIEDO DPTO. CIENCIAS NATURALES TEMA 2: Los cambios de aspecto de la materia 1º ESO ALUMNO: GRUPO: TEMA 2: LOS CAMBIOS DE ASPECTO DE LA MATERIA Nombre y apellidos: Fecha:
PALACORRE I.E.S. LA CORREDORIA OVIEDO DPTO. CIENCIAS NATURALES TEMA 2: Los cambios de aspecto de la materia 1º ESO ALUMNO: GRUPO: TEMA 2: LOS CAMBIOS DE ASPECTO DE LA MATERIA Nombre y apellidos: Fecha:
Todo lo que vemos es materia
 Todo lo que vemos es materia CLASIFICACIÓN DE LA MATERIA La materia se presenta en la naturaleza en forma de sustancias puras y mezclas, de modo que podemos establecer la siguiente clasificación: CLASIFICACIÓN
Todo lo que vemos es materia CLASIFICACIÓN DE LA MATERIA La materia se presenta en la naturaleza en forma de sustancias puras y mezclas, de modo que podemos establecer la siguiente clasificación: CLASIFICACIÓN
SUSTANCIA PURA ELEMENTO COMPUESTO 1
 SUSTANCIA PURA ELEMENTO COMPUESTO 1 MATERIA MEZCLA Sustancia pura Sistema material en el que se han combinado dos o más sustancias Mezcla de agua y azúcar Mezcla homogénea Sistema formado por dos o más
SUSTANCIA PURA ELEMENTO COMPUESTO 1 MATERIA MEZCLA Sustancia pura Sistema material en el que se han combinado dos o más sustancias Mezcla de agua y azúcar Mezcla homogénea Sistema formado por dos o más
ACTIVIDAD DE INTERPRETASCION EN LA MEDICION
 1 ACTIVIDAD DE INTERPRETASCION EN LA MEDICION 1. El sulfuro de hierro es una sustancia sólida a temperatura ambiente y está compuesta de hierro y azufre. Estas sustancias tienen las siguientes propiedades:
1 ACTIVIDAD DE INTERPRETASCION EN LA MEDICION 1. El sulfuro de hierro es una sustancia sólida a temperatura ambiente y está compuesta de hierro y azufre. Estas sustancias tienen las siguientes propiedades:
SEPARACIÓN DE LOS COMPONENTES DE UNA MEZCLA
 PRÁCTICA Nº 3 SEPARACIÓN DE LOS COMPONENTES DE UNA MEZCLA OBJETIVOS: Establecer los fundamentos teóricos de los proceso de separación. Separar los componentes de diversas muestras problema. I. FUNDAMENTOS
PRÁCTICA Nº 3 SEPARACIÓN DE LOS COMPONENTES DE UNA MEZCLA OBJETIVOS: Establecer los fundamentos teóricos de los proceso de separación. Separar los componentes de diversas muestras problema. I. FUNDAMENTOS
1. Disoluciones una disolución es cualquier mezcla homogénea disolvente soluto Medidas de composición
 1. Disoluciones En general, una disolución es cualquier mezcla homogénea. Por ejemplo, el aire, mezcla de nitrógeno, oxígeno y otros gases en proporciones menores; o el bronce, que es una aleación metálica
1. Disoluciones En general, una disolución es cualquier mezcla homogénea. Por ejemplo, el aire, mezcla de nitrógeno, oxígeno y otros gases en proporciones menores; o el bronce, que es una aleación metálica
Si un objeto tiene mayor densidad que otro y ambos tienen el mismo tamaño. Cuál es el que tiene menos masa?
 TITULO (edite antes de imprimir) NOMBRE: CURSO: 1) Calcular la densidad de los siguientes materiales: a) 9 litros de nafta que tienen una masa de 6,120 gramos. b) 2 litros de leche que tienen una masa
TITULO (edite antes de imprimir) NOMBRE: CURSO: 1) Calcular la densidad de los siguientes materiales: a) 9 litros de nafta que tienen una masa de 6,120 gramos. b) 2 litros de leche que tienen una masa
Materia. Mezclas Son aquellas que están formados por 2 o más sustancias.
 Qué es la materia? Materia Sustancias Puras Son aquellas que tienen una composición y propiedades DEFINIDAS. Mezclas Son aquellas que están formados por 2 o más sustancias. Elementos No se pueden separar
Qué es la materia? Materia Sustancias Puras Son aquellas que tienen una composición y propiedades DEFINIDAS. Mezclas Son aquellas que están formados por 2 o más sustancias. Elementos No se pueden separar
Práctica 2. Densidad
 Universidad Nacional Autónoma de México Facultad de Química Laboratorio de Química General I 1 Grupo Equipo Práctica 2. Densidad Problema 1 Realizar experimentalmente una curva de calibración que relacione
Universidad Nacional Autónoma de México Facultad de Química Laboratorio de Química General I 1 Grupo Equipo Práctica 2. Densidad Problema 1 Realizar experimentalmente una curva de calibración que relacione
PROBLEMAS MEZCLAS Y DISOLUCIONES
 PROBLEMAS MEZCLAS Y DISOLUCIONES 1. Clasifica como homogéneos o heterogéneos los siguientes sistemas materiales: un trozo de cobre, agua salada, hierro oxidado, una ensalada. 2. Al mezclar dos sistemas
PROBLEMAS MEZCLAS Y DISOLUCIONES 1. Clasifica como homogéneos o heterogéneos los siguientes sistemas materiales: un trozo de cobre, agua salada, hierro oxidado, una ensalada. 2. Al mezclar dos sistemas
1) Una estrella de neutrones tiene un radio de 5 km y una masa de. Cuánto pesaría un
 TITULO (edite antes de imprimir) NOMBRE: CURSO: 1) Una estrella de neutrones tiene un radio de 5 km y una masa de. Cuánto pesaría un volumen de de esa estrella bajo la influencia de la atracción gravitacional
TITULO (edite antes de imprimir) NOMBRE: CURSO: 1) Una estrella de neutrones tiene un radio de 5 km y una masa de. Cuánto pesaría un volumen de de esa estrella bajo la influencia de la atracción gravitacional
PRÁCTICA 3 -De preparación de DISOLUCIONES
 1 Far X, Módulo Formulación Magistral De la UT1 PRÁCTICA 3 -De preparación de DISOLUCIONES acuosas, y de Interpretación de los Pictogramas de productos químicos comunes en un laboratorio 1ª Preparación
1 Far X, Módulo Formulación Magistral De la UT1 PRÁCTICA 3 -De preparación de DISOLUCIONES acuosas, y de Interpretación de los Pictogramas de productos químicos comunes en un laboratorio 1ª Preparación
Aplicación y control de procesos químicos de purificación Siglema: AQPU-02
 PRACTICA: 1 Método de purificación de líquidos Objetivos Reconocer las diferentes técnicas de destilación, métodos ampliamente utilizados en laboratorio de química orgánica para la purificación de sustancias
PRACTICA: 1 Método de purificación de líquidos Objetivos Reconocer las diferentes técnicas de destilación, métodos ampliamente utilizados en laboratorio de química orgánica para la purificación de sustancias
LAS PROPIEDADES DE LA MATERIA
 LAS PROPIEDADES DE LA MATERIA En la siguiente tabla encontraras las propiedades características de la materia que tendrás que utilizar en las siguientes actividades Sustancia P. de Fusión P. de Ebullición
LAS PROPIEDADES DE LA MATERIA En la siguiente tabla encontraras las propiedades características de la materia que tendrás que utilizar en las siguientes actividades Sustancia P. de Fusión P. de Ebullición
OBJETIVO Aprender a preparar disoluciones de concentración dada, ya que la mayor parte de las reacciones químicas tienen lugar en forma de disolución.
 OBJETIVO Aprender a preparar disoluciones de concentración dada, ya que la mayor parte de las reacciones químicas tienen lugar en forma de disolución. FUNDAMENTO TEÓRICO Una disolución es una mezcla homogénea
OBJETIVO Aprender a preparar disoluciones de concentración dada, ya que la mayor parte de las reacciones químicas tienen lugar en forma de disolución. FUNDAMENTO TEÓRICO Una disolución es una mezcla homogénea
1 Propiedades de la materia
 1 La materia 1 Propiedades de la materia La materia, o sistema material, es todo lo que posee una propiedad fundamental llamada masa, y que ocupa un espacio, es decir, un volumen. Cuando nos referimos
1 La materia 1 Propiedades de la materia La materia, o sistema material, es todo lo que posee una propiedad fundamental llamada masa, y que ocupa un espacio, es decir, un volumen. Cuando nos referimos
1. a) Define Sustancia pura: Es aquella que tiene la misma composición y las mismas propiedades. b) Define Disolución: Es una mezcla homogénea.
 Tema 3. LA MATERIA Y SU ASPECTO MEZCLAS Y SUSTANCIAS PURAS 1. a) Define Sustancia pura: Es aquella que tiene la misma composición y las mismas propiedades. b) Define Disolución: Es una mezcla homogénea.
Tema 3. LA MATERIA Y SU ASPECTO MEZCLAS Y SUSTANCIAS PURAS 1. a) Define Sustancia pura: Es aquella que tiene la misma composición y las mismas propiedades. b) Define Disolución: Es una mezcla homogénea.
Practica 2ª : Destilación continua computerizada
 Practica 2ª : Destilación continua computerizada DESTILACIÓN DE SISTEMAS BINARIOS CON COMPORTAMIENTO AZEOTRÓPICO Unidad de Des
Practica 2ª : Destilación continua computerizada DESTILACIÓN DE SISTEMAS BINARIOS CON COMPORTAMIENTO AZEOTRÓPICO Unidad de Des
Unidad 2. La materia
 Física y Química Unidad 2: La materia Unidad 2. La materia Índice de contenido 1. Estados de agregación de la materia...3 2. Cambios de estado...4 3. Clasificación de la materia...6 3.1.- Métodos de separación
Física y Química Unidad 2: La materia Unidad 2. La materia Índice de contenido 1. Estados de agregación de la materia...3 2. Cambios de estado...4 3. Clasificación de la materia...6 3.1.- Métodos de separación
Práctica 2. Densidad
 Equipo: Nombre: Nombre: Nombre: Práctica 2. Densidad Preguntas al responder al final de la práctica La densidad es una propiedad intensiva o extensiva? Por qué? Porqué al aumentar la temperatura disminuye
Equipo: Nombre: Nombre: Nombre: Práctica 2. Densidad Preguntas al responder al final de la práctica La densidad es una propiedad intensiva o extensiva? Por qué? Porqué al aumentar la temperatura disminuye
DEPARTAMENTO DE QUÍMICA AGRÍCOLA Y EDAFOLOGÍA ESCUELA TÉCNICA SUPERIOR DE INGENIERÍA AGRONÓMICA Y DE MONTES
 DEPARTAMENTO DE QUÍMICA AGRÍCOLA Y EDAFOLOGÍA ESCUELA TÉCNICA SUPERIOR DE INGENIERÍA AGRONÓMICA Y DE MONTES GRADO EN INGENIERÍA AGROALIMENTARIA Y DEL MEDIO RURAL (PLAN 2010) QUÍMICA GENERAL 1 er curso
DEPARTAMENTO DE QUÍMICA AGRÍCOLA Y EDAFOLOGÍA ESCUELA TÉCNICA SUPERIOR DE INGENIERÍA AGRONÓMICA Y DE MONTES GRADO EN INGENIERÍA AGROALIMENTARIA Y DEL MEDIO RURAL (PLAN 2010) QUÍMICA GENERAL 1 er curso
Tema 4: Sustancias puras y mezclas
 Tema 4: Sustancias puras y mezclas Esquema de trabajo: 1. Sustancias puras: Tipos: elementos y compuestos. 2. Mezclas: Tipos: Homogénea y heterogénea 3. Disoluciones Concepto Componentes Tipos de disoluciones
Tema 4: Sustancias puras y mezclas Esquema de trabajo: 1. Sustancias puras: Tipos: elementos y compuestos. 2. Mezclas: Tipos: Homogénea y heterogénea 3. Disoluciones Concepto Componentes Tipos de disoluciones
ESTADOS DE AGREGACIÓN DE LA MATERIA
 LA MATERIA LA MATERIA Materia es todo aquello que ocupa un lugar en el espacio y tiene masa. La madera, el agua, el corcho, la sal,.. Son clases diferentes de materia. Las clases de materia que se utilizan
LA MATERIA LA MATERIA Materia es todo aquello que ocupa un lugar en el espacio y tiene masa. La madera, el agua, el corcho, la sal,.. Son clases diferentes de materia. Las clases de materia que se utilizan
PRÁCTICAS TÉCNICAS DE SEPARACIÓN Y PREPARACIÓN DE DISOLUCIONES FÍSICA Y QUÍMICA 2º
 PRÁCTICAS TÉCNICAS DE SEPARACIÓN Y PREPARACIÓN DE DISOLUCIONES FÍSICA Y QUÍMICA 2º CURSO: NOMBRE: COMPAÑEROS QUE FORMAN TU GRUPO: 1 FILTRACIÓN DE AGUA Y ARENA La filtración es la separación de las partículas
PRÁCTICAS TÉCNICAS DE SEPARACIÓN Y PREPARACIÓN DE DISOLUCIONES FÍSICA Y QUÍMICA 2º CURSO: NOMBRE: COMPAÑEROS QUE FORMAN TU GRUPO: 1 FILTRACIÓN DE AGUA Y ARENA La filtración es la separación de las partículas
ACTIVIDADES DE PENDIENTES DE FÍSICA Y QUÍMICA DE 3º ESO
 ACTIVIDADES DE PENDIENTES DE FÍSICA Y QUÍMICA DE 3º ESO 1. a) Qué es la Ciencia? Qué es la Física? Qué es la Química? b) Señala qué procesos se estudian la Física y cuáles estudia la Química: a. Descenso
ACTIVIDADES DE PENDIENTES DE FÍSICA Y QUÍMICA DE 3º ESO 1. a) Qué es la Ciencia? Qué es la Física? Qué es la Química? b) Señala qué procesos se estudian la Física y cuáles estudia la Química: a. Descenso
PRÁCTICA # 01 PREPARACIÓN DE DISOLUCIONES
 REPÚBLICA BOLIVARIANA DE VENEZUELA MINISTERIO DEL PODER POPULAR PARA LA DEFENSA AVIACIÓN MILITAR VENEZOLANA U.E.A.M LIBERTADOR ASIGNATURA: QUÍMICA PROF(A): ANGÉLICA RODRÍGUEZ MARBELIS MELENDEZ CURSO: 4to
REPÚBLICA BOLIVARIANA DE VENEZUELA MINISTERIO DEL PODER POPULAR PARA LA DEFENSA AVIACIÓN MILITAR VENEZOLANA U.E.A.M LIBERTADOR ASIGNATURA: QUÍMICA PROF(A): ANGÉLICA RODRÍGUEZ MARBELIS MELENDEZ CURSO: 4to
COLEGIO DE BACHILLERES DEL ESTADO DE TLAXCALA
 COLEGIO DE BACHILLERES DEL ESTADO DE TLAXCALA DIRECCIÓN ACADÉMICA DEPARTAMENTO DE BIBLIOTECAS Y LABORATORIOS. MANUAL DE ACTIVIDADES EXPERIMENTALES DE: PRUEBAS FÍSICAS I (QUINTO SEMESTRE) SEMESTRE 2009-B
COLEGIO DE BACHILLERES DEL ESTADO DE TLAXCALA DIRECCIÓN ACADÉMICA DEPARTAMENTO DE BIBLIOTECAS Y LABORATORIOS. MANUAL DE ACTIVIDADES EXPERIMENTALES DE: PRUEBAS FÍSICAS I (QUINTO SEMESTRE) SEMESTRE 2009-B
CLASE # 5. UNIDAD II. Mediciones cuantitativas OBJETIVO GENERAL
 CLASE # 5 UNIDAD II. Mediciones cuantitativas OBJETIVO GENERAL 1. Interpretar diferentes unidades cuantitativas de medida, volumen, masa y temperatura teniendo en cuenta las condiciones específicas del
CLASE # 5 UNIDAD II. Mediciones cuantitativas OBJETIVO GENERAL 1. Interpretar diferentes unidades cuantitativas de medida, volumen, masa y temperatura teniendo en cuenta las condiciones específicas del
Materia: es aquello que ocupa un lugar en el espacio y cuyas propiedades percibimos por los sentidos. Es diversa y discontinua.
 Sistemas materiales Materia: es aquello que ocupa un lugar en el espacio y cuyas propiedades percibimos por los sentidos. Es diversa y discontinua. Mezcla Heterogénea: unión de dos o más sustancias de
Sistemas materiales Materia: es aquello que ocupa un lugar en el espacio y cuyas propiedades percibimos por los sentidos. Es diversa y discontinua. Mezcla Heterogénea: unión de dos o más sustancias de
ESAS METAS SON RESPONSABILIDAD DE TODOS Y CADA UNO DE LOS QUE PARTICIPAN EN LABORATORIO. PAUTAS PARA LA PRESENTACION DE LOS TRABAJOS
 INTRODUCCION AL TRABAJO DE LABORATORIO En el trabajo cotidiano existen riesgos y con mucha más razón si el trabajo se desarrolla en el laboratorio, debido a que se experimentan una serie de situaciones
INTRODUCCION AL TRABAJO DE LABORATORIO En el trabajo cotidiano existen riesgos y con mucha más razón si el trabajo se desarrolla en el laboratorio, debido a que se experimentan una serie de situaciones
1º Control 2ª Evaluación. Física y Química 1º Bachillerato D. 1.- (2 puntos) Formula o nombra los siguientes compuestos químicos:
 1º Control 2ª Evaluación Física y Química 1º Bachillerato D a) Seleniuro de hidrógeno; b) Yodato de cobre (II); c) Li 2 O 2; d) K 2 S; e) Na 3 PO 4 2. (2 puntos) a) Calcula los gramos de hidróxido potásico
1º Control 2ª Evaluación Física y Química 1º Bachillerato D a) Seleniuro de hidrógeno; b) Yodato de cobre (II); c) Li 2 O 2; d) K 2 S; e) Na 3 PO 4 2. (2 puntos) a) Calcula los gramos de hidróxido potásico
Materia es todo aquello que tiene masa y ocupa un lugar en el espacio (tiene volumen). La ciencia que estudia la materia es la Química.
 Alfonso García Materia es todo aquello que tiene masa y ocupa un lugar en el espacio (tiene volumen). La ciencia que estudia la materia es la Química. Un sistema material es una porción de materia. Ejemplos:
Alfonso García Materia es todo aquello que tiene masa y ocupa un lugar en el espacio (tiene volumen). La ciencia que estudia la materia es la Química. Un sistema material es una porción de materia. Ejemplos:
FÍSICA Y QUÍMICA 2º ESO Tema 2: LA MATERIA Mezclas y Soluciones. Sustancias puras y mezclas
 Sustancias puras y mezclas La materia que nos rodea es, en la mayoría de los casos, una mezcla de sustancias. Los científicos han intentado clasificar las sustancias desde el principio de los tiempos.
Sustancias puras y mezclas La materia que nos rodea es, en la mayoría de los casos, una mezcla de sustancias. Los científicos han intentado clasificar las sustancias desde el principio de los tiempos.
MEZCLAS Y DISOLUCIONES. Física y Química 3º de E.S.O. IES Isidra de Guzmán
 MEZCLAS Y DISOLUCIONES Física y Química 3º de E.S.O. IES Isidra de Guzmán Introducción Ya sabes que los sistemas materiales se pueden clasificar según su composición en sustancias puras y mezclas. Las
MEZCLAS Y DISOLUCIONES Física y Química 3º de E.S.O. IES Isidra de Guzmán Introducción Ya sabes que los sistemas materiales se pueden clasificar según su composición en sustancias puras y mezclas. Las
CRISTALIZACIÓN: PURIFICACIÓN DEL ÁCIDO BENZOICO. Purificar un compuesto orgánico mediante cristalización y determinar su punto de fusión
 EXPERIMENTO 1 CRISTALIZACIÓN: PURIFICACIÓN DEL ÁCIDO BENZOICO Objetivo general Purificar un compuesto orgánico mediante cristalización y determinar su punto de fusión Objetivos específicos 1.- Determinar
EXPERIMENTO 1 CRISTALIZACIÓN: PURIFICACIÓN DEL ÁCIDO BENZOICO Objetivo general Purificar un compuesto orgánico mediante cristalización y determinar su punto de fusión Objetivos específicos 1.- Determinar
gravilla o canto rodado húmedos MAMPOSTERIAS ladrillos huecos con mezcla de cemento ladrillos prensados con mezcla de cemento
 PESOS ESPECIFICOS CUERPOS A GRANEL tierra seca tierra húmeda tierra saturada arena seca arena húmeda arena saturada gravilla o canto rodado secos gravilla o canto rodado húmedos piedra partida Cemento
PESOS ESPECIFICOS CUERPOS A GRANEL tierra seca tierra húmeda tierra saturada arena seca arena húmeda arena saturada gravilla o canto rodado secos gravilla o canto rodado húmedos piedra partida Cemento
PRÁCTICA 1. IDENTIFICACIÓN Y MANEJO DE MATERIAL DE LABORATORIO: PREPARACIÓN DE DISOLUCIONES Y MEDIDA DE DENSIDADES
 PRÁCTICA 1. IDENTIFICACIÓN Y MANEJO DE MATERIAL DE LABORATORIO: PREPARACIÓN DE DISOLUCIONES Y MEDIDA DE DENSIDADES OBJETIVOS ESPECÍFICOS 1) Identificar y manejar el material básico de laboratorio. 2) Preparar
PRÁCTICA 1. IDENTIFICACIÓN Y MANEJO DE MATERIAL DE LABORATORIO: PREPARACIÓN DE DISOLUCIONES Y MEDIDA DE DENSIDADES OBJETIVOS ESPECÍFICOS 1) Identificar y manejar el material básico de laboratorio. 2) Preparar
M A T E R I A L E S SOLUCIONES
 M A T E R I A L E S SOLUCIONES I Componentes Mayor proporción solvente Menor proporción soluto Concentración: indica la cantidad de soluto presente en una dada cantidad de solvente o una dada cantidad
M A T E R I A L E S SOLUCIONES I Componentes Mayor proporción solvente Menor proporción soluto Concentración: indica la cantidad de soluto presente en una dada cantidad de solvente o una dada cantidad
DETERMINACIÓN POR DESTILACIÓN DEL LIGANTE RESIDUAL Y DEL FLUIDIFICANTE EN LAS EMULSIONES BITUMINOSAS UNE-EN 1431:2009
 DETERMINACIÓN POR DESTILACIÓN DEL LIGANTE RESIDUAL Y DEL FLUIDIFICANTE EN LAS EMULSIONES BITUMINOSAS UNE-EN 1431:2009 PT-03 Rev. 0 Fecha: Junio 2017 Redactado GT1 ATEB Aprobado COMITÉ TÉCNICO ATEB Página
DETERMINACIÓN POR DESTILACIÓN DEL LIGANTE RESIDUAL Y DEL FLUIDIFICANTE EN LAS EMULSIONES BITUMINOSAS UNE-EN 1431:2009 PT-03 Rev. 0 Fecha: Junio 2017 Redactado GT1 ATEB Aprobado COMITÉ TÉCNICO ATEB Página
PREPARACIÓN DE DISOLUCIONES
 PREPARACIÓN DE DISOLUCIONES Objetivo El alumno debe ser capaz de preparar una disolución de concentración determinada a partir de sus componentes, soluto y disolvente. Aquí se van a preparar las disoluciones
PREPARACIÓN DE DISOLUCIONES Objetivo El alumno debe ser capaz de preparar una disolución de concentración determinada a partir de sus componentes, soluto y disolvente. Aquí se van a preparar las disoluciones
COLEGIO JORGE ELIÉCER GAITÁN. QUÍMICA II SOLUCIONES 1 Parte: Conceptos, Clases de soluciones, Solubilidad, concentración física de las soluciones.
 COLEGIO JORGE ELIÉCER GAITÁN QUÍMICA II SOLUCIONES 1 Parte: Conceptos, Clases de soluciones,, concentración física de las soluciones. NOMBRE: CURSO LAS SOLUCIONES En la naturaleza es muy raro encontrar
COLEGIO JORGE ELIÉCER GAITÁN QUÍMICA II SOLUCIONES 1 Parte: Conceptos, Clases de soluciones,, concentración física de las soluciones. NOMBRE: CURSO LAS SOLUCIONES En la naturaleza es muy raro encontrar
SOLUCIONES EJERCICIOS TEMA 3
 SOLUCIONES EJERCICIOS TEMA 3 1 Completar la definición siguiente: Los sistemas materiales son los que presentan distinta y distintas en las diferentes partes del sistema. Los componentes de un pueden distinguirse
SOLUCIONES EJERCICIOS TEMA 3 1 Completar la definición siguiente: Los sistemas materiales son los que presentan distinta y distintas en las diferentes partes del sistema. Los componentes de un pueden distinguirse
03 DISOLUCIONES. 2 Observando la curva de solubilidad del clorato potásico, responder:
 03 DISOLUCIONES 1 Sabemos que cierta disolución tiene una concentración de c = 512 g/l. Si su densidad es1,43 g/l, expresa el valor de su concentración en tanto por ciento. 2 Observando la curva de solubilidad
03 DISOLUCIONES 1 Sabemos que cierta disolución tiene una concentración de c = 512 g/l. Si su densidad es1,43 g/l, expresa el valor de su concentración en tanto por ciento. 2 Observando la curva de solubilidad
ESAS METAS SON RESPONSABILIDAD DE TODOS Y CADA UNO DE LOS QUE PARTICIPAN EN LABORATORIO. PAUTAS PARA LA PRESENTACION DE LOS TRABAJOS
 INTRODUCCION AL TRABAJO DE LABORATORIO En el trabajo cotidiano existen riesgos y con mucha más razón si el trabajo se desarrolla en el laboratorio, debido a que se experimentan una serie de situaciones
INTRODUCCION AL TRABAJO DE LABORATORIO En el trabajo cotidiano existen riesgos y con mucha más razón si el trabajo se desarrolla en el laboratorio, debido a que se experimentan una serie de situaciones
FÍSICA Y QUÍMICA 2º ESO TEMA VI COMPOSICIÓN DE LA MATERIA
 FÍSICA Y QUÍMICA 2º ESO TEMA VI COMPOSICIÓN DE LA MATERIA 1) MEZCLAS HOMOGÉNEAS Y HETEROGÉNEAS Una mezcla es una composición de sustancias con distintas propiedades. Una mezcla es homogénea si está formada
FÍSICA Y QUÍMICA 2º ESO TEMA VI COMPOSICIÓN DE LA MATERIA 1) MEZCLAS HOMOGÉNEAS Y HETEROGÉNEAS Una mezcla es una composición de sustancias con distintas propiedades. Una mezcla es homogénea si está formada
DETERMINACIÓN DE LA DENSIDAD
 REV. 0 Pág. 1/7 DETERMINACIÓN DE LA DENSIDAD CURSO: 2016-17 MANUEL GUTIÉRREZ PALMA GRUPO: 1º LACC REV. 0 Pág. 2/7 ÍNDICE 1. INTRODUCCIÓN TEÓRICA.... 3 2. OBJETIVO.... 3 3. MATERIALES Y METODOS... 4 3.1.
REV. 0 Pág. 1/7 DETERMINACIÓN DE LA DENSIDAD CURSO: 2016-17 MANUEL GUTIÉRREZ PALMA GRUPO: 1º LACC REV. 0 Pág. 2/7 ÍNDICE 1. INTRODUCCIÓN TEÓRICA.... 3 2. OBJETIVO.... 3 3. MATERIALES Y METODOS... 4 3.1.
METALES Y ALEACIONES. 1. Calcula la concentración de carbono en un acero que tiene 1200 Kg de hierro puro y 8,5 Kg de carbono. Solución: 0,70% de C
 METALES Y ALEACIONES 1. Calcula la concentración de carbono en un acero que tiene 1200 Kg de hierro puro y 8,5 Kg de carbono. Solución: 0,70% de C 2. Tenemos 2000 kg de acero, con una concentración del
METALES Y ALEACIONES 1. Calcula la concentración de carbono en un acero que tiene 1200 Kg de hierro puro y 8,5 Kg de carbono. Solución: 0,70% de C 2. Tenemos 2000 kg de acero, con una concentración del
Práctica 2. Densidad
 Universidad Nacional Autónoma de México Facultad de Química Laboratorio de Química General I 1 Grupo Equipo Práctica 2. Elaboró: M. en C. Ruy F. Cervantes Díaz de Guzmán Revisaron: M. en C. Martha Magdalena
Universidad Nacional Autónoma de México Facultad de Química Laboratorio de Química General I 1 Grupo Equipo Práctica 2. Elaboró: M. en C. Ruy F. Cervantes Díaz de Guzmán Revisaron: M. en C. Martha Magdalena
Clasifica los siguientes sistemas materiales en elementos, compuestos o mezclas homogéneas o heterogéneas:
 TITULO (edite antes de imprimir) NOMBRE: CURSO: 1) Clasifica los siguientes sistemas materiales en elementos, compuestos o mezclas homogéneas o heterogéneas: Plomo ; acero ; mercurio ; óxido de hierro
TITULO (edite antes de imprimir) NOMBRE: CURSO: 1) Clasifica los siguientes sistemas materiales en elementos, compuestos o mezclas homogéneas o heterogéneas: Plomo ; acero ; mercurio ; óxido de hierro
Área de Ciencias Naturales LABORATORIO DE FISICA. Física II. Actividad experimental No.1. Propiedades Particulares de la Materia
 Área de Ciencias Naturales LABORATORIO DE FISICA Física II ALUMNO(A): GRUPO: EQUIPO: PROFESOR(A): FECHA: CALIFICACION: Actividad experimental No.1 Propiedades Particulares de la Materia EXPERIMENTO No.
Área de Ciencias Naturales LABORATORIO DE FISICA Física II ALUMNO(A): GRUPO: EQUIPO: PROFESOR(A): FECHA: CALIFICACION: Actividad experimental No.1 Propiedades Particulares de la Materia EXPERIMENTO No.
Instrumentos de medida y material de laboratorio
 El estudio y comprensión de la Física y la Química requiere de cierto trabajo en el laboratorio. Para poder llevarlo a cabo necesitamos, además de una serie de reactivos químicos, distinto material de
El estudio y comprensión de la Física y la Química requiere de cierto trabajo en el laboratorio. Para poder llevarlo a cabo necesitamos, además de una serie de reactivos químicos, distinto material de
MATERIALES DE LABORATORIO
 MATERIALES DE LABORATORIO Instrumentos para realizar diversas medidas Balanza de laboratorio Se utiliza para medir la masa de un cuerpo. Su sensibilidad no llega más allá del centígramo. Instrumentos para
MATERIALES DE LABORATORIO Instrumentos para realizar diversas medidas Balanza de laboratorio Se utiliza para medir la masa de un cuerpo. Su sensibilidad no llega más allá del centígramo. Instrumentos para
El papel de los métodos simplificados en la prevención del riesgo químico
 El papel de los métodos simplificados en la prevención del riesgo químico A Coruña, 17 de febrero de 2012 Mª Encarnación Sousa Rodríguez INSHT Aplicaciones Estimación inicial. UNE-EN 689. Fase de diseño.
El papel de los métodos simplificados en la prevención del riesgo químico A Coruña, 17 de febrero de 2012 Mª Encarnación Sousa Rodríguez INSHT Aplicaciones Estimación inicial. UNE-EN 689. Fase de diseño.
QUÍMICA 2º BACHILLERATO
 DISOLUCIONES: CONCENTRACIÓN DE LAS MISMAS 1.-/ Se disuelven 7 g de cloruro de sodio en 43 g de agua. Determine la concentración centesimal de la disolución, así como la fracción molar de cada componente
DISOLUCIONES: CONCENTRACIÓN DE LAS MISMAS 1.-/ Se disuelven 7 g de cloruro de sodio en 43 g de agua. Determine la concentración centesimal de la disolución, así como la fracción molar de cada componente
PRÁCTICA # 5 PREPARACIÓN DE DISOLUCIONES. 1. Preparar soluciones de diversas sustancias poniendo en práctica las
 PRÁCTICA # 5 PREPARACIÓN DE DISOLUCIONES OBJETIVOS 1. Preparar soluciones de diversas sustancias poniendo en práctica las técnicas más comunes. 2. Practicar cálculos que involucren cantidades de soluto,
PRÁCTICA # 5 PREPARACIÓN DE DISOLUCIONES OBJETIVOS 1. Preparar soluciones de diversas sustancias poniendo en práctica las técnicas más comunes. 2. Practicar cálculos que involucren cantidades de soluto,
TEMA 3: Composición de la Materia
 TEMA 3: Composición de la Materia 1. Mezclas homogéneas y heterogéneas Una mezcla es una composición de varias sustancias con distintas propiedades. Distinguimos dos tipos de mezclas: Mezclas homogéneas:
TEMA 3: Composición de la Materia 1. Mezclas homogéneas y heterogéneas Una mezcla es una composición de varias sustancias con distintas propiedades. Distinguimos dos tipos de mezclas: Mezclas homogéneas:
Sede central Mendoza Argentina San Martín 430 Ciudad Mendoza Argentina Tel.: Fax:
 Sede central Mendoza Argentina San Martín 430 Ciudad Mendoza Argentina Tel.: 54 261 521 6604 521 6605 521 6773 Fax: 54 261 5216606 DETERMINACIÓN DEL EXTRACTO SECO TOTAL DENSIMÉTRICO Lic. Luciana Garcia
Sede central Mendoza Argentina San Martín 430 Ciudad Mendoza Argentina Tel.: 54 261 521 6604 521 6605 521 6773 Fax: 54 261 5216606 DETERMINACIÓN DEL EXTRACTO SECO TOTAL DENSIMÉTRICO Lic. Luciana Garcia
Prácticas de análisis de los vinos. Dpto. Nutrición y Bromatología II. Facultad de Farmacia. UCM
 Prácticas de análisis de los vinos. Dpto. Nutrición y Bromatología II. Facultad de Farmacia. UCM DETERMINACIONES ANALÍTICAS EN EL VINO ph ACIDEZ TOTAL ACIDEZ VOLÁTIL GRADO ALCOHÓLICO SULFUROSO ÍNDICE DE
Prácticas de análisis de los vinos. Dpto. Nutrición y Bromatología II. Facultad de Farmacia. UCM DETERMINACIONES ANALÍTICAS EN EL VINO ph ACIDEZ TOTAL ACIDEZ VOLÁTIL GRADO ALCOHÓLICO SULFUROSO ÍNDICE DE
SOL 1 Química Básica e Industrial
 SOL 1 Química Básica e Industrial - 2016 Materiales de laboratorio de vidrio y porcelana.- Embudo Embudo Buchner Embudo de decantación Desecadores Vaso de bohemia Matraz Erlenmeyer Probetas Buretas Pipetas
SOL 1 Química Básica e Industrial - 2016 Materiales de laboratorio de vidrio y porcelana.- Embudo Embudo Buchner Embudo de decantación Desecadores Vaso de bohemia Matraz Erlenmeyer Probetas Buretas Pipetas
DETERMINACIÓN DEL PORCENTAJE DE PLOMO MTC E
 DETERMINACIÓN DEL PORCENTAJE DE PLOMO MTC E 1219 2000 Este Modo Operativo está basado en la Norma ASTM D 49, el mismo que se han adaptado al nivel de implementación y a las condiciones propias de nuestra
DETERMINACIÓN DEL PORCENTAJE DE PLOMO MTC E 1219 2000 Este Modo Operativo está basado en la Norma ASTM D 49, el mismo que se han adaptado al nivel de implementación y a las condiciones propias de nuestra
QUÍMICA 2º BACHILLERATO
 DISOLUCIONES: CONCENTRACIÓN DE LAS MISMAS 1.-/ Se disuelven 7 g de cloruro de sodio en 43 g de agua. Determine la concentración centesimal de la disolución, así como la fracción molar de cada componente
DISOLUCIONES: CONCENTRACIÓN DE LAS MISMAS 1.-/ Se disuelven 7 g de cloruro de sodio en 43 g de agua. Determine la concentración centesimal de la disolución, así como la fracción molar de cada componente
PROPIEDADES DE LA MATERIA. Prof. Jackeline Ruttell torres Química Febrero 2017
 PROPIEDADES DE LA MATERIA Prof. Jackeline Ruttell torres Química Febrero 2017 DEFINICIONES IMPORTANTES Sustancia: materia con composición uniforme y constante Ej. Agua siempre posee dos átomos de hidrógeno
PROPIEDADES DE LA MATERIA Prof. Jackeline Ruttell torres Química Febrero 2017 DEFINICIONES IMPORTANTES Sustancia: materia con composición uniforme y constante Ej. Agua siempre posee dos átomos de hidrógeno
PRÁCTICA 11 COEFICIENTE DE REPARTO 1.- FUNDAMENTO TEÓRICO
 PRÁCTICA 11 COEFICIENTE DE REPARTO 1.- FUNDAMENTO TEÓRICO Cuando una sustancia se distribuye entre dos líquidos miscibles entre sí o ligeramente miscibles, la relación de las concentraciones de dicha sustancia
PRÁCTICA 11 COEFICIENTE DE REPARTO 1.- FUNDAMENTO TEÓRICO Cuando una sustancia se distribuye entre dos líquidos miscibles entre sí o ligeramente miscibles, la relación de las concentraciones de dicha sustancia
OXIDACION DE n-butanol A. a) Ejemplificar un método para obtener aldehídos alifáticos mediante la oxidación de alcoholes.
 PRÁCTICA OXIDACION DE n-butanol A n-butiraldehído I. OBJETIVOS a) Ejemplificar un método para obtener aldehídos alifáticos mediante la oxidación de alcoholes. b) Formar un derivado sencillo del aldehído
PRÁCTICA OXIDACION DE n-butanol A n-butiraldehído I. OBJETIVOS a) Ejemplificar un método para obtener aldehídos alifáticos mediante la oxidación de alcoholes. b) Formar un derivado sencillo del aldehído
Actividades para repasar el examen de septiembre
 Actividades para repasar el examen de septiembre 1. Qué es una magnitud? Qué es medir? Pon un ejemplo que ayude a entender este concepto, utiliza un dibujo explicativo. Pon ejemplos de magnitudes y de
Actividades para repasar el examen de septiembre 1. Qué es una magnitud? Qué es medir? Pon un ejemplo que ayude a entender este concepto, utiliza un dibujo explicativo. Pon ejemplos de magnitudes y de
La materia se puede definir como todo aquello que tiene masa y ocupa un volumen.
 Tema 2: LA MATERIA Que es la materia? La materia se puede definir como todo aquello que tiene masa y ocupa un volumen. Clasificación de la materia (criterio: separación) Mezclas Sustancias puras Composición
Tema 2: LA MATERIA Que es la materia? La materia se puede definir como todo aquello que tiene masa y ocupa un volumen. Clasificación de la materia (criterio: separación) Mezclas Sustancias puras Composición
TEMA 3 MEZCLAS, DISOLUCIONES Y SUSTANCIAS PURAS. 1. Distinguir mezcla homogénea de mezcla heterogénea.* х
 TEMA 3 MEZCLAS, DISOLUCIONES Y SUSTANCIAS PURAS 3º F/Q OBJETIVOS Estudiar los distintos tipos de mezclas, sus aplicaciones y sus técnicas de separación. Realizar su clasificación atendiendo a diversos
TEMA 3 MEZCLAS, DISOLUCIONES Y SUSTANCIAS PURAS 3º F/Q OBJETIVOS Estudiar los distintos tipos de mezclas, sus aplicaciones y sus técnicas de separación. Realizar su clasificación atendiendo a diversos
TEMA: CAMBIOS FÍSICOS, QUÍMICOS Y TÉCNICAS DE SEPARACIÓN
 Guía de Laboratorio Nº 2 TEMA: CAMBIOS FÍSICOS, QUÍMICOS Y TÉCNICAS DE SEPARACIÓN I. Introducción La materia existe en tres estados normales, sólidos, líquidos y gaseosos, y puede transformarse de un estado
Guía de Laboratorio Nº 2 TEMA: CAMBIOS FÍSICOS, QUÍMICOS Y TÉCNICAS DE SEPARACIÓN I. Introducción La materia existe en tres estados normales, sólidos, líquidos y gaseosos, y puede transformarse de un estado
DESTILACIÓN SIMPLE Y FRACCIONADA. a) Conocer una destilación simple, sus principales características y factores que en ella intervienen.
 DESTILACIÓN SIMPLE Y FRACCIONADA I. OBJETIVOS a) Conocer una destilación simple, sus principales características y factores que en ella intervienen. b) Conocer una destilación fraccionada, sus principales
DESTILACIÓN SIMPLE Y FRACCIONADA I. OBJETIVOS a) Conocer una destilación simple, sus principales características y factores que en ella intervienen. b) Conocer una destilación fraccionada, sus principales
LA DESTILACIÓN POR: LINA GÓMEZ, SANTIAGO GÓMEZ, CAROLINA FADUL
 LA DESTILACIÓN POR: LINA GÓMEZ, SANTIAGO GÓMEZ, CAROLINA FADUL QUÉ ES LA DESTILACIÓN? La destilación es un método comúnmente utilizado para la purificación de líquidos y la separación de mezclas con el
LA DESTILACIÓN POR: LINA GÓMEZ, SANTIAGO GÓMEZ, CAROLINA FADUL QUÉ ES LA DESTILACIÓN? La destilación es un método comúnmente utilizado para la purificación de líquidos y la separación de mezclas con el
ACTIVIDADES DE RECUPERACIÓN DE FÍSICA Y QUÍMICA 3º ESO
 ACTIVIDADES DE RECUPERACIÓN DE FÍSICA Y QUÍMICA 3º ESO [ E s c r i b i r e l n o m b r e d e l a c o m p a ñ í a ] F E C H A D E E N T R E G A 6 D E F E B R E R O S e r e a l i z a r á u n a p r u e b
ACTIVIDADES DE RECUPERACIÓN DE FÍSICA Y QUÍMICA 3º ESO [ E s c r i b i r e l n o m b r e d e l a c o m p a ñ í a ] F E C H A D E E N T R E G A 6 D E F E B R E R O S e r e a l i z a r á u n a p r u e b
EXTRACCION SIMPLE Y MULTIPLE Y DEL PRINCIPIO ACTIVO DEL CLORASEPTIC
 PRACTICA X EXTRACCION SIMPLE Y MULTIPLE Y DEL PRINCIPIO ACTIVO DEL CLORASEPTIC I. OBJETIVOS II MATERIAL a) Conocer la técnica de extracción como método de separación y purificación de las sustancias integrantes
PRACTICA X EXTRACCION SIMPLE Y MULTIPLE Y DEL PRINCIPIO ACTIVO DEL CLORASEPTIC I. OBJETIVOS II MATERIAL a) Conocer la técnica de extracción como método de separación y purificación de las sustancias integrantes
RESOLUCIÓN OENO 25/2004
 DICARBONATO DE DIMETILO (DMDC) LA ASAMBLEA GENERAL, Visto el artículo 2, párrafo 2 iv del Acuerdo del 3 de abril de 2001 por el cual se creó la Organización Internacional de la Viña y el Vino, A propuesta
DICARBONATO DE DIMETILO (DMDC) LA ASAMBLEA GENERAL, Visto el artículo 2, párrafo 2 iv del Acuerdo del 3 de abril de 2001 por el cual se creó la Organización Internacional de la Viña y el Vino, A propuesta
Materiales de uso técnico. La Madera y los Metales
 Materiales de uso técnico La Madera y los Metales El hombre a lo largo de la historia ha utilizado la naturaleza para satisfacer sus necesidades y mejorar sus condiciones de vida. Para ello ha fabricado
Materiales de uso técnico La Madera y los Metales El hombre a lo largo de la historia ha utilizado la naturaleza para satisfacer sus necesidades y mejorar sus condiciones de vida. Para ello ha fabricado
TEMA 1: LA MEDIDA DE LA MATERIA
 TEMA 1: LA MEDIDA DE LA MATERIA 1. LA MATERIA: las magnitudes físicas La materia constituye todo aquello que ocupa un lugar en el espacio y tiene una determinada masa. En esta unidad vamos a estudiar alguna
TEMA 1: LA MEDIDA DE LA MATERIA 1. LA MATERIA: las magnitudes físicas La materia constituye todo aquello que ocupa un lugar en el espacio y tiene una determinada masa. En esta unidad vamos a estudiar alguna
CORPORACION MUNICIPAL DE DESARROLLO SOCIAL LICEO INDUSTRIAL EULOGIO GORDO MONEO ANTOFAGASTA FONO FAX:
 CORPORACION MUNICIPAL DE DESARROLLO SOCIAL LICEO INDUSTRIAL EULOGIO GORDO MONEO ANTOFAGASTA FONO FAX:55-2231189 WWW.LICEOINDUSTRIALEGM.CL GUÍA DE APRENDIZAJE Profesor Asignatura Objetivo de Aprendizaje
CORPORACION MUNICIPAL DE DESARROLLO SOCIAL LICEO INDUSTRIAL EULOGIO GORDO MONEO ANTOFAGASTA FONO FAX:55-2231189 WWW.LICEOINDUSTRIALEGM.CL GUÍA DE APRENDIZAJE Profesor Asignatura Objetivo de Aprendizaje
LA MATERIA. Física y Química 3º ESO
 LA MATERIA Física y Química 3º ESO Índice Propiedades de la materia Estados de agregación de la materia Cambios de estado Teoría cinética de la materia Temperatura y presión Cambios de estado Leyes de
LA MATERIA Física y Química 3º ESO Índice Propiedades de la materia Estados de agregación de la materia Cambios de estado Teoría cinética de la materia Temperatura y presión Cambios de estado Leyes de
Práctica 3. Densidad
 Práctica 3. Densidad PREGUNTAS A RESPONDER AL FINAL DE LA PRÁCTICA La densidad es una propiedad intensiva o extensiva? Por qué? Cómo influye la temperatura en la densidad de una disolución de azúcar? PROBLEMA
Práctica 3. Densidad PREGUNTAS A RESPONDER AL FINAL DE LA PRÁCTICA La densidad es una propiedad intensiva o extensiva? Por qué? Cómo influye la temperatura en la densidad de una disolución de azúcar? PROBLEMA
Qué cantidad de agua destilada se necesita para preparar 350 g de una loción cosmética que tiene una concentración del 8 en masa?
 TITULO (edite antes de imprimir) NOMBRE: CURSO: 1) Qué cantidad de agua destilada se necesita para preparar 350 g de una loción cosmética que tiene una concentración del 8 en masa? Si la disolución debe
TITULO (edite antes de imprimir) NOMBRE: CURSO: 1) Qué cantidad de agua destilada se necesita para preparar 350 g de una loción cosmética que tiene una concentración del 8 en masa? Si la disolución debe
MANUAL DE PRÁCTICAS DE LABORATORIO I DE QUÍMICA
 Página 70 de 92 PRÁCTICA 8. 8. PROPIEDADES DE LAS SUSTANCIAS: SOLUBILIDAD 8.1. OBJETIVOS - Adquirir destreza en la determinación cualitativa de la solubilidad de un sólido y de un líquido. - Reconocer
Página 70 de 92 PRÁCTICA 8. 8. PROPIEDADES DE LAS SUSTANCIAS: SOLUBILIDAD 8.1. OBJETIVOS - Adquirir destreza en la determinación cualitativa de la solubilidad de un sólido y de un líquido. - Reconocer
Disoluciones y cálculos de concentraciones
 Disoluciones y cálculos de concentraciones Disoluciones Una disolución es una mezcla homogénea (los componentes no se pueden distinguir a simple vista) de dos o más sustancias en proporciones variables.
Disoluciones y cálculos de concentraciones Disoluciones Una disolución es una mezcla homogénea (los componentes no se pueden distinguir a simple vista) de dos o más sustancias en proporciones variables.
Sustituir fotografía. Sustituir texto
 Soluciones Sustituir fotografía Sustituir texto Tipos de soluciones. Hidrólisis. Solubilidad y el efecto de la temperatura. Unidades de concentración: Expresiones físicas de concentración (%m/m, %m/v,
Soluciones Sustituir fotografía Sustituir texto Tipos de soluciones. Hidrólisis. Solubilidad y el efecto de la temperatura. Unidades de concentración: Expresiones físicas de concentración (%m/m, %m/v,
6.5. OBTENCIÓN DE MATERIAS PRIMAS.
 6.5. OBTENCIÓN DE MATERIAS PRIMAS. 6.5.1. MINERIA. La minería es la obtención selectiva de minerales y otros materiales no orgánicos de la corteza terrestre para su aprovechamiento por el hombre. Es una
6.5. OBTENCIÓN DE MATERIAS PRIMAS. 6.5.1. MINERIA. La minería es la obtención selectiva de minerales y otros materiales no orgánicos de la corteza terrestre para su aprovechamiento por el hombre. Es una
SOLUCIONARIO Guía Estándar Anual
 SOLUCIONARIO Guía Estándar Anual Disoluciones I: mezclas, disoluciones y unidades porcentuales de concentración SGUICES010CB33-A16V1 Ítem Alternativa Habilidad 1 D Reconocimiento 2 A Reconocimiento 3 C
SOLUCIONARIO Guía Estándar Anual Disoluciones I: mezclas, disoluciones y unidades porcentuales de concentración SGUICES010CB33-A16V1 Ítem Alternativa Habilidad 1 D Reconocimiento 2 A Reconocimiento 3 C
TEMA 2: LA MATERIA: CÓMO SE PRESENTA?
 TEMA 2: LA MATERIA: CÓMO SE PRESENTA? 1.- La materia: sustancias puras y mezclas. 1.1.- Recordatorio. 1.2.- Sustancias puras. 1.3.- Mezclas. 1.4.- Cómo distinguir un coloide de una mezcla homogénea. 2.-
TEMA 2: LA MATERIA: CÓMO SE PRESENTA? 1.- La materia: sustancias puras y mezclas. 1.1.- Recordatorio. 1.2.- Sustancias puras. 1.3.- Mezclas. 1.4.- Cómo distinguir un coloide de una mezcla homogénea. 2.-
1. Se dispone de una disolución acuosa de ácido sulfúrico del 98% de riqueza en masa y densidad 1,84 g/ml.
 ESTEQUIOMETRÍA,DISOLUCIONES: ACTIVIDADES DE SELECTIVIDAD. 1. Se dispone de una disolución acuosa de ácido sulfúrico del 98% de riqueza en masa y densidad 1,84 g/ml. a) Qué volumen de esta disolución se
ESTEQUIOMETRÍA,DISOLUCIONES: ACTIVIDADES DE SELECTIVIDAD. 1. Se dispone de una disolución acuosa de ácido sulfúrico del 98% de riqueza en masa y densidad 1,84 g/ml. a) Qué volumen de esta disolución se
Tema 7. Las mezclas. Introducción
 Tema 7. Las mezclas Introducción Ya sabes que los sistemas materiales se pueden clasificar según su composición en sustancias puras y mezclas. Las sustancias puras son los elementos y los compuestos que
Tema 7. Las mezclas Introducción Ya sabes que los sistemas materiales se pueden clasificar según su composición en sustancias puras y mezclas. Las sustancias puras son los elementos y los compuestos que
UNAM- Facultad de Química Prof. Mario Alfredo García Carrillo
 GUIA DE ESTUDIOS PARA EL PRIMER EXAMEN. 1. El punto de fusión del ácido benzoico puro y del 2-naftol puro son 122.5 C y 123 C respectivamente. Se tiene una muestra que no se sabe si es ácido benzoico o
GUIA DE ESTUDIOS PARA EL PRIMER EXAMEN. 1. El punto de fusión del ácido benzoico puro y del 2-naftol puro son 122.5 C y 123 C respectivamente. Se tiene una muestra que no se sabe si es ácido benzoico o
OBTENCIÓN DE ACETATO DE ISOAMILO. a) Preparar un éster a partir de un alcohol y un ácido carboxílico.
 PRÁCTICA 11 OBTENCIÓN DE ACETATO DE ISOAMILO (ACEITE DE PLATANO) I. OBJETIVO a) Preparar un éster a partir de un alcohol y un ácido carboxílico. b) Aplicar algunas técnicas de laboratorio ya conocidas
PRÁCTICA 11 OBTENCIÓN DE ACETATO DE ISOAMILO (ACEITE DE PLATANO) I. OBJETIVO a) Preparar un éster a partir de un alcohol y un ácido carboxílico. b) Aplicar algunas técnicas de laboratorio ya conocidas
ADHESIVIDAD DE LOS LIGANTES BITUMINOSOS A LOS AGREGADOS FINOS (Método Riedel-Weber) I.N.V. E
 ADHESIVIDAD DE LOS LIGANTES BITUMINOSOS A LOS AGREGADOS FINOS (Método Riedel-Weber) I.N.V. E 774 07 1. OBJETO 1.1 Esta norma describe el procedimiento que se debe seguir para determinar la adhesividad
ADHESIVIDAD DE LOS LIGANTES BITUMINOSOS A LOS AGREGADOS FINOS (Método Riedel-Weber) I.N.V. E 774 07 1. OBJETO 1.1 Esta norma describe el procedimiento que se debe seguir para determinar la adhesividad
Universidad Metropolitana Centro de Aguadilla Laboratorio de Química. Medidas de Masa y Densidad e Incertidumbre
 Universidad Metropolitana Centro de Aguadilla Laboratorio de Química Medidas de Masa y Densidad e Incertidumbre Objetivos: Reconocer la incertidumbre en las medidas Familiarizarse con las medidas de longitud,
Universidad Metropolitana Centro de Aguadilla Laboratorio de Química Medidas de Masa y Densidad e Incertidumbre Objetivos: Reconocer la incertidumbre en las medidas Familiarizarse con las medidas de longitud,
IES SIERRA DEL AGUA ACTIVIDADES DE FÍSICA Y QUÍMICA DE ALUMNOS PENDIENTES DE 3º DE ESO
 IES SIERRA DEL AGUA ACTIVIDADES DE FÍSICA Y QUÍMICA DE ALUMNOS PENDIENTES DE 3º DE ESO Tema 1: Medida y método científico. 1. Transforme las siguientes magnitudes al S.I de unidades: a) 228 Gm b) 436 ns
IES SIERRA DEL AGUA ACTIVIDADES DE FÍSICA Y QUÍMICA DE ALUMNOS PENDIENTES DE 3º DE ESO Tema 1: Medida y método científico. 1. Transforme las siguientes magnitudes al S.I de unidades: a) 228 Gm b) 436 ns
