Adsorción (Tomado de Tejeda y col., 1995)
|
|
|
- Felisa Lozano Soriano
- hace 7 años
- Vistas:
Transcripción
1 Adsorción (Tomado de Tejeda y col., 1995) Sergio Huerta Ochoa UAM-Iztapalapa
2 La adsorción es una de las operaciones más utilizadas en la etapa de concentración de caldos acuosos diluidos. Mediante la adsorción, las moléculas de un soluto se concentran en una superficie sólida por la acción de fuerzas intermoleculares entre el soluto y el sólido. Debido a estas fuerzas el fenómeno es fácilmente reversible. La adsorción es esencialmente un fenómeno de superficie. 1. Contacto del adsorbente y la solución La operación de adsorción requiere de cuatro pasos 2. Al efectuarse la adsorción el soluto se une preferentemente a la superficie del adsorbente respecto a otros solutos 3. Lavado de la columna con una solución que no provoque la desorción del soluto de interés 4. Finalmente se efectúa la recuperación del soluto utilizando un fluído que favorezca la desorción, elución
3 El establecimiento de las relaciones de equilibrio y de la capacidad de adsorción de los sistemas El análisis de la operación de adsorción mediante la formulación de algunos modelos requiere: El establecimiento de la rapidez de la adsorción con respecto a los fenómenos difusivos y cinéticas de superficie Los balances de masa y energía del sistema de adsorción específico (intermitente, continuo, serie, paralelo, etc.) Las condiciones iniciales y de frontera
4 Fundamentos Las operaciones de adsorción son utilizadas en la obtención de varios tipos de productos biotecnológicos como aminoácidos, antibióticos, vitaminas y proteínas. Debido a lo anterior cada vez existe una mayor necesidad de profundizar en los aspectos fundamentales de la operación, tales como: Los tipos de adsorción según el tipo de interacción soluto-adsorbente. Aspectos fundamentales que requieren mayor análisis Los tipos de adsorbente Las relaciones de equilibrio La cinética de la adsorción
5 Tipos de adsorción según el tipo de interacción soluto-adsorbente Física Iónica Se pueden distinguir cuatro tipos básico de adsorción: Hidrofóbica Por afinidad
6 Relaciones de equilibrio En el análisis de los procesos de adsorción los datos de equilibrio se expresan normalmente como isotermas de adsorción: Las isotermas son parte esencial para modelar la adsorción y por lo tanto para el diseño, cálculo de eficiencias y costos de la adsorción. Las isotermas nos permiten estimar el grado de purificación que puede ser alcanzado, la cantidad de adsorbente requerido, y la sensibilidad del proceso respecto a la concentración del producto. Freundlich (Adsorción por intercambio iónico) Cuatro tipos básicos de isotermas Lineal (Aprox. de isotermas en la región baja de concentración del soluto) Langmuir (Adsorción por afinidad) Irreversible (Sistemas altamente específicos)
7 Isoterma de Freundlich: se describe por medio de una ecuación exponencial empírica: n q=ky q = cantidad de soluto adsorbida por cantidad de adsorbente y = concentración de soluto en la solución n = constante adimensional K = constante cuyas unidades dependen de n n < 1 isoterma favorable n > 1 isotermas desfavorables Isoterma lineal: se describe por medio de una ecuación recta que pasa por el origen: q=ky Isoterma Langmuir: se describe por medio de expresiones del tipo: q q K = 0 d + y y q 0 = capacidad máxima del adsorbente K d = constante de equilibrio de desorción
8 Cinética de la adsorción El estudio de las isotermas de adsorción nos permite determinar para un sistema soluto-adsorbente dado, el grado de separación que puede ser logrado y la sensibilidad del proceso respecto a la concentración del soluto. Sin embargo, para el desarrollo del modelo de la adsorción es necesario poder establecer, mediante el empleo de coeficientes de transferencia de masa, la velocidad de la adsorción o el tiempo necesario para alcanzar una cierta separación. La velocidad efectiva de la adsorción depende tanto de las condiciones de operación (Flujo, temperatura, composición y presión), como de la configuración del sistema (intermitente, columna, etc.) y del tamaño del equipo donde se realizará la operación. El estudio de estos efectos se divide en dos grandes conceptos: Los mecanismos de transporte (físicos y químicos) Los efectos de mezclado
9 Mecanismos de transporte Para que una partícula de soluto pueda ser adsorbida en la superficie de un poro del adsorbente, el soluto tiene que pasar del seno de la fase líquida a la superficie del adsorbente. Varias resistencias al movimiento del soluto existen en este proceso que pueden visualizarse principalmente como: Resistencia de la película del líquido que rodea al adsorbente El soluto difunde desde el seno del líquido a través de la película de líquido que rodea a la partícula de adsorbente Resistencia a la difusión en el seno del adsorbente El soluto difunde a través del seno del adsorbente, llamado difusión en la fase del adsorbente Resistencia a la difusión dentro del poro La adsorción se efectúa principalmente dentro del poro, por lo que el soluto debe difundir a través del líquido al interior de los poros. Resistencia a la reacción en la superficie El soluto se une al sitio de adsorción por medio de una reacción de superficie, la cual es más rápida que los procesos anteriores.
10 Control de la resistencia en la película Cuando la resistencia de la película es mucho mayor que la del poro o la de la reacción de superficie, la velocidad de adsorción está controlada a nivel local por el flujo del soluto a través de la película que rodea al adsorbente. En este caso la velocidad de adsorción puede expresarse como: R= kla * ( y y ) k L = Coeficiente de transferencia de masa a = área del adsorbente por unidad de volumen del lecho (adsorbente y líquido) y = Concentración de soluto en el seno de la fase líquida y* = Concentración hipotética de soluto en el líquido, en equilibrio con la concentración de soluto en el adsorbente R =Velocidad de adsorción referida al volumen del lecho (adsorbente y solución) El parámetro a puede ser correlacionado con la porosidad del lecho ε (volumen de líquido sin incluir el líquido de los poros/volumen del lecho) y el diámetro de la partícula del adsorbente d p de acuerdo a la expresión: a ( ) = 6 1 ε d p
11 La resistencia de la película por si misma rara vez controla la rapidez de la transferencia de masa, excepto en los casos en que la partícula de adsorbente es pequeña y la difusividad en el poro es grande. Para sistemas de adsorción en columnas, k L generalmente puede correlacionarse con una expresión de la forma: Sh = C 1 + C 2 ( Re) a ( Sc) b donde C 1, C 2, a y b son constantes y Sh, Re y Sc son los números adimensionales de Sherwood, Reynolds y Schmidt dados por las siguientes relaciones: Sh= k L D d AB p Re = v ρ L d p µ Sc= µ L ρ D L AB
12 Control de la difusión del soluto en el seno del adsorbente La difusión en la fase sólida del soluto una vez que ha pasado del seno del líquido a la fase sólida, se presenta en algunos sólidos homogéneos permeables como las resinas que se utilizan en intercambio iónico o en adsorbentes con poros cubiertos con películas móviles, o en líquidos utilizados para impregnar la partícula porosa. Considerando una geometría esférica uniforme el balance de soluto en la película está dado por: q t = D S 2 q 2 r + 2 r q r D S = Difusividad efectiva del soluto en la fase sólida [L 2 /t] r = La coordenada radial al interior de la partícula [L] q = Concentración de soluto en la fase sólida [M/L 3 ] La velocidad de transferencia de masa entre las fases puede ser expresada por la Ley de Fick como: R a = es el radio externo de la partícula q r R = ad S r= R a
13 El balance de masa del soluto suele ser aproximado utilizando una fuerza impulsora lineal de la siguiente forma: = ψ Sksa * q t ( q q) q* = Concentración hipotética de equilibrio con la concentración de soluto en el seno de la fase líquida ψ S = Factor de corrección adimensional que se introduce al linearizar la expresión k s = Coeficiente de transferencia de masa (L 3 total/área-tiempo) Con la linearización anterior la expresión de la velocidad de transferencia de masa por unidad de volumen de lecho es: R = ( ) ( * 1 ε ψ k a q q) S s k s a se correlaciona con la difusividad mediante la ecuación: k a = s 60D d 2 p S
14 Control de la difusión del soluto en la fase líquida al interior de los poros Cuando la velocidad de adsorción está controlada por la difusión del soluto al interior de los poros de la partícula de adsorbente, hasta el sitio de adsorción, el balance de soluto al interior de la partícula está dado por la expresión: 2 y i yi 2 y i εi = D p t + r r r 1 2 ( ε) q t y i = Concentración de soluto en la fase líquida al interior del poro [M/L 3 ] q i = Concentración de soluto en la fase sólida [M/L 3 ] D p = Difusividad efectiva del soluto al interior del poro [L 2 /t] ε i = Porosidad de la partícula al soluto de interés [L 3 /L 3 ] Para el caso en que la acumulación del soluto al interior del poro sea mucho menor que la velocidad de adsorción, el balance de soluto puede ser escrito como: q t 2 y 2 r i 1 i 2 = D p + 1 εi r La velocidad de transferencia de masa entre las fases puede ser expresada por la ley de Fick como: y r i R = ad p r= R a y r i i
15 Para líquidos la difusividad D p puede ser expresada como: DABεi D = p Γ 0 = Tortuosidad del adsorbente (una medida de la estructura de los sólidos) D AB = Difusión molecular del soluto en un líquido libre de adsorbente ε i = Porosidad de la partícula al soluto de interés [L 3 /L 3 ] El balance de soluto puede aproximarse utilizando una fuerza impulsora lineal: * q ψ pk pa( q q) = t q ( 1 ε) de tal manera que, * ψ k a( q q) R = p R p Γ 0 y A qr ya q* = Concentración hipotética de equilibrio con la concentración de soluto en el seno del líquido q = Concentración promedio de soluto en el adsorbente q R = Concentración de la fase sólida en equilibrio con la concentración y A de la solución que se va a tratar ψ p = Factor de corrección por linearización k p a puede correlacionarse con la difusividad efectiva del poro mediante la expresión k p a = 60 D p d ( 1 ε) 2 p
16 Control de la reacción de superficie Generalmente la reacción de adsorción en la superficie del adsorbente es mucho más rápida que los otros mecanismos y rara vez es el mecanismo controlante. En las expresiones cinéticas más utilizadas la reacción de superficie es tratada como una reacción química, reversible o irreversible, de un cierto orden. Dos expresiones comunmente utilizadas principalmente para sistemas de intercambio iónico son: Cinética reversible de primer orden: Cinética reversible de segundo orden: ( k y k q) R 1 2 = ε [ k y( q q) k q] R = ε k 1 y k 2 son las constantes cinéticas de adsorción y desorción, respectivamente. q 0 es la capacidad máxima de adorción del adsorbente.
17 Efectos de mezclado La velocidad de adsorción efectiva también puede disminuir por efectos de un mezcaldo imperfecto. Uno de los modelos más utilizados para describir la desviación del comportamiento ideal del flujo al interior de las columnas, es el modelo de flujo tapón con dispersión, donde los efectos de la dispersión axial debida a remolinos y de la difusión molecular, se agrupan en el concepto del coeficiente efectivo de dispersión axial, en función del cual se puede definir un coeficiente aparente de transferencia de masa dado por: 2 v k da = E E = Coeficiente de dispersión axial [L 2 /t] v = Velocidad superficial de flujo [L/t] Para flujo laminar en lechos empacados el número de Reynolds basado en el diámetro de las partículas de lecho es menor a 10. Bajo esta consideración el número de Peclet (grado de dispersión en la columna) toma un valor constante de 2 d pv Pe = = 2 E De tal manera que la velocidad de adsorción se puede expresar en función de un coeficiente aparente de transferencia de masa por dispersión R = kda * ( y y )
18 Resistencias combinadas En algunos sistemas, la cinética de adsorción puede ser descrita en forma más adecuada utilizando un modelo donde la combinación de resistencias (p. ej. Película y poro) describen en forma más precisa la cinética. En estos casos, la combinación de resistencias se presenta por medio de un coeficiente de transferencia de masa global que agrupa el efecto de las resistencias individuales. Para el establecimiento del coeficiente global de transferencia de masa es necesario fijar la forma en que las resistencias individuales están relacionadas: en serie o en paralelo. Si se considera como ejemplo el caso de la resistencia de la película y la del poro actuando en serie, para el cálculo del coeficiente global se deben sumar los inversos de los coeficientes individuales (para equilibrios lineales). 1 K 0 = k L k p K 0 = Coeficiente global de transferencia de masa referido a la fase líquida
19 Tipos de cromatografía líquida según el principio de separación Cromatografía líquido-líquido Tipos básicos de cromatografía por elución Cromatografía de filtración en gel Cromatografía por adsorción Física Por intercambio iónico Cromatografía por adsorción De interacción hidrofóbica De fase inversa De afinidad
20 Tipos de cromatografía de acuerdo a la presión de operación Presión baja (1 atm, µm) (Cromatografía de baja presión, FPLC) De acuerdo a la presión de operación y al tamaño de partícula Presión moderada (2-50 atm, µm) Presión alta ( atm, 5-10 µm) (Cromatografía de alta resolución, HPLC)
21 Cromatografía por elución La cromatografía por elución es un método para separar en sus componentes una mezcla de solutos y es empleada con el propósito de purificar productos de interés Eluyente (fase móvil) Muestra a t = 0 Adsorbente (fase estacionaria)
22 Tipos de cromatografía por elución Eluyente (composición constante) Eluyente (composición varía gradualmente) Muestra a t = 0 Muestra a t = 0 Elución isocrática Elución por gradiente La operación de una columna de cromatografía por elución es similar a la de una columna de adsorción. Sin embargo, en la cromatografía por elución la columna no se satura completamente con soluto.
23 Adsorción frontal o cromatografía por elución? Eluyente + A y B diluidos Eluyente + A y B concentrados Adsorción frontal Cromatografía por elución En la cromatografía por elución el soluto se purifica a expensas de un cierto grado de dilución, mientras que en la adsorción el soluto se retiene en la columna y posteriormente se eluye concentrado.
24 Mezcla Filtración en gel Separación por tamaño Flujo Flujo
25 + - Mezcla Intercambio iónico Gradiente salino Matriz cargada positivamente + - Las cargas en las proteínas son debidas a: Cargas positivas: Histidina, lisina, argenina y en menor grado N-aminos terminales Cargas negativas: Ácidos aspártico y glutámico, C-grupos carboxilo terminales y en menor grado residuos de cisteina Arriba de su pi las proteínas tienen carga neta negativa Debajo de su pi las proteínas tienen carga neta positiva
26 Cromatoenfoque ph 9 ph 6 ph 6 ph 9 ph 9 Intercambio iónico Cromatoenfoque
27 Cromatoenfoque Buffer de elución a ph 8 8 ph 4 Tasa de migración Tasa de flujo Proteína con pi Columna equilibrada a ph 10
28 Cromatografía de interacción hidrofóbica ± Mezcla Gradiente salino Matriz cargada con grupos noiónicos ± La hidrofobicidad en la superficie de las proteínas ocurre debido a: La presencia en la superficie de cadenas de aminoácidos no polares tales como: alanina, metionina, triftofano y fenilalanina Iones del salting out decrecen la disponibilidad de agua en solución, incrementan la tensión superficial y mejoran las interacciones hidrofóbicas
29 Protein Lab Planta Piloto de Fermentaciones
30
31
Purificación de la enzima lactato deshidrogenasa de músculo esquelético de pollo
 Purificación de la enzima lactato deshidrogenasa de músculo esquelético de pollo ESQUEMA GENERAL Sesión 1. Extracción y precipitación con sulfato de amonio. Sesión 2. Purificación por cromatografía Sesión
Purificación de la enzima lactato deshidrogenasa de músculo esquelético de pollo ESQUEMA GENERAL Sesión 1. Extracción y precipitación con sulfato de amonio. Sesión 2. Purificación por cromatografía Sesión
TEMA 8: CINÉTICA HETEROGÉNEA CATALÍTICA CQA-8/1
 TEMA 8: CINÉTICA HETEROGÉNEA CATALÍTICA CQA-8/1 CARACTERÍSTICAS DE LAS REACCIONES HETEROGÉNEAS CATALÍTICAS FLUIDO-SÓLIDO Velocidad afectada por la presencia de sustancias ( catalizadores ): modifican la
TEMA 8: CINÉTICA HETEROGÉNEA CATALÍTICA CQA-8/1 CARACTERÍSTICAS DE LAS REACCIONES HETEROGÉNEAS CATALÍTICAS FLUIDO-SÓLIDO Velocidad afectada por la presencia de sustancias ( catalizadores ): modifican la
CROMATOGRAFÍA LÍQUIDA DE ALTA RESOLUCIÓN
 CROMATOGRAFÍA LÍQUIDA DE ALTA RESOLUCIÓN Curso: Química Analítica II Loreto Ascar 2012 Esquema de las bases de la separación en cromatografía de: (a)absorción, (b) partición, (c) Intercambio iónico y (d)
CROMATOGRAFÍA LÍQUIDA DE ALTA RESOLUCIÓN Curso: Química Analítica II Loreto Ascar 2012 Esquema de las bases de la separación en cromatografía de: (a)absorción, (b) partición, (c) Intercambio iónico y (d)
1.5 Métodos de separación de mezclas Decantación, filtración, extracción, cristalización, destilación, cromatografía.
 1.5 Métodos de separación de mezclas Decantación, filtración, extracción, cristalización, destilación, cromatografía. 1 Para tomar apuntes MÉTODO DE SEPARACIÓN PROPIEDAD(ES) EN LAS QUE SE BASA MEZCLAS
1.5 Métodos de separación de mezclas Decantación, filtración, extracción, cristalización, destilación, cromatografía. 1 Para tomar apuntes MÉTODO DE SEPARACIÓN PROPIEDAD(ES) EN LAS QUE SE BASA MEZCLAS
Procesos de membrana Sergio Huerta Ochoa UAM-Iztapalapa
 Procesos de membrana Sergio Huerta Ochoa UAM-Iztapalapa Criterios para considerar el uso de membranas Considere el uso de membranas si: Se considera la concentración de una alimentación diluida La diferencia
Procesos de membrana Sergio Huerta Ochoa UAM-Iztapalapa Criterios para considerar el uso de membranas Considere el uso de membranas si: Se considera la concentración de una alimentación diluida La diferencia
6 APENDICE. A. Curvas de Calibración
 6 APENDICE A. Curvas de Calibración Las muestras colectadas en las hidrólisis contenían básicamente carbohidratos como, glucosa, xilosa y arabinosa, entre otros. Se realizaron curvas de calibración para
6 APENDICE A. Curvas de Calibración Las muestras colectadas en las hidrólisis contenían básicamente carbohidratos como, glucosa, xilosa y arabinosa, entre otros. Se realizaron curvas de calibración para
DISOLUCIONES UNIDAD IV. Licda. Miriam Marroquín Leiva
 DISOLUCIONES UNIDAD IV 1 DISOLUCIÓN Es una mezcla homogénea de dos o más sustancias; el soluto y el disolvente. Es un término utilizado para describir un sistema en el cual una o más sustancias están mezcladas
DISOLUCIONES UNIDAD IV 1 DISOLUCIÓN Es una mezcla homogénea de dos o más sustancias; el soluto y el disolvente. Es un término utilizado para describir un sistema en el cual una o más sustancias están mezcladas
EXTRACCIÓN SÓLIDO - LÍQUIDO. Se le llama también: Lixiviación. Lavado. Percolación Infusión. Decantación por sedimentación
 LIXIVIACIÓN Es la disolución preferente de uno o más componentes de una mezcla sólida por contacto con un disolvente líquido. Es la eliminación de una fracción soluble, en forma de solución, a partir de
LIXIVIACIÓN Es la disolución preferente de uno o más componentes de una mezcla sólida por contacto con un disolvente líquido. Es la eliminación de una fracción soluble, en forma de solución, a partir de
TEMA 1: SISTEMAS MODELADOS POR ECUACIONES DIFERENCIALES EN INGENIERÍA QUÍMICA. CLASIFICACIÓN. GENERALIDADES.
 TEMA 1: SISTEMAS MODELADOS POR ECUACIONES DIFERENCIALES EN INGENIERÍA QUÍMICA. CLASIFICACIÓN. GENERALIDADES. 1. INTRODUCCIÓN. PLANTEAMIENTO DE PROBLEMAS EN INGENIERÍA QUÍMICA 2. PROBLEMAS EXPRESADOS MEDIANTE
TEMA 1: SISTEMAS MODELADOS POR ECUACIONES DIFERENCIALES EN INGENIERÍA QUÍMICA. CLASIFICACIÓN. GENERALIDADES. 1. INTRODUCCIÓN. PLANTEAMIENTO DE PROBLEMAS EN INGENIERÍA QUÍMICA 2. PROBLEMAS EXPRESADOS MEDIANTE
SISTEMAS MATERIALES. Departamento de Física y Química 2º ESO
 SISTEMAS MATERIALES Departamento de Física y Química 2º ESO 0. Mapa conceptual MATERIA Sustancias puras Mezclas Heterogéneas Homogéneas Sistemas coloidales Técnicas de separación Disoluciones Soluto Disolvente
SISTEMAS MATERIALES Departamento de Física y Química 2º ESO 0. Mapa conceptual MATERIA Sustancias puras Mezclas Heterogéneas Homogéneas Sistemas coloidales Técnicas de separación Disoluciones Soluto Disolvente
FOURIER Y NEWTON). LEY DE FICK PARA DIFUSIÓN
 INTRODUCCIÓN. SEMEJANZA ENTRE TRANSFERENCIA DE MASA, CALOR Y MOMENTO (LEYES DE FICK, FOURIER Y NEWTON). LEY DE FICK PARA DIFUSIÓN MOLECULAR. E-mail: williamsscm@hotmail.com TRANSFERENCIA DE MASAS El transporte
INTRODUCCIÓN. SEMEJANZA ENTRE TRANSFERENCIA DE MASA, CALOR Y MOMENTO (LEYES DE FICK, FOURIER Y NEWTON). LEY DE FICK PARA DIFUSIÓN MOLECULAR. E-mail: williamsscm@hotmail.com TRANSFERENCIA DE MASAS El transporte
4. DIFUSION EN SÓLIDO
 4. DIFUSION EN SÓLIDO MATERIALES 13/14 ÍNDICE 1. Conceptos generales. Mecanismos de difusión. 3. Leyes de Fick. 1. Estado estacionario.. Estado no estacionario. 4. Factores de difusión. 5. Aplicaciones
4. DIFUSION EN SÓLIDO MATERIALES 13/14 ÍNDICE 1. Conceptos generales. Mecanismos de difusión. 3. Leyes de Fick. 1. Estado estacionario.. Estado no estacionario. 4. Factores de difusión. 5. Aplicaciones
TÉCNICAS DE MUESTREO, ANÁLISIS E INTERPRETACIÓN. Ingeniería Ambiental
 TÉCNICAS DE MUESTREO, ANÁLISIS E INTERPRETACIÓN Ingeniería Ambiental Problema Elección del método analítico Toma de muestra Tratamiento de la muestra Proceso de medida Tratamiento de los datos Valoración
TÉCNICAS DE MUESTREO, ANÁLISIS E INTERPRETACIÓN Ingeniería Ambiental Problema Elección del método analítico Toma de muestra Tratamiento de la muestra Proceso de medida Tratamiento de los datos Valoración
TRANSFERENCIA DE CALOR
 Conducción Convección Radiación TRANSFERENCIA DE CALOR Ing. Rubén Marcano Temperatura es una propiedad que depende del nivel de interacción molecular. Específicamente la temperatura es un reflejo del nivel
Conducción Convección Radiación TRANSFERENCIA DE CALOR Ing. Rubén Marcano Temperatura es una propiedad que depende del nivel de interacción molecular. Específicamente la temperatura es un reflejo del nivel
CONCEPTOS BÁSICOS DE CATÁLISIS HETEROGÉNEA
 CONCEPTOS BÁSICOS DE CATÁLISIS HETEROGÉNEA Conceptos básicos de catálisis heterogénea 2 Se dice que un reactor opera en fase homogénea si se trabaja en una sola fase. En contraste, el reactor que opera
CONCEPTOS BÁSICOS DE CATÁLISIS HETEROGÉNEA Conceptos básicos de catálisis heterogénea 2 Se dice que un reactor opera en fase homogénea si se trabaja en una sola fase. En contraste, el reactor que opera
REACTOR DE COCHADA CON MEZCLA COMPLETA
 REACTOR DE COCHADA CON MEZCLA COMPLETA PARA UNA REACCIÓN EN LA CUAL LA CONCENTRACIÓN DE LA SUSTANCIA DISMINUYE CON EL TIEMPO, R ES NEGATIVO; CUANDO HAY PRODUCCIÓN O GENERACIÓN DE LA SUSTANCIA DENTRO DEL
REACTOR DE COCHADA CON MEZCLA COMPLETA PARA UNA REACCIÓN EN LA CUAL LA CONCENTRACIÓN DE LA SUSTANCIA DISMINUYE CON EL TIEMPO, R ES NEGATIVO; CUANDO HAY PRODUCCIÓN O GENERACIÓN DE LA SUSTANCIA DENTRO DEL
Contenido. xv xvii xix xxi. Prefacio Agradecimientos Acerca del antor Nomenclatnra. Capítulo 2 Destilación instantánea
 Contenido Prefacio Agradecimientos Acerca del antor Nomenclatnra Capítulo 1 Introdncción a la ingeniería de procesos de separación 1.1. Importancia de las separaciones 1.2. El concepto de equilibrio 1.3.
Contenido Prefacio Agradecimientos Acerca del antor Nomenclatnra Capítulo 1 Introdncción a la ingeniería de procesos de separación 1.1. Importancia de las separaciones 1.2. El concepto de equilibrio 1.3.
PROCESOS DE TRANSFERENCIA DE MASA
 PROCESOS DE TRANSFERENCIA DE MASA 1. Advección La advección es el fenómeno por el cual el agua arrastra las partículas, en cuyo caso, un soluto se mueve con el agua a una velocidad v: donde: K es la permeabilidad
PROCESOS DE TRANSFERENCIA DE MASA 1. Advección La advección es el fenómeno por el cual el agua arrastra las partículas, en cuyo caso, un soluto se mueve con el agua a una velocidad v: donde: K es la permeabilidad
Análisis Funcional Orgánico. Cromatografía Líquida de Alta Resolución (HPLC/CLAR)
 Análisis Funcional Orgánico Cromatografía Líquida de Alta Resolución (HPLC/CLAR) PARTE A Introducción Técnicas instrumentales cromatográficas 1. Gaseosa líquida (CGL) o sólida (CGS) 2. Líquida de Alta
Análisis Funcional Orgánico Cromatografía Líquida de Alta Resolución (HPLC/CLAR) PARTE A Introducción Técnicas instrumentales cromatográficas 1. Gaseosa líquida (CGL) o sólida (CGS) 2. Líquida de Alta
convección (4.1) 4.1. fundamentos de la convección Planteamiento de un problema de convección
 convección El modo de transferencia de calor por convección se compone de dos mecanismos de transporte, que son, la transferencia de energía debido al movimiento aleatorio de las moléculas (difusión térmica)
convección El modo de transferencia de calor por convección se compone de dos mecanismos de transporte, que son, la transferencia de energía debido al movimiento aleatorio de las moléculas (difusión térmica)
Operaciones Básicas de Transferencia de Materia Problemas Tema 6
 1º.- En una torre de relleno, se va a absorber acetona de una corriente de aire. La sección de la torre es de 0.186 m 2, la temperatura de trabajo es 293 K y la presión total es de 101.32 kpa. La corriente
1º.- En una torre de relleno, se va a absorber acetona de una corriente de aire. La sección de la torre es de 0.186 m 2, la temperatura de trabajo es 293 K y la presión total es de 101.32 kpa. La corriente
TRANSPORTE A TRAVÉS DE LA MEMBRANA CELULAR
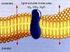 TRANSPORTE A TRAVÉS DE LA MEMBRANA CELULAR Introducción Compartimientos Acuosos separados por Barreras Biológicas Organelos selectivos, autocatalíticos, autoreproductivos, competitivos, adaptativos...
TRANSPORTE A TRAVÉS DE LA MEMBRANA CELULAR Introducción Compartimientos Acuosos separados por Barreras Biológicas Organelos selectivos, autocatalíticos, autoreproductivos, competitivos, adaptativos...
TEMA 6: INTRODUCCIÓN A LA INGENIERÍA DE LA REACCIÓN QUÍMICA. IngQui-6 [1]
![TEMA 6: INTRODUCCIÓN A LA INGENIERÍA DE LA REACCIÓN QUÍMICA. IngQui-6 [1] TEMA 6: INTRODUCCIÓN A LA INGENIERÍA DE LA REACCIÓN QUÍMICA. IngQui-6 [1]](/thumbs/55/36097675.jpg) TEMA 6: INTRODUCCIÓN A LA INGENIERÍA DE LA REACCIÓN QUÍMICA IngQui-6 [1] 6.1 La etapa de reacción en el proceso químico Ingeniería de la Reacción Química: Disciplina que sintetiza la información, los conocimientos
TEMA 6: INTRODUCCIÓN A LA INGENIERÍA DE LA REACCIÓN QUÍMICA IngQui-6 [1] 6.1 La etapa de reacción en el proceso químico Ingeniería de la Reacción Química: Disciplina que sintetiza la información, los conocimientos
Balance de masa con reacción química. Balances de masa con reacción química en reactores discontinuos y continuos.
 Balance de masa con química. Balances de masa con química en reactores discontinuos y continuos. La aparición de una química en un proceso impone las restricciones adicionales dadas por la ecuación estequiométrica
Balance de masa con química. Balances de masa con química en reactores discontinuos y continuos. La aparición de una química en un proceso impone las restricciones adicionales dadas por la ecuación estequiométrica
La solubilidad es la medida de la capacidad de disolverse una cierta sustancia en un determinado medio, a una temperatura y presión determinadas.
 La solubilidad es la medida de la capacidad de disolverse una cierta sustancia en un determinado medio, a una temperatura y presión determinadas. Las proteínas en disolución muestran grandes cambios en
La solubilidad es la medida de la capacidad de disolverse una cierta sustancia en un determinado medio, a una temperatura y presión determinadas. Las proteínas en disolución muestran grandes cambios en
Nutrición Vegetal. Absorción de sales minerales
 Nutrición Vegetal Absorción de sales minerales Absorción - Es el proceso mediante el cual un ión o molécula ingresa a una célula o un cuerpo a través de una membrana. No intervienen fuerzas intermoleculares.
Nutrición Vegetal Absorción de sales minerales Absorción - Es el proceso mediante el cual un ión o molécula ingresa a una célula o un cuerpo a través de una membrana. No intervienen fuerzas intermoleculares.
DESARROLLO COGNOSCITIVO Y APRENDIZAJE
 Prof. Jhonis Valbuena Cátedra: Análisis Instrumental La Electrofóresis es un método de la Química Analítica que utiliza corriente eléctrica controlada con la finalidad de separar biomolèculas según su
Prof. Jhonis Valbuena Cátedra: Análisis Instrumental La Electrofóresis es un método de la Química Analítica que utiliza corriente eléctrica controlada con la finalidad de separar biomolèculas según su
Flujo de Fluidos: Interacción Sólido-Fluido
 Flujo de Fluidos: Interacción Sólido-Fluido Existen operaciones básicas de separación sólido-fluido que tienen gran aplicación y se presentan en muchos de los procesos industriales: filtración, sedimentación,
Flujo de Fluidos: Interacción Sólido-Fluido Existen operaciones básicas de separación sólido-fluido que tienen gran aplicación y se presentan en muchos de los procesos industriales: filtración, sedimentación,
Respuesta: a) La fracción molar de NaCl es 0,072 b) La concentración másica volumétrica de NaCl es 0,231 g/cc
 Ejercicio 1: La densidad a 4 ºC de una solución acuosa de NaCl al 20% en peso es 1,155 g/cc a) Calcule la fracción molar de NaCl b) Calcule la concentración másica volumétrica de NaCl La masa molecular
Ejercicio 1: La densidad a 4 ºC de una solución acuosa de NaCl al 20% en peso es 1,155 g/cc a) Calcule la fracción molar de NaCl b) Calcule la concentración másica volumétrica de NaCl La masa molecular
Las funciones de los seres vivos. Fisiología celular
 Las funciones de los seres vivos Fisiología celular La célula, como unidad funcional de los seres vivos, está capacitada para llevar a cabo las funciones características de éstos: nutrición, reproducción
Las funciones de los seres vivos Fisiología celular La célula, como unidad funcional de los seres vivos, está capacitada para llevar a cabo las funciones características de éstos: nutrición, reproducción
Colegio San Lorenzo - Copiapó - Región de Atacama Per Laborem ad Lucem
 TEMARIO EXAMENES QUIMICA 2012 7º BASICO Descubrimiento del átomo: Quién lo descubrió y su significado Estructura atómica: Partes del átomo, características del núcleo y la corteza, cálculo del protón,
TEMARIO EXAMENES QUIMICA 2012 7º BASICO Descubrimiento del átomo: Quién lo descubrió y su significado Estructura atómica: Partes del átomo, características del núcleo y la corteza, cálculo del protón,
TEMA 1. MECANISMOS BÁSICOS DE TRANSMISIÓN DE CALOR
 TEMA 1. MECANISMOS BÁSICOS DE TRANSMISIÓN DE CALOR El calor: Es una forma de energía en tránsito. La Termodinámica y La Transferencia de calor. Diferencias. TERMODINAMICA 1er. Principio.Permite determinar
TEMA 1. MECANISMOS BÁSICOS DE TRANSMISIÓN DE CALOR El calor: Es una forma de energía en tránsito. La Termodinámica y La Transferencia de calor. Diferencias. TERMODINAMICA 1er. Principio.Permite determinar
Técnicas de Estudio de las células
 Técnicas de Estudio de las células Microscopia Preparaciones permanentes: Fijación Deshidratación Inclusión Corte Fijación: Acidos, solventes orgánicos como alcohol, aldehídos (Formaldehído, glutaraldehídos)
Técnicas de Estudio de las células Microscopia Preparaciones permanentes: Fijación Deshidratación Inclusión Corte Fijación: Acidos, solventes orgánicos como alcohol, aldehídos (Formaldehído, glutaraldehídos)
CROMATOGRAFÍA DE AMINOÁCIDOS
 CROMATOGRAFÍA DE AMINOÁCIDOS Electroforesis.- Es un método de laboratorio en el que se utiliza una corriente eléctrica controlada con la finalidad de separar aminoácidos (y otras biomoléculas) según su
CROMATOGRAFÍA DE AMINOÁCIDOS Electroforesis.- Es un método de laboratorio en el que se utiliza una corriente eléctrica controlada con la finalidad de separar aminoácidos (y otras biomoléculas) según su
Capítulo 10. Efectos de superficie. Sistema respiratorio
 Capítulo 10 Efectos de superficie. Sistema respiratorio 1 Tensión superficial El coeficiente de tensión superficial γ es la fuerza por unidad de longitud que hay que realizar para aumentar una superficie:
Capítulo 10 Efectos de superficie. Sistema respiratorio 1 Tensión superficial El coeficiente de tensión superficial γ es la fuerza por unidad de longitud que hay que realizar para aumentar una superficie:
Departamento de Química Física Facultad de Ciencias
 Interacciones electrostáticas. Interacciones electrostáticas. Los fenómenos de interacción con el disolvente y cosolventes. Interacciones electrostáticas. El origen de las cargas en proteínas. Fuentes
Interacciones electrostáticas. Interacciones electrostáticas. Los fenómenos de interacción con el disolvente y cosolventes. Interacciones electrostáticas. El origen de las cargas en proteínas. Fuentes
13. REACTOR CSTR. X r
 13. REACTOR CSTR 1. OBJETIVOS 1.1. Definir paquetes fluidos que incluyan reacciones de tipo cinético 1.2. Determinar los grados de libertad requeridos para simular un reactor CSTR de tipo cinético 1.3.
13. REACTOR CSTR 1. OBJETIVOS 1.1. Definir paquetes fluidos que incluyan reacciones de tipo cinético 1.2. Determinar los grados de libertad requeridos para simular un reactor CSTR de tipo cinético 1.3.
SEPARACIONES POR CROMATOGRAFÍA
 SEPARACIONES POR CROMATOGRAFÍA Conceptos generales. Clasificación de los métodos cromatográficos. Separación cromatográfica Esquema básico de un cromatógrafo Cromatografía líquida de alta resolución. HPLC.
SEPARACIONES POR CROMATOGRAFÍA Conceptos generales. Clasificación de los métodos cromatográficos. Separación cromatográfica Esquema básico de un cromatógrafo Cromatografía líquida de alta resolución. HPLC.
Procedimientos. de muestreo y preparación de la muestra
 Procedimientos de muestreo y preparación de la muestra Consulte nuestra página web: www.sintesis.com En ella encontrará el catálogo completo y comentado Procedimientos de muestreo y preparación de la muestra
Procedimientos de muestreo y preparación de la muestra Consulte nuestra página web: www.sintesis.com En ella encontrará el catálogo completo y comentado Procedimientos de muestreo y preparación de la muestra
Física para Ciencias: Principio de Arquímedes, Ecuaciones de Continuidad y Bernoulli.
 Física para Ciencias: Principio de Arquímedes, Ecuaciones de Continuidad y Bernoulli. Dictado por: Profesor Aldo Valcarce 1 er semestre 2014 Presión de un fluido Presión depende de la profundidad P = ρ
Física para Ciencias: Principio de Arquímedes, Ecuaciones de Continuidad y Bernoulli. Dictado por: Profesor Aldo Valcarce 1 er semestre 2014 Presión de un fluido Presión depende de la profundidad P = ρ
Biotecnología - Bioprocesos II. INTRODUCCION A LOS PROCESOS BIOTECNOLOGICOS Separación y purificación en Biotecnología ( Downstream processing )
 Biotecnología - Bioprocesos II INTRODUCCION A LOS PROCESOS BIOTECNOLOGICOS Separación y purificación en Biotecnología ( Downstream processing ) La comercialización de nuevos productos obtenidos a través
Biotecnología - Bioprocesos II INTRODUCCION A LOS PROCESOS BIOTECNOLOGICOS Separación y purificación en Biotecnología ( Downstream processing ) La comercialización de nuevos productos obtenidos a través
Bioquímica Tema 2: Soluciones. Unidades Año: 2013
 TEMA 2: SOLUCIONES Al estudio de las soluciones se le asigna gran importancia, teniendo en cuenta que la mayoría de las reacciones químicas ocurren entre soluciones, particularmente en medios acuosos.
TEMA 2: SOLUCIONES Al estudio de las soluciones se le asigna gran importancia, teniendo en cuenta que la mayoría de las reacciones químicas ocurren entre soluciones, particularmente en medios acuosos.
líquido sólido Interfase sólido-líquido
 INTERFASES La mayoría de los procesos fisicoquímicos naturales y artificiales ocurren en sistemas heterogéneos en donde las diferentes fases que las componen están separadas por una interfase, definida
INTERFASES La mayoría de los procesos fisicoquímicos naturales y artificiales ocurren en sistemas heterogéneos en donde las diferentes fases que las componen están separadas por una interfase, definida
CROMATOGRAFÍA. En la siguiente tabla se observan diferentes fases móviles y fases estacionarias en diferentes técnicas de cromatografía:
 CROMATOGRAFÍA La palabra cromatografía significa gráfica de colores y fue diseñada por Michael Tswett en el 1903. Tswett llevó a cabo una extracción de una mezcla de pigmentos de hojas verdes y luego pasó
CROMATOGRAFÍA La palabra cromatografía significa gráfica de colores y fue diseñada por Michael Tswett en el 1903. Tswett llevó a cabo una extracción de una mezcla de pigmentos de hojas verdes y luego pasó
SENSORES DE FLUJO. Transducers for Biomedical Measurements: Principles and Applications, R.S.C. Cobbold, Ed. John Wiley & Sons
 SENSORES DE FLUJO Referencias bibliográficas Transducers for Biomedical Measurements: Principles and Applications, R.S.C. Cobbold, Ed. John Wiley & Sons Sensores y acondicionamiento de señal, R. Pallás
SENSORES DE FLUJO Referencias bibliográficas Transducers for Biomedical Measurements: Principles and Applications, R.S.C. Cobbold, Ed. John Wiley & Sons Sensores y acondicionamiento de señal, R. Pallás
FÍSICA Y QUÍMICA 3º ESO. OBJETIVOS, CONTENIDOS Y CRITERIOS DE EVALUACIÓN 1ª Evaluación: Unidad 1. La medida y el método científico.
 FÍSICA Y QUÍMICA 3º ESO. OBJETIVOS, CONTENIDOS Y CRITERIOS DE EVALUACIÓN 1ª Evaluación: Unidad 1. La medida y el método científico. OBJETIVOS 1. Reconocer las etapas del trabajo científico y elaborar informes
FÍSICA Y QUÍMICA 3º ESO. OBJETIVOS, CONTENIDOS Y CRITERIOS DE EVALUACIÓN 1ª Evaluación: Unidad 1. La medida y el método científico. OBJETIVOS 1. Reconocer las etapas del trabajo científico y elaborar informes
UNIVERSIDAD SANTO TOMAS SECCIONAL BUCARAMANGA. División de Ingenierías - Facultad de Química Ambiental
 UNIVERSIDAD SANTO TOMAS SECCIONAL BUCARAMANGA División de Ingeniería Facultad de Química Ambiental Nombre de Asignatura: QUÍMICA INSTRUMENTAL II Àrea: Básicas de Química / Química Analítica Créditos: 4
UNIVERSIDAD SANTO TOMAS SECCIONAL BUCARAMANGA División de Ingeniería Facultad de Química Ambiental Nombre de Asignatura: QUÍMICA INSTRUMENTAL II Àrea: Básicas de Química / Química Analítica Créditos: 4
PROPIEDADES FISICOQUÍMICAS DE LOS ÁCIDOS NUCLEICOS. Es un ácido capaz de formar sales con iones cargados
 Extracción de ADN Genética molecular PROPIEDADES FISICOQUÍMICAS DE LOS ÁCIDOS NUCLEICOS Es un ácido capaz de formar sales con iones cargados positivamente (cationes). Es soluble en soluciones concentradas
Extracción de ADN Genética molecular PROPIEDADES FISICOQUÍMICAS DE LOS ÁCIDOS NUCLEICOS Es un ácido capaz de formar sales con iones cargados positivamente (cationes). Es soluble en soluciones concentradas
MECANISMOS DISIPATIVOS Y SUS FUERZAS IMPULSORAS
 MECANISMOS DISIPATIVOS Y SUS FUERZAS IMPULSORAS Temas de Biofísica Mario Parisi Bibliografía Capítulo 3: Los Grandes Mecanismos Disipativos y sus Fuerzas Impulsoras Gradiente Variación de una cierta cantidad
MECANISMOS DISIPATIVOS Y SUS FUERZAS IMPULSORAS Temas de Biofísica Mario Parisi Bibliografía Capítulo 3: Los Grandes Mecanismos Disipativos y sus Fuerzas Impulsoras Gradiente Variación de una cierta cantidad
Conceptos basicos del equilibrio de quimico en medio acuoso
 Conceptos basicos del equilibrio de quimico en medio acuoso Elaborado por: Gustavo Gomez Sosa Facultad de Quimica UNAM QU ÍM IC A A N A LÍTIC A I C LAV E 1402 G rupo 4, s em es tre 2010-2 CONCEPTOS BASICOS
Conceptos basicos del equilibrio de quimico en medio acuoso Elaborado por: Gustavo Gomez Sosa Facultad de Quimica UNAM QU ÍM IC A A N A LÍTIC A I C LAV E 1402 G rupo 4, s em es tre 2010-2 CONCEPTOS BASICOS
Intercambiadores de calor
 UNIVERSIDAD NACIONAL EXPERIMENTAL FRANCISCO DE MIRANDA AREA DE TECNOLOGÍA DEPARTAMENTO DE ENERGÉTICA UNIDAD CURRICULAR: TRANSFERENCIA DE CALOR Intercambiadores de calor Profesor: Ing. Isaac Hernández Isaachernandez89@gmail.com
UNIVERSIDAD NACIONAL EXPERIMENTAL FRANCISCO DE MIRANDA AREA DE TECNOLOGÍA DEPARTAMENTO DE ENERGÉTICA UNIDAD CURRICULAR: TRANSFERENCIA DE CALOR Intercambiadores de calor Profesor: Ing. Isaac Hernández Isaachernandez89@gmail.com
Dinámica de Fluidos. Mecánica y Fluidos VERANO
 Dinámica de Fluidos Mecánica y Fluidos VERANO 1 Temas Tipos de Movimiento Ecuación de Continuidad Ecuación de Bernouilli Circulación de Fluidos Viscosos 2 TIPOS DE MOVIMIENTO Régimen Laminar: El flujo
Dinámica de Fluidos Mecánica y Fluidos VERANO 1 Temas Tipos de Movimiento Ecuación de Continuidad Ecuación de Bernouilli Circulación de Fluidos Viscosos 2 TIPOS DE MOVIMIENTO Régimen Laminar: El flujo
UNIDADES DE ESTUDIO Y SUS CONTENIDOS Unidad 1: PROPIEDADES DE LOS FLUIDOS PUROS.
 1. DATOS INFORMATIVOS ASIGNATURA: QUÌMICA-FÌSICA DEPARTAMENTO: CIENCIAS EXACTAS ELEMENTO DE COMPETENCIA: CÓDIGO: EXCT-22318 CARRERAS: PETROQUÌMICA NRC 4548 NIVEL: QUINTO ÁREA DEL CONOCIMIENTO: QUÌMICA
1. DATOS INFORMATIVOS ASIGNATURA: QUÌMICA-FÌSICA DEPARTAMENTO: CIENCIAS EXACTAS ELEMENTO DE COMPETENCIA: CÓDIGO: EXCT-22318 CARRERAS: PETROQUÌMICA NRC 4548 NIVEL: QUINTO ÁREA DEL CONOCIMIENTO: QUÌMICA
Modelado de Disolvente
 Seminario Fuerzas Intermoleculares Modelado de Disolvente Presentado por: David Ignacio Ramírez Palma Instituto de Química, Universidad Nacional Autónoma de México Noviembre 2014. 1 Contenido - Concepto
Seminario Fuerzas Intermoleculares Modelado de Disolvente Presentado por: David Ignacio Ramírez Palma Instituto de Química, Universidad Nacional Autónoma de México Noviembre 2014. 1 Contenido - Concepto
CENTRIFUGACIÓN. Fundamentos. Teoría de la centrifugación
 CENTRIFUGACIÓN Fundamentos. Teoría de la centrifugación Fuerzas intervinientes Tipos de centrífugas Tubular De discos Filtración centrífuga 1 SEDIMENTACIÓN Se basa en la diferencia de densidades entre
CENTRIFUGACIÓN Fundamentos. Teoría de la centrifugación Fuerzas intervinientes Tipos de centrífugas Tubular De discos Filtración centrífuga 1 SEDIMENTACIÓN Se basa en la diferencia de densidades entre
CINÉTICA QUÍMICA. Química General e Inorgánica Licenciatura en Ciencias Biológicas Profesorado en Biología Analista Biológico
 Química General e Inorgánica Licenciatura en Ciencias Biológicas Profesorado en Biología Analista Biológico CINÉTICA QUÍMICA La cinética química estudia la variación de la concentración de reactantes o
Química General e Inorgánica Licenciatura en Ciencias Biológicas Profesorado en Biología Analista Biológico CINÉTICA QUÍMICA La cinética química estudia la variación de la concentración de reactantes o
LA MATERIA: ESTADOS DE AGREGACIÓN
 LA MATERIA: ESTADOS DE AGREGACIÓN 1. PROPIEDADES DE LA MATERIA Materia: es todo aquello que existe, tiene masa y ocupa un volumen, los distintos tipos de materia se llaman sustancias. El sistema material
LA MATERIA: ESTADOS DE AGREGACIÓN 1. PROPIEDADES DE LA MATERIA Materia: es todo aquello que existe, tiene masa y ocupa un volumen, los distintos tipos de materia se llaman sustancias. El sistema material
Electroforesis de proteínas en geles de poliacrilamida
 Electroforesis de proteínas en geles de poliacrilamida Electroforesis de proteínas en geles de poliacrilamida: Introducción y técnica básica La electroforesis de proteínas en geles con una matriz de poliacrilamida,
Electroforesis de proteínas en geles de poliacrilamida Electroforesis de proteínas en geles de poliacrilamida: Introducción y técnica básica La electroforesis de proteínas en geles con una matriz de poliacrilamida,
LA MATERIA 1. Teoría atómica de Dalton. 2. La materia. 3. Leyes químicas. 4. El mol. 5. Leyes de los gases ideales. 6. Símbolos y fórmulas.
 LA MATERIA 1. Teoría atómica de Dalton. 2. La materia. 3. Leyes químicas. 4. El mol. 5. Leyes de los gases ideales. 6. Símbolos y fórmulas. Química 1º bachillerato La materia 1 1. TEORÍA ATÓMICA DE DALTON
LA MATERIA 1. Teoría atómica de Dalton. 2. La materia. 3. Leyes químicas. 4. El mol. 5. Leyes de los gases ideales. 6. Símbolos y fórmulas. Química 1º bachillerato La materia 1 1. TEORÍA ATÓMICA DE DALTON
Tema 12 Termoquímica. Desprende o absorbe calor? Cuánto calor? Criterio de espontaneidad En qué dirección se produce? Reacciones Químicas
 Tema 1 Estequiometría Cuánto se produce? Cuánto reacciona? Tema 15 Equilibrio Cuándo se alcanza? Cómo modificarlo? Tema 12 Termoquímica Desprende o absorbe calor? Cuánto calor? Criterio de espontaneidad
Tema 1 Estequiometría Cuánto se produce? Cuánto reacciona? Tema 15 Equilibrio Cuándo se alcanza? Cómo modificarlo? Tema 12 Termoquímica Desprende o absorbe calor? Cuánto calor? Criterio de espontaneidad
TEMA II.5. Viscosidad. Dr. Juan Pablo Torres-Papaqui. Departamento de Astronomía Universidad de Guanajuato DA-UG (México)
 TEMA II.5 Viscosidad Dr. Juan Pablo Torres-Papaqui Departamento de Astronomía Universidad de Guanajuato DA-UG (México) papaqui@astro.ugto.mx División de Ciencias Naturales y Exactas, Campus Guanajuato,
TEMA II.5 Viscosidad Dr. Juan Pablo Torres-Papaqui Departamento de Astronomía Universidad de Guanajuato DA-UG (México) papaqui@astro.ugto.mx División de Ciencias Naturales y Exactas, Campus Guanajuato,
Una mezcla es un compuesto formado por varias sustancias con distintas propiedades
 COMPOSICIÓN DE LA MATERIA Mezclas homogéneas y heterogéneas Una mezcla es un compuesto formado por varias sustancias con distintas propiedades Algunos sistemas materiales como la leche a simple vista parecen
COMPOSICIÓN DE LA MATERIA Mezclas homogéneas y heterogéneas Una mezcla es un compuesto formado por varias sustancias con distintas propiedades Algunos sistemas materiales como la leche a simple vista parecen
MATERIA: ES TODO LO QUE TIENE MASA Y VOLUMEN.
 MATERIA: ES TODO LO QUE TIENE MASA Y VOLUMEN. CLASIFICACIÓN DE LA MATERIA: SEGÚN: A. ESTADO DE AGREGACIÓN. B. COMPOSICIÓN. A. ESTADO DE AGREGACIÓN. SE REFIERE A LA FORMA DE INTERACCIÓN ENTRE LAS MOLÉCULAS
MATERIA: ES TODO LO QUE TIENE MASA Y VOLUMEN. CLASIFICACIÓN DE LA MATERIA: SEGÚN: A. ESTADO DE AGREGACIÓN. B. COMPOSICIÓN. A. ESTADO DE AGREGACIÓN. SE REFIERE A LA FORMA DE INTERACCIÓN ENTRE LAS MOLÉCULAS
Modelación de la absorción de metales pesados y lixiviación en presencia de ligandos orgánicos en la zona radicular
 Modelación de la absorción de metales pesados y lixiviación en presencia de ligandos orgánicos en la zona radicular Root-zone modeling of heavy metal uptake and leaching in the presence of organic ligands
Modelación de la absorción de metales pesados y lixiviación en presencia de ligandos orgánicos en la zona radicular Root-zone modeling of heavy metal uptake and leaching in the presence of organic ligands
TEMA 4 (Parte I) Ley de Darcy. Flujos hidráulicos a través de terrenos.
 TEMA 4 (Parte I) Ley de Darcy. Flujos hidráulicos a través de terrenos. 4.1. Introducción DEFINICIÓN DE SUELO: geólogo, ingeniero agrónomo, arquitecto. Delgada capa sobre la corteza terrestre de material
TEMA 4 (Parte I) Ley de Darcy. Flujos hidráulicos a través de terrenos. 4.1. Introducción DEFINICIÓN DE SUELO: geólogo, ingeniero agrónomo, arquitecto. Delgada capa sobre la corteza terrestre de material
Tema 4. Fuerzas intermoleculares
 Tema 4: Fuerzas intermoleculares Química para biólogos Slide 1 of 35 Contenidos 4-1 Electronegatividad 4-2 Polaridad de enlace y molécula: momento dipolar 4-3 Fuerzas intermoleclares 4-4 Puentes de hidrógeno
Tema 4: Fuerzas intermoleculares Química para biólogos Slide 1 of 35 Contenidos 4-1 Electronegatividad 4-2 Polaridad de enlace y molécula: momento dipolar 4-3 Fuerzas intermoleclares 4-4 Puentes de hidrógeno
La Química Analítica nos permite medir, monitorear o caracterizar una, varias especies o procesos químicos para la resolución de diversos problemas:
 QUÍMICA ANALÍTICA I Documento de apoyo (1) : Formación de soluciones analíticas. Dr. Alejandro Baeza. Semestre 2010-II. Antecedentes La Química Analítica nos permite medir, monitorear o caracterizar una,
QUÍMICA ANALÍTICA I Documento de apoyo (1) : Formación de soluciones analíticas. Dr. Alejandro Baeza. Semestre 2010-II. Antecedentes La Química Analítica nos permite medir, monitorear o caracterizar una,
FISICOQUIMICA. La energía total de un sistema puede ser: externa, interna o de tránsito. CLASIFICACION TIPOS DETERMINACION Energía Potencial:
 FISICOQUIMICA ENERGIA: No puede definirse de forma precisa y general, sin embargo, puede decirse que es la capacidad para realizar trabajo. No se puede determinar de manera absoluta, solo evaluar los cambios.
FISICOQUIMICA ENERGIA: No puede definirse de forma precisa y general, sin embargo, puede decirse que es la capacidad para realizar trabajo. No se puede determinar de manera absoluta, solo evaluar los cambios.
CROMATOGRAFIA DE GASES
 CROMATOGRAFIA DE GASES Prof. Jorge Mendoza C. Dpto. Química Inorgánica y Analítica Definición: La cromatografía es un método de separación física en la cual los componentes aser separados son distribuidos
CROMATOGRAFIA DE GASES Prof. Jorge Mendoza C. Dpto. Química Inorgánica y Analítica Definición: La cromatografía es un método de separación física en la cual los componentes aser separados son distribuidos
A continuación se detallan cada una de las propiedades coligativas:
 PREGUNTA (Técnico Profesional) Se prepara una solución con 2 mol de agua y 0,5 mol de un electrolito no volátil. Al respecto, cuál es la presión de vapor a 25 ºC de esta solución, si la presión del agua
PREGUNTA (Técnico Profesional) Se prepara una solución con 2 mol de agua y 0,5 mol de un electrolito no volátil. Al respecto, cuál es la presión de vapor a 25 ºC de esta solución, si la presión del agua
CAPÍTULO 5. CONCLUSIONES
 CAPÍTULO 5. CONCLUSIONES Este trabajo ha tenido como objetivos el análisis y modelado del proceso de purificación de estireno mediante adsorción en alúmina y el análisis del cambio de escala del sistema,
CAPÍTULO 5. CONCLUSIONES Este trabajo ha tenido como objetivos el análisis y modelado del proceso de purificación de estireno mediante adsorción en alúmina y el análisis del cambio de escala del sistema,
MÓDULO: CONTAMINACIÓN DE LAS AGUAS TEMA: FILTRACIÓN
 MÓDULO: CONTAMINACIÓN DE LAS AGUAS TEMA: FILTRACIÓN DOCUMENTACIÓN ELABORADA POR: NIEVES CIFUENTES MASTE EN INGENIERÍA MEDIOAMBIENTAL Y GESTION DEL AGUA C. DE LAS AGUAS ÍNDICE 1. INTRODUCCIÓN... 1 2. FILTROS
MÓDULO: CONTAMINACIÓN DE LAS AGUAS TEMA: FILTRACIÓN DOCUMENTACIÓN ELABORADA POR: NIEVES CIFUENTES MASTE EN INGENIERÍA MEDIOAMBIENTAL Y GESTION DEL AGUA C. DE LAS AGUAS ÍNDICE 1. INTRODUCCIÓN... 1 2. FILTROS
Equilibrio Químico. CI4102 Ingeniería Ambiental Profesor Marcelo Olivares A.
 Equilibrio Químico CI4102 Ingeniería Ambiental Profesor Marcelo Olivares A. Introducción Las reacciones químicas que se ha considerado hasta este punto se denominan irreversibles debido a que ellas proceden
Equilibrio Químico CI4102 Ingeniería Ambiental Profesor Marcelo Olivares A. Introducción Las reacciones químicas que se ha considerado hasta este punto se denominan irreversibles debido a que ellas proceden
1 Dr. Rogelio Cuevas García. En las reacciones homogéneas lo usual es que la expresión de A A B
 1 En las reacciones homogéneas lo usual es que la expresión de velocidad de reacción sea una simple ley de potencia; esto es n ( R ) k m A A in embargo, existen diversas reacciones cuyo comportamiento
1 En las reacciones homogéneas lo usual es que la expresión de velocidad de reacción sea una simple ley de potencia; esto es n ( R ) k m A A in embargo, existen diversas reacciones cuyo comportamiento
T 1 T 2. x L. Con frecuencia es importante el valor de la resistencia térmica multiplicado por el área de flujo de calor, en este caso sera
 1. ey de Fourier ué flujo de calor es necesario hacer pasar a través de una barra circular de madera de 5 cm de diámetro y 10 cm de longitud, cuya temperatura en los extremos es de 50 C y 10 C en sus extremos?
1. ey de Fourier ué flujo de calor es necesario hacer pasar a través de una barra circular de madera de 5 cm de diámetro y 10 cm de longitud, cuya temperatura en los extremos es de 50 C y 10 C en sus extremos?
CINÉTICA QUÍMICA. Dr. Hugo Cerecetto. Prof. Titular de Química
 CINÉTICA QUÍMICA Dr. Hugo Cerecetto Prof. Titular de Química Temario 2) La reacción química: - Nociones de Termoquímica y Termodinámica. Conceptos de entalpía y entropía de reacción. Energía libre. Espontaneidad
CINÉTICA QUÍMICA Dr. Hugo Cerecetto Prof. Titular de Química Temario 2) La reacción química: - Nociones de Termoquímica y Termodinámica. Conceptos de entalpía y entropía de reacción. Energía libre. Espontaneidad
Estados de la materia y cambios de fase
 3 Año de Química: Sistemas Materiales Prof. Javier Ponce Qué es Ciencia? Ciencia (en latíns cientia, de scire, conocer ), término que en su sentido más amplio se emplea para referirse al conocimiento sistematizado
3 Año de Química: Sistemas Materiales Prof. Javier Ponce Qué es Ciencia? Ciencia (en latíns cientia, de scire, conocer ), término que en su sentido más amplio se emplea para referirse al conocimiento sistematizado
Sustancia que tiene una composición química fija. Una sustancia pura no tiene que ser de un solo elemento, puede ser mezcla homogénea.
 Sustancia que tiene una composición química fija. Una sustancia pura no tiene que ser de un solo elemento, puede ser mezcla homogénea. Mezcla de aceite y agua Mezcla de hielo y agua Las sustancias existen
Sustancia que tiene una composición química fija. Una sustancia pura no tiene que ser de un solo elemento, puede ser mezcla homogénea. Mezcla de aceite y agua Mezcla de hielo y agua Las sustancias existen
GUÍA DE DISCUSIÓN DE PROBLEMAS 4 TEMA DIFUSIÓN EN MATERIALES DE INGENIERÍA
 UNIVERSIDAD DON BOSCO FACULTAD DE INGENIERÍA ESCUELA DE INGENIERÍA MECÁNICA Asignatura: "Ciencia de los Materiales" I- SECCION DE PREGUNTAS: GUÍA DE DISCUSIÓN DE PROBLEMAS 4 TEMA DIFUSIÓN EN MATERIALES
UNIVERSIDAD DON BOSCO FACULTAD DE INGENIERÍA ESCUELA DE INGENIERÍA MECÁNICA Asignatura: "Ciencia de los Materiales" I- SECCION DE PREGUNTAS: GUÍA DE DISCUSIÓN DE PROBLEMAS 4 TEMA DIFUSIÓN EN MATERIALES
Concepto de difusión. Leyes de Fick
 Difusión en Química Concepto de difusión. Leyes de Fick Concepto de difusión. Leyes de Fick fuerza impulsora sólo existe cambio en una coordenada Difusión. Primera ley de Fick Flujo de soluto, J, se define
Difusión en Química Concepto de difusión. Leyes de Fick Concepto de difusión. Leyes de Fick fuerza impulsora sólo existe cambio en una coordenada Difusión. Primera ley de Fick Flujo de soluto, J, se define
Tema 2: Tratamiento de muestras y técnicas de separación de analitos. Tratamiento de muestras (algunas directrices) ecosistema ( contaminado?
 Tema 2: Tratamiento de s y técnicas de separación de analitos. Tratamiento de s (algunas directrices) ecosistema ( contaminado?) toma y preparación, técnica analítica 1) Toma de una representativa: réplica
Tema 2: Tratamiento de s y técnicas de separación de analitos. Tratamiento de s (algunas directrices) ecosistema ( contaminado?) toma y preparación, técnica analítica 1) Toma de una representativa: réplica
Tema 1. Introducción a las separaciones analíticas
 Tema 1 Introducción a las separaciones analíticas Problemas analíticos: matrices complejas Pocos métodos específicos Necesidad de separaciones Ejemplo: Digitoxina nivel tóxico 25 ng/ml de sangre Equivale
Tema 1 Introducción a las separaciones analíticas Problemas analíticos: matrices complejas Pocos métodos específicos Necesidad de separaciones Ejemplo: Digitoxina nivel tóxico 25 ng/ml de sangre Equivale
1. MATERIA Y SU ASPECTO
 1. MATERIA Y SU ASPECTO El aspecto de un sistema material puede variar según el método de observación. Algunos sistemas materiales como la leche, la sangre o la mantequilla a simple vista parecen uniformes,
1. MATERIA Y SU ASPECTO El aspecto de un sistema material puede variar según el método de observación. Algunos sistemas materiales como la leche, la sangre o la mantequilla a simple vista parecen uniformes,
Equilibrio físico. Prof. Jesús Hernández Trujillo. Facultad de Química, UNAM. Equilibrio físico/j. Hdez. T p.
 Equilibrio físico/j. Hdez. T p. 1/34 Equilibrio físico Prof. Jesús Hernández Trujillo jesus.hernandezt@gmail.com Facultad de Química, UNAM Equilibrio físico/j. Hdez. T p. 2/34 Interacciones intermoleculares
Equilibrio físico/j. Hdez. T p. 1/34 Equilibrio físico Prof. Jesús Hernández Trujillo jesus.hernandezt@gmail.com Facultad de Química, UNAM Equilibrio físico/j. Hdez. T p. 2/34 Interacciones intermoleculares
REGIMENES DE CORRIENTES O FLUJOS
 LINEAS DE CORRIENTE Ø Las líneas de corriente son líneas imaginarias dibujadas a través de un fluido en movimiento y que indican la dirección de éste en los diversos puntos del flujo de fluidos. Ø Una
LINEAS DE CORRIENTE Ø Las líneas de corriente son líneas imaginarias dibujadas a través de un fluido en movimiento y que indican la dirección de éste en los diversos puntos del flujo de fluidos. Ø Una
IV UNIDAD TRANSFERENCIA DE MASA
 IV UNIDAD TRANSFERENCIA DE MASA La transferencia de masa es la tendencia de uno o más componentes de una mezcla a transportarse desde una zona de alta concentración del o de los componentes a otra zona
IV UNIDAD TRANSFERENCIA DE MASA La transferencia de masa es la tendencia de uno o más componentes de una mezcla a transportarse desde una zona de alta concentración del o de los componentes a otra zona
BLOQUE 1: ASPECTOS CUANTATIVOS DE LA QUÍMICA
 BLOQUE 1: ASPECTOS CUANTATIVOS DE LA QUÍMICA Unidad 2: Los gases ideales Teresa Esparza araña 1 Índice 1. Los estados de agregación de la materia a. Los estados de la materia b. Explicación según la teoría
BLOQUE 1: ASPECTOS CUANTATIVOS DE LA QUÍMICA Unidad 2: Los gases ideales Teresa Esparza araña 1 Índice 1. Los estados de agregación de la materia a. Los estados de la materia b. Explicación según la teoría
LABORATORIO N 6 AGITACION Y MEZCLADO DE LIQUIDOS
 UNIVERSIDAD NACIONAL DEL CENTRO DEL PERÚ FACAP EAP DE INGENIERIA AGROINDUSTRIAL CURSO: OPERACIONES UNITARIAS II CATEDRATICO: ING. MIGUEL ANGEL QUISPE SOLANO LABORATORIO N 6 AGITACION Y MEZCLADO DE LIQUIDOS
UNIVERSIDAD NACIONAL DEL CENTRO DEL PERÚ FACAP EAP DE INGENIERIA AGROINDUSTRIAL CURSO: OPERACIONES UNITARIAS II CATEDRATICO: ING. MIGUEL ANGEL QUISPE SOLANO LABORATORIO N 6 AGITACION Y MEZCLADO DE LIQUIDOS
GUIA DE EJERCICIOS II. (Primera Ley Segunda Ley - Ciclo de Carnot)
 UNIVERSIDAD PEDRO DE VALDIVIA TERMODINAMICA. GUIA DE EJERCICIOS II. (Primera Ley Segunda Ley - Ciclo de Carnot) 1. Deducir qué forma adopta la primera ley de la termodinámica aplicada a un gas ideal para
UNIVERSIDAD PEDRO DE VALDIVIA TERMODINAMICA. GUIA DE EJERCICIOS II. (Primera Ley Segunda Ley - Ciclo de Carnot) 1. Deducir qué forma adopta la primera ley de la termodinámica aplicada a un gas ideal para
Picnómetro: Medidas de Densidad.
 1 TEMA 7: POROSIDAD Y ÁREA SUPERFICIAL 1.- Clasificación de los poros de acuerdo a su tamaño Los materiales porosos se clasifican como microporosos con un tamaño de poro de 0.3-2 nm, mesoporosos de 2-50
1 TEMA 7: POROSIDAD Y ÁREA SUPERFICIAL 1.- Clasificación de los poros de acuerdo a su tamaño Los materiales porosos se clasifican como microporosos con un tamaño de poro de 0.3-2 nm, mesoporosos de 2-50
Proceso de Difusión para el Dopado de Silicio en la Fabricación de Circuitos Integrados
 Proceso de Difusión para el Dopado de Silicio en la Fabricación de Circuitos Integrados Oscar Sosa, Cód.:261826, Ferney Molina, Cód.:261786, y Carlos Barreto, Cód.:261856 (oasosap, fsmolinas, carabarretonei)
Proceso de Difusión para el Dopado de Silicio en la Fabricación de Circuitos Integrados Oscar Sosa, Cód.:261826, Ferney Molina, Cód.:261786, y Carlos Barreto, Cód.:261856 (oasosap, fsmolinas, carabarretonei)
LOS GASES Y LAS DISOLUCIONES. Departamento de Física y Química 3º ESO
 LOS GASES Y LAS DISOLUCIONES Departamento de Física y Química 3º ESO 0. Mapa conceptual SÓLIDO ESTADOS DE LA MATERIA LÍQUIDO Presión atmosférica GAS Solubilidad Disolución saturada Disoluciones Soluto
LOS GASES Y LAS DISOLUCIONES Departamento de Física y Química 3º ESO 0. Mapa conceptual SÓLIDO ESTADOS DE LA MATERIA LÍQUIDO Presión atmosférica GAS Solubilidad Disolución saturada Disoluciones Soluto
GUIA DE PROBLEMAS. Velocidad de aproximación al equilibrio = kr(c-ceq)
 GUIA DE PROBLEMAS 1. La conversión de hidrógeno molecular de la forma orto a la forma para es catalizada por NiO. Se dipone de un catalizador soportado con un área específica de 305 m 2 /g y un volumen
GUIA DE PROBLEMAS 1. La conversión de hidrógeno molecular de la forma orto a la forma para es catalizada por NiO. Se dipone de un catalizador soportado con un área específica de 305 m 2 /g y un volumen
CLASIFICACIÓN DE LA MATERIA
 1. Clasificación de la materia por su aspecto CLASIFICACIÓN DE LA MATERIA La materia homogénea es la que presenta un aspecto uniforme, en la cual no se pueden distinguir a simple vista sus componentes.
1. Clasificación de la materia por su aspecto CLASIFICACIÓN DE LA MATERIA La materia homogénea es la que presenta un aspecto uniforme, en la cual no se pueden distinguir a simple vista sus componentes.
ESTUDIO DEL PROCESO DE TRANSFERENCIA MASA EN MEMBRANAS LÍQUIDAS SOPORTADAS
 ESTUDIO DEL PROCESO DE TRANSFERENCIA MASA EN MEMBRANAS LÍQUIDAS SOPORTADAS Mario Avila-Rodríguez Diana Fabiola Cholico González María del Pilar González Muñoz Mireya Edith Martínez Pérez José Antonio Reyes
ESTUDIO DEL PROCESO DE TRANSFERENCIA MASA EN MEMBRANAS LÍQUIDAS SOPORTADAS Mario Avila-Rodríguez Diana Fabiola Cholico González María del Pilar González Muñoz Mireya Edith Martínez Pérez José Antonio Reyes
Unidad 16: Temperatura y gases ideales
 Apoyo para la preparación de los estudios de Ingeniería y Arquitectura Física (Preparación a la Universidad) Unidad 16: Temperatura y gases ideales Universidad Politécnica de Madrid 14 de abril de 2010
Apoyo para la preparación de los estudios de Ingeniería y Arquitectura Física (Preparación a la Universidad) Unidad 16: Temperatura y gases ideales Universidad Politécnica de Madrid 14 de abril de 2010
SUSTANCIA QUÍMICA mercurio oxígeno
 ELEMENTO O SUSTANCIA ELEMENTAL: Sustancia formada por un mismo tipo de átomos, por ejemplo: Hg, H 2, Cu, O 2 SUSTANCIA QUÍMICA mercurio oxígeno COMPUESTO O SUSTANCIA COMPUESTA: Sustancia formada por dos
ELEMENTO O SUSTANCIA ELEMENTAL: Sustancia formada por un mismo tipo de átomos, por ejemplo: Hg, H 2, Cu, O 2 SUSTANCIA QUÍMICA mercurio oxígeno COMPUESTO O SUSTANCIA COMPUESTA: Sustancia formada por dos
Diseño de Reactores Heterogéneos Catalíticos Reactores de Lecho Fijo
 Diseño de Reactores Heterogéneos Catalíticos Reactores de Lecho Fio En un reactor catalítico de lecho fio para llevar a cabo una reacción fluido-sólido, el catalizador se presenta coo un lecho de partículas
Diseño de Reactores Heterogéneos Catalíticos Reactores de Lecho Fio En un reactor catalítico de lecho fio para llevar a cabo una reacción fluido-sólido, el catalizador se presenta coo un lecho de partículas
Prefacio... ix COMO UTILIZAR ESTE LIBRO... 1 QUE ES LA QUIMICA... 2 EL METODO CIENTIFICO... 3 LAS RAMAS DE LA QUIMICA... 3
 ÍNDICE Prefacio... ix 1 introducción a la química... 1 COMO UTILIZAR ESTE LIBRO... 1 QUE ES LA QUIMICA... 2 EL METODO CIENTIFICO... 3 LAS RAMAS DE LA QUIMICA... 3 2 el sistema métrico y la medición científica...
ÍNDICE Prefacio... ix 1 introducción a la química... 1 COMO UTILIZAR ESTE LIBRO... 1 QUE ES LA QUIMICA... 2 EL METODO CIENTIFICO... 3 LAS RAMAS DE LA QUIMICA... 3 2 el sistema métrico y la medición científica...
