Trastornos del equilibrio ácido-base
|
|
|
- Felipe Carrasco Ferreyra
- hace 7 años
- Vistas:
Transcripción
1 NOTA DELS COMISSIONARIS: hi ha aclaracions i correccions importants al document Fe d errades, és important que us el mireu de cara a l examen!! Trastornos del equilibrio ácidobase INTRODUCCIÓN CONCEPTOS BÁSICOS Ácido: sustancia capaz de ceder hidrogeniones. Base: sustancia captar de captar hidrogeniones. ph : logaritmo negativo de la concentración de hidrogeniones en una solución. [H + ] Liq extracel lular = 40 nmol/l ph= log [H + ] El ph sanguíneo ( ) debe estar dentro de unos márgenes estrechos, pues determina la cinética enzimática y con ello el metabolismo celular, de tal forma que desviaciones de este parámetro pueden producir alteraciones importantes en el funcionamiento celular y por ende del funcionamiento del organismo. Entre es el margen fuera del cual nos encontramos en una situación incompatible con la vida. Existen tres grandes sistemas de regulación del ph: Sistema tampón intracelular o extracelular: permiten una respuesta rápida para corregir los trastornos de este equilibrio. Compensación respiratoria: modificando la respiración; hiperventilando eliminamos CO 2 y perdemos carga ácida. Compensación renal: los niveles de excreción renal de ácido y reabsorción de bicarbonato permiten mantener el ph dentro de los márgenes adecuados. El primer mecanismo de corrección es el sistema de tampones, seguido de la respiración y, por último, de la función renal, que tiene una acción más tardía. La situación ideal de tamponamiento es aquella en la que tenemos en una solución un ácido y una base en estado de equilibrio, pues ello nos permite corregir mejor los desequilibrios en los dos sentidos de la ecuación. Esto ocurre cuando el pka del tampón utilizado es igual al ph de la solución a tamponar. AH A + H + [H + ]= Ke x [AH] / [A ] Ke=cte de equilibrio, la mitad de las moléculas se encuentran disociadas en [AH] i [A ] log[h + ]= logke + log[ah] / [A ] ph= pk + log [A ] / [AH] Cuando ph= pk, el log [A ] = [AH], la mitad de AH está disociada y la otra mitad no, situación ideal para poder hacer frente a cualquier exceso o defecto de H+. 505
2 TIPOS DE ÁCIDOS Ácidos volátiles: son aquellos que al combinarse con bicarbonato llevan a la producción de CO 2 que, cuando está en exceso, se elimina por la respiración. Es decir, los eliminables por aire. HCO 3 + H + H 2 CO 3 CO 2 + H 2 O (pulmones) Ácidos no volátiles: ácidos que siempre están en solución (ácido sulfúrico, fosfórico, clorhídrico, láctico, cetoácidos procedentes del catabolismo de los AA, ácidos nucleicos, fosfolípidos) y que no suelen circular como ácidos ya que son amortiguados por iones HCO 3 dando lugar a la formación de CO 2, una sal y H 2 O HCl + NaHCO 3 NaCl + CO 2 + H 2 O EXCRECIÓN DE ÁCIDO: Como consecuencia del metabolismo del organismo, generamos una carga ácida de forma constante, que también se elimina de forma constante pero lenta. La excreción de H + es de 1mEq/kg/día, por lo que hay que tener en cuenta que cuanto más peso, más metabolismo basal, más carga ácida y mayor eliminación de H +. Los ácidos los introducimos en el organismo por medio de la dieta y por medio del metabolismo que genera ácido láctico o cetoácidos. Estos ácidos a nivel intracelular y extracelular serán compensados por medio de los diferentes sistemas tampón y el exceso se eliminará por vía pulmonar o renal. El tampón más importante a nivel extracelular es el bicarbonato: H + + HCO3 H 2 CO 3 CO 2 + H 2 O Este se combina con los hidrogeniones para dar lugar a la producción de H 2 O y CO 2, que será eliminado del organismo por medio de la respiración. Ecuación HendersonHasselbach La ecuación HendersonHasselbach permite conocer las concentraciones de bicarbonato en sangre a partir de datos que podemos obtener directamente de una analítica, como el ph y la pco 2. Es importante! ph = log TAMPONAMIENTO INTRACELULAR Los tampones intracelulares asumen el 60% de una carga ácida en minutos o pocas horas. Los fundamentales son las proteínas y el fosfato (H 2 PO 4 /HPO 4 2 ). También encontramos otros como la histidina (anillo imidazólico), HCO 3 /CO 2. Hay dos tipos celulares que tienen un sistema particular: los hematíes, que utilizan la hemoglobina como tampón, y las células óseas, que utilizan el CaCO 3. Existe una comunicación a través de la célula, de tal forma que cuando hay acidosis, uno de los mecanismos que permite la acción del tampón es el paso de los hidrogeniones del medio extracelular al medio intracelular. Este supone una expulsión al medio extracelular de iones K +. Así pues, la entrada de H + supone salida de K +, y la salida de H + supone la entrada de K + : es por ello que la acidosis se asocia a hiperpotasemina y la alcalosis se asocia a hipopotasemia (se cumple casi siempre y es importante acordarse!!!). 506
3 Carbonato cálcico: Con este tampón el hueso se desmineraliza, pues su acción supone una pérdida de calcio. Es importante en situación de acidosis crónica, pues interfiere en el desarrollo óseo normal al existir una desmineralización progresiva que lleva a una situación de hipercalciuria asociada frecuentemente a litiasis y nefrocalcinosis. CaCO 3 + 2H + HCO 3 + H + + Ca 2+ CO 2 + H Ca 2+ Tampón Hemoglobina: sistema tampón intracelular relacionado con la función pulmonar. La hemoglobina en el interior del hematíe se encuentra tamponando los ácidos producidos a nivel intracelular como consecuencia del metabolismo anaerobio. Cuando el hematíe a nivel pulmonar capta O 2, la Hb se combina con éste y libera los hidrogeniones, que pasarán a ser tamponados por medio del tampón bicarbonato intracelular, que vía anhidrasa carbónica llevará a la producción de CO 2 que saldrá de la célula y será eliminado por medio de la respiración. PAPEL DEL PULMÓN El organismo tiene la capacidad de captar la concentración de H + gracias a los quimiorreceptores bulbares (LCR) y los que encontramos a nivel del cuerpo carotídeo. Cuando la concentración de H + es elevada, este lleva a la estimulación del centro respiratorio, lo que induce la hiperventilación, eliminación de CO 2 y consecuente disminución de la carga ácida. Para este proceso está a nivel de los hematíes la anhidrasa carbónica. Papel del riñón 1. Reabsorción del HCO 3 : el riñón reabsorbe casi todo lo que filtra, el HCO 3 se reabsorbe sobre todo para evitar la acidosis. 2. Excreción de hidrogeniones. Reabsorción de bicarbonato La reabsorción de HCO 3 en condiciones normales es total: se produce un 90% por el TCP y un 10% en el TCD, dando lugar a una bicarbonaturia negativa. La reabsorción del HCO 3 se produce gracias a la anhidrasa carbónica. El HCO 3 a nivel de la luz tubular renal se combina con los H + excretados, dando lugar por medio de su disociación a CO 2 y agua. Este CO 2 difundirá a nivel de las células tubulares renales y por acción de la anhidrasa carbónica volverá a formar HCO 3 que pasará a sangre e H + que volverán a ser excretados a nivel renal. 507
4 Tamponamiento urinario 1. Sistema amonio A nivel renal, tanto en la célula tubular renal como en la luz tubular, el amoníaco se combina con protones para dar lugar a ión amonio que permitirá mantener un ph adecuado en orina y evitará la posible reabsorción de hidrogeniones. 2. Acidez titulable Sistema de sales (fosfato, nitrato, sulfato) que se combinan con los hidrogeniones excretados y permiten neutralizar el ph. Aldosterona La aldosterona regula la volemia, favorece la reabsorción de sodio a nivel del túbulo distal a costa de excreción de potasio e hidrogeniones. En las células tubulares principales tendrá lugar el intercambio de Na + por K +, mientras que a nivel de las células intercaladas tipo A, se producirá un intercambio de Na + por H +, los cuales, al ser excretados, se combinarán con los tampones amonio, fosfato, etc., intraluminales. Así pues, si hay una hiperaldosteronemia, nos encontraremos ante una situación de hipernatremia, hipocalemia y alcalosis metabólica, mientras que si tenemos una hipoaldosteronemia, encontraremos asociada una hiperpotasemia, hiponatremia, y acidosis metabólica. 508
5 Medida del ph Para medir el ph realizamos una gasometría sanguínea en sangre arterial o venosa, en condiciones anaerobias, y sangre heparinizada. Así obtenemos una medida directa del ph y pco 2 que nos permiten calcular los valores de bicarbonato por medio de la ecuación de HendersonHasselbach. Valores normales: ph= 7.40 PCO 2 = 40 mmhg [HCO 3 ] =24 meq/l Valores fisiológicos ph pco 2 HCO 3 Arteria 7,377, Vena 7,327, La sangre venosa es ligeramente más ácida que la arterial. Si no queremos hacer una determinación de oxígeno, hacemos un equilibrio venoso. Cuestiones enfrente de cualquier alteración del equilibrio ácidobase De qué trastorno se trata? Es adecuada la respuesta compensadora? Cuál es la causa del trastorno? 1. De qué trastorno se trata? Pedimos una analítica, si el ph es bajo es una acidosis, y si es alto, una alcalosis. Metabólica o respiratoria? Si encontramos una disminución del HCO 3, acidosis metabólica, mientras que si hay aumento del CO 2, acidosis respiratoria. En lo que respecta a la alcalosis, si los HCO 3 están elevados, tendremos alcalosis metabólica, mientras que si el CO 2 está bajo, tendremos alcalosis respiratoria. Cabe destacar la existencia de trastornos mixtos del equilibrio AB: ph : Acidosis metabólica + acidosis respiratoria. Ej: paciente con EPOC (acidosis respiratoria de base) que hace una acidosis metabólica que no podrá compensar debido al problema pulmonar. ph : Alcalosis metabólica + alcalosis respiratoria. 509
6 2. Compensación en trastornos simples: Trastorno Compensación Acidosis metabólica 1 mmol CO 3 H 1.25 mmhg PCO 2 Alcalosis metabólica 1 mmol CO 3 H 0.75 mmhg PCO 2 Alcalosis resp aguda 10 mmhg PCO 2 2 mmol/l CO 3 H crónica 10 mmhg PCO 2 4 mmol/l CO 3 H Acidosis resp aguda 10 mmhg PCO 2 1 mmol/l CO 3 H crónica 10 mmhg PCO 2 4 mmol/l CO 3 H Cuando tenemos un paciente podemos hacernos una idea de si la compensación es adecuada o no observando las variaciones del CO 2 y el HCO 3. Por ejemplo: en una acidosis metabólica, por cada mmol que disminuye el HCO 3, observamos un descenso de 1.25 mmhg de la PCO 2. De este modo, si en vez de 24mmol de HCO 3 tenemos 23, pues en vez de 40mmHg de CO 2 tendremos 38,75. Cuando tenemos una alteración respiratoria, los mecanismos compensadores dependen de si ésta es aguda o crónica. Si es aguda, la acción compensadora rápida del pulmón puede ser suficiente para resolver la situación, no llegando así a actuar el riñón debido a que el problema se resuelve antes de que éste pueda actuar (la función compensadora renal es más tardía), mientras que si es crónica, tanto el pulmón como el riñón actuarán de forma reguladora conjunta y el efecto compensador será mayor (no es necesario saberse la tabla, sólo el concepto). ACIDOSIS METABÓLICA Acidosis metabólica: se define como un aumento de hidrogeniones que pueden tener una procedencia endógena (metabolismo) o exógena (dieta), o por dificultad para excretar hidrogeniones o bien por pérdida de HCO 3. ANION GAP Ahora bien, cómo saber si la acidosis metabólica es debida a un aumento de los hidrogeniones o a una pérdida de bicarbonato? Por medio del cálculo del anion gap: El catión principal en sangre es el Na +, mientras que los aniones principales en sangre son el Cl y el HCO 3. Éstos son iones que podemos encontrar en una analítica básica. En condiciones de electroneutralidad, las cargas negativas o aniones son iguales a las cargas positivas o cationes, de tal forma que la diferencia entre estas debería ser nula; no obstante, dado que esta diferencia la hacemos tomando únicamente los valores de los iones principales, obtenemos un valor que representa a todos aquellos otros iones que se encuentran extracelularmente pero que no han sido tenidos en cuenta a la hora de realizar el cálculo. Esto es lo que llamamos anión gap o aniones no medidos, y suele tener un valor normal de 1012mEq/l. AG = Na + (Cl + CO 3 H ) = 1012 meql/l Las situaciones de anión gap aumentado indican que tenemos una cantidad mayor de cationes con respecto a la normalidad, lo que puede interpretarse como una ganancia de ácidos (más H + ). Cuando tenemos un anión gap normal podemos interpretar que existe una pérdida de HCO 3 (se entiende que al disminuir el HCO 3 el anión gap es normal debido a que las concentraciones de Na + son muy superiores a las de HCO 3 y las diferencias se sienten de forma mínima). 510
7 1. Anión Gap Aumentado: ganancia de ácidos, acidosis hipoclorémica a. Exógena: Por metabolismo de metanol a formaldehido Por metabolismo de etilenglicol a oxalato. Salicilatos Inhalación de tolueno b. Endógena: Cetoacidosis diabética con producción de Bhidroxibutirato y aceoacetato. Acidosis láctica por hipoxia tisular, enfermedad hepática etc. Ayuno prolongado 2. Anión Gap normal: pérdida de HCO 3, acidosis hiperclorémica a. Causa digestiva Diarrea Fístula pancreática o Fístula biliar Laxantes Derivación ureterointestinal b. Causa renal Acidosis renal proximal Acidosis renal distal O incapacidad de excreción de H + como tiene lugar en el hipoaldosteronismo ETIOLOGÍA Cuadro que hay que ir siguiendo al observar un anión gap elevado o normal. Por ejemplo, si está elevado, miramos las cetonas; si éstas están aumentadas, miramos la glucosa, que si está aumentada nos indica una cetoacidosis diabética, etc. 511
8 CLÍNICA La propia de la entidad (diarreas...). Hiperventilación (respiración acidótica de Kussmaul). Hipocapnia (intento de compensar). Si es grave: o Disminución saturación de oxígeno o VD arteriolar o Depresión miocárdica o Aumento de las catecolaminas (pueden conducir a shock) o Anorexia, vómitos o Obnubilación, coma (afectación del sistema nervioso) Deshidratación (se inhibe la reabsorción de Na+) En casos crónicos Desmineralización ósea, hipercalciuria, hiperfosfaturia Hiperpotasemia!! TRATAMIENTO Soporte vital Tratamiento específico: Insulina en cetoacidosis diabética. Soporte hemodinámico en el shock/restablecer perfusión tisular. Diálisis e infusión de etanol en intoxicación per metanol y etilenglicol. Tratamiento general Mantenimiento de la ventilación Infusión de HCO 3 : Déficit de HCO 3 = δhco 3 δhco 3 = HCO 3 diana [HCO 3 ] x 0.5 x peso Para ello se calcula el déficit de HCO 3 : el HCO 3 que tiene el enfermo menos el HCO 3 al que quiero llegar (normal) por el peso y por 0.5. Pero en la práctica clínica, cuando el paciente se encuentra en una situación muy grave, se va infundiendo periódicamente 1Molar de HCO 3 hasta que más o menos se estabiliza (está ya fuera de peligro) y entonces se van corrigiendo más poco a poco las concentraciones. Control de la hiperpotasemia ALCALOSIS METABÓLICA Se define la alcalosis metabólica como una elevación primaria del HCO 3 bien por un aumento de su aporte o bien por pérdida de hidrogeniones. Independientemente de la causa que la genera, su persistencia depende de la alteración de los mecanismos renales que controlan la excreción de HCO 3 tales como: Déficit de potasio (según el mecanismo intercambiador de K + e H + explicado anteriormente). Si estamos en situación de acidosis entran los H + en la célula y sale el K +, mientras que en una situación de alcalosis los H + salen de la célula y el K + entra en ella; así pues, si tenemos un déficit de K +, estos H + no podrán salir al medio extracelular y compensar la situación de alcalosis, por lo que se agravará la situación). Contracción del volumen Exceso de actividad mineralocorticoide (en estos dos últimos casos, la acción de la aldosterona favorece la retención de Na + a costa de excreción de K + e H + que llevará a la disminución de la carga ácida y consecuente alcalosis). 512
9 ETIOLOGÍA Aumento de los aportes: a. Infusión de HCO 3 b. Hemoderivados (citrato=base) c. Sd. leche alcalinos por ingesta excesiva de lácteos. Pérdida de H + a. Pérdida digestiva drenaje gástrico. b. Pérdida renal contracción del volumen con activación del sistema reninaangiotensina y catecolaminas que aumentan la secreción de H + por parte del intercambiador de Na + e H + en el túbulo poximal, dietas pobres en NaCl, diuréticos tiacídicos y de asa, hiperaldosteronismo c. Desplazamiento intracelular de protones hipopotasemia. Conocer el estado de hidratación del paciente es importante, pues como comentábamos, la depleción del volumen trae consigo una excreción de H + que actúa como agravante de la situación de alcalosis metabólica. En estos casos, el estado de hidratación se valora por medio de la determinación de la concentración de iones cloruro en orina. CLÍNICA Deshidratación Hipopotasemia Apatía Rampas Debilidad muscular Tetania Arritmias cardíacas. 513
10 ACIDOSIS RESPIRATORIA La acidosis respiratoria se produce por una retención primaria de CO 2 que lleva a una situación de hipercapnia que debe ser compensada por parte del organismo. En una situación aguda, la compensación es llevada a cabo por parte de los tampones intracelulares de la hemoglobina y proteínas, ya que a nivel extracelular el tampón HCO 3 no puede abarcar todos los ácidos. Cuando esta hipercapnia es crónica entonces existe suficiente tiempo para que el organismo ponga en marcha los mecanismos de compensación renales que incrementan la excreción de H +. Estos H + a su vez en orina serán también tamponados por el tampón amonio y los diversos mecanismos de titulación de la acidez, lo que favorece que los H + no sean reabsorbidos. ETIOLOGÍA La causa principal de acidosis respiratoria es la afectación pulmonar, frecuentemente EPOC. CLÍNICA Cefalea Confusión, disminución de conciencia Irritabilidad Asterixis TRATAMIENTO Disminución de la contractibilidad miocárdica Disminución de las resistencias periféricas. Broncodilatadores Fisioterapia respiratoria Tratamiento infecciones Ventilación mecánica no invasiva o invasiva El aporte excesivo de O 2 puede inhibir el centro respiratorio y agravar la sintomatología. 514
11 ALCALOSIS RESPIRATORIA Disminución de la concentración de CO 2 por hiperventilación. La compensación de la alcalosis respiratoria es fundamentalmente renal. La respuesta renal tarda unos 34 días y consiste en la disminución de la reabsorción proximal de HCO 3, la disminución de la excreción de amonio y la disminución de la acidez titulable. Por cada 10 mmhg pco 2, 4 meq/l HCO 3. Las situaciones más frecuentes de alcalosis respiratoria son las crisis de ansiedad, en las cuales pueden producirse contracciones tetánicas como consecuencia de la alcalosis. ETIOLOGÍA RESUMEN El ph sanguíneo ( ) debe estar está dentro de unos márgenes estrechos ( a lo sumo), pues este determina la cinética enzimática, el metabolismo celular y el buen funcionamiento del organismo. A fin de compensar los desequilibrios que se producen continuamente debido a la ingesta de ácidos y la producción de estos por medio del metabolismo celular, disponemos de sistemas de tamponamiento (ácidos y bases que se unen o ceden hidrogeniones tratando de estabilizar el ph) intracelular (proteínas, fosfatos, hemoglobina, CaCO 3 ) y extracelular (bicarbonato), función pulmonar (el pulmón variando la frecuencia respiratoria permite variar la carga ácida en sangre) y función renal (el riñón regula la concentración de H + por medio de la excreción de ácido y reabsorción de HCO 3 ). El principal tampón extracelular es el HCO 3, así pues, conociendo las concentraciones de los componentes de este tampón así como el ph y el anion gap por medio de la realización de una analítica sanguínea y la utilización de la ecuación de HendersonHasselbach, podemos detectar alteraciones en el equilibrio AB del organismo y conocer su causa: 515
12 Acidosis metabólica: ph<7.4, HCO 3 <24mmol, pco 2 =40mmHg Clínica: Propia de la entidad, hiperventilación, hipocapnia, disminución saturación de oxígeno, VD arteriolar, depresión miocárdica, aumento de las catecolaminas, anorexia, vómitos, obnubilación, coma, deshidratación, desmineralización ósea, hipercalciuria, hiperfosfaturia, hiperpotasemia. Etiología más frecuente: o o Anion gap aumentado ganancia de ácidos: metabolismo del metanol, cetoacidosis... Anión gap disminuido pérdida de bicarbonatos: diarreas, acidosis renal Tratamiento: Soporte vital, tratamiento específico, tratamiento general (mantenimiento de la ventilación, infusión de HCO 3 ). Acidosis respiratoria: ph<7.4, HCO 3 =24mmol, pco 2 >40mmHg Clínica: Cefalea, confusión, irritabilidad, asterixis, disminución de conciencia, de la contractibilidad miocárdica y las resistencias periféricas. Etiología más frecuente: afectación respiratoria (EPOC). Tratamiento: Broncodilatadores, fisioterapia respiratoria, tratamiento de infecciones, ventilación mecánica no invasiva o invasiva. Alcalosis metabólica: ph>7.4, HCO 3 >24mmol, pco 2 =40mmHg Clínica: Deshidratación, hipopotasemia, apatía, rampas, debilidad muscular, tetania, arritmias cardíacas. Etiología más frecuente: Aumento de los aportes (ej: ingesta de bebidas carbonatadas), disminución de H + (ej. Vómitos). IMPORTANTE: conocer el estado de hidratación del paciente por medio del Cl en orina, un paciente deshidratado eliminará mayor cantidad de H + y ello agravará la situación. Alcalosis respiratoria: ph>7.4, HCO 3 =24mmol, pco 2 <40mmHg Clínica: contracciones tetánicas Etiología más frecuente: crisis de ansiedad. También podemos encontrar trastornos mixtos: Acidosis metabólica + acidosis respiratoria. Ej: EPOC Alcalosis metabólica + alcalosis respiratoria. 516
Equilibrio Acido-Base
 UNIVERSIDAD DE SAN CARLOS DE GUATEMALA FACULTAD DE CIENCIAS MÉDICAS FASE I, Unidad Didáctica: BIOQUÍMICA MÉDICA 2º AÑO CICLO ACADÉMICO 2,007 Equilibrio Acido-Base Dr. Mynor A. Leiva Enríquez Conceptos
UNIVERSIDAD DE SAN CARLOS DE GUATEMALA FACULTAD DE CIENCIAS MÉDICAS FASE I, Unidad Didáctica: BIOQUÍMICA MÉDICA 2º AÑO CICLO ACADÉMICO 2,007 Equilibrio Acido-Base Dr. Mynor A. Leiva Enríquez Conceptos
EQUILIBRIO ÁCIDO-BASE
 EQUILIBRIO ÁCIDO-BASE - Departamento de Fisiopatología - Facultad de Medicina Br. Inés Lujambio CONCEPTOS BÁSICOS. Ácido: toda sustancias capaz de ceder protones de hidrógeno (H + ). HCl H + + Cl - Base:
EQUILIBRIO ÁCIDO-BASE - Departamento de Fisiopatología - Facultad de Medicina Br. Inés Lujambio CONCEPTOS BÁSICOS. Ácido: toda sustancias capaz de ceder protones de hidrógeno (H + ). HCl H + + Cl - Base:
Control del Equilibrio ácido-base
 Control del Equilibrio ácido-base Escala de ph ph Concentración de H + en Eq/L 1 0.1 2 0.01 3 0.001 4 0.0001 5 0.00001 6 0.000001 7 0.0000001 7.4 0.0000004 8 0.00000001 9 0.000000001 ÁLCALI: sustancia
Control del Equilibrio ácido-base Escala de ph ph Concentración de H + en Eq/L 1 0.1 2 0.01 3 0.001 4 0.0001 5 0.00001 6 0.000001 7 0.0000001 7.4 0.0000004 8 0.00000001 9 0.000000001 ÁLCALI: sustancia
[A-] Citrato 3- ph = pka + log. 7 = log [AH] Citrato 2- 7 = log = = x x
![[A-] Citrato 3- ph = pka + log. 7 = log [AH] Citrato 2- 7 = log = = x x [A-] Citrato 3- ph = pka + log. 7 = log [AH] Citrato 2- 7 = log = = x x](/thumbs/55/35730009.jpg) Una reacción enzimática transcurre en 10 ml de una disolución cuya concentración total de citrato es 120 mm y su ph inicial es de 7. Durante la reacción se producen 0.2 miliequivalentes de un ácido. Calcular
Una reacción enzimática transcurre en 10 ml de una disolución cuya concentración total de citrato es 120 mm y su ph inicial es de 7. Durante la reacción se producen 0.2 miliequivalentes de un ácido. Calcular
lunes 27 de febrero de 12 Desequilibrio Acido-Base
 Desequilibrio Acido-Base Equilibrio Ácido-Base H + es un anión con muy baja concentración en el cuerpo humano. Na + 3.5 millones de veces mas que H + Escala de ph: mide el grado de acidez de una solución.
Desequilibrio Acido-Base Equilibrio Ácido-Base H + es un anión con muy baja concentración en el cuerpo humano. Na + 3.5 millones de veces mas que H + Escala de ph: mide el grado de acidez de una solución.
GASES EN SANGRE. modifican el ph sanguineo.
 GASES EN SANGRE ESTADO ACIDO-BASE ESTADO DE OXIGENACION Detectar o confirmar alteraciones metabolicas y/o respiratorias que modifican el ph sanguineo. Determinar si la oxigenacion tisular es la adecuada.
GASES EN SANGRE ESTADO ACIDO-BASE ESTADO DE OXIGENACION Detectar o confirmar alteraciones metabolicas y/o respiratorias que modifican el ph sanguineo. Determinar si la oxigenacion tisular es la adecuada.
Actualización en Medio Interno Conceptos básicos
 Actualización en Medio Interno Conceptos básicos Bioquímica Lucrecia Drago Bioquímica M. Fernanda Pontoriero Ácidos Moléculas capaces de liberar H + HCl H + + Cl H 2 CO 3 H + + HCO 3 Bases Moléculas capaces
Actualización en Medio Interno Conceptos básicos Bioquímica Lucrecia Drago Bioquímica M. Fernanda Pontoriero Ácidos Moléculas capaces de liberar H + HCl H + + Cl H 2 CO 3 H + + HCO 3 Bases Moléculas capaces
Líquidos corporales Compartimiento Equilibrio de líquidos. Q.F. Adriana Cordero
 Líquidos corporales Compartimiento Equilibrio de líquidos Q.F. Adriana Cordero INTRODUCCIÒN El agua y los solutos disueltos en cada uno de los compartimentos corporales de fluidos constituyen los líquidos
Líquidos corporales Compartimiento Equilibrio de líquidos Q.F. Adriana Cordero INTRODUCCIÒN El agua y los solutos disueltos en cada uno de los compartimentos corporales de fluidos constituyen los líquidos
EQUILIBRIO ACIDO - BASE
 EQUILIBRIO ACIDO - BASE Carrera de Médicos Especialistas Universitarios en Medicina Crítica y Terapia Intensiva. Universidad de Buenos Aires CONCEPTOS GENERALES EQUILIBRIO ACIDO-BASE EN FORMA ESTEQUIOMÉTRICA
EQUILIBRIO ACIDO - BASE Carrera de Médicos Especialistas Universitarios en Medicina Crítica y Terapia Intensiva. Universidad de Buenos Aires CONCEPTOS GENERALES EQUILIBRIO ACIDO-BASE EN FORMA ESTEQUIOMÉTRICA
EQUILIBRIO ÁCIDO-BASE MANTENIMIENTO DE LA HOMEOSTASIS
 EQUILIBRIO ÁCIDO-BASE MANTENIMIENTO DE LA HOMEOSTASIS EQUILÍBRIO ÁCIDO-BASE La regulación de ph a nivel celular, es necesaria para la supervivencia. Los ácidos y bases entran continuamente en la sangre
EQUILIBRIO ÁCIDO-BASE MANTENIMIENTO DE LA HOMEOSTASIS EQUILÍBRIO ÁCIDO-BASE La regulación de ph a nivel celular, es necesaria para la supervivencia. Los ácidos y bases entran continuamente en la sangre
Revista de Actualización Clínica Volumen
 ACIDOSIS METABOLICA Vargas Flores Tatiana 1 Colaboración: Condori Canaza Claudia 2 RESUMEN El ph responsable del equilibrio ácidobase a nivel del líquido extracelular tiene un valor de 7,35 a 7,40; el
ACIDOSIS METABOLICA Vargas Flores Tatiana 1 Colaboración: Condori Canaza Claudia 2 RESUMEN El ph responsable del equilibrio ácidobase a nivel del líquido extracelular tiene un valor de 7,35 a 7,40; el
Agua, electrolitos, balance acido-base. Dra. Luz E. Cuevas-Molina NURS 1231
 Agua, electrolitos, balance acido-base Dra. Luz E. Cuevas-Molina NURS 1231 1 Introducción Para mantener la homoestasis debe haber un balance entre las cantidades de fluido y electrolitos Los electrolitos
Agua, electrolitos, balance acido-base Dra. Luz E. Cuevas-Molina NURS 1231 1 Introducción Para mantener la homoestasis debe haber un balance entre las cantidades de fluido y electrolitos Los electrolitos
METABOLISMO ACIDO / BASE
 METABOLISMO ACIDO / BASE Dr Sergio Octavio GRANADOS TINAJERO Hospital Angeles de Villahermosa, Villahermosa, Tabasco, México. Course : 3 Year : 2003 Language : Spanish Country : Mexico City : Baja California
METABOLISMO ACIDO / BASE Dr Sergio Octavio GRANADOS TINAJERO Hospital Angeles de Villahermosa, Villahermosa, Tabasco, México. Course : 3 Year : 2003 Language : Spanish Country : Mexico City : Baja California
ESTADO ACIDO BASE ACIDOSIS METABOLICA. ETIOLOGÍA DE LA ACIDOSIS METABÓLICA Inhabilidad Para Secretar La Carga Acida De La Dieta +
 ESTADO ACIDO BASE Los siguientes pasos son usados para evaluar los desordenes acidobase: 1.Determinar la anormalidad de base acidosis metabólica y/o alcalosis metabólica. 2.Determinar los factores contribuyentes
ESTADO ACIDO BASE Los siguientes pasos son usados para evaluar los desordenes acidobase: 1.Determinar la anormalidad de base acidosis metabólica y/o alcalosis metabólica. 2.Determinar los factores contribuyentes
INTERPRETACION DE LOS GASES ARTERIALES
 INTERPRETACION DE LOS GASES ARTERIALES ph PaO2 PaCO2 HCO3 BE Hb SaO2 Bloque 6 Modulo 2 Dr Erick Valencia Anestesiologo Intensivista. Que son los Gases Arteriales? Una muestra de sangre anticoagulada que
INTERPRETACION DE LOS GASES ARTERIALES ph PaO2 PaCO2 HCO3 BE Hb SaO2 Bloque 6 Modulo 2 Dr Erick Valencia Anestesiologo Intensivista. Que son los Gases Arteriales? Una muestra de sangre anticoagulada que
SOLUCIONES BUFFERS. pk = valor de ph en el cual las concentraciones del ácido y la sal son iguales
 SOLUCIONES BUFFERS Constituidas por un ácido débil y su base conjugada (sal) permite la adición de ácido o base sin variar considerablemente el ph. La capacidad búffer es máximo una unidad por encima y
SOLUCIONES BUFFERS Constituidas por un ácido débil y su base conjugada (sal) permite la adición de ácido o base sin variar considerablemente el ph. La capacidad búffer es máximo una unidad por encima y
7. ESTUDIO DEL EQUILIBRIO ACIDO BASE DE UN PACIENTE
 Departamento de Bioquímica y Biología Molecular ph y equilibrios acido-base 7. ESTUDIO DEL EQUILIBRIO ACIDO BASE DE UN PACIENTE ESQUEMA - Estudio del equilibrio ácido-base de un paciente - Trastornos del
Departamento de Bioquímica y Biología Molecular ph y equilibrios acido-base 7. ESTUDIO DEL EQUILIBRIO ACIDO BASE DE UN PACIENTE ESQUEMA - Estudio del equilibrio ácido-base de un paciente - Trastornos del
Cátedra de Fisiología Humana CAPÍTULO I CAPITULO III. Equilibrio Acido Base PH. Carrera de Enfermería. Universidad Nacional del Nordeste
 CAPÍTULO I Cátedra de Fisiología Humana CAPITULO III Equilibrio Acido Base PH Carrera de Enfermería. Universidad Nacional del Nordeste 37 CAPITULO 3: Cada soluto del organismo, el sodio, el potasio, el
CAPÍTULO I Cátedra de Fisiología Humana CAPITULO III Equilibrio Acido Base PH Carrera de Enfermería. Universidad Nacional del Nordeste 37 CAPITULO 3: Cada soluto del organismo, el sodio, el potasio, el
Fisiopatología del aparato respiratorio II _ Pruebas complementarias
 Fisiopatología del aparato respiratorio II _ Pruebas complementarias Gasometría arterial (GSA) Gasometría arterial: Punción de una arteria periférica Determina el equilibrio ácido-base: - ph - Las concentraciones
Fisiopatología del aparato respiratorio II _ Pruebas complementarias Gasometría arterial (GSA) Gasometría arterial: Punción de una arteria periférica Determina el equilibrio ácido-base: - ph - Las concentraciones
Carvajal Ramos M, Sánchez Sánchez M, Cornide Santos I, Panadero Carlavilla FJ
 ALTERACIONES DEL EQUILIBRIO ÁCIDO-BASE Carvajal Ramos M, Sánchez Sánchez M, Cornide Santos I, Panadero Carlavilla FJ El ph refleja la concentración de cationes de hidrógeno presentes en una determinada
ALTERACIONES DEL EQUILIBRIO ÁCIDO-BASE Carvajal Ramos M, Sánchez Sánchez M, Cornide Santos I, Panadero Carlavilla FJ El ph refleja la concentración de cationes de hidrógeno presentes en una determinada
6. MANTENIMIENTO DEL ph EN EL MEDIO EXTRACELULAR
 Departamento de Bioquímica y Biología Molecular ph y equilibrios acido-base 6. MANTENIMIENTO DEL ph EN EL MEDIO EXTRACELULAR ESQUEMA - Composición iónica de los medios corporales - Capacidad tampón - Mantenimiento
Departamento de Bioquímica y Biología Molecular ph y equilibrios acido-base 6. MANTENIMIENTO DEL ph EN EL MEDIO EXTRACELULAR ESQUEMA - Composición iónica de los medios corporales - Capacidad tampón - Mantenimiento
Acidosis y Alcalosis Metabolica.
 Acidosis y Alcalosis Metabolica. Acidosis metabólica Se caracteriza por: ph arterial bajo (concentración alta de hidrogeniones) Reducción en la concentración plasmática de HCO3. Hiperventilación compensatoria.
Acidosis y Alcalosis Metabolica. Acidosis metabólica Se caracteriza por: ph arterial bajo (concentración alta de hidrogeniones) Reducción en la concentración plasmática de HCO3. Hiperventilación compensatoria.
Organización Funcional y el Medio Interno
 Organización Funcional y el Medio Interno Aproximadamente el 50 % del cuerpo humano es líquido y la mayor parte es intracelular, la tercera parte es extracelular, la misma que se encuentra en movimiento
Organización Funcional y el Medio Interno Aproximadamente el 50 % del cuerpo humano es líquido y la mayor parte es intracelular, la tercera parte es extracelular, la misma que se encuentra en movimiento
Fisiopatología Del Equilibrio Ácido-Base: Alcalosis
 Fisiopatología Del Equilibrio Ácido-Base: Alcalosis La alcalosis mucho menos frecuente que la acidosis, pero muy complicada para el organismo. Cuando el organismo sufre alcalosis va a tener problemas bastante
Fisiopatología Del Equilibrio Ácido-Base: Alcalosis La alcalosis mucho menos frecuente que la acidosis, pero muy complicada para el organismo. Cuando el organismo sufre alcalosis va a tener problemas bastante
Programa 3º Curso. Curso (Prof. M García-Caballero)
 Programa 3º Curso Departamento de Cirugía Curso 2008-09 Equilibrio i hidroelectrolítico lí i y ácido-base (Prof. M García-Caballero) http://www.cirugiadelaobesidad.net/ CAMBIOS DE FLUIDOS Y ELECTROLITOS
Programa 3º Curso Departamento de Cirugía Curso 2008-09 Equilibrio i hidroelectrolítico lí i y ácido-base (Prof. M García-Caballero) http://www.cirugiadelaobesidad.net/ CAMBIOS DE FLUIDOS Y ELECTROLITOS
1. Líquidos corporales. 2. Anatomía y función renal. 3. Hormonas ADH y aldosterona
 1. Líquidos corporales 2. Anatomía y función renal 3. Hormonas ADH y aldosterona Propiedades de la Homeostasis 1. Importancia tanto del sistema nervioso como del endocrino. 2. Controles antagónicos. 3.
1. Líquidos corporales 2. Anatomía y función renal 3. Hormonas ADH y aldosterona Propiedades de la Homeostasis 1. Importancia tanto del sistema nervioso como del endocrino. 2. Controles antagónicos. 3.
TALLER DE ANALISIS DE GASES ARTERIALES
 TALLER DE ANALISIS DE GASES ARTERIALES Dr. Menfil A Orellana-Barrios Medicina Interna Cursos Precongreso Congreso de Residentes 2012 HGSJDD www.drmenfilorellana.wordpress.com Para qué se utilizan los Gases
TALLER DE ANALISIS DE GASES ARTERIALES Dr. Menfil A Orellana-Barrios Medicina Interna Cursos Precongreso Congreso de Residentes 2012 HGSJDD www.drmenfilorellana.wordpress.com Para qué se utilizan los Gases
2. Sobre los valores de las diferentes presiones parciales de los gases, marca con una cruz (X) la respuesta correcta según corresponda.
 Semana 7 Consolidación 7. 1. Acerca de la mecánica de la ventilación pulmonar, escribe en el espacio en blanco (V) si son verdaderos o (F) si son falsos los siguientes planteamientos: a) _F_ Los intercostales
Semana 7 Consolidación 7. 1. Acerca de la mecánica de la ventilación pulmonar, escribe en el espacio en blanco (V) si son verdaderos o (F) si son falsos los siguientes planteamientos: a) _F_ Los intercostales
TALLER DE GASES ARTERIALES
 TALLER DE GASES ARTERIALES MOP 24 de Agosto 2010 Objetivos Aprender a reconocer los trastornos del equilibrio ácido-base: Acidosis metabólica y respiratoria, alcalosis metabólica y respiratoria. Familiarizarse
TALLER DE GASES ARTERIALES MOP 24 de Agosto 2010 Objetivos Aprender a reconocer los trastornos del equilibrio ácido-base: Acidosis metabólica y respiratoria, alcalosis metabólica y respiratoria. Familiarizarse
FISIOPATOLOGIA. Concentración normal H+: 40 nmoles/l. -PH : 6.8-7.35 < -( H+) : 16-160 nmoles/l -PCO2: 36-44 mmhg -BE: -3 a 3
 FISIOPATOLOGIA Concentración normal H+: 40 nmoles/l -PH : 6.8-7.35 < -( H+) : 16-160 nmoles/l -PCO2: 36-44 mmhg -BE: -3 a 3 FISIOPATOLOGIA ACIDO-BASE ACIDO: sustancia capaz de ceder protones BASE: sustancia
FISIOPATOLOGIA Concentración normal H+: 40 nmoles/l -PH : 6.8-7.35 < -( H+) : 16-160 nmoles/l -PCO2: 36-44 mmhg -BE: -3 a 3 FISIOPATOLOGIA ACIDO-BASE ACIDO: sustancia capaz de ceder protones BASE: sustancia
Conclusiones. Siempre antes del análisis, esta la Clínica o que espero yo en mi paciente
 Gases en Sepsis Conclusiones Siempre antes del análisis, esta la Clínica o que espero yo en mi paciente El análisis de los gases no debe retrasar tomar el Lactato e iniciar EGDT No tratamos solo números
Gases en Sepsis Conclusiones Siempre antes del análisis, esta la Clínica o que espero yo en mi paciente El análisis de los gases no debe retrasar tomar el Lactato e iniciar EGDT No tratamos solo números
Fisiopatología Equilibrio Hidrosalino. Potasio
 Fisiopatología Equilibrio Hidrosalino Potasio Prof. Marcos Moreira Espinoza Instituto de Farmacología y Morfofisiología Universidad Austral de Chile Valdivia- Chile FISIOPATOLOGIA DEL EQUILIBRIO DEL K+:
Fisiopatología Equilibrio Hidrosalino Potasio Prof. Marcos Moreira Espinoza Instituto de Farmacología y Morfofisiología Universidad Austral de Chile Valdivia- Chile FISIOPATOLOGIA DEL EQUILIBRIO DEL K+:
8. CASOS PRACTICOS DE ALTERACIONES DEL EQUILIBRIO ACIDO BASE
 Departamento de Bioquímica y Biología Molecular ph y equilibrios acido-base 8. CASOS PRACTICOS DE ALTERACIONES DEL EQUILIBRIO ACIDO BASE A continuación se presentan una serie de casos prácticos resueltos,
Departamento de Bioquímica y Biología Molecular ph y equilibrios acido-base 8. CASOS PRACTICOS DE ALTERACIONES DEL EQUILIBRIO ACIDO BASE A continuación se presentan una serie de casos prácticos resueltos,
Tema 9: Interpretación de una gasometría
 Tema 9: Interpretación de una gasometría Concepto de gasometría Gasometría en muestras de sangre (arterial, capilar, venosa) Valores normales Hipoxemia Hipercapnia e hipocapnia Acidosis y alcalosis: Introducción
Tema 9: Interpretación de una gasometría Concepto de gasometría Gasometría en muestras de sangre (arterial, capilar, venosa) Valores normales Hipoxemia Hipercapnia e hipocapnia Acidosis y alcalosis: Introducción
UNIVERSIDAD AUSTRAL DE CHILE INSTITUTO DE FARMACOLOGIA Prof. Marcos Moreira Espinoza 1
 INSTITUTO DE FARMACOLOGIA Prof. Marcos Moreira Espinoza 1 EQUILIBRIO ACIDO-BASE La función celular es óptima cuando el ph del LEC es 7.4 ([H+] de 40 nmoles/litro). Sin embargo hay muchas situaciones, especialmente
INSTITUTO DE FARMACOLOGIA Prof. Marcos Moreira Espinoza 1 EQUILIBRIO ACIDO-BASE La función celular es óptima cuando el ph del LEC es 7.4 ([H+] de 40 nmoles/litro). Sin embargo hay muchas situaciones, especialmente
Alteraciones de los Fluidos Corporales, Electrolitos
 Alteraciones de los Fluidos Corporales, Electrolitos Introducción Abner J. Gutiérrez Chávez, MVZ, MC. Facultad de Medicina Veterinaria y Zootecnia, UNAM. Dpto. Producción Animal: Rumiantes Existen diversas
Alteraciones de los Fluidos Corporales, Electrolitos Introducción Abner J. Gutiérrez Chávez, MVZ, MC. Facultad de Medicina Veterinaria y Zootecnia, UNAM. Dpto. Producción Animal: Rumiantes Existen diversas
ENFERMERÍA CLÍNICA I Felicitas Merino de la Hoz TEMA 1.2.2 DESEQUILIBRIOS ACIDOBÁSICOS
 TEMA 1.2.2 DESEQUILIBRIOS ACIDOBÁSICOS ÍNDICE 1. Introducción. 2. Análisis e interpretación de los gases arteriales. 3. Alteraciones del equilibrio ácido- base. 3.1. Acidosis respiratoria. 3.2. Alcalosis
TEMA 1.2.2 DESEQUILIBRIOS ACIDOBÁSICOS ÍNDICE 1. Introducción. 2. Análisis e interpretación de los gases arteriales. 3. Alteraciones del equilibrio ácido- base. 3.1. Acidosis respiratoria. 3.2. Alcalosis
1.- FOSFATO MONOSUSTITUIDO/FOSFATO DISUSTITUIDO (H2PO4 - /HPO4 = )
 1. FOSFATO MONOSUSTITUIDO/FOSFATO DISUSTITUIDO (H2PO4 /HPO4 = ) El ácido fosfórico (H 3 PO 4 ), además de formar parte de numerosos compuestos orgánicos (ácidos nucleicos, fosfolípidos, azúcares, etc.)
1. FOSFATO MONOSUSTITUIDO/FOSFATO DISUSTITUIDO (H2PO4 /HPO4 = ) El ácido fosfórico (H 3 PO 4 ), además de formar parte de numerosos compuestos orgánicos (ácidos nucleicos, fosfolípidos, azúcares, etc.)
VARIACIONES SANGUÍNEAS: - pco2 - EL ph ESTIMULO C.R.B., NO COMPENSA DISNEA - po2 - NaHCO3 5 mmol/l
 Fisiopatología Del Equilibrio Ácido-Base: Acidosis PH debe ser menor a 7.35. a) Acidosis Respiratorias b) Acidosis Metabólicas También se habla de acidosis compensadas y no compensadas. Una acidosis puede
Fisiopatología Del Equilibrio Ácido-Base: Acidosis PH debe ser menor a 7.35. a) Acidosis Respiratorias b) Acidosis Metabólicas También se habla de acidosis compensadas y no compensadas. Una acidosis puede
Pauta de corrección guía IV medio Homeostasis
 Pauta de corrección guía IV medio Homeostasis Actividad 1.- Registra la temperatura ambiental en un día cada una hora. Así mismo registra la temperatura corporal que tu cuerpo tiene en cada hora. Grafica
Pauta de corrección guía IV medio Homeostasis Actividad 1.- Registra la temperatura ambiental en un día cada una hora. Así mismo registra la temperatura corporal que tu cuerpo tiene en cada hora. Grafica
ALTERACIONES DEL EQUILIBRIO ACIDO-BASE
 ALTERACIONES DEL EQUILIBRIO ACIDO-BASE El equilibrio ácido-base puede alterarse por dos tipos de mecanismos fundamentales. a) Cambios en la función respiratoria, con aumento o disminución de la P a CO
ALTERACIONES DEL EQUILIBRIO ACIDO-BASE El equilibrio ácido-base puede alterarse por dos tipos de mecanismos fundamentales. a) Cambios en la función respiratoria, con aumento o disminución de la P a CO
EQUILIBRIO ACIDO BASE
 EQUILIBRIO ACIDO BASE ASPECTO FISIOLÓGICO CONCENTRACIÒN NORMAL DE HIDROGENIONES 35 A 45 NM / L HAY MECANISMOS QUE ACTÚAN PERMANENTEMENTE PARA MANTENER ESTE RANGO FUERA DE ESTE HAY ALTERACIÓN DEL FUNCIONAMIENTO
EQUILIBRIO ACIDO BASE ASPECTO FISIOLÓGICO CONCENTRACIÒN NORMAL DE HIDROGENIONES 35 A 45 NM / L HAY MECANISMOS QUE ACTÚAN PERMANENTEMENTE PARA MANTENER ESTE RANGO FUERA DE ESTE HAY ALTERACIÓN DEL FUNCIONAMIENTO
Líquidos y Electrolitos en Cirugía. R o d o l f o A. C a b r a l e s MD D o c e n t e A r e a d e C i r u g í a
 Líquidos y Electrolitos en Cirugía R o d o l f o A. C a b r a l e s MD D o c e n t e A r e a d e C i r u g í a OBJETIVOS Reconocer las bases teóricas de la homeostasis de líquidos y electrolitos en condiciones
Líquidos y Electrolitos en Cirugía R o d o l f o A. C a b r a l e s MD D o c e n t e A r e a d e C i r u g í a OBJETIVOS Reconocer las bases teóricas de la homeostasis de líquidos y electrolitos en condiciones
METABOLISMO DE CALCIO y FOSFORO
 METABOLISMO DE CALCIO y FOSFORO CONTENIDO Y DISTRIBUCION CORPORAL DE CALCIO, FOSFATO Y MAGNESIO: ADULTO: 1kg de calcio ~ 1,7% del peso corporal 5º elemento en abundancia en el cuerpo humano 1 TOTAL DE
METABOLISMO DE CALCIO y FOSFORO CONTENIDO Y DISTRIBUCION CORPORAL DE CALCIO, FOSFATO Y MAGNESIO: ADULTO: 1kg de calcio ~ 1,7% del peso corporal 5º elemento en abundancia en el cuerpo humano 1 TOTAL DE
MEDIO INTERNO ACIDOSIS METABÓLICA DRA. STELLA MARIS DIEGUEZ HTAL. GRAL DE AGUDOS DR. T. ÁLVAREZ
 MEDIO INTERNO ACIDOSIS METABÓLICA DRA. STELLA MARIS DIEGUEZ HTAL. GRAL DE AGUDOS DR. T. ÁLVAREZ 1-Historia clínica G D Varón de 1 año y 5 meses MOTIVO DE CONSULTA retraso del crecimiento ANTECEDENTES RNTPAEG
MEDIO INTERNO ACIDOSIS METABÓLICA DRA. STELLA MARIS DIEGUEZ HTAL. GRAL DE AGUDOS DR. T. ÁLVAREZ 1-Historia clínica G D Varón de 1 año y 5 meses MOTIVO DE CONSULTA retraso del crecimiento ANTECEDENTES RNTPAEG
2.- Sistema renal: Instauración tardía (24-48 horas) y de acción más duradera. Los riñones regulan el bicarbonato plasmático mediante tres procesos:
 Santos Nores, Juan*; Borrajo Prol, María Paz*; Camba Caride, María Jesús* *Servicio de Nefrología INTRODUCCIÓN Y CONCEPTOS: El metabolismo normal produce constantemente radicales ácidos. Sin embargo, el
Santos Nores, Juan*; Borrajo Prol, María Paz*; Camba Caride, María Jesús* *Servicio de Nefrología INTRODUCCIÓN Y CONCEPTOS: El metabolismo normal produce constantemente radicales ácidos. Sin embargo, el
O Un elemento químico es una sustancia que no puede dividirse en otras sustancias por medios químicos comunes. Actualmente los químicos reconocen 92
 BIOELEMENTOS BIOELEMENTOS O La vida se compone de materia, que es todo lo que ocupa espacio y tiene masa. La materia, en forma tan diversas como una roca, madera, metal y aire, se compone de elementos
BIOELEMENTOS BIOELEMENTOS O La vida se compone de materia, que es todo lo que ocupa espacio y tiene masa. La materia, en forma tan diversas como una roca, madera, metal y aire, se compone de elementos
Ventilación Pulmonar. -durante al ejercicio- Elaborado por Lic. Manuel Salazar Leitón
 Ventilación Pulmonar -durante al ejercicio- Elaborado por Lic. Manuel Salazar Leitón Funciones básicas de la ventilación pulmonar Intercambio gaseoso con el ambiente. Regular el acidez en sangre. Comunicación
Ventilación Pulmonar -durante al ejercicio- Elaborado por Lic. Manuel Salazar Leitón Funciones básicas de la ventilación pulmonar Intercambio gaseoso con el ambiente. Regular el acidez en sangre. Comunicación
SGUICEL009QM11-A16V1. Ácido base I: conceptos y teorías
 SGUICEL009QM11-A16V1 Ácido base I: conceptos y teorías Ítem Alternativa Habilidad 1 B Reconocimiento 2 A Comprensión 3 E Reconocimiento 4 E Comprensión 5 E ASE 6 E Comprensión 7 D Comprensión 8 E Comprensión
SGUICEL009QM11-A16V1 Ácido base I: conceptos y teorías Ítem Alternativa Habilidad 1 B Reconocimiento 2 A Comprensión 3 E Reconocimiento 4 E Comprensión 5 E ASE 6 E Comprensión 7 D Comprensión 8 E Comprensión
Tema 1. Introducción
 Tema 1. Introducción - Bioquímica: concepto, y objetivos - Importancia de la Bioquímica en la Lic. De Farmacia - Composición química del cuerpo humano: Bioelementos Bioelementos primarios o principales
Tema 1. Introducción - Bioquímica: concepto, y objetivos - Importancia de la Bioquímica en la Lic. De Farmacia - Composición química del cuerpo humano: Bioelementos Bioelementos primarios o principales
JORNADA CIENTÍFICA COMENTARIOS INTERPRETATIVOS EN EL INFORME ANALÍTICO Y SEGURIDAD DEL PACIENTE
 JORNADA CIENTÍFICA COMENTARIOS INTERPRETATIVOS EN EL INFORME ANALÍTICO Y SEGURIDAD DEL PACIENTE SOCIEDAD ANDALUZA DE ANÁLISIS CLÍNICOS (SANAC) Antequera, 27 de Enero de 2011 COMENTARIOS INTERPRETATIVOS
JORNADA CIENTÍFICA COMENTARIOS INTERPRETATIVOS EN EL INFORME ANALÍTICO Y SEGURIDAD DEL PACIENTE SOCIEDAD ANDALUZA DE ANÁLISIS CLÍNICOS (SANAC) Antequera, 27 de Enero de 2011 COMENTARIOS INTERPRETATIVOS
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO. Bicarbonato sódico 1/6 M Braun Solución para perfusión 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA
 FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Bicarbonato sódico 1/6 M Braun Solución para perfusión 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Contenido: 1 ml 250 ml Hidrogenocarbonato de sodio 14 mg 3,5 g Concentración
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Bicarbonato sódico 1/6 M Braun Solución para perfusión 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Contenido: 1 ml 250 ml Hidrogenocarbonato de sodio 14 mg 3,5 g Concentración
Lección 24. Fármacos Diuréticos UNIDAD VII: PROBLEMAS CARDIOVASCULARES Y SANGUÍNEOS. Ricardo Brage e Isabel Trapero - Farmacología Lección 24
 Ricardo Brage e Isabel Trapero - Lección 24 UNIDAD VII: PROBLEMAS CARDIOVASCULARES Y SANGUÍNEOS Lección 24 Fármacos Diuréticos Guión Ricardo Brage e Isabel Trapero - Lección 24 1. BASES CONCEPTUALES. 2.
Ricardo Brage e Isabel Trapero - Lección 24 UNIDAD VII: PROBLEMAS CARDIOVASCULARES Y SANGUÍNEOS Lección 24 Fármacos Diuréticos Guión Ricardo Brage e Isabel Trapero - Lección 24 1. BASES CONCEPTUALES. 2.
DESORDEN ACIDO BASICO
 DESORDEN ACIDO BASICO Cuando se habla de regulacion del equilibrio acido base, se habla en realidad de la Regulacion de la concentracion de iones hidrogenos en los liquidos corporales 1 Como la concentracion
DESORDEN ACIDO BASICO Cuando se habla de regulacion del equilibrio acido base, se habla en realidad de la Regulacion de la concentracion de iones hidrogenos en los liquidos corporales 1 Como la concentracion
Fisiología y envejecimiento Aparato urinario. Tema 11
 Tema 11 Funciones generales. Anatomía Nefrona Filtración glomerular Reabsorción tubular Secreción tubular Micción Envejecimiento Funciones generales * Mantenimiento de la homeostasis hídrica y electrolítica.
Tema 11 Funciones generales. Anatomía Nefrona Filtración glomerular Reabsorción tubular Secreción tubular Micción Envejecimiento Funciones generales * Mantenimiento de la homeostasis hídrica y electrolítica.
La acidosis metabólica es un trastorno ácido-base que tiende a producir acidemia (descenso en el ph) por cambios primarios en la
 Fecha actualización: 27/09/16 Algoritmos diagnósticos: Equilibrio ácido base Use CTRL+F para buscar en este artículo Roberto Alcazar Arroyo Elena Corchete Prats Servicio de Nefrología Hospital Infanta
Fecha actualización: 27/09/16 Algoritmos diagnósticos: Equilibrio ácido base Use CTRL+F para buscar en este artículo Roberto Alcazar Arroyo Elena Corchete Prats Servicio de Nefrología Hospital Infanta
Fisiopatología del Equilibrio del K+
 A. IMPORTANCIA DEL K+ Fisiopatología del Equilibrio del K+ 1. Determina el volumen celular. 2. Potencial de membrana: - Función neuromuscular, excitab. eléctrica, nervio y músculo, corazón. 3. Equilibrio
A. IMPORTANCIA DEL K+ Fisiopatología del Equilibrio del K+ 1. Determina el volumen celular. 2. Potencial de membrana: - Función neuromuscular, excitab. eléctrica, nervio y músculo, corazón. 3. Equilibrio
SALES MINERALES , CO 3. Aniones: Cl -, PO 4. , NO 3, Cationes: Na +, Ca 2+, Mg 2+, Fe 2+, Fe 3+, K +
 SALES MINERALES Aniones: Cl -, PO 4 3-, CO 3 2-, NO 3, Cationes: Na +, Ca 2+, Mg 2+, Fe 2+, Fe 3+, K + SALES PRECIPITADAS Vieira SALES PRECIPITADAS: CaCO 3 Exoesqueleto de Ca Sales de Ca: caparazones
SALES MINERALES Aniones: Cl -, PO 4 3-, CO 3 2-, NO 3, Cationes: Na +, Ca 2+, Mg 2+, Fe 2+, Fe 3+, K + SALES PRECIPITADAS Vieira SALES PRECIPITADAS: CaCO 3 Exoesqueleto de Ca Sales de Ca: caparazones
El sistema excretor es el encargado de eliminar las sustancias tóxicas y los desechos de nuestro cuerpo. La sangre recoge, en cada tejido y órgano,
 El sistema excretor es el encargado de eliminar las sustancias tóxicas y los desechos de nuestro cuerpo. La sangre recoge, en cada tejido y órgano, desechos que son producto del metabolismo celular. Estos
El sistema excretor es el encargado de eliminar las sustancias tóxicas y los desechos de nuestro cuerpo. La sangre recoge, en cada tejido y órgano, desechos que son producto del metabolismo celular. Estos
Cuidados de enfermería a pacientes con trastornos del ion potasio
 MEDICO QUIRúRGICA Cuidados de enfermería a pacientes con trastornos del ion potasio Bertv Suñé Ysamat* El 98 por ciento del potasio orgánico es intracelular; es el catión más importante de este compartimento.
MEDICO QUIRúRGICA Cuidados de enfermería a pacientes con trastornos del ion potasio Bertv Suñé Ysamat* El 98 por ciento del potasio orgánico es intracelular; es el catión más importante de este compartimento.
Un adulto sano, suele ser capaz de mantener los equilibrios hidroelectrolíticos y ácido-base.
 BALANCE HIDRICO BALANCE HIDRICO Para conservar la salud y mantener las funcíones corporales, es necesario un EQUILIBRIO líquido, electrolítico y ácido báse. El requerimiento es: aporte y eliminación armónico
BALANCE HIDRICO BALANCE HIDRICO Para conservar la salud y mantener las funcíones corporales, es necesario un EQUILIBRIO líquido, electrolítico y ácido báse. El requerimiento es: aporte y eliminación armónico
Dra. María Eugenia Victoria Bianchi Dr. Gustavo Borda Dra Marcela Young. Estudiantes por Concurso según Resolución 1311/95-C-D.
 Dra. María Eugenia Victoria Bianchi Dr. Gustavo Borda Dra Marcela Young. Estudiantes por Concurso según Resolución 1311/95-C-D. Vallejos Javier Serial Marcos Sebastián Rausch Ricardo Simón Laura Solé Juan
Dra. María Eugenia Victoria Bianchi Dr. Gustavo Borda Dra Marcela Young. Estudiantes por Concurso según Resolución 1311/95-C-D. Vallejos Javier Serial Marcos Sebastián Rausch Ricardo Simón Laura Solé Juan
DIURETICOS. Profa. Almudena Albillos Martínez Departamento de Farmacología y Terapéutica Facultad de Medicina Universidad Autónoma de Madrid
 DIURETICOS Profa. Almudena Albillos Martínez Departamento de Farmacología y Terapéutica Facultad de Medicina Universidad Autónoma de Madrid Fisiología renal FUNCION DEL RIÑON - LA NEFRONA Función del riñón:
DIURETICOS Profa. Almudena Albillos Martínez Departamento de Farmacología y Terapéutica Facultad de Medicina Universidad Autónoma de Madrid Fisiología renal FUNCION DEL RIÑON - LA NEFRONA Función del riñón:
Tema 34 Fisiología del sistema excretor. Filtración glomerular. Presiones y permeabilidad. Aclaramiento renal.
 Tema 34 Fisiología del sistema excretor. Filtración glomerular. Presiones y permeabilidad. Aclaramiento renal. 1. Funciones generales del sistema excretor. 2. Anatomía del sistema excretor. 3. La nefrona.
Tema 34 Fisiología del sistema excretor. Filtración glomerular. Presiones y permeabilidad. Aclaramiento renal. 1. Funciones generales del sistema excretor. 2. Anatomía del sistema excretor. 3. La nefrona.
MEDIO INTERNO HOMEOSTASIS. Estructura del medio interno. Se denomina asi al medio extracelular, el medio que rodea a las celulas
 MEDIO INTERNO Se denomina asi al medio extracelular, el medio que rodea a las celulas HOMEOSTASIS Estructura del medio interno El agua representa el 40-60% del peso corporal del organismo. 1 Distribución
MEDIO INTERNO Se denomina asi al medio extracelular, el medio que rodea a las celulas HOMEOSTASIS Estructura del medio interno El agua representa el 40-60% del peso corporal del organismo. 1 Distribución
ACIDOSIS Y GASES SANGUINEOS DURANTE LA HEMOFILTRACION Y LA HEMODIALISIS * María de la Paz Bermejo, María Dolores Gómez, Julia Píerre
 INTRODUCCION ACIDOSIS Y GASES SANGUINEOS DURANTE LA HEMOFILTRACION Y LA HEMODIALISIS * María de la Paz Bermejo, María Dolores Gómez, Julia Píerre Servicio de Nefrología Hospital Clínico de «San Carlos»
INTRODUCCION ACIDOSIS Y GASES SANGUINEOS DURANTE LA HEMOFILTRACION Y LA HEMODIALISIS * María de la Paz Bermejo, María Dolores Gómez, Julia Píerre Servicio de Nefrología Hospital Clínico de «San Carlos»
CHOQUE HIPOVOLEMICO DR. MARIO LOMELI EGUIA SEPTIEMBRE 11, 2013
 CHOQUE HIPOVOLEMICO DR. MARIO LOMELI EGUIA SEPTIEMBRE 11, 2013 CHOQUE HIPOVOLEMICO PERDIDA VOLUMEN CIRCULANTE MECANISMOS DE COMPENSACION ALTERACIONES HEMODINAMICAS CALCULAR PERDIDA CON DATOS CLINICOS IDENTIFICAR
CHOQUE HIPOVOLEMICO DR. MARIO LOMELI EGUIA SEPTIEMBRE 11, 2013 CHOQUE HIPOVOLEMICO PERDIDA VOLUMEN CIRCULANTE MECANISMOS DE COMPENSACION ALTERACIONES HEMODINAMICAS CALCULAR PERDIDA CON DATOS CLINICOS IDENTIFICAR
Equilibrio acido-base
 Equilibrio acido-base Vamos a ver otro de los grandes problemas que tiene el organismo. El organismo siempre tiene una lucha para tratar de mantener el equilibrio ácido-base. Cuando se habla de equilibrio
Equilibrio acido-base Vamos a ver otro de los grandes problemas que tiene el organismo. El organismo siempre tiene una lucha para tratar de mantener el equilibrio ácido-base. Cuando se habla de equilibrio
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO. Bicarbonato Sódico 1M Grifols Solución inyectable 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA
 FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Bicarbonato Sódico 1M Grifols Solución inyectable 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada ampolla de 10 ml de solución contiene: Hidrogenocarbonato de sodio
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Bicarbonato Sódico 1M Grifols Solución inyectable 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada ampolla de 10 ml de solución contiene: Hidrogenocarbonato de sodio
EXCRECIÓN RENAL DE POTASIO ALDOSTERONA HIPERKALEMIA CAUSAS 05/05/2012
 EXCRECIÓN RENAL DE POTASIO El niño con trastornos del potasio : Temas críticos en las decisiones de manejo 5 Congreso Asociación Colombiana de Nefrología Pediátrica ACONEPE Bogotá Filtración de potasio
EXCRECIÓN RENAL DE POTASIO El niño con trastornos del potasio : Temas críticos en las decisiones de manejo 5 Congreso Asociación Colombiana de Nefrología Pediátrica ACONEPE Bogotá Filtración de potasio
PROSPECTO: INFORMACIÓN PARA EL USUARIO. Bicarbonato Sódico 1M Grifols Solución inyectable Hidrogenocarbonato de sodio
 PROSPECTO: INFORMACIÓN PARA EL USUARIO Bicarbonato Sódico 1M Grifols Solución inyectable Hidrogenocarbonato de sodio Lea todo el prospecto detenidamente antes de empezar a usar el medicamento. - Conserve
PROSPECTO: INFORMACIÓN PARA EL USUARIO Bicarbonato Sódico 1M Grifols Solución inyectable Hidrogenocarbonato de sodio Lea todo el prospecto detenidamente antes de empezar a usar el medicamento. - Conserve
Trastornos respiratorios. Acidosis y alcalosis
 Trastornos respiratorios Acidosis y alcalosis Acidosis Respiratoria Trastorno que se caracteriza por aumento primario de la paco2 con elevación de la concentración de H+ en sangre, disminución del ph y
Trastornos respiratorios Acidosis y alcalosis Acidosis Respiratoria Trastorno que se caracteriza por aumento primario de la paco2 con elevación de la concentración de H+ en sangre, disminución del ph y
Deberíamos ver hoy, terminar lo que estábamos viendo ayer y ver todo lo que es alcalosis. Algunas cosas de las que falto
 Clase 9 23/09/08 acidosis láctica y alcalosis Deberíamos ver hoy, terminar lo que estábamos viendo ayer y ver todo lo que es alcalosis. Algunas cosas de las que falto ACIDOSIS LACTICA HIPOXIA INSUF. HEPATICA
Clase 9 23/09/08 acidosis láctica y alcalosis Deberíamos ver hoy, terminar lo que estábamos viendo ayer y ver todo lo que es alcalosis. Algunas cosas de las que falto ACIDOSIS LACTICA HIPOXIA INSUF. HEPATICA
TEST APARATO RESPIRATORIO BIR 2015-2016
 1.- Cuál de los siguientes es el estímulo directo para las neuronas del área quimiosensible de la zona bulbar reguladora de la respiración?: 1. po 2. 2. pco 2. 3. CO 3 H 2. 4. CO 3 H -. 5. Concentración
1.- Cuál de los siguientes es el estímulo directo para las neuronas del área quimiosensible de la zona bulbar reguladora de la respiración?: 1. po 2. 2. pco 2. 3. CO 3 H 2. 4. CO 3 H -. 5. Concentración
Prospecto: información para el usuario. Bicarbonato Sódico 1/6 M Braun solución para perfusión Hidrogenocarbonato de sodio
 Prospecto: información para el usuario Bicarbonato Sódico 1/6 M Braun solución para perfusión Hidrogenocarbonato de sodio Lea todo el prospecto detenidamente antes de empezar a usar el medicamento - Conserve
Prospecto: información para el usuario Bicarbonato Sódico 1/6 M Braun solución para perfusión Hidrogenocarbonato de sodio Lea todo el prospecto detenidamente antes de empezar a usar el medicamento - Conserve
Ventilación Mecánica en el RN Cardiópata con Hiperflujo Pulmonar
 Ventilación Mecánica en el RN Cardiópata con Hiperflujo Pulmonar Dra. Ximena Alegría Palazón Profesor Adjunto Universidad de Valparaíso Unidad de Neonatología Hospital Carlos Van Buren VM Cardiopatías
Ventilación Mecánica en el RN Cardiópata con Hiperflujo Pulmonar Dra. Ximena Alegría Palazón Profesor Adjunto Universidad de Valparaíso Unidad de Neonatología Hospital Carlos Van Buren VM Cardiopatías
Equilibrio ácido-básico
 Equilibrio ácido-básico El mayor problema de salud con el que nos encontramos actualmente es la hiperacidificación crónica de nuestro organismo. La vida es el metabolismo. El metabolismo es la vida. Nuestro
Equilibrio ácido-básico El mayor problema de salud con el que nos encontramos actualmente es la hiperacidificación crónica de nuestro organismo. La vida es el metabolismo. El metabolismo es la vida. Nuestro
Equipo 5 Sistemas amortiguadores
 Equipo 5 Sistemas amortiguadores Anaya Gutiérrez Erick Jesús García García Esmira Jazmin García Montesinos Ana Paola Gonzales Galindo Jesús Antonio Jóse Ruíz Diego Mendez Silva Clara Anaid Yépez Cancino
Equipo 5 Sistemas amortiguadores Anaya Gutiérrez Erick Jesús García García Esmira Jazmin García Montesinos Ana Paola Gonzales Galindo Jesús Antonio Jóse Ruíz Diego Mendez Silva Clara Anaid Yépez Cancino
ACIDIFICANTES EN ALIMENTOS PARA GATOS
 ACIDIFICANTES EN ALIMENTOS PARA GATOS Flávia Maria de Oliveira Borges Saad Médica Veterinária, MSc., PhD Nutrição Animal Universidade Federal de Lavras - DZO - UFLA POR QUÉ UTILIZAR ACIDIFICANTES EN ALIMENTOS
ACIDIFICANTES EN ALIMENTOS PARA GATOS Flávia Maria de Oliveira Borges Saad Médica Veterinária, MSc., PhD Nutrição Animal Universidade Federal de Lavras - DZO - UFLA POR QUÉ UTILIZAR ACIDIFICANTES EN ALIMENTOS
Fisiología del evento ISQUEMIA / ANOXIA. Rodolfo A. Cabrales Vega MD Docente Programa de Medicina Universidad Tecnológica de Pereira
 Fisiología del evento ISQUEMIA / ANOXIA Rodolfo A. Cabrales Vega MD Docente Programa de Medicina Universidad Tecnológica de Pereira Porque cualquier miembro suelto, ya esté recubierto por piel o por carne,
Fisiología del evento ISQUEMIA / ANOXIA Rodolfo A. Cabrales Vega MD Docente Programa de Medicina Universidad Tecnológica de Pereira Porque cualquier miembro suelto, ya esté recubierto por piel o por carne,
Bioelementos y biomoléculas 1-Moleculas inorganicas Sales minerales. Verónica Pantoja. Lic. MSP.
 Bioelementos y biomoléculas 1-Moleculas inorganicas Sales minerales Professor: Kinesiologia Verónica Pantoja. Lic. MSP. 1.Precipitadas Formando estructuras sólidas, insolubles, con función esquelética.
Bioelementos y biomoléculas 1-Moleculas inorganicas Sales minerales Professor: Kinesiologia Verónica Pantoja. Lic. MSP. 1.Precipitadas Formando estructuras sólidas, insolubles, con función esquelética.
INTRODUCCION AL EQUILIBRIO ACIDO- BASE 22
 INTRODUCCION AL EQUILIBRIO ACIDO- BASE 22 Medio Interno Denominamos medio interno a los líquidos que rodean las células (líquidos intersticial e intravascular). Estos fluídos tienen la función proteger,
INTRODUCCION AL EQUILIBRIO ACIDO- BASE 22 Medio Interno Denominamos medio interno a los líquidos que rodean las células (líquidos intersticial e intravascular). Estos fluídos tienen la función proteger,
Fisiología renal Rafael Porcile. Universidad Abierta Interamericana
 Fisiología renal Rafael Porcile rafael.porcile@vaneduc.edu.ar D E P A R T A M E N T O D E C A R D I O L O G I A C A T E D R A D E F I S I O L O G Í A Universidad Abierta Interamericana rafael.porcile@vaneduc.edu.ar
Fisiología renal Rafael Porcile rafael.porcile@vaneduc.edu.ar D E P A R T A M E N T O D E C A R D I O L O G I A C A T E D R A D E F I S I O L O G Í A Universidad Abierta Interamericana rafael.porcile@vaneduc.edu.ar
TRASTORNOS MIXTOS DEL EQUILIBRIO ACIDO BASE
 TRASTORNOS MIXTOS DEL EQUILIBRIO ACIDO BASE El presente artículo es una actualización al mes de julio del 2006 del Capítulo del Dr. Carlos Lovesio, del Libro Medicina Intensiva, Dr. Carlos Lovesio, Editorial
TRASTORNOS MIXTOS DEL EQUILIBRIO ACIDO BASE El presente artículo es una actualización al mes de julio del 2006 del Capítulo del Dr. Carlos Lovesio, del Libro Medicina Intensiva, Dr. Carlos Lovesio, Editorial
Curso Superior de Medicina Intensiva y Cuidados Críticos Necochea, 2007-2009
 Trastornos del equilibrio ácido-base Introducción Las primeras definiciones contemporáneas de ácido y base pueden atribuirse a Arrhenius, quien en 1887 definió ácido como un donante de ion hidrógeno y
Trastornos del equilibrio ácido-base Introducción Las primeras definiciones contemporáneas de ácido y base pueden atribuirse a Arrhenius, quien en 1887 definió ácido como un donante de ion hidrógeno y
ANÁLISIS DUPLICIDAD TERAPÉUTICA SUBGRUPO C03-DIURÉTICOS
 ANÁLISIS DUPLICIDAD TERAPÉUTICA SUBGRUPO C03-DIURÉTICOS C03-. DIURÉTICOS Clasificación ATC C03A-. DIURÉTICOS DE BAJO TECHO, TIAZIDAS C03AA.Tiazidas solas C03AX.Tiazidas asociadas a otras sustancias concentrado
ANÁLISIS DUPLICIDAD TERAPÉUTICA SUBGRUPO C03-DIURÉTICOS C03-. DIURÉTICOS Clasificación ATC C03A-. DIURÉTICOS DE BAJO TECHO, TIAZIDAS C03AA.Tiazidas solas C03AX.Tiazidas asociadas a otras sustancias concentrado
COMPLICACIONES AGUDAS DE LA DIABETES MELLITUS
 COMPLICACIONES AGUDAS DE LA DIABETES MELLITUS Jornadas Inter-Hospitalarias Hospital Universitario La Paz Octubre 2005 EVA CASADO AMANDA OSPINA R4 DE BIOQUIMICA CLINICA COMPLICACIONES AGUDAS CETOACIDOSIS
COMPLICACIONES AGUDAS DE LA DIABETES MELLITUS Jornadas Inter-Hospitalarias Hospital Universitario La Paz Octubre 2005 EVA CASADO AMANDA OSPINA R4 DE BIOQUIMICA CLINICA COMPLICACIONES AGUDAS CETOACIDOSIS
TRASTORNOS DEL EQUILIBRIO ÁCIDO-BASE
 TRASTORNOS DEL EQUILIBRIO ÁCIDO-BASE AUTORES: MARIA JOSE RUIZ MARQUEZ CARMEN ORTIZ GARCIA JUAN JOSE SANCHEZ LUQUE ANA PEÑA AGÜERA LABORATORIO DEL HOSPITAL CLÍNICO UNIVERSITARIO VIRGEN DE LA VICTORIA DE
TRASTORNOS DEL EQUILIBRIO ÁCIDO-BASE AUTORES: MARIA JOSE RUIZ MARQUEZ CARMEN ORTIZ GARCIA JUAN JOSE SANCHEZ LUQUE ANA PEÑA AGÜERA LABORATORIO DEL HOSPITAL CLÍNICO UNIVERSITARIO VIRGEN DE LA VICTORIA DE
Tema 2. El agua, el ph y los equilibrios iónicos
 Tema 2. El agua, el ph y los equilibrios iónicos -Interacciones débiles en sistemas acuosos: puentes de hidrógeno, fuerzas de van der Waals e interacciones iónicas. -Enlaces hidrofóbicos. -Estructura y
Tema 2. El agua, el ph y los equilibrios iónicos -Interacciones débiles en sistemas acuosos: puentes de hidrógeno, fuerzas de van der Waals e interacciones iónicas. -Enlaces hidrofóbicos. -Estructura y
FICHA TÉCNICA CORREO ELECTRÓNICO C/ CAMPEZO, 1 EDIFICIO MADRID.
 FICHA TÉCNICA CORREO ELECTRÓNICO Sugerencias_ft@aemps.es C/ CAMPEZO, 1 EDIFICIO 8 28022 MADRID 1. NOMBRE DEL MEDICAMENTO Potasio Grifols 10 meq/500 ml en Salina Fisiológica solución para perfusión 2. COMPOSICIÓN
FICHA TÉCNICA CORREO ELECTRÓNICO Sugerencias_ft@aemps.es C/ CAMPEZO, 1 EDIFICIO 8 28022 MADRID 1. NOMBRE DEL MEDICAMENTO Potasio Grifols 10 meq/500 ml en Salina Fisiológica solución para perfusión 2. COMPOSICIÓN
INSUFICIENCIA RENAL AGUDA
 INSUFICIENCIA RENAL AGUDA La insuficiencia renal aguda es un síndrome clínico que se produce por una reducción brusca de la filtración glomerular con retención progresiva de productos nitrogenados en sangre
INSUFICIENCIA RENAL AGUDA La insuficiencia renal aguda es un síndrome clínico que se produce por una reducción brusca de la filtración glomerular con retención progresiva de productos nitrogenados en sangre
- FALTAN COLOCAR LAS REFERENCIAS BIBLIOGRÁFICAS DENTRO DEL TEXTO. - FAVOR TRADUCIR EL TÍTULO DE SU ARTÍCULO AL INGLÉS.
 Los desórdenes del equilibrio ácido-básico siempre son una complicación de alguna enfermedad de fondo. Una acidosis o alcalosis no existe por sí misma, sino que puede aparecer en el contexto de alguna
Los desórdenes del equilibrio ácido-básico siempre son una complicación de alguna enfermedad de fondo. Una acidosis o alcalosis no existe por sí misma, sino que puede aparecer en el contexto de alguna
ENFOQUE SISTEMÁTICO PARA LA INTERPRETACIÓN DE GASES SANGUÍNEOS EN LA PRÁCTICA CLÍNICA
 Capítulo V ENFOQUE SISTEMÁTICO PARA LA INTERPRETACIÓN DE GASES SANGUÍNEOS EN LA PRÁCTICA CLÍNICA INTRODUCCIÓN L a determinación que se conoce como GASES SANGUÍNEOS permite, por una parte, la valoración
Capítulo V ENFOQUE SISTEMÁTICO PARA LA INTERPRETACIÓN DE GASES SANGUÍNEOS EN LA PRÁCTICA CLÍNICA INTRODUCCIÓN L a determinación que se conoce como GASES SANGUÍNEOS permite, por una parte, la valoración
FISIOLOGIA MEDICINA FISIOLOGÍA DEL APARATO DIGESTIVO
 FISIOLOGIA MEDICINA FISIOLOGÍA DEL APARATO DIGESTIVO 2006 Ximena Páez TEMA 11 I. ABSORCIÓN AGUA Y ELECTROLITOS II. SECRECIÓN ELECTROLITOS III. ABSORCIÓN MINERALES, VIT HIDROSOLUBLES IV. MALABSORCIÓN I.
FISIOLOGIA MEDICINA FISIOLOGÍA DEL APARATO DIGESTIVO 2006 Ximena Páez TEMA 11 I. ABSORCIÓN AGUA Y ELECTROLITOS II. SECRECIÓN ELECTROLITOS III. ABSORCIÓN MINERALES, VIT HIDROSOLUBLES IV. MALABSORCIÓN I.
Acidosis metabólica en Medicina Intensiva
 Acidosis metabólica en Medicina Intensiva Curso Alteraciones nefrológicas y de medio interno en Medicina Intensiva Hospital Español - 20/11/14 Dr Jordán Tenzi - UMI Hospital Español Alteraciones metabólicas
Acidosis metabólica en Medicina Intensiva Curso Alteraciones nefrológicas y de medio interno en Medicina Intensiva Hospital Español - 20/11/14 Dr Jordán Tenzi - UMI Hospital Español Alteraciones metabólicas
ANALISIS DE DUPLICIDAD TERAPÉUTICA DEL SUBGRUPO A12 SUPLEMENTOS MINERALES
 ANALISIS DE TERAPÉUTICA DEL SUBGRUPO A12 SUPLEMENTOS MINERALES CLASIFICACIÓN ATC A12A CALCIO A12AA fosfato carbonato Complejo oseina-hidroxiapatita pidolato glubionato calcio carbonato A12AX asociado a
ANALISIS DE TERAPÉUTICA DEL SUBGRUPO A12 SUPLEMENTOS MINERALES CLASIFICACIÓN ATC A12A CALCIO A12AA fosfato carbonato Complejo oseina-hidroxiapatita pidolato glubionato calcio carbonato A12AX asociado a
Anatomía y Fisiología del Sistema Urinario y Escretor
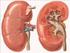 Anatomía y Fisiología del Sistema Urinario y Escretor La excreción Es el proceso biológico por el que un ser vivo elimina de su organismo las sustancias tóxicas, adquiridas por la alimentación o producidas
Anatomía y Fisiología del Sistema Urinario y Escretor La excreción Es el proceso biológico por el que un ser vivo elimina de su organismo las sustancias tóxicas, adquiridas por la alimentación o producidas
Trastornos Hidroelectrolíticos y Acidos Básicos en Diarrea Aguda
 Trastornos Hidroelectrolíticos y Acidos Básicos en Diarrea Aguda Dra. Mariana Bercovich Médico Jefe Unidad de Lactantes Hospital Luis Calvo Mackenna Los trastornos hidroelectrolíticos y ácido-básicos que
Trastornos Hidroelectrolíticos y Acidos Básicos en Diarrea Aguda Dra. Mariana Bercovich Médico Jefe Unidad de Lactantes Hospital Luis Calvo Mackenna Los trastornos hidroelectrolíticos y ácido-básicos que
Sección 26: Soluciones correctoras de los trastornos hidroelectrolíticos y del equilibrio ácido-base
 396 Sección 26: Soluciones correctoras de los trastornos hidroelectrolíticos y del equilibrio ácido-base 26.1 Soluciones electrolíticas orales...397 26.1.1 Rehidratación oral...397 26.1.2 Potasio oral...398
396 Sección 26: Soluciones correctoras de los trastornos hidroelectrolíticos y del equilibrio ácido-base 26.1 Soluciones electrolíticas orales...397 26.1.1 Rehidratación oral...397 26.1.2 Potasio oral...398
