NOCIONES ELEMENTALES DE MINERALES
|
|
|
- José Miguel Peña Serrano
- hace 7 años
- Vistas:
Transcripción
1 NOCIONES ELEMENTALES DE MINERALES ROCA Agregado de uno o más minerales Minerales: juntos, mezclados, pero reteniendo sus propiedades individuales formadas por más de un mineral, algunos minerales por sí solos en grandes cantidades. = rocas y minerales (Ej. calcita y caliza) 1
2 Caliza Roca = Mineral Onix Rocas monominerálicas (Ej. calcita y caliza) Calcita 2
3 Mineral Sólido inorgánico natural estructura interna definida y composición química específica. Formado de uno o más elementos unidos para formar un compuesto químico estable. Más de 100 elementos (algunos sólo de laboratorio). Algunos minerales formados por un solo elemento (Ej. Cu y Au y S) Elemento sustancia mínima que la materia se puede dividir y analizar por métodos químicos comunes. cada elemento es identificado por un símbolo. Ejemplos H (hidrógeno), Si (sílice). Muchos símbolos provienen del nombre del elemento en inglés. Otros tienen su raíz en otros idiomas: Fe: del latín ferrum Cu: del latín cuprum, que deriva del griego Kyprios (isla de Chipre, donde se explotaba Cu en la antigüedad) Na: del latín natrium 3
4 Estructura compuesto por una serie de átomos dispuestos ordenadamente y unidos químicamente forman una particular estructura cristalina. apilamiento ordenado de átomos se refleja en los cristales = objetos regularmente formados 4
5 ATOMOS Partículas más pequeñas de materia que retienen las características de un elemento. Cada átomo está formado por: un núcleo, que contiene protones muy densos y cargados positivamente (+) y neutrones, partículas igualmente densas y de carga neutral. electrones (en igual número que los protones), orbitando alrededor del núcleo, partículas de carga negativa que se mueven a tan gran velocidad que se visualizan como una nube en torno al núcleo. NUMERO ATOMICO Definido por el número de protones Ej. todos los átomos con 6 protones son de C, los de 8 son O. La carga positiva de los neutrones es equilibrada por la negativa de los electrones, == que los átomos son partículas eléctricamente neutrales El elemento más simple (H) está formado por un protón y 1 electrón, cada partícula más pesada va aumentando el número de p y e. El agregado de electrones sigue un cierto orden de niveles de energía más bajos a más altos. Los electrones de las capas exteriores se involucran en las uniones químicas. 5
6 TABLA PERIODICA DE LOS ELEMENTOS Uniones o vínculos químicos - cuando átomos de uno a más elementos se unen para formar un compuesto a través de fuerzas eléctricas y resultan de un cambio en la estructura electrónica de los átomos unidos. -la configuración electrónica de los átomos es importante para determinar la naturaleza y fortaleza de las uniones químicas. - La mayoría de los átomos tiene incompletas sus capas exteriores - en busca del equilibrio (sólo al estar completas) se combina para llegar a tener 8 electrones exteriores. - un átomo puede ganar, perder o compartir electrones con uno o más átomos. - Los electrones que se involucran en esta unión se llaman electrones de valencia y su número determina él # de uniones que formará (Ej. Si tiene 4, O 2 e H 1). 6
7 Unión iónica - uno o más electrones valencia se transfieren de un átomo a otro para ambos tener una capa externa completa. - Ej. NaCl, Na pierde su único electrón de la capa externa y Cl lo agrega a la suya. Ya no son átomos electrónicamente neutros ya que ninguno tiene electrones = protones. - átomos conocidos como iones - Ión: átomo con carga desigual debido a la pérdida o ganancia de electrones (Los átomos son eléctricamente neutros). Na se hace + y Cl -. - La unión iónica resulta de la atracción de estos átomos de cargas opuestas; aquella en que iones con cargas opuestas se atraen para formar un compuesto químico neutral. Nota: las propiedades de un compuesto químico son dramáticamente diferentes de las de los elementos que las compones Ej. Cl es venenoso, Na metal reactivo que puede quemar Unión covalente No todos los átomos se combinan formando iones. En algunos elementos se comparten los electrones exteriores para adquirir el arreglo estable de los gases nobles. La Si rápidamente forma uniones covalentes con O para original los silicatos. Unión metálica La mayor parte de las uniones químicas son una combinación de ambas. caso extremo de compartir la electricidad es el de la donde los electrones se mueven libremente de un átomo a otro lo que explica la conductividad de los metales y su facilidad para ser manipulados (reshaped) 7
8 Masa Atómica Las partículas subatómicas como protones y electrones requieren una unidad especial de medición: unidad de masa atómica. El número de masa de un átomo se obtiene de sumar los neutrones+protones. Como átomos de un mismo elemento pueden tener distintos números de neutrones, y en consecuencia distinto números de masa. Estos átomos se conocen como isótopos de ese elemento. Ej. C 12 y 14. Las masas atómicas promedio se conocen como peso atómico. En el caso del carbón es cercano a 12 porque 12 es el isótopo más común. Masa Atómica Aunque la mayor parte de los elementos son estables, hay isótopos inestables que se desintegran naturalmente: radioactividad. Ocurre cuando las fuerzas que unen al núcleo no son suficientes. La tasa a que estos se desintegran (decaen) es medible y se utiliza en geocronología: vida media. 8
9 ESTRUCTURA DE LOS MINERALES Mineral compuesto por un arreglo ordenado de átomos químicamente unidos para formar una particular estructura cristalina. el orden se refleja en los objetos de formas regulares que denominamos cristales. Qué determina la particular forma cristaliza de un mineral? - En caso de estar formado por iones, el arreglo atómico interno es determinado en parte por la carga de los iones, pero más por el tamaño de los iones involucrados. Para establecer compuestos iónicos estables cada ion positivo (+) será rodeado por el mayor número de iones negativos (-) que puedan acomodar mientras mantenga la neutralidad eléctrica. ESTRUCTURA DE LOS MINERALES 9
10 Polimorfos - Aunque cada mineral tiene una estructura interna particular, algunos elementos pueden - ordenarse en más de una forma y dar origen a dos minerales químicamente idénticos y con distintas propiedades -Ej.- Grafito (hojas de átomos de C ampliamente espaciados y débilmente unidos fácilmente deslizables, excelente lubricante. Diamante 200 Km > P, estructura muy compacta. Propiedades físicas de los minerales 1. Forma cristalina 2. Lustre o brillo 3. Color 4. Raya 5. Dureza 6. Clivaje o exfoliación 7. Fractura 8. Peso específico 10
11 FORMA CRISTALINA cristales no son escasos aunque no se ven normalmente. Forma cristalina es la expresión externa de un mineral y refleja el ordenamiento interno de los átomos. FORMA CRISTALINA Sólo se desarrollará si no tiene restricciones de espacio y tiempo al momento de formarse. Lo más común es que el crecimiento de un cristal se interrumpa por competencia de espacio 11
12 apariencia o cualidad de como se refleja la luz en la superficie de un mineral. Minerales con apariencia metálica independientemente del color----> lustre metálico. no metálicos: vítreo, perlado, sedoso, resinoso y terroso (opaco) LUSTRE 12
13 COLOR obvio, no confiable, muchas variaciones Ej. Cuarzo, otros como S, siempre amarillos 13
14 RAYA color de un mineral cuando está molido. Requiere una placa de porcelana. Varía menos que el color externo. Los minerales metálicos en general tienen raya oscura y densa y los no metálicos no Dureza Mineral Equivalente diario DUREZA resistencia de un mineral a la abrasión y a ser rayado. Propiedad relativa que se determina rayando el mineral de dureza desconocida con uno de dureza conocida o vice versa. Un valor numérico se obtiene de la "Escala de Dureza de Mohs": minerales arreglados en orden creciente de dureza (1-10) Talco Yeso Calcita Fluorita Apatito Ortoclasa Cuarzo Topacio Polvo de talco el más blando Uñas del dedo Moneda de bronce Clavo de hierro vidrio Cortaplumas Cuchillo de acero Papel abrasivo eccionar/dureza_escala_de_mohs.ht m 9 Corindón Rubí 10 Diamante Diamante sintético El más duro 14
15 DUREZA La escala la desarrolló Friedrich Mohs, hace aproximadamente 200 años. Los minerales más suaves tienen números bajos, y los más duros, números elevados. Ejemplos Uña = 2,5; moneda de Cu = 3; Vidrio = 5,5. El yeso (2) se raya con la uña, calcita raya mi uña, pero no al cuarzo y cuarzo raya vidrio Clivaje: - tendencia de un mineral a romperse a lo largo de planos de debilidad--->superficies suaves. -va de bien, ha débilmente desarrollado a ausente; -distinto de forma cristalina, -cuando se rompe forma pedazos igual al original, el cz no tiene clivaje 15
16 Superficies lisas producidas cuando se rompe un mineral a lo largo de los planos de debilidad (clivaje) A la izquierda, fluorita con 4 planos de clivaje (8 lados) Al centro, halita, con tres planos de clivaje a 90 A la derecha, calcita, con 3 planos de clivaje en 75 Clivaje hojoso, característico de las micas FRACTURA cuando un mineral no tiene clivaje, al romperse muestra una fractura. Los que se rompen desarrollando curvas suaves concoidal; otros en astillas o fibras, pero la mayoría irregularmente 16
17 Gravedad o peso específico razón del peso del mineral al peso de un volumen idéntico de agua Ejemplo: si un mineral pesa 3 veces un volumen igual de agua su peso específico es 3 Los minerales metálicos en general tienen un alto peso específico La galena (PbS): 7,5 Oro de 24 kilates: 20 Grupos de minerales > 2000 conocidos, otros por conocerse 2 docenas son los más abundantes, forman mayoritariamente la corteza terrestre y se clasifican como los minerales formadores de rocas. compuestos mayoritariamente por sólo 8 elementos los que a su vez forman el 98% Elemento Oxígeno Sílice Aluminio Hierro Calcio Sodio Potasio Símbolo Magnesio Mg 2,1 corteza; Otros 1,7 O Si Al Fe Ca Na P % en peso 46,6 27,7 8,1 5 3,6 2,8 2,6 17
18 Grupos de minerales Si y O se combinan para formar el marco o esqueleto de los minerales más comunes --> silicatos = Si + O + 1 o más elementos (- SiO2). Siguiente grupo más común carbonatos donde la calcita es el más prominente. También son comunes la sal y el yeso Grupos de minerales Otros minerales son valorados por su valor económico, en especial el grupo de metales: Fe, Zn, Pb, nativos: Au, Ag y C, fluorita, etc. 18
19 LOS SILICATOS Todos formados por el mismo ladrillo fundamental el tetraedro de Si y O Tetrahedro de sílice. 4 átomos de O que rodean a uno mucho más pequeño de Si ubicado en el espacio entre ellos En la figura inferior las varillas muestran los enlaces que conectan los iones LOS SILICATOS Todos formados por el mismo ladrillo fundamental el tetraedro de Si y O Compuesto inestable, corresponde a un ion complejo cargado con 4- (cada O aporta 2- y Si aporta 4+). En la naturaleza, la forma más sencilla de neutralizar este tetraedro es con la adición de iones cargados +. Así es como se origina una estructura químicamente estable formada por tetraedros individuales unidos * Los tetraedros se pueden unir en una variedad de configuraciones (cadenas simples...etc.). La unión de tetraedros en cada una de estas configuraciones resulta de compartir los átomos de O por pares de átomos de Si * Dependiendo de la forma en que se unan los tetraedros se obtienen distintas razones O/Si (4 a 1 a 2 a 1) ==> mientras más O se comporten ==> mayor porcentaje de Si en la estructura. Por lo tanto los silicatos se describen como de alto o bajo Si dependiendo de este radio. * Tamaño relativo y cargas eléctricas de los iones de los 8 elementos de más comunes en la corteza y formadores de minerales de roca 19
20 LOS SILICATOS Todos formados por el mismo ladrillo fundamental el tetraedro de Si y O * Estas estructuras silicatadas no son compuestos químicos neutros en si mismas, por lo tanto son neutralizadas por la inclusión de iones metálicos cargados que las unen en una variedad de formas cristalinas. * Los iones más comunes son: Fe, Mg, K, Na, Al y Ca, cada uno con una particular carga y tamaño atómico. Los de tamaño similar se pueden sustituir fácilmente (Ej. Fe+2 y Mg+2); Ca y Na; Si y Al sin alterar la estructura mineral==> que debido a esta habilidad de acomodar distintos iones, un mineral puede variar en el contenido de ciertos elementos. Por esta razón se expresan en una fórmula química con los elementos variables dentro de ( ). Ejemplo; olivino (Fe, Mg)2 SiO4 = familia de minerales con un rango de composisiones entre dos miembros extremos. * Cuando la sustitución de iones ==> distinta carga (ej. Ca2+ --> Na1+) ==> que para mantener la estabilidad Al3+ es reemplazado por Si4+ ==> doble sustitución. Ocurre con los Feldespatos que son muy abundantes en la corteza. Tamaño relativo y cargas eléctricas de los iones de los 8 elementos de más comunes en la corteza y formadores de minerales de roca 20
21 LOS SILICATOS aprox. 50% minerales de corteza, sílice 2º Cada grupo caracterizado por estructura particular estructura. Se forman cuando se enfría la roca fundida (magma). el ambiente de cristalización y la composición del magma define los minerales que se forman (indican condiciones de formación) Ferromagnesianos (con Fe o Mg; oscuros, gravedad específica: 3,2-3,6) No ferromagnesianos (sin Fe, Mg; claros, gravedad específica: 2,7). FERROMAGNESIANOS Olivino Piroxeno Hornblendas Biotita Granate Olivino: Alta Tº, negro, verde oliva, lustre vítreo y fractura concoidal, cristales chicos y redondeados; de apariencia granular; tetraedros unidos por una mezcla de iones de Fe y Mg que origina una red en 3 dimensiones sin uniones débiles==> sin clivaje. 21
22 Piroxeno: Negro opaco, 2 planos de clivaje a 90º; prismáticos. Cadenas simples de tetraedros unidas por iones de Fe y Mg; con clivajes paralelos a las cadenas de silicatos Hornblenda: Anfíbola más común; complejo; verde oscuro a negro, similar al piroxeno; clivaje en 60º y 120º; elongados. Formada por cadenas dobles de tetraedros 22
23 Biotita: miembro férrico de las micas; estructura hojosa que origina buen clivaje en una dirección; negro, brillante. Granate: similar al olivino, lustre vítreo, sin clivaje, concoidal café a burdeos o rojo oscuro, cristales equidimensionales, los traslúcido se usan como gemas No Ferromagnesianos Muscovita Feldespato Plagioclasa Feldespato potásico Cuarzo Arcillas Muscovita: Familia de las micas, clara, lustre perlado, buen clivaje. 23
24 Feldespato: El más común de los silicatos, formado en gran variedades y temperatura y P; todos con propiedades físicas similares, clivaje a 90º, duros (6), lustre vítreo a perlado, forma rectangular y caras lisas y brillantes. Estructura tridimensional que se forma cuando átomos de oxígeno son compartidos por el próximo átomo de Si. ¼ de los átomos de Si están reemplazados por Al. Formado por Si, Al, O además de iones K(+1), Na(+1) y Ca (+2). Porque el ion K es más grande que los de Ca y Na, forman dos tipos diferentes de estructuras de feldespato: ortoclasas (K) y plagioclasas donde Na y Ca son libremente sustituibles. Plagioclasas y anfíbolas en 2 rocas igneas 24
25 Cuarzo: Solo Si y O, sílice (SiO2); estructura tridimensional, mediante la total compartición de los oxígenos por los Si de al lado; fuerte unión de los átomos Si-O duro, resistente a la erosión y sin clivaje; fractura concoidal, cristales hexagonales con formas piramidales, translúcido o coloreado ARCILLA minerales complejos con estructura hojosa, grano muy fino (solo se ve microscópicamente) resultan de meteorización química de otros silicatos forman los suelos; muy importantes como minerales industriales; Ej. caolinita (porcelana), higroscópico, espesantes 25
26 MINERALES NO SILICATADOS Escasos, pero de gran importancia económica Óxidos e Hidróxidos minerales en los que el oxígeno forma enlaces con los metales: sólo oxígeno en el caso de los óxidos, y oxígeno con hidrógeno (OH-) en los hidróxidos. Comprenden unos 250 minerales: Carbonatos: Estructura simple, calcita (CaCO 3 ) y dolomita CaMg (CO 3 ) 2 ; lustre vítreo, dureza 3-4, clivaje rómbico; calcita reacciona con ácido clorhídrico; dolomita sólo cuando molida; forman calizas y dolomitas (tipos de rocas sedimentarias). Halita y Yeso: capas de antiguos océanos y salares Recursos Minerales: Dependen del uso, las menas recursos, % y explotabilidad. 26
Suelos formados por viento (Loess)
 Suelos formados por viento (Loess) Procesos generales de formación de los suelos (continuación). Los elementos más facilmente lixiviables son las sales (carbonatos, cloruros, sulfatos, nitratos, bicarbonatos).
Suelos formados por viento (Loess) Procesos generales de formación de los suelos (continuación). Los elementos más facilmente lixiviables son las sales (carbonatos, cloruros, sulfatos, nitratos, bicarbonatos).
Capítulo 2: Los Minerales. Geología Física
 Capítulo 2: Los Minerales Geología Física La materia y su composición TODO lo que tenga masa y ocupe espacio es materia La materia se presenta en uno de tres estados o fases, todos ellos importantes para
Capítulo 2: Los Minerales Geología Física La materia y su composición TODO lo que tenga masa y ocupe espacio es materia La materia se presenta en uno de tres estados o fases, todos ellos importantes para
MINERALOGÍA Profesora: Priscilla Guzmán C.
 MINERALOGÍA Profesora: Priscilla Guzmán C. Habilidades Conocimiento. Comprensión. Aplicación. Contenidos Definición de mineral. Propiedades físicas y químicas de los minerales. Definición de roca y clasificación.
MINERALOGÍA Profesora: Priscilla Guzmán C. Habilidades Conocimiento. Comprensión. Aplicación. Contenidos Definición de mineral. Propiedades físicas y químicas de los minerales. Definición de roca y clasificación.
5ª UNIDAD ELEMENTOS Y COMPUESTOS
 5ª UNIDAD ELEMENTOS Y COMPUESTOS 3º E.S.O. Grupo Apellidos: Nombre: INTRODUCCIÓN Comenzamos recordando los conceptos más importantes del tema anterior: Cómo son los átomos? Cómo están distribuidos los
5ª UNIDAD ELEMENTOS Y COMPUESTOS 3º E.S.O. Grupo Apellidos: Nombre: INTRODUCCIÓN Comenzamos recordando los conceptos más importantes del tema anterior: Cómo son los átomos? Cómo están distribuidos los
Sistemática de minerales. 2. Silicatos
 Sistemática de minerales 2. Silicatos Silicatos Enlace Si-O Geometría: tetraedros Estabilidad máxima Posibilidad polimerización Grupos de Silicatos Nesosilicatos [SiO4] -4 Grupos de Silicatos Sorosilicatos
Sistemática de minerales 2. Silicatos Silicatos Enlace Si-O Geometría: tetraedros Estabilidad máxima Posibilidad polimerización Grupos de Silicatos Nesosilicatos [SiO4] -4 Grupos de Silicatos Sorosilicatos
FÍSICA Y QUÍMICA - 3º ESO ESTRUCTURA ATOMICA Y ENLACE 2
 FÍSICA Y QUÍMICA - 3º ESO ESTRUCTURA ATOMICA Y ENLACE 2 1. Define y explica los siguientes conceptos: número atómico, número másico e isótopos de un elemento químico. 2. Copia el siguiente párrafo y complétalo:
FÍSICA Y QUÍMICA - 3º ESO ESTRUCTURA ATOMICA Y ENLACE 2 1. Define y explica los siguientes conceptos: número atómico, número másico e isótopos de un elemento químico. 2. Copia el siguiente párrafo y complétalo:
Los minerales son sustancias químicas y como tales, tienen una composición
 4.2. MINERALES. Los minerales son sustancias químicas y como tales, tienen una composición química fija. Están formados siempre por los mismos elementos y en la misma proporción. Los minerales siempre
4.2. MINERALES. Los minerales son sustancias químicas y como tales, tienen una composición química fija. Están formados siempre por los mismos elementos y en la misma proporción. Los minerales siempre
FÍSICA Y QUÍMICA Solucionario ELECTRONES Y ENLACES
 FÍSICA Y QUÍMICA Solucionario ELECTRONES Y ENLACES 1.* Indicad cuántos electrones tienen en la última capa cada uno de estos elementos. a) C 4 f) O 6 k) K 1 b) F 7 g) P 5 l) S 6 c) Ne 8 h) H 1 m) He 8
FÍSICA Y QUÍMICA Solucionario ELECTRONES Y ENLACES 1.* Indicad cuántos electrones tienen en la última capa cada uno de estos elementos. a) C 4 f) O 6 k) K 1 b) F 7 g) P 5 l) S 6 c) Ne 8 h) H 1 m) He 8
Los elementos químicos
 Los elementos químicos Física y Química Las primeras clasificaciones de los elementos Oxford University Press España, S. A. Física y Química 3º ESO 2 Un elemento químico es un tipo de materia constituido
Los elementos químicos Física y Química Las primeras clasificaciones de los elementos Oxford University Press España, S. A. Física y Química 3º ESO 2 Un elemento químico es un tipo de materia constituido
Minerales: Clasificación y Propiedades de los Minerales. Hernán Santos, Ph.D. Departamento de Geología Recinto Universitario de Mayagüez
 Minerales: Clasificación y Propiedades de los Minerales Hernán Santos, Ph.D. Departamento de Geología Recinto Universitario de Mayagüez 1 Qué es un Mineral? Un mineral es un sólido inorgánico que ocurre
Minerales: Clasificación y Propiedades de los Minerales Hernán Santos, Ph.D. Departamento de Geología Recinto Universitario de Mayagüez 1 Qué es un Mineral? Un mineral es un sólido inorgánico que ocurre
GUÍA PARA EXAMEN DE REGULARIZACIÓN DE QUÍMICA 1
 GUÍA PARA EXAMEN DE REGULARIZACIÓN DE QUÍMICA 1 1.- Ciencia que estudia la composición, estructura de la materia y sus transformaciones. R= Química 2.-Es todo lo que tiene masa y posee inercia R= Materia
GUÍA PARA EXAMEN DE REGULARIZACIÓN DE QUÍMICA 1 1.- Ciencia que estudia la composición, estructura de la materia y sus transformaciones. R= Química 2.-Es todo lo que tiene masa y posee inercia R= Materia
UNIDAD 10.- LAS UNIONES ENTRE ÁTOMOS. Cuestiones de evaluación inicial. 2.- Cuántos protones y cuantos neutrones tiene el Carbono?
 UNIDAD 10.- LAS UNIONES ENTRE ÁTOMOS Cuestiones de evaluación inicial 1.- Cuántos elementos químicos conoces? 2.- Cuántos protones y cuantos neutrones tiene el Carbono? 3.- Qué es el sistema periódico?
UNIDAD 10.- LAS UNIONES ENTRE ÁTOMOS Cuestiones de evaluación inicial 1.- Cuántos elementos químicos conoces? 2.- Cuántos protones y cuantos neutrones tiene el Carbono? 3.- Qué es el sistema periódico?
Tema 5: El átomo y sus uniones.
 Tema 5: El átomo y sus uniones. 1. Teoría Atómica de Dalton. En 1803, John Dalton expone su Teoría Atómica que se basa en los siguientes puntos: Los elementos químicos están formados por partículas muy
Tema 5: El átomo y sus uniones. 1. Teoría Atómica de Dalton. En 1803, John Dalton expone su Teoría Atómica que se basa en los siguientes puntos: Los elementos químicos están formados por partículas muy
TEMA 8 SISTEMA PERIÓDICO Y ENLACES
 TEMA 8 SISTEMA PERIÓDICO Y ENLACES 1. LA TABLA PERIÓDICA Elementos químicos son el conjunto de átomos que tienen en común su número atómico, Z. Hoy conocemos 111 elementos diferentes. Los elementos que
TEMA 8 SISTEMA PERIÓDICO Y ENLACES 1. LA TABLA PERIÓDICA Elementos químicos son el conjunto de átomos que tienen en común su número atómico, Z. Hoy conocemos 111 elementos diferentes. Los elementos que
LA CORTEZA TERRESTRE
 LA CORTEZA TERRESTRE La corteza es la capa superficial sólida de la geosfera, es una capa muy delgada, pues su espesor oscila entre los 60 km en los continentes y los 7 km en los fondos oceánicos. Tipos
LA CORTEZA TERRESTRE La corteza es la capa superficial sólida de la geosfera, es una capa muy delgada, pues su espesor oscila entre los 60 km en los continentes y los 7 km en los fondos oceánicos. Tipos
Una mezcla es un compuesto formado por varias sustancias con distintas propiedades
 COMPOSICIÓN DE LA MATERIA Mezclas homogéneas y heterogéneas Una mezcla es un compuesto formado por varias sustancias con distintas propiedades Algunos sistemas materiales como la leche a simple vista parecen
COMPOSICIÓN DE LA MATERIA Mezclas homogéneas y heterogéneas Una mezcla es un compuesto formado por varias sustancias con distintas propiedades Algunos sistemas materiales como la leche a simple vista parecen
ByG 1º Bto. Tema 2 Los materiales terrestres: minerales.
 ByG 1º Bto. Tema 2 Los materiales terrestres: minerales. 1. Los cristales. El ser humano siempre se ha sentido atraído por los colores, el brillo y la forma de los cristales que aparecen en las rocas.
ByG 1º Bto. Tema 2 Los materiales terrestres: minerales. 1. Los cristales. El ser humano siempre se ha sentido atraído por los colores, el brillo y la forma de los cristales que aparecen en las rocas.
PROPIEDADES FÍSICAS DE LOS MINERALES
 PROPIEDADES FÍSICAS DE LOS MINERALES INTRODUCCIÓN La identificación de un mineral, basándose en la estructura interna y la composición química, es difícil sin la ayuda de ensayos y aparatos sofisticados.
PROPIEDADES FÍSICAS DE LOS MINERALES INTRODUCCIÓN La identificación de un mineral, basándose en la estructura interna y la composición química, es difícil sin la ayuda de ensayos y aparatos sofisticados.
La geosfera. Biología y Geología 1.º ESO
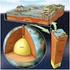 La geosfera Biología y Geología 1.º ESO El origen del universo Acreción de planetesimales Diferenciación por densidades Biología y Geología 1.º ESO 2 Las capas de la geosfera Corteza continental Más de
La geosfera Biología y Geología 1.º ESO El origen del universo Acreción de planetesimales Diferenciación por densidades Biología y Geología 1.º ESO 2 Las capas de la geosfera Corteza continental Más de
Unidad I: Propiedades Periódicas: Masa y Enlace
 Unidad I: Propiedades Periódicas: Masa y Enlace 1. Nociones de teoría atómica moderna 2. Propiedades periódicas de los elementos 3. Enlace iónico y covalente 4. Masas atómicas y moleculares 1. Nociones
Unidad I: Propiedades Periódicas: Masa y Enlace 1. Nociones de teoría atómica moderna 2. Propiedades periódicas de los elementos 3. Enlace iónico y covalente 4. Masas atómicas y moleculares 1. Nociones
ENLACES QUÍMICOS. Los enlaces químicos, son las fuerzas que mantienen unidos a los átomos.
 1. Generalidades de los enlaces químicos ENLACES QUÍMICOS Los enlaces químicos, son las fuerzas que mantienen unidos a los átomos. Cuando los átomos se enlazan entre sí, ceden, aceptan o comparten electrones.
1. Generalidades de los enlaces químicos ENLACES QUÍMICOS Los enlaces químicos, son las fuerzas que mantienen unidos a los átomos. Cuando los átomos se enlazan entre sí, ceden, aceptan o comparten electrones.
Las que tienen relación con el de tamaño: LAS PROPIEDADES PERIÓDICAS. Se pueden separar en dos grupos: PERIODICIDAD
 LAS PROPIEDADES PERIÓDICAS Se pueden separar en dos grupos: 1- Las que tienen relación con el de tamaño: Los radios atómicos y los radios iónicos o cristalinos. La densidad. (ρ) El punto de fusión y ebullición.
LAS PROPIEDADES PERIÓDICAS Se pueden separar en dos grupos: 1- Las que tienen relación con el de tamaño: Los radios atómicos y los radios iónicos o cristalinos. La densidad. (ρ) El punto de fusión y ebullición.
La geosfera. La geosfera. Biología y Geología 1.º ESO
 La geosfera Biología y Geología 1.º ESO El origen del universo Acreción de planetesimales Diferenciación por densidades Oxford University Press España, S. A. Biología y Geología 1.º ESO 2 Las capas de
La geosfera Biología y Geología 1.º ESO El origen del universo Acreción de planetesimales Diferenciación por densidades Oxford University Press España, S. A. Biología y Geología 1.º ESO 2 Las capas de
FÍSICA Y QUÍMICA 3º ESO ACTIVIDADES DE RECUPERACIÓN
 FÍSICA Y QUÍMICA 3º ESO ACTIVIDADES DE RECUPERACIÓN (PARTE 2) CURSO 2012/13 Nombre y apellidos: 1 LA CIENCIA Y SU MÉTODO. MEDIDA DE MAGNITUDES LOS ÁTOMOS Y SU COMPLEJIDAD 1. Qué explica el modelo atómico
FÍSICA Y QUÍMICA 3º ESO ACTIVIDADES DE RECUPERACIÓN (PARTE 2) CURSO 2012/13 Nombre y apellidos: 1 LA CIENCIA Y SU MÉTODO. MEDIDA DE MAGNITUDES LOS ÁTOMOS Y SU COMPLEJIDAD 1. Qué explica el modelo atómico
b) La zona externa del átomo se llama CORTEZA. y ahí es donde se mueven los ELECTRONES
 PREGUNTAS DE RESPUESTA BREVE 1. Completa las siguientes frases relativas a los átomos de los elementos: a) La parte del átomo en donde se puede considerar que se concentra toda su masa es el NÚCLEO y ahí
PREGUNTAS DE RESPUESTA BREVE 1. Completa las siguientes frases relativas a los átomos de los elementos: a) La parte del átomo en donde se puede considerar que se concentra toda su masa es el NÚCLEO y ahí
La materia mineral. Entre los grupos de minerales más presentes en la tierra podemos mencionar los siguientes.
 La materia mineral Un mineral es una materia generalmente inorgánica la cual es definida por su composición química constante y la disposición definida desus átomos. Cada especie de mineral se compone
La materia mineral Un mineral es una materia generalmente inorgánica la cual es definida por su composición química constante y la disposición definida desus átomos. Cada especie de mineral se compone
UNIDAD 1: LA MATERIA CRISTALINA
 UNIDAD 1: LA MATERIA CRISTALINA CONCEPTOS MATERIA CRISTALINA: Aquella cuyas partículas están perfectamente ordenadas en el espacio, ocupando posiciones fijas y a distancias regulares unas de otras, formando
UNIDAD 1: LA MATERIA CRISTALINA CONCEPTOS MATERIA CRISTALINA: Aquella cuyas partículas están perfectamente ordenadas en el espacio, ocupando posiciones fijas y a distancias regulares unas de otras, formando
A su vez, una molécula está compuesta por átomos. Cada uno de ellos posee unas propiedades diferentes en el interior de la molécula que constituyen.
 Constitución de la materia. Supongamos que cualquier sustancia de la naturaleza la dividimos en partes cada vez más pequeñas, conservando cada una de ellas las propiedades de la sustancia inicial. Si seguimos
Constitución de la materia. Supongamos que cualquier sustancia de la naturaleza la dividimos en partes cada vez más pequeñas, conservando cada una de ellas las propiedades de la sustancia inicial. Si seguimos
PORTAFOLIO DE EVIDENCIAS QUÍMICA I DE SEGUNDA OPORTUNIDAD I LEE DETENIDAMENTE CADA ENUNCIADO Y CONTESTA SEGÚN SE TE PIDA.
 PORTAFOLIO DE EVIDENCIAS QUÍMICA I DE SEGUNDA OPORTUNIDAD I LEE DETENIDAMENTE CADA ENUNCIADO Y CONTESTA SEGÚN SE TE PIDA. 1.- Ciencia que estudia las características y la composición de los materiales,
PORTAFOLIO DE EVIDENCIAS QUÍMICA I DE SEGUNDA OPORTUNIDAD I LEE DETENIDAMENTE CADA ENUNCIADO Y CONTESTA SEGÚN SE TE PIDA. 1.- Ciencia que estudia las características y la composición de los materiales,
Propiedades Físicas de los Minerales
 Propiedades Físicas de los Minerales Mineralogía y Petrografía. Semestre Otoño 2015 Tatiana Ordenes Cataldo tatiordenes@gmail.com Departamento de Ingeniería en Minas. Facultad de Ingeniería. Universidad
Propiedades Físicas de los Minerales Mineralogía y Petrografía. Semestre Otoño 2015 Tatiana Ordenes Cataldo tatiordenes@gmail.com Departamento de Ingeniería en Minas. Facultad de Ingeniería. Universidad
MINERALES Y ROCAS PROCESOS DE FORMACIÓN ROCAS ÍGNEAS
 II Unidad MINERALES Y ROCAS PROCESOS DE FORMACIÓN ROCAS ÍGNEAS Carla Navea G. Magma Es un material móvil, caliente, constituido por fases sólidas, gaseosas y liquidas, es decir, es un sistema multicomponente,
II Unidad MINERALES Y ROCAS PROCESOS DE FORMACIÓN ROCAS ÍGNEAS Carla Navea G. Magma Es un material móvil, caliente, constituido por fases sólidas, gaseosas y liquidas, es decir, es un sistema multicomponente,
OBJETIVO.- Diferenciar los distintos tipos de enlace químico para establecer las propiedades de cada compuesto.
 OBJETIVO.- Diferenciar los distintos tipos de enlace químico para establecer las propiedades de cada compuesto. 1. Generalidades de los enlaces químicos Los enlaces químicos, son las fuerzas que mantienen
OBJETIVO.- Diferenciar los distintos tipos de enlace químico para establecer las propiedades de cada compuesto. 1. Generalidades de los enlaces químicos Los enlaces químicos, son las fuerzas que mantienen
Ciencias del Mar. Meteorización de las Rocas. Oceanografía Química. Meteorización de las rocas
 Ciencias del Mar Meteorización de las Rocas Oceanografía Química Meteorización de las rocas La meteorización es el proceso de transformaciones físicas y químicas de las rocas parentales y minerales primarios
Ciencias del Mar Meteorización de las Rocas Oceanografía Química Meteorización de las rocas La meteorización es el proceso de transformaciones físicas y químicas de las rocas parentales y minerales primarios
TEMA 17. LOS MINERALES
 TEMA 17. LOS MINERALES Lee atentamente. 1. LOS MINERALES: MATERIA AMORFA Y MATERIA CRISTALINA La capa más externa de la Tierra se llama Litosfera. Los elementos químicos que forman parte de la Tierra reciben
TEMA 17. LOS MINERALES Lee atentamente. 1. LOS MINERALES: MATERIA AMORFA Y MATERIA CRISTALINA La capa más externa de la Tierra se llama Litosfera. Los elementos químicos que forman parte de la Tierra reciben
UNIDAD 3. MODIFICACIÓN DE LAS PROPIEDADES DE LOS METALES
 UNIDAD 3. MODIFICACIÓN DE LAS PROPIEDADES DE LOS METALES 1. GENERALIDADES... Pág. 49 2. ESTRUCTURA INTERNA DE LOS METALES... Pág. 49 2.1. Estructuras cristalinas... Pág. 49 2.2. Estructura cristalina cúbica
UNIDAD 3. MODIFICACIÓN DE LAS PROPIEDADES DE LOS METALES 1. GENERALIDADES... Pág. 49 2. ESTRUCTURA INTERNA DE LOS METALES... Pág. 49 2.1. Estructuras cristalinas... Pág. 49 2.2. Estructura cristalina cúbica
LA LA ESTRUCTURA DE LA MATERIA. 1.-Desarrollo histórico del concepto de átomo. Teoría de Demócrito. Teoría de Dalton. Componentes del átomo
 ANEXO AL TEMA 4 LA LA ESTRUCTURA DE LA MATERIA 1.-Desarrollo histórico del concepto de átomo Teoría de Demócrito Teoría de Dalton Modelo actual Componentes del átomo Concepto de ión 2.-Elememtos y compuestos
ANEXO AL TEMA 4 LA LA ESTRUCTURA DE LA MATERIA 1.-Desarrollo histórico del concepto de átomo Teoría de Demócrito Teoría de Dalton Modelo actual Componentes del átomo Concepto de ión 2.-Elememtos y compuestos
ESTRUCTURA ATÓMICA DE LA MATERIA. SISTEMA PERIÓDICO ESTRUCTURA ATÓMICA DE LA MATERIA
 ESTRUCTURA ATÓMICA DE LA MATERIA. SISTEMA PERIÓDICO ESTRUCTURA ATÓMICA DE LA MATERIA La teoría atómica de Dalton se mantuvo con éxito durante casi un siglo pero tuvo que ser abandonada a partir del descubrimiento
ESTRUCTURA ATÓMICA DE LA MATERIA. SISTEMA PERIÓDICO ESTRUCTURA ATÓMICA DE LA MATERIA La teoría atómica de Dalton se mantuvo con éxito durante casi un siglo pero tuvo que ser abandonada a partir del descubrimiento
1. Los elementos químicos
 RESUMEN de la UNIDAD 3. ELEMENTOS Y COMPUESTOS 1. Los elementos químicos La materia está formada por partículas denominadas átomos que, a su vez, están formados por otras partículas más pequeñas: protones,
RESUMEN de la UNIDAD 3. ELEMENTOS Y COMPUESTOS 1. Los elementos químicos La materia está formada por partículas denominadas átomos que, a su vez, están formados por otras partículas más pequeñas: protones,
3. El sistema periódico de los elementos. 3. El sistema periódico de los elementos. 3. El sistema periódico de los elementos
 3. El sistema periódico de los elementos Clasificación de los elementos químicos en el siglo XIX: los químicos de la época tenían una idea vaga de los átomos; no conocían p + ni e -. Clasificaban los elementos
3. El sistema periódico de los elementos Clasificación de los elementos químicos en el siglo XIX: los químicos de la época tenían una idea vaga de los átomos; no conocían p + ni e -. Clasificaban los elementos
Alianza para el Aprendizaje de Ciencias y Matemáticas
 Alianza para el Aprendizaje de Ciencias y Matemáticas Identificación de Minerales Guía del Maestro Objetivos Educacionales: Actividad #6 Una vez finalizada esta actividad los estudiantes, en general, saben
Alianza para el Aprendizaje de Ciencias y Matemáticas Identificación de Minerales Guía del Maestro Objetivos Educacionales: Actividad #6 Una vez finalizada esta actividad los estudiantes, en general, saben
Colección de problemas Unidad 2
 Facultad de Química, UNAM Curso: Química General I Colección de problemas Unidad 2 1. Describe una contribución importante a la ciencia hecha por cada uno de los científicos siguientes: Dalton, Thomson,
Facultad de Química, UNAM Curso: Química General I Colección de problemas Unidad 2 1. Describe una contribución importante a la ciencia hecha por cada uno de los científicos siguientes: Dalton, Thomson,
Profesor: Carlos Gutiérrez Arancibia. Temas a tratar: - - Sustancias Puras - Mezclas - Enlaces Químicos - Fuerzas Intermoleculares
 Profesor: Carlos Gutiérrez Arancibia Temas a tratar: - - Sustancias Puras - Mezclas - Enlaces Químicos - Fuerzas Intermoleculares A. Sustancia Pura: SUSTANCIAS PURAS Y MEZCLAS Una sustancia pura es un
Profesor: Carlos Gutiérrez Arancibia Temas a tratar: - - Sustancias Puras - Mezclas - Enlaces Químicos - Fuerzas Intermoleculares A. Sustancia Pura: SUSTANCIAS PURAS Y MEZCLAS Una sustancia pura es un
Estudio del átomo: 1. Átomos e isótopos 2. Modelos Atómicos 3. Teoría cuántica. Ing. Sol de María Jiménez González
 Estudio del átomo: 1. Átomos e isótopos 2. Modelos Atómicos 3. Teoría cuántica 1 Núcleo: protones y neutrones Los electrones se mueven alrededor. Característica Partículas Protón Neutrón Electrón Símbolo
Estudio del átomo: 1. Átomos e isótopos 2. Modelos Atómicos 3. Teoría cuántica 1 Núcleo: protones y neutrones Los electrones se mueven alrededor. Característica Partículas Protón Neutrón Electrón Símbolo
LECTURA DIFERENCIA ENTRE METALES Y NO METALES POR SU COMPORTAMIENTO FRENTE AL OXÍGENO.
 LECTURA DIFERENCIA ENTRE METALES Y NO METALES POR SU COMPORTAMIENTO FRENTE AL OXÍGENO. Prácticamente todos los elementos conocidos, metales y no metales, reaccionan o son oxidados por el oxígeno formando
LECTURA DIFERENCIA ENTRE METALES Y NO METALES POR SU COMPORTAMIENTO FRENTE AL OXÍGENO. Prácticamente todos los elementos conocidos, metales y no metales, reaccionan o son oxidados por el oxígeno formando
Enlace Químico. Colegio San Esteban Diácono Departamento de Ciencias Química Iº Medio Prof. Juan Pastrián / Sofía Ponce de León
 Enlace Químico Colegio San Esteban Diácono Departamento de Ciencias Química Iº Medio Prof. Juan Pastrián / Sofía Ponce de León Objetivos u u u u u Comprender la interacción entre átomos a partir de su
Enlace Químico Colegio San Esteban Diácono Departamento de Ciencias Química Iº Medio Prof. Juan Pastrián / Sofía Ponce de León Objetivos u u u u u Comprender la interacción entre átomos a partir de su
Estructura de sólidos
 Estructura de sólidos Química Inorgánica - 2006 Tipos de estructuras cristalinas cristal enlace características molecular covalente-baja energía cristales blandos, bajo p.f. red covalente covalente cristales
Estructura de sólidos Química Inorgánica - 2006 Tipos de estructuras cristalinas cristal enlace características molecular covalente-baja energía cristales blandos, bajo p.f. red covalente covalente cristales
4.000 minerales minerales formadores
 Grupos de Minerales Se conocen por su nombre casi 4.000 minerales y se identifican cada año varios minerales nuevos. Por fortuna, para los estudiantes que están empezando a estudiar los minerales, sólo
Grupos de Minerales Se conocen por su nombre casi 4.000 minerales y se identifican cada año varios minerales nuevos. Por fortuna, para los estudiantes que están empezando a estudiar los minerales, sólo
LOS MATERIALES DE LA SUPERFICIE TERRESTRE. MINERALES Y ROCAS
 LOS MATERIALES DE LA SUPERFICIE TERRESTRE. MINERALES Y ROCAS Sobre la superficie terrestre podemos encontrar materiales, generalmente en estado sólido, cuya variedad de orígenes y composición conforman
LOS MATERIALES DE LA SUPERFICIE TERRESTRE. MINERALES Y ROCAS Sobre la superficie terrestre podemos encontrar materiales, generalmente en estado sólido, cuya variedad de orígenes y composición conforman
Solución: Son sustancias moleculares la a) y la e), porque los átomos que las forman son de elementos no metálicos.
 1 El azufre es un elemento que está en el período 3 y el grupo 6 del sistema periódico. Escribe su distribución electrónica en capas. Si capta 2 electrones, qué configuración electrónica adquiere? Será
1 El azufre es un elemento que está en el período 3 y el grupo 6 del sistema periódico. Escribe su distribución electrónica en capas. Si capta 2 electrones, qué configuración electrónica adquiere? Será
0,225. 0, ,15 0,92
 1.- El ácido clorhídrico reacciona con el mármol (carbonato de calcio) formando cloruro de calcio, dióxido de carbono gas y agua. a) Escribe y ajusta la reacción química. (0,5 p) b) Halla el volumen de
1.- El ácido clorhídrico reacciona con el mármol (carbonato de calcio) formando cloruro de calcio, dióxido de carbono gas y agua. a) Escribe y ajusta la reacción química. (0,5 p) b) Halla el volumen de
Colección de ejercicios UNIDAD 2
 Facultad de Química, UNAM Curso: Química General I, gpo 8 Colección de ejercicios UNIDAD 2 1. Describe cuál fue la contribución al conocimiento de la estructura atómica hecha por cada uno de los siguientes
Facultad de Química, UNAM Curso: Química General I, gpo 8 Colección de ejercicios UNIDAD 2 1. Describe cuál fue la contribución al conocimiento de la estructura atómica hecha por cada uno de los siguientes
PRÁCTICA: RECONOCIMIENTO DE MINERALES
 PRÁCTICA: RECONOCIMIENTO DE MINERALES OBJETIVO Identificar minerales a partir de la observación directa de sus propiedades físicas principales. CONCEPTOS BÁSICOS Un mineral es una sustancia inorgánica
PRÁCTICA: RECONOCIMIENTO DE MINERALES OBJETIVO Identificar minerales a partir de la observación directa de sus propiedades físicas principales. CONCEPTOS BÁSICOS Un mineral es una sustancia inorgánica
SOLUCIONARIO Guía Estándar Anual
 SOLUCIONARIO Guía Estándar Anual El enlace químico SGUICES004CB33-A16V1 Ítem Alternativa Habilidad 1 E Reconocimiento 2 B Aplicación 3 C Comprensión 4 D Comprensión 5 D Aplicación 6 D Aplicación 7 D Comprensión
SOLUCIONARIO Guía Estándar Anual El enlace químico SGUICES004CB33-A16V1 Ítem Alternativa Habilidad 1 E Reconocimiento 2 B Aplicación 3 C Comprensión 4 D Comprensión 5 D Aplicación 6 D Aplicación 7 D Comprensión
ADAPTACIÓN CURRICULAR LA GEOSFERA
 ADAPTACIÓN CURRICULAR 3 LA GEOSFERA 1. Las capas de la geosfera 2. Los minerales 3. Propiedades de los minerales 4. Clasificación de las rocas 5. Tipos de rocas 6. El ciclo de las rocas 7. Utilidad de
ADAPTACIÓN CURRICULAR 3 LA GEOSFERA 1. Las capas de la geosfera 2. Los minerales 3. Propiedades de los minerales 4. Clasificación de las rocas 5. Tipos de rocas 6. El ciclo de las rocas 7. Utilidad de
Ejercicios UD. 4 Elementos y Compuestos Física y Química CEPA COSLADA
 1.- En qué consistía la ley de las triadas? Quién la propuso? 2.- Por qué la tabla donde se ordenan los elementos químicos se llama tabla periódica? Los elementos están ordenados en la tabla periódica
1.- En qué consistía la ley de las triadas? Quién la propuso? 2.- Por qué la tabla donde se ordenan los elementos químicos se llama tabla periódica? Los elementos están ordenados en la tabla periódica
Niveles de Organización Conceptos, átomos y enlaces
 Niveles de Organización Conceptos, átomos y enlaces Cómo se organiza la materia viva? NIVELES DE ORGANIZACIÓN ÁTOMO MOLÉCULA (ELEMENTO- COMPUESTO) MACROMOLÉCULA CÉLULA TEJIDO ÓRGANO SISTEMA ORGANISMO MULTICELULAR
Niveles de Organización Conceptos, átomos y enlaces Cómo se organiza la materia viva? NIVELES DE ORGANIZACIÓN ÁTOMO MOLÉCULA (ELEMENTO- COMPUESTO) MACROMOLÉCULA CÉLULA TEJIDO ÓRGANO SISTEMA ORGANISMO MULTICELULAR
SOLUCIONES EJERCICIOS DE ENLACE QUÍMICO. 1º BCT
 SOLUCIOES EJERCICIOS DE ELACE QUÍMICO. 1º CT 1. La teoría de la repulsión de los pares electrónicos de la capa de valencia (TRPECV) dice que los pares electrónicos que rodean al átomo central se disponen
SOLUCIOES EJERCICIOS DE ELACE QUÍMICO. 1º CT 1. La teoría de la repulsión de los pares electrónicos de la capa de valencia (TRPECV) dice que los pares electrónicos que rodean al átomo central se disponen
LA PARTE SÓLIDA DE LA TIERRA
 UNIDAD DIDÁCTICA ADAPTADA CIENCIAS DE LA NATURALEZA 1º ESO TEMA 7 LA PARTE SÓLIDA DE LA TIERRA VAMOS A APRENDER 1.- QUÉ SON LOS MINERALES? 2.- QUÉ USO LE DAMOS A LOS MINERALES? 3.- QUÉ SON LAS ROCAS? 4.-
UNIDAD DIDÁCTICA ADAPTADA CIENCIAS DE LA NATURALEZA 1º ESO TEMA 7 LA PARTE SÓLIDA DE LA TIERRA VAMOS A APRENDER 1.- QUÉ SON LOS MINERALES? 2.- QUÉ USO LE DAMOS A LOS MINERALES? 3.- QUÉ SON LAS ROCAS? 4.-
Tubo de ensayo. binocular o de mano. Minerales para identificar. Escala de Mohs. (Simplificada).
 Colegio Virgen Inmaculada - Sta. María de la Victoria Hijas de Jesús Departamento de Ciencias Naturales. Dr. Lazárraga, 14 29010 MÁLAGA DEPARTAMENTO DE CC.NN Utilización de claves para identificar minerales
Colegio Virgen Inmaculada - Sta. María de la Victoria Hijas de Jesús Departamento de Ciencias Naturales. Dr. Lazárraga, 14 29010 MÁLAGA DEPARTAMENTO DE CC.NN Utilización de claves para identificar minerales
MINERALES Y ROCAS. POLIMORFISMO. Dos minerales o más son polimorfos cuando presentan la misma composición química y distinto sistema cristalino.
 MINERALES Y ROCAS QUÉ ES UN MINERAL? Un mineral es un sólido de composición química y estructura cristalina determinadas, que se ha formado de modo natural. Frecuentemente los minerales forman granos pequeños
MINERALES Y ROCAS QUÉ ES UN MINERAL? Un mineral es un sólido de composición química y estructura cristalina determinadas, que se ha formado de modo natural. Frecuentemente los minerales forman granos pequeños
INTRODUCCIÓN A LA QUÍMICA
 INTRODUCCIÓN A LA QUÍMICA TRABAJO PRÁCTICO N 1 4 Año A, B, C, D 2.015 Prof. María Laura Sepúlveda Broky INTRODUCCIÓN A LA QUÍMICA Prof. María Laura Sepúlveda Broky 1)A- Realizar un esquema de la Tabla
INTRODUCCIÓN A LA QUÍMICA TRABAJO PRÁCTICO N 1 4 Año A, B, C, D 2.015 Prof. María Laura Sepúlveda Broky INTRODUCCIÓN A LA QUÍMICA Prof. María Laura Sepúlveda Broky 1)A- Realizar un esquema de la Tabla
UNIDAD 1 La materia y sus cambios
 UNIDAD 1 La materia y sus cambios Tema 1.2 Composición de la materia. Sustancias y mezclas. Mezclas homogéneas, heterogéneas y coloides. Introducción a las disoluciones: no saturadas, saturadas y sobresaturadas.
UNIDAD 1 La materia y sus cambios Tema 1.2 Composición de la materia. Sustancias y mezclas. Mezclas homogéneas, heterogéneas y coloides. Introducción a las disoluciones: no saturadas, saturadas y sobresaturadas.
Física y Química 3º ESO
 1. Física y Química. Ciencias de la medida forman parte de las necesitan Ciencias de la naturaleza medir las propiedades de los cuerpos que se dividen en para lo cual se emplean lo que siempre conlleva
1. Física y Química. Ciencias de la medida forman parte de las necesitan Ciencias de la naturaleza medir las propiedades de los cuerpos que se dividen en para lo cual se emplean lo que siempre conlleva
ACTIVIDADES Tema 10. 2. Qué relación hay entre los minerales y las rocas? Los minerales se mezclan para formar las rocas.
 ACTIVIDADES Tema 10 1. Escribe en tu cuaderno una definición de mineral en la que se especifiquen las tres características que lo identifican. Un mineral es un sólido creado por la combinación química
ACTIVIDADES Tema 10 1. Escribe en tu cuaderno una definición de mineral en la que se especifiquen las tres características que lo identifican. Un mineral es un sólido creado por la combinación química
ÁTOMOS Y RADIACTIVIDAD
 ÁTOMOS Y RADIACTIVIDAD 1 ATOMOS, MOLECULAS E IONES Atomo: Según Dalton un átomo se define como la cantidad básica de un elemento que puede intervenir en una combinación química. Los átomos están formados
ÁTOMOS Y RADIACTIVIDAD 1 ATOMOS, MOLECULAS E IONES Atomo: Según Dalton un átomo se define como la cantidad básica de un elemento que puede intervenir en una combinación química. Los átomos están formados
Unidad 3 Curso: Química General 1 Mtra. Norma Mónica López.
 Unidad 3 Curso: Química General 1 Mtra. Norma Mónica López. Interacciones eléctricas De atracción +, - De repulsión +, + ó -,- Entre Átomos de una misma molécula Moléculas vecinas 2 ENLACE QUÍMICO Siempre
Unidad 3 Curso: Química General 1 Mtra. Norma Mónica López. Interacciones eléctricas De atracción +, - De repulsión +, + ó -,- Entre Átomos de una misma molécula Moléculas vecinas 2 ENLACE QUÍMICO Siempre
TEMA 1: ESTRUCTURA INTERNA DE LOS MATERIALES
 PERIODO Departamento de Tecnología. IES Nuestra Señora de la Almudena Mª Jesús Saiz TEMA 1: ESTRUCTURA INTERNA DE LOS MATERIALES El átomo: Toda la materia está compuesta por átomos y éstos por partículas
PERIODO Departamento de Tecnología. IES Nuestra Señora de la Almudena Mª Jesús Saiz TEMA 1: ESTRUCTURA INTERNA DE LOS MATERIALES El átomo: Toda la materia está compuesta por átomos y éstos por partículas
Características de electrones protones y neutrones
 Características de electrones protones y neutrones Carga eléctrica Masa Espín SI (C) Atómica SI(g) Atómica (uma) Protón +1,6021 10-19 +1 1,6725 10-24 1,0073 1/2 neutrón 0 0 1,6748 10-24 1,0087 1/2 electrón
Características de electrones protones y neutrones Carga eléctrica Masa Espín SI (C) Atómica SI(g) Atómica (uma) Protón +1,6021 10-19 +1 1,6725 10-24 1,0073 1/2 neutrón 0 0 1,6748 10-24 1,0087 1/2 electrón
Materia: FÍSICA Y QUÍMICA Curso
 ACTIVIDADES DE REFUERZO FÍSICA Y QUÍMICA 3º ESO. JUNIO 2015. 1.- Realizar las configuraciones electrónicas de todos los elementos de los tres primeros periodos de la tabla periódica. 2.- Razonar cuales
ACTIVIDADES DE REFUERZO FÍSICA Y QUÍMICA 3º ESO. JUNIO 2015. 1.- Realizar las configuraciones electrónicas de todos los elementos de los tres primeros periodos de la tabla periódica. 2.- Razonar cuales
Tema 1.3 Estados de agregación de la materia. Tema 1.4 Composición de la materia
 Tema 1.3 Estados de agregación de la materia Tema 1.4 Composición de la materia 1 MATERIA Todo aquello que ocupa un lugar en el espacio, tiene una energía medible y está sujeto a cambios en el tiempo y
Tema 1.3 Estados de agregación de la materia Tema 1.4 Composición de la materia 1 MATERIA Todo aquello que ocupa un lugar en el espacio, tiene una energía medible y está sujeto a cambios en el tiempo y
Explicación de las propiedades y los estados de agregación en los compuestos químicos en función de los tipos de enlace. vs.
 Explicación de las propiedades y los estados de agregación en los compuestos químicos en función de los tipos de enlace. vs. Usar las propiedades y los estados de agregación en los compuestos químicos
Explicación de las propiedades y los estados de agregación en los compuestos químicos en función de los tipos de enlace. vs. Usar las propiedades y los estados de agregación en los compuestos químicos
CONTENIDO T1 EL ÁTOMO Y EL SISTEMA PERIÓDICO...3 T2 EL ENLACE QUÍMICO...7 T3 FORMULACIÓN Y NOMENCLATURA INORGÁNICA...13
 CONTENIDO T1 EL ÁTOMO Y EL SISTEMA PERIÓDICO...3 T2 EL ENLACE QUÍMICO...7 T3 FORMULACIÓN Y NOMENCLATURA INORGÁNICA...13 T4 REACCIONES QUÍMICAS: Cálculos, Energías y Velocidades...19 T5 ESTUDIO DEL MOVIMIENTO...25
CONTENIDO T1 EL ÁTOMO Y EL SISTEMA PERIÓDICO...3 T2 EL ENLACE QUÍMICO...7 T3 FORMULACIÓN Y NOMENCLATURA INORGÁNICA...13 T4 REACCIONES QUÍMICAS: Cálculos, Energías y Velocidades...19 T5 ESTUDIO DEL MOVIMIENTO...25
ENLACE QUÍMICO 2º BACH EJERCICIOS DE ENLACE QUÍMICO DEL LIBRO 28. H-CHO H C = O : CH 3 OH H C O H H H H C O C H H H CH 3 OCH 3
 EJERCICIOS DE ENLACE QUÍMICO DEL LIBRO 28. -CO C = O : C 3 O C O C 3 OC 3 C O C a) La longitud de enlace CO es menor en el formaldehido, ya que tiene un doble enlace. b) El metanol puede formar enlaces
EJERCICIOS DE ENLACE QUÍMICO DEL LIBRO 28. -CO C = O : C 3 O C O C 3 OC 3 C O C a) La longitud de enlace CO es menor en el formaldehido, ya que tiene un doble enlace. b) El metanol puede formar enlaces
Átomos polielectrónicos Espín y configuraciones electrónicas Número y masa atómicos (isótopos) Tabla periódica y configuraciones electrónicas
 ESTRUCTURA ELECTRÓNICA Espín y configuraciones electrónicas Número y masa atómicos (isótopos) Tabla periódica y configuraciones electrónicas Átomos con un solo electrón: La energía depende solamente del
ESTRUCTURA ELECTRÓNICA Espín y configuraciones electrónicas Número y masa atómicos (isótopos) Tabla periódica y configuraciones electrónicas Átomos con un solo electrón: La energía depende solamente del
Alianza para el Aprendizaje de Ciencias y Matemáticas
 Alianza para el Aprendizaje de Ciencias y Matemáticas Actividad #4 Planos de Crucero (Clivaje) Guía del Maestro Objetivos Educacionales: Una vez finalizada esta actividad los estudiantes, en general, saben
Alianza para el Aprendizaje de Ciencias y Matemáticas Actividad #4 Planos de Crucero (Clivaje) Guía del Maestro Objetivos Educacionales: Una vez finalizada esta actividad los estudiantes, en general, saben
GEOLOGÍA BÁSICA PARA EL CURSO DE AGRONOMÍA I
 Prof. Donato García López GEOLOGÍA BÁSICA PARA EL CURSO DE AGRONOMÍA I GEOLOGÍA es una palabra del idioma griego, que se puede traducir al español de la manera siguiente: geo = tierra y logos = tratado.
Prof. Donato García López GEOLOGÍA BÁSICA PARA EL CURSO DE AGRONOMÍA I GEOLOGÍA es una palabra del idioma griego, que se puede traducir al español de la manera siguiente: geo = tierra y logos = tratado.
La tabla periódica es la estrella orientadora para la exploración en el capo de la química, la física, la mineralogía y la técnica.
 SISTEMA PERIÓDICO DE LOS ELEMENTOS La tabla periódica es la estrella orientadora para la exploración en el capo de la química, la física, la mineralogía y la técnica. Niels Bohr Principio de exclusión
SISTEMA PERIÓDICO DE LOS ELEMENTOS La tabla periódica es la estrella orientadora para la exploración en el capo de la química, la física, la mineralogía y la técnica. Niels Bohr Principio de exclusión
3 - Cómo podemos diferenciar un elemento químico de un compuesto, según la teoría de Dalton?
 TEORÍA ATÓMICA 1- A partir de los siguientes datos, cuántas veces es maor la masa del protón que la del electrón? Masa del protón =1,673 10-27 kg Masa del electrón =9,1 10-31 kg 2 - El modelo del átomo
TEORÍA ATÓMICA 1- A partir de los siguientes datos, cuántas veces es maor la masa del protón que la del electrón? Masa del protón =1,673 10-27 kg Masa del electrón =9,1 10-31 kg 2 - El modelo del átomo
Ejercicios resueltos de 3º de E.S.O.
 Ejercicios resueltos de 3º de E.S.O. Estructura de la materia. Modelos atómicos Ejercicio resuelto nº 1 Si el número másico de un átomo es A = 30 y tiene 12 protones, calcula su número de neutrones. Resolución
Ejercicios resueltos de 3º de E.S.O. Estructura de la materia. Modelos atómicos Ejercicio resuelto nº 1 Si el número másico de un átomo es A = 30 y tiene 12 protones, calcula su número de neutrones. Resolución
4 Elementos y compuestos
 4 Elementos y compuestos Elementos Las sustancias puras son aquellas que se caracterizan por el hecho de que todas sus partes tienen las mismas propiedades, es decir, todas sus partículas son del mismo
4 Elementos y compuestos Elementos Las sustancias puras son aquellas que se caracterizan por el hecho de que todas sus partes tienen las mismas propiedades, es decir, todas sus partículas son del mismo
1. Uno de los grandes aciertos de los postulados de Mendeleiev respecto a la ordenación de los elementos fue:
 miniprueba Clase 04 Problemas 1. Uno de los grandes aciertos de los postulados de Mendeleiev respecto a la ordenación de los elementos fue: a. Designar un lugar fijo para el hidrogeno. b. Ordenar los elementos
miniprueba Clase 04 Problemas 1. Uno de los grandes aciertos de los postulados de Mendeleiev respecto a la ordenación de los elementos fue: a. Designar un lugar fijo para el hidrogeno. b. Ordenar los elementos
Guía de Estudio para 1er Parcial Temas Selectos de Química
 Guía de Estudio para 1er Parcial Temas Selectos de Química 1. Menciona que científicos ordenaron los elementos conocidos en su época en triadas (grupos de tres), en octavas, por número atómico y quien
Guía de Estudio para 1er Parcial Temas Selectos de Química 1. Menciona que científicos ordenaron los elementos conocidos en su época en triadas (grupos de tres), en octavas, por número atómico y quien
ADAPTACIÓN CURRICULAR LA GEOSFERA
 ADAPTACIÓN CURRICULAR LA GEOSFERA 1. Las capas de la geosfera 2. Los minerales. Propiedades de los minerales 4. Clasificación de las rocas 5. Tipos de rocas 6. El ciclo de las rocas 7. Utilidad de las
ADAPTACIÓN CURRICULAR LA GEOSFERA 1. Las capas de la geosfera 2. Los minerales. Propiedades de los minerales 4. Clasificación de las rocas 5. Tipos de rocas 6. El ciclo de las rocas 7. Utilidad de las
ALEACIONES 1. INTRODUCCION 2. CLASIFICACION 3. SOLUCIONES SÓLIDAS 4. FASES INTERMEDIAS 5. SOLUCIONES SÓLIDAS ORDENADAS M.V.M.G ALEACIONES 1
 ALEACIONES 1. INTRODUCCION 2. CLASIFICACION 3. SOLUCIONES SÓLIDAS 4. FASES INTERMEDIAS 5. SOLUCIONES SÓLIDAS ORDENADAS 2007-08 ALEACIONES 1 INTRODUCCIÓN Una aleación es la combinación de dos o más metales,
ALEACIONES 1. INTRODUCCION 2. CLASIFICACION 3. SOLUCIONES SÓLIDAS 4. FASES INTERMEDIAS 5. SOLUCIONES SÓLIDAS ORDENADAS 2007-08 ALEACIONES 1 INTRODUCCIÓN Una aleación es la combinación de dos o más metales,
CLASE Nº 4 ENLACE QUÍMICO
 UNIVERSIDAD NACIONAL EXPERIMENTAL POLITECNICA ANTONIO JOSÉ DE SUCRE VICERRECTORADO BARQUISIMETO DEPARTAMENTO DE INGENIERÍA QUÍMICA QUÍMICA GENERAL CLASE Nº 4 ENLACE QUÍMICO 2012 1 Moléculas y compuestos
UNIVERSIDAD NACIONAL EXPERIMENTAL POLITECNICA ANTONIO JOSÉ DE SUCRE VICERRECTORADO BARQUISIMETO DEPARTAMENTO DE INGENIERÍA QUÍMICA QUÍMICA GENERAL CLASE Nº 4 ENLACE QUÍMICO 2012 1 Moléculas y compuestos
Colegio San Lorenzo - Copiapó - Región de Atacama Per Laborem ad Lucem
 TEMARIO EXAMENES QUIMICA 2012 7º BASICO Descubrimiento del átomo: Quién lo descubrió y su significado Estructura atómica: Partes del átomo, características del núcleo y la corteza, cálculo del protón,
TEMARIO EXAMENES QUIMICA 2012 7º BASICO Descubrimiento del átomo: Quién lo descubrió y su significado Estructura atómica: Partes del átomo, características del núcleo y la corteza, cálculo del protón,
Departamento de Física y Química. 2.- Deduce el número de neutrones, protones y electrones de los átomos siguientes:
 1.- Para el átomo de Galio, 69 31Ga ; deduce el número de protones, electrones y neutrones. 2.- Deduce el número de neutrones, protones y electrones de los átomos siguientes: U ; Hg ; Th ; He; Ne 235 200
1.- Para el átomo de Galio, 69 31Ga ; deduce el número de protones, electrones y neutrones. 2.- Deduce el número de neutrones, protones y electrones de los átomos siguientes: U ; Hg ; Th ; He; Ne 235 200
CRISTALES Y MI ERALES
 CRISTALES Y MI ERALES ÁTOMOS, ELEME TOS, MI ERALES, CRISTALES Y ROCAS Un átomo es la partícula más pequeña de un elemento químico que tiene las características del elemento. Formado por protones, neutrones
CRISTALES Y MI ERALES ÁTOMOS, ELEME TOS, MI ERALES, CRISTALES Y ROCAS Un átomo es la partícula más pequeña de un elemento químico que tiene las características del elemento. Formado por protones, neutrones
A. VIVENCIA Elabora la siguiente sopa de letras y define los conceptos:
 INSTITUCIÓN EDUCATIVA COLEGIO ARTISTICO RAFAEL CONTRERAS NAVARRO AREA: CIENCIAS NATURALES PROFESOR; JESÚS ALONSO PABA LEÓN ENLACES QUIMICOS Cómo se forman las sustancias químicas? COMPETENCIA: Construye
INSTITUCIÓN EDUCATIVA COLEGIO ARTISTICO RAFAEL CONTRERAS NAVARRO AREA: CIENCIAS NATURALES PROFESOR; JESÚS ALONSO PABA LEÓN ENLACES QUIMICOS Cómo se forman las sustancias químicas? COMPETENCIA: Construye
LA MATERIA. Características de los átomos
 LA MATERIA Características de los átomos Años más tarde del modelo atómico de Rutherford (1911) se descubrió una nueva partícula en el núcleo, el neutrón. Esta fue descubierta por Chadwick en 1932, y se
LA MATERIA Características de los átomos Años más tarde del modelo atómico de Rutherford (1911) se descubrió una nueva partícula en el núcleo, el neutrón. Esta fue descubierta por Chadwick en 1932, y se
UNIVERSIDAD NACIONAL DE INGENIERÍA SEDE - ESTELÍ
 UNIVERSIDAD NACIONAL DE INGENIERÍA SEDE - ESTELÍ 1. Introducción Los materiales empleados en la construcción pueden ser clasificados en diferentes maneras. De lo dicho se desprende que existen dos clases
UNIVERSIDAD NACIONAL DE INGENIERÍA SEDE - ESTELÍ 1. Introducción Los materiales empleados en la construcción pueden ser clasificados en diferentes maneras. De lo dicho se desprende que existen dos clases
Tema 2: MINERALOGÍA. - Concepto de mineral y cristal - Propiedades y características - Clasificación de los minerales (Strunz)
 Tema 2: MINERALOGÍA - Concepto de mineral y cristal - Propiedades y características - Clasificación de los minerales (Strunz) Concepto de mineral y cristal: Mineral: Sólido homogéneo por naturaleza con
Tema 2: MINERALOGÍA - Concepto de mineral y cristal - Propiedades y características - Clasificación de los minerales (Strunz) Concepto de mineral y cristal: Mineral: Sólido homogéneo por naturaleza con
QUÍMICA. La MATERIA REPRESENTACIÓN. Observación Datos Ley Hipótesis Teoría DEFINICIONES BÁSICAS. Propiedades
 QUÍMICA La MATERIA Relación constante TEORÍA EXPERIMENTACIÓN Ciencia básica - Estructura - Composición - Propiedades - Transformaciones REPRESENTACIÓN OBSERVACIÓN mundo macroscópico Técnica sistemática
QUÍMICA La MATERIA Relación constante TEORÍA EXPERIMENTACIÓN Ciencia básica - Estructura - Composición - Propiedades - Transformaciones REPRESENTACIÓN OBSERVACIÓN mundo macroscópico Técnica sistemática
Departamento de Física y Química. Ies Dr. Rodríguez Delgado. Ronda Nivel 1º Bachillerato
 Departamento de Física y Química. Ies Dr. Rodríguez Delgado. Ronda Nivel 1º Bachillerato Planteamiento del problema 1. La mina de un lápiz se compone de grafito y arcilla. El grafito es una sustancia simple
Departamento de Física y Química. Ies Dr. Rodríguez Delgado. Ronda Nivel 1º Bachillerato Planteamiento del problema 1. La mina de un lápiz se compone de grafito y arcilla. El grafito es una sustancia simple
ESTRUCTURA DE LOS ATOMOS Ing. Alfredo Luis Rojas B.
 CAPITULO 4 ESTRUCTURA DE LOS ATOMOS Ing. Alfredo Luis Rojas B. Aproximadamente 400 a.c. el filosofo griego Democrito sugirió que toda la materia esta formada por partículas minúsculas, discretas e indivisibles,
CAPITULO 4 ESTRUCTURA DE LOS ATOMOS Ing. Alfredo Luis Rojas B. Aproximadamente 400 a.c. el filosofo griego Democrito sugirió que toda la materia esta formada por partículas minúsculas, discretas e indivisibles,
Longitud y energía de enlace
 Longitud y energía de enlace ENLACES QUIMICOS Los enlaces interatómicos se clasifican en: Enlaces iónicos Enlaces covalentes Enlaces metálicos ENLACE IÓNICO: Transferencia de electrones Li F El litio le
Longitud y energía de enlace ENLACES QUIMICOS Los enlaces interatómicos se clasifican en: Enlaces iónicos Enlaces covalentes Enlaces metálicos ENLACE IÓNICO: Transferencia de electrones Li F El litio le
EL ENLACE QUÍMICO 1. El enlace químico. 2. Enlace intramolecular. 3. Enlace intermolecular. 4. Propiedades del enlace.
 EL ENLACE QUÍMICO 1. El enlace químico. 2. Enlace intramolecular. 3. Enlace intermolecular. 4. Propiedades del enlace. Química 1º bachillerato El enlace químico 1 1. EL ENLACE QUÍMICO El enlace químico
EL ENLACE QUÍMICO 1. El enlace químico. 2. Enlace intramolecular. 3. Enlace intermolecular. 4. Propiedades del enlace. Química 1º bachillerato El enlace químico 1 1. EL ENLACE QUÍMICO El enlace químico
Conceptos básicos en estequiometría
 Conceptos básicos en estequiometría Tomado de: http://www.eis.uva.es/~qgintro/esteq/tutorial-01.html El Mol Un mol se define como la cantidad de materia que tiene tantos objetos como el número de átomos
Conceptos básicos en estequiometría Tomado de: http://www.eis.uva.es/~qgintro/esteq/tutorial-01.html El Mol Un mol se define como la cantidad de materia que tiene tantos objetos como el número de átomos
TABLA PERIÓDICA. La clasificación más sencilla de los elementos químicos consiste en catalogarlos en metales, no metales y gases nobles.
 TABLA PERIÓDICA En la tabla periódica, los elementos químicos se encuentran ordenados en orden creciente a su número atómico (Z), es decir, al número de protones que tienen en el núcleo. La tabla periódica
TABLA PERIÓDICA En la tabla periódica, los elementos químicos se encuentran ordenados en orden creciente a su número atómico (Z), es decir, al número de protones que tienen en el núcleo. La tabla periódica
LOS ÁTOMOS Y LAS PROPIEDADES DE LA MATERIA. (Ciencias Elemental) PROFESORA GILDA DIAZ MAT H AND S C I ENCE PAR T NERSHIP FOR T HE 21S T CENTURY
 LOS ÁTOMOS Y LAS PROPIEDADES DE LA MATERIA (Ciencias Elemental) PROFESORA GILDA DIAZ MAT H AND S C I ENCE PAR T NERSHIP FOR T HE 21S T CENTURY ELEMENTARY AND MIDDLE S C HOOL MSP -21 ACADEMIA DE VERANO
LOS ÁTOMOS Y LAS PROPIEDADES DE LA MATERIA (Ciencias Elemental) PROFESORA GILDA DIAZ MAT H AND S C I ENCE PAR T NERSHIP FOR T HE 21S T CENTURY ELEMENTARY AND MIDDLE S C HOOL MSP -21 ACADEMIA DE VERANO
