TEMA 1 NATURALEZA ELÉCTRICA DE LA MATERIA
|
|
|
- Manuela Serrano Molina
- hace 7 años
- Vistas:
Transcripción
1 TEMA 1 NATURALEZA ELÉCTRICA DE LA MATERIA Hoy en día el mundo científico tiene una idea lo suficientemente precisa de la estructura atómica, como para poder explicar el comportamiento de los átomos y moléculas en las reacciones químicas. Ahora bien, a nadie se le escapa que este conocimiento de la estructura atómica es el resultado de numerosos experimentos, los cuales comenzaron a finales del sioglo XIX. El objetivo de este primer capítulo es efectuar una revisión de los experimentos que contribuyeron de forma más relevante a forjar la actual teoría atómica. Los tres pasos más importantes fueron: 1.- El conocimiento de la estructura eléctrica de la materia. 2.- El descubrimiento de que el átomo está formado por un núcleo rodeado de electrones. 3.- El descubrimiento de las leyes mecánicas que rigen el comportamiento de los electrones en los átomos.
2 Naturaleza eléctrica de la materia Los primeros indicios importantes acerca de la naturaleza de la electricidad y de la estructura eléctrica de los átomos aparecieron en 1833 como resultado de las investigaciones de la electrólisis por Faraday. Sus hallazgos pueden ser resumidos en dos enunciados: 1.- El peso de una sustancia dada que se deposita en un electrodo por una cierta cantidad de electricidad es siempre el mismo. 2.- Los pesos de las diversas sustancias que se depositan, desprenden o disuelven en un electrodo, por una cantidad fija de electricidad, son proporcionales a los pesos equivalentes de esas sustancias. La segunda de estas leyes es particularmente reveladora, si recordamos que el peso equivalente de una sustancia contiene el mismo número de moléculas o un múltiplo de él. Si un número fijo de átomos (el peso equivalente) reacciona solamente con una cierta cantidad fija de electricidad, parece razonable suponer que la electricidad misma está compuesta por partículas. Era necesario encontrar un indicio experimental de la existencia de estas partículas eléctricas fundamentales. G.J. Stoney fue el primero en sugerir el nombre de electrón para la partícula eléctrica fundamental. Sin embargo, hasta el año 1897 no se encontró la evidencia experimental de la existencia y propiedades del electrón, como resultado del estudio de la conductividad de los gases a baja presión: los gases son ordinariamente aislantes eléctrico, pero cuando se los somete a altos voltajes y a presiones inferiores a 10-2 atmósferas, se descomponen y sobreviene la conducción eléctrica acompañada por emisión de luz. Si la presión es reducida 10-4 atmósferas, la conducción eléctrica persiste, y la luminosidad del gas disminuye; y si los voltajes que intervienen son lo suficientemente altos ( V.), el recipiente de vidrio comienza a brillar o a fluorescer ténuamente. Hacia 1890 varios experimentos habían demostrado que esta fluorescencia es el resultado del bombardeo del vidrio por rayos que se originan en el cátodo, o electrodo negativo, y viajan en líneas rectas hasta que chocan ya sea con el electrodo positivo o con las paredes del tubo. Son los rayos catódicos. Los rayos canales son rayos con carga positiva que van en dirección opuesta a la de los rayos catódicos. La masa de los rayos canales varía según el gas que se encuentra presente en el tubo de descarga.
3 Experimentos de J. J. Thomson En el año 1987 J. J. Thomson mostró: Si los rayos catódicos son desviados hacia el electrodo de un electrómetro, este instrumento adquiere una carga negativa. Los rayos catódicos pueden ser desviados por la aplicación de un campo eléctrico y que estos rayos catódicos se alejaban de las regiones de densidad de carga negativa. El hecho de que estos resultados fueran encontrados independientemente de la clase de gas empleado en el tubo de descarga sugería que ellos no eran un tipo particular de átomo electrificado, sino más bien un fragmento universal que se encuentra en todos los átomos. Thomson reconoció que una determinación del cociente carga/masa de la partícula de los rayos catódicos ayudaría a identificar a éstos. El valor aceptado corrientemente para esta relación e/m es 1.76x10 8 cb/g ó 5.27x10 17 unidades electrostáticas por gramo (uee/g). La relación carga a masa de los rayos catódicos era más de 1000 veces mayor que la de cualquier ión. Además, mientras que los cocientes carga a masa de varios iones eran diferentes, e/m de los rayos catódicos era una cantidad constante independientemente del gas que se utilizaba en el tubo de descarga. Estos hechos condujeron a Thomson a deducir que los rayos catódicos no eran átomos electrificados sino fragmentos corpusculares de átomos, o sea, electrones según nuestra terminología moderna.
4 Contribución de Millikan Esta contribución permitió conocer cuál es el valor de la unidad de carga fundamental o electrón, y el valor de su masa. Para realizar el experimento se llevan gotas esféricas de aceite desde el atomizador hacia la cámara de observación. Allí se cargan al chocar con los iones gaseosos producidos por la acción de los rayos X sobre el aire (los rayos X arrancan electrones de algunas moléculas de aire, estos electrones son captados por las gotas de aceite). Se puede reconocer una gota de aceite cargada por su respuesta a un campo eléctrico y por su movimiento observado a través del microscopio. Cuando el campo eléctrico es cero, la gota de aceite está sometida solamente a la fuerza de la gravedad, y cae; debido a la resistencia del aire, la gota no acelera continuamente, sino que alcanza una velocidad constante dada por: v6p r = mg v= (mg) / 6p r = fuerza gravitacional / resistencia por viscosidad del aire siendo g la aceleración de la gravedad; m y r son la masa y el radio de la gota y la viscosidad del aire. Esta ecuación, junto con la expresión r= m / (4/3) p r 3 que relaciona a la densidad de la gota de aceite con su masa y su radio, permite calcular m y r, a partir de la velocidad y densidad medidas.
5 Si la misma gota contiene una cantidad de carga q, y es sometida a un campo E, la fuerza eléctrica que causa un movimiento ascendente de la gota es qe. Debido a la acción de la gravedad, la fuerza neta sobre la gota es qe mg, de modo que su velocidad en la dirección ascendente es: v 6p r = qe mg v = (qe mg) / 6p r Puesto que v y E son medibles y m, g,, r son conocidas, se puede calcular q. Millikan encontró que q era siempre un múltiplo entero de 1.602x10-19 cb. La suposición de que esta unidad fundamental es igual a la carga del electrón, junto con el valor medido de e/m, da 9.108x10-28 g como masa del electrón.
6 Estructura del átomo El primer modelo atómico propuesto fue el de Thomson; el átomo es una esfera uniforme de electricidad positiva con un radio de aproximadamente 10-8 cm, con los electrones dentro de esta esfera, de modo que resulte el agrupamiento electrostático más estable.
7 Experimento de E. Rutherford Este experimento rebate el modelo de Thomson. El experimento de la dispersión de las partículas a es tal vez el experimento aislado de mayor influencia en el desarrollo de la teoría de la estructura atómica. Un delgado haz paralelo de partículas a incide sobre una lámina metálica de oro (de espesor 10 4 átomos), y la distribución angular de las partículas dispersadas se obtiene contando los centelleos, o relámpagos de luz, que se producen sobre una pantalla de ZnS. La importancia cualitativa del resultado del experimento es que mientras la mayoría de las partículas a atraviesan la lámina sin desviarse, o desviadas solamente en pequeños ángulos, unas cuantas partículas son dispersadas a ángulos grandes, hasta de 180. En el tiempo en que fue realizado el experimento por primera vez, Rutherford conocía que las partículas a eran átomos de helio doblemente ionizados (He 2+ ) de masa atómica 4; además, sus velocidades habían sido medidas por el método de la desviación magnética. En consecuencia, Rutherford sabía que la energía cinética de las partículas a era grande, y comprendía que a fin de producir una desviación grande de una partícula tan energética, el átomo debía ser el asiento de una enorme fuerza eléctrica. También era claro que esta fuerza tenía que ser ejercida por un cuerpo de masa considerable, porque un cuerpo liviano, tal como el electrón, sería arrastrado por la partícula a, más pesada. Finalmente, el hecho de que solamente unas cuantas partículas a experimentan grandes desviaciones sugería que la gran fuerza eléctrica estaba confinada en regiones de espacio muy pequeñas, las cuales no eran alcanzadas por la mayoría de las partículas a. En otras palabras, en lugar de ser una esfera de masa y densidad de carga uniformes, como Thomson había propuesto, el átomo era altamente no uniforme. Aunque los electrones podrían ocupar el volumen asociado con la dimensión del átomo 10-8 cm, la electricidad positiva tenía que estar concentrada en un núcleo diminuto pero pesado.
8 Se ha indicado que el núcleo es pequeño en comparación con 10-8 cm. El experimento de la dispersión de las partículas a puede proporcionar el tamaño del núcleo, Cuando una partícula a es desviada 180, ella ha sufrido una colisión frontal con un núcleo. En dicha colisión, la partícula a se acerca al núcleo hasta que la energía potencial culómbica de repulsión zze 2 / r, llega a ser igual a su energía cinética inicial, (1/2)mv 2. De este modo la ecuación: (1/2mv 2 = (zze 2 ) / r min [V=W/q ; V= Kq /r =W/q ; W= Kqq /r ; q=ze ; q = Ze] [Donde z y Z son los números atómicos (número de unidades fundamentales de carga positiva 4.8x10-10 uee que hay en el átomo, de las partículas a y del núcleo dispersante)] nos permite calcular r min, la distancia de mayor acercamiento, si se conocen todos los otros factores. Para las partículas a, obtenidas de la desintegración del radio, v= 1.6x10 9 cm/s (velocidad máxima de la partícula a, para que llegue al núcleo pero no lo rompa; será la velocidad de la partícula cuando es emitida por el núcleo); e= 4.8x10-10 uee, m= 6.68x10-24 g, y si el núcleo dispersante es el cobre, Z= 29. Así, r min = (zze 2 ) / (1/2)mv 2 = [2x29x(4.8x10-10 ) 2 ] / (1/2)(6.68x10-24 )x(1.6x10 9 ) 2 = 1.7x10-12 cm
MODELOS ATÓMICOS 2ª PARTE
 MODELOS ATÓMICOS 2ª PARTE Teoría Atómica de Joseph John Thomson Diseño Experimental de Joseph John Thomson (1856-1940) Utiliza Tubos de Rayos Catódicos, en los cuales estudia el comportamiento de los gases
MODELOS ATÓMICOS 2ª PARTE Teoría Atómica de Joseph John Thomson Diseño Experimental de Joseph John Thomson (1856-1940) Utiliza Tubos de Rayos Catódicos, en los cuales estudia el comportamiento de los gases
LA TEORIA ATOMICA John Dalton
 LA TEORIA ATOMICA En 1808, un científico inglés, el profesor John Dalton, formuló una definición precisa de las unidades indivisibles con las que está formada la materia y que llamamos átomos 1766-1844
LA TEORIA ATOMICA En 1808, un científico inglés, el profesor John Dalton, formuló una definición precisa de las unidades indivisibles con las que está formada la materia y que llamamos átomos 1766-1844
Tema 2. Estructura atómica y sistema periódico
 Tema 2. Estructura atómica y sistema periódico Dalton: átomos par9culas indivisibles Nuevos experimentos: átomos cons>tuidos por unidades más pequeñas: par9culas subatómicas 1. Primeras evidencias de la
Tema 2. Estructura atómica y sistema periódico Dalton: átomos par9culas indivisibles Nuevos experimentos: átomos cons>tuidos por unidades más pequeñas: par9culas subatómicas 1. Primeras evidencias de la
Nacimiento de la teoría cuántica Antecedentes
 Estructura de la Materia Nacimiento de la teoría cuántica Antecedentes Martha M. Flores Leonar FQ UNAM 10 de febrero de 2016 CONTENIDO Magnitudes atómicas Nacimiento de la teoría cuántica Descubrimiento
Estructura de la Materia Nacimiento de la teoría cuántica Antecedentes Martha M. Flores Leonar FQ UNAM 10 de febrero de 2016 CONTENIDO Magnitudes atómicas Nacimiento de la teoría cuántica Descubrimiento
Enseñanza - Aprendizaje.
 Desde hace siglos el hombre consideró al átomo como una partícula componente de la materia. No podía verlo ni separarlo, pero su presencia fue admitida para explicar los diferentes fenómenos que se conocían.
Desde hace siglos el hombre consideró al átomo como una partícula componente de la materia. No podía verlo ni separarlo, pero su presencia fue admitida para explicar los diferentes fenómenos que se conocían.
La Teoría Cuántica Preguntas de Multiopcion
 Slide 1 / 71 La Teoría Cuántica Preguntas de Multiopcion Slide 2 / 71 1 El experimento de "rayos catódicos" se asocia con: A B C D E Millikan Thomson Townsend Plank Compton Slide 3 / 71 2 La carga del
Slide 1 / 71 La Teoría Cuántica Preguntas de Multiopcion Slide 2 / 71 1 El experimento de "rayos catódicos" se asocia con: A B C D E Millikan Thomson Townsend Plank Compton Slide 3 / 71 2 La carga del
Teoría de DALTON. Hechos experimentales que evidencian una estructura interna de átomo.
 Teoría de DALTON. 1- Los elementos químicos están construidos por partículas denominadas átomos, que son invisibles e inalterables, en cualquier proceso, químico o físico. 2- Los átomos de un mismo elemento,
Teoría de DALTON. 1- Los elementos químicos están construidos por partículas denominadas átomos, que son invisibles e inalterables, en cualquier proceso, químico o físico. 2- Los átomos de un mismo elemento,
EL ÁTOMO Modelos Atómicos
 EL ÁTOMO Modelos Atómicos Cómo está formada la materia en su interior? Desde los tiempos de la antigua Grecia,los pensadores venían haciéndose esta pregunta, acerca de cómo estaba constituida la materia
EL ÁTOMO Modelos Atómicos Cómo está formada la materia en su interior? Desde los tiempos de la antigua Grecia,los pensadores venían haciéndose esta pregunta, acerca de cómo estaba constituida la materia
Complejo Educacional Joaquín Edwards Bello QUIMICA 2º MEDIO TRABAJO 2 LEA CUIDADOSAMENTE EL SIGUIENTE TEXTO Y CONTESTE LAS PREGUNTAS
 Complejo Educacional Joaquín Edwards Bello QUIMICA 2º MEDIO TRABAJO 2 NOMBRE: CURSO: LEA CUIDADOSAMENTE EL SIGUIENTE TEXTO Y CONTESTE LAS PREGUNTAS..Naturaleza Eléctrica de la Materia La electricidad fue
Complejo Educacional Joaquín Edwards Bello QUIMICA 2º MEDIO TRABAJO 2 NOMBRE: CURSO: LEA CUIDADOSAMENTE EL SIGUIENTE TEXTO Y CONTESTE LAS PREGUNTAS..Naturaleza Eléctrica de la Materia La electricidad fue
INSTITUCION EDUCATIVA LA PRESENTACION NOMBRE DE LA ALUMNA: CIENCIAS NATURALES Y EDUCACION AMBIENTAL ASIGNATURA: CIENCIAS NATURALES NOTA:
 INSTITUCION EDUCATIVA LA PRESENTACION NOMBRE DE LA ALUMNA: AREA : CIENCIAS NATURALES Y EDUCACION AMBIENTAL ASIGNATURA: CIENCIAS NATURALES NOTA: DOCENTE: JOSÉ ROMÁN TIPO DE GUIA: CONCEPTUAL - EJERCITACION.
INSTITUCION EDUCATIVA LA PRESENTACION NOMBRE DE LA ALUMNA: AREA : CIENCIAS NATURALES Y EDUCACION AMBIENTAL ASIGNATURA: CIENCIAS NATURALES NOTA: DOCENTE: JOSÉ ROMÁN TIPO DE GUIA: CONCEPTUAL - EJERCITACION.
Física Cuántica Problemas de Practica AP Física B de PSI
 Física Cuántica Problemas de Practica AP Física B de PSI Nombre 1. El experimento de "rayos catódicos" se asocia con: (A) R. A. Millikan (B) J. J. Thomson (C) J. S. Townsend (D) M. Plank (E) A. H. Compton
Física Cuántica Problemas de Practica AP Física B de PSI Nombre 1. El experimento de "rayos catódicos" se asocia con: (A) R. A. Millikan (B) J. J. Thomson (C) J. S. Townsend (D) M. Plank (E) A. H. Compton
Atomos, Moleculas, y Iones
 Atomos, Moleculas, y Iones La teoría atómica de la materia John Dalton: Cada elemento esta compuesto por átomos. Todos los átomos de un elemento son iguales. En las reacciones químicas los átomos no sufren
Atomos, Moleculas, y Iones La teoría atómica de la materia John Dalton: Cada elemento esta compuesto por átomos. Todos los átomos de un elemento son iguales. En las reacciones químicas los átomos no sufren
Estructura de la Materia
 Estructura de la Materia Antes de 1800, se pensaba que la materia era continua, es decir que podía ser dividida en infinitas partes más pequeñas sin cambiar la naturaleza del elemento. Sin embargo, alrededor
Estructura de la Materia Antes de 1800, se pensaba que la materia era continua, es decir que podía ser dividida en infinitas partes más pequeñas sin cambiar la naturaleza del elemento. Sin embargo, alrededor
ESTRUCTURA DE LOS ATOMOS Ing. Alfredo Luis Rojas B.
 CAPITULO 4 ESTRUCTURA DE LOS ATOMOS Ing. Alfredo Luis Rojas B. Aproximadamente 400 a.c. el filosofo griego Democrito sugirió que toda la materia esta formada por partículas minúsculas, discretas e indivisibles,
CAPITULO 4 ESTRUCTURA DE LOS ATOMOS Ing. Alfredo Luis Rojas B. Aproximadamente 400 a.c. el filosofo griego Democrito sugirió que toda la materia esta formada por partículas minúsculas, discretas e indivisibles,
Enseñanza - Aprendizaje
 El primer modelo atómico con bases científicas, fue formulado por John Dalton descubrió a los átomos en 1804. Pensaba que eran las partículas más pequeñas de la materia, que no podían ser divididas en
El primer modelo atómico con bases científicas, fue formulado por John Dalton descubrió a los átomos en 1804. Pensaba que eran las partículas más pequeñas de la materia, que no podían ser divididas en
Tercero: una reacción química incluye sólo la separación combinación o reordenamiento de átomos sin crearlos o destruirlos.
 Coomppoonneennt teess ffuunnddaameennt taalleess ddeell áát toomoo El filósofo griego demócrito en el siglo V a.c. propuso la idea de que la materia estaba formada por partículas muy pequeñas indivisibles
Coomppoonneennt teess ffuunnddaameennt taalleess ddeell áát toomoo El filósofo griego demócrito en el siglo V a.c. propuso la idea de que la materia estaba formada por partículas muy pequeñas indivisibles
ÍNDICE. Primera Unidad: MECANICA. Segunda Unidad: CALOR 1. MEDIDA Y MOVIMIENTO
 ÍNDICE Primera Unidad: MECANICA 1. MEDIDA Y MOVIMIENTO El Sistema Métrico de Unidades modernizado Movimiento uniforme Movimiento acelerado INVESTIGACION: Movimiento acelerado La medida 2. FUERZA Y MOVIMIENTO
ÍNDICE Primera Unidad: MECANICA 1. MEDIDA Y MOVIMIENTO El Sistema Métrico de Unidades modernizado Movimiento uniforme Movimiento acelerado INVESTIGACION: Movimiento acelerado La medida 2. FUERZA Y MOVIMIENTO
EL ÁTOMO CONTENIDOS. ANTECEDENTES HISTÓRICOS. ( ) MODELOS ATÓMICOS. RAYOS CATÓDICOS. MODELO DE THOMSON.
 EL ÁTOMO CONTENIDOS. 1.- Antecedentes históricos.( ) 2.- Partículas subatómicas. ( ) 3.- Modelo atómico de Thomsom. 4.- Los rayos X. 5.- La radiactividad. 6.- Modelo atómico de Rutherford. 7.- Radiación
EL ÁTOMO CONTENIDOS. 1.- Antecedentes históricos.( ) 2.- Partículas subatómicas. ( ) 3.- Modelo atómico de Thomsom. 4.- Los rayos X. 5.- La radiactividad. 6.- Modelo atómico de Rutherford. 7.- Radiación
Como esta formada la materia?
 Como esta formada la materia? Demócrito, filósofo griego que vivió en el siglo IV a. C. propuso que, si se dividía la materia en trozos cada vez más pequeños, debería llegarse a una porción que ya no podría
Como esta formada la materia? Demócrito, filósofo griego que vivió en el siglo IV a. C. propuso que, si se dividía la materia en trozos cada vez más pequeños, debería llegarse a una porción que ya no podría
FISICA III. Departamento de Física y Química Escuela de Formación Básica GUÍA DE PROBLEMAS 1 - INTERACCIÓN ELÉCTRICA
 : FISICA III Departamento de Física y Química Escuela de Formación Básica GUÍA DE PROBLEMAS 1 - INTERACCIÓN ELÉCTRICA Temas Ley de Coulomb. Campo eléctrico Movimiento de una partícula cargada en un campo
: FISICA III Departamento de Física y Química Escuela de Formación Básica GUÍA DE PROBLEMAS 1 - INTERACCIÓN ELÉCTRICA Temas Ley de Coulomb. Campo eléctrico Movimiento de una partícula cargada en un campo
Modelo de Thomson. Este modelo del átomo es estable bajo fuerzas eléctricas. Figura 1.
 Modelo de Thomson El modelo atómico de Thomson es una teoría sobre la estructura atómica propuesta en 1904 por Joseph John Thomson, quien descubrió el electrón en 1898. El átomo está compuesto por electrones
Modelo de Thomson El modelo atómico de Thomson es una teoría sobre la estructura atómica propuesta en 1904 por Joseph John Thomson, quien descubrió el electrón en 1898. El átomo está compuesto por electrones
Técnico Profesional QUÍMICA
 Convenio Programa Técnico Profesional QUÍMICA Modelos atómicos, estructura atómica y tipos de átomos Nº Ejercicios PSU 1. Rutherford, luego de realizar pruebas con una lámina de oro bombardeada por partículas
Convenio Programa Técnico Profesional QUÍMICA Modelos atómicos, estructura atómica y tipos de átomos Nº Ejercicios PSU 1. Rutherford, luego de realizar pruebas con una lámina de oro bombardeada por partículas
Origen del Concepto Átomo MODELOS ATÓMICOS. Teoría o Modelo Atómico de Dalton (1808) Qué es un modelo en Ciencias?
 MODELOS ATÓMICOS Origen del Concepto Átomo Demócrito: Siglo IV (A.C.) Fundador de la Escuela Atomista los átomos son indivisibles (átomo), y se distinguen por forma, tamaño, orden y posición. Los átomos
MODELOS ATÓMICOS Origen del Concepto Átomo Demócrito: Siglo IV (A.C.) Fundador de la Escuela Atomista los átomos son indivisibles (átomo), y se distinguen por forma, tamaño, orden y posición. Los átomos
ELECTRONES PROTONES NEUTRONES
 C U R S O: QUÍMICA COMÚN MATERIAL QC N 01 PARTÍCULAS SUBATÓMICAS ELECTRONES Partícula subatómica de carga negativa. Se ubica fuera del núcleo y su masa es de aproximadamente 9,11 10-28 gramos. La cantidad
C U R S O: QUÍMICA COMÚN MATERIAL QC N 01 PARTÍCULAS SUBATÓMICAS ELECTRONES Partícula subatómica de carga negativa. Se ubica fuera del núcleo y su masa es de aproximadamente 9,11 10-28 gramos. La cantidad
UNIDAD 2. Tema 2.1 Estructura del átomo. Partículas subatómicas. Número atómico, masa atómica, número de masa. Isótopos.
 UNIDAD 2 Tema 2.1 Estructura del átomo. Partículas subatómicas. Número atómico, masa atómica, número de masa. Isótopos. 1 Teoría atómica de la materia Demócrito (460-370 a.c.): el mundo material está formado
UNIDAD 2 Tema 2.1 Estructura del átomo. Partículas subatómicas. Número atómico, masa atómica, número de masa. Isótopos. 1 Teoría atómica de la materia Demócrito (460-370 a.c.): el mundo material está formado
Si nosotros observamos a nuestro alrededor podríamos predecir de qué esta formada cada una de las cosas que nos rodea?
 Introducción Si nosotros observamos a nuestro alrededor podríamos predecir de qué esta formada cada una de las cosas que nos rodea? Por ejemplo: Podrías predecir de que están elaborados los objetos y sustancias
Introducción Si nosotros observamos a nuestro alrededor podríamos predecir de qué esta formada cada una de las cosas que nos rodea? Por ejemplo: Podrías predecir de que están elaborados los objetos y sustancias
El Campo Eléctrico. Distribuciones discretas de carga
 El Campo Eléctrico. Distribuciones discretas de carga 1. A qué distancia deben encontrarse dos cargas de 1 nc para que la fuerza de repulsión entre ellas sea de 0 1 N? DATO: K = 9 10 9 N m 2 /C 2 2. Dos
El Campo Eléctrico. Distribuciones discretas de carga 1. A qué distancia deben encontrarse dos cargas de 1 nc para que la fuerza de repulsión entre ellas sea de 0 1 N? DATO: K = 9 10 9 N m 2 /C 2 2. Dos
PARTÍCULAS DEL ÁTOMO MODELOS ATÓMICOS. TEMA 7 Pág. 155 libro nuevo
 PARTÍCULAS DEL ÁTOMO MODELOS ATÓMICOS TEMA 7 Pág. 155 libro nuevo DESCUBRIMIENTO DEL ÁTOMO. PARTÍCULAS SUBATÓMICAS En la antigua Grecia ya había dos teorías sobre la materia: Teoría Atomística (siglo IV
PARTÍCULAS DEL ÁTOMO MODELOS ATÓMICOS TEMA 7 Pág. 155 libro nuevo DESCUBRIMIENTO DEL ÁTOMO. PARTÍCULAS SUBATÓMICAS En la antigua Grecia ya había dos teorías sobre la materia: Teoría Atomística (siglo IV
Modelos Atómicos Objetivo:
 CORPORACION EDUCACIONAL JUAN XXIII COLEGIO "CARDENAL RAÚL SILVA HENRÍQUEZ" DEPARTAMENTO DE CIENCIAS QUÍMICA Modelos Atómicos Objetivo: Comprender la utilidad de los modelos atómicos y la teoría atómica
CORPORACION EDUCACIONAL JUAN XXIII COLEGIO "CARDENAL RAÚL SILVA HENRÍQUEZ" DEPARTAMENTO DE CIENCIAS QUÍMICA Modelos Atómicos Objetivo: Comprender la utilidad de los modelos atómicos y la teoría atómica
Física Experimental IV. Práctica III Determinación de e/m. Funes, Gustavo Giordano, Leandro Gulich, Damián Sotuyo, Sara.
 Física Experimental IV Práctica III Determinación de e/m Funes, Gustavo Giordano, Leandro Gulich, Damián Sotuyo, Sara Departamento de Física Facultad de Ciencias Exactas UNLP Sinopsis En el presente informe
Física Experimental IV Práctica III Determinación de e/m Funes, Gustavo Giordano, Leandro Gulich, Damián Sotuyo, Sara Departamento de Física Facultad de Ciencias Exactas UNLP Sinopsis En el presente informe
2º Bachillerato. Química. Unidad 1 (Estructura atómica de la materia). Fotocopia 1.
 Partículas subatómicas Los átomos están formados por un núcleo (formado por protones y neutrones) rodeado por una nube de electrones, que se encuentran en la corteza. Entre núcleo y corteza hay espacio
Partículas subatómicas Los átomos están formados por un núcleo (formado por protones y neutrones) rodeado por una nube de electrones, que se encuentran en la corteza. Entre núcleo y corteza hay espacio
Colegio Pasionista de Quilpué Departamento de Ciencias Ciencias Naturales 8 año básico 2015 Miss. Cecilia Rojas Olguín. El átomo.
 Colegio Pasionista de Quilpué Departamento de Ciencias Ciencias Naturales 8 año básico 2015 Miss. Cecilia Rojas Olguín El átomo 06 de Marzo 2015 Objetivos de la clase Comprender el Modelo corpuscular de
Colegio Pasionista de Quilpué Departamento de Ciencias Ciencias Naturales 8 año básico 2015 Miss. Cecilia Rojas Olguín El átomo 06 de Marzo 2015 Objetivos de la clase Comprender el Modelo corpuscular de
Colegio Alberto Pérez Institución Teresiana Departamento de Ciencias Química Profesora Caterina González Poblete. Núcleo. (protones y neutrones)
 Colegio Alberto Pérez Institución Teresiana Departamento de Ciencias Química Profesora Caterina González Poblete EL ÁTOMO Núcleo Envoltura (electrones) (protones y neutrones) El átomo, como lo conocemos
Colegio Alberto Pérez Institución Teresiana Departamento de Ciencias Química Profesora Caterina González Poblete EL ÁTOMO Núcleo Envoltura (electrones) (protones y neutrones) El átomo, como lo conocemos
MAGNETISMO. MsC Alexander Pérez García Video 1
 MAGNETISMO MsC Alexander Pérez García Video 1 http://www.dailymotion.com/video/xqqir9_campomagnetico-terrestre-inversion-de-los-polos_school FUERZA MAGNÉTICA SOBRE UNA CARGA EN MOVIMIENTO LA SEGUNDA
MAGNETISMO MsC Alexander Pérez García Video 1 http://www.dailymotion.com/video/xqqir9_campomagnetico-terrestre-inversion-de-los-polos_school FUERZA MAGNÉTICA SOBRE UNA CARGA EN MOVIMIENTO LA SEGUNDA
Potencial Eléctrico Preguntas de Multiopción
 Slide 1 / 72 Potencial Eléctrico Preguntas de Multiopción Slide 2 / 72 1 Una carga negativa se coloca en una esfera de conducción. Cual de las afirmaciones es verdadera acerca a la distribución de carga?
Slide 1 / 72 Potencial Eléctrico Preguntas de Multiopción Slide 2 / 72 1 Una carga negativa se coloca en una esfera de conducción. Cual de las afirmaciones es verdadera acerca a la distribución de carga?
2 La carga del electrón fue determinada por primera vez en: D Difracción de electrones a partir del papel de aluminio.
 Slide 1 / 32 1 Un Tubo de Crooke (un tubo que contiene gas rarificado a través del cual se hace pasar una corriente entre un cátodo y un ánodo) fue utilizado en el descubrimiento del electrón por: A R.
Slide 1 / 32 1 Un Tubo de Crooke (un tubo que contiene gas rarificado a través del cual se hace pasar una corriente entre un cátodo y un ánodo) fue utilizado en el descubrimiento del electrón por: A R.
Clase 4:Radiación del cuerpo, efecto fotoeléctrico y modelos atómicos
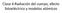 Clase 4:Radiación del cuerpo, efecto fotoeléctrico y modelos atómicos El experimento de Millikan Determina la carga del electrón 1.602 x 10-19 C Atomizador de gotas de aceite Fuente de Rayos X (ioniza
Clase 4:Radiación del cuerpo, efecto fotoeléctrico y modelos atómicos El experimento de Millikan Determina la carga del electrón 1.602 x 10-19 C Atomizador de gotas de aceite Fuente de Rayos X (ioniza
El mundo material: los átomos. Física y Química 2º ESO
 El mundo material: los átomos Física y Química 2º ESO Viaje a lo más profundo de la materia Oxford University Press España, S. A. Física y Química 2º ESO 2 Hoy en día sabemos que la materia está constituida
El mundo material: los átomos Física y Química 2º ESO Viaje a lo más profundo de la materia Oxford University Press España, S. A. Física y Química 2º ESO 2 Hoy en día sabemos que la materia está constituida
U N A M. Facultad de Ingeniería MODELO ATÓMICO DE J. J. THOMSON MODELO ATÓMICO DE ERNEST RUTHERFORD DESCUBRIMIENTO DEL PROTÓN Y DEL NEUTRON
 MODELO ATÓMICO DE J. J. THOMSON MODELO ATÓMICO DE ERNEST RUTHERFORD DESCUBRIMIENTO DEL PROTÓN Y DEL NEUTRON M. C. Q. Alfredo Velásquez Márquez Modelo Atómico de J. J. Thomson Electrones de Carga Negativa
MODELO ATÓMICO DE J. J. THOMSON MODELO ATÓMICO DE ERNEST RUTHERFORD DESCUBRIMIENTO DEL PROTÓN Y DEL NEUTRON M. C. Q. Alfredo Velásquez Márquez Modelo Atómico de J. J. Thomson Electrones de Carga Negativa
J.J Thomson propone el primer modelo de átomo:
 MODELOS ATÓMICOS. DALTON En 1808, Dalton publicó sus ideas sobre el modelo atómico de la materia las cuales han servido de base a la química moderna. Los principios fundamentales de esta teoría son: 1.
MODELOS ATÓMICOS. DALTON En 1808, Dalton publicó sus ideas sobre el modelo atómico de la materia las cuales han servido de base a la química moderna. Los principios fundamentales de esta teoría son: 1.
Unidad II 2.1 Estructura del átomo
 Unidad II 2.1 Estructura del átomo Química general I Alfonso Rito Norma López 1 El átomo en la antigüedad Demócrito introdujo el concepto de átomo, como la constitución de la materia por partículas indivisibles.
Unidad II 2.1 Estructura del átomo Química general I Alfonso Rito Norma López 1 El átomo en la antigüedad Demócrito introdujo el concepto de átomo, como la constitución de la materia por partículas indivisibles.
Primeros modelos atómicos. Demócrito y Leucipo. Aristóteles
 Primeros modelos atómicos Demócrito y Leucipo Aristóteles Según la teoría atómica de la materia de Demócrito: Todas las cosas están compuestas de partículas diminutas, invisibles e indestructibles de materia
Primeros modelos atómicos Demócrito y Leucipo Aristóteles Según la teoría atómica de la materia de Demócrito: Todas las cosas están compuestas de partículas diminutas, invisibles e indestructibles de materia
Evolución de los modelos atómicos
 Evolución de los modelos atómicos Un paso importante hacia el desarrollo de la química como ciencia fue el desarrollo de la comprensión de la estructura atómica. Por ejemplo, era posible comprender lo
Evolución de los modelos atómicos Un paso importante hacia el desarrollo de la química como ciencia fue el desarrollo de la comprensión de la estructura atómica. Por ejemplo, era posible comprender lo
TEMA 4: ESTRUCTURA DEL ÁTOMO IES ATENEA 3º DE ESO FÍSICA Y QUÍMICA
 TEMA 4: ESTRUCTURA DEL ÁTOMO IES ATENEA 3º DE ESO FÍSICA Y QUÍMICA 1. MATERIA DIVISIBLE O INDIVISIBLE El término átomo aparece en el siglo IV a.c. para designar a la porción indivisible más pequeña que
TEMA 4: ESTRUCTURA DEL ÁTOMO IES ATENEA 3º DE ESO FÍSICA Y QUÍMICA 1. MATERIA DIVISIBLE O INDIVISIBLE El término átomo aparece en el siglo IV a.c. para designar a la porción indivisible más pequeña que
g planeta = g tierra / 2 = 4 9 m/s 2 v planeta = 11 2 / 2 = 5 6 km/s
 PAU MADRID JUNIO 2003 Cuestión 1.- Suponiendo un planeta esférico que tiene un radio la mitad del radio terrestre e igual densidad que la tierra, calcule: a) La aceleración de la gravedad en la superficie
PAU MADRID JUNIO 2003 Cuestión 1.- Suponiendo un planeta esférico que tiene un radio la mitad del radio terrestre e igual densidad que la tierra, calcule: a) La aceleración de la gravedad en la superficie
XXVII Olimpiada Española de Física
 XXVII Olimpiada Española de Física FASE LOCAL-UNIVERSIDADES DE GALICIA- 26 de febrero de 2016 APELLIDOS...NOMBRE... CENTRO... Nota: En el caso de que la respuesta a alguna de las cuestiones planteadas
XXVII Olimpiada Española de Física FASE LOCAL-UNIVERSIDADES DE GALICIA- 26 de febrero de 2016 APELLIDOS...NOMBRE... CENTRO... Nota: En el caso de que la respuesta a alguna de las cuestiones planteadas
Actividad introductoria
 Grado 10 Ciencias naturales Unidad 2 De qué está hecho todo lo que nos rodea? Tema Qué tan rápido viajan las moléculas de nitrógeno y oxígeno en el aire? Curso: Nombre: Actividad introductoria Lee con
Grado 10 Ciencias naturales Unidad 2 De qué está hecho todo lo que nos rodea? Tema Qué tan rápido viajan las moléculas de nitrógeno y oxígeno en el aire? Curso: Nombre: Actividad introductoria Lee con
PROBLEMAS COMPLEMENTARIOS
 Problema nº1 Indica si dos protones separados por 10-18 m tenderán a acercarse por efecto de la gravedad o a repelerse por efecto electrostático. Datos: G = 6,6 10-11 N m 2 / 2, m p = 1,6 10-27, q p =
Problema nº1 Indica si dos protones separados por 10-18 m tenderán a acercarse por efecto de la gravedad o a repelerse por efecto electrostático. Datos: G = 6,6 10-11 N m 2 / 2, m p = 1,6 10-27, q p =
RELACIÓN CARGA - MASA DEL ELECTRÓN
 Práctica 5 RELACIÓN CARGA - MASA DEL ELECTRÓN OBJETIVO Determinar la relación carga-masa del electrón (e/m e ), a partir de las trayectorias observadas de un haz de electrones que cruza una región en la
Práctica 5 RELACIÓN CARGA - MASA DEL ELECTRÓN OBJETIVO Determinar la relación carga-masa del electrón (e/m e ), a partir de las trayectorias observadas de un haz de electrones que cruza una región en la
25 12 Mg. 1. En la especie el numero atómico corresponde a: A) 22 B) 12 C) 25 D) 13 E) ninguna de las anteriores.
 MINIPRUEBA CLASE 02 25 12 Mg 1. En la especie el numero atómico corresponde a: A) 22 B) 12 C) 25 D) 13 E) ninguna de las anteriores. 25 12 Mg Z 2. Se puede afirmar que: I) La masa del electrón es aproximadamente
MINIPRUEBA CLASE 02 25 12 Mg 1. En la especie el numero atómico corresponde a: A) 22 B) 12 C) 25 D) 13 E) ninguna de las anteriores. 25 12 Mg Z 2. Se puede afirmar que: I) La masa del electrón es aproximadamente
R 5,69 10 m. q v B 1, ,6 10 N
 Campo Magnético 01. Un electrón que se mueve a través de un tubo de rayos catódicos a 10 7 m/s, penetra perpendicularmente en un campo de 10-3 T que actúa sobre una zona de 4 cm a lo largo del tubo. Calcula:
Campo Magnético 01. Un electrón que se mueve a través de un tubo de rayos catódicos a 10 7 m/s, penetra perpendicularmente en un campo de 10-3 T que actúa sobre una zona de 4 cm a lo largo del tubo. Calcula:
NATURALEZA CORPUSCULAR DE LA MATERIA
 NATURALEZA CORPUSCULAR DE LA MATERIA Naturaleza atómica de la materia. Composición de los átomos. Modelo atómico de Thompson. Modelo atómico de Rutherford. Espectros de emisión. Modelo atómico de Bohr
NATURALEZA CORPUSCULAR DE LA MATERIA Naturaleza atómica de la materia. Composición de los átomos. Modelo atómico de Thompson. Modelo atómico de Rutherford. Espectros de emisión. Modelo atómico de Bohr
DEPARTAMENTO DE QUÍMICA SERIE DE EJERCICIOS. Tema 1: Estructura Atómica Semestre
 DEPARTAMENTO DE QUÍMICA SERIE DE EJERCICIOS (Basada en reactivos de exámenes colegiados) Tema 1: Estructura Atómica Semestre 2017-2 Experimento de Thomson 1. En un experimento como el de Thomson, un haz
DEPARTAMENTO DE QUÍMICA SERIE DE EJERCICIOS (Basada en reactivos de exámenes colegiados) Tema 1: Estructura Atómica Semestre 2017-2 Experimento de Thomson 1. En un experimento como el de Thomson, un haz
Bloque 1. La descripción del movimiento y la fuerza... 14
 Conoce tu libro 10 Bloque 1. La descripción del movimiento y la fuerza... 14 Entrada de bloque 14 Secuencia 1. El movimiento de los objetos 16 Marco de referencia y trayectoria; diferencia entre desplazamiento
Conoce tu libro 10 Bloque 1. La descripción del movimiento y la fuerza... 14 Entrada de bloque 14 Secuencia 1. El movimiento de los objetos 16 Marco de referencia y trayectoria; diferencia entre desplazamiento
Un modelo atómico, por lo tanto consiste en representar de manera grafica, la dimensión atómica de la materia. El objetivo de estos modelos es que el
 Modelos atómicos Debido a que no se podían ver los átomos los científicos crearon modelos para describirlos, éstos fueron evolucionando a lo largo de la historia a medida que se descubrieron nuevas cosas.
Modelos atómicos Debido a que no se podían ver los átomos los científicos crearon modelos para describirlos, éstos fueron evolucionando a lo largo de la historia a medida que se descubrieron nuevas cosas.
producción de energía en las estrellas interiores estelares
 producción de energía en las estrellas interiores estelares porqué brillan las estrellas? la energía emitida por las estrellas tiene su origen en reacciones termonucleares que tienen lugar en su interior
producción de energía en las estrellas interiores estelares porqué brillan las estrellas? la energía emitida por las estrellas tiene su origen en reacciones termonucleares que tienen lugar en su interior
Teoría atómica de la materia Demócrito ( a.c.): el mundo material está formado de pequeñas partículas indestructibles (átomos), desprovistas de
 UNIDAD 2 Tema 2.1 Estructura del átomo. Partículas subatómicas. Número atómico, masa atómica, número de masa. Isótopos. 1 Teoría atómica de la materia Demócrito (460-370 a.c.): el mundo material está formado
UNIDAD 2 Tema 2.1 Estructura del átomo. Partículas subatómicas. Número atómico, masa atómica, número de masa. Isótopos. 1 Teoría atómica de la materia Demócrito (460-370 a.c.): el mundo material está formado
Antecedentes de Química. Autora: Violeta Luz María Bravo Hernández
 Antecedentes de Química Autora: Violeta Luz María Bravo Hernández CONTENIDO 1. Descubrimiento del electrón, protón y neutrón. 2. Modelo atómico de Thomson. 3. Modelo atómico de Rutherford. 4. Modelo atómico
Antecedentes de Química Autora: Violeta Luz María Bravo Hernández CONTENIDO 1. Descubrimiento del electrón, protón y neutrón. 2. Modelo atómico de Thomson. 3. Modelo atómico de Rutherford. 4. Modelo atómico
Teoría es un principio unificador que explica un conjunto de hechos y aquellas leyes que se basan en ellos.
 Página 1 de 6 Repaso de Química 105 I. Método científico Pasos Basicos Observación Representación Interpretación Hipótesis explicación tentativa de un problema. Nos guia para planear experimentos adicionales.
Página 1 de 6 Repaso de Química 105 I. Método científico Pasos Basicos Observación Representación Interpretación Hipótesis explicación tentativa de un problema. Nos guia para planear experimentos adicionales.
ESTRUCTURA ATÓMICA DE LA MATERIA
 ESTRUCTURA ATÓMICA DE LA MATERIA 1.MODELOS ATÓMICOS: EVOLUCIÓN HISTÓRICA. Fueron los griegos los primeros en profundizar en el conocimiento de la estructura íntima de la materia. Postularon que la materia
ESTRUCTURA ATÓMICA DE LA MATERIA 1.MODELOS ATÓMICOS: EVOLUCIÓN HISTÓRICA. Fueron los griegos los primeros en profundizar en el conocimiento de la estructura íntima de la materia. Postularon que la materia
RELACIÓN CARGA/MASA DEL ELECTRÓN
 RELACIÓN CARGA/MASA DEL ELECTRÓN Objetivo Determinar el cociente de la carga eléctrica del electrón entre su masa. Introducción En 1897 J. J. Thomson realizó un experimento crucial que consistió en medir
RELACIÓN CARGA/MASA DEL ELECTRÓN Objetivo Determinar el cociente de la carga eléctrica del electrón entre su masa. Introducción En 1897 J. J. Thomson realizó un experimento crucial que consistió en medir
Descarga Glow. Introducción. Características de la descarga glow
 Descarga Glow Introducción La descarga glow es una descarga eléctrica autosostenida que se produce en un medio gaseoso. Consideremos un dispositivo como el que se esquematiza en la Figura 1. Una fuente
Descarga Glow Introducción La descarga glow es una descarga eléctrica autosostenida que se produce en un medio gaseoso. Consideremos un dispositivo como el que se esquematiza en la Figura 1. Una fuente
TEMA 7: ELEMENTOS Y COMPUESTOS
 TEMA 7: ELEMENTOS Y COMPUESTOS FÍSICA Y QUÍMICA 4º ESO IES ZOCO LAS PARTÍCULAS DEL ÁTOMO MODELO ATÓMICO DE DALTON Cada elemento químico se compone de partículas diminutas e indestructibles denominadas
TEMA 7: ELEMENTOS Y COMPUESTOS FÍSICA Y QUÍMICA 4º ESO IES ZOCO LAS PARTÍCULAS DEL ÁTOMO MODELO ATÓMICO DE DALTON Cada elemento químico se compone de partículas diminutas e indestructibles denominadas
UNIDAD 2: ESTADO GASEOSO
 UNIDAD 2: ESTADO GASEOSO 1 CARACTERISTICAS DE LOS GASES Los gases poseen masa y ocupan un determinado volumen en el espacio, este volumen queda determinado por el volumen del recipiente que los contiene.
UNIDAD 2: ESTADO GASEOSO 1 CARACTERISTICAS DE LOS GASES Los gases poseen masa y ocupan un determinado volumen en el espacio, este volumen queda determinado por el volumen del recipiente que los contiene.
Teoría atómica de Dalton (1803)
 EL ÁTOMO DIVISIBLE El átomo Desde los tiempos de la antigua Grecia,los pensadores se preguntaban cómo estaba constituida la materia en su interior? Demócrito (S.V a.c.) introduce el término de átomo como
EL ÁTOMO DIVISIBLE El átomo Desde los tiempos de la antigua Grecia,los pensadores se preguntaban cómo estaba constituida la materia en su interior? Demócrito (S.V a.c.) introduce el término de átomo como
PORTAFOLIO DE EVIDENCIAS QUÍMICA I DE SEGUNDA OPORTUNIDAD I LEE DETENIDAMENTE CADA ENUNCIADO Y CONTESTA SEGÚN SE TE PIDA.
 PORTAFOLIO DE EVIDENCIAS QUÍMICA I DE SEGUNDA OPORTUNIDAD I LEE DETENIDAMENTE CADA ENUNCIADO Y CONTESTA SEGÚN SE TE PIDA. 1.- Ciencia que estudia las características y la composición de los materiales,
PORTAFOLIO DE EVIDENCIAS QUÍMICA I DE SEGUNDA OPORTUNIDAD I LEE DETENIDAMENTE CADA ENUNCIADO Y CONTESTA SEGÚN SE TE PIDA. 1.- Ciencia que estudia las características y la composición de los materiales,
Unidad 1 Estructura atómica de la materia. Teoría cuántica
 Unidad 1 Estructura atómica de la materia. Teoría cuántica 1.El átomo y la constitución de la materia DALTON NO ACEPTADO POR LOS FÍSICOS que creían en la idea de que los átomos se encontraban como disueltos
Unidad 1 Estructura atómica de la materia. Teoría cuántica 1.El átomo y la constitución de la materia DALTON NO ACEPTADO POR LOS FÍSICOS que creían en la idea de que los átomos se encontraban como disueltos
Modelos atómicos. JOHN DALTON: Modelo atómico en forma de esfera
 M1 Modelos atómicos JOHN DALTON: Modelo atómico en forma de esfera Muchos años después de que se planteó la existencia de los átomos y que éstos eran la parte fundamental de todo lo que fuera materia,
M1 Modelos atómicos JOHN DALTON: Modelo atómico en forma de esfera Muchos años después de que se planteó la existencia de los átomos y que éstos eran la parte fundamental de todo lo que fuera materia,
DINÁMICA DE UN ELÉCTRON EN UN CAMPO ELÉCTRICO UNIFORME
 DINÁMICA DE UN ELÉCTRON EN UN CAMPO ELÉCTRICO UNIFORME Maicol Llano Moncada, Alex Rollero Dita, Carlos Martínez Agudelo, Luis Santos ID: 000294172, ID: 000293236, ID: 000170111, ID: 000292336 Maicol.llano@upb.edu.co,
DINÁMICA DE UN ELÉCTRON EN UN CAMPO ELÉCTRICO UNIFORME Maicol Llano Moncada, Alex Rollero Dita, Carlos Martínez Agudelo, Luis Santos ID: 000294172, ID: 000293236, ID: 000170111, ID: 000292336 Maicol.llano@upb.edu.co,
Pasaje de partículas cargadas por la materia. Efecto Cherenkov. Bremsstrahlung Laura C. Damonte 2014
 Pasaje de partículas cargadas por la materia. Efecto Cherenkov. Bremsstrahlung Laura C. Damonte 014 Pasaje de partículas cargadas por la materia Cuando una partícula cargada atraviesa materia, alguno o
Pasaje de partículas cargadas por la materia. Efecto Cherenkov. Bremsstrahlung Laura C. Damonte 014 Pasaje de partículas cargadas por la materia Cuando una partícula cargada atraviesa materia, alguno o
PROGRAMA DE ESTUDIOS
 PROPÓSITO DEL MODULO: Interpretar las partículas cargadas que componen el átomo y el comportamiento cuántico de la luz a partir del análisis de estos elementos en la materia y de sus demostraciones analíticas
PROPÓSITO DEL MODULO: Interpretar las partículas cargadas que componen el átomo y el comportamiento cuántico de la luz a partir del análisis de estos elementos en la materia y de sus demostraciones analíticas
Modelo atómico de la materia.
 Modelo atómico de la materia. La Teoría Atómica se basa en la suposición (ratificada después por datos experimentales) de que la materia no es continua, sino que está formada por partículas distintas.
Modelo atómico de la materia. La Teoría Atómica se basa en la suposición (ratificada después por datos experimentales) de que la materia no es continua, sino que está formada por partículas distintas.
Contenidos 1. La medida: Magnitud y unidad. Sistema internacional de unidades. Múltiplos y submúltiplos. Notación científica.
 Objetivos La enseñanza de la Física y Química de 3º ESO tendrá como finalidad el desarrollo de las siguientes capacidades: 1. Reconocer y valorar las aportaciones de la ciencia para la mejora de las condiciones
Objetivos La enseñanza de la Física y Química de 3º ESO tendrá como finalidad el desarrollo de las siguientes capacidades: 1. Reconocer y valorar las aportaciones de la ciencia para la mejora de las condiciones
Definición de unidad de masa atómica
 Definición de unidad de masa atómica Página Definición de amu (atomic mass unit): amu es la doceava parte de la masa de un átomo C aislado, en reposo, y en su estado fundamental. amu g N A g N A,66054.0
Definición de unidad de masa atómica Página Definición de amu (atomic mass unit): amu es la doceava parte de la masa de un átomo C aislado, en reposo, y en su estado fundamental. amu g N A g N A,66054.0
Carga Eléctrica. Una propiedad fundamental de la materia ya observada desde la antigüedad. Los cuerpos pueden cargarse eléctricamente por frotamiento.
 ELECTROSTATICA Carga Eléctrica Una propiedad fundamental de la materia ya observada desde la antigüedad. Los cuerpos pueden cargarse eléctricamente por frotamiento. Aparecen fuerzas de atracción n o repulsión
ELECTROSTATICA Carga Eléctrica Una propiedad fundamental de la materia ya observada desde la antigüedad. Los cuerpos pueden cargarse eléctricamente por frotamiento. Aparecen fuerzas de atracción n o repulsión
LEY DE COULOMB Y CAMPO ELECTRICO
 LEY DE COULOMB Y CAMPO ELECTRICO 1. Dos monedas reposan sobre una mesa, con una separación de 1.5m y contienen cargas idénticas. De qué magnitud es la carga en cada una si una de las monedas experimenta
LEY DE COULOMB Y CAMPO ELECTRICO 1. Dos monedas reposan sobre una mesa, con una separación de 1.5m y contienen cargas idénticas. De qué magnitud es la carga en cada una si una de las monedas experimenta
CÓMO DETECTAR UN CAMPO ELÉCTRICO?
 CAMPO ELÉCTRICO! E Es aquella región de espacio que rodea a una carga eléctrica. Este campo funciona como transmisor mediante el cual una carga interactúa con otra que está a su alrededor CÓMO DETECTAR
CAMPO ELÉCTRICO! E Es aquella región de espacio que rodea a una carga eléctrica. Este campo funciona como transmisor mediante el cual una carga interactúa con otra que está a su alrededor CÓMO DETECTAR
Programa de Acceso Inclusivo, Equidad y Permanencia PAIEP U. de Santiago. Química
 Modelos atómicos Los filósofos de la antigüedad especularon sobre cómo estaba formada la materia. Demócrito (460-370 a.c) y otros filósofos anteriores a él, pensaban que el mundo material debería estar
Modelos atómicos Los filósofos de la antigüedad especularon sobre cómo estaba formada la materia. Demócrito (460-370 a.c) y otros filósofos anteriores a él, pensaban que el mundo material debería estar
índice ~
 - ---------------- índice ~ Página CAPíTULO 1 CONCEPTOS FUNDAMENTALES 23 1. MATERIA 2. MASA Y PESO 3. VOLUMEN 4. MEDICIÓN 4.1 Unidades fundamentales o patrones de medición unidades SI 5. OPERACIONES MATEMÁTICAS
- ---------------- índice ~ Página CAPíTULO 1 CONCEPTOS FUNDAMENTALES 23 1. MATERIA 2. MASA Y PESO 3. VOLUMEN 4. MEDICIÓN 4.1 Unidades fundamentales o patrones de medición unidades SI 5. OPERACIONES MATEMÁTICAS
Tema 5.-Corriente eléctrica
 Tema 5: Corriente eléctrica Fundamentos Físicos de la ngeniería Primer curso de ngeniería ndustrial Curso 2009/2010 Dpto. Física plicada 1 Índice ntroducción Corriente eléctrica Sentido de la corriente
Tema 5: Corriente eléctrica Fundamentos Físicos de la ngeniería Primer curso de ngeniería ndustrial Curso 2009/2010 Dpto. Física plicada 1 Índice ntroducción Corriente eléctrica Sentido de la corriente
ESTRUCTURA ATOMICA FINES DEL SIGLO XIX Y COMIENZOS DEL SIGLO XX
 ESTRUCTURA ATOMICA FINES DEL SIGLO XIX Y COMIENZOS DEL SIGLO XX William Crookes, (1832-1919). Químico y Físico inglés. Inventó y diseñó el tubo electrónico conocido como «tubo de Crookes». Demostró que
ESTRUCTURA ATOMICA FINES DEL SIGLO XIX Y COMIENZOS DEL SIGLO XX William Crookes, (1832-1919). Químico y Físico inglés. Inventó y diseñó el tubo electrónico conocido como «tubo de Crookes». Demostró que
El átomo y el sistema periódico
 El átomo y el sistema periódico Conceptos previos Notación A-Z Conceptos previos En las reacciones químicas se cumple: 1) La ley de conservación de la masa 2) La ley de proporciones definidas Modelos atómicos
El átomo y el sistema periódico Conceptos previos Notación A-Z Conceptos previos En las reacciones químicas se cumple: 1) La ley de conservación de la masa 2) La ley de proporciones definidas Modelos atómicos
Capítulo 1. Antecedentes de la Química Cuántica y primeras Teorías Atómicas
 Capítulo 1. Antecedentes de la Química Cuántica y primeras Teorías Atómicas Objetivos: Recordar y actualizar los conocimientos sobre las características de electrones, protones y neutrones Describir la
Capítulo 1. Antecedentes de la Química Cuántica y primeras Teorías Atómicas Objetivos: Recordar y actualizar los conocimientos sobre las características de electrones, protones y neutrones Describir la
TEMA 3 LA MATERIA Y SU ESTRUCTURA
 TEMA 3 LA MATERIA Y SU ESTRUCTURA 1. Clasificación de la materia (página 58) Def. Sistema material: Es una porción de materia seleccionada para su estudio. Def. Sustancia pura: Decimos que una sustancia
TEMA 3 LA MATERIA Y SU ESTRUCTURA 1. Clasificación de la materia (página 58) Def. Sistema material: Es una porción de materia seleccionada para su estudio. Def. Sustancia pura: Decimos que una sustancia
Tema 5.-Corriente eléctrica
 Tema 5: Corriente eléctrica Fundamentos Físicos de la Ingeniería Primer curso de Ingeniería Industrial Curso 2006/2007 Dpto. Física Aplicada III Universidad de Sevilla 1 Índice Introducción Corriente eléctrica
Tema 5: Corriente eléctrica Fundamentos Físicos de la Ingeniería Primer curso de Ingeniería Industrial Curso 2006/2007 Dpto. Física Aplicada III Universidad de Sevilla 1 Índice Introducción Corriente eléctrica
Problemas de Potencial Eléctrico
 Problemas de Potencial Eléctrico Física de PSI Nombre Multiopción 1. Una carga negativa se coloca en una esfera de conducción. Cual de las afirmaciones es verdadera acerca a la distribución de la carga?
Problemas de Potencial Eléctrico Física de PSI Nombre Multiopción 1. Una carga negativa se coloca en una esfera de conducción. Cual de las afirmaciones es verdadera acerca a la distribución de la carga?
QUIMICA CUANTICA. Trabajos Prácticos: Resolución de problemas Cálculos computacionales
 Contenidos Mínimos: Formalismos Matemáticos de Química Cuántica Métodos computacionales Formalismos mecano cuánticos. Tratamiento atómico y molecular Aplicaciones a moléculas sencillas. Trabajos Prácticos:
Contenidos Mínimos: Formalismos Matemáticos de Química Cuántica Métodos computacionales Formalismos mecano cuánticos. Tratamiento atómico y molecular Aplicaciones a moléculas sencillas. Trabajos Prácticos:
SOLUCIONARIO Guía Estándar Anual
 SOLUCIONARIO Guía Estándar Anual Teoría atómica I: modelos atómicos, estructura atómica y tipos de átomos SGUICES001CB33-A16V1 Ítem Alternativa Habilidad 1 E Reconocimiento 2 B Aplicación 3 B Aplicación
SOLUCIONARIO Guía Estándar Anual Teoría atómica I: modelos atómicos, estructura atómica y tipos de átomos SGUICES001CB33-A16V1 Ítem Alternativa Habilidad 1 E Reconocimiento 2 B Aplicación 3 B Aplicación
MODELOS ATÓMICOS. Demócrito
 MODELOS ATÓMICOS Demócrito En enseñaban la teoría de que todas las cosas materiales del mundo que nos rodea estaban formadas por partículas pequeñas e indivisibles a las que llamó átomo (del griego: a=no,
MODELOS ATÓMICOS Demócrito En enseñaban la teoría de que todas las cosas materiales del mundo que nos rodea estaban formadas por partículas pequeñas e indivisibles a las que llamó átomo (del griego: a=no,
SEGUNDA EVALUACIÓN DE FÍSICA NIVEL 0-B
 ESCUELA SUPERIOR POLITÉCNICA DEL LITORAL INSTITUTO DE CIENCIAS FÍSICAS SEGUNDA EVALUACIÓN DE FÍSICA NIVEL 0-B (Septiembre 3 del 2010) NO ABRIR esta prueba hasta que los profesores den la autorización.
ESCUELA SUPERIOR POLITÉCNICA DEL LITORAL INSTITUTO DE CIENCIAS FÍSICAS SEGUNDA EVALUACIÓN DE FÍSICA NIVEL 0-B (Septiembre 3 del 2010) NO ABRIR esta prueba hasta que los profesores den la autorización.
LOS ÁTOMOS. En una reacción química, la masa total de los reactivos es igual a la masa total de las sustancias obtenidas tras el proceso.
 LOS ÁTOMOS 1. LEYES PONDERALES. MODELO ATÓMICO DE DALTON Se denominan leyes ponderales de las reacciones químicas aquellas que establecen las proporciones de los pesos en cualquier proceso químico. Son
LOS ÁTOMOS 1. LEYES PONDERALES. MODELO ATÓMICO DE DALTON Se denominan leyes ponderales de las reacciones químicas aquellas que establecen las proporciones de los pesos en cualquier proceso químico. Son
EXPERIMENTO DE J. J. THOMSON
 EXPERIMENTO DE J. J. THOMSON (Determinación de la Relación Carga/Masa de los Electrones) M. C. Q. Alfredo Velásquez Márquez Tubo de Geissler (~1857) Con gas a presión normal se observa poca conductividad,
EXPERIMENTO DE J. J. THOMSON (Determinación de la Relación Carga/Masa de los Electrones) M. C. Q. Alfredo Velásquez Márquez Tubo de Geissler (~1857) Con gas a presión normal se observa poca conductividad,
Última modificación: 1 de agosto de
 Contenido CAMPO ELÉCTRICO EN CONDICIONES ESTÁTICAS 1.- Naturaleza del electromagnetismo. 2.- Ley de Coulomb. 3.- Campo eléctrico de carga puntual. 4.- Campo eléctrico de línea de carga. 5.- Potencial eléctrico
Contenido CAMPO ELÉCTRICO EN CONDICIONES ESTÁTICAS 1.- Naturaleza del electromagnetismo. 2.- Ley de Coulomb. 3.- Campo eléctrico de carga puntual. 4.- Campo eléctrico de línea de carga. 5.- Potencial eléctrico
DEPARTAMENTO DE FÍSICA DE LA UNIVERSIDAD DE SONORA ORGANIZACIÓN DE LA MATERIA DE FÍSICA III
 DEPARTAMENTO DE FÍSICA DE LA UNIVERSIDAD DE SONORA ORGANIZACIÓN DE LA MATERIA DE FÍSICA III HERMOSILLO, SONORA, OCTUBRE DEL 2005 NOMBRE: FISICA III CON LABORATORIO UNIDAD REGIONAL: CENTRO EJE BÁSICO DE
DEPARTAMENTO DE FÍSICA DE LA UNIVERSIDAD DE SONORA ORGANIZACIÓN DE LA MATERIA DE FÍSICA III HERMOSILLO, SONORA, OCTUBRE DEL 2005 NOMBRE: FISICA III CON LABORATORIO UNIDAD REGIONAL: CENTRO EJE BÁSICO DE
QUIMICA GENERAL. Docente : Raquel Villafrades Torres
 Universidad Pontificia Bolivariana QUIMICA GENERAL Docente : Raquel Villafrades Torres TEORIA ATOMICA DE DALTON (1808) BASES Ley de conservación de la masa: La masa total de las sustancias presentes después
Universidad Pontificia Bolivariana QUIMICA GENERAL Docente : Raquel Villafrades Torres TEORIA ATOMICA DE DALTON (1808) BASES Ley de conservación de la masa: La masa total de las sustancias presentes después
Física y Química 3º ESO
 1. Física y Química. Ciencias de la medida forman parte de las necesitan Ciencias de la naturaleza medir las propiedades de los cuerpos que se dividen en para lo cual se emplean lo que siempre conlleva
1. Física y Química. Ciencias de la medida forman parte de las necesitan Ciencias de la naturaleza medir las propiedades de los cuerpos que se dividen en para lo cual se emplean lo que siempre conlleva
Tecnología Industrial II
 I.E.S. el Doctoral 2009-2010 Tecnología Industrial II Tema 1 Estructura y propiedades de los materiales Pedro Rodas Martín Departamento de Tecnología 1. ESTRUCTURA INTERNA DE LOS MATERIALES En 1808, el
I.E.S. el Doctoral 2009-2010 Tecnología Industrial II Tema 1 Estructura y propiedades de los materiales Pedro Rodas Martín Departamento de Tecnología 1. ESTRUCTURA INTERNA DE LOS MATERIALES En 1808, el
a) La distancia que ha recorrido el electrón cuando su velocidad se ha reducido a 0' m/s
 1- Un electrón es lanzado con una velocidad de 2.10 6 m/s paralelamente a las líneas de un campo eléctrico uniforme de 5000 V/m. Determinar: a) La distancia que ha recorrido el electrón cuando su velocidad
1- Un electrón es lanzado con una velocidad de 2.10 6 m/s paralelamente a las líneas de un campo eléctrico uniforme de 5000 V/m. Determinar: a) La distancia que ha recorrido el electrón cuando su velocidad
COMO SE DESCUBRIO EL ATOMO?
 COMO SE DESCUBRIO EL ATOMO? OBJETIVO: Caracterizar la estructura interna de la materia, basándose en los modelos atómicos desarrollados por los científicos a través del tiempo Átomo: Unidad más pequeña
COMO SE DESCUBRIO EL ATOMO? OBJETIVO: Caracterizar la estructura interna de la materia, basándose en los modelos atómicos desarrollados por los científicos a través del tiempo Átomo: Unidad más pequeña
d 0,42 0,42cos 1,26 10 m
 0. Una partícula con carga y masa m penetra con una elocidad en una zona donde hay un campo magnético uniforme. Calcular: a) la fuerza ue actúa sobre la partícula y el trabajo efectuado por dicha fuerza.
0. Una partícula con carga y masa m penetra con una elocidad en una zona donde hay un campo magnético uniforme. Calcular: a) la fuerza ue actúa sobre la partícula y el trabajo efectuado por dicha fuerza.
