FORMULACIÓN INORGÁNICA
|
|
|
- Claudia Pinto Escobar
- hace 7 años
- Vistas:
Transcripción
1 INORGÁNICA 1.- Introducción. Elemento químico es cada sustancia que contiene una sola clase de átomos. Compuesto sustancia formada por una combinación fija y constante de átomos de diferentes elementos. Fórmula química de una sustancia cualquiera, indica los elementos que la forman y la proporción en que se encuentran sus átomos. Las normas de formulación y nomenclatura las establece la Unión Internacional de Química Pura y Aplicada: IUPAC (International Union of Pure and Applied Chemistry). Existen tres sistemas de formulación: - Notación Stock, consiste en colocar con números romanos y entre paréntesis, el número de oxidación del elemento que no es oxígeno, en los óxidos, que no es hidrógeno en los hidruros etc. - Nomenclatura sistemática, se utilizan prefijos numerales griegos, mono, di, tri, tetra, penta..para indicar la composición del compuesto. - Nomenclatura tradicional, sigue unas determinadas reglas. 2.- Estados de oxidación Algunas reglas básicas para conocer el número de oxidación son: - El número de oxidación de todos los elementos, o átomos aislados es cero. - El número de oxidación del oxígeno en todos sus compuestos es II excepto en los peróxidos que es I y cuando se combina con el fluor que es +II. - El número de oxidación del hidrógeno es siempre +I excepto en los hidruros metálicos que es I. - El número de oxidación de los metales es siempre positivo. - En las sales binarias, el metal tiene número de oxidación positivo y el no metal negativo. - En los oxoácidos, el oxígeno actúa con número de oxidación II, el no metal con número de oxidación positivo y el hidrógeno con +I. - En los compuestos neutros, la suma de los números de oxidación de todos sus átomos ha de ser igual a cero. - En los iones, la suma de los números de oxidación de todos sus átomos ha de ser igual a la carga del ión. 1
2 TABLA DE VALENCIAS Los elementos que vamos a considerar y sus estados de oxidación más frecuentes son los que aparecen en la siguiente tabla: I II III IV V VI VII VIII IX X XI XII XIII XIV XV XVI XVII H + 1 Li Na K Rb Cs Be Mg Ca Sr Ba Cr,3,6 Mn,3,4,6,7 Fe,3 Co,3 Ni,3 Pd,4 Pt,4 Cu,2 Ag Au,3 Zn Cd Hg,2 B +3-3 Al +3 C,4-4 Si +4 Sn,4 Pb,4 N,2,3,4,5-3 P,3,5-3 As +3,5-3 Sb +3,5-3 Bi +3 O -2,1 S,4,6-2 Se,4,6-2 Te,4,6-2 F Cl,3,5, 7 Br,3,5, 7 I,3,5, 7 XV III 2
3 3.- Sustancias simples Son las que están formadas por átomos de un único elemento. - Los gases nobles son siempre monoatómicos. - Algunos elementos, cuando se encuentran en estado gaseoso, se presentan como moléculas diatómicas. Los más frecuentes son H 2 (hidrógeno gas), O 2 (oxígeno gas), N 2 (nitrógeno gas), F 2 (flúor gas), Cl 2 (cloro gas), Br 2 (bromo gas), I 2 (yodo gas) - El oxígeno se puede presentar también en forma de molécula triatómica O 3 (ozono). - El resto de los elementos son poliatómicos pero se representan simplemente por el símbolo del elemento. 4.- Normas generales de formulación y nomenclatura de combinaciones binarias Combinaciones binarias son compuestos en los que intervienen dos elementos distintos. - Se escriben los elementos en el orden que indica la siguiente lista: Metales B Si C Sb As P N H Te Se S I Br Cl O F - Se coloca como subíndice de cada elemento la valencia del otro y se simplifica si se puede. - Se nombra el elemento situado en segundo lugar con la terminación -uro, seguido del nombre del elemento escrito en primer lugar. (Las combinaciones binarias del oxígeno se nombran con el término óxido). LiF fluoruro de litio SrH 2 hidruro de estroncio SiO 2 oxido de silicio Al 2 S 3 sulfuro de aluminio Ag 3 P fosfuro de plata ZnTe telururo de cinc - Si el elemento que esta escrito a al izquierda puede presentar varios estados de oxidación, los diferentes compuestos se distinguen de alguna de las siguientes maneras: Nomenclatura sistemática: Se utilizan los prefijos mono, di, tri, etc., para indicar el número de átomos de cada elemento que hay en la fórmula. (el prefijo mono se omite en la segunda parte del nombre) Sistema Stock: Se indica la valencia del elemento de la izquierda en números romanos entre paréntesis. Fór Nomenclatura sistemática Sistema Stock mula FeO monóxido de hierro oxido de hierro (II) Fe 2 O 3 trióxido de dihierro óxido de hierro (III) PCl 3 tricloruro de fósforo cloruro de fósforo (III) 5.- Combinaciones binarias del hidrógeno El estado de oxidación del hidrógeno es I si se combina con un metal y +I si lo hace con un no metal. Podemos clasificarlos en tres grupos: Hidruros metálicos Se formulan y se nombran siguiendo las normas generales. LiH hidruro de litio mono hidruro de litio SrH 2 hidruro de estroncio dihidruro de estroncio AlH 3 hidruro de aluminio trihidruro de aluminio FeH 2 ohidruro de hierro (II) dihidruro de hierro 3
4 5.2.- Hidruros no metálicos 5.2.a.-Hidrácidos Son las combinaciones del hidrógeno con los elementos del grupo 17 (F, Cl, Br, I) y del grupo16 (S, Se, Te). Su fórmula general es H a X, donde X es el no metal y a = 1 si X es F, Cl, Br o I y a = 2 si se trata de S, Se, o Te. Se pueden nombrar siguiendo las normas generales, pero también con la palabra ácido seguida del nombre del elemento con la terminación -hídrico. La segunda forma es la utilizada cuando estos compuestos están en disolución acuosa. HCl cloruro de hidrógeno o ácido clorhídrico H 2 S sulfuro de hidrógeno (dihidrógeno) o ácido sulfhídrico H 2 Te telururo de hidrógeno (dihidrógeno) o ácido telurhídrico HF fluoruro de hidrógeno o ácido fluorhídrico Hay un compuesto formado por H, C y N que se nombra siguiendo el mismo sistema: HCN cianuro de hidrógeno o ácido cianhídrico 5.2.b.-Combinaciones del hidrógeno con el resto de los no metales Su fórmula general es XH a. De la misma forma que el compuesto de fórmula H 2 O lo conocemos con el nombre de agua y no utilizamos la nomenclatura sistemática, todos estos compuestos se conocen con nombres no sistemáticos: NH 3 amoníaco CH 4 metano BH 3 borano PH 3 fosfina SiH 4 silano AsH 3 arsina SbH 3 estibina 6.- Combinaciones binarias del oxígeno El oxígeno se combina con casi todos los elementos, con estado de oxidación II. El oxígeno se escribe siempre en segundo lugar, pues con la excepción del flúor, el oxígeno es el elemento más electronegativo (el penúltimo de la lista). Se nombran utilizando el término óxido. Si el elemento presenta varios estados de oxidación, y por tanto, puede tener varios posibles óxidos se especifica con el sistema Stock o mediante los prefijos de la nomenclatura sistemática. Ag 2 O monóxido de diplata óxido de plata Cl 2 O 5 pentaóxido de dicloro óxido de cloro (V) SO 3 dióxido de azufre óxido de azufre (IV) SiO 2 Dióxido de silicio oxido de silicio FeO monóxido de hierro óxido de hierro (II) Fe 2 O 3 trióxido de dihierro óxido de hierro (III) Los combinaciones del oxígeno con algunos elementos presentan algunas particularidades: Óxidos del carbono CO monóxido de carbono u óxido de carbono (II) CO 2 dióxido de carbono u óxido de carbono (IV) 4
5 El CO es el único compuesto de carbono con estado de oxidación +II. Oxidos de: Cr, Mn y N Cr : CrO monóxido de cromo. Oxido de cromo (II) Cr 2 O 3.trióxido de dicromo. Oxido de cromo (III) CrO 3...trióxido de cromo. Oxido de cromo (VI) Mn: MnO.monóxido de manganeso. Oxido de manganeso (II) Mn 2 O 3 trióxido de dimanganeso Oxido de manganeso (III) MnO 2 dióxido de manganeso Oxido de manganeso (IV) MnO 3...trióxido de manganeso Oxido de manganeso (VI) Mn 2 O 7...heptaóxido de manganeso Oxido de manganeso (VII) N N 2 O.. monóxido de dinitrógeno Oxido de nitrógeno (I) NO...monóxido de nitrógeno Oxido de nitrógeno (II) N 2 O 3...trióxido de dinitrógeno Oxido de nitrógeno (III) NO 2..dióxido de nitrógeno Oxido de nitrógeno (IV) N 2 O 5...pentaóxido de dinitrógeno Oxido de nitrógeno (V) 7.- Otros compuestos binarios Sales binarias Las combinaciones de un metal con un no metal, que no sea el hidrógeno ni el oxígeno, se denominan sales binarias. Se formulan y nombran según las normas generales de los compuestos binarios. El no metal actúa con su estado de oxidación negativo por situarse siempre a la derecha. KBr bromuro de potasio SnSe seleniuro de estaño (II) o diseleniuro dre estaño BaCl 2 cloruro de bario Au 2 S 3 sulfuro de oro (III) o disulfuro de oro Combinaciones no metal-no metal Para su formulación y nomenclatura se siguen las normas generales. Es muy importante tener en cuenta que el elemento de la derecha actúa siempre con estado de oxidación negativo y el de la izquierda con estado de oxidación positivo. PCl 5 pentacloruro de fósforo cloruro de fósfor (V) CS 2 disulfuro de carbono sulfuro de carbono As 2 Se 3 triseleniuro de arsénico seleniuro de arsénico (III) 8.- Hidróxidos La fórmula general de los hidróxidos es M(OH) n, donde M es el metal y n su número de oxidación. Se nombran de forma similar a los compuestos binarios, utilizando la palabra hidróxido.. NaOH hidróxido de sodio Ca(OH) 2 hidróxido de calcio Cr(OH) 2 hidróxido de cromo (II) o dihidróxido de cromo Cr(OH) 3 hidróxido de cromo (III) o trihidróxido de cromo En el caso de los metales de transición (los del centro de la tabla) sólo generan hidróxidos los estados de oxidación más bajos, es decir, no existen los hidróxidos de de cromo (VI), de manganeso (VII) (VI) El amoníaco (NH 3 ) es un gas, al disolverlo en agua se produce un compuesto de propiedades básicas que recibe el nombre de hidróxido de amonio NH 3 + H 2 O NH 4 OH El grupo amonio (NH + 4 ) puede aparecer en otros compuestos y se comporta como si en conjunto tuviese estado de oxidación +I. NH 4 Cl cloruro de amonio (NH 4 ) 2 S sulfuro de amonio NH 4 CN cianuro de amonio 5
6 9.- Oxoácidos (sencillos) Por ácidos entendemos un conjunto de sustancias que tienen propiedades comunes. Desde el punto de vista químico se caracterizan porque en disolución acuosa se disocian liberando protones. Se clasifican en hidrácidos (ya han sido estudiados) oxoácidos y ácidos orgánicos. La fórmula general de los oxoácidos es siempre del tipo H a X b O c donde X es un no metal o un metal de transición en los estados de oxidación más elevados( +VI en el cromo o +VI y +VII en el manganeso, el nitrógeno sólo con valencias impares). En los oxoácidos sencillos b= 1 En estos compuestos el estado de oxidación del hidrógeno es +I y el del oxígeno es II. Se tiene que cumplir que la suma algebraica de los números de oxidación tienen que ser igual a cero: a.1 + b.nº ox X + c.(-2) = 0 Nomenclaturas sistemáticas de oxoácidos La IUPAC ha ideado varios sistemas para conseguir la máxima sistematización en la nomenclatura de oxoácidos. Los ejemplos que siguen explican por sí solos cuál es el criterio seguido para alcanzar dicha sistematización. Fórmula (A) Nomenclatura sistemática funcional (B) Nomenclatura sistemática (Stock) Nombre estequiométrico HClO ácido oxoclórico (I) oxoclorato (I) de hidrógeno monoxoclorato de hidrógeno HClO 2 ácido dioxoclórico (III) dioxoclorato (III) de dioxoclorato de hidrógeno hidrógeno H 2 SO 3 ácido trioxosulfúrico(iv) trioxosulfato (IV) de trioxosulfato de dihidrógeno hidrógeno H 4 SiO 4 ácido tetraoxosilícico tetraoxosilicato de tetraoxosilicato de tetrahidrógeno H hidrógeno 2 S 2 O 7 ácido heptaoxodisulfúrico(vi) heptaoxodisulfato (VI) heptaoxodisulfato de dihidrógeno (VI) dehidrógen OBSERVACION - Para nombrar oxoácidos (maneras A y B) es necesario conocer el estado de oxidación del elemento central. Para calcularlo se debe tener en cuenta que: - El número de oxidación del H en todos los oxoácidos es. - El número de oxidación del O en todos los oxoácidos es 2. - La suma de los números de oxidación de todos los átomos ha de ser 0. - Si el elemento central lleva subíndice se emplean los prefijos habituales mono- di- etc. - Si el elemento central tiene un solo estado de oxidación, se omite. Ej (H 4 SiO 4 ).. Regla nomenclatura sistemática funcional Acido numeral-oxo-raíz (X)- terminación-ico (valencia X) HBrO 2 Acido dioxobrómico (III). Regla nomenclatura sistemática Stock Numeral-oxo-raíz(X)-terminación-ato (valencia X) de hidrógeno HBrO 2 dioxobromato (III) de hidrógeno. Regla nomenclatura estequiométrica Numeral-oxo-raíz(X) terminación ato de numeral-hidrógeno HBrO 2 dioxobromato de (mono)hidrógeno - Para formular oxoácidos ( maneras A y B ) es necesario conocer el número de hidrógenos aplicando la fórmula: suma de todos los estados de oxidación igual a cero. 6
7 10.-Sales neutras Sales binarias: Ya estudiadas cuando se habló de combinaciones binarias no metal-metal. Ejemplo: KCl cloruro de potasio. Oxisales. Son las sales de los oxoácidos. Derivan de éstos por sustitución de los átomos de hidrógeno por átomos metálicos o grupos atómicos (normalmente, el grupo NH 4 + ).También podemos considerarlas como la unión de un catión y un oxoanión ( el conjunto ha de ser eléctricamente neutro). FORMULACION M x (R) n M es el símbolo del metal x es el número de hidrógenos sustituidos Hay que calcularlo aplicando la fórmula suma de todos los estados de oxidación igual a cero. R representa el resto del ácido, es decir, el conjunto de átomos que quedan en la molécula del ácido después de sustituir sus átomos de hidrógeno por metales. N valencia del metal M SISTEMÁTICA STOCK: - Se sigue el mismo sistema de la nomenclatura sistemática Stock de los ácidos. - Si el resto de ácido (oxoanión) tiene subíndice, se puede hacer constar con los prefijos: bis-, tris-, tetrakis-, pentakis-, etc. En este caso el nombre del oxoanión se encierra entre corchetes. - No obstante, si se indica el estado de oxidación del metal (catión ) no son necesarios estos últimos prefijos, pues la fórmula quedaría perfectamente establecida, sin embargo se facilita la comprensión. - Para nombrar estas sales es necesario calcular la valencia del elemento central (no metal) de la misma forma que en los ácidos. - Si el metal (catión) tiene más de una valencia, es necesario tantear Veamos algunos ejemplos: Fe 2 (CO 3 ) 3 tris[trioxocarbonato] de hierro trioxocarbonato de hierro (III) Ca(ClO 2 ) 2 Bis [dioxoclorato (III) ]de calcio dioxoclorato (III) de calcio Fe(NO 3 ) 2 bis[trioxonitrato(v)] de hierro trioxonitrato(v) de hierro (II) Mn 2 (SO 4 ) 3 tris[tetraoxosulfato(vi)] de manganeso tetraoxosulfato (VI) de manganeso(iii) NaNO 3 trioxonitrato (V) de sodio K 2 SO 4 tetraoxosulfato(vi) de potasio Fe 2 (Cr 2 O 7 ) 3 tris [heptaoxodicromarto(vi)] de hierro heptaoxodicromato (VI) de hierro (III) Regla: Numeral-oxo-raíz(X)-terminación-ato (valencia X) de M (valencia M) Fe(NO 3 ) trioxonitrato(v) de hierro (II) ESTEQUIOMÉTRICA: Se sigue el mismo sistema de nomenclatura estequiométrica de los oxoácidos. Regla: Numeral griego-numeral-oxo-raíz(x) terminación ato (ValenciaX)de numeral-metal Al 2 (CO 3 ) Ni 3 (PO 3 ) 2 tris[trioxocarbonato ] de dialuminio bis[trioxofosfato(v) ] de triniquel 7
8 11- Iones Son átomos o grupos de átomos con carga eléctrica. Si tienen carga positiva se denominan cationes y si tienen carga negativa aniones Cationes Se forman cuando un átomo de un metal pierde electrones (los de su última capa) y por tanto queda cargado positivamente. Se representan mediante la fórmula : X n+ Donde n representa el número de cargas positivas en exceso del elemento X (su nº de oxidación). H +, Li +, Ca 2+, Fe 3+,, Al 3+, Pb 4+ : Se antepone la palabra catión o ión al nombre del elemento y a continuación la carga expresada en números romanos entre paréntesis si es necesario y que corresponde a la nomenclatura Stock. H + ión hidrógeno Li + ión litio Fe 3+ ión hierro (III) Sn 2+ ión estaño (II) (El cromo y el manganeso sólo forman cationes con nº de oxidación y +3 y el nitrógeno no forma cationes porque no es un metal)) Cationes poliatómicos Grupo de átomos con carga positiva. Se nombrar añadiendo la terminación onio a un prefijo indicativo del compuesto de procedencia. + + NH 4 ión amonio PH 4 ión fosfonio H 3 O + ión hidronio u oxonio Aniones monoatómicos. Se forman cuando un átomo de un no metal gana electrones y por tanto queda cargado negativamente. FORMULACION: Se representan mediante la fórmula: X n- Donde n simboliza el número de cargas negativas en exceso. : Basta con anteponer la palabra catión o ión al nombre del elemento y a continuación el nombre del no metal terminado en -uro Cl - ión cloruro Te 2+ ión telururo P 3+ ión fosfuro Aniones poliatómicos Se pueden considerar que provienen de otras moléculas por pérdida de uno o más iones hidrógeno. El más sencillo es el OH - ión hidróxido hidroxilo u oxidrilo, que procede de la pérdida de un ión hidrógeno del agua H 2 O - H + OH - Sin embargo la mayoría proceden de un oxoácido que ha perdido o cedido sus hidrógenos. - Así: HClO 3 ClO 3 + H + SISTEMATICA STOCK Se utiliza la palabra anión o ión seguido del nombre sistemático del ácido (sin nombrar los hidrógenos). Nomenclatura sistemática(stock) ClO - ClO 2 - ClO 3 - ClO 4 - SO 4 2- Cr 2 O 7 2- Ión monoxoclorato (I) Ión dioxoclorato (III) Ión trioxoclorato (V) Ión tetraoxoclorato (VII) Ión tetraoxosulfato (VI) Ión heptaoxodicromato (VI) (en los iones siempre se cumple que la suma del número de oxidación de cada átomo por el número de ellos ha de ser igual a la carga del ión) 8
9 9
Lo primero que hay que conocer para formular y nombrar los compuestos químicos es el número de oxidación de cada elemento.
 Tema 5. NOMENCLATURA Y FORMULACIÓN DE QUÍMICA INORGÁNICA Introducción La IUPAC (Unión Internacional de Química Pura y Aplicada) es el organismo que coordina y actualiza las normas que permiten formular
Tema 5. NOMENCLATURA Y FORMULACIÓN DE QUÍMICA INORGÁNICA Introducción La IUPAC (Unión Internacional de Química Pura y Aplicada) es el organismo que coordina y actualiza las normas que permiten formular
NOMENCLATURA Y FORMULACIÓN DE QUÍMICA INORGÁNICA. Física y Química 3º de E.S.O. IES Isidra de Guzmán
 NOMENCLATURA Y FORMULACIÓN DE QUÍMICA INORGÁNICA Física y Química 3º de E.S.O. IES Isidra de Guzmán INTRODUCCIÓN La IUPAC ( Unión Internacional de Química Pura y Aplicada) es el organismo que coordina
NOMENCLATURA Y FORMULACIÓN DE QUÍMICA INORGÁNICA Física y Química 3º de E.S.O. IES Isidra de Guzmán INTRODUCCIÓN La IUPAC ( Unión Internacional de Química Pura y Aplicada) es el organismo que coordina
La fórmula química expresa la composición de moléculas y compuestos mediante símbolos químicos. 13 millones!!!
 La fórmula química expresa la composición de moléculas y compuestos mediante símbolos químicos El Nº de compuestos químicos conocidos es superior a 13 millones!!! Método sistemático de nombrar los compuestos:
La fórmula química expresa la composición de moléculas y compuestos mediante símbolos químicos El Nº de compuestos químicos conocidos es superior a 13 millones!!! Método sistemático de nombrar los compuestos:
Química General Básica. Nomenclatura de Compuestos Inorgánicos
 Química General Básica Nomenclatura de Compuestos Inorgánicos Estelí, 11 de marzo de 2011 Formulación y Nomenclatura en Química Inorgánica La fórmula química expresa la composición de moléculas y compuestos
Química General Básica Nomenclatura de Compuestos Inorgánicos Estelí, 11 de marzo de 2011 Formulación y Nomenclatura en Química Inorgánica La fórmula química expresa la composición de moléculas y compuestos
FORMULACIÓN Y NOMENCLATURA
 1. SUSTANCIAS SIMPLES. FORMULACIÓN Y NOMENCLATURA Están constituidas por átomos de un solo elemento. En ellas las moléculas están formadas por átomos idénticos. Su fórmula indica el número de átomos de
1. SUSTANCIAS SIMPLES. FORMULACIÓN Y NOMENCLATURA Están constituidas por átomos de un solo elemento. En ellas las moléculas están formadas por átomos idénticos. Su fórmula indica el número de átomos de
FORMULACIÓN DE QUÍMICA INORGÁNICA.
 FORMULACIÓN DE QUÍMICA INORGÁNICA. 1. VALENCIA. Es la capacidad que tiene un átomo de un elemento para combinarse con los átomos de otros elementos y formar compuestos. La valencia es un número, positivo
FORMULACIÓN DE QUÍMICA INORGÁNICA. 1. VALENCIA. Es la capacidad que tiene un átomo de un elemento para combinarse con los átomos de otros elementos y formar compuestos. La valencia es un número, positivo
NOMENCLATURA y FORMULACIÓN en QUÍMICA INORGÁNICA. Nivel: Educación Secundaria Obligatoria
 NOMENCLATURA y FORMULACIÓN en QUÍMICA INORGÁNICA Nivel: Educación Secundaria Obligatoria Conceptos básicos Los elementos químicos se representan mediante símbolos, que consisten en una o dos letras que
NOMENCLATURA y FORMULACIÓN en QUÍMICA INORGÁNICA Nivel: Educación Secundaria Obligatoria Conceptos básicos Los elementos químicos se representan mediante símbolos, que consisten en una o dos letras que
FORMULACIÓN QUÍMICA INORGÁNICA
 FORMULACIÓN QUÍMICA INORGÁNICA 1. VALENCIAS DE LOS ELEMENTOS QUÍMICOS MÁS CONOCIDOS Se entiende que las valencias con signo negativo se dan frente a elementos electropositivos y las valencias con signo
FORMULACIÓN QUÍMICA INORGÁNICA 1. VALENCIAS DE LOS ELEMENTOS QUÍMICOS MÁS CONOCIDOS Se entiende que las valencias con signo negativo se dan frente a elementos electropositivos y las valencias con signo
FORMULACIÓN Y NOMENCLATURA DE QUÍMICA INORGÁNICA
 FORMULACIÓN Y NOMENCLATURA DE QUÍMICA INORGÁNICA Índice de contenido TABLAS DE NÚMEROS DE OXIDACIÓN MÁS COMUNES...2 MECANISMO DE FORMULACIÓN...2 NOMENCLATURAS EN QUÍMICA INORGÁNICA...2 NOMENCLATURA CON
FORMULACIÓN Y NOMENCLATURA DE QUÍMICA INORGÁNICA Índice de contenido TABLAS DE NÚMEROS DE OXIDACIÓN MÁS COMUNES...2 MECANISMO DE FORMULACIÓN...2 NOMENCLATURAS EN QUÍMICA INORGÁNICA...2 NOMENCLATURA CON
Colegio Superior de Señoritas Tema: Formación de Compuestos Químicos Septiembre 2010 Prof.: NVM 8vo Nivel Departamento de Ciencias
 COMPUESTOS QUÍMICOS Y SU CLASIFICACIÓN El número de oxidación: representa la cantidad de electrones que puede ganar o perder un elemento. El hidrógeno tiene número de oxidación +1 y puede perder un electrón;
COMPUESTOS QUÍMICOS Y SU CLASIFICACIÓN El número de oxidación: representa la cantidad de electrones que puede ganar o perder un elemento. El hidrógeno tiene número de oxidación +1 y puede perder un electrón;
NOMENCLATURA y FORMULACIÓN en QUÍMICA INORGÁNICA
 NOMENCLATURA y FORMULACIÓN en QUÍMICA INORGÁNICA Adaptado a las normas de la IUPAC 1990 Nivel: 3º ESO 1 0. Introducción Valencia Es la capacidad que posee un elemento de combinarse con otro. Como el hidrógeno
NOMENCLATURA y FORMULACIÓN en QUÍMICA INORGÁNICA Adaptado a las normas de la IUPAC 1990 Nivel: 3º ESO 1 0. Introducción Valencia Es la capacidad que posee un elemento de combinarse con otro. Como el hidrógeno
FORMULACIÓN Y NOMENCLATURA (SISTEMÁTICA)
 FORMULACIÓN Y NOMENCLATURA (SISTEMÁTICA) FORMULACIÓN: el conjunto de reglas que se emplean para la representación simbólica de los compuestos químicos. NOMENCLATURA: la forma de nombrar los compuestos.
FORMULACIÓN Y NOMENCLATURA (SISTEMÁTICA) FORMULACIÓN: el conjunto de reglas que se emplean para la representación simbólica de los compuestos químicos. NOMENCLATURA: la forma de nombrar los compuestos.
FORMULACIÓN INORGÁNICA. Departamento de Física y Química 3º ESO
 FORMULACIÓN INORGÁNICA Departamento de Física y Química 3º ESO 1. Tabla periódica de los elementos -1 Valencia: capacidad que posee un elemento para combinarse con otro Número de oxidación: número de electrones
FORMULACIÓN INORGÁNICA Departamento de Física y Química 3º ESO 1. Tabla periódica de los elementos -1 Valencia: capacidad que posee un elemento para combinarse con otro Número de oxidación: número de electrones
1.- CONCEPTOS PREVIOS
 TEMA 6: FORMULACIÓN 1.- CONCEPTOS PREVIOS Compuesto químico: es la unión de varios átomos que no pueden separarse por procedimientos físicos pero sí mediante procedimientos químicos. Ejemplo: dos átomos
TEMA 6: FORMULACIÓN 1.- CONCEPTOS PREVIOS Compuesto químico: es la unión de varios átomos que no pueden separarse por procedimientos físicos pero sí mediante procedimientos químicos. Ejemplo: dos átomos
M m+ + X n- M n X m. Qué es formular un compuesto binario?
 Qué es formular un compuesto binario? Cuando tenemos dos elementos, uno menos electronegativo que otro, es decir uno con tendencia a ceder electrones M m+ (m es número de oxidación o valencia) y otro con
Qué es formular un compuesto binario? Cuando tenemos dos elementos, uno menos electronegativo que otro, es decir uno con tendencia a ceder electrones M m+ (m es número de oxidación o valencia) y otro con
TEMA 4: FORMULACIÓN 1.- CONCEPTOS PREVIOS
 TEMA 4: FORMULACIÓN 1.- CONCEPTOS PREVIOS Compuesto químico: es la unión de varios átomos que no pueden separarse por procedimientos físicos pero sí mediante procedimientos químicos. Ejemplo: dos átomos
TEMA 4: FORMULACIÓN 1.- CONCEPTOS PREVIOS Compuesto químico: es la unión de varios átomos que no pueden separarse por procedimientos físicos pero sí mediante procedimientos químicos. Ejemplo: dos átomos
TEMA 4: FORMULACIÓN 1.- CONCEPTOS PREVIOS
 TEMA 4: FORMULACIÓN 1.- CONCEPTOS PREVIOS Compuesto químico: es la unión de varios átomos que no pueden separarse por procedimientos físicos pero sí mediante procedimientos químicos. Ejemplo: dos átomos
TEMA 4: FORMULACIÓN 1.- CONCEPTOS PREVIOS Compuesto químico: es la unión de varios átomos que no pueden separarse por procedimientos físicos pero sí mediante procedimientos químicos. Ejemplo: dos átomos
Número de oxidación. Es un número que da la carga que presentaría un átomo si los electrones de cada enlace se asignaran al átomo más electronegativo
 FORMULACIÓN Número de oxidación Es un número que da la carga que presentaría un átomo si los electrones de cada enlace se asignaran al átomo más electronegativo Las reglas de asignación del número de oxidación
FORMULACIÓN Número de oxidación Es un número que da la carga que presentaría un átomo si los electrones de cada enlace se asignaran al átomo más electronegativo Las reglas de asignación del número de oxidación
Trióxido de dihierro
 Curso 2012-13 FORMULACIÓN QUÍMICA INORGÁNICA COMBINACIONES BINARIAS CPI Conde de Fenosa Ares Los óxidos son combinaciones de los elementos con el oxígeno. El nombre de estos compuestos siempre incluye
Curso 2012-13 FORMULACIÓN QUÍMICA INORGÁNICA COMBINACIONES BINARIAS CPI Conde de Fenosa Ares Los óxidos son combinaciones de los elementos con el oxígeno. El nombre de estos compuestos siempre incluye
PROGRAMA TOTAL FÓRMULAS QUÍMICAS Y SISTEMAS DE NOMENCLATURA CLASIFICACIÓN DE LOS COMPUESTOS QUÍMICOS INORGÁNICOS
 Departamento de Física y Química FÍSICA Y QUÍMICA ESO FORMULACIÓN Y NOMENCLATURA DE LOS COMPUESTOS QUÍMICOS INORGÁNICOS PROGRAMA TOTAL INTRODUCCIÓN FÓRMULAS QUÍMICAS Y SISTEMAS DE NOMENCLATURA CLASIFICACIÓN
Departamento de Física y Química FÍSICA Y QUÍMICA ESO FORMULACIÓN Y NOMENCLATURA DE LOS COMPUESTOS QUÍMICOS INORGÁNICOS PROGRAMA TOTAL INTRODUCCIÓN FÓRMULAS QUÍMICAS Y SISTEMAS DE NOMENCLATURA CLASIFICACIÓN
Tema 6 : Nomenclatura y formulación Química Inorgánica
 Tema 6 : Nomenclatura y formulación Química Inorgánica Esquema de trabajo: Introducción Compuestos Binarios 1. Combinaciones binarias del oxígeno: A. Oxidos B. Anhídridos 2. Combinaciones binarias del
Tema 6 : Nomenclatura y formulación Química Inorgánica Esquema de trabajo: Introducción Compuestos Binarios 1. Combinaciones binarias del oxígeno: A. Oxidos B. Anhídridos 2. Combinaciones binarias del
Iniciación a la formulación y nomenclatura en Química Inorgánica.
 1.- Generalidades. 2.- Compuestos monarios. 2.1.- Sustancias neutras. 2.2.- Cationes. 2.3.- Aniones. 3.- Compuestos binarios. 3.1.- Compuestos con oxígeno. 3.2.- Sales binarias. 4.- Compuestos ternarios.
1.- Generalidades. 2.- Compuestos monarios. 2.1.- Sustancias neutras. 2.2.- Cationes. 2.3.- Aniones. 3.- Compuestos binarios. 3.1.- Compuestos con oxígeno. 3.2.- Sales binarias. 4.- Compuestos ternarios.
FORMULACIÓN Y NOMENCLATURA
 FORMULACIÓN Y NOMENCLATURA.- Formulación: Es la representación escrita de una molécula que se rige por unas normas universales establecidas por acuerdo de la comunidad científica..- Nomenclatura: Es el
FORMULACIÓN Y NOMENCLATURA.- Formulación: Es la representación escrita de una molécula que se rige por unas normas universales establecidas por acuerdo de la comunidad científica..- Nomenclatura: Es el
NOMENCLATURA INORGÁNICA
 NOMENCLATURA INORGÁNICA Elemento: Se denomina elemento a toda sustancia que no puede descomponerse en otras más sencillas por métodos químicos. Nombre y símbolo de un elemento: Cada elemento se identifica
NOMENCLATURA INORGÁNICA Elemento: Se denomina elemento a toda sustancia que no puede descomponerse en otras más sencillas por métodos químicos. Nombre y símbolo de un elemento: Cada elemento se identifica
FORMULACIÓN INORGÁNICA
 INORGÁNICA 1.- Introducción. Elemento químico es cada sustancia que contiene una sola clase de átomos. Compuesto sustancia formada por una combinación fija y constante de átomos de diferentes elementos.
INORGÁNICA 1.- Introducción. Elemento químico es cada sustancia que contiene una sola clase de átomos. Compuesto sustancia formada por una combinación fija y constante de átomos de diferentes elementos.
QUÍMICA INORGÁNICA. Elementos Símbolo Valencia Elemento Símbolo Valencia. Hidrógeno H Oxigeno O -2. Flúor F -1 Nitrógeno N
 QUÍMICA INORGÁNICA VALENCIAS NO METALES Elementos Símbolo Valencia Elemento Símbolo Valencia Hidrógeno H -1 +1 Oxigeno O -2 Flúor F -1 Nitrógeno N -3 +1+3+5 Cloro Cl -1 +1+3+5+7 Fósforo P -3 +1+3+5 Bromo
QUÍMICA INORGÁNICA VALENCIAS NO METALES Elementos Símbolo Valencia Elemento Símbolo Valencia Hidrógeno H -1 +1 Oxigeno O -2 Flúor F -1 Nitrógeno N -3 +1+3+5 Cloro Cl -1 +1+3+5+7 Fósforo P -3 +1+3+5 Bromo
M m+ + X n-! M n X m EJERCICIOS/ESTUDIO. Qué es formular un compuesto binario?
 EJERCICIOS/ESTUDIO Materia: Tema: Física y Química 3º ESO Curso: Qué es formular un compuesto binario? Cuando tenemos dos elementos, uno menos electronegativo que otro, es decir uno con tendencia a ceder
EJERCICIOS/ESTUDIO Materia: Tema: Física y Química 3º ESO Curso: Qué es formular un compuesto binario? Cuando tenemos dos elementos, uno menos electronegativo que otro, es decir uno con tendencia a ceder
NOMENCLATURA DE QUÍMICA INORGÁNICA COMPUESTOS BINARIOS (3.º ESO)
 NOMENCLATURA DE QUÍMICA INORGÁNICA COMPUESTOS BINARIOS Para qué la nomenclatura química? Cuando estudiamos química nos encontramos con multitud de sustancias a las que debemos de asignar un nombre y una
NOMENCLATURA DE QUÍMICA INORGÁNICA COMPUESTOS BINARIOS Para qué la nomenclatura química? Cuando estudiamos química nos encontramos con multitud de sustancias a las que debemos de asignar un nombre y una
SUMARIO FÓRMULAS QUÍMICAS Y SISTEMAS DE NOMENCLATURA CLASIFICACIÓN DE LOS COMPUESTOS QUÍMICOS INORGÁNICOS INTRODUCCIÓN SUSTANCIAS SIMPLES
 Departamento de Ciencias Naturales IES Benalmádena FÍSICA Y QUÍMICA 3º ESO FORMULACIÓN Y NOMENCLATURA DE LOS COMPUESTOS QUÍMICOS INORGÁNICOS FORMULACIÓN Y NOMENCLATURA COMBINACIONES BINARIAS INTRODUCCIÓN
Departamento de Ciencias Naturales IES Benalmádena FÍSICA Y QUÍMICA 3º ESO FORMULACIÓN Y NOMENCLATURA DE LOS COMPUESTOS QUÍMICOS INORGÁNICOS FORMULACIÓN Y NOMENCLATURA COMBINACIONES BINARIAS INTRODUCCIÓN
Trióxido de dihierro
 ÓXIDOS Los óxidos son combinaciones de los elementos con el oxígeno. El nombre de estos compuestos siempre incluye la palabra óxido que puede estar precedida de prefijos numerales indicadores del número
ÓXIDOS Los óxidos son combinaciones de los elementos con el oxígeno. El nombre de estos compuestos siempre incluye la palabra óxido que puede estar precedida de prefijos numerales indicadores del número
Formulación Inorgánica
 Formulación Inorgánica 1.- Sustancias Simples Por sustancias simples entendemos aquellas sustancias formadas por un solo tipo de elementos, podemos encontrar casos: Sustancias simples metálicas: se formulan
Formulación Inorgánica 1.- Sustancias Simples Por sustancias simples entendemos aquellas sustancias formadas por un solo tipo de elementos, podemos encontrar casos: Sustancias simples metálicas: se formulan
FORMULACIÓN Y NOMENCLATURA INORGÁNICA
 FORMULACIÓN Y NOMENCLATURA INORGÁNICA Número de oxidación (n.o.): es la carga real (si es un ion) o aparente (si no es un ion) que tienen los elementos que forman parte de un compuesto. (Ver la tabla de
FORMULACIÓN Y NOMENCLATURA INORGÁNICA Número de oxidación (n.o.): es la carga real (si es un ion) o aparente (si no es un ion) que tienen los elementos que forman parte de un compuesto. (Ver la tabla de
Trióxido de dihierro
 COMBINACIONES BINARIAS (4ª ESO) ÓXIDOS Los óxidos son combinaciones de los elementos con el oxígeno. El nombre de estos compuestos siempre incluye la palabra óxido que puede estar precedida de prefijos
COMBINACIONES BINARIAS (4ª ESO) ÓXIDOS Los óxidos son combinaciones de los elementos con el oxígeno. El nombre de estos compuestos siempre incluye la palabra óxido que puede estar precedida de prefijos
INSTITUTO EDUCACIÓN SECUNDARIA POLITÉCNICO. CARTAGENA. 3º E.S.O.
 Cartagena-2012 1 FORMULACIÓN Y NOMENCLATURA INORGÁNICA 0. SÍMBOLOS Y VALENCIAS DE LOS ELEMENTOS Los símbolos y valencias de los elementos más comunes vienen recogidos en el ANEXO I. Por último, indicaremos
Cartagena-2012 1 FORMULACIÓN Y NOMENCLATURA INORGÁNICA 0. SÍMBOLOS Y VALENCIAS DE LOS ELEMENTOS Los símbolos y valencias de los elementos más comunes vienen recogidos en el ANEXO I. Por último, indicaremos
Los elementos químicos se caracterizan por un nombre y un símbolo, acordados por la IUPAC (International Union of Pure and Applied Chemistry).
 4. FORMULACIÓN. 4.1. SÍMBOLOS E HIDRUROS. 4.1.1. SÍMBOLOS Y VALENCIAS. Los elementos químicos se caracterizan por un nombre y un símbolo, acordados por la IUPAC (International Union of Pure and Applied
4. FORMULACIÓN. 4.1. SÍMBOLOS E HIDRUROS. 4.1.1. SÍMBOLOS Y VALENCIAS. Los elementos químicos se caracterizan por un nombre y un símbolo, acordados por la IUPAC (International Union of Pure and Applied
Nomenclatura Inorgánica
 Nomenclatura Inorgánica Nomenclatura Química O Es el sistema de normas, comunes en todo el mundo, para denominar a los elementos y compuestos químicos. O El organismo encargado de dictar tales normas se
Nomenclatura Inorgánica Nomenclatura Química O Es el sistema de normas, comunes en todo el mundo, para denominar a los elementos y compuestos químicos. O El organismo encargado de dictar tales normas se
11 Dióxido de carbono. 12 Trióxido de monoazufre. 13 Pentaóxido de difósforo. 14 Dióxido de monoselenio. 15 Dióxido de selenio. 16 Óxido de dimercurio
 1 FÍSICA Y QUÍMICA 3º ESO QUÍMICA - FORMULACIÓN Y SISTEMÁTICAMENTE LOS SIGUIENTES ÓXIDOS 1 Cu 2 O 2 Be O 3 I 2 O 5 4 CO 2 5 NiO 6 Ag 2 O 7 Li 2 O 8 N 2 O 3 9 CrO 10 Ni 2 O 3 11 Dióxido de carbono 12 Trióxido
1 FÍSICA Y QUÍMICA 3º ESO QUÍMICA - FORMULACIÓN Y SISTEMÁTICAMENTE LOS SIGUIENTES ÓXIDOS 1 Cu 2 O 2 Be O 3 I 2 O 5 4 CO 2 5 NiO 6 Ag 2 O 7 Li 2 O 8 N 2 O 3 9 CrO 10 Ni 2 O 3 11 Dióxido de carbono 12 Trióxido
TEMA 5.- Formulación y nomenclatura
 Tema 5.- Formulación y nomenclatura de compuestos binarios 0.- Introducción. 1.- Óxidos. 2.- Peróxidos. 3.- Combinaciones binarias del hidrógeno. 3.1.- Hidruros. 3.2.- Haluros. 3.3.- Hidruros volátiles.
Tema 5.- Formulación y nomenclatura de compuestos binarios 0.- Introducción. 1.- Óxidos. 2.- Peróxidos. 3.- Combinaciones binarias del hidrógeno. 3.1.- Hidruros. 3.2.- Haluros. 3.3.- Hidruros volátiles.
FORMULACIÓN INORGÁNICA 2º ESO. COLEGIO HIJAS DE JESÚS PAMPLONA.
 0. INTRODUCCIÓN. Formulación de química inorgánica basada en las recomendaciones de IUPAC (Internacional Union of Pure and Applied Chemistry) INDICE: 1. Sustancias elementales o simples 2. Compuestos binarios
0. INTRODUCCIÓN. Formulación de química inorgánica basada en las recomendaciones de IUPAC (Internacional Union of Pure and Applied Chemistry) INDICE: 1. Sustancias elementales o simples 2. Compuestos binarios
EJRCICIOS de FORMULACIÓN DE FÍSICA Y QUÍMICA 3º ESO
 EJRCICIOS de FORMULACIÓN DE FÍSICA Y QUÍMICA 3º ESO Pablo Martín CURSO 2014-2015 1 EJERCICIOS DE FORMULACIÓN DE INORGÁNICA: Escribe el nombre de los siguientes compuestos 1. Cl 2 O 5 2. PbCl 4 3. HCl 4.
EJRCICIOS de FORMULACIÓN DE FÍSICA Y QUÍMICA 3º ESO Pablo Martín CURSO 2014-2015 1 EJERCICIOS DE FORMULACIÓN DE INORGÁNICA: Escribe el nombre de los siguientes compuestos 1. Cl 2 O 5 2. PbCl 4 3. HCl 4.
H, Li, Na, K, Rb, Cs, Fr 1. Be, Mg, Ca, Sr, Ba, Ra, Zn, Cd 2. B, Al 3. N, P, As, Sb 1, 3, 5. F, Cl, Br, I 1, 3, 5, 7. C, Si, Ge, Sn, Pb 2, 4 O 2
 H, Li, Na, K, Rb, Cs, Fr 1 Be, Mg, Ca, Sr, Ba, Ra, Zn, Cd 2 B, Al 3 N, P, As, Sb 1, 3, 5 F, Cl, Br, I 1, 3, 5, 7 C, Si, Ge, Sn, Pb 2, 4 O 2 S, Se, Te 2, 4, 6 Cr 2, 3, 3, 6 Mn 2, 3, 4, 6, 7 Fe, Co, Ni 2,
H, Li, Na, K, Rb, Cs, Fr 1 Be, Mg, Ca, Sr, Ba, Ra, Zn, Cd 2 B, Al 3 N, P, As, Sb 1, 3, 5 F, Cl, Br, I 1, 3, 5, 7 C, Si, Ge, Sn, Pb 2, 4 O 2 S, Se, Te 2, 4, 6 Cr 2, 3, 3, 6 Mn 2, 3, 4, 6, 7 Fe, Co, Ni 2,
FORMULACIÓN DE QUÍMICA INORGÁNICA
 DE QUÍMICA INORGÁNICA Del mismo modo que utilizamos las palabras para comunicarnos, en química recurrimos a las fórmulas para representar los compuestos. Estas fórmulas no son arbitrarias, sino que responden
DE QUÍMICA INORGÁNICA Del mismo modo que utilizamos las palabras para comunicarnos, en química recurrimos a las fórmulas para representar los compuestos. Estas fórmulas no son arbitrarias, sino que responden
FORMULACIÓN DE QUÍMICA INORGÁNICA
 DE QUÍMICA INORGÁNICA Del mismo modo que utilizamos las palabras para comunicarnos, en química recurrimos a las fórmulas para representar los compuestos. Estas fórmulas no son arbitrarias, sino que responden
DE QUÍMICA INORGÁNICA Del mismo modo que utilizamos las palabras para comunicarnos, en química recurrimos a las fórmulas para representar los compuestos. Estas fórmulas no son arbitrarias, sino que responden
CONFERENCIA No. 1 Página 1 de 4. DE: Septiembre 7 del 2015 A : Septiembre 25 del 2015
 CONFERENCIA No. 1 Página 1 de 4 ÁREA: TEMA: PROFESOR: TIEMPO DE REALIZACIÓN: CIENCIAS NATURALES Y EDUCACIÓN GRADO: DÉCIMO AMBIENTAL - QUÍMICA Nomenclatura y reacciones de obtención de óxido, ácidos, bases
CONFERENCIA No. 1 Página 1 de 4 ÁREA: TEMA: PROFESOR: TIEMPO DE REALIZACIÓN: CIENCIAS NATURALES Y EDUCACIÓN GRADO: DÉCIMO AMBIENTAL - QUÍMICA Nomenclatura y reacciones de obtención de óxido, ácidos, bases
Ti: +,+,+ en los hidruros no metálicos. +,+ en los óxidos, hidróxidos, hidruros metálicos. Cr: +,+ en las sales binarias. Mn:
 Número de oxidación de un átomo en un compuesto es un número teórico que indica el número de electrones que el átomo habría perdido o ganado, si el compuesto fuera completamente iónico. El número de oxidación,
Número de oxidación de un átomo en un compuesto es un número teórico que indica el número de electrones que el átomo habría perdido o ganado, si el compuesto fuera completamente iónico. El número de oxidación,
DEPARTAMENTO DE FÍSICA Y QUÍMICA
 Qué es formular un compuesto binario? Cuando tenemos dos elementos, uno menos electronegativo que otro, es decir uno con tendencia a ceder electrones Mm+ (m es número de oxidación o valencia) y otro con
Qué es formular un compuesto binario? Cuando tenemos dos elementos, uno menos electronegativo que otro, es decir uno con tendencia a ceder electrones Mm+ (m es número de oxidación o valencia) y otro con
FORMULACIÓN QUÍMICA INORGÁNICA NÚMEROS DE OXIDACIÓN MÁS USUALES DE ALGUNOS ELEMENTOS METALES. Número de oxidación. + 1 Li, Na, K, Rb, Cs y Ag
 1 FORMULACIÓN QUÍMICA INORGÁNICA NÚMEROS DE OXIDACIÓN MÁS USUALES DE ALGUNOS ELEMENTOS METALES Número de oxidación Elementos + 1 Li, Na, K, Rb, Cs y Ag +2 Be, Mg, Ca, Sr, Ba ; Zn y Cd +3 B, Al +1, +2 Cu
1 FORMULACIÓN QUÍMICA INORGÁNICA NÚMEROS DE OXIDACIÓN MÁS USUALES DE ALGUNOS ELEMENTOS METALES Número de oxidación Elementos + 1 Li, Na, K, Rb, Cs y Ag +2 Be, Mg, Ca, Sr, Ba ; Zn y Cd +3 B, Al +1, +2 Cu
Formulación: Introducción y compuesto binarios. Teoría. Compuestos binarios y ternarios
 Compuestos binarios y ternarios 1. Compuestos binarios son aquellos que están formados por dos elementos diferentes. Ejemplos: - NaH está formado por dos elementos el Na y el H - Cl 2 O está formado por
Compuestos binarios y ternarios 1. Compuestos binarios son aquellos que están formados por dos elementos diferentes. Ejemplos: - NaH está formado por dos elementos el Na y el H - Cl 2 O está formado por
NOMENCLATURA DE ÁCIDOS Y BASES
 COLEGIO SAN ESTEBAN DIÁCONO Departamento de Ciencias Química IVº Electivo Prof. Juan Pastrián Lisboa NOMENCLATURA DE ÁCIDOS Y BASES Objetivo: - Reconocer y aplicar reglas de nomenclatura tradicional y
COLEGIO SAN ESTEBAN DIÁCONO Departamento de Ciencias Química IVº Electivo Prof. Juan Pastrián Lisboa NOMENCLATURA DE ÁCIDOS Y BASES Objetivo: - Reconocer y aplicar reglas de nomenclatura tradicional y
APUNTES DE FORMULACIÓN Y NOMENCLATURA DE QUÍMICA INORGÁNICA 3º ESO - CURSO METALES
 CONSEJERÍA DE EDUCACIÓN APUNTES DE FORMULACIÓN Y NOMENCLATURA DE QUÍMICA INORGÁNICA 3º ESO - CURSO 2012-2013 1. ELEMENTOS, SÍMBOLOS Y NÚMEROS DE OXIDACIÓN MÁS FRECUENTES EN LA FORMULACIÓN DE QUÍMICA INORGÁNICA
CONSEJERÍA DE EDUCACIÓN APUNTES DE FORMULACIÓN Y NOMENCLATURA DE QUÍMICA INORGÁNICA 3º ESO - CURSO 2012-2013 1. ELEMENTOS, SÍMBOLOS Y NÚMEROS DE OXIDACIÓN MÁS FRECUENTES EN LA FORMULACIÓN DE QUÍMICA INORGÁNICA
QUÍMICA INORGÁNICA: INTRODUCCIÓN A LA NOMENCLATURA Y FORMULACIÓN DE COMPUESTOS BINARIOS.
 QUÍMICA INORGÁNICA: INTRODUCCIÓN A LA NOMENCLATURA Y FORMULACIÓN DE COMPUESTOS BINARIOS. En el ámbito de la Química a cada sustancia le corresponde un nombre, que nos permite identificarla, y una fórmula,
QUÍMICA INORGÁNICA: INTRODUCCIÓN A LA NOMENCLATURA Y FORMULACIÓN DE COMPUESTOS BINARIOS. En el ámbito de la Química a cada sustancia le corresponde un nombre, que nos permite identificarla, y una fórmula,
5. ELEMENTOS Y COMPUESTOS IES ATENEA 3º DE ESO FÍSICA Y QUÍMICA
 5. ELEMENTOS Y COMPUESTOS IES ATENEA 3º DE ESO FÍSICA Y QUÍMICA 1. CLASIFICACIÓN DE LOS ELEMENTOS QUÍMICOS. 1.1. METALES Y NO METALES En términos generales, se clasifican como: METALES: Poseen brillo metálico.
5. ELEMENTOS Y COMPUESTOS IES ATENEA 3º DE ESO FÍSICA Y QUÍMICA 1. CLASIFICACIÓN DE LOS ELEMENTOS QUÍMICOS. 1.1. METALES Y NO METALES En términos generales, se clasifican como: METALES: Poseen brillo metálico.
Calcio(2+) Hierro(3+)
 CATIONES MONOATÓMICOS MONOATÓMICOS La carga se indica con un superíndice a la derecha del símbolo del elemento seguido del signo + Ca + Fe 3+ La carga se indica con un superíndice a la derecha seguido
CATIONES MONOATÓMICOS MONOATÓMICOS La carga se indica con un superíndice a la derecha del símbolo del elemento seguido del signo + Ca + Fe 3+ La carga se indica con un superíndice a la derecha seguido
TEMA 5. SISTEMA PERIÓDICO. FORMULACIÓN Y NOMENCLATURA DE COMPUESTOS INORGÁNICOS
 TEMA 5. SISTEMA PERIÓDICO. FORMULACIÓN Y NOMENCLATURA DE COMPUESTOS INORGÁNICOS SISTEMA PERIÓDICO El sistema periódico actual está formado por más de 100 elementos (114 en la actualidad), los cuales están
TEMA 5. SISTEMA PERIÓDICO. FORMULACIÓN Y NOMENCLATURA DE COMPUESTOS INORGÁNICOS SISTEMA PERIÓDICO El sistema periódico actual está formado por más de 100 elementos (114 en la actualidad), los cuales están
metal + H 2 hidruro metálico
 Hidruros metálicos Compuestos binarios formados por la combinación del hidrógeno con metales, especialmente con los del grupo IA y IIA (con excepción del berilio, del manganeso). En los Hidruros el metal
Hidruros metálicos Compuestos binarios formados por la combinación del hidrógeno con metales, especialmente con los del grupo IA y IIA (con excepción del berilio, del manganeso). En los Hidruros el metal
Óxido de hierro (III)
 COMPUESTOS BINARIOS: ÓXIDOS Los óxidos son combinaciones del oxígeno con otro elemento. El nombre de estos compuestos siempre incluye la palabra óxido que puede estar precedida de prefijos indicadores
COMPUESTOS BINARIOS: ÓXIDOS Los óxidos son combinaciones del oxígeno con otro elemento. El nombre de estos compuestos siempre incluye la palabra óxido que puede estar precedida de prefijos indicadores
QUÍMICA INORGÁNICA REGLAS DE FORMULACIÓN
 QUÍMICA INORGÁNICA REGLAS DE FORMULACIÓN Rafael Jiménez Prieto FORMULACIÓN INORGÁNICA FORMULACIÓN INORGÁNICA VALENCIAS MÁS COMUNES DE LOS ELEMENTOS QUÍMICOS TIPOS DE COMPUESTOS Consideraciones generales
QUÍMICA INORGÁNICA REGLAS DE FORMULACIÓN Rafael Jiménez Prieto FORMULACIÓN INORGÁNICA FORMULACIÓN INORGÁNICA VALENCIAS MÁS COMUNES DE LOS ELEMENTOS QUÍMICOS TIPOS DE COMPUESTOS Consideraciones generales
Como en los óxidos, pero cambiando la palabra óxido por peróxido. Ej: Cs 2 O 2 : peróxido de cesio
 Sustancias simples Formadas por átomos de un mismo elemento. Se nombran usando un prefijo indicando el número de átomos seguido del nombre del elemento. Sustancia Nombre sistemático Nombre común H Monohidrógeno
Sustancias simples Formadas por átomos de un mismo elemento. Se nombran usando un prefijo indicando el número de átomos seguido del nombre del elemento. Sustancia Nombre sistemático Nombre común H Monohidrógeno
Nomenclatura de compuestos inorgánicos
 1 Nomenclatura de compuestos inorgánicos De pequeños nos comunicamos con otras personas aprendiendo el nombre de los objetos que nos rodean. Conforme vamos creciendo aprendemos a hablar y utilizamos el
1 Nomenclatura de compuestos inorgánicos De pequeños nos comunicamos con otras personas aprendiendo el nombre de los objetos que nos rodean. Conforme vamos creciendo aprendemos a hablar y utilizamos el
Reglas generales. n Se nombra electronegativo de electropositivo. n Fórmula electropositivo electronegativo
 nomenclatura Reglas generales n Se nombra electronegativo de electropositivo n El electropositivo no se modifica n El electronegativo se modificará según las reglas de n compuestos binarios, n ternarios
nomenclatura Reglas generales n Se nombra electronegativo de electropositivo n El electropositivo no se modifica n El electronegativo se modificará según las reglas de n compuestos binarios, n ternarios
Material complementario PRÁCTICO 1
 Material complementario PRÁCTICO 1 Conceptos a repasar: u (ex uma): Se define como la 1/12 de la masa del isótopo de 12 C y equivale a 1,66056 x 10-24 g Número atómico (Z): Es el número de protones contenido
Material complementario PRÁCTICO 1 Conceptos a repasar: u (ex uma): Se define como la 1/12 de la masa del isótopo de 12 C y equivale a 1,66056 x 10-24 g Número atómico (Z): Es el número de protones contenido
TEMA 1 NOMENCLATURA Y FORMULACIÓN DE LOS COMPUESTOS QUÍMICOS INORGÁNICOS
 TEMA 1 NOMENCLATURA Y FORMULACIÓN DE LOS COMPUESTOS QUÍMICOS INORGÁNICOS ÍNDICE 1. Tipos de nomenclatura 2. Compuestos binarios 2.1. Combinaciones con hidrógeno 2.2. Combinaciones con oxígeno 2.3. Sales
TEMA 1 NOMENCLATURA Y FORMULACIÓN DE LOS COMPUESTOS QUÍMICOS INORGÁNICOS ÍNDICE 1. Tipos de nomenclatura 2. Compuestos binarios 2.1. Combinaciones con hidrógeno 2.2. Combinaciones con oxígeno 2.3. Sales
FÍSICA Y QUÍMICA cuaderno de ejercicios
 FÍSICA Y QUÍMICA cuaderno de ejercicios FORMULACIÓN y nomenclatura 1.** Determinen si las siguientes afirmaciones se refieren a metales o a no metales. 1.1. Presentan un brillo característico. 1.2. Los
FÍSICA Y QUÍMICA cuaderno de ejercicios FORMULACIÓN y nomenclatura 1.** Determinen si las siguientes afirmaciones se refieren a metales o a no metales. 1.1. Presentan un brillo característico. 1.2. Los
UD 2 ENLACE QUÍMICO Y FUERZAS INTERMOLECULARES FORMULACIÓN Y NOMENCLATURA DE COMPUESTOS TERNARIOS
 FORMULACIÓN Y NOMENCLATURA DE COMPUESTOS TERNARIOS Ácidos oxoácidos o ternarios Se formulan añadiendo una molécula de agua a los óxidos no metálicos. Óxidos no metálicos Cl 2 O SO Cl 2 O 3 SO 2 N 2 O 3
FORMULACIÓN Y NOMENCLATURA DE COMPUESTOS TERNARIOS Ácidos oxoácidos o ternarios Se formulan añadiendo una molécula de agua a los óxidos no metálicos. Óxidos no metálicos Cl 2 O SO Cl 2 O 3 SO 2 N 2 O 3
Tema 1 : Nomenclatura y formulación Química Inorgánica
 Tema 1 : Nomenclatura y formulación Química Inorgánica Esquema de trabajo: Introducción Compuestos Binarios 1. Combinaciones binarias del oxígeno 2. Combinaciones binarias del hidrógeno 3. Sales binarias
Tema 1 : Nomenclatura y formulación Química Inorgánica Esquema de trabajo: Introducción Compuestos Binarios 1. Combinaciones binarias del oxígeno 2. Combinaciones binarias del hidrógeno 3. Sales binarias
FORMULACIÓN Y NOMENCLATURA
 CONTENIDOS. FORMULACIÓN Y NOMENCLATURA 1.- Fórmulas empíricas y moleculares. 2.- Concepto de número de oxidación. 3.- Determinación del nº de oxidación 4.- Combinaciones binarias. Nomenclatura Stock y
CONTENIDOS. FORMULACIÓN Y NOMENCLATURA 1.- Fórmulas empíricas y moleculares. 2.- Concepto de número de oxidación. 3.- Determinación del nº de oxidación 4.- Combinaciones binarias. Nomenclatura Stock y
Formulación Inorgánica
 Formulación Inorgánica Sustancias elementales: Son las que están constituidas por átomos de un elemento, constituyen la molécula del elemento. A. Sustancias monoatómicas: Se representan y nombran igual
Formulación Inorgánica Sustancias elementales: Son las que están constituidas por átomos de un elemento, constituyen la molécula del elemento. A. Sustancias monoatómicas: Se representan y nombran igual
METALES. Número de oxidación. + 1 Li, Na, K, Rb, Cs y Ag. +2 Be, Mg, Ca, Sr, Ba ; Zn y Cd. +2, +3 Fe, Co, Ni. +2, +4 Pt, Pb, Sn. -2, +4, +6 S, Se, Te
 NÚMEROS DE OXIDACIÓN MÁS USUALES DE ALGUNOS ELEMENTOS METALES Número de oxidación Elementos + 1 Li, Na, K, Rb, Cs y Ag +2 Be, Mg, Ca, Sr, Ba ; Zn y Cd +3 B, Al +1, +2 Cu y Hg +1, +3 Au +2, +3 Fe, Co, Ni
NÚMEROS DE OXIDACIÓN MÁS USUALES DE ALGUNOS ELEMENTOS METALES Número de oxidación Elementos + 1 Li, Na, K, Rb, Cs y Ag +2 Be, Mg, Ca, Sr, Ba ; Zn y Cd +3 B, Al +1, +2 Cu y Hg +1, +3 Au +2, +3 Fe, Co, Ni
Óxido de hierro(iii)
 ÓXIDOS Los óxidos son combinaciones de los elementos con el oxígeno. El nombre de estos compuestos siempre incluye la palabra óxido que puede estar precedida de prefijos numerales indicadores del número
ÓXIDOS Los óxidos son combinaciones de los elementos con el oxígeno. El nombre de estos compuestos siempre incluye la palabra óxido que puede estar precedida de prefijos numerales indicadores del número
FORMULACIÓN Y NOMENCLATURA I.E.S. LOS NEVEROS INORGÁNICA HUÉTOR VEGA - 1 -
 - 1 - FORMULACIÓN Y NOMENCLATURA - 2 - NORMAS GENERALES PARA ESCRIBIR LAS FÓRMULAS DE SUSTANCIAS Para escribir la fórmula de un compuesto se escriben juntos los símbolos de los átomos y un número al lado
- 1 - FORMULACIÓN Y NOMENCLATURA - 2 - NORMAS GENERALES PARA ESCRIBIR LAS FÓRMULAS DE SUSTANCIAS Para escribir la fórmula de un compuesto se escriben juntos los símbolos de los átomos y un número al lado
NOMENCLATURA y FORMULACIÓN en QUÍMICA INORGÁNICA
 NOMENCLATURA y FORMULACIÓN en QUÍMICA INORGÁNICA I. Sustancias Simples Aquéllas constituidas por átomos de un mismo elemento. Los gases nobles son monoatómicos: He, Ne, Ar, Kr, Xe, Rn Las moléculas de
NOMENCLATURA y FORMULACIÓN en QUÍMICA INORGÁNICA I. Sustancias Simples Aquéllas constituidas por átomos de un mismo elemento. Los gases nobles son monoatómicos: He, Ne, Ar, Kr, Xe, Rn Las moléculas de
TEMA 4: Formulación inorgánica
 TEMA 4: Formulación inorgánica Tema 4: Formulación Inorgánica 1 1.- CMPUESTS BINARIS Son sustancias formadas por la unión de dos elementos químicos, como por ejemplo NaH, Co 3, Li S y PCl 3 1.1.- los En
TEMA 4: Formulación inorgánica Tema 4: Formulación Inorgánica 1 1.- CMPUESTS BINARIS Son sustancias formadas por la unión de dos elementos químicos, como por ejemplo NaH, Co 3, Li S y PCl 3 1.1.- los En
PLAN DE REFUERZO ÁREA PENDIENTE DE CIENCIAS NATURALES 3ºESO
 PLAN DE REFUERZO ÁREA PENDIENTE DE CIENCIAS NATURALES 3ºESO Para superar la materia, el alumno deberá realizar las actividades que se indican a continuación. Se realizarán en un cuaderno destinado únicamente
PLAN DE REFUERZO ÁREA PENDIENTE DE CIENCIAS NATURALES 3ºESO Para superar la materia, el alumno deberá realizar las actividades que se indican a continuación. Se realizarán en un cuaderno destinado únicamente
EJERCICIOS DE REPASO DE FORMULACIÓN Y NOMENCLATURA DE QUÍMICA INORGÁNICA COMPUESTOS BINARIOS
 EJERCICIOS DE REPASO DE FORMULACIÓN Y NOMENCLATURA DE QUÍMICA INORGÁNICA COMPUESTOS BINARIOS No hace falta hacerlos todos, ya os habréis dado cuenta de que si entendéis la lógica que hay detrás de la formulación
EJERCICIOS DE REPASO DE FORMULACIÓN Y NOMENCLATURA DE QUÍMICA INORGÁNICA COMPUESTOS BINARIOS No hace falta hacerlos todos, ya os habréis dado cuenta de que si entendéis la lógica que hay detrás de la formulación
OXIDOS METÁLICOS O BÁSICOS. Regla 1: se escribe la palabra óxido + nombre del metal (catión) + número de oxidación en números romanos
 OXIDOS METÁLICOS O BÁSICOS Nomenclatura Stock Regla 1: se escribe la palabra óxido + nombre del metal (catión) + número de oxidación en números romanos Hg +1 O -2 = Hg2O = óxido de mercurio (I) Hg +2 O
OXIDOS METÁLICOS O BÁSICOS Nomenclatura Stock Regla 1: se escribe la palabra óxido + nombre del metal (catión) + número de oxidación en números romanos Hg +1 O -2 = Hg2O = óxido de mercurio (I) Hg +2 O
Universidad Técnica Nacional
 Universidad Técnica Nacional Química I-CB005 Nomenclatura de Compuestos Inorgánicos Lic. Diego Orozco González Nomenclatura Clasificación de los compuestos Compuestos orgánicos Contienen carbono y otros
Universidad Técnica Nacional Química I-CB005 Nomenclatura de Compuestos Inorgánicos Lic. Diego Orozco González Nomenclatura Clasificación de los compuestos Compuestos orgánicos Contienen carbono y otros
Formulación y Nomenclatura
 Formulación y Nomenclatura La enorme variedad de compuestos químicos hizo necesario desarrollar un método que permitiera entenderse y evitara que un mismo compuesto fuera nombrado de formas distintas según
Formulación y Nomenclatura La enorme variedad de compuestos químicos hizo necesario desarrollar un método que permitiera entenderse y evitara que un mismo compuesto fuera nombrado de formas distintas según
Formulación y Nomenclatura
 La enorme variedad de compuestos químicos hizo necesario desarrollar un método que permitiera entenderse y evitara que un mismo compuesto fuera nombrado de formas distintas según el criterio personal.
La enorme variedad de compuestos químicos hizo necesario desarrollar un método que permitiera entenderse y evitara que un mismo compuesto fuera nombrado de formas distintas según el criterio personal.
Compuestos binarios (combinaciones de dos elementos) HIDRUROS METÁLICOS= Metal - Hidrógeno. X H m. H : - 1 Metales: el suyo. FeH 3
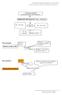 HIDRUROS METÁLICOS= Metal - Hidrógeno AlH 3 ; LiH; CuH 2 X H m KH ; FeH 3 ; ZnH 2 os N de H : - 1 Metales: el suyo Hidruro de hierro(iii) Metal a la izquierda FeH 3 Hidrógeno a la derecha (el mas electronegativo
HIDRUROS METÁLICOS= Metal - Hidrógeno AlH 3 ; LiH; CuH 2 X H m KH ; FeH 3 ; ZnH 2 os N de H : - 1 Metales: el suyo Hidruro de hierro(iii) Metal a la izquierda FeH 3 Hidrógeno a la derecha (el mas electronegativo
Formulación Inorgánica Ejercicios (II)
 Ejercicios (II) EJERCICIOS DE FORMULACIÓN INORGÁNICA (II) COMPUESTOS BINARIOS DEL OXÍGENO 1.- Nombrar: Cl2O7 FeO N2O SO3 Cr2O3 Br2O P2O5 CO2 I2O5 2.- Formular: MnO2 Trióxido de dicromo Óxido de nitrógeno
Ejercicios (II) EJERCICIOS DE FORMULACIÓN INORGÁNICA (II) COMPUESTOS BINARIOS DEL OXÍGENO 1.- Nombrar: Cl2O7 FeO N2O SO3 Cr2O3 Br2O P2O5 CO2 I2O5 2.- Formular: MnO2 Trióxido de dicromo Óxido de nitrógeno
Introducción a la Formulación y Nomenclatura de las Sustancias Inorgánicas
 D EPA R T A M ENTO D E FÍSICA Y Q UÍM ICA Introducción a la Formulación y Nomenclatura de las Sustancias Inorgánicas José Manuel Ramírez Fernández Valencias y estados, grados o números de oxidación Con
D EPA R T A M ENTO D E FÍSICA Y Q UÍM ICA Introducción a la Formulación y Nomenclatura de las Sustancias Inorgánicas José Manuel Ramírez Fernández Valencias y estados, grados o números de oxidación Con
trisulfuro de dialuminio
 NOMENCLATURA DE QUÍMICA INORGÁNICA COMPUESTOS BINARIOS (BACHILLERATO) Para qué la nomenclatura química? Cuando estudiamos química nos encontramos con multitud de sustancias a las que debemos de asignar
NOMENCLATURA DE QUÍMICA INORGÁNICA COMPUESTOS BINARIOS (BACHILLERATO) Para qué la nomenclatura química? Cuando estudiamos química nos encontramos con multitud de sustancias a las que debemos de asignar
FORMULACIÓN INORGÁNICA
 FORMULACIÓN INORGÁNICA La nomenclatura (lista de nombre de los compuestos químicos) y la formulación (fórmula de los compuestos químicos) constituyen el lenguaje químico. Número de oxidación. El número
FORMULACIÓN INORGÁNICA La nomenclatura (lista de nombre de los compuestos químicos) y la formulación (fórmula de los compuestos químicos) constituyen el lenguaje químico. Número de oxidación. El número
Formulación de Química Inorgánica
 Formulación de Química Inorgánica F. G. Calvo-Flores 1. VALENCIA. Es la capacidad que tiene un átomo de un elemento para combinarse con los átomos de otros elementos y formar compuestos. La valencia es
Formulación de Química Inorgánica F. G. Calvo-Flores 1. VALENCIA. Es la capacidad que tiene un átomo de un elemento para combinarse con los átomos de otros elementos y formar compuestos. La valencia es
FORMULACIÓN Y NOMENCLATURA INORGÁNICA
 FORMULACIÓN Y INORGÁNICA (IUPAC 2005) 0 COLEGIO COLÓN MARISTAS HUELVA CURSO ACADÉMICO 2015-2016 ÍNDICE 1. COMPUESTOS BINARIOS.. 2 1.1 ÓXIDOS 2 1.2 HALUROS DE OXÍGENO... 3 1.3 PERÓXIDOS...4 1.4 HIDRUROS..
FORMULACIÓN Y INORGÁNICA (IUPAC 2005) 0 COLEGIO COLÓN MARISTAS HUELVA CURSO ACADÉMICO 2015-2016 ÍNDICE 1. COMPUESTOS BINARIOS.. 2 1.1 ÓXIDOS 2 1.2 HALUROS DE OXÍGENO... 3 1.3 PERÓXIDOS...4 1.4 HIDRUROS..
ÓXIDOS EJEMPLOS EJERCICICIOS. Br 2 O As 2 O 3 B 2 O 3 SnO 2 Cl 2 O 3 As 2 O 5 P 2 O 3. SeO 2 TeO 3 P 2 O 5. Óxido selenioso
 ÓXIDOS EJEMPLOS Fórmula N. Sistemática N. Stock N. tradicional CO Monóxido de carbono Óxido de carbono (I) Óxido carbonoso CO 2 Dióxido de carbono Óxido de carbono (II) Óxido carbónico SO Monóxido de azufre
ÓXIDOS EJEMPLOS Fórmula N. Sistemática N. Stock N. tradicional CO Monóxido de carbono Óxido de carbono (I) Óxido carbonoso CO 2 Dióxido de carbono Óxido de carbono (II) Óxido carbónico SO Monóxido de azufre
trisulfuro de dialuminio
 NOMENCLATURA DE QUÍMICA INORGÁNICA COMPUESTOS BINARIOS Para qué la nomenclatura química? Cuando estudiamos química nos encontramos con multitud de sustancias a las que debemos de asignar un nombre y una
NOMENCLATURA DE QUÍMICA INORGÁNICA COMPUESTOS BINARIOS Para qué la nomenclatura química? Cuando estudiamos química nos encontramos con multitud de sustancias a las que debemos de asignar un nombre y una
FORMULACIÓN (4º ESO)
 FORMULACIÓN (4º ESO) Valencia. Es un número entero que representa el número de electrones que un átomo pone en juego cuando forma un compuesto determinado. NO METALES H (1) -1 +1 METALES Li, Na, K, Rb,
FORMULACIÓN (4º ESO) Valencia. Es un número entero que representa el número de electrones que un átomo pone en juego cuando forma un compuesto determinado. NO METALES H (1) -1 +1 METALES Li, Na, K, Rb,
LOS COMPUESTOS QUÍMICOS
 CONTENIDOS Definición de los compuestos químicos. Clasificación de los compuestos químicos. Escritura y Nomenclatura de los compuestos químicos. Los óxidos básicos o metálicos. Los óxidos ácidos o anhídridos.
CONTENIDOS Definición de los compuestos químicos. Clasificación de los compuestos químicos. Escritura y Nomenclatura de los compuestos químicos. Los óxidos básicos o metálicos. Los óxidos ácidos o anhídridos.
NOMENCLATURA INORGÁNICA
 NOMENCLATURA INORGÁNICA Símbolos y números de oxidación Reglas para conocer el número de oxidación de un elemento. a. El número de oxidación del hidrógeno en sus compuestos es +1, excepto en los hidruros
NOMENCLATURA INORGÁNICA Símbolos y números de oxidación Reglas para conocer el número de oxidación de un elemento. a. El número de oxidación del hidrógeno en sus compuestos es +1, excepto en los hidruros
Características de electrones protones y neutrones
 Características de electrones protones y neutrones Carga eléctrica Masa Espín SI (C) Atómica SI(g) Atómica (uma) Protón +1,6021 10-19 +1 1,6725 10-24 1,0073 1/2 neutrón 0 0 1,6748 10-24 1,0087 1/2 electrón
Características de electrones protones y neutrones Carga eléctrica Masa Espín SI (C) Atómica SI(g) Atómica (uma) Protón +1,6021 10-19 +1 1,6725 10-24 1,0073 1/2 neutrón 0 0 1,6748 10-24 1,0087 1/2 electrón
FORMULACIÓN Y NOMENCLATURA
 FORMULACIÓN Y NOMENCLATURA FORMULACIÓN Una fórmula química es la representación escrita de una molécula o compuesto iónico. Para expresar una fórmula química se utilizan los símbolos de los elementos que
FORMULACIÓN Y NOMENCLATURA FORMULACIÓN Una fórmula química es la representación escrita de una molécula o compuesto iónico. Para expresar una fórmula química se utilizan los símbolos de los elementos que
Formación de compuestos inorgánicos binarios y ternarios
 Formación de compuestos inorgánicos binarios y ternarios Números de oxidación (valencia) Cuando los átomos se unen intercambian o comparten electrones; en general lo hacen de forma tal que completan su
Formación de compuestos inorgánicos binarios y ternarios Números de oxidación (valencia) Cuando los átomos se unen intercambian o comparten electrones; en general lo hacen de forma tal que completan su
FORMACIÓN DE COMPUESTOS INORGÁNICOS. FORMULACIÓN Y NOMENCLATURA
 U.N.P.S.J.B. FACULTAD DE CIENCIAS NATURALES SEDE TRELEW CÁTEDRA DE QUÍMICA GENERAL FORMACIÓN DE COMPUESTOS INORGÁNICOS. FORMULACIÓN Y NOMENCLATURA AÑO 2016 Lic. Maite L. Domínguez Ing. Sebastián Polacco
U.N.P.S.J.B. FACULTAD DE CIENCIAS NATURALES SEDE TRELEW CÁTEDRA DE QUÍMICA GENERAL FORMACIÓN DE COMPUESTOS INORGÁNICOS. FORMULACIÓN Y NOMENCLATURA AÑO 2016 Lic. Maite L. Domínguez Ing. Sebastián Polacco
APUNTES DE FORMULACIÓN Y NOMENCLATURA DE QUÍMICA INORGÁNICA 4º ESO - CURSO METALES
 CONSEJERÍA DE EDUCACIÓN APUNTES DE FORMULACIÓN Y NOMENCLATURA DE QUÍMICA INORGÁNICA 4º ESO - CURSO 2012-2013 1. ELEMENTOS, SÍMBOLOS Y NÚMEROS DE OXIDACIÓN MÁS FRECUENTES EN LA FORMULACIÓN DE QUÍMICA INORGÁNICA
CONSEJERÍA DE EDUCACIÓN APUNTES DE FORMULACIÓN Y NOMENCLATURA DE QUÍMICA INORGÁNICA 4º ESO - CURSO 2012-2013 1. ELEMENTOS, SÍMBOLOS Y NÚMEROS DE OXIDACIÓN MÁS FRECUENTES EN LA FORMULACIÓN DE QUÍMICA INORGÁNICA
FÍSICA Y QUÍMICA. TEMA 3 (parte 2): FORMULACIÓN Y NOMENCLATURA INORGÁNICA
 1 Física y Química 3º Curso Educación Secundaria Obligatoria Curso académico 2016/2017 FÍSICA Y QUÍMICA TEMA 3 (parte 2): FORMULACIÓN Y NOMENCLATURA INORGÁNICA 2 Física y Química 3º Curso Educación Secundaria
1 Física y Química 3º Curso Educación Secundaria Obligatoria Curso académico 2016/2017 FÍSICA Y QUÍMICA TEMA 3 (parte 2): FORMULACIÓN Y NOMENCLATURA INORGÁNICA 2 Física y Química 3º Curso Educación Secundaria
Acuerdo 286. Química. Nomenclatura Inorgánica. Recopiló: M.C. Macaria Hernández Chávez
 Acuerdo 286 Química Nomenclatura Inorgánica Recopiló: M.C. Macaria Hernández Chávez Nomenclatura química inorgánica La Química tiene un lenguaje propio para nombrar las sustancias puras, ya sean simples
Acuerdo 286 Química Nomenclatura Inorgánica Recopiló: M.C. Macaria Hernández Chávez Nomenclatura química inorgánica La Química tiene un lenguaje propio para nombrar las sustancias puras, ya sean simples
Ejemplo 2.- Cuando tiene 4 valencias como el Cl, I, Br, Fluor se usa HIPO-OSO e HIPER-ICO
 FUNCIONES QUÍMICAS INORGANICAS 1. FUNCION QUIMICA.- Es el conjunto de compuestos que tienen ciertas propiedades en común, como por ejemplo un átomo común para todos. Las funciones químicas pueden ser inorgánicas
FUNCIONES QUÍMICAS INORGANICAS 1. FUNCION QUIMICA.- Es el conjunto de compuestos que tienen ciertas propiedades en común, como por ejemplo un átomo común para todos. Las funciones químicas pueden ser inorgánicas
FORMULACIÓN QUÍMICA (3 o ESO) Prof. Jorge Rojo Carrascosa
 FORMULACIÓN QUÍMICA (3 o ESO) QUÍMICA INORGÁNICA Prof. Jorge Rojo Carrascosa Índice general I FORMULACIÓN QUÍMICA INORGÁNICA 2 1. NÚMEROS DE OXIDACIÓN 4 2. COMBINACIONES CON EL OXÍGENO 5 2.1. ÓXIDOS METÁLICOS.........................
FORMULACIÓN QUÍMICA (3 o ESO) QUÍMICA INORGÁNICA Prof. Jorge Rojo Carrascosa Índice general I FORMULACIÓN QUÍMICA INORGÁNICA 2 1. NÚMEROS DE OXIDACIÓN 4 2. COMBINACIONES CON EL OXÍGENO 5 2.1. ÓXIDOS METÁLICOS.........................
