ISOMERÍA CLASIFICACIÓN DE LOS ISÓMEROS:
|
|
|
- Luis Miguel Castilla Mendoza
- hace 7 años
- Vistas:
Transcripción
1 1 ISOMERÍA ISOMERÍA La isomería consiste en el hecho de que dos o más compuestos tienen la misma fórmula molecular, pero diferente estructura molecular; en consecuencia poseen diferentes propiedades físicas y químicas. Se denominan isómeros a los compuestos que tienen la misma fórmula molecular, (tienen el mismo número de átomos de cada tipo, tienen la misma composición química y el mismo peso molecular), pero tienen diferente estructura química (diferente formula estructural). Los isómeros tienen diferentes propiedades físicas y/o químicas. Los isómeros no son superponibles, CLASIFICACIÓN DE LOS ISÓMEROS: Isómeros Estructurales: Los isómeros estructurales son los compuestos que a pesar de tener la misma fórmula molecular difieren en su estructura, bien por la conectividad de la cadena hidrocarbonada (isómería de cadena) o por la conectividad de las funciones (isomería de posición) o bien por poseer funciones diferentes (isomería de función); por tanto sus propiedades físicas y químicas son diferentes. La isomería estructural se clasifica en: Isómeros de cadena: Difieren en la forma en que están unidos los átomos de carbono entre sí para formar una cadena. Por ejemplo: Butano, Isopropano. Las propiedades químicas apenas varían y las propiedades físicas varían gradualmente. QUIMICA ORGÁNICA Página 1
2 2 Metilpropano Butano Dimetilpropano 3 C C 3 C C C 3 3 C C C C C 3 3 C C 3 C C 3 C 3 Metilbutano n-pentano C 3 C 3 C 3 o-dimetilbenceno C 3 m-dimetilbenceno Isómeros de posición: Son compuestos que difieren en las posiciones que ocupan sus grupos funcionales en la estructura carbonada, (tienen las mismas funciones químicas, pero sobre átomos de carbono con números localizadores diferentes). Sus propiedades químicas son muy parecidas y las diferencias en las propiedades físicas son mayores.. Ejemplo 1-Butanol; 2- Butanol. 3 C C C 2 Br 3 C C C 3 Br 1-Bromopropano 2-Bromopropano 2-Butanona 3-Butanona 1-butanol C 3 C 2 C 2 C 2 O 2-butanol C 3 C 2 COC 3 QUIMICA ORGÁNICA Página 2
3 3 Isómeros de función: Son compuestos de igual fórmula molecular, pero la forma en que están unidos los heteroátomos da lugar a que difieran en sus grupos funcionales (presentan funciones químicas diferentes). Sus propiedades físicas y químicas son muy diferentes. Ejemplo. 3 C Propanal C C O O 3 C C C 3 C C C O O 2-idroxipropanal Ácido propanoico 2-idroxi-2-metilpropano O 3 C C C 3 OC 3 Isopropilmetileter C 3 3 C C C 3 O Propanona 1-idroxipropanol Etilmetileter C 3 COC 3 ESTEREOQUIMICA: Es la parte de la química que se ocupa del estudio de la disposición espacial de los átomos que componen las moléculas y de cómo afecta esto a las propiedades y reactividad de dichas moléculas. ISOMERÍA EN EL ESPACIO O ESTEREOISOMERÍA Es la isomería que presentan los compuestos que se diferencian únicamente en la disposición de sus átomos en el espacio. Moléculas con fórmulas moleculares idénticas pueden presentar estructuras espaciales diferentes y se denominan estereoisómeros (moléculas isómeras, que aun teniendo los mismos enlaces y ordenación entre sus átomos difieren en el modo en que estos átomos están dispuestos en el espacio). Se clasifican por sus propiedades de simetría. QUIMICA ORGÁNICA Página 3
4 4 Estereoisomero quiral Es aquel estereoisómero que no es superponible con su imagen en el espejo. La molécula de un esteroisómero quiral no tiene elementos de simetría, es ópticamente activa y desvía el plano de la luz polarizada, hacia la derecha: dextrógiros o hacia la izquierda: levógiros Una molécula puede ser quiral debido a que posee: Con centro quiral: 1 átomo quiral, ay varias circunstancias que posibilitan que un átomo de C sea quiral, el caso que nos interesa es el de un átomo de C tetraédrico (hibridación sp 3 ) con 4 sustituyentes diferentes; también la estructura del adamantano, los átomos piramidales con 3 sustituyentes diferentes, los complejos octaédricos convenientemente sustituidos presentan centro quiral. Sin centro quiral pero con eje quiral (planos disimétricos perpendiculares) Con dos o más centros quirales Sin centro quiral pero con plano quiral (compuestos sándwich) QUIMICA ORGÁNICA Página 4
5 5 C tetraédrico quiral N trigonal quiral Moléculas quirales (no superponibles) Estereoisomero aquiral o no quiral Es aquel que es superponible con su imagen en el espejo (tiene elementos de simetría). Cuando una molécula es superponible con su imagen especular no es ópticamente activa y, por tanto, es incapaz de desviar el plano de la luz polarizada. En resumen: Cuando hay más de un carbono asimétrico (como en la mayoría de los azúcares) aumentan las posibilidades de isomería. El número de estereoisómeros posibles es 2 n (siendo n el número de carbonos asimétricos) y, de entre todos estos estereoisómeros ópticos, aquellos que sean imágenes especulares entre sí reciben el nombre de enantiomorfos, enantiómeros o isómeros quirales. Pero puede ocurrir que dos isómeros ópticos no sean imágenes especulares entre sí. Son los llamados diastereoisómeros. Las moléculas que contienen sólo un átomo de carbono asimétrico son siempre quirales. Las moléculas con más de un átomo de carbono asimétrico no son necesariamente quirales, éste es el caso de las formas meso En las estructuras anteriores (Ácido 2,3,dihidroxibutanodioco) los C-2 y C-3 son asimétricos, pero las moléculas son aquirales porque poseen un plano de simetría en la propia molécula. QUIMICA ORGÁNICA Página 5
6 6 (Puedes comprobar que por rotación de 180º de la 2ª molécula según un eje perpendicular al plano del papel obtienes la 1ª; son, por tanto, la misma estructura, no son estereoisómeros) Estereoisómeros conformacionales: Son estereoisómeros que se caracterizan por poder modificar su orientación espacial, por rotación en torno a enlaces simples (los C tienen hibridación sp 3 ) convirtiéndose en otro isómero de la misma molécula; existen conformaciones: anti, eclipsada o alternada. Los estereoisómeros conformacionales o confórmeros de un compuesto se interconvierten rápidamente a temperatura ambiente debido a que la barrera energética que hay que superar para la interconversión es muy baja; por esta razón resulta imposible mantenerlos aislados por separado. Confórmeros del ciclobutano Confórmeros del ciclohexano Estereoisómeros configuracionales: Son estereoisómeros que tienen la misma forma estructural y diferente disposición de sus átomos en el espacio pero son estructuralmente estables, se pueden aislar, por separado a temperatura ambiente. En la mayor parte de los casos para transformar uno en otro no basta con realizar giros alrededor de enlaces sencillos sino que es necesario romper y formar enlaces teniendo que vencer una barrera energética alta). QUIMICA ORGÁNICA Página 6
7 7 Estereoisomeros geométricos: Son estereoisómeros porque difieren únicamente en la disposición espacial de los grupos, en concreto difieren en la ordenación de los grupos en el plano. La isomería geométrica es característica de los compuestos orgánicos que poseen dos átomos de carbonos unidos por un doble enlace, recuerda que, debido a la hibridación de los átomos de C que participan en el doble enlace la estructura es plana (3 orbitales híbridos sp 2 dirigidos hacia los vértices de un triángulo equilátero). Recuerda que el doble enlace consiste en un enlace sigma, σ, más un enlace π, éste último se halla en un plano perpendicular al plano definido por el enlace σ e impide la rotación libre de la molécula en torno al enlace doble que une C=C. Además, para que se produzca este tipo de isomería, cada uno de los C que soportan el doble enlace tienen que tener 2 sustituyentes diferentes. Ejemplos aclaratorios: ClC=CCl ; ClC=CBr; sí presentan isomería geométrica 2 C=CCl; 2 C=C 2 no presentan isomería geométrica QUIMICA ORGÁNICA Página 7
8 8 Los sustituyentes iguales pueden estar situados al mismo lado del doble enlace (cis) o en lados opuestos (trans). No se presenta isomería geométrica si tiene tres o los cuatro sustituyentes iguales. Tampoco puede presentarse con triples enlaces. La primera estructura es cis- porque los grupos isopropilo y metilo quedan al mismo lado del plano que contiene al orbital molecular π, en la segunda estructura quedan a lados opuestos, razón por la que esta ultima estructura es trans-. Los estereoisómeros geométricos no pueden convertirse uno en otro sin que se rompa un enlace químico. El doble enlace C=C no permite el giro cuyo eje sea dicho enlace. Supongamos un doble enlace C=C, disustituido, siendo ambos sustituyentes idénticos, por ejemplo, el 2- buteno, C 3 C=CC 3, éste presenta 2 isómeros geométricos. Si los dos sustituyentes están del mismo lado del plano que contiene a la nube π el compuesto es CIS. Si están en distinto lado es TRANS. Los isómeros cis, trans no son convertibles el uno en el otro porque carecen de libre rotación en torno al doble enlace Cis-1,2-dimetilciclopentano Trans-1,2-dimetilciclpopentano QUIMICA ORGÁNICA Página 8
9 9 Esta isomería puede aparecer también en compuestos cíclicos. Isomería cis-trans en ciclos: Los cicloalcanos tienen dos caras o lados debido al plano que contiene el esqueleto carbonado; cuando en el ciclo hay dos sustituyentes en átomos de carbono distintos, existen dos isómeros. Si los sustituyentes se encuentran del mismo lado del plano que contiene al esqueleto carbonado es el isómero cis, y si están en lados opuestos es el isómero trans.las reglas de Can-Ingold y Prelog permiten la notación Z si los sustituyentes de mayor prioridad están al mismo lado y E si los sustituyentes prioritarios están alados opuestos. Isómeros Cis y Trans del 1,3-dimetilciclobutano ISOMERÍA ÓPTICA: La isomería óptica (estereoisomería óptica) es la isomería que presentan aquellos compuestos orgánicos que se diferencian únicamente en el efecto que tienen sobre el plano de polarización de la luz polarizada, lo desvían hacia la izquierda, (isómeros ópticos levógiros), (-), y se identifica con la letra S; o hacia la derecha (isómeros ópticos dextrógiros), (+), y se identifica con la letra R; decimos en estos casos que son compuestos ópticamente activos. Las moléculas de los compuestos ópticamente activos son moléculas quirales. Existen varias causas de quiralidad en las moléculas, la que nos interesa es la producida por la presencia de C quirales (un C*, asimétrico, o más de uno). Para que un C sea quiral o asimétrico tiene que tener hibridación sp 3 (C tetraédrico) y tener 4 sustituyentes distintos. Para una molécula con estas características siempre es posible encontrar otra, que es su imagen especular, (imagen formada en el espejo), ambas son entre sí enantiomorfas o enantioméricas o enantiómeras/os y no son superponibles. Toda molécula no quiral, (sin actividad óptica) recibe el nombre de aquiral. Ahora bien, si una molécula es aquiral puede deberse: no tiene átomos de C quirales aunque tiene átomos de C quirales posee un plano de simetría interno que la hace QUIMICA ORGÁNICA Página 9
10 10 inactiva ópticamente, la misma molécula desvía el plano de la luz polarizada en sentidos opuestos en igual magnitud). Enantiómeros: Pareja de estereoisómeros configuracionales ópticamente activos, no superponibles, que guardan entre sí una relación de imagen especular uno del otro. Dos compuestos son entre sí enantiómeros si la imagen especular de uno no puede ser superpuesta con la del otro, en otros términos: ellos no son superponibles. Dos enantiómeros desvían el plano de la luz polarizada en la misma magnitud pero en sentidos opuestos. Al enantiómero que rota el plano de vibración de la luz polarizada en el sentido de las agujas del reloj, (hacia la derecha), se le denomina isómero dextro-, dextrorrotatorio o dextrógiro y se nombra anteponiendo al nombre del compuesto el signo (+) o también la letra d minúscula; y análogamente, al enantiómero que rota el plano de vibración de la luz polarizada en sentido contrario a las agujas del reloj, (hacia la izquierda), se le denomina isómero levo levorrotatorio o levógiro y se nombra anteponiendo al nombre del compuesto el signo (-) o también la letra l minúscula. Propiedades de los enantiómeros: Los enantiómeros tienen las mismas propiedades químicas y físicas, a excepción de su respuesta ante la luz polarizada (actividad óptica), de ahí al nombre de isómeros ópticos. Los enantiómeros se interconvierten a temperatura ambiente por efecto de sombrilla. La rotación específica de la luz polarizada, se mide por medio de un polarímetro, es una propiedad física característica de la estructura de cada enantiómero, de su concentración y del disolvente empleado en la medición. La mezcla equimolecular de enantiómeros se denomina mezcla racémica o racemato. Una mezcla racémica no rota el plano de vibración de la luz polarizada. Las propiedades del racemato no son siempre las mismas que las de los enantiómeros por separado, depende del estado de agregación. Se denomina resolución del racemato a la separación de los componentes de un racémico QUIMICA ORGÁNICA Página 10
11 11 A B C D A y B forman una pareja de enantiómeros; C y D forman otra pareja distinta QUIMICA ORGÁNICA Página 11
12 12 Diastereoisómeros Son estereoisómeros configuracionales que no son imágenes especulares entre si Flechas horizontales: enantiómeros Flechas verticales y oblicuas: diastereoisómeros QUIMICA ORGÁNICA Página 12
13 13 Propiedades de los diastereoisómeros: Los diastereoisómeros difieren en sus propiedades físicas y químicas, razón por la que pueden separarse mediante procedimientos de destilación, cristalización o cromatografía. QUIMICA ORGÁNICA Página 13
14 14 Resumiendo: Dentro del grupo de los diasterómeros se encuentran los isómeros cis-trans (antes conocido como Isómeros Geométricos), los confórmeros o isómeros conformacionales y, en las moléculas con varios centros quirales, los isómeros que pertenecen a distintas parejas de enantiómeros. Si una molécula tiene varios centros quirales obtendremos diastereómeros cambiando la configuración absoluta de uno de los centros quirales y manteniendo la del resto. QUIMICA ORGÁNICA Página 14
15 15 PROYECCIONES DE FISCER Las proyecciones de Fischer son utilizadas en química orgánica para representar en dos dimensiones la disposición espacial de moléculas tridimensionales en las que uno o más átomos de carbono están unidos a 4 sustituyentes diferentes. En una proyección de Fischer, un átomo de carbono tetraédrico se representa por dos líneas cruzadas. Por convenio, las líneas horizontales representan enlaces que salen de la página hacia el lector, y las líneas verticales representan enlaces que entran en la página y se alejan del lector. El esquema anterior representa un compuesto con un átomo tetraédrico, asimétrico, (hibridación sp 3 y 4 sustituyentes diferentes dirigidos hacia los vértices de un tetraedro). Giramos el compuesto de forma que dos de sus enlaces queden en un plano vertical y hacia atrás, (alejándose del lector) y los otros dos en un plano horizontal y hacia delante, (acercándose al lector) (es fácil si te ayudas de los dedos índice y pulgar de cada mano); a continuación proyectamos la molécula sobre el plano del papel como si la aplastásemos. Cuando la molécula tiene dos carbonos asimétricos, para realizar la proyección de Fischer los carbonos quirales C*-C*queden en línea. QUIMICA ORGÁNICA Página 15
16 16 Nomenclatura de los estereoisómeros (R, S) - - Proyección de Newman Fischer QUIMICA ORGÁNICA Página 16
17 17 Tienen los compuestos la misma fórmula molecular? NO SI Isómeros No Isómeros NO Tienen los compuestos la misma conectividad? SI Estereoisómeros Son interconvertibles por rotación en torno a enlaces simples C-C? NO SI Configuracional SI Es producida por un doble enlace? NO Óptica NO Son los compuestos imágenes especulares no superponibles? SI QUIMICA ORGÁNICA Página 17
Clasificación de los isómeros:
 ISOMERÍA onsiste en que dos o más compuestos tienen la misma fórmula molecular, pero diferente estructura molecular. En consecuencia poseen diferentes propiedades físicas y químicas. Se denominan isómeros
ISOMERÍA onsiste en que dos o más compuestos tienen la misma fórmula molecular, pero diferente estructura molecular. En consecuencia poseen diferentes propiedades físicas y químicas. Se denominan isómeros
TEMA 2 ESTEREOQUÍMICA
 TEMA 2 ESTEREOQUÍMICA La estereoquímica es el estudio de las moléculas en tres dimensiones. Quiralidad vs Aquiralidad Imagen especular original Molécula original Molécula quiral: La molécula rotada no
TEMA 2 ESTEREOQUÍMICA La estereoquímica es el estudio de las moléculas en tres dimensiones. Quiralidad vs Aquiralidad Imagen especular original Molécula original Molécula quiral: La molécula rotada no
QUÍMICA. 2º Bachilerrato orgánica Estereoisomería:
 TEMA 10: QUÍMICA ORÁNICA. 1.- Isomerías. En química orgánica es usual encontrar compuestos químicos diferentes que poseen igual fórmula molecular. Estos compuestos se denominan isómeros. 1.1. Isómeros
TEMA 10: QUÍMICA ORÁNICA. 1.- Isomerías. En química orgánica es usual encontrar compuestos químicos diferentes que poseen igual fórmula molecular. Estos compuestos se denominan isómeros. 1.1. Isómeros
Isomería estructural o constitucional
 TEMA 7.- Estereoisomería. Isomería: constitucional y estereoisomería. Isomería óptica. Quiralidad y enantiomería. Configuraciones absoluta y relativa. Moléculas con dos o más estereocentros: diastereoisomería
TEMA 7.- Estereoisomería. Isomería: constitucional y estereoisomería. Isomería óptica. Quiralidad y enantiomería. Configuraciones absoluta y relativa. Moléculas con dos o más estereocentros: diastereoisomería
Lección 6: ESTEREOQUÍMICA II
 Lección 6: ETEEOQUÍMICA II 1.Configuración absoluta y relativa. 2. Notaciones y. eglas de prioridad. 3. Fórmulas de proyección de Fischer. 4. Moléculas con más de un centro estereogénico. 5. Diastereoisómeros
Lección 6: ETEEOQUÍMICA II 1.Configuración absoluta y relativa. 2. Notaciones y. eglas de prioridad. 3. Fórmulas de proyección de Fischer. 4. Moléculas con más de un centro estereogénico. 5. Diastereoisómeros
TEMA 4 ESTEREOQUÍMICA
 TEMA 4 ESTEREOQUÍMICA 1. Estereoisomería. 2. Isomería geométrica (cis/trans). 3. Isomería óptica. 4. Configuración del estereocentro: Nomenclatura R y S. 5. Proyecciones de Fisher. 6. Moléculas con más
TEMA 4 ESTEREOQUÍMICA 1. Estereoisomería. 2. Isomería geométrica (cis/trans). 3. Isomería óptica. 4. Configuración del estereocentro: Nomenclatura R y S. 5. Proyecciones de Fisher. 6. Moléculas con más
QUÍMICA. 1º A bachillerato.
 QUÍMIA. º A bachillerato. Isomería y nomenclatura 9/ebrero/05.. Establece la jerarquía, de mayor a menor, de los grupos funcionales que se formulan a continuación, nombra cada grupo funcional y la familia
QUÍMIA. º A bachillerato. Isomería y nomenclatura 9/ebrero/05.. Establece la jerarquía, de mayor a menor, de los grupos funcionales que se formulan a continuación, nombra cada grupo funcional y la familia
TEMA 8 ESTEREOQUIMICA II
 TEMA 8 ESTEREQUIMIA II 1. Isomería geométrica. 2. Quiralidad: noción de centro esteroquímico. Nomenclatura R y S. 3. ompuestos con varios carbonos quirales: diastereoisómeros y compuestos meso. 4. Actividad
TEMA 8 ESTEREQUIMIA II 1. Isomería geométrica. 2. Quiralidad: noción de centro esteroquímico. Nomenclatura R y S. 3. ompuestos con varios carbonos quirales: diastereoisómeros y compuestos meso. 4. Actividad
1. Composición. Clase y número de átomos que dan lugar a la molécula.
 Tema 2 Principios estereoquímicos. 2. QUIALIDAD Y ELEMENTOS DE SIMETÍA. uatro aspectos generales definen la estructura de la molécula:. omposición. lase y número de átomos que dan lugar a la molécula.
Tema 2 Principios estereoquímicos. 2. QUIALIDAD Y ELEMENTOS DE SIMETÍA. uatro aspectos generales definen la estructura de la molécula:. omposición. lase y número de átomos que dan lugar a la molécula.
Tema 11. CONCEPTOS FUNDAMENTALES EN QUÍMICA ORGÁNICA
 Tema 11. EPTS FUDAMETALES E QUÍMIA RGÁIA o metales con electronegatividad similar (,,, ). Uniones covalentes debilmente polares o apolares Reactividad: interacciones entre áreas o zonas de las moléculas
Tema 11. EPTS FUDAMETALES E QUÍMIA RGÁIA o metales con electronegatividad similar (,,, ). Uniones covalentes debilmente polares o apolares Reactividad: interacciones entre áreas o zonas de las moléculas
10.-Estudio de la Isomería
 10.-Estudio de la Isomería Isomeria http://www.juntadeandalucia.es/averroes/recursos_informaticos/concu rso1998/accesit8/ci.htm Isomeria http://www.telecable.es/personales/albatros1/quimica/isomeria/isomeri
10.-Estudio de la Isomería Isomeria http://www.juntadeandalucia.es/averroes/recursos_informaticos/concu rso1998/accesit8/ci.htm Isomeria http://www.telecable.es/personales/albatros1/quimica/isomeria/isomeri
Cátedra de Química Orgánica I Instituto de Química Orgánica Fac. de Bioquímica, Química y Farmacia Universidad Nacional de Tucumán
 átedra de Química Orgánica I Instituto de Química Orgánica Fac. de Bioquímica, Química y Farmacia Universidad Nacional de Tucumán Objetivos Al finalizar la misma los alumnos deben: omprender el significado
átedra de Química Orgánica I Instituto de Química Orgánica Fac. de Bioquímica, Química y Farmacia Universidad Nacional de Tucumán Objetivos Al finalizar la misma los alumnos deben: omprender el significado
Clase No.11: Estereoquímica, Isomería óptica y Rotación específica
 Clase No.11: Estereoquímica, Isomería óptica y Rotación específica Departamento de Química Orgánica Facultad de Ciencias Químicas y Farmacia Universidad de San Carlos de Guatemala Quiralidad Porqué no
Clase No.11: Estereoquímica, Isomería óptica y Rotación específica Departamento de Química Orgánica Facultad de Ciencias Químicas y Farmacia Universidad de San Carlos de Guatemala Quiralidad Porqué no
Ejercicios variados resueltos
 Ejercicios variados resueltos Programa de Acceso Inclusivo, Equidad y Permanencia 1. Cuál de los siguientes compuestos es isómero del CH 3 CH 2 COOH? a) CH 3 CO CH 2 OH b) CH 3 CH 2 CHO c) CH 2 =CH COOH
Ejercicios variados resueltos Programa de Acceso Inclusivo, Equidad y Permanencia 1. Cuál de los siguientes compuestos es isómero del CH 3 CH 2 COOH? a) CH 3 CO CH 2 OH b) CH 3 CH 2 CHO c) CH 2 =CH COOH
ALCANOS. Estructura y propiedades
 TEMA 5.- idrocarburos y alcanos. idrocarburos: tipos y clasificación. idrocarburos saturados. Características generales. Formas de representación espacial. Análisis conformacional. Reactividad. Los hidrocarburos
TEMA 5.- idrocarburos y alcanos. idrocarburos: tipos y clasificación. idrocarburos saturados. Características generales. Formas de representación espacial. Análisis conformacional. Reactividad. Los hidrocarburos
ORGÁNICA I. 1.- Escribir y nombrar el compuesto obtenido por reacción entre a) el ácido acético y el 2-propanol. b) cloruro de acetilo con agua.
 ORGÁNICA I 1.- Escribir y nombrar el compuesto obtenido por reacción entre a) el ácido acético y el 2-propanol. b) cloruro de acetilo con agua. 2.- Escribir y nombrar el producto principal obtenido en
ORGÁNICA I 1.- Escribir y nombrar el compuesto obtenido por reacción entre a) el ácido acético y el 2-propanol. b) cloruro de acetilo con agua. 2.- Escribir y nombrar el producto principal obtenido en
Facultad de Ciencias Forestales UNIVERSIDAD NACIONAL DE SANTIAGO DEL ESTERO
 Serie Didáctica N 32 Facultad de Ciencias Forestales UNIVERSIDAD NACIONAL DE SANTIAGO DEL ESTERO E-Book ISBN 978-987-1676-42-2. Fecha de catalogación: 19/12/2014. C A T E D R A D E Química Orgánica y Biológica
Serie Didáctica N 32 Facultad de Ciencias Forestales UNIVERSIDAD NACIONAL DE SANTIAGO DEL ESTERO E-Book ISBN 978-987-1676-42-2. Fecha de catalogación: 19/12/2014. C A T E D R A D E Química Orgánica y Biológica
Tema 2. Alcanos y cicloalcanos, isomería conformacional y geométrica
 Tema 2. Alcanos y cicloalcanos, isomería conformacional y geométrica Existen tres clases principales de Hidrocarburos: Hidrocarburos saturados (alcanos y cicloalcanos) Hidrocarburos insaturados (alquenos
Tema 2. Alcanos y cicloalcanos, isomería conformacional y geométrica Existen tres clases principales de Hidrocarburos: Hidrocarburos saturados (alcanos y cicloalcanos) Hidrocarburos insaturados (alquenos
Enlace químico II: geometría molecular e hibridación de orbitales atómicos
 Enlace químico II: geometría e hibridación de orbitales atómicos Capítulo 10 Modelo de la repulsión de los pares de electrones de la capa de valencia (): Predice la geometría de la molécula a partir de
Enlace químico II: geometría e hibridación de orbitales atómicos Capítulo 10 Modelo de la repulsión de los pares de electrones de la capa de valencia (): Predice la geometría de la molécula a partir de
TEMA 7 ESTEREOQUIMICA I
 TEMA 7 ESTEREOQUIMIA I. oncepto de estereoquímica.. Isomería conformacional.. onformaciones y estabilidades de los cicloalcanos. Fundamentos de Química Orgánica TEMA 7. ESTEREOQUIMIA I.. oncepto de estereoquímica..
TEMA 7 ESTEREOQUIMIA I. oncepto de estereoquímica.. Isomería conformacional.. onformaciones y estabilidades de los cicloalcanos. Fundamentos de Química Orgánica TEMA 7. ESTEREOQUIMIA I.. oncepto de estereoquímica..
Isomería óptica. Química Orgánica I (Química) Preparado por Licda. Nora Guzmán (USAC) Basado en C. Coronel (Universidad de Tucuman)
 Isomería óptica Química Orgánica I (Química) Preparado por Licda. Nora Guzmán (USAC) Basado en C. Coronel (Universidad de Tucuman) Isómeros Son compuestos que presentan la misma fórmula molecular, pero
Isomería óptica Química Orgánica I (Química) Preparado por Licda. Nora Guzmán (USAC) Basado en C. Coronel (Universidad de Tucuman) Isómeros Son compuestos que presentan la misma fórmula molecular, pero
Tema 3: Estereoisomería
 Tema 3: Estereoisomería En la portada vemos dos moléculas, una es la imagen especular de la otra. Se trata del hidrocarburo limoneno que puede tener dos configuraciones distintas: una es como la mano izquierda
Tema 3: Estereoisomería En la portada vemos dos moléculas, una es la imagen especular de la otra. Se trata del hidrocarburo limoneno que puede tener dos configuraciones distintas: una es como la mano izquierda
Análisis Conformacional de Cicloalcanos. Facultad de CC.QQ y Farmacia USAC Departamento de Química Orgánica Química Orgánica 1 Sección D 2014
 Análisis Conformacional de Cicloalcanos Facultad de CC.QQ y Farmacia USAC Departamento de Química Orgánica Química Orgánica 1 Sección D 2014 La forma de los Cicloalcanos: Son Planos o No? Rotación restringida
Análisis Conformacional de Cicloalcanos Facultad de CC.QQ y Farmacia USAC Departamento de Química Orgánica Química Orgánica 1 Sección D 2014 La forma de los Cicloalcanos: Son Planos o No? Rotación restringida
Química Orgánica. por átomos de carbono. A diferencia de otros
 Química Orgánica La definición moderna de la química orgánica es el estudio de los compuestos que se componen por átomos de carbono. A diferencia de otros elementos, el carbono crea enlaces muy fuertes
Química Orgánica La definición moderna de la química orgánica es el estudio de los compuestos que se componen por átomos de carbono. A diferencia de otros elementos, el carbono crea enlaces muy fuertes
Tema 9. Química Orgánica
 Tema 9. Química Orgánica ÍNDICE 1. Enlace covalente en las moléculas orgánicas 1.1. ibridaciones del carbono 1.2. Resonancia 1.3. Polaridad de enlace 2. Representación de moléculas orgánicas 3. idrocarburos
Tema 9. Química Orgánica ÍNDICE 1. Enlace covalente en las moléculas orgánicas 1.1. ibridaciones del carbono 1.2. Resonancia 1.3. Polaridad de enlace 2. Representación de moléculas orgánicas 3. idrocarburos
Lección 1: GENERALIDADES
 Lección 1: GENERALIDADES 1.Concepto de Química Orgánica. Introducción histórica. 2. Estructuras de Lewis. Estructuras resonantes. 3. Geometría de las moléculas. 4. Representaciones de las moléculas orgánicas
Lección 1: GENERALIDADES 1.Concepto de Química Orgánica. Introducción histórica. 2. Estructuras de Lewis. Estructuras resonantes. 3. Geometría de las moléculas. 4. Representaciones de las moléculas orgánicas
TEMA 2: Resonancia Magnética Nuclear RMN-1H y 13C Fundamentos
 Fundamentos La Resonancia Magnética Nuclear (RMN) es la técnica que mayor información estructural proporciona. Ello se debe a que se observan los núcleos de los átomos y se puede conocer la influencia
Fundamentos La Resonancia Magnética Nuclear (RMN) es la técnica que mayor información estructural proporciona. Ello se debe a que se observan los núcleos de los átomos y se puede conocer la influencia
Hibridación y Momento Dipolar
 Hibridación y Momento Dipolar Conceptos Previos El orbital o capa de valencia es el orbital asociado al más alto nivel cuántico que contiene electrones. La forma de como se ordenan los electrones de valencia
Hibridación y Momento Dipolar Conceptos Previos El orbital o capa de valencia es el orbital asociado al más alto nivel cuántico que contiene electrones. La forma de como se ordenan los electrones de valencia
MATERIA: ES TODO LO QUE TIENE MASA Y VOLUMEN.
 MATERIA: ES TODO LO QUE TIENE MASA Y VOLUMEN. CLASIFICACIÓN DE LA MATERIA: SEGÚN: A. ESTADO DE AGREGACIÓN. B. COMPOSICIÓN. A. ESTADO DE AGREGACIÓN. SE REFIERE A LA FORMA DE INTERACCIÓN ENTRE LAS MOLÉCULAS
MATERIA: ES TODO LO QUE TIENE MASA Y VOLUMEN. CLASIFICACIÓN DE LA MATERIA: SEGÚN: A. ESTADO DE AGREGACIÓN. B. COMPOSICIÓN. A. ESTADO DE AGREGACIÓN. SE REFIERE A LA FORMA DE INTERACCIÓN ENTRE LAS MOLÉCULAS
Química orgánica. Carrera: IAC Participantes. Representantes de las academias de Ingeniería Ambiental. Academia de Ingeniería
 1.- DATOS DE LA ASIGNATURA Nombre de la asignatura: Carrera: Clave de la asignatura: Horas teoría-horas práctica-créditos Química orgánica Ingeniería Ambiental IAC - 0428 4-2-10 2.- HISTORIA DEL PROGRAMA
1.- DATOS DE LA ASIGNATURA Nombre de la asignatura: Carrera: Clave de la asignatura: Horas teoría-horas práctica-créditos Química orgánica Ingeniería Ambiental IAC - 0428 4-2-10 2.- HISTORIA DEL PROGRAMA
ESTEREOQUÍMICA. Química Orgánica 2º LECCIÓN 3 Antonio Galindo Brito 1. Objetivos
 Química rgánica º LEIÓN ntonio Galindo rito ESTEEQUÍMI bjetivos onocer el fenómeno de la estereoisomería y los conceptos derivados como centro quiral, quiralidad, aquiralidad, enantiomería, mezcla racémica,
Química rgánica º LEIÓN ntonio Galindo rito ESTEEQUÍMI bjetivos onocer el fenómeno de la estereoisomería y los conceptos derivados como centro quiral, quiralidad, aquiralidad, enantiomería, mezcla racémica,
INTRODUCCIÓN A LA QUÍMICA ORGÁNICA
 CONTENIDOS. INTRODUCCIÓN A LA QUÍMICA ORGÁNICA 1.- Primeros pasos de la Química Orgánica. 2.- Características del carbono y de los compuestos orgánicos. 3.- Tipos de enlaces del carbono. 4.- Representación
CONTENIDOS. INTRODUCCIÓN A LA QUÍMICA ORGÁNICA 1.- Primeros pasos de la Química Orgánica. 2.- Características del carbono y de los compuestos orgánicos. 3.- Tipos de enlaces del carbono. 4.- Representación
Susana Latorre Licenciada en Ciencias químicas
 Susana Latorre Licenciada en Ciencias químicas QUIMICA INORGANICA QUIMICA ORGANICA TIPOS DE ENLACES QUE ES UN ELEMENTO QUIMICO QUE ES UNA MOLECULA QUE ES UNA REACCION. COMO SE ESCRIBE ELEMENTO QUIMICO
Susana Latorre Licenciada en Ciencias químicas QUIMICA INORGANICA QUIMICA ORGANICA TIPOS DE ENLACES QUE ES UN ELEMENTO QUIMICO QUE ES UNA MOLECULA QUE ES UNA REACCION. COMO SE ESCRIBE ELEMENTO QUIMICO
Los elementos químicos
 Los elementos químicos Física y Química Las primeras clasificaciones de los elementos Oxford University Press España, S. A. Física y Química 3º ESO 2 Un elemento químico es un tipo de materia constituido
Los elementos químicos Física y Química Las primeras clasificaciones de los elementos Oxford University Press España, S. A. Física y Química 3º ESO 2 Un elemento químico es un tipo de materia constituido
ESTEREOQUIMICA ISOMERIA OPTICA
 ESTEREOQUIMICA ISOMERIA OPTICA Importancia de la enantioselectividad en los medicamentos "Durante su embarazo, a mi madre le recetaron talidomida contra los mareos matutinos. Mi madre tomó talidomida dos
ESTEREOQUIMICA ISOMERIA OPTICA Importancia de la enantioselectividad en los medicamentos "Durante su embarazo, a mi madre le recetaron talidomida contra los mareos matutinos. Mi madre tomó talidomida dos
Enlace químico II: geometría molecular e hibridación de orbitales atómicos
 Enlace químico II: geometría molecular e hibridación de orbitales atómicos Capítulo 10 Copyright The McGraw-Hill Companies, Inc. Permission required for reproduction or display. Teorías de cómo ocurren
Enlace químico II: geometría molecular e hibridación de orbitales atómicos Capítulo 10 Copyright The McGraw-Hill Companies, Inc. Permission required for reproduction or display. Teorías de cómo ocurren
CARACTERIZACIÓN DE ISÓMEROS ÓPTICOS POR POLARIMETRÍA
 CARACTERIZACIÓN DE ISÓMEROS ÓPTICOS POR POLARIMETRÍA OBJETIVO Caracterizar los diastereoisómeros puros del complejo [Co(en) 3 ]. 3 I 3 previamente sintetizado por medio de la medición de su actividad óptica
CARACTERIZACIÓN DE ISÓMEROS ÓPTICOS POR POLARIMETRÍA OBJETIVO Caracterizar los diastereoisómeros puros del complejo [Co(en) 3 ]. 3 I 3 previamente sintetizado por medio de la medición de su actividad óptica
TEMA 4. EFECTOS ELECTRÓNICOS. ENLACES DESLOCALIZADOS.
 TEMA 4. EFECTOS ELECTRÓNICOS. ENLACES DESLOCALIZADOS. 1. Estructuras de resonancia. 1.1. Contribución de las estructuras resonantes. 1.2. Cómo dibujar estructuras resonantes 2. Efecto inductivo. 3. Efecto
TEMA 4. EFECTOS ELECTRÓNICOS. ENLACES DESLOCALIZADOS. 1. Estructuras de resonancia. 1.1. Contribución de las estructuras resonantes. 1.2. Cómo dibujar estructuras resonantes 2. Efecto inductivo. 3. Efecto
Teoría atómica: Leyes de la combinación química
 Teoría atómica: Leyes de la combinación química La materia y la química. Disoluciones vs sustancias. Sustancias puras (elementos y compuestos) I. La materia y la química Uno de los primeros objetivos que
Teoría atómica: Leyes de la combinación química La materia y la química. Disoluciones vs sustancias. Sustancias puras (elementos y compuestos) I. La materia y la química Uno de los primeros objetivos que
Técnico Profesional QUÍMICA
 Programa Técnico Profesional QUÍMICA Geometría molecular Nº Ejercicios PSU 1. La siguiente figura muestra la estructura del gas metano. C Al respecto, qué valor adopta el ángulo de enlace en este compuesto?
Programa Técnico Profesional QUÍMICA Geometría molecular Nº Ejercicios PSU 1. La siguiente figura muestra la estructura del gas metano. C Al respecto, qué valor adopta el ángulo de enlace en este compuesto?
PROBLEMAS RESUELTOS SELECTIVIDAD ANDALUCÍA 2010 QUÍMICA TEMA 3: ENLACES QUÍMICOS
 PROBLEMAS RESUELTOS SELECTIVIDAD ANDALUCÍA 010 QUÍMICA TEMA : ENLACES QUÍMICOS Junio, Ejercicio, Opción A Reserva 1, Ejercicio, Opción A Reserva, Ejercicio, Opción B Reserva, Ejercicio, Opción B Septiembre,
PROBLEMAS RESUELTOS SELECTIVIDAD ANDALUCÍA 010 QUÍMICA TEMA : ENLACES QUÍMICOS Junio, Ejercicio, Opción A Reserva 1, Ejercicio, Opción A Reserva, Ejercicio, Opción B Reserva, Ejercicio, Opción B Septiembre,
TEMA 3.2 El Enlace Covalente
 TEMA 3.2 El Enlace Covalente» Estructuras de Lewis: Regla del ctete Formas resonantes Carga formal Excepciones a la regla del octete» Geometría Molecular: Teoría RPENV (Repulsión de los pares de electrones
TEMA 3.2 El Enlace Covalente» Estructuras de Lewis: Regla del ctete Formas resonantes Carga formal Excepciones a la regla del octete» Geometría Molecular: Teoría RPENV (Repulsión de los pares de electrones
Programa de Acceso Inclusivo, Equidad y Permanencia PAIEP U. de Santiago. Biología. Glúcidos o hidratos de carbono.
 Glúcidos o hidratos de carbono. Son también denominados carbohidratos, hidratos de carbono, glúcido o azúcares. Los componentes químicos estructurales de los glúcidos son los azúcares simples o monosacáridos.
Glúcidos o hidratos de carbono. Son también denominados carbohidratos, hidratos de carbono, glúcido o azúcares. Los componentes químicos estructurales de los glúcidos son los azúcares simples o monosacáridos.
UNIDAD 1: LA MATERIA CRISTALINA
 UNIDAD 1: LA MATERIA CRISTALINA CONCEPTOS MATERIA CRISTALINA: Aquella cuyas partículas están perfectamente ordenadas en el espacio, ocupando posiciones fijas y a distancias regulares unas de otras, formando
UNIDAD 1: LA MATERIA CRISTALINA CONCEPTOS MATERIA CRISTALINA: Aquella cuyas partículas están perfectamente ordenadas en el espacio, ocupando posiciones fijas y a distancias regulares unas de otras, formando
Temario FÍSICA Y QUÍMICA 59
 Temario FÍSICA Y QUÍMICA 59 Química del carbono. Estructura y enlaces del carbono. Nomenclatura. Isomería. Comprobación experimental de la actividad óptica. 25-15223-13 FÍSICA Y QUÍMICA 59 3 1. ENLACES
Temario FÍSICA Y QUÍMICA 59 Química del carbono. Estructura y enlaces del carbono. Nomenclatura. Isomería. Comprobación experimental de la actividad óptica. 25-15223-13 FÍSICA Y QUÍMICA 59 3 1. ENLACES
Tema 12. PREPARACIÓN DE ALQUENOS
 Tema 12. PREPARACIÓN DE ALQUENOS 2.- Principales familias de compuestos orgánicos: Tema 11. Alcanos Tema 12. Alquenos (I) Tema 13. Alquenos (II) Tema 14. Alquinos. Tema 15. Hidrocarburos aromáticos (I).
Tema 12. PREPARACIÓN DE ALQUENOS 2.- Principales familias de compuestos orgánicos: Tema 11. Alcanos Tema 12. Alquenos (I) Tema 13. Alquenos (II) Tema 14. Alquinos. Tema 15. Hidrocarburos aromáticos (I).
La Química Orgánica es el estudio de los compuestos de carbono. El carbono puede formar más compuestos
 QUÍMICA ORGÁNICA La Química Orgánica es el estudio de los compuestos de carbono. El carbono puede formar más compuestos que ningún otro elemento, por tener la capacidad de unirse entre sí formando cadenas
QUÍMICA ORGÁNICA La Química Orgánica es el estudio de los compuestos de carbono. El carbono puede formar más compuestos que ningún otro elemento, por tener la capacidad de unirse entre sí formando cadenas
DIENOS. Los dienos conjugados son aquellos donde los enlaces dobles se alternan con enlaces simples. Ej: 1,3-pentadieno CH 2 =CH-CH=CH-CH 3
 Teoría de Química Orgánica I DIENOS Un hidrocarburo que contiene dos dobles enlaces se denomina dieno y la relación entre los dobles enlaces puede clasificarse como aislados, conjugados o acumulados. Los
Teoría de Química Orgánica I DIENOS Un hidrocarburo que contiene dos dobles enlaces se denomina dieno y la relación entre los dobles enlaces puede clasificarse como aislados, conjugados o acumulados. Los
Figura 1: Esquema de polímero
 Eje temático: Química: Fenómenos nucleares Polímeros Procesos químicos industriales Contenido: Tipos de polímeros y polimerización Nivel: Cuarto medio Polímeros. Polímeros sintéticos y naturales Polímeros
Eje temático: Química: Fenómenos nucleares Polímeros Procesos químicos industriales Contenido: Tipos de polímeros y polimerización Nivel: Cuarto medio Polímeros. Polímeros sintéticos y naturales Polímeros
Temas 4 y 5. Estereoisomería. Estereoisomería de configuración. Isomería geométrica
 Temas 4 y 5. Estereoisomería Estereoisomería de conformación Estereoisomería de configuración Isomería geométrica Isomería óptica Introducción ISÓMEROS Isómeros de constitución Estereoisómeros Isómeros
Temas 4 y 5. Estereoisomería Estereoisomería de conformación Estereoisomería de configuración Isomería geométrica Isomería óptica Introducción ISÓMEROS Isómeros de constitución Estereoisómeros Isómeros
Química Orgánica Grupos funcionales con oxígeno o nitrógeno
 Química rgánica Grupos funcionales con oxígeno o nitrógeno IES La Magdalena. Avilés. Asturias La parte carbonada constituye el esqueleto fundamental de las moléculas orgánicas. En esta estructura básica
Química rgánica Grupos funcionales con oxígeno o nitrógeno IES La Magdalena. Avilés. Asturias La parte carbonada constituye el esqueleto fundamental de las moléculas orgánicas. En esta estructura básica
PROPIEDADES FÍSICAS Y QUÍMICAS DE LOS ALCANOS (II)
 PROPIEDADES FÍSICAS Y QUÍMICAS DE LOS ALCANOS (II) Propiedades Físicas y Químicas de los Cicloalcanos Los Calores de Combustión de los cicloalcanos revelan la existencia de Tensión de Anillo 1. Anillos
PROPIEDADES FÍSICAS Y QUÍMICAS DE LOS ALCANOS (II) Propiedades Físicas y Químicas de los Cicloalcanos Los Calores de Combustión de los cicloalcanos revelan la existencia de Tensión de Anillo 1. Anillos
CONJUGACIÓN, RESONANCIA Y ESTABILIDAD DE ALQUENOS
 CONJUGACIÓN, RESONANCIA Y ESTABILIDAD DE ALQUENOS Universidad de San Carlos de Guatemala Facultad de Ciencias Químicas y Farmacia Departamento de Química Orgánica Sistemas Conjugados Los sistemas insaturados
CONJUGACIÓN, RESONANCIA Y ESTABILIDAD DE ALQUENOS Universidad de San Carlos de Guatemala Facultad de Ciencias Químicas y Farmacia Departamento de Química Orgánica Sistemas Conjugados Los sistemas insaturados
Composición química de los seres vivos
 Composición química de los seres vivos Elementos químicos de la materia viva BIOELEMENTOS Se clasifican por su abundancia En proporcion superior al 96% PRIMARIOS En una proporción aprox. 3,9% SECUNDARIOS
Composición química de los seres vivos Elementos químicos de la materia viva BIOELEMENTOS Se clasifican por su abundancia En proporcion superior al 96% PRIMARIOS En una proporción aprox. 3,9% SECUNDARIOS
ESTRUCTURA DE LA MATERIA QCA 01 ANDALUCÍA. 1.- Defina: a) Energía de ionización. b) Afinidad electrónica. c) Electronegatividad.
 1.- Defina: a) Energía de ionización. b) Afinidad electrónica. c) Electronegatividad. 2.- Razone si son verdaderas o falsas las siguientes afirmaciones: a) El punto de ebullición del butano es menor que
1.- Defina: a) Energía de ionización. b) Afinidad electrónica. c) Electronegatividad. 2.- Razone si son verdaderas o falsas las siguientes afirmaciones: a) El punto de ebullición del butano es menor que
ÓPTICA GEOMÉTRICA 1. Conceptos básicos. 2. Espejos planos. 3. Espejos esféricos. 4. Dioptrios. 5. Lentes delgadas. 6. La visión.
 ÓPTICA GEOMÉTRICA 1. Conceptos básicos. 2. Espejos planos. 3. Espejos esféricos. 4. Dioptrios. 5. Lentes delgadas. 6. La visión. Física 2º bachillerato Óptica geométrica 1 ÓPTICA GEOMÉTRICA La óptica geométrica
ÓPTICA GEOMÉTRICA 1. Conceptos básicos. 2. Espejos planos. 3. Espejos esféricos. 4. Dioptrios. 5. Lentes delgadas. 6. La visión. Física 2º bachillerato Óptica geométrica 1 ÓPTICA GEOMÉTRICA La óptica geométrica
Química Agrícola Profesora: Ing. Cecilia Moldes Primer año-tecnicatura en Producción Agrícola Ganadera UNIDAD Nº3
 UNIDAD Nº3 Química orgánica: átomo de carbono. Hidrocarburos, aromáticos, cíclicos. Funciones oxigenadas simples y mixtas Cuestionario Nº 3: ejercicios y preguntas teóricas Trabajo práctico Nº 2: Análisis
UNIDAD Nº3 Química orgánica: átomo de carbono. Hidrocarburos, aromáticos, cíclicos. Funciones oxigenadas simples y mixtas Cuestionario Nº 3: ejercicios y preguntas teóricas Trabajo práctico Nº 2: Análisis
QUÍMICA ORGÁNICA GENERAL
 UNIVERSIDAD DEL VALLE VICERRECTORIA ACADÉMICA DIRECCIÓN DE EDUCACIÓN DESESCOLARIZADA CURSO DE QUÍMICA ORGÁNICA GENERAL AUTORA: LUZ MARINA JARAMILLO PhD Profesora Titular Facultad de Ciencias - Departamento
UNIVERSIDAD DEL VALLE VICERRECTORIA ACADÉMICA DIRECCIÓN DE EDUCACIÓN DESESCOLARIZADA CURSO DE QUÍMICA ORGÁNICA GENERAL AUTORA: LUZ MARINA JARAMILLO PhD Profesora Titular Facultad de Ciencias - Departamento
5ª UNIDAD ELEMENTOS Y COMPUESTOS
 5ª UNIDAD ELEMENTOS Y COMPUESTOS 3º E.S.O. Grupo Apellidos: Nombre: INTRODUCCIÓN Comenzamos recordando los conceptos más importantes del tema anterior: Cómo son los átomos? Cómo están distribuidos los
5ª UNIDAD ELEMENTOS Y COMPUESTOS 3º E.S.O. Grupo Apellidos: Nombre: INTRODUCCIÓN Comenzamos recordando los conceptos más importantes del tema anterior: Cómo son los átomos? Cómo están distribuidos los
Algunos conceptos básicos de Trigonometría DEFINICIÓN FIGURA OBSERVACIONES. Nombre y definición Figura Característica
 Ángulos. DEFINICIÓN FIGURA OBSERVACIONES Ángulo. Es la abertura formada por dos semirrectas unidas en un solo punto llamado vértice. Donde: α = Ángulo O = Vértice OA = Lado inicial OB = Lado terminal Un
Ángulos. DEFINICIÓN FIGURA OBSERVACIONES Ángulo. Es la abertura formada por dos semirrectas unidas en un solo punto llamado vértice. Donde: α = Ángulo O = Vértice OA = Lado inicial OB = Lado terminal Un
SESIÓN 10 DERIVACIÓN DE FUNCIONES TRIGONOMÉTRICAS DIRECTAS
 SESIÓN 0 DERIVACIÓN DE FUNCIONES TRIGONOMÉTRICAS DIRECTAS I. CONTENIDOS:. Derivadas de funciones trigonométricas directas. Ejercicios resueltos. Estrategias Centradas en el Aprendizaje: Ejercicios propuestos
SESIÓN 0 DERIVACIÓN DE FUNCIONES TRIGONOMÉTRICAS DIRECTAS I. CONTENIDOS:. Derivadas de funciones trigonométricas directas. Ejercicios resueltos. Estrategias Centradas en el Aprendizaje: Ejercicios propuestos
SOLUCIONARIO Guía Estándar Anual
 SOLUCIONARIO Guía Estándar Anual Polaridad de las moléculas y fuerzas intermoleculares. SGUICES034CB33-A16V1 Ítem Alternativa Habilidad 1 A ASE 2 E Reconocimiento 3 D ASE 4 B ASE 5 C ASE 6 D Reconocimiento
SOLUCIONARIO Guía Estándar Anual Polaridad de las moléculas y fuerzas intermoleculares. SGUICES034CB33-A16V1 Ítem Alternativa Habilidad 1 A ASE 2 E Reconocimiento 3 D ASE 4 B ASE 5 C ASE 6 D Reconocimiento
Mosaicos y frisos. Adela Salvador
 Mosaicos y frisos Adela Salvador Isometrías en el plano Traslación Giro Simetría Simetría con deslizamiento Traslaciones La traslación queda definida al conocer el vector de traslación Busca dos vectores
Mosaicos y frisos Adela Salvador Isometrías en el plano Traslación Giro Simetría Simetría con deslizamiento Traslaciones La traslación queda definida al conocer el vector de traslación Busca dos vectores
PORTAFOLIO DE EVIDENCIAS QUÍMICA I DE SEGUNDA OPORTUNIDAD I LEE DETENIDAMENTE CADA ENUNCIADO Y CONTESTA SEGÚN SE TE PIDA.
 PORTAFOLIO DE EVIDENCIAS QUÍMICA I DE SEGUNDA OPORTUNIDAD I LEE DETENIDAMENTE CADA ENUNCIADO Y CONTESTA SEGÚN SE TE PIDA. 1.- Ciencia que estudia las características y la composición de los materiales,
PORTAFOLIO DE EVIDENCIAS QUÍMICA I DE SEGUNDA OPORTUNIDAD I LEE DETENIDAMENTE CADA ENUNCIADO Y CONTESTA SEGÚN SE TE PIDA. 1.- Ciencia que estudia las características y la composición de los materiales,
QUÍMICA ORGÁNICA BÁSICA
 QUÍMICA ORGÁNICA BÁSICA 1. INTRODUCCIÓN: NATURALEZA DE LA QUÍMICA ORGÁNICA Panorama histórico y situación actual El carácter químico especial del carbono Fuentes y transformaciones de los compuestos orgánicos.
QUÍMICA ORGÁNICA BÁSICA 1. INTRODUCCIÓN: NATURALEZA DE LA QUÍMICA ORGÁNICA Panorama histórico y situación actual El carácter químico especial del carbono Fuentes y transformaciones de los compuestos orgánicos.
Hibridación de orbitales.
 Hibridación de orbitales. REACCIONES ORGANICAS Las formas características de enlace del átomo de carbono en los compuestos orgánicos se describe frecuentemente de acuerdo con el modelo de hibridación de
Hibridación de orbitales. REACCIONES ORGANICAS Las formas características de enlace del átomo de carbono en los compuestos orgánicos se describe frecuentemente de acuerdo con el modelo de hibridación de
FORMULACIÓN ORGÁNICA E ISOMERÍA
 FORMULACIÓN ORGÁNICA E ISOMERÍA Actualmente se conocen varios millones de compuestos orgánicos y cada día se sintetizan otros nuevos. Este elevado número de compuestos tiene como elemento básico de su
FORMULACIÓN ORGÁNICA E ISOMERÍA Actualmente se conocen varios millones de compuestos orgánicos y cada día se sintetizan otros nuevos. Este elevado número de compuestos tiene como elemento básico de su
Tabla Periódica y Propiedades Periódicas
 Tabla Periódica y Propiedades Periódicas Primeras clasificaciones periódicas. Fines S. XVIII Metales y no metales. 1829, Döbereiner Tríadas de comportamiento químico similar. A principios del siglo XIX
Tabla Periódica y Propiedades Periódicas Primeras clasificaciones periódicas. Fines S. XVIII Metales y no metales. 1829, Döbereiner Tríadas de comportamiento químico similar. A principios del siglo XIX
QUÍMICA ORGANICA. Ejemplos de compuestos orgánicos que a menudo usamos en nuestro diario vivir son: el gas natural, la parafina
 QUÍMICA ORGANICA La química orgánica es una especialidad de la química que estudia las estructuras, propiedades y reacciones de compuestos que contienen al elemento Carbono como átomo central. Ejemplos
QUÍMICA ORGANICA La química orgánica es una especialidad de la química que estudia las estructuras, propiedades y reacciones de compuestos que contienen al elemento Carbono como átomo central. Ejemplos
Según Lewis el enlace covalente consiste en la unión de dos átomos que comparten uno o más pares de electrones.
 En 1916, Lewis resaltó que los gases nobles eran muy poco reactivos debido a que su configuración electrónica era muy estable, y sugirió que los átomos pueden adquirir estabilidad compartiendo electrones
En 1916, Lewis resaltó que los gases nobles eran muy poco reactivos debido a que su configuración electrónica era muy estable, y sugirió que los átomos pueden adquirir estabilidad compartiendo electrones
Material elaborado por F. Agius, O. Borsani, P.Díaz, S. Gonnet, P. Irisarri, F. Milnitsky y J. Monza. Bioquímica. Facultad de Agronomía.
 AMINOACIDOS Las proteínas de bacterias, hongos, plantas y animales están constituidas a partir de las mismas 20 unidades o monómeros: los á-aminoácidos. Los aminoácidos tienen un grupo amino y un grupo
AMINOACIDOS Las proteínas de bacterias, hongos, plantas y animales están constituidas a partir de las mismas 20 unidades o monómeros: los á-aminoácidos. Los aminoácidos tienen un grupo amino y un grupo
TEMA 9 CUERPOS GEOMÉTRICOS
 Tel: 98 9 6 91 Fax: 98 1 89 96 TEMA 9 CUERPOS GEOMÉTRICOS Objetivos / Criterios de evaluación O.1.1 Conocer las fórmulas de áreas y volúmenes de figuras geométricas sencillas de D. O.1. Resolver problemas
Tel: 98 9 6 91 Fax: 98 1 89 96 TEMA 9 CUERPOS GEOMÉTRICOS Objetivos / Criterios de evaluación O.1.1 Conocer las fórmulas de áreas y volúmenes de figuras geométricas sencillas de D. O.1. Resolver problemas
ACADEMIA DE QUÍMICA TURNO VESPERTINO
 INSTITUTO POLITÉCNICO NACIONAL CENTRO DE ESTUDIOS CIENTÍFICOS Y TECNOLÓGICOS No. 3 ESTANISLAO RAMÍREZ RUIZ ACADEMIA DE QUÍMICA TURNO VESPERTINO GUIA PARA EL SEGUNDO EXAMEN DEPARTAMENTALDE QUÍMICA I UNIDAD
INSTITUTO POLITÉCNICO NACIONAL CENTRO DE ESTUDIOS CIENTÍFICOS Y TECNOLÓGICOS No. 3 ESTANISLAO RAMÍREZ RUIZ ACADEMIA DE QUÍMICA TURNO VESPERTINO GUIA PARA EL SEGUNDO EXAMEN DEPARTAMENTALDE QUÍMICA I UNIDAD
CONFORMACIONES DE CICLOALCANOS
 ONFORMAIONES DE ILOALANOS Estabilidad de los cicloalcanos: tensión en el anillo A finales del 800, aunque se conocían varios compuestos que contenían anillos con cinco y seis miembros, no se habían podido
ONFORMAIONES DE ILOALANOS Estabilidad de los cicloalcanos: tensión en el anillo A finales del 800, aunque se conocían varios compuestos que contenían anillos con cinco y seis miembros, no se habían podido
17 Principios generales de química orgánica
 174 Química General. Grupo B. urso 1993/94 17 Principios generales de química orgánica 17.1 Los compuestos orgánicos 17.2 Isomería 17.3 aracterísticas químicas generales de los compuestos orgánicos 17.4
174 Química General. Grupo B. urso 1993/94 17 Principios generales de química orgánica 17.1 Los compuestos orgánicos 17.2 Isomería 17.3 aracterísticas químicas generales de los compuestos orgánicos 17.4
QUIMICA ORGANICA 1 ALCANOS Y CICLOALCANOS 20/08/2010 ALCANOS
 0/0/00 QUIMICA ORGANICA Y CICLO Son la primera clase de hidrocarburos simples y contienen sólo enlaces sencillos de carbono carbono, solo poseen carbono e hidrogeno y no tienen grupos funcionales. El enlace
0/0/00 QUIMICA ORGANICA Y CICLO Son la primera clase de hidrocarburos simples y contienen sólo enlaces sencillos de carbono carbono, solo poseen carbono e hidrogeno y no tienen grupos funcionales. El enlace
Temas 4 y 5. Estereoisomería. Estereoisomería de configuración. Isomería geométrica
 Temas 4 y 5. Estereoisomería Estereoisomería de conformación Estereoisomería de configuración Isomería geométrica Isomería óptica Tema 4. Estereoisomería Estereoisomería de conformación Estereoisomería
Temas 4 y 5. Estereoisomería Estereoisomería de conformación Estereoisomería de configuración Isomería geométrica Isomería óptica Tema 4. Estereoisomería Estereoisomería de conformación Estereoisomería
2. Métodos de separación de los componentes de una mezcla.
 TEMA 3: Mezclas, disoluciones y sustancias puras. 1. Clasificación de la materia. 2. Métodos de separación de los componentes de una mezcla. 3. Disoluciones. a) Definición. b) Cómo se preparan. c) Concentración.
TEMA 3: Mezclas, disoluciones y sustancias puras. 1. Clasificación de la materia. 2. Métodos de separación de los componentes de una mezcla. 3. Disoluciones. a) Definición. b) Cómo se preparan. c) Concentración.
UNIDAD IV ALCOHOLES. Alcoholes: Introducción y Nomenclatura. Pte. M. en C.Q. Macaria Hernández Chávez
 UNIDAD IV ALCOHOLES Alcoholes: Introducción y Nomenclatura Pte. M. en C.Q. Macaria Hernández Chávez ALCOHOLES Introducción. Los alcoholes son compuestos orgánicos que contienen grupos hidroxilo (-OH).
UNIDAD IV ALCOHOLES Alcoholes: Introducción y Nomenclatura Pte. M. en C.Q. Macaria Hernández Chávez ALCOHOLES Introducción. Los alcoholes son compuestos orgánicos que contienen grupos hidroxilo (-OH).
1. Clasificación. 2. Monosacáridos. 2.1 Nomenclatura y propiedades. Nomenclatura
 TEMA 2: LOS GLÚCIDOS 1. Clasificación Los glúcidos también se conocen como carbohidratos, glícidos, azúcares y sacáridos. Son biomoléculas orgánicas formadas por C, H y O y su fórmula empírica es Cn(H
TEMA 2: LOS GLÚCIDOS 1. Clasificación Los glúcidos también se conocen como carbohidratos, glícidos, azúcares y sacáridos. Son biomoléculas orgánicas formadas por C, H y O y su fórmula empírica es Cn(H
- Leyes ponderales: Las leyes ponderales relacionan las masas de las sustancias que intervienen en una reacción química.
 FÍSICA Y QUÍMICA 4ºESO COLEGIO GIBRALJAIRE CÁLCULOS QUÍMICOS 1.- LA REACCIÓN QUÍMICA. LEYES PONDERALES Una reacción química es el proceso en el que, mediante una reorganización de enlaces y átomos, una
FÍSICA Y QUÍMICA 4ºESO COLEGIO GIBRALJAIRE CÁLCULOS QUÍMICOS 1.- LA REACCIÓN QUÍMICA. LEYES PONDERALES Una reacción química es el proceso en el que, mediante una reorganización de enlaces y átomos, una
GUIA DE ESTUDIO Nº 1 TABLA PERIÓDICA ENLACE QUÍMICO NÚMERO DE OXIDACIÓN - COMPUESTOS DE COORDINACIÓN
 GUIA DE ESTUDIO Nº 1 TABLA PERIÓDICA ENLACE QUÍMICO NÚMERO DE OXIDACIÓN - COMPUESTOS DE COORDINACIÓN 1. REVISIÓN DE TABLA PERIÓDICA 1.1 Completa el siguiente cuadro. Configuración electrónica externa Bloque
GUIA DE ESTUDIO Nº 1 TABLA PERIÓDICA ENLACE QUÍMICO NÚMERO DE OXIDACIÓN - COMPUESTOS DE COORDINACIÓN 1. REVISIÓN DE TABLA PERIÓDICA 1.1 Completa el siguiente cuadro. Configuración electrónica externa Bloque
CONCEPTOS BÁSICOS TRIGONOMETRÍA DEFINICIÓN FIGURA OBSERVACIONES
 Ángulos. DEFINICIÓN FIGURA OBSERVACIONES Ángulo. Es la abertura formada por dos semirrectas unidas en un solo punto llamado vértice. Donde: α = Ángulo O = Vértice OA = Lado inicial OB = Lado terminal Un
Ángulos. DEFINICIÓN FIGURA OBSERVACIONES Ángulo. Es la abertura formada por dos semirrectas unidas en un solo punto llamado vértice. Donde: α = Ángulo O = Vértice OA = Lado inicial OB = Lado terminal Un
TEMA 5: INTRODUCCIÓN A LA SIMETRÍA MOLECULAR
 Tema 5 Simetría Molecular 1 TEMA 5: INTRODUCCIÓN A LA SIMETRÍA MOLECULAR La simetría de una molécula determina muchas de sus propiedades e incluso determina cómo se producen algunas reacciones. El estudio
Tema 5 Simetría Molecular 1 TEMA 5: INTRODUCCIÓN A LA SIMETRÍA MOLECULAR La simetría de una molécula determina muchas de sus propiedades e incluso determina cómo se producen algunas reacciones. El estudio
Conceptos geométricos II
 Conceptos geométricos II Ángulo Ángulos Consecutivos Ángulos Alternos y Ángulos Correspondientes Polígono Polígono Regular Polígono Irregular Triángulo Cuadrilátero Superficie Círculo Superficie reglada
Conceptos geométricos II Ángulo Ángulos Consecutivos Ángulos Alternos y Ángulos Correspondientes Polígono Polígono Regular Polígono Irregular Triángulo Cuadrilátero Superficie Círculo Superficie reglada
ESTUDIO DE LA ESTRUCTURA TRIMENSIONAL DE LAS MOLÉCULAS. ES IMPOSIBLE ESTUDIAR QUÍMICA ORGÁNICA SIN EMPLEAR LA ESTEREOQUÍMICA.
 1 ESTEREOQUÍMICA ESTUDIO DE LA ESTRUCTURA TRIMENSIONAL DE LAS MOLÉCULAS. ES IMPOSIBLE ESTUDIAR QUÍMICA ORGÁNICA SIN EMPLEAR LA ESTEREOQUÍMICA. EL DESCUBRIMIENTO DE LA ESTEREOISOMERÍA FUE UNO DE LOS EVENTOS
1 ESTEREOQUÍMICA ESTUDIO DE LA ESTRUCTURA TRIMENSIONAL DE LAS MOLÉCULAS. ES IMPOSIBLE ESTUDIAR QUÍMICA ORGÁNICA SIN EMPLEAR LA ESTEREOQUÍMICA. EL DESCUBRIMIENTO DE LA ESTEREOISOMERÍA FUE UNO DE LOS EVENTOS
La tabla periódica es la estrella orientadora para la exploración en el capo de la química, la física, la mineralogía y la técnica.
 SISTEMA PERIÓDICO DE LOS ELEMENTOS La tabla periódica es la estrella orientadora para la exploración en el capo de la química, la física, la mineralogía y la técnica. Niels Bohr Principio de exclusión
SISTEMA PERIÓDICO DE LOS ELEMENTOS La tabla periódica es la estrella orientadora para la exploración en el capo de la química, la física, la mineralogía y la técnica. Niels Bohr Principio de exclusión
UNIDAD 8 QUIMICA ORGANICA
 UNIDAD 8 ONTENIDOS NOIONES QUIMIA ORGANIA. arbono. Enlaces del carbono. ompuestos orgánicos. Alifáticos. íclicos. Nomenclatura. idrocarburos aromáticos. Grupos funcionales. Alcohol. Aldehído. etona. Acido.
UNIDAD 8 ONTENIDOS NOIONES QUIMIA ORGANIA. arbono. Enlaces del carbono. ompuestos orgánicos. Alifáticos. íclicos. Nomenclatura. idrocarburos aromáticos. Grupos funcionales. Alcohol. Aldehído. etona. Acido.
EJERCICIOS DE ENLACE. a) Amoniaco. b) Tricloruro de boro. c) Metano.
 EJERCICIOS DE ENLACE 1. Deduzca, según la teoría de Repulsión de Pares de Electrones de la Capa de Valencia, la geometría de las siguientes moléculas e indique la polaridad de las mismas: a) Amoniaco.
EJERCICIOS DE ENLACE 1. Deduzca, según la teoría de Repulsión de Pares de Electrones de la Capa de Valencia, la geometría de las siguientes moléculas e indique la polaridad de las mismas: a) Amoniaco.
Punto. Recta. Semirrecta. Segmento. Rectas Secantes. Rectas Paralelas. Rectas Perpendiculares
 Punto El punto es un objeto geométrico que no tiene dimensión y que sirve para indicar una posición. A Recta Es una sucesión continua e indefinida de puntos en una sola dimensión. Semirrecta Es una línea
Punto El punto es un objeto geométrico que no tiene dimensión y que sirve para indicar una posición. A Recta Es una sucesión continua e indefinida de puntos en una sola dimensión. Semirrecta Es una línea
La solubilidad es la medida de la capacidad de disolverse una cierta sustancia en un determinado medio, a una temperatura y presión determinadas.
 La solubilidad es la medida de la capacidad de disolverse una cierta sustancia en un determinado medio, a una temperatura y presión determinadas. Las proteínas en disolución muestran grandes cambios en
La solubilidad es la medida de la capacidad de disolverse una cierta sustancia en un determinado medio, a una temperatura y presión determinadas. Las proteínas en disolución muestran grandes cambios en
Resonancia Magnética Nuclear
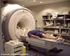 Resonancia Magnética Nuclear Por qué algunas señales aparecen como señales múltiples (multipletes)? Dos átomos que se encuentren contiguos interaccionan modificándose mutuamente. La forma de la señal depende
Resonancia Magnética Nuclear Por qué algunas señales aparecen como señales múltiples (multipletes)? Dos átomos que se encuentren contiguos interaccionan modificándose mutuamente. La forma de la señal depende
La Química y los sentidos
 La Química de lo cotidiano. La Química y los sentidos. Bernardo Herradón 15 de abril de 2009 La Química y los sentidos Mecanismo de la visión La RETINA recibe las impresiones luminosas y las transmite
La Química de lo cotidiano. La Química y los sentidos. Bernardo Herradón 15 de abril de 2009 La Química y los sentidos Mecanismo de la visión La RETINA recibe las impresiones luminosas y las transmite
LA FORMA DE LAS MOLÉCULAS
 LA FORMA DE LAS MOLÉCULAS Dr. Hugo Cerecetto Prof. Titular de Química Temario 7. Las formas de las moléculas: Estructura de Lewis Distancias de enlace Ángulos de enlace Geometría molecular Bibliografía
LA FORMA DE LAS MOLÉCULAS Dr. Hugo Cerecetto Prof. Titular de Química Temario 7. Las formas de las moléculas: Estructura de Lewis Distancias de enlace Ángulos de enlace Geometría molecular Bibliografía
BIOQUÍMICA Y BIOLOGÍA MOLECULAR I CURSO 2003/04 ENLACE QUÍMICO
 BIQUÍMIA Y BILGÍA MLEULAR I URS 2003/04 Problemas 1º de Medicina UIVERSIDAD DE AVARRA DEPARTAMET DE BIQUÍMIA ELAE QUÍMI 1. rdenar por su estabilidad relativa (menor energía de ionización) los siguientes
BIQUÍMIA Y BILGÍA MLEULAR I URS 2003/04 Problemas 1º de Medicina UIVERSIDAD DE AVARRA DEPARTAMET DE BIQUÍMIA ELAE QUÍMI 1. rdenar por su estabilidad relativa (menor energía de ionización) los siguientes
Carbohidratos. Adrianís Canales Hiram Delgado Mearly Bracero Maeliz Cruz. Profr Balaguera Quimica Organica II 29 de noviembre de 2012
 Universidad Interamericana de Puerto Rico Recinto de Bayamón Departamento de Ciencias Naturales y Matemáticas Carbohidratos Adrianís Canales Hiram Delgado Mearly Bracero Maeliz Cruz Profr Balaguera Quimica
Universidad Interamericana de Puerto Rico Recinto de Bayamón Departamento de Ciencias Naturales y Matemáticas Carbohidratos Adrianís Canales Hiram Delgado Mearly Bracero Maeliz Cruz Profr Balaguera Quimica
Conocer las formas de clasificación de los elementos según grupo y periodo. Identificar los criterios de clasificación de los elementos químicos.
 Conocer las formas de clasificación de los elementos según grupo y periodo. Identificar los criterios de clasificación de los elementos químicos. Relacionar características de los átomos y su orden en
Conocer las formas de clasificación de los elementos según grupo y periodo. Identificar los criterios de clasificación de los elementos químicos. Relacionar características de los átomos y su orden en
SIMETRÍA. http://www.chem.ox.ac.uk/courses/molecular_symmetry/part2.html http://www.chem.ox.ac.uk/vrchemistry/sym/splash.html
 SIMETRÍA Elementos y operaciones de simetría Grupos puntuales de simetría Modelo de repulsión de pares de electrones de la capa de valencia (VSEPR) Simetría de las moléculas Tablas de caracteres http://www.chem.ox.ac.uk/courses/molecular_symmetry/part2.html
SIMETRÍA Elementos y operaciones de simetría Grupos puntuales de simetría Modelo de repulsión de pares de electrones de la capa de valencia (VSEPR) Simetría de las moléculas Tablas de caracteres http://www.chem.ox.ac.uk/courses/molecular_symmetry/part2.html
CÁLCULO VECTORIAL I. B, es un nuevo vector que se define del siguiente modo: Si A ybson (LI), entonces el vector A. B se caracteriza por:
 PRODUCTO VECTORIAL DE DOS VECTORES El producto vectorial de dos vectores A y, y escribimos A, es un nuevo vector que se define del siguiente modo: Si A yson (LI), entonces el vector A se caracteriza por:
PRODUCTO VECTORIAL DE DOS VECTORES El producto vectorial de dos vectores A y, y escribimos A, es un nuevo vector que se define del siguiente modo: Si A yson (LI), entonces el vector A se caracteriza por:
ALCANOS. Antología de química. Definición de Hidrocarburos. Clasificación de Hidrocarburos. Clasificación de los Hidrocarburos.
 Definición de idrocarburos Los hidrocarburos son compuestos orgánicos formados únicamente por átomos de carbono e hidrógeno, enlazados entre sí por uniones covalentes. Su estructura molecular comprende
Definición de idrocarburos Los hidrocarburos son compuestos orgánicos formados únicamente por átomos de carbono e hidrógeno, enlazados entre sí por uniones covalentes. Su estructura molecular comprende
