FORMULACIÓN Y NOMENCLATURA DE QUÍMICA INORGÁNICA. NORMAS DE LA I.U.P.A.C
|
|
|
- Vicente Guzmán Méndez
- hace 7 años
- Vistas:
Transcripción
1 FORMULACIÓN Y NOMENCLATURA DE QUÍMICA INORGÁNICA. NORMAS DE LA I.U.P.A.C El aprendizaje de la Química necesita como paso previo conocer su lenguaje. La unificación de éste fue llevada a cabo por la IUPAC (Unión Internacional de Química Pura y Aplicada) en las convenciones de París, 1957, y con las modificaciones de En ellas se establecen las normas para designar los compuestos químicos mediante nombres sistemáticos. 1. SÍMBOLOS QUÍMICOS. Sólo 92 de los elementos químicos conocidos son naturales; los demás se han obtenido artificialmente. Para su identificación, a cada elemento se le ha asignado un símbolo, que es la forma abreviada, aceptada internacionalmente, de escribir el nombre del elemento. Para algunos elementos, se emplea como símbolo la letra inicial de su nombre, escrita con mayúscula: C Carbono N Nitrógeno H Hidrógeno O Oxígeno F Flúor U Uranio En otros casos, se escriben las dos primeras letras de su nombre, la primera en mayúscula y la segunda siempre en minúscula: Cl Cloro Ca Calcio Br Bromo Ba Bario latín: Para algunos elementos, el símbolo deriva, de igual manera, de su nombre en S Azufre (Sulphur) Cu Cobre (Cuprum) P Fósforo (Phosphorus) K Potasio (Kalium) Au Oro (Aurum) Ag Plata (Argentum) Respecto a la etimología, la denominación de otros elementos es diversa: - El nombre de unos hace referencia a alguna de sus propiedades: Cr Cromo : indica que forma compuestos coloreados. - El de otros, recuerda el nombre del descubridor o el nombre de científicos: Md Mendelevio, en honor de Dimitri Mendeleiev Es Einstenio, en honor de Albert Einstein. - Otros toman el nombre del país donde se descubrieron:
2 Ge Germanio, de Germania, nombre latino de Alemania. - Algunos nombres hacen referencia al nombre de ciertos astros: He Helio, de griego Helio, el Sol Te Teluro, del latín Tellus, La Tierra. Se Selenio, del griego Selene, La Luna. Es necesario conocer, como mínimo, el nombre y el símbolo de los elementos existentes, siendo éste el paso previo para poder formular correctamente los diversos compuestos. 2. SISTEMA PERÓDICO Los elementos químicos están clasificados en lo que se conoce como el Sistema Periódico. Está formado por filas horizontales llamadas períodos, y por columnas verticales, los grupos. Los elementos de la parte izquierda y del centro son los metales. Los de la derecha, son los no metales. Los elementos de la diagonal de la derecha, formada por boro, silicio, germanio, arsénico, antimonio, teluro y polonio, son considerados semimetales. El grupo situado más a la derecha está formado por los gases nobles. Son elementos monoatómicos y poco reactivos. Los elementos de propiedades químicas parecidas se encuentran en el mismo grupo del S.P. 3. VALENCIA DE LOS ELEMENTOS QUÍMICOS. La valencia de un elemento químico representa la capacidad que posee dicho elemento para combinarse con otros elementos. Viene dada por el número de electrones captados, cedidos o compartidos por un átomo de dicho elemento al formar un compuesto. En general, los metales tienen tendencia a perder electrones y los metales a captarlos. En la tabla siguiente se muestran las valencias de los elementos más frecuentes:
3 METALES ELEMENTOS Litio Sodio Potasio Rubidio Cesio Plata SÍMBOLOS VALENCIAS Li Na K Rb Cs Ag 1 Berilio Magnesio Calcio Estroncio Bario Radio Cinc Cadmio Cobre Mercurio Be Mg Ca Sr Ba Ra Zn Cd Cu Hg 2 1, 2 Aluminio Al 3 Oro Au 1, 3 Hierro Cobalto Níquel Estaño Plomo Platino Fe Co Ni Sn Pb Pt 2, 3 2, 4 Cromo Cr 2, 3, 6 Manganeso Mn 2, 3, 4, 6, 7 NO METALES
4 NO METALES ELEMENTOS SÍMBOLOS VALENCIAS Hidrógeno H -1, 1 Flúor F -1 Cloro Bromo Iodo Cl Br I -1, 1, 3, 5, 7 Oxígeno O -2 Azufre Selenio Nitrógeno Fósforo Arsénico Antimonio S Se N P As Sb -2 2, 4, 6-3 1, 3, 5-3 3, 5 Boro B 3 Carbono C -4 2, 4 Silicio Si -4, 4
5 4. NORMAS PRÁCTICAS ELEMENTALES SOBRE LA FORMULACIÓN. 1. Se escribe siempre en primer lugar el símbolo del elemento o radical menos electronegativo (metal o grupo que actúe como tal), y a continuación el del elemento o radical más electronegativo. Al nombrarlos se hacen en orden inverso. 2. Las valencias de los elementos o grupos de elementos (radicales), se intercambian y se escriben como subíndice en los átomos o radicales. 3. Si se puede, hay que simplificar los subíndices, teniendo en cuenta que deben ser números enteros y que el subíndice 1 no se escribe. 5. ESQUEMA GENERAL. 5.1 COMPUESTOS BINARIOS Combinaciones binarias del oxígeno: ÓXIDOS Combinaciones binarias del hidrógeno: a) Hidrógeno + metales: HIDRUROS b) Hidrógeno + no metal Sales: a) Metal + no metal b) No metal + no metal 5.2 COMPUETOS TERNARIOS Hidróxidos Oxoácidos Sales neutras. 5.3 CATIONES Y ANIONES.
6 5.1 COMPUESTOS BINARIOS Combinaciones binarias del oxígeno: ÓXIDOS. El oxígeno se combina con todos los elementos químicos excepto con los gases nobles. En todos estos compuestos actúa con la valencia -2 (O -2 ) El oxígeno se escribe siempre a la derecha y el otro elemento a la izquierda. Las valencias se intercambian, y se escriben como subíndices. Si se pueden simplificar, hay que hacerlo. A) En la nomenclatura sistemática de la IUPAC, la palabra genérica es óxido, precedida de los prefijos griegos mono-, di- tri- tetra-, penta- hexa- hepta- etc. Según el número de átomos de oxígeno que existan e indicando de la misma forma, a continuación, la cantidad del otro elemento. N 2 O 5 pentaóxido de dinitrógeno MgO monóxido de magnesio B) En la nomenclatura de Stock, la valencia del metal o no metal, se indica con números romanos y entre paréntesis, inmediatamente detrás del nombre. Fe 2 O 3 óxido de hierro (III) N 2 O 5 óxido de nitrógeno (V) Si el elemento que se combina con el oxígeno posee valencia única, no se indica: Li 2 O óxido de litio MgO óxido de magnesio EJERCICIOS: 1) Nombra los compuestos siguientes con las dos nomenclaturas: BeO Au 2 O 3 CaO
7 ZnO CrO Cl 2 O 3 SO 2 SeO P 2 O 5 I 2 O 3 Ag 2 O Hg 2 O Cl 2 O 7 FeO N 2 O 3 SO 3 Cr 2 O 3 Br 2 O 7 P 2 O 3 CO I 2 O 5 2) Formular los siguientes compuestos: Óxido de sodio Óxido de plomo (IV) Monóxido de manganeso Dióxido de carbono Óxido de azufre (IV) Trióxido de dicromo Óxido de hierro (II) Óxido de potasio Óxido de cobre (I) Óxido de bromo (VII) Pentaóxido de dinitrógeno Óxido de nitrógeno (V)
8 Heptaóxido de dicloro Trióxido de dinitrógeno Óxido de hierro (II) Pentáoxido de difósforo Trióxido de teluro Trióxido de azufre Óxido de níquel (III) Dióxido de azufre Pentaóxido de dibromo Óxido de fósforo (III) Pentaóxido de diyodo Óxido de azufre (IV) Óxido de nitrógeno (III) Óxido de hierro (III) Óxido de aluminio Óxido de cobalto (II) Óxido de cobre (I) Trióxido de selenio Óxido de azufre (VI) Óxido de plata Combinaciones binarias del hidrógeno. a) HIDRÓGENO + METAL: HIDRUROS En estos compuestos, el hidrógeno actúa con valencia -1 (H -1 ). El hidrógeno se escribe a la derecha, y el metal a la izquierda. La valencia del metal se escribe como subíndice en el hidrógeno A) En la nomenclatura sistemática, se utilizan los prefijos griegos para indicar el número de átomos de hidrógeno que hay en el compuesto: NaH monohidruro de sodio AlH 3 trihidruro de aluminio CuH monohidruro de cobre SnH 2 dihidruro de estaño B) En la nomenclatura de Stock, la valencia del metal, se indica entre paréntesis y en números romanos. Si tiene una única valencia, no se indica. NaH hidruro de sodio AlH 3 hidruro de aluminio CuH hidruro de cobre (I) SnH 2 hidruro de estaño (II)
9 b) HIDRÓGENO + NO METAL En estos compuestos, la valencia del hidrógeno es +1 (H +1 ), y los no metales, con su valencia negativa. En estos compuestos, el hidrógeno se escribe a la izquierda, y el no metal a la derecha. La valencia de éste se escribe como subíndice en el hidrógeno. Los haluros de hidrógeno, en disolución acuosa dan disoluciones ácidas, y reciben el nombre de ácidos hidrácidos. Se nombran: 1) Añadiendo el sufijo -uro al no metal, y a continuación la palabra hidrógeno. 2) La palabra ácido, seguido el nombre del no metal acabado en hídrico. HCl cloruro de hidrógeno / ácido clorhídrico HBr bromuro de hidrógeno / ácido bromhídrico H 2 S sulfuro de hidrógeno / ácido sulfhídrico c) OTRAS COMBINACIONES DEL HIDRÓGENO Los elementos que forman estos compuestos son: nitrógeno, fósforo, arsénico, antimonio, carbono, silicio y boro. Todos estos compuestos tienen nombres especiales admitidos por la IUPAC, que son los más utilizados por los químicos. En estos compuestos, el hidrógeno se escribe a la derecha. NH 3 amoniaco PH 3 fosfina AsH 3 arsina CH 4 metano SbH 3 estibina
10 EJERCICIOS: 1) Nombra lo siguientes compuestos: LiH HI PH 3 CuH HF NaH CrH 3 CoH 2 CdH 2 NH 3 H 2 Se CH 4 H 2 S HCl BaH 2 KH CaH 2 HBr AsH 3 AlH 3 FeH 2
11 2) Formula los siguientes compuestos: Hidruro de platino (IV) Amoniaco Ácido telurhídrico Hidruro de aluminio Ioduro de hidrógeno Hidruro de litio Dihidruro de mercurio Tetrahidruro de estaño Hidruro de oro (I) Ácido bromhídrico Cloruro de hidrógeno Sulfuro de hidrógeno Metano Ácido clorhídrico Fluoruro de hidrógeno Trihidruro de hierro Seleniuro de hidrógeno Hidruro de plata Arsina Hidruro de manganeso (VI) SALES Son las combinaciones binarias que no son óxidos ni compuestos hidrogenados. a) Metal + no metal El no metal se coloca a la derecha y el metal a la izquierda. Las valencias se intercambian y se escriben como subíndices; si se puede, hay que simplificarlas. Para nombrarlas, utilizaremos dos nomenclaturas: - En la nomenclatura sistemática, utilizaremos los prefijos para indicar la cantidad que hay de los elementos: LiF monofluoruro de litio AlCl 3 tricloruro de aluminio CaF 2 difluroruo de calcio CuBr 2 dibromuro de cobre MnS monosulfuro de manganeso KI monoyoduro de potasio FeCl 3 tricloruro de hierro MgCl 2 dicloruro de magnesio
12 - En la nomenclatura de Stock, se indica la valencia del metal en números romanos y entre paréntesis. Si tiene una única valencia, no se indica. LiF fluoruro de litio AlCl 3 cloruro de aluminio MnS sulfuro de manganeso (II) FeCl 3 cloruro de hierro (III) CaF 2 fluoruro de calcio CuBr 2 bromuro de cobre (II) KI ioduro de potasio MgCl 2 cloruro de magnesio b) No metal + no metal. La IUPAC establece que en las combinaciones binarias entre no metales, se coloque a la izquierda en la fórmula el símbolo del elemento que figura antes en la siguiente relación: B, Si, C, Sb, As, P, N, Te, Se, S, I, Br, Cl, F Estos compuestos se nombran añadiendo la terminación uro al elemento cuyo símbolo está colocado a la derecha de la fórmula. Fórmula Nom.sistemática Nom. de Stock BrF 3 Trifluoruro de bromo Fluoruro de bromo (III) SeI 2 Diyoduro de selenio Ioduro de selenio (II) CS 2 Disulfuro de carbono Sulfuro de carbono (IV) EJERCICIOS: 1) Nombra los siguientes compuestos: FeCl 2 B 2 S 3 MnS AlF 3 CuI Fe 2 S 3 NaBr
13 PbS 2 AuI CuS NH 4 Cl 2) Formula los siguientes compuestos: Fluoruro de cobre (II) Bromuro de iodo (III) Dibromuro de cobre Fluoruro de calcio Cloruro de hierro (II) Hexafluoruro de azufre Bromuro de amonio Sulfuro de plomo (IV) Sulfuro de carbono (II) Cloruro de aluminio Monosulfuro de magnesio Tricloruro de nitrógeno Ioduro de mercurio (I) Fluoruro de magnesio
14 EJERCICIOS DE REPASO. 1) Formula los siguientes compuestos: Sulfuro de hidrógeno Amoniaco Hidruro de cesio Heptaóxido de dicloro Fosfina Cloruro de hidrógeno Hidruro de sodio Hidruro de aluminio Ácido clorhídrico Hidruro de plomo (II) Fluoruro de hidrógeno Dióxido de silicio Ácido fluorhídrico Hidruro de berilio Estibina Sulfuro de aluminio Metano Bromuro de calcio Sulfuro de platino (IV) Óxido de bromo (I) Ácido bromhídrico Trióxido de dihierro Ácido telurhídrico Monóxido de dicobre Hidruro de magnesio Dióxido de azufre Ácido sulfhídrico Dióxido de manganeso Trióxido de dicromo Hidruro de potasio Dióxido de estaño Pentaóxido de difósforo Arsina Óxido de hierro (III) Bromuro de hidrógeno Hidruro de plata Cloruro de mercurio (II) Ioduro de oro (I) Trisulfuro de diníquel Estibina Monóxido de dimercurio Bromuro de hidrógeno
15 2) Nombra los siguientes compuestos: H 2 S Fe 2 O 3 MgH 2 Cu 2 O PH 3 SO 2 HCl Cl 2 O 7 PCl 3 AlH 3 N 2 O 5 CoBr 3 CH 4 Cr 2 O 3 BeH 2 Cr 2 S 3 N 2 O 5 SrH 2 Al 2 O 3 CrS HF Cl 2 O 5 CrH 3 PbI 2 N 2 O 3
16 MgO BaO V 2 O 5 CuBr KH FeO PbH 4 FeCl 3 LiH BaH 2 CaF 2 Cl 2 O CaO FeCl 2 AsH 3 P 2 O 5 MnO CaH 2 NaH SO 3 AuI Cl 2 O 3 SiO 2 PtS 2
17 5.2 COMPUESTOS TERNARIOS HIDRÓXIDOS. metal. Los hidróxidos son los compuestos formados por el grupo (OH) -1, unido a un Según la IUPAC, se escribe el grupo hidróxido a la derecha y el metal a la izquierda, intercambiando las valencias. Se nombran con la palabra genérica hidróxido, seguida del nombre del metal. La valencia del metal, si fuese necesario, se especifica según la notación de Stock, es decir, entre paréntesis y en números romanos. Fe(OH) 2 K(OH) Cr(OH) 3 hidróxido de hierro (II) hidróxido de potasio hidróxido de cromo (III) EJERCICIOS 1) Nombra los siguientes compuestos: NaOH Ca(OH) 2 Al(OH) 3 Mg(OH) 2 Cr(OH) 3 Ni(OH) 2 Sn(OH) 4 Ba(OH) 2 Co(OH) 3 Fe(OH) 2 Pb(OH) 2 Cr(OH) 2 HgOH NH 4 (OH)
18 Sn(OH) 4 AgOH Cd(OH) 2 Au(OH) 3 2) Formula los siguientes compuestos: Hidróxido de plata Hidróxido de cromo (VI) Hidróxido de calcio Hidróxido de platino (II) Hidróxido de cobre (I) Hidróxido de hierro (II) Hidróxido de mercurio (II) Hidróxido de cobalto (II) Hidróxido de bario Hidróxido de amonio Hidróxido de manganeso (II) Hidróxido de cadmio Hidróxido de plomo (IV) Hidróxido de berilio Hidróxido de estaño (IV) Hidróxido de aluminio Hidróxido de níquel (III) Hidróxido de magnesio Hidróxido de potasio Hidróxido de estroncio Hidróxido de cinc Hidróxido de oro (III) Hidróxido de estaño (II) Hidróxido de sodio Hidróxido de litio Hidróxido de hierro (III)
FORMULACIÓN DE QUÍMICA INORGÁNICA.
 FORMULACIÓN DE QUÍMICA INORGÁNICA. 1. VALENCIA. Es la capacidad que tiene un átomo de un elemento para combinarse con los átomos de otros elementos y formar compuestos. La valencia es un número, positivo
FORMULACIÓN DE QUÍMICA INORGÁNICA. 1. VALENCIA. Es la capacidad que tiene un átomo de un elemento para combinarse con los átomos de otros elementos y formar compuestos. La valencia es un número, positivo
Lo primero que hay que conocer para formular y nombrar los compuestos químicos es el número de oxidación de cada elemento.
 Tema 5. NOMENCLATURA Y FORMULACIÓN DE QUÍMICA INORGÁNICA Introducción La IUPAC (Unión Internacional de Química Pura y Aplicada) es el organismo que coordina y actualiza las normas que permiten formular
Tema 5. NOMENCLATURA Y FORMULACIÓN DE QUÍMICA INORGÁNICA Introducción La IUPAC (Unión Internacional de Química Pura y Aplicada) es el organismo que coordina y actualiza las normas que permiten formular
FORMULACIÓN Y NOMENCLATURA
 1. SUSTANCIAS SIMPLES. FORMULACIÓN Y NOMENCLATURA Están constituidas por átomos de un solo elemento. En ellas las moléculas están formadas por átomos idénticos. Su fórmula indica el número de átomos de
1. SUSTANCIAS SIMPLES. FORMULACIÓN Y NOMENCLATURA Están constituidas por átomos de un solo elemento. En ellas las moléculas están formadas por átomos idénticos. Su fórmula indica el número de átomos de
NOMENCLATURA Y FORMULACIÓN DE QUÍMICA INORGÁNICA. Física y Química 3º de E.S.O. IES Isidra de Guzmán
 NOMENCLATURA Y FORMULACIÓN DE QUÍMICA INORGÁNICA Física y Química 3º de E.S.O. IES Isidra de Guzmán INTRODUCCIÓN La IUPAC ( Unión Internacional de Química Pura y Aplicada) es el organismo que coordina
NOMENCLATURA Y FORMULACIÓN DE QUÍMICA INORGÁNICA Física y Química 3º de E.S.O. IES Isidra de Guzmán INTRODUCCIÓN La IUPAC ( Unión Internacional de Química Pura y Aplicada) es el organismo que coordina
Tema 6 : Nomenclatura y formulación Química Inorgánica
 Tema 6 : Nomenclatura y formulación Química Inorgánica Esquema de trabajo: Introducción Compuestos Binarios 1. Combinaciones binarias del oxígeno: A. Oxidos B. Anhídridos 2. Combinaciones binarias del
Tema 6 : Nomenclatura y formulación Química Inorgánica Esquema de trabajo: Introducción Compuestos Binarios 1. Combinaciones binarias del oxígeno: A. Oxidos B. Anhídridos 2. Combinaciones binarias del
FORMULA LOS SIGUIENTES COMPUESTOS. 1) Óxido crómico: CrO 3. 2) Trióxido de difósforo: P 2 O 3. 3) Óxido de cromo (III): Cr 2 O 3
 FORMULA LOS SIGUIENTES COMPUESTOS 1) Óxido crómico: CrO 3 2) Trióxido de difósforo: P 2 O 3 3) Óxido de cromo (III): Cr 2 O 3 4) Óxido de hierro (II): FeO 5) Pentaóxido de dinitrógeno: N 2 O 5 6) Óxido
FORMULA LOS SIGUIENTES COMPUESTOS 1) Óxido crómico: CrO 3 2) Trióxido de difósforo: P 2 O 3 3) Óxido de cromo (III): Cr 2 O 3 4) Óxido de hierro (II): FeO 5) Pentaóxido de dinitrógeno: N 2 O 5 6) Óxido
11 Dióxido de carbono. 12 Trióxido de monoazufre. 13 Pentaóxido de difósforo. 14 Dióxido de monoselenio. 15 Dióxido de selenio. 16 Óxido de dimercurio
 1 FÍSICA Y QUÍMICA 3º ESO QUÍMICA - FORMULACIÓN Y SISTEMÁTICAMENTE LOS SIGUIENTES ÓXIDOS 1 Cu 2 O 2 Be O 3 I 2 O 5 4 CO 2 5 NiO 6 Ag 2 O 7 Li 2 O 8 N 2 O 3 9 CrO 10 Ni 2 O 3 11 Dióxido de carbono 12 Trióxido
1 FÍSICA Y QUÍMICA 3º ESO QUÍMICA - FORMULACIÓN Y SISTEMÁTICAMENTE LOS SIGUIENTES ÓXIDOS 1 Cu 2 O 2 Be O 3 I 2 O 5 4 CO 2 5 NiO 6 Ag 2 O 7 Li 2 O 8 N 2 O 3 9 CrO 10 Ni 2 O 3 11 Dióxido de carbono 12 Trióxido
FORMULACIÓN Y NOMENCLATURA (SISTEMÁTICA)
 FORMULACIÓN Y NOMENCLATURA (SISTEMÁTICA) FORMULACIÓN: el conjunto de reglas que se emplean para la representación simbólica de los compuestos químicos. NOMENCLATURA: la forma de nombrar los compuestos.
FORMULACIÓN Y NOMENCLATURA (SISTEMÁTICA) FORMULACIÓN: el conjunto de reglas que se emplean para la representación simbólica de los compuestos químicos. NOMENCLATURA: la forma de nombrar los compuestos.
FORMULACIÓN Y NOMENCLATURA DE QUÍMICA INORGÁNICA
 FORMULACIÓN Y NOMENCLATURA DE QUÍMICA INORGÁNICA Índice de contenido TABLAS DE NÚMEROS DE OXIDACIÓN MÁS COMUNES...2 MECANISMO DE FORMULACIÓN...2 NOMENCLATURAS EN QUÍMICA INORGÁNICA...2 NOMENCLATURA CON
FORMULACIÓN Y NOMENCLATURA DE QUÍMICA INORGÁNICA Índice de contenido TABLAS DE NÚMEROS DE OXIDACIÓN MÁS COMUNES...2 MECANISMO DE FORMULACIÓN...2 NOMENCLATURAS EN QUÍMICA INORGÁNICA...2 NOMENCLATURA CON
QUÍMICA INORGÁNICA: INTRODUCCIÓN A LA NOMENCLATURA Y FORMULACIÓN DE COMPUESTOS BINARIOS.
 QUÍMICA INORGÁNICA: INTRODUCCIÓN A LA NOMENCLATURA Y FORMULACIÓN DE COMPUESTOS BINARIOS. En el ámbito de la Química a cada sustancia le corresponde un nombre, que nos permite identificarla, y una fórmula,
QUÍMICA INORGÁNICA: INTRODUCCIÓN A LA NOMENCLATURA Y FORMULACIÓN DE COMPUESTOS BINARIOS. En el ámbito de la Química a cada sustancia le corresponde un nombre, que nos permite identificarla, y una fórmula,
Trióxido de dihierro
 ÓXIDOS Los óxidos son combinaciones de los elementos con el oxígeno. El nombre de estos compuestos siempre incluye la palabra óxido que puede estar precedida de prefijos numerales indicadores del número
ÓXIDOS Los óxidos son combinaciones de los elementos con el oxígeno. El nombre de estos compuestos siempre incluye la palabra óxido que puede estar precedida de prefijos numerales indicadores del número
ísica y uímica FORMULACIÓN Y NOMENCLATURA Nombre Óxido de bario Óxido de sodio Óxido de plata Fórmula
 Formula los siguientes compuestos: EJERCICIOS DE RECAPITULACIÓN Óxido de bario Óxido de sodio Óxido de plata BaO Na 2 O Ag 2 O Óxido de aluminio Al 2 O 3 Óxido de níquel (III) Ni 2 O 3 Óxido de cloro (VII)
Formula los siguientes compuestos: EJERCICIOS DE RECAPITULACIÓN Óxido de bario Óxido de sodio Óxido de plata BaO Na 2 O Ag 2 O Óxido de aluminio Al 2 O 3 Óxido de níquel (III) Ni 2 O 3 Óxido de cloro (VII)
La fórmula química expresa la composición de moléculas y compuestos mediante símbolos químicos. 13 millones!!!
 La fórmula química expresa la composición de moléculas y compuestos mediante símbolos químicos El Nº de compuestos químicos conocidos es superior a 13 millones!!! Método sistemático de nombrar los compuestos:
La fórmula química expresa la composición de moléculas y compuestos mediante símbolos químicos El Nº de compuestos químicos conocidos es superior a 13 millones!!! Método sistemático de nombrar los compuestos:
Trióxido de dihierro
 Curso 2012-13 FORMULACIÓN QUÍMICA INORGÁNICA COMBINACIONES BINARIAS CPI Conde de Fenosa Ares Los óxidos son combinaciones de los elementos con el oxígeno. El nombre de estos compuestos siempre incluye
Curso 2012-13 FORMULACIÓN QUÍMICA INORGÁNICA COMBINACIONES BINARIAS CPI Conde de Fenosa Ares Los óxidos son combinaciones de los elementos con el oxígeno. El nombre de estos compuestos siempre incluye
FORMULACIÓN Y NOMENCLATURA
 FORMULACIÓN Y NOMENCLATURA.- Formulación: Es la representación escrita de una molécula que se rige por unas normas universales establecidas por acuerdo de la comunidad científica..- Nomenclatura: Es el
FORMULACIÓN Y NOMENCLATURA.- Formulación: Es la representación escrita de una molécula que se rige por unas normas universales establecidas por acuerdo de la comunidad científica..- Nomenclatura: Es el
NOMENCLATURA DE QUÍMICA INORGÁNICA COMPUESTOS BINARIOS (3.º ESO)
 NOMENCLATURA DE QUÍMICA INORGÁNICA COMPUESTOS BINARIOS Para qué la nomenclatura química? Cuando estudiamos química nos encontramos con multitud de sustancias a las que debemos de asignar un nombre y una
NOMENCLATURA DE QUÍMICA INORGÁNICA COMPUESTOS BINARIOS Para qué la nomenclatura química? Cuando estudiamos química nos encontramos con multitud de sustancias a las que debemos de asignar un nombre y una
Trióxido de dihierro
 COMBINACIONES BINARIAS (4ª ESO) ÓXIDOS Los óxidos son combinaciones de los elementos con el oxígeno. El nombre de estos compuestos siempre incluye la palabra óxido que puede estar precedida de prefijos
COMBINACIONES BINARIAS (4ª ESO) ÓXIDOS Los óxidos son combinaciones de los elementos con el oxígeno. El nombre de estos compuestos siempre incluye la palabra óxido que puede estar precedida de prefijos
Colegio Superior de Señoritas Tema: Formación de Compuestos Químicos Septiembre 2010 Prof.: NVM 8vo Nivel Departamento de Ciencias
 COMPUESTOS QUÍMICOS Y SU CLASIFICACIÓN El número de oxidación: representa la cantidad de electrones que puede ganar o perder un elemento. El hidrógeno tiene número de oxidación +1 y puede perder un electrón;
COMPUESTOS QUÍMICOS Y SU CLASIFICACIÓN El número de oxidación: representa la cantidad de electrones que puede ganar o perder un elemento. El hidrógeno tiene número de oxidación +1 y puede perder un electrón;
TEMA 5.- Formulación y nomenclatura
 Tema 5.- Formulación y nomenclatura de compuestos binarios 0.- Introducción. 1.- Óxidos. 2.- Peróxidos. 3.- Combinaciones binarias del hidrógeno. 3.1.- Hidruros. 3.2.- Haluros. 3.3.- Hidruros volátiles.
Tema 5.- Formulación y nomenclatura de compuestos binarios 0.- Introducción. 1.- Óxidos. 2.- Peróxidos. 3.- Combinaciones binarias del hidrógeno. 3.1.- Hidruros. 3.2.- Haluros. 3.3.- Hidruros volátiles.
FORMULACIÓN INORGÁNICA. Departamento de Física y Química 3º ESO
 FORMULACIÓN INORGÁNICA Departamento de Física y Química 3º ESO 1. Tabla periódica de los elementos -1 Valencia: capacidad que posee un elemento para combinarse con otro Número de oxidación: número de electrones
FORMULACIÓN INORGÁNICA Departamento de Física y Química 3º ESO 1. Tabla periódica de los elementos -1 Valencia: capacidad que posee un elemento para combinarse con otro Número de oxidación: número de electrones
TEMA 5. SISTEMA PERIÓDICO. FORMULACIÓN Y NOMENCLATURA DE COMPUESTOS INORGÁNICOS
 TEMA 5. SISTEMA PERIÓDICO. FORMULACIÓN Y NOMENCLATURA DE COMPUESTOS INORGÁNICOS SISTEMA PERIÓDICO El sistema periódico actual está formado por más de 100 elementos (114 en la actualidad), los cuales están
TEMA 5. SISTEMA PERIÓDICO. FORMULACIÓN Y NOMENCLATURA DE COMPUESTOS INORGÁNICOS SISTEMA PERIÓDICO El sistema periódico actual está formado por más de 100 elementos (114 en la actualidad), los cuales están
TEMA 4: FORMULACIÓN 1.- CONCEPTOS PREVIOS
 TEMA 4: FORMULACIÓN 1.- CONCEPTOS PREVIOS Compuesto químico: es la unión de varios átomos que no pueden separarse por procedimientos físicos pero sí mediante procedimientos químicos. Ejemplo: dos átomos
TEMA 4: FORMULACIÓN 1.- CONCEPTOS PREVIOS Compuesto químico: es la unión de varios átomos que no pueden separarse por procedimientos físicos pero sí mediante procedimientos químicos. Ejemplo: dos átomos
EJRCICIOS de FORMULACIÓN DE FÍSICA Y QUÍMICA 3º ESO
 EJRCICIOS de FORMULACIÓN DE FÍSICA Y QUÍMICA 3º ESO Pablo Martín CURSO 2014-2015 1 EJERCICIOS DE FORMULACIÓN DE INORGÁNICA: Escribe el nombre de los siguientes compuestos 1. Cl 2 O 5 2. PbCl 4 3. HCl 4.
EJRCICIOS de FORMULACIÓN DE FÍSICA Y QUÍMICA 3º ESO Pablo Martín CURSO 2014-2015 1 EJERCICIOS DE FORMULACIÓN DE INORGÁNICA: Escribe el nombre de los siguientes compuestos 1. Cl 2 O 5 2. PbCl 4 3. HCl 4.
Química General Básica. Nomenclatura de Compuestos Inorgánicos
 Química General Básica Nomenclatura de Compuestos Inorgánicos Estelí, 11 de marzo de 2011 Formulación y Nomenclatura en Química Inorgánica La fórmula química expresa la composición de moléculas y compuestos
Química General Básica Nomenclatura de Compuestos Inorgánicos Estelí, 11 de marzo de 2011 Formulación y Nomenclatura en Química Inorgánica La fórmula química expresa la composición de moléculas y compuestos
http://recursos-itaca.blogspot.com.es/ Formulación Inorgánica 1º) Nombra los compuestos siguientes por las tres nomenclaturas:
 1º) Nombra los compuestos siguientes por las tres nomenclaturas: COMPUESTOS BINARIOS CON OXÍGENO OXÍGENO + METAL-- ÓXIDOS BÁSICOS OXÍGENO + NO METAL ÓXIDOS ÁCIDOS El oxígeno se combina con todos los elementos
1º) Nombra los compuestos siguientes por las tres nomenclaturas: COMPUESTOS BINARIOS CON OXÍGENO OXÍGENO + METAL-- ÓXIDOS BÁSICOS OXÍGENO + NO METAL ÓXIDOS ÁCIDOS El oxígeno se combina con todos los elementos
M m+ + X n- M n X m. Qué es formular un compuesto binario?
 Qué es formular un compuesto binario? Cuando tenemos dos elementos, uno menos electronegativo que otro, es decir uno con tendencia a ceder electrones M m+ (m es número de oxidación o valencia) y otro con
Qué es formular un compuesto binario? Cuando tenemos dos elementos, uno menos electronegativo que otro, es decir uno con tendencia a ceder electrones M m+ (m es número de oxidación o valencia) y otro con
NOMENCLATURA INORGÁNICA
 NOMENCLATURA INORGÁNICA Elemento: Se denomina elemento a toda sustancia que no puede descomponerse en otras más sencillas por métodos químicos. Nombre y símbolo de un elemento: Cada elemento se identifica
NOMENCLATURA INORGÁNICA Elemento: Se denomina elemento a toda sustancia que no puede descomponerse en otras más sencillas por métodos químicos. Nombre y símbolo de un elemento: Cada elemento se identifica
QUÍMICA INORGÁNICA 3º E.S.O.
 QUÍMICA INORGÁNICA 3º E.S.O. Formulación y nomenclatura. Normas de la IUPAC (2005) 1 2 CONCEPTOS GENERALES 1. NORMAS PARA ESCRIBIR LAS FÓRMULAS Se escriben juntos los símbolos de los átomos, el más electronegativo
QUÍMICA INORGÁNICA 3º E.S.O. Formulación y nomenclatura. Normas de la IUPAC (2005) 1 2 CONCEPTOS GENERALES 1. NORMAS PARA ESCRIBIR LAS FÓRMULAS Se escriben juntos los símbolos de los átomos, el más electronegativo
PROGRAMA TOTAL FÓRMULAS QUÍMICAS Y SISTEMAS DE NOMENCLATURA CLASIFICACIÓN DE LOS COMPUESTOS QUÍMICOS INORGÁNICOS
 Departamento de Física y Química FÍSICA Y QUÍMICA ESO FORMULACIÓN Y NOMENCLATURA DE LOS COMPUESTOS QUÍMICOS INORGÁNICOS PROGRAMA TOTAL INTRODUCCIÓN FÓRMULAS QUÍMICAS Y SISTEMAS DE NOMENCLATURA CLASIFICACIÓN
Departamento de Física y Química FÍSICA Y QUÍMICA ESO FORMULACIÓN Y NOMENCLATURA DE LOS COMPUESTOS QUÍMICOS INORGÁNICOS PROGRAMA TOTAL INTRODUCCIÓN FÓRMULAS QUÍMICAS Y SISTEMAS DE NOMENCLATURA CLASIFICACIÓN
FÍSICA Y QUÍMICA cuaderno de ejercicios
 FÍSICA Y QUÍMICA cuaderno de ejercicios FORMULACIÓN y nomenclatura 1.** Determinen si las siguientes afirmaciones se refieren a metales o a no metales. 1.1. Presentan un brillo característico. 1.2. Los
FÍSICA Y QUÍMICA cuaderno de ejercicios FORMULACIÓN y nomenclatura 1.** Determinen si las siguientes afirmaciones se refieren a metales o a no metales. 1.1. Presentan un brillo característico. 1.2. Los
Ejercicios y respuestas del apartado: Formulación de compuestos inorgánicos: Reglas básicas; Compuestos binarios; Compuestos ternarios más habituales
 Ejercicios y respuestas del apartado: Formulación de compuestos inorgánicos: Reglas básicas; Compuestos binarios; Compuestos ternarios más habituales 2 de 12 Tipo de compuesto Relaciona estos compuestos:
Ejercicios y respuestas del apartado: Formulación de compuestos inorgánicos: Reglas básicas; Compuestos binarios; Compuestos ternarios más habituales 2 de 12 Tipo de compuesto Relaciona estos compuestos:
PLAN DE REFUERZO ÁREA PENDIENTE DE CIENCIAS NATURALES 3ºESO
 PLAN DE REFUERZO ÁREA PENDIENTE DE CIENCIAS NATURALES 3ºESO Para superar la materia, el alumno deberá realizar las actividades que se indican a continuación. Se realizarán en un cuaderno destinado únicamente
PLAN DE REFUERZO ÁREA PENDIENTE DE CIENCIAS NATURALES 3ºESO Para superar la materia, el alumno deberá realizar las actividades que se indican a continuación. Se realizarán en un cuaderno destinado únicamente
UD 2 ENLACE QUÍMICO Y FUERZAS INTERMOLECULARES FORMULACIÓN Y NOMENCLATURA DE COMPUESTOS TERNARIOS
 FORMULACIÓN Y NOMENCLATURA DE COMPUESTOS TERNARIOS Ácidos oxoácidos o ternarios Se formulan añadiendo una molécula de agua a los óxidos no metálicos. Óxidos no metálicos Cl 2 O SO Cl 2 O 3 SO 2 N 2 O 3
FORMULACIÓN Y NOMENCLATURA DE COMPUESTOS TERNARIOS Ácidos oxoácidos o ternarios Se formulan añadiendo una molécula de agua a los óxidos no metálicos. Óxidos no metálicos Cl 2 O SO Cl 2 O 3 SO 2 N 2 O 3
REPASO FORMULACIÓN INORGÁNICA 1
 REPASO FORMULACIÓN INORGÁNICA 1 IES TURANIANA Nombre: Fecha: RELACIÓN 1: ÓXIDOS Trióxido de azufre Dióxido de azufre Oxido de cobalto (II) Oxido de magnesio Oxido de estaño (II) Oxido de potasio Oxido
REPASO FORMULACIÓN INORGÁNICA 1 IES TURANIANA Nombre: Fecha: RELACIÓN 1: ÓXIDOS Trióxido de azufre Dióxido de azufre Oxido de cobalto (II) Oxido de magnesio Oxido de estaño (II) Oxido de potasio Oxido
NOMENCLATURA DE ÁCIDOS Y BASES
 COLEGIO SAN ESTEBAN DIÁCONO Departamento de Ciencias Química IVº Electivo Prof. Juan Pastrián Lisboa NOMENCLATURA DE ÁCIDOS Y BASES Objetivo: - Reconocer y aplicar reglas de nomenclatura tradicional y
COLEGIO SAN ESTEBAN DIÁCONO Departamento de Ciencias Química IVº Electivo Prof. Juan Pastrián Lisboa NOMENCLATURA DE ÁCIDOS Y BASES Objetivo: - Reconocer y aplicar reglas de nomenclatura tradicional y
INSTITUTO EDUCACIÓN SECUNDARIA POLITÉCNICO. CARTAGENA. 3º E.S.O.
 Cartagena-2012 1 FORMULACIÓN Y NOMENCLATURA INORGÁNICA 0. SÍMBOLOS Y VALENCIAS DE LOS ELEMENTOS Los símbolos y valencias de los elementos más comunes vienen recogidos en el ANEXO I. Por último, indicaremos
Cartagena-2012 1 FORMULACIÓN Y NOMENCLATURA INORGÁNICA 0. SÍMBOLOS Y VALENCIAS DE LOS ELEMENTOS Los símbolos y valencias de los elementos más comunes vienen recogidos en el ANEXO I. Por último, indicaremos
TEMA 4: FORMULACIÓN 1.- CONCEPTOS PREVIOS
 TEMA 4: FORMULACIÓN 1.- CONCEPTOS PREVIOS Compuesto químico: es la unión de varios átomos que no pueden separarse por procedimientos físicos pero sí mediante procedimientos químicos. Ejemplo: dos átomos
TEMA 4: FORMULACIÓN 1.- CONCEPTOS PREVIOS Compuesto químico: es la unión de varios átomos que no pueden separarse por procedimientos físicos pero sí mediante procedimientos químicos. Ejemplo: dos átomos
Formulación de Química Inorgánica
 Formulación de Química Inorgánica F. G. Calvo-Flores 1. VALENCIA. Es la capacidad que tiene un átomo de un elemento para combinarse con los átomos de otros elementos y formar compuestos. La valencia es
Formulación de Química Inorgánica F. G. Calvo-Flores 1. VALENCIA. Es la capacidad que tiene un átomo de un elemento para combinarse con los átomos de otros elementos y formar compuestos. La valencia es
EJERCICIOS DE REPASO DE FORMULACIÓN Y NOMENCLATURA DE QUÍMICA INORGÁNICA COMPUESTOS BINARIOS
 EJERCICIOS DE REPASO DE FORMULACIÓN Y NOMENCLATURA DE QUÍMICA INORGÁNICA COMPUESTOS BINARIOS No hace falta hacerlos todos, ya os habréis dado cuenta de que si entendéis la lógica que hay detrás de la formulación
EJERCICIOS DE REPASO DE FORMULACIÓN Y NOMENCLATURA DE QUÍMICA INORGÁNICA COMPUESTOS BINARIOS No hace falta hacerlos todos, ya os habréis dado cuenta de que si entendéis la lógica que hay detrás de la formulación
QUÍMICA INORGÁNICA. Elementos Símbolo Valencia Elemento Símbolo Valencia. Hidrógeno H Oxigeno O -2. Flúor F -1 Nitrógeno N
 QUÍMICA INORGÁNICA VALENCIAS NO METALES Elementos Símbolo Valencia Elemento Símbolo Valencia Hidrógeno H -1 +1 Oxigeno O -2 Flúor F -1 Nitrógeno N -3 +1+3+5 Cloro Cl -1 +1+3+5+7 Fósforo P -3 +1+3+5 Bromo
QUÍMICA INORGÁNICA VALENCIAS NO METALES Elementos Símbolo Valencia Elemento Símbolo Valencia Hidrógeno H -1 +1 Oxigeno O -2 Flúor F -1 Nitrógeno N -3 +1+3+5 Cloro Cl -1 +1+3+5+7 Fósforo P -3 +1+3+5 Bromo
1.- CONCEPTOS PREVIOS
 TEMA 6: FORMULACIÓN 1.- CONCEPTOS PREVIOS Compuesto químico: es la unión de varios átomos que no pueden separarse por procedimientos físicos pero sí mediante procedimientos químicos. Ejemplo: dos átomos
TEMA 6: FORMULACIÓN 1.- CONCEPTOS PREVIOS Compuesto químico: es la unión de varios átomos que no pueden separarse por procedimientos físicos pero sí mediante procedimientos químicos. Ejemplo: dos átomos
Óxido de hierro (III)
 COMPUESTOS BINARIOS: ÓXIDOS Los óxidos son combinaciones del oxígeno con otro elemento. El nombre de estos compuestos siempre incluye la palabra óxido que puede estar precedida de prefijos indicadores
COMPUESTOS BINARIOS: ÓXIDOS Los óxidos son combinaciones del oxígeno con otro elemento. El nombre de estos compuestos siempre incluye la palabra óxido que puede estar precedida de prefijos indicadores
SUMARIO FÓRMULAS QUÍMICAS Y SISTEMAS DE NOMENCLATURA CLASIFICACIÓN DE LOS COMPUESTOS QUÍMICOS INORGÁNICOS INTRODUCCIÓN SUSTANCIAS SIMPLES
 Departamento de Ciencias Naturales IES Benalmádena FÍSICA Y QUÍMICA 3º ESO FORMULACIÓN Y NOMENCLATURA DE LOS COMPUESTOS QUÍMICOS INORGÁNICOS FORMULACIÓN Y NOMENCLATURA COMBINACIONES BINARIAS INTRODUCCIÓN
Departamento de Ciencias Naturales IES Benalmádena FÍSICA Y QUÍMICA 3º ESO FORMULACIÓN Y NOMENCLATURA DE LOS COMPUESTOS QUÍMICOS INORGÁNICOS FORMULACIÓN Y NOMENCLATURA COMBINACIONES BINARIAS INTRODUCCIÓN
FORMULACIÓN DE QUÍMICA INORGÁNICA
 DE QUÍMICA INORGÁNICA Del mismo modo que utilizamos las palabras para comunicarnos, en química recurrimos a las fórmulas para representar los compuestos. Estas fórmulas no son arbitrarias, sino que responden
DE QUÍMICA INORGÁNICA Del mismo modo que utilizamos las palabras para comunicarnos, en química recurrimos a las fórmulas para representar los compuestos. Estas fórmulas no son arbitrarias, sino que responden
Los elementos químicos se caracterizan por un nombre y un símbolo, acordados por la IUPAC (International Union of Pure and Applied Chemistry).
 4. FORMULACIÓN. 4.1. SÍMBOLOS E HIDRUROS. 4.1.1. SÍMBOLOS Y VALENCIAS. Los elementos químicos se caracterizan por un nombre y un símbolo, acordados por la IUPAC (International Union of Pure and Applied
4. FORMULACIÓN. 4.1. SÍMBOLOS E HIDRUROS. 4.1.1. SÍMBOLOS Y VALENCIAS. Los elementos químicos se caracterizan por un nombre y un símbolo, acordados por la IUPAC (International Union of Pure and Applied
NOMENCLATURA y FORMULACIÓN en QUÍMICA INORGÁNICA. Nivel: Educación Secundaria Obligatoria
 NOMENCLATURA y FORMULACIÓN en QUÍMICA INORGÁNICA Nivel: Educación Secundaria Obligatoria Conceptos básicos Los elementos químicos se representan mediante símbolos, que consisten en una o dos letras que
NOMENCLATURA y FORMULACIÓN en QUÍMICA INORGÁNICA Nivel: Educación Secundaria Obligatoria Conceptos básicos Los elementos químicos se representan mediante símbolos, que consisten en una o dos letras que
Formulación: Introducción y compuesto binarios. Teoría. Compuestos binarios y ternarios
 Compuestos binarios y ternarios 1. Compuestos binarios son aquellos que están formados por dos elementos diferentes. Ejemplos: - NaH está formado por dos elementos el Na y el H - Cl 2 O está formado por
Compuestos binarios y ternarios 1. Compuestos binarios son aquellos que están formados por dos elementos diferentes. Ejemplos: - NaH está formado por dos elementos el Na y el H - Cl 2 O está formado por
Óxido de hierro(iii)
 ÓXIDOS Los óxidos son combinaciones de los elementos con el oxígeno. El nombre de estos compuestos siempre incluye la palabra óxido que puede estar precedida de prefijos numerales indicadores del número
ÓXIDOS Los óxidos son combinaciones de los elementos con el oxígeno. El nombre de estos compuestos siempre incluye la palabra óxido que puede estar precedida de prefijos numerales indicadores del número
M m+ + X n-! M n X m EJERCICIOS/ESTUDIO. Qué es formular un compuesto binario?
 EJERCICIOS/ESTUDIO Materia: Tema: Física y Química 3º ESO Curso: Qué es formular un compuesto binario? Cuando tenemos dos elementos, uno menos electronegativo que otro, es decir uno con tendencia a ceder
EJERCICIOS/ESTUDIO Materia: Tema: Física y Química 3º ESO Curso: Qué es formular un compuesto binario? Cuando tenemos dos elementos, uno menos electronegativo que otro, es decir uno con tendencia a ceder
Nomenclatura Inorgánica
 Nomenclatura Inorgánica Nomenclatura Química O Es el sistema de normas, comunes en todo el mundo, para denominar a los elementos y compuestos químicos. O El organismo encargado de dictar tales normas se
Nomenclatura Inorgánica Nomenclatura Química O Es el sistema de normas, comunes en todo el mundo, para denominar a los elementos y compuestos químicos. O El organismo encargado de dictar tales normas se
Tema 1 : Nomenclatura y formulación Química Inorgánica
 Tema 1 : Nomenclatura y formulación Química Inorgánica Esquema de trabajo: Introducción Compuestos Binarios 1. Combinaciones binarias del oxígeno 2. Combinaciones binarias del hidrógeno 3. Sales binarias
Tema 1 : Nomenclatura y formulación Química Inorgánica Esquema de trabajo: Introducción Compuestos Binarios 1. Combinaciones binarias del oxígeno 2. Combinaciones binarias del hidrógeno 3. Sales binarias
FORMULACIÓN DE QUÍMICA INORGÁNICA 3ºESO
 Euclides Enseñanza Sociedad Cooperativa Andaluza Colegio Privado Concertado Arboleda C/ Reina Victoria 2. 41020 Sevilla Telf. 954 408126 Fax 954 440186 www.colegioarboleda.es arboleda@aces-andalucia.org
Euclides Enseñanza Sociedad Cooperativa Andaluza Colegio Privado Concertado Arboleda C/ Reina Victoria 2. 41020 Sevilla Telf. 954 408126 Fax 954 440186 www.colegioarboleda.es arboleda@aces-andalucia.org
FORMULACIÓN QUÍMICA INORGÁNICA
 FORMULACIÓN QUÍMICA INORGÁNICA 1. VALENCIAS DE LOS ELEMENTOS QUÍMICOS MÁS CONOCIDOS Se entiende que las valencias con signo negativo se dan frente a elementos electropositivos y las valencias con signo
FORMULACIÓN QUÍMICA INORGÁNICA 1. VALENCIAS DE LOS ELEMENTOS QUÍMICOS MÁS CONOCIDOS Se entiende que las valencias con signo negativo se dan frente a elementos electropositivos y las valencias con signo
NOMENCLATURA y FORMULACIÓN en QUÍMICA INORGÁNICA
 NOMENCLATURA y FORMULACIÓN en QUÍMICA INORGÁNICA Adaptado a las normas de la IUPAC 1990 Nivel: 3º ESO 1 0. Introducción Valencia Es la capacidad que posee un elemento de combinarse con otro. Como el hidrógeno
NOMENCLATURA y FORMULACIÓN en QUÍMICA INORGÁNICA Adaptado a las normas de la IUPAC 1990 Nivel: 3º ESO 1 0. Introducción Valencia Es la capacidad que posee un elemento de combinarse con otro. Como el hidrógeno
TEMA 4: Formulación inorgánica
 TEMA 4: Formulación inorgánica Tema 4: Formulación Inorgánica 1 1.- CMPUESTS BINARIS Son sustancias formadas por la unión de dos elementos químicos, como por ejemplo NaH, Co 3, Li S y PCl 3 1.1.- los En
TEMA 4: Formulación inorgánica Tema 4: Formulación Inorgánica 1 1.- CMPUESTS BINARIS Son sustancias formadas por la unión de dos elementos químicos, como por ejemplo NaH, Co 3, Li S y PCl 3 1.1.- los En
3.5. FORMULACIÓN Y NOMENCLATURA II
 3.5. FORMULACIÓN Y NOMENCLATURA II 3.5.1. HIDRUROS METÁLICOS. Los compuestos binarios son aquellos en los que únicamente intervienen dos tipos de átomos, es decir, que están formados por sólo dos elementos
3.5. FORMULACIÓN Y NOMENCLATURA II 3.5.1. HIDRUROS METÁLICOS. Los compuestos binarios son aquellos en los que únicamente intervienen dos tipos de átomos, es decir, que están formados por sólo dos elementos
FORMULACIÓN DE QUÍMICA INORGÁNICA.
 FORMULACIÓN DE QUÍMICA INORGÁNICA. A medida que fueron conociéndose los diferentes elementos químicos de la tabla periódica se vio que el número era relativamente pequeño si se compara con la gran variedad
FORMULACIÓN DE QUÍMICA INORGÁNICA. A medida que fueron conociéndose los diferentes elementos químicos de la tabla periódica se vio que el número era relativamente pequeño si se compara con la gran variedad
Se conocen como sales binarias a las combinaciones de un metal con un no. metal o de dos no metales entre sí. En los compuestos de un metal y un no
 4.2. COMPUESTOS BINARIOS. 4.2.1. METAL Y NO METAL. Se conocen como sales binarias a las combinaciones de un metal con un no metal o de dos no metales entre sí. En los compuestos de un metal y un no metal,
4.2. COMPUESTOS BINARIOS. 4.2.1. METAL Y NO METAL. Se conocen como sales binarias a las combinaciones de un metal con un no metal o de dos no metales entre sí. En los compuestos de un metal y un no metal,
REPASO: FORMULACIÓN INORGÁNICA
 COMPUESTOS BINARIOS REPASO: FORMULACIÓN INORGÁNICA OXÍGENO + METAL ÓXIDOS BÁSICOS COMPUESTOS BINARIOS CON OXÍGENO OXÍGENO + NO METAL ÓXIDOS ÁCIDOS El oxígeno se combina con todos los elementos excepto
COMPUESTOS BINARIOS REPASO: FORMULACIÓN INORGÁNICA OXÍGENO + METAL ÓXIDOS BÁSICOS COMPUESTOS BINARIOS CON OXÍGENO OXÍGENO + NO METAL ÓXIDOS ÁCIDOS El oxígeno se combina con todos los elementos excepto
Formulación Inorgánica
 Formulación Inorgánica 1.- Sustancias Simples Por sustancias simples entendemos aquellas sustancias formadas por un solo tipo de elementos, podemos encontrar casos: Sustancias simples metálicas: se formulan
Formulación Inorgánica 1.- Sustancias Simples Por sustancias simples entendemos aquellas sustancias formadas por un solo tipo de elementos, podemos encontrar casos: Sustancias simples metálicas: se formulan
3º ESO 1. 1, 2, 3, 4, 5 Y
 FÍSICA Y QUÍMICA 2º ESO 1. Debe hacer un resumen de los temas 1, 2, 3, 4, 5, 6 y 7. 2. Debe entregar un folio con el esquema de las ecuaciones utilizadas en cada uno de los temas de física y química. 3.
FÍSICA Y QUÍMICA 2º ESO 1. Debe hacer un resumen de los temas 1, 2, 3, 4, 5, 6 y 7. 2. Debe entregar un folio con el esquema de las ecuaciones utilizadas en cada uno de los temas de física y química. 3.
H, Li, Na, K, Rb, Cs, Fr 1. Be, Mg, Ca, Sr, Ba, Ra, Zn, Cd 2. B, Al 3. N, P, As, Sb 1, 3, 5. F, Cl, Br, I 1, 3, 5, 7. C, Si, Ge, Sn, Pb 2, 4 O 2
 H, Li, Na, K, Rb, Cs, Fr 1 Be, Mg, Ca, Sr, Ba, Ra, Zn, Cd 2 B, Al 3 N, P, As, Sb 1, 3, 5 F, Cl, Br, I 1, 3, 5, 7 C, Si, Ge, Sn, Pb 2, 4 O 2 S, Se, Te 2, 4, 6 Cr 2, 3, 3, 6 Mn 2, 3, 4, 6, 7 Fe, Co, Ni 2,
H, Li, Na, K, Rb, Cs, Fr 1 Be, Mg, Ca, Sr, Ba, Ra, Zn, Cd 2 B, Al 3 N, P, As, Sb 1, 3, 5 F, Cl, Br, I 1, 3, 5, 7 C, Si, Ge, Sn, Pb 2, 4 O 2 S, Se, Te 2, 4, 6 Cr 2, 3, 3, 6 Mn 2, 3, 4, 6, 7 Fe, Co, Ni 2,
DEPARTAMENTO DE FÍSICA Y QUÍMICA
 Qué es formular un compuesto binario? Cuando tenemos dos elementos, uno menos electronegativo que otro, es decir uno con tendencia a ceder electrones Mm+ (m es número de oxidación o valencia) y otro con
Qué es formular un compuesto binario? Cuando tenemos dos elementos, uno menos electronegativo que otro, es decir uno con tendencia a ceder electrones Mm+ (m es número de oxidación o valencia) y otro con
APUNTES DE FORMULACIÓN Y NOMENCLATURA DE QUÍMICA INORGÁNICA 3º ESO
 APUNTES DE FORMULACIÓN Y NOMENCLATURA DE QUÍMICA INORGÁNICA 3º ESO 1. ELEMENTOS, SÍMBOLOS Y NÚMEROS DE OXIDACIÓN MÁS FRECUENTES EN LA FORMULACIÓN DE QUÍMICA INORGÁNICA Para poder formular y nombrar los
APUNTES DE FORMULACIÓN Y NOMENCLATURA DE QUÍMICA INORGÁNICA 3º ESO 1. ELEMENTOS, SÍMBOLOS Y NÚMEROS DE OXIDACIÓN MÁS FRECUENTES EN LA FORMULACIÓN DE QUÍMICA INORGÁNICA Para poder formular y nombrar los
Formulación inorgánica. Tema 5
 Formulación inorgánica Tema 5 Valencia A valencia é a capacidade que ten un átomo dun determinado elemento para combinarse con outros átomos A valencia é un número negativo ou positivo e indica o número
Formulación inorgánica Tema 5 Valencia A valencia é a capacidade que ten un átomo dun determinado elemento para combinarse con outros átomos A valencia é un número negativo ou positivo e indica o número
TEORÍA Y EJERCICIOS DE FORMULACIÓN QUÍMICA INORGÁNICA
 TEORÍA Y EJERCICIOS DE FORMULACIÓN QUÍMICA INORGÁNICA COMPUESTOS BINARIOS OXÍGENO + METAL-- ÓXIDOS BÁSICOS COMPUESTOS BINARIOS CON OXÍGENO OXÍGENO + NO METAL ÓXIDOS ÁCIDOS El oxígeno se combina con todos
TEORÍA Y EJERCICIOS DE FORMULACIÓN QUÍMICA INORGÁNICA COMPUESTOS BINARIOS OXÍGENO + METAL-- ÓXIDOS BÁSICOS COMPUESTOS BINARIOS CON OXÍGENO OXÍGENO + NO METAL ÓXIDOS ÁCIDOS El oxígeno se combina con todos
GUIA Nº 1 LABORATORIO QUIMICA GENERAL NOMENCLATURA DE QUIMICA INORGÁNICA.
 1 GUIA Nº 1 LABORATORIO QUIMICA GENERAL NOMENCLATURA DE QUIMICA INORGÁNICA. 1. Estado de Oxidación Es la capacidad que tiene un átomo de un elemento para combinarse con los átomos de otros elementos y
1 GUIA Nº 1 LABORATORIO QUIMICA GENERAL NOMENCLATURA DE QUIMICA INORGÁNICA. 1. Estado de Oxidación Es la capacidad que tiene un átomo de un elemento para combinarse con los átomos de otros elementos y
Número de oxidación. Es un número que da la carga que presentaría un átomo si los electrones de cada enlace se asignaran al átomo más electronegativo
 FORMULACIÓN Número de oxidación Es un número que da la carga que presentaría un átomo si los electrones de cada enlace se asignaran al átomo más electronegativo Las reglas de asignación del número de oxidación
FORMULACIÓN Número de oxidación Es un número que da la carga que presentaría un átomo si los electrones de cada enlace se asignaran al átomo más electronegativo Las reglas de asignación del número de oxidación
Ti: +,+,+ en los hidruros no metálicos. +,+ en los óxidos, hidróxidos, hidruros metálicos. Cr: +,+ en las sales binarias. Mn:
 Número de oxidación de un átomo en un compuesto es un número teórico que indica el número de electrones que el átomo habría perdido o ganado, si el compuesto fuera completamente iónico. El número de oxidación,
Número de oxidación de un átomo en un compuesto es un número teórico que indica el número de electrones que el átomo habría perdido o ganado, si el compuesto fuera completamente iónico. El número de oxidación,
Nombrar Compuesto Sistemática Stok HI. Seleniuro de hidrógeno. Cloruro de hidrógeno. Fluoruro de hidrógeno. Sulfuro de hidrógeno
 Nombrar Compuesto Sistemática Stok HI Yoduro de hidrógeno H 2 Se HF H 2 S Seleniuro de hidrógeno Cloruro de hidrógeno Fluoruro de hidrógeno Sulfuro de hidrógeno Ácido yodhídrico Ácido selenhídrico Ácido
Nombrar Compuesto Sistemática Stok HI Yoduro de hidrógeno H 2 Se HF H 2 S Seleniuro de hidrógeno Cloruro de hidrógeno Fluoruro de hidrógeno Sulfuro de hidrógeno Ácido yodhídrico Ácido selenhídrico Ácido
Acuerdo 286. Química. Nomenclatura Inorgánica. Recopiló: M.C. Macaria Hernández Chávez
 Acuerdo 286 Química Nomenclatura Inorgánica Recopiló: M.C. Macaria Hernández Chávez Nomenclatura química inorgánica La Química tiene un lenguaje propio para nombrar las sustancias puras, ya sean simples
Acuerdo 286 Química Nomenclatura Inorgánica Recopiló: M.C. Macaria Hernández Chávez Nomenclatura química inorgánica La Química tiene un lenguaje propio para nombrar las sustancias puras, ya sean simples
FORMULACIÓN Y NOMENCLATURA INORGÁNICA
 FORMULACIÓN Y NOMENCLATURA INORGÁNICA Número de oxidación (n.o.): es la carga real (si es un ion) o aparente (si no es un ion) que tienen los elementos que forman parte de un compuesto. (Ver la tabla de
FORMULACIÓN Y NOMENCLATURA INORGÁNICA Número de oxidación (n.o.): es la carga real (si es un ion) o aparente (si no es un ion) que tienen los elementos que forman parte de un compuesto. (Ver la tabla de
APUNTES DE FORMULACIÓN Y NOMENCLATURA DE QUÍMICA INORGÁNICA 3º ESO - CURSO METALES
 CONSEJERÍA DE EDUCACIÓN APUNTES DE FORMULACIÓN Y NOMENCLATURA DE QUÍMICA INORGÁNICA 3º ESO - CURSO 2012-2013 1. ELEMENTOS, SÍMBOLOS Y NÚMEROS DE OXIDACIÓN MÁS FRECUENTES EN LA FORMULACIÓN DE QUÍMICA INORGÁNICA
CONSEJERÍA DE EDUCACIÓN APUNTES DE FORMULACIÓN Y NOMENCLATURA DE QUÍMICA INORGÁNICA 3º ESO - CURSO 2012-2013 1. ELEMENTOS, SÍMBOLOS Y NÚMEROS DE OXIDACIÓN MÁS FRECUENTES EN LA FORMULACIÓN DE QUÍMICA INORGÁNICA
Compuestos binarios (combinaciones de dos elementos) HIDRUROS METÁLICOS= Metal - Hidrógeno. X H m. H : - 1 Metales: el suyo. FeH 3
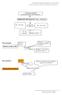 HIDRUROS METÁLICOS= Metal - Hidrógeno AlH 3 ; LiH; CuH 2 X H m KH ; FeH 3 ; ZnH 2 os N de H : - 1 Metales: el suyo Hidruro de hierro(iii) Metal a la izquierda FeH 3 Hidrógeno a la derecha (el mas electronegativo
HIDRUROS METÁLICOS= Metal - Hidrógeno AlH 3 ; LiH; CuH 2 X H m KH ; FeH 3 ; ZnH 2 os N de H : - 1 Metales: el suyo Hidruro de hierro(iii) Metal a la izquierda FeH 3 Hidrógeno a la derecha (el mas electronegativo
trisulfuro de dialuminio
 NOMENCLATURA DE QUÍMICA INORGÁNICA COMPUESTOS BINARIOS (BACHILLERATO) Para qué la nomenclatura química? Cuando estudiamos química nos encontramos con multitud de sustancias a las que debemos de asignar
NOMENCLATURA DE QUÍMICA INORGÁNICA COMPUESTOS BINARIOS (BACHILLERATO) Para qué la nomenclatura química? Cuando estudiamos química nos encontramos con multitud de sustancias a las que debemos de asignar
IES Lluís Vives Departamento de Física y Química Física y Química 3º ESO EJERCICIOS DE FORMULACIÓN Y NOMENCLATURA. Hidruro de calcio.
 FISICA Y QUIMICA 3º ESO Óxido de potasio IES Lluís Vives Departamento de Física y Química Física y Química 3º ESO EJERCICIOS DE FORMULACIÓN Y NOMENCLATURA CaCO3 CO 2 Hidruro de calcio Fe 2 O 3 H 2 O Ácido
FISICA Y QUIMICA 3º ESO Óxido de potasio IES Lluís Vives Departamento de Física y Química Física y Química 3º ESO EJERCICIOS DE FORMULACIÓN Y NOMENCLATURA CaCO3 CO 2 Hidruro de calcio Fe 2 O 3 H 2 O Ácido
trisulfuro de dialuminio
 NOMENCLATURA DE QUÍMICA INORGÁNICA COMPUESTOS BINARIOS Para qué la nomenclatura química? Cuando estudiamos química nos encontramos con multitud de sustancias a las que debemos de asignar un nombre y una
NOMENCLATURA DE QUÍMICA INORGÁNICA COMPUESTOS BINARIOS Para qué la nomenclatura química? Cuando estudiamos química nos encontramos con multitud de sustancias a las que debemos de asignar un nombre y una
Reglas generales. n Se nombra electronegativo de electropositivo. n Fórmula electropositivo electronegativo
 nomenclatura Reglas generales n Se nombra electronegativo de electropositivo n El electropositivo no se modifica n El electronegativo se modificará según las reglas de n compuestos binarios, n ternarios
nomenclatura Reglas generales n Se nombra electronegativo de electropositivo n El electropositivo no se modifica n El electronegativo se modificará según las reglas de n compuestos binarios, n ternarios
FORMULACIÓN DE QUÍMICA INORGÁNICA
 FORMULACIÓN DE QUÍMICA INORGÁNICA 1. VALENCIA. Es la capacidad que tiene un átomo de un elemento para combinarse con los átomos de otros elementos y formar compuestos. La valencia es un número, positivo
FORMULACIÓN DE QUÍMICA INORGÁNICA 1. VALENCIA. Es la capacidad que tiene un átomo de un elemento para combinarse con los átomos de otros elementos y formar compuestos. La valencia es un número, positivo
1. Nombra los siguientes compuestos por medio de dos tipos de nomenclatura:
 FORMULACIÓN Y NOMENCLATURA DE QUÍMICA Bachillerato Especies químicas inorgánicas 1. Nombra los siguientes compuestos por medio de dos tipos de nomenclatura: a) SO 2 b) CO c) Rb 2 O d) Sc 2 O 3 e) OF 2
FORMULACIÓN Y NOMENCLATURA DE QUÍMICA Bachillerato Especies químicas inorgánicas 1. Nombra los siguientes compuestos por medio de dos tipos de nomenclatura: a) SO 2 b) CO c) Rb 2 O d) Sc 2 O 3 e) OF 2
APUNTES DE FORMULACIÓN QUÍMICA INORGÁNICA 3º DE E.S.O
 APUNTES DE FORMULACIÓN QUÍMICA INORGÁNICA 3º DE E.S.O Colegio Cardenal Spínola Huelva FORMULACIÓN DE QUÍMICA INORGÁNICA. 1. VALENCIA. Es la capacidad que tiene un átomo de un elemento para combinarse con
APUNTES DE FORMULACIÓN QUÍMICA INORGÁNICA 3º DE E.S.O Colegio Cardenal Spínola Huelva FORMULACIÓN DE QUÍMICA INORGÁNICA. 1. VALENCIA. Es la capacidad que tiene un átomo de un elemento para combinarse con
FÍSICA Y QUÍMICA Solucionario
 FÍSICA Y QUÍMICA Solucionario FORMULACIÓN y nomenclatura 1.** Determinad si las siguientes afirmaciones se refieren a metales o a no metales. 1.1. Presentan un brillo característico. Metales 1.2. Los componentes
FÍSICA Y QUÍMICA Solucionario FORMULACIÓN y nomenclatura 1.** Determinad si las siguientes afirmaciones se refieren a metales o a no metales. 1.1. Presentan un brillo característico. Metales 1.2. Los componentes
ESTRUCTURA INTERNA DE LA MATERIA. LOS ÁTOMOS
 1. DE DEMÓCRITO A DALTON ESTRUCTURA INTERNA DE LA MATERIA. LOS ÁTOMOS Hasta dónde podemos dividir una sustancia? Tomamos un terrón de azúcar y lo partimos por la mitad. Elegimos una de las dos mitades
1. DE DEMÓCRITO A DALTON ESTRUCTURA INTERNA DE LA MATERIA. LOS ÁTOMOS Hasta dónde podemos dividir una sustancia? Tomamos un terrón de azúcar y lo partimos por la mitad. Elegimos una de las dos mitades
EJERCICIOS DE FORMULACIÓN Y NOMENCLATURA
 EJERCICIOS DE FORMULACIÓN Y NOMENCLATURA 1. Determina el número de oxidación del manganeso en los compuestos: MnO 2 Mn 2 O 3 2. Determina el número de oxidación del Cl en los compuestos: Cl 2 O 7 Cl 2
EJERCICIOS DE FORMULACIÓN Y NOMENCLATURA 1. Determina el número de oxidación del manganeso en los compuestos: MnO 2 Mn 2 O 3 2. Determina el número de oxidación del Cl en los compuestos: Cl 2 O 7 Cl 2
EJERCICIOS DE FORMULACIÓN Y NOMENCLATURA DE QUÍMICA INORGÁNICA 4º ESO
 EJERCICIOS DE FORMULACIÓN Y DE QUÍMICA INORGÁNICA 4º ESO 1 COMPUESTOS BINARIOS 1.1 CON OXÍGENO 1.1.1 Y UN METAL (ÓXIDOS) 1 BaO Monóxido de bario Óxido de bario 2 Na 2 O Monóxido de disodio Óxido de sodio
EJERCICIOS DE FORMULACIÓN Y DE QUÍMICA INORGÁNICA 4º ESO 1 COMPUESTOS BINARIOS 1.1 CON OXÍGENO 1.1.1 Y UN METAL (ÓXIDOS) 1 BaO Monóxido de bario Óxido de bario 2 Na 2 O Monóxido de disodio Óxido de sodio
FORMULACIÓN DE QUÍMICA INORGÁNICA
 DE QUÍMICA INORGÁNICA Del mismo modo que utilizamos las palabras para comunicarnos, en química recurrimos a las fórmulas para representar los compuestos. Estas fórmulas no son arbitrarias, sino que responden
DE QUÍMICA INORGÁNICA Del mismo modo que utilizamos las palabras para comunicarnos, en química recurrimos a las fórmulas para representar los compuestos. Estas fórmulas no son arbitrarias, sino que responden
Formulación Inorgánica Ejercicios (II)
 Ejercicios (II) EJERCICIOS DE FORMULACIÓN INORGÁNICA (II) COMPUESTOS BINARIOS DEL OXÍGENO 1.- Nombrar: Cl2O7 FeO N2O SO3 Cr2O3 Br2O P2O5 CO2 I2O5 2.- Formular: MnO2 Trióxido de dicromo Óxido de nitrógeno
Ejercicios (II) EJERCICIOS DE FORMULACIÓN INORGÁNICA (II) COMPUESTOS BINARIOS DEL OXÍGENO 1.- Nombrar: Cl2O7 FeO N2O SO3 Cr2O3 Br2O P2O5 CO2 I2O5 2.- Formular: MnO2 Trióxido de dicromo Óxido de nitrógeno
COLECCIÓN DE EXERCICIOS FORMULACIÓN INORGÁNICA
 COLECCIÓN DE EXERCICIOS FORMULACIÓN INORGÁNICA 1.- Completa a seguinte táboa Fórmula N. sistemática N. stock N. tradicional F2O I2O7 As2O5 CaO Fe2O3 PbO2 Al2O3 SnO N2O5 Au20 TeO2 Óxido aúrico Óxido cuproso
COLECCIÓN DE EXERCICIOS FORMULACIÓN INORGÁNICA 1.- Completa a seguinte táboa Fórmula N. sistemática N. stock N. tradicional F2O I2O7 As2O5 CaO Fe2O3 PbO2 Al2O3 SnO N2O5 Au20 TeO2 Óxido aúrico Óxido cuproso
Un átomo de sodio (Na) y otro de cloro(cl) Dos átomos de hidrógeno (H) y uno de oxígeno (O)
 Símbolos Un elemento químico es aquel compuesto químico que no puede ser descompuesto en otros más simples. Se conocen más de cien elementos químicos, aunque en la naturaleza sólo aparecen noventa, los
Símbolos Un elemento químico es aquel compuesto químico que no puede ser descompuesto en otros más simples. Se conocen más de cien elementos químicos, aunque en la naturaleza sólo aparecen noventa, los
OXIDOS METÁLICOS O BÁSICOS. Regla 1: se escribe la palabra óxido + nombre del metal (catión) + número de oxidación en números romanos
 OXIDOS METÁLICOS O BÁSICOS Nomenclatura Stock Regla 1: se escribe la palabra óxido + nombre del metal (catión) + número de oxidación en números romanos Hg +1 O -2 = Hg2O = óxido de mercurio (I) Hg +2 O
OXIDOS METÁLICOS O BÁSICOS Nomenclatura Stock Regla 1: se escribe la palabra óxido + nombre del metal (catión) + número de oxidación en números romanos Hg +1 O -2 = Hg2O = óxido de mercurio (I) Hg +2 O
Combinaciones Binarias
 Combinaciones Binarias Se llama combinaciones binarias a los compuestos formados por átomos de dos elementos diferentes. Antes de estudiar los diferentes tipos de combinaciones binarias veremos unas normas
Combinaciones Binarias Se llama combinaciones binarias a los compuestos formados por átomos de dos elementos diferentes. Antes de estudiar los diferentes tipos de combinaciones binarias veremos unas normas
NOMENCLATURA DE QUÍMICA INORGÁNICA COMPUESTOS BINARIOS. AMPLIACIÓN (3.º ESO) Nomenclatura de compuestos binarios usando números de oxidación
 NOMENCLATURA DE QUÍMICA INORGÁNICA COMPUESTOS BINARIOS. AMPLIACIÓN Nomenclatura de compuestos binarios usando números de oxidación La nomenclatura de composición permite usar los números de oxidación para
NOMENCLATURA DE QUÍMICA INORGÁNICA COMPUESTOS BINARIOS. AMPLIACIÓN Nomenclatura de compuestos binarios usando números de oxidación La nomenclatura de composición permite usar los números de oxidación para
ACTIVIDADES DE FORMULACIÓN INORGÁNICA 1º BACHILLERATO.
 ACTIVIDADES DE FORMULACIÓN INORGÁNICA 1º BACHILLERATO. Esteban Calvo Marín Página 1 ÓXIDOS Y PERÓXIDOS: 1.- Ag 2 O H 2 O P 2 O 3 N 2 O 5 CO 2 Br 2 O 3 I 2 O 7 MgO 2 PbO As 2 O 3 SnO 2 Al 2 O 3 GeO 2 ZnO
ACTIVIDADES DE FORMULACIÓN INORGÁNICA 1º BACHILLERATO. Esteban Calvo Marín Página 1 ÓXIDOS Y PERÓXIDOS: 1.- Ag 2 O H 2 O P 2 O 3 N 2 O 5 CO 2 Br 2 O 3 I 2 O 7 MgO 2 PbO As 2 O 3 SnO 2 Al 2 O 3 GeO 2 ZnO
Ejemplo 2.- Cuando tiene 4 valencias como el Cl, I, Br, Fluor se usa HIPO-OSO e HIPER-ICO
 FUNCIONES QUÍMICAS INORGANICAS 1. FUNCION QUIMICA.- Es el conjunto de compuestos que tienen ciertas propiedades en común, como por ejemplo un átomo común para todos. Las funciones químicas pueden ser inorgánicas
FUNCIONES QUÍMICAS INORGANICAS 1. FUNCION QUIMICA.- Es el conjunto de compuestos que tienen ciertas propiedades en común, como por ejemplo un átomo común para todos. Las funciones químicas pueden ser inorgánicas
1 EJERCICIOS (Nomenclatura de Compuestos inorgánicos)
 1 EJERCICIOS (Nomenclatura de Compuestos inorgánicos) HCl Bromato de bario H 2 Te Hidróxido de manganeso (II) Yoduro de cobre (II) Ayala MnO 2 NO Hidruro de bario Óxido de férrico FeCl 3 Zn(OH) 2 Sulfato
1 EJERCICIOS (Nomenclatura de Compuestos inorgánicos) HCl Bromato de bario H 2 Te Hidróxido de manganeso (II) Yoduro de cobre (II) Ayala MnO 2 NO Hidruro de bario Óxido de férrico FeCl 3 Zn(OH) 2 Sulfato
Trabajo de repaso. Física y Química
 Departamento de Física y Química IES Salvador Allende Trabajo de repaso De Física y Química Nombre del alumno: Curso: Objetivo del trabajo: ayudar a preparar la asignatura durante el verano Fecha de entrega
Departamento de Física y Química IES Salvador Allende Trabajo de repaso De Física y Química Nombre del alumno: Curso: Objetivo del trabajo: ayudar a preparar la asignatura durante el verano Fecha de entrega
Ejercicios Nomenclatura Inorgánica
 Ejercicios Nomenclatura Inorgánica 1. De nombre a los siguientes compuestos: 1. Cl 2 O 7 2. FeO 3. N 2 O 4. SO 3 5. Cr 2 O 3 6. P 2 O 5 2. Indique la fórmula de los siguientes compuestos: 1. Trióxido de
Ejercicios Nomenclatura Inorgánica 1. De nombre a los siguientes compuestos: 1. Cl 2 O 7 2. FeO 3. N 2 O 4. SO 3 5. Cr 2 O 3 6. P 2 O 5 2. Indique la fórmula de los siguientes compuestos: 1. Trióxido de
COMPUESTOS INORGÁNICOS
 COMPUESTOS INORGÁNICOS ELEMENTO METÁLICO NO METÁLICO con con metal oxígeno hidrógeno metal oxígeno hidrógeno ALEACIÓN ÓXIDO METÁLICO HIDRURO SAL HALOIDEA ÓXIDO NO METÁLICO ÁCIDO HIDRÁCIDO con H 2O con
COMPUESTOS INORGÁNICOS ELEMENTO METÁLICO NO METÁLICO con con metal oxígeno hidrógeno metal oxígeno hidrógeno ALEACIÓN ÓXIDO METÁLICO HIDRURO SAL HALOIDEA ÓXIDO NO METÁLICO ÁCIDO HIDRÁCIDO con H 2O con
FÍSICA Y QUÍMICA 4º DE ESO CURSO 16/ 17
 FÍSICA Y QUÍMICA 4º DE ESO CURSO 16/ 17 Alumno/a: 1. Completa la tabla, utilizando el SP: NOMBRE SÍMBOLO Z A P + e - N CARGA *catión *anión *carga 0 24 28 3+ 65 28 35 Cobre 63 29 0 33 75 36 18 16 2-29
FÍSICA Y QUÍMICA 4º DE ESO CURSO 16/ 17 Alumno/a: 1. Completa la tabla, utilizando el SP: NOMBRE SÍMBOLO Z A P + e - N CARGA *catión *anión *carga 0 24 28 3+ 65 28 35 Cobre 63 29 0 33 75 36 18 16 2-29
Universidad Técnica Nacional
 Universidad Técnica Nacional Química I-CB005 Nomenclatura de Compuestos Inorgánicos Lic. Diego Orozco González Nomenclatura Clasificación de los compuestos Compuestos orgánicos Contienen carbono y otros
Universidad Técnica Nacional Química I-CB005 Nomenclatura de Compuestos Inorgánicos Lic. Diego Orozco González Nomenclatura Clasificación de los compuestos Compuestos orgánicos Contienen carbono y otros
