PRÁCTICA 5. Aislamiento de Microorganismos (1ª Sesión)
|
|
|
- María del Carmen Alvarado Botella
- hace 7 años
- Vistas:
Transcripción
1 PRÁCTICA 5. Aislamiento de Microorganismos (1ª Sesión) Objetivos Al finalizar esta práctica el alumno será capaz de: Explicar el fundamento de diferentes medios de cultivo y condiciones de incubación para el aislamiento de microorganismos con características específicas. Aplicar diferentes técnicas para el aislamiento de microorganismos. Obtener y comprobar la pureza de los cultivos aislados. Aplicar una técnica de conservación de corto o mediano plazo a los cultivos puros obtenidos. Introducción En todos los ambientes naturales habitan múltiples microorganismos de diversos tipos y actividad fisiológica. Para efectuar el estudio de un organismo particular es necesario separarlo de la población mixta en la que se encuentra. Para tal fin se emplean técnicas de aislamiento que conduzcan a la obtención de un cultivo puro. De manera general los métodos de aislamiento incluyen: 1. Separación física de los microorganismos mediante: a) Diluciones seriadas y siembra por vertido en placa. b) Siembra por agotamiento. 2. Utilización de medios de cultivo selectivos y diferenciales. 3. Aprovechamiento de características particulares de los microorganismos, tales como la formación de esporas, el metabolismo anaerobio y/ o facultativo, la capacidad para utilizar sustratos poco comunes, etc. Para facilitar el proceso de aislamiento y obtener mejores resultados, frecuentemente se emplean combinaciones de las técnicas anteriores. Materiales Muestras Tortilla o fruta con hongos Cultivo mixto con dos bacterias: una grampositiva y una gramnegativa. Material por grupo: Baño María a 50ºC Incubadoras a 28 y 37 C Tubo con solución de estreptomicina (3000 µg/ ml) estéril. 1 microscopio Reactivos para tinción de Gram Aceite de inmersión Cajas de Petri con: Eosina azul de metileno (EMB) Manitol sal agar (MSA) Tubos de ensayo de 22x175 con 15 ml de Sabouraud Rosa de Bengala (SRB)
2 Material que deben tener los alumnos: Asas Gradilla Tubos de ensayo de 16x150 con 9.0 ml de SSI estéril Pipetas graduadas de 1.0 ml estériles Pipetas graduadas de 10 ml estériles Cajas de Petri de plástico estériles desechables Método 1. Rotular todo el material indicando dilución, o técnica de siembra, medio de cultivo. a) Bacterias. Siembra por agotamiento en medios selectivos y diferenciales. 1. Rotular un tubo son solución salina isotónica estéril (SSIE) y las placas con MSA y EMB. 2. Suspender de 3 a 5 asadas del cultivo mixto en un tubo con SSIE. 3. Tomar una asada de la suspensión y sembrar por estría en cuadrante radial en placas con MSA y EMB. 4. Incubar a 37 C durante 24 horas b) Hongos. Siembra por vertido en placa en medio selectivo. 1. Rotular un tubo son solución salina isotónica estéril (SSIE) y las cajas de Petri estériles para verter el medio de cultivo. 2. Fundir el agar sabouraud rosa de bengala (SRB) contenido en los tubos de ensayo de 22x175 y mantenerlos a 45ºC. Agregar al medio fundido la estreptomicina estéril a una concentración de 3000 µg/ ml (0.15 ml/15 ml del medio para una concentración final 30 µg/ ml). 3. Hacer una suspensión de esporas, para ello, esterilizar el asa y dejar que se enfríe, rozar la superficie del micelio con el asa micológica e introducirla en el tubo con SSIE. Repetir el procedimiento 2 ó 3 veces. 4. A partir de la suspensión, transferir 0.1 ml a una caja de Petri. 5. Colocar la pipeta después de su uso en un pipetero que contenga una solución sanitizante. 6. Agregar a cada caja, el medio SRB con estreptomicina. 7. Mezclar suavemente el inóculo con el medio. Para ello colocar la caja sobre la mesa y girar 5 veces en el sentido de las manecillas del reloj, 5 veces en sentido inverso, 5 veces hacía delante y atrás y 5 en sentido horizontal. 8. Dejar solidificar. 9. Asegurar cada una de las cajas con maskin-tape. 10. Incubar a 28 C durante 5 a 7 días. Precauciones generales Las estrías hechas para la siembra por agotamiento deben ser cerradas y trazadas rápidamente. Etiqueta perfectamente tu material a sembrar. Disposición de desechos 1. Esterilizar el matraz y tubos en los que preparó las diluciones y posteriormente lavarlos. 2. Escurrir el exceso de sanitizante de las pipetas, envolverlas, esterilizarlas y lavarlas.
3 Materiales PRÁCTICA 5. Aislamiento de Microorganismos (2ª Sesión) Microscopio Aceite de inmersión Reactivos para tinción de Gram Material que deben tener los alumnos: Asas bacteriológicas Portaobjetos Charola para tinción Piseta Puente de vidrio Pinzas de madera para ropa Material para profesores: Placas con EMB y MSA. a) Aislamiento de bacterias Método i) Comparación de las colonias desarrolladas en los diferentes medios de cultivo. En las placas con EMB y MSA, proceder a: 1. Comparar la abundancia, separación y diversidad de las colonias desarrolladas en las cajas sembradas. 2. Seleccionar de cada medio de cultivo aquélla placa que presente mayor número de colonias diferentes y separadas. 3. Seleccionar de cada placa 2 colonias diferentes. 4. Identificar con una clave las colonias seleccionadas y de cada una hacer una tinción de Gram (tener cuidado de no arrastrar toda la colonia) y efectuar la observación microscópica. 5. Registrar en el cuadro 1 las características de las colonias aisladas en los diferentes medios de cultivo. NOTA: Hacer tres copias del cuadro 1 para el registro de las características observadas, cuadro 1 para la bacteria grampositiva, cuadro 2 para la gramnegativa y cuadro 3 más para el hongo. ii) Aislamiento primario. 1. Identificar las colonias en las que se observó un solo tipo de morfología y Gram. 1. A partir de la colonia seleccionada inocular por agotamiento una placa que contenga el medio de procedencia (1ª resiembra). 2. Incubar 24 horas a una temperatura que debe ser acorde con la procedencia de la colonia. 3. Guardar en refrigeración las cajas a partir de las cuales se realizó el aislamiento.
4 Cuadro 1, 2 ó 3. Características de colonias seleccionadas para el aislamiento y de las colonias obtenidas en resiembras subsecuentes. Medio de cultivo Clave de la colonia Características macroscópicas* Características microscópicas (incluir esquema) Características iniciales 1ª resiembra 2ª resiembra 3ª resiembra * Describir las colonias de acuerdo con las características revisadas en la Práctica Técnicas de Siembra. Precauciones generales Marca y rotula perfectamente las colonias seleccionadas para realizar el aislamiento primario. Guarda en refrigeración las placas de las cuales se seleccionó la colonia para el aislamiento primario. Disposición de desechos 1. Verter los desechos de colorantes en los contenedores dispuestos en los laboratorios. 2. Después de observar las preparaciones, sumergir los portaobjetos en una solución sanitizante durante 10 minutos, lavar con detergente, enjuagarlos y colocarlos en un frasco con alcohol al 95%. 3. En el caso de ruptura de las preparaciones, envolver los fragmentos con papel, esterilizar el paquete en autoclave y después desecharlos en el contenedor de vidrio roto. 1. Sellar con maskin-tape las cajas de Petri no seleccionadas y colocarlas en el contenedor ubicado en el laboratorio 1A. Discusión de resultados 1. Cómo clasificas a los medios de cultivo empleados de acuerdo a su aplicación? 2. De acuerdo con tu respuesta, Pudiste confirmar esta característica? A qué lo atribuyes?
5 PRÁCTICA 5. Aislamiento de Microorganismos (3ª Sesión) a) Continuación del aislamiento de la bacteria problema (2ª resiembra) b) Resultados. Aislamiento de hongos. Materiales Microscopio Colorantes para tinción de Gram Asas micológicas Lactofenol azul de algodón Placas de TSA o BHI, agar sabouraud Material que deben tener los alumnos: Asas bacteriológicas Portaobjetos Cubreobjetos Charola para tinción Puente de vidrio para tinción Pinzas de madera para ropa Piseta Método a) Continuación del aislamiento de la bacteria problema. 1. Seleccionar tres colonias de cada medio que estén separadas e identificarlas con una clave en el reverso de la caja. 2. A partir de cada colonia realizar un frotis y teñir por la técnica de Gram para verificar la pureza. 3. Registrar en los cuadros 1 ó 2 (de acuerdo a la bacteria a aislar) las características de las colonias desarrolladas. 4. A partir de las observaciones, seleccionar una colonia que microscópicamente muestre un solo tipo de morfología y reacción a la tinción de Gram. 5. Resembrar la colonia por agotamiento en una placa de TSA o BHI e incubar a 37 C durante 24 horas. b) Resultados del crecimiento de hongos. 1. Observar y comparar las características macroscópicas de las colonias desarrolladas en SRB. 2. Registrar en el cuadro 3 la cantidad y características de las colonias desarrolladas. 3. Seleccionar 2 a 3 colonias que se encuentren separadas y sean diferentes. 4. Marcar las colonias con clave al reverso de la caja. 5. Hacer preparaciones por impronta con lactofenol azul de algodón a partir de las colonias seleccionadas en SRB. 6. Observar al microscopio y registrar los resultados en el cuadro 3.
6 Disposición de desechos 1. Verter los desechos de colorantes en los contenedores dispuestos en los laboratorios. 2. Después de observar las preparaciones, sumergir los portaobjetos en una solución sanitizante durante 10 minutos, lavar con detergente, enjuagarlos y colocarlos en un frasco con alcohol al 95%. 3. En el caso de ruptura de las preparaciones, envolver los fragmentos con papel, esterilizar el paquete en autoclave y después desecharlos en el contenedor de vidrio roto. 4. Sellar con maskin tape las cajas de Petri que contengan los cultivos de actinomicetos y hongos y colocar en el contenedor ubicado en el laboratorio 1A Discusión de resultados 1. La cantidad de colonias bacterianas es mayor o menor a la de colonias de hongos filamentosos? A qué lo atribuyes? 2. Qué criterios seguiste para seleccionar la colonia para realizar el aislamiento primario? 3. Cuáles han sido las dificultades a las que te has enfrentado para purificar tu cultivo microbiano? PRÁCTICA 5 Aislamiento de Microorganismos (4ª Sesión) a) Continuación del aislamiento de la bacteria problema Materiales Microscopio Colorantes para tinción de Gram Aceite de inmersión Tubos de ensayo de 13x100 con TSA o BHI inclinado Material que deben tener los alumnos: Asas Portaobjetos Charola para tinción Puente de vidrio para tinción Pinzas de madera para ropa Piseta Material para profesores: Placas con TSA Metodología i) Continuación del aislamiento de la bacteria problema. 1. Seleccionar tres colonias que estén separadas e identificarlas con una clave en el reverso de la caja. 2. A partir de cada colonia realice un frotis y teñir con Gram para verificar la pureza. 3. Observar las características coloniales y microscópicas y registrar en el cuadro 1 ó En el caso de observar cultivos mixtos repetir la resiembra en una placa de TSA o BHI, incubar y repetir los incisos 1 a 3.
7 ii) Conservación del cultivo puro. 1. Una vez confirmada la pureza de las colonias, proceder a resembrar en dos tubos de ensaye de 13x100 con TSA o BHI inclinado (estría ondulada), debidamente etiquetados e incubar a 35 C durante 24 horas. 2. Al término de la incubación sellar con papel Parafilm MR y guardar en refrigeración. b) Aislamiento de hongos 1. Hacer una preparación por impronta de la o las colonias obtenidas. 2. Registrar las características observadas en el cuadro Si está pura, resembrar por picadura en un tubo con agar sabouraud inclinado. 4. Incubar a 28 C por 5 días. Al término de la incu bación sellar con papel ParafilmMR y guardar en refrigeración Precauciones. Para asegurar la obtención de la pureza de tu cultivo, procura en cada resiembra la obtención de colonias aisladas, realizar buenas tinciones y observaciones microscópicas, y respetar los tiempos de incubación de acuerdo al tipo de microorganismo a aislar. Disposición de desechos 1. Verter los desechos de colorantes en los contenedores dispuestos en los laboratorios. 2. Después de observar las preparaciones, sumergir los portaobjetos en una solución sanitizante durante 10 minutos, lavar con detergente, enjuagarlos y colocarlos en un frasco con alcohol al 95%. 3. En caso de ruptura de las preparaciones, envolver los fragmentos con papel, esterilizar el paquete en autoclave y después desecharlos en el contenedor de vidrio roto. Discusión de resultados 1. Comparar la eficiencia de técnicas de separación empleadas. 2. Con base en las observaciones microscópicas, la abundancia y la diversidad de las colonias desarrolladas, discutir si se comprobó la función de los medios selectivos y diferenciales. 3. Comparar las principales diferencias de crecimiento de bacterias y hongos, y su relación con la técnica de siembra, condiciones de incubación y medio selectivo empleados para su aislamiento. Literatura recomendada Madigan, M. T., J. M. Martinko y J. Parker Brock. Biología de los microorganismos. 10ª Ed. Prentice Hall Iberia. España. Ramírez-Gama, R. M., B. Luna Millán, O. Velásquez Madrazo, L. Vierna García, A. Mejía Chávez, G. Tsuzuki Reyes, L. Hernández Gómez, I. Müggenburg, A. Camacho Cruz y M del C. Urzúa Hernández Manual de Prácticas de Microbiología General. 5ª edición. Facultad de Química, UNAM. México. Tortora Gerard J., Fonke Beidell R. y Case Christine L Microbiology an Introduction. 5a. ed. The Benjamin/Cummings Publishing Company, Inc. 801 pp Vullo, D., M. Wachsman, L. Alche Microbiología en Práctica. Manual de laboratorio para la enseñanza de Microbiología básica y aplicada. 1ª edición. Atlante S. R. L. Argentina.
PRÁCTICA 5.1 Aislamiento de Microorganismos
 PRÁCTICA 5.1 Aislamiento de Microorganismos Objetivos Al finalizar esta práctica el alumno será capaz de: Explicar el fundamento de diferentes medios de cultivo y condiciones de incubación para el aislamiento
PRÁCTICA 5.1 Aislamiento de Microorganismos Objetivos Al finalizar esta práctica el alumno será capaz de: Explicar el fundamento de diferentes medios de cultivo y condiciones de incubación para el aislamiento
Aislamiento de Microorganismos (1ª Sesión)
 Aislamiento de Microorganismos (1ª Sesión) Objetivos Al finalizar esta práctica el alumno será capaz de: Explicar el fundamento de diferentes medios de cultivo y condiciones de incubación para el aislamiento
Aislamiento de Microorganismos (1ª Sesión) Objetivos Al finalizar esta práctica el alumno será capaz de: Explicar el fundamento de diferentes medios de cultivo y condiciones de incubación para el aislamiento
PRÁCTICA 8. CONDICIONES AMBIENTALES PARA EL DESARROLLO, INHIBICIÓN Y DESTRUCCIÓN DE LOS MICROORGANISMOS
 PRÁCTICA 8. CONDICIONES AMBIENTALES PARA EL DESARROLLO, INHIBICIÓN Y DESTRUCCIÓN DE LOS MICROORGANISMOS Objetivos Al finalizar este ejercicio el alumno será capaz de: Explicar el efecto de factores físicos
PRÁCTICA 8. CONDICIONES AMBIENTALES PARA EL DESARROLLO, INHIBICIÓN Y DESTRUCCIÓN DE LOS MICROORGANISMOS Objetivos Al finalizar este ejercicio el alumno será capaz de: Explicar el efecto de factores físicos
Materiales. Cultivos puros de bacterias: Streptomyces griseus Streptomyces erythraeus
 Unidad 3. Estudio de cultivos bacterianos puros y Unidad 4. Estudio microscópico y cultivo de hongos, algas y protozoarios Práctica 6. Técnicas de siembra y cultivo de actinomicetos y hongos Objetivos
Unidad 3. Estudio de cultivos bacterianos puros y Unidad 4. Estudio microscópico y cultivo de hongos, algas y protozoarios Práctica 6. Técnicas de siembra y cultivo de actinomicetos y hongos Objetivos
Bioseguridad en el Laboratorio de Microbiología
 Bioseguridad en el Laboratorio de Microbiología Objetivos Al finalizar la práctica el estudiante será capaz de: Aplicar las reglas básicas de higiene y seguridad para los laboratorios del área microbiológica.
Bioseguridad en el Laboratorio de Microbiología Objetivos Al finalizar la práctica el estudiante será capaz de: Aplicar las reglas básicas de higiene y seguridad para los laboratorios del área microbiológica.
PRÁCTICA Esterilización y Preparación de Medios de Cultivo (1ª sesión)
 Objetivos PRÁCTICA Esterilización y Preparación de Medios de Cultivo (1ª sesión) Al finalizar este ejercicio el alumno será capaz de: Explicar el concepto de esterilización y su aplicación en microbiología.
Objetivos PRÁCTICA Esterilización y Preparación de Medios de Cultivo (1ª sesión) Al finalizar este ejercicio el alumno será capaz de: Explicar el concepto de esterilización y su aplicación en microbiología.
Bioseguridad en el Laboratorio de Microbiología
 Objetivos Bioseguridad en el Laboratorio de Microbiología Al finalizar la práctica el estudiante será capaz de: Analizar la importancia que tienen las reglas básicas de higiene y seguridad, tanto en las
Objetivos Bioseguridad en el Laboratorio de Microbiología Al finalizar la práctica el estudiante será capaz de: Analizar la importancia que tienen las reglas básicas de higiene y seguridad, tanto en las
Unidad 6. Nutrición microbiana y caracterización de bacterias. Práctica 9 Metabolismo de bacterias.
 Unidad 6. Nutrición microbiana y caracterización de bacterias. Práctica 9 Metabolismo de bacterias. Objetivos Relacionar la actividad metabólica de los microorganismos con los cambios producidos en diferentes
Unidad 6. Nutrición microbiana y caracterización de bacterias. Práctica 9 Metabolismo de bacterias. Objetivos Relacionar la actividad metabólica de los microorganismos con los cambios producidos en diferentes
PRACTICA Núm. 12 AISLAMIENTO DE 2 MICROORGANISMOS Y OBTENCION DE UN CULTIVO AXENICO
 PRACTICA Núm. 12 AISLAMIENTO DE 2 MICROORGANISMOS Y OBTENCION DE UN CULTIVO AXENICO I. OBJETIVO Aislar dos microorganismos por la técnica de siembra de dilución por estría en placa de agar y obtener un
PRACTICA Núm. 12 AISLAMIENTO DE 2 MICROORGANISMOS Y OBTENCION DE UN CULTIVO AXENICO I. OBJETIVO Aislar dos microorganismos por la técnica de siembra de dilución por estría en placa de agar y obtener un
PRÁCTICA 2.3 Esterilización y Preparación de Medios de Cultivo
 PRÁCTICA 2.3 Esterilización y Preparación de Medios de Cultivo Objetivos Al finalizar este ejercicio el alumno será capaz de: Explicar el concepto de esterilización y su utilidad en microbiología. Preparar
PRÁCTICA 2.3 Esterilización y Preparación de Medios de Cultivo Objetivos Al finalizar este ejercicio el alumno será capaz de: Explicar el concepto de esterilización y su utilidad en microbiología. Preparar
PRÁCTICA PARA EL ESTUDIO DE CULTIVOS BACTERIANOS PUROS (Siembra)
 PRÁCTICA PARA EL ESTUDIO DE CULTIVOS BACTERIANOS PUROS (Siembra) OBJETIVOS GENERALES. Al finalizar este ejercicio el alumno será capaz de: Aplicar las diferentes técnicas de siembra que se emplean para
PRÁCTICA PARA EL ESTUDIO DE CULTIVOS BACTERIANOS PUROS (Siembra) OBJETIVOS GENERALES. Al finalizar este ejercicio el alumno será capaz de: Aplicar las diferentes técnicas de siembra que se emplean para
LABORATORIO DE MICROBIOLOGÍA EXPERIMENTAL Grupo 2 (10:00 13:00 hrs) Semestre Profesores: Guadalupe Tsuzuki Reyes y Rosalba Esquivel-Cote
 Semana 2 Semana 1 LABORATORIO DE EXPERIMENTAL Grupo 2 (10:00 13:00 hrs) Semestre 2013-2 Profesores: Guadalupe Tsuzuki Reyes y Rosalba Esquivel-Cote CALENDARIO DE ACTIVIDADES UNIDAD Lunes 28 ENERO Miércoles
Semana 2 Semana 1 LABORATORIO DE EXPERIMENTAL Grupo 2 (10:00 13:00 hrs) Semestre 2013-2 Profesores: Guadalupe Tsuzuki Reyes y Rosalba Esquivel-Cote CALENDARIO DE ACTIVIDADES UNIDAD Lunes 28 ENERO Miércoles
Materiales. Cultivos puros de hongos: Saccharomyces cerevisiae Rhodototula sp Penicillum sp Aspergillus niger Rhizopous sp Alternaria sp Fusarium sp
 Unidad 3. Estudio de cultivos bacterianos puros y Unidad 4. Estudio microscópico y cultivo de hongos algas y protozoarios Práctica 5. Técnicas de siembra y cultivo de bacterias y hongos Objetivos Aplicar
Unidad 3. Estudio de cultivos bacterianos puros y Unidad 4. Estudio microscópico y cultivo de hongos algas y protozoarios Práctica 5. Técnicas de siembra y cultivo de bacterias y hongos Objetivos Aplicar
Práctica 3. ESTUDIO DE CULTIVOS BACTERIANOS PUROS Práctica 4. ESTUDIO MICROSCÓPICO Y CULTIVO DE HONGOS
 Práctica 3. ESTUDIO DE CULTIVOS BACTERIANOS PUROS Práctica 4. ESTUDIO MICROSCÓPICO Y CULTIVO DE HONGOS OBJETIVOS GENERALES. Al finalizar este ejercicio el alumno será capaz de: Aplicar las diferentes técnicas
Práctica 3. ESTUDIO DE CULTIVOS BACTERIANOS PUROS Práctica 4. ESTUDIO MICROSCÓPICO Y CULTIVO DE HONGOS OBJETIVOS GENERALES. Al finalizar este ejercicio el alumno será capaz de: Aplicar las diferentes técnicas
PRÁCTICAS DEL LABORATORIO DE MICROBIOLOGÍA GENERAL Trimestre 14-I
 PRÁCTICAS DEL LABORATORIO DE MICROBIOLOGÍA GENERAL Trimestre 14-I P # 1 P # 2 P # 3 P # 4 P # 5 P # 6 Uso y cuidados en el manejo del Microscopio Esterilización de materiales y medios Técnicas de Tinción
PRÁCTICAS DEL LABORATORIO DE MICROBIOLOGÍA GENERAL Trimestre 14-I P # 1 P # 2 P # 3 P # 4 P # 5 P # 6 Uso y cuidados en el manejo del Microscopio Esterilización de materiales y medios Técnicas de Tinción
GUÍA DE LABORATORIO Nº 1 MEDIOS DE CULTIVO. OBJETIVO Comprender la utilidad de los medios de cultivo en el trabajo microbiológico.
 GUÍA DE LABORATORIO Nº 1 MEDIOS DE CULTIVO OBJETIVO Comprender la utilidad de los medios de cultivo en el trabajo microbiológico. MATERIALES Placas de agar sangre y agar McConkey. Tubos con agar TSI, agar
GUÍA DE LABORATORIO Nº 1 MEDIOS DE CULTIVO OBJETIVO Comprender la utilidad de los medios de cultivo en el trabajo microbiológico. MATERIALES Placas de agar sangre y agar McConkey. Tubos con agar TSI, agar
PRÁCTICO N 3. Técnicas para la observación, aislamiento y conservación de microorganismos
 PRÁCTICO N 3 Técnicas para la observación, aislamiento y conservación de microorganismos Objetivos Conocer el manejo del microscopio óptico, sus partes y utilidad en el laboratorio de microbiología. Conocer
PRÁCTICO N 3 Técnicas para la observación, aislamiento y conservación de microorganismos Objetivos Conocer el manejo del microscopio óptico, sus partes y utilidad en el laboratorio de microbiología. Conocer
PRACTICA Núm. 22 INVESTIGACION DE COLIFORMES TOTALES Y FECALES EN DESECHOS SOLIDOS Y COMPOSTA
 PRACTICA Núm. 22 INVESTIGACION DE COLIFORMES TOTALES Y FECALES EN DESECHOS SOLIDOS Y COMPOSTA I. OBJETIVO Determinar la presencia de coliformes totales y fecales en un desecho sólido por el método del
PRACTICA Núm. 22 INVESTIGACION DE COLIFORMES TOTALES Y FECALES EN DESECHOS SOLIDOS Y COMPOSTA I. OBJETIVO Determinar la presencia de coliformes totales y fecales en un desecho sólido por el método del
TÉCNICAS PARA LA ENUMERACIÓN DE MICROORGANISMOS.
 TÉCNICAS PARA LA ENUMERACIÓN DE MICROORGANISMOS. ANÁLISIS MICROBIOLÓGICO DEL AGUA Y OTRAS MUESTRAS. Objetivos Al finalizar este ejercicio el alumno será capaz de: Explicar el fundamento de la técnicas
TÉCNICAS PARA LA ENUMERACIÓN DE MICROORGANISMOS. ANÁLISIS MICROBIOLÓGICO DEL AGUA Y OTRAS MUESTRAS. Objetivos Al finalizar este ejercicio el alumno será capaz de: Explicar el fundamento de la técnicas
PROCEDIMIENTO DETECCIÓN Y ENUMERACIÓN POR NUMERO MAS PROBABLE (NMP) CON ETAPA DE PRE- ENRIQUECIMIENTO DE ENTEROBACTERIACEAE EN ALIMENTOS
 Página 1 de 5 1. OBJETIVO Estimar el número de Enterobacteriaceae presentes en el alimento. 2. CAMPO DE APLICACIÓN Y ALCANCE Aplicar este procedimiento a todas las muestras de alimentos de consumo humano
Página 1 de 5 1. OBJETIVO Estimar el número de Enterobacteriaceae presentes en el alimento. 2. CAMPO DE APLICACIÓN Y ALCANCE Aplicar este procedimiento a todas las muestras de alimentos de consumo humano
Unidad 3. Estudio de cultivos bacterianos puros Práctica 4. Técnicas de siembra y cultivo de bacterias
 Unidad 3. Estudio de cultivos bacterianos puros Práctica 4. Técnicas de siembra y cultivo de bacterias Objetivos Aplicar las diferentes técnicas de siembra que se emplean para el estudio y asilamiento
Unidad 3. Estudio de cultivos bacterianos puros Práctica 4. Técnicas de siembra y cultivo de bacterias Objetivos Aplicar las diferentes técnicas de siembra que se emplean para el estudio y asilamiento
Objetivos Describir los efectos de diferentes factores físicos en el crecimiento de bacterias.
 Unidad 8. Condiciones ambientales para el desarrollo, inhibición y destrucción de microorganismos. Práctica 8. Efecto de los factores ambientales y químicos Objetivos Describir los efectos de diferentes
Unidad 8. Condiciones ambientales para el desarrollo, inhibición y destrucción de microorganismos. Práctica 8. Efecto de los factores ambientales y químicos Objetivos Describir los efectos de diferentes
1ª sesión. Unidad 2. Técnicas básicas de microbiología. Práctica 2. Esterilización y preparación de medios de cultivo
 Unidad 2. Técnicas básicas de microbiología. Práctica 2. Esterilización y preparación de medios de cultivo Objetivos Explicar el concepto de esterilización y su utilidad en microbiología. Preparar correctamente
Unidad 2. Técnicas básicas de microbiología. Práctica 2. Esterilización y preparación de medios de cultivo Objetivos Explicar el concepto de esterilización y su utilidad en microbiología. Preparar correctamente
AISLAMIENTO DE MICROORGANISMOS
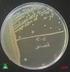 PRÁCTICA5 AISLAMIENTO DE MICROORGANISMOS Introducción En la naturaleza, la mayoría de los microorganismos no se encuentran aislados, sino integrados en poblaciones mixtas. Para llevar a cabo el estudio
PRÁCTICA5 AISLAMIENTO DE MICROORGANISMOS Introducción En la naturaleza, la mayoría de los microorganismos no se encuentran aislados, sino integrados en poblaciones mixtas. Para llevar a cabo el estudio
ENUMERACIÓN DE ENTEROBACTERIACEAE EN ALIMENTOS SIN RESUSCITACIÓN. TÉCNICA RECUENTO EN PLACA
 PRT-712.03-040 Página 1 de 6 1. OBJETIVO Determinar el número de Enterobactereaceae presentes en un alimento. 2. CAMPO DE APLICACIÓN Y ALCANCE Aplicar este procedimiento a todas las muestras de alimentos
PRT-712.03-040 Página 1 de 6 1. OBJETIVO Determinar el número de Enterobactereaceae presentes en un alimento. 2. CAMPO DE APLICACIÓN Y ALCANCE Aplicar este procedimiento a todas las muestras de alimentos
- Mencionar las Normas de Bioseguridad y precauciones necesarias para trabajar en el laboratorio microbiológico.
 Microbiología General e Inmunología Año 2012 Trabajo Práctico Nº1 Objetivos: Que el alumno sea capaz de: - Mencionar las Normas de Bioseguridad y precauciones necesarias para trabajar en el laboratorio
Microbiología General e Inmunología Año 2012 Trabajo Práctico Nº1 Objetivos: Que el alumno sea capaz de: - Mencionar las Normas de Bioseguridad y precauciones necesarias para trabajar en el laboratorio
1ª PRÁCTICA DE MICROBIOLOGÍA:
 1ª PRÁCTICA DE MICROBIOLOGÍA: INTRODUCCIÓN A LAS TÉCNICAS DE CULTIVO EN MICROBIOLOGÍA (O COMO HACER VISIBLES ORGANISMOS INVISIBLES) INTRODUCCIÓN El objetivo de esta práctica es aislar y observar algunos
1ª PRÁCTICA DE MICROBIOLOGÍA: INTRODUCCIÓN A LAS TÉCNICAS DE CULTIVO EN MICROBIOLOGÍA (O COMO HACER VISIBLES ORGANISMOS INVISIBLES) INTRODUCCIÓN El objetivo de esta práctica es aislar y observar algunos
Objetivos. S Determinar la presencia de bacterias coliformes en una muestra de agua
 Análisis del agua S Objetivos S Determinar la presencia de bacterias coliformes en una muestra de agua Introducción S Las tres pruebas básicas para determinar la presencia de bacterias coliformes (asociada
Análisis del agua S Objetivos S Determinar la presencia de bacterias coliformes en una muestra de agua Introducción S Las tres pruebas básicas para determinar la presencia de bacterias coliformes (asociada
Protocolos Laboratorio de Microbiología Experimental 2014 PREPARACIONES MICROBIOLÓGICAS
 PREPARACIONES MICROBIOLÓGICAS Objetivos PREPARACIONES HÚMEDAS (EN FRESCO) Al finalizar esta práctica el alumno será capaz de: Realizar diferentes preparaciones microbiológicas a partir de muestras naturales.
PREPARACIONES MICROBIOLÓGICAS Objetivos PREPARACIONES HÚMEDAS (EN FRESCO) Al finalizar esta práctica el alumno será capaz de: Realizar diferentes preparaciones microbiológicas a partir de muestras naturales.
Cultivo Puro. Técnicas de aislamiento Mantenimiento y preservación de cultivos puros Morfología macroscópica Morfología microscópica
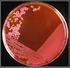 Cultivo Puro Técnicas de aislamiento Mantenimiento y preservación de cultivos puros Morfología macroscópica Morfología microscópica Definición El cultivo puro representa las condiciones artificiales para
Cultivo Puro Técnicas de aislamiento Mantenimiento y preservación de cultivos puros Morfología macroscópica Morfología microscópica Definición El cultivo puro representa las condiciones artificiales para
NMP PARA LA DETERMINACION DE COLIFORMESY COLIFORMES FECALES EN AGUAS
 PRT-712.03-005 Página 1 de 6 1. OBJETIVO Este método es utilizado para estimar la densidad de bacterias del grupo coliformes y conocer la calidad sanitaria en aguas crudas 2. CAMPO DE APLICACIÓN Y ALCANCE
PRT-712.03-005 Página 1 de 6 1. OBJETIVO Este método es utilizado para estimar la densidad de bacterias del grupo coliformes y conocer la calidad sanitaria en aguas crudas 2. CAMPO DE APLICACIÓN Y ALCANCE
Unidad 2. Técnicas básicas de microbiología Práctica 3. Preparaciones Microbiológicas
 Unidad 2. Técnicas básicas de microbiología Práctica 3. Preparaciones Microbiológicas Objetivos Realizar diferentes preparaciones microbiológicas a partir de muestras naturales y cultivos puros. Describir
Unidad 2. Técnicas básicas de microbiología Práctica 3. Preparaciones Microbiológicas Objetivos Realizar diferentes preparaciones microbiológicas a partir de muestras naturales y cultivos puros. Describir
Unidad 2. Técnicas básicas de microbiología Práctica 5. Preparaciones Microbiológicas
 Unidad 2. Técnicas básicas de microbiología Práctica 5. Preparaciones Microbiológicas Objetivos Realizar diferentes preparaciones microbiológicas a partir de muestras naturales y cultivos puros. Describir
Unidad 2. Técnicas básicas de microbiología Práctica 5. Preparaciones Microbiológicas Objetivos Realizar diferentes preparaciones microbiológicas a partir de muestras naturales y cultivos puros. Describir
UNIVERSIDAD AUTONOMA DE TAMAULIPAS
 R-RS-01-25-03 UNIVERSIDAD AUTONOMA DE TAMAULIPAS UNIDAD ACADÉMICA MULTIDISCIPLINARIA REYNOSA-AZTLÁN NOMBRE DE LA CARRERA LICENCIADO EN NUTRICION Y CIENCIA DE LOS ALIMENTOS NOMBRE DE LA ASIGNATURA LABORATORIO
R-RS-01-25-03 UNIVERSIDAD AUTONOMA DE TAMAULIPAS UNIDAD ACADÉMICA MULTIDISCIPLINARIA REYNOSA-AZTLÁN NOMBRE DE LA CARRERA LICENCIADO EN NUTRICION Y CIENCIA DE LOS ALIMENTOS NOMBRE DE LA ASIGNATURA LABORATORIO
PRÁCTICA 6.1 Nutrición Microbiana y Requerimientos de Oxígeno
 PRÁCTICA 6.1 Nutrición Microbiana y Requerimientos de Oxígeno Objetivos Determinar las características nutricionales de diferentes microorganismos considerando las fuentes de carbono, energía y nitrógeno.
PRÁCTICA 6.1 Nutrición Microbiana y Requerimientos de Oxígeno Objetivos Determinar las características nutricionales de diferentes microorganismos considerando las fuentes de carbono, energía y nitrógeno.
PRACTICA Núm. 20 DETERMINACION DE CLOSTRIDIOS SULFITO REDUCTORES EN AGUA
 PRACTICA Núm. 20 DETERMINACION DE CLOSTRIDIOS SULFITO REDUCTORES EN AGUA I. OBJETIVO Determinar la presencia de Clostridios sulfito reductores en agua por el método de recuento en tubo. II. INTRODUCCION
PRACTICA Núm. 20 DETERMINACION DE CLOSTRIDIOS SULFITO REDUCTORES EN AGUA I. OBJETIVO Determinar la presencia de Clostridios sulfito reductores en agua por el método de recuento en tubo. II. INTRODUCCION
RECOPILADO POR: EL PROGRAMA UNIVERSITARIO DE ALIMENTOS
 NMX-F-187-1978. DETERMINACIÓN DEL NÚMERO MÁS PROBABLE DE GÉRMENES. METHOD OF TEST FOR GERMS MOST PROBABLE NUMBER. NORMAS MEXICANAS. DIRECCIÓN GENERAL DE NORMAS. PREFACIO En la elaboración de esta Norma
NMX-F-187-1978. DETERMINACIÓN DEL NÚMERO MÁS PROBABLE DE GÉRMENES. METHOD OF TEST FOR GERMS MOST PROBABLE NUMBER. NORMAS MEXICANAS. DIRECCIÓN GENERAL DE NORMAS. PREFACIO En la elaboración de esta Norma
UNIVERSIDAD DE CIENCIAS Y ARTES DE CHIAPAS
 1 FACULTAD DE CIENCIAS DE LA NUTRICIÓN Y ALIMENTOS LICENCIATURA EN NUTRIOLOGÍA MANUAL DE PRÁCTICAS PARA LA EXPERIENCIA ACADÉMICA MICROBIOLOGÍA DE ALIMENTOS ELABORO: M. EN C. GILBER VELA GUTIÉRREZ Y M.
1 FACULTAD DE CIENCIAS DE LA NUTRICIÓN Y ALIMENTOS LICENCIATURA EN NUTRIOLOGÍA MANUAL DE PRÁCTICAS PARA LA EXPERIENCIA ACADÉMICA MICROBIOLOGÍA DE ALIMENTOS ELABORO: M. EN C. GILBER VELA GUTIÉRREZ Y M.
PREPARACIONES Y TINCIONES
 PREPARACIONES Y TINCIONES PREPARACIONES En fresco Temporales: Microcultivos de hongos, preparaciones de tejidos Fijas: Gram, Ziehl Nielsen, Sheaffer y fulton, SEM, TEM, naranja de acridina. CONTRASTE DE
PREPARACIONES Y TINCIONES PREPARACIONES En fresco Temporales: Microcultivos de hongos, preparaciones de tejidos Fijas: Gram, Ziehl Nielsen, Sheaffer y fulton, SEM, TEM, naranja de acridina. CONTRASTE DE
UNIVERSIDAD NACIONAL AUTÓNOMA DE MÉXICO FACULTAD DE QUÍMICA Departamento de Biología PROTOCOLO DE PRÁCTICAS MICROBIOLOGÍA EXPERIMENTAL
 UNIVERSIDAD NACIONAL AUTÓNOMA DE MÉXICO FACULTAD DE QUÍMICA Departamento de Biología PROTOCOLO DE PRÁCTICAS MICROBIOLOGÍA EXPERIMENTAL Semestre 2014-1 INDICE Página UNIDAD I. INTRODUCCIÓN A LA MICROBIOLOGÍA
UNIVERSIDAD NACIONAL AUTÓNOMA DE MÉXICO FACULTAD DE QUÍMICA Departamento de Biología PROTOCOLO DE PRÁCTICAS MICROBIOLOGÍA EXPERIMENTAL Semestre 2014-1 INDICE Página UNIDAD I. INTRODUCCIÓN A LA MICROBIOLOGÍA
UNIVERSIDAD DE EL SALVADOR FACULTAD DE QUÍMICA Y FARMACIA
 1 UNIVERSIDAD DE EL SALVADOR MANUAL PARA LA CONSERVACIÓN DE CEPAS BACTERIANAS DE TRABAJO SAN SALVADOR, EL SALVADOR, CENTRO AMERICA UNIVERSIDAD DE EL SALVADOR DEPARTAMENTO DE BIOQUIMICA Y Código CONTAMINACIÓN
1 UNIVERSIDAD DE EL SALVADOR MANUAL PARA LA CONSERVACIÓN DE CEPAS BACTERIANAS DE TRABAJO SAN SALVADOR, EL SALVADOR, CENTRO AMERICA UNIVERSIDAD DE EL SALVADOR DEPARTAMENTO DE BIOQUIMICA Y Código CONTAMINACIÓN
UNIVERSIDAD NACIONAL AUTÓNOMA DE MÉXICO FACULTAD DE QUÍMICA Departamento de Biología PROTOCOLO DE PRÁCTICAS MICROBIOLOGÍA EXPERIMENTAL
 UNIVERSIDAD NACIONAL AUTÓNOMA DE MÉXICO FACULTAD DE QUÍMICA Departamento de Biología PROTOCOLO DE PRÁCTICAS MICROBIOLOGÍA EXPERIMENTAL 2012 INDICE Página UNIDAD I. INTRODUCCIÓN A LA MICROBIOLOGÍA PRÁCTICA
UNIVERSIDAD NACIONAL AUTÓNOMA DE MÉXICO FACULTAD DE QUÍMICA Departamento de Biología PROTOCOLO DE PRÁCTICAS MICROBIOLOGÍA EXPERIMENTAL 2012 INDICE Página UNIDAD I. INTRODUCCIÓN A LA MICROBIOLOGÍA PRÁCTICA
BIORREACTRES. Estudios básicos y aplicados sobre procesos de fermentación
 BIORREACTRES Ing. en Alimentos Estudios básicos y aplicados sobre procesos de fermentación Mg. Anahí V. Cuellas Docente investigadora Universidad Nacional de Quilmes TRABAJO PRACTICO Obtención de enzimas
BIORREACTRES Ing. en Alimentos Estudios básicos y aplicados sobre procesos de fermentación Mg. Anahí V. Cuellas Docente investigadora Universidad Nacional de Quilmes TRABAJO PRACTICO Obtención de enzimas
UNIVERSIDAD AUTÓNOMA CHAPINGO DEPARTAMENTO DE INGENIERÍA AGROINDUSTRIAL FICHA CURRICULAR
 UNIVERSIDAD AUTÓNOMA CHAPINGO DEPARTAMENTO DE INGENIERÍA AGROINDUSTRIAL FICHA CURRICULAR 1. Datos Generales: Departamento Nombre del Programa Licenciatura Línea curricular Tecnológica Asignatura Biología
UNIVERSIDAD AUTÓNOMA CHAPINGO DEPARTAMENTO DE INGENIERÍA AGROINDUSTRIAL FICHA CURRICULAR 1. Datos Generales: Departamento Nombre del Programa Licenciatura Línea curricular Tecnológica Asignatura Biología
PROCEDIMIENTO RECUENTO MOHOS Y LEVADURAS EN ALIMENTOS NORMA ISO 7954
 PRT- 712.02-031 Página 1 de 9 1. OBJETIVO Conocer el número de Mohos y Levaduras que contiene un alimento. 2. CAMPO DE APLICACIÓN Y ALCANCE Este procedimiento se aplica a todos los alimentos de consumos
PRT- 712.02-031 Página 1 de 9 1. OBJETIVO Conocer el número de Mohos y Levaduras que contiene un alimento. 2. CAMPO DE APLICACIÓN Y ALCANCE Este procedimiento se aplica a todos los alimentos de consumos
PROCEDIMIENTO TECNICA NMP STAPHYLOCOCCUS AUREUS EN ALIMENTOS. BAM ONLINE 2001
 PRT-712.02-025 Página 1 de 9 1. OBJETIVO Estimar la densidad de bacterias S. aureus en matrices de alimento o agua como indicador sanitario 2. CAMPO DE APLICACIÓN Y ALCANCE El método de NMP es recomendado
PRT-712.02-025 Página 1 de 9 1. OBJETIVO Estimar la densidad de bacterias S. aureus en matrices de alimento o agua como indicador sanitario 2. CAMPO DE APLICACIÓN Y ALCANCE El método de NMP es recomendado
Trabajo Práctico Nº 2
 Introducción Objetivo Fundamento Trabajo Práctico Nº 2 MÉTODO DE LA MEMBRANA FILTRANTE PARA EL ANÁLISIS MICROBIOLÓGICO DEL AGUA Materiales Procedimiento Resultados Conclusiones Actividades Adicionales
Introducción Objetivo Fundamento Trabajo Práctico Nº 2 MÉTODO DE LA MEMBRANA FILTRANTE PARA EL ANÁLISIS MICROBIOLÓGICO DEL AGUA Materiales Procedimiento Resultados Conclusiones Actividades Adicionales
Clostridium perfringens
 Clostridium perfringens Introducción Cuando se lanza un producto alimentario al mercado se deben tener en cuenta varios parámetros que le otorgan calidad al producto, uno de ellos es la inocuidad. Los
Clostridium perfringens Introducción Cuando se lanza un producto alimentario al mercado se deben tener en cuenta varios parámetros que le otorgan calidad al producto, uno de ellos es la inocuidad. Los
PRÁCTICO N 4. Análisis de fertilidad del suelo
 PRÁCTICO N 4 Análisis de fertilidad del suelo OBJETIVOS Conocer las técnicas actuales de recuento de microorganismos. Conocer la importancia del monitoreo de abundancia, actividad y diversidad de los microorganismos
PRÁCTICO N 4 Análisis de fertilidad del suelo OBJETIVOS Conocer las técnicas actuales de recuento de microorganismos. Conocer la importancia del monitoreo de abundancia, actividad y diversidad de los microorganismos
TEMA 10. DIAGNÓSTICO DE LABORATORIO DE LAS ENFERMEDADES INFECCIOSAS BUCODENTALES
 TEMA 10. DIAGNÓSTICO DE LABORATORIO DE LAS ENFERMEDADES INFECCIOSAS BUCODENTALES 1. Objetivo del diagnóstico microbiológico 2. Toma de muestra 3. Diagnóstico directo - bacterias - hongos - protozoos -
TEMA 10. DIAGNÓSTICO DE LABORATORIO DE LAS ENFERMEDADES INFECCIOSAS BUCODENTALES 1. Objetivo del diagnóstico microbiológico 2. Toma de muestra 3. Diagnóstico directo - bacterias - hongos - protozoos -
Laboratorio Nacional de Salud Pública
 1. Tinción de Gram 2. Objeto y campo de aplicación La técnica de tinción de Gram se utiliza para la tinción de bacterias, levaduras y actinomicetos aerobios. Este procedimiento operativo estándar es aplicable
1. Tinción de Gram 2. Objeto y campo de aplicación La técnica de tinción de Gram se utiliza para la tinción de bacterias, levaduras y actinomicetos aerobios. Este procedimiento operativo estándar es aplicable
PRÁCTICA 2.2 Preparaciones microbiológicas
 PRÁCTICA 2.2 Preparaciones microbiológicas Objetivos Al finalizar esta práctica el alumno será capaz de: Realizar diferentes preparaciones microbiológicas a partir de muestras naturales y cultivos puros.
PRÁCTICA 2.2 Preparaciones microbiológicas Objetivos Al finalizar esta práctica el alumno será capaz de: Realizar diferentes preparaciones microbiológicas a partir de muestras naturales y cultivos puros.
Dr. Oscar Gutiérrez Coronado Microbiologia Práctica No. 1 Preparación y esterilización de materiales y medios de cultivo
 Dr. Oscar Gutiérrez Coronado Microbiologia Práctica No. 1 Preparación y esterilización de materiales y medios de cultivo Objetivos. Que el alumno conozca los principios generales de las técnicas de esterilización
Dr. Oscar Gutiérrez Coronado Microbiologia Práctica No. 1 Preparación y esterilización de materiales y medios de cultivo Objetivos. Que el alumno conozca los principios generales de las técnicas de esterilización
MANUAL DE OPERACIONES. DIRECCIÓN DE INVESTIGACIÓN Fecha: JUN 15 SUBDIRECCIÓN DE INVESTIGACIÓN BIOMÉDICA MANUAL DE TINCIONES
 A Hoja: de 0 MANUAL DE TINCIONES Elaboró: Autorizó: Puesto QUÍMICO JEFE DE LABORATORIO Firma Hoja: 2 de 0. Propósito Establecer las técnicas y condiciones para la realización de tinciones utilizadas en
A Hoja: de 0 MANUAL DE TINCIONES Elaboró: Autorizó: Puesto QUÍMICO JEFE DE LABORATORIO Firma Hoja: 2 de 0. Propósito Establecer las técnicas y condiciones para la realización de tinciones utilizadas en
FICHAS DE PRÁCTICAS DE BIOLOGÍA 4º ESO BIOLOGÍA
 FICHAS DE PRÁCTICAS DE BIOLOGÍA 4º ESO BIOLOGÍA UNIDAD DIDÁCTICA : CÉLULAS Y TEJIDOS 01.- Células animales y vegetales Duración Estimada: 1h 40 min Capacidad Terminal Observación de células animales y
FICHAS DE PRÁCTICAS DE BIOLOGÍA 4º ESO BIOLOGÍA UNIDAD DIDÁCTICA : CÉLULAS Y TEJIDOS 01.- Células animales y vegetales Duración Estimada: 1h 40 min Capacidad Terminal Observación de células animales y
i) EVALUACIÓN DE LA DIVERSIDAD MICROBIANA EN UNA MUESTRA NATURAL ii) PRODUCCIÓN DE ANTIBIÓTICOS A PARTIR DE Streptomyces sp.
 Módulo 5: Microorganismos en acción Docente Responsable: Erina Petrera La idea de este módulo es trabajar sobre dos temas: i) EVALUACIÓN DE LA DIVERSIDAD MICROBIANA EN UNA MUESTRA NATURAL ii) PRODUCCIÓN
Módulo 5: Microorganismos en acción Docente Responsable: Erina Petrera La idea de este módulo es trabajar sobre dos temas: i) EVALUACIÓN DE LA DIVERSIDAD MICROBIANA EN UNA MUESTRA NATURAL ii) PRODUCCIÓN
UNIVERSIDAD DE CIENCIAS Y ARTES DE CHIAPAS
 FACULTAD DE CIENCIAS DE LA NUTRICIÓN Y ALIMENTOS LICENCIATURA EN NUTRIOLOGÍA MANUAL DE PRÁCTICAS PARA LA EXPERIENCIA ACADÉMICA MICROBIOLOGÍA Y PARASITOLOGÍA ELABORO: Q.F.B. MARÍA DOLORES TOLEDO MEZA ACTUALIZÓ:
FACULTAD DE CIENCIAS DE LA NUTRICIÓN Y ALIMENTOS LICENCIATURA EN NUTRIOLOGÍA MANUAL DE PRÁCTICAS PARA LA EXPERIENCIA ACADÉMICA MICROBIOLOGÍA Y PARASITOLOGÍA ELABORO: Q.F.B. MARÍA DOLORES TOLEDO MEZA ACTUALIZÓ:
PROCEDIMIENTO TECNICA DE COAGULASA EN TUBO PRT
 Página 1 de 7 1. OBJETIVO Comprobar la facultad de las unidades formadoras de colonias de S. aureus presentes en una muestra de alimento, de coagular el plasma de conejo por acción de la enzima coagulasa
Página 1 de 7 1. OBJETIVO Comprobar la facultad de las unidades formadoras de colonias de S. aureus presentes en una muestra de alimento, de coagular el plasma de conejo por acción de la enzima coagulasa
PRÁCTICA 2.3 Esterilización y Preparación de Medios de Cultivo (1ª sesión)
 Objetivos PRÁCTICA 2.3 Esterilización y Preparación de Medios de Cultivo (1ª sesión) Al finalizar este ejercicio el alumno será capaz de: Explicar el concepto de esterilización y su aplicación en microbiología.
Objetivos PRÁCTICA 2.3 Esterilización y Preparación de Medios de Cultivo (1ª sesión) Al finalizar este ejercicio el alumno será capaz de: Explicar el concepto de esterilización y su aplicación en microbiología.
2. Observación de hongos de interés industrial
 2. Observación de hongos de interés industrial En esta práctica se realizarán observaciones en fresco de varios hongos de interés industrial. 2.1 Preparaciones para el estudio microscópico de los aislados
2. Observación de hongos de interés industrial En esta práctica se realizarán observaciones en fresco de varios hongos de interés industrial. 2.1 Preparaciones para el estudio microscópico de los aislados
PRÁCTICA No. 4 Métodos de cultivo y descripción morfológica de hongos Introducción
 PRÁCTICA No. 4 Métodos de cultivo y descripción morfológica de hongos Objetivos. Que el alumno aprenda las técnicas de cultivo y manipulación de diferentes tipos de hongos. Que el estudiante conozca las
PRÁCTICA No. 4 Métodos de cultivo y descripción morfológica de hongos Objetivos. Que el alumno aprenda las técnicas de cultivo y manipulación de diferentes tipos de hongos. Que el estudiante conozca las
UNIVERSIDAD DE PUERTO RICO EN HUMACAO DEPARTAMENTO DE BIOLOGÍA PRONTUARIO DEL LABORATORIO DE MICROBIOLOGÍA GENERAL BIOL 3707
 UNIVERSIDAD DE PUERTO RICO EN HUMACAO DEPARTAMENTO DE BIOLOGÍA PRONTUARIO DEL LABORATORIO DE MICROBIOLOGÍA GENERAL BIOL 3707 Actualizado por: DR. HÉCTOR L. AYALA DEL RÍO 2005 UPR-H Departamento de Biología-BIOL
UNIVERSIDAD DE PUERTO RICO EN HUMACAO DEPARTAMENTO DE BIOLOGÍA PRONTUARIO DEL LABORATORIO DE MICROBIOLOGÍA GENERAL BIOL 3707 Actualizado por: DR. HÉCTOR L. AYALA DEL RÍO 2005 UPR-H Departamento de Biología-BIOL
PRACTICA Núm. 6 TINCION DE FLAGELOS BACTERIANOS POR EL METODO DE LEIFSON
 PRACTICA Núm. 6 TINCION DE FLAGELOS BACTERIANOS POR EL METODO DE LEIFSON I. OBJETIVO Demostrar la presencia de flagelos mediante tinción y observar la movilidad que presentan algunas bacterias diferenciándola
PRACTICA Núm. 6 TINCION DE FLAGELOS BACTERIANOS POR EL METODO DE LEIFSON I. OBJETIVO Demostrar la presencia de flagelos mediante tinción y observar la movilidad que presentan algunas bacterias diferenciándola
Asignaturas antecedentes y subsecuentes
 PROGRAMA DE ESTUDIOS Microbiología General Área a la que pertenece: AREA SUSTANTIVA PROFESIONAL Horas teóricas: 3 Horas practicas: 3 Créditos: 9 Clave: F0219 Ninguna. Asignaturas antecedentes y subsecuentes
PROGRAMA DE ESTUDIOS Microbiología General Área a la que pertenece: AREA SUSTANTIVA PROFESIONAL Horas teóricas: 3 Horas practicas: 3 Créditos: 9 Clave: F0219 Ninguna. Asignaturas antecedentes y subsecuentes
PRÁCTICA 8. CONDICIONES AMBIENTALES PARA EL DESARROLLO, INHIBICIÓN Y DESTRUCCIÓN DE LOS MICROORGANISMOS
 PRÁCTICA 8. CONDICIONES AMBIENTALES PARA EL DESARROLLO, INHIBICIÓN Y DESTRUCCIÓN DE LOS MICROORGANISMOS Objetivos Al finalizar este ejercicio el alumno será capaz de: Explicar el efecto de factores físicos
PRÁCTICA 8. CONDICIONES AMBIENTALES PARA EL DESARROLLO, INHIBICIÓN Y DESTRUCCIÓN DE LOS MICROORGANISMOS Objetivos Al finalizar este ejercicio el alumno será capaz de: Explicar el efecto de factores físicos
PRÁCTICAS DEL LABORATORIO DE MICROBIOLOGÍA: BACTERIOLOGÍA Y MICOLOGÍA
 PRÁCTICAS DEL LABORATORIO DE MICROBIOLOGÍA: BACTERIOLOGÍA Y MICOLOGÍA Mª PAZ MERINO JIMÉNEZ MIREIA LLINARES MARCELO PRÁCTICAS DEL LABORATORIO DE MICROBIOLOGÍA: BACTERIOLOGÍA Y MICOLOGÍA A mi padre. M.
PRÁCTICAS DEL LABORATORIO DE MICROBIOLOGÍA: BACTERIOLOGÍA Y MICOLOGÍA Mª PAZ MERINO JIMÉNEZ MIREIA LLINARES MARCELO PRÁCTICAS DEL LABORATORIO DE MICROBIOLOGÍA: BACTERIOLOGÍA Y MICOLOGÍA A mi padre. M.
UNIVERSIDAD AUTÓNOMA DE CHIHUAHUA FACULTAD DE CIENCIAS QUÍMICAS. Dr. Iván Salmerón María A. Anaya Castro 4 de abril de 2011
 UNIVERSIDAD AUTÓNOMA DE CHIHUAHUA FACULTAD DE CIENCIAS QUÍMICAS Dr. Iván Salmerón María A. Anaya Castro 4 de abril de 2011 LECHE PASTEURIZADA DE VACA Leche de vaca para consumo humano, producto proveniente
UNIVERSIDAD AUTÓNOMA DE CHIHUAHUA FACULTAD DE CIENCIAS QUÍMICAS Dr. Iván Salmerón María A. Anaya Castro 4 de abril de 2011 LECHE PASTEURIZADA DE VACA Leche de vaca para consumo humano, producto proveniente
Tema 4.- Técnicas de siembra y aislamiento
 Tema 4.- Técnicas de siembra y aislamiento La siembra consiste en tomar con el asa de platino, previamente flameado, o con hisopo estéril una pequeña cantidad de muestra a estudiar y repartirla por toda
Tema 4.- Técnicas de siembra y aislamiento La siembra consiste en tomar con el asa de platino, previamente flameado, o con hisopo estéril una pequeña cantidad de muestra a estudiar y repartirla por toda
Ciclo de Introducción a las ciencias de la salud, UC Introducción a la biología celular y molecular.
 Ciclo de Introducción a las ciencias de la salud, 2017. UC Introducción a la biología celular y molecular. Unidad 3: MICROORGANISMOS Y SALUD HUMANA (Depto. Bacteriología y Virología). TALLER 9: La célula
Ciclo de Introducción a las ciencias de la salud, 2017. UC Introducción a la biología celular y molecular. Unidad 3: MICROORGANISMOS Y SALUD HUMANA (Depto. Bacteriología y Virología). TALLER 9: La célula
GUÍA OBSERVACIÓN DE MICROORGANISMOS Y USO DE TINCIONES
 ESCUELA DE SALUD GUÍA OBSERVACIÓN DE MICROORGANISMOS Y USO DE TINCIONES DIRIGIDO A ALUMNOS DE: Técnico de laboratorio Clínico y Banco de Sangre Técnico de Enfermería Técnico de Radiodiagnóstico y Radioterapia
ESCUELA DE SALUD GUÍA OBSERVACIÓN DE MICROORGANISMOS Y USO DE TINCIONES DIRIGIDO A ALUMNOS DE: Técnico de laboratorio Clínico y Banco de Sangre Técnico de Enfermería Técnico de Radiodiagnóstico y Radioterapia
TRANSPORTE A TRAVÉS DE LA MEMBRANA PRÁCTICA UNIDAD TEMÁTICA 9
 TRANSPORTE A TRAVÉS DE LA MEMBRANA PRÁCTICA UNIDAD TEMÁTICA 9 PERMEABILIDAD DIFERENCIAL DE LA MEMBRANA I. INTRODUCCIÓN. Las membranas que rodean a las células y organelos, poseen permeabilidad diferencial,
TRANSPORTE A TRAVÉS DE LA MEMBRANA PRÁCTICA UNIDAD TEMÁTICA 9 PERMEABILIDAD DIFERENCIAL DE LA MEMBRANA I. INTRODUCCIÓN. Las membranas que rodean a las células y organelos, poseen permeabilidad diferencial,
PRACTICA Núm. 18 INVESTIGACION DE COLIFORMES TOTALES Y FECALES EN AGUA RESIDUAL
 I. OBJETIVO PRACTICA Núm. 18 INVESTIGACION DE COLIFORMES TOTALES Y FECALES EN AGUA RESIDUAL Determinar la presencia de coliformes totales y fecales en agua residual por el método del Número Más Probable,
I. OBJETIVO PRACTICA Núm. 18 INVESTIGACION DE COLIFORMES TOTALES Y FECALES EN AGUA RESIDUAL Determinar la presencia de coliformes totales y fecales en agua residual por el método del Número Más Probable,
TRANSFERENCIAS ASÉPTICAS
 Introducción Objetivo Procedimiento Trabajo Práctico Nº 3 TRANSFERENCIAS ASÉPTICAS Resultados Observaciones Bibliografía INTRODUCCIÓN La inoculación de medios de cultivo y la manipulación de cultivos microbianos
Introducción Objetivo Procedimiento Trabajo Práctico Nº 3 TRANSFERENCIAS ASÉPTICAS Resultados Observaciones Bibliografía INTRODUCCIÓN La inoculación de medios de cultivo y la manipulación de cultivos microbianos
MANUAL DE PREPARACIÓN DE MEDIOS DE CULTIVO
 Rev. 02 Hoja: 1 de 14 MANUAL DE PREPARACIÓN DE MEDIOS DE Elaboró: Revisó: Autorizó: Puesto QUÍMICO JEFE DEL LABORATORIO SUBDIRECTOR DE INVESTIGACIÓN Firma Hoja: 2 de 14 1. Propósito Definir y describir
Rev. 02 Hoja: 1 de 14 MANUAL DE PREPARACIÓN DE MEDIOS DE Elaboró: Revisó: Autorizó: Puesto QUÍMICO JEFE DEL LABORATORIO SUBDIRECTOR DE INVESTIGACIÓN Firma Hoja: 2 de 14 1. Propósito Definir y describir
Universidad Autónoma Metropolitana- Iztapalapa. Academia de Microbiología, Departamento de Biotecnología
 Universidad Autónoma Metropolitana- Iztapalapa MANUAL DE PRÁCTICAS DEL LABORATORIO DE MICROBIOLOGIA GENERAL Academia de Microbiología, Departamento de Biotecnología Participantes: Dra. María de los Angeles
Universidad Autónoma Metropolitana- Iztapalapa MANUAL DE PRÁCTICAS DEL LABORATORIO DE MICROBIOLOGIA GENERAL Academia de Microbiología, Departamento de Biotecnología Participantes: Dra. María de los Angeles
PROCEDIMIENTO ENUMERACION DE LEVADURAS Y MOHOS EN ALIMENTOS BAM ONLINE
 PRT-712.02-048 Página 1 de 7 1. OBJETIVO Detectar el número de unidades formadoras de colonias (ufc) de levaduras y de mohos en el alimento 2. CAMPO DE APLICACIÓN Y ALCANCE Aplicar este procedimiento a
PRT-712.02-048 Página 1 de 7 1. OBJETIVO Detectar el número de unidades formadoras de colonias (ufc) de levaduras y de mohos en el alimento 2. CAMPO DE APLICACIÓN Y ALCANCE Aplicar este procedimiento a
PRÁCTICAS DE MICROBIOLOGÍA CLÍNICA (CURSO )
 PRÁCTICAS DE MICROBIOLOGÍA CLÍNICA (CURSO 2012 2013) PRÁCTICAS A REALIZAR ANÁLISIS CUALITATIVO DE ORINA PRUEBA DE BAUER KIRBY (ANTIBIOGRAMA) PRUEBA DE EPSILON (DETERMINACIÓN DE LA CMI) ANÁLISIS CUALITATIVO
PRÁCTICAS DE MICROBIOLOGÍA CLÍNICA (CURSO 2012 2013) PRÁCTICAS A REALIZAR ANÁLISIS CUALITATIVO DE ORINA PRUEBA DE BAUER KIRBY (ANTIBIOGRAMA) PRUEBA DE EPSILON (DETERMINACIÓN DE LA CMI) ANÁLISIS CUALITATIVO
BUENAS PRÁCTICAS DE MUESTREO PARA LA RECOLECCION DE AGUA PARA EL ANALISIS MICROBIOLOGICO
 BUENAS PRÁCTICAS DE MUESTREO PARA LA RECOLECCION DE AGUA PARA EL ANALISIS MICROBIOLOGICO OBJETIVO Asegurar las condiciones de las tareas de toma de muestra de aguas a las que luego se les realizará análisis
BUENAS PRÁCTICAS DE MUESTREO PARA LA RECOLECCION DE AGUA PARA EL ANALISIS MICROBIOLOGICO OBJETIVO Asegurar las condiciones de las tareas de toma de muestra de aguas a las que luego se les realizará análisis
APÉNDICE G. Identificación bioquímica de enterobacterias por el sistema API 20E
 APÉNDICE G Identificación bioquímica de enterobacterias por el sistema API 20E OBJETIVO: - Establecer la metodología en la identificación de enterobacterias por medio de pruebas bioquímicas estandarizadas
APÉNDICE G Identificación bioquímica de enterobacterias por el sistema API 20E OBJETIVO: - Establecer la metodología en la identificación de enterobacterias por medio de pruebas bioquímicas estandarizadas
OBJETIVOS CRECIMIENTO MICROBIANO EN MEDIO SÓLIDO
 UNIVERSIDAD NACIONAL EXPERIMENTAL FRANCISCO DE MIRANDA PROGRAMA: CIENCIAS AMBIENTALES ÁREA: AGRO Y MAR CÁTEDRA: Microbiología e Inmunología Veterinaria PROF: JOSÉ ARAUJO Actividad Prática 3 OBJETIVOS 1
UNIVERSIDAD NACIONAL EXPERIMENTAL FRANCISCO DE MIRANDA PROGRAMA: CIENCIAS AMBIENTALES ÁREA: AGRO Y MAR CÁTEDRA: Microbiología e Inmunología Veterinaria PROF: JOSÉ ARAUJO Actividad Prática 3 OBJETIVOS 1
GUÍA REALIZACIÓN DE CULTIVOS MICROBIOLÓGICOS
 ESCUELA DE SALUD GUÍA REALIZACIÓN DE CULTIVOS MICROBIOLÓGICOS DIRIGIDO A ALUMNOS DE: Técnico de laboratorio Clínico y Banco de Sangre Técnico de Enfermería Técnico de Radiodiagnóstico y Radioterapia Informática
ESCUELA DE SALUD GUÍA REALIZACIÓN DE CULTIVOS MICROBIOLÓGICOS DIRIGIDO A ALUMNOS DE: Técnico de laboratorio Clínico y Banco de Sangre Técnico de Enfermería Técnico de Radiodiagnóstico y Radioterapia Informática
NORMA OFICIAL MEXICANA NOM-113-SSA1-1994, BIENES Y SERVICIOS. MÉTODO PARA LA CUENTA DE MICROORGANISMOS COLIFORMES TOTALES EN PLACA.
 NORMA OFICIAL MEXICANA NOM-113-SSA1-1994, BIENES Y SERVICIOS. MÉTODO PARA LA CUENTA DE MICROORGANISMOS COLIFORMES TOTALES EN PLACA. Al margen un sello con el Escudo Nacional, que dice: Estados Unidos Mexicanos.-
NORMA OFICIAL MEXICANA NOM-113-SSA1-1994, BIENES Y SERVICIOS. MÉTODO PARA LA CUENTA DE MICROORGANISMOS COLIFORMES TOTALES EN PLACA. Al margen un sello con el Escudo Nacional, que dice: Estados Unidos Mexicanos.-
UNIVERSIDAD AUTONOMA DE CHIAPAS FACULTAD DE CIENCIAS QUIMICAS CAMPUS IV OCOZOCOAUTLA DE ESPINOZA. LABORATORIO DE BIOLOGIA CELULAR
 UNIVERSIDAD AUTONOMA DE CHIAPAS FACULTAD DE CIENCIAS QUIMICAS CAMPUS IV OCOZOCOAUTLA DE ESPINOZA. LABORATORIO DE BIOLOGIA CELULAR Catedrático: Dra. Ana Olivia cañas Urbina. PRACTICA No. 3: TINCIONES Equipo:
UNIVERSIDAD AUTONOMA DE CHIAPAS FACULTAD DE CIENCIAS QUIMICAS CAMPUS IV OCOZOCOAUTLA DE ESPINOZA. LABORATORIO DE BIOLOGIA CELULAR Catedrático: Dra. Ana Olivia cañas Urbina. PRACTICA No. 3: TINCIONES Equipo:
NMP PARA LA DETERMINACION DE COLIFORMES Y ESCHERICHIA COLI EN ALIMENTOS PRT
 Página 1 de 8 1. OBJETIVO Estimar la densidad de bacterias del grupo coliformes, como indicador sanitario. 2. CAMPO DE APLICACIÓN Y ALCANCE Aplicar este procedimiento a todas las muestras de alimentos
Página 1 de 8 1. OBJETIVO Estimar la densidad de bacterias del grupo coliformes, como indicador sanitario. 2. CAMPO DE APLICACIÓN Y ALCANCE Aplicar este procedimiento a todas las muestras de alimentos
PROCEDIMIENTO ENUMERACION DE LEVADURAS Y MOHOS EN ALIMENTOS BAM ONLINE
 PRT-712.02-048 Página 1 de 7 1. OBJETIVO Detectar el número de unidades formadoras de colonias (ufc) de levaduras y de mohos en el alimento 2. CAMPO DE APLICACIÓN Y ALCANCE Aplicar este procedimiento a
PRT-712.02-048 Página 1 de 7 1. OBJETIVO Detectar el número de unidades formadoras de colonias (ufc) de levaduras y de mohos en el alimento 2. CAMPO DE APLICACIÓN Y ALCANCE Aplicar este procedimiento a
PRÁCTICAS DE MICROBIOLOGÍA CLÍNICA (CURSO )
 PRÁCTICAS DE MICROBIOLOGÍA CLÍNICA (CURSO 2012 2013) PRÁCTICAS A REALIZAR ANÁLISIS CUANTITATIVO DE ORINA ANÁLISIS CUALITATIVO DE ORINA M-1 M-2 M-3 M-4 Lectura de la placa de Agar CLED Identificación presuntiva
PRÁCTICAS DE MICROBIOLOGÍA CLÍNICA (CURSO 2012 2013) PRÁCTICAS A REALIZAR ANÁLISIS CUANTITATIVO DE ORINA ANÁLISIS CUALITATIVO DE ORINA M-1 M-2 M-3 M-4 Lectura de la placa de Agar CLED Identificación presuntiva
Métodos de aislamiento
 Métodos de aislamiento Aislamiento de hongos y bacterias Unidad de Fitopatología Dto. de Protección Vegetal Facultad de Agronomía. Dr. Pedro Mondino Métodos de aislamiento Técnicas de Aislamiento de hongos
Métodos de aislamiento Aislamiento de hongos y bacterias Unidad de Fitopatología Dto. de Protección Vegetal Facultad de Agronomía. Dr. Pedro Mondino Métodos de aislamiento Técnicas de Aislamiento de hongos
LABORATORIO GRUPO 16
 Química Inorgánica Laboratorio Grupo 16 1 LABORATORIO GRUPO 16 A) DESCOMPOSICIÓN DEL AGUA OXIGENADA Materiales: balanza granataria, tubos de ensayos,... Reactivos: agua oxigenada de 10 vol, dióxido de
Química Inorgánica Laboratorio Grupo 16 1 LABORATORIO GRUPO 16 A) DESCOMPOSICIÓN DEL AGUA OXIGENADA Materiales: balanza granataria, tubos de ensayos,... Reactivos: agua oxigenada de 10 vol, dióxido de
RepublicofEcuador EDICTOFGOVERNMENT±
 RepublicofEcuador EDICTOFGOVERNMENT± Inordertopromotepubliceducationandpublicsafety,equaljusticeforal, abeterinformedcitizenry,theruleoflaw,worldtradeandworldpeace, thislegaldocumentisherebymadeavailableonanoncommercialbasis,asit
RepublicofEcuador EDICTOFGOVERNMENT± Inordertopromotepubliceducationandpublicsafety,equaljusticeforal, abeterinformedcitizenry,theruleoflaw,worldtradeandworldpeace, thislegaldocumentisherebymadeavailableonanoncommercialbasis,asit
TRABAJO PRÁCTICO N 6 FERTILIZANTES BIOLÓGICOS: DESARROLLO Y CONTROL DE CALIDAD DE INOCULANTES
 TRABAJO PRÁCTICO N 6 FERTILIZANTES BIOLÓGICOS: DESARROLLO Y CONTROL DE CALIDAD DE INOCULANTES Objetivos Conocer los parámetros para la selección de cepas. Conocer las metodologías y procedimientos microbiológicos
TRABAJO PRÁCTICO N 6 FERTILIZANTES BIOLÓGICOS: DESARROLLO Y CONTROL DE CALIDAD DE INOCULANTES Objetivos Conocer los parámetros para la selección de cepas. Conocer las metodologías y procedimientos microbiológicos
UNIVERSIDAD DE MAYORES PRÁCTICAS DE MICROBIOLOGÍA DEPARTAMENTO DE BIOMEDICINA Y BIOTECNOLOGÍA MICROBIOLOGÍA I
 UNIVERSIDAD DE MAYORES PRÁCTICAS DE MICROBIOLOGÍA DEPARTAMENTO DE BIOMEDICINA Y BIOTECNOLOGÍA MICROBIOLOGÍA I DRAS. MARÍA LUISA ORTIZ Y ANA PEDREGOSA 1 PRÁCTICAS DE MICROBIOLOGÍA DEPARTAMENTO DE BIOMEDICINA
UNIVERSIDAD DE MAYORES PRÁCTICAS DE MICROBIOLOGÍA DEPARTAMENTO DE BIOMEDICINA Y BIOTECNOLOGÍA MICROBIOLOGÍA I DRAS. MARÍA LUISA ORTIZ Y ANA PEDREGOSA 1 PRÁCTICAS DE MICROBIOLOGÍA DEPARTAMENTO DE BIOMEDICINA
UNIVERSIDAD NACIONAL DE COLOMBIA FACULTAD DE MEDICINA DEPARTAMENTO DE MICROBIOLOGIA PRACTICAS DE LABORATORIO IDENTIFICACION BACTERIANA II
 UNIVERSIDAD NACIONAL DE COLOMBIA FACULTAD DE MEDICINA DEPARTAMENTO DE MICROBIOLOGIA PRACTICAS DE LABORATORIO IDENTIFICACION BACTERIANA II Maye Bernal Rivera PARTE II. LECTURA E INTERPRETACION DE LOS CULTIVOS
UNIVERSIDAD NACIONAL DE COLOMBIA FACULTAD DE MEDICINA DEPARTAMENTO DE MICROBIOLOGIA PRACTICAS DE LABORATORIO IDENTIFICACION BACTERIANA II Maye Bernal Rivera PARTE II. LECTURA E INTERPRETACION DE LOS CULTIVOS
INSTITUTO TECNOLOGICO Y DE ESTUDIOS DE MONTERREY. Ingeniería Industrial y de Sistemas. Laboratorio de Química
 INSTITUTO TECNOLOGICO Y DE ESTUDIOS DE MONTERREY CAMPUS HIDALGO María Guadalupe Hidal, 8/2/2015 23:26 Comentario [1]: 58/100 Ingeniería Industrial y de Sistemas Laboratorio de Química Practica #2 María
INSTITUTO TECNOLOGICO Y DE ESTUDIOS DE MONTERREY CAMPUS HIDALGO María Guadalupe Hidal, 8/2/2015 23:26 Comentario [1]: 58/100 Ingeniería Industrial y de Sistemas Laboratorio de Química Practica #2 María
Trabajo Práctico Nº 5
 Introducción Objetivo Procedimiento Resultados Trabajo Práctico Nº 5 INFLUENCIA DE LAS CONDICIONES AM- BIENTALES EN EL CRECIMIENTO MICRO- BIANO Conclusiones Bibliografía INTRODUCCIÓN Las diferentes especies
Introducción Objetivo Procedimiento Resultados Trabajo Práctico Nº 5 INFLUENCIA DE LAS CONDICIONES AM- BIENTALES EN EL CRECIMIENTO MICRO- BIANO Conclusiones Bibliografía INTRODUCCIÓN Las diferentes especies
PRACTICA Núm. 21 RECUENTO DE INDICADORES DE CONTAMINACION FECAL EN AGUA MEDIANTE FILTRACION POR MEMBRANA
 PRAICA Núm. 21 RECUENTO DE INDICADORES DE CONTAMINACION FECAL EN AGUA MEDIANTE FILTRACION POR MEMBRANA I. OBJETIVO Efectuar el recuento de Indicadores de contaminación fecal en diferentes tipos de agua.
PRAICA Núm. 21 RECUENTO DE INDICADORES DE CONTAMINACION FECAL EN AGUA MEDIANTE FILTRACION POR MEMBRANA I. OBJETIVO Efectuar el recuento de Indicadores de contaminación fecal en diferentes tipos de agua.
Easy PDF Creator is professional software to create PDF. If you wish to remove this line, buy it now.
 1 Bacteriología Veterinaria. TRABAJO PRÁCTICO No. 2 CULTIVO DE BACTERIAS OBJETIVOS 1. Manejar con destreza las diferentes técnicas empleadas para la siembra y aislamiento de bacterias. 2. Obtener cultivos
1 Bacteriología Veterinaria. TRABAJO PRÁCTICO No. 2 CULTIVO DE BACTERIAS OBJETIVOS 1. Manejar con destreza las diferentes técnicas empleadas para la siembra y aislamiento de bacterias. 2. Obtener cultivos
PRACTICA Núm. 19 DETERMINACION DE ESTREPTOCOCOS FECALES EN AGUA
 PRACTICA Núm. 19 DETERMINACION DE ESTREPTOCOCOS FECALES EN AGUA I. OBJETIVO Investigar la presencia de Estreptococos fecales en una muestra de agua mediante la técnica del Número Más Probable (NMP) usando
PRACTICA Núm. 19 DETERMINACION DE ESTREPTOCOCOS FECALES EN AGUA I. OBJETIVO Investigar la presencia de Estreptococos fecales en una muestra de agua mediante la técnica del Número Más Probable (NMP) usando
NORMA Oficial Mexicana NOM-113-SSA1-1994, Bienes y servicios. Método para la cuenta de microorganismos coliformes totales en placa.
 08-25-95 NORMA Oficial Mexicana NOM-113-SSA1-1994, Bienes y servicios. Método para la cuenta de microorganismos coliformes totales en placa. Al margen un sello con el Escudo Nacional, que dice: Estados
08-25-95 NORMA Oficial Mexicana NOM-113-SSA1-1994, Bienes y servicios. Método para la cuenta de microorganismos coliformes totales en placa. Al margen un sello con el Escudo Nacional, que dice: Estados
Programa BIO 252 Biología de Microorganismos
 Programa BIO 252 Biología de Microorganismos 1. Identificación 1.- Profesor : Dr. Victoriano Campos 2.- Sigla : BIO 252 3.- Créditos : 4 4.- Pre-requisitos : BIO 240 5.- Horas Teóricas : 4 6.- Horas Prácticas
Programa BIO 252 Biología de Microorganismos 1. Identificación 1.- Profesor : Dr. Victoriano Campos 2.- Sigla : BIO 252 3.- Créditos : 4 4.- Pre-requisitos : BIO 240 5.- Horas Teóricas : 4 6.- Horas Prácticas
