GUIAS DE LABORATORIO DE BIOQUIMICA BASICA FACULTAD DE SALUD PROGRAMA DE ENFERMERIA Docente: MANUEL ANDRES GIRALDO JACOBO
|
|
|
- Eduardo Herrero Hidalgo
- hace 7 años
- Vistas:
Transcripción
1 LABORATORIO N 5 REGULACIÓN DEL EQUILIBRIO ÁCIDO-BASE DESPUÉS DEL EJERCICIO Tiempo de práctica: 2 horas MUSCULAR INTENSO Y DE LA INGESTIÓN DE BICARBONATO DE SODIO Objetivos 1. Al finalizar la práctica, el alumno constatará las actividades reguladoras del pulmón y el riñón para mantener el equilibrio ácido-base en condiciones que tienden a romperlo. 2. Mediante la determinación del ph observará la variación de la concentración de hidrogeniones en la orina de un individuo que ha realizado ejercicio muscular intenso. 3. Relacionará los resultados obtenidos con los cambios metabólicos originados por el ejercicio muscular intenso. Conteste las siguientes preguntas: 1. Por qué es importante que se mantenga constante, dentro de ciertos límites, el ph en el organismo? 2. Cuáles son las fuentes de iones H+ en el organismo? 3. Cuáles son los sistemas reguladores que facilitan la eliminación del H+ producido en el organismo con el fin de mantener constante el ph sanguíneo? 4. Cuáles son las reacciones de formación del ácido carbonico (H2CO3) a partir de CO2 y agua y de su disociación para formar el ion bicarbonato? Escríbalas. 5. Qué sistemas amortiguadores participan directamente en la regulación del ph sanguíneo? 6. Cuáles son los sistemas extrasanguíneos que tienden a mantener el ph extracelular? Escriba la ecuación de Henderson y Hasselbalch aplicada HCO3 - / H2CO3 y, con base en ella, conteste la siguiente pregunta: a). Cómo participan el aparato respiratorio y el riñón en el control del ph sanguíneo? INTRODUCCIÓN Dentro de los mecanismos de regulación de que dispone el organismo para mantener la integridad fisiológica, aquellos involucrados en la homeostasis del ph en los fluidos extracelulares desempeñan un papel crucial para la supervivencia del individuo. En este sentido cabe señalar:
2
3 intenso) donde se incrementa la excreción de H+ Gran parte de este último aparece en la orina acomplejado con el amoniaco en forma de ión amonio (NH4 +) o asociado con el fosfato en forma de fosfato monobásico de sodio (NaH2PO4), representando este último la llamada acidez titulable. En general, el ph de la orina será un reflejo de la producción de ácidos no volátiles por el organismo. El resultado final de los mecanismos fisiológicos que participan en el mantenimiento del equilibrio ácido-base es el de mantener el ph extracelular en un rango compatible con el funcionamiento adecuado del organismo. Materiales Diez probetas o vasos de precipitado de 100 ml. Orina. Solución de bicarbonato de sodio a 3%. Potenciómetro. Agua para consumo Método Un estudiante por equipo desayunará o comerá normalmente (evitar ingestión de jugos ácidos); después hará lo que se indica a continuación. 1. Tomar 250 ml de agua una hora antes de la clase práctica. Vaciar la vejiga y descartar esa orina. 2. Tomar 250 ml de agua inmediatamente antes de la clase práctica. 3.-Orinar en un vaso de precipitado de 100 ml. Registrar su ph 4. Ingerir 250 ml de agua. 5. Realizar ejercicio muscular intenso por 15 minutos, como subir y bajar varias veces las escaleras de tres o cuatro pisos u otro ejercicio sugerido por el profesor. 6. Obtener muestras de orina cada 15 minutos, como en el inciso 3, hasta completar por lo menos cinco muestras.
4 7. A cada muestra se le determinará el ph inmediatamente después de haber sido obtenida ya que con el tiempo el ph tiende a aumentar debido a la pérdida de dióxido de carbono y a que el crecimiento bacteriano produce amoniaco a partir de la urea. Análisis de resultados Una vez obtenido el valor del ph para cada una de las 5 muestras de orina, trazar una gráfica de ph contra tiempo; interpretar los resultados y discutirlos en grupo. Objetivos (Segunda parte) 1. El estudiante constatará el papel del riñón en el mantenimiento del equilibrio ácido-base en una situación de alcalosis metabólica provocada por la ingestión de bicarbonato de sodio. 2. Mediante la medición del ph, observar la variación de la concentración de hidrogeniones en la orina de un individuo que ha ingerido una carga de bicarbonato de sodio. Hipótesis Elabore la hipótesis apropiada. Material Orina Solución de bicarbonato de sodio al 3% Potenciómetro Método Otro estudiante por equipo desayunará o comerá normalmente (evitar ingestión de jugos ácidos); después hará lo que se indica a continuación. 1. Tomar 250 ml de agua una hora antes de la clase práctica. Vaciar la vejiga y descartar esa orina. 2. Tomar 250 ml de agua inmediatamente antes de la clase práctica. 3. Orinar en un vaso de precipitado de 100 ml. Registrar su ph 4. Ingerir 250 ml de agua con 7.5 g de bicarbonato de sodio. 5. Obtener muestras de orina cada 15 minutos, hasta completar por lo menos 5 muestras. 6. A cada muestra se le determinará el ph inmediatamente después de haber sido obtenida.
5 Análisis de resultados Una vez obtenido el valor del ph para cada una de las cinco muestras de orina, trazar una gráfica de ph contra tiempo; interpretar los resultados y discutirlos en grupo. Referencias 1. Devlin TM. Bioquímica. Libro de texto con aplicaciones clínicas. 4a. ed. Barcelona: Editorial Reverte; Montgomery R. Bioquímica: casos y texto. 6a. ed. Editorial Harcourt-Brace; 1998: cap Villazón SA, Cárdenas CO, Villazón. Atentamente MANUEL ANDRÉS GIRALDO JACOBO Docente de Bioquímica
GUIAS DE LABORATORIO DE BIOQUIMICA BASICA FACULTAD DE SALUD PROGRAMA DE ENFERMERIA Docente: MANUEL ANDRES GIRALDO JACOBO LABORATORIO N 7
 LABORATORIO N 7 REGULACIÓN DEL EQUILIBRIO ÁCIDO-BASE DESPUÉS DEL EJERCICIO MUSCULAR INTENSO Y DE LA INGESTIÓN DE BICARBONATO DE SODIO Tiempo de práctica: 2 horas Integrantes: INTRODUCCIÓN Dentro de los
LABORATORIO N 7 REGULACIÓN DEL EQUILIBRIO ÁCIDO-BASE DESPUÉS DEL EJERCICIO MUSCULAR INTENSO Y DE LA INGESTIÓN DE BICARBONATO DE SODIO Tiempo de práctica: 2 horas Integrantes: INTRODUCCIÓN Dentro de los
Sistema Integrado de Gestión
 Sistema Integrado de Gestión GUÍA PRÁCTICA N 52 REGULACIÓN DEL EQUILIBRIO ÁCIDO-BASE DESPUÉS DEL EJERCICIO MUSCULAR INTENSO Y DE LA INGESTIÓN DE BICARBONATO DE SODIO Versión 1 Proceso: Investigación -
Sistema Integrado de Gestión GUÍA PRÁCTICA N 52 REGULACIÓN DEL EQUILIBRIO ÁCIDO-BASE DESPUÉS DEL EJERCICIO MUSCULAR INTENSO Y DE LA INGESTIÓN DE BICARBONATO DE SODIO Versión 1 Proceso: Investigación -
3. Regulación del equilibrio ácido/base después del ejercicio muscular
 3. Regulación del equilibrio ácido/base después del ejercicio muscular intenso a. Guía inicial Tome como base la siguiente premisa para aprender los conceptos fundamentales que ella encierra: Mientras
3. Regulación del equilibrio ácido/base después del ejercicio muscular intenso a. Guía inicial Tome como base la siguiente premisa para aprender los conceptos fundamentales que ella encierra: Mientras
Equilibrio Ácido - Base
 Equilibrio Ácido - Base OBJETIVOS Comprender la importancia de mantener los valores de ph dentro del rango normal Analizar los diferentes mecanismos de regulación que permiten mantener el equilibrio ácido-base
Equilibrio Ácido - Base OBJETIVOS Comprender la importancia de mantener los valores de ph dentro del rango normal Analizar los diferentes mecanismos de regulación que permiten mantener el equilibrio ácido-base
Amortiguadores o Buffer. SEMANA 13 Licda. Lilian Judith Guzman melgar
 Amortiguadores o Buffer SEMANA 13 Licda. Lilian Judith Guzman melgar Soluciones amortiguadoras También llamadas soluciones: Buffer Reguladoras Tampón Solución Buffer Es una solución de un ácido débil y
Amortiguadores o Buffer SEMANA 13 Licda. Lilian Judith Guzman melgar Soluciones amortiguadoras También llamadas soluciones: Buffer Reguladoras Tampón Solución Buffer Es una solución de un ácido débil y
METABOLISMO ACIDO / BASE
 METABOLISMO ACIDO / BASE Dr Sergio Octavio GRANADOS TINAJERO Hospital Angeles de Villahermosa, Villahermosa, Tabasco, México. Course : 3 Year : 2003 Language : Spanish Country : Mexico City : Baja California
METABOLISMO ACIDO / BASE Dr Sergio Octavio GRANADOS TINAJERO Hospital Angeles de Villahermosa, Villahermosa, Tabasco, México. Course : 3 Year : 2003 Language : Spanish Country : Mexico City : Baja California
GUIA DE ESTUDIO SEMANA 13 DISOLUCIONES TAMPON, AMORTIGUADORES O BUFFER Elaborado por: Licda. Edda García
 UNIVERSIDAD DE SAN CARLOS DE GUATEMALA FACULTAD DE CIENCIAS MÉDICAS, CUM UNIDAD DIDACTICA QUIMICA, PRIMER AÑO GUIA DE ESTUDIO 2015 SEMANA 13 DISOLUCIONES TAMPON, AMORTIGUADORES O BUFFER Elaborado por:
UNIVERSIDAD DE SAN CARLOS DE GUATEMALA FACULTAD DE CIENCIAS MÉDICAS, CUM UNIDAD DIDACTICA QUIMICA, PRIMER AÑO GUIA DE ESTUDIO 2015 SEMANA 13 DISOLUCIONES TAMPON, AMORTIGUADORES O BUFFER Elaborado por:
REGULACIÓN DEL EQUILIBRIO ÁCIDO-BASE. Bqca. Sofía Langton Fisiología Humana Junio 2014
 REGULACIÓN DEL EQUILIBRIO ÁCIDOBASE Bqca. Sofía Langton Fisiología Humana Junio 2014 Objetivos 1. Estudiar la importancia del balance ácidobase en el organismo. 2. Comprender los tres sistemas (amortiguadores,
REGULACIÓN DEL EQUILIBRIO ÁCIDOBASE Bqca. Sofía Langton Fisiología Humana Junio 2014 Objetivos 1. Estudiar la importancia del balance ácidobase en el organismo. 2. Comprender los tres sistemas (amortiguadores,
Equilibrio Acido-Base
 UNIVERSIDAD DE SAN CARLOS DE GUATEMALA FACULTAD DE CIENCIAS MÉDICAS FASE I, Unidad Didáctica: BIOQUÍMICA MÉDICA 2º AÑO CICLO ACADÉMICO 2,008 Equilibrio Acido-Base Dr. Mynor A. Leiva Enríquez Las moléculas
UNIVERSIDAD DE SAN CARLOS DE GUATEMALA FACULTAD DE CIENCIAS MÉDICAS FASE I, Unidad Didáctica: BIOQUÍMICA MÉDICA 2º AÑO CICLO ACADÉMICO 2,008 Equilibrio Acido-Base Dr. Mynor A. Leiva Enríquez Las moléculas
Equilibrio Acido-Base. Dr Jorge Brenes Dittel. Nefrología.
 Equilibrio Acido-Base Dr Jorge Brenes Dittel. Nefrología. Equilibrio Acido-base. Fisiología ph es el logaritmo de la concentracíon del ión hidrogenion expresada en milimoles por litro. [H+] en sangre es
Equilibrio Acido-Base Dr Jorge Brenes Dittel. Nefrología. Equilibrio Acido-base. Fisiología ph es el logaritmo de la concentracíon del ión hidrogenion expresada en milimoles por litro. [H+] en sangre es
1.-EQUILIBRIOS IÓNICOS EN DISOLUCIONES ACUOSAS.
 TEMA 5 EQUILIBRIOS IÓNICOS y SISTEMAS TAMPÓN. GUIÓN. ( 2 sesiones). 1.- EQUILIBRIOS IÓNICOS EN DISOLUCIÓN ACUOSA 2.- CONCEPTO DE SISTEMA TAMPÓN. 3.- IMPORTANCIA DE LA REGULACIÓN DEL PH FISIOLÓGICO. 4.-
TEMA 5 EQUILIBRIOS IÓNICOS y SISTEMAS TAMPÓN. GUIÓN. ( 2 sesiones). 1.- EQUILIBRIOS IÓNICOS EN DISOLUCIÓN ACUOSA 2.- CONCEPTO DE SISTEMA TAMPÓN. 3.- IMPORTANCIA DE LA REGULACIÓN DEL PH FISIOLÓGICO. 4.-
b. Base es la sustancia que en disolución acuosa se disocia, liberando aniones de hidroxilo (OH ) según la ecuación general:
 ACIDOS y BASES Teorías ácido - base Los ácidos y las bases fueron definidos por primera vez por el científico sueco Svante Arrhenius en 1887 en su teoría disociación iónica, en la que establecía que hay
ACIDOS y BASES Teorías ácido - base Los ácidos y las bases fueron definidos por primera vez por el científico sueco Svante Arrhenius en 1887 en su teoría disociación iónica, en la que establecía que hay
SOLUCIONES BUFFERS. pk = valor de ph en el cual las concentraciones del ácido y la sal son iguales
 SOLUCIONES BUFFERS Constituidas por un ácido débil y su base conjugada (sal) permite la adición de ácido o base sin variar considerablemente el ph. La capacidad búffer es máximo una unidad por encima y
SOLUCIONES BUFFERS Constituidas por un ácido débil y su base conjugada (sal) permite la adición de ácido o base sin variar considerablemente el ph. La capacidad búffer es máximo una unidad por encima y
PROPÓSITO DE MEDIR LOS GASES ARTERIALES
 FISIOLOGÍA DE GASES ARTERIALES La primera parte de este módulo comprende elementos básicos sobre la fisiología de los gases arteriales. Este módulo ayudará a los profesionales de la enfermería y cardiorrespiratorios
FISIOLOGÍA DE GASES ARTERIALES La primera parte de este módulo comprende elementos básicos sobre la fisiología de los gases arteriales. Este módulo ayudará a los profesionales de la enfermería y cardiorrespiratorios
Equilibrio Acido-Base
 UNIVERSIDAD DE SAN CARLOS DE GUATEMALA FACULTAD DE CIENCIAS MÉDICAS FASE I, Unidad Didáctica: BIOQUÍMICA MÉDICA 2º AÑO CICLO ACADÉMICO 2,007 Equilibrio Acido-Base Dr. Mynor A. Leiva Enríquez Conceptos
UNIVERSIDAD DE SAN CARLOS DE GUATEMALA FACULTAD DE CIENCIAS MÉDICAS FASE I, Unidad Didáctica: BIOQUÍMICA MÉDICA 2º AÑO CICLO ACADÉMICO 2,007 Equilibrio Acido-Base Dr. Mynor A. Leiva Enríquez Conceptos
Líquidos corporales Compartimiento Equilibrio de líquidos. Q.F. Adriana Cordero
 Líquidos corporales Compartimiento Equilibrio de líquidos Q.F. Adriana Cordero INTRODUCCIÒN El agua y los solutos disueltos en cada uno de los compartimentos corporales de fluidos constituyen los líquidos
Líquidos corporales Compartimiento Equilibrio de líquidos Q.F. Adriana Cordero INTRODUCCIÒN El agua y los solutos disueltos en cada uno de los compartimentos corporales de fluidos constituyen los líquidos
Lic. Cintia Mendez Vedia Lic. en Nutrición Univesidad de Buenos Aires
 ÁCIDOS Y BASES Lic. Cintia Mendez Vedia Lic. en Nutrición Univesidad de Buenos Aires OBJETIVOS: - Reconocer ácidos, bases y sales, determinar sus disociaciones en agua, según sean electrolitos fuertes
ÁCIDOS Y BASES Lic. Cintia Mendez Vedia Lic. en Nutrición Univesidad de Buenos Aires OBJETIVOS: - Reconocer ácidos, bases y sales, determinar sus disociaciones en agua, según sean electrolitos fuertes
Actualización en Medio Interno Conceptos básicos
 Actualización en Medio Interno Conceptos básicos Bioquímica Lucrecia Drago Bioquímica M. Fernanda Pontoriero Ácidos Moléculas capaces de liberar H + HCl H + + Cl H 2 CO 3 H + + HCO 3 Bases Moléculas capaces
Actualización en Medio Interno Conceptos básicos Bioquímica Lucrecia Drago Bioquímica M. Fernanda Pontoriero Ácidos Moléculas capaces de liberar H + HCl H + + Cl H 2 CO 3 H + + HCO 3 Bases Moléculas capaces
Para resolver ésta guía deberá leer el tema en el Capítulo 10 del libro de texto.
 UNIVERSIDAD DE SAN CARLOS DE GUATEMALA FACULTAD DE CIENCIAS MÉDICAS, CUM UNIDAD DIDACTICA QUIMICA, PRIMER AÑO GUIA DE ESTUDIO 2016 SEMANA 13 DISOLUCIONES TAMPON, AMORTIGUADORES O BUFFER Elaborado por:
UNIVERSIDAD DE SAN CARLOS DE GUATEMALA FACULTAD DE CIENCIAS MÉDICAS, CUM UNIDAD DIDACTICA QUIMICA, PRIMER AÑO GUIA DE ESTUDIO 2016 SEMANA 13 DISOLUCIONES TAMPON, AMORTIGUADORES O BUFFER Elaborado por:
Agua, electrolitos, balance acido-base. Dra. Luz E. Cuevas-Molina NURS 1231
 Agua, electrolitos, balance acido-base Dra. Luz E. Cuevas-Molina NURS 1231 1 Introducción Para mantener la homoestasis debe haber un balance entre las cantidades de fluido y electrolitos Los electrolitos
Agua, electrolitos, balance acido-base Dra. Luz E. Cuevas-Molina NURS 1231 1 Introducción Para mantener la homoestasis debe haber un balance entre las cantidades de fluido y electrolitos Los electrolitos
PRÁCTICA 4 DISOLUCIONES AMORTIGUADORAS
 PRÁCTICA 4 DISOLUCIONES AMORTIGUADORAS INTRODUCCIÓN Las disoluciones amortiguadoras son frecuentes en la naturaleza, como es el caso del sistema H 2 CO 3 /NaHCO 3 que predomina en el plasma y fluido intersticial
PRÁCTICA 4 DISOLUCIONES AMORTIGUADORAS INTRODUCCIÓN Las disoluciones amortiguadoras son frecuentes en la naturaleza, como es el caso del sistema H 2 CO 3 /NaHCO 3 que predomina en el plasma y fluido intersticial
[A-] Citrato 3- ph = pka + log. 7 = log [AH] Citrato 2- 7 = log = = x x
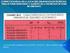
![[A-] Citrato 3- ph = pka + log. 7 = log [AH] Citrato 2- 7 = log = = x x [A-] Citrato 3- ph = pka + log. 7 = log [AH] Citrato 2- 7 = log = = x x](/thumbs/55/35730009.jpg) Una reacción enzimática transcurre en 10 ml de una disolución cuya concentración total de citrato es 120 mm y su ph inicial es de 7. Durante la reacción se producen 0.2 miliequivalentes de un ácido. Calcular
Una reacción enzimática transcurre en 10 ml de una disolución cuya concentración total de citrato es 120 mm y su ph inicial es de 7. Durante la reacción se producen 0.2 miliequivalentes de un ácido. Calcular
Fisiopatología Del Equilibrio Ácido-Base Alcalosis
 Fisiopatología Del Equilibrio Ácido-Base Alcalosis Prof. Marcos Moreira Espinoza Instituto de Farmacología y Morfofisiologia Universidad Austral de Chile ALTERACIONES DEL EQUILIBRIO ACIDO BASE: II. ALCALOSIS
Fisiopatología Del Equilibrio Ácido-Base Alcalosis Prof. Marcos Moreira Espinoza Instituto de Farmacología y Morfofisiologia Universidad Austral de Chile ALTERACIONES DEL EQUILIBRIO ACIDO BASE: II. ALCALOSIS
LA MATERIA VIVA Y EL AGUA
 Página 1 de 11 LA MATERIA VIVA Y EL AGUA Haga clic en la respuesta correcta. Mostrar las preguntas individualmente 1. Tipo C. Siempre se produce una variación en el ph de una disolución reguladora si simultáneamente
Página 1 de 11 LA MATERIA VIVA Y EL AGUA Haga clic en la respuesta correcta. Mostrar las preguntas individualmente 1. Tipo C. Siempre se produce una variación en el ph de una disolución reguladora si simultáneamente
Fundación H.A. Barceló Facultad de Medicina
 Fundación H.A. Barceló Facultad de Medicina LICENCIATURA EN NUTRICION PRIMER AÑO FISIOLOGIA MODULO 16 LECCIONES 1 Y 2 1 MODULO 16: Equilibrio Electrolítico y Control de ph OBJETIVOS - Conocer las vías
Fundación H.A. Barceló Facultad de Medicina LICENCIATURA EN NUTRICION PRIMER AÑO FISIOLOGIA MODULO 16 LECCIONES 1 Y 2 1 MODULO 16: Equilibrio Electrolítico y Control de ph OBJETIVOS - Conocer las vías
BALANCE ÁCIDO-BASE Y REGULACIÓN DEL ph
 BALANCE ÁCIDO-BASE Y REGULACIÓN DEL ph INTRODUCCION Importancia del mantenimiento del ph [H + ] afecta: Conformación de proteínas Reacciones donde el H + es producto o reactivo Liberación de O 2 de la
BALANCE ÁCIDO-BASE Y REGULACIÓN DEL ph INTRODUCCION Importancia del mantenimiento del ph [H + ] afecta: Conformación de proteínas Reacciones donde el H + es producto o reactivo Liberación de O 2 de la
UNIVERSIDAD DE SAN CARLOS DE GUATEMALA FACULTAD DE CIENCIAS MÉDICAS FASE I, Unidad Didáctica: BIOQUÍMICA MÉDICA CICLO ACADÉMICO 2,009
 UNIVERSIDAD DE SAN CARLOS DE GUATEMALA FACULTAD DE CIENCIAS MÉDICAS FASE I, Unidad Didáctica: BIOQUÍMICA MÉDICA 2º AÑO CICLO ACADÉMICO 2,009 Equilibrio AcidoAcido-Base Dr. Mynor A. Leiva Enríquez Las moléculas
UNIVERSIDAD DE SAN CARLOS DE GUATEMALA FACULTAD DE CIENCIAS MÉDICAS FASE I, Unidad Didáctica: BIOQUÍMICA MÉDICA 2º AÑO CICLO ACADÉMICO 2,009 Equilibrio AcidoAcido-Base Dr. Mynor A. Leiva Enríquez Las moléculas
TRASTORNOS METABOLICOS DEL ESTADO ACIDO-BASE
 TRASTORNOS METABOLICOS DEL ESTADO ACIDO-BASE ALTERACIONES ACIDO-BASE Los ácidos son producidos en forma continua, durante el metabolismo normal La concentración de hidrógeno en el LEC se mantiene en un
TRASTORNOS METABOLICOS DEL ESTADO ACIDO-BASE ALTERACIONES ACIDO-BASE Los ácidos son producidos en forma continua, durante el metabolismo normal La concentración de hidrógeno en el LEC se mantiene en un
GUIA DE LABORATORIOS DC-LI-FR-001
 Versión: 00 Fecha: 28-02-2014 Página 1 de 6 NOMBRE DEL CURSO LABORATORIO DE BIOQUIMICA NOMBRE DE LA PRÁCTICA SOLUCIONES AMORTIGUADORAS Y ph 1. OBJETIVO DE LA PRÁCTICA Determinar el ph de soluciones amortiguadoras
Versión: 00 Fecha: 28-02-2014 Página 1 de 6 NOMBRE DEL CURSO LABORATORIO DE BIOQUIMICA NOMBRE DE LA PRÁCTICA SOLUCIONES AMORTIGUADORAS Y ph 1. OBJETIVO DE LA PRÁCTICA Determinar el ph de soluciones amortiguadoras
REGULACIÓN DEL BALANCE ÁCIDO-BÁSICO:
 REGULACIÓN DEL BALANCE ÁCIDO-BÁSICO: - FISIOLOGÍA DE ÁCIDOS Y BASES - EXCRECIÓN RENAL DE H + Miryam Romero R. MSc. PhD. Profesora de Fisiología Departamento de Ciencias Fisiológicas Universidad del Valle
REGULACIÓN DEL BALANCE ÁCIDO-BÁSICO: - FISIOLOGÍA DE ÁCIDOS Y BASES - EXCRECIÓN RENAL DE H + Miryam Romero R. MSc. PhD. Profesora de Fisiología Departamento de Ciencias Fisiológicas Universidad del Valle
PH y SISTEMAS TAMPÓN
 PH y SISTEMAS TAMPÓN DISOCIACIÓN DEL AGUA.- El agua se disocia de la manera siguiente: HOH H+ OH- El valor de Kéq. a 25ºC es muy pequeña, siendo del orden de 1 8 x 10(-16). Esto significa
PH y SISTEMAS TAMPÓN DISOCIACIÓN DEL AGUA.- El agua se disocia de la manera siguiente: HOH H+ OH- El valor de Kéq. a 25ºC es muy pequeña, siendo del orden de 1 8 x 10(-16). Esto significa
Tema: Soluciones Buffer-Amortiguadoras
 ESCUELA DE CIENCIAS AGRICOLA, PECUARIAS Y DEL MEDIO AMBIENTE ECAPMA Nombre l Curso: 334001-Sistema Metabólico Nutricional Tema: Soluciones Buffer-Amortiguadoras JAIRO ENRIQUE GRANADOS MORENO.,MSc (Director
ESCUELA DE CIENCIAS AGRICOLA, PECUARIAS Y DEL MEDIO AMBIENTE ECAPMA Nombre l Curso: 334001-Sistema Metabólico Nutricional Tema: Soluciones Buffer-Amortiguadoras JAIRO ENRIQUE GRANADOS MORENO.,MSc (Director
Sistema Integrado de Gestión. SOLUCIONES REGULADORAS DEL ph (SOLUCIONES BUFFER O TAMPÓN) PROGRAMA DE DEPORTE GUIA PRÁCTICA N 5
 Sistema Integrado de Gestión SOLUCIONES REGULADORAS DEL ph (SOLUCIONES BUFFER O Versión 5 Proceso: Investigación - IV Febrero de 2016 Página 2 de 14 1. OBJETIVOS Determinar experimentalmente el ph de una
Sistema Integrado de Gestión SOLUCIONES REGULADORAS DEL ph (SOLUCIONES BUFFER O Versión 5 Proceso: Investigación - IV Febrero de 2016 Página 2 de 14 1. OBJETIVOS Determinar experimentalmente el ph de una
DEPARTAMENTO DE BIOQUÍMICA ESFUNO EUTM. ACIDOS Y BASES, ph, BUFFERS
 DEPARTAMENTO DE BIOQUÍMICA ESFUNO EUTM ACIDOS Y BASES, ph, BUFFERS Ionización del agua y producto iónico del agua (K w ) H 2 O H + + OH - K eq = [H + ][OH - ] [H 2 O] K eq = [H + ][OH - ] [H 2 O] K eq
DEPARTAMENTO DE BIOQUÍMICA ESFUNO EUTM ACIDOS Y BASES, ph, BUFFERS Ionización del agua y producto iónico del agua (K w ) H 2 O H + + OH - K eq = [H + ][OH - ] [H 2 O] K eq = [H + ][OH - ] [H 2 O] K eq
GUIAS DE ESTUDIO PARA QUINTO PARCIAL DE TEORIA
 UNIVERSIDAD DE SAN CARLOS DE GUATEMALA FACULTAD DE CIENCIAS MÉDICAS 2017 CIENCIAS BASICAS Y BIOLOGICAS U.D. BIOQUIMICA SEGUNDO AÑO GUIAS DE ESTUDIO PARA QUINTO PARCIAL DE TEORIA GUIA DE ESTUDIO No. 27:
UNIVERSIDAD DE SAN CARLOS DE GUATEMALA FACULTAD DE CIENCIAS MÉDICAS 2017 CIENCIAS BASICAS Y BIOLOGICAS U.D. BIOQUIMICA SEGUNDO AÑO GUIAS DE ESTUDIO PARA QUINTO PARCIAL DE TEORIA GUIA DE ESTUDIO No. 27:
La Composición del medio que rodea a las células debe permanecer constante: (HOMEOSTASIS) y entre límites compatibles con las reacciones vitales
 pulmones Tracto Gastrointestinal FLUIDOS INTRA- Y EXTRA-CELULARES Al pasar por los pulmones el CO2 sale y entra O2 a la sangre nutrientes Nutrientes y O2 entran a cls Deshechos y CO2 salen de las cls Los
pulmones Tracto Gastrointestinal FLUIDOS INTRA- Y EXTRA-CELULARES Al pasar por los pulmones el CO2 sale y entra O2 a la sangre nutrientes Nutrientes y O2 entran a cls Deshechos y CO2 salen de las cls Los
GUÍA DE EJERCICIOS EQUILIBRIO IÓNICO Área Química
 Resultados de aprendizaje GUÍA DE EJERCICIOS EQUILIBRIO IÓNICO Área Química Identifica, interpreta y analiza conceptos básicos sobre equilibrio iónico, para la resolución de ejercicios, desarrollando pensamiento
Resultados de aprendizaje GUÍA DE EJERCICIOS EQUILIBRIO IÓNICO Área Química Identifica, interpreta y analiza conceptos básicos sobre equilibrio iónico, para la resolución de ejercicios, desarrollando pensamiento
LABORATORIO N 3 SOLUCIONES ACIDO-BASE Y BUFFER
 LABORATORIO N 3 SOLUCIONES ACIDO-BASE Y BUFFER 1.- INTRODUCCIÓN Soluciones Ácido-Base Los solutos disueltos en agua pueden clasificarse como electrolitos y no electrolitos en función de su capacidad de
LABORATORIO N 3 SOLUCIONES ACIDO-BASE Y BUFFER 1.- INTRODUCCIÓN Soluciones Ácido-Base Los solutos disueltos en agua pueden clasificarse como electrolitos y no electrolitos en función de su capacidad de
ÁCIDOS Y BASES MPSS GÓMEZ CHANG ERIKA. Todos los derechos reservados. Julio 2007 M. en C. Alicia Cea Bonilla -
 ÁCIDOS Y BASES MPSS GÓMEZ CHANG ERIKA 1 Probablemente no haya otro tipo de equilibrio tan importante como el de ácidos y bases B. M. Mahan y R. J. Myers 2 CASO AMC de 52 años de edad, acostumbraba consumir
ÁCIDOS Y BASES MPSS GÓMEZ CHANG ERIKA 1 Probablemente no haya otro tipo de equilibrio tan importante como el de ácidos y bases B. M. Mahan y R. J. Myers 2 CASO AMC de 52 años de edad, acostumbraba consumir
Organización Funcional y el Medio Interno
 Organización Funcional y el Medio Interno Aproximadamente el 50 % del cuerpo humano es líquido y la mayor parte es intracelular, la tercera parte es extracelular, la misma que se encuentra en movimiento
Organización Funcional y el Medio Interno Aproximadamente el 50 % del cuerpo humano es líquido y la mayor parte es intracelular, la tercera parte es extracelular, la misma que se encuentra en movimiento
Guía soluciones acuosas
 UNIVERSIDAD N LA REPUBLICA Nombre del Estudiante: Guía soluciones acuosas Carrera Asignatura Nivel Enfermería Bioquímica Segundo Nivel Semestre 2 semestre Año 2016 Docente Dr. Patricio Muñoz Torres Puntaje
UNIVERSIDAD N LA REPUBLICA Nombre del Estudiante: Guía soluciones acuosas Carrera Asignatura Nivel Enfermería Bioquímica Segundo Nivel Semestre 2 semestre Año 2016 Docente Dr. Patricio Muñoz Torres Puntaje
Sistema Integrado de Gestión GUÍA PRÁCTICA N 5
 Sistema Integrado de Gestión GUÍA PRÁCTICA N 5 SOLUCIONES REGULADORAS DEL ph (SOLUCIONES BUFFER O TAMPÓN) PROGRAMA VERSIÓN 5 Proceso: Investigación - IV Febrero de 2016 Página 2 de 13 1. OBJETIVOS Determinar
Sistema Integrado de Gestión GUÍA PRÁCTICA N 5 SOLUCIONES REGULADORAS DEL ph (SOLUCIONES BUFFER O TAMPÓN) PROGRAMA VERSIÓN 5 Proceso: Investigación - IV Febrero de 2016 Página 2 de 13 1. OBJETIVOS Determinar
UD 8. Aplicaciones de los equilibrios ácido-base
 UD 8. Aplicaciones de los equilibrios ácido-base 8.1 Efecto del ion común. 8.2 Disoluciones reguladoras del ph. 8.3 Sistemas reguladores biológicos. 8.4 Valoraciones ácido-base. 8.5 Indicadores ácido-base.
UD 8. Aplicaciones de los equilibrios ácido-base 8.1 Efecto del ion común. 8.2 Disoluciones reguladoras del ph. 8.3 Sistemas reguladores biológicos. 8.4 Valoraciones ácido-base. 8.5 Indicadores ácido-base.
EQUILIBRIO ÁCIDO-BASE
 EQUILIBRIO ÁCIDO-BASE - Departamento de Fisiopatología - Facultad de Medicina Br. Inés Lujambio CONCEPTOS BÁSICOS. Ácido: toda sustancias capaz de ceder protones de hidrógeno (H + ). HCl H + + Cl - Base:
EQUILIBRIO ÁCIDO-BASE - Departamento de Fisiopatología - Facultad de Medicina Br. Inés Lujambio CONCEPTOS BÁSICOS. Ácido: toda sustancias capaz de ceder protones de hidrógeno (H + ). HCl H + + Cl - Base:
PROBLEMAS RESUELTOS SELECTIVIDAD ANDALUCÍA 2009 QUÍMICA TEMA 6: EQUILIBRIOS ÁCIDO-BASE
 PROBLEMAS RESUELTOS SELECTIVIDAD ANDALUCÍA 009 QUÍMICA TEMA 6: EQUILIBRIOS ÁCIDO-BASE Junio, Ejercicio, Opción A Junio, Ejercicio 5, Opción B Reserva 1, Ejercicio 5, Opción A Reserva 1, Ejercicio 4, Opción
PROBLEMAS RESUELTOS SELECTIVIDAD ANDALUCÍA 009 QUÍMICA TEMA 6: EQUILIBRIOS ÁCIDO-BASE Junio, Ejercicio, Opción A Junio, Ejercicio 5, Opción B Reserva 1, Ejercicio 5, Opción A Reserva 1, Ejercicio 4, Opción
TEMA 3. FUNCIÓN TUBULAR (II). EQUILIBRIO DEL AGUA. EQUILIBRIO ÁCIDO- BÁSICO
 TEMA 3. FUNCIÓN TUBULAR (II). EQUILIBRIO DEL AGUA. EQUILIBRIO ÁCIDO- BÁSICO Equilibrio del agua. Resorción de agua en túbulo proximal y en asa de Henle. Mecanismos de concentración y de dilución de la
TEMA 3. FUNCIÓN TUBULAR (II). EQUILIBRIO DEL AGUA. EQUILIBRIO ÁCIDO- BÁSICO Equilibrio del agua. Resorción de agua en túbulo proximal y en asa de Henle. Mecanismos de concentración y de dilución de la
1. Líquidos corporales. 2. Anatomía y función renal. 3. Hormonas ADH y aldosterona
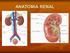 1. Líquidos corporales 2. Anatomía y función renal 3. Hormonas ADH y aldosterona Propiedades de la Homeostasis 1. Importancia tanto del sistema nervioso como del endocrino. 2. Controles antagónicos. 3.
1. Líquidos corporales 2. Anatomía y función renal 3. Hormonas ADH y aldosterona Propiedades de la Homeostasis 1. Importancia tanto del sistema nervioso como del endocrino. 2. Controles antagónicos. 3.
EQUILIBRIO ÁCIDO-BASE MANTENIMIENTO DE LA HOMEOSTASIS
 EQUILIBRIO ÁCIDO-BASE MANTENIMIENTO DE LA HOMEOSTASIS EQUILÍBRIO ÁCIDO-BASE La regulación de ph a nivel celular, es necesaria para la supervivencia. Los ácidos y bases entran continuamente en la sangre
EQUILIBRIO ÁCIDO-BASE MANTENIMIENTO DE LA HOMEOSTASIS EQUILÍBRIO ÁCIDO-BASE La regulación de ph a nivel celular, es necesaria para la supervivencia. Los ácidos y bases entran continuamente en la sangre
PROBLEMAS RESUELTOS SELECTIVIDAD ANDALUCÍA 2009 QUÍMICA TEMA 6: EQUILIBRIOS ÁCIDO-BASE
 PROBLEMAS RESUELTOS SELECTIVIDAD ANDALUCÍA 009 QUÍMICA TEMA 6: EQUILIBRIOS ÁCIDO-BASE Junio, Ejercicio, Opción A Junio, Ejercicio 5, Opción B Reserva 1, Ejercicio 5, Opción A Reserva 1, Ejercicio 4, Opción
PROBLEMAS RESUELTOS SELECTIVIDAD ANDALUCÍA 009 QUÍMICA TEMA 6: EQUILIBRIOS ÁCIDO-BASE Junio, Ejercicio, Opción A Junio, Ejercicio 5, Opción B Reserva 1, Ejercicio 5, Opción A Reserva 1, Ejercicio 4, Opción
TEMA 28. REGULACIÓN DEL PH
 TEMA 28. REGULACIÓN DEL PH 28.1. MECANISMOS DE COMPENSACIÓN ANTE VARIACIONES DEL PH El equilibrio ácido-base (también denominado homeostasis del ph) es una de las funciones esenciales del cuerpo. El ph
TEMA 28. REGULACIÓN DEL PH 28.1. MECANISMOS DE COMPENSACIÓN ANTE VARIACIONES DEL PH El equilibrio ácido-base (también denominado homeostasis del ph) es una de las funciones esenciales del cuerpo. El ph
GUÍA DE EJERCICIOS ADICIONALES N 2 Acido-base, neutralización y buffer
 1 GUÍA DE EJERCICIOS ADICIONALES N 2 Acido-base, neutralización y buffer 1.- Un ácido según la teoría de Arrhenius es aquella sustancia que: a) Libera uno o más iones hidroxilos (OH - ) por cada molécula
1 GUÍA DE EJERCICIOS ADICIONALES N 2 Acido-base, neutralización y buffer 1.- Un ácido según la teoría de Arrhenius es aquella sustancia que: a) Libera uno o más iones hidroxilos (OH - ) por cada molécula
Fisiopatología del Equilibrio Ácido-Base ACIDOSIS
 Fisiopatología del Equilibrio Ácido-Base ACIDOSIS Prof. Marcos Moreira Espinoza Instituto de Farmacología y Morfofisiologia Universidad Austral de Chile ALTERACIONES DEL EQUILIBRIO ACIDO BASE: I. ACIDOSIS:
Fisiopatología del Equilibrio Ácido-Base ACIDOSIS Prof. Marcos Moreira Espinoza Instituto de Farmacología y Morfofisiologia Universidad Austral de Chile ALTERACIONES DEL EQUILIBRIO ACIDO BASE: I. ACIDOSIS:
BIOQUIMICA CLINICA II
 Universidad Autónoma de Chiapas Facultad de Ciencias Químicas Campus IV BIOQUIMICA CLINICA II UNIDAD 5 EQUILIBRIO ACIDO-BASE TITULAR DEL CURSO : M.C. CONSUELO CHANG RUEDA CICLO ENERO - DICIEMBRE - 2015
Universidad Autónoma de Chiapas Facultad de Ciencias Químicas Campus IV BIOQUIMICA CLINICA II UNIDAD 5 EQUILIBRIO ACIDO-BASE TITULAR DEL CURSO : M.C. CONSUELO CHANG RUEDA CICLO ENERO - DICIEMBRE - 2015
Nombre Grupo. Unidad 6 Ácido-base
 Nombre Grupo OPCIÓN A Unidad 6 Ácido-base 1. (2 p) a) Calcule el ph de una disolución 0.1 M de hidróxido potásico. El hidróxido potásico, como base fuerte que es, está completamente disociada en disolución
Nombre Grupo OPCIÓN A Unidad 6 Ácido-base 1. (2 p) a) Calcule el ph de una disolución 0.1 M de hidróxido potásico. El hidróxido potásico, como base fuerte que es, está completamente disociada en disolución
LABORATORIO DE QUÍMICA ANALÍTICA I LQ-218. Práctica de Laboratorio No. 6 PROPIEDADES DE LOS AMORTIGUADORES SIMPLES Y PREPARACION DE SOLUCIONES BUFFERS
 UNIVERSIDAD NACIONAL AUTÓNOMA DE HONDURAS FACULTAD DE CIENCIAS QUÍMICAS Y FARMACIA DEPARTAMENTO DE QUÍMICA LABORATORIO DE QUÍMICA ANALÍTICA I LQ-218 Práctica de Laboratorio No. 6 COMPETENCIAS 1. Prepara
UNIVERSIDAD NACIONAL AUTÓNOMA DE HONDURAS FACULTAD DE CIENCIAS QUÍMICAS Y FARMACIA DEPARTAMENTO DE QUÍMICA LABORATORIO DE QUÍMICA ANALÍTICA I LQ-218 Práctica de Laboratorio No. 6 COMPETENCIAS 1. Prepara
TRBAJO PRÁCTICO N 5: ph. Objetivo: Determinar el ph de soluciones ácidas y básicas de concentraciones diferentes.
 QUÍMICA GENERAL Y TECNOLÓGICA 2010 TRBAJO PRÁCTICO N 5: ph Objetivo: Determinar el ph de soluciones ácidas y básicas de concentraciones diferentes. Fundamentos Teóricos: La mayoría de las reacciones químicas
QUÍMICA GENERAL Y TECNOLÓGICA 2010 TRBAJO PRÁCTICO N 5: ph Objetivo: Determinar el ph de soluciones ácidas y básicas de concentraciones diferentes. Fundamentos Teóricos: La mayoría de las reacciones químicas
TRANSFERENCIA DE PROTONES. CUESTIONES Y PROBLEMAS. E1B.S2009 Para las especies CN, HF y CO 3
 TRANSFERENCIA DE PROTONES. CUESTIONES Y PROBLEMAS. E1B.S2009 Para las especies CN, HF y CO 3 2, en disolución acuosa: a.- Escriba, según corresponda, la fórmula del ácido o de la base conjugados. b.- Justifique,
TRANSFERENCIA DE PROTONES. CUESTIONES Y PROBLEMAS. E1B.S2009 Para las especies CN, HF y CO 3 2, en disolución acuosa: a.- Escriba, según corresponda, la fórmula del ácido o de la base conjugados. b.- Justifique,
7. ESTUDIO DEL EQUILIBRIO ACIDO BASE DE UN PACIENTE
 Departamento de Bioquímica y Biología Molecular ph y equilibrios acido-base 7. ESTUDIO DEL EQUILIBRIO ACIDO BASE DE UN PACIENTE ESQUEMA - Estudio del equilibrio ácido-base de un paciente - Trastornos del
Departamento de Bioquímica y Biología Molecular ph y equilibrios acido-base 7. ESTUDIO DEL EQUILIBRIO ACIDO BASE DE UN PACIENTE ESQUEMA - Estudio del equilibrio ácido-base de un paciente - Trastornos del
Bases Científicas 1 Autor: Marta Adonis
 ACIDO-BASE En los organismos vivos la concentración de protones debe mantenerse dentro de límites muy estrechos, como requisito indispensable para el desarrollo normal de los procesos metabólicos intracelulares.
ACIDO-BASE En los organismos vivos la concentración de protones debe mantenerse dentro de límites muy estrechos, como requisito indispensable para el desarrollo normal de los procesos metabólicos intracelulares.
QUIMICA GENERAL GUIA DE EJERCICIOS Nº4 Soluciones Ácido-base. 1.- Defina los ácidos y bases según las teorías ácido base que usted conoce.
 1 QUIMICA GENERAL GUIA DE EJERCICIOS Nº4 Soluciones Ácido-base PRIMERA PARTE: Ejercicios de desarrollo. 1.- Defina los ácidos y bases según las teorías ácido base que usted conoce. 2.- Defina el ph y poh.
1 QUIMICA GENERAL GUIA DE EJERCICIOS Nº4 Soluciones Ácido-base PRIMERA PARTE: Ejercicios de desarrollo. 1.- Defina los ácidos y bases según las teorías ácido base que usted conoce. 2.- Defina el ph y poh.
Primer Informe de laboratorio de bioquímica SOLUCIONES AMORTIGUADORAS O BUFFERS RESUMEN Se prepararon las soluciones amortiguadoras correspondientes
 Primer Informe de laboratorio de bioquímica SOLUCIONES AMORTIGUADORAS O BUFFERS RESUMEN Se prepararon las soluciones amortiguadoras correspondientes para determinar el ph de las mismas y obtener nuestros
Primer Informe de laboratorio de bioquímica SOLUCIONES AMORTIGUADORAS O BUFFERS RESUMEN Se prepararon las soluciones amortiguadoras correspondientes para determinar el ph de las mismas y obtener nuestros
TEMA 6. ÁCIDOS Y BASES
 TEMA 6. ÁCIDOS Y BASES 9.1) Responda a las siguientes cuestiones: a) Defina el concepto de ácido y base según la teoría de Arrhenius. b) Clasifique, según la definición anterior, las siguientes especies,
TEMA 6. ÁCIDOS Y BASES 9.1) Responda a las siguientes cuestiones: a) Defina el concepto de ácido y base según la teoría de Arrhenius. b) Clasifique, según la definición anterior, las siguientes especies,
ENFERMERIA DE ALTO RIESGO HCO3 GASOMETRIA ARTERIAL. PaCO2. PaO2
 ENFERMERIA DE ALTO RIESGO HCO3 ph GASOMETRIA ARTERIAL PaO2 PaCO2 DEFINICION La gasometría arterial es una de las técnicas más frecuentes realizadas a pacientes en estado crítico. Para realizar una correcta
ENFERMERIA DE ALTO RIESGO HCO3 ph GASOMETRIA ARTERIAL PaO2 PaCO2 DEFINICION La gasometría arterial es una de las técnicas más frecuentes realizadas a pacientes en estado crítico. Para realizar una correcta
EDUCATIVO. Alteraciones del. - Departamento de Fisiopatología - Facultad de Medicina 2011MATERIAL. Dr MSc José Boggia
 - Departamento de Fisiopatología - Facultad de Medicina Alteraciones del equilibrio i ácido-base 2011 Dr MSc José Boggia PANORAMICA GLOBAL I. Recordatorio de la fisiología ácido-base II. Diagnóstico de
- Departamento de Fisiopatología - Facultad de Medicina Alteraciones del equilibrio i ácido-base 2011 Dr MSc José Boggia PANORAMICA GLOBAL I. Recordatorio de la fisiología ácido-base II. Diagnóstico de
ARTICULOS DE INTERES
 ARTICULOS DE INTERES TEORIA DE BRÖNSTED Y LOWRY Dra. Zeballos López Lourdes 1 RESUMEN Johannes Brönsted y Thomas Lowry fueron científicos que desarrollaron una teoría sobre los ácidos y las bases, sustancias
ARTICULOS DE INTERES TEORIA DE BRÖNSTED Y LOWRY Dra. Zeballos López Lourdes 1 RESUMEN Johannes Brönsted y Thomas Lowry fueron científicos que desarrollaron una teoría sobre los ácidos y las bases, sustancias
Práctica No 11. Determinación del calor de neutralización del acido clorhídrico con hidróxido de sodio.
 Práctica No 11 Determinación del calor de neutralización del acido clorhídrico con hidróxido de sodio. 1. Objetivo general: Determinar la variación de entalpía cuando un ácido fuerte, es neutralizado por
Práctica No 11 Determinación del calor de neutralización del acido clorhídrico con hidróxido de sodio. 1. Objetivo general: Determinar la variación de entalpía cuando un ácido fuerte, es neutralizado por
6. MANTENIMIENTO DEL ph EN EL MEDIO EXTRACELULAR
 Departamento de Bioquímica y Biología Molecular ph y equilibrios acido-base 6. MANTENIMIENTO DEL ph EN EL MEDIO EXTRACELULAR ESQUEMA - Composición iónica de los medios corporales - Capacidad tampón - Mantenimiento
Departamento de Bioquímica y Biología Molecular ph y equilibrios acido-base 6. MANTENIMIENTO DEL ph EN EL MEDIO EXTRACELULAR ESQUEMA - Composición iónica de los medios corporales - Capacidad tampón - Mantenimiento
Unidad 2. Ácidos y Bases Capítulo 2 Dióxido de Carbono en disolución
 Unidad 2. Ácidos y Bases Capítulo 2 Dióxido de Carbono en disolución En este capítulo prestaremos atención al dióxido de carbono en disolución acuosa y a las especies con las que se encuentra en equilibrio:
Unidad 2. Ácidos y Bases Capítulo 2 Dióxido de Carbono en disolución En este capítulo prestaremos atención al dióxido de carbono en disolución acuosa y a las especies con las que se encuentra en equilibrio:
Índice. Sección I. 1. Química y amortiguamiento acidobásicos Homeostasis acidobásica intracelular... 35
 Índice Prefacio... V Prólogo... VII Indice... IX Colaboradores... XVII Sección I 1. Química y amortiguamiento acidobásicos... 21 - John H. Galla Introducción... 21 Amortiguamiento... 24 El papel de los
Índice Prefacio... V Prólogo... VII Indice... IX Colaboradores... XVII Sección I 1. Química y amortiguamiento acidobásicos... 21 - John H. Galla Introducción... 21 Amortiguamiento... 24 El papel de los
Química. Equilibrio ácido-base Nombre:
 Química DEPARTAMENTO DE FÍSICA E QUÍMICA Equilibrio ácido-base 25-02-08 Nombre: Cuestiones y problemas 1. a) Qué concentración tiene una disolución de amoníaco de ph =10,35? [1½ PUNTO] b) Qué es una disolución
Química DEPARTAMENTO DE FÍSICA E QUÍMICA Equilibrio ácido-base 25-02-08 Nombre: Cuestiones y problemas 1. a) Qué concentración tiene una disolución de amoníaco de ph =10,35? [1½ PUNTO] b) Qué es una disolución
GUÍA DE EJERCICIOS N 4: Ácido-base, neutralización y buffer. 1.- Defina los ácidos y bases según las teorías ácido-base de Arrhenius y Brönsted-Lowry
 1 GUÍA DE EJERCICIOS N 4: Ácido-base, neutralización y buffer PRIMERA PARTE: Ejercicios de desarrollo. 1.- Defina los ácidos y bases según las teorías ácido-base de Arrhenius y Brönsted-Lowry 2.- Defina
1 GUÍA DE EJERCICIOS N 4: Ácido-base, neutralización y buffer PRIMERA PARTE: Ejercicios de desarrollo. 1.- Defina los ácidos y bases según las teorías ácido-base de Arrhenius y Brönsted-Lowry 2.- Defina
Objetivos
 CONTENIDO CAPITULO I Transporte a travbs de membranas y epitelios... 1-1 Objetivos... 1-1.. Introduccion... 1-3 Movimientos de solutos... 1-4 Flujo de disolvente... 1-7 Intercambio ionicos a través de
CONTENIDO CAPITULO I Transporte a travbs de membranas y epitelios... 1-1 Objetivos... 1-1.. Introduccion... 1-3 Movimientos de solutos... 1-4 Flujo de disolvente... 1-7 Intercambio ionicos a través de
UNIDAD RENAL. Anatomía y fisiología del aparato urinario. LEI. JAVIER CESPEDES MATA ME.
 UNIDAD RENAL Anatomía y fisiología del aparato urinario. LEI. JAVIER CESPEDES MATA ME. Funciones de la nefrona Filtración glomerular. Reabsorción glomerular. Secreción tubular. Excresion Tasa de filtración
UNIDAD RENAL Anatomía y fisiología del aparato urinario. LEI. JAVIER CESPEDES MATA ME. Funciones de la nefrona Filtración glomerular. Reabsorción glomerular. Secreción tubular. Excresion Tasa de filtración
QUÍMICA. Calcular la molaridad de una solución que contiene 456 gr de cloruro de sodio en 125 ml de solución.
 UNIDAD I LIQUIDOS VITALES QUÍMICA Concentración (molar y normal) Calcular la molaridad de una solución que contiene 456 gr de cloruro de sodio en 125 ml de solución. Cuantos gramos de ácido nítrico debo
UNIDAD I LIQUIDOS VITALES QUÍMICA Concentración (molar y normal) Calcular la molaridad de una solución que contiene 456 gr de cloruro de sodio en 125 ml de solución. Cuantos gramos de ácido nítrico debo
ACIDIFICANTES EN ALIMENTOS PARA GATOS
 ACIDIFICANTES EN ALIMENTOS PARA GATOS Flávia Maria de Oliveira Borges Saad Médica Veterinária, MSc., PhD Nutrição Animal Universidade Federal de Lavras - DZO - UFLA POR QUÉ UTILIZAR ACIDIFICANTES EN ALIMENTOS
ACIDIFICANTES EN ALIMENTOS PARA GATOS Flávia Maria de Oliveira Borges Saad Médica Veterinária, MSc., PhD Nutrição Animal Universidade Federal de Lavras - DZO - UFLA POR QUÉ UTILIZAR ACIDIFICANTES EN ALIMENTOS
Equipo 5 Sistemas amortiguadores
 Equipo 5 Sistemas amortiguadores Anaya Gutiérrez Erick Jesús García García Esmira Jazmin García Montesinos Ana Paola Gonzales Galindo Jesús Antonio Jóse Ruíz Diego Mendez Silva Clara Anaid Yépez Cancino
Equipo 5 Sistemas amortiguadores Anaya Gutiérrez Erick Jesús García García Esmira Jazmin García Montesinos Ana Paola Gonzales Galindo Jesús Antonio Jóse Ruíz Diego Mendez Silva Clara Anaid Yépez Cancino
UNIDAD 7: LA EXCRECIÓN URINARIA
 UNIDAD 7: LA EXCRECIÓN URINARIA Lee atentamente. 1. LA EXCRECIÓN Las células de nuestro cuerpo producen desechos, sustancias nocivas para el organismo, que deben ser expulsadas al exterior. El dióxido
UNIDAD 7: LA EXCRECIÓN URINARIA Lee atentamente. 1. LA EXCRECIÓN Las células de nuestro cuerpo producen desechos, sustancias nocivas para el organismo, que deben ser expulsadas al exterior. El dióxido
DETERMINACIÓN PORCENTUAL DE NaHCO 3 EN TABLETAS EFERVESCENTES
 DETERMINACIÓN PORCENTUAL DE NaHCO EN TABLETAS EFERVESCENTES Objetivos. Evaluar la importancia de las reacciones de formación de gases en análisis cuantitativo.. Determinar el contenido de bicarbonato de
DETERMINACIÓN PORCENTUAL DE NaHCO EN TABLETAS EFERVESCENTES Objetivos. Evaluar la importancia de las reacciones de formación de gases en análisis cuantitativo.. Determinar el contenido de bicarbonato de
Comprobar la reversibilidad de algunas reacciones químicas, por medio de la modificación de las condiciones de equilibrio.
 Laboratorio de Análisis Cuantitativo Hoja 1 de 5 Elaboró: M.C. Yolanda Ángeles Cruz 1. OBJETIVOS. Demostrar que un estado de equilibrio puede alcanzarse haciendo reaccionar a los reactivos para formar
Laboratorio de Análisis Cuantitativo Hoja 1 de 5 Elaboró: M.C. Yolanda Ángeles Cruz 1. OBJETIVOS. Demostrar que un estado de equilibrio puede alcanzarse haciendo reaccionar a los reactivos para formar
PROBLEMAS RESUELTOS SELECTIVIDAD ANDALUCÍA 2004 QUÍMICA TEMA 6: EQUILIBRIOS ÁCIDO-BASE
 PROBLEMAS RESUELTOS SELECTIVIDAD ANDALUCÍA 2004 QUÍMICA TEMA 6: EQUILIBRIOS ÁCIDO-BASE Junio, Ejercicio 3, Opción A Junio, Ejercicio 5, Opción B Reserva 1, Ejercicio 6, Opción A Reserva 1, Ejercicio 4,
PROBLEMAS RESUELTOS SELECTIVIDAD ANDALUCÍA 2004 QUÍMICA TEMA 6: EQUILIBRIOS ÁCIDO-BASE Junio, Ejercicio 3, Opción A Junio, Ejercicio 5, Opción B Reserva 1, Ejercicio 6, Opción A Reserva 1, Ejercicio 4,
Guía para el docente
 Guía para el docente Descripción curricular: - Nivel: 1.º medio - Subsector: Biología - Unidad temática: - Palabras clave: nefrón, cápsula de Bowman, túbulo contorneado proximal y distal, asa de Henle,
Guía para el docente Descripción curricular: - Nivel: 1.º medio - Subsector: Biología - Unidad temática: - Palabras clave: nefrón, cápsula de Bowman, túbulo contorneado proximal y distal, asa de Henle,
Regulación de las funciones corporales y homeostasis
 Eje temático: Regulación de las funciones corporales y homeostasis Contenido: Homeostasis y función renal Nivel: Tercero medio Regulación de las funciones corporales y homeostasis A pesar de las constantes
Eje temático: Regulación de las funciones corporales y homeostasis Contenido: Homeostasis y función renal Nivel: Tercero medio Regulación de las funciones corporales y homeostasis A pesar de las constantes
Trabajo Práctico N o 2 BUFFERS BIOLÓGICOS
 1 Trabajo Práctico N o 2 BUFFERS BIOLÓGICOS OBJETIVOS A partir de la ecuación de HendersonHasselbach calcular la concentración de (H + ),(Aceptor de H + ) o (Dador de H + ). Conocer cómo se mantiene el
1 Trabajo Práctico N o 2 BUFFERS BIOLÓGICOS OBJETIVOS A partir de la ecuación de HendersonHasselbach calcular la concentración de (H + ),(Aceptor de H + ) o (Dador de H + ). Conocer cómo se mantiene el
HOJA DE PROBLEMAS 7: ENUNCIADOS
 Tema: ÁCIDOS Y BASES HOJA DE PROBLEMAS 7: ENUNCIADOS 1. ( ) Calcular el ph de las siguientes disoluciones: a) ácido clorhídrico 0,2 N; b) ácido sulfúrico 0,05 M. 2. ( ) Calcular el ph de una disolución
Tema: ÁCIDOS Y BASES HOJA DE PROBLEMAS 7: ENUNCIADOS 1. ( ) Calcular el ph de las siguientes disoluciones: a) ácido clorhídrico 0,2 N; b) ácido sulfúrico 0,05 M. 2. ( ) Calcular el ph de una disolución
Regulación de (H+) Equilibrio ácido-básico
 Regulación de (H+) Equilibrio ácido-básico Introducción v CO2 es generado dentro de las células à Forma H2CO3 (ácido carbónico) al disolverse en agua Introducción ácidos no volátiles v Ácidos no volátiles:
Regulación de (H+) Equilibrio ácido-básico Introducción v CO2 es generado dentro de las células à Forma H2CO3 (ácido carbónico) al disolverse en agua Introducción ácidos no volátiles v Ácidos no volátiles:
Pauta de corrección guía IV medio Homeostasis
 Pauta de corrección guía IV medio Homeostasis Actividad 1.- Registra la temperatura ambiental en un día cada una hora. Así mismo registra la temperatura corporal que tu cuerpo tiene en cada hora. Grafica
Pauta de corrección guía IV medio Homeostasis Actividad 1.- Registra la temperatura ambiental en un día cada una hora. Así mismo registra la temperatura corporal que tu cuerpo tiene en cada hora. Grafica
PROBLEMAS RESUELTOS SELECTIVIDAD ANDALUCÍA QUÍMICA TEMA 6: EQUILIBRIOS ÁCIDO-BASE.
 PROBLEMAS RESUELTOS SELECTIVIDAD ANDALUCÍA 000 QUÍMICA TEMA 6: EQUILIBRIOS ÁCIDO-BASE http://emestrada.wordpress.com Complete los siguientes equilibrios ácido-base identificando, de forma razonada, los
PROBLEMAS RESUELTOS SELECTIVIDAD ANDALUCÍA 000 QUÍMICA TEMA 6: EQUILIBRIOS ÁCIDO-BASE http://emestrada.wordpress.com Complete los siguientes equilibrios ácido-base identificando, de forma razonada, los
TEMA 1: LA NATURALEZA BÁSICA DE LA MATERIA QUÉ ELEMENTOS INTEGRAN LA MATERIA VIVA?
 TEMA 1: LA NATURALEZA BÁSICA DE LA MATERIA QUÉ ELEMENTOS INTEGRAN LA MATERIA VIVA? Concepto de Bioquímica Concepto de Bioelemento Los bioelementos, también conocidos como elementos biogénicos, son los
TEMA 1: LA NATURALEZA BÁSICA DE LA MATERIA QUÉ ELEMENTOS INTEGRAN LA MATERIA VIVA? Concepto de Bioquímica Concepto de Bioelemento Los bioelementos, también conocidos como elementos biogénicos, son los
5. PROBLEMAS SOBRE EQUILIBRIOS ACIDO BASE & AMINOACIDOS
 Departamento de Bioquímica y Biología Molecular ph y equilibrios acido-base 5. PROBLEMAS SOBRE EQUILIBRIOS ACIDO BASE & AMINOACIDOS Para realizar estos problemas se aconseja consultar una tabla con las
Departamento de Bioquímica y Biología Molecular ph y equilibrios acido-base 5. PROBLEMAS SOBRE EQUILIBRIOS ACIDO BASE & AMINOACIDOS Para realizar estos problemas se aconseja consultar una tabla con las
Escala de ph. Concentración de H + en Eq/L
 Escala de ph ph Concentración de H + en Eq/L 1 0.1 2 0.01 3 0.001 4 0.0001 5 0.00001 6 0.000001 7 0.0000001 7.4 0.0000004 8 0.00000001 9 0.000000001 ÁLCALI: sustancia capaz de aceptar un H + ÁCIDO: sustancia
Escala de ph ph Concentración de H + en Eq/L 1 0.1 2 0.01 3 0.001 4 0.0001 5 0.00001 6 0.000001 7 0.0000001 7.4 0.0000004 8 0.00000001 9 0.000000001 ÁLCALI: sustancia capaz de aceptar un H + ÁCIDO: sustancia
Química P.A.U. ÁCIDOS Y BASES 1 ÁCIDOS Y BASES. Rta.: a) [NH₃]ₑ = 0,0096 mol/dm³; [OH ]ₑ = [NH₄+]ₑ = 4,2 10 ⁴ mol/dm³; b) ph = 10,6; K = 1,8 10 ⁵
![Química P.A.U. ÁCIDOS Y BASES 1 ÁCIDOS Y BASES. Rta.: a) [NH₃]ₑ = 0,0096 mol/dm³; [OH ]ₑ = [NH₄+]ₑ = 4,2 10 ⁴ mol/dm³; b) ph = 10,6; K = 1,8 10 ⁵ Química P.A.U. ÁCIDOS Y BASES 1 ÁCIDOS Y BASES. Rta.: a) [NH₃]ₑ = 0,0096 mol/dm³; [OH ]ₑ = [NH₄+]ₑ = 4,2 10 ⁴ mol/dm³; b) ph = 10,6; K = 1,8 10 ⁵](/thumbs/54/35035616.jpg) Química P.A.U. ÁCIDOS Y BASES 1 ÁCIDOS Y BASES PROBLEMAS ÁCIDO/BASE DÉBIL 1. Una disolución de amonuíaco de concentración 0,01 mol/dm³ está ionizada en un 4,2 %. a) Escribe la reacción de disociación y
Química P.A.U. ÁCIDOS Y BASES 1 ÁCIDOS Y BASES PROBLEMAS ÁCIDO/BASE DÉBIL 1. Una disolución de amonuíaco de concentración 0,01 mol/dm³ está ionizada en un 4,2 %. a) Escribe la reacción de disociación y
El CO2, en presencia de anhidrasa carbónica (AC), se hidrata de la siguiente forma: CO2 + H2O <------> CO3H2 < > H+ + HCO3-
 Equilibro Acido Base El equilibrio ácido-base requiere la integración de tres sistemas orgánicos, el hígado, los pulmones y el riñón. En resumen, el hígado metaboliza las proteínas produciendo iones hidrógeno
Equilibro Acido Base El equilibrio ácido-base requiere la integración de tres sistemas orgánicos, el hígado, los pulmones y el riñón. En resumen, el hígado metaboliza las proteínas produciendo iones hidrógeno
Guía del docente. 1. Descripción curricular:
 Guía del docente. 1. Descripción curricular: - Nivel: 3º medio. - Subsector: Ciencias Químicas. - Unidad temática: Cinética química. - Palabras claves: reactividad, velocidad de reacción, cinética química,
Guía del docente. 1. Descripción curricular: - Nivel: 3º medio. - Subsector: Ciencias Químicas. - Unidad temática: Cinética química. - Palabras claves: reactividad, velocidad de reacción, cinética química,
 Minino de Cheshire, podrías decirme, por favor, qué camino debo seguir para salir de aquí? Esto depende en gran parte del si>o al que quieras llegar - dijo el Gato. - - No me importa mucho el si>o... -
Minino de Cheshire, podrías decirme, por favor, qué camino debo seguir para salir de aquí? Esto depende en gran parte del si>o al que quieras llegar - dijo el Gato. - - No me importa mucho el si>o... -
Dra. María Eugenia Victoria Bianchi Dr. Gustavo Borda Dra Marcela Young. Estudiantes por Concurso según Resolución 1311/95-C-D.
 Dra. María Eugenia Victoria Bianchi Dr. Gustavo Borda Dra Marcela Young. Estudiantes por Concurso según Resolución 1311/95-C-D. Vallejos Javier Serial Marcos Sebastián Rausch Ricardo Simón Laura Solé Juan
Dra. María Eugenia Victoria Bianchi Dr. Gustavo Borda Dra Marcela Young. Estudiantes por Concurso según Resolución 1311/95-C-D. Vallejos Javier Serial Marcos Sebastián Rausch Ricardo Simón Laura Solé Juan
Biología y Geología 1º Bachillerato
 TEMA 14: TRANSPORTE Y EXCRECIÓN EN ANIMALES 1. El transporte de sustancias en los animales 1.0. Introducción. 1.1. Animales sencillos 1.2. Animales más complejos: aparatos circulatorios 1.2.1. Componentes
TEMA 14: TRANSPORTE Y EXCRECIÓN EN ANIMALES 1. El transporte de sustancias en los animales 1.0. Introducción. 1.1. Animales sencillos 1.2. Animales más complejos: aparatos circulatorios 1.2.1. Componentes
LABORATORIO Nº 3 Determinación de la capacidad amortiguadora de un buffer
 LABORATORIO Nº 3 - Es obligatorio la asistencia al práctico con túnica y lentes de seguridad. - El protocolo de la práctica y el fundamento teórico de la misma deben haber sido leídos por el estudiante
LABORATORIO Nº 3 - Es obligatorio la asistencia al práctico con túnica y lentes de seguridad. - El protocolo de la práctica y el fundamento teórico de la misma deben haber sido leídos por el estudiante
Problemas resueltos de ácidos y bases.
 Problemas resueltos de ácidos y bases. 5 de abril de 2011 1. Una disolución acuosa de ácido metanoico (fórmico), cuya constante de disociación es K d 1, 77 10 4, tiene un grado de disociación α 0,0412.
Problemas resueltos de ácidos y bases. 5 de abril de 2011 1. Una disolución acuosa de ácido metanoico (fórmico), cuya constante de disociación es K d 1, 77 10 4, tiene un grado de disociación α 0,0412.
GUÍA N 5: Soluciones Buffer o amortiguadoras
 1 PRIMERA PARTE: Ejercicios de desarrollo. 1.- Defina los siguientes términos: a) Buffer ácido b) Buffer básico c) Buffer salino d) Concentración de un buffer e) Rango de amortiguación f) Capacidad amortiguadora
1 PRIMERA PARTE: Ejercicios de desarrollo. 1.- Defina los siguientes términos: a) Buffer ácido b) Buffer básico c) Buffer salino d) Concentración de un buffer e) Rango de amortiguación f) Capacidad amortiguadora
GUIA DE ESTUDIO PARA EL EXAMEN DE ADMISIÓN A LA MAESTRIA EN BIOTECNOLOGÍA BIOQUÍMICA
 GUIA DE ESTUDIO PARA EL EXAMEN DE ADMISIÓN A LA MAESTRIA EN BIOTECNOLOGÍA 2015 BIOQUÍMICA 1. Compuestos orgánicos. 1.1 Estructura de los compuestos orgánicos. 1.2 Grupos funcionales y uniones. 2. Estructura
GUIA DE ESTUDIO PARA EL EXAMEN DE ADMISIÓN A LA MAESTRIA EN BIOTECNOLOGÍA 2015 BIOQUÍMICA 1. Compuestos orgánicos. 1.1 Estructura de los compuestos orgánicos. 1.2 Grupos funcionales y uniones. 2. Estructura
