TEMA 2: LA MATERIA: CÓMO SE PRESENTA?
|
|
|
- José Miguel Piñeiro Quintero
- hace 7 años
- Vistas:
Transcripción
1 TEMA 2: LA MATERIA: CÓMO SE PRESENTA? 1.- La materia: sustancias puras y mezclas Recordatorio Sustancias puras Mezclas Cómo distinguir un coloide de una mezcla homogénea. 2.- Separación de mezclas. 3.- Mezclas homogéneas: disoluciones Modos de expresar la concentración de las disoluciones Porcentaje en masa Porcentaje en volumen Concentración en masa Solubilidad. 4.- Diversidad de la materia: teoría-atómico molecular de Dalton Definiciones La teoría atómico molecular de Dalton. 1.- LA MATERIA: SUSTANCIAS PURAS Y MEZCLAS Recordatorio Materia es todo lo que ocupa un lugar en el espacio y tiene masa La materia la podemos encontrar en tres estados: Sólido: un cuerpo en estado sólido se caracteriza porque opone resistencia a cambios de forma y volumen. Líquido: un cuerpo en estado líquido se caracteriza porque el volumen que ocupa es constante si no se alteran las condiciones de presión y temperatura y su forma es esférica, sin embargo debido a la gravedad la forma de un líquido queda definida por el recipiente que lo contiene. Gaseoso: un cuerpo en estado gaseoso se caracteriza porque no tiene forma ni volumen propio. La materia tiene dos tipos de propiedades: - Propiedades generales: son comunes a toda la materia y no sirven para identificar las sustancias (masa, volumen, temperatura...). - Propiedades características: son características de la materia, por lo que sirven para identificar una sustancia (punto de ebullición, densidad...). Tema 2. La materia: cómo se presenta? Página 1
2 Clasificación de la materia Sustancias Puras Elementos Compuestos Materia Mezclas homogéneas Mezclas Mezclas heterogéneas Coloides Sustancias puras Las sustancias puras son las que no se pueden descomponer en otras sustancias más sencillas mediante procedimientos físicos, ya que están formadas por partículas del mismo tipo. Un elemento es una sustancia pura que no puede descomponerse en otras sustancias más sencillas ni mediante procedimientos físicos ni mediante procedimientos químicos. Un compuesto es una sustancia pura que aunque no pueda descomponerse en otras sustancias más sencillas mediante procedimientos físicos, sí puede hacerlo mediante procedimientos químicos Mezclas Son sustancias formadas por la combinación de varias sustancias puras que se pueden separar mediante procedimientos físicos. Hay tres tipos de mezclas: - Mezcla homogénea: es aquella en la que no se distinguen los componentes que la forman. Ejemplos: puré, azúcar o sal disuelta en agua - Mezcla heterogénea: es aquella en la que se distinguen los componentes que la forman. Ejemplos: agua y aceite, una pizza... - Coloide: es una mezcla heterogénea que a simple vista parece homogénea. Ejemplos: la niebla, las emulsiones... Las emulsiones son mezclas de sustancias inmiscibles (es decir, que en principio no se puede mezclar). La mezcla de este tipo de sustancias se consigue al añadir una tercera sustancia llamada emulsionante. Un ejemplo de emulsión es la mayonesa casera que se hace al añadir al huevo aceite mientras se bate. En principio el agua que contiene la clara del huevo y el aceite que se añade para hacerla no se puede mezclar, sin embargo la yema del huevo contiene una sustancia emulsionante llamada lecitina gracias a la cual el agua y el aceite termina mezclándose Cómo distinguir una mezcla homogénea de un coloide Los coloides cumplen una propiedad llamada efecto Tyndall que no cumplen las mezclas homogéneas. Este efecto consiste en que cuando un rayo de luz se proyecta sobre un coloide este se refleja en las partículas que forman el coloide y se hacen visibles. Tema 2. La materia: cómo se presenta? Página 2
3 Coloide Mezcla homogénea 2.- SEPARACIÓN DE MEZCLAS Las mezclas son sustancias que están formadas por varios componentes que pueden separarse por procedimientos físicos. En esta pregunta estudiaremos algunos de esos procedimientos: Criba Tipos de mezclas: heterogéneas entre sólidos de distinto tamaño. Ejemplo: una mezcla de arena y piedras. Procedimiento: se pasa la mezcla por una criba o tamiz cuyos orificios dejarán pasar las partículas más pequeñas y retendrán las más grandes. Se utiliza para separar el café recién cogido. Filtración Tipos de mezclas: este método sirve para separar los componentes de una mezcla heterogénea entre un sólido y un líquido en el que no se puede disolver. Ejemplo: agua y arena. Procedimiento: este método consiste en pasar la mezcla por un filtro cuyos poros dejarán pasar únicamente el líquido y retendrá al componente sólido. Cristalización Tipos de mezclas: este método se utiliza para separar los componentes de una mezcla homogénea de un sólido disuelto en un líquido en el que queda disuelto. Ejemplo: una mezcla de azúcar disuelta en agua. Procedimiento: este método consiste en dejar reposar la mezcla hasta que la temperatura ambiente evapore el líquido y quede en el recipiente la sustancia sólida formando cristales. La cristalización es el método que se utiliza en las salinas para obtener la sal. Separación magnética Tipos de mezclas: este procedimiento se utiliza para separar los componentes de una mezcla heterogénea en la que uno de los componentes es un metal (habitualmente hierro, cobalto o níquel). Ejemplos: una mezcla de hierro y madera, limaduras de hierro y arena Procedimiento: consiste en pasar un imán por encima de la mezcla que atraerá a la sustancia metálica dejándola separada del resto de la mezcla. Decantación Tipos de mezclas: este método se utiliza para separar los componentes de una mezcla heterogénea entre dos o más líquidos inmiscibles (que no se pueden mezclar), ya que tienen distinta densidad (por lo tanto los líquidos quedarán unos encimas de otros formando capas). Ejemplo: agua y aceite. Tema 2. La materia: cómo se presenta? Página 3
4 Procedimiento: este método consiste en introducir la mezcla en un embudo especial llamado embudo de decantación y cuando los líquidos estén perfectamente separados se abre la válvula inferior del embudo para que vaya saliendo el primer líquido. Cuando este haya salido se cierra la válvula quedando los demás líquidos dentro del embudo. Si quedan varios líquidos en él se repetiría el procedimiento de la válvula. Destilación Tipos de mezclas: este método se utiliza para separar los componentes de una mezcla homogénea de dos o más líquidos que hierven a temperaturas muy diferentes, como por ejemplo el agua y el alcohol. Procedimiento: este método consiste en calentar la mezcla hasta que alcance la temperatura a la que hierve la sustancia con menor punto de ebullición. Esa sustancia se convierte entonces en vapor gaseoso que se hace pasar por un tubo refrigerante que lo enfría convirtiéndolo en líquido de nuevo que se recogerá en otro recipiente quedando así separada de la otra sustancia. Cromatografía Tipos de mezclas: este método sirve para separar los componentes de una mezcla homogénea en la que cada componente tarda un tiempo distinto en disolverse en una sustancia determinada, como por ejemplo los componentes de la tinta de un rotulador. Procedimiento: este método consiste en poner en contacto la mezcla con la sustancia en la que cada componente de la mezcla tarda un tiempo diferente en disolverse, de manera que cada una se irá separando conforme vaya disolviéndose. 3.- MEZCLAS HOMOGÉNEAS: DISOLUCIONES Una disolución es una mezcla homogénea de dos o más componentes. En una disolución se distinguen: - Un disolvente: es de todos los componentes de la disolución el que se encuentra en mayor proporción y en el que se disuelven el resto de componentes. - Uno o más solutos: son los componentes de la disolución que se encuentran en menor proporción y que están disueltos en el disolvente. Ejemplo: imagina que mezclamos un litro de agua y una cucharada de azúcar. a) Quién crees que será el disolvente de la disolución que se forma? El agua, ya que se encuentra en mayor proporción que el azúcar y además el azúcar se disolverá en ella. b) Quién será el soluto? El azúcar, porque se encuentra en menor proporción que el agua y es la sustancia que se disuelve en la otra. Ejemplo: imagina un recipiente que contiene agua en la que hay disueltos azúcar y sal. a) Es una disolución? Sí porque es una mezcla homogénea. Tema 2. La materia: cómo se presenta? Página 4
5 b) Nombra los componentes de la misma. Agua, azúcar y sal c) Di cuál es el disolvente y cuáles son los solutos. El disolvente es el agua, porque es la sustancia en la que se encuentran disueltas las demás. Los solutos son el azúcar y la sal Modos de expresar la concentración de las disoluciones La concentración de una disolución es una información que nos dice la cantidad de solutos que hay disueltos en una cantidad determinada de la disolución. Ejemplo: la concentración de una disolución de sal en agua será la información que nos diga si la disolución está poco salada o muy salada, lo cual dependerá de la cantidad de sal que hayamos utilizado y la cantidad de disolución que tengamos. Importancia de la concentración de una disolución: para obtener una disolución determinada es importante mezclar unas cantidades concretas de los componentes que la forman, ya que si se alteran esas cantidades no se obtendría exactamente la disolución que buscamos. Por ejemplo, el suero fisiológico es una disolución de sal en agua destilada en la que para obtener 1000 gramos de suero hay que disolver exactamente 9 gramos de sal en 991 gramos de agua destilada. Si en vez de 9 gramos disolvemos otra cantidad de sal (por ejemplo 40 gramos) en 960 gramos de agua destilada, lo que obtenemos no será suero fisiológico. La concentración de una disolución se puede expresar de tres formas: utilizando el porcentaje en masa, utilizando el porcentaje en volumen y utilizando la concentración en masa Porcentaje en masa Nos indica los gramos de soluto que hay en 100 gramos de disolución. Este porcentaje se calcula con la siguiente fórmula: % en masa de soluto = Ejemplo: se ha preparado una disolución añadiéndole a 100 gramos de agua, 10 gramos de azúcar y 5 gramos de sal. a) Quiénes son el disolvente y los solutos? El disolvente es el agua porque es la sustancia que se encuentra en mayor proporción. Los solutos son el azúcar y la sal que son las sustancias que se encuentran en menor proporción. b) Calcula el porcentaje en masa de azúcar. % en masa de soluto = masa azúcar % en masa de azúcar = Tema 2. La materia: cómo se presenta? Página 5
6 Calculamos la masa de la disolución: Masa disolución = masa disolvente + s Masa disolución = Masa disolución = 115 gramos 10 % en masa de azúcar = 115 % en masa de azúcar = 8,7 % c) Calcula el porcentaje en masa de sal. % en masa de soluto = masa sal % en masa de sal = 5 % en masa de sal = 115 % en masa de sal = 4,3 % Porcentaje en volumen Nos indica el volumen de soluto que hay en 100 unidades de volumen de disolución. Se calcula con la siguiente fórmula: volumen soluto % en volumen de soluto = Ejemplo: se ha preparado una disolución mezclando 10 ml de alcohol y 100 ml de agua. Calcula el porcentaje en volumen de alcohol. volumen soluto % en volumen de soluto = Calculamos el volumen de la disolución: Volumen disolución = volumen disolvente + volumen solutos Volumen disolución = Volumen disolución = 110 ml volumen alcohol % en volumen de alcohol = Tema 2. La materia: cómo se presenta? Página 6
7 3.4.- Concentración en masa 10 % en volumen de alcohol = 110 % en volumen de alcohol = 9,09 % Nos indica la masa de soluto que hay en un volumen determinado de disolución. Se puede calcular con la siguiente fórmula: Concentración en masa de soluto = La concentración en masa de soluto se mide en g. ml Ejemplo: se ha preparado una disolución disolviendo 5 g de azúcar en agua hasta tener un volumen total de 100 ml. Calcula la concentración en masa de azúcar. Concentración en masa de soluto = masa Concentración en masa de azúcar = volumen azúcar disolución Concentración en masa de azúcar = 5 10 Concentración en masa de azúcar = 0,05 g ml Observación: no confundir la densidad de una sustancia con la concentración en masa en una disolución. La densidad de una sustancia es una propiedad de la sustancia entera, mientras que la concentración en masa es una propiedad que relaciona la cantidad de una sustancia con el volumen de otra sustancia Solubilidad Recordatorio: se llama solubilidad en agua de una sustancia a la cantidad máxima de esa sustancia que se puede disolver en 100 gramos de agua. Las disoluciones, según la cantidad de soluto que hay disuelto en una cantidad determinada de disolvente, se clasifican en: Disoluciones diluidas: son aquellas en las que hay poco soluto en comparación con la cantidad de disolvente. Disoluciones concentradas: son aquellas en las que hay mucha cantidad de soluto en comparación con la cantidad de disolvente. Disoluciones saturadas: son aquellas que no admiten más cantidad de soluto. Tema 2. La materia: cómo se presenta? Página 7
8 Solubilidad en los sólidos Cuando el soluto que hay disuelto en agua es un sólido, la solubilidad de ese soluto aumenta al aumentar la temperatura de la disolución. Ejemplo: sabemos que la solubilidad de la sal es 36 g; es decir, en 100 g de agua se pueden disolver como máximo 36 g de sal cuando la temperatura de la disolución es de 20 ºC. Se puede comprobar que si la disolución se calienta hasta alcanzar una temperatura de 100 ºC, entonces se pueden disolver más de 40 g de sal. Solubilidad en los gases Cuando el soluto es un gas su solubilidad disminuye a medida que aumenta la temperatura. Así por ejemplo, si tenemos una disolución saturada en la que el soluto es un gas y la calentamos, parte del gas tiende a escapar de la disolución. La presencia de burbujas en la disolución es señal de que el gas escapa de ella. Ejemplo: el agua caliente que vierten las fábricas a los ríos y embalses, a veces hacen que la temperatura de estos aumente y como consecuencia la solubilidad del oxígeno que hay disuelto en ellos disminuya, por lo que parte de este oxígeno se libera dejando menos cantidad para que los seres vivos que habitan en estos medios acuáticos puedan respirar y muchos de ellos mueren. 4.- DIVERSIDAD DE LA MATERIA: TEORÍA ATÓMICO-MOLECULAR DE DALTON Definiciones Átomo: es la parte más pequeña en la que se puede dividir la materia. Molécula: es la unión de varios átomos que pueden ser del mismo elemento o de distintos elementos. Notas: - Existen tantos átomos diferentes como elementos existen en la naturaleza. Así hay átomos de oxígeno, de carbono, de hierro - Ejemplos de moléculas: la unión de dos átomos de hidrógeno y uno de oxígeno forman una molécula de agua. Otro ejemplo sería la unión de tres átomos de hidrógeno y uno de nitrógeno que da lugar a la molécula de amoniaco La teoría atómico-molecular de Dalton Dalton fue uno de los primeros científicos en describir con acierto la materia. Los estudios que llevó a cabo le permitieron elaborar una teoría en la que detalla cómo es por dentro la materia, llamada teoría atómico-molecular de Dalton y que se resume en estos tres postulados: La materia está formada por átomos, que son partículas indivisibles e indestructibles. Todos los átomos del mismo elemento tienen la misma masa y propiedades y son diferentes a las de los átomos de cualquier otro elemento. Los compuestos son combinaciones de átomos de diversos elementos. FIN DEL TEMA Tema 2. La materia: cómo se presenta? Página 8
TEMA 2: DIVERSIDAD DE LA MATERIA
 TEMA 2: DIVERSIDAD DE LA MATERIA 1.- La materia: sustancias puras y mezclas. 1.1.- La materia. 1.1.1.- Estados de agregación de la materia. 1.1.2.- Propiedades generales y características de la materia.
TEMA 2: DIVERSIDAD DE LA MATERIA 1.- La materia: sustancias puras y mezclas. 1.1.- La materia. 1.1.1.- Estados de agregación de la materia. 1.1.2.- Propiedades generales y características de la materia.
TEMA 2: Diversidad de la materia. T_m[ 2: Div_rsi^[^ ^_ l[ m[t_ri[ 1
 TEMA 2: Diversidad de la materia T_m[ 2: Div_rsi^[^ ^_ l[ m[t_ri[ 1 ESQUEMA DE LA UNIDAD 1.- La materia: sustancias puras y mezclas. 1.1.- La materia. 1.1.1.- Estados de agregación de la materia. 1.1.2.-
TEMA 2: Diversidad de la materia T_m[ 2: Div_rsi^[^ ^_ l[ m[t_ri[ 1 ESQUEMA DE LA UNIDAD 1.- La materia: sustancias puras y mezclas. 1.1.- La materia. 1.1.1.- Estados de agregación de la materia. 1.1.2.-
1. La materia: sustancias puras y mezclas
 RESUMEN de la UNIDAD 3. DIVERSIDAD DE LA MATERIA 1. La materia: sustancias puras y mezclas La principal clasificación que se hace de la materia es en sustancias puras y mezclas. Las sustancias puras tienen
RESUMEN de la UNIDAD 3. DIVERSIDAD DE LA MATERIA 1. La materia: sustancias puras y mezclas La principal clasificación que se hace de la materia es en sustancias puras y mezclas. Las sustancias puras tienen
Tema 3 CLASIFICACIÓN DE LA MATERIA
 Clasificación de la materia 1 Tema 3 CLASIFICACIÓN DE LA MATERIA 1. ÁTOMOS Y MOLÉCULAS... 1 2. SUSTANCIAS PURAS Y MEZCLAS.... 2 2.1. SUSTANCIAS PURAS... 2 2.2. MEZCLAS... 2 3. SEPARACIÓN DE LOS COMPONENTES
Clasificación de la materia 1 Tema 3 CLASIFICACIÓN DE LA MATERIA 1. ÁTOMOS Y MOLÉCULAS... 1 2. SUSTANCIAS PURAS Y MEZCLAS.... 2 2.1. SUSTANCIAS PURAS... 2 2.2. MEZCLAS... 2 3. SEPARACIÓN DE LOS COMPONENTES
Todo lo que vemos es materia
 Todo lo que vemos es materia CLASIFICACIÓN DE LA MATERIA La materia se presenta en la naturaleza en forma de sustancias puras y mezclas, de modo que podemos establecer la siguiente clasificación: CLASIFICACIÓN
Todo lo que vemos es materia CLASIFICACIÓN DE LA MATERIA La materia se presenta en la naturaleza en forma de sustancias puras y mezclas, de modo que podemos establecer la siguiente clasificación: CLASIFICACIÓN
1. MATERIA Y SU ASPECTO
 1. MATERIA Y SU ASPECTO El aspecto de un sistema material puede variar según el método de observación. Algunos sistemas materiales como la leche, la sangre o la mantequilla a simple vista parecen uniformes,
1. MATERIA Y SU ASPECTO El aspecto de un sistema material puede variar según el método de observación. Algunos sistemas materiales como la leche, la sangre o la mantequilla a simple vista parecen uniformes,
LA MATERIA Y SU DIVERSIDAD
 LA MATERIA Y SU DIVERSIDAD La materia es todo aquello que tiene masa y ocupa un espacio, es decir, tiene volumen. Propiedades generales La masa y el volumen, son comunes a toda la materia y no nos sirven
LA MATERIA Y SU DIVERSIDAD La materia es todo aquello que tiene masa y ocupa un espacio, es decir, tiene volumen. Propiedades generales La masa y el volumen, son comunes a toda la materia y no nos sirven
LA MATERIA, CÓMO SE PRESENTA
 LA MATERIA, CÓMO SE PRESENTA DEFINICIÓN DE MATERIA Materia es cualquier cosa que tiene masa y que ocupa un espacio. La materia es de lo que están hechos todos los objetos materiales Cuáles de los siguientes
LA MATERIA, CÓMO SE PRESENTA DEFINICIÓN DE MATERIA Materia es cualquier cosa que tiene masa y que ocupa un espacio. La materia es de lo que están hechos todos los objetos materiales Cuáles de los siguientes
TEMA 3: MEZCLAS, DISOLUCIONES Y SUSTANCIAS PURAS
 TEMA 3: MEZCLAS, DISOLUCIONES Y SUSTANCIAS PURAS 1. LA MATERIA Y SU ASPECTO Los sistemas materiales, formados por una o varias sustancias, pueden clasificarse en: - Sistemas materiales heterogéneos: presentan
TEMA 3: MEZCLAS, DISOLUCIONES Y SUSTANCIAS PURAS 1. LA MATERIA Y SU ASPECTO Los sistemas materiales, formados por una o varias sustancias, pueden clasificarse en: - Sistemas materiales heterogéneos: presentan
CLASIFICACIÓN DE LA MATERIA
 1. Clasificación de la materia por su aspecto CLASIFICACIÓN DE LA MATERIA La materia homogénea es la que presenta un aspecto uniforme, en la cual no se pueden distinguir a simple vista sus componentes.
1. Clasificación de la materia por su aspecto CLASIFICACIÓN DE LA MATERIA La materia homogénea es la que presenta un aspecto uniforme, en la cual no se pueden distinguir a simple vista sus componentes.
Tema 4: Sustancias puras y mezclas
 Tema 4: Sustancias puras y mezclas Esquema de trabajo: 1. Sustancias puras: Tipos: elementos y compuestos. 2. Mezclas: Tipos: Homogénea y heterogénea 3. Disoluciones Concepto Componentes Tipos de disoluciones
Tema 4: Sustancias puras y mezclas Esquema de trabajo: 1. Sustancias puras: Tipos: elementos y compuestos. 2. Mezclas: Tipos: Homogénea y heterogénea 3. Disoluciones Concepto Componentes Tipos de disoluciones
DIVERSIDAD DE LA MATERIA TEMA 3
 DIVERSIDAD DE LA MATERIA TEMA 3 Cómo se presenta la materia Sistema homogéneos Sistemas materiales que tienen el mismo aspecto en cualquiera de sus partes. Ejemplo: agua, leche, gelatina Sistemas heterogéneos
DIVERSIDAD DE LA MATERIA TEMA 3 Cómo se presenta la materia Sistema homogéneos Sistemas materiales que tienen el mismo aspecto en cualquiera de sus partes. Ejemplo: agua, leche, gelatina Sistemas heterogéneos
FÍSICA Y QUÍMICA 2º ESO Tema 2: LA MATERIA Mezclas y Soluciones. Sustancias puras y mezclas
 Sustancias puras y mezclas La materia que nos rodea es, en la mayoría de los casos, una mezcla de sustancias. Los científicos han intentado clasificar las sustancias desde el principio de los tiempos.
Sustancias puras y mezclas La materia que nos rodea es, en la mayoría de los casos, una mezcla de sustancias. Los científicos han intentado clasificar las sustancias desde el principio de los tiempos.
Materia. Mezclas Son aquellas que están formados por 2 o más sustancias.
 Qué es la materia? Materia Sustancias Puras Son aquellas que tienen una composición y propiedades DEFINIDAS. Mezclas Son aquellas que están formados por 2 o más sustancias. Elementos No se pueden separar
Qué es la materia? Materia Sustancias Puras Son aquellas que tienen una composición y propiedades DEFINIDAS. Mezclas Son aquellas que están formados por 2 o más sustancias. Elementos No se pueden separar
1.- Como se presenta la materia a) Sistemas homogéneos: b) Sistemas heterogéneos: 2.- Las mezclas: a) Mezclas heterogéneas:
 T3: Diversidad de la materia. 1.- Como se presenta la materia. a) Sistemas homogéneos: Son sistemas materiales que tienen el mismo aspecto en cualquiera de sus partes. Ejm: agua, aluminio, agua de mar
T3: Diversidad de la materia. 1.- Como se presenta la materia. a) Sistemas homogéneos: Son sistemas materiales que tienen el mismo aspecto en cualquiera de sus partes. Ejm: agua, aluminio, agua de mar
La materia se puede definir como todo aquello que tiene masa y ocupa un volumen.
 Tema 2: LA MATERIA Que es la materia? La materia se puede definir como todo aquello que tiene masa y ocupa un volumen. Clasificación de la materia (criterio: separación) Mezclas Sustancias puras Composición
Tema 2: LA MATERIA Que es la materia? La materia se puede definir como todo aquello que tiene masa y ocupa un volumen. Clasificación de la materia (criterio: separación) Mezclas Sustancias puras Composición
Materia es todo aquello que tiene masa y ocupa un lugar en el espacio (tiene volumen). La ciencia que estudia la materia es la Química.
 Alfonso García Materia es todo aquello que tiene masa y ocupa un lugar en el espacio (tiene volumen). La ciencia que estudia la materia es la Química. Un sistema material es una porción de materia. Ejemplos:
Alfonso García Materia es todo aquello que tiene masa y ocupa un lugar en el espacio (tiene volumen). La ciencia que estudia la materia es la Química. Un sistema material es una porción de materia. Ejemplos:
TEMA 3: Composición de la Materia
 TEMA 3: Composición de la Materia 1. Mezclas homogéneas y heterogéneas Una mezcla es una composición de varias sustancias con distintas propiedades. Distinguimos dos tipos de mezclas: Mezclas homogéneas:
TEMA 3: Composición de la Materia 1. Mezclas homogéneas y heterogéneas Una mezcla es una composición de varias sustancias con distintas propiedades. Distinguimos dos tipos de mezclas: Mezclas homogéneas:
TEMA 3: MEZCLAS REFLEXIÓN INICIAL
 TEMA 3: MEZCLAS REFLEXIÓN INICIAL El aire que respiramos es una mezcla de muchos gases: nitrógeno, oxígeno, dióxido de carbono Casi todos los materiales naturales o artificiales de nuestro entorno son
TEMA 3: MEZCLAS REFLEXIÓN INICIAL El aire que respiramos es una mezcla de muchos gases: nitrógeno, oxígeno, dióxido de carbono Casi todos los materiales naturales o artificiales de nuestro entorno son
Departamento Ciencias. Física y Química MATERIA. se clasifica en. SUSTANCIAS PURAS pueden ser. por métodos. físicos originan. Compuestos.
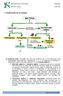 1. Clasificación de la materia MATERIA se clasifica en MEZCLAS pueden ser por métodos físicos originan SUSTANCIAS PURAS pueden ser Heterogéneas Homogéneas Compuestos como las Disoluciones formados por
1. Clasificación de la materia MATERIA se clasifica en MEZCLAS pueden ser por métodos físicos originan SUSTANCIAS PURAS pueden ser Heterogéneas Homogéneas Compuestos como las Disoluciones formados por
1. a) Define Sustancia pura: Es aquella que tiene la misma composición y las mismas propiedades. b) Define Disolución: Es una mezcla homogénea.
 Tema 3. LA MATERIA Y SU ASPECTO MEZCLAS Y SUSTANCIAS PURAS 1. a) Define Sustancia pura: Es aquella que tiene la misma composición y las mismas propiedades. b) Define Disolución: Es una mezcla homogénea.
Tema 3. LA MATERIA Y SU ASPECTO MEZCLAS Y SUSTANCIAS PURAS 1. a) Define Sustancia pura: Es aquella que tiene la misma composición y las mismas propiedades. b) Define Disolución: Es una mezcla homogénea.
Unidad 13. Mix. Sustancias puras y mezclas
 Unidad 13. Mix. Sustancias puras y mezclas La materia y su clasificación Recuerda que materia es todo aquello que tiene masa y ocupa un volumen. Según su composición la materia se puede clasificar en sustancias
Unidad 13. Mix. Sustancias puras y mezclas La materia y su clasificación Recuerda que materia es todo aquello que tiene masa y ocupa un volumen. Según su composición la materia se puede clasificar en sustancias
LA MATERIA. - Masa - Volumen -Energía - Carga eléctrica. Propiedades generales
 TEMA 2 La Materia LA MATERIA Propiedades generales - Masa - Volumen -Energía - Carga eléctrica Propiedades características - Densidad - Punto de fusión - Punto de ebullición -Conductividad eléctrica -
TEMA 2 La Materia LA MATERIA Propiedades generales - Masa - Volumen -Energía - Carga eléctrica Propiedades características - Densidad - Punto de fusión - Punto de ebullición -Conductividad eléctrica -
Una mezcla es un compuesto formado por varias sustancias con distintas propiedades
 COMPOSICIÓN DE LA MATERIA Mezclas homogéneas y heterogéneas Una mezcla es un compuesto formado por varias sustancias con distintas propiedades Algunos sistemas materiales como la leche a simple vista parecen
COMPOSICIÓN DE LA MATERIA Mezclas homogéneas y heterogéneas Una mezcla es un compuesto formado por varias sustancias con distintas propiedades Algunos sistemas materiales como la leche a simple vista parecen
TEMA 3.- Naturaleza de la. materia (II)
 TEMA 3.- Naturaleza de la 1.- Concepto de mezcla. Tipos. materia (II) ÍNDICE GENERAL 2.- Separación de los componentes de una mezcla. 2.1.- Separación de los componentes de mezclas heterogéneas. 2.1.1.-
TEMA 3.- Naturaleza de la 1.- Concepto de mezcla. Tipos. materia (II) ÍNDICE GENERAL 2.- Separación de los componentes de una mezcla. 2.1.- Separación de los componentes de mezclas heterogéneas. 2.1.1.-
Unidad 2. La materia
 Física y Química Unidad 2: La materia Unidad 2. La materia Índice de contenido 1. Estados de agregación de la materia...3 2. Cambios de estado...4 3. Clasificación de la materia...6 3.1.- Métodos de separación
Física y Química Unidad 2: La materia Unidad 2. La materia Índice de contenido 1. Estados de agregación de la materia...3 2. Cambios de estado...4 3. Clasificación de la materia...6 3.1.- Métodos de separación
MEZCLAS Y DISOLUCIONES. Física y Química 3º de E.S.O. IES Isidra de Guzmán
 MEZCLAS Y DISOLUCIONES Física y Química 3º de E.S.O. IES Isidra de Guzmán Introducción Ya sabes que los sistemas materiales se pueden clasificar según su composición en sustancias puras y mezclas. Las
MEZCLAS Y DISOLUCIONES Física y Química 3º de E.S.O. IES Isidra de Guzmán Introducción Ya sabes que los sistemas materiales se pueden clasificar según su composición en sustancias puras y mezclas. Las
Tema 7. Las mezclas. Introducción
 Tema 7. Las mezclas Introducción Ya sabes que los sistemas materiales se pueden clasificar según su composición en sustancias puras y mezclas. Las sustancias puras son los elementos y los compuestos que
Tema 7. Las mezclas Introducción Ya sabes que los sistemas materiales se pueden clasificar según su composición en sustancias puras y mezclas. Las sustancias puras son los elementos y los compuestos que
2. Métodos de separación de los componentes de una mezcla.
 TEMA 3: Mezclas, disoluciones y sustancias puras. 1. Clasificación de la materia. 2. Métodos de separación de los componentes de una mezcla. 3. Disoluciones. a) Definición. b) Cómo se preparan. c) Concentración.
TEMA 3: Mezclas, disoluciones y sustancias puras. 1. Clasificación de la materia. 2. Métodos de separación de los componentes de una mezcla. 3. Disoluciones. a) Definición. b) Cómo se preparan. c) Concentración.
Métodos de separación en mezclas
 Los métodos de separación están basados en las diferentes propiedades físicas (como la densidad, la temperatura de ebullición, la solubilidad, el estado de agregación, etc.) de las sustancias que componen
Los métodos de separación están basados en las diferentes propiedades físicas (como la densidad, la temperatura de ebullición, la solubilidad, el estado de agregación, etc.) de las sustancias que componen
LOS ESTADOS DE LA MATERIA
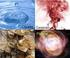 LOS ESTADOS DE LA MATERIA Como ya hemos estudiado, la materia se presenta en cuatro estados físicos: sólido, líquido, gas y plasma. El plasma es el estado de la materia en las estrellas. Una sustancia,
LOS ESTADOS DE LA MATERIA Como ya hemos estudiado, la materia se presenta en cuatro estados físicos: sólido, líquido, gas y plasma. El plasma es el estado de la materia en las estrellas. Una sustancia,
La diversidad de la materia
 La diversidad de la materia Física y Química Los sistemas materiales Oxford University Press España, S. A. Física y Química 3º ESO 2 Un sistema material es una porción de materia que se aísla física o
La diversidad de la materia Física y Química Los sistemas materiales Oxford University Press España, S. A. Física y Química 3º ESO 2 Un sistema material es una porción de materia que se aísla física o
Clasificación de la materia
 Clasificación de la materia Sustancias Puras Son caracterizados por su composición y propiedades definidas y constantes bajo condiciones determinadas. Sustancias puras: Elementos Son sustancias puras formadas
Clasificación de la materia Sustancias Puras Son caracterizados por su composición y propiedades definidas y constantes bajo condiciones determinadas. Sustancias puras: Elementos Son sustancias puras formadas
U3. CLASIFICACIÓN DE LA MATERIA: METODOS DE SEPARACIÓN
 FÍSICA Y QUÍMICA. 3º ESO 1 NOM: ; GRUP: U3. CLASIFICACIÓN DE LA MATERIA: METODOS DE SEPARACIÓN (Puedes encontrar más información del punto que vamos a tratar en las páginas siguientes del libro: Pag. 53,
FÍSICA Y QUÍMICA. 3º ESO 1 NOM: ; GRUP: U3. CLASIFICACIÓN DE LA MATERIA: METODOS DE SEPARACIÓN (Puedes encontrar más información del punto que vamos a tratar en las páginas siguientes del libro: Pag. 53,
FÍSICA Y QUÍMICA TEMA 3: MEZCLAS, DISOLUCIONES Y SUSTANCIAS PURAS
 Física y Química 3º Curso Educación Secundaria Obligatoria Curso académico 2015/2016 1 FÍSICA Y QUÍMICA TEMA 3: MEZCLAS, DISOLUCIONES Y SUSTANCIAS PURAS Física y Química 3º Curso Educación Secundaria Obligatoria
Física y Química 3º Curso Educación Secundaria Obligatoria Curso académico 2015/2016 1 FÍSICA Y QUÍMICA TEMA 3: MEZCLAS, DISOLUCIONES Y SUSTANCIAS PURAS Física y Química 3º Curso Educación Secundaria Obligatoria
La diversidad de la materia
 3 La diversidad de la materia Contenidos Índice 1 2 3 4 Clasificación de los sistemas materiales Separación de mezclas heterogéneas Las disoluciones Sustancias puras: elementos y compuestos 1. Clasificación
3 La diversidad de la materia Contenidos Índice 1 2 3 4 Clasificación de los sistemas materiales Separación de mezclas heterogéneas Las disoluciones Sustancias puras: elementos y compuestos 1. Clasificación
TEMA 2: LA DIVERSIDAD DE LA MATERIA 3º ESO
 TEMA 2: LA DIVERSIDAD DE LA MATERIA 3º ESO 1. Clasificaciones de los sistema materiales. Un sistema material es una porción de materia que se separa para facilitar su estudio experimental. Como existe
TEMA 2: LA DIVERSIDAD DE LA MATERIA 3º ESO 1. Clasificaciones de los sistema materiales. Un sistema material es una porción de materia que se separa para facilitar su estudio experimental. Como existe
SISTEMAS MATERIALES. Departamento de Física y Química 2º ESO
 SISTEMAS MATERIALES Departamento de Física y Química 2º ESO 0. Mapa conceptual MATERIA Sustancias puras Mezclas Heterogéneas Homogéneas Sistemas coloidales Técnicas de separación Disoluciones Soluto Disolvente
SISTEMAS MATERIALES Departamento de Física y Química 2º ESO 0. Mapa conceptual MATERIA Sustancias puras Mezclas Heterogéneas Homogéneas Sistemas coloidales Técnicas de separación Disoluciones Soluto Disolvente
Materia: es aquello que ocupa un lugar en el espacio y cuyas propiedades percibimos por los sentidos. Es diversa y discontinua.
 Sistemas materiales Materia: es aquello que ocupa un lugar en el espacio y cuyas propiedades percibimos por los sentidos. Es diversa y discontinua. Mezcla Heterogénea: unión de dos o más sustancias de
Sistemas materiales Materia: es aquello que ocupa un lugar en el espacio y cuyas propiedades percibimos por los sentidos. Es diversa y discontinua. Mezcla Heterogénea: unión de dos o más sustancias de
U.D. 2 LA MATERIA. Para describir un cuerpo o un sistema material, necesitamos conocer sus propiedades. Así, distinguimos entre:
 U.D. 2 LA MATERIA 1. Propiedades de la materia La materia, o sistema material, es todo lo que posee una propiedad fundamental llamada masa, y que ocupa un espacio, es decir, un volumen. Para describir
U.D. 2 LA MATERIA 1. Propiedades de la materia La materia, o sistema material, es todo lo que posee una propiedad fundamental llamada masa, y que ocupa un espacio, es decir, un volumen. Para describir
Qué es la materia? A qué llamamos sustancias? Qué dos clases de propiedades posee la materia? Por qué se llaman propiedades generales?
 La materia es aquello que ocupa un lugar en el espacio y cuyas propiedades percibimos por los sentidos ( vista, tacto...). Todos los objetos que observamos a nuestro alrededor tienen algo en común : es
La materia es aquello que ocupa un lugar en el espacio y cuyas propiedades percibimos por los sentidos ( vista, tacto...). Todos los objetos que observamos a nuestro alrededor tienen algo en común : es
UNIDAD II. Transformaciones de la materia. Tema 2: Clasificación de la materia.
 UNIDAD II. Transformaciones de la materia. Tema 2: Clasificación de la materia. Qué es materia? Es todo lo que tiene masa y volumen. CLASIFICACIÓN DE LA MATERIA: Según: A. Estado de agregación. B. Composición.
UNIDAD II. Transformaciones de la materia. Tema 2: Clasificación de la materia. Qué es materia? Es todo lo que tiene masa y volumen. CLASIFICACIÓN DE LA MATERIA: Según: A. Estado de agregación. B. Composición.
1 Propiedades de la materia
 1 La materia 1 Propiedades de la materia La materia, o sistema material, es todo lo que posee una propiedad fundamental llamada masa, y que ocupa un espacio, es decir, un volumen. Cuando nos referimos
1 La materia 1 Propiedades de la materia La materia, o sistema material, es todo lo que posee una propiedad fundamental llamada masa, y que ocupa un espacio, es decir, un volumen. Cuando nos referimos
PROBLEMAS MEZCLAS Y DISOLUCIONES
 PROBLEMAS MEZCLAS Y DISOLUCIONES 1. Clasifica como homogéneos o heterogéneos los siguientes sistemas materiales: un trozo de cobre, agua salada, hierro oxidado, una ensalada. 2. Al mezclar dos sistemas
PROBLEMAS MEZCLAS Y DISOLUCIONES 1. Clasifica como homogéneos o heterogéneos los siguientes sistemas materiales: un trozo de cobre, agua salada, hierro oxidado, una ensalada. 2. Al mezclar dos sistemas
1º ESO IES MURIEDAS Bonifacio San Millán
 1º ESO IES MURIEDAS Bonifacio San Millán En las mezclas se aprecia, a simple vista, que están formadas por varios componentes En las mezclas NO se aprecia, a simple vista, que están formadas por varios
1º ESO IES MURIEDAS Bonifacio San Millán En las mezclas se aprecia, a simple vista, que están formadas por varios componentes En las mezclas NO se aprecia, a simple vista, que están formadas por varios
filosofiatotal.blogspot.com depcienat1.blogspot.com
 www.alambiques.info filosofiatotal.blogspot.com depcienat1.blogspot.com www.panreac.es Ahhhh! Un vaso de limonada helada es muy refrescante en un día caluroso. La limonada es una combinación de jugo de
www.alambiques.info filosofiatotal.blogspot.com depcienat1.blogspot.com www.panreac.es Ahhhh! Un vaso de limonada helada es muy refrescante en un día caluroso. La limonada es una combinación de jugo de
La materia y sus propiedades
 La materia y sus propiedades Las sustancias puras simples: ELEMENTOS QUÍMICOS Los elementos químicos Algunos pueden encontrarse fácilmente en nuestro entorno Hierro (Fe) Cobre (Cu) ASPECTO HOMOGÉNEO Oxígeno
La materia y sus propiedades Las sustancias puras simples: ELEMENTOS QUÍMICOS Los elementos químicos Algunos pueden encontrarse fácilmente en nuestro entorno Hierro (Fe) Cobre (Cu) ASPECTO HOMOGÉNEO Oxígeno
2. LOS ESTADOS DE LA MATERIA. Nuria Montiel Guardiola - 1 -
 1. LA MATERIA La materia es todo aquello que existe, tiene masa y ocupa lugar en un espacio. Las cosas materiales se pueden medir y contar y las cosas inmateriales no. 2. LOS ESTADOS DE LA MATERIA Nuria
1. LA MATERIA La materia es todo aquello que existe, tiene masa y ocupa lugar en un espacio. Las cosas materiales se pueden medir y contar y las cosas inmateriales no. 2. LOS ESTADOS DE LA MATERIA Nuria
oluciones del apartado «Resuelve problemas»
 S oluciones del apartado «Resuelve problemas» Pág. 1 19 Un café con azúcar es una mezcla homogénea o heterogénea? Es una disolución de sólidos (café y azúcar) en agua. 20 Un material formado por moléculas
S oluciones del apartado «Resuelve problemas» Pág. 1 19 Un café con azúcar es una mezcla homogénea o heterogénea? Es una disolución de sólidos (café y azúcar) en agua. 20 Un material formado por moléculas
Apuntes Disoluciones
 Una disolución es una mezcla homogénea (los componentes no se pueden distinguir a simple vista) de dos a más sustancias. En las disoluciones hay que distinguir el soluto, el disolvente y la propia disolución
Una disolución es una mezcla homogénea (los componentes no se pueden distinguir a simple vista) de dos a más sustancias. En las disoluciones hay que distinguir el soluto, el disolvente y la propia disolución
CURSO 2016 / Tema 3. Sistemas. materiales. Física y química para 2º ESO. Nombre..
 CURSO 2016 / 2017 Tema 3. Sistemas materiales. Física y química para 2º ESO Nombre.. Índice general: 1. Concepto de mezcla. Tipos. 2. Las disoluciones. 3. Tipos de disoluciones. 3.1. Según el estado físico
CURSO 2016 / 2017 Tema 3. Sistemas materiales. Física y química para 2º ESO Nombre.. Índice general: 1. Concepto de mezcla. Tipos. 2. Las disoluciones. 3. Tipos de disoluciones. 3.1. Según el estado físico
TEMA 13: LA MATERIA, BASE DEL UNIVERSO
 TEMA 13: LA MATERIA, BASE DEL UNIVERSO Qué es materia? Materia es todo aquello que posee masa y ocupa un volumen. Está formada de partículas muy pequeñas llamadas átomos. La masa y el volumen se consideran
TEMA 13: LA MATERIA, BASE DEL UNIVERSO Qué es materia? Materia es todo aquello que posee masa y ocupa un volumen. Está formada de partículas muy pequeñas llamadas átomos. La masa y el volumen se consideran
Profesor: Carlos Gutiérrez Arancibia
 Profesor: Carlos Gutiérrez Arancibia Temas a tratar: - Sustancias puras - Mezclas - Disoluciones - Procesos de Disoluciones - Solubilidad - Factores que afectan la solubilidad - Unidades de Concentraciones
Profesor: Carlos Gutiérrez Arancibia Temas a tratar: - Sustancias puras - Mezclas - Disoluciones - Procesos de Disoluciones - Solubilidad - Factores que afectan la solubilidad - Unidades de Concentraciones
LOS ESTADOS DE LA MATERIA
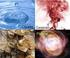 LOS ESTADOS DE LA MATERIA Como ya hemos estudiado, la materia se presenta en cuatro estados físicos: sólido, líquido, gas y plasma. El plasma es el estado de la materia en las estrellas. Una sustancia,
LOS ESTADOS DE LA MATERIA Como ya hemos estudiado, la materia se presenta en cuatro estados físicos: sólido, líquido, gas y plasma. El plasma es el estado de la materia en las estrellas. Una sustancia,
CONTENIDOS MÍNIMOS Y CRITERIOS DE EVALUACIÓN
 4 La materia: estados de agregación. Objetivos Observar el aspecto y otras características de la materia, en sus diversos estados de agregación: sólido, líquido y gaseoso. Distinguir y aplicar a ejercicios
4 La materia: estados de agregación. Objetivos Observar el aspecto y otras características de la materia, en sus diversos estados de agregación: sólido, líquido y gaseoso. Distinguir y aplicar a ejercicios
Métodos de separación de sistemas materiales sencillos
 Métodos de separación de sistemas materiales sencillos SISTEMAS MATERIALES Mezclas Separación física Sustancias Puras no Son uniformes? si si Pueden descomponerse por reacciones químicas? no Mezclas heterogéneas
Métodos de separación de sistemas materiales sencillos SISTEMAS MATERIALES Mezclas Separación física Sustancias Puras no Son uniformes? si si Pueden descomponerse por reacciones químicas? no Mezclas heterogéneas
CLASIFICACIÓN DE LA MATERIA
 CLASIFICACIÓN DE LA MATERIA Clasificación de la materia SUSTACIACIAS PURAS SIMPLES UN SOLO TIPO DE ÁTOMO Mercurio (l) átomo de Hg Cloro(g) átomo de Cl SUSTANCIA PURA COMPUESTA S C O Zn Un solo tipo de
CLASIFICACIÓN DE LA MATERIA Clasificación de la materia SUSTACIACIAS PURAS SIMPLES UN SOLO TIPO DE ÁTOMO Mercurio (l) átomo de Hg Cloro(g) átomo de Cl SUSTANCIA PURA COMPUESTA S C O Zn Un solo tipo de
FÍSICA Y QUÍMICA 2º ESO TEMA VI COMPOSICIÓN DE LA MATERIA
 FÍSICA Y QUÍMICA 2º ESO TEMA VI COMPOSICIÓN DE LA MATERIA 1) MEZCLAS HOMOGÉNEAS Y HETEROGÉNEAS Una mezcla es una composición de sustancias con distintas propiedades. Una mezcla es homogénea si está formada
FÍSICA Y QUÍMICA 2º ESO TEMA VI COMPOSICIÓN DE LA MATERIA 1) MEZCLAS HOMOGÉNEAS Y HETEROGÉNEAS Una mezcla es una composición de sustancias con distintas propiedades. Una mezcla es homogénea si está formada
FyQ 1. IES de Castuera Bloque 2 Aspectos Cuantitativos de la Química Unidad Didáctica 2
 Física y Química 1º Bachillerato LOMCE FyQ 1 IES de Castuera Bloque 2 Aspectos Cuantitativos de la Química 2015 2016 Unidad Didáctica 2 Rev 01 Las Disoluciones. Métodos Actuales para el Análisis de Sustancias
Física y Química 1º Bachillerato LOMCE FyQ 1 IES de Castuera Bloque 2 Aspectos Cuantitativos de la Química 2015 2016 Unidad Didáctica 2 Rev 01 Las Disoluciones. Métodos Actuales para el Análisis de Sustancias
LA DIVERSIDAD DE LA MATERIA
 Tema 3 LA DIVERSIDAD DE LA MATERIA 1 Clasificación de la materia Un sistema material es una porción de materia que se separa para realizar un estudio experimental. Es aquella parte del universo que se
Tema 3 LA DIVERSIDAD DE LA MATERIA 1 Clasificación de la materia Un sistema material es una porción de materia que se separa para realizar un estudio experimental. Es aquella parte del universo que se
MATERIA: ES TODO LO QUE TIENE MASA Y VOLUMEN.
 MATERIA: ES TODO LO QUE TIENE MASA Y VOLUMEN. CLASIFICACIÓN DE LA MATERIA: SEGÚN: A. ESTADO DE AGREGACIÓN. B. COMPOSICIÓN. A. ESTADO DE AGREGACIÓN. SE REFIERE A LA FORMA DE INTERACCIÓN ENTRE LAS MOLÉCULAS
MATERIA: ES TODO LO QUE TIENE MASA Y VOLUMEN. CLASIFICACIÓN DE LA MATERIA: SEGÚN: A. ESTADO DE AGREGACIÓN. B. COMPOSICIÓN. A. ESTADO DE AGREGACIÓN. SE REFIERE A LA FORMA DE INTERACCIÓN ENTRE LAS MOLÉCULAS
SUSTANCIA QUÍMICA mercurio oxígeno
 ELEMENTO O SUSTANCIA ELEMENTAL: Sustancia formada por un mismo tipo de átomos, por ejemplo: Hg, H 2, Cu, O 2 SUSTANCIA QUÍMICA mercurio oxígeno COMPUESTO O SUSTANCIA COMPUESTA: Sustancia formada por dos
ELEMENTO O SUSTANCIA ELEMENTAL: Sustancia formada por un mismo tipo de átomos, por ejemplo: Hg, H 2, Cu, O 2 SUSTANCIA QUÍMICA mercurio oxígeno COMPUESTO O SUSTANCIA COMPUESTA: Sustancia formada por dos
Física y Química: guía interactiva para la resolución de ejercicios
 Física y Química: guía interactiva para la resolución de ejercicios CLASIFICACIÓN DE LA MATERIA I.E.S. Élaios Departamento de Física y Química EJERCICIO 1 (a) En un vaso tenemos alcohol que calentamos
Física y Química: guía interactiva para la resolución de ejercicios CLASIFICACIÓN DE LA MATERIA I.E.S. Élaios Departamento de Física y Química EJERCICIO 1 (a) En un vaso tenemos alcohol que calentamos
1) (1 PUNTO) Lee el siguiente texto y responde a las preguntas.
 2º ESO Control del tema 3 La diversidad de la materia NOMBRE GRUPO FECHA: 1) (1 PUNTO) Lee el siguiente texto y responde a las preguntas. LA GANADERÍA Y EL CAMBIO CLIMÁTICO Como hemos visto en la unidad
2º ESO Control del tema 3 La diversidad de la materia NOMBRE GRUPO FECHA: 1) (1 PUNTO) Lee el siguiente texto y responde a las preguntas. LA GANADERÍA Y EL CAMBIO CLIMÁTICO Como hemos visto en la unidad
EJERCICIOS TEMA 2. LA MATERIA Y SUS PROPIEDADES.
 EJERCICIOS TEMA 2. LA MATERIA Y SUS PROPIEDADES. 1. La materia puede presentarse en tres estados de agregación. Cuáles son? 2. Cómo son la forma y el volumen de un sólido? Y de un líquido? Y de un gas?
EJERCICIOS TEMA 2. LA MATERIA Y SUS PROPIEDADES. 1. La materia puede presentarse en tres estados de agregación. Cuáles son? 2. Cómo son la forma y el volumen de un sólido? Y de un líquido? Y de un gas?
03 DISOLUCIONES. 2 Observando la curva de solubilidad del clorato potásico, responder:
 03 DISOLUCIONES 1 Sabemos que cierta disolución tiene una concentración de c = 512 g/l. Si su densidad es1,43 g/l, expresa el valor de su concentración en tanto por ciento. 2 Observando la curva de solubilidad
03 DISOLUCIONES 1 Sabemos que cierta disolución tiene una concentración de c = 512 g/l. Si su densidad es1,43 g/l, expresa el valor de su concentración en tanto por ciento. 2 Observando la curva de solubilidad
MEZCLAS. Lic. Lisbeth Villarroel Garzaro
 INTRODUCCION En la vida diaria nos encontramos con mezclas y sustancias puras; sin embargo pocas veces las podemos diferenciar. Por ello debemos tener presente que una sustancia pura es un material homogéneo
INTRODUCCION En la vida diaria nos encontramos con mezclas y sustancias puras; sin embargo pocas veces las podemos diferenciar. Por ello debemos tener presente que una sustancia pura es un material homogéneo
Para la solución de algunos de los ejercicios propuestos, se adjunta una parte del sistema periódico hasta el elemento Nº 20.
 Programa Estándar Anual Nº Guía práctica Disoluciones I: mezclas, disoluciones y unidades porcentuales de concentración Ejercicios PSU Para la solución de algunos de los ejercicios propuestos, se adjunta
Programa Estándar Anual Nº Guía práctica Disoluciones I: mezclas, disoluciones y unidades porcentuales de concentración Ejercicios PSU Para la solución de algunos de los ejercicios propuestos, se adjunta
MOL. Nº AVOGADRO GASES. TEMA 4 Pág. 198 libro (Unidad 10)
 MOL. Nº AVOGADRO GASES TEMA 4 Pág. 198 libro (Unidad 10) CONCEPTOS PREVIOS Supuestos de Dalton Teoría atómica de Dalton Elementos constituidos por átomos, partículas separadas e indivisibles Átomos de
MOL. Nº AVOGADRO GASES TEMA 4 Pág. 198 libro (Unidad 10) CONCEPTOS PREVIOS Supuestos de Dalton Teoría atómica de Dalton Elementos constituidos por átomos, partículas separadas e indivisibles Átomos de
Sustancias puras y mezclas: Qué es una sustancia? Qué es una sustancia pura?: Clasificación de las sustancias puras: elementos y compuestos;
 SEXTO Sustancias puras y mezclas: Qué es una sustancia?: Es cualquier variedad de materia que tiene composición definida y reconocible. Las sustancias se clasifican en sustancias puras y mezclas. Qué es
SEXTO Sustancias puras y mezclas: Qué es una sustancia?: Es cualquier variedad de materia que tiene composición definida y reconocible. Las sustancias se clasifican en sustancias puras y mezclas. Qué es
LA MATERIA: ESTADOS DE AGREGACIÓN
 LA MATERIA: ESTADOS DE AGREGACIÓN 1. PROPIEDADES DE LA MATERIA Materia: es todo aquello que existe, tiene masa y ocupa un volumen, los distintos tipos de materia se llaman sustancias. El sistema material
LA MATERIA: ESTADOS DE AGREGACIÓN 1. PROPIEDADES DE LA MATERIA Materia: es todo aquello que existe, tiene masa y ocupa un volumen, los distintos tipos de materia se llaman sustancias. El sistema material
1. Disoluciones una disolución es cualquier mezcla homogénea disolvente soluto Medidas de composición
 1. Disoluciones En general, una disolución es cualquier mezcla homogénea. Por ejemplo, el aire, mezcla de nitrógeno, oxígeno y otros gases en proporciones menores; o el bronce, que es una aleación metálica
1. Disoluciones En general, una disolución es cualquier mezcla homogénea. Por ejemplo, el aire, mezcla de nitrógeno, oxígeno y otros gases en proporciones menores; o el bronce, que es una aleación metálica
La materia y los cambios químicos 4. Sustancias puras y mezclas
 4. Sustancias puras y mezclas Materia Sustancias puras Formadas por un único tipo de componente Mezclas Formada por dos o más sustancias puras Elementos Formados por la misma clase de átomos Compuestos
4. Sustancias puras y mezclas Materia Sustancias puras Formadas por un único tipo de componente Mezclas Formada por dos o más sustancias puras Elementos Formados por la misma clase de átomos Compuestos
ESTADOS DE AGREGACIÓN DE LA MATERIA
 LA MATERIA LA MATERIA Materia es todo aquello que ocupa un lugar en el espacio y tiene masa. La madera, el agua, el corcho, la sal,.. Son clases diferentes de materia. Las clases de materia que se utilizan
LA MATERIA LA MATERIA Materia es todo aquello que ocupa un lugar en el espacio y tiene masa. La madera, el agua, el corcho, la sal,.. Son clases diferentes de materia. Las clases de materia que se utilizan
Soluciones y unidades de concentración
 MATERIA Soluciones y unidades de concentración MEZCLAS SISTEMAS HETEROGÉNEOS Leche Arena Sal y azúcar SISTEMAS HOMOGÉNEOS Sal en agua Aire Acero COMPUESTOS Agua Etanol Benceno SUSTANCIAS PURAS ELEMENTOS
MATERIA Soluciones y unidades de concentración MEZCLAS SISTEMAS HETEROGÉNEOS Leche Arena Sal y azúcar SISTEMAS HOMOGÉNEOS Sal en agua Aire Acero COMPUESTOS Agua Etanol Benceno SUSTANCIAS PURAS ELEMENTOS
Soluciones y unidades de concentración
 Soluciones y unidades de concentración Dra. Dra. Patricia Patricia Satti, Satti, UNRN UNRN MATERIA MEZCLAS SUSTANCIAS PURAS SISTEMAS HETEROGÉNEOS Leche Arena Sal y azúcar SISTEMAS HOMOGÉNEOS Sal en agua
Soluciones y unidades de concentración Dra. Dra. Patricia Patricia Satti, Satti, UNRN UNRN MATERIA MEZCLAS SUSTANCIAS PURAS SISTEMAS HETEROGÉNEOS Leche Arena Sal y azúcar SISTEMAS HOMOGÉNEOS Sal en agua
TEMA 3 CLASIFICACIÓN DE LA MATERIA
 TEMA 3 CLASIFICACIÓN DE LA MATERIA Cuál es agua pura y cual es AGUA CON SAL? NECESITAMOS COMPROBAR ALGUNA PROPIEDAD, COMO EL SABOR HAY OTRAS PORPIEDADES QUE LAS DISTINGUEN A PESAR DE SER MUY PARECIDAS
TEMA 3 CLASIFICACIÓN DE LA MATERIA Cuál es agua pura y cual es AGUA CON SAL? NECESITAMOS COMPROBAR ALGUNA PROPIEDAD, COMO EL SABOR HAY OTRAS PORPIEDADES QUE LAS DISTINGUEN A PESAR DE SER MUY PARECIDAS
TEMA 3. CLASIFICANDO LA MATERIA
 TEMA 3. CLASIFICANDO LA MATERIA 1. CLASIFICANDO LA MATERIA: SUSTANCIAS PURAS Y MEZCLAS 1. Completa las frases con las siguientes palabras: elementos-combinar-sustancias puras-compuestosmezcla. La materia
TEMA 3. CLASIFICANDO LA MATERIA 1. CLASIFICANDO LA MATERIA: SUSTANCIAS PURAS Y MEZCLAS 1. Completa las frases con las siguientes palabras: elementos-combinar-sustancias puras-compuestosmezcla. La materia
CÓMO SE SEPARAN LOS COMPONENTES DE UNA MEZCLA? 2. TÉCNICAS DE SEPARACIÓN DE LOS COMPONENTES DE UNA MEZCLA.
 1. INTRODUCCIÓN. CÓMO SE SEPARAN LOS COMPONENTES DE UNA MEZCLA? Cuando una sustancia cualquiera contiene a otra distribuida en su seno como partículas muy pequeñas, se habla de un sistema disperso o de
1. INTRODUCCIÓN. CÓMO SE SEPARAN LOS COMPONENTES DE UNA MEZCLA? Cuando una sustancia cualquiera contiene a otra distribuida en su seno como partículas muy pequeñas, se habla de un sistema disperso o de
TEMA 2. COMPOSICIÓN DE LA MATERIA
 TEMA 2. COMPOSICIÓN DE LA MATERIA 1 COMPOSICIÓN DE LA MATERIA La materia se presenta en pedazos o porciones limitadas que llamamos cuerpos o sistemas materiales. Por lo tanto un sistema material es un
TEMA 2. COMPOSICIÓN DE LA MATERIA 1 COMPOSICIÓN DE LA MATERIA La materia se presenta en pedazos o porciones limitadas que llamamos cuerpos o sistemas materiales. Por lo tanto un sistema material es un
CLASIFICACIÓN DE LA MATERIA
 CLASIFICACIÓN DE LA MATERIA Clasificación de la materia. Sistemas materiales Sustancias puras Mezclas Un solo componente Dos o mas componentes Simples Compuestas Homogénas Heterogénas Un solo tipo de átomo.
CLASIFICACIÓN DE LA MATERIA Clasificación de la materia. Sistemas materiales Sustancias puras Mezclas Un solo componente Dos o mas componentes Simples Compuestas Homogénas Heterogénas Un solo tipo de átomo.
MOL. Nº AVOGADRO DISOLUCIONES. TEMA 4 Pág. 198 libro (Unidad 10)
 MOL. Nº AVOGADRO DISOLUCIONES TEMA 4 Pág. 198 libro (Unidad 10) CONCEPTOS PREVIOS Supuestos de Dalton Teoría atómica de Dalton Elementos consitudios por átomos, partícuals separads e indivisibles Átomos
MOL. Nº AVOGADRO DISOLUCIONES TEMA 4 Pág. 198 libro (Unidad 10) CONCEPTOS PREVIOS Supuestos de Dalton Teoría atómica de Dalton Elementos consitudios por átomos, partícuals separads e indivisibles Átomos
Actividades para repasar el examen de septiembre
 Actividades para repasar el examen de septiembre 1. Qué es una magnitud? Qué es medir? Pon un ejemplo que ayude a entender este concepto, utiliza un dibujo explicativo. Pon ejemplos de magnitudes y de
Actividades para repasar el examen de septiembre 1. Qué es una magnitud? Qué es medir? Pon un ejemplo que ayude a entender este concepto, utiliza un dibujo explicativo. Pon ejemplos de magnitudes y de
CARACTERISTICAS DE LAS DISOLUCIONES Mezcla: unión de dos o mas sustancias, que no se combinan químicamente
 CARACTERISTICAS DE LAS DISOLUCIONES Mezcla: unión de dos o mas sustancias, que no se combinan químicamente Las mezclas están formadas por una sustancia que se encuentra en mayor proporción llamada fase
CARACTERISTICAS DE LAS DISOLUCIONES Mezcla: unión de dos o mas sustancias, que no se combinan químicamente Las mezclas están formadas por una sustancia que se encuentra en mayor proporción llamada fase
INTRODUCCIÓN DISOLUCIONES
 QUIMICA COMUN INTRODUCCIÓN DISOLUCIONES EBULLICIÓN V/S EVAPORACIÓN Ambos conceptos tienen relación con la presión de vapor. La presión de vapor es la fuerza que tienen las moléculas de un líquido para
QUIMICA COMUN INTRODUCCIÓN DISOLUCIONES EBULLICIÓN V/S EVAPORACIÓN Ambos conceptos tienen relación con la presión de vapor. La presión de vapor es la fuerza que tienen las moléculas de un líquido para
Componentes de una disolución. El disolvente El soluto Concentración de una disolución. concentración solubilidad
 Componentes de una disolución. Todas las disoluciones tienen dos componentes: El disolvente es el componente que se encuentra en mayor proporción. Este componente no cambia de estado. El soluto es el componente
Componentes de una disolución. Todas las disoluciones tienen dos componentes: El disolvente es el componente que se encuentra en mayor proporción. Este componente no cambia de estado. El soluto es el componente
3º ESO Física y Química A. Puebla T3: Sustancias puras y mezclas. FICHA 2: LA MATERIA. COMO SE PRESENTA
 FICHA 2: LA MATERIA. COMO SE PRESENTA 1. Lee detenidamente las siguientes descripciones (de A a E) y clasifica como elemento o compuesto las sustancias: A) Caliza. Se coloca en un matraz varias piedras
FICHA 2: LA MATERIA. COMO SE PRESENTA 1. Lee detenidamente las siguientes descripciones (de A a E) y clasifica como elemento o compuesto las sustancias: A) Caliza. Se coloca en un matraz varias piedras
ACTIVIDADES DE PENDIENTES DE FÍSICA Y QUÍMICA DE 3º ESO
 ACTIVIDADES DE PENDIENTES DE FÍSICA Y QUÍMICA DE 3º ESO 1. a) Qué es la Ciencia? Qué es la Física? Qué es la Química? b) Señala qué procesos se estudian la Física y cuáles estudia la Química: a. Descenso
ACTIVIDADES DE PENDIENTES DE FÍSICA Y QUÍMICA DE 3º ESO 1. a) Qué es la Ciencia? Qué es la Física? Qué es la Química? b) Señala qué procesos se estudian la Física y cuáles estudia la Química: a. Descenso
SOLUCIONES SOLIDA LIQUIDA GASEOSA. mezclas homogéneas de dos sustancias: SEGÚN EL ESTADO FISICO DEL SOLVENTE
 Soluciones SOLUCIONES mezclas homogéneas de dos sustancias: SOLUTO SOLVENTE SEGÚN EL ESTADO FISICO DEL SOLVENTE SOLIDA LIQUIDA GASEOSA Cuando un sólido se disuelve en un líquido las partículas que lo
Soluciones SOLUCIONES mezclas homogéneas de dos sustancias: SOLUTO SOLVENTE SEGÚN EL ESTADO FISICO DEL SOLVENTE SOLIDA LIQUIDA GASEOSA Cuando un sólido se disuelve en un líquido las partículas que lo
DISOLUCIONES. Las disoluciones son mezclas homogéneas de dos o más sustancias (componentes) en proporciones variables.
 DISOLUCIONES Las disoluciones son mezclas homogéneas de dos o más sustancias (componentes) en proporciones variables. Soluto es la sustancia que se encuentra en menor proporción. Disolvente es la sustancia
DISOLUCIONES Las disoluciones son mezclas homogéneas de dos o más sustancias (componentes) en proporciones variables. Soluto es la sustancia que se encuentra en menor proporción. Disolvente es la sustancia
Teoría Disoluciones Fórmula empírica y molecular Física y Química. 1º bachiller DISOLUCIONES
 Teoría Disoluciones Fórmula empírica y molecular Física y Química. 1º bachiller 18-1-2015 CONCEPTO DE DISOLUCIÓN DISOLUCIONES Una disolución es una mezcla homogénea de sustancias en igual o distintos estados
Teoría Disoluciones Fórmula empírica y molecular Física y Química. 1º bachiller 18-1-2015 CONCEPTO DE DISOLUCIÓN DISOLUCIONES Una disolución es una mezcla homogénea de sustancias en igual o distintos estados
Clasifica los siguientes sistemas materiales en elementos, compuestos o mezclas homogéneas o heterogéneas:
 TITULO (edite antes de imprimir) NOMBRE: CURSO: 1) Clasifica los siguientes sistemas materiales en elementos, compuestos o mezclas homogéneas o heterogéneas: Plomo ; acero ; mercurio ; óxido de hierro
TITULO (edite antes de imprimir) NOMBRE: CURSO: 1) Clasifica los siguientes sistemas materiales en elementos, compuestos o mezclas homogéneas o heterogéneas: Plomo ; acero ; mercurio ; óxido de hierro
DISOLUCIONES. Líquido (H 2 O)
 DISOLUCIONES IES La Magdalena. Avilés. Asturias Una disolución es una mezcla homogénea (los componentes no se pueden distinguir a simple vista) de dos a más sustancias. En las disoluciones hay que distinguir
DISOLUCIONES IES La Magdalena. Avilés. Asturias Una disolución es una mezcla homogénea (los componentes no se pueden distinguir a simple vista) de dos a más sustancias. En las disoluciones hay que distinguir
Anselmo Lorenzo-Sección Morata de Tajuña FISICA Y QUIMICA 2ºESO. Apoyo Libro de Texto (sí): tema 3.
 Instituto de Educación Secundaria Anselmo Lorenzo-Sección Morata de Tajuña Consejería de Educación Comunidad de Madrid FISICA Y QUIMICA 2ºESO 2ª EVALUACIÓN TÉCNICAS DE SEPARACIÓN Ficha: 1 de 7 Alumno/a:
Instituto de Educación Secundaria Anselmo Lorenzo-Sección Morata de Tajuña Consejería de Educación Comunidad de Madrid FISICA Y QUIMICA 2ºESO 2ª EVALUACIÓN TÉCNICAS DE SEPARACIÓN Ficha: 1 de 7 Alumno/a:
SISTEMA MATERIAL TEMA 3. DIVERSIDAD DE LA MATERIA. I. E. S. Gamonares (Lopera Jaén) Departamento de Ciencias Naturales 1. CLASIFICACIÓN DE LA MATERIA.
 I. E. S. Gamonares (Lopera Jaén) Departamento de Ciencias Naturales TEMA 3. DIVERSIDAD DE LA MATERIA 1. CLASIFICACIÓN DE LA MATERIA. 1. Completa el siguiente diagrama, con las definiciones correspondientes:
I. E. S. Gamonares (Lopera Jaén) Departamento de Ciencias Naturales TEMA 3. DIVERSIDAD DE LA MATERIA 1. CLASIFICACIÓN DE LA MATERIA. 1. Completa el siguiente diagrama, con las definiciones correspondientes:
En la primera unidad clasificábamos estos sistemas materiales de la siguiente forma: MATERIA
 La materia dispersa. Las mezclas. Disoluciones En temas anteriores ya hemos estudiado algunas características de las mezclas. Por su extraordinaria importancia vamos a dedicar un capítulo a un tipo de
La materia dispersa. Las mezclas. Disoluciones En temas anteriores ya hemos estudiado algunas características de las mezclas. Por su extraordinaria importancia vamos a dedicar un capítulo a un tipo de
III. D ISOLU L CIONES E
 III. DISOLUCIONES III. DISOLUCIONES Índice 1. Disoluciones 2. Solubilidad 3. Factores que favorecen la disolución de las sustancias 4. Propiedades coligativas de las disoluciones 5. Suspensiones y disoluciones
III. DISOLUCIONES III. DISOLUCIONES Índice 1. Disoluciones 2. Solubilidad 3. Factores que favorecen la disolución de las sustancias 4. Propiedades coligativas de las disoluciones 5. Suspensiones y disoluciones
TEMA 4.- LA MATERIA QUE NOS RODEA
 TEMA 4.- LA MATERIA QUE NOS RODEA MATERIA Y SUSTANCIA Módulo 2 La MATERIA está formada por átomos y moléculas Tiene masa y volumen Llamamos SUSTANCIA a cada una de las distintas formas de materia CUERPOS
TEMA 4.- LA MATERIA QUE NOS RODEA MATERIA Y SUSTANCIA Módulo 2 La MATERIA está formada por átomos y moléculas Tiene masa y volumen Llamamos SUSTANCIA a cada una de las distintas formas de materia CUERPOS
