Geología de Grado en Química. Prácticas. 8. Estructuras
|
|
|
- Germán Díaz Rojas
- hace 7 años
- Vistas:
Transcripción
1 Geología de Grado en Química. Prácticas. 8. Estructuras José Manuel Astilleros García-Monge. Sol López-Andrés. Cristóbal Viedma Molero. Elena Vindel Catena. Dpto. de Cristalografía y Mineralogía. Facultad de Ciencias Geológicas. Universidad Complutense. c/ José Antonio Novais nº Madrid. jmastill@geo.ucm.es antares@geo.ucm.es viedma@geo.ucm.es evindel@geo.ucm.es Resumen: La distribución de los átomos en el cristal define la estructura cristalina de un material. Conocer dicha estructura, es fundamental pues nos informa no sólo sobre la localización de todos los átomos, si no sobre la simetría de la estructura, las posiciones de enlace y el contenido químico de la celda unidad. Además, todas las propiedades fisicoquímicas de un material cristalino y su variación a lo largo de las distintas direcciones dependen en gran media de la localización concreta de los átomos en la estructura del cristal. Para conocer la estructura cristalina de un material es imprescindible visualizarla de algún modo sencillo mediante su proyección bidimensional. Palabras clave: Proyección de la estructura cristalina. Posiciones equivalentes. INTRODUCCIÓN En la Práctica nº 7 (Simetría IV) realizamos una serie de ejercicios sobre localización de elementos de simetría a partir de la distribución de las posiciones generales correspondientes a alguno de los 230 grupos espaciales tridimensionales. También vimos cómo es posible reconstruir la distribución de dichas posiciones generales una vez conocida la disposición de los elementos de simetría que sobre ellos operan. En el cristal real, los átomos iones o moléculas que lo conforman aparecen localizados en posiciones muy concretas, sean estas generales o especiales. Esta distribución de los átomos en el cristal va a definir la estructura cristalina. Conocer la estructura de los materiales cristalinos resulta fundamental pues nos informa no sólo sobre la localización de todos los átomos y, por tanto, de la simetría de que posee la estructura, sino también sobre las posiciones de enlace y el contenido químico de la celda unidad. Además, todas las propiedades fisicoquímicas de un material cristalino como son su dureza, birrefringencia, exfoliación, conductividad eléctrica y térmica, etc. y su variación de las mismas a lo largo de las distintas direcciones (anisotropía) 88
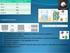
2 dependen en gran media de la localización concreta de los átomos en la estructura del cristal. Para conocer la estructura cristalina de un material es imprescindible visualizarla de algún modo sencillo, pues la información sobre las estructuras cristalinas viene descrita frecuentemente mediante el empleo de coordenadas fraccionarias y símbolos cristalográficos a veces de difícil visualización en tres dimensiones. Mediante la proyección de las estructuras conseguiremos traducir esta información a un modelo visual bidimensional. Una forma corriente para describir una estructura cristalina determinada es el empleo de coordenadas (x, y, z). Así, la posición de cada átomo en la celda puede definirse mediante la asignación de estas tres coordenadas cuyos valores corresponden a una fracción (comprendidos entre 0 y 1) de las aristas a, b y c de la celda. Mientras que este sistema resulta muy eficaz a la hora de proyectar estructuras sencillas y con pocos átomos, para estructuras con un gran número de átomos en su celda, enumerar las coordenadas de cada uno de sus átomos resultaría un proceso tedioso y poco eficaz. Para estos casos, lo más apropiado es el empleo de las Tablas Internacionales de Cristalografía (Vol. A), en donde para cada Grupo Espacial se indican todas las posiciones en donde teóricamente pueden localizarse los átomos de cualquier estructura cristalina. Ello permite no sólo sistematizar la información sino simplificar en gran medida la descripción de una estructura cristalina. Por ejemplo, si en la descripción de una estructura determinada, se informa que pertenece al grupo espacial F (Fig. 1) y que los átomos A de dicha estructura ocupan las posiciones h siendo x = 0,22, y = 0,17 y z = 0, 19, en realidad nos están dando las coordenadas de 192 átomos. La aplicación sobre los valores de x, y, z del signo + o -, la suma o resta de fracciones y otras características que están recogidas en la ficha del Grupo Espacial F en las Tablas Internacionales de Cristalografía, nos facilitará todas las posiciones de forma mucho más eficaz que enumerar una tras otra las coordenadas de los 192 átomos. El empleo de las Tablas Internacionales de Cristalografía aporta, además, información adicional sobre dicha estructura como por ejemplo sobre su simetría, sobre la relación entre cada uno de sus átomos y los elementos de simetría de la estructura, así como información para trabajar con rayos X y otras cuestiones. En los distintos ejercicios de esta práctica los alumnos deberán proyectar determinadas estructuras cristalinas sobre papel milimetrado. En los primeros ejercicios las coordenadas atómicas aparecerán enumeradas unas tras otras, mientras que en los siguientes ejercicios el alumno deberá hacer uso de las Tablas Internacionales de Cristalografía (Vol. A) o del Programa WYCKPOS para generar las posiciones de Wyckoff necesarias para realizar la proyección. 89
3 Figura 1. Reproducción parcial de las páginas correspondientes al grupo espacial F de las Tablas Internacionales de la Cristalografía, vol. A. En el recuadro azul están señaladas las Posiciones de Wyckoff para este grupo. 90
4 PROBLEMAS 1. El ReO 3 posee estructura cúbica (grupo espacial Pm 3 m, nº 221), con a = 3,748 Å. Los átomos de Re ocupan las posiciones 0,0,0 mientras que los átomos de O ocupan las posiciones ½,0,0; 0,½,0 y 0,0,½. a. Proyecta la estructura del ReO 3 sobre el plano (001) y deduce las posiciones equivalentes. b. Localiza y proyecta al menos dos elementos de simetría paralelos a la dirección de (001). c. Calcula cuántos átomos de Re y O hay en una celda unidad. 91
5 2. La cooperita (PtS) posee estructura tetragonal (grupo espacial P4 2 /mmc, nº 131), con a = 3, 48 Å y c = 6,11 Å. Los átomos de Pt ocupan las posiciones 0, ½,0 y ½, 0, ½, mientras que los átomos de S ocupan las posiciones ½,½,¼ y ½,½,¾. a. Proyecta la estructura del PtS sobre los planos plano (001) y deduce las posiciones equivalentes. b. Localiza y proyecta al menos dos elementos de simetría paralelos a la dirección (001). c. Calcula cuántos átomos de Pt y S hay en una celda unidad. 92
6 3. El CsCl posee estructura cúbica (grupo espacial Pm 3 m, nº 221), con a = 4,110 Å. Los átomos de Cs ocupan las posiciones especiales 1 a m 3 m y los átomos de Cl las posiciones, también especiales 1 b m 3 m. Con ayuda de las tablas internacionales de la Cristalografía: a. Proyecta la estructura del CsCl sobre el plano (001) y deduce las posiciones equivalentes. b. Localiza y proyecta al menos dos elementos de simetría paralelos a la dirección de (001). c. Cuántos átomos de Cs y Cl hay en una celda unidad? 93
7 4. Los compuestos de tipo perovskita, ABO 3 pueden considerarse derivados de la estructura tipo ReO 3. Podemos describir la estructura de la perovskita CaTiO 3 como idealmente cúbica (grupo espacial Pm 3 m, nº 221). Los átomos de Ti ocupan las posiciones especiales 1 a m 3 m, los átomos de Ca, las posiciones 1 b m 3 m. Finalmente, los átomos de O ocupan las posiciones, también especiales 3 d 4/mmm. Con ayuda de las tablas internacionales de la Cristalografía: a) Proyecta la estructura del CaTiO 3 sobre el plano (001) y deduce las posiciones equivalentes. b) Localiza y proyecta al menos dos elementos de simetría paralelos a la dirección de (001). c) Cuántos átomos de Ca, O y Ti hay en una celda unidad? 94
8 5. El Cromo, Cr, posee estructura cúbica (grupo espacial I m 3 m, nº 229), con a = 2,880 Å. Los átomos de Cr ocupan las posiciones especiales 2 a m 3 m. Esta información describe completamente la estructura. Con ayuda de la tabla de posiciones equivalentes (ver extracto abajo), proyecta la estructura del Cr sobre el plano (001) y deduce las posiciones equivalentes. Localiza y proyecta al menos dos elementos de simetría paralelos a la dirección de (001). Cuántos átomos de Cr hay en una celda unidad? Multiplicidad Posiciones de Wykoff del grupo espacial I m 3 m Letra de Wykoff Localización de los elementos de simetría Coordenadas (0,0,0)+ (½,½,½)+ 2 a m 3 m 0, 0, 0 95
9 6. El MgO posee estructura cúbica (grupo espacial Fm 3 m, nº 225), con a = 4,212 Å. Los átomos de O ocupan las posiciones especiales 4 a m 3 m y los átomos de Mg las posiciones, también especiales 4 b m 3 m. Con ayuda de la tabla de posiciones equivalentes (ver extracto abajo), proyecta la estructura del MgO sobre el plano (001) y deduce las posiciones equivalentes. Localiza y proyecta al menos dos elementos de simetría paralelos a la dirección de (001). Cuántos átomos de O y Mg hay en una celda unidad? Cuáles son las diferencias principales entre la estructura del MgO y la del ReO 3? Multiplicidad Posiciones de Wykoff del grupo espacial Fm 3 m Letra de Wykoff Localización de los elementos de simetría Coordenadas (0,0,0)+ (0,½,½)+ (½,0, ½)+ (½,½,0)+ 4 b m 3 m ½,½,½ 4 a m 3 m 0, 0, 0 96
10 7. El Rutilo (TiO 2 ) cristaliza en el grupo espacial P4 2 /mnm (nº 136) y posee los siguientes parámetros de red: a = 4,59 Å y c = 2,96 Å. En la estructura del rutilo, los átomos de Ti ocupan las posiciones especiales 2 a m.mm, mientras que los átomos de O las posiciones 4f m.2m., siendo x = 0.3. Con ayuda de las Tablas Internacionales de la Cristalografía, vol. A o el Servidor de Cristalografía de Bilbao, proyecta la estructura del rutilo sobre los planos (001) y (100), y deduce las posiciones equivalentes. Cuántos átomos de Ti y O hay en una celda unidad? Localiza los elementos de simetría perpendiculares a (001). 97
11 8. El β-sic posee estructura cúbica (grupo espacial F 4 3m, nº 216), con a = 4,3596 Å. Los átomos de C ocupan las posiciones especiales 4 a 4 3m y los átomos de Si las posiciones, también especiales 4 c 4 3m. Proyecta la estructura del β-sic sobre el plano (001) y deduce las posiciones equivalentes. Localiza y proyecta al menos dos elementos de simetría paralelos a la dirección de (001). Cuántos átomos de C y Si hay en una celda unidad? 98
12 9. La calcopirita (CuFeS 2 ) cristaliza en el grupo espacial I 4 2d (nº 122) y posee los siguientes parámetros de red: a = 5,25 Å y c = 10,32 Å. En la estructura de la calcopirita, los átomos de Cu ocupan las posiciones especiales 4 a 4, los átomos de Fe las posiciones 4 b 4 y los átomos de S las posiciones 8 d 2, siendo x 0,25. Proyecta la estructura de la calcopirita sobre los planos (001) y (100), y deduce las posiciones equivalentes. Cuántos átomos de Cu, Fe y S hay en una celda unidad? Existe alguna similitud con la estructura del β-sic (ejercicio 8)? 99
13 10. El compuesto imaginario AB, cuya celda tiene dimensiones a = 5 Å; y c = 7 Å, pertenece al grupo espacial P4 2 (nº 77). Los átomos de A ocupan las posiciones generales 4 d 1, siendo x = 0,1; y = 0,2 y z = 0,25. Los átomos B ocupan las posiciones especiales 2 a 2 con z = 0,5 y 2 b 2 siendo z = 0,25. Proyecta la estructura de este compuesto sobre los planos (001) y (100) y deduce las posiciones equivalentes. Localiza sus elementos de simetría. 100
14 BIBLIOGRAFÍA Arroyo, M.I.; Pérez-Mato, J.M.; Capillas, C.; Kroumova, S.; Madariaga, G.; Kirov, A. y Wondratschek Bilbao Crystallographic Server I: Databases and crystallographic programs. Zeitschnift fuer Kristallographie, 221(1), BIBLIOGRAFÍA DE CONSULTA Internacional Tables for Crystallography, Volume A, Space Group Symetry Editor: Theo Hahn. IUCr series. López-Acevedo Cornejo, V Modelos en Cristalografía. Madrid. 233 pp. RECURSOS ELECTRÓNICOS Bilbao Crystallographic Server. WYCKPOS (Wykoff Possitions of Space Groups) Recibido: 1 diciembre Aceptado: 28 diciembre
Geología de Grado en Química. Prácticas. 6. Simetría (III)
 Geología de Grado en Química. Prácticas. 6. Simetría (III) José Manuel Astilleros García-Monge. Sol López-Andrés. Cristóbal Viedma Molero. Elena Vindel Catena. Dpto. de Cristalografía y Mineralogía. Facultad
Geología de Grado en Química. Prácticas. 6. Simetría (III) José Manuel Astilleros García-Monge. Sol López-Andrés. Cristóbal Viedma Molero. Elena Vindel Catena. Dpto. de Cristalografía y Mineralogía. Facultad
SIMETRÍA INFINITA. nt = kt
 SIMETRÍA INFINITA Al considerar el cristal como un medio periódico en el cual un grupo de átomos (el motivo) se repite en las tres dimensiones del espacio, de manera que entre dos puntos homólogos de dos
SIMETRÍA INFINITA Al considerar el cristal como un medio periódico en el cual un grupo de átomos (el motivo) se repite en las tres dimensiones del espacio, de manera que entre dos puntos homólogos de dos
CAP. 1:ESTRUCTURAS CRISTALINAS
 CAP. 1:ESTRUCTURAS CRISTALINAS Sólidos cristalinos: amorfos: Disposiciones periódicas en el espacio Disposición al azar Situaciones intermedias: (no periódicas pero ordenadas) Estructuras moduladas Casicristales
CAP. 1:ESTRUCTURAS CRISTALINAS Sólidos cristalinos: amorfos: Disposiciones periódicas en el espacio Disposición al azar Situaciones intermedias: (no periódicas pero ordenadas) Estructuras moduladas Casicristales
TEMA 8: SÓLIDOS INORGÁNICOS. 2.- Redes bidimensionales y tridimensionales
 TEMA 8: SÓLIDOS INORGÁNICOS 1.- Tipos de sólidos 2.- Redes bidimensionales y tridimensionales 3.- Celda unidad y sus parámetros: - nº de átomos / celda - nº de coordinación (NC) - fracción de volumen ocupado
TEMA 8: SÓLIDOS INORGÁNICOS 1.- Tipos de sólidos 2.- Redes bidimensionales y tridimensionales 3.- Celda unidad y sus parámetros: - nº de átomos / celda - nº de coordinación (NC) - fracción de volumen ocupado
QUÍMICA INORGÁNICA I 9/1/17. El enlace iónico. Iones. Rafael Moreno Esparza
 QUÍMICA INORGÁNICA I Rafael Moreno Esparza 0 El enlace iónico Procedencia: La fuerza electrostática que mantiene unidos a dos átomos. Los átomos tratan de tener 8 electrones en la capa de valencia Los
QUÍMICA INORGÁNICA I Rafael Moreno Esparza 0 El enlace iónico Procedencia: La fuerza electrostática que mantiene unidos a dos átomos. Los átomos tratan de tener 8 electrones en la capa de valencia Los
CRISTALOGRAFIA. Es un sólido compuesto de átomos, iones o moléculas ordenados de una cierta forma y que se repite en tres dimensiones.
 CRISTALOGRAFIA CRISTAL SÓLIDO MONOCRISTALINO SÓLIDO POLICRISTALINO Es un sólido compuesto de átomos, iones o moléculas ordenados de una cierta forma y que se repite en tres dimensiones. Región donde el
CRISTALOGRAFIA CRISTAL SÓLIDO MONOCRISTALINO SÓLIDO POLICRISTALINO Es un sólido compuesto de átomos, iones o moléculas ordenados de una cierta forma y que se repite en tres dimensiones. Región donde el
Síntesis y Caracterización Estructural de los Materiales Ángel Carmelo Prieto Colorado
 Síntesis y Caracterización Estructural de los Materiales Ángel Carmelo Prieto Colorado Física de la Materia Condensada, Cristalografía y Mineralogía. Facultad de Ciencias. Universidad de Valladolid. Tema
Síntesis y Caracterización Estructural de los Materiales Ángel Carmelo Prieto Colorado Física de la Materia Condensada, Cristalografía y Mineralogía. Facultad de Ciencias. Universidad de Valladolid. Tema
Síntesis y Caracterización Estructural de los Materiales. Grado en Física.
 El hierro (Fe) sufre una tranformación polimórfica a 912 ºC, pasando de una estructura cubica centrada en el cuerpo (I o bcc) a una estructura cubica centrada en todas las caras (F o fcc). Sabiendo que
El hierro (Fe) sufre una tranformación polimórfica a 912 ºC, pasando de una estructura cubica centrada en el cuerpo (I o bcc) a una estructura cubica centrada en todas las caras (F o fcc). Sabiendo que
Guía Docente: GEOLOGÍA FACULTAD DE CIENCIAS QUÍMICAS UNIVERSIDAD COMPLUTENSE DE MADRID
 GEOLOGÍA FACULTAD DE CIENCIAS QUÍMICAS UNIVERSIDAD COMPLUTENSE DE MADRID I.- IDENTIFICACIÓN NOMBRE DE LA ASIGNATURA: CARÁCTER: MATERIA: MÓDULO: TITULACIÓN: SEMESTRE/CUATRIMESTRE: DEPARTAMENTO/S: Obligatoria
GEOLOGÍA FACULTAD DE CIENCIAS QUÍMICAS UNIVERSIDAD COMPLUTENSE DE MADRID I.- IDENTIFICACIÓN NOMBRE DE LA ASIGNATURA: CARÁCTER: MATERIA: MÓDULO: TITULACIÓN: SEMESTRE/CUATRIMESTRE: DEPARTAMENTO/S: Obligatoria
Grupos espaciales de simetría
 Grupos espaciales de simetría La simetría de los átomos que constituyen el cristal se describe con un grupo de simetría espacial constituido por un subgrupo de traslación (el retículo) y determinados elementos
Grupos espaciales de simetría La simetría de los átomos que constituyen el cristal se describe con un grupo de simetría espacial constituido por un subgrupo de traslación (el retículo) y determinados elementos
Síntesis y Caracterización Estructural de los Materiales Ángel Carmelo Prieto Colorado
 Síntesis y Caracterización Estructural de los Materiales Ángel Carmelo Prieto Colorado Física de la Materia Condensada, Cristalografía y Mineralogía. Facultad de Ciencias. Universidad de Valladolid. Tema
Síntesis y Caracterización Estructural de los Materiales Ángel Carmelo Prieto Colorado Física de la Materia Condensada, Cristalografía y Mineralogía. Facultad de Ciencias. Universidad de Valladolid. Tema
Estructura cristalina. Materiales para ingeniería en energía
 Estructura cristalina Materiales para ingeniería en energía Definiciones Además de la composición, otro aspecto fundamental que gobierna las propiedades físicas y químicas de los sólidos es la organización
Estructura cristalina Materiales para ingeniería en energía Definiciones Además de la composición, otro aspecto fundamental que gobierna las propiedades físicas y químicas de los sólidos es la organización
DRX Notación y Grupos Espaciales. Presentado por: Heiddy Paola Quiroz Gaitán Grupo de Materiales Nanoestructurados y sus Aplicaciones 2017
 DRX Notación y Grupos Espaciales Presentado por: Heiddy Paola Quiroz Gaitán Grupo de Materiales Nanoestructurados y sus Aplicaciones 2017 Contenido 1. Repaso sobre el Refinamiento. 2. Resultados del refinamiento.
DRX Notación y Grupos Espaciales Presentado por: Heiddy Paola Quiroz Gaitán Grupo de Materiales Nanoestructurados y sus Aplicaciones 2017 Contenido 1. Repaso sobre el Refinamiento. 2. Resultados del refinamiento.
CELDAS, DIRECCIONES Y PLANOS CRISTALOGRÁFICOS
 Programa de Actualización Mayo-Junio 2018 Módulo 2: Técnicas de caracterización de sólidos cristalinos I: Difracción de Rayos X. CELDAS, DIRECCIONES Y PLANOS CRISTALOGRÁFICOS Florencia Di Salvo Sebastián
Programa de Actualización Mayo-Junio 2018 Módulo 2: Técnicas de caracterización de sólidos cristalinos I: Difracción de Rayos X. CELDAS, DIRECCIONES Y PLANOS CRISTALOGRÁFICOS Florencia Di Salvo Sebastián
UNIVERSIDAD DE GRANADA
 UNIVERSIDAD DE GRANADA Departamento de Mineralogía y Petrología FACULTAD DE CIENCIAS, FUENTENUEVA S/N, 18002-GRANADA, ESPAÑA TEL.: 34 (9) 248535; FAX.: 34 (9) 58 243368; E-MAIL: MIPETRO@AZAHAR.UGR.ES PROGRAMA
UNIVERSIDAD DE GRANADA Departamento de Mineralogía y Petrología FACULTAD DE CIENCIAS, FUENTENUEVA S/N, 18002-GRANADA, ESPAÑA TEL.: 34 (9) 248535; FAX.: 34 (9) 58 243368; E-MAIL: MIPETRO@AZAHAR.UGR.ES PROGRAMA
Sólidos Iónicos El enlace Iónico (1)
 1 Sólidos Iónicos El enlace Iónico (1) 2 * Huheey, J. E., Keiter, R. L., Keiter, E. A., Inorganic Chemistry: Principles of Structure and Reactivity, 4ª Ed., Harper Collins, 1993. Capítulo 4. * Douglas,
1 Sólidos Iónicos El enlace Iónico (1) 2 * Huheey, J. E., Keiter, R. L., Keiter, E. A., Inorganic Chemistry: Principles of Structure and Reactivity, 4ª Ed., Harper Collins, 1993. Capítulo 4. * Douglas,
UNIDAD 1: LA MATERIA CRISTALINA
 UNIDAD 1: LA MATERIA CRISTALINA CONCEPTOS MATERIA CRISTALINA: Aquella cuyas partículas están perfectamente ordenadas en el espacio, ocupando posiciones fijas y a distancias regulares unas de otras, formando
UNIDAD 1: LA MATERIA CRISTALINA CONCEPTOS MATERIA CRISTALINA: Aquella cuyas partículas están perfectamente ordenadas en el espacio, ocupando posiciones fijas y a distancias regulares unas de otras, formando
ESTRUCTURA CRISTALINA
 SOLIDOS ESTRUCTURA CRISTALINA Dr. Andres Ozols 2005 Dr. A. Ozols 1 ALCANCE del ORDEN ATOMICO Estructura de corto alcance Estructura de alcance intermedio Estructura de largo alcance Dr. A. Ozols 2 TIPOS
SOLIDOS ESTRUCTURA CRISTALINA Dr. Andres Ozols 2005 Dr. A. Ozols 1 ALCANCE del ORDEN ATOMICO Estructura de corto alcance Estructura de alcance intermedio Estructura de largo alcance Dr. A. Ozols 2 TIPOS
Tema 1: Sólidos cristalinos Curso 2016/17
 Física del Estado Sólido I Tema 1: Sólidos cristalinos Curso 2016/17 Qué es un cristal? Un cristal ideal está formado por una distribución periódica tridimensional de átomos Desde hace siglos se observó
Física del Estado Sólido I Tema 1: Sólidos cristalinos Curso 2016/17 Qué es un cristal? Un cristal ideal está formado por una distribución periódica tridimensional de átomos Desde hace siglos se observó
Empaquetamiento compacto
 Empaquetamiento compacto Energía y empaquetamiento No denso, empaquetamiento aleatorio Energy Distancia del enlace energía de enlace Denso, empaquetamiento ordenado Energy distancia del enlace r Energía
Empaquetamiento compacto Energía y empaquetamiento No denso, empaquetamiento aleatorio Energy Distancia del enlace energía de enlace Denso, empaquetamiento ordenado Energy distancia del enlace r Energía
Jornada Docente sobre Cristalografía y Crecimiento de Cristales
 Jornada Docente sobre Cristalografía y Crecimiento de Cristales Unidad 2: Materiales sólidos y elementos de Cristalografía Clasificaciones de los materiales sólidos. Uniones químicas. Definición de Estructura
Jornada Docente sobre Cristalografía y Crecimiento de Cristales Unidad 2: Materiales sólidos y elementos de Cristalografía Clasificaciones de los materiales sólidos. Uniones químicas. Definición de Estructura
Luis Alberto Laguado Villamizar. Diseñador Industrial Mg Ingeniería de Materiales
 Luis Alberto Laguado Villamizar Diseñador Industrial Mg Ingeniería de Materiales CONTENIDO Estructura amorfa y cristalina Celdas Unitarias Redes de Bravais Parámetros de Red Índices de Miller Estructuras
Luis Alberto Laguado Villamizar Diseñador Industrial Mg Ingeniería de Materiales CONTENIDO Estructura amorfa y cristalina Celdas Unitarias Redes de Bravais Parámetros de Red Índices de Miller Estructuras
SÓLIDOS LÍQUIDOS - GASES
 Cristalografía 1 Fases Introducción Definición: n: porción de la materia con propiedades homogéneas La materia puede encontrarse en un gran número de fases. Las más conocidas están asociadas a sus estados
Cristalografía 1 Fases Introducción Definición: n: porción de la materia con propiedades homogéneas La materia puede encontrarse en un gran número de fases. Las más conocidas están asociadas a sus estados
Guía Docente: GEOLOGÍA
 GEOLOGÍA FACULTAD DE CIENCIAS QUÍMICAS UNIVERSIDAD COMPLUTENSE DE MADRID CURSO 2012-2013 I.- IDENTIFICACIÓN NOMBRE DE LA ASIGNATURA: CARÁCTER: MATERIA: MÓDULO: TITULACIÓN: SEMESTRE/CUATRIMESTRE: DEPARTAMENTO/S:
GEOLOGÍA FACULTAD DE CIENCIAS QUÍMICAS UNIVERSIDAD COMPLUTENSE DE MADRID CURSO 2012-2013 I.- IDENTIFICACIÓN NOMBRE DE LA ASIGNATURA: CARÁCTER: MATERIA: MÓDULO: TITULACIÓN: SEMESTRE/CUATRIMESTRE: DEPARTAMENTO/S:
CRISTALOQUÍMICA TEMA 6 ESTRUCTURAS CRISTALINAS. Empaquetados compactos. Coordinación
 CRISTALOQUÍMICA TEMA 6 ESTRUCTURAS CRISTALINAS Empaquetados compactos. Coordinación ÍNDICE 6.1 Introducción 6.2 Estructuras cristalinas 6.3 Enlace en las estructuras cristalinas 6.4 Cristales iónicos 6.5
CRISTALOQUÍMICA TEMA 6 ESTRUCTURAS CRISTALINAS Empaquetados compactos. Coordinación ÍNDICE 6.1 Introducción 6.2 Estructuras cristalinas 6.3 Enlace en las estructuras cristalinas 6.4 Cristales iónicos 6.5
UNIVERSIDAD NACIONAL AUTÓNOMA DE MÉXICO FACULTAD DE INGENIERÍA PROGRAMA DE ESTUDIO
 UNIVERSIDAD NACIONAL AUTÓNOMA DE MÉXICO FACULTAD DE INGENIERÍA PROGRAMA DE ESTUDIO MINERALOGÍA 0487 3 09 Asignatura Clave Semestre Créditos Ingeniería en Ciencias de la Tierra Geología Ingeniería Geofísica
UNIVERSIDAD NACIONAL AUTÓNOMA DE MÉXICO FACULTAD DE INGENIERÍA PROGRAMA DE ESTUDIO MINERALOGÍA 0487 3 09 Asignatura Clave Semestre Créditos Ingeniería en Ciencias de la Tierra Geología Ingeniería Geofísica
Estructuras Cristalinas
 Estructuras Cristalinas Bibliografía: Solid State Chemistry: An introduction, L. Smart and E. Moore. 1992 Solid State Chemistry and its applications, A.R. West. 1984 1 Enlace en Cerámicos Iónico Mezcla
Estructuras Cristalinas Bibliografía: Solid State Chemistry: An introduction, L. Smart and E. Moore. 1992 Solid State Chemistry and its applications, A.R. West. 1984 1 Enlace en Cerámicos Iónico Mezcla
4. El ClNa cristaliza en el sistema cúbico con parámetro [a]=5.631å. Calcular su densidad sabiendo que su masa molecular es 58.45 uma.
![4. El ClNa cristaliza en el sistema cúbico con parámetro [a]=5.631å. Calcular su densidad sabiendo que su masa molecular es 58.45 uma. 4. El ClNa cristaliza en el sistema cúbico con parámetro [a]=5.631å. Calcular su densidad sabiendo que su masa molecular es 58.45 uma.](/thumbs/28/12696458.jpg) Síntesis y Caracterización Estructural de los Materiales: Bases Cristalográficas. 1. Dibuje en las celdas fundamentales cúbicas adjuntas (a = 3 Å): a. Las filas reticulares de índices de Weiss [02-1],
Síntesis y Caracterización Estructural de los Materiales: Bases Cristalográficas. 1. Dibuje en las celdas fundamentales cúbicas adjuntas (a = 3 Å): a. Las filas reticulares de índices de Weiss [02-1],
FACULTAD DE CIENCIAS GRADO DE QUÍMICA CURSO 2013/14 ASIGNATURA: CRISTALOGRAFÍA Y MINERALOGÍA APLICADA DATOS DE LA ASIGNATURA
 FACULTAD DE CIENCIAS GRADO DE QUÍMICA CURSO 2013/14 ASIGNATURA: DATOS DE LA ASIGNATURA Denominación: Código: 100440 Plan de estudios: GRADO DE QUÍMICA Curso: 1 Denominación del módulo al que pertenece:
FACULTAD DE CIENCIAS GRADO DE QUÍMICA CURSO 2013/14 ASIGNATURA: DATOS DE LA ASIGNATURA Denominación: Código: 100440 Plan de estudios: GRADO DE QUÍMICA Curso: 1 Denominación del módulo al que pertenece:
 Caso de varios vectores primitivos de un mismo arreglo. Base o Motivo: Átomo o conjunto de átomos que se asocian con un punto de la malla Malla o Lattice: Es un arreglo infinito de puntos en el espacio,
Caso de varios vectores primitivos de un mismo arreglo. Base o Motivo: Átomo o conjunto de átomos que se asocian con un punto de la malla Malla o Lattice: Es un arreglo infinito de puntos en el espacio,
ESTRUCTURA * MOLÉCULAS COVALENTES (TRPECV) * METALES * COMPUESTOS IÓNICOS
 REPARTIDO 4 2007 ESTRUCTURA * MOLÉCULAS COVALENTES (TRPECV) * METALES * COMPUESTOS IÓNICOS Bibliografía: - Química, La Ciencia Central, T.L.Brown, H.E.LeMay, Jr., B. Bursten. Ed. Prentice-Hall, México,
REPARTIDO 4 2007 ESTRUCTURA * MOLÉCULAS COVALENTES (TRPECV) * METALES * COMPUESTOS IÓNICOS Bibliografía: - Química, La Ciencia Central, T.L.Brown, H.E.LeMay, Jr., B. Bursten. Ed. Prentice-Hall, México,
Aplicaciones de la teoría de grupos cristalográficos en cristaloquímica
 Aplicaciones de la teoría de grupos cristalográficos en cristaloquímica Manuales de químicas PROYECTO EDITORIAL CIENCIAS QUÍMICAS Director: Guillermo Calleja Pardo Áreas de publicación: QUÍMICA BÁSICA
Aplicaciones de la teoría de grupos cristalográficos en cristaloquímica Manuales de químicas PROYECTO EDITORIAL CIENCIAS QUÍMICAS Director: Guillermo Calleja Pardo Áreas de publicación: QUÍMICA BÁSICA
Geología de Grado en Química. Prácticas. 2. Reconocimiento de minerales y rocas mediante microscopía óptica
 Geología de Grado en Química. Prácticas. 2. Reconocimiento de minerales y rocas mediante microscopía óptica José Manuel Astilleros García-Monge. Sol López-Andrés. Cristóbal Viedma Molero. Elena Vindel
Geología de Grado en Química. Prácticas. 2. Reconocimiento de minerales y rocas mediante microscopía óptica José Manuel Astilleros García-Monge. Sol López-Andrés. Cristóbal Viedma Molero. Elena Vindel
ESTRUCTURAS CARACTERÍSTICAS
 ESTRUCTURAS CARACTERÍSTICAS En este capítulo se describen algunas estructuras muy simples que permitirán analizar la disposición de los átomos de diversos compuestos característicos en los que el enlace
ESTRUCTURAS CARACTERÍSTICAS En este capítulo se describen algunas estructuras muy simples que permitirán analizar la disposición de los átomos de diversos compuestos característicos en los que el enlace
Fisica de Celdas Fotovoltaicas. Parte I: Conceptos Previos
 Fisica de Celdas Fotovoltaicas Parte I: Conceptos Previos José L. Solis Universidad Nacional de Ingenieria Instituto Peruano de Energia Nuclear Materiales Semiconductores Los Semiconductores son un grupo
Fisica de Celdas Fotovoltaicas Parte I: Conceptos Previos José L. Solis Universidad Nacional de Ingenieria Instituto Peruano de Energia Nuclear Materiales Semiconductores Los Semiconductores son un grupo
2.2 Simetría en los sólidos cristalinos
 2.2 Simetría en los sólidos cristalinos Observación: Distribución de las caras en los cristales Sentido de proporción y equilibrio geométrico Simetría externa de los cristales permite: - Placer estético
2.2 Simetría en los sólidos cristalinos Observación: Distribución de las caras en los cristales Sentido de proporción y equilibrio geométrico Simetría externa de los cristales permite: - Placer estético
Determinación estructural. Grupos A y C. Curso Examen de la parte Químico Física. 22 de mayo de 2002
 Determinación estructural. Grupos A y C. Curso 2001-2002. Examen de la parte Químico íca. 22 de mayo de 2002 Completa, en letras mayúsculas, los datos personales que aparecen a continuación. Lee atentamente
Determinación estructural. Grupos A y C. Curso 2001-2002. Examen de la parte Químico íca. 22 de mayo de 2002 Completa, en letras mayúsculas, los datos personales que aparecen a continuación. Lee atentamente
CIENCIA E INGENIERÍA DE LOS MATERIALES
 CIENCIA E INGENIERÍA DE LOS MATERIALES ARREGLOS ATÓMICOS E IÓNICOS En los distintos estados de la materia podemos encontrar 4 clases de arreglos atómicos o iónicos: Sin orden Orden de corto alcance Orden
CIENCIA E INGENIERÍA DE LOS MATERIALES ARREGLOS ATÓMICOS E IÓNICOS En los distintos estados de la materia podemos encontrar 4 clases de arreglos atómicos o iónicos: Sin orden Orden de corto alcance Orden
Determinación estructural. Grupos A y C. Curso Examen de la parte Químico Física. Septiembre de 2002
 Determinación estructural. Grupos A y C. Curso 2001-2002. Examen de la parte Químico Fíca. Septiembre de 2002 Completa, en letras mayúsculas, los datos personales que aparecen a continuación. Lee atentamente
Determinación estructural. Grupos A y C. Curso 2001-2002. Examen de la parte Químico Fíca. Septiembre de 2002 Completa, en letras mayúsculas, los datos personales que aparecen a continuación. Lee atentamente
Los sólidos iónicos. Estructuras características de los sólidos iónicos
 Los sólidos iónicos Los compuestos iónicos suelen presentar una serie de características físicas que los distinguen de los covalentes. Así, los sólidos iónicos como el cloruro sódico y el nitrato de potasio
Los sólidos iónicos Los compuestos iónicos suelen presentar una serie de características físicas que los distinguen de los covalentes. Así, los sólidos iónicos como el cloruro sódico y el nitrato de potasio
Examen de Mejoramiento: Ciencias de Materiales
 Capítulo 2: Estructura atómica y enlaces interatómicos 1. El número atómico (para un representa: a) El número de protones b) El número de neutrones c) El número de electrones d) El número de protones,
Capítulo 2: Estructura atómica y enlaces interatómicos 1. El número atómico (para un representa: a) El número de protones b) El número de neutrones c) El número de electrones d) El número de protones,
Copyright The McGraw-Hill Companies, Inc. Permission required for reproduction or display ESTRUCTURAS CRISTALINAS
 ESTRUCTURAS CRISTALINAS PREGUNTAS SOBRE LA ESTRUCTURA DE MATERIALES SOLIDOS Cuál es la distribución de los átomos en los materiales sólidos? Qué es polimorfismo y alotropía en materiales? Cómo se describen
ESTRUCTURAS CRISTALINAS PREGUNTAS SOBRE LA ESTRUCTURA DE MATERIALES SOLIDOS Cuál es la distribución de los átomos en los materiales sólidos? Qué es polimorfismo y alotropía en materiales? Cómo se describen
uco.es/grados GUÍA DOCENTE DENOMINACIÓN DE LA ASIGNATURA DATOS DEL PROFESORADO REQUISITOS Y RECOMENDACIONES COMPETENCIAS OBJETIVOS
 Curso 17/18 DENOMINACIÓN DE LA ASIGNATURA Denominación: CRISTALOGRAFÍA Y MINERALOGÍA APLICADA Código: 144 Plan de estudios: GRADO DE QUÍMICA Curso: 1 Denominación del módulo al que pertenece: BÁSICO Materia:
Curso 17/18 DENOMINACIÓN DE LA ASIGNATURA Denominación: CRISTALOGRAFÍA Y MINERALOGÍA APLICADA Código: 144 Plan de estudios: GRADO DE QUÍMICA Curso: 1 Denominación del módulo al que pertenece: BÁSICO Materia:
Las fases condensadas (1)
 1 Las fases condensadas (1) 2 * Huheey, J. E., Keiter, R. L., Keiter, E. A., Inorganic Chemistry: Principles of Structure and Reactivity, 4ª Ed., Harper Collins, 1993. Capítulo 4 y 7. * Casabó i Gispert,
1 Las fases condensadas (1) 2 * Huheey, J. E., Keiter, R. L., Keiter, E. A., Inorganic Chemistry: Principles of Structure and Reactivity, 4ª Ed., Harper Collins, 1993. Capítulo 4 y 7. * Casabó i Gispert,
Estructura de la Materia
 Estructura de la Materia Décimo tercera sesión Propiedades periódicas de los elementos Alrededor de 30 propiedades de los elementos muestran periodicidad Propiedades Periódicas 1 Radio atómico Radio iónico
Estructura de la Materia Décimo tercera sesión Propiedades periódicas de los elementos Alrededor de 30 propiedades de los elementos muestran periodicidad Propiedades Periódicas 1 Radio atómico Radio iónico
Nombre, apellidos, DNI y Grupo. Pregunta 1 (25 puntos) Pregunta 2 (25 puntos) Pregunta 3 (25 puntos) Pregunta 4 (25 puntos)
 Determinación estructural. Grupos A y. urso 2001-2002. Examen de la parte Químico íca. 4 de diciembre de 2001 ompleta, en letras mayúsculas, los datos personales que aparecen a continuación. Lee atentamente
Determinación estructural. Grupos A y. urso 2001-2002. Examen de la parte Químico íca. 4 de diciembre de 2001 ompleta, en letras mayúsculas, los datos personales que aparecen a continuación. Lee atentamente
Tema 4. Cristaloquímica. Descripción estructural y
 Tema 4. Cristaloquímica. Descripción estructural y estructuras tipos Qué objetivos tiene la Cristaloquímica? Las fases cristalinas son componentes esenciales de los materiales, y especificamente de los
Tema 4. Cristaloquímica. Descripción estructural y estructuras tipos Qué objetivos tiene la Cristaloquímica? Las fases cristalinas son componentes esenciales de los materiales, y especificamente de los
Física Cuántica. Sólidos II. Requerimientos previos. José Manuel López y Luis Enrique González. Universidad de Valladolid. Curso p.
 Física Cuántica Sólidos II. Requerimientos previos. José Manuel López y Luis Enrique González Universidad de Valladolid Curso 2004-2005 p. 1/20 Red cristalina El primer dibujo de un cristal apareció en
Física Cuántica Sólidos II. Requerimientos previos. José Manuel López y Luis Enrique González Universidad de Valladolid Curso 2004-2005 p. 1/20 Red cristalina El primer dibujo de un cristal apareció en
Estado Sólido. Estado Sólido. Estado Sólido. Estado Sólido - + Sólidos cristalinos y sólidos amorfos
 Sólidos cristalinos y sólidos amorfos Sólidos cristalinos: presentan un ordenamiento regular en el espacio Sólidos amorfos: no presentan el ordenamiento típico de los cristalinos Región cristalina Región
Sólidos cristalinos y sólidos amorfos Sólidos cristalinos: presentan un ordenamiento regular en el espacio Sólidos amorfos: no presentan el ordenamiento típico de los cristalinos Región cristalina Región
PRACTICA 4: EMPAQUETAMIENTOS ATOMICOS. Laboratorio de Metalotecnia ETSIMO
 PRACTICA 4: EMPAQUETAMIENTOS ATOMICOS EMPAQUETAMIENOS ATOMICOS REFERENCIAS BIBLIOGRÁFICAS: Capítulo I del libro CIENCIA E INGENIERIA DE MATERIALES. Prof. José Antonio Pero-Sanz Elorz Cueva de Naica Chihuahua,
PRACTICA 4: EMPAQUETAMIENTOS ATOMICOS EMPAQUETAMIENOS ATOMICOS REFERENCIAS BIBLIOGRÁFICAS: Capítulo I del libro CIENCIA E INGENIERIA DE MATERIALES. Prof. José Antonio Pero-Sanz Elorz Cueva de Naica Chihuahua,
ALEACIONES 1. INTRODUCCION 2. CLASIFICACION 3. SOLUCIONES SÓLIDAS 4. FASES INTERMEDIAS 5. SOLUCIONES SÓLIDAS ORDENADAS M.V.M.G ALEACIONES 1
 ALEACIONES 1. INTRODUCCION 2. CLASIFICACION 3. SOLUCIONES SÓLIDAS 4. FASES INTERMEDIAS 5. SOLUCIONES SÓLIDAS ORDENADAS 2007-08 ALEACIONES 1 INTRODUCCIÓN Una aleación es la combinación de dos o más metales,
ALEACIONES 1. INTRODUCCION 2. CLASIFICACION 3. SOLUCIONES SÓLIDAS 4. FASES INTERMEDIAS 5. SOLUCIONES SÓLIDAS ORDENADAS 2007-08 ALEACIONES 1 INTRODUCCIÓN Una aleación es la combinación de dos o más metales,
Guía Docente: GEOLOGÍA
 GEOLOGÍA FACULTAD DE CIENCIAS QUÍMICAS UNIVERSIDAD COMPLUTENSE DE MADRID CURSO 2015-2016 I.- IDENTIFICACIÓN NOMBRE DE LA ASIGNATURA: CARÁCTER: MATERIA: MÓDULO: TITULACIÓN: SEMESTRE/CUATRIMESTRE: DEPARTAMENTO/S:
GEOLOGÍA FACULTAD DE CIENCIAS QUÍMICAS UNIVERSIDAD COMPLUTENSE DE MADRID CURSO 2015-2016 I.- IDENTIFICACIÓN NOMBRE DE LA ASIGNATURA: CARÁCTER: MATERIA: MÓDULO: TITULACIÓN: SEMESTRE/CUATRIMESTRE: DEPARTAMENTO/S:
ESTRU R C U T C UR U A R S A D E D LOS O MAT A ERI R AL A ES
 ESTRUCTURAS DE LOS MATERIALES Cristalina CRISTALINOS METALES COMPUESTOS IÓNICOS COMPUESTOS COMPLEJOS COV.-ION. SÓLIDOS COVALENTES COVALENTE PURO SÓLIDOS MOLECULARES NO CRISTALINOS (AMORFOS) VIDRIOS INORGÁNICOS
ESTRUCTURAS DE LOS MATERIALES Cristalina CRISTALINOS METALES COMPUESTOS IÓNICOS COMPUESTOS COMPLEJOS COV.-ION. SÓLIDOS COVALENTES COVALENTE PURO SÓLIDOS MOLECULARES NO CRISTALINOS (AMORFOS) VIDRIOS INORGÁNICOS
Ing. Fredy Velázquez Soto
 Ing. Fredy Velázquez Soto TIPOS DE SÓLIDOS Sólidos cristalinos Los átomos, iones o moléculas se empaquetan en un arreglo ordenado Sólidos covalentes ( diamante, cristales de cuarzo), sólidos metálicos,
Ing. Fredy Velázquez Soto TIPOS DE SÓLIDOS Sólidos cristalinos Los átomos, iones o moléculas se empaquetan en un arreglo ordenado Sólidos covalentes ( diamante, cristales de cuarzo), sólidos metálicos,
PROBLEMAS GEOMÉTRICOS SOBRE CRISTALES SIMPLES
 PROBLEMAS GEOMÉTRICOS SOBRE CRISTALES SIMPLES Control de Lectura 3 La materia del Control de Lectura 3 corresponderá principalmente a la geometría de cristales simples, en el contexto de un curso de Ciencia
PROBLEMAS GEOMÉTRICOS SOBRE CRISTALES SIMPLES Control de Lectura 3 La materia del Control de Lectura 3 corresponderá principalmente a la geometría de cristales simples, en el contexto de un curso de Ciencia
Materiales-G704/G742. Jesús Setién Marquínez Jose Antonio Casado del Prado Soraya Diego Cavia Carlos Thomas García
 Materiales-G704/G742 Lección 3. Estructura cristalina y amorfa Jesús Setién Marquínez Jose Antonio Casado del Prado Soraya Diego Cavia Carlos Thomas García Departamento de Ciencia e Ingeniería del Terreno
Materiales-G704/G742 Lección 3. Estructura cristalina y amorfa Jesús Setién Marquínez Jose Antonio Casado del Prado Soraya Diego Cavia Carlos Thomas García Departamento de Ciencia e Ingeniería del Terreno
SÓLIDOS INORGÁNICOS. Tema 6. FUNDAMENTOS
 SÓLIDOS INORGÁNICOS Tema 6. Fundamentos Tema 7. Sólidos metálicos Tema 8. Sólidos iónicos Tema 9. Sólidos covalentes Tema 10. Sólidos moleculares Tema 11. Defectos y no-estequiometría Tema 12. Propiedades
SÓLIDOS INORGÁNICOS Tema 6. Fundamentos Tema 7. Sólidos metálicos Tema 8. Sólidos iónicos Tema 9. Sólidos covalentes Tema 10. Sólidos moleculares Tema 11. Defectos y no-estequiometría Tema 12. Propiedades
Guía Docente: GEOLOGÍA
 GEOLOGÍA FACULTAD DE CIENCIAS QUÍMICAS UNIVERSIDAD COMPLUTENSE DE MADRID CURSO 2018-2019 I.- IDENTIFICACIÓN NOMBRE DE LA ASIGNATURA: CARÁCTER: MATERIA: MÓDULO: TITULACIÓN: SEMESTRE/CUATRIMESTRE: DEPARTAMENTO/S:
GEOLOGÍA FACULTAD DE CIENCIAS QUÍMICAS UNIVERSIDAD COMPLUTENSE DE MADRID CURSO 2018-2019 I.- IDENTIFICACIÓN NOMBRE DE LA ASIGNATURA: CARÁCTER: MATERIA: MÓDULO: TITULACIÓN: SEMESTRE/CUATRIMESTRE: DEPARTAMENTO/S:
Estructuras Cristalinas. Julio Alberto Aguilar Schafer
 Estructuras Cristalinas Julio Alberto Aguilar Schafer Modelo del estado líquido los metales Modelo del paso del estado líquido al estado sólido de los metales Equilibrio líquido-vapor Presión de vapor
Estructuras Cristalinas Julio Alberto Aguilar Schafer Modelo del estado líquido los metales Modelo del paso del estado líquido al estado sólido de los metales Equilibrio líquido-vapor Presión de vapor
UNIVERSIDAD NACIONAL DE EDUCACIÓN A DISTANCIA
 UNIVERSIDAD NACIONAL DE EDUCACIÓN A DISTANCIA NOMBRE.............................................. APELLIDOS........................................... CALLE................................................
UNIVERSIDAD NACIONAL DE EDUCACIÓN A DISTANCIA NOMBRE.............................................. APELLIDOS........................................... CALLE................................................
Proyecto de Innovación y Mejora de la Calidad Docente. Convocatoria Nº de proyecto: 12. Título del proyecto: Modelos de redes cristalográficas
 Proyecto de Innovación y Mejora de la Calidad Docente Convocatoria 2015 Nº de proyecto: 12 Título del proyecto: Modelos de redes cristalográficas Nombre del responsable del proyecto: Victoria López-Acevedo
Proyecto de Innovación y Mejora de la Calidad Docente Convocatoria 2015 Nº de proyecto: 12 Título del proyecto: Modelos de redes cristalográficas Nombre del responsable del proyecto: Victoria López-Acevedo
EL TAMAÑO DE LAS MOLECULAS ES FUNDAMENTAL EN ESTOS PROCESOS Y, EN ESTE CASO, LOS MODELOS USADOS DEVALORAN ESTE PARAMETRO
 2500 BIOMOLECULAS (REPRESENTADAS POR MODELOS DE ESFERAS Y TUBOS) A TRAVES DE UN CANAL CELULAR EL TAMAÑO DE LAS MOLECULAS ES FUNDAMENTAL EN ESTOS PROCESOS Y, EN ESTE CASO, LOS MODELOS USADOS DEVALORAN ESTE
2500 BIOMOLECULAS (REPRESENTADAS POR MODELOS DE ESFERAS Y TUBOS) A TRAVES DE UN CANAL CELULAR EL TAMAÑO DE LAS MOLECULAS ES FUNDAMENTAL EN ESTOS PROCESOS Y, EN ESTE CASO, LOS MODELOS USADOS DEVALORAN ESTE
ENLACE IÓNICO. Dra. Silvia Elena Castillo Blum
 ENLACE IÓNICO Dra. Silvia Elena Castillo Blum Enlace Químico ENLACE IÓNICO ENLACE COVALENTE ENLACE METÁLICO 2 Definición IUPAC Hay un enlace químico entre dos átomos o grupos de átomos cuando las fuerzas
ENLACE IÓNICO Dra. Silvia Elena Castillo Blum Enlace Químico ENLACE IÓNICO ENLACE COVALENTE ENLACE METÁLICO 2 Definición IUPAC Hay un enlace químico entre dos átomos o grupos de átomos cuando las fuerzas
TITULACIÓN DE FORMACIÓN CONTINUA BONIFICADA EXPEDIDA POR EL INSTITUTO EUROPEO DE ESTUDIOS EMPRESARIALES
 Técnico Profesional en Cristaloquímica de Materiales TITULACIÓN DE FORMACIÓN CONTINUA BONIFICADA EXPEDIDA POR EL INSTITUTO EUROPEO DE ESTUDIOS EMPRESARIALES Técnico Profesional en Cristaloquímica de Materiales
Técnico Profesional en Cristaloquímica de Materiales TITULACIÓN DE FORMACIÓN CONTINUA BONIFICADA EXPEDIDA POR EL INSTITUTO EUROPEO DE ESTUDIOS EMPRESARIALES Técnico Profesional en Cristaloquímica de Materiales
Complementos de Geología
 Master de Profesor de Educación Secundaria Obligatoria y Bachillerato, Formación Profesional y Enseñanzas de Idioma (Módulo Específico de Biología y Geología) Complementos de Geología Ángel Carmelo Prieto
Master de Profesor de Educación Secundaria Obligatoria y Bachillerato, Formación Profesional y Enseñanzas de Idioma (Módulo Específico de Biología y Geología) Complementos de Geología Ángel Carmelo Prieto
Tema 9. SOLIDOS COVALENTES
 Tema 9. SOLIDOS COVALENTES Introducción Estructuras de no-metales Boro Carbono Fósforo Arsénico, Antimonio y Bismuto Selenio y Telurio Estructuras de óxidos Estructuras basadas en tetraedros Estructuras
Tema 9. SOLIDOS COVALENTES Introducción Estructuras de no-metales Boro Carbono Fósforo Arsénico, Antimonio y Bismuto Selenio y Telurio Estructuras de óxidos Estructuras basadas en tetraedros Estructuras
Estructura de los Sólidos
 Estructura de los Sólidos Estructura Cristalina OBJETIVOS a) Definir sólidos cristalinos y amorfos b) Definir estructura cristalina c) Describir las diferentes estructuras cristalinas d) Utilizar índices
Estructura de los Sólidos Estructura Cristalina OBJETIVOS a) Definir sólidos cristalinos y amorfos b) Definir estructura cristalina c) Describir las diferentes estructuras cristalinas d) Utilizar índices
PRACTICA 4: EMPAQUETAMIENTOS ATOMICOS. Laboratorio de Metalotecnia ETSIMO
 PRACTICA 4: EMPAQUETAMIENTOS ATOMICOS EMPAQUETAMIENOS ATOMICOS REFERENCIAS BIBLIOGRÁFICAS: Capítulo I del libro CIENCIA E INGENIERIA DE MATERIALES. Prof. José Antonio Pero-Sanz Elorz Cueva de Naica Chihuahua,
PRACTICA 4: EMPAQUETAMIENTOS ATOMICOS EMPAQUETAMIENOS ATOMICOS REFERENCIAS BIBLIOGRÁFICAS: Capítulo I del libro CIENCIA E INGENIERIA DE MATERIALES. Prof. José Antonio Pero-Sanz Elorz Cueva de Naica Chihuahua,
EL ESTADO SÓLIDO CLASE I
 EL ESTADO SÓLIDO CLASE I CARACTERISTICAS DEL ESTADO SOLIDO Los átomos, iones o moléculas que componen un compuesto sólido están unidas entre sí por fuerzas intensas de cohesión, formando un todo compacto
EL ESTADO SÓLIDO CLASE I CARACTERISTICAS DEL ESTADO SOLIDO Los átomos, iones o moléculas que componen un compuesto sólido están unidas entre sí por fuerzas intensas de cohesión, formando un todo compacto
INTERACCIONES QUIMICAS
 UNIDAD 2 INTERACCIONES QUIMICAS 2.1) PARAMETROS DE ENLACE. DISTANCIA Y ENERGIA. ELECTRONEGATIVIDAD. 2.2) GEOMETRIA MOLECULAR Y MOMENTO DIPOLAR. POLARIZACION 2.3) CLASIFICACION DE INTERACCIONES QUIMICAS
UNIDAD 2 INTERACCIONES QUIMICAS 2.1) PARAMETROS DE ENLACE. DISTANCIA Y ENERGIA. ELECTRONEGATIVIDAD. 2.2) GEOMETRIA MOLECULAR Y MOMENTO DIPOLAR. POLARIZACION 2.3) CLASIFICACION DE INTERACCIONES QUIMICAS
TEMA 3º.- MINERALES 1º.- INTRODUCCIÓN
 1 1º.- INTRODUCCIÓN TEMA 3º.- MINERALES Mineral: Sólido, homogéneo, natural, con estructura atómica ordenada y una composición química definida. Excepciones: Sólido: Hg es sólido a temperatura ambiente
1 1º.- INTRODUCCIÓN TEMA 3º.- MINERALES Mineral: Sólido, homogéneo, natural, con estructura atómica ordenada y una composición química definida. Excepciones: Sólido: Hg es sólido a temperatura ambiente
CAPITULO 4 SISTEMAS IONICOS
 CAPITULO 4 SISTEMAS IONICOS 1 CUÁL DE LAS SIGUIENTES REACCIONES OCURRE EN SENTIDO INVERSO AL INDICADO? A) HCl + NaBr HBr + NaCl B) CsF + LiBr CsBr + LiF C) CaO + SrS CaS + SrO D) CaSO 4 + 2LiF Li 2 SO
CAPITULO 4 SISTEMAS IONICOS 1 CUÁL DE LAS SIGUIENTES REACCIONES OCURRE EN SENTIDO INVERSO AL INDICADO? A) HCl + NaBr HBr + NaCl B) CsF + LiBr CsBr + LiF C) CaO + SrS CaS + SrO D) CaSO 4 + 2LiF Li 2 SO
TEMA 4 (Parte I) EL ENLACE QUÍMICO. IÓNICO
 TEMA 4 (Parte I) EL ENLACE QUÍMICO. IÓNICO Mª PILAR RUIZ OJEDA BORJA MUÑOZ LEOZ Contenidos: 1. Introducción 2. Representaciones de Lewis. Regla del Octeto 3. El enlace Iónico 3.1. Redes iónicas 3.2. Energía
TEMA 4 (Parte I) EL ENLACE QUÍMICO. IÓNICO Mª PILAR RUIZ OJEDA BORJA MUÑOZ LEOZ Contenidos: 1. Introducción 2. Representaciones de Lewis. Regla del Octeto 3. El enlace Iónico 3.1. Redes iónicas 3.2. Energía
Guía Docente: GEOLOGÍA
 GEOLOGÍA FACULTAD DE CIENCIAS QUÍMICAS UNIVERSIDAD COMPLUTENSE DE MADRID CURSO 2013-2014 I.- IDENTIFICACIÓN NOMBRE DE LA ASIGNATURA: NÚMERO DE CRÉDITOS: 6 CARÁCTER: Obligatoria MATERIA: MÓDULO: Materias
GEOLOGÍA FACULTAD DE CIENCIAS QUÍMICAS UNIVERSIDAD COMPLUTENSE DE MADRID CURSO 2013-2014 I.- IDENTIFICACIÓN NOMBRE DE LA ASIGNATURA: NÚMERO DE CRÉDITOS: 6 CARÁCTER: Obligatoria MATERIA: MÓDULO: Materias
Tema 2: Enlace y propiedades de los materiales
 En la mayoría de moléculas, los enlaces entre los átomos que las constituyen no es mediante la interacción coulombiana que hemos analizado en el caso del enlace iónico. Se necesita tener en cuenta el llamado
En la mayoría de moléculas, los enlaces entre los átomos que las constituyen no es mediante la interacción coulombiana que hemos analizado en el caso del enlace iónico. Se necesita tener en cuenta el llamado
qwertyuiopasdfghjklzxcvbnmqwertyui opasdfghjklzxcvbnmqwertyuiopasdfgh jklzxcvbnmqwertyuiopasdfghjklzxcvb nmqwertyuiopasdfghjklzxcvbnmqwer
 qwertyuiopasdfghjklzxcvbnmqwertyui opasdfghjklzxcvbnmqwertyuiopasdfgh jklzxcvbnmqwertyuiopasdfghjklzxcvb nmqwertyuiopasdfghjklzxcvbnmqwer Cuestionario de Química 4 tyuiopasdfghjklzxcvbnmqwertyuiopas dfghjklzxcvbnmqwertyuiopasdfghjklzx
qwertyuiopasdfghjklzxcvbnmqwertyui opasdfghjklzxcvbnmqwertyuiopasdfgh jklzxcvbnmqwertyuiopasdfghjklzxcvb nmqwertyuiopasdfghjklzxcvbnmqwer Cuestionario de Química 4 tyuiopasdfghjklzxcvbnmqwertyuiopas dfghjklzxcvbnmqwertyuiopasdfghjklzx
Contenido. 5. Estructura cristalina. Omar De la Peña-Seaman IFUAP Física del Estado Sólido Maestría (Física) 1/51 51
 Contenido 5. Estructura cristalina 1 / Omar De la Peña-Seaman IFUAP Física del Estado Sólido Maestría (Física) 1/51 51 Contenido: Tema 05 5. Estructura cristalina 5.1 Arreglo periódico de átomos: bases,
Contenido 5. Estructura cristalina 1 / Omar De la Peña-Seaman IFUAP Física del Estado Sólido Maestría (Física) 1/51 51 Contenido: Tema 05 5. Estructura cristalina 5.1 Arreglo periódico de átomos: bases,
El Modelo Moderno y resultados de nuestro interés
 CLASES 3 Y 4 ESTRUCTURA ELECTRÓNICA DE LOS ELEMENTOS AL ESTADO FUNDAMENTAL. TABLA PERIÓDICA. ELECTRONEGATIVIDAD. El Modelo Moderno y resultados de nuestro interés Así es como el Modelo Moderno (MM) reemplazó
CLASES 3 Y 4 ESTRUCTURA ELECTRÓNICA DE LOS ELEMENTOS AL ESTADO FUNDAMENTAL. TABLA PERIÓDICA. ELECTRONEGATIVIDAD. El Modelo Moderno y resultados de nuestro interés Así es como el Modelo Moderno (MM) reemplazó
Tema 0. Conceptos Básicos en Química
 Tema 0. Conceptos Básicos en Química Química Átomo: números másicos y atómicos Mol Fórmulas empíricas y moleculares Reacciones químicas Gases Disoluciones Qué es la Química? Ciencia que estudia la composición
Tema 0. Conceptos Básicos en Química Química Átomo: números másicos y atómicos Mol Fórmulas empíricas y moleculares Reacciones químicas Gases Disoluciones Qué es la Química? Ciencia que estudia la composición
DIFRACCIÓN DE RAYOS X
 DIFRACCIÓN DE RAYOS X Difracción La difracción es el resultado de la dispersión de la radiación producida por una disposición regular de los centros de dispersión, cuyo espaciado es aproximadamente igual
DIFRACCIÓN DE RAYOS X Difracción La difracción es el resultado de la dispersión de la radiación producida por una disposición regular de los centros de dispersión, cuyo espaciado es aproximadamente igual
Objetivo. Introducción. Palabras clave. Desarrollo. Química Unidad 8 Enlace químico. 1. Interacciones entre átomos
 Química Unidad 8 Enlace químico Objetivo Comprender los conceptos básicos de los modelos de enlace iónico, covalente y metálico. Introducción Los electrones cumplen un papel fundamental en la formación
Química Unidad 8 Enlace químico Objetivo Comprender los conceptos básicos de los modelos de enlace iónico, covalente y metálico. Introducción Los electrones cumplen un papel fundamental en la formación
Actividad: Cómo son las configuraciones electrónicas?
 Cómo son las configuraciones electrónicas de los elementos que forman una familia? Nivel: 2º Medio Subsector: Ciencias químicas Unidad temática: Actividad: Cómo son las configuraciones electrónicas? En
Cómo son las configuraciones electrónicas de los elementos que forman una familia? Nivel: 2º Medio Subsector: Ciencias químicas Unidad temática: Actividad: Cómo son las configuraciones electrónicas? En
Modelo de Esferas Duras en Contacto.
 Modelo de Esferas Duras en Contacto. Este modelo explica las estructuras cristalinas que forman los metales puros, cuando estos metales presentan una simetría electrónica suficientemente esférica. Se ha
Modelo de Esferas Duras en Contacto. Este modelo explica las estructuras cristalinas que forman los metales puros, cuando estos metales presentan una simetría electrónica suficientemente esférica. Se ha
Estructura cristalina: Índices de Miller. Y en términos de grado de compacidad? Volumen de átomos= Volumen de la celda= ( ) 3
 1 Cuántos átomos hay en una celda unidad? Vértices 1/8 Caras 1/2 Número total de átomos en la celda unidad: 8 en los vértices: 8 x 1/8 = 1 6 en las caras: 6 x 1/2 = 3 Total: 4 átomos Y en términos de grado
1 Cuántos átomos hay en una celda unidad? Vértices 1/8 Caras 1/2 Número total de átomos en la celda unidad: 8 en los vértices: 8 x 1/8 = 1 6 en las caras: 6 x 1/2 = 3 Total: 4 átomos Y en términos de grado
ESTRUCTURA ATÓMICA Y PROPIEDADES PERIÓDICAS
 ESTRUCTURA ATÓMICA Y PROPIEDADES PERIÓDICAS 1.- Escriba la configuración electrónica de los siguientes iones o elementos: 8 O -2, 9 F - y 10 Ne, e indique el período y grupo de los elementos correspondientes.
ESTRUCTURA ATÓMICA Y PROPIEDADES PERIÓDICAS 1.- Escriba la configuración electrónica de los siguientes iones o elementos: 8 O -2, 9 F - y 10 Ne, e indique el período y grupo de los elementos correspondientes.
CRISTALOGRAFÍA GEOMÉTRICA TEMA 2 PERIODICIDAD, REDES CRISTALINAS, SÍMBOLOS Y NOTACIONES ÍNDICE
 CRISTALOGRAFÍA GEOMÉTRICA TEMA 2 PERIODICIDAD, REDES CRISTALINAS, SÍMBOLOS Y NOTACIONES REDES 2.1 Traslación 2.2 Red cristalina 2.3 Redes planas 2.4 Redes espaciales 2.5 Origen de la red 2.6 Celda elemental
CRISTALOGRAFÍA GEOMÉTRICA TEMA 2 PERIODICIDAD, REDES CRISTALINAS, SÍMBOLOS Y NOTACIONES REDES 2.1 Traslación 2.2 Red cristalina 2.3 Redes planas 2.4 Redes espaciales 2.5 Origen de la red 2.6 Celda elemental
MINERALOGÍA TEMA 27.3 CICLOSILICATOS. ÍNDICE 27.3 Ciclosilicatos. Celia Marcos Pascual
 MINERALOGÍA TEMA 27.3 CICLOSILICATOS ÍNDICE 27.3 Ciclosilicatos 1 Los ciclosilicatos están formados por anillos de tetraedros enlazados, con una relación Si:O = 1:3, pudiendo presentar tres posibles configuraciones
MINERALOGÍA TEMA 27.3 CICLOSILICATOS ÍNDICE 27.3 Ciclosilicatos 1 Los ciclosilicatos están formados por anillos de tetraedros enlazados, con una relación Si:O = 1:3, pudiendo presentar tres posibles configuraciones
REFUERZO ESPECIAL CIENCIAS NATURALES. APRENDIZAJE ESPERADO: Afianzar los procesos básicos del área para su promoción al siguiente grado.
 REFUERZO ESPECIAL CIENCIAS NATURALES SÉPTIMO PERIODO IV IVON GÓMEZ APRENDIZAJE ESPERADO: Afianzar los procesos básicos del área para su promoción al siguiente grado. Apreciado estudiante: Las actividades
REFUERZO ESPECIAL CIENCIAS NATURALES SÉPTIMO PERIODO IV IVON GÓMEZ APRENDIZAJE ESPERADO: Afianzar los procesos básicos del área para su promoción al siguiente grado. Apreciado estudiante: Las actividades
ESTRUCTURA DE LOS MATERIALES 2. 25/02/2012 Elaboró Ing. Efrén Giraldo T. 1
 ESTRUCTURA DE LOS MATERIALES 2 25/02/2012 Elaboró Ing. Efrén Giraldo T. 1 FACTOR DE EMPAQUETAMIENTO FEA = (No de átomos por celda. Vol de un átomo) / V (celda) 25/02/2012 Elaboró Ing. Efrén Giraldo T.
ESTRUCTURA DE LOS MATERIALES 2 25/02/2012 Elaboró Ing. Efrén Giraldo T. 1 FACTOR DE EMPAQUETAMIENTO FEA = (No de átomos por celda. Vol de un átomo) / V (celda) 25/02/2012 Elaboró Ing. Efrén Giraldo T.
EL ESTADO SOLIDO CLASE II
 EL ESTADO SOLIDO CLASE II ESTRUCTURA DE LOS METALES En la unión metálica puede considerarse que los átomos ceden sus electrones de valencia - formando una nube de e - - y se convierten en cationes Teoría
EL ESTADO SOLIDO CLASE II ESTRUCTURA DE LOS METALES En la unión metálica puede considerarse que los átomos ceden sus electrones de valencia - formando una nube de e - - y se convierten en cationes Teoría
UNIDAD IV. 4.6 Índices de Miller. Direcciones y Planos compactos. e ** Para Sistema cubico y hexagonal.
 Fundamentos de Metalurgia y Materiales UNIDAD IV 4.6 Índices de Miller. Direcciones y Planos compactos. e ** Para Sistema cubico y hexagonal. 4.7 Huecos Intersticiales. Huecos Tetraédricos y Octaédricos.
Fundamentos de Metalurgia y Materiales UNIDAD IV 4.6 Índices de Miller. Direcciones y Planos compactos. e ** Para Sistema cubico y hexagonal. 4.7 Huecos Intersticiales. Huecos Tetraédricos y Octaédricos.
