Química Anaĺıtica I (CLAVE 1402) Laboratorio
|
|
|
- César Luna Iglesias
- hace 7 años
- Vistas:
Transcripción
1 Química Anaĺıtica I (CLAVE 1402) Laboratorio Silvia Citlalli Gama González Ciudad Universitaria a, 10 de agosto de 2016
2 Contenido 1 Conceptos básicos de Matemáticas 2
3 Contenido 1 Conceptos básicos de Matemáticas 2
4 1 Conceptos básicos de Matemáticas 2
5 Definición Conceptos básicos de Matemáticas En matemáticas, el logaritmo de un número -en una base determinada-es el exponente al cual hay que elevar la base para obtener dicho número. log (b) X = n x = b n Por ejemplo, el logaritmo de 1000 en base 10 es 3, porque 1000 es igual a 10 a la potencia 3: 10 3 = 10x10x10.
6 Propiedades e Identidades Propiedades De la misma manera que la operación opuesta a la suma es la resta y de la multiplicación la división, la logaritmación es la operación inversa a la exponenciación de la base del logaritmo. La base b tiene que ser positiva y distinta a 1. X tiene que ser un número positivo. n puede ser cualquier número real. Identidades log(ab) = log(a) + log(b) ( a ) ( ) log(a) log = b log(b) log(a x ) = xlog(a) log( x y) = log(y) x
7 1 Conceptos básicos de Matemáticas 2
8 Definición Conceptos básicos de Matemáticas es una operación matemática entre dos términos denominados: base a y exponente n. Se escribe a n y se lee usualmente como a elevado a n y el sufijo en femenino correspondiente al exponenten. Hay algunos números especiales, como el 2 al cuadrado o el 3 al cubo. Cuando el exponente es un número natural, equivalea multiplicar un número por si mismo varias veces: el exponente determina la cantidad de veces. a n = ax...xa n veces Cuando el exponente es un número entero negativo, equivala a la fracción inversa de la base pero con exponente positivo. a p = 1 a p Cuando el exponente es una fracción irreducible n/m, equivale a una raíz. a n/m = m a n La definición de potenciación puede exterderse a exponentes reales, complejo o incluso matriciales.
9 Propiedades I Conceptos básicos de Matemáticas Potencia de exponente 0. Un número elevado al exponente 0 da como resultado la unidad, puesto que: 1 = an a n = an n = a 0 Potencia de exponente 1. Toda potencia de exponente 1 es igual a la base: a 1 = a Potencia de exponente negativo. Un número elevado a un expoente negativo, es igual al inverso de la misma expresión pero con exponente positivo: a n = a 0 n = a0 a n = 1 a n Multiplicación de potencias de igual base. El producto de dos potencias que tienene la misma base es otra potencia de la misma base y de exponente la suma de los exponentes: a m a n = a m+n
10 Propiedades II Conceptos básicos de Matemáticas División de potencias de igual base. El cociente de dos potencias que tienen la misma base es otra potencia de la misma base y de exponente la diferencia de los exponentes: Potencia de un producto. a m a n = am n La potencia de un producto es igual al producto de cada uno de los factores elevado al mismo exponente: (a b) n = a n b n Potencia de una potencia. La potencia de una potencia de base a es igual a la potencia de base a cuyo exponente es el producto de ambos exponentes: (a m ) n = a m n Propiedades que NO cumple la potenciación. No es distributiva con respecto a la adición y sustracción, es decir, no se puede distribuir cuando dentro del paréntesis se suma o se resta: (a + b) n a m + b m (a b) n a m b m
11 Propiedades III Conceptos básicos de Matemáticas No cumple la propiedad conmutativa, exceptuando aquellos casos en que base y exponente tengan el mismo valor o son equivalentes. En general: a b b a Tampoco cumple la propiedad asociativa: a bc = a (bc ) ( a b) c = a (bc) = a bc
12 1 Conceptos básicos de Matemáticas 2
13 Obtener la igualdad según el caso ( [Pb(CH3 COO) 1 2 ][H + ] 2 ) log [Pb 2+ ][CH 3 COOH] 2 = ( ) 2 ) 2 ) log 7.8 ) 2 ) 2 = 3 log( [OH ] [OH ] [OH ] 3 ) = 4 log ) = 5 log( ) = 6 log( [OH ] [OH ] [OH ] 3 ) = Evaluar la función a ph 11
14 Obtener la igualdad según el caso ( [Pb(CH3 COO) 1 2 ][H + ] 2 ) log [Pb 2+ ][CH 3 COOH] 2 = log[pb(ch 3 COO) 2 ] + 2log[H 2 ] log[pb 2+ ] 2log[CH 3 COOH] ( ) ( ) 5.9 ) 2 ) ) 2 log 7.8 ) 2 ) 2 = log 10 ( = log ) = 10 ( ) = ) 3 log( [OH ] [OH ] [OH ] 3 ) = log(1) + log 8 [OH ]) + log 14 [OH ] 2 ) + log 18 [OH ] 3 ) 4 log ) =log 1 ) 5 log( ) = log(43.28) = log( [OH ] [OH ] [OH ] 3 ) = Evaluar la función a ph 11 log( ) = log( ) = log ) =
15 Obtener la igualdad según el caso ( [Pb(CH3 COO) 1 2 ][H + ] 2 ) log [Pb 2+ ][CH 3 COOH] 2 = log[pb(ch 3 COO) 2 ] + 2log[H 2 ] log[pb 2+ ] 2log[CH 3 COOH] ( ) ( ) 5.9 ) 2 ) ) 2 log 7.8 ) 2 ) 2 = log 10 ( = log ) = 10 ( ) = ) 3 log( [OH ] [OH ] [OH ] 3 ) = log(1) + log 8 [OH ]) + log 14 [OH ] 2 ) + log 18 [OH ] 3 ) 4 log ) =log 1 ) 5 log( ) = log(43.28) = log( [OH ] [OH ] [OH ] 3 ) = Evaluar la función a ph 11 log( ) = log( ) = log ) =
16 Obtener la igualdad según el caso ( [Pb(CH3 COO) 1 2 ][H + ] 2 ) log [Pb 2+ ][CH 3 COOH] 2 = log[pb(ch 3 COO) 2 ] + 2log[H 2 ] log[pb 2+ ] 2log[CH 3 COOH] ( ) ( ) 5.9 ) 2 ) ) 2 log 7.8 ) 2 ) 2 = log 10 ( = log ) = 10 ( ) = ) 3 log( [OH ] [OH ] [OH ] 3 ) = log(1) + log 8 [OH ]) + log 14 [OH ] 2 ) + log 18 [OH ] 3 ) 4 log ) =log 1 ) 5 log( ) = log(43.28) = log( [OH ] [OH ] [OH ] 3 ) = Evaluar la función a ph 11 log( ) = log( ) = log ) =
17 Obtener la igualdad según el caso ( [Pb(CH3 COO) 1 2 ][H + ] 2 ) log [Pb 2+ ][CH 3 COOH] 2 = log[pb(ch 3 COO) 2 ] + 2log[H 2 ] log[pb 2+ ] 2log[CH 3 COOH] ( ) ( ) 5.9 ) 2 ) ) 2 log 7.8 ) 2 ) 2 = log 10 ( = log ) = 10 ( ) = ) 3 log( [OH ] [OH ] [OH ] 3 ) = log(1) + log 8 [OH ]) + log 14 [OH ] 2 ) + log 18 [OH ] 3 ) 4 log ) =log 1 ) 5 log( ) = log(43.28) = log( [OH ] [OH ] [OH ] 3 ) = Evaluar la función a ph 11 log( ) = log( ) = log ) =
18 Obtener la igualdad según el caso ( [Pb(CH3 COO) 1 2 ][H + ] 2 ) log [Pb 2+ ][CH 3 COOH] 2 = log[pb(ch 3 COO) 2 ] + 2log[H 2 ] log[pb 2+ ] 2log[CH 3 COOH] ( ) ( ) 5.9 ) 2 ) ) 2 log 7.8 ) 2 ) 2 = log 10 ( = log ) = 10 ( ) = ) 3 log( [OH ] [OH ] [OH ] 3 ) = log(1) + log 8 [OH ]) + log 14 [OH ] 2 ) + log 18 [OH ] 3 ) 4 log ) =log 1 ) 5 log( ) = log(43.28) = log( [OH ] [OH ] [OH ] 3 ) = Evaluar la función a ph 11 log( ) = log( ) = log ) =
19 Obtener la igualdad según el caso ( [Pb(CH3 COO) 1 2 ][H + ] 2 ) log [Pb 2+ ][CH 3 COOH] 2 = log[pb(ch 3 COO) 2 ] + 2log[H 2 ] log[pb 2+ ] 2log[CH 3 COOH] ( ) ( ) 5.9 ) 2 ) ) 2 log 7.8 ) 2 ) 2 = log 10 ( = log ) = 10 ( ) = ) 3 log( [OH ] [OH ] [OH ] 3 ) = log(1) + log 8 [OH ]) + log 14 [OH ] 2 ) + log 18 [OH ] 3 ) 4 log ) =log 1 ) 5 log( ) = log(43.28) = log( [OH ] [OH ] [OH ] 3 ) = Evaluar la función a ph 11 log( ) = log( ) = log ) =
20 Obtener la igualdad según el caso ( [Pb(CH3 COO) 1 2 ][H + ] 2 ) log [Pb 2+ ][CH 3 COOH] 2 = log[pb(ch 3 COO) 2 ] + 2log[H 2 ] log[pb 2+ ] 2log[CH 3 COOH] ( ) ( ) 5.9 ) 2 ) ) 2 log 7.8 ) 2 ) 2 = log 10 ( = log ) = 10 ( ) = ) 3 log( [OH ] [OH ] [OH ] 3 ) = log(1) + log 8 [OH ]) + log 14 [OH ] 2 ) + log 18 [OH ] 3 ) 4 log ) =log 1 ) 5 log( ) = log(43.28) = log( [OH ] [OH ] [OH ] 3 ) = Evaluar la función a ph 11 log( ) = log( ) = log ) =
21 Obtener la igualdad según el caso ( [Pb(CH3 COO) 1 2 ][H + ] 2 ) log [Pb 2+ ][CH 3 COOH] 2 = log[pb(ch 3 COO) 2 ] + 2log[H 2 ] log[pb 2+ ] 2log[CH 3 COOH] ( ) ( ) 5.9 ) 2 ) ) 2 log 7.8 ) 2 ) 2 = log 10 ( = log ) = 10 ( ) = ) 3 log( [OH ] [OH ] [OH ] 3 ) = log(1) + log 8 [OH ]) + log 14 [OH ] 2 ) + log 18 [OH ] 3 ) 4 log ) =log 1 ) 5 log( ) = log(43.28) = log( [OH ] [OH ] [OH ] 3 ) = Evaluar la función a ph 11 log( ) = log( ) = log ) =
22 Obtener la igualdad según el caso ( [Pb(CH3 COO) 1 2 ][H + ] 2 ) log [Pb 2+ ][CH 3 COOH] 2 = log[pb(ch 3 COO) 2 ] + 2log[H 2 ] log[pb 2+ ] 2log[CH 3 COOH] ( ) ( ) 5.9 ) 2 ) ) 2 log 7.8 ) 2 ) 2 = log 10 ( = log ) = 10 ( ) = ) 3 log( [OH ] [OH ] [OH ] 3 ) = log(1) + log 8 [OH ]) + log 14 [OH ] 2 ) + log 18 [OH ] 3 ) 4 log ) =log 1 ) 5 log( ) = log(43.28) = log( [OH ] [OH ] [OH ] 3 ) = Evaluar la función a ph 11 log( ) = log( ) = log ) =
23 Obtener la igualdad según el caso ( [Pb(CH3 COO) 1 2 ][H + ] 2 ) log [Pb 2+ ][CH 3 COOH] 2 = log[pb(ch 3 COO) 2 ] + 2log[H 2 ] log[pb 2+ ] 2log[CH 3 COOH] ( ) ( ) 5.9 ) 2 ) ) 2 log 7.8 ) 2 ) 2 = log 10 ( = log ) = 10 ( ) = ) 3 log( [OH ] [OH ] [OH ] 3 ) = log(1) + log 8 [OH ]) + log 14 [OH ] 2 ) + log 18 [OH ] 3 ) 4 log ) =log 1 ) 5 log( ) = log(43.28) = log( [OH ] [OH ] [OH ] 3 ) = Evaluar la función a ph 11 log( ) = log( ) = log ) =
24 Obtener la igualdad según el caso ( [Pb(CH3 COO) 1 2 ][H + ] 2 ) log [Pb 2+ ][CH 3 COOH] 2 = log[pb(ch 3 COO) 2 ] + 2log[H 2 ] log[pb 2+ ] 2log[CH 3 COOH] ( ) ( ) 5.9 ) 2 ) ) 2 log 7.8 ) 2 ) 2 = log 10 ( = log ) = 10 ( ) = ) 3 log( [OH ] [OH ] [OH ] 3 ) = log(1) + log 8 [OH ]) + log 14 [OH ] 2 ) + log 18 [OH ] 3 ) 4 log ) =log 1 ) 5 log( ) = log(43.28) = log( [OH ] [OH ] [OH ] 3 ) = Evaluar la función a ph 11 log( ) = log( ) = log ) =
25 Obtener la igualdad según el caso ( [Pb(CH3 COO) 1 2 ][H + ] 2 ) log [Pb 2+ ][CH 3 COOH] 2 = log[pb(ch 3 COO) 2 ] + 2log[H 2 ] log[pb 2+ ] 2log[CH 3 COOH] ( ) ( ) 5.9 ) 2 ) ) 2 log 7.8 ) 2 ) 2 = log 10 ( = log ) = 10 ( ) = ) 3 log( [OH ] [OH ] [OH ] 3 ) = log(1) + log 8 [OH ]) + log 14 [OH ] 2 ) + log 18 [OH ] 3 ) 4 log ) =log 1 ) 5 log( ) = log(43.28) = log( [OH ] [OH ] [OH ] 3 ) = Evaluar la función a ph 11 log( ) = log( ) = log ) =
26 Obtener la igualdad según el caso ( [Pb(CH3 COO) 1 2 ][H + ] 2 ) log [Pb 2+ ][CH 3 COOH] 2 = log[pb(ch 3 COO) 2 ] + 2log[H 2 ] log[pb 2+ ] 2log[CH 3 COOH] ( ) ( ) 5.9 ) 2 ) ) 2 log 7.8 ) 2 ) 2 = log 10 ( = log ) = 10 ( ) = ) 3 log( [OH ] [OH ] [OH ] 3 ) = log(1) + log 8 [OH ]) + log 14 [OH ] 2 ) + log 18 [OH ] 3 ) 4 log ) =log 1 ) 5 log( ) = log(43.28) = log( [OH ] [OH ] [OH ] 3 ) = Evaluar la función a ph 11 log( ) = log( ) = log ) =
27 Obtener la igualdad según el caso ( [Pb(CH3 COO) 1 2 ][H + ] 2 ) log [Pb 2+ ][CH 3 COOH] 2 = log[pb(ch 3 COO) 2 ] + 2log[H 2 ] log[pb 2+ ] 2log[CH 3 COOH] ( ) ( ) 5.9 ) 2 ) ) 2 log 7.8 ) 2 ) 2 = log 10 ( = log ) = 10 ( ) = ) 3 log( [OH ] [OH ] [OH ] 3 ) = log(1) + log 8 [OH ]) + log 14 [OH ] 2 ) + log 18 [OH ] 3 ) 4 log ) =log 1 ) 5 log( ) = log(43.28) = log( [OH ] [OH ] [OH ] 3 ) = Evaluar la función a ph 11 log( ) = log( ) = log ) =
28 1 Conceptos básicos de Matemáticas 2
29 Ecuación de Nerst Fe 3+ (ac) + 1e Fe 2+ (ac) E 0 = 0.771V Cu 2+ (ac) + 2e Cu 0 (s) E 0 = 0.337V Ecuación de Nernst de una media celda o semicelda E = 0.771V V log [Fe3+ ] 1 [Fe 2+ ] E = 0.337V V log[cu 2+ ] 2 Pb(CH 3 COO) 4 + OH + 2e Pb(OH) + + 4CH 3 COO E 0 Ecuación de Nernst se incluye al oxidante, al reductor y todo lo que los acompaña E = E V log [Pb(CH 3COO) 4 ][OH ] 2 [Pb(OH) + ][CH 3 COO ] 4
30 Reacciones Oxido-Reducción La cuantitatividad de cualquier reacción esta determinada por su constante de equilibrio Calculo de la constante de reacción a partir de datos de potencial logk eq = ( E 0 )n etotales 0.006v Es fundamental hacer notar que la constante de reacción depende no solo del E 0 sino también del número total de electrones. EJEMPLO 2(Fe 3+ (ac) + 1e Fe 2+ (ac) ) E 0 = 0.771V Cu(s) 0 Cu2+ (ac) + 2e E 0 = 0.337V - 2Fe 3+ (ac) + Cu0 (s) Cu2+ (ac) + 2Fe2+ (ac) E 0 = 0.434V logk eq = (0.434V )2 0.06V = 14.47
31 Predicción de reacciones Para determinar si un proceso esta favoresido o no termodinamicamente se puede recurrir a una estrategia esquemática rápida ubicando en una escala de potencial, E, los E 0 de las medias celdas correspondientes. MUY IMPORTANTE Observar que ésta escala nos permite identificar cuándo una reacción SI es cuantitativa o cuándo NO lo es, termodinamicamente hablando, sin embargo, nos nos da informacin sobre el tiempo que tomara para que la reaccin se lleve a cabo, esto es campo de la cintica que no esta contemplada en este modelo. Por otro lado s tenemos varais reacciones posibles, la escala nos permite identificar aquella que es ms favorecida termodinamicamente como aquella que tiene los valores de E 0 ms separados; esto est directamente relacionado con el G de la reaccin.
32 Anfolitos I Conceptos básicos de Matemáticas No es extraño que en función de las condiciones presentes en el medio de reacción se encuentren anfolitos redox que cambian de ser estables a inestables; cuando lo segundo sucede es necesario determinar cuál será el nuevo par redox que impondrá el potencial de la disolución y su correspondiente E 0. Calculo del E 0 del nuevo par E 0 = n oxe 0 ox + n red E 0 red n ox + n red
33 Anfolitos II Ejemplo Conceptos básicos de Matemáticas Se sabe que a ph=0 los valores de E 0 del sistema de nitratos-nitritos-oxodo nitroso son: NO 3 + 2e + 2H + NO 2 + H 2O E 0 = 0.850V NO 2 + 1e + 2H + NO (g) + H 2 O E 0 = 1.22V Al obtener la Escala de Predicción de Reacciones se encuentra que al ph indicado el anfolito NO2 es inestable y dismuta para dar los productos NO3 y NO (g). Por ellos se concluye que éste será el nuevo par redox, el que impondrá las propiedades de la disolución y su potencial normal estara dado por: 2(0.850V ) + 1(1.22V ) E NO 3 /NO = = 0.973V (g) 1 + 2
34 1 Conceptos básicos de Matemáticas 2
35 División del comportamiento ácido-base Para su estudio se ha encontrado que es práctico dividir el comportamiento de las especies con propiedades ácidas o básicas en fuertes, de fuerza media o débiles de acuerdo al siguiente criterio 1. 1 α es el grado de disociación
36 Ácidos Conceptos básicos de Matemáticas HA + H 2 O H 3 O + + A Ka = [A ][H 3 O + ] [HA] Ácido nivelado. ph = log(c HA ) Se disocia al 100 % sin importar su concentración. Ácido no nivelado fuerte. ph = log(c HA ) Se disocia más del 90 %. Ácido no nivelado de fuerza media. [H + ] 2 + Ka[H + ] KaC HA = 0 Se disocia menos del 90 % pero más del 10 %. Ácido no nivelado débil. ph = 1 2 pka 1 2 log(c HA) Se disocia menos del 10 %. ph de una mezcla de ácidos que no reaccionan entre si y anfolitos. ph = pka 1 + pka 2 2
37 Bases Conceptos básicos de Matemáticas A + H 2 O HA + OH Kb = [HA][OH ] [A ] Base fuerte. ph = 14 log(c A ) Se disocia más del 90 %. Base de fuerza media. C A [H + ] 2 + Kw[H + ] KaKw = 0 Se disocia menos del 90 % pero más del 10 %. Base débil. ph = pka log(c A) Se disocia menos del 10 %.
38 Relaciones fundamentales Relación entre Ka y Kb. Kb = Kw ó pkb = pkw + pka Ka Relación entre [H + ] y [OH ]. Kw = [H + ][OH ] = ó pkw = ph + poh = 14 ph para los sistemas amortiguados. ph = pka + log [BASE] [ACIDO]
39 Escala de predicción de reacciones
40 1 Conceptos básicos de Matemáticas 2
41 Constantes comunes en los equilibrios de complejación Constante Equilibrio Características Relación con otras constantes β n M m+ + nl ML m+ n FORMACIÓN β n = k f1 k f2... k fn GLOBAL β n = 1 k dis1 k dis2... k disn k fn ML m+ n 1 + L MLm+ n FORMACIÓN k fn = βn β n 1 SUSCESIVA k fn = 1 k disn k disn ML m+ n ML m+ n 1 + L DISOCIACIÓN k dis n = β n 1 β n SUSCESIVA k disn = 1 k fn
42 Ejemplo Conceptos básicos de Matemáticas Constante Equilibrio Características Relación con otras constantes β 3 Fe Cl FeCl 3 FORMACIÓN β 3 = k f1 k f2 k 3 GLOBAL β 3 = 1 k dis1 k dis2 k dis3 k f3 FeCl Cl FeCl 3 FORMACIÓN k f3 = β 3 β 2 SUSCESIVA k f3 = 1 k dis3 k dis3 FeCl 3 FeCl Cl DISOCIACIÓN k disn = β 2 β 3 SUSCESIVA k disn = 1 k f3
QUÍMICA ANALÍTICA II Curso Intersemestral
 QUÍMICA ANALÍTICA II Curso Intersemestral Del 9 al 20 de enero de 2011 ( total de 40 hrs.) 9:00 13:30 hrs. con media hora de descanso El objetivo principal es lograr que los estudiantes adquieran los conocimientos
QUÍMICA ANALÍTICA II Curso Intersemestral Del 9 al 20 de enero de 2011 ( total de 40 hrs.) 9:00 13:30 hrs. con media hora de descanso El objetivo principal es lograr que los estudiantes adquieran los conocimientos
DEPARTAMENTO DE BIOQUÍMICA ESFUNO EUTM. ACIDOS Y BASES, ph, BUFFERS
 DEPARTAMENTO DE BIOQUÍMICA ESFUNO EUTM ACIDOS Y BASES, ph, BUFFERS Ionización del agua y producto iónico del agua (K w ) H 2 O H + + OH - K eq = [H + ][OH - ] [H 2 O] K eq = [H + ][OH - ] [H 2 O] K eq
DEPARTAMENTO DE BIOQUÍMICA ESFUNO EUTM ACIDOS Y BASES, ph, BUFFERS Ionización del agua y producto iónico del agua (K w ) H 2 O H + + OH - K eq = [H + ][OH - ] [H 2 O] K eq = [H + ][OH - ] [H 2 O] K eq
1. ADICIÓN O SUMA Caso (a): Adición de un número Racional con uno Irracional: La suma de un número racional con uno Irracional es otro irracional.
 ADICIÓN, SUSTRACCIÓN, MULTIPLICACIÓN, DIVISIÓN, POTENCIACIÓN Y RADICACIÓN EN LOS NÚMEROS REALES. Hoy en día si hablamos de números seguramente nos damos cuenta de que es un tema muy extenso. Pero, hace
ADICIÓN, SUSTRACCIÓN, MULTIPLICACIÓN, DIVISIÓN, POTENCIACIÓN Y RADICACIÓN EN LOS NÚMEROS REALES. Hoy en día si hablamos de números seguramente nos damos cuenta de que es un tema muy extenso. Pero, hace
Prof. Mario Alfredo García Carrillo Semestre 2017-I
 Tarea 2 1. Se tienen los siguientes sistemas redox: Sistema E 0 (V) Sistema E 0 (V) Ba 2+ /Ba 0 2.92 IO 3 / IO 0.14 Al 3+ /Al 0 1.68 I 2 /I 0.62 Ga 3+ /Ga 2+ 0.65 IO 3 /I 2 1.19 Ga 2+ /Ga 0 0.45 Fe 3+
Tarea 2 1. Se tienen los siguientes sistemas redox: Sistema E 0 (V) Sistema E 0 (V) Ba 2+ /Ba 0 2.92 IO 3 / IO 0.14 Al 3+ /Al 0 1.68 I 2 /I 0.62 Ga 3+ /Ga 2+ 0.65 IO 3 /I 2 1.19 Ga 2+ /Ga 0 0.45 Fe 3+
Suma. Propiedades de la suma.
 Suma. La suma es la operación matemática que resulta al reunir en una sola a varias cantidades. También se conoce a la suma como adición. Las cantidades que se suman se llaman sumandos y el resultado suma
Suma. La suma es la operación matemática que resulta al reunir en una sola a varias cantidades. También se conoce a la suma como adición. Las cantidades que se suman se llaman sumandos y el resultado suma
Conjuntos numéricos. Apuntes de Matemática I. Tatiana Inés Gibelli C.U.R.Z.A.
 Conjuntos numéricos Apuntes de Matemática I Tatiana Inés Gibelli C.U.R.Z.A. Un concepto básico y elemental del lenguaje matemático es el de número. Para poder trabajar en matemática, es imprescindible
Conjuntos numéricos Apuntes de Matemática I Tatiana Inés Gibelli C.U.R.Z.A. Un concepto básico y elemental del lenguaje matemático es el de número. Para poder trabajar en matemática, es imprescindible
ÍNDICE PRÓLOGO RECOMENDACIONES PARA EL ESTUDIO CAPÍTULO 1. Expresión de los resultados analíticos... 17
 ÍNDICE PRÓLOGO... 13 RECOMENDACIONES PARA EL ESTUDIO... 15 CAPÍTULO 1. Expresión de los resultados analíticos... 17 1. Unidades químicas más utilizadas... 19 2. Formas de expresar la concentración... 20
ÍNDICE PRÓLOGO... 13 RECOMENDACIONES PARA EL ESTUDIO... 15 CAPÍTULO 1. Expresión de los resultados analíticos... 17 1. Unidades químicas más utilizadas... 19 2. Formas de expresar la concentración... 20
Reacciones Ácido Base
 Reacciones Ácido Base Prof. Sergio Casas-Cordero E. sacce Contenido: (parte uno) 1. Definiciones 2. Equilibrio iónico del agua 3. Potencial de acidez; escala de ph 4. Fuerza de ácidos y bases 5. Medición
Reacciones Ácido Base Prof. Sergio Casas-Cordero E. sacce Contenido: (parte uno) 1. Definiciones 2. Equilibrio iónico del agua 3. Potencial de acidez; escala de ph 4. Fuerza de ácidos y bases 5. Medición
TEMA 3. NÚMEROS RACIONALES.
 TEMA 3. NÚMEROS RACIONALES. Concepto de fracción Una fracción es el cociente de dos números enteros a y b, que representamos de la siguiente forma: b denominador, indica el número de partes en que se ha
TEMA 3. NÚMEROS RACIONALES. Concepto de fracción Una fracción es el cociente de dos números enteros a y b, que representamos de la siguiente forma: b denominador, indica el número de partes en que se ha
OBJETIVOS ESPECÍFICOS. Al finalizar el Tema el estudiante:
 OBJETIVOS ESPECÍFICOS TEMA IV: ELECTROQUÍMICA: Al finalizar el Tema el estudiante: 1.1 Establecerá qué tipo de proceso es el que ocurre en una celda galvánica o pila. 1.2 Identificará los diferentes tipos
OBJETIVOS ESPECÍFICOS TEMA IV: ELECTROQUÍMICA: Al finalizar el Tema el estudiante: 1.1 Establecerá qué tipo de proceso es el que ocurre en una celda galvánica o pila. 1.2 Identificará los diferentes tipos
QUÍMICA ANALÍTICA I. Serie de problemas Reactividad Química. DR. ALEJANDRO BAEZA
 1 QUÍMICA ANALÍTICA I Serie de problemas Reactividad Química DR. 2004 http://mx.geocities.com/electroquimika 2 QUIMICA ANALITICA I Ejercicio de clase, REAC(1): Pares conjugados, escalas de reactividad
1 QUÍMICA ANALÍTICA I Serie de problemas Reactividad Química DR. 2004 http://mx.geocities.com/electroquimika 2 QUIMICA ANALITICA I Ejercicio de clase, REAC(1): Pares conjugados, escalas de reactividad
UNIDAD DE APRENDIZAJE II
 UNIDAD DE APRENDIZAJE II Saberes procedimentales 1. Multiplicar y dividir números enteros y fraccionarios 2. Utilizar las propiedad conmutativas y asociativa Saberes declarativos A Concepto de base, potencia
UNIDAD DE APRENDIZAJE II Saberes procedimentales 1. Multiplicar y dividir números enteros y fraccionarios 2. Utilizar las propiedad conmutativas y asociativa Saberes declarativos A Concepto de base, potencia
K a = K b = Algunos ejercicios resueltos de FISICOQUIMICA- I ( , Grupo 3º) Hoja nº 5 (Modulo 2, tema 9: Eq.
 Algunos ejercicios resueltos de FISICOQUIMICA- I (2017-2018, Grupo 3º) Hoja nº 5 (Modulo 2, tema 9: Eq. Químico ionico) 3) Considerando comportamiento ideal, calcúlese el ph de las siguientes disoluciones
Algunos ejercicios resueltos de FISICOQUIMICA- I (2017-2018, Grupo 3º) Hoja nº 5 (Modulo 2, tema 9: Eq. Químico ionico) 3) Considerando comportamiento ideal, calcúlese el ph de las siguientes disoluciones
PROBLEMAS RESUELTOS SELECTIVIDAD ANDALUCÍA 2009 QUÍMICA TEMA 6: EQUILIBRIOS ÁCIDO-BASE
 PROBLEMAS RESUELTOS SELECTIVIDAD ANDALUCÍA 009 QUÍMICA TEMA 6: EQUILIBRIOS ÁCIDO-BASE Junio, Ejercicio, Opción A Junio, Ejercicio 5, Opción B Reserva 1, Ejercicio 5, Opción A Reserva 1, Ejercicio 4, Opción
PROBLEMAS RESUELTOS SELECTIVIDAD ANDALUCÍA 009 QUÍMICA TEMA 6: EQUILIBRIOS ÁCIDO-BASE Junio, Ejercicio, Opción A Junio, Ejercicio 5, Opción B Reserva 1, Ejercicio 5, Opción A Reserva 1, Ejercicio 4, Opción
EQUILIBRIO QUÍMICO ÁCIDO - BASE
 EQUILIBRIO QUÍMICO ÁCIDO - BASE TEMARIO 1) Química Analítica. Análisis Químico Cualitativo y Análisis Químico Cuantitativo 2) Importancia de la Química Analítica en la carrera de Agronomía 3) Equilibrio
EQUILIBRIO QUÍMICO ÁCIDO - BASE TEMARIO 1) Química Analítica. Análisis Químico Cualitativo y Análisis Químico Cuantitativo 2) Importancia de la Química Analítica en la carrera de Agronomía 3) Equilibrio
INSTITUCIÓN EDUCATIVA TÉCNICA SAGRADO CORAZÓN Aprobada según Resolución No NIT DANE SOLEDAD ATLÁNTICO.
 Página 1 de 16 GUÍA N 1 ÁREA: Docente: Matemáticas LAURA PACHECO C EJE TEMÁTICO DESEMPEÑO NÚCLEO TEMÁTICO: GRADO: Noveno PERIODO: Primero IH (en horas): 4 NÚMEROS REALES Resuelve problemas y simplifica
Página 1 de 16 GUÍA N 1 ÁREA: Docente: Matemáticas LAURA PACHECO C EJE TEMÁTICO DESEMPEÑO NÚCLEO TEMÁTICO: GRADO: Noveno PERIODO: Primero IH (en horas): 4 NÚMEROS REALES Resuelve problemas y simplifica
Matemáticas. Matías Puello Chamorro. Algebra Operativa. 9 de agosto de 2016
 Matemáticas Algebra Operativa Matías Puello Chamorro http://www.unilibrebaq.edu.co 9 de agosto de 2016 Índice 1. Introducción 3 2. Definiciones básicas del Algebra 4 2.1. Definición de igualdad............................
Matemáticas Algebra Operativa Matías Puello Chamorro http://www.unilibrebaq.edu.co 9 de agosto de 2016 Índice 1. Introducción 3 2. Definiciones básicas del Algebra 4 2.1. Definición de igualdad............................
Reacciones ácido-base: equilibrios cotidianos. Prof: Mario Azan
 Reacciones ácido-base: equilibrios cotidianos Prof: Mario Azan Diferenciando ácidos y bases Indicadores ácido-base Extracto vegetal, el cual adquiere dos colores claramente diferenciados según se encuentre
Reacciones ácido-base: equilibrios cotidianos Prof: Mario Azan Diferenciando ácidos y bases Indicadores ácido-base Extracto vegetal, el cual adquiere dos colores claramente diferenciados según se encuentre
RESUMEN DE CONCEPTOS
 RESUMEN DE CONCEPTOS 1º ESO MATEMÁTICAS NÚMEROS NATURALES (1) Múltiplo de un número: Un número es múltiplo de otro si el segundo está contenido en el primero un número exacto de veces. Ejemplo: 16 es múltiplo
RESUMEN DE CONCEPTOS 1º ESO MATEMÁTICAS NÚMEROS NATURALES (1) Múltiplo de un número: Un número es múltiplo de otro si el segundo está contenido en el primero un número exacto de veces. Ejemplo: 16 es múltiplo
5.1 Números Reales Mate 3041 Milena Salcedo V. Copyright Cengage Learning. All rights reserved.
 5.1 Números Reales Mate 3041 Milena Salcedo V R Copyright Cengage Learning. All rights reserved. Números Reales Números Naturales: N = 1,2,3, Números Enteros no negativos (Cardinales): 0,1,2,3, Números
5.1 Números Reales Mate 3041 Milena Salcedo V R Copyright Cengage Learning. All rights reserved. Números Reales Números Naturales: N = 1,2,3, Números Enteros no negativos (Cardinales): 0,1,2,3, Números
PROBLEMAS RESUELTOS SELECTIVIDAD ANDALUCÍA 2009 QUÍMICA TEMA 6: EQUILIBRIOS ÁCIDO-BASE
 PROBLEMAS RESUELTOS SELECTIVIDAD ANDALUCÍA 009 QUÍMICA TEMA 6: EQUILIBRIOS ÁCIDO-BASE Junio, Ejercicio, Opción A Junio, Ejercicio 5, Opción B Reserva 1, Ejercicio 5, Opción A Reserva 1, Ejercicio 4, Opción
PROBLEMAS RESUELTOS SELECTIVIDAD ANDALUCÍA 009 QUÍMICA TEMA 6: EQUILIBRIOS ÁCIDO-BASE Junio, Ejercicio, Opción A Junio, Ejercicio 5, Opción B Reserva 1, Ejercicio 5, Opción A Reserva 1, Ejercicio 4, Opción
Colegio La Salle Envigado FORMANDO EN VALORES PARA LA VIDA GUIA FACTORIZACION
 GUIA FACTORIZACION Esta guía tiene como objetivo afianzar los conocimientos teórico-prácticos en los diferentes casos de factorización, para ello se darán en esta guía algunos ejercicios de factorización
GUIA FACTORIZACION Esta guía tiene como objetivo afianzar los conocimientos teórico-prácticos en los diferentes casos de factorización, para ello se darán en esta guía algunos ejercicios de factorización
OPERACIONES CON NÚMEROS ENTEROS.
 OPERACIONES CON NÚMEROS ENTEROS. SUMA DE NÚMEROS ENTEROS. 1) Si tengo en mi bolsillo $50 y en la cartera tengo $350 en total tengo la cantidad de $400 Esto es: $50 + $350 = $400 2) Si debo a un amigo $80
OPERACIONES CON NÚMEROS ENTEROS. SUMA DE NÚMEROS ENTEROS. 1) Si tengo en mi bolsillo $50 y en la cartera tengo $350 en total tengo la cantidad de $400 Esto es: $50 + $350 = $400 2) Si debo a un amigo $80
La fracción disociada dependerá del valor del Ka y de Co: HCl. El nuevo estado de equilibrio dependerá de la cantidad adicionada de HCl.
 QUÍMICA ANALÍTICA I Documento de apoyo (4b): Reactividad Química. Equilibrio forzado. Diagramas Unidimensionales de Predominio de Especies, DUZP. Dr. Alejandro Baeza. Semestre 2010-II. Equilibrio forzado
QUÍMICA ANALÍTICA I Documento de apoyo (4b): Reactividad Química. Equilibrio forzado. Diagramas Unidimensionales de Predominio de Especies, DUZP. Dr. Alejandro Baeza. Semestre 2010-II. Equilibrio forzado
INSTITUCION EDUCATIVA LA PRESENTACION
 INSTITUCION EDUCATIVA LA PRESENTACION Nombre de la alumna: Área: MATEMATICAS Asignatura: Matemáticas Docente: Luis López Zuleta Tipo de Guía: Conceptual PERIODO GRADO FECHA DURACION DOS 6º 04 de mayo de
INSTITUCION EDUCATIVA LA PRESENTACION Nombre de la alumna: Área: MATEMATICAS Asignatura: Matemáticas Docente: Luis López Zuleta Tipo de Guía: Conceptual PERIODO GRADO FECHA DURACION DOS 6º 04 de mayo de
PARES CONJUGADOS/PARTÍCULA INTERCAMBIADA
 QUÍMICA ANALÍTICA I Documento de apoyo (4a): Reactividad Química. K reacción. Conceptos. Dr. Alejandro Baeza. Semestre 200II. REACCIÓN QUÍMICA: Generalización Predicción Reproducibilidad CONTROL MODELO:
QUÍMICA ANALÍTICA I Documento de apoyo (4a): Reactividad Química. K reacción. Conceptos. Dr. Alejandro Baeza. Semestre 200II. REACCIÓN QUÍMICA: Generalización Predicción Reproducibilidad CONTROL MODELO:
Capítulo. Multiplicación y división de enteros. Copyright 2013, 2010, and 2007, Pearson Education, Inc.
 Capítulo 5 Multiplicación y división de enteros Definición informal de la multiplicación de enteros Modelo de fichas Interpretación del signo: 3 grupos de 2 fichas rojas Modelo de cargas Interpretación
Capítulo 5 Multiplicación y división de enteros Definición informal de la multiplicación de enteros Modelo de fichas Interpretación del signo: 3 grupos de 2 fichas rojas Modelo de cargas Interpretación
Soluciones reguladoras
 Soluciones reguladoras Química General e Inorgánica 18 de abril de 2016 Prof. Dra. Marisa Repetto Primer cuatrimestre 2016 Neutralización ácido-base 17 ml HNO 2 0,25 M Ka= 4,6 x 10-4 20 ml NaOH 0,18 M
Soluciones reguladoras Química General e Inorgánica 18 de abril de 2016 Prof. Dra. Marisa Repetto Primer cuatrimestre 2016 Neutralización ácido-base 17 ml HNO 2 0,25 M Ka= 4,6 x 10-4 20 ml NaOH 0,18 M
MODELOS NO LINEALES. Alejandro Vera Trejo
 MODELOS NO LINEALES Alejandro Vera Trejo Objetivo Se representará una situación determinada a través de la construcción de una o varias ecuaciones no lineales. Se solucionarán situaciones reales a través
MODELOS NO LINEALES Alejandro Vera Trejo Objetivo Se representará una situación determinada a través de la construcción de una o varias ecuaciones no lineales. Se solucionarán situaciones reales a través
Operaciones con números racionales. SUMA/RESTA.
 http//www.colegiovirgendegracia.org/eso/dmate.htm ARITMÉTICA Números racionales.9. Operaciones con números racionales. SUMA/RESTA. (A) Reducción a común denominador 4 y 7 4 4 y 7 6 y 4 80 80 80 80 (B)
http//www.colegiovirgendegracia.org/eso/dmate.htm ARITMÉTICA Números racionales.9. Operaciones con números racionales. SUMA/RESTA. (A) Reducción a común denominador 4 y 7 4 4 y 7 6 y 4 80 80 80 80 (B)
Algebra Operativa. Definiciones Básicas. Matías Enrique Puello Chamorro
 Algebra Operativa. Definiciones Básicas Matías Enrique Puello Chamorro www.matiaspuello.wordpress.com 21 de febrero de 2018 Índice 1. Introducción 3 2. Definiciones básicas del Algebra 4 2.1. Definición
Algebra Operativa. Definiciones Básicas Matías Enrique Puello Chamorro www.matiaspuello.wordpress.com 21 de febrero de 2018 Índice 1. Introducción 3 2. Definiciones básicas del Algebra 4 2.1. Definición
ANÁLISIS VOLUMÉTRICO
 ANÁLISIS VOLUMÉTRICO Análisis Volumétrico mc + nr Cm Rn Reacción cuantitativa Sol. de conc. exactamente conocida Medición exacta de Volumen Pto. Equivalencia Soluciones patrones Valoración o Titulación
ANÁLISIS VOLUMÉTRICO Análisis Volumétrico mc + nr Cm Rn Reacción cuantitativa Sol. de conc. exactamente conocida Medición exacta de Volumen Pto. Equivalencia Soluciones patrones Valoración o Titulación
COMPRENDER EL CONCEPTO DE POTENCIA
 REPASO Y APOYO OBJETIVO 1 COMPRENDER EL CONCEPTO DE POTENCIA Una potencia de un número entero es una forma abreviada de escribir una multiplicación de números enteros iguales. a " Base: el número entero
REPASO Y APOYO OBJETIVO 1 COMPRENDER EL CONCEPTO DE POTENCIA Una potencia de un número entero es una forma abreviada de escribir una multiplicación de números enteros iguales. a " Base: el número entero
QUIMICA ANALITICA III Documento de Apoyo: Acidez-precipitación. Casos generales: HA/MA y H 2 A/HA - /MA. Dr. Alejandro Baeza.
 QUIMICA ANALITICA III Documento de Apoyo: Acidez-precipitación. Casos generales: A/MA y A/A - /MA. Dr.. Planteamiento del sistema en estudio Las propiedades ácido-base de un par conjugado cambian en presencia
QUIMICA ANALITICA III Documento de Apoyo: Acidez-precipitación. Casos generales: A/MA y A/A - /MA. Dr.. Planteamiento del sistema en estudio Las propiedades ácido-base de un par conjugado cambian en presencia
TEMA 8. Equilibrios Redox y de Solubilidad. Grabado de Heinrich Khunrath, Amphitheatrum Sapientiae Aeternae Hannover, 1609
 TEMA 8. Equilibrios Redox y de Solubilidad Grabado de Heinrich Khunrath, Amphitheatrum Sapientiae Aeternae Hannover, 1609 Equilibrio Redox: Estados de Oxidación ESTADOS DE OXIDACIÓN Muchos elementos forman
TEMA 8. Equilibrios Redox y de Solubilidad Grabado de Heinrich Khunrath, Amphitheatrum Sapientiae Aeternae Hannover, 1609 Equilibrio Redox: Estados de Oxidación ESTADOS DE OXIDACIÓN Muchos elementos forman
Números Naturales. Cero elemento neutro: = 12 Sucesión fundamental : se obtiene el siguiente número = 9
 Números Naturales Cuando comenzamos a contar los objetos, los años, etc, nos hemos encontrado con los números de forma natural; por eso a este conjunto de números así aprendidos se les denomina números
Números Naturales Cuando comenzamos a contar los objetos, los años, etc, nos hemos encontrado con los números de forma natural; por eso a este conjunto de números así aprendidos se les denomina números
Problemas y cuestiones de REACCIONES ÁCIDO-BASE 2º de bachillerato. Química
 1 Problemas y cuestiones de REACCIONES ÁCIDO-BASE 2º de bachillerato. Química 1. Se prepara 500 ml de una disolución que contiene 0,2 moles de un ácido orgánico monoprótico cuyo ph es 5,7. calcule: a)
1 Problemas y cuestiones de REACCIONES ÁCIDO-BASE 2º de bachillerato. Química 1. Se prepara 500 ml de una disolución que contiene 0,2 moles de un ácido orgánico monoprótico cuyo ph es 5,7. calcule: a)
Los números reales. Álvarez S., Caballero M.V. y Sánchez M a M. Contenidos. Full Screen.
 Los números reales Álvarez S., Caballero M.V. y Sánchez M a M salvarez@um.es, m.victori@um.es, marvega@um.es Índice 1. Definiciones 3 2. Herramientas 5 2.1. Propiedades de los números reales.....................
Los números reales Álvarez S., Caballero M.V. y Sánchez M a M salvarez@um.es, m.victori@um.es, marvega@um.es Índice 1. Definiciones 3 2. Herramientas 5 2.1. Propiedades de los números reales.....................
TEMA 7. Equilibrio Ácido-Base. Grabado de Heinrich Khunrath, Amphitheatrum Sapientiae Aeternae Hannover, 1609
 Grabado de Heinrich Khunrath, Amphitheatrum Sapientiae Aeternae Hannover, 1609 Concepto de ácidos y bases: evolución histórica 1. TEORÍA DE ARRHENIUS (1884) Los ácidos son aquellas sustancias que en disolución
Grabado de Heinrich Khunrath, Amphitheatrum Sapientiae Aeternae Hannover, 1609 Concepto de ácidos y bases: evolución histórica 1. TEORÍA DE ARRHENIUS (1884) Los ácidos son aquellas sustancias que en disolución
Reacciones Ácido Base
 Reacciones Ácido Base Prof. Sergio Casas-Cordero E. sacce Contenido: 1. Hidrólisis 2. Solución Amortiguadora (Buffer) 3. Indicadores 4. Valoración ácido - base sacce Prof. Sergio Casas-Cordero E. 2 HIDRÓLISIS:
Reacciones Ácido Base Prof. Sergio Casas-Cordero E. sacce Contenido: 1. Hidrólisis 2. Solución Amortiguadora (Buffer) 3. Indicadores 4. Valoración ácido - base sacce Prof. Sergio Casas-Cordero E. 2 HIDRÓLISIS:
Conjunto de Números Racionales.
 Conjunto de Números Racionales. El conjunto de los números racionales está formado por: el conjunto de los números enteros (-2, -1, 0, 1, 2, ) y los números fraccionarios y se representan con una Q. Números
Conjunto de Números Racionales. El conjunto de los números racionales está formado por: el conjunto de los números enteros (-2, -1, 0, 1, 2, ) y los números fraccionarios y se representan con una Q. Números
NOTA CALI/ORDEN/PRES ORTOGRAFÍA PUNTUACIÓN EXPRESIÓN NOTA FINAL
 1.- Formule o nombre los compuestos siguientes: a) Nitrito de escandio b) Peróxido de plata c) Ácido 2-hidroxiprop-2-enoico d) NH 4 H 2 PO 4 e) Y(CN) 3 f) C H 2 =CHCON(CH 3 ) 2 Res. a) Sc(NO 2 ) 3 ; b)
1.- Formule o nombre los compuestos siguientes: a) Nitrito de escandio b) Peróxido de plata c) Ácido 2-hidroxiprop-2-enoico d) NH 4 H 2 PO 4 e) Y(CN) 3 f) C H 2 =CHCON(CH 3 ) 2 Res. a) Sc(NO 2 ) 3 ; b)
Tema 2-Equilibrios ácido-base
 Tema 2-Equilibrios ácido-base CONTENIDO Especies ácido-base. Acidez de la disolución Calculo numérico y gráfico de ph Disoluciones amortiguadoras. Capacidad reguladora. DEFINICIONES DE ÁCIDOS Y BASES.
Tema 2-Equilibrios ácido-base CONTENIDO Especies ácido-base. Acidez de la disolución Calculo numérico y gráfico de ph Disoluciones amortiguadoras. Capacidad reguladora. DEFINICIONES DE ÁCIDOS Y BASES.
7.1 Números Racionales: números enteros, propiedades de los números y orden de operaciones. Prof. Kyria A. Pérez
 7.1 Números Racionales: números enteros, propiedades de los números y orden de operaciones Prof. Kyria A. Pérez Estándares de contenido y expectativas N.SO.7.2.1- Modela la suma, Resta, multiplicación
7.1 Números Racionales: números enteros, propiedades de los números y orden de operaciones Prof. Kyria A. Pérez Estándares de contenido y expectativas N.SO.7.2.1- Modela la suma, Resta, multiplicación
Ácidos y bases. Definiciones ácido-base
 Ácidos y bases Definiciones ácido-base Definición de Arrhenihus Sevate August Arrhenius 1858-1927 Ácido Aquella sustancia, que en solución acuosa, libera iones Hidrógeno (H 3 O + (ac)) Base HCl (ac) +
Ácidos y bases Definiciones ácido-base Definición de Arrhenihus Sevate August Arrhenius 1858-1927 Ácido Aquella sustancia, que en solución acuosa, libera iones Hidrógeno (H 3 O + (ac)) Base HCl (ac) +
PROBLEMAS RESUELTOS SELECTIVIDAD ANDALUCÍA QUÍMICA TEMA 6: EQUILIBRIOS ÁCIDO-BASE.
 PROBLEMAS RESUELTOS SELECTIVIDAD ANDALUCÍA 000 QUÍMICA TEMA 6: EQUILIBRIOS ÁCIDO-BASE http://emestrada.wordpress.com Complete los siguientes equilibrios ácido-base identificando, de forma razonada, los
PROBLEMAS RESUELTOS SELECTIVIDAD ANDALUCÍA 000 QUÍMICA TEMA 6: EQUILIBRIOS ÁCIDO-BASE http://emestrada.wordpress.com Complete los siguientes equilibrios ácido-base identificando, de forma razonada, los
Universidad de Puerto Rico en Arecibo Departamento de Matemáticas Sec. 5.1: Polinomios
 Universidad de Puerto Rico en Arecibo Departamento de Matemáticas Sec. 5.1: Polinomios Prof. Caroline Rodríguez Martínez Polinomios Un polinomio es un solo término o la suma de dos o más términos se compone
Universidad de Puerto Rico en Arecibo Departamento de Matemáticas Sec. 5.1: Polinomios Prof. Caroline Rodríguez Martínez Polinomios Un polinomio es un solo término o la suma de dos o más términos se compone
TEORIA DE EXPONENTES ING. CRISTHIAN VELANDIA
 TEORIA DE EXPONENTES ING. CRISTHIAN VELANDIA Conceptos preliminares. Epresión algebraica.- es el conjunto de letras y números interrelacionados entre si, mediante las operaciones de adición y sustracción,
TEORIA DE EXPONENTES ING. CRISTHIAN VELANDIA Conceptos preliminares. Epresión algebraica.- es el conjunto de letras y números interrelacionados entre si, mediante las operaciones de adición y sustracción,
Asignaturas antecedentes y subsecuentes
 PROGRAMA DE ESTUDIOS Equilibrio Químico Homogéneo Área a la que pertenece: AREA SUSTANTIVA PROFESIONAL Horas teóricas: 3 Horas practicas: 4 Créditos: 10 Clave: F0215 Ninguna. Asignaturas antecedentes y
PROGRAMA DE ESTUDIOS Equilibrio Químico Homogéneo Área a la que pertenece: AREA SUSTANTIVA PROFESIONAL Horas teóricas: 3 Horas practicas: 4 Créditos: 10 Clave: F0215 Ninguna. Asignaturas antecedentes y
Reacciones ácido-base
 Reacciones ácido-base 1 Brønsted-Lowry (1923) Ácido: Especie que tiene tendencia a ceder un H + Base: Especie que tiene tendencia a aceptar un H + CH 3 COOH (aq) + H 2 O (l) H 3 O + (aq) + CH 3 COO (aq)
Reacciones ácido-base 1 Brønsted-Lowry (1923) Ácido: Especie que tiene tendencia a ceder un H + Base: Especie que tiene tendencia a aceptar un H + CH 3 COOH (aq) + H 2 O (l) H 3 O + (aq) + CH 3 COO (aq)
ÍNDICE 1. Medición 2. Métodos para medir cantidades de materia Fórmulas Químicas 4. Reacciones químicas
 ÍNDICE CAPÍTULO 1. Medición... 15 1. El lenguaje de la química... 15 2. Medición... 16 3. Patrones... 16 Tabla I. Patrones básicos para la medición... 17 4. Unidades... 18 Tabla II. Algunas unidades métricas
ÍNDICE CAPÍTULO 1. Medición... 15 1. El lenguaje de la química... 15 2. Medición... 16 3. Patrones... 16 Tabla I. Patrones básicos para la medición... 17 4. Unidades... 18 Tabla II. Algunas unidades métricas
INSTITUTO TECNICO MARIA INMACULADA Formando líderes estudiantiles para un futuro mejor
 INSTITUTO TECNICO MARIA INMACULADA Formando líderes estudiantiles para un futuro mejor Coordinación Vo. Bo. Eje temático: OPERACIONES Y PROPIEDADES EN LOS NÚMEROS REALES Área: MATEMÁTICAS Asignatura: Matemáticas
INSTITUTO TECNICO MARIA INMACULADA Formando líderes estudiantiles para un futuro mejor Coordinación Vo. Bo. Eje temático: OPERACIONES Y PROPIEDADES EN LOS NÚMEROS REALES Área: MATEMÁTICAS Asignatura: Matemáticas
POTENCIACIÓN Y RADICACIÓN
 Potenciación POTENCIACIÓN Y RADICACIÓN La potenciación o exponenciación es una multiplicación de varios factores iguales, al igual que la multiplicación es una suma de varios sumandos iguales. En la nomenclatura
Potenciación POTENCIACIÓN Y RADICACIÓN La potenciación o exponenciación es una multiplicación de varios factores iguales, al igual que la multiplicación es una suma de varios sumandos iguales. En la nomenclatura
GUÍA DE EJERCICIOS EQUILIBRIO IÓNICO Área Química
 Resultados de aprendizaje GUÍA DE EJERCICIOS EQUILIBRIO IÓNICO Área Química Identifica, interpreta y analiza conceptos básicos sobre equilibrio iónico, para la resolución de ejercicios, desarrollando pensamiento
Resultados de aprendizaje GUÍA DE EJERCICIOS EQUILIBRIO IÓNICO Área Química Identifica, interpreta y analiza conceptos básicos sobre equilibrio iónico, para la resolución de ejercicios, desarrollando pensamiento
CONJUTOS NÚMERICOS NÚMEROS NATURALES
 CONJUTOS NÚMERICOS NÚMEROS NATURALES El conjunto de números naturales tiene gran importancia en la vida práctica ya que con sus elementos se pueden encontrar elementos u objetos de otros conjuntos. El
CONJUTOS NÚMERICOS NÚMEROS NATURALES El conjunto de números naturales tiene gran importancia en la vida práctica ya que con sus elementos se pueden encontrar elementos u objetos de otros conjuntos. El
NÚMEROS REALES---AGUERRERO
 Contenido NÚMEROS REALES... 2 IGUALDAD Y SUS PROPIEDADES... 4 NÚMEROS MÚLTIPLOS, COMPUESTOS Y PRIMOS... 4 NÚMEROS PRIMOS... 5 DESCOMPOSICIÓN DE UN NÚMERO EN SUS FACTORES PRIMOS... 7 MÁXIMO COMÚN DIVISOR...
Contenido NÚMEROS REALES... 2 IGUALDAD Y SUS PROPIEDADES... 4 NÚMEROS MÚLTIPLOS, COMPUESTOS Y PRIMOS... 4 NÚMEROS PRIMOS... 5 DESCOMPOSICIÓN DE UN NÚMERO EN SUS FACTORES PRIMOS... 7 MÁXIMO COMÚN DIVISOR...
OPCIÓN A. S = 4 = 4, moles L 1.
 OPCIÓN A CUESTIÓN 1.- a) Razona con los correspondientes equilibrios en disolución acuosa si las siguientes especies tienen carácter ácido, básico o anfótero: ion hidrogenocarbonato, ion hidrogenosulfuro
OPCIÓN A CUESTIÓN 1.- a) Razona con los correspondientes equilibrios en disolución acuosa si las siguientes especies tienen carácter ácido, básico o anfótero: ion hidrogenocarbonato, ion hidrogenosulfuro
UNA ECUACIÓN es una igualdad de dos expresiones algebraicas.
 UNA EXPRESIÓN ALGEBRAICA es una combinación de números, variables (o símbolos) y operaciones como la suma, resta, multiplicación, división, potenciación y radicación. Ejemplos. UNA ECUACIÓN es una igualdad
UNA EXPRESIÓN ALGEBRAICA es una combinación de números, variables (o símbolos) y operaciones como la suma, resta, multiplicación, división, potenciación y radicación. Ejemplos. UNA ECUACIÓN es una igualdad
GUÍA DE EJERCICIOS EQUILIBRIO IÓNICO Área Química
 Resultados de aprendizaje GUÍA DE EJERCICIOS EQUILIBRIO IÓNICO Área Química Identifica, interpreta y analiza conceptos básicos sobre equilibrio iónico, para la resolución de ejercicios, desarrollando pensamiento
Resultados de aprendizaje GUÍA DE EJERCICIOS EQUILIBRIO IÓNICO Área Química Identifica, interpreta y analiza conceptos básicos sobre equilibrio iónico, para la resolución de ejercicios, desarrollando pensamiento
Suma de números enteros
 NÚMEROS ENTEROS. RESUMEN Los números enteros son del tipo: = {... 5, 4, 3, 2, 1, 0, 1, 2, 3, 4, 5...} Es decir, los naturales, sus opuestos (negativos) y el cero. Valor absoluto El valor absoluto de un
NÚMEROS ENTEROS. RESUMEN Los números enteros son del tipo: = {... 5, 4, 3, 2, 1, 0, 1, 2, 3, 4, 5...} Es decir, los naturales, sus opuestos (negativos) y el cero. Valor absoluto El valor absoluto de un
Universidad de Puerto Rico Recinto de Río Piedras Departamento de Química
 Universidad de Puerto Rico Recinto de Río Piedras Departamento de Química Laboratorio Química General (QUÍM3001) Liz Díaz, PhD, Coordinadora 2007-2008 Introducción Las matemáticas se utilizan extensamente
Universidad de Puerto Rico Recinto de Río Piedras Departamento de Química Laboratorio Química General (QUÍM3001) Liz Díaz, PhD, Coordinadora 2007-2008 Introducción Las matemáticas se utilizan extensamente
Tema 6: Equilibrio ácido-base
 Tema 6: Equilibrio ácido-base Equilibrios en disolución. Producto iónico del agua. Disoluciones neutras, ácidas y básicas. Concepto de ph. Modelos ácido-base. Ácidos y bases fuertes y débiles: K a y K
Tema 6: Equilibrio ácido-base Equilibrios en disolución. Producto iónico del agua. Disoluciones neutras, ácidas y básicas. Concepto de ph. Modelos ácido-base. Ácidos y bases fuertes y débiles: K a y K
Semana 1: Números Reales y sus Operaciones
 Semana 1: Números Reales y sus Operaciones Taller de Preparación para Prueba PLANEA Ing. Jonathan Quiroga Tinoco Conalep Tehuacán P.T.B. en ADMO, SOMA y EMEC UNIDAD 04 Los números enteros y sus operaciones
Semana 1: Números Reales y sus Operaciones Taller de Preparación para Prueba PLANEA Ing. Jonathan Quiroga Tinoco Conalep Tehuacán P.T.B. en ADMO, SOMA y EMEC UNIDAD 04 Los números enteros y sus operaciones
Operaciones directas e inversas
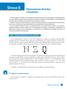 Operaciones directas e inversas Como ya sabés, la adición y la sustracción son operaciones inversas. Por ejemplo, el efecto de sumar 6 a una cantidad se puede anular restándole 6 al primer resultado. En
Operaciones directas e inversas Como ya sabés, la adición y la sustracción son operaciones inversas. Por ejemplo, el efecto de sumar 6 a una cantidad se puede anular restándole 6 al primer resultado. En
Capítulo 5. Los números reales y sus representaciones Pearson Education, Inc. Diapositiva 5-2-1
 Capítulo 5 Los números reales y sus representaciones 2012 Pearson Education, Inc. Diapositiva 5-2-1 Capítulo 5: Los números reales y sus representaciones 5.1 Números reales, orden y valor absoluto 5.2
Capítulo 5 Los números reales y sus representaciones 2012 Pearson Education, Inc. Diapositiva 5-2-1 Capítulo 5: Los números reales y sus representaciones 5.1 Números reales, orden y valor absoluto 5.2
UN CONJUNTO QUEDA DETERMINADO POR SUS ELEMENTOS QUE PERTENECEN A ÉL.. 2) PARA QUE UN CONJUNTO EXISTA ES NECESARIO QUE SUS ELEMENTOS
 CONJUNTOS La palabra CONJUNTO nos remite, intuitivamente a una agrupación o colección de objetos. Sin embargo para que una colección de objetos sea un conjunto, deberá cumplir algunas condiciones: UN CONJUNTO
CONJUNTOS La palabra CONJUNTO nos remite, intuitivamente a una agrupación o colección de objetos. Sin embargo para que una colección de objetos sea un conjunto, deberá cumplir algunas condiciones: UN CONJUNTO
TEMA 7: REACCIONES DE TRANSFERENCIA DE PROTONES
 TEMA 7: REACCIONES DE TRANSFERENCIA DE PROTONES 1. Concepto de ácido y de base De las distintas teorías que existen de ácidos y bases, sólo vamos a exponer dos de las más utilizadas, la teoría de Arrhenius
TEMA 7: REACCIONES DE TRANSFERENCIA DE PROTONES 1. Concepto de ácido y de base De las distintas teorías que existen de ácidos y bases, sólo vamos a exponer dos de las más utilizadas, la teoría de Arrhenius
6. Equilibrio ácido-base I
 6. Equilibrios ácido-base I Química (1S, Grado Biología) UAM 6. Equilibrio ácido-base I Contenidos Equilibrios ácido-base I Ácidos y bases Producto iónico del agua. Disoluciones neutras, ácidas y básicas.
6. Equilibrios ácido-base I Química (1S, Grado Biología) UAM 6. Equilibrio ácido-base I Contenidos Equilibrios ácido-base I Ácidos y bases Producto iónico del agua. Disoluciones neutras, ácidas y básicas.
Concepto de ph. Bases
 Concepto de ph El concepto de ph nace de dos tipos de especies químicas llamadas ácidos y bases, las que se pueden clasificar como tal y predecir su potencia o fuerza de acuerdo al valor de su ph. Características
Concepto de ph El concepto de ph nace de dos tipos de especies químicas llamadas ácidos y bases, las que se pueden clasificar como tal y predecir su potencia o fuerza de acuerdo al valor de su ph. Características
Sistemas de Ecuaciones Exponenciales y Logarítmicas
 Sistemas de Ecuaciones Exponenciales y Logarítmicas Siguiendo con los s de ecuaciones veremos a continuación aquellos que están compuestos por ecuaciones exponenciales y logarítmicas. I. Sistemas de Ecuaciones
Sistemas de Ecuaciones Exponenciales y Logarítmicas Siguiendo con los s de ecuaciones veremos a continuación aquellos que están compuestos por ecuaciones exponenciales y logarítmicas. I. Sistemas de Ecuaciones
EL AGUA COMO DISOLVENTE UNIVERSAL
 Universidad Nacional de Cuyo Instituto de Ciencias Básicas Carrera: LICENCIATURA y PROFESORADO de GRADO UNIVERSITARIO en CIENCIAS BÁSICAS Ordenanzas 129/04 C.S. 39/11 C.S. y 131/04 C. S. QUÍMICA GENERAL
Universidad Nacional de Cuyo Instituto de Ciencias Básicas Carrera: LICENCIATURA y PROFESORADO de GRADO UNIVERSITARIO en CIENCIAS BÁSICAS Ordenanzas 129/04 C.S. 39/11 C.S. y 131/04 C. S. QUÍMICA GENERAL
TÉCNICAS DE MUESTREO, ANÁLISIS E INTERPRETACIÓN. Ingeniería Ambiental
 TÉCNICAS DE MUESTREO, ANÁLISIS E INTERPRETACIÓN Ingeniería Ambiental UNIDAD Nº3 VOLUMETRÍAS Problema Elección del método analítico Toma de muestra Tratamiento de la muestra Proceso de medida Tratamiento
TÉCNICAS DE MUESTREO, ANÁLISIS E INTERPRETACIÓN Ingeniería Ambiental UNIDAD Nº3 VOLUMETRÍAS Problema Elección del método analítico Toma de muestra Tratamiento de la muestra Proceso de medida Tratamiento
Examen de Química de 2º de Bachillerato
 Examen de Química de 2º de Bachillerato Nombre: Fecha: 1. La reacción 2X + Y X 2 Y tiene órdenes de reacción 2 y 1 en relación con los reactivos X e Y, respectivamente. Responde a estas cuestiones: a)
Examen de Química de 2º de Bachillerato Nombre: Fecha: 1. La reacción 2X + Y X 2 Y tiene órdenes de reacción 2 y 1 en relación con los reactivos X e Y, respectivamente. Responde a estas cuestiones: a)
Sales en agua. Introducción a las curvas de titulación. Química General e Inorgánica 13 de abril de 2016 Prof. Dra.
 Sales en agua. Introducción a las curvas de titulación Química General e Inorgánica 13 de abril de 2016 Prof. Dra. Sandra Ferreira Tipos de sales 1.- Sales de ácido fuerte y base fuerte solubles. 2.- Sales
Sales en agua. Introducción a las curvas de titulación Química General e Inorgánica 13 de abril de 2016 Prof. Dra. Sandra Ferreira Tipos de sales 1.- Sales de ácido fuerte y base fuerte solubles. 2.- Sales
Los Números Enteros (Z)
 Los Números Enteros (Z) Los números enteros: representación gráfica, orden, modulo o valor absoluto. Operaciones en Z, procedimientos y propiedades de estas. Prioridades de operaciones y paréntesis. Problemas
Los Números Enteros (Z) Los números enteros: representación gráfica, orden, modulo o valor absoluto. Operaciones en Z, procedimientos y propiedades de estas. Prioridades de operaciones y paréntesis. Problemas
Reacciones ácido-base
 Reacciones ácido-base 1. Concepto de ácido y base 2. Teoría de Arrhenius (SUE, 1884) de los ácidos y de las bases 3. Teoría de Brönsted (DIN)-Lowry (GB) de los ácidos y de las bases (1923) (I) 4. Teoría
Reacciones ácido-base 1. Concepto de ácido y base 2. Teoría de Arrhenius (SUE, 1884) de los ácidos y de las bases 3. Teoría de Brönsted (DIN)-Lowry (GB) de los ácidos y de las bases (1923) (I) 4. Teoría
ÁCIDOS y BASES (Reacciones de transferencia de protones)
 transparent www.profesorjrc.es ÁCIDOS y BASES (Reacciones de transferencia de protones) 29 de junio de 2016 ÁCIDOS y BASES (Reacciones de transferencia de protones) Teorias ÁCIDOS y BASES (Reacciones de
transparent www.profesorjrc.es ÁCIDOS y BASES (Reacciones de transferencia de protones) 29 de junio de 2016 ÁCIDOS y BASES (Reacciones de transferencia de protones) Teorias ÁCIDOS y BASES (Reacciones de
Logaritmos y sus propiedades
 Universidad Rural de Guatemala Curso: Matemática II TEMA: Logaritmos Catedrático: Lic. Francisco Escobar Logaritmos y sus propiedades 1- Definición de Logaritmo Se define logaritmo como el exponente de
Universidad Rural de Guatemala Curso: Matemática II TEMA: Logaritmos Catedrático: Lic. Francisco Escobar Logaritmos y sus propiedades 1- Definición de Logaritmo Se define logaritmo como el exponente de
TEMA 8: REACCIONES DE TRANSFERENCIA DE PROTONES.
 TEMA 8: REACCIONES DE TRANSFERENCIA DE PROTONES. 1.- Concepto de ácido base. 1.1. Teoría de Arrhenius sobre ácidos y bases. Para el químico sueco Arrhenius, un ácido es toda aquella sustancia eléctricamente
TEMA 8: REACCIONES DE TRANSFERENCIA DE PROTONES. 1.- Concepto de ácido base. 1.1. Teoría de Arrhenius sobre ácidos y bases. Para el químico sueco Arrhenius, un ácido es toda aquella sustancia eléctricamente
PROBLEMAS RESUELTOS SELECTIVIDAD ANDALUCÍA 2006 QUÍMICA TEMA 6: EQUILIBRIOS ÁCIDO-BASE
 PROBLEMAS RESUELTOS SELECTIVIDAD ANDALUCÍA 2006 QUÍMICA TEMA 6: EQUILIBRIOS ÁCIDO-BASE Junio, Ejercicio 4, Opción A Reserva 1, Ejercicio 6, Opción A Reserva 1, Ejercicio 4, Opción B Reserva 2, Ejercicio
PROBLEMAS RESUELTOS SELECTIVIDAD ANDALUCÍA 2006 QUÍMICA TEMA 6: EQUILIBRIOS ÁCIDO-BASE Junio, Ejercicio 4, Opción A Reserva 1, Ejercicio 6, Opción A Reserva 1, Ejercicio 4, Opción B Reserva 2, Ejercicio
Suma de números enteros
 NÚMEROS ENTEROS. RESUMEN Los números enteros son del tipo: = {... 5, 4, 3, 2, 1, 0, 1, 2, 3, 4, 5...} Es decir, los naturales, sus opuestos (negativos) y el cero. Valor absoluto El valor absoluto de un
NÚMEROS ENTEROS. RESUMEN Los números enteros son del tipo: = {... 5, 4, 3, 2, 1, 0, 1, 2, 3, 4, 5...} Es decir, los naturales, sus opuestos (negativos) y el cero. Valor absoluto El valor absoluto de un
FISICA I Repaso. Si el alumno no supera al maestro, ni es bueno el alumno; ni es bueno el maestro (Proverbio Chino)
 Si el alumno no supera al maestro, ni es bueno el alumno; ni es bueno el maestro (Proverbio Chino) Profesor: Cazzaniga, Alejandro J. Física I E.T.N : 28 - República Francesa Pág. 1 de 9 Conjuntos numéricos
Si el alumno no supera al maestro, ni es bueno el alumno; ni es bueno el maestro (Proverbio Chino) Profesor: Cazzaniga, Alejandro J. Física I E.T.N : 28 - República Francesa Pág. 1 de 9 Conjuntos numéricos
2. Realiza las siguientes operaciones: = = = = : 1759 =
 Ejercicios Navidades 0-0. Realiza las siguientes operaciones: 7 + 6876 + 967 +67 + 968 = 68 +798 + 79 + 0 + 79 = 976 086 76 + 69 + 7 + 906 + = 90 697 + 69 + 97 +86 + 97 = 8. Realiza las siguientes operaciones:
Ejercicios Navidades 0-0. Realiza las siguientes operaciones: 7 + 6876 + 967 +67 + 968 = 68 +798 + 79 + 0 + 79 = 976 086 76 + 69 + 7 + 906 + = 90 697 + 69 + 97 +86 + 97 = 8. Realiza las siguientes operaciones:
GUÍA DE EJERCICIOS ADICIONALES N 2 Acido-base, neutralización y buffer
 1 GUÍA DE EJERCICIOS ADICIONALES N 2 Acido-base, neutralización y buffer 1.- Un ácido según la teoría de Arrhenius es aquella sustancia que: a) Libera uno o más iones hidroxilos (OH - ) por cada molécula
1 GUÍA DE EJERCICIOS ADICIONALES N 2 Acido-base, neutralización y buffer 1.- Un ácido según la teoría de Arrhenius es aquella sustancia que: a) Libera uno o más iones hidroxilos (OH - ) por cada molécula
UNIDAD III. EXPONENTES Y RADICALES. RAZONES, PROPORCIONES Y VARIACIONES.
 UNIDAD III. EXPONENTES Y RADICALES. RAZONES, PROPORCIONES Y VARIACIONES. Ley asociativa El producto de tres o más números, es el mismo sin importar la manera en que se agrupan al multiplicarlos. abc=(ac)b=c(ab)
UNIDAD III. EXPONENTES Y RADICALES. RAZONES, PROPORCIONES Y VARIACIONES. Ley asociativa El producto de tres o más números, es el mismo sin importar la manera en que se agrupan al multiplicarlos. abc=(ac)b=c(ab)
GUÍA DE EJERCICIOS TITULACIÓN ÁCIDO BASE Área Química
 Resultados de aprendizaje GUÍA DE EJERCICIOS TITULACIÓN ÁCIDO BASE Área Química Identifica, interpreta y analiza conceptos básicos sobre métodos de análisis por titulación, para la resolución de ejercicios,
Resultados de aprendizaje GUÍA DE EJERCICIOS TITULACIÓN ÁCIDO BASE Área Química Identifica, interpreta y analiza conceptos básicos sobre métodos de análisis por titulación, para la resolución de ejercicios,
UNIVERSIDADES PÚBLICAS DE LA COMUNIDAD DE MADRID PRUEBA DE ACCESO A LAS ENSEÑANZAS UNIVERSITARIAS OFICIALES DE GRADO
 UNIVERSIDADES PÚBLICAS DE LA COMUNIDAD DE MADRID PRUEBA DE ACCESO A LAS ENSEÑANZAS UNIVERSITARIAS OFICIALES DE GRADO MATERIA: QUÍMICA Curso 010-011 INSTRUCCIONES Y CRITERIOS GENERALES DE CALIFICACIÓN La
UNIVERSIDADES PÚBLICAS DE LA COMUNIDAD DE MADRID PRUEBA DE ACCESO A LAS ENSEÑANZAS UNIVERSITARIAS OFICIALES DE GRADO MATERIA: QUÍMICA Curso 010-011 INSTRUCCIONES Y CRITERIOS GENERALES DE CALIFICACIÓN La
REACCIONES DE TRANSFERENCIA DE PROTONES ELECTROLITOS
 REACCIONES DE TRANSFERENCIA DE PROTONES CURSO: 2º DE BACHILLERATO ASIGNATURA: QUÍMICA ELECTROLITOS Un electrolito es una sustancia que al disolverse en agua experimenta una disociación (o ionización) total
REACCIONES DE TRANSFERENCIA DE PROTONES CURSO: 2º DE BACHILLERATO ASIGNATURA: QUÍMICA ELECTROLITOS Un electrolito es una sustancia que al disolverse en agua experimenta una disociación (o ionización) total
GUÍA DE EJERCICIOS TITULACIÓN ÁCIDO BASE Área Química
 Resultados de aprendizaje GUÍA DE EJERCICIOS TITULACIÓN ÁCIDO BASE Área Química Identifica, interpreta y analiza conceptos básicos sobre métodos de análisis por titulación, para la resolución de ejercicios,
Resultados de aprendizaje GUÍA DE EJERCICIOS TITULACIÓN ÁCIDO BASE Área Química Identifica, interpreta y analiza conceptos básicos sobre métodos de análisis por titulación, para la resolución de ejercicios,
REACCIONES DE TRANSFERENCIA DE ELECTRONES
 transparent www.profesorjrc.es REACCIONES DE TRANSFERENCIA DE ELECTRONES 29 de junio de 2016 Números de oxidación Oxidación: Reducción: Átomo o grupo de átomos que pierden e, n.o. Átomo o grupo de átomos
transparent www.profesorjrc.es REACCIONES DE TRANSFERENCIA DE ELECTRONES 29 de junio de 2016 Números de oxidación Oxidación: Reducción: Átomo o grupo de átomos que pierden e, n.o. Átomo o grupo de átomos
EL EXAMEN SE POSPONE HASTA REGRESO DE SEMANA SANTA, LA PRIMERA CLASE REGRESANDO NOS PONEMOS DE ACUERDO SOBRE FECHA DEL PARCIAL.
 Facultad de Química-UNAM, Departamento de Química Analítica, Química Analítica I (1402), Serie 1: Equilibrio químico y de óxido reducción, Elaboraron: Dr. Tomás Guerrero B.; pqa. Toki Nishide A. Instrucciones:
Facultad de Química-UNAM, Departamento de Química Analítica, Química Analítica I (1402), Serie 1: Equilibrio químico y de óxido reducción, Elaboraron: Dr. Tomás Guerrero B.; pqa. Toki Nishide A. Instrucciones:
Volumetrías ácido-base. Química Analítica Autor: Joaquín A. Ortuño
 Volumetrías ácido-base VALORACIÓN DE UN ÁCIDO FUERTE (HCl) CON UNA BASE FUERTE (NaOH) Etapas: 1. Antes del punto de equivalencia: ph de una disolución de ácido fuerte. 2. En el punto de equivalencia: ph
Volumetrías ácido-base VALORACIÓN DE UN ÁCIDO FUERTE (HCl) CON UNA BASE FUERTE (NaOH) Etapas: 1. Antes del punto de equivalencia: ph de una disolución de ácido fuerte. 2. En el punto de equivalencia: ph
SOLUCIONARIO. EJERCICIOS - REPASO - 1ª EVALUACIÓN. r = =
 SOLUCIONARIO. EJERCICIOS - REPASO - ª EVALUACIÓN. Escribe como fracciones irreducibles los siguientes números decimales:,7 -,... c) -,... d),... Si r,7 entonces.000r 7. Por tanto 7 7 r 000 Si r -,... entonces.000r
SOLUCIONARIO. EJERCICIOS - REPASO - ª EVALUACIÓN. Escribe como fracciones irreducibles los siguientes números decimales:,7 -,... c) -,... d),... Si r,7 entonces.000r 7. Por tanto 7 7 r 000 Si r -,... entonces.000r
EXAMEN DE PENDIENTES PRIMER PARCIAL MATEMÁTICAS DE 1º DE ESO
 EXAMEN DE PENDIENTES PRIMER PARCIAL MATEMÁTICAS DE 1º DE ESO 1.- NÚMEROS NATURALES *Los números naturales. *El sistema de numeración decimal. Cifras y orden de las cifras. *Cardinal y ordinal. *Operación
EXAMEN DE PENDIENTES PRIMER PARCIAL MATEMÁTICAS DE 1º DE ESO 1.- NÚMEROS NATURALES *Los números naturales. *El sistema de numeración decimal. Cifras y orden de las cifras. *Cardinal y ordinal. *Operación
PROBLEMAS RESUELTOS ÁLGEBRA LINEAL Tema 2. Espacios Vectoriales
 SUBTEMA: ESPACIOS VECTORIALES Problema 1: Sea V = {a} el conjunto con el único elemento a. Determinar si V es un Espacio Vectorial sobre los reales con las operaciones de adición y multiplicación por un
SUBTEMA: ESPACIOS VECTORIALES Problema 1: Sea V = {a} el conjunto con el único elemento a. Determinar si V es un Espacio Vectorial sobre los reales con las operaciones de adición y multiplicación por un
Diagrama de Sillen. Introducción
 Diagrama de Sillen Introducción El diagrama de sillen es uno de los 2 diagramas conocidos por el cual se puede graficar la hidrólisis. Utilizando métodos matemáticos, combinándolos con los métodos analíticos
Diagrama de Sillen Introducción El diagrama de sillen es uno de los 2 diagramas conocidos por el cual se puede graficar la hidrólisis. Utilizando métodos matemáticos, combinándolos con los métodos analíticos
