Enzimas Sesión 01. Cinética de lar reacciones químicas
|
|
|
- Francisco Julio Farías Vidal
- hace 7 años
- Vistas:
Transcripción
1 Enzimas Sesión 01 Cinética de lar reacciones químicas Una reacción química tiene dos características de importancia: la posición de equilibrio (estabilidad de la concentración de productos y reactivos) y la velocidad de reacción (las reacciones tienen por objeto determinar el mecanismo y la velocidad con que interaccionan las moléculas bajo determinadas condiciones). La velocidad de una reacción química puede medirse como la velocidad de formación de uno o más de su productos o bien la velocidad de utilización de sus reactivos. Intuitivamente podemos suponer que al aumentar la concentración de los reactivos la probabilidad de interacción de los mismos aumenta conjuntamente con la velocidad que procede tal reacción. Ambas variables (velocidad de reacción y concentración de los reactivos) son directamente proporcionales, así que matemáticamente debe existir un valor constante, de esta manera podemos escribir: v r = k. [reactivos] n. (velocidad de reacción) = (constante). (concentración de reactivos) n El valor del exponente n es el orden de la reacción. Así si n = 1, estamos en presencia de una reacción de primer orden donde la velocidad es proporcional a la reacción de un solo reactivo. v r = k. [A] Análogamente, cuando n = 2, la velocidad es proporcional al producto de las concentraciones de dos reactivos o al cuadrado de la concentración de uno solo. Este tipo de reacciones reciben el nombre de segundo orden. v r = k. [A] [B] = k [A] 2 La importancia de determinar el orden de una reacción química radica en que a partir de ese parámetro puede obtenerse información sobre el mecanismo molecular en que opera. Velocidad de reacción y equilibrio En un estado de equilibrio químico las velocidades de reacciones directa e inversa son exactamente iguales. Considerando una reacción de primer orden: k 1 [A] = k 1 [B] Este principio nos permite llegar fácilmente a una reacción entre las constantes de velocidad y de equilibrio:
2 Efecto de la temperatura sobre la velocidad de reacción: Energía de activación La clave llevó al descubrimiento del criterio más importante para las reacciones químicas, las velocidades de reacción son generalmente sensibles a la temperatura. En el caso de las reacciones biomoleculares, un aumento de 10º C incrementa su velocidad entre 1,5 y 5 veces. Para explicar este hecho se postuló que al acrecentar la temperatura aumenta la fracción de moléculas capaces de tener una energía suficiente para alcanzar un "estado activado" que luego se transforme en producto de la reacción por formación o ruptura de enlaces químicos. Se admite que las únicas moléculas que reaccionan son aquellas que al chocar llevan consigo una energía mayor que un cierto valor mínimo. A este valor de energía necesaria se lo denomina energía de activación y es un factor de suma importancia para determinar la magnitud de la velocidad de reacción. Catalizadores Para que una reacción química tenga lugar se debe superar el valor de la energía de activación. Una vez vencida esa barrera el sistema evoluciona de forma tal que llegará al estado final de la reacción. La velocidad de reacción podría incrementarse de dos maneras: aumentando la concentración del "complejo activado" o eventualmente disminuyendo la energía de activación. Este último mecanismo es el que se pone de manifiesto cuando se emplea determinadas sustancias llamadas catalizadores. Estas sustancias aceleran las reacciones químicas disminuyendo la energía libre de activación, se combinan con los reactivos para producir un estrato de transición de menor energía que el estado de transición de la reacción no catalizada. Cuando los productos de la reacción se forman, se regenera el catalizador al estado libre. Enzimas: catalizadores biológicos Las reacciones químicas en sistemas biológicos raramente ocurren en ausencia de un catalizador. Estos catalizadores se denominan enzimas y son en su totalidad moléculas de naturaleza proteica (aunque ha habido estudios acerca de enzimas de naturaleza glucosídica). Es razonable pensar en la necesidad que tienen los seres vivos de poseer estos catalizadores, ya que las funciones vitales de cualquier célula serían imposibles de mantener si las reacciones que ocurren en ella fueran extremadamente lentas. Además de incrementar la velocidad las enzimas exhiben una elevada especificidad y en algunos casos pueden ser reguladas por diferentes metabolitos, aumentando y otras veces disminuyendo, de acuerdo a las necesidades del momento, su actividad. Todas estas propiedades pueden ser cumplidas por moléculas altamente complejas, que al ser moléculas orgánicas (macromoléculas) comparten características con las proteínas no enzimáticas y difieren de los catalizadores inorgánicos: a) Son termolábiles y su actividad depende en ciertos casos del ph del medio.
3 b) El reconocimiento de la enzima con el reactivo a procesar (denominado sustrato) es altamente específico. c) Tienen gran eficiencia, es decir, transforman un gran número de moléculas de sustrato por unidad de tiempo. d) Están sujetas a una gran variedad de controles celulares, genéticos y alostéricos. Como todos los catalizadores las enzimas aceleran notablemente la velocidad de una reacción química y cumplen con las siguientes características: 1) Son efectivas en pequeñas cantidades 2) No sufren modificaciones químicas irreversibles durante la catálisis. Es decir que luego de la reacción enzimática, las moléculas de enzimas que reaccionaron son indistinguibles de las que no lo han hecho, (la estructura de la molécula se mantiene, al principio y final de la reacción, exactamente igual). 3) No afectan la posición de equilibrio de la reacción que catalizan. El estado inicial y final de la reacción es el mismo, solo que se llega al equilibrio mucho más rápidamente. Nomenclatura y clasificación Una forma general de denominar a las enzimas es añadir el sufijo "asa" al nombre del sustrato. Así, la ureasa es la enzima que cataliza la hidrólisis de la urea formando amoníaco y dióxido de carbono. Sin embargo con el descubrimiento de nuevas enzimas esta nomenclatura resulta a veces confusa. Actualmente se ha adoptado ciertas recomendaciones de la Internacional Enzime Comission, que pretende sistemetizar la nomenclatura y clasificación de las diferentes enzimas conocidas. Este sistema divide a las enzimas en seis clases que a su vez pueden tener diferentes subclases. Clasificación Internacional de las Enzimas Óxido Reductasas (reacciones de oxido- reducción) Actúan sobre ": CH OH " Actúan sobre ": C = O " Actúan sobre ": C = CH " Actúan sobre ": CH NH 2 " Actúan sobre ": CH NH "
4 Hidrolasas (reacciones de hidrólisis) Esteres Enlaces glucosídico Enlaces pepsídicos Otros enlaces C N Anhídridos de ácido Transferasas (transferencia de grupos funcionales) Grupos de un átomo de C Grupos aldehídos o cetónicos Grupos acilos Grupos glucosilos Grupos fosfatos Grupos que contienen azufre Liasas (Adición a los dobles enlaces) : C = C : : C = O : C = N Isomerasas (reacción de isomerización) Racemasas Ligasas (Formación de enlaces con escisión de ATP) : C O : C N : C S
5 : C C Los nombres propuestos en este sistema son los que se emplean cuando es necesaria una identificación exacta de las enzimas, (por ejemplo en revistas científicas). Sin embargo, cotidianamente pueden emplearse los nombres triviales por ser mucho más conocidos. Cofactores Algunas enzimas dependen para su actividad catalítica además de la estructura proteica, de otras moléculas de naturaleza no proteica. Estas estructuras reciben el nombre de cofactores. Estos son resistentes al calor mientras que las proteínas generalmente no lo son. El complejo enzima cofactor recibe el nombre de holoenzima. A la fracción proteica aislada del cofactor que es inactiva se la denomina apoenzima. Los cofactores pueden ser simplemente iones metálicos o en algunos casos moléculas orgánicas complejas. Estas últimas el nombre de coenzimas. Activadores Metálicos Elemento Enzima Activada Zn ++ Holoenzima = Apoenzima + Coenzima Deshidrogenasas, anhidrasa carbónica, ARN y ADN polimerasas. Mg ++ Fosfohidrolasas, fosfotransferasas, fosfatasas. Mn ++ Arginasas, peptidasas, quinasas. Mo Nitratoreductasa, nitrogenasa. Fe 2+, Fe 3+ Citocromos, catalasas, ferredoxina, peroxidasas, nitritoreductasa. Cu 2+ Citocromo oxidasa, tirosinasa, ácido ascórbico oxidasa, plastocianina
6 Ca 2+ 1,3 β glucansintetasa, calmodulina. K + Piruvato fosfoquinasa, ATPasa. Co Vitamina B 12 hallada en microorganismos y animales, pero no en plantas. Importante en la fijación simbiótica de nitrógeno. Ni Ureasa. En ciertos casos las coenzimas están estrechamente unidas a la molécula de la enzima y reciben el nombre del grupo prostético. Un ejemplo clásico lo constituye el grupo hemo del citocromo C, unido covalentemente a la proteína. Entre los cofactores que requieren las enzimas para su funcionamiento están las coenzimas: NADPH + H (nicotinamida adenina dinucleótido fosfato reducido), NAD (nicotinamida adenina dinucleotido), FAD (flavina adenina dinucleótido), piridoxal, biotina, tiamina, ácido tetra hidrofólico, cobalamina. Cinética de las Reacciones Enzimáticas En principio, las consideraciones generales de la cinética química pueden aplicarse a las reacciones catalizadas enzimáticamente, aunque estas últimas tienen la particularidad de mostrar el fenómeno de saturación por el sustrato. A una concentración constante de enzima, si vemos el gráfico de la velocidad de la reacción catalizada enzimáticamente en función de la concentración del sustrato, es evidente que a bajas concentraciones del mismo la velocidad de formación de producto es proporcional a la concentración del sustrato. A medida que se aumenta la concentración de sustrato se aprecia una pérdida de la proporcionalidad, en esta zona la reacción es de orden mixto y finalmente, a altas concentraciones, la velocidad de la reacción es independiente de esta. Ya se ha dicho que el sustrato se une a la enzima en una región determinada del mismo llamada sitio activo. El fenómeno de saturación junto con otras evidencias llevaron a postular la existencia de un complejo enzima sustrato (E S) como etapa previa a la formación de productos. En 1913 Lenor Michelis dedujo la relación entre la velocidad máxima (v m ) de una reacción catalizada enzimáticamente en términos de la formación del complejo E S. En base a estas consideraciones es lógico suponer que a altas concentraciones de sustrato, todos los sitios activos de la enzima están ocupados y por lo tanto la velocidad alcanza un máximo. El modelo propuesto sirve de base para explicar las propiedades de
7 la mayoría de las enzimas y como se dijo antes asume la existencia de un complejo E S como intermediario en la catálisis. Una enzima E se combina con un sustrato S para formar el complejo E S, con una constante de velocidad k 1. Este complejo E S puede seguir dos caminos: a) puede proceder para formar el producto con una constante de velocidad k 3 ; b) el camino alternativo es disociándose, generando nuevamente E y S con una constante de velocidad k 2. En base al modelo, la velocidad de la reacción catalizada enzimáticamente será : v = k 3 [E S] El valor [E S] no es fácilmente estimable de modo que se necesita una expresión equivalente con valores conocidos. Mediante desarrollo matemático se ha desarrollado la siguiente ecuación: Efecto de la concentración del sustrato sobre la velocidad de una reacción catalizada enzimáticamente. Obtención del k m. y la v max. Resumiendo, si se mantiene la concentración de la enzima constante y variamos la concentración de substrato se obtiene una curva hiperbólica como la de la figura (arriba izquierda). Al principio un aumento de la concentración de substrato produce un aumento rápido de la velocidad de reacción, pero si se sigue aumentando la concentración de substrato, la velocidad de reacción comienza a disminuir; vemos que a muy altas concentraciones de substrato se observa que no cambia la velocidad de reacción, se dice que los centros activos de la enzima se encuentran saturados. La velocidad de reacción que se obtiene a esa alta concentración de substrato se define como la velocidad máxima (v m ) de la reacción enzimática bajo las condiciones especificadas. La concentración de substrato [S], a la semivelocidad máxima de reacción (½ v ) se puede determinar de la figura y representa la constante de Michaelis o k m, la cual es una característica para cada enzima. La inversa de k m, o 1/ k m, mide aproximadamente la afinidad de la enzima por el substrato. Mientras más pequeño sea el valor de k m, mayor será la afinidad de la enzima por el substrato. Si varias enzimas compiten en el metabolismo por el mismo substrato, éste será transformado preferentemente por la enzima con mayor afinidad.
8 Así tendremos: (simplificando) Si reordenamos la ecuación tendremos que: [S] + k m = 2 [S] (despejamos) k m = [S] Esto significa que la concentración del sustrato necesaria para alcanzar la mitad de la velocidad es el valor de k m de la enzima. La expresión de Michelis Menten puede ser transformada algebraicamente en otras formas, que son más útiles para la expresión de los datos experimentales. Una de esas formas consiste en tomar los recíprocos (inversa) de ambos miembros de la ecuación. Esta expresión conocida con el nombre de ecuación Lineweaver Burk, corresponde a una recta de ecuación : y = a.m + b Midiendo las velocidades para distintas concentraciones de sustrato y representando gráficamente (al lado) obtendremos una gráfica del tipo lineal. Centro activo de una enzima Ya se había mencionado que la porción de la molécula en la enzima que se una al o a los sustratos es una zona relativamente pequeña de la misma. Esta zona, responsable de la actividad catalítica, que favorece la orientación de los grupos químicos (que reaccionan para dar los productos de la reacción) recibe el nombre de centro activo.
9 Los grupos responsables de la actividad catalítica propiamente dicho se los denomina sitios catalíticos. En algunos casos esos grupos pueden corresponder a los grupos prostéticos de los cuales ya se ha hablado. Expresión de la actividad enzimática La cantidad de enzimas presentes en un fluido biológico es muy difícil de determinar en valores absolutos, mg. o moles, una forma de resolver este problema es midiendo la velocidad de reacción catalizada por la misma empleando un sustrato específico. La velocidad de reacción puede expresarse como la cantidad de reactivo que se transforman en producto por unidad de tiempo. De allí que la unidad internacional (UI) de cualquier enzima se define como la cantidad de la misma que cataliza la transformación de un mol de sustrato por minuto, bajo condiciones definidas: ph, temperatura, concentración de sustrato/s y cofactores, etc. En base a lo que se acaba de explicar es posible expresar la cantidad de una enzima en un fluido biológico en UI/cm 3 o en UI/ mg. de proteína total. Esta última expresión denominada actividad específica es la cantidad de moles de sustrato transformados por minuto y por mg. de proteína, debiéndose indicar la temperatura, el ph, etc. Es importante recordar que la actividad específica de una enzima es una medida indirecta de la fracción de la proteína total en una preparación que contienen a la enzima. Factores que influyen en la velocidad de las reacciones enzimáticas Temperatura: Un aumento en la temperatura provoca un aumento de la velocidad de reacción hasta cierta temperatura óptima, ya que después de aproximadamente 45 0 C se comienza a producir la desnaturalización térmica. Las enzimas de muchos mamíferos tienen una temperatura óptima de 37 0 C, por encima de esa temperatura comienzan a inactivarse y se destruyen Sin embargo existen especies de bacterias y algas que habitan en fuentes de aguas termales y en el otro extremo ciertas bacterias árticas tienen temperaturas óptimas cercanas a 0 0 C. Efecto Del ph Sobre La Actividad Enzimática: El ph no afecta la actividad enzimática directamente sino que modifica la concentración de protones. Los protones además de alterar la estructura de la enzima y el substrato, pueden participar también en la reacción como substrato o producto. En esos casos, la concentración de protones afecta directamente la velocidad de la reacción. Cualquier cambio brusco de ph, sabiendo que las enzimas son proteínas, puede alterar el carácter iónico de los grupos amino y carboxilo en la superficie proteica, afectando así las propiedades catalíticas de una enzima. A ph alto o bajo se puede producir la desnaturalización de la enzima y en consecuencia su inactivación. Enzimas: Pepsina 1,5 (ph óptimo) Tripsina 7,7 Catalasa 7,6
10 Arginasa 9,7 Fumarasa 7,8 Ribonucleasa 7,8 Inhibición Enzimática La actividad enzimática puede ser disminuida o eliminada por la acción de ciertas sustancias a las cuales se les conoce con el nombre de inhibidores enzimáticos. Mediante el uso de inhibidores enzimáticos se ha obtenido información muy valiosa sobre la conformación del centro activo de algunas enzimas. Las distintas formas de interacción se traducen en varios tipos de inhibición perfectamente diferenciables experimentalmente. Los dos tipos más comunes son la competitiva y la no competitiva. La primera es cuando el inhibidor compite con el substrato por la unión con el centro activo de la enzima. Este tipo de inhibición puede reducirse si se aumenta la concentración de substrato. Un ejemplo clásico lo constituye la inhibición del malonato sobre la enzima succinato deshidrogenasa que cataliza la eliminación de dos átomos de hidrógeno de los átomos de carbono metilénico del succinato. En la segunda el inhibidor forma un enlace covalente con las enzimas cerca del centro activo sin modificarla irreversiblemente. Un ejemplo son los gases nerviosos, como el fluorofosfato de di isopropilo (DFP) que forma un complejo con la enzima acetilcolinesterasa. Los animales envenenados con este gas quedan paralizados, debido a la imposibilidad de transmitir adecuadamente los impulsos nerviosos. Ciertos metales como el plomo, mercurio y arsénico inhiben enzimas que tienen en su centro activo grupos SH libres. El proceso de inhibición enzimática es útil para comprender los mecanismos de acción tóxica y farmacológica de algunos compuestos. Isoenzimas Son enzimas que difieren en su forma estructural pero que poseen la misma actividad catalítica, catalizan la misma reacción.
Fases del Metabolismo ENZIMAS
 Fases del Metabolismo ENZIMAS Definición: son macromoléculas, en su mayoría de origen proteico, que catalizan las reacciones bioquímicas que se producen en la células de los seres vivos. Propiedades: Eficiencia:
Fases del Metabolismo ENZIMAS Definición: son macromoléculas, en su mayoría de origen proteico, que catalizan las reacciones bioquímicas que se producen en la células de los seres vivos. Propiedades: Eficiencia:
ENZIMAS: CONCEPTOS BÁSICOS Y CINÉTICA
 ENZIMAS: CONCEPTOS BÁSICOS Y CINÉTICA Enzimas: catalizadores de naturaleza proteica Seis clases de enzimas Clase 1. Oxidoreductasas 2. Transferasas 3. Hidrolasas 4. Liasas 5. Isomerasas 6. Ligasas Tipo
ENZIMAS: CONCEPTOS BÁSICOS Y CINÉTICA Enzimas: catalizadores de naturaleza proteica Seis clases de enzimas Clase 1. Oxidoreductasas 2. Transferasas 3. Hidrolasas 4. Liasas 5. Isomerasas 6. Ligasas Tipo
TEMA 11.- CINÉTICA ENZIMÁTICA
 TEMA 11.- CINÉTICA ENZIMÁTICA Introducción: Cinética enzimática. Ecuación de Michaelis-Menten. Ecuación de Lineweaver-Burk. Reacciones con múltiples substratos. Inhibición enzimática: - Reversible Competitiva.
TEMA 11.- CINÉTICA ENZIMÁTICA Introducción: Cinética enzimática. Ecuación de Michaelis-Menten. Ecuación de Lineweaver-Burk. Reacciones con múltiples substratos. Inhibición enzimática: - Reversible Competitiva.
CAPÍTULO 6. ENZIMAS 1. Bioquímica Facultad de Agronomía
 CAPÍTULO 6. ENZIMAS 1 Bioquímica Facultad de Agronomía INTRODUCCIÓN Las enzimas son catalizadores, más eficaces y específicos que muchos otros compuestos químicos. Hasta 1982 era común escuchar Todas las
CAPÍTULO 6. ENZIMAS 1 Bioquímica Facultad de Agronomía INTRODUCCIÓN Las enzimas son catalizadores, más eficaces y específicos que muchos otros compuestos químicos. Hasta 1982 era común escuchar Todas las
ENZIMAS Catalizadores biológicos
 ENZIMAS Catalizadores biológicos Las enzimas están en el centro de cada proceso bioquímico. Son el origen de la compleja sinfonía altamente regulada que denominamos vida. ENDOCELULARES EXOCELULARES Citosol
ENZIMAS Catalizadores biológicos Las enzimas están en el centro de cada proceso bioquímico. Son el origen de la compleja sinfonía altamente regulada que denominamos vida. ENDOCELULARES EXOCELULARES Citosol
UNIVERSIDAD PERUANA CAYETANO HEREDIA CENTRO FORMATIVO PREUNIVERSITARIO BIOLOGÍA METABOLISMO
 UNIVERSIDAD PERUANA CAYETANO HEREDIA CENTRO FORMATIVO PREUNIVERSITARIO BIOLOGÍA METABOLISMO METABOLISMO Ciclo interdependendiente, intercambio de E y materia. AUTOTROFOS FOTOSINTETICOS HETEROTROFOS Procesos
UNIVERSIDAD PERUANA CAYETANO HEREDIA CENTRO FORMATIVO PREUNIVERSITARIO BIOLOGÍA METABOLISMO METABOLISMO Ciclo interdependendiente, intercambio de E y materia. AUTOTROFOS FOTOSINTETICOS HETEROTROFOS Procesos
CARACTERÍSTICAS DE LAS ENZIMAS
 BIOQUÍMICA I CARACTERÍSTICAS DE LAS ENZIMAS 1. Son los catalizadores de las reacciones químicas de los sistemas biológicos. 2. Tienen gran poder catalítico. 3. Poseen un elevado grado de especificidad
BIOQUÍMICA I CARACTERÍSTICAS DE LAS ENZIMAS 1. Son los catalizadores de las reacciones químicas de los sistemas biológicos. 2. Tienen gran poder catalítico. 3. Poseen un elevado grado de especificidad
Universidad Nacional de Tucumán ENZIMAS
 ENZIMAS INTRODUCIÓN Las reacciones químicas en sistemas biológicos raramente ocurren en ausencia de un catalizador. Estos catalizadores se denominan enzimas y son casi en su totalidad de naturaleza proteica,
ENZIMAS INTRODUCIÓN Las reacciones químicas en sistemas biológicos raramente ocurren en ausencia de un catalizador. Estos catalizadores se denominan enzimas y son casi en su totalidad de naturaleza proteica,
Enzimas. Proteínas de forma globular Aceleran reacciones específicas químicas ( ) Catalizadores biológicos. Pepsina
 Enzimas Enzimas Proteínas de forma globular Aceleran reacciones específicas químicas (10 3-10 20 ) Catalizadores biológicos. Pepsina Específicas para un substrato particular (Estereo especificidad) COO
Enzimas Enzimas Proteínas de forma globular Aceleran reacciones específicas químicas (10 3-10 20 ) Catalizadores biológicos. Pepsina Específicas para un substrato particular (Estereo especificidad) COO
Enzimas. Determinación de su actividad catalítica en distintos materiales biológicos
 Enzimas Determinación de su actividad catalítica en distintos materiales biológicos Qué son? La mayoría son proteínas ( existe ARN catalítico ). que función cumplen? Catalizadores biológicos Sus propiedades
Enzimas Determinación de su actividad catalítica en distintos materiales biológicos Qué son? La mayoría son proteínas ( existe ARN catalítico ). que función cumplen? Catalizadores biológicos Sus propiedades
ACTIVIDAD ENZIMÁTICA. Curvas temporales de la actividad enzimática de la lactato deshidrogenasa de músculo esquelético de pollo.
 ACTIVIDAD ENZIMÁTICA Curvas temporales de la actividad enzimática de la lactato deshidrogenasa de músculo esquelético de pollo. Monitoreo de la purificación de la lactato deshidrogenasa SDS PAGE Actividad
ACTIVIDAD ENZIMÁTICA Curvas temporales de la actividad enzimática de la lactato deshidrogenasa de músculo esquelético de pollo. Monitoreo de la purificación de la lactato deshidrogenasa SDS PAGE Actividad
ENZIMAS GENERALIDADES DE LAS ENZIMAS. Material extraído de:
 ENZIMAS GENERALIDADES DE LAS ENZIMAS Material extraído de: Bioquimica y Biologia molecular para ciencias de la salud. José A. Lozano. Pags 133-157 McKee, T. y McKeeJ. R. (2003). Bioquímica. La base molecular
ENZIMAS GENERALIDADES DE LAS ENZIMAS Material extraído de: Bioquimica y Biologia molecular para ciencias de la salud. José A. Lozano. Pags 133-157 McKee, T. y McKeeJ. R. (2003). Bioquímica. La base molecular
ENZIMAS SON BIOCATALIZADORES AUMENTAN LA VELOCIDAD DE REACCIÓN NO SE GASTAN EN CANTIDADES MUY PEQUEÑAS
 ENZIMAS SON BIOCATALIZADORES AUMENTAN LA VELOCIDAD DE REACCIÓN NO SE GASTAN EN CANTIDADES MUY PEQUEÑAS ENZIMAS: CATALIZADORES BIOLOGICOS ACELERAN LA VELOCIDAD DE LA REACCIÓN SON PROTEÍNAS GLOBULARES NO
ENZIMAS SON BIOCATALIZADORES AUMENTAN LA VELOCIDAD DE REACCIÓN NO SE GASTAN EN CANTIDADES MUY PEQUEÑAS ENZIMAS: CATALIZADORES BIOLOGICOS ACELERAN LA VELOCIDAD DE LA REACCIÓN SON PROTEÍNAS GLOBULARES NO
Tema 6. Cinética Enzimática TEMA 7 CINÉTICA ENZIMÁTICA 3. INHIBICIONES EN REACCIONES ENZIMÁTICAS INHIBICIÓN COMPETITIVA Y NO COMPETITIVA
 Tema 6 Cinética Enzimática 1 TEMA 7 CINÉTICA ENZIMÁTICA 1. DEFINICIONES CÓMO ACTÚAN LOS ENZIMAS? 2. CINÉTICA ENZIMÁTICA MODELO DE MICHAELIS-MENTEN REPRESENTACIONES 3. INHIBICIONES EN REACCIONES ENZIMÁTICAS
Tema 6 Cinética Enzimática 1 TEMA 7 CINÉTICA ENZIMÁTICA 1. DEFINICIONES CÓMO ACTÚAN LOS ENZIMAS? 2. CINÉTICA ENZIMÁTICA MODELO DE MICHAELIS-MENTEN REPRESENTACIONES 3. INHIBICIONES EN REACCIONES ENZIMÁTICAS
El metabolismo es un conjunto de reacciones químicas que tienen lugar en las células del cuerpo
 METABOLISMO El metabolismo es un conjunto de reacciones químicas que tienen lugar en las células del cuerpo El metabolismo transforma la energía que contienen los alimentos que ingerimos en el combustible
METABOLISMO El metabolismo es un conjunto de reacciones químicas que tienen lugar en las células del cuerpo El metabolismo transforma la energía que contienen los alimentos que ingerimos en el combustible
Fisiología del tubo digestivo. Metabolismo intermedio
 Fisiología de la Nutrición Fisiología del tubo digestivo Metabolismo intermedio Nutrición Fisiología de la Nutrición Fisiología del tubo digestivo Trata los movimientos y las secreciones del tubo digestivo,
Fisiología de la Nutrición Fisiología del tubo digestivo Metabolismo intermedio Nutrición Fisiología de la Nutrición Fisiología del tubo digestivo Trata los movimientos y las secreciones del tubo digestivo,
EL CONTROL DE LAS ACTIVIDADES CELULARES
 EL CONTROL DE LAS ACTIVIDADES CELULARES LAS REACCIONES CELULARES BÁSICAS Todas las células llevan a cabo funciones vitales: Ingestión de nutrientes Eliminación de desperdicios Crecimiento Reproducción
EL CONTROL DE LAS ACTIVIDADES CELULARES LAS REACCIONES CELULARES BÁSICAS Todas las células llevan a cabo funciones vitales: Ingestión de nutrientes Eliminación de desperdicios Crecimiento Reproducción
Enzimas y co-enzimas. Dra. Emilia I. Cruz Li
 Enzimas y co-enzimas Dra. Emilia I. Cruz Li Reacciones que se catalizan por enzimas todas las reacciones orgánicas que tienen lugar en los sistemas biológicos necesitan un catalizador ENZIMAS proteínas
Enzimas y co-enzimas Dra. Emilia I. Cruz Li Reacciones que se catalizan por enzimas todas las reacciones orgánicas que tienen lugar en los sistemas biológicos necesitan un catalizador ENZIMAS proteínas
1.- Explica cuáles son los principales factores que afectan a la actividad enzimática.
 PREGUNTAS RESUELTAS. LOS ENZIMAS 1.- Explica cuáles son los principales factores que afectan a la actividad enzimática. 2.- Qué es un inhibidor y de cuántos tipos puede ser la acción que realizan? 3.-
PREGUNTAS RESUELTAS. LOS ENZIMAS 1.- Explica cuáles son los principales factores que afectan a la actividad enzimática. 2.- Qué es un inhibidor y de cuántos tipos puede ser la acción que realizan? 3.-
1. Características generales
 1. Características generales Los enzimas son proteínas que catalizan reacciones químicas en los seres vivos. Los enzimas son catalizadores, es decir, sustancias que, sin consumirse en una reacción, aumentan
1. Características generales Los enzimas son proteínas que catalizan reacciones químicas en los seres vivos. Los enzimas son catalizadores, es decir, sustancias que, sin consumirse en una reacción, aumentan
Tema: Bioactividad de Enzimas
 UNIVERSIDAD NACIONAL ESCUELA DE CIENCIAS AGRICOLA, PECUARIAS Y DEL MEDIO AMBIENTE ECAPMA Nombre del Curso: 334001-Sistema Metabólico Nutricional Tema: Bioactividad de Enzimas JAIRO ENRIQUE GRANADOS MORENO.,MSc
UNIVERSIDAD NACIONAL ESCUELA DE CIENCIAS AGRICOLA, PECUARIAS Y DEL MEDIO AMBIENTE ECAPMA Nombre del Curso: 334001-Sistema Metabólico Nutricional Tema: Bioactividad de Enzimas JAIRO ENRIQUE GRANADOS MORENO.,MSc
DEPARTAMENTO DE BIOQUÍMICA ESFUNO EUTM E N Z I M A S
 DEPARTAMENTO DE BIOQUÍMICA ESFUNO EUTM E N Z I M A S Enzimas A. Propiedades generales B. Principios fundamentales de su acción catalítica C. Introducción a la cinética enzimática D. Regulación de la actividad
DEPARTAMENTO DE BIOQUÍMICA ESFUNO EUTM E N Z I M A S Enzimas A. Propiedades generales B. Principios fundamentales de su acción catalítica C. Introducción a la cinética enzimática D. Regulación de la actividad
Cinética Enzimática. Enrique Rivera González
 Cinética Enzimática Enrique Rivera González Importancia Las enzimas son proteínas capaces de catalizar específicamente reacciones bioquímicas. La actividad catalítica de las enzimas depende de su estructura.
Cinética Enzimática Enrique Rivera González Importancia Las enzimas son proteínas capaces de catalizar específicamente reacciones bioquímicas. La actividad catalítica de las enzimas depende de su estructura.
Enzimas Departamento de Bioquímica Noviembre de 2005
 U.T.I. Biología Celular Enzimas Departamento de Bioquímica Noviembre de 2005 Enzimas A. Propiedades generales de las enzimas B. Principios fundamentales de su acción catalítica C. Introducción a la cinética
U.T.I. Biología Celular Enzimas Departamento de Bioquímica Noviembre de 2005 Enzimas A. Propiedades generales de las enzimas B. Principios fundamentales de su acción catalítica C. Introducción a la cinética
ENZIMAS. 3)- La mayor parte de las rutas metabólicas son comunes a todos los seres vivos.
 ENZIMAS Son sustancias encargadas de facilitar las reacciones químicas (reacciones metabólicas), son catalizadores de las reacciones son biocatalizadores. Las enzimas tienen una naturaleza proteica (salvo
ENZIMAS Son sustancias encargadas de facilitar las reacciones químicas (reacciones metabólicas), son catalizadores de las reacciones son biocatalizadores. Las enzimas tienen una naturaleza proteica (salvo
Importancia de la energía
 Energía y la Célula Importancia de la energía Todos los seres vivos necesitan energía porque los procesos biológicos implican la realización de trabajo. Las células que forman los seres vivientes usan
Energía y la Célula Importancia de la energía Todos los seres vivos necesitan energía porque los procesos biológicos implican la realización de trabajo. Las células que forman los seres vivientes usan
TEMA 13. LAS REACCIONES METABÓLICAS. LA IMPORTANCIA DE LAS ENZIMAS.
 TEMA 13. LAS REACCIONES METABÓLICAS. LA IMPORTANCIA DE LAS ENZIMAS. 1.-Características de las reacciones metabólicas. 2.- Enzimas y reacciones enzimáticas. 2.1. Mecanismo de las reacciones enzimáticas.
TEMA 13. LAS REACCIONES METABÓLICAS. LA IMPORTANCIA DE LAS ENZIMAS. 1.-Características de las reacciones metabólicas. 2.- Enzimas y reacciones enzimáticas. 2.1. Mecanismo de las reacciones enzimáticas.
1.- CONCEPTO DE ENZIMA
 ENZIMAS 1.- CONCEPTO DE ENZIMA Los enzimas son catalizadores muy potentes y eficaces, Químicamente son proteínas Actúan en pequeña cantidad y se recuperan indefinidamente No llevan a cabo reacciones energéticamente
ENZIMAS 1.- CONCEPTO DE ENZIMA Los enzimas son catalizadores muy potentes y eficaces, Químicamente son proteínas Actúan en pequeña cantidad y se recuperan indefinidamente No llevan a cabo reacciones energéticamente
Enzimas Catalizadores bioquímicos. Rogelio Valadez Blanco
 Enzimas Catalizadores bioquímicos Rogelio Valadez Blanco COFACTORES Algunas enzimas tienen necesidad de cofactores para realizar su actividad catalítica Una proteína inactiva por sí sola se llama apoenzima
Enzimas Catalizadores bioquímicos Rogelio Valadez Blanco COFACTORES Algunas enzimas tienen necesidad de cofactores para realizar su actividad catalítica Una proteína inactiva por sí sola se llama apoenzima
1. Necesidad energética de las células. Concepto de metabolismo.
 1. Necesidad energética de las células. Concepto de metabolismo. Las células intercambian continuamente materia y energía con su entorno. La materia y energía son transformadas en su interior con objeto
1. Necesidad energética de las células. Concepto de metabolismo. Las células intercambian continuamente materia y energía con su entorno. La materia y energía son transformadas en su interior con objeto
ENZIMAS. Kuhne en el año de 1876 les llamó enzima a los catalizadores que producían
 ENZIMAS Dr. Santiago René Anzaldúa Arce. Kuhne en el año de 1876 les llamó enzima a los catalizadores que producían fermentaciones de diversos compuestos, La palabra enzima significa en la levadura, pues
ENZIMAS Dr. Santiago René Anzaldúa Arce. Kuhne en el año de 1876 les llamó enzima a los catalizadores que producían fermentaciones de diversos compuestos, La palabra enzima significa en la levadura, pues
TEMA 5 ENZIMAS. Cualquier complejidad intelectual puede ser transmitida en el lenguaje corriente «Brontosaurus» y la nalga del ministro S.J.
 TEMA 5 ENZIMAS Cualquier complejidad intelectual puede ser transmitida en el lenguaje corriente «Brontosaurus» y la nalga del ministro S.J.Gould BIOLOGÍA 2º BACHILLERATO Enzimas Concepto Biocatalizador
TEMA 5 ENZIMAS Cualquier complejidad intelectual puede ser transmitida en el lenguaje corriente «Brontosaurus» y la nalga del ministro S.J.Gould BIOLOGÍA 2º BACHILLERATO Enzimas Concepto Biocatalizador
ENZIMAS SE TRATA DE PROTEÍNAS ESPECIALES QUE EJERCEN SU ACCIÓN UNIÉNDOSE SELECTIVAMENTE A OTRAS MOLÉCULAS DENOMINADAS SUSTRATOS.
 ENZIMAS SE TRATA DE PROTEÍNAS ESPECIALES QUE EJERCEN SU ACCIÓN UNIÉNDOSE SELECTIVAMENTE A OTRAS MOLÉCULAS DENOMINADAS SUSTRATOS. INDUCEN MODIFICACIONES QUÍMICAS EN LOS SUSTRATOS A LOS QUE SE UNEN POR:
ENZIMAS SE TRATA DE PROTEÍNAS ESPECIALES QUE EJERCEN SU ACCIÓN UNIÉNDOSE SELECTIVAMENTE A OTRAS MOLÉCULAS DENOMINADAS SUSTRATOS. INDUCEN MODIFICACIONES QUÍMICAS EN LOS SUSTRATOS A LOS QUE SE UNEN POR:
Estructurales: dan forma a la proteína.
 1. Concepto de biocatalizador. Son sustancias que consiguen que las reacciones se realicen a gran velocidad a bajas temperaturas, ya que disminuyen la energía de activación de los reactivos. Pueden ser:
1. Concepto de biocatalizador. Son sustancias que consiguen que las reacciones se realicen a gran velocidad a bajas temperaturas, ya que disminuyen la energía de activación de los reactivos. Pueden ser:
FACULTAD DE QUÍMICA DEPARTAMENTO DE BIOQUÍMICA. CURSO DE BIOQUÍMICA (CLAVE 1508) Licenciaturas de QFB y QA
 FACULTAD DE QUÍMICA DEPARTAMENTO DE BIOQUÍMICA CURSO DE BIOQUÍMICA (CLAVE 1508) Licenciaturas de QFB y QA Prof. Laura Carmona Salazar Grupos: 03 Semestre: 13-I Este material es exclusivamente para uso
FACULTAD DE QUÍMICA DEPARTAMENTO DE BIOQUÍMICA CURSO DE BIOQUÍMICA (CLAVE 1508) Licenciaturas de QFB y QA Prof. Laura Carmona Salazar Grupos: 03 Semestre: 13-I Este material es exclusivamente para uso
FACULTAD DE QUÍMICA DEPARTAMENTO DE BIOQUÍMICA. CURSO DE BIOQUÍMICA (CLAVE 1508) Licenciaturas de QFB y QA
 FACULTAD DE QUÍMICA DEPARTAMENTO DE BIOQUÍMICA CURSO DE BIOQUÍMICA (CLAVE 1508) Licenciaturas de QFB y QA Prof. Laura Carmona Salazar Grupos: 03 Semestre: 13-I Este material es exclusivamente para uso
FACULTAD DE QUÍMICA DEPARTAMENTO DE BIOQUÍMICA CURSO DE BIOQUÍMICA (CLAVE 1508) Licenciaturas de QFB y QA Prof. Laura Carmona Salazar Grupos: 03 Semestre: 13-I Este material es exclusivamente para uso
CINETICA ENZIMATICA ESTUDIA LA VELOCIDAD DE LAS REACCIONES BIOQUÍMICAS
 CINETICA ENZIMATICA ESTUDIA LA VELOCIDAD DE LAS REACCIONES BIOQUÍMICAS Es la medida de la formación de producto o la desapariciónde sustrato por unidad de tiempo. E S P Velocidad de una reacción se muestra
CINETICA ENZIMATICA ESTUDIA LA VELOCIDAD DE LAS REACCIONES BIOQUÍMICAS Es la medida de la formación de producto o la desapariciónde sustrato por unidad de tiempo. E S P Velocidad de una reacción se muestra
IES Francisco Pacheco
 6. ENZIMAS. 6.1. Concepto y estructura. 6.2. Mecanismo de acción enzimática. 6.3. Cinética enzimática. 6.4. Regulación de la actividad enzimática: temperatura, ph, inhibidores. 6.5. Nomenclatura y clasificación
6. ENZIMAS. 6.1. Concepto y estructura. 6.2. Mecanismo de acción enzimática. 6.3. Cinética enzimática. 6.4. Regulación de la actividad enzimática: temperatura, ph, inhibidores. 6.5. Nomenclatura y clasificación
ACTIVIDAD ENZIMÁTICA. Curvas temporales
 ACTIVIDAD ENZIMÁTICA Curvas temporales POR QUÉ SON IMPORTANTES LAS Una gran variedad de las reacciones bioquímicas que se llevan a cabo en los seres vivos son mediadas por una serie de catalizadores biológicos
ACTIVIDAD ENZIMÁTICA Curvas temporales POR QUÉ SON IMPORTANTES LAS Una gran variedad de las reacciones bioquímicas que se llevan a cabo en los seres vivos son mediadas por una serie de catalizadores biológicos
Energía y enzimas: bioenergética. n Los organismos obtienen su energía de la luz o de compuestos químicos y la conservan en forma de ATP.
 Enzimas y catálisis Patricio Muñoz Torres patricio.munozt@gmail.com Energía y enzimas: bioenergética n Los organismos obtienen su energía de la luz o de compuestos químicos y la conservan en forma de ATP.
Enzimas y catálisis Patricio Muñoz Torres patricio.munozt@gmail.com Energía y enzimas: bioenergética n Los organismos obtienen su energía de la luz o de compuestos químicos y la conservan en forma de ATP.
Química Bioinorgánica Introducción General 5
 Química Bioinorgánica Introducción General 5 Cinética Enzimática Estudia la velocidad de las reacciones catalizadas enzimáticamente. Los principios generales de las reacciones químicas se aplican también
Química Bioinorgánica Introducción General 5 Cinética Enzimática Estudia la velocidad de las reacciones catalizadas enzimáticamente. Los principios generales de las reacciones químicas se aplican también
CARACTERÍSTICAS DE LAS ENZIMAS MECANISMOS DE ACCIÓN ENZIMÁTICA CINÉTICA ENZIMÁTICA REGULACIÓN DE LA ACTIVIDAD ENZIMÁTICA
 CARACTERÍSTICAS DE LAS ENZIMAS MECANISMOS DE ACCIÓN ENZIMÁTICA CINÉTICA ENZIMÁTICA REGULACIÓN DE LA ACTIVIDAD ENZIMÁTICA Las enzimas son, en su gran mayoría, proteínas globulares sintetizadas por las células
CARACTERÍSTICAS DE LAS ENZIMAS MECANISMOS DE ACCIÓN ENZIMÁTICA CINÉTICA ENZIMÁTICA REGULACIÓN DE LA ACTIVIDAD ENZIMÁTICA Las enzimas son, en su gran mayoría, proteínas globulares sintetizadas por las células
ENZIMAS-2005 CINÉTICA ENZIMÁTICA
 ENZIMAS-00 Las enzimas son catalizadores biológicos en su mayoría de naturaleza proteica (99,99%) y las ribosimas (fragmentos de RNA) (0,%). Las enzimas tienen tres propiedades bien definidas e inigualables
ENZIMAS-00 Las enzimas son catalizadores biológicos en su mayoría de naturaleza proteica (99,99%) y las ribosimas (fragmentos de RNA) (0,%). Las enzimas tienen tres propiedades bien definidas e inigualables
Concepto de velocidad inicial [ ] d[ ] v =, t -> 0 dt
![Concepto de velocidad inicial [ ] d[ ] v =, t -> 0 dt Concepto de velocidad inicial [ ] d[ ] v =, t -> 0 dt](/thumbs/70/63569259.jpg) VARIABLES QUE INFLUYEN EN LA VELOCIDAD DE UNA REACIÓN ENZIMÁTICA Concepto de velocidad inicial [ ] d[ ] v =, t -> 0 dt p s t VARIABLES QUE INFLUYEN EN LA VELOCIDAD DE UNA REACIÓN ENZIMÁTICA Concentración
VARIABLES QUE INFLUYEN EN LA VELOCIDAD DE UNA REACIÓN ENZIMÁTICA Concepto de velocidad inicial [ ] d[ ] v =, t -> 0 dt p s t VARIABLES QUE INFLUYEN EN LA VELOCIDAD DE UNA REACIÓN ENZIMÁTICA Concentración
TEMA 5:BIOCATALIZADORES: ENZIMAS, VITAMINAS Y HORMONAS
 TEMA 5:BIOCATALIZADORES: ENZIMAS, VITAMINAS Y HORMONAS INDICE 1. BIOCATALIZADORES 2. ENZIMAS 2.1. CONCEPTO, PROPIEDADES Y COMPOSICIÓN QUÍMICA 2.2. MECANISMOS DE ACCIÓN 2.3. ESPECIFICIDAD ENZIMÁTICA 2.4.
TEMA 5:BIOCATALIZADORES: ENZIMAS, VITAMINAS Y HORMONAS INDICE 1. BIOCATALIZADORES 2. ENZIMAS 2.1. CONCEPTO, PROPIEDADES Y COMPOSICIÓN QUÍMICA 2.2. MECANISMOS DE ACCIÓN 2.3. ESPECIFICIDAD ENZIMÁTICA 2.4.
ENZIMAS Las enzimas son proteínas
 ENZIMAS Las enzimas son proteínas Actúan como catalizadores de las reacciones químicas necesarias para la supervivencia celular Que es un catalizador??? Es una sustancia que acelera la velocidad de la
ENZIMAS Las enzimas son proteínas Actúan como catalizadores de las reacciones químicas necesarias para la supervivencia celular Que es un catalizador??? Es una sustancia que acelera la velocidad de la
PRACTICO Nº 3 ENZIMOLOGÍA II
 PRACTICO Nº 3 ENZIMOLOGÍA II I. - INTRODUCCIÓN FACTORES QUE AFECTAN LA ACTIVIDAD ENZIMATICA Para definir la actividad de una preparación enzimática se utiliza en la práctica distintas expresiones. La cantidad
PRACTICO Nº 3 ENZIMOLOGÍA II I. - INTRODUCCIÓN FACTORES QUE AFECTAN LA ACTIVIDAD ENZIMATICA Para definir la actividad de una preparación enzimática se utiliza en la práctica distintas expresiones. La cantidad
UNIDAD 12. METABOLISMO Y ENZIMAS.
 UNIDAD 12. METABOLISMO Y ENZIMAS. 1.- REACCIONES METABÓLICAS. Reacción metabólica. Cualquier reacción entre biomoléculas que ocurre en los seres vivos. Características de las reacciones metabólicas: -
UNIDAD 12. METABOLISMO Y ENZIMAS. 1.- REACCIONES METABÓLICAS. Reacción metabólica. Cualquier reacción entre biomoléculas que ocurre en los seres vivos. Características de las reacciones metabólicas: -
OBJETIVO: Poner en evidencia enzimas mediante su actividad frente a sustratos específicos.
 Trabajo Prático 7: Enzimas OBJETIVO: Poner en evidencia enzimas mediante su actividad frente a sustratos específicos. FUNDAMENTO: Las funciones vitales de una célula, ya sea esta de origen animal, vegetal
Trabajo Prático 7: Enzimas OBJETIVO: Poner en evidencia enzimas mediante su actividad frente a sustratos específicos. FUNDAMENTO: Las funciones vitales de una célula, ya sea esta de origen animal, vegetal
1. Necesidad energética de las células. Concepto de metabolismo.
 1. Necesidad energética de las células. Concepto de metabolismo. Las células intercambian continuamente materia y energía con su entorno. La materia y energía son transformadas en su interior con objeto
1. Necesidad energética de las células. Concepto de metabolismo. Las células intercambian continuamente materia y energía con su entorno. La materia y energía son transformadas en su interior con objeto
SUMARIO: 1- Cofactores enzimáticos. Vitaminas. 2- Regulación de la actividad enzimática.
 Conferencia: Biocatalizadores. Regulación. Autor: Dr. Daniel Sánchez Serrano SUMARIO: 1- Cofactores enzimáticos. Vitaminas. 2- Regulación de la actividad enzimática. 3- Significado biológico de la regulación
Conferencia: Biocatalizadores. Regulación. Autor: Dr. Daniel Sánchez Serrano SUMARIO: 1- Cofactores enzimáticos. Vitaminas. 2- Regulación de la actividad enzimática. 3- Significado biológico de la regulación
3º SESIÓN DE APRENDIZAJE VERSIÓN DE IMPRESION CINETICA ENZIMATICA I
 3º SESIÓN DE APRENDIZAJE VERSIÓN DE IMPRESION CINETICA ENZIMATICA I MODO DE ACCIÓN DE LAS ENZIMAS En las reacciones espontáneas, los productos finales tienen menos energía libre de Gibbs (DG) que los reactantes
3º SESIÓN DE APRENDIZAJE VERSIÓN DE IMPRESION CINETICA ENZIMATICA I MODO DE ACCIÓN DE LAS ENZIMAS En las reacciones espontáneas, los productos finales tienen menos energía libre de Gibbs (DG) que los reactantes
Fisiología del tubo digestivo. Metabolismo intermedio
 Fisiología de la Nutrición Fisiología del tubo digestivo Metabolismo intermedio Nutrición PROTEÍNAS AGUA LÍPIDOS CARBOHIDRATOS Á. NUCLEICOS VITAMINAS MINERALES Qué cosas entran y cuáles salen de la
Fisiología de la Nutrición Fisiología del tubo digestivo Metabolismo intermedio Nutrición PROTEÍNAS AGUA LÍPIDOS CARBOHIDRATOS Á. NUCLEICOS VITAMINAS MINERALES Qué cosas entran y cuáles salen de la
TEMA: Enzimas II. Cinética de la reacciones enzimáticas Ecuación de Michaelis-Menten Tipos de inhibición enzimática Métodos de representación gráfica
 TEMA: Enzimas II Cinética de la reacciones enzimáticas Ecuación de Michaelis-Menten Tipos de inhibición enzimática Métodos de representación gráfica CINÉTICA ENZIMÁTICA k 1 E + S E:S E + P k -1 v f =
TEMA: Enzimas II Cinética de la reacciones enzimáticas Ecuación de Michaelis-Menten Tipos de inhibición enzimática Métodos de representación gráfica CINÉTICA ENZIMÁTICA k 1 E + S E:S E + P k -1 v f =
Las enzimas son, en su gran mayoría, proteínas globulares sintetizadas por las células para catalizar reacciones bioquímicas.
 ENZIMAS Estudiar características de las enzimas y su clasificacción Conocer la función de las enzimas y su mecanismo de acción Comprender el significado de los principales parámetros cinéticos Interpretar
ENZIMAS Estudiar características de las enzimas y su clasificacción Conocer la función de las enzimas y su mecanismo de acción Comprender el significado de los principales parámetros cinéticos Interpretar
PRACTICO Nº 3 ENZIMOLOGÍA II
 PRACTICO Nº 3 ENZIMOLOGÍA II I. - INTRODUCCIÓN FACTORES QUE AFECTAN LA ACTIVIDAD ENZIMATICA Para definir la actividad de una preparación enzimática se utiliza en la práctica distintas expresiones. La cantidad
PRACTICO Nº 3 ENZIMOLOGÍA II I. - INTRODUCCIÓN FACTORES QUE AFECTAN LA ACTIVIDAD ENZIMATICA Para definir la actividad de una preparación enzimática se utiliza en la práctica distintas expresiones. La cantidad
Profesora: María Antonia Rojas Serrano
 Profesora: María Antonia Rojas Serrano CATALIZADORES BIOLÓGICOS Los catalizadores biológicos o biocatalizadores de las reacciones metabólicas del organismo son las enzimas. Todas las enzimas son proteínas,
Profesora: María Antonia Rojas Serrano CATALIZADORES BIOLÓGICOS Los catalizadores biológicos o biocatalizadores de las reacciones metabólicas del organismo son las enzimas. Todas las enzimas son proteínas,
QUE SON? Biocatalizadoras. ENZIMA: griego zymos (fermento)
 Enzimas QUE SON? Biocatalizadoras. ENZIMA: griego zymos (fermento) CATALIZADOR: Sustancia que aumenta la velocidad de una reacción, sin alterarse en el proceso. NATURALEZA QUIMICA: proteica PROPIEDADES
Enzimas QUE SON? Biocatalizadoras. ENZIMA: griego zymos (fermento) CATALIZADOR: Sustancia que aumenta la velocidad de una reacción, sin alterarse en el proceso. NATURALEZA QUIMICA: proteica PROPIEDADES
ESTRUCTURA DE LA TRIOSAFOSFATO ISOMERASA esta proteína es una eficiente enzima involucrada en la vía glucolítica.
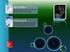 ESTRUCTURA DE LA TRIOSAFOSFATO ISOMERASA esta proteína es una eficiente enzima involucrada en la vía glucolítica. Características generales Cinética química Nomenclatura Centro activo Cofactores Factores
ESTRUCTURA DE LA TRIOSAFOSFATO ISOMERASA esta proteína es una eficiente enzima involucrada en la vía glucolítica. Características generales Cinética química Nomenclatura Centro activo Cofactores Factores
2. Con respecto a la energía de activación de una reacción, cuál de las siguientes alternativas es correcta?
 Nº GUÍA PRÁCTICA Cinética química I: velocidad de reacción Ejercicios PSU 1. La velocidad de una reacción química está considerada como I) una fórmula que expresa los mol de productos obtenidos por segundo.
Nº GUÍA PRÁCTICA Cinética química I: velocidad de reacción Ejercicios PSU 1. La velocidad de una reacción química está considerada como I) una fórmula que expresa los mol de productos obtenidos por segundo.
METABOLISMO. Contenidos trabajados en clase.
 METABOLISMO Contenidos trabajados en clase. Qué son? Donde actúan? Como actúan? Propiedades o características Toda reacción exergónica necesita calor (energía )para comenzar Ej La combustión de la madera
METABOLISMO Contenidos trabajados en clase. Qué son? Donde actúan? Como actúan? Propiedades o características Toda reacción exergónica necesita calor (energía )para comenzar Ej La combustión de la madera
Son proteínas globulares altamente especializadas que provocan o aceleran una reacción bioquímica.
 1.7.- Enzimas Las reacciones precisan de una cierta cantidad de energía para iniciarse. Esta energía, denominada energía de activación, permite romper los enlaces de las moléculas que están reaccionando
1.7.- Enzimas Las reacciones precisan de una cierta cantidad de energía para iniciarse. Esta energía, denominada energía de activación, permite romper los enlaces de las moléculas que están reaccionando
FUNCIÓN DE LAS PR DE L O AS PR TE O ÍNAS
 FUNCIÓN DE LAS PROTEÍNAS PROTEÍNAS.- PUEDEN DESEMPEÑAR DIVERSAS FUNCIONES BIOLÓGICAS a) Enzimas.- Actividad catalítica b) Hormonas c) Anticuerpos Reconocimiento específico d) Receptores en membranas e)
FUNCIÓN DE LAS PROTEÍNAS PROTEÍNAS.- PUEDEN DESEMPEÑAR DIVERSAS FUNCIONES BIOLÓGICAS a) Enzimas.- Actividad catalítica b) Hormonas c) Anticuerpos Reconocimiento específico d) Receptores en membranas e)
METABOLISMO Y BIOENERGÉTICA BIOQUÍMICA. CAPÍTULO 14
 METABOLISMO Y BIOENERGÉTICA BIOQUÍMICA. CAPÍTULO 14 METABOLISMO Estudio de las reacciones bioquímicas que se llevan a cabo, incluidas su coordinación, regulación y necesidades energéticas. La energía que
METABOLISMO Y BIOENERGÉTICA BIOQUÍMICA. CAPÍTULO 14 METABOLISMO Estudio de las reacciones bioquímicas que se llevan a cabo, incluidas su coordinación, regulación y necesidades energéticas. La energía que
PROTEINAS COMO CATALIZADORES ENZIMAS
 PROTEINAS COMO CATALIZADORES ENZIMAS ENZIMAS son proteínas que catalizan reacciones químicas en los seres vivos. son catalizadores: sustancias que, sin consumirse en una reacción, aumentan notablemente
PROTEINAS COMO CATALIZADORES ENZIMAS ENZIMAS son proteínas que catalizan reacciones químicas en los seres vivos. son catalizadores: sustancias que, sin consumirse en una reacción, aumentan notablemente
Proteínas como blancos farmacológicos. Dra. Jenny Fiedler.
 Proteínas como blancos farmacológicos. Enzimas Dra. Jenny Fiedler. Estructura de proteínas Estructura primaria Secuencia de aminoácidos en una proteína 1 2 3 4 5 126 127 128 129 Lys-Val-Phe-Gly-Arg...Gly-Cys-Arg-Leu
Proteínas como blancos farmacológicos. Enzimas Dra. Jenny Fiedler. Estructura de proteínas Estructura primaria Secuencia de aminoácidos en una proteína 1 2 3 4 5 126 127 128 129 Lys-Val-Phe-Gly-Arg...Gly-Cys-Arg-Leu
METABOLISMO Y ENZIMAS
 Guía de Actividades N 7 METABOLISMO Y ENZIMAS SECTOR EJE 1 UNIDAD 1 : CIENCIAS NATURALES - BIOLOGÍA : ESTRUCTURA Y FUNCIÓN DE LOS SERES VIVOS : ESTRUCTURA Y FUNCIÓN DE LA CÉLULA ESTUDIANTE : PROFESOR :
Guía de Actividades N 7 METABOLISMO Y ENZIMAS SECTOR EJE 1 UNIDAD 1 : CIENCIAS NATURALES - BIOLOGÍA : ESTRUCTURA Y FUNCIÓN DE LOS SERES VIVOS : ESTRUCTURA Y FUNCIÓN DE LA CÉLULA ESTUDIANTE : PROFESOR :
ACTIVIDAD ENZIMÁTICA. SOLUCIONARIO
 ACTIVIDAD ENZIMÁTICA. SOLUCIONARIO 1) Respuestas: a) Se trata de una reacción en la que el nivel energético de los reactivos (estado inicial) es superior al de los productos (estado final); por tanto,
ACTIVIDAD ENZIMÁTICA. SOLUCIONARIO 1) Respuestas: a) Se trata de una reacción en la que el nivel energético de los reactivos (estado inicial) es superior al de los productos (estado final); por tanto,
Las Proteínas BIOLOGÍA 2º BACHILLERATO TEMA 4: Actividades: 1º DÍA Los aminoácidos. Pg
 BIOLOGÍA 2º BACHILLERATO TEMA 4: Las Proteínas Actividades: 1º DÍA Los aminoácidos Pg 58-59-60 1. Define el concepto de aminoácido. Escribe su fórmula general explicando su estructura molecular. 2. a)
BIOLOGÍA 2º BACHILLERATO TEMA 4: Las Proteínas Actividades: 1º DÍA Los aminoácidos Pg 58-59-60 1. Define el concepto de aminoácido. Escribe su fórmula general explicando su estructura molecular. 2. a)
endoenzimas exoenzimas:
 Enzimas Enzimas:son proteínas altamente especializadas que tienen como función la catálisis o regulación de la velocidad de las reacciones químicas que se llevan a cabo en los seres vivos. Son macromoléculas
Enzimas Enzimas:son proteínas altamente especializadas que tienen como función la catálisis o regulación de la velocidad de las reacciones químicas que se llevan a cabo en los seres vivos. Son macromoléculas
QUÍMICA BIOLÓGICA. Enzimas Cinética Enzimática
 QUÍMICA BIOLÓGICA Enzimas Cinética Enzimática 2017 INTRODUCCIÓN Proteínas (única excepción: RNAs catalíticos o ribozimas) Holoenzima (complejo catalíticamente activo) Apoenzima (inactiva) Cofactor (coenzimas,
QUÍMICA BIOLÓGICA Enzimas Cinética Enzimática 2017 INTRODUCCIÓN Proteínas (única excepción: RNAs catalíticos o ribozimas) Holoenzima (complejo catalíticamente activo) Apoenzima (inactiva) Cofactor (coenzimas,
aa + bb cc + dd 1.Velocidad de reacción d dt c dt b dt La velocidad de la reacción se puede expresar:
 1.Velocidad de reacción La velocidad de una reacción química indica cómo varía la concentración de reactivos o productos con el tiempo Ejemplo: Para la reacción concentración productos reactivos aa + bb
1.Velocidad de reacción La velocidad de una reacción química indica cómo varía la concentración de reactivos o productos con el tiempo Ejemplo: Para la reacción concentración productos reactivos aa + bb
CINÉTICA ENZIMÁTICA. Ecuación de Michaelis-Menten Efecto de inhibidores
 CINÉTICA ENZIMÁTICA Ecuación de Michaelis-Menten Efecto de inhibidores Producto [P] CINÉTICA ENZIMÁTICA La cinética enzimática estudia la velocidad de las reacciones catalizadas por enzimas. Proporciona
CINÉTICA ENZIMÁTICA Ecuación de Michaelis-Menten Efecto de inhibidores Producto [P] CINÉTICA ENZIMÁTICA La cinética enzimática estudia la velocidad de las reacciones catalizadas por enzimas. Proporciona
METABOLISMO Y ENZIMAS
 DESAFÍO Nº 12 Profesora Verónica Abasto Córdova Biología 1 Medio Nombre del Estudiante : Curso : METABOLISMO Y ENZIMAS TIMBRE METABOLISMO En las clases anteriores, estudiamos los principios de la teoría
DESAFÍO Nº 12 Profesora Verónica Abasto Córdova Biología 1 Medio Nombre del Estudiante : Curso : METABOLISMO Y ENZIMAS TIMBRE METABOLISMO En las clases anteriores, estudiamos los principios de la teoría
Son CATALIZADORES, es decir, disminuyen la energía de activación de las reacciones químicas. Son PROTEÍNAS con estructura tridimensional, que poseen
 Son CATALIZADORES, es decir, disminuyen la energía de activación de las reacciones químicas. Son PROTEÍNAS con estructura tridimensional, que poseen un centro activo en el que se acopla el sustrato para
Son CATALIZADORES, es decir, disminuyen la energía de activación de las reacciones químicas. Son PROTEÍNAS con estructura tridimensional, que poseen un centro activo en el que se acopla el sustrato para
SERIE Nº 6. Enzimas y Coenzimas
 SERIE Nº 6. Enzimas Las reacciones químicas que ocurren en los organismos vivos presentan casi siempre una energía de activación tan elevada, que en condiciones compatibles con la vida ocurrirían a velocidades
SERIE Nº 6. Enzimas Las reacciones químicas que ocurren en los organismos vivos presentan casi siempre una energía de activación tan elevada, que en condiciones compatibles con la vida ocurrirían a velocidades
Universidad Nacional de la Patagonia S. J. B Facultad de Ciencias Naturales Química Biológica. Química Biológica TP 5 ENZIMAS, Introducción
 TP 5 ENZIMAS, Introducción Las funciones vitales de la célula no son más que una serie de reacciones químicas, que en conjunto determinan la existencia de una verdadera maraña de procesos y vías metabólicas.
TP 5 ENZIMAS, Introducción Las funciones vitales de la célula no son más que una serie de reacciones químicas, que en conjunto determinan la existencia de una verdadera maraña de procesos y vías metabólicas.
ENZIMAS I TEMA Introducción
 TEMA 7 ENZIMAS I 1. Introducción 2. Las enzimas como catalizadores 3. Nomenclatura y clasificación de enzimas 4. Cofactores enzimáticos 5. Modelos de actuación de las enzimas 1. Introducción La vida depende
TEMA 7 ENZIMAS I 1. Introducción 2. Las enzimas como catalizadores 3. Nomenclatura y clasificación de enzimas 4. Cofactores enzimáticos 5. Modelos de actuación de las enzimas 1. Introducción La vida depende
Generalidades de ENZIMAS
 UNIVERSIDAD DE SAN CARLOS DE GUATEMALA FACULTAD DE CIENCIAS MÉDICAS FASE I, Unidad Didáctica: BIOQUÍMICA MÉDICA 2º AÑO CICLO ACADÉMICO 2,009 Generalidades de ENZIMAS Dr. Mynor Leiva Desde los nutrientes
UNIVERSIDAD DE SAN CARLOS DE GUATEMALA FACULTAD DE CIENCIAS MÉDICAS FASE I, Unidad Didáctica: BIOQUÍMICA MÉDICA 2º AÑO CICLO ACADÉMICO 2,009 Generalidades de ENZIMAS Dr. Mynor Leiva Desde los nutrientes
TEMA 4 (II). LAS ENZIMAS.
 TEMA 4 (II). LAS ENZIMAS. 1. Introducción. Las transformaciones que ocurren en los seres vivos son el resultado de un conjunto de reacciones químicas que constituyen el metabolismo celular. Estas reacciones
TEMA 4 (II). LAS ENZIMAS. 1. Introducción. Las transformaciones que ocurren en los seres vivos son el resultado de un conjunto de reacciones químicas que constituyen el metabolismo celular. Estas reacciones
Velocidad es la variación de la concentración de una de las sustancias de la reacción con el tiempo. Su unidad es: mol L 1 s 1.
 Cinética es el estudio de la velocidad a la que tienen lugar las reacciones químicas. Los resultados sólo pueden obtenerse por vía experimental y de ellos puede predecirse el camino por el que transcurren
Cinética es el estudio de la velocidad a la que tienen lugar las reacciones químicas. Los resultados sólo pueden obtenerse por vía experimental y de ellos puede predecirse el camino por el que transcurren
BIOCATALIZADOR. sustrato. producto
 BIOCATALIZADOR puede ser proteína catalítica (enzima) o RNA catalítico (ribosima) - aumenta la velocidad de una reacción sin gastarse a si mismo - su presencia no cambia la naturaleza o las características
BIOCATALIZADOR puede ser proteína catalítica (enzima) o RNA catalítico (ribosima) - aumenta la velocidad de una reacción sin gastarse a si mismo - su presencia no cambia la naturaleza o las características
ESTUDIOS CINÉTICOS SE MIDE LA VELOCIDAD DE LA REACCIÓN CATALIZADA. La velocidad de reacciones químicas: Para una reacción:
 ESTUDIOS CINÉTICOS SE MIDE LA VELOCIDAD DE LA REACCIÓN CATALIZADA La velocidad de reacciones químicas: Para una reacción: A B La velocidad depende de la concentración del reactante: v = k[a] k = constante
ESTUDIOS CINÉTICOS SE MIDE LA VELOCIDAD DE LA REACCIÓN CATALIZADA La velocidad de reacciones químicas: Para una reacción: A B La velocidad depende de la concentración del reactante: v = k[a] k = constante
GUÍA DE TRABAJOS PRÁCTICOS
 Departamento de Electrónica y Automática Facultad de Ingeniería Universidad Nacional de San Juan QUÍMICA II GUÍA DE TRABAJOS PRÁCTICOS Laboratorio Nº 4 Enzimas Bioingeniería Año 2017 Trabajo práctico N
Departamento de Electrónica y Automática Facultad de Ingeniería Universidad Nacional de San Juan QUÍMICA II GUÍA DE TRABAJOS PRÁCTICOS Laboratorio Nº 4 Enzimas Bioingeniería Año 2017 Trabajo práctico N
CURSO BIOQUÍMICA Y FITOQUÍMICA. FACULTAD DE CIENCIAS AGRARIAS Y FORESTALES UNLP. Primer cuatrimestre 2011 UNIDAD Nº 3
 CURSO BIOQUÍMICA Y FITOQUÍMICA. FACULTAD DE CIENCIAS AGRARIAS Y FORESTALES UNLP. Primer cuatrimestre 2011 UNIDAD Nº 3 FACTORES QUE INCIDEN EN LA ACTIVIDAD ENZIMÁTICA: PRESENCIA DE INHIBIDORES. Dentro de
CURSO BIOQUÍMICA Y FITOQUÍMICA. FACULTAD DE CIENCIAS AGRARIAS Y FORESTALES UNLP. Primer cuatrimestre 2011 UNIDAD Nº 3 FACTORES QUE INCIDEN EN LA ACTIVIDAD ENZIMÁTICA: PRESENCIA DE INHIBIDORES. Dentro de
Las células llevan a cabo una gran variedad de reacciones químicas: Degradación de moléculas alimenticias Síntesis de los constituyentes celulares
 Grado Medicina Biología Celular 1 er Curso TEMA 3 METABOLISMO CELULAR 3.1 Papel central de las enzimas como catalizadores biológicos. 3.2 Energía metabólica. Biosíntesis de los componentes celulares. Las
Grado Medicina Biología Celular 1 er Curso TEMA 3 METABOLISMO CELULAR 3.1 Papel central de las enzimas como catalizadores biológicos. 3.2 Energía metabólica. Biosíntesis de los componentes celulares. Las
CINETICA ENZIMATICA LA CINÉTICA QUÍMICA ESTUDIA LA VELOCIDAD DE LAS REACCIONES BIOQUÍMICAS
 CINETICA ENZIMATICA LA CINÉTICA QUÍMICA ESTUDIA LA VELOCIDAD DE LAS REACCIONES BIOQUÍMICAS Realizar ensayos en el laboratorio en diferentes condiciones experimentales para estudiar la velocidad de las
CINETICA ENZIMATICA LA CINÉTICA QUÍMICA ESTUDIA LA VELOCIDAD DE LAS REACCIONES BIOQUÍMICAS Realizar ensayos en el laboratorio en diferentes condiciones experimentales para estudiar la velocidad de las
EL CONTROL DE LAS ACTIVIDADES CELULARES. Por Wilfredo Santiago
 EL CONTROL DE LAS ACTIVIDADES CELULARES Por Wilfredo Santiago LAS REACCIONES CELULARES Todas las células llevan a cabo ciertas funciones vitales básicas: Ingestión de nutrientes. Eliminación de desperdicios.
EL CONTROL DE LAS ACTIVIDADES CELULARES Por Wilfredo Santiago LAS REACCIONES CELULARES Todas las células llevan a cabo ciertas funciones vitales básicas: Ingestión de nutrientes. Eliminación de desperdicios.
IV electivo. Unidad 1: Integración célula organismo Genes, proteínas y enzimas
 IV electivo Unidad 1: Integración célula organismo Genes, proteínas y enzimas Objetivo Analizar la composición de un gen y la respectiva formación de proteínas Material genético Material genético Cromosoma
IV electivo Unidad 1: Integración célula organismo Genes, proteínas y enzimas Objetivo Analizar la composición de un gen y la respectiva formación de proteínas Material genético Material genético Cromosoma
Cinética enzimática. La velocidad enzimática sigue una curva denominada hipérbola descripta por la Ecuación de Michaelis y Menten:
 Cinética enzimática Hemos visto que la concentración de sustrato es uno de los factores más importantes que determinan la velocidad de una reacción enzimática. La velocidad enzimática sigue una curva denominada
Cinética enzimática Hemos visto que la concentración de sustrato es uno de los factores más importantes que determinan la velocidad de una reacción enzimática. La velocidad enzimática sigue una curva denominada
Enzimas: catalizadores biológicos
 Enzimas: catalizadores biológicos Son capaces de aumentar la velocidad de reacciones químicas. Son muy eficientes, específicas y no se consumen en la reacción. PUEDEN AUMENTAR LA VELOCIDAD DE LA REACCION
Enzimas: catalizadores biológicos Son capaces de aumentar la velocidad de reacciones químicas. Son muy eficientes, específicas y no se consumen en la reacción. PUEDEN AUMENTAR LA VELOCIDAD DE LA REACCION
BLOQUE I: LAS MOLÉCULAS DE LA VIDA ENZIMAS. 2. Mecanismo de acción y cinética enzimática.
 ENZIMAS 1. Concepto y estructura. 2. Mecanismo de acción y cinética enzimática. 3. Regulación de la actividad enzimática: temperatura, ph, inhibidores. 4. Bibliografía. 5. Preguntas selectividad. Imagen
ENZIMAS 1. Concepto y estructura. 2. Mecanismo de acción y cinética enzimática. 3. Regulación de la actividad enzimática: temperatura, ph, inhibidores. 4. Bibliografía. 5. Preguntas selectividad. Imagen
CURSO DE BIOQUÍMICA APLICADA GENERALIDADES DE MÉTODOS ENZIMÁTICOS
 CURSO DE BIOQUÍMICA APLICADA GENERALIDADES DE MÉTODOS ENZIMÁTICOS Escuela de Tecnología Médica Universidad de Chile Primera Versión 2007 Propiedades de Enzimas en Solución Acuosa Conocer las características
CURSO DE BIOQUÍMICA APLICADA GENERALIDADES DE MÉTODOS ENZIMÁTICOS Escuela de Tecnología Médica Universidad de Chile Primera Versión 2007 Propiedades de Enzimas en Solución Acuosa Conocer las características
Generalidades de ENZIMAS
 UNIVERSIDAD DE SAN CARLOS DE GUATEMALA FACULTAD DE CIENCIAS MÉDICAS FASE I, Unidad Didáctica: BIOQUÍMICA MÉDICA 2º AÑO CICLO ACADÉMICO 2,007 Generalidades de ENZIMAS Dr. Mynor Leiva 1 ENZIMAS Proteínas
UNIVERSIDAD DE SAN CARLOS DE GUATEMALA FACULTAD DE CIENCIAS MÉDICAS FASE I, Unidad Didáctica: BIOQUÍMICA MÉDICA 2º AÑO CICLO ACADÉMICO 2,007 Generalidades de ENZIMAS Dr. Mynor Leiva 1 ENZIMAS Proteínas
03/08/2009 DESORDEN ENERGÍA DISIPADA ENERGÍA CONVERTIDA EN: -SÍNTESIS -MOVIMIENTO -REPRODUCCIÓN -PENSAMIENTO
 Enzimas, vitaminas y nutrientes INTRODUCCIÓN VIDA organización ió estructuras simple complejo Leyes universales: Orden desorden La energía se disipa Caos, aleatoriedad: Flecha del tiempo ENERGÍA 1 Fuente
Enzimas, vitaminas y nutrientes INTRODUCCIÓN VIDA organización ió estructuras simple complejo Leyes universales: Orden desorden La energía se disipa Caos, aleatoriedad: Flecha del tiempo ENERGÍA 1 Fuente
LA ENERGÍA EN LAS REACCIONES METABÓLICAS
 LA ENERGÍA EN LAS REACCIONES METABÓLICAS ENERGIA DE ACTIVACIÓN. CATALIZADORES ENERGIA DE ACTIVACIÓN. CATALIZADORES REACTIVOS PRODUCTOS ENERGIA DE ACTIVACIÓN. ENZIMAS Las ENZIMAS son proteínas que ACTÚAN
LA ENERGÍA EN LAS REACCIONES METABÓLICAS ENERGIA DE ACTIVACIÓN. CATALIZADORES ENERGIA DE ACTIVACIÓN. CATALIZADORES REACTIVOS PRODUCTOS ENERGIA DE ACTIVACIÓN. ENZIMAS Las ENZIMAS son proteínas que ACTÚAN
BIOCATÁLISIS APLICADA
 CARRERA DE ESPECIALIZACION EN BIOTECNOLOGIA INDUSTRIAL FCEyN-INTI Materia de Articulación CEBI-E5 BIOCATÁLISIS APLICADA Docente a cargo: Dra. Cristina dos Santos Ferreira crisf02@hotmail.com CEBI- E5-2
CARRERA DE ESPECIALIZACION EN BIOTECNOLOGIA INDUSTRIAL FCEyN-INTI Materia de Articulación CEBI-E5 BIOCATÁLISIS APLICADA Docente a cargo: Dra. Cristina dos Santos Ferreira crisf02@hotmail.com CEBI- E5-2
LAS ENZIMAS ENZIMAS CLASIFICACIÓN ESTRUCTURA FUNCIÓN. Biocatalizadores. proteica. velocidad reacción. Energía activación. Inorgánica.
 LAS ENZIMAS ENZIMAS ESTRUCTURA puede ser FUNCIÓN CLASIFICACIÓN Holoenzima formada Estrictamente proteica Biocatalizadores actúan Ligasas Isomerasas Liasas Hidrolasas Transferasas Oxidorreductasas de naturaleza
LAS ENZIMAS ENZIMAS ESTRUCTURA puede ser FUNCIÓN CLASIFICACIÓN Holoenzima formada Estrictamente proteica Biocatalizadores actúan Ligasas Isomerasas Liasas Hidrolasas Transferasas Oxidorreductasas de naturaleza
Tema 7. Actividad enzimática
 Tema 7. Actividad enzimática Definición, clasificación y nomenclatura de las enzimas Coenzimas y cofactores Mecanismos de la catálisis enzimática Centro activo y especificidad Tipos de catálisis Generalidades
Tema 7. Actividad enzimática Definición, clasificación y nomenclatura de las enzimas Coenzimas y cofactores Mecanismos de la catálisis enzimática Centro activo y especificidad Tipos de catálisis Generalidades
