Capítulo 6 QUENCHING DE FLUORESCENCIA
|
|
|
- Gustavo Ponce Salinas
- hace 7 años
- Vistas:
Transcripción
1 Capítulo 6 QUENCHING DE FLUORESCENCIA El fenómeno de quenching de fluorescencia se refiere a procesos que provocan una disminución de la intensidad de fluorescencia de una sustancia dada. El quenching puede ser resultado de varios mecanismos. Estos mecanismos incluyen reacciones de los estados excitados, transferencia de energía, formación de complejos y quenching por colisiones [Lakowicz, 1983]. El quenching de fluorescencia provee evidencia de interacciones moleculares. El fenómeno puede dividirse en dos grupos: quenching colisional o dinámico, cuando la desactivación es resultado de los choques entre moléculas (molécula fluorescente y quencher), y quenching estático, cuando es el resultado de formación de complejos. A veces no resulta fácil distinguir entre uno y otro, pero es posible con un estudio adecuado de los tiempos de vida de fluorescencia. Ambos tipos de desactivación requieren de contacto molecular entre la molécula fluorescente y la molécula quencher. Este fenómeno es especialmente importante en soluciones acuosas donde las colisiones son frecuentes. En solución, el proceso difusional limita la velocidad con que ambas moléculas, especie excitada y quencher, se encuentran, pero hace prolongado el encuentro pudiendo ocurrir cientos de choques antes de separarse. Una gran variedad de sustancias pueden actuar como quenchers de fluorescencia. Uno de los mejores ejemplos de quenching colisional está dado por el oxígeno molecular. Por ello muy frecuentemente es necesario eliminar el oxígeno disuelto de las muestras sobre las que se desea medir tiempos de vida de fluorescencia o rendimientos cuánticos de fluorescencia. Otros ejemplos son las aminas alifáticas y aromáticas, xenón, peróxido de hidrógeno, acrilamida, 6
2 bromato, yoduro, etc. Debido a la gran variedad de moléculas quenchers, se debe identificar aquéllas de interés para cada molécula fluorescente en particular. Quenching dinámico. Esquemáticamente, el quenching dinámico puede representarse como una transferencia de energía entre una especie excitada (M*) y una especie quencher (Q): M + Q M + Q* El quenching dinámico se describe por la ecuación de Stern-Volmer: I F /I F = 1 + K SV [Q] = 1 + k q τ [Q] donde I F e I F son las intensidades de emisión fluorescente en ausencia y presencia del quencher respectivamente, K SV es la constante de Stern-Volmer, [Q] es la concentración del quencher, kq es la constante bimolecular de quenching y τ es el tiempo de vida de fluorescencia de la especie emisora. Esta ecuación puede deducirse planteando estado estacionario de la fluorescencia de una molécula excitada en presencia de un quencher. La molécula quencher puede ser cualquiera, pero debe permanecer químicamente invariable para que la disminución de la concentración del estado excitado, y, por consiguiente, de la emisión fluorescente, se deba a una única interacción entre la molécula emisora y ella. Para realizar el análisis de este estado estacionario debemos considerar las siguientes ecuaciones: Etapas: Velocidad: Absorción de luz: M + hν M* I A Fluorescencia: M* M + hν k F [M*] Decaimientos distintos de quenching: M* M Σ ki [M*] Quenching: M* + Q M + Q kq [M*] [Q] 61
3 donde k F es la constante de fluorescencia intrínseca. Si se asumen condiciones de estado estacionario (-d[m*]/dt = ), entonces: [M*] = I A Σ k i + k q [Q] El rendimiento cuántico de fluorescencia está dado por: k F Φ F = Σ ki + kq [Q] = k F kf + kq [Q] donde k F definida en el Capítulo anterior como el coeficiente de velocidad de emisión espontánea, es igual a la suma de las constantes de velocidad que contribuyen al decaimiento de M* (Σ k i ), excepto k q. Debe observarse que el rendimiento cuántico disminuye en una cantidad proporcional a la concentración del quencher. Se obtiene el valor máximo de rendimiento cuántico (Φ F ) en ausencia de quencher. La relación Φ F / Φ F está dada por: Φ F k F k F + k q [Q] k q [Q] = = 1 + Φ F kf kf kf Esta ecuación indica que la relación de los rendimientos cuánticos de fluorescencia es linealmente dependiente de la concentración del quencher, siendo la ordenada al origen igual a 1. Esta relación se denomina relación de Stern- Volmer. La determinación de los rendimientos cuánticos de fluorescencia requiere del conocimiento de la luz absorbida. Sin embargo, si se realizan medidas de intensidad de fluorescencia en función de la concentración del quencher, bajo idénticas condiciones de geometría de irradiación, concentración de molécula fluorescente, intensidad de excitación, longitud de onda y sensibilidad de detector, entonces la luz absorbida es idéntica para cada medida. Bajo dichas circunstancias, la relación de rendimientos cuánticos es igual a la relación de intensidades de emisión fluorescente: 62
4 I F IF = 1 + k q [Q] kf Así una gráfica de I F /I F versus [Q] (gráfica de Stern-Volmer) debería ser lineal, e interceptar en la unidad al eje IF /IF. La pendiente de dicha gráfica se denomina constante de Stern-Volmer (K SV ), y es igual a k q / k F = τ F k q. En esta última expresión τ F es el parámetro τ F definido en el Capítulo anterior. Sin embargo, en los experimentos de quenching se le suele agregar el superíndice para diferenciarlo de los tiempos de vida en presencia de quencher. El análisis de las gráficas de Stern-Volmer permite obtener valiosa información. Por ejemplo, el determinar el coeficiente de Stern-Volmer da un método indirecto para obtener el tiempo de vida de fluorescencia si se conoce o puede calcularse kq, o por el contrario, se puede determinar kq si se conocen los tiempos de vida de fluorescencia. Por otro lado, una gráfica de Stern-Volmer lineal generalmente indica la presencia de un solo fluoróforo o especie emisora. Por el contrario, si la gráfica de Stern-Volmer no es lineal puede suponerse la presencia de dos poblaciones distintas de fluoroforos. Es importante remarcar que una gráfica de Stern-Volmer lineal no asegura que el proceso de quenching estudiado sea de tipo dinámico. Como se explicará a continuación, un proceso de quenching de tipo estático también genera un comportamiento lineal en las gráficas de Stern-Volmer. Debido a ello, debe recurrirse a otras medidas, que serán expuestas más adelante, para distinguir entre ambos tipos de quenching. Quenching estático. El quenching estático se produce, generalmente, como consecuencia de la formación de un complejo no fluorescente entre la molécula emisora y la molécula quencher. 63
5 M + Q M-Q La dependencia de la intensidad de fluorescencia (I F ) con la concentración de quencher puede deducirse considerando la constante de asociación (K S ): K S = [M-Q] [M]. [Q] Si el complejo M-Q no emite, la relación de intensidades I F /I F será igual a la relación de concentraciones [M] / [M], donde [M] es la concentración total del fluoróforo. [M] = [M] + [M-Q] Combinando ambas ecuaciones se obtiene: [M] - [M] [M] 1 K S = = - [M]. [Q] [M]. [Q] [Q] [M] IF = = 1 + KS [Q] [M] I F Puede apreciarse que, tal como se dijo, un proceso de quenching estático también conduce a una relación de Stern-Volmer lineal. Sin embargo, en este caso, K SV es igual a K S. 64
6 Metodología para diferenciar tipos de quenching. Existen varios métodos tendientes a distinguir entre un proceso de quenching dinámico y uno estático. Entre ellos se encuentran el estudio de la dependencia del quenching con la temperatura y la viscosidad de medio. Sin embargo, el método más conveniente para este propósito es el análisis de la dependencia de los tiempos de vida de fluorescencia con la concentración del quencher. Puede deducirse rápidamente que, si el quenching es dinámico el cociente de los tiempos de vida de fluorescencia en ausencia y presencia de quencher (τf / τf) es igual al cociente de los correspondientes rendimientos cuánticos de fluorescencia (Φ F / Φ F ). Por consiguiente, puede escribirse la siguiente ecuación para describir la dependencia de los tiempos de vida de fluorescencia con la concentración de quencher: τf τ F = 1 + k q τ F [Q] Si por el contrario, existe un quenching estático una fracción del compuesto emisor se encuentra secuestrado formando parte del complejo no emisor. Por lo tanto, la fluorescencia observada proviene del fluoróforo libre. Esta fracción no ha sido alterada, por lo que el tiempo de vida de fluorescencia que se mide es igual al tiempo de vida en ausencia del quencher (τf ). En definitiva, el cociente de tiempos de vida de fluorescencia (τ F / τ F ) no demostrará dependencia con la concentración del quencher: τ F τ F = 1 Puede apreciarse, entonces, que midiendo el tiempo de vida τ F a distintas concentraciones del quencher y luego realizando las graficas de τ F / τ F versus [Q] puede diferenciarse claramente entre un proceso de quenching de tipo dinámico y 65
7 otro estático. En el primer caso se obtendrán curvas lineales con pendientes idénticas a las constantes K SV encontradas en las gráficas de Stern-Volmer obtenidas de las medidas de intensidad de fluorescencia. En el segundo caso, se obtendrá una línea horizontal. Ambos comportamientos están representados en la Figura 6.1. Este método fue el empleado en el presente trabajo de tesis para analizar los procesos de quenching estudiados. τ F / τf m = k q. τ F quenching dinámico 1 quenching estático [Q] Figura 6.1: Representación de Stern-Volmer a partir de tiempos de vida de fluorescencia para quenching dinámico (-) y quenching estático (-). En el presente trabajo de tesis se realizaron experimentos de quenching por aniones. Muchos trabajos que se encuentran en literatura sobre pterinas se refieren a medidas de emisión de fluorescencia en presencia de solución reguladora. Por ello se decidió realizar un estudio sobre la influencia de los aniones que contienen las soluciones reguladoras, con el fin de conocer su efecto sobre las propiedades fluorescentes de las pterinas en soluciones acuosas. Los resultados de este estudio se presentan en el Capítulo 1. Los estudios de quenching de fluorescencia se realizaron con el equipo Single Photon Counting FL9CDT (Edinburgh Analytical Instruments), 66
8 detallado en el capítulo anterior. Preliminarmente se realizaron experimentos midiendo la emisión, en el espectrofotómentro Cary 3 de Varian. En este estudio previo se buscó la presencia de procesos de quenching realizando un gran número de experimentos cambiando el derivado pterínico, el quencher (anión) y su concentración y el ph. Luego se realizó un estudio sistemático midiendo los espectros de emisión y los tiempos de vida de fluorescencia en soluciones de pterinas a diferentes concentraciones de aniones. Las soluciones se prepararon a partir de soluciones madres a las que se les ajustó el ph al valor final y agua al mismo ph. Se mezcló 2 ml de la solución madre de pterina con 2 ml de una solución del anión a diferente concentración del mismo ph. Esta última solución fue preparada a partir de la solución madre del anión y agua. En todos los casos se registraron los espectros de absorción. 67
QUENCHING DE FLUORESCENCIA POR ANIONES
 Capítulo QUENCHING DE FLUORESCENCIA POR ANIONES Como se mencionó en el Capítulo 6 algunas sustancias pueden producir una disminución de la emisión fluorescente, siguiendo una comportamiento de Stern-Volmer.
Capítulo QUENCHING DE FLUORESCENCIA POR ANIONES Como se mencionó en el Capítulo 6 algunas sustancias pueden producir una disminución de la emisión fluorescente, siguiendo una comportamiento de Stern-Volmer.
PRODUCCIÓN DE OXIGENO SINGLETE
 Capítulo 11 PRODUCCIÓN DE OXIGENO SINGLETE Como se detalló en el Capítulo 2 existen muchas moléculas orgánicas que pueden actuar como sensibilizadores y producir oxígeno singlete al iluminar soluciones
Capítulo 11 PRODUCCIÓN DE OXIGENO SINGLETE Como se detalló en el Capítulo 2 existen muchas moléculas orgánicas que pueden actuar como sensibilizadores y producir oxígeno singlete al iluminar soluciones
PRACTICA 3: ESPECTROSCOPIA DE FLUORESCENCIA
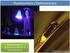 Práctica 3: Espectroscopia de Fluorescencia PRACTICA 3: ESPECTROSCOPIA DE FLUORESCENCIA Objetivos. La práctica se divide en dos partes. En la primera, se registran los espectros de absorción, fluorescencia
Práctica 3: Espectroscopia de Fluorescencia PRACTICA 3: ESPECTROSCOPIA DE FLUORESCENCIA Objetivos. La práctica se divide en dos partes. En la primera, se registran los espectros de absorción, fluorescencia
Tema 7.- Principios de fotoquímica
 Tema 7.- Principios de fotoquímica Introducción La rama de la química que estudia las transformaciones de las moléculas producidas por la absorción de energía electromagnética Muchas especies en la atmósfera
Tema 7.- Principios de fotoquímica Introducción La rama de la química que estudia las transformaciones de las moléculas producidas por la absorción de energía electromagnética Muchas especies en la atmósfera
Determinación de constantes de ionización
 Capítulo 5. Determinación de constantes de ionización Se determinaron las constantes de ionización de diversos compuestos mediante curvas de titulación ácido-base empleando métodos espectrofotométricos
Capítulo 5. Determinación de constantes de ionización Se determinaron las constantes de ionización de diversos compuestos mediante curvas de titulación ácido-base empleando métodos espectrofotométricos
DETERMINACION DEL NÚMERO DE AGREGACIÓN MEDIO DE UN SISTEMA MICELAR
 DETERMINACION DEL NÚMERO DE AGREGACIÓN MEDIO DE UN SISTEMA MICELAR OBJETIVO: Determinar el número de agregación medio del bromuro de cetiltrimetilamonio (CTAB) en disolución acuosa. INTRODUCCIÓN: Una disolución
DETERMINACION DEL NÚMERO DE AGREGACIÓN MEDIO DE UN SISTEMA MICELAR OBJETIVO: Determinar el número de agregación medio del bromuro de cetiltrimetilamonio (CTAB) en disolución acuosa. INTRODUCCIÓN: Una disolución
PRACTICA 3: ESPECTROSCOPIA DE FLUORESCENCIA
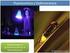 PRACTICA 3: ESPECTROSCOPIA DE FLUORESCENCIA Objetivos. La práctica se divide en dos partes. En la primera, se registran los espectros de absorción, fluorescencia y excitación de un conjunto de colorantes
PRACTICA 3: ESPECTROSCOPIA DE FLUORESCENCIA Objetivos. La práctica se divide en dos partes. En la primera, se registran los espectros de absorción, fluorescencia y excitación de un conjunto de colorantes
Fundamentos de la microscopía de fluorescencia
 Fundamentos de la microscopía de fluorescencia Andrés Esteban Cantos y Covadonga Alonso Martí Laboratorio de Interacción virus-célula Departamento de Biotecnología del INIA 1) La fluorescencia y sus propiedades
Fundamentos de la microscopía de fluorescencia Andrés Esteban Cantos y Covadonga Alonso Martí Laboratorio de Interacción virus-célula Departamento de Biotecnología del INIA 1) La fluorescencia y sus propiedades
Efectos del solvente y del entorno local sobre la fluorescencia
 Efectos del solvente y del entorno local sobre la fluorescencia C 6 C 7 Temario Efectos generales del solvente Efectos específicos del solvente Efectos de la temperatura Transferencia interna de carga
Efectos del solvente y del entorno local sobre la fluorescencia C 6 C 7 Temario Efectos generales del solvente Efectos específicos del solvente Efectos de la temperatura Transferencia interna de carga
Capítulo 9. Estudio espectrofotométrico de los equilibrios ácido-base.
 Capítulo 9. Estudio espectrofotométrico de los equilibrios ácido-base. Antes de comenzar con el desarrollo de este capítulo es necesario mencionar que el mismo no se ocupa de describir resultados de experimentos
Capítulo 9. Estudio espectrofotométrico de los equilibrios ácido-base. Antes de comenzar con el desarrollo de este capítulo es necesario mencionar que el mismo no se ocupa de describir resultados de experimentos
Presentación y objetivos
 Capítulo 1. Presentación y objetivos La absorción de radiación electromagnética por parte de una molécula puede conducir a la formación de especies electrónicamente excitadas, las cuales pueden exhibir
Capítulo 1. Presentación y objetivos La absorción de radiación electromagnética por parte de una molécula puede conducir a la formación de especies electrónicamente excitadas, las cuales pueden exhibir
Espectroscopía Clase integradora
 Espectroscopía Clase integradora Qué es la espectroscopía? La espectroscopia es el estudio de la INTERACCIÓN entre la materia y energía radiante, por ejemplo, radiación electromagnética. Busca relacionar
Espectroscopía Clase integradora Qué es la espectroscopía? La espectroscopia es el estudio de la INTERACCIÓN entre la materia y energía radiante, por ejemplo, radiación electromagnética. Busca relacionar
INTRODUCCIÓN. sensores o interruptores moleculares es fundamental en el desarrollo de nuevas técnicas de
 1 ITRODUCCIÓ En la ciencia de los materiales, el diseño de moléculas capaces de funcionar como sensores o interruptores moleculares es fundamental en el desarrollo de nuevas técnicas de análisis químico
1 ITRODUCCIÓ En la ciencia de los materiales, el diseño de moléculas capaces de funcionar como sensores o interruptores moleculares es fundamental en el desarrollo de nuevas técnicas de análisis químico
LISTA DE FIGURAS. 1 Estructura de los primeros quimiosensores fluorescentes reportados para cationes metálicos... 3
 LISTA DE FIGURAS Fig. Pág. 1 Estructura de los primeros quimiosensores fluorescentes reportados para cationes metálicos... 3 2 Representación esquemática de un quimiosensor fluorescente.. 4 3 Estructura
LISTA DE FIGURAS Fig. Pág. 1 Estructura de los primeros quimiosensores fluorescentes reportados para cationes metálicos... 3 2 Representación esquemática de un quimiosensor fluorescente.. 4 3 Estructura
-Cromatografía de permeación en gel (GPC) La cromatografía de permeación en gel se utiliza principalmente para separar moléculas en función de su tama
 Otro instrumental científico Además de las técnicas instrumentales anteriormente mostradas, el CIQSO también dispone de otros equipos que pone al servicio de la comunidad científica: -Cromatografía de
Otro instrumental científico Además de las técnicas instrumentales anteriormente mostradas, el CIQSO también dispone de otros equipos que pone al servicio de la comunidad científica: -Cromatografía de
ESPECTROSCOPIA DE FLUORESCENCIA, FOSFORESCENCIA Y QUIMIOLUMINISCENCIA MOLECULAR Q.F. ALEX SILVA ARAUJO
 FOSFORESCENCIA Y QUIMIOLUMINISCENCIA Q.F. ALEX SILVA ARAUJO GENERALIDADES Aquí se considerarán tres tipos de métodos ópticos relacionados entre sí: fluorescencia, fosforescencia y quimioluminiscencia.
FOSFORESCENCIA Y QUIMIOLUMINISCENCIA Q.F. ALEX SILVA ARAUJO GENERALIDADES Aquí se considerarán tres tipos de métodos ópticos relacionados entre sí: fluorescencia, fosforescencia y quimioluminiscencia.
TEMA 5: CINÉTICA HETEROGÉNEA. TRANSFERENCIA DE MATERIA CQA-5/1
 TEMA 5: CINÉTICA HETEROGÉNEA. TRANSFERENCIA DE MATERIA CQA-5/1 CARACTERÍSTICAS DE LAS REACCIONES HETEROGÉNEAS! Se requiere más de una fase para que la reacción transcurra del modo que lo hace.! Reacción
TEMA 5: CINÉTICA HETEROGÉNEA. TRANSFERENCIA DE MATERIA CQA-5/1 CARACTERÍSTICAS DE LAS REACCIONES HETEROGÉNEAS! Se requiere más de una fase para que la reacción transcurra del modo que lo hace.! Reacción
Espectroscopía de Absorción Molecular
 Espectroscopía de Absorción Molecular La espectroscopía consiste en el estudio cualitativo y cuantitativo de la estructura de los átomos o moléculas o de distintos procesos físicos y químicos mediante
Espectroscopía de Absorción Molecular La espectroscopía consiste en el estudio cualitativo y cuantitativo de la estructura de los átomos o moléculas o de distintos procesos físicos y químicos mediante
TEMA II: DISPERSIÓN DE LUZ
 TEMA II: DISPERSIÓN DE LUZ 1- TIPOS DE DISPERSIÓN 2- ORIGEN DE LA DISPERSIÓN 3- FACTORES DE LOS QUE DEPENDE LA DISPERSIÓN 4- MEDIDA DE LUZ DISPERSA 4A: DISPERSIÓN ESTÁTICA 4B: DISPERSIÓN DINÁMICA 5- MEDIDA
TEMA II: DISPERSIÓN DE LUZ 1- TIPOS DE DISPERSIÓN 2- ORIGEN DE LA DISPERSIÓN 3- FACTORES DE LOS QUE DEPENDE LA DISPERSIÓN 4- MEDIDA DE LUZ DISPERSA 4A: DISPERSIÓN ESTÁTICA 4B: DISPERSIÓN DINÁMICA 5- MEDIDA
6 APENDICE. A. Curvas de Calibración
 6 APENDICE A. Curvas de Calibración Las muestras colectadas en las hidrólisis contenían básicamente carbohidratos como, glucosa, xilosa y arabinosa, entre otros. Se realizaron curvas de calibración para
6 APENDICE A. Curvas de Calibración Las muestras colectadas en las hidrólisis contenían básicamente carbohidratos como, glucosa, xilosa y arabinosa, entre otros. Se realizaron curvas de calibración para
CINETICA QUIMICA. ó M s s
 CINETICA QUIMICA La Cinética Química se encarga de estudiar las características de una reacción química, con respecto a su velocidad y a sus posibles mecanismos de explicación. La velocidad de una reacción
CINETICA QUIMICA La Cinética Química se encarga de estudiar las características de una reacción química, con respecto a su velocidad y a sus posibles mecanismos de explicación. La velocidad de una reacción
Determinación de la constante de enfriamiento de un líquido.
 Determinación de la constante de enfriamiento de un líquido. Laboratorio de Física: 1210 Unidad 3 Temas de interés. 1. Medidas directa e indirectas. 2. Regresión lineal. 3. Análisis gráfico mediante cambio
Determinación de la constante de enfriamiento de un líquido. Laboratorio de Física: 1210 Unidad 3 Temas de interés. 1. Medidas directa e indirectas. 2. Regresión lineal. 3. Análisis gráfico mediante cambio
0.5. Absorbancia
 GUIA DE PROBLEMAS DE FLUORESCENCIA: 1. Se registraron espectros de emisión de fluorescencia a 2 longitudes de onda de excitación diferentes de una mezcla equimolar de 2 compuestos obteniéndose los resultados
GUIA DE PROBLEMAS DE FLUORESCENCIA: 1. Se registraron espectros de emisión de fluorescencia a 2 longitudes de onda de excitación diferentes de una mezcla equimolar de 2 compuestos obteniéndose los resultados
TRANSDUCTORES OPTOELECTRONICOS
 TRANSDUCTORES OPTOELECTRONICOS Hay dos aspectos relacionados con la luz que se utilizan, juntos o separados, para explicar muchos fenómenos relacionados con ella. Fenómenos ópticos, tales como la interferencia
TRANSDUCTORES OPTOELECTRONICOS Hay dos aspectos relacionados con la luz que se utilizan, juntos o separados, para explicar muchos fenómenos relacionados con ella. Fenómenos ópticos, tales como la interferencia
TEMA 7: CINÉTICA HETEROGÉNEA FLUIDO - SÓLIDO CQA-7/1
 TEMA 7: CINÉTICA HETEROGÉNEA FLUIDO - SÓLIDO CQA-7/1 PLANTEAMIENTO DEL MODELO CINÉTICO Reacciones heterogéneas fluido-sólido: numerosas y de gran importancia industrial: Se ponen en contacto un gas o un
TEMA 7: CINÉTICA HETEROGÉNEA FLUIDO - SÓLIDO CQA-7/1 PLANTEAMIENTO DEL MODELO CINÉTICO Reacciones heterogéneas fluido-sólido: numerosas y de gran importancia industrial: Se ponen en contacto un gas o un
QUÍMICA FÍSICA II Grupo A. Tercer control, 10 de mayo de Escoged 2 de las 3 preguntas que os propongo, cada una de las preguntas vale 5 puntos.
 QUÍMICA FÍSICA II Grupo A. Tercer control, 10 de mayo de 2011 Escoged 2 de las 3 preguntas que os propongo, cada una de las preguntas vale 5 puntos. 1. Qué significado tienen los parámetros termodinámicos
QUÍMICA FÍSICA II Grupo A. Tercer control, 10 de mayo de 2011 Escoged 2 de las 3 preguntas que os propongo, cada una de las preguntas vale 5 puntos. 1. Qué significado tienen los parámetros termodinámicos
Cinética Química. Velocidad de reacción Factores que afectan la velocidad de reacción. Basado en el material preparado por: Licda.
 Cinética Química Velocidad de reacción Factores que afectan la velocidad de reacción Basado en el material preparado por: Licda. Victoria Chan Cinética de reacción Cinética química, es el área de la química
Cinética Química Velocidad de reacción Factores que afectan la velocidad de reacción Basado en el material preparado por: Licda. Victoria Chan Cinética de reacción Cinética química, es el área de la química
N = γ net (N / V) (u av / 4) (2πrl)
 Anexo III III- Teoría de los reactores tubulares de flujo Según la teoría cinética molecular, el número de colisiones por segundo, J s, de moléculas en fase gaseosa sobre una superficie de área A s se
Anexo III III- Teoría de los reactores tubulares de flujo Según la teoría cinética molecular, el número de colisiones por segundo, J s, de moléculas en fase gaseosa sobre una superficie de área A s se
GUIA DE ESTUDIO Nº 7: Equilibrio Químico
 Página26 GUIA DE ESTUDIO Nº 7: Equilibrio Químico I.- Conceptos básicos: Equilibrio químico y constante de equilibrio. Concentraciones en el equilibrio y evolución de un sistema hacia el equilibrio. Principio
Página26 GUIA DE ESTUDIO Nº 7: Equilibrio Químico I.- Conceptos básicos: Equilibrio químico y constante de equilibrio. Concentraciones en el equilibrio y evolución de un sistema hacia el equilibrio. Principio
CONTENIDOS MÍNIMOS septiembre
 DEPARTAMENTO DE FÍSICA Y QUÍMICA CONTENIDOS MÍNIMOS septiembre CONTENIDOS MÍNIMOS curso 2015/16 1º BACHILLERATO-FÍSICA Y QUÍMICA QUÍMICA ESTRUCTURA ATÓMICA -Partículas subatómicas. -Modelo atómico de Thompson.
DEPARTAMENTO DE FÍSICA Y QUÍMICA CONTENIDOS MÍNIMOS septiembre CONTENIDOS MÍNIMOS curso 2015/16 1º BACHILLERATO-FÍSICA Y QUÍMICA QUÍMICA ESTRUCTURA ATÓMICA -Partículas subatómicas. -Modelo atómico de Thompson.
Química Biológica TP 1: ESPECTROFOTOMETRIA.
 TP 1: ESPECTROFOTOMETRIA. Introducción Al observar una solución acuosa de un colorante a trasluz, observamos una leve coloración, la cual se debe a la interacción entre las moléculas del colorante y la
TP 1: ESPECTROFOTOMETRIA. Introducción Al observar una solución acuosa de un colorante a trasluz, observamos una leve coloración, la cual se debe a la interacción entre las moléculas del colorante y la
EL MÉTODO DE JOB OBJETIVO
 EL MÉTODO DE JOB OBJETIVO Identificar las diferentes especies que se forman en solución usando el método de las variaciones continuas (Método de Job) en el sistema níquel etilendiamina. INTRODUCCIÓN En
EL MÉTODO DE JOB OBJETIVO Identificar las diferentes especies que se forman en solución usando el método de las variaciones continuas (Método de Job) en el sistema níquel etilendiamina. INTRODUCCIÓN En
Espectrometría de luminiscencia molecular Cap.15
 Espectrometría de luminiscencia molecular Cap.15 Luz cuyo origen no radica exclusivamente en las altas temperaturas Se da en sustancias que pueden absorber energía, excitándose a niveles mayores y emitirla
Espectrometría de luminiscencia molecular Cap.15 Luz cuyo origen no radica exclusivamente en las altas temperaturas Se da en sustancias que pueden absorber energía, excitándose a niveles mayores y emitirla
ESPECTROCOPIA DE RESONANCIA MAGNETICA NUCLEAR
 ESPECTROCOPIA DE RESONANCIA MAGNETICA NUCLEAR La Espectroscopía de Resonancia Magnética Nuclear (RMN) es la herramienta de determinación estructural más potente del químico orgánico. Mediante el RMN podemos
ESPECTROCOPIA DE RESONANCIA MAGNETICA NUCLEAR La Espectroscopía de Resonancia Magnética Nuclear (RMN) es la herramienta de determinación estructural más potente del químico orgánico. Mediante el RMN podemos
C. Trallero-Giner CINVESTAV-DF (2010) IV. - Dispersión Raman. Interpretación macroscópica Dinámica de la luz dispersada Sección eficaz
 Dispersión Raman en Sólidos C. Trallero-Giner CINVESTAV-DF (2010) IV. - Dispersión Raman. Interpretación macroscópica Dinámica de la luz dispersada Sección eficaz Reglas de selección Dinámica de la luz
Dispersión Raman en Sólidos C. Trallero-Giner CINVESTAV-DF (2010) IV. - Dispersión Raman. Interpretación macroscópica Dinámica de la luz dispersada Sección eficaz Reglas de selección Dinámica de la luz
Disminución de velocidad reactivos con el tiempo, véase como disminuye la pte. t (s) [Sustancia] d[sustancia] v = lim = t dt
![Disminución de velocidad reactivos con el tiempo, véase como disminuye la pte. t (s) [Sustancia] d[sustancia] v = lim = t dt Disminución de velocidad reactivos con el tiempo, véase como disminuye la pte. t (s) [Sustancia] d[sustancia] v = lim = t dt](/thumbs/55/36684723.jpg) CINÉTICA QUÍMICA QUÍMICA º BACHILLERATO 1.- Velocidad de reacción 1.1. Expresión de la velocidad de una reacción química..- Ecuación y constante de velocidad..1. Orden de reacción... Forma de determinar
CINÉTICA QUÍMICA QUÍMICA º BACHILLERATO 1.- Velocidad de reacción 1.1. Expresión de la velocidad de una reacción química..- Ecuación y constante de velocidad..1. Orden de reacción... Forma de determinar
Biopolímero s (4831)
 Biopolímero s (4831) 5.4. Factores que determinan la estructura de los ácidos nucleicos. 5.4.4 Apilamiento de bases Cuando se examinan los cristales de ácidos nucleicos helicoidales se observa que los
Biopolímero s (4831) 5.4. Factores que determinan la estructura de los ácidos nucleicos. 5.4.4 Apilamiento de bases Cuando se examinan los cristales de ácidos nucleicos helicoidales se observa que los
CAPÍTULO II. Reacciones nucleares y sus secciones eficaces 12
 CAPÍTULO II. Reacciones nucleares y sus secciones eicaces 12 En este capítulo se describen todos los tipos de reacciones que se pueden producir en el núcleo de un reactor nuclear y se muestran ejemplos
CAPÍTULO II. Reacciones nucleares y sus secciones eicaces 12 En este capítulo se describen todos los tipos de reacciones que se pueden producir en el núcleo de un reactor nuclear y se muestran ejemplos
Fluorescencia. Biología celular 2017 Dra. Melisa Monteleone
 Fluorescencia Biología celular 2017 Dra. Melisa Monteleone Para qué sirve? Visualizar partes de la célula: membrana plasmática, núcleo, vacuolas, retículo endoplásmico, etc. Estudiar procesos celulares:
Fluorescencia Biología celular 2017 Dra. Melisa Monteleone Para qué sirve? Visualizar partes de la célula: membrana plasmática, núcleo, vacuolas, retículo endoplásmico, etc. Estudiar procesos celulares:
Espectroscopía de emisión molecular
 Espectroscopía de emisión molecular 1 2 3 4 5 RELAJACION NO RADIATIVA no se emite luz, sino que el estado excitado decae a traves de mecanismos vibracionales y rotacionales CONVERSION INTERNA de un estado
Espectroscopía de emisión molecular 1 2 3 4 5 RELAJACION NO RADIATIVA no se emite luz, sino que el estado excitado decae a traves de mecanismos vibracionales y rotacionales CONVERSION INTERNA de un estado
Estados singulete y triplete
 Fluorescencia Estados singulete y triplete π* π* π* Singulete fundamental π π π Singulete excitado Triplete excitado Niveles de energía moleculares Fluoreno y bifenilo fluoreno bifenilo Fluoresceína y
Fluorescencia Estados singulete y triplete π* π* π* Singulete fundamental π π π Singulete excitado Triplete excitado Niveles de energía moleculares Fluoreno y bifenilo fluoreno bifenilo Fluoresceína y
ANÁLISIS CUANTITATIVO POR WDFRX
 ANÁLISIS CUANTITATIVO POR WDFRX El análisis cuantitativo se obtiene mediante la medida de las intensidades de las energías emitidas por la muestra. Siendo la intensidad de la emisión (número de fotones)
ANÁLISIS CUANTITATIVO POR WDFRX El análisis cuantitativo se obtiene mediante la medida de las intensidades de las energías emitidas por la muestra. Siendo la intensidad de la emisión (número de fotones)
MATERIAL 09 TEMA: ESPECTROSCOPÍA DE ABSORCION MOLECULAR EN EL ULTRAVIOLETA
 MATERIAL 09 TEMA: ESPECTROSCOPÍA DE ABSORCION MOLECULAR EN EL ULTRAVIOLETA y EL VISIBLE La espectroscopia de absorción molecular en el ultravioleta y visible se emplea en el análisis cuantitativo y es
MATERIAL 09 TEMA: ESPECTROSCOPÍA DE ABSORCION MOLECULAR EN EL ULTRAVIOLETA y EL VISIBLE La espectroscopia de absorción molecular en el ultravioleta y visible se emplea en el análisis cuantitativo y es
APÉNDICE I. Calibración de la señal cromatográfica como función de la concentración: Sistema Ternario
 APÉNDICE I Calibración de la señal cromatográfica como función de la concentración: Sistema Ternario En este apéndice se muestra la información correspondiente a la elaboración de las diferentes curvas
APÉNDICE I Calibración de la señal cromatográfica como función de la concentración: Sistema Ternario En este apéndice se muestra la información correspondiente a la elaboración de las diferentes curvas
Bloque 1. Las magnitudes físicas y su medida
 Bloque 1. Las magnitudes físicas y su medida El sistema métrico decimal El sistema internacional de unidades Conversiones de unidades con factores de conversión. Unidades compuestas Magnitudes escalares
Bloque 1. Las magnitudes físicas y su medida El sistema métrico decimal El sistema internacional de unidades Conversiones de unidades con factores de conversión. Unidades compuestas Magnitudes escalares
Resolución de los Ejercicios Propuestos (2), 2006
 Resolución de los Ejercicios Propuestos (2), 2006 Dr. L. J. Rodríguez 18 de mayo de 2006 1. Se obtuvieron los siguientes datos de transmitancia para disoluciones acuosas de oxihemoglobina (M: 66 500 g/mol)
Resolución de los Ejercicios Propuestos (2), 2006 Dr. L. J. Rodríguez 18 de mayo de 2006 1. Se obtuvieron los siguientes datos de transmitancia para disoluciones acuosas de oxihemoglobina (M: 66 500 g/mol)
(II-1) V = Flujos determinados por los controladores de flujo: (1) 1000 sccm, (2) 10 sccm, respectivamente. P (II-2)
 Anexo II II-Principio de funcionamiento del saturador Asumiendo condiciones de gas ideal, la presión parcial de un compuesto para una presión y temperaturas determinadas en el saturador es (ecuación II-1):
Anexo II II-Principio de funcionamiento del saturador Asumiendo condiciones de gas ideal, la presión parcial de un compuesto para una presión y temperaturas determinadas en el saturador es (ecuación II-1):
Cinética Química. Velocidad de Reacción
 Cinética Química Velocidad de Reacción A. Velocidad de reacción B. Naturaleza química y física de los reactivos. Perfil de una reacción química Ley de velocidad. A. Velocidad de reacción La cinética química
Cinética Química Velocidad de Reacción A. Velocidad de reacción B. Naturaleza química y física de los reactivos. Perfil de una reacción química Ley de velocidad. A. Velocidad de reacción La cinética química
Universidad Nacional de La Plata Facultad de Ciencias Astronómicas y Geofísicas. INTRODUCCIÓN a las CIENCIAS de la ATMÓSFERA
 Universidad Nacional de La Plata Facultad de Ciencias Astronómicas y Geofísicas INTRODUCCIÓN a las CIENCIAS de la ATMÓSFERA Práctica 2 : ENERGÍA, CALOR, RADIACIÓN SOLAR Y TERRESTRE. Definiciones, ecuaciones
Universidad Nacional de La Plata Facultad de Ciencias Astronómicas y Geofísicas INTRODUCCIÓN a las CIENCIAS de la ATMÓSFERA Práctica 2 : ENERGÍA, CALOR, RADIACIÓN SOLAR Y TERRESTRE. Definiciones, ecuaciones
Fluorescencia. Jaime Gómez Delfín Àgora Sant Cugat International School (Sant Cugat del Valles) 4º ESO D Curso Física i Química
 Fluorescencia Jaime Gómez Delfín Àgora Sant Cugat International School (Sant Cugat del Valles) 4º ESO D Curso 2014-2015 Física i Química ÍNDICE Apartado Página 1. Objetivo 3 2. Introducción. 4-2.1. Qué
Fluorescencia Jaime Gómez Delfín Àgora Sant Cugat International School (Sant Cugat del Valles) 4º ESO D Curso 2014-2015 Física i Química ÍNDICE Apartado Página 1. Objetivo 3 2. Introducción. 4-2.1. Qué
Departamento de Física
 Departamento de Física ------------------------------------------------------------------------------------------------------------------------ LABORATORIO DE FUNDAMENTOS FÍSICOS II Grados TIC PRÁCTICA
Departamento de Física ------------------------------------------------------------------------------------------------------------------------ LABORATORIO DE FUNDAMENTOS FÍSICOS II Grados TIC PRÁCTICA
Capítulo 5 ESPECTROSCOPÍA ELECTRÓNICA
 Capítulo 5 ESPECTROSCOPÍA ELECTRÓNICA Existen numerosas técnicas espectroscópicas que permiten estudiar los estados excitados de las moléculas orgánicas. En particular, los espectros de absorción y emisión
Capítulo 5 ESPECTROSCOPÍA ELECTRÓNICA Existen numerosas técnicas espectroscópicas que permiten estudiar los estados excitados de las moléculas orgánicas. En particular, los espectros de absorción y emisión
UNIDAD II. VARIACION DIRECTAMENTE PROPORCIONAL Y FUNCIONES LINEALES
 UNIDAD II. VARIACION DIRECTAMENTE PROPORCIONAL Y FUNCIONES LINEALES Al finalizar esta unidad: - Describirás verbalmente en que consiste el cambio y cuáles son los aspectos involucrados en él. - Identificarás
UNIDAD II. VARIACION DIRECTAMENTE PROPORCIONAL Y FUNCIONES LINEALES Al finalizar esta unidad: - Describirás verbalmente en que consiste el cambio y cuáles son los aspectos involucrados en él. - Identificarás
Cinética de reacciones. CI4102 Ingeniería Ambiental Profesor Marcelo Olivares A.
 Cinética de reacciones CI4102 Ingeniería Ambiental Profesor Marcelo Olivares A. Demanda de Oxígeno Determinar la demanda teórica de oxígeno para descomponer la glucosa (C 6 H 2 O 6 ) en dióxido de carbono
Cinética de reacciones CI4102 Ingeniería Ambiental Profesor Marcelo Olivares A. Demanda de Oxígeno Determinar la demanda teórica de oxígeno para descomponer la glucosa (C 6 H 2 O 6 ) en dióxido de carbono
CINÉTICA QUÍMICA. Química General e Inorgánica Licenciatura en Ciencias Biológicas Profesorado en Biología Analista Biológico
 Química General e Inorgánica Licenciatura en Ciencias Biológicas Profesorado en Biología Analista Biológico CINÉTICA QUÍMICA La cinética química estudia la variación de la concentración de reactantes o
Química General e Inorgánica Licenciatura en Ciencias Biológicas Profesorado en Biología Analista Biológico CINÉTICA QUÍMICA La cinética química estudia la variación de la concentración de reactantes o
ESPECTROFOTOMETRIA. BASES FISICAS
 ESPECTROFOTOMETRIA. BASES FISICAS Radiación Electromagnética y su Interacción con la Materia El principio de funcionamiento de la espectrofotometría se basa en el empleo de las interacciones entre la radiación
ESPECTROFOTOMETRIA. BASES FISICAS Radiación Electromagnética y su Interacción con la Materia El principio de funcionamiento de la espectrofotometría se basa en el empleo de las interacciones entre la radiación
UNIVERSIDAD DE PUERTO RICO EN HUMACAO DEPARTAMENTO DE QUÍMICA (http://cuhwww.upr.clu.edu/~quimgen) QUIM Módulo de Cinética
 UNIVERSIDAD DE PUERTO RICO EN HUMACAO DEPARTAMENTO DE QUÍMICA (http://cuhwww.upr.clu.edu/~quimgen) QUIM 3004 Módulo de Cinética OBJETIVOS Al finalizar este módulo usted podrá: Relacionar la rapidez con
UNIVERSIDAD DE PUERTO RICO EN HUMACAO DEPARTAMENTO DE QUÍMICA (http://cuhwww.upr.clu.edu/~quimgen) QUIM 3004 Módulo de Cinética OBJETIVOS Al finalizar este módulo usted podrá: Relacionar la rapidez con
Tema 4: La Estratosfera
 4.1 Fotoquímica del O 2 y del O. Mecanismo de Chapman Tema 4: La Estratosfera El oxígeno molecular se fotodisocia por absorción de radiación ultravioleta de pequeña longitud de onda (UV-C): O 2 + h ν O
4.1 Fotoquímica del O 2 y del O. Mecanismo de Chapman Tema 4: La Estratosfera El oxígeno molecular se fotodisocia por absorción de radiación ultravioleta de pequeña longitud de onda (UV-C): O 2 + h ν O
SESIÓN 13 EQUILIBRIO QUÍMICO EN FASE GASEOSA
 I. CONTENIDOS: 1. Leyes de los gases. 2. Presión y temperatura. 3. Principio de Le Chatelier. 4. Constante de equilibrio. SESIÓN 13 EQUILIBRIO QUÍMICO EN FASE GASEOSA II. OBJETIVOS: Al término de la Sesión,
I. CONTENIDOS: 1. Leyes de los gases. 2. Presión y temperatura. 3. Principio de Le Chatelier. 4. Constante de equilibrio. SESIÓN 13 EQUILIBRIO QUÍMICO EN FASE GASEOSA II. OBJETIVOS: Al término de la Sesión,
Ecuaciones diferenciales ordinarias
 Tema 9 Ecuaciones diferenciales ordinarias Versión: 13 de mayo de 29 9.1 Introducción El objetivo de este tema es exponer muy brevemente algunos de los conceptos básicos relacionados con las ecuaciones
Tema 9 Ecuaciones diferenciales ordinarias Versión: 13 de mayo de 29 9.1 Introducción El objetivo de este tema es exponer muy brevemente algunos de los conceptos básicos relacionados con las ecuaciones
Puntos de ebullición.
 1.-Indica el tipo de enlace de los siguientes hidruros. Ayundándote de la siguiente tabla comenta la polaridad de los enlaces. Hidruro % carácter iónico HF 43 HCl 17 HBr 11 HI 6 Representa gráficamente
1.-Indica el tipo de enlace de los siguientes hidruros. Ayundándote de la siguiente tabla comenta la polaridad de los enlaces. Hidruro % carácter iónico HF 43 HCl 17 HBr 11 HI 6 Representa gráficamente
INTERACCION DE LAS RADIACIONES ELECTROMAGNETICAS CON LA MATERIA
 NTERACCON DE LAS RADACONES ELECTROMAGNETCAS CON LA MATERA B.C. Paola Audicio Asistente de Radiofarmacia, CN Radiación ionizante: ionización del material atravesado M M + + e - excitación de las estructuras
NTERACCON DE LAS RADACONES ELECTROMAGNETCAS CON LA MATERA B.C. Paola Audicio Asistente de Radiofarmacia, CN Radiación ionizante: ionización del material atravesado M M + + e - excitación de las estructuras
La ley de desplazamiento de Wien (Premio Nobel 1911):
 Trabajo de laboratorio Nro 1: Verificación de la ley de Stefan Boltzmann y determinación de la constante de Planck mediante el análisis de la radiación del cuerpo negro Introducción Toda superficie cuya
Trabajo de laboratorio Nro 1: Verificación de la ley de Stefan Boltzmann y determinación de la constante de Planck mediante el análisis de la radiación del cuerpo negro Introducción Toda superficie cuya
Transferencia de masa en la interfase
 INSTITUTO TECNOLÓGICO DE DURANGO Transferencia de masa en la interfase Dr. Carlos Francisco Cruz Fierro Revisión 2 65259.63 10-dic-11 6.1 EQUILIBRIO QUÍMICO 2 Sistema en Equilibrio Un sistema está en equilibrio
INSTITUTO TECNOLÓGICO DE DURANGO Transferencia de masa en la interfase Dr. Carlos Francisco Cruz Fierro Revisión 2 65259.63 10-dic-11 6.1 EQUILIBRIO QUÍMICO 2 Sistema en Equilibrio Un sistema está en equilibrio
EQUILIBRIO LÍQUIDO-VAPOR PRESIÓN DE VAPOR Y ENTALPÍA DE VAPORIZACIÓN DEL AGUA
 EQUILIBRIO LÍQUIDO-VAPOR PRESIÓN DE VAPOR Y ENTALPÍA DE VAPORIZACIÓN DEL AGUA I. OBJETIVO GENERAL Comprender e interpretar el significado de las variables termodinámicas involucradas en la ecuación de
EQUILIBRIO LÍQUIDO-VAPOR PRESIÓN DE VAPOR Y ENTALPÍA DE VAPORIZACIÓN DEL AGUA I. OBJETIVO GENERAL Comprender e interpretar el significado de las variables termodinámicas involucradas en la ecuación de
Velocidad es la variación de la concentración de una de las sustancias de la reacción con el tiempo. Su unidad es: mol L 1 s 1.
 Cinética es el estudio de la velocidad a la que tienen lugar las reacciones químicas. Los resultados sólo pueden obtenerse por vía experimental y de ellos puede predecirse el camino por el que transcurren
Cinética es el estudio de la velocidad a la que tienen lugar las reacciones químicas. Los resultados sólo pueden obtenerse por vía experimental y de ellos puede predecirse el camino por el que transcurren
CAPÍTULO VI TRANSPORTE DE ENERGÍA POR RADIACIÓN
 CAPÍTULO VI TRANSPORTE DE ENERGÍA POR RADIACIÓN 6.1 El espectro de radiación electromagnética El transporte de energía por conducción y convección necesitan la existencia de un medio material. La conducción
CAPÍTULO VI TRANSPORTE DE ENERGÍA POR RADIACIÓN 6.1 El espectro de radiación electromagnética El transporte de energía por conducción y convección necesitan la existencia de un medio material. La conducción
Procesos estocásticos. Definición
 Procesos estocásticos Definición http://humberto-r-alvarez-a.webs.com Definición de proceso estocástico Estudio del comportamiento de una variable aleatoria a lo largo del tiempo El ajuste de cualquier
Procesos estocásticos Definición http://humberto-r-alvarez-a.webs.com Definición de proceso estocástico Estudio del comportamiento de una variable aleatoria a lo largo del tiempo El ajuste de cualquier
Al hacer clic en el vínculo al simulador, en tu navegador se abre la hoja del programa, con una interface como la de la figura siguiente:
 Taller de Modelado de Cinética Enzimática Emplearas el programa de simulación de cinética enzimática que se encuentra en el sitio: (htpp://www.kscience.co.uk/-animations/model.swf) para realiza los ejercicios
Taller de Modelado de Cinética Enzimática Emplearas el programa de simulación de cinética enzimática que se encuentra en el sitio: (htpp://www.kscience.co.uk/-animations/model.swf) para realiza los ejercicios
Capítulo 24. Emisión y absorción de la luz. Láser
 Capítulo 24 Emisión y absorción de la luz. Láser 1 Absorción y emisión La frecuencia luminosa depende de los niveles atómicos entre los que se produce la transición electrónica a través de: hν = E f E
Capítulo 24 Emisión y absorción de la luz. Láser 1 Absorción y emisión La frecuencia luminosa depende de los niveles atómicos entre los que se produce la transición electrónica a través de: hν = E f E
Tema 4: Cinética química
 Tema 4: Cinética química Velocidad de reacción. Velocidad media e instantánea. Ecuación de velocidad. Obtención de la ecuación de velocidad: método de las concentraciones iniciales. Ecuaciones de velocidad
Tema 4: Cinética química Velocidad de reacción. Velocidad media e instantánea. Ecuación de velocidad. Obtención de la ecuación de velocidad: método de las concentraciones iniciales. Ecuaciones de velocidad
Teniendo en cuenta que si el voltaje se mide en Volts y la corriente en Amperes las unidades de resistencia resultan ser
 Ley de Ohm La resistencia eléctrica de un resistor se define como la razón entre la caída de tensión, entre los extremos del resistor, y la corriente que circula por éste, tal que Teniendo en cuenta que
Ley de Ohm La resistencia eléctrica de un resistor se define como la razón entre la caída de tensión, entre los extremos del resistor, y la corriente que circula por éste, tal que Teniendo en cuenta que
Tema 3.-Espectroscopía de biomoléculas
 Tema 3.-Espectroscopía de biomoléculas Tema 3.-Espectroscopía de biomoléculas 3.1.-El espectro electromagnético 3.2.-Espectros de absorción y de emisión (espontánea y estimulada) 3.2.1.-Momento dipolar
Tema 3.-Espectroscopía de biomoléculas Tema 3.-Espectroscopía de biomoléculas 3.1.-El espectro electromagnético 3.2.-Espectros de absorción y de emisión (espontánea y estimulada) 3.2.1.-Momento dipolar
1 EL OSCILADOR ARMONICO
 1 EL OSCILADOR ARMONICO 1.1 Autofunciones y Autovalores El potencial del oscilador armónico en una dimensión corresponde a la siguiente expresión matemática: V = 1 kx (1) donde k es la constante de la
1 EL OSCILADOR ARMONICO 1.1 Autofunciones y Autovalores El potencial del oscilador armónico en una dimensión corresponde a la siguiente expresión matemática: V = 1 kx (1) donde k es la constante de la
INTRODUCCIÓN GENERAL Y OBJETIVOS
 Capítulo 1 INTRODUCCIÓN GENERAL Y OBJETIVOS La luz tiene un papel fundamental sobre los seres vivos. La energía de la radiación ultravioleta y visible del sol da lugar a fenómenos que permiten la continuidad
Capítulo 1 INTRODUCCIÓN GENERAL Y OBJETIVOS La luz tiene un papel fundamental sobre los seres vivos. La energía de la radiación ultravioleta y visible del sol da lugar a fenómenos que permiten la continuidad
TÉCNICAS BASADAS EN LA ABSORCIÓN DE RADIACIÓN
 TÉCNICAS BASADAS EN LA ABSORCIÓN DE RADIACIÓN Absorción de radiación y concentración. Ley de Beer. La espectroscopia de absorción molecular se basa en la medida de la transmitancia T o de la absorbancia
TÉCNICAS BASADAS EN LA ABSORCIÓN DE RADIACIÓN Absorción de radiación y concentración. Ley de Beer. La espectroscopia de absorción molecular se basa en la medida de la transmitancia T o de la absorbancia
TEMA 3: CINÉTICA DE REACCIONES COMPLEJAS
 TEMA 3: CINÉTICA DE REACCIONES COMPLEJAS Entre todas las reacciones que se han estudiado cinéticamente en fase gaseosa, la proporción en que se dan reacciones elementales o sencillas es muy pequeña. La
TEMA 3: CINÉTICA DE REACCIONES COMPLEJAS Entre todas las reacciones que se han estudiado cinéticamente en fase gaseosa, la proporción en que se dan reacciones elementales o sencillas es muy pequeña. La
I. Análisis gráfico de un experimento físico
 I. Análisis gráfico de un experimento físico Objetivos 1) Aprender a identificar las variables que intervienen en un experimento físico 2) Aprender a elaborar correctamente gráficas en papel milimetrado
I. Análisis gráfico de un experimento físico Objetivos 1) Aprender a identificar las variables que intervienen en un experimento físico 2) Aprender a elaborar correctamente gráficas en papel milimetrado
Tema 3.-Espectroscopía de biomoléculas
 Tema 3.Espectroscopía de biomoléculas Tema 3.Espectroscopía de biomoléculas 3..El espectro electromagnético 3.2.Espectros de absorción y de emisión (espontánea y estimulada) 3.2..Momento dipolar de transición:
Tema 3.Espectroscopía de biomoléculas Tema 3.Espectroscopía de biomoléculas 3..El espectro electromagnético 3.2.Espectros de absorción y de emisión (espontánea y estimulada) 3.2..Momento dipolar de transición:
ESTRUCTURA DEL SEMINARIO:
 ESTRUCTURA DEL SEMINARIO: S1.1. Introducción a la espectrofotometría 1 S1.2. Radiación electromagnética 1 S1.3. Espectroscopía ultravioleta/visible 2 S1.4. Colorimetría 5 S1.1. Introducción a la espectrofotometría
ESTRUCTURA DEL SEMINARIO: S1.1. Introducción a la espectrofotometría 1 S1.2. Radiación electromagnética 1 S1.3. Espectroscopía ultravioleta/visible 2 S1.4. Colorimetría 5 S1.1. Introducción a la espectrofotometría
III. CONCEPTOS TEORICOS
 III. CONCEPTOS TEORICOS Los conceptos que se presentan en este capitulo son términos que permitirán entender mejor este trabajo de tesis. Asimismo en el anexo N G se muestra el Diagrama de Procesos de
III. CONCEPTOS TEORICOS Los conceptos que se presentan en este capitulo son términos que permitirán entender mejor este trabajo de tesis. Asimismo en el anexo N G se muestra el Diagrama de Procesos de
2. Distancia entre dos puntos. Punto medio de un segmento
 Geometría 1 Geometría anaĺıtica Una ecuación de primer grado con dos incógnitas x e y tiene infinitas soluciones Por ejemplo x + y = 3 tiene como soluciones (0, 3), (1, ), ( 1, 4), etc Hasta ahora se han
Geometría 1 Geometría anaĺıtica Una ecuación de primer grado con dos incógnitas x e y tiene infinitas soluciones Por ejemplo x + y = 3 tiene como soluciones (0, 3), (1, ), ( 1, 4), etc Hasta ahora se han
Teniendo en cuenta que si el voltaje se mide en Volts y la corriente en Amperes las unidades de resistencia resultan ser
 Ley de Ohm La resistencia se define como la razón entre la caída de tensión, entre los dos extremos de una resistencia, y la corriente que circula por ésta, tal que 1 Teniendo en cuenta que si el voltaje
Ley de Ohm La resistencia se define como la razón entre la caída de tensión, entre los dos extremos de una resistencia, y la corriente que circula por ésta, tal que 1 Teniendo en cuenta que si el voltaje
CÁTEDRA: QUIMICA GUIA DE PROBLEMAS Nº 7
 CÁTEDRA: QUIMICA GUIA DE PROBLEMAS Nº 7 TEMA: CINÉTICA QUÍMICA OBJETIVOS: Aplicar los conceptos teóricos de las velocidades de las reacciones químicas y de los factores de los que dependen dichas velocidades
CÁTEDRA: QUIMICA GUIA DE PROBLEMAS Nº 7 TEMA: CINÉTICA QUÍMICA OBJETIVOS: Aplicar los conceptos teóricos de las velocidades de las reacciones químicas y de los factores de los que dependen dichas velocidades
EFECTO SOLVENTE. Los espectros de emisión de algunos fluoróforos son muy sensibles al ambiente circundante, incluyendo al solvente
 EFECTO SOLVENTE EFECTO SOLVENTE Los espectros de emisión de algunos fluoróforos son muy sensibles al ambiente circundante, incluyendo al solvente A partir de los espectros de emisión de estos fluoróforos
EFECTO SOLVENTE EFECTO SOLVENTE Los espectros de emisión de algunos fluoróforos son muy sensibles al ambiente circundante, incluyendo al solvente A partir de los espectros de emisión de estos fluoróforos
PROBLEMARIO DE QUÍMICA ANALÍTICA II. Espectrometría UV-Visible
 UNIVERSIDAD DEL ZULIA FACULTAD EXPERIMENTAL DE CIENCIAS DEPARTAMENT DE QUIMICA UNIDAD ACADÉMICA DE QUÍMICA ANALÍTICA MATERIA: QUÍMICA ANALÍTICA II PRBLEMARI DE QUÍMICA ANALÍTICA II Espectrometría UV-Visible
UNIVERSIDAD DEL ZULIA FACULTAD EXPERIMENTAL DE CIENCIAS DEPARTAMENT DE QUIMICA UNIDAD ACADÉMICA DE QUÍMICA ANALÍTICA MATERIA: QUÍMICA ANALÍTICA II PRBLEMARI DE QUÍMICA ANALÍTICA II Espectrometría UV-Visible
CINÉTICA QUÍMICA. También deberemos tener en cuenta los coeficientes estequiométricos.
 CINETICA CINÉTICA QUÍMICA Estudia la velocidad con la que tienen lugar las reacciones, los factores que influyen en ella y el mecanismo mediante el que se lleva a cabo. VELOCIDAD DE REACCIÓN Cuando se
CINETICA CINÉTICA QUÍMICA Estudia la velocidad con la que tienen lugar las reacciones, los factores que influyen en ella y el mecanismo mediante el que se lleva a cabo. VELOCIDAD DE REACCIÓN Cuando se
1.1 Sustancias húmicas
 Abreviaturas y Símbolos 5 Introducción 7 Capítulo 1: Antecedentes y Objetivos 12 1.1 Sustancias húmicas 1.2 Seguimiento del proceso de compostaje mediante diferentes técnicas 1.3 Experiencias de láser
Abreviaturas y Símbolos 5 Introducción 7 Capítulo 1: Antecedentes y Objetivos 12 1.1 Sustancias húmicas 1.2 Seguimiento del proceso de compostaje mediante diferentes técnicas 1.3 Experiencias de láser
GRAFICAS LINEALES REGLAS GENERALES PARA LA CONSTRUCCIÓN DE GRÁFICAS
 GRAFICAS LINEALES OBJETIVOS 1. Realizar linealización de gráficos por el método de cambios de variables. 2. Obtener experimentalmente la relación matemática, más adecuada, entre dos cantidades o magnitudes
GRAFICAS LINEALES OBJETIVOS 1. Realizar linealización de gráficos por el método de cambios de variables. 2. Obtener experimentalmente la relación matemática, más adecuada, entre dos cantidades o magnitudes
Velocidad: aplicación física
 Cinética Química Velocidad: aplicación física Cinética Química: aplicación a las reacciones QUIMICAS del concepto de Velocidad Reacción Química rápida. Reacción Química lenta. Cinética Química Estudio
Cinética Química Velocidad: aplicación física Cinética Química: aplicación a las reacciones QUIMICAS del concepto de Velocidad Reacción Química rápida. Reacción Química lenta. Cinética Química Estudio
Repaso de Reacciones no elementales y mecanismos de reacción
 Repaso de Reacciones no elementales y mecanismos de reacción C A R O L I N A M O N T E R O C, P H D U N I D A D D E T I T U L A C I O N E S P E C I A L F A C U L T A D D E I N G E N I E R I A Q U I M I
Repaso de Reacciones no elementales y mecanismos de reacción C A R O L I N A M O N T E R O C, P H D U N I D A D D E T I T U L A C I O N E S P E C I A L F A C U L T A D D E I N G E N I E R I A Q U I M I
Cuestiones de Bioquímica
 1º de Química, gr. D http://www.uv.es/bbm Tema 4 Cuestiones de Bioquímica 1) Una reacción enzimática puede escribirse como dos reacciones sucesivas, donde el complejo ES es el intermediario en la conversión
1º de Química, gr. D http://www.uv.es/bbm Tema 4 Cuestiones de Bioquímica 1) Una reacción enzimática puede escribirse como dos reacciones sucesivas, donde el complejo ES es el intermediario en la conversión
UNIVERSIDAD CENTRAL DEL ECUADOR FACULTAD DE CIENCIAS QUÍMICAS ESPECTROSCOPÍA ORBITALES ATÓMICOS
 UNIVERSIDAD CENTRAL DEL ECUADOR FACULTAD DE CIENCIAS QUÍMICAS ESPECTROSCOPÍA NOMBRES: Carpio Diana (clínicos) Gallegos Mayra (clínicos) PARALELO: jueves de 10 a 12 DEFINICIÓN DE ORBITAL ATÓMICO ORBITALES
UNIVERSIDAD CENTRAL DEL ECUADOR FACULTAD DE CIENCIAS QUÍMICAS ESPECTROSCOPÍA NOMBRES: Carpio Diana (clínicos) Gallegos Mayra (clínicos) PARALELO: jueves de 10 a 12 DEFINICIÓN DE ORBITAL ATÓMICO ORBITALES
Equilibrio de fuerzas Σ F z = 0. Σ M y = 0 Σ M x = 0 Σ M z = 0. Equilibrio de momentos. Segunda ley de Newton (masa)
 Estática: leyes de Newton: equilibrio, masa, acción y reacción Primera ley de Newton (equilibrio) Un cuerpo permanece en reposo o en movimiento rectilíneo uniforme (M.R.U. = velocidad constante) si la
Estática: leyes de Newton: equilibrio, masa, acción y reacción Primera ley de Newton (equilibrio) Un cuerpo permanece en reposo o en movimiento rectilíneo uniforme (M.R.U. = velocidad constante) si la
TEMA 4: CINÉTICA HOMOGÉNEA: REACCIONES MÚLTIPLES Y CATALIZADAS CQA-4/1
 TEMA 4: CINÉTICA HOMOGÉNEA: REACCIONES MÚLTIPLES Y CATALIZADAS CQA-4/1 CINÉTICA DE REACCIONES MÚLTIPLES Reacciones múltiples : Reacciones con más de una ecuación cinética que describe su comportamiento.
TEMA 4: CINÉTICA HOMOGÉNEA: REACCIONES MÚLTIPLES Y CATALIZADAS CQA-4/1 CINÉTICA DE REACCIONES MÚLTIPLES Reacciones múltiples : Reacciones con más de una ecuación cinética que describe su comportamiento.
Radiaciones Ionizantes: Utilización y Riesgos RIUR. Guía de estudio
 Radiaciones Ionizantes: Utilización y Riesgos RIUR . Estructura y radiaciones atómicas Esta guía describe el conjunto de actividades que forman el tema 2 del módulo 1: " Estructura y radiaciones atómicas"
Radiaciones Ionizantes: Utilización y Riesgos RIUR . Estructura y radiaciones atómicas Esta guía describe el conjunto de actividades que forman el tema 2 del módulo 1: " Estructura y radiaciones atómicas"
QUÍMICA. [ΔH afinidad Cl(g)] = -349 kj mol -1 (0,25 puntos) K + (g) + Cl - (g)
![QUÍMICA. [ΔH afinidad Cl(g)] = -349 kj mol -1 (0,25 puntos) K + (g) + Cl - (g) QUÍMICA. [ΔH afinidad Cl(g)] = -349 kj mol -1 (0,25 puntos) K + (g) + Cl - (g)](/thumbs/49/25837773.jpg) OPCIÓN A QUÍMICA. 1. (2,5 puntos) Construya el ciclo de Born-aber y calcule la energía de red (Δ red ) del KCl(s) a partir de los siguientes datos: Entalpía estándar de formación del KCl(s) [Δ f (KCl)]
OPCIÓN A QUÍMICA. 1. (2,5 puntos) Construya el ciclo de Born-aber y calcule la energía de red (Δ red ) del KCl(s) a partir de los siguientes datos: Entalpía estándar de formación del KCl(s) [Δ f (KCl)]
RADIACIÓN ELECTROMAGNÉTICA
 FACULTAD DE CIENCIAS QUÍMICAS Espectrometría Objeto de Estudio Nº 1 LECTURA N 1 RADIACIÓN ELECTROMAGNÉTICA Bibliografía: SKOOG, D.A.; Leary J.J.; ANÁLISIS INSTRUMENTAL, 4 ed.; Ed. McGraw-Hill (1994), págs.
FACULTAD DE CIENCIAS QUÍMICAS Espectrometría Objeto de Estudio Nº 1 LECTURA N 1 RADIACIÓN ELECTROMAGNÉTICA Bibliografía: SKOOG, D.A.; Leary J.J.; ANÁLISIS INSTRUMENTAL, 4 ed.; Ed. McGraw-Hill (1994), págs.
Introducción. Concepto de oxidación y reducción Reacciones Ácido base v/s reacciones REDOX. Reacciones de Oxidación y reducción. Oxidación: básica.
 Reacciones de Oxidación y reducción Introducción Las reacciones de oxidoreducción son aquellas en las que existe una transferencia de electrones o un cambio en los estados de oxidación de las sustancias
Reacciones de Oxidación y reducción Introducción Las reacciones de oxidoreducción son aquellas en las que existe una transferencia de electrones o un cambio en los estados de oxidación de las sustancias
Reacciones de Oxidación y reducción
 Reacciones de Oxidación y reducción Introducción Las reacciones de oxidoreducción son aquellas en las que existe una transferencia de electrones o un cambio en los estados de oxidación de las sustancias
Reacciones de Oxidación y reducción Introducción Las reacciones de oxidoreducción son aquellas en las que existe una transferencia de electrones o un cambio en los estados de oxidación de las sustancias
