(Leyes y Decreto Reglamentario 1089 / 2012)
|
|
|
- Lucas Farías Río
- hace 7 años
- Vistas:
Transcripción
1 CONSENTIMIENTO INFORMADO PARA LA INYECCIÓN DE UN DISPOSITIVO INTRAVÍTREO DE LIBERACIÓN DE CORTICOIDE EN EL EDEMA MACULAR SECUNDARIO A UNA OCLUSIÓN DE RAMA VENOSA DE LA RETINA. ( OZURDEX - DEXAMETASONA-) (Leyes y Decreto Reglamentario 1089 / 2012) Nota: El diseño y contenido de este consentimiento, evaluado y aprobado por el Consejo Argentino de Oftalmología, es autoría del Prof. Dr. Roberto Borrone. Su texto original no debe ser modificado. DERECHO A NO RECIBIR INFORMACIÓN SANITARIA Ejerzo mi derecho a no recibir información sanitaria vinculada a mi patología ocular, los procedimientos diagnósticos relacionados ni los tratamientos planificados. Firma del paciente DNI Firma del profesional DNI Autorizo a disponer de la información sanitaria vinculada a mi patología ocular y a decidir sobre mi tratamiento a DNI Firma del paciente DNI Firma del representante legal DNI 1) Constancia de recepción del formulario En el día de la fecha,, recibí de mi oftalmólogo, Dr., este formulario que contiene información sobre mi enfermedad ocular, el tratamiento que me ha propuesto, sus riesgos y las posibilidades alternativas terapéuticas que tengo a mi disponibilidad. Luego de leer en mi casa detenidamente con mis familiares esta información, he sido citado el día para que el oftalmólogo aclare todas mis dudas. 2) Qué es el edema macular secundario a una oclusión de rama venosa de la retina? La retina es la membrana sensible que tapiza por dentro la pared posterior del ojo como si fuera el empapelado de una habitación. En ella hay células fotorreceptoras (conos y bastones) que reciben la luz y la convierten en una señal eléctrica que es transportada hacia el cerebro por intermedio del nervio óptico. La retina tiene una gran actividad metabólica y por ello necesita un aporte importante de oxígeno que le llega por sus vasos y capilares sanguíneos. La sangre oxigenada llega a las capas internas de la retina por intermedio de la arteria central de la retina: Esta vaso sanguíneo se subdivide en múltiples pequeñas arterias que terminan en diminutos capilares. A ese nivel, el oxígeno pasa desde la sangre hacia las células de la retina. Los capilares se continúan con las venas. La sangre 1
2 abandona la retina por medio de ramas venosas que desembocan en una vena mayor denominada Vena Central de la Retina. Cuando se obstruye una de aquéllas ramas venosas hablamos de OCLUSIÓN DE RAMA VENOSA DE LA RETINA. Al detenerse parcial ó totalmente el retorno de la sangre venosa (que viene de la retina y se dirige al sistema venoso mayor por fuera del ojo), se altera la nutrición de la retina. No llega la necesaria cantidad de oxígeno y a esta situación la llamamos ISQUEMIA. Como el requerimiento de oxígeno por parte de la retina es muy alto, debido a su gran actividad metabólica, rápidamente las células de la retina isquémica sintetizan una sustancia llamada FACTOR DE CRECIMIENTO VASCULAR ENDOTELIAL (VEGF por sus siglas en inglés). Esta sustancia crea nuevos vasos sanguíneos denominados NEOVASOS (a este proceso lo llamamos angiogénesis) para tratar de transportar sangre oxigenada a la retina, pero, estos neovasos tiene paredes muy frágiles pudiendo generar hemorragias y también puede tironear la retina provocando un desprendimiento de retina. Además, este factor VEGF provoca un aumento importante en la permeabilidad de los pequeños vasos sanguíneos de la retina (capilares). El resultado es lo que denominamos EDEMA. Esto significa que pasa líquido desde los vasos sanguíneos hacia los tejidos provocando un engrosamiento de la retina, es decir un aumento de su espesor. Cuando este edema afecta la parte central de la retina (denominada MÁCULA) se produce un EDEMA MACULAR. En esta situación dejan de funcionar las células fotorreceptoras de la mácula (los conos) y esto provoca una gran disminución de la agudeza visual. En síntesis, la OCLUSIÓN VENOSA DE RAMA DE LA RETINA puede provocar el EDEMA MACULAR al aumentar la presión dentro de los capilares por la dificultad en el retorno venoso y, paralelamente por la producción del factor VEGF. Además, como ya fue explicado, el factor VEGF puede generar neovasos. Las oclusiones de rama venosa se clasifican en isquémicas y no isquémicas, de acuerdo a la superficie de la retina que quedó sin el aporte necesario de oxígeno. Cuando la superficie de retina isquémica es importante y se detecta el inicio de crecimiento de neovasos, está indicado el tratamiento con fotocoagulación láser. En cuanto a las causas que generar una oclusión venosa de la retina, los factores de riesgo conocidos mas frecuentes son: la hipertensión arterial; hiperlipidemias; la Diabetes; la edad (mas frecuente en mayores de 55 años) ; el glaucoma; la hiperhomocistinemia y todos los cuadros en lo que existe una hipercoagulabilidad de la sangre: policitemia, síndrome antifosfolípido, resistencia a la Proteína C activada; déficit de Proteína C, mutación del gen de protrombina; déficit del factor XII; cuadros de periflebitis oclusivas (enfermedad de Behcet, Sacrcoidosis), etc. Los corticoides como la dexametasona (droga contenida en el dispositivo Ozurdex ) son drogas que logran impedir que el factor de crecimiento vascular endotelial (VEGF) se genere y pueda actuar y además bloquean otras sustancias que intervienen en los procesos inflamatorios (citoquinas y prostaglandinas) También mejoran la hermeticidad de la unión entre las células que forman la pared de los vasos sanguíneos para que actúen como una barrera que impida el escape de líquido hacia la retina. 3) En qué consiste el tratamiento del edema macular secundario a una oclusión de rama venosa de la retina mediante el implante de un dispositivo de liberación de corticoide dentro de la cavidad vítrea ( Ozurdex )? La dexametasona es el corticoide ubicado dentro del dispositivo de liberación lenta biodegradable ( Ozurdex 0.7 mg).- El dispositivo mide 0,46 mm de diámetro y 6 mm de longitud. El dispositivo de liberación de dexametasona ( Ozurdex ) se inyecta en el interior del ojo, en una cámara ubicada en la parte posterior del ojo, delante de la retina, denominada cámara vítrea (ocupada por una gelatina llamada humor o cuerpo vítreo). 2
3 Este procedimiento se efectúa bajo estrictas condiciones de asepsia, equivalentes a las de una cirugía ocular. Se realiza con anestesia local y en forma ambulatoria. El dispositivo es ubicado dentro de la cámara vítrea mediante un inyector provisto en una unidad sellada. El cirujano realiza la inyección a través de la pared blanca del ojo (esclera), realizando una delicada punción autosellante. El dispositivo puede liberar el corticoide (dexametasona) durante un período de hasta 6 meses. El médico oftalmólogo tratante decidirá, de acuerdo a la evolución (agudeza visual y espesor de la macula) si es necesario realizar nuevas inyecciones del dispositivo intravítreo ( Ozurdex ). 4) Beneficio que se espera conseguir con el implante de liberación de corticoide en la cámara vítrea del ojo ( Ozurdex ) en pacientes con edema macular secundario a una oclusión de rama venosa de la retina: El beneficio que se espera conseguir es mejorar la visión mediante la reducción del edema macular. El resultado se mide por la cantidad de letras ganadas es decir cuantas letras pueden leer los pacientes luego de la inyección (y que antes de la inyección no leían), en un cartel de prueba de la visión que tiene 5 letras por renglón. (Cartel ETDRS). En uno de los estudios realizados, la mejor visión corregida (con la corrección óptica que cada paciente requiera) a los 6 meses de realizada la inyección del implante intravítreo de dexametasona ( Ozurdex ) significó una ganancia de 15 letras o mas en el 37.3 % de los pacientes respecto a la visión que tenían antes del tratamiento.- Es frecuente que parte de la mejoría de la agudeza visual se pierda y sea necesario repetir la inyección del dispositivo intravítreo. 5) RIESGOS QUE PODRÍA GENERAR EL PROCEDIMIENTO DE IMPLANTE INTRAVÍTREO DE UN DISPOSITIVO DE LIBERACIÓN DE CORTICOIDE ( Ozurdex Dexametasona-) Un concepto importante: todo procedimiento intraocular tiene graves riesgos visuales potenciales. El riesgo más grave es la pérdida definitiva de la visión del ojo en el que se efectúa el implante intravítreo. Esto sería excepcional pero no es imposible. Algunas de las más frecuentes y/o más graves complicaciones posibles son: A. Ojo rojo por hemorragia subconjuntival (hemorragia en la pared blanca del ojo). Se reportó en el 20 % de los casos y se resuelve espontáneamente. B. Visión borrosa. Es en general temporario. Es recomendable evitar la conducción de vehículos inmediatamente después del procedimiento.- C. Inflamación interna del ojo no infecciosa. D. Aumento de la presión ocular (glaucoma cortisónico). Se lo ha reportado en el 25 % luego de un procedimiento, pero en los casos que requirieron tres procedimientos se eleva al 40 %. En este tipo de glaucoma la presión ocular se controla habitualmente con medicación local (gotas). Sólo algunos pacientes requerirán una intervención quirúrgica para controlar la presión ocular. E. Partículas flotando en el campo visual o flotadores vítreos. El paciente percibe puntos negros, filamentos negros o una nube flotando en el campo visual. Generalmente es transitorio pero puede ser definitivo. Fue reportado en el 1 % de los casos. F. Lagrimeo. Reportado en el 1,7 % de los casos. G. Migración (desplazamiento) del implante dentro del ojo. H. Hipotonía del ojo. I. Hemorragia intraocular. Puede resolverse espontáneamente pero ciertos casos pueden requerir una cirugía ocular invasiva denominado vitrectomía. 3
4 Los casos más severos pueden generar un desprendimiento de retina con la posibilidad de pérdida definitiva de la visión. J. Desgarro en la retina K. Oclusión de una vena de la retina. (Reportado en el 1 % de los casos) L. Desprendimiento de retina. Requiere una o más intervenciones quirúrgicas con el riesgo infrecuente de pérdida de la visión. M. Endoftalmitis (infección interna del ojo). En ciertos casos puede evolucionar hacia la perdida de visión del ojo a pesar de un oportuno y correcto tratamiento. Una endoftalmitis puede ocurrir en cirugías perfectamente realizadas por los oftalmólogos más expertos. Aún cumpliendo con las más estrictas medidas de bioseguridad (asepsia) es imposible la prevención de una endoftalmitis con un 100% de seguridad. En prácticamente todos los casos el germen que la causa está en los tejidos vecinos al ojo del propio paciente. Es sumamente grave y puede terminar con la pérdida definitiva de la visión e inclusive del ojo. Es fundamental el diagnóstico precoz. Usted debe consultar inmediatamente si en el postoperatorio siente: dolor si nota disminución de la visión si los párpados están inflamados si el ojo está muy rojo o con secreción si nota sensibilidad a la luz. Advertencia: no frotar el ojo tratado o ni nadar al menos por siete días después de la cirugía. N. Catarata cortisónica. Los corticoides pueden generar la opacificación del cristalino (lente interna del ojo). Esta situación requiere habitualmente una cirugía. Luego de un procedimiento se ha detectado catarata en el 30 % de los pacientes, pero si se requirieron tres procedimientos se eleva al 50 %. O. Atrofia del globo ocular (ptisis bulbi). Un ojo que pierde la visión ya sea como consecuencia de una infección (endoftalmitis) o por un desprendimiento de retina, puede sufrir la disminución de su tamaño. A esta situación se la denomina ptisis bulbi. 6) Existe otra posibilidad para tratar el edema macular secundario a una oclusión de rama venosa de la retina? (tratamientos alternativos) Una opción son las inyecciones intravítreas de drogas antiangiogénicas. Estas drogas bloquean la acción de una sustancia denominada factor de crecimiento endotelial vascular que, en el caso específico de la oclusión de rama venosa de la retina, generan un aumento en la permeabilidad de las paredes vasculares de la mácula con filtración de líquido desde la sangre hacia la retina (edema). El problema es que se requiere varias de estas inyecciones (mensuales) en cada ojo con el riesgo que esto significa. (Dosis de ataque y luego de mantenimiento) Una de las drogas mas recientes es el Aflibercept (nombre comercial Eylia). En un estudio se comparó la mejoría en la visión luego de las inyecciones intraoculares de Aflibercept (Eylia) con el tratamiento convencional con láser (Estudio VIBRANT). A las 24 semanas de iniciado el tratamiento, el porcentaje de pacientes cuya agudeza visual aumentó en 15 o mas letras fue del 52.7 % en los tratados con Eylia vs. 26,7 % en el grupo tratado con láser. Respecto a los riesgos de este tipo de drogas antiangiogénicas debemos distinguir entre: a) los riesgos que pueden comprometer a la salud general y aún la vida del paciente y b) los riesgos para el ojo. A. Respecto a los riesgos que pueden comprometer la salud general del paciente son, potencialmente, lo que se denomina EVENTOS TROMBOEMBÓLICOS ARTERIALES,es decir oclusiones de las arterias que pueden generar, por 4
5 ejemplo, un infarto agudo de miocardio o un accidente cerebro vascular (ACV). En los estudios Galileo y Copérnico, a las 76 a 100 semanas se registró un evento trombótico arterial en el 0,6 % de los pacientes Otros efectos generales muy infrecuentes que potencialmente puede generar la inyección de un antiangiogénico en el ojo son los siguientes: Hipertensión arterial. Trombosis venosa profunda. Muerte presuntamente vinculable a la inyección (luego de accidente cerebro vascular ó infarto de miocardio). Desórdenes gastrointestinales (dolor abdominal; colitis; obstrucción intestinal). Perforaciones gastrointestinales. Nasofaringitis Anemia. Accesos de tos. Artralgias. Sinusitis. B. Riesgos para el ojo inyectado con las sustancias antiangiogénicas: Un concepto importante: toda inyección dentro del ojo tiene graves riesgos visuales potenciales. El riesgo más grave es la pérdida definitiva de la visión del ojo inyectado. Esto es muy infrecuente pero no es imposible. A. Ojo rojo por hemorragia subconjuntival (hemorragia en la pared blanca del ojo) B. Visión borrosa C. Inflamación interna del ojo no infecciosa D. Desgarro del epitelio pigmentario de la retina E. Aumento transitorio de la presión ocular F. Partículas flotando en el campo visual G. Dolor ocular H. Lagrimeo I. Desgarro en la retina J. Endoftalmitis (infección interna del ojo) que en ciertos casos puede evolucionar hacia la pérdida de visión del ojo a pesar de un oportuno y correcto tratamiento. K. Hemorragia intraocular. Puede resolverse espontáneamente pero ciertos casos pueden requerir una cirugía ocular invasiva denominado vitrectomía. Los casos más severos pueden generar un desprendimiento de retina con la posibilidad de pérdida definitiva de la visión. Desprendimiento de retina. Esto lleva a la necesidad de realizar una o mas cirugías. Existe, aunque reducida, la posibilidad de la pérdida definitiva de la visión. L. Catarata. Toda inyección intraocular puede tener, como complicación, la generación de una catarata. Esta situación puede requerir de una cirugía de la catarata. M. Atrofia del globo ocular (ptisis bulbi). Un ojo que pierde la visión ya sea como consecuencia de una infección (endoftalmitis) o por un desprendimiento de retina, puede sufrir la disminución de su tamaño. a esta situación se la denomina ptisis bulbi. Existe una droga similar en su acción al Aflibercept, denominada Avastín (Bevacizumab). Su utilización en inyecciones intraoculares no ha sido aprobada aún 5
6 para su uso en oftalmología por las agencias gubernamentales como la F.D.A. en Estados Unidos ó la ANMAT en Argentina. Sin embargo existe una gran cantidad de publicaciones científicas internacionales de primer nivel que avalan su utilización demostrando una eficacia y seguridad equivalente al Aflibercept. Su uso en estas condiciones se lo considera off label, es decir que se le está dando un uso no contemplado por el laboratorio que elabora la droga. Otra droga dentro del mismo grupo de drogas antiangiogénicas es el RANIBIZUMAB (LUCENTIS). En este caso cuenta con la aprobación para el uso intraocular tanto de la FDA como de la ANMAT. Sus beneficios y riesgos potenciales son similares a los del AFLIBERCEPT. La ventaja del Aflibercept sería la de necesitar, en muchos casos, un menor número de dosis y su eficacia en ciertos casos que no responden al Lucentis. Todas las drogas que requieren una inyecciones intraoculares reiteradas (intravítreas) comparten los riesgos de infección (endoftalmitis); hemorragia intraocular; desgarros retinales; desprendimiento de retina; catarata, oclusiones vasculares de la retina y aumento de la presión ocular. Existen otros corticoides que se utilizan en inyecciones intravítreas como la triamcinolona o en implantes intravítreos como la fluocinolona ( retisert ). Sus efectos sobre la presión ocular (glaucoma) y la opacificación del cristalino (catarata) son significativos (80 a 87 % de cataratas y 5 a 8 % de los pacientes con glaucoma secundario al implante requirieron cirugías en el caso del implante con fluocinolona). La ventaja del dispositivo biodegradable de liberación de corticoide es precisamente evitar esas inyecciones reiteradas (en muchos casos mensuales). El número de procedimientos de inyección del dispositivo siempre es menor al número de inyecciones intraoculares que requieren las drogas antiangiogénicas. El resultado en cuanto a recuperación visual es estadísticamente mejor con las drogas antiangiogénicas. Una opción también utilizada es el tratamiento combinado. 7) Qué ocurre si no se trata el edema macular secundario a una oclusión de rama venosa de la retina? Dejado el edema macular a su libre evolución y sin ser tratado, el final, en algunos casos, puede ser la pérdida de la capacidad de lectura del ojo afectado y la presencia de una mancha (escotoma) en el centro del campo visual. Es importante que Ud. entienda que esta situación NO SIGNIFICA CEGUERA TOTAL, ya que el ojo mantiene el campo visual periférico. Otra consecuencia posible es la aparición de hemorragias intraoculares y eventualmente el desarrollo de un desprendimiento de retina que si no responde a la o las cirugías que requiere, puede terminar con la pérdida de la visión del ojo afectado. 8) Características particulares que presenta su caso: 9) Espacio para anotar dudas o preguntas 6
7 10) Autorización del consentimiento informado Habiendo recibido este formulario con tiempo suficiente para su estudio y habiendo aclarado satisfactoriamente todas mis dudas, mi firma al pie certifica que doy voluntariamente mi autorización (consentimiento) para que se me realice un procedimiento de implante de un dispositivo intravítreo de liberación de corticoide ( Ozurdex ) en mi ojo por el equipo médico constituido por los doctores Firma del paciente: Aclaración: Firma del testigo: Aclaración: 11) Fotografías y/o videos de la cirugía con finalidad científico-técnica: El paciente SI / NO AUTORIZA al equipo médico a obtener fotografías, videos o registros gráficos para difundir resultados o iconografía en publicaciones médicas y/o ámbitos científicos preservando su identidad.- (Rodear con un círculo la opción elegida). Firma del paciente: Aclaración: Firma del testigo: Aclaración: 7
8 12) Revocación del consentimiento informado Dejo asentado mi voluntad de ejercer mi derecho a revocar el Consentimiento Informado previamente firmado en el que autorizaba al equipo médico integrado por los Dres. a efectuarme un procedimiento de implante de un dispositivo intravítreo de liberación de corticoide en mi ojo. He sido informado sobre las consecuencias previsibles (riesgos) de esta decisión, descriptas en el ítem 7 de este formulario. Firma del paciente: Aclaración: Fecha: Firma del representante legal (de corresponder): Aclaración: Fecha: Firma del médico: 8
(Leyes y Decreto Reglamentario 1089 / 2012)
 CONSENTIMIENTO INFORMADO PARA LA INYECCIÓN DE UN DISPOSITIVO INTRAVÍTREO DE LIBERACIÓN DE CORTICOIDE EN EL EDEMA MACULAR SECUNDARIO A LA OCLUSIÓN DE LA VENA CENTRAL DE LA RETINA. ( OZURDEX - DEXAMETASONA-)
CONSENTIMIENTO INFORMADO PARA LA INYECCIÓN DE UN DISPOSITIVO INTRAVÍTREO DE LIBERACIÓN DE CORTICOIDE EN EL EDEMA MACULAR SECUNDARIO A LA OCLUSIÓN DE LA VENA CENTRAL DE LA RETINA. ( OZURDEX - DEXAMETASONA-)
CONSENTIMIENTO INFORMADO PARA LA INYECCIÓN INTRAOCULAR DE AFLIBERCEPT (EYLIA) EN EL EDEMA MACULAR SECUNDARIO A UNA OCLUSIÓN VENOSA DE LA RETINA
 CONSENTIMIENTO INFORMADO PARA LA INYECCIÓN INTRAOCULAR DE AFLIBERCEPT (EYLIA) EN EL EDEMA MACULAR SECUNDARIO A UNA OCLUSIÓN VENOSA DE LA RETINA (Leyes 26.529 y 26742 y Decreto Reglamentario 1089/2012)
CONSENTIMIENTO INFORMADO PARA LA INYECCIÓN INTRAOCULAR DE AFLIBERCEPT (EYLIA) EN EL EDEMA MACULAR SECUNDARIO A UNA OCLUSIÓN VENOSA DE LA RETINA (Leyes 26.529 y 26742 y Decreto Reglamentario 1089/2012)
CONSENTIMIENTO INFORMADO PARA LA INYECCIÓN INTRAOCULAR DE RANIBIZUMAB (LUCENTIS) EN EL EDEMA MACULAR SECUNDARIO A UNA OCLUSIÓN VENOSA DE LA RETINA
 CONSENTIMIENTO INFORMADO PARA LA INYECCIÓN INTRAOCULAR DE RANIBIZUMAB (LUCENTIS) EN EL EDEMA MACULAR SECUNDARIO A UNA OCLUSIÓN VENOSA DE LA RETINA (Leyes 26.529-26742 y Decreto Reglamentario 1089 / 2012)
CONSENTIMIENTO INFORMADO PARA LA INYECCIÓN INTRAOCULAR DE RANIBIZUMAB (LUCENTIS) EN EL EDEMA MACULAR SECUNDARIO A UNA OCLUSIÓN VENOSA DE LA RETINA (Leyes 26.529-26742 y Decreto Reglamentario 1089 / 2012)
(Leyes y Decreto Reglamentario 1089 / 2012)
 CONSENTIMIENTO INFORMADO PARA LA INYECCIÓN DE UN DISPOSITIVO INTRAVÍTREO DE LIBERACIÓN DE CORTICOIDE EN EL EDEMA MACULAR DIABÉTICO. ( OZURDEX - DEXAMETASONA-) (Leyes 26.529-26742 y Decreto Reglamentario
CONSENTIMIENTO INFORMADO PARA LA INYECCIÓN DE UN DISPOSITIVO INTRAVÍTREO DE LIBERACIÓN DE CORTICOIDE EN EL EDEMA MACULAR DIABÉTICO. ( OZURDEX - DEXAMETASONA-) (Leyes 26.529-26742 y Decreto Reglamentario
CONSENTIMIENTO INFORMADO PARA LA INYECCIÓN INTRAOCULAR DE RANIBIZUMAB (LUCENTIS) EN EL EDEMA MACULAR DIABÉTICO.
 CONSENTIMIENTO INFORMADO PARA LA INYECCIÓN INTRAOCULAR DE RANIBIZUMAB (LUCENTIS) EN EL EDEMA MACULAR DIABÉTICO. (Leyes 26.529-26742 y Decreto Reglamentario 1089 / 2012) Nota: El diseño y contenido de este
CONSENTIMIENTO INFORMADO PARA LA INYECCIÓN INTRAOCULAR DE RANIBIZUMAB (LUCENTIS) EN EL EDEMA MACULAR DIABÉTICO. (Leyes 26.529-26742 y Decreto Reglamentario 1089 / 2012) Nota: El diseño y contenido de este
(Leyes y y Decreto Reglamentario 1089/2012)
 CONSENTIMIENTO INFORMADO PARA LA INYECCIÓN DE UN DISPOSITIVO INTRAVÍTREO DE LIBERACIÓN DE CORTICOIDE EN UVEÍTIS NO INFECCIOSAS INTERMEDIAS Y POSTERIORES ( OZURDEX - DEXAMETASONA-) (Leyes 26.529 y 26742
CONSENTIMIENTO INFORMADO PARA LA INYECCIÓN DE UN DISPOSITIVO INTRAVÍTREO DE LIBERACIÓN DE CORTICOIDE EN UVEÍTIS NO INFECCIOSAS INTERMEDIAS Y POSTERIORES ( OZURDEX - DEXAMETASONA-) (Leyes 26.529 y 26742
CONSENTIMIENTO INFORMADO PARA LA INYECCIÓN INTRAOCULAR DE RANIBIZUMAB (LUCENTIS) EN LA DEGENERACIÓN MACULAR RELACIONADA CON LA EDAD EXUDATIVA ó HÚMEDA
 CONSENTIMIENTO INFORMADO PARA LA INYECCIÓN INTRAOCULAR DE RANIBIZUMAB (LUCENTIS) EN LA DEGENERACIÓN MACULAR RELACIONADA CON LA EDAD EXUDATIVA ó HÚMEDA (Leyes 26.529 y 26742 y Decreto Reglamentario 1089/2012)
CONSENTIMIENTO INFORMADO PARA LA INYECCIÓN INTRAOCULAR DE RANIBIZUMAB (LUCENTIS) EN LA DEGENERACIÓN MACULAR RELACIONADA CON LA EDAD EXUDATIVA ó HÚMEDA (Leyes 26.529 y 26742 y Decreto Reglamentario 1089/2012)
CONSENTIMIENTO INFORMADO PARA LA INYECCIÓN INTRAVÍTREA DE BEVACIZUMAB ( AVASTÍN ) EN EL EDEMA MACULAR DIABÉTICO.
 CONSENTIMIENTO INFORMADO PARA LA INYECCIÓN INTRAVÍTREA DE BEVACIZUMAB ( AVASTÍN ) EN EL EDEMA MACULAR DIABÉTICO. (Leyes 26.529-26742 y Decreto Reglamentario 1089 / 2012) Nota: El diseño y contenido de
CONSENTIMIENTO INFORMADO PARA LA INYECCIÓN INTRAVÍTREA DE BEVACIZUMAB ( AVASTÍN ) EN EL EDEMA MACULAR DIABÉTICO. (Leyes 26.529-26742 y Decreto Reglamentario 1089 / 2012) Nota: El diseño y contenido de
CONSENTIMIENTO INFORMADO PARA LA INYECCIÓN INTRAOCULAR DE AFLIBERCEPT (EYLIA) EN LA DEGENERACIÓN MACULAR RELACIONADA CON LA EDAD EXUDATIVA ó HÚMEDA
 CONSENTIMIENTO INFORMADO PARA LA INYECCIÓN INTRAOCULAR DE AFLIBERCEPT (EYLIA) EN LA DEGENERACIÓN MACULAR RELACIONADA CON LA EDAD EXUDATIVA ó HÚMEDA (Leyes 26.529-26742 y Decreto Reglamentario 1089 / 2012)
CONSENTIMIENTO INFORMADO PARA LA INYECCIÓN INTRAOCULAR DE AFLIBERCEPT (EYLIA) EN LA DEGENERACIÓN MACULAR RELACIONADA CON LA EDAD EXUDATIVA ó HÚMEDA (Leyes 26.529-26742 y Decreto Reglamentario 1089 / 2012)
CONSENTIMIENTO INFORMADO PARA ELTRATAMIENTO DE LA VASCULOPATÍA COROIDEA POLIPOIDEA CON TERAPIA FOTODINÁMICA
 CONSENTIMIENTO INFORMADO PARA ELTRATAMIENTO DE LA VASCULOPATÍA COROIDEA POLIPOIDEA CON TERAPIA FOTODINÁMICA (Leyes 26.529-26742 y Decreto Reglamentario 1089 / 2012) Nota: El diseño y contenido de este
CONSENTIMIENTO INFORMADO PARA ELTRATAMIENTO DE LA VASCULOPATÍA COROIDEA POLIPOIDEA CON TERAPIA FOTODINÁMICA (Leyes 26.529-26742 y Decreto Reglamentario 1089 / 2012) Nota: El diseño y contenido de este
CONSENTIMIENTO INFORMADO PARA ELTRATAMIENTO DE LA DEGENERACIÓN MACULAR RELACIONADA CON LA EDAD EXUDATIVA (SUBFOVEAL) CON TERAPIA FOTODINÁMICA
 CONSENTIMIENTO INFORMADO PARA ELTRATAMIENTO DE LA DEGENERACIÓN MACULAR RELACIONADA CON LA EDAD EXUDATIVA (SUBFOVEAL) CON TERAPIA FOTODINÁMICA (Leyes 26.529-26742 y Decreto Reglamentario 1089 / 2012) Nota:
CONSENTIMIENTO INFORMADO PARA ELTRATAMIENTO DE LA DEGENERACIÓN MACULAR RELACIONADA CON LA EDAD EXUDATIVA (SUBFOVEAL) CON TERAPIA FOTODINÁMICA (Leyes 26.529-26742 y Decreto Reglamentario 1089 / 2012) Nota:
CONSENTIMIENTO INFORMADO PARA LA CIRUGÍA DE EVISCERACIÓN OCULAR. (Leyes y y Decreto Reglamentario 1089/2012)
 CONSENTIMIENTO INFORMADO PARA LA CIRUGÍA DE EVISCERACIÓN OCULAR (Leyes 26.529 y 26742 y Decreto Reglamentario 1089/2012) Nota: El diseño y contenido de este consentimiento, evaluado y aprobado por el Consejo
CONSENTIMIENTO INFORMADO PARA LA CIRUGÍA DE EVISCERACIÓN OCULAR (Leyes 26.529 y 26742 y Decreto Reglamentario 1089/2012) Nota: El diseño y contenido de este consentimiento, evaluado y aprobado por el Consejo
CONSENTIMIENTO INFORMADO PARA LA CAPSULOTOMÍA POSTERIOR CON YAG LÁSER. (Leyes y y Decreto Reglamentario 1089/2012)
 CONSENTIMIENTO INFORMADO PARA LA CAPSULOTOMÍA POSTERIOR CON YAG LÁSER (Leyes 26.529 y 26742 y Decreto Reglamentario 1089/2012) Nota: El diseño y contenido de este consentimiento, evaluado y aprobado por
CONSENTIMIENTO INFORMADO PARA LA CAPSULOTOMÍA POSTERIOR CON YAG LÁSER (Leyes 26.529 y 26742 y Decreto Reglamentario 1089/2012) Nota: El diseño y contenido de este consentimiento, evaluado y aprobado por
(Leyes y y Decreto Reglamentario 1089/2012)
 CONSENTIMIENTO INFORMADO PARA LA INYECCIÓN INTRAOCULAR DE BEVACIZUMAB (AVASTIN) EN LA DEGENERACIÓN MACULAR RELACIONADA CON LA EDAD EXUDATIVA ( Húmeda o Neovascular ) (Leyes 26.529 y 26742 y Decreto Reglamentario
CONSENTIMIENTO INFORMADO PARA LA INYECCIÓN INTRAOCULAR DE BEVACIZUMAB (AVASTIN) EN LA DEGENERACIÓN MACULAR RELACIONADA CON LA EDAD EXUDATIVA ( Húmeda o Neovascular ) (Leyes 26.529 y 26742 y Decreto Reglamentario
CONSENTIMIENTO INFORMADO PARA LA CIRUGÍA DE EXTRACCIÓN DE ACEITE DE SILICÓN INTRAOCULAR. (Leyes y Decreto Reglamentario 1089 / 2012)
 CONSENTIMIENTO INFORMADO PARA LA CIRUGÍA DE EXTRACCIÓN DE ACEITE DE SILICÓN INTRAOCULAR (Leyes 26.529-26742 y Decreto Reglamentario 1089 / 2012) Nota: El diseño y contenido de este consentimiento, evaluado
CONSENTIMIENTO INFORMADO PARA LA CIRUGÍA DE EXTRACCIÓN DE ACEITE DE SILICÓN INTRAOCULAR (Leyes 26.529-26742 y Decreto Reglamentario 1089 / 2012) Nota: El diseño y contenido de este consentimiento, evaluado
CONSENTIMIENTO INFORMADO PARA LA CIRUGÍA DEL RECUBRIMIENTO CONJUNTIVAL. (Leyes y y Decreto Reglamentario 1089/2012)
 CONSENTIMIENTO INFORMADO PARA LA CIRUGÍA DEL RECUBRIMIENTO CONJUNTIVAL (Leyes 26.529 y 26742 y Decreto Reglamentario 1089/2012) Nota: El diseño y contenido de este consentimiento, evaluado y aprobado por
CONSENTIMIENTO INFORMADO PARA LA CIRUGÍA DEL RECUBRIMIENTO CONJUNTIVAL (Leyes 26.529 y 26742 y Decreto Reglamentario 1089/2012) Nota: El diseño y contenido de este consentimiento, evaluado y aprobado por
CONSENTIMIENTO INFORMADO PARA LA CIRUGÍA DEL VÍTREO Y LA RETINA. (Leyes y y Decreto Reglamentario 1089/2012)
 CONSENTIMIENTO INFORMADO PARA LA CIRUGÍA DEL VÍTREO Y LA RETINA (Leyes 26.529 y 26742 y Decreto Reglamentario 1089/2012) Nota: El diseño y contenido de este consentimiento, evaluado y aprobado por el Consejo
CONSENTIMIENTO INFORMADO PARA LA CIRUGÍA DEL VÍTREO Y LA RETINA (Leyes 26.529 y 26742 y Decreto Reglamentario 1089/2012) Nota: El diseño y contenido de este consentimiento, evaluado y aprobado por el Consejo
CONSENTIMIENTO INFORMADO PARA LA FOTOCOAGULACIÓN CON LÁSER DE LA RETINOPATÍA Y/Ó MACULOPATÍA DIABÉTICA
 CONSENTIMIENTO INFORMADO PARA LA FOTOCOAGULACIÓN CON LÁSER DE LA RETINOPATÍA Y/Ó MACULOPATÍA DIABÉTICA (Leyes 26.529 y 26742 y Decreto Reglamentario 1089/2012) Nota: El diseño y contenido de este consentimiento,
CONSENTIMIENTO INFORMADO PARA LA FOTOCOAGULACIÓN CON LÁSER DE LA RETINOPATÍA Y/Ó MACULOPATÍA DIABÉTICA (Leyes 26.529 y 26742 y Decreto Reglamentario 1089/2012) Nota: El diseño y contenido de este consentimiento,
CONSENTIMIENTO INFORMADO PARA LA CIRUGÍA DE EXTRACCIÓN DE EXPLANTE ESCLERAL POSTERIOR A CIRUGÍA DE LA RETINA
 CONSENTIMIENTO INFORMADO PARA LA CIRUGÍA DE EXTRACCIÓN DE EXPLANTE ESCLERAL POSTERIOR A CIRUGÍA DE LA RETINA (Leyes 26.529-26742 y Decreto Reglamentario 1089 / 2012) Nota: El diseño y contenido de este
CONSENTIMIENTO INFORMADO PARA LA CIRUGÍA DE EXTRACCIÓN DE EXPLANTE ESCLERAL POSTERIOR A CIRUGÍA DE LA RETINA (Leyes 26.529-26742 y Decreto Reglamentario 1089 / 2012) Nota: El diseño y contenido de este
CONSENTIMIENTO INFORMADO PARA LA CIRUGÍA DEL INJERTO LAMINAR DE CÓRNEA CON LAS TÉCNICAS DE TRANSPLANTE ENDOTELIAL (DSAEK / DMEK / DMAEK)
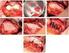 CONSENTIMIENTO INFORMADO PARA LA CIRUGÍA DEL INJERTO LAMINAR DE CÓRNEA CON LAS TÉCNICAS DE TRANSPLANTE ENDOTELIAL (DSAEK / DMEK / DMAEK) (Leyes 26.529 y 26742 y Decreto Reglamentario 1089/2012) Nota: El
CONSENTIMIENTO INFORMADO PARA LA CIRUGÍA DEL INJERTO LAMINAR DE CÓRNEA CON LAS TÉCNICAS DE TRANSPLANTE ENDOTELIAL (DSAEK / DMEK / DMAEK) (Leyes 26.529 y 26742 y Decreto Reglamentario 1089/2012) Nota: El
CONSENTIMIENTO INFORMADO PARA LA CIRUGÍA DE LA CATARATA CONGÉNITA. (Leyes y y Decreto Reglamentario 1089/2012)
 CONSENTIMIENTO INFORMADO PARA LA CIRUGÍA DE LA CATARATA CONGÉNITA (Leyes 26.529 y 26742 y Decreto Reglamentario 1089/2012) Nota: El diseño y contenido de este consentimiento, evaluado y aprobado por el
CONSENTIMIENTO INFORMADO PARA LA CIRUGÍA DE LA CATARATA CONGÉNITA (Leyes 26.529 y 26742 y Decreto Reglamentario 1089/2012) Nota: El diseño y contenido de este consentimiento, evaluado y aprobado por el
CONSENTIMIENTO INFORMADO PARA LA INYECCIÓN PERIBULBAR DE CORTICOIDE EN LA ORBITOPATÍA TIROIDEA (Oftalmopatía Tiroidea o Enfermedad de Graves)
 CONSENTIMIENTO INFORMADO PARA LA INYECCIÓN PERIBULBAR DE CORTICOIDE EN LA ORBITOPATÍA TIROIDEA (Oftalmopatía Tiroidea o Enfermedad de Graves) (Leyes 26.529 y 26742 y Decreto Reglamentario 1089/2012) Nota:
CONSENTIMIENTO INFORMADO PARA LA INYECCIÓN PERIBULBAR DE CORTICOIDE EN LA ORBITOPATÍA TIROIDEA (Oftalmopatía Tiroidea o Enfermedad de Graves) (Leyes 26.529 y 26742 y Decreto Reglamentario 1089/2012) Nota:
CONSENTIMIENTO INFORMADO PARA LA CIRUGÍA DE IMPLANTE DE QUERATOPRÓTESIS. (Leyes y y Decreto Reglamentario 1089/2012)
 CONSENTIMIENTO INFORMADO PARA LA CIRUGÍA DE IMPLANTE DE QUERATOPRÓTESIS (Leyes 26.529 y 26742 y Decreto Reglamentario 1089/2012) Nota: El diseño y contenido de este consentimiento, evaluado y aprobado
CONSENTIMIENTO INFORMADO PARA LA CIRUGÍA DE IMPLANTE DE QUERATOPRÓTESIS (Leyes 26.529 y 26742 y Decreto Reglamentario 1089/2012) Nota: El diseño y contenido de este consentimiento, evaluado y aprobado
CONSENTIMIENTO INFORMADO PARA LA INYECCIÓN PERIBULBAR DE CORTICOIDE EN LA ORBITOPATÍA TIROIDEA (Oftalmopatía Tiroidea o Enfermedad de Graves)
 CONSENTIMIENTO INFORMADO PARA LA INYECCIÓN PERIBULBAR DE CORTICOIDE EN LA ORBITOPATÍA TIROIDEA (Oftalmopatía Tiroidea o Enfermedad de Graves) (Leyes 26.529-26742 y Decreto Reglamentario 1089 / 2012) Nota:
CONSENTIMIENTO INFORMADO PARA LA INYECCIÓN PERIBULBAR DE CORTICOIDE EN LA ORBITOPATÍA TIROIDEA (Oftalmopatía Tiroidea o Enfermedad de Graves) (Leyes 26.529-26742 y Decreto Reglamentario 1089 / 2012) Nota:
CONSENTIMIENTO INFORMADO PARA LA DACRIOCISTOGRAFÍA (Estudio radiográfico de la vía lagrimal con medio de contraste)
 CONSENTIMIENTO INFORMADO PARA LA DACRIOCISTOGRAFÍA (Estudio radiográfico de la vía lagrimal con medio de contraste) (Leyes 26.529 y 26742 y Decreto Reglamentario 1089/2012) Nota: El diseño y contenido
CONSENTIMIENTO INFORMADO PARA LA DACRIOCISTOGRAFÍA (Estudio radiográfico de la vía lagrimal con medio de contraste) (Leyes 26.529 y 26742 y Decreto Reglamentario 1089/2012) Nota: El diseño y contenido
CONSENTIMIENTO INFORMADO PARA LA IRIDOPLASTIA. (Leyes y y Decreto Reglamentario 1089/2012)
 CONSENTIMIENTO INFORMADO PARA LA IRIDOPLASTIA (Leyes 26.529 y 26742 y Decreto Reglamentario 1089/2012) Nota: El diseño y contenido de este consentimiento, evaluado y aprobado por el Consejo Argentino de
CONSENTIMIENTO INFORMADO PARA LA IRIDOPLASTIA (Leyes 26.529 y 26742 y Decreto Reglamentario 1089/2012) Nota: El diseño y contenido de este consentimiento, evaluado y aprobado por el Consejo Argentino de
CONSENTIMIENTO INFORMADO PARA LA CIRUGÍA DE DESCOMPRESIÓN ORBITARIA (Oftalmopatía Tiroidea o Enfermedad de Graves)
 CONSENTIMIENTO INFORMADO PARA LA CIRUGÍA DE DESCOMPRESIÓN ORBITARIA (Oftalmopatía Tiroidea o Enfermedad de Graves) (Leyes 26.529 y 26742 y Decreto Reglamentario 1089/2012) Nota: El diseño y contenido de
CONSENTIMIENTO INFORMADO PARA LA CIRUGÍA DE DESCOMPRESIÓN ORBITARIA (Oftalmopatía Tiroidea o Enfermedad de Graves) (Leyes 26.529 y 26742 y Decreto Reglamentario 1089/2012) Nota: El diseño y contenido de
CONSENTIMIENTO PARA EL TRATAMIENTO MEDICO ANESTESICO Y QUIRURGICO
 CONSENTIMIENTO PARA EL TRATAMIENTO MEDICO ANESTESICO Y QUIRURGICO Escobar, a los... días del mes de... de... Yo...he sido informado/a por el Doctor...la necesidad de realizar un adecuado tratamiento por
CONSENTIMIENTO PARA EL TRATAMIENTO MEDICO ANESTESICO Y QUIRURGICO Escobar, a los... días del mes de... de... Yo...he sido informado/a por el Doctor...la necesidad de realizar un adecuado tratamiento por
CONSENTIMIENTO INFORMADO PARA LA CIRUGÍA DEL GLAUCOMA CON PROCEDIMIENTOS CICLODESTRUCTIVOS. (Leyes y y Decreto Reglamentario 1089/2012)
 CONSENTIMIENTO INFORMADO PARA LA CIRUGÍA DEL GLAUCOMA CON PROCEDIMIENTOS CICLODESTRUCTIVOS (Leyes 26.529 y 26742 y Decreto Reglamentario 1089/2012) Nota: El diseño y contenido de este consentimiento, evaluado
CONSENTIMIENTO INFORMADO PARA LA CIRUGÍA DEL GLAUCOMA CON PROCEDIMIENTOS CICLODESTRUCTIVOS (Leyes 26.529 y 26742 y Decreto Reglamentario 1089/2012) Nota: El diseño y contenido de este consentimiento, evaluado
CONSENTIMIENTO INFORMADO PARA LA CIRUGÍA DEL PTERIGION. (Leyes y y Decreto Reglamentario 1089/2012)
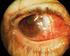 CONSENTIMIENTO INFORMADO PARA LA CIRUGÍA DEL PTERIGION (Leyes 26.529 y 26742 y Decreto Reglamentario 1089/2012) Nota: El diseño y contenido de este consentimiento, evaluado y aprobado por el Consejo Argentino
CONSENTIMIENTO INFORMADO PARA LA CIRUGÍA DEL PTERIGION (Leyes 26.529 y 26742 y Decreto Reglamentario 1089/2012) Nota: El diseño y contenido de este consentimiento, evaluado y aprobado por el Consejo Argentino
CONSENTIMIENTO INFORMADO PARA EL TRATAMIENTO DEL QUERATOCONO CON LA TÉCNICA CROSS-LINKING. (Leyes y y Decreto Reglamentario 1089/2012)
 CONSENTIMIENTO INFORMADO PARA EL TRATAMIENTO DEL QUERATOCONO CON LA TÉCNICA CROSS-LINKING (Leyes 26.529 y 26742 y Decreto Reglamentario 1089/2012) Nota: El diseño y contenido de este consentimiento, evaluado
CONSENTIMIENTO INFORMADO PARA EL TRATAMIENTO DEL QUERATOCONO CON LA TÉCNICA CROSS-LINKING (Leyes 26.529 y 26742 y Decreto Reglamentario 1089/2012) Nota: El diseño y contenido de este consentimiento, evaluado
CONSENTIMIENTO INFORMADO PARA LA CIRUGÍA DEL CHALAZION. (Leyes y y Decreto Reglamentario 1089/2012)
 CONSENTIMIENTO INFORMADO PARA LA CIRUGÍA DEL CHALAZION (Leyes 26.529 y 26742 y Decreto Reglamentario 1089/2012) Nota: El diseño y contenido de este consentimiento, evaluado y aprobado por el Consejo Argentino
CONSENTIMIENTO INFORMADO PARA LA CIRUGÍA DEL CHALAZION (Leyes 26.529 y 26742 y Decreto Reglamentario 1089/2012) Nota: El diseño y contenido de este consentimiento, evaluado y aprobado por el Consejo Argentino
CONSENTIMIENTO INFORMADO PARA EL TRATAMIENTO DEL GLAUCOMA MEDIANTE TRABECULOPASTIA CON LÁSER. (Leyes y y Decreto Reglamentario 1089/2012)
 CONSENTIMIENTO INFORMADO PARA EL TRATAMIENTO DEL GLAUCOMA MEDIANTE TRABECULOPASTIA CON LÁSER (Leyes 26.529 y 26742 y Decreto Reglamentario 1089/2012) Nota: El diseño y contenido de este consentimiento,
CONSENTIMIENTO INFORMADO PARA EL TRATAMIENTO DEL GLAUCOMA MEDIANTE TRABECULOPASTIA CON LÁSER (Leyes 26.529 y 26742 y Decreto Reglamentario 1089/2012) Nota: El diseño y contenido de este consentimiento,
CONSENTIMIENTO INFORMADO PARA LA CIRUGÍA DEL GLAUCOMA CON LA TÉCNICA DE ESCLERECTOMÍA PROFUNDA NO PENETRANTE
 CONSENTIMIENTO INFORMADO PARA LA CIRUGÍA DEL GLAUCOMA CON LA TÉCNICA DE ESCLERECTOMÍA PROFUNDA NO PENETRANTE (Leyes 26.529 y 26742 y Decreto Reglamentario 1089/2012) Nota: El diseño y contenido de este
CONSENTIMIENTO INFORMADO PARA LA CIRUGÍA DEL GLAUCOMA CON LA TÉCNICA DE ESCLERECTOMÍA PROFUNDA NO PENETRANTE (Leyes 26.529 y 26742 y Decreto Reglamentario 1089/2012) Nota: El diseño y contenido de este
CONSENTIMIENTO INFORMADO PARA LA CIRUGÍA DE LA CATARATA
 CONSENTIMIENTO INFORMADO PARA LA CIRUGÍA DE LA CATARATA (Leyes 26.529 y 26742 y Decreto Reglamentario 1089/2012) Nota: El diseño y contenido de este consentimiento, evaluado y aprobado por el Consejo Argentino
CONSENTIMIENTO INFORMADO PARA LA CIRUGÍA DE LA CATARATA (Leyes 26.529 y 26742 y Decreto Reglamentario 1089/2012) Nota: El diseño y contenido de este consentimiento, evaluado y aprobado por el Consejo Argentino
CONSENTIMIENTO INFORMADO PARA LA CIRUGÍA DEL GLAUCOMA CON IMPLANTE DE DISPOSITIVO DE DRENAJE ( VÁLVULA )
 CONSENTIMIENTO INFORMADO PARA LA CIRUGÍA DEL GLAUCOMA CON IMPLANTE DE DISPOSITIVO DE DRENAJE ( VÁLVULA ) (Leyes 26.529-26742 y Decreto Reglamentario 1089 / 2012) Nota: El diseño y contenido de este consentimiento,
CONSENTIMIENTO INFORMADO PARA LA CIRUGÍA DEL GLAUCOMA CON IMPLANTE DE DISPOSITIVO DE DRENAJE ( VÁLVULA ) (Leyes 26.529-26742 y Decreto Reglamentario 1089 / 2012) Nota: El diseño y contenido de este consentimiento,
CONSENTIMIENTO INFORMADO PARA LA BRAQUITERAPIA EN EL TRATAMIENTO DEL RETINOBLASTOMA. (Leyes y y Decreto Reglamentario 1089/2012)
 CONSENTIMIENTO INFORMADO PARA LA BRAQUITERAPIA EN EL TRATAMIENTO DEL RETINOBLASTOMA (Leyes 26.529 y 26742 y Decreto Reglamentario 1089/2012) Nota: El diseño y contenido de este consentimiento, evaluado
CONSENTIMIENTO INFORMADO PARA LA BRAQUITERAPIA EN EL TRATAMIENTO DEL RETINOBLASTOMA (Leyes 26.529 y 26742 y Decreto Reglamentario 1089/2012) Nota: El diseño y contenido de este consentimiento, evaluado
RETINOPATÍA DEL PREMATURO
 RETINOPATÍA DEL PREMATURO INFORMACIÓN PARA PADRES SOBRE LOS CONTROLES LUEGO DEL ALTA DE LA UNIDAD DE CUIDADOS INTENSIVOS NEONATALES EN NIÑOS NO TRATADOS Nota: el presente texto, evaluado y aprobado por
RETINOPATÍA DEL PREMATURO INFORMACIÓN PARA PADRES SOBRE LOS CONTROLES LUEGO DEL ALTA DE LA UNIDAD DE CUIDADOS INTENSIVOS NEONATALES EN NIÑOS NO TRATADOS Nota: el presente texto, evaluado y aprobado por
CONSENTIMIENTO INFORMADO PARA LA CIRUGÍA DEL ESTRABISMO EN EL NIÑO. (Leyes 26.529-26742 y Decreto Reglamentario 1089 / 2012)
 CONSENTIMIENTO INFORMADO PARA LA CIRUGÍA DEL ESTRABISMO EN EL NIÑO (Leyes 26.529-26742 y Decreto Reglamentario 1089 / 2012) Nota: El diseño y contenido de este consentimiento, evaluado y aprobado por el
CONSENTIMIENTO INFORMADO PARA LA CIRUGÍA DEL ESTRABISMO EN EL NIÑO (Leyes 26.529-26742 y Decreto Reglamentario 1089 / 2012) Nota: El diseño y contenido de este consentimiento, evaluado y aprobado por el
CONSENTIMIENTO INFORMADO PARA LA CIRUGÍA DEL ECTROPION. (Leyes y Decreto Reglamentario 1089 / 2012)
 CONSENTIMIENTO INFORMADO PARA LA CIRUGÍA DEL ECTROPION (Leyes 26.529-26742 y Decreto Reglamentario 1089 / 2012) Nota: El diseño y contenido de este consentimiento, evaluado y aprobado por el Consejo Argentino
CONSENTIMIENTO INFORMADO PARA LA CIRUGÍA DEL ECTROPION (Leyes 26.529-26742 y Decreto Reglamentario 1089 / 2012) Nota: El diseño y contenido de este consentimiento, evaluado y aprobado por el Consejo Argentino
CONSENTIMIENTO INFORMADO PARA LA CIRUGÍA DEL ESTRABISMO EN EL NIÑO. (Leyes y y Decreto Reglamentario 1089/2012)
 CONSENTIMIENTO INFORMADO PARA LA CIRUGÍA DEL ESTRABISMO EN EL NIÑO (Leyes 26.529 y 26742 y Decreto Reglamentario 1089/2012) Nota: El diseño y contenido de este consentimiento, evaluado y aprobado por el
CONSENTIMIENTO INFORMADO PARA LA CIRUGÍA DEL ESTRABISMO EN EL NIÑO (Leyes 26.529 y 26742 y Decreto Reglamentario 1089/2012) Nota: El diseño y contenido de este consentimiento, evaluado y aprobado por el
CONSENTIMIENTO INFORMADO PARA LA CIRUGÍA DE TRANSPLANTE DE CÓRNEA
 CONSENTIMIENTO INFORMADO PARA LA CIRUGÍA DE TRANSPLANTE DE CÓRNEA Nota: El diseño y contenido de este consentimiento evaluado y aprobado por el Consejo Argentino de Oftalmología, es autoría del Dr. Roberto
CONSENTIMIENTO INFORMADO PARA LA CIRUGÍA DE TRANSPLANTE DE CÓRNEA Nota: El diseño y contenido de este consentimiento evaluado y aprobado por el Consejo Argentino de Oftalmología, es autoría del Dr. Roberto
(Leyes y y Decreto Reglamentario 1089/2012)
 CONSENTIMIENTO INFORMADO PARA LA CIRUGÍA DEL TRAUMATISMO OCULAR (TRAUMAS OCULARES CONTUSOS, PENETRANTES Y/O PERFORANTES CON Ó SIN CUERPO EXTRAÑO INTRAOCULAR) (Leyes 26.529 y 26742 y Decreto Reglamentario
CONSENTIMIENTO INFORMADO PARA LA CIRUGÍA DEL TRAUMATISMO OCULAR (TRAUMAS OCULARES CONTUSOS, PENETRANTES Y/O PERFORANTES CON Ó SIN CUERPO EXTRAÑO INTRAOCULAR) (Leyes 26.529 y 26742 y Decreto Reglamentario
CONSENTIMIENTO INFORMADO PARA EL SONDAJE Y/O LA INTUBACIÓN DE LA OBSTRUCCIÓN CONGÉNITA DE LA VÍA LAGRIMAL
 CONSENTIMIENTO INFORMADO PARA EL SONDAJE Y/O LA INTUBACIÓN DE LA OBSTRUCCIÓN CONGÉNITA DE LA VÍA LAGRIMAL (Leyes 26.529 y 26742 y Decreto Reglamentario 1089/2012) Nota: El diseño y contenido de este consentimiento,
CONSENTIMIENTO INFORMADO PARA EL SONDAJE Y/O LA INTUBACIÓN DE LA OBSTRUCCIÓN CONGÉNITA DE LA VÍA LAGRIMAL (Leyes 26.529 y 26742 y Decreto Reglamentario 1089/2012) Nota: El diseño y contenido de este consentimiento,
CONSENTIMIENTO INFORMADO PARA LA CIRUGÍA DE LA FRACTURA DEL PISO DE LA ÒRBITA. (Leyes y y Decreto Reglamentario 1089/2012)
 CONSENTIMIENTO INFORMADO PARA LA CIRUGÍA DE LA FRACTURA DEL PISO DE LA ÒRBITA (Leyes 26.529 y 26742 y Decreto Reglamentario 1089/2012) Nota: El diseño y contenido de este consentimiento, evaluado y aprobado
CONSENTIMIENTO INFORMADO PARA LA CIRUGÍA DE LA FRACTURA DEL PISO DE LA ÒRBITA (Leyes 26.529 y 26742 y Decreto Reglamentario 1089/2012) Nota: El diseño y contenido de este consentimiento, evaluado y aprobado
CONSENTIMIENTO INFORMADO PARA LA CIRUGÍA REFRACTIVA CON EXCÍMER LÁSER ( L.A.S.I.K. ) EN DISTINTAS SESIONES QUIRÚRGICAS PARA CADA OJO
 CONSENTIMIENTO INFORMADO PARA LA CIRUGÍA REFRACTIVA CON EXCÍMER LÁSER ( L.A.S.I.K. ) EN DISTINTAS SESIONES QUIRÚRGICAS PARA CADA OJO (Leyes 26.529 y 26742 y Decreto Reglamentario 1089/2012) Nota: El diseño
CONSENTIMIENTO INFORMADO PARA LA CIRUGÍA REFRACTIVA CON EXCÍMER LÁSER ( L.A.S.I.K. ) EN DISTINTAS SESIONES QUIRÚRGICAS PARA CADA OJO (Leyes 26.529 y 26742 y Decreto Reglamentario 1089/2012) Nota: El diseño
CONSENTIMIENTO INFORMADO PARA LA TARSORRAFIA (CIRUGÍA DEL LAGOFTALMOS Y OTRAS INDICACIONES)
 CONSENTIMIENTO INFORMADO PARA LA TARSORRAFIA (CIRUGÍA DEL LAGOFTALMOS Y OTRAS INDICACIONES) (Leyes 26.529 y 26742 y Decreto Reglamentario 1089/2012) Nota: El diseño y contenido de este consentimiento,
CONSENTIMIENTO INFORMADO PARA LA TARSORRAFIA (CIRUGÍA DEL LAGOFTALMOS Y OTRAS INDICACIONES) (Leyes 26.529 y 26742 y Decreto Reglamentario 1089/2012) Nota: El diseño y contenido de este consentimiento,
CONSENTIMIENTO PARA EL TRATAMIENTO MEDICO ANESTESICO Y QUIRURGICO
 CONSENTIMIENTO PARA EL TRATAMIENTO MEDICO ANESTESICO Y QUIRURGICO Escobar, a los... días del mes de... de... Yo...he sido informado/a por el Doctor...la necesidad de realizar un adecuado tratamiento por
CONSENTIMIENTO PARA EL TRATAMIENTO MEDICO ANESTESICO Y QUIRURGICO Escobar, a los... días del mes de... de... Yo...he sido informado/a por el Doctor...la necesidad de realizar un adecuado tratamiento por
CONSENTIMIENTO INFORMADO PARA ELTRATAMIENTO DE LA RETINOPATÍA DEL PREMATURO (ROP)
 CONSENTIMIENTO INFORMADO PARA ELTRATAMIENTO DE LA RETINOPATÍA DEL PREMATURO (ROP) Texto acorde a las leyes 26.529-26742 y Decreto Reglamentario 1089 / 2012 Res. No 561/2014 de la Superintendencia de Servicios
CONSENTIMIENTO INFORMADO PARA ELTRATAMIENTO DE LA RETINOPATÍA DEL PREMATURO (ROP) Texto acorde a las leyes 26.529-26742 y Decreto Reglamentario 1089 / 2012 Res. No 561/2014 de la Superintendencia de Servicios
CONSENTIMIENTO INFORMADO PARA LA CIRUGÍA DE IMPLANTE DE LENTES INTRAOCULARES FÁQUICAS
 CONSENTIMIENTO INFORMADO PARA LA CIRUGÍA DE IMPLANTE DE LENTES INTRAOCULARES FÁQUICAS Nota: El diseño y contenido de este consentimiento evaluado y aprobado por el Consejo Argentino de Oftalmología, es
CONSENTIMIENTO INFORMADO PARA LA CIRUGÍA DE IMPLANTE DE LENTES INTRAOCULARES FÁQUICAS Nota: El diseño y contenido de este consentimiento evaluado y aprobado por el Consejo Argentino de Oftalmología, es
CONSENTIMIENTO INFORMADO PARA EL TRANSPLANTE DE CÓRNEA (QUERATOPLASTIA PENETRANTE) (Leyes y y Decreto Reglamentario 1089/2012)
 CONSENTIMIENTO INFORMADO PARA EL TRANSPLANTE DE CÓRNEA (QUERATOPLASTIA PENETRANTE) (Leyes 26.529 y 26742 y Decreto Reglamentario 1089/2012) Nota: El diseño y contenido de este consentimiento, evaluado
CONSENTIMIENTO INFORMADO PARA EL TRANSPLANTE DE CÓRNEA (QUERATOPLASTIA PENETRANTE) (Leyes 26.529 y 26742 y Decreto Reglamentario 1089/2012) Nota: El diseño y contenido de este consentimiento, evaluado
CONSENTIMIENTO INFORMADO PARA LA INYECCIÓN INTRAOCULAR DE AFLIBERCEPT (EYLIA) EN EL EDEMA MACULAR DIABÉTICO.
 CONSENTIMIENTO INFORMADO PARA LA INYECCIÓN INTRAOCULAR DE AFLIBERCEPT (EYLIA) EN EL EDEMA MACULAR DIABÉTICO. (Leyes 26.529-26742 y Decreto Reglamentario 1089 / 2012) Nota: El diseño y contenido de este
CONSENTIMIENTO INFORMADO PARA LA INYECCIÓN INTRAOCULAR DE AFLIBERCEPT (EYLIA) EN EL EDEMA MACULAR DIABÉTICO. (Leyes 26.529-26742 y Decreto Reglamentario 1089 / 2012) Nota: El diseño y contenido de este
CONSENTIMIENTO INFORMADO PARA LA CIRUGÍA DEL ENTROPION. (Leyes y Decreto Reglamentario 1089 / 2012)
 CONSENTIMIENTO INFORMADO PARA LA CIRUGÍA DEL ENTROPION (Leyes 26.529-26742 y Decreto Reglamentario 1089 / 2012) Nota: El diseño y contenido de este consentimiento, evaluado y aprobado por el Consejo Argentino
CONSENTIMIENTO INFORMADO PARA LA CIRUGÍA DEL ENTROPION (Leyes 26.529-26742 y Decreto Reglamentario 1089 / 2012) Nota: El diseño y contenido de este consentimiento, evaluado y aprobado por el Consejo Argentino
CONSENTIMIENTO INFORMADO PARA LA CIRUGÍA DE IMPLANTE DE LENTE INTRAOCULAR FÁQUICO. (Leyes y y Decreto Reglamentario 1089/2012)
 CONSENTIMIENTO INFORMADO PARA LA CIRUGÍA DE IMPLANTE DE LENTE INTRAOCULAR FÁQUICO (Leyes 26.529 y 26742 y Decreto Reglamentario 1089/2012) Nota: El diseño y contenido de este consentimiento, evaluado y
CONSENTIMIENTO INFORMADO PARA LA CIRUGÍA DE IMPLANTE DE LENTE INTRAOCULAR FÁQUICO (Leyes 26.529 y 26742 y Decreto Reglamentario 1089/2012) Nota: El diseño y contenido de este consentimiento, evaluado y
CONSENTIMIENTO INFORMADO PARA LA CAPSULOTOMÍA POSTERIOR CON YAG-LÁSER
 CONSENTIMIENTO INFORMADO PARA LA CAPSULOTOMÍA POSTERIOR CON YAG-LÁSER Nota: El diseño y contenido de este consentimiento evaluado y aprobado por el Consejo Argentino de Oftalmología, es autoría del Dr.
CONSENTIMIENTO INFORMADO PARA LA CAPSULOTOMÍA POSTERIOR CON YAG-LÁSER Nota: El diseño y contenido de este consentimiento evaluado y aprobado por el Consejo Argentino de Oftalmología, es autoría del Dr.
1. DOCUMENTO DE INFORMACIÓN PARA (*) CRIOTERAPIA TRANSESCLERAL
 FORMULARIO DE INFORMACIÓN Y CONSENTIMIENTO INFORMADO ESCRITO Orden de 8 de julio de 2009 (BOJA nº 152 de fecha 6 de agosto) por la que se dictan instrucciones a los Centros del Sistema Sanitario Público
FORMULARIO DE INFORMACIÓN Y CONSENTIMIENTO INFORMADO ESCRITO Orden de 8 de julio de 2009 (BOJA nº 152 de fecha 6 de agosto) por la que se dictan instrucciones a los Centros del Sistema Sanitario Público
(Leyes y Decreto Reglamentario 1089 / 2012)
 CONSENTIMIENTO INFORMADO PARA LA CIRUGÍA REFRACTIVA L.A.S.I.K. (EXCIMER LÁSER) BILATERAL SIMULTÁNEA (AMBOS OJOS OPERADOS EN LA MISMA SESIÓN QUIRÚRGICA). (Leyes 26.529-26742 y Decreto Reglamentario 1089
CONSENTIMIENTO INFORMADO PARA LA CIRUGÍA REFRACTIVA L.A.S.I.K. (EXCIMER LÁSER) BILATERAL SIMULTÁNEA (AMBOS OJOS OPERADOS EN LA MISMA SESIÓN QUIRÚRGICA). (Leyes 26.529-26742 y Decreto Reglamentario 1089
CONSENTIMIENTO INFORMADO PARA LA CIRUGÍA DEL GLAUCOMA CONGÉNITO. (Leyes y y Decreto Reglamentario 1089/2012)
 CONSENTIMIENTO INFORMADO PARA LA CIRUGÍA DEL GLAUCOMA CONGÉNITO (Leyes 26.529 y 26742 y Decreto Reglamentario 1089/2012) Nota: El diseño y contenido de este consentimiento, evaluado y aprobado por el Consejo
CONSENTIMIENTO INFORMADO PARA LA CIRUGÍA DEL GLAUCOMA CONGÉNITO (Leyes 26.529 y 26742 y Decreto Reglamentario 1089/2012) Nota: El diseño y contenido de este consentimiento, evaluado y aprobado por el Consejo
CONSENTIMIENTO INFORMADO PARA EL SONDAJE Y Ó LA INTUBACIÓN DE LA OBSTRUCCIÓN CONGÉNITA DE LA VÍA LAGRIMAL
 CONSENTIMIENTO INFORMADO PARA EL SONDAJE Y Ó LA INTUBACIÓN DE LA OBSTRUCCIÓN CONGÉNITA DE LA VÍA LAGRIMAL (Leyes 26.529-26742 y Decreto Reglamentario 1089 / 2012) Nota: El diseño y contenido de este consentimiento,
CONSENTIMIENTO INFORMADO PARA EL SONDAJE Y Ó LA INTUBACIÓN DE LA OBSTRUCCIÓN CONGÉNITA DE LA VÍA LAGRIMAL (Leyes 26.529-26742 y Decreto Reglamentario 1089 / 2012) Nota: El diseño y contenido de este consentimiento,
PROGRAMA DE ESTÍMULOS A LA INNOVACIÓN
 TÍTULO DEL PROYECTO: TRIAMCINOLONA ACETÓNIDO CONTENIDO EN UNA FORMULACIÓN INNOVADORA QUE PERMITE LLEGAR AL SEGMENTO POSTERIOR DEL OJO. EMPRESA BENEFICIADA: PHARMACOS EXAKTA, S.A. DE C.V. MODALIDAD: INNOVAPYME
TÍTULO DEL PROYECTO: TRIAMCINOLONA ACETÓNIDO CONTENIDO EN UNA FORMULACIÓN INNOVADORA QUE PERMITE LLEGAR AL SEGMENTO POSTERIOR DEL OJO. EMPRESA BENEFICIADA: PHARMACOS EXAKTA, S.A. DE C.V. MODALIDAD: INNOVAPYME
RETINOPATÍA DIABÉTICA
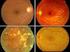 Qué es la retinopatía diabética? Las personas con diabetes pueden tener una enfermedad ocular llamada retinopatía diabética. Esta enfermedad ocurre porque los niveles altos de azúcar en la sangre causan
Qué es la retinopatía diabética? Las personas con diabetes pueden tener una enfermedad ocular llamada retinopatía diabética. Esta enfermedad ocurre porque los niveles altos de azúcar en la sangre causan
CONSENTIMIENTO INFORMADO PARA LA CIRUGÍA DEL GLAUCOMA CON LA TÉCNICA DE TRABECULECTOMÍA. (Leyes y y Decreto Reglamentario 1089/2012)
 CONSENTIMIENTO INFORMADO PARA LA CIRUGÍA DEL GLAUCOMA CON LA TÉCNICA DE TRABECULECTOMÍA (Leyes 26.529 y 26742 y Decreto Reglamentario 1089/2012) Nota: El diseño y contenido de este consentimiento, evaluado
CONSENTIMIENTO INFORMADO PARA LA CIRUGÍA DEL GLAUCOMA CON LA TÉCNICA DE TRABECULECTOMÍA (Leyes 26.529 y 26742 y Decreto Reglamentario 1089/2012) Nota: El diseño y contenido de este consentimiento, evaluado
PROTOCOLO CONSENSO DE TRATAMIENTO DEL EDEMA MACULAR SECUNDARIO A OCLUSIÓN DE LA VENA DE LA RETINA. COMUNIDAD VALENCIANA Noviembre 2012
 PROTOCOLO CONSENSO DE TRATAMIENTO DEL EDEMA MACULAR SECUNDARIO A OCLUSIÓN DE LA VENA DE LA RETINA COMUNIDAD VALENCIANA Noviembre 2012 PROTOCOLO CONSENSO DE TRATAMIENTO DEL EDEMA MACULAR SECUNDARIO A OCLUSIÓN
PROTOCOLO CONSENSO DE TRATAMIENTO DEL EDEMA MACULAR SECUNDARIO A OCLUSIÓN DE LA VENA DE LA RETINA COMUNIDAD VALENCIANA Noviembre 2012 PROTOCOLO CONSENSO DE TRATAMIENTO DEL EDEMA MACULAR SECUNDARIO A OCLUSIÓN
Realizado por:
 Este artículo médico salió de la página web de Médicos de El Salvador. http://www.medicosdeelsalvador.com Realizado por: Clínica de Especialidades Ramírez Amaya http://www.medicosdeelsalvador.com/clinica/ramirezamaya
Este artículo médico salió de la página web de Médicos de El Salvador. http://www.medicosdeelsalvador.com Realizado por: Clínica de Especialidades Ramírez Amaya http://www.medicosdeelsalvador.com/clinica/ramirezamaya
Valor del examen 28 puntos, nota mínima para acreditar 20 puntos
 COD. NOMBRE DEL PARTICIPANTE: 27 DE ABRIL 2013 NOMBRE DE LA ACTIVIDAD: SEMINARIO DE OFTALMOLOGIA FECHA: NÚMERO DE PREGUNTAS CORRECTAS APROBÓ SÍ NO Valor del examen 28 puntos, nota mínima para acreditar
COD. NOMBRE DEL PARTICIPANTE: 27 DE ABRIL 2013 NOMBRE DE LA ACTIVIDAD: SEMINARIO DE OFTALMOLOGIA FECHA: NÚMERO DE PREGUNTAS CORRECTAS APROBÓ SÍ NO Valor del examen 28 puntos, nota mínima para acreditar
CONSENTIMIENTO INFORMADO PARA LA CIRUGÍA DE LA PTOSIS PALPEBRAL. (Leyes y y Decreto Reglamentario 1089/2012)
 CONSENTIMIENTO INFORMADO PARA LA CIRUGÍA DE LA PTOSIS PALPEBRAL (Leyes 26.529 y 26742 y Decreto Reglamentario 1089/2012) Nota: El diseño y contenido de este consentimiento, evaluado y aprobado por el Consejo
CONSENTIMIENTO INFORMADO PARA LA CIRUGÍA DE LA PTOSIS PALPEBRAL (Leyes 26.529 y 26742 y Decreto Reglamentario 1089/2012) Nota: El diseño y contenido de este consentimiento, evaluado y aprobado por el Consejo
DOCUMENTO DE CONSENTIMIENTO INFORMADO PARA LA OPERACIÓN DE CATARATAS
 DOCUMENTO DE CONSENTIMIENTO INFORMADO PARA LA OPERACIÓN DE CATARATAS En cumplimiento de la Ley 41/2002, Básica reguladora de la autonomía del paciente y de derechos y obligaciones en materia de información
DOCUMENTO DE CONSENTIMIENTO INFORMADO PARA LA OPERACIÓN DE CATARATAS En cumplimiento de la Ley 41/2002, Básica reguladora de la autonomía del paciente y de derechos y obligaciones en materia de información
Hablemos sobre Maculopatía. Dr. Rodrigo Santos.
 Hablemos sobre Maculopatía. Dr. Rodrigo Santos. Uno de los temas mas problemáticos con que debemos lidiar los médicos es el exceso de información a la que tienen acceso los pacientes en la actualidad.
Hablemos sobre Maculopatía. Dr. Rodrigo Santos. Uno de los temas mas problemáticos con que debemos lidiar los médicos es el exceso de información a la que tienen acceso los pacientes en la actualidad.
CONSENTIMIENTO INFORMADO PARA TRATAMIENTO DE LA ISQUEMIA ARTERIAL AGUDA DE EXTREMIDADES 1.- IDENTIFICACIÓN DEL PACIENTE/ REPRESENTANTE LEGAL
 CONSENTIMIENTO INFORMADO PARA TRATAMIENTO DE LA ISQUEMIA ARTERIAL AGUDA DE EXTREMIDADES 1.- IDENTIFICACIÓN DEL PACIENTE/ REPRESENTANTE LEGAL Don(ña) Nombre:...Apellidos de.años, Rut N. Don /Doña Nombre:...
CONSENTIMIENTO INFORMADO PARA TRATAMIENTO DE LA ISQUEMIA ARTERIAL AGUDA DE EXTREMIDADES 1.- IDENTIFICACIÓN DEL PACIENTE/ REPRESENTANTE LEGAL Don(ña) Nombre:...Apellidos de.años, Rut N. Don /Doña Nombre:...
FORMULARIO DE INFORMACIÓN Y CONSENTIMIENTO INFORMADO ESCRITO
 FORMULARIO DE INFORMACIÓN Y CONSENTIMIENTO INFORMADO ESCRITO Orden de 8 de julio de 2009 (BOJA nº 152 de fecha 6 de agosto) por la que se dictan instrucciones a los Centros del Sistema Sanitario Público
FORMULARIO DE INFORMACIÓN Y CONSENTIMIENTO INFORMADO ESCRITO Orden de 8 de julio de 2009 (BOJA nº 152 de fecha 6 de agosto) por la que se dictan instrucciones a los Centros del Sistema Sanitario Público
CONSENTIMIENTO INFORMADO PARA LA IRIDOTOMÍA PERIFÉRICA CON LÁSER. (Leyes y y Decreto Reglamentario 1089/2012)
 CONSENTIMIENTO INFORMADO PARA LA IRIDOTOMÍA PERIFÉRICA CON LÁSER (Leyes 26.529 y 26742 y Decreto Reglamentario 1089/2012) Nota: El diseño y contenido de este consentimiento, evaluado y aprobado por el
CONSENTIMIENTO INFORMADO PARA LA IRIDOTOMÍA PERIFÉRICA CON LÁSER (Leyes 26.529 y 26742 y Decreto Reglamentario 1089/2012) Nota: El diseño y contenido de este consentimiento, evaluado y aprobado por el
Dra. Jaysi Pastrana Arias Oftalmología Especialista en Retina y Vítreo
 Dra. Jaysi Pastrana Arias Oftalmología Especialista en Retina y Vítreo Medicina Oftalmología Retina y Vítreo Universidad de Cartagena Universidad de Panamá Caja del Seguro Social Universidad Autónoma de
Dra. Jaysi Pastrana Arias Oftalmología Especialista en Retina y Vítreo Medicina Oftalmología Retina y Vítreo Universidad de Cartagena Universidad de Panamá Caja del Seguro Social Universidad Autónoma de
FORMULARIO DE INFORMACIÓN Y CONSENTIMIENTO INFORMADO ESCRITO
 FORMULARIO DE INFORMACIÓN Y CONSENTIMIENTO INFORMADO ESCRITO Orden de 8 de julio de 2009 (BOJA nº 152 de fecha 6 de agosto) por la que se dictan instrucciones a los Centros del Sistema Sanitario Público
FORMULARIO DE INFORMACIÓN Y CONSENTIMIENTO INFORMADO ESCRITO Orden de 8 de julio de 2009 (BOJA nº 152 de fecha 6 de agosto) por la que se dictan instrucciones a los Centros del Sistema Sanitario Público
CONSENTIMIENTO INFORMADO PARA REPARACION DE FISTULA ARTERIO-VENOSA / PRÓTESIS VASCULAR 1.- IDENTIFICACIÓN DEL PACIENTE/ REPRESENTANTE LEGAL
 CONSENTIMIENTO INFORMADO PARA REPARACION DE FISTULA ARTERIO-VENOSA / PRÓTESIS VASCULAR 1.- IDENTIFICACIÓN DEL PACIENTE/ REPRESENTANTE LEGAL Don(ña) Nombre:...Apellidos de.años, Rut N. Don /Doña Nombre:...
CONSENTIMIENTO INFORMADO PARA REPARACION DE FISTULA ARTERIO-VENOSA / PRÓTESIS VASCULAR 1.- IDENTIFICACIÓN DEL PACIENTE/ REPRESENTANTE LEGAL Don(ña) Nombre:...Apellidos de.años, Rut N. Don /Doña Nombre:...
PROTOCOLO DE TRABECULECTOMÍA
 PROTOCOLO DE TRABECULECTOMÍA ÍNDICE 1. Objetivos Ámbito 2. Definición 3. Diagnóstico y evaluación 4. Indicaciones 5. Técnica quirúrgicas 6. Complicaciones 7. Cuidados postoperatorios 1. OBJETIVOS DEL PROTOCOLO
PROTOCOLO DE TRABECULECTOMÍA ÍNDICE 1. Objetivos Ámbito 2. Definición 3. Diagnóstico y evaluación 4. Indicaciones 5. Técnica quirúrgicas 6. Complicaciones 7. Cuidados postoperatorios 1. OBJETIVOS DEL PROTOCOLO
CONSENTIMIENTO INFORMADO PARA EL TRATAMIENTO DEL GLAUCOMA CON LÁSER DE ARGÓN (TRABECULOPLASTIA)
 CONSENTIMIENTO INFORMADO PARA EL TRATAMIENTO DEL GLAUCOMA CON LÁSER DE ARGÓN (TRABECULOPLASTIA) Nota: El diseño y contenido de este consentimiento evaluado y aprobado por el Consejo Argentino de Oftalmología,
CONSENTIMIENTO INFORMADO PARA EL TRATAMIENTO DEL GLAUCOMA CON LÁSER DE ARGÓN (TRABECULOPLASTIA) Nota: El diseño y contenido de este consentimiento evaluado y aprobado por el Consejo Argentino de Oftalmología,
deterioro de la visión causado por un edema macular provocado por la diabetes;
 EMA/677928/2015 EMA/H/C/002392 Resumen del EPAR para el público general aflibercept El presente documento resume el Informe Público Europeo de Evaluación (EPAR) de. En él se explica cómo el Comité de Medicamentos
EMA/677928/2015 EMA/H/C/002392 Resumen del EPAR para el público general aflibercept El presente documento resume el Informe Público Europeo de Evaluación (EPAR) de. En él se explica cómo el Comité de Medicamentos
CONSENTIMIENTO INFORMADO PARA LA FOTOCOAGULACIÓN CON LÁSER DE ARGÓN PARA LA RETINOPATÍA Y/O MACULOPATÍA DIABÉTICA
 CONSENTIMIENTO INFORMADO PARA LA FOTOCOAGULACIÓN CON LÁSER DE ARGÓN PARA LA RETINOPATÍA Y/O MACULOPATÍA DIABÉTICA Nota: El diseño y contenido de este consentimiento evaluado y aprobado por el Consejo Argentino
CONSENTIMIENTO INFORMADO PARA LA FOTOCOAGULACIÓN CON LÁSER DE ARGÓN PARA LA RETINOPATÍA Y/O MACULOPATÍA DIABÉTICA Nota: El diseño y contenido de este consentimiento evaluado y aprobado por el Consejo Argentino
CONSENTIMIENTO INFORMADO PARA LA CIRUGÍA DEL GLAUCOMA
 CONSENTIMIENTO INFORMADO PARA LA CIRUGÍA DEL GLAUCOMA Nota: El diseño y contenido de este consentimiento evaluado y aprobado por el Consejo Argentino de Oftalmología, es autoría del Dr. Roberto Borrone.
CONSENTIMIENTO INFORMADO PARA LA CIRUGÍA DEL GLAUCOMA Nota: El diseño y contenido de este consentimiento evaluado y aprobado por el Consejo Argentino de Oftalmología, es autoría del Dr. Roberto Borrone.
CONSENTIMIENTO INFORMADO PARA LA CIRUGÍA DE LA CATARATA. (Leyes 26.529-26742 y Decreto Reglamentario 1089 / 2012)
 CONSENTIMIENTO INFORMADO PARA LA CIRUGÍA DE LA CATARATA (Leyes 26.529-26742 y Decreto Reglamentario 1089 / 2012) Nota: El diseño y contenido de este consentimiento, evaluado y aprobado por el Consejo Argentino
CONSENTIMIENTO INFORMADO PARA LA CIRUGÍA DE LA CATARATA (Leyes 26.529-26742 y Decreto Reglamentario 1089 / 2012) Nota: El diseño y contenido de este consentimiento, evaluado y aprobado por el Consejo Argentino
(Leyes 26.529-26742 y Decreto Reglamentario 1089 / 2012)
 CONSENTIMIENTO INFORMADO PARA LA INYECCIÓN INTRAOCULAR DE BEVACIZUMAB (AVASTÍN) EN LA DEGENERACIÓN MACULAR RELACIONADA CON LA EDAD EXUDATIVA ( HUMEDA Ó NEOVASCULAR) (Leyes 26.529-26742 y Decreto Reglamentario
CONSENTIMIENTO INFORMADO PARA LA INYECCIÓN INTRAOCULAR DE BEVACIZUMAB (AVASTÍN) EN LA DEGENERACIÓN MACULAR RELACIONADA CON LA EDAD EXUDATIVA ( HUMEDA Ó NEOVASCULAR) (Leyes 26.529-26742 y Decreto Reglamentario
CONSENTIMIENTO INFORMADO PARA TRAUMATISMOS DE MANO
 CONSENTIMIENTO INFORMADO PARA TRAUMATISMOS DE MANO Nombre del paciente: No de historia: Nombre del médico que le informa: Fecha: EN QUÉ CONSISTE El propósito de la intervención consiste en reparar las
CONSENTIMIENTO INFORMADO PARA TRAUMATISMOS DE MANO Nombre del paciente: No de historia: Nombre del médico que le informa: Fecha: EN QUÉ CONSISTE El propósito de la intervención consiste en reparar las
DG de Farmacia y Productos Sanitarios PAISE
 Plan de Gestión riesgos para la administración de fármacos antiangiogénicos en la degeneración macular asociada a la edad, edema macular diabético, edema macular secundario a la oclusión de la vena retiniana,
Plan de Gestión riesgos para la administración de fármacos antiangiogénicos en la degeneración macular asociada a la edad, edema macular diabético, edema macular secundario a la oclusión de la vena retiniana,
1. DOCUMENTO DE INFORMACIÓN PARA (*) IRIDOTOMIA LASER YAG
 FORMULARIO DE INFORMACIÓN Y CONSENTIMIENTO INFORMADO ESCRITO Orden de 8 de julio de 2009 (BOJA nº 152 de fecha 6 de agosto) por la que se dictan instrucciones a los Centros del Sistema Sanitario Público
FORMULARIO DE INFORMACIÓN Y CONSENTIMIENTO INFORMADO ESCRITO Orden de 8 de julio de 2009 (BOJA nº 152 de fecha 6 de agosto) por la que se dictan instrucciones a los Centros del Sistema Sanitario Público
CATARATA Y FUNCIÓN VISUAL
 QUÉ ES LA CATARATA? La catarata se produce cuando el cristalino pierde su trasparencia y se vuelve opaco. El cristalino es una estructura interna del ojo cuya función es actuar a modo de lente, para poder
QUÉ ES LA CATARATA? La catarata se produce cuando el cristalino pierde su trasparencia y se vuelve opaco. El cristalino es una estructura interna del ojo cuya función es actuar a modo de lente, para poder
CAPÍTULO 2. Retinopatía diabética
 CAPÍTULO 2. Retinopatía diabética 2.1. Aspectos preliminares Antes de comenzar a describir el trabajo realizado en este proyecto es conveniente que se haga una breve descripción de la diabetes y cómo afecta
CAPÍTULO 2. Retinopatía diabética 2.1. Aspectos preliminares Antes de comenzar a describir el trabajo realizado en este proyecto es conveniente que se haga una breve descripción de la diabetes y cómo afecta
CONSENTIMIENTO PARA EL TRATAMIENTO MEDICO ANESTESICO Y QUIRURGICO
 CONSENTIMIENTO PARA EL TRATAMIENTO MEDICO ANESTESICO Y QUIRURGICO Escobar, a los... días del mes de... de... Yo...he sido informado/a por el Doctor...la necesidad de realizar un adecuado tratamiento por
CONSENTIMIENTO PARA EL TRATAMIENTO MEDICO ANESTESICO Y QUIRURGICO Escobar, a los... días del mes de... de... Yo...he sido informado/a por el Doctor...la necesidad de realizar un adecuado tratamiento por
CONSENTIMIENTO PARA EL TRATAMIENTO MEDICO ANESTESICO Y QUIRURGICO
 CONSENTIMIENTO PARA EL TRATAMIENTO MEDICO ANESTESICO Y QUIRURGICO Escobar, a los... días del mes de... de... Yo...he sido informado/a por el Doctor...la necesidad de realizar un adecuado tratamiento por
CONSENTIMIENTO PARA EL TRATAMIENTO MEDICO ANESTESICO Y QUIRURGICO Escobar, a los... días del mes de... de... Yo...he sido informado/a por el Doctor...la necesidad de realizar un adecuado tratamiento por
Plan de Gestión riesgos para la administración de fármacos antiangiogénicos en la degeneración macular asociada a la edad.
 Plan de Gestión riesgos para la administración de fármacos antiangiogénicos en la degeneración macular asociada a la edad. (Adaptado de la plantilla Doc.Ref. EMEA/192632/2006) 1 Objeto Definir el plan
Plan de Gestión riesgos para la administración de fármacos antiangiogénicos en la degeneración macular asociada a la edad. (Adaptado de la plantilla Doc.Ref. EMEA/192632/2006) 1 Objeto Definir el plan
CONSENTIMIENTO PARA EL TRATAMIENTO MEDICO ANESTESICO Y QUIRURGICO
 CONSENTIMIENTO PARA EL TRATAMIENTO MEDICO ANESTESICO Y QUIRURGICO Escobar, a los... días del mes de... de... Yo...he sido informado/a por el Doctor...la necesidad de realizar un adecuado tratamiento por
CONSENTIMIENTO PARA EL TRATAMIENTO MEDICO ANESTESICO Y QUIRURGICO Escobar, a los... días del mes de... de... Yo...he sido informado/a por el Doctor...la necesidad de realizar un adecuado tratamiento por
PROGRAMA DE LECCIONES TEÓRICAS: OFTALMOLOGIA (4º) curso BASES ANATOMOFISIOLOGICAS DEL SISTEMA VISUAL
 PROGRAMA DE LECCIONES TEÓRICAS: OFTALMOLOGIA (4º) curso 2013-14 Las clases se impartirán en el AULA 6. BASES ANATOMOFISIOLOGICAS DEL SISTEMA VISUAL 1. PRESENTACION DEL CURSO El globo ocular. (I) Lunes,
PROGRAMA DE LECCIONES TEÓRICAS: OFTALMOLOGIA (4º) curso 2013-14 Las clases se impartirán en el AULA 6. BASES ANATOMOFISIOLOGICAS DEL SISTEMA VISUAL 1. PRESENTACION DEL CURSO El globo ocular. (I) Lunes,
URGENCIAS EN OFTALMOLOGÍA
 URGENCIAS EN OFTALMOLOGÍA OJO ROJO NO DOLOROSO 99% de casos: HEMORRAGIA SUBCONJUNTIVAL. NIVEL 1 Actitud: Control de TA por su médico de cabecera; si se repite varias veces en poco tiempo, búsqueda sistémica
URGENCIAS EN OFTALMOLOGÍA OJO ROJO NO DOLOROSO 99% de casos: HEMORRAGIA SUBCONJUNTIVAL. NIVEL 1 Actitud: Control de TA por su médico de cabecera; si se repite varias veces en poco tiempo, búsqueda sistémica
Grants4Apps Bogotá 2017 Ficha Técnica Reto B
 Grants4Apps Bogotá 2017 Ficha Técnica Reto B Identificar una solución que movilice a los actores que están involucrados en el tratamiento del Edema macular diabético (EMD) 1. Relevancia de la problemática
Grants4Apps Bogotá 2017 Ficha Técnica Reto B Identificar una solución que movilice a los actores que están involucrados en el tratamiento del Edema macular diabético (EMD) 1. Relevancia de la problemática
alguna forma de evitar la retinopatía diabética?
 los diabéticos de forma más precoz que en otras personas. Se trata con cirugía (ultrasonidos) y consiste en sustituir la catarata por una lente intraocular transparente. 2.- EL GLAUCOMA Es el aumento de
los diabéticos de forma más precoz que en otras personas. Se trata con cirugía (ultrasonidos) y consiste en sustituir la catarata por una lente intraocular transparente. 2.- EL GLAUCOMA Es el aumento de
Eylia debe ser administrado únicamente por un médico cualificado con experiencia en la administración de inyecciones intravítreas.
 1. NOMBRE DEL MEDICAMENTO Eylia 40 mg/ml solución inyectable en jeringa precargada. 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA 1 ml de solución inyectable contiene 40 mg de aflibercept. 3. FORMA FARMACÉUTICA
1. NOMBRE DEL MEDICAMENTO Eylia 40 mg/ml solución inyectable en jeringa precargada. 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA 1 ml de solución inyectable contiene 40 mg de aflibercept. 3. FORMA FARMACÉUTICA
RETINA QUÉ ES LA RETINA? DEGENERACIÓN MACULAR ASOCIADA A LA EDAD (DMAE)
 QUÉ ES LA? La retina es la capa más interna del ojo. Está formada por un conjunto de neuronas cuya misión es transformar la información que recibe el ojo en forma de luz en impulsos nerviosos que viajarán
QUÉ ES LA? La retina es la capa más interna del ojo. Está formada por un conjunto de neuronas cuya misión es transformar la información que recibe el ojo en forma de luz en impulsos nerviosos que viajarán
Infarto y Derrame Cerebral
 Infarto y Derrame Cerebral Los ataques o derrames cerebrales ocupan el tercer lugar entre las principales causas de muerte en Costa Rica y son una de las principales causas de invalidez grave y prolongada
Infarto y Derrame Cerebral Los ataques o derrames cerebrales ocupan el tercer lugar entre las principales causas de muerte en Costa Rica y son una de las principales causas de invalidez grave y prolongada
