TEMA 2 SISTEMAS MATERIALES
|
|
|
- José Ángel Prado Vidal
- hace 7 años
- Vistas:
Transcripción
1 TEMA 2 SISTEMAS MATERIALES. Objetivos / Criterios de evaluación O.2.1 Conocer las características de los estados de agregación de la materia. O.2.2 Conocer la teoría cinética de la materia y sus consecuencias. O.2.3 Explicar la existencia de la presión atmosférica. O.2.4 Conocer el concepto de calor latente. O.2.5 Aplicar los cambios de estado para obtener alguna sustancia de gran interés comercial. O.3.1 Sustancias puras y mezclas. O.3.2 Diferenciar entre elemento y compuesto. O.3.3 Explicar las diferencias entre mezclas homogéneas y heterogéneas. O.3.4 Identificar los componentes de una disolución y los tipos de disoluciones. O.3.5 Mencionar ejemplos de mezclas de uso cotidiano. O.3.6 Conocer las formas de medir la concentración de una disolución. O.3.7 Reconocer las técnicas de separación de mezclas heterogéneas y homogéneas. O.3.8 Conocer el concepto de solubilidad y los factores que la afectan. O.3.9 Manejar material de laboratorio sencillo. O.3.10 Preparar diseños experimentales adecuados para separar los componentes de una mezcla. O.3.11 Reconocer que existen mezclas perjudiciales para la salud y el medio ambiente. 1. Materia y densidad (página 38) Def. Materia: Es todo aquello que tiene masa y que ocupa un volumen. Def. Densidad: Es una magnitud física que indica la masa que tiene un cuerpo por unidad de volumen. Sus unidades en el S.I. son el kg/m 3. d= m v 2. Estados de agregación y teoría cinética (página 40) Cualquier sustancia, en función de sus condiciones de temperatura o presión, puede presentar 4 estados de agregación distintos: sólido, líquido, gaseoso o plasmático. La teoría cinética considera que la materia está formada por partículas diminutas que se encuentran en continuo movimiento. El movimiento de las partículas tiene relación con su energía, es decir, con su temperatura. A mayor temperatura, mayor energía y mayor movimiento. Los estados de agregación. Cuando las partículas están frías ocupan un lugar determinado en el cuerpo, y vibran alrededor de ese lugar, la forma del cuerpo y su volumen permanecen constantes. Este estado se denomina sólido. Cuando las partículas tienen más energía abandonan su posición fija pero permanecen más o menos unidas unas con otras, el cuerpo tiene volumen fijo pero no forma fija. Este estado se denomina líquido.
2 Si las partículas tienen más energía aún, alcanzan mayor temperatura, la energía del movimiento de cada una es mayor que la que las mantiene unidas y por tanto se separan. El cuerpo no tiene forma fija ni volumen constante. Este estado se llama gas. Cuando las partículas se mueven libremente y, al colisionar entre ellas, debido a su altísima temperatura, se desprenden electrones, podemos considerar que estamos ante un estado de plasma. Es decir, gases con muy alta temperatura y con partículas ionizadas. 3. Escalas de temperatura (página 41) Def.: La Temperatura: es la magnitud que mide la energía cinética media de las partículas de un cuerpo. El valor de la temperatura se mide con los termómetros. La escala de temperatura absoluta Kelvin es una escala científica cuyo cero se encuentra a la temperatura a la que se supone que las partículas de un cuerpo dejan de vibrar. Es una escala centígrada, que significa que entre los puntos de fusión y de ebullición del agua hay 100 grados. El punto de fusión del agua se encuentra a 273 K y el de ebullición a 373 K. La escala de temperatura Fahrenheit es la que se utiliza en los países de tradición anglosajona. No es una escala centígrada. El punto de fusión del agua es 32ºF y el de ebullición 212ºF. La escala de temperatura Celsius es la escala de uso internacional en los países de tradición no anglosajona, es una escala centígrada. El punto de fusión del agua es de 0ºC y el de ebullición 100ºC. Cambios de escala de temperatura C = 100 F 32 K 273 = Los cambios de estado (página 42) La temperatura incrementa la movilidad de las partículas de los cuerpos y produce como consecuencia cambios de estado de agregación de los cuerpos. En estos cambios de estado también influyen otras magnitudes como la presión. Cambios de estado Son procesos físicos por los que una sustancia pasa de un estado a otro sin que se altera la naturaleza de la sustancia
3 5. Efectos de la temperatura y la presión (página 42) Solidif Def.: Presión: es una magnitud física escalar que mide la fuerza icació ejercida por unidad de superficie. Se calcula dividiendo la Fuerza entre la superficie sobre la que ésta se ejerce. Sus unidades en el SI son el Pascal (Pa). Otras unidades son los milímetros de mercurio (mm de Hg), milibares, (mb) y atmósferas (atm). Para cambiar de unidades 1 atm = 760 mmhg = Pa = 1013 mb Def.: Presión de vapor: es la fuerza ejercida sobre un gas encerrado en un recipiente cerrado contra las paredes del recipiente. Un incremento de la presión dificulta los cambios de estado en los que hay un incremento de volumen, como de sólido a líquido o de líquido a gaseoso. Un descenso de la presión facilita los cambios de estado en los que hay un incremento de volumen. Cambios ebulloscópicos y crioscópicos Punto de fusión es la temperatura a la que se funde un sólido a una presión atmosférica de 1 atmósfera. Punto de ebullición es la temperatura a la que hierve un líquido a una presión atmosférica de 1 atmósfera. Cuando una sustancia tiene disuelta otra, sea cual sea esta, desciende su temperatura de fusión (descenso crioscópico) e incrementa su punto de ebullición (aumento ebulloscópico) 6. La presión atmosférica Def.: Presión atmosférica: es el peso que ejerce la atmósfera sobre la superficie terrestre y sobre los cuerpos que se encuentran en ella. Es el peso de la columna de aire sobre los cuerpos. La presión atmosférica se mide con barómetros. Las unidades utilizadas actualmente son los hectopascales (hpa). Una presión atmosférica normal es de 1013,25 hpa. También podemos decir que es 1 atmósfera, 760 mmhg, 1013,25 mb o Pa Cuando la presión atmosférica es baja, menos de 1013 hpa, se dice que estamos en una Borrasca (B) y el clima es inestable y nuboso. Cuando la presión atmosférica es alta, más de 1013 hpa, se dice que estamos en un Anticiclón (A) y el clima es estable y despejado. Se llaman isobaras a las líneas que unen los puntos con igual presión atmosférica en los mapas meteorológicos.
4 7. Cambios de estado y teoría cinética (página 44) Evaporación, ebullición y condensación: Las partículas con más energía del líquido se acercan a la superficie y pueden escapar convirtiéndose en gas. Cuanta más temperatura tiene el líquido, más partículas se acercan a la superficie y escapan. Al contrario, cuando las partículas del gas van perdiendo energía, se van deteniendo y chocando entre sí o con las paredes del recipiente convirtiéndose en líquido. En el caso de la ebullición, la energía suministrada hace que las partículas venzan la presión a que están sometidas y se conviertan en gas formando burbujas. El punto de ebullición, la temperatura a la que ebulle una sustancia, es una propiedad característica de ella y sirve para identificarla, pero como varía con la presión, suele tomarse como referencia la temperatura de ebullición a 1000 hpa. Fusión y Solidificación: La temperatura que se suministra a un sólido se utiliza en romper los enlaces entre sus partículas, no para incrementar la temperatura. El sólido se desmorona y se convierte en líquido. Al contrario, cuando pierde energía, sus partículas se van deteniendo, se aproximan y los enlaces se hacen más fuertes. Su estructura se forma y se convierte en líquido. El punto de fusión, la temperatura a la que funde una sustancia, es una propiedad característica de ella y sirve para identificarla, pero como varía con la presión, suele tomarse como referencia la temperatura de fusión a 1000 hpa. Sublimación directa e inversa: Cuando las partículas de la superficie de un sólido tienen energía suficiente, se separan y pasan al estado gaseoso directamente. Al contrario, algunas partículas gaseosas al chocar contra el sólido pueden perder la energía suficiente para pasar al estado sólido de una vez. 8. Calor latente y calor específico Def. Calor específico: es la energía que debe suministrarse a un kg de sustancia para que incremente su temperatura un grado centígrado. Q = Ce m t Donde Q es el calor que hace falta suministrar Ce es el Calor específico del cuerpo M es la masa del cuerpo t es el incremento de temperatura experimentado (t f -t i ) Def. Calor latente: es la cantidad de energía que hay que suministrar a un kg de sustancia para producir un cambio de estado sin incremento de temperatura. Calor latente de fusión: Es el calor necesario para que un kg de una sustancia pase de estado sólido a líquido sin incremento de temperatura. Se representa L f. Calor latente de vaporización: Es el calor necesario para que un kg de una sustancia pase de líquido a gas sin incrementar la temperatura. Se representa L v Q = m L f Q = m L v Donde Q es el calor que hace falta suministrar M es la masa del cuerpo L f o L v es el calor latente de fusión o de vaporización, según el caso
5 .10. La presión. Leyes de los gases (página 48) Son variables de estado de un gas su temperatura, su volumen y la presión que ejerce sobre el recipiente que lo contiene. Un gas se encuentra en un estado determinado cuando tiene un valor concreto para cada una de estas variables. Leyes de los gases Ley de Boyle-Mariotte. La presión y el volumen de un gas, a temperatura constante, son inversamente proporcionales. A mayor presión, menor volumen y viceversa. P V= constante Ley de Charles-Gay-Lussac. La temperatura y la presión en un gas, a volumen constante, son directamente proporcionales. A mayor presión, mayor temperatura y viceversa. P T = constante La temperatura y el volumen en un gas, a presión constante, son directamente proporcionales. A mayor temperatura mayor volumen, y viceversa. V T = constante Ley de gases ideales En la ley que refunde, en una sola, las dos anteriores P 0 V 0 T = constante P 0 V 0 T 0 = P 1 V 1 T Clasificación de la materia (página 52) Podemos clasificar las sustancias atendiendo a su aspecto: Def. Sustancia homogénea: Decimos que una sustancia es homogénea cuando tiene un aspecto uniforme y no se distinguen partes en él. Algunas de estas sustancias son mezclas y otras no. Def. Sustancia heterogénea: Decimos que una sustancia es heterogénea cuando no tiene un aspecto uniforme y se distinguen partes diferenciadas en él. Todas estas sustancias son mezclas. Podemos clasificar las sustancias atendiento a su composición: Def. Sustancia pura: Decimos que una sustancia es pura cuando mantiene sus propiedades al dividirla en partes tan pequeñas como podamos. En términos químicos, una sustancia es pura cuando todos sus átomos o todas sus moléculas son iguales.
6 Las sustancias puras pueden ser de dos tipos: Def. Elemento: Una sustancia pura es un elemento si todos los átomos son iguales. Los elementos pueden estar formados por átomos individuales, todos iguales, como el hierro, o átomos iguales agrupados en moléculas, como el oxígeno, O 2, cuyos átomos están agrupados de dos en dos. Def. Compuesto químico: Es una sustancia pura formada por moléculas todas iguales entre sí, constituidas a su vez por átomos de distintos elementos químicos, como el agua, H 2 O (dos átomos de hidrógeno y uno de agua), o la sal común, NaCl, (un átomo de sodio Na y otro de cloro Cl). Def. Sustancia compuesta (mezcla): Es aquella que está formada por moléculas pertenecientes a distintas sustancias. Tipos de Mezclas: Def. Mezclas homogéneas: son aquellas en las que no podemos distinguir sus partes a simple vista. También se llaman disoluciones. Def. Mezclas heterogéneas: Son aquellas en la que podemos distinguir sus partes. 12. Disoluciones (página 54) Def. Disolución: es una mezcla homogénea de dos o más componentes. Al que se encuentra en mayor cantidad se le llama disolvente. A los demás solutos. Sólido+sólido (aleación metálica) Sólidas Sólido+líquido (amalgama de Hg) Tipos de disolución Por el estado de agregación Por el grado de saturación Líquidas Gaseosas Insaturadas Saturadas Sobresaturadas Sólido+gas (piedras gasificadas) Líquido+sólido (agua salada) Líquido+líquido (agua y vino) Líquido+gas (bebida gaseosa) Gas+sólido (humo) Gas+líquido (aire húmedo) Gas+gas (atmósfera) Diluidas Concentradas
7 Def. Concentración: de una disolución es la medida de la cantidad de soluto por unidad de disolvente que hay en la disolución. Formas de medir la concentración Tanto por ciento en masa: Se calcula dividiendo la masa de soluto entre la masa de disolución y multiplicando por cien. Una disolución del 20 % en masa de cobre en oro significa que de cada 100 gramos del total, 20 son de cobre y 80 de oro. masa de soluto 100 % enmasa masa de disolución Tanto por ciento en volumen: Se calcula dividiendo el volumen de soluto entre el volumen de disolución y multiplicando por cien. Es la forma en que se mide el alcohol de las bebidas alcohólicas. Por ejemplo, un licor en cuya etiqueta figura % vol 40, significa que de cada 100 partes de volumen, 40 son alcohol puro y 60 de otro líquido. % vol volumen de soluto 100 volumen de disolución Masa de soluto por volumen de disolución: Se calcula dividiendo la masa de soluto en gramos entre el volumen de disolución en litros. Por ejemplo, 1 litro de una disolución 20 g/l de sal en agua se prepara poniendo 20 gramos de sal y añadiendo agua hasta rellenar 1 litro. masa de soluto( gramos) Concentración Volumen de la disolución ( litros) Def. Solubilidad: es la máxima cantidad de soluto que puede disolverse en una cantidad fija de disolvente a una temperatura determinada Def. Curvas de solubilidad: Son gráficas en las que representamos la solubilidad entre un soluto y un disolvente a distintas temperaturas. Variación de la solubilidad con la temperatura Al incrementar la temperatura disminuye la solubilidad de gases en líquidos. Por ejemplo, en un refresco con gas, si está caliente y lo abres se va el gas porque no está disuelto. Al incrementar la presión aumenta la solubilidad de gases en líquidos. Por ejemplo, en un refresco con gas, mientras está cerrado (a presión) el gas se encuentra dentro del líquido disuelto, al abrirlo salen las burbujas del gas. 13. Ósmosis y capilaridad Def. Membrana semipermeable: Es una membrana que permite el paso de disolvente líquido pero no el de sales disueltas. Def. Ósmosis: Es el paso de un disolvente a través de una membrana semipermeable de una disolución diluida a otra más concentrada. Es el mecanismo por el que se preparan, por ejemplo, los jamones serranos. La carne fresca se recubre de sal y el agua de la sal sale del jamón, éste se seca y se cura.
8 Def. Capilaridad: Es el ascenso de un líquido húmedo por las paredes de un recipiente. Es el proceso, por ejemplo, por el que asciende el líquido por el interior de una pajita dentro de un refresco, aunque no sorbamos por ella. 14. Separación de mezclas
TEMA 3 LA MATERIA Y SU ESTRUCTURA
 TEMA 3 LA MATERIA Y SU ESTRUCTURA 1. Clasificación de la materia (página 58) Def. Sistema material: Es una porción de materia seleccionada para su estudio. Def. Sustancia pura: Decimos que una sustancia
TEMA 3 LA MATERIA Y SU ESTRUCTURA 1. Clasificación de la materia (página 58) Def. Sistema material: Es una porción de materia seleccionada para su estudio. Def. Sustancia pura: Decimos que una sustancia
LA MATERIA: ESTADOS DE AGREGACIÓN
 LA MATERIA: ESTADOS DE AGREGACIÓN 1. PROPIEDADES DE LA MATERIA Materia: es todo aquello que existe, tiene masa y ocupa un volumen, los distintos tipos de materia se llaman sustancias. El sistema material
LA MATERIA: ESTADOS DE AGREGACIÓN 1. PROPIEDADES DE LA MATERIA Materia: es todo aquello que existe, tiene masa y ocupa un volumen, los distintos tipos de materia se llaman sustancias. El sistema material
FÍSICA Y QUÍMICA 2º ESO Tema 2: LA MATERIA Propiedades características Estados de agregación de la materia
 FÍSICA Y QUÍMICA 2º ESO Estados de agregación de la materia Como ya sabes, la materia se puede encontrar en estado sólido, líquido y gaseoso. Son los llamados estados físicos de la materia. Existe un cuarto
FÍSICA Y QUÍMICA 2º ESO Estados de agregación de la materia Como ya sabes, la materia se puede encontrar en estado sólido, líquido y gaseoso. Son los llamados estados físicos de la materia. Existe un cuarto
LA MATERIA Y SU DIVERSIDAD
 LA MATERIA Y SU DIVERSIDAD La materia es todo aquello que tiene masa y ocupa un espacio, es decir, tiene volumen. Propiedades generales La masa y el volumen, son comunes a toda la materia y no nos sirven
LA MATERIA Y SU DIVERSIDAD La materia es todo aquello que tiene masa y ocupa un espacio, es decir, tiene volumen. Propiedades generales La masa y el volumen, son comunes a toda la materia y no nos sirven
FÍSICA Y QUÍMICA TEMA 2: LA MATERIA Y SUS ESTADOS DE AGREGACIÓN
 1 Física y Química 3º Curso Educación Secundaria Obligatoria Curso académico 2015/2016 FÍSICA Y QUÍMICA TEMA 2: LA MATERIA Y SUS ESTADOS DE AGREGACIÓN 2 Física y Química 3º Curso Educación Secundaria Obligatoria
1 Física y Química 3º Curso Educación Secundaria Obligatoria Curso académico 2015/2016 FÍSICA Y QUÍMICA TEMA 2: LA MATERIA Y SUS ESTADOS DE AGREGACIÓN 2 Física y Química 3º Curso Educación Secundaria Obligatoria
UNIDAD DIDÁCTICA 2. EL MODELO DE PARTÍCULAS DE LA MATERIA PROPUESTA DIDÁCTICA. LA MATERIA Y EL MODELO DOCUMENTO PARA EL ALUMNO
 UNIDAD DIDÁCTICA 2. EL MODELO DE PARTÍCULAS DE LA MATERIA PROPUESTA DIDÁCTICA. LA MATERIA Y EL MODELO DOCUMENTO PARA EL ALUMNO 1. LOS ESTADOS DE AGREGACIÓN DE LA MATERIA. CAMBIOS DE ESTADO Una misma sustancia
UNIDAD DIDÁCTICA 2. EL MODELO DE PARTÍCULAS DE LA MATERIA PROPUESTA DIDÁCTICA. LA MATERIA Y EL MODELO DOCUMENTO PARA EL ALUMNO 1. LOS ESTADOS DE AGREGACIÓN DE LA MATERIA. CAMBIOS DE ESTADO Una misma sustancia
FÍSICA Y QUÍMICA TEMA 2: LOS SISTEMAS MATERIALES
 Física y Química 3º Curso Educación Secundaria Obligatoria Curso académico 2015/2016 1 FÍSICA Y QUÍMICA TEMA 2: LOS SISTEMAS MATERIALES Física y Química 3º Curso Educación Secundaria Obligatoria Curso
Física y Química 3º Curso Educación Secundaria Obligatoria Curso académico 2015/2016 1 FÍSICA Y QUÍMICA TEMA 2: LOS SISTEMAS MATERIALES Física y Química 3º Curso Educación Secundaria Obligatoria Curso
LOS GASES Y LAS DISOLUCIONES. Departamento de Física y Química 3º ESO
 LOS GASES Y LAS DISOLUCIONES Departamento de Física y Química 3º ESO 0. Mapa conceptual SÓLIDO ESTADOS DE LA MATERIA LÍQUIDO Presión atmosférica GAS Solubilidad Disolución saturada Disoluciones Soluto
LOS GASES Y LAS DISOLUCIONES Departamento de Física y Química 3º ESO 0. Mapa conceptual SÓLIDO ESTADOS DE LA MATERIA LÍQUIDO Presión atmosférica GAS Solubilidad Disolución saturada Disoluciones Soluto
Materia: es aquello que ocupa un lugar en el espacio y cuyas propiedades percibimos por los sentidos. Es diversa y discontinua.
 Sistemas materiales Materia: es aquello que ocupa un lugar en el espacio y cuyas propiedades percibimos por los sentidos. Es diversa y discontinua. Mezcla Heterogénea: unión de dos o más sustancias de
Sistemas materiales Materia: es aquello que ocupa un lugar en el espacio y cuyas propiedades percibimos por los sentidos. Es diversa y discontinua. Mezcla Heterogénea: unión de dos o más sustancias de
TEMA 13: LA MATERIA, BASE DEL UNIVERSO
 TEMA 13: LA MATERIA, BASE DEL UNIVERSO Qué es materia? Materia es todo aquello que posee masa y ocupa un volumen. Está formada de partículas muy pequeñas llamadas átomos. La masa y el volumen se consideran
TEMA 13: LA MATERIA, BASE DEL UNIVERSO Qué es materia? Materia es todo aquello que posee masa y ocupa un volumen. Está formada de partículas muy pequeñas llamadas átomos. La masa y el volumen se consideran
PROPIEDADES DE LA MATERIA. Departamento de Física y Química 2º ESO
 PROPIEDADES DE LA MATERIA Departamento de Física y Química 2º ESO 0. Mapa conceptual Estados de agregación Sólido Líquido Gaseoso Propiedades MATERIA Teoría cinética Generales Específicas Leyes de los
PROPIEDADES DE LA MATERIA Departamento de Física y Química 2º ESO 0. Mapa conceptual Estados de agregación Sólido Líquido Gaseoso Propiedades MATERIA Teoría cinética Generales Específicas Leyes de los
1. Los estados de la materia
 1. Los estados de la materia Propiedades La materia que nos rodea aparece ante nosotros con muy diversos aspectos. Presenta distintas formas, colores, dureza, fluidez pero en general, consideramos que
1. Los estados de la materia Propiedades La materia que nos rodea aparece ante nosotros con muy diversos aspectos. Presenta distintas formas, colores, dureza, fluidez pero en general, consideramos que
La materia: estados físicos
 2 La materia: estados físicos PARA EMPEZAR ESQUEMA INTERNET Esquema de contenidos Para empezar, experimenta y piensa Estados físicos de la materia Gases Estados de la materia y teoría cinética Cambios
2 La materia: estados físicos PARA EMPEZAR ESQUEMA INTERNET Esquema de contenidos Para empezar, experimenta y piensa Estados físicos de la materia Gases Estados de la materia y teoría cinética Cambios
La materia y los estados de agregación
 La materia y los estados de agregación Pantallas LCD por todos lados 1. Propiedades de la materia y los estados físicos PROPIEDADES GENERALES La masa: Cantidad de materia que tiene un objeto, se mide
La materia y los estados de agregación Pantallas LCD por todos lados 1. Propiedades de la materia y los estados físicos PROPIEDADES GENERALES La masa: Cantidad de materia que tiene un objeto, se mide
FyQ 1. IES de Castuera Bloque 2 Aspectos Cuantitativos de la Química Unidad Didáctica 2
 Física y Química 1º Bachillerato LOMCE FyQ 1 IES de Castuera Bloque 2 Aspectos Cuantitativos de la Química 2015 2016 Unidad Didáctica 2 Rev 01 Las Disoluciones. Métodos Actuales para el Análisis de Sustancias
Física y Química 1º Bachillerato LOMCE FyQ 1 IES de Castuera Bloque 2 Aspectos Cuantitativos de la Química 2015 2016 Unidad Didáctica 2 Rev 01 Las Disoluciones. Métodos Actuales para el Análisis de Sustancias
TEMA 2 La naturaleza corpuscular de la materia
 EMA 2 La naturaleza corpuscular de la materia Los estados de la materia Los tres estados de la materia poseen masa y ocupan un volumen * Los gases tienen forma variable (adoptan la del recipiente que los
EMA 2 La naturaleza corpuscular de la materia Los estados de la materia Los tres estados de la materia poseen masa y ocupan un volumen * Los gases tienen forma variable (adoptan la del recipiente que los
SISTEMAS MATERIALES. Departamento de Física y Química 2º ESO
 SISTEMAS MATERIALES Departamento de Física y Química 2º ESO 0. Mapa conceptual MATERIA Sustancias puras Mezclas Heterogéneas Homogéneas Sistemas coloidales Técnicas de separación Disoluciones Soluto Disolvente
SISTEMAS MATERIALES Departamento de Física y Química 2º ESO 0. Mapa conceptual MATERIA Sustancias puras Mezclas Heterogéneas Homogéneas Sistemas coloidales Técnicas de separación Disoluciones Soluto Disolvente
1. MATERIA Y SU ASPECTO
 1. MATERIA Y SU ASPECTO El aspecto de un sistema material puede variar según el método de observación. Algunos sistemas materiales como la leche, la sangre o la mantequilla a simple vista parecen uniformes,
1. MATERIA Y SU ASPECTO El aspecto de un sistema material puede variar según el método de observación. Algunos sistemas materiales como la leche, la sangre o la mantequilla a simple vista parecen uniformes,
UNIDAD 6 - LA MATERIA
 UNIDAD 6 - LA MATERIA La materia es todo lo que pesa y ocupa un lugar en el espacio. A través de los sentidos (vista, oído, tacto, gusto y olfato) recibimos y percibimos información sobre todo lo que nos
UNIDAD 6 - LA MATERIA La materia es todo lo que pesa y ocupa un lugar en el espacio. A través de los sentidos (vista, oído, tacto, gusto y olfato) recibimos y percibimos información sobre todo lo que nos
DISOLUCIONES. Las disoluciones son mezclas homogéneas de dos o más sustancias (componentes) en proporciones variables.
 DISOLUCIONES Las disoluciones son mezclas homogéneas de dos o más sustancias (componentes) en proporciones variables. Soluto es la sustancia que se encuentra en menor proporción. Disolvente es la sustancia
DISOLUCIONES Las disoluciones son mezclas homogéneas de dos o más sustancias (componentes) en proporciones variables. Soluto es la sustancia que se encuentra en menor proporción. Disolvente es la sustancia
MEZCLAS Y DISOLUCIONES. Física y Química 3º de E.S.O. IES Isidra de Guzmán
 MEZCLAS Y DISOLUCIONES Física y Química 3º de E.S.O. IES Isidra de Guzmán Introducción Ya sabes que los sistemas materiales se pueden clasificar según su composición en sustancias puras y mezclas. Las
MEZCLAS Y DISOLUCIONES Física y Química 3º de E.S.O. IES Isidra de Guzmán Introducción Ya sabes que los sistemas materiales se pueden clasificar según su composición en sustancias puras y mezclas. Las
TEMA 3: Composición de la Materia
 TEMA 3: Composición de la Materia 1. Mezclas homogéneas y heterogéneas Una mezcla es una composición de varias sustancias con distintas propiedades. Distinguimos dos tipos de mezclas: Mezclas homogéneas:
TEMA 3: Composición de la Materia 1. Mezclas homogéneas y heterogéneas Una mezcla es una composición de varias sustancias con distintas propiedades. Distinguimos dos tipos de mezclas: Mezclas homogéneas:
Tema 12. Gases. Química General e Inorgánica A ESTADOS DE AGREGACION DE LA MATERIA
 Tema 12 Gases Química General e Inorgánica A ESTADOS DE AGREGACION DE LA MATERIA 2.1 2.1 Variables que determinan el estado de agregación Tipo de material o materia Temperatura Presión 2.2 Elementos que
Tema 12 Gases Química General e Inorgánica A ESTADOS DE AGREGACION DE LA MATERIA 2.1 2.1 Variables que determinan el estado de agregación Tipo de material o materia Temperatura Presión 2.2 Elementos que
Tema 7. Las mezclas. Introducción
 Tema 7. Las mezclas Introducción Ya sabes que los sistemas materiales se pueden clasificar según su composición en sustancias puras y mezclas. Las sustancias puras son los elementos y los compuestos que
Tema 7. Las mezclas Introducción Ya sabes que los sistemas materiales se pueden clasificar según su composición en sustancias puras y mezclas. Las sustancias puras son los elementos y los compuestos que
PSU MÓDULO COMÚN QUÍMICA PROPIEDADES COLIGATIVAS
 DEPARTAMENTO DE CIENCIAS PSU_MÓDULO COMÚN DE QUÍMICA PSU MÓDULO COMÚN QUÍMICA PROPIEDADES COLIGATIVAS Corresponden a las nuevas propiedades del solvente, debido que el soluto altera al solvente puro en
DEPARTAMENTO DE CIENCIAS PSU_MÓDULO COMÚN DE QUÍMICA PSU MÓDULO COMÚN QUÍMICA PROPIEDADES COLIGATIVAS Corresponden a las nuevas propiedades del solvente, debido que el soluto altera al solvente puro en
PROPIEDADES DE LA MATERIA. Prof. Jackeline Ruttell torres Química Febrero 2017
 PROPIEDADES DE LA MATERIA Prof. Jackeline Ruttell torres Química Febrero 2017 DEFINICIONES IMPORTANTES Sustancia: materia con composición uniforme y constante Ej. Agua siempre posee dos átomos de hidrógeno
PROPIEDADES DE LA MATERIA Prof. Jackeline Ruttell torres Química Febrero 2017 DEFINICIONES IMPORTANTES Sustancia: materia con composición uniforme y constante Ej. Agua siempre posee dos átomos de hidrógeno
Una mezcla es un compuesto formado por varias sustancias con distintas propiedades
 COMPOSICIÓN DE LA MATERIA Mezclas homogéneas y heterogéneas Una mezcla es un compuesto formado por varias sustancias con distintas propiedades Algunos sistemas materiales como la leche a simple vista parecen
COMPOSICIÓN DE LA MATERIA Mezclas homogéneas y heterogéneas Una mezcla es un compuesto formado por varias sustancias con distintas propiedades Algunos sistemas materiales como la leche a simple vista parecen
E.E.T. Nº9. Físico-Química de 2do año. Guía Nº3. Profesor: Alumno: Curso:
 E.E.T. Nº9 Físico-Química de 2do año Guía Nº3 Profesor: Alumno: Curso: Soluciones Una solución es un sistema homogéneo formado por dos o más componentes. En una solución formada por dos componentes se
E.E.T. Nº9 Físico-Química de 2do año Guía Nº3 Profesor: Alumno: Curso: Soluciones Una solución es un sistema homogéneo formado por dos o más componentes. En una solución formada por dos componentes se
A continuación se detallan cada una de las propiedades coligativas:
 PREGUNTA (Técnico Profesional) Se prepara una solución con 2 mol de agua y 0,5 mol de un electrolito no volátil. Al respecto, cuál es la presión de vapor a 25 ºC de esta solución, si la presión del agua
PREGUNTA (Técnico Profesional) Se prepara una solución con 2 mol de agua y 0,5 mol de un electrolito no volátil. Al respecto, cuál es la presión de vapor a 25 ºC de esta solución, si la presión del agua
Por la relación con el exterior los sistemas se clasifican: Sistema. Intercambia energía con el exterior. Cerrado. Sistema.
 Por la relación con el exterior los sistemas se clasifican: Sistema Intercambia materia y energía con el exterior. Abierto Intercambia energía con el exterior. Cerrado No intercambia ni materia ni energía
Por la relación con el exterior los sistemas se clasifican: Sistema Intercambia materia y energía con el exterior. Abierto Intercambia energía con el exterior. Cerrado No intercambia ni materia ni energía
SOLUCIONES BLOQUE 3. TEORÍA CINÉTICO-MOLECULAR.
 SOLUCIONES BLOQUE 3. TEORÍA CINÉTICO-MOLECULAR. Cuestiones. 1. Solución: En los líquidos las partículas tienen más libertad para moverse, debido a que las fuerzas intermoleculares presentes en ellos son
SOLUCIONES BLOQUE 3. TEORÍA CINÉTICO-MOLECULAR. Cuestiones. 1. Solución: En los líquidos las partículas tienen más libertad para moverse, debido a que las fuerzas intermoleculares presentes en ellos son
La materia se puede definir como todo aquello que tiene masa y ocupa un volumen.
 Tema 2: LA MATERIA Que es la materia? La materia se puede definir como todo aquello que tiene masa y ocupa un volumen. Clasificación de la materia (criterio: separación) Mezclas Sustancias puras Composición
Tema 2: LA MATERIA Que es la materia? La materia se puede definir como todo aquello que tiene masa y ocupa un volumen. Clasificación de la materia (criterio: separación) Mezclas Sustancias puras Composición
MOL. Nº AVOGADRO DISOLUCIONES. TEMA 4 Pág. 198 libro (Unidad 10)
 MOL. Nº AVOGADRO DISOLUCIONES TEMA 4 Pág. 198 libro (Unidad 10) CONCEPTOS PREVIOS Supuestos de Dalton Teoría atómica de Dalton Elementos consitudios por átomos, partícuals separads e indivisibles Átomos
MOL. Nº AVOGADRO DISOLUCIONES TEMA 4 Pág. 198 libro (Unidad 10) CONCEPTOS PREVIOS Supuestos de Dalton Teoría atómica de Dalton Elementos consitudios por átomos, partícuals separads e indivisibles Átomos
M A T E R I A L E S SOLUCIONES
 M A T E R I A L E S SOLUCIONES I Componentes Mayor proporción solvente Menor proporción soluto Concentración: indica la cantidad de soluto presente en una dada cantidad de solvente o una dada cantidad
M A T E R I A L E S SOLUCIONES I Componentes Mayor proporción solvente Menor proporción soluto Concentración: indica la cantidad de soluto presente en una dada cantidad de solvente o una dada cantidad
MOL. Nº AVOGADRO GASES. TEMA 4 Pág. 198 libro (Unidad 10)
 MOL. Nº AVOGADRO GASES TEMA 4 Pág. 198 libro (Unidad 10) CONCEPTOS PREVIOS Supuestos de Dalton Teoría atómica de Dalton Elementos constituidos por átomos, partículas separadas e indivisibles Átomos de
MOL. Nº AVOGADRO GASES TEMA 4 Pág. 198 libro (Unidad 10) CONCEPTOS PREVIOS Supuestos de Dalton Teoría atómica de Dalton Elementos constituidos por átomos, partículas separadas e indivisibles Átomos de
Sustituir fotografía. Sustituir texto
 Soluciones Sustituir fotografía Sustituir texto Tipos de soluciones. Hidrólisis. Solubilidad y el efecto de la temperatura. Unidades de concentración: Expresiones físicas de concentración (%m/m, %m/v,
Soluciones Sustituir fotografía Sustituir texto Tipos de soluciones. Hidrólisis. Solubilidad y el efecto de la temperatura. Unidades de concentración: Expresiones físicas de concentración (%m/m, %m/v,
LA DIVERSIDAD DE LA MATERIA
 Tema 3 LA DIVERSIDAD DE LA MATERIA 1 Clasificación de la materia Un sistema material es una porción de materia que se separa para realizar un estudio experimental. Es aquella parte del universo que se
Tema 3 LA DIVERSIDAD DE LA MATERIA 1 Clasificación de la materia Un sistema material es una porción de materia que se separa para realizar un estudio experimental. Es aquella parte del universo que se
Física y Química. 2º ESO. LA MATERIA Y SUS PROPIEDADES La materia. La materia es todo aquello que tiene masa y ocupa un espacio.
 La materia es todo aquello que tiene masa y ocupa un espacio. Es materia por tanto el plástico, el carbón, la madera, el aire, el agua, el hierro, etc. y no lo es la alegría, la tristeza, la velocidad,
La materia es todo aquello que tiene masa y ocupa un espacio. Es materia por tanto el plástico, el carbón, la madera, el aire, el agua, el hierro, etc. y no lo es la alegría, la tristeza, la velocidad,
TEMA 3: MEZCLAS, DISOLUCIONES Y SUSTANCIAS PURAS
 TEMA 3: MEZCLAS, DISOLUCIONES Y SUSTANCIAS PURAS 1. LA MATERIA Y SU ASPECTO Los sistemas materiales, formados por una o varias sustancias, pueden clasificarse en: - Sistemas materiales heterogéneos: presentan
TEMA 3: MEZCLAS, DISOLUCIONES Y SUSTANCIAS PURAS 1. LA MATERIA Y SU ASPECTO Los sistemas materiales, formados por una o varias sustancias, pueden clasificarse en: - Sistemas materiales heterogéneos: presentan
EJERCICIOS TEMA 2. LA MATERIA Y SUS PROPIEDADES.
 EJERCICIOS TEMA 2. LA MATERIA Y SUS PROPIEDADES. 1. La materia puede presentarse en tres estados de agregación. Cuáles son? 2. Cómo son la forma y el volumen de un sólido? Y de un líquido? Y de un gas?
EJERCICIOS TEMA 2. LA MATERIA Y SUS PROPIEDADES. 1. La materia puede presentarse en tres estados de agregación. Cuáles son? 2. Cómo son la forma y el volumen de un sólido? Y de un líquido? Y de un gas?
Contenido de Física y Química de la Primera Evaluación
 Contenido de Física y Química de la Primera Evaluación Concepto Teoría Práctica Óxidos básicos (M+O) Nomenclatura. Tablas de formulación. Óxidos ácidos (NM+O) Nomenclatura. En tradicional se denominan
Contenido de Física y Química de la Primera Evaluación Concepto Teoría Práctica Óxidos básicos (M+O) Nomenclatura. Tablas de formulación. Óxidos ácidos (NM+O) Nomenclatura. En tradicional se denominan
Propiedades de la materia que nos rodea
 Propiedades de la materia que nos rodea Propiedades generales La masa: Cantidad de materia que tiene un objeto, se mide en Kg en el SI. DOS SUSTANCIAS DIFERENTES PUEDEN TENER IGUAL MASA NO SIRVE PARA DIFERENCIAR
Propiedades de la materia que nos rodea Propiedades generales La masa: Cantidad de materia que tiene un objeto, se mide en Kg en el SI. DOS SUSTANCIAS DIFERENTES PUEDEN TENER IGUAL MASA NO SIRVE PARA DIFERENCIAR
FÍSICA Y QUÍMICA 2º ESO TEMA VI COMPOSICIÓN DE LA MATERIA
 FÍSICA Y QUÍMICA 2º ESO TEMA VI COMPOSICIÓN DE LA MATERIA 1) MEZCLAS HOMOGÉNEAS Y HETEROGÉNEAS Una mezcla es una composición de sustancias con distintas propiedades. Una mezcla es homogénea si está formada
FÍSICA Y QUÍMICA 2º ESO TEMA VI COMPOSICIÓN DE LA MATERIA 1) MEZCLAS HOMOGÉNEAS Y HETEROGÉNEAS Una mezcla es una composición de sustancias con distintas propiedades. Una mezcla es homogénea si está formada
Materia es todo aquello que tiene masa y ocupa un lugar en el espacio (tiene volumen). La ciencia que estudia la materia es la Química.
 Alfonso García Materia es todo aquello que tiene masa y ocupa un lugar en el espacio (tiene volumen). La ciencia que estudia la materia es la Química. Un sistema material es una porción de materia. Ejemplos:
Alfonso García Materia es todo aquello que tiene masa y ocupa un lugar en el espacio (tiene volumen). La ciencia que estudia la materia es la Química. Un sistema material es una porción de materia. Ejemplos:
Estructura de la materia
 LA MATERIA 1. Qué es la materia? 2. Estructura de la materia. 3. Propiedades de la materia 4. Estados de la materia. 5. Los cambios de estado. 6. Actividades. 7. Soluciones de las actividades. Qué es la
LA MATERIA 1. Qué es la materia? 2. Estructura de la materia. 3. Propiedades de la materia 4. Estados de la materia. 5. Los cambios de estado. 6. Actividades. 7. Soluciones de las actividades. Qué es la
IES SIERRA DEL AGUA ACTIVIDADES DE FÍSICA Y QUÍMICA DE ALUMNOS PENDIENTES DE 3º DE ESO
 IES SIERRA DEL AGUA ACTIVIDADES DE FÍSICA Y QUÍMICA DE ALUMNOS PENDIENTES DE 3º DE ESO Tema 1: Medida y método científico. 1. Transforme las siguientes magnitudes al S.I de unidades: a) 228 Gm b) 436 ns
IES SIERRA DEL AGUA ACTIVIDADES DE FÍSICA Y QUÍMICA DE ALUMNOS PENDIENTES DE 3º DE ESO Tema 1: Medida y método científico. 1. Transforme las siguientes magnitudes al S.I de unidades: a) 228 Gm b) 436 ns
LA MATERIA. - Masa - Volumen -Energía - Carga eléctrica. Propiedades generales
 TEMA 2 La Materia LA MATERIA Propiedades generales - Masa - Volumen -Energía - Carga eléctrica Propiedades características - Densidad - Punto de fusión - Punto de ebullición -Conductividad eléctrica -
TEMA 2 La Materia LA MATERIA Propiedades generales - Masa - Volumen -Energía - Carga eléctrica Propiedades características - Densidad - Punto de fusión - Punto de ebullición -Conductividad eléctrica -
UNIDAD 2: ESTADO GASEOSO
 UNIDAD 2: ESTADO GASEOSO 1 CARACTERISTICAS DE LOS GASES Los gases poseen masa y ocupan un determinado volumen en el espacio, este volumen queda determinado por el volumen del recipiente que los contiene.
UNIDAD 2: ESTADO GASEOSO 1 CARACTERISTICAS DE LOS GASES Los gases poseen masa y ocupan un determinado volumen en el espacio, este volumen queda determinado por el volumen del recipiente que los contiene.
Acuerdo 286. Química. Disoluciones. Recopiló: M.C. Macaria Hernández Chávez
 Acuerdo 286 Química Disoluciones Recopiló: M.C. Macaria Hernández Chávez Disolución: Es una mezcla homogénea de dos o más sustancias. La sustancia que se encuentra en mayor proporción se llama disolvente
Acuerdo 286 Química Disoluciones Recopiló: M.C. Macaria Hernández Chávez Disolución: Es una mezcla homogénea de dos o más sustancias. La sustancia que se encuentra en mayor proporción se llama disolvente
CLASIFICACIÓN DE LA MATERIA
 CLASIFICACIÓN DE LA MATERIA Clasificación de la materia SUSTACIACIAS PURAS SIMPLES UN SOLO TIPO DE ÁTOMO Mercurio (l) átomo de Hg Cloro(g) átomo de Cl SUSTANCIA PURA COMPUESTA S C O Zn Un solo tipo de
CLASIFICACIÓN DE LA MATERIA Clasificación de la materia SUSTACIACIAS PURAS SIMPLES UN SOLO TIPO DE ÁTOMO Mercurio (l) átomo de Hg Cloro(g) átomo de Cl SUSTANCIA PURA COMPUESTA S C O Zn Un solo tipo de
Actividades para repasar el examen de septiembre (2017)
 Actividades para repasar el examen de septiembre (2017) 1. Qué es una magnitud? Qué es medir? Pon un ejemplo que ayude a entender este concepto, utiliza un dibujo explicativo. Pon ejemplos de magnitudes
Actividades para repasar el examen de septiembre (2017) 1. Qué es una magnitud? Qué es medir? Pon un ejemplo que ayude a entender este concepto, utiliza un dibujo explicativo. Pon ejemplos de magnitudes
Teoría Disoluciones Fórmula empírica y molecular Física y Química. 1º bachiller DISOLUCIONES
 Teoría Disoluciones Fórmula empírica y molecular Física y Química. 1º bachiller 18-1-2015 CONCEPTO DE DISOLUCIÓN DISOLUCIONES Una disolución es una mezcla homogénea de sustancias en igual o distintos estados
Teoría Disoluciones Fórmula empírica y molecular Física y Química. 1º bachiller 18-1-2015 CONCEPTO DE DISOLUCIÓN DISOLUCIONES Una disolución es una mezcla homogénea de sustancias en igual o distintos estados
ESTADOS DE LA MATERIA
 ESTADOS DE LA MATERIA M en C Alicia Cea Bonilla 1 Existen tres estados de la materia: sólido, líquido y gaseoso, dependiendo de la distancia entre sus partículas, de las fuerzas de atracción entre éstas
ESTADOS DE LA MATERIA M en C Alicia Cea Bonilla 1 Existen tres estados de la materia: sólido, líquido y gaseoso, dependiendo de la distancia entre sus partículas, de las fuerzas de atracción entre éstas
TAREA 1. Nombre Núm. de lista Grupo Turno Núm. de Expediente Fecha
 TAREA 1 Nombre Núm. de lista Grupo Turno Núm. de Expediente Fecha INSTRUCCIONES: Investiga como es el puente de Hidrógeno en las estructuras del H 2 O, NH 3 y HF. Dibuja los modelos resaltando con color
TAREA 1 Nombre Núm. de lista Grupo Turno Núm. de Expediente Fecha INSTRUCCIONES: Investiga como es el puente de Hidrógeno en las estructuras del H 2 O, NH 3 y HF. Dibuja los modelos resaltando con color
Disoluciones Químicas
 Disoluciones Químicas Las disoluciones son mezclas homogéneas de dos o más sustancias, es decir, cuyos componentes no se pueden distinguir a simple vista. Siempre que se esta en presencia de una mezcla
Disoluciones Químicas Las disoluciones son mezclas homogéneas de dos o más sustancias, es decir, cuyos componentes no se pueden distinguir a simple vista. Siempre que se esta en presencia de una mezcla
Por qué es importante conocer. componentes de una disolución química?
 Por qué es importante conocer la proporción de los componentes de una disolución química? Qué será más conveniente cuando calentamos agua para cocinar algún alimento: agregar sal antes o después que hierva
Por qué es importante conocer la proporción de los componentes de una disolución química? Qué será más conveniente cuando calentamos agua para cocinar algún alimento: agregar sal antes o después que hierva
TEMA 2. ESTADOS DE LA MATERIA
 TEMA 2. ESTADOS DE LA MATERIA Estados de la materia Cambios de estado Leyes de los gases (Ver libro) 1 Estados de la materia Aire (gas) Agua sólida (hielo) Agua líquida Piensa y deduce La piedra está dentro
TEMA 2. ESTADOS DE LA MATERIA Estados de la materia Cambios de estado Leyes de los gases (Ver libro) 1 Estados de la materia Aire (gas) Agua sólida (hielo) Agua líquida Piensa y deduce La piedra está dentro
Concepto Teoría Práctica Óxidos básicos (M+O) Nomenclatura. Tablas de formulación. Nomenclatura. En tradicional se denominan anhídridos.
 Concepto Teoría Práctica Óxidos básicos (M+O) Nomenclatura. Tablas de formulación. Óxidos ácidos (NM+O) Nomenclatura. En tradicional se denominan anhídridos. Tablas de formulación. Hidruros metálicos (M+H)
Concepto Teoría Práctica Óxidos básicos (M+O) Nomenclatura. Tablas de formulación. Óxidos ácidos (NM+O) Nomenclatura. En tradicional se denominan anhídridos. Tablas de formulación. Hidruros metálicos (M+H)
03 DISOLUCIONES. 2 Observando la curva de solubilidad del clorato potásico, responder:
 03 DISOLUCIONES 1 Sabemos que cierta disolución tiene una concentración de c = 512 g/l. Si su densidad es1,43 g/l, expresa el valor de su concentración en tanto por ciento. 2 Observando la curva de solubilidad
03 DISOLUCIONES 1 Sabemos que cierta disolución tiene una concentración de c = 512 g/l. Si su densidad es1,43 g/l, expresa el valor de su concentración en tanto por ciento. 2 Observando la curva de solubilidad
ESTADOS DE AGREGACIÓN DE LA MATERIA
 LA MATERIA LA MATERIA Materia es todo aquello que ocupa un lugar en el espacio y tiene masa. La madera, el agua, el corcho, la sal,.. Son clases diferentes de materia. Las clases de materia que se utilizan
LA MATERIA LA MATERIA Materia es todo aquello que ocupa un lugar en el espacio y tiene masa. La madera, el agua, el corcho, la sal,.. Son clases diferentes de materia. Las clases de materia que se utilizan
Apuntes Disoluciones. Fórmula empírica y molecular. Propiedades coligativas Física y Química. 1º bachiller
 Apuntes Disoluciones. Fórmula empírica y molecular. Propiedades coligativas Física y Química. 1º bachiller 27-10-2016 DISOLUCIONES CONCEPTO DE DISOLUCIÓN Una disolución es una mezcla homogénea de sustancias
Apuntes Disoluciones. Fórmula empírica y molecular. Propiedades coligativas Física y Química. 1º bachiller 27-10-2016 DISOLUCIONES CONCEPTO DE DISOLUCIÓN Una disolución es una mezcla homogénea de sustancias
SUSTANCIAS PURAS (Repaso) MEZCLAS (Repaso)
 Física y Química 4 ESO DISOLUCIONES Pág. 1 SUSTANCIAS PURAS (Repaso) MEZCLAS (Repaso) Pág. 2 DISOLUCIONES Física y Química 4 ESO DISOLUCIONES CONCEPTO DE DISOLUCIÓN. COMPONENTES DE UNA DISOLUCIÓN. Una
Física y Química 4 ESO DISOLUCIONES Pág. 1 SUSTANCIAS PURAS (Repaso) MEZCLAS (Repaso) Pág. 2 DISOLUCIONES Física y Química 4 ESO DISOLUCIONES CONCEPTO DE DISOLUCIÓN. COMPONENTES DE UNA DISOLUCIÓN. Una
Algunas sustancias gaseosas a T y P ambiente
 LOS GASES Algunas sustancias gaseosas a T y P ambiente Fórmula Nombre Características O2 Oxígeno Incoloro,inodoro e insípido H 2 Hidrógeno Inflamable, más ligero que el aire. He Helio Incoloro, inerte,
LOS GASES Algunas sustancias gaseosas a T y P ambiente Fórmula Nombre Características O2 Oxígeno Incoloro,inodoro e insípido H 2 Hidrógeno Inflamable, más ligero que el aire. He Helio Incoloro, inerte,
UNIDAD 11 CALOR Y TEMPERATURA
 UNIDAD 11 CALOR Y TEMPERATURA 1.- La energía térmica Todos cuerpos están formados por partículas (átomos o moléculas) que están en continuo movimiento. Pues bien, hay una energía relacionada con el movimiento
UNIDAD 11 CALOR Y TEMPERATURA 1.- La energía térmica Todos cuerpos están formados por partículas (átomos o moléculas) que están en continuo movimiento. Pues bien, hay una energía relacionada con el movimiento
SOLUCIONES. Coordinadora de Enseñanza de Bioquímica y Biología Molecular. Fac. de Medicina. UNAM
 SOLUCIONES M. en C. Alicia Cea Bonilla Coordinadora de Enseñanza de Bioquímica y Biología Molecular. Fac. de Medicina. UNAM 1 Qué es una solución? Es una mezcla homogénea de dos o más sustancias. La sustancia
SOLUCIONES M. en C. Alicia Cea Bonilla Coordinadora de Enseñanza de Bioquímica y Biología Molecular. Fac. de Medicina. UNAM 1 Qué es una solución? Es una mezcla homogénea de dos o más sustancias. La sustancia
ACTIVIDADES DE PENDIENTES DE FÍSICA Y QUÍMICA DE 3º ESO
 ACTIVIDADES DE PENDIENTES DE FÍSICA Y QUÍMICA DE 3º ESO 1. a) Qué es la Ciencia? Qué es la Física? Qué es la Química? b) Señala qué procesos se estudian la Física y cuáles estudia la Química: a. Descenso
ACTIVIDADES DE PENDIENTES DE FÍSICA Y QUÍMICA DE 3º ESO 1. a) Qué es la Ciencia? Qué es la Física? Qué es la Química? b) Señala qué procesos se estudian la Física y cuáles estudia la Química: a. Descenso
FÍSICA Y QUÍMICA 3ºACT
 TEMA 2. LOS ESTADOS DE AGREGACIÓN DE LA MATERIA 1. DENSIDAD Todo el universo, desde las estrellas hasta la mota de polvo más pequeña, está constituido por materia. En la vida diaria, la palabra materia
TEMA 2. LOS ESTADOS DE AGREGACIÓN DE LA MATERIA 1. DENSIDAD Todo el universo, desde las estrellas hasta la mota de polvo más pequeña, está constituido por materia. En la vida diaria, la palabra materia
FACULTAD DE INGENIERÍA QUÍMICA ESCUELA DE INGENIERÍA QUÍMICA VASQUEZ BRIONES VÍCTOR ZAVALETA GARCÍA LUIS RODRIGUEZ LÁZARO YOVANY RUIZ BARAHONA EDUARDO
 ACULTAD DE INGENIERÍA QUÍMICA ESCUELA DE INGENIERÍA QUÍMICA TEMA: CURSO: PROPIEDADES DE LA MATERIA QUÍMICA GENERAL INTEGRANTES: CICLO: I-C VASQUEZ BRIONES VÍCTOR ZAVALETA GARCÍA LUIS RODRIGUEZ LÁZARO YOVANY
ACULTAD DE INGENIERÍA QUÍMICA ESCUELA DE INGENIERÍA QUÍMICA TEMA: CURSO: PROPIEDADES DE LA MATERIA QUÍMICA GENERAL INTEGRANTES: CICLO: I-C VASQUEZ BRIONES VÍCTOR ZAVALETA GARCÍA LUIS RODRIGUEZ LÁZARO YOVANY
LA MATERIA. El volumen de un líquido se mide con un recipiente graduado (pipetas y probetas) o aforados (matraz aforado.
 LA MATERIA Materia es todo aquello que ocupa espacio y tiene masa. Las propiedades de los sistemas materiales pueden ser: Propiedades generales, como la masa o el volumen. Todos los sistemas los poseen
LA MATERIA Materia es todo aquello que ocupa espacio y tiene masa. Las propiedades de los sistemas materiales pueden ser: Propiedades generales, como la masa o el volumen. Todos los sistemas los poseen
QUÍMICA. Tema 4. Estados de Agregación de la Materia
 Tema 4. Estados de Agregación de la Materia Índice - Características de sólidos, líquidos y gases - Volumen molar de los gases - Ecuación de estado de los gases - Disoluciones Objetivos específicos - Que
Tema 4. Estados de Agregación de la Materia Índice - Características de sólidos, líquidos y gases - Volumen molar de los gases - Ecuación de estado de los gases - Disoluciones Objetivos específicos - Que
EJERCICIOS DE REPASO PARA NAVIDADES
 EJERCICIOS DE REPASO PARA NAVIDADES 1) Un volumen gaseoso de un litro es calentado a presión constante desde 18 C hasta 58 C, qué volumen final ocupará el gas? (Sol: 1,14 L) 2) Una masa gaseosa a 32 C
EJERCICIOS DE REPASO PARA NAVIDADES 1) Un volumen gaseoso de un litro es calentado a presión constante desde 18 C hasta 58 C, qué volumen final ocupará el gas? (Sol: 1,14 L) 2) Una masa gaseosa a 32 C
CLASIFICACIÓN DE LA MATERIA
 1. Clasificación de la materia por su aspecto CLASIFICACIÓN DE LA MATERIA La materia homogénea es la que presenta un aspecto uniforme, en la cual no se pueden distinguir a simple vista sus componentes.
1. Clasificación de la materia por su aspecto CLASIFICACIÓN DE LA MATERIA La materia homogénea es la que presenta un aspecto uniforme, en la cual no se pueden distinguir a simple vista sus componentes.
Soluciones y unidades de concentración
 MATERIA Soluciones y unidades de concentración MEZCLAS SISTEMAS HETEROGÉNEOS Leche Arena Sal y azúcar SISTEMAS HOMOGÉNEOS Sal en agua Aire Acero COMPUESTOS Agua Etanol Benceno SUSTANCIAS PURAS ELEMENTOS
MATERIA Soluciones y unidades de concentración MEZCLAS SISTEMAS HETEROGÉNEOS Leche Arena Sal y azúcar SISTEMAS HOMOGÉNEOS Sal en agua Aire Acero COMPUESTOS Agua Etanol Benceno SUSTANCIAS PURAS ELEMENTOS
TEMA 1. LA MATERIA. PROPIEDADES. ESTADOS DE AGREGACIÓN
 TEMA 1. LA MATERIA. PROPIEDADES. ESTADOS DE AGREGACIÓN Propiedades generales de la materia Materia es todo aquello que tiene masa y volumen. La masa (cantidad de materia que posee un cuerpo) y el volumen
TEMA 1. LA MATERIA. PROPIEDADES. ESTADOS DE AGREGACIÓN Propiedades generales de la materia Materia es todo aquello que tiene masa y volumen. La masa (cantidad de materia que posee un cuerpo) y el volumen
Disoluciones y cálculos de concentraciones
 Disoluciones y cálculos de concentraciones Disoluciones Una disolución es una mezcla homogénea (los componentes no se pueden distinguir a simple vista) de dos o más sustancias en proporciones variables.
Disoluciones y cálculos de concentraciones Disoluciones Una disolución es una mezcla homogénea (los componentes no se pueden distinguir a simple vista) de dos o más sustancias en proporciones variables.
Temperatura de fusión Conductividad Longitud Color
 TEMA 2: Sistemas materiales. 1. Propiedades de los sistemas materiales: a) Masa y volumen. b) Densidad. 2. Cambios de estado. 3. Teoría cinético molecular. a) Postulados. b) Interpretación de las características
TEMA 2: Sistemas materiales. 1. Propiedades de los sistemas materiales: a) Masa y volumen. b) Densidad. 2. Cambios de estado. 3. Teoría cinético molecular. a) Postulados. b) Interpretación de las características
El aire de la atmósfera (78% N 2 ; 21% O 2 ; 1% Ar, He, CO 2 y vapor de agua) y el agua del mar son ejemplos de soluciones.
 SOLUCIONES la materia se presenta, con mayor frecuencia, en forma de mezcla de sustancias puras. dentro de éstas mezclas hay que distinguir las: I) mezclas propiamente dichas II) y las soluciones. El aire
SOLUCIONES la materia se presenta, con mayor frecuencia, en forma de mezcla de sustancias puras. dentro de éstas mezclas hay que distinguir las: I) mezclas propiamente dichas II) y las soluciones. El aire
La infinidad de cosas que nos rodean están constituidas de pequeñas partículas en movimiento.
 La infinidad de cosas que nos rodean están constituidas de pequeñas partículas en movimiento. Estas partículas no las podemos ver con nuestros ojos, pero las podemos imaginar así De los materiales que
La infinidad de cosas que nos rodean están constituidas de pequeñas partículas en movimiento. Estas partículas no las podemos ver con nuestros ojos, pero las podemos imaginar así De los materiales que
BLOQUE 1: ASPECTOS CUANTATIVOS DE LA QUÍMICA
 BLOQUE 1: ASPECTOS CUANTATIVOS DE LA QUÍMICA Unidad 2: Los gases ideales Teresa Esparza araña 1 Índice 1. Los estados de agregación de la materia a. Los estados de la materia b. Explicación según la teoría
BLOQUE 1: ASPECTOS CUANTATIVOS DE LA QUÍMICA Unidad 2: Los gases ideales Teresa Esparza araña 1 Índice 1. Los estados de agregación de la materia a. Los estados de la materia b. Explicación según la teoría
TEMA 7: Problemas de Química
 TEMA 7: Problemas de Química Tema 7: Problemas de Química 1 1.- REACCIONES QUÍMICAS Una reacción química es un proceso en el que se unen varias sustancias llamadas reactivos y se transforman en otras sustancias
TEMA 7: Problemas de Química Tema 7: Problemas de Química 1 1.- REACCIONES QUÍMICAS Una reacción química es un proceso en el que se unen varias sustancias llamadas reactivos y se transforman en otras sustancias
TEMA 2 La materia y sus propiedades QUÉ ES LA MATERIA? ESTADOS DE LA MATERIA CAMBIOS DE ESTADO MODELO CINÉTICO-MOLECULAR
 TEMA 2 La materia y sus propiedades QUÉ ES LA MATERIA? ESTADOS DE LA MATERIA CAMBIOS DE ESTADO MODELO CINÉTICO-MOLECULAR 1. QUÉ ES LA MATERIA? El universo que conocemos, puede definirse en términos de
TEMA 2 La materia y sus propiedades QUÉ ES LA MATERIA? ESTADOS DE LA MATERIA CAMBIOS DE ESTADO MODELO CINÉTICO-MOLECULAR 1. QUÉ ES LA MATERIA? El universo que conocemos, puede definirse en términos de
EL ESTADO GASEOSO P R E S I Ó N
 EL ESTADO GASEOSO El aire está compuesto, principalmente, de los elementos oxígeno y nitrógeno. Otros elementos no metálicos existen en la naturaleza como gases en condiciones ordinarias como hidrógeno
EL ESTADO GASEOSO El aire está compuesto, principalmente, de los elementos oxígeno y nitrógeno. Otros elementos no metálicos existen en la naturaleza como gases en condiciones ordinarias como hidrógeno
Qué es la materia? A qué llamamos sustancias? Qué dos clases de propiedades posee la materia? Por qué se llaman propiedades generales?
 La materia es aquello que ocupa un lugar en el espacio y cuyas propiedades percibimos por los sentidos ( vista, tacto...). Todos los objetos que observamos a nuestro alrededor tienen algo en común : es
La materia es aquello que ocupa un lugar en el espacio y cuyas propiedades percibimos por los sentidos ( vista, tacto...). Todos los objetos que observamos a nuestro alrededor tienen algo en común : es
1 Características de los estados de agregación
 2 Estados de agregación 1 Características de los estados de agregación Qué caracteriza cada estado de la materia Forma y volumen La forma que tienen los sólidos es constante. Los líquidos adaptan su forma
2 Estados de agregación 1 Características de los estados de agregación Qué caracteriza cada estado de la materia Forma y volumen La forma que tienen los sólidos es constante. Los líquidos adaptan su forma
3. Física del Buceo. Séptima Compañía de Bomberos Acción y Disciplina Tome Dichato Fundada el 24 de Octubre de 1975 GERSA
 3. Física del Buceo Séptima Compañía de Bomberos Acción y Disciplina Tome Dichato Fundada el 24 de Octubre de 1975 GERSA 1. Conceptos básicos y unidades de medida 1.1 Materia y sus estados Es todo aquello
3. Física del Buceo Séptima Compañía de Bomberos Acción y Disciplina Tome Dichato Fundada el 24 de Octubre de 1975 GERSA 1. Conceptos básicos y unidades de medida 1.1 Materia y sus estados Es todo aquello
SOLUCIONES SOLIDA LIQUIDA GASEOSA. mezclas homogéneas de dos sustancias: SEGÚN EL ESTADO FISICO DEL SOLVENTE
 Soluciones SOLUCIONES mezclas homogéneas de dos sustancias: SOLUTO SOLVENTE SEGÚN EL ESTADO FISICO DEL SOLVENTE SOLIDA LIQUIDA GASEOSA Cuando un sólido se disuelve en un líquido las partículas que lo
Soluciones SOLUCIONES mezclas homogéneas de dos sustancias: SOLUTO SOLVENTE SEGÚN EL ESTADO FISICO DEL SOLVENTE SOLIDA LIQUIDA GASEOSA Cuando un sólido se disuelve en un líquido las partículas que lo
FÍSICA Y QUÍMICA 2º ESO TEMA V LA MATERIA Y SUS PROPIEDADES
 FÍSICA Y QUÍMICA 2º ESO TEMA V LA MATERIA Y SUS PROPIEDADES 1. MASA Y VOLUMEN. La masa (m) es la cantidad de materia que tiene un cuerpo. Su unidad en el S.I. es el kg. Para medir la masa de un cuerpo
FÍSICA Y QUÍMICA 2º ESO TEMA V LA MATERIA Y SUS PROPIEDADES 1. MASA Y VOLUMEN. La masa (m) es la cantidad de materia que tiene un cuerpo. Su unidad en el S.I. es el kg. Para medir la masa de un cuerpo
1 TEMA 11: La materia CRA Sexma de La Sierra. CoNoTiC. *Esquema conceptual: 11. LA MATERIA
 1 TEMA 11: La materia CRA Sexma de La Sierra. CoNoTiC *Esquema conceptual: 11. LA MATERIA 2 TEMA 11: La materia CRA Sexma de La Sierra. CoNoTiC 1. La materia y sus propiedades A través de los sentidos
1 TEMA 11: La materia CRA Sexma de La Sierra. CoNoTiC *Esquema conceptual: 11. LA MATERIA 2 TEMA 11: La materia CRA Sexma de La Sierra. CoNoTiC 1. La materia y sus propiedades A través de los sentidos
TEMA 3 LAS DISOLUCIONES
 TEMA 3 LAS DISOLUCIONES 1.- DISOLUCIÓN: COMPONENTES Y TIPOS DE DISOLUCIONES 1.1- EL PROCESO DE DISOLUCIÓN - FACTORES QUE AFECTAN AL PROCESO DE DISOLUCIÓN 1.2-LA CONCENTRACIÓN - % EN MASA -% EN VOLUMEN
TEMA 3 LAS DISOLUCIONES 1.- DISOLUCIÓN: COMPONENTES Y TIPOS DE DISOLUCIONES 1.1- EL PROCESO DE DISOLUCIÓN - FACTORES QUE AFECTAN AL PROCESO DE DISOLUCIÓN 1.2-LA CONCENTRACIÓN - % EN MASA -% EN VOLUMEN
Principios y conceptos básicos de Química
 Principios y conceptos básicos de Química Se estudiarán durante las dos primeras quincenas, estos contenidos están en el tema 2 del libro de texto. Quincena 1ª - Repaso de conceptos estudiados en ESO (Densidad,
Principios y conceptos básicos de Química Se estudiarán durante las dos primeras quincenas, estos contenidos están en el tema 2 del libro de texto. Quincena 1ª - Repaso de conceptos estudiados en ESO (Densidad,
2. Métodos de separación de los componentes de una mezcla.
 TEMA 3: Mezclas, disoluciones y sustancias puras. 1. Clasificación de la materia. 2. Métodos de separación de los componentes de una mezcla. 3. Disoluciones. a) Definición. b) Cómo se preparan. c) Concentración.
TEMA 3: Mezclas, disoluciones y sustancias puras. 1. Clasificación de la materia. 2. Métodos de separación de los componentes de una mezcla. 3. Disoluciones. a) Definición. b) Cómo se preparan. c) Concentración.
LA MATERIA 1. Teoría atómica de Dalton. 2. La materia. 3. Leyes químicas. 4. El mol. 5. Leyes de los gases ideales. 6. Símbolos y fórmulas.
 LA MATERIA 1. Teoría atómica de Dalton. 2. La materia. 3. Leyes químicas. 4. El mol. 5. Leyes de los gases ideales. 6. Símbolos y fórmulas. Química 1º bachillerato La materia 1 1. TEORÍA ATÓMICA DE DALTON
LA MATERIA 1. Teoría atómica de Dalton. 2. La materia. 3. Leyes químicas. 4. El mol. 5. Leyes de los gases ideales. 6. Símbolos y fórmulas. Química 1º bachillerato La materia 1 1. TEORÍA ATÓMICA DE DALTON
Departamento Ciencias. Física y Química MATERIA. se clasifica en. SUSTANCIAS PURAS pueden ser. por métodos. físicos originan. Compuestos.
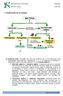 1. Clasificación de la materia MATERIA se clasifica en MEZCLAS pueden ser por métodos físicos originan SUSTANCIAS PURAS pueden ser Heterogéneas Homogéneas Compuestos como las Disoluciones formados por
1. Clasificación de la materia MATERIA se clasifica en MEZCLAS pueden ser por métodos físicos originan SUSTANCIAS PURAS pueden ser Heterogéneas Homogéneas Compuestos como las Disoluciones formados por
TEMA 2: LA DIVERSIDAD DE LA MATERIA 3º ESO
 TEMA 2: LA DIVERSIDAD DE LA MATERIA 3º ESO 1. Clasificaciones de los sistema materiales. Un sistema material es una porción de materia que se separa para facilitar su estudio experimental. Como existe
TEMA 2: LA DIVERSIDAD DE LA MATERIA 3º ESO 1. Clasificaciones de los sistema materiales. Un sistema material es una porción de materia que se separa para facilitar su estudio experimental. Como existe
Teoría Mol Nº Avogadro Gases perfectos Física y Química. 1º bachiller CONCEPTOS PREVIOS
 CONCEPTOS PREVIOS Masa atómica: Es la masa de un átomo en reposo. En cursos anteriores denominábamos número atómico a la masa de un átomo (protones + neutrones). Pero los elementos tienen átomos con diferente
CONCEPTOS PREVIOS Masa atómica: Es la masa de un átomo en reposo. En cursos anteriores denominábamos número atómico a la masa de un átomo (protones + neutrones). Pero los elementos tienen átomos con diferente
REACCIONES QUÍMICAS MASA MOLES MOLÉCULAS ÁTOMOS ÁTOMOS. Factor de conversión N A = 6, partículas/mol
 REACCIONES QUÍMICAS CANTIDAD DE MATERIA La cantidad de sustancia se puede expresar en gramos (masa), en moles, moléculas o átomos. Podemos pasar de unas unidades a otras utilizando el siguiente esquema:
REACCIONES QUÍMICAS CANTIDAD DE MATERIA La cantidad de sustancia se puede expresar en gramos (masa), en moles, moléculas o átomos. Podemos pasar de unas unidades a otras utilizando el siguiente esquema:
TEMA 2: LA MATERIA: CÓMO SE PRESENTA?
 TEMA 2: LA MATERIA: CÓMO SE PRESENTA? 1.- La materia: sustancias puras y mezclas. 1.1.- Recordatorio. 1.2.- Sustancias puras. 1.3.- Mezclas. 1.4.- Cómo distinguir un coloide de una mezcla homogénea. 2.-
TEMA 2: LA MATERIA: CÓMO SE PRESENTA? 1.- La materia: sustancias puras y mezclas. 1.1.- Recordatorio. 1.2.- Sustancias puras. 1.3.- Mezclas. 1.4.- Cómo distinguir un coloide de una mezcla homogénea. 2.-
Unidad 2. La materia
 Física y Química Unidad 2: La materia Unidad 2. La materia Índice de contenido 1. Estados de agregación de la materia...3 2. Cambios de estado...4 3. Clasificación de la materia...6 3.1.- Métodos de separación
Física y Química Unidad 2: La materia Unidad 2. La materia Índice de contenido 1. Estados de agregación de la materia...3 2. Cambios de estado...4 3. Clasificación de la materia...6 3.1.- Métodos de separación
ESTADO GASEOSO LEYES PARA GASES IDEALES
 ESTADO GASEOSO LEYES PARA GASES IDEALES Estados de agregación COMPORTAMIENTO DE LOS GASES No tienen forma definida ni volumen propio Sus moléculas se mueven libremente y al azar ocupando todo el volumen
ESTADO GASEOSO LEYES PARA GASES IDEALES Estados de agregación COMPORTAMIENTO DE LOS GASES No tienen forma definida ni volumen propio Sus moléculas se mueven libremente y al azar ocupando todo el volumen
PROBLEMAS MEZCLAS Y DISOLUCIONES
 PROBLEMAS MEZCLAS Y DISOLUCIONES 1. Clasifica como homogéneos o heterogéneos los siguientes sistemas materiales: un trozo de cobre, agua salada, hierro oxidado, una ensalada. 2. Al mezclar dos sistemas
PROBLEMAS MEZCLAS Y DISOLUCIONES 1. Clasifica como homogéneos o heterogéneos los siguientes sistemas materiales: un trozo de cobre, agua salada, hierro oxidado, una ensalada. 2. Al mezclar dos sistemas
