Kit de lisis BD GeneOhm MRSA ACP
|
|
|
- Ernesto Hidalgo Segura
- hace 7 años
- Vistas:
Transcripción
1 REF pruebas P0071(03)_ES Fecha:
2 ÍNDICE USO PREVISTO... 3 RESUMEN Y EXPLICACIÓN DEL PROCEDIMIENTO... 3 REACTIVOS... 3 PRECAUCIONES... 3 MATERIALES SUMINISTRADOS... 4 CONSERVACIÓN, MANEJO Y ESTABILIDAD... 4 MUESTRAS RECOGIDAS... 4 TAMPÓN DE MUESTRAS CON LA MUESTRA ELUÍDA... 4 LISADOS DE MUESTRAS Y DE CONTROL... 4 REACTIVOS... 4 MATERIALES NECESARIOS PERO NO SUMINISTRADOS... 5 INSTRUCCIONES DE USO... 5 PREPARACIÓN Y CONSERVACIÓN DEL REACTIVO DE LISIS... 5 OBTENCIÓN DE LAS MUESTRAS... 5 PREPARACIÓN DE LAS MUESTRAS... 6 LISIS DE LAS MUESTRAS... 6 CONTROL DE CALIDAD... 7 CONTROLES (POSITIVOS Y NEGATIVOS) DE LA PRUEBA... 7 CONTROLES (POSITIVOS Y NEGATIVOS) DE PROCESAMIENTO DE MUESTRAS... 7 CULTIVO DE MUESTRAS CLÍNICAS... 7 MÉTODO DE EXTENSIÓN EN PLACA... 7 CALDO DE ENRIQUECIMIENTO... 7 LIMITACIONES DEL PROCEDIMIENTO... 8 EFICIENCIA DE LA LISIS... 8 REFERENCIAS... 8 ÍNDICE DE SÍMBOLOS... 9 P0071(03)_ES - 2 -
3 ESPAÑOL Uso previsto El kit de lisis BD GeneOhm MRSA ACP ofrece un método simplificado para la lisis de células de Staphylococcus aureus a partir de muestras obtenidas mediante torunda nasal antes de su análisis con la prueba BD GeneOhm MRSA ACP. Resumen y explicación del procedimiento El kit de lisis BD GeneOhm MRSA ACP incorpora una tecnología de lisis enzimática con acromopeptidasa (ACP) para la preparación de las muestras, obtenidas mediante torundas nasales, que serán utilizadas con la prueba BD GeneOhm MRSA ACP. El reactivo de lisis se reconstituye con diluyente de lisis y se dispensa en alícuotas en tubos de lisis de un solo uso. La muestra se recoge mediante una torunda nasal y se transporta al laboratorio utilizando el dispositivo de transporte de torundas recomendado (véase Materiales necesarios pero no suministrados ). La torunda nasal se rompe dentro de un tubo de tampón de muestras. Después se transfiere una alícuota de la suspensión obtenida al tubo que contiene el reactivo de lisis y se incuba para romper la pared celular bacteriana y liberar el material genético de la célula. Después se procesa una alícuota de la muestra lisada con la prueba BD GeneOhm MRSA ACP. Reactivos Diluyente de lisis (Lysis Diluent) Cantidad 1 x 3,7 ml Tampón tris-edta para la reconstitución enzimática Reactivo de lisis (Lysis Reagent) 1 frasco Enzima lítica seca ACP (15,1 KU) Tampón de muestras (Sample Buffer) 162 x 600 µl Tampón tris-edta para la preparación de las muestras y del control negativo, y para la reconstitución del ADN de control positivo. Precauciones Para uso diagnóstico in vitro. No utilizar el kit si el precinto de seguridad de la caja exterior está roto. No utilizar los reactivos si las bolsas protectoras están abiertas o desgarradas a su llegada. Cerrar las bolsas protectoras del tampón de muestras con el cierre rápido después de cada uso. No utilizar el reactivo de lisis si el desecante está roto o ausente dentro de la bolsa. No mezclar reactivos ni intercambiar lotes de reactivos. No utilizar los reactivos después de su fecha de caducidad. Evitar la contaminación de los reactivos con microorganismos y con desoxirribonucleasa (ADNasa) cuando se extraigan alícuotas de los tubos. Se recomienda el uso de puntas de pipeta estériles y desechables, libres de ADNasa y con filtro, o puntas para pipetas de desplazamiento positivo. Aunque la principal operación técnica es el pipeteo, es esencial una buena práctica de laboratorio para la realización correcta de este procedimiento. Debido a la elevada sensibilidad analítica de la prueba BD GeneOhm MRSA ACP, hay que tener un cuidado especial en conservar la pureza de todos los reactivos, especialmente en caso de que se extraigan varias alícuotas de un tubo. Utilizar una punta de pipeta con un diámetro lo bastante pequeño para llegar hasta el líquido que está en el fondo de cada tubo de muestra o de reactivo. La realización de los pasos de lisis fuera de los plazos recomendados puede afectar a la amplificación del ADN y producir resultados inválidos. Las lisis no realizadas dentro de los plazos especificados deben repetirse. Se pueden analizar controles adicionales de acuerdo con las directrices o requisitos de la normativa local, estatal, provincial o federal, o de las organizaciones de acreditación. En los casos en que se lleven a cabo pruebas de PCR con tubo abierto en la misma zona general del laboratorio, hay que utilizar zonas de trabajo separadas y segregadas para la preparación de muestras y para las actividades de amplificación/detección. El material y los equipos utilizados deben ser específicos para cada zona y no deben trasladarse de una zona a otra. Hay que llevar siempre guantes y cambiarlos antes de trasladarse de una zona a otra. Manejar siempre las muestras como si fueran infecciosas y de conformidad con procedimientos de laboratorio seguros tales como los descritos en Biosafety in Microbiological and Biomedical Laboratories 1 y en el Documento M29 del CLSI 2. Llevar indumentaria protectora y guantes desechables cuando se manejen reactivos del kit. Lavarse bien las manos después de realizar la prueba. No pipetear con la boca. P0071(03)_ES - 3 -
4 No fumar, beber ni comer en áreas donde se manipulen muestras o reactivos del kit. Desechar los reactivos no utilizados y los desechos de conformidad con la normativa nacional, federal, provincial, estatal y local. Materiales suministrados Diluyente de lisis (Lysis Diluent) Reactivo de lisis (Lysis Reagent) Tubos de tampón de muestras (Sample Buffer) Tapones a rosca Tapones con septum Tubos de almacenamiento Conservación, manejo y estabilidad Muestras recogidas Las muestras deben mantenerse entre 2 y 25 C durante el transporte. Proteger las muestras frente a la congelación o la exposición a un calor excesivo. Las muestras pueden conservarse hasta 48 horas a C o 5 días a 2 8 C antes de su análisis. Tampón de muestras con la muestra eluída La muestra eluída en el tubo de tampón de muestras es estable hasta 72 horas a 2 8 C (p. ej., para repetir el análisis). Lisados de muestras y del control Los lisados de muestras y del control son estables hasta 4 horas a 2 8 C en tubo con tapón a rosca o con septum, o bien 8 días a -20 C en tubos con tapón a rosca. Reactivos Nota: Se deben seguir las especificaciones escritas en cada bolsa en relación a las condiciones de conservación. Condiciones de conservación del tampón de muestras (Sample Buffer, tapón azul) Bolsa cerrada Bolsa abierta Temperatura 2 25 C Estabilidad Fecha de caducidad Temperatura C Estabilidad 2 1 mes 1 Aunque estos reactivos se pueden conservar a temperatura ambiente, deben mantenerse con sus reactivos acompañantes del mismo lote a 2 8 C. 2 Siempre que la bolsa se cierre debidamente con el cierre rápido después de cada uso. Condiciones de conservación del reactivo de lisis (Lysis Reagent) Reactivo de lisis (en frasco original sin reconstituir) Reconstituido y dispensado en alícuotas en el tubo de lisis cerrado con tapón con septum Reconstituido y dispensado en alícuotas en el tubo de lisis cerrado con tapón a rosca 15,1 KU 20 µl 20 µl Temperatura 2 25 C Estabilidad Fecha de caducidad Temperatura 2 8 ºC Estabilidad 1 semana Temperatura 2 8 ºC Estabilidad 1 mes P0071(03)_ES - 4 -
5 Materiales necesarios pero no suministrados Torunda sencilla o doble con líquido de Stuart BBL CultureSwab (Nº de catálogo de BD ó ), torunda sencilla o doble con líquido de Stuart Copan (Venturi) Transystem (Nº de catálogo de Copan 141C o 139C), o bien Torunda sencilla o doble con líquido de Amies BBL CultureSwab (Nº de catálogo de BD ó ), torunda sencilla o doble con líquido de Amies Copan (Venturi) Transystem (Nº de catálogo de Copan 140C o 138C), o bien Torunda sencilla o doble con gel de Amies sin carbón BBL CultureSwab Plus (Nº de catálogo de BD ó ), torunda sencilla o doble con gel de agar de Amies sin carbón Copan (Venturi) Transystem (Nº de catálogo de Copan 180C o 134C). Prueba BD GeneOhm MRSA ACP (Nº de catálogo de BD ó ). Vórtex Genie 2 (Nº de catálogo de VWR ) con soporte para microtubos de 1,5 ml o equivalente; para procesar múltiples muestras se puede usar un adaptador diseñado para múltiples tubos (Nº de catálogo de VWR ) O BIEN VWR Signature Multi-Tube Vortexer (VWR ). Bloque térmico seco específico para tubos de 1,5 ml a 37 +/- 2 ºC. Bloque térmico seco específico para tubos de 1,5 ml a 99 +/- 2 ºC. Hielo o bloque refrigerador para tubos de 1,5 ml. Micropipetas calibradas (intervalo de precisión entre µl y µl). Puntas de micropipeta estériles, libres de ADNasa y bloqueadas con filtro o de desplazamiento positivo ( µl y µl). Reactivos para tinción de Gram (opcionales). BBL CHROMagar Staph. aureus (Nº de catálogo de BD Diagnostic Systems ), BBL CHROMagar MRSA (Nº de catálogo de BD Diagnostic Systems ), agar manitol sal (MSA, Nº de catálogo de BD Diagnostic Systems ó o medios equivalentes; opcional). TSB (caldo de triptona y soja) suplementado con NaCl al 6,5% (Nº de catálogo de BD Diagnostic Systems , opcional). Placa de agar sangre de carnero al 5% (p. ej., agar de triptona y soja BBL Trypticase Soy Agar [TSA II] con sangre de carnero al 5%, Nº de catálogo de BD Diagnostic Systems ó ; opcional). Guantes desechables, sin talco. Tijeras (opcionales). Gasa. Cronómetro o temporizador. Instrucciones de uso Preparación y conservación del reactivo de lisis 1. Verter la totalidad del contenido del tubo de diluyente de lisis en el frasco del reactivo de lisis. 2. Volver a cerrar herméticamente el frasco y agitar en vórtex a alta velocidad durante 30 segundos. 3. Dejar reposar el reactivo de lisis reconstituido a temperatura ambiente durante 20 minutos. 4. Agitar el frasco de reactivo de lisis en vórtex a alta velocidad durante 30 segundos. Nota: una vez reconstituido, todo el contenido del frasco de reactivo de lisis debe repartirse en alícuotas dentro de los tubos de lisis individuales de un solo uso 5. Utilizando una pipeta de repetición, dispensar 20 µl de reactivo de lisis reconstituido en los tubos de lisis de un solo uso (1 frasco de reactivo de lisis a granel es suficiente para un máximo de 160 reacciones). 6. Tapar los tubos con tapones con septum o con tapones a rosca y rotularlos con la fecha de caducidad correspondiente. 7. Conservar los tubos de lisis entre 2 y 8 C. Nota: el reactivo de lisis conservado en un tubo con tapón con septum es estable hasta 7 días, y hasta 30 días cuando se conserva en tubo con tapón a rosca (véase la sección titulada Conservación, manejo y estabilidad: reactivos). Obtención de las muestras Utilizando un dispositivo de transporte de torundas recomendado (véase Materiales necesarios pero no suministrados ), las muestras nasales deben recogerse conforme a los procedimientos operativos habituales del hospital y teniendo en cuenta las siguientes recomendaciones: 1. Humedecer la(s) torunda(s) con solución salina fisiológica estéril o utilizarla(s) seca(s). 2. Insertar cuidadosamente la torunda en una fosa nasal del paciente (la punta de la torunda debe introducirse hasta 2,5 cm desde el borde del orificio nasal). 3. Hacer girar la(s) torunda(s) 5 veces sobre la mucosa interior de la fosa nasal. 4. Insertar la(s) misma(s) torunda(s) en la otra fosa nasal y repetir los pasos 2 y Volver a colocar la(s) torunda(s) en su tubo de transporte. 6. Rotular el tubo de transporte. 7. Enviar la(s) torunda(s) al laboratorio siguiendo los procedimientos habituales del hospital (véase la section Conservación, manejo y estabilidad: muestras recogidas). P0071(03)_ES - 5 -
6 Preparación de las muestras Nota: Se necesita un (1) tubo de tampón de muestras (Sample Buffer, tapón azul) por cada muestra a procesar. En su caso, harían falta dos (2) tubos adicionales de tampón de muestras (tapón azul) por serie para los controles de procesamiento de las muestras (CPM; véase la sección de "Control de calidad" más abajo para conocer datos acerca de la preparación). Extraer el número necesario de tubos de su bolsa protectora y después extraer el exceso de aire y cerrar la bolsa con el cierre rápido tras extraer los tubos. Comprobar que la bolsa protectora quede herméticamente cerrada. Importante: para cultivar muestras clínicas, consultar más abajo la sección Cultivo de muestras clínicas. 1. Rotular cada tubo de tampón de muestras (tapón azul) con la identificación adecuada. 2. Retirar la torunda del tubo de transporte de muestras y colocarla en el tubo de tampón de muestras (tapón azul) correspondiente. 3. Romper el vástago de la torunda y cerrar bien el tubo con el tapón a rosca. Sostener la torunda por el vástago cerca del borde del tubo (utilizar una gasa para reducir al mínimo el riesgo de contaminación). Levantar la torunda aproximadamente un (1) cm del fondo (cerca del nivel del líquido) y doblar el vástago contra el borde del tubo para romperlo. Método alternativo: usar unas tijeras limpias para cortar el vástago. 4. Agitar los tubos de tampón de muestras en vórtex durante 60 segundos a alta velocidad. Para procesar múltiples muestras se puede utilizar un adaptador diseñado para múltiples tubos. Lisis de las muestras Nota: En cada serie se necesita un (1) tubo de tampón de muestras (Sample Buffer, tapón azul) para la reconstitución del ADN de control (Control DNA, control positivo) y para utilizarlo como control negativo. También es necesario un (1) tubo de lisis con 20 µl de reactivo de lisis alicuotado por cada muestra. Además, son necesarios dos (2) tubos de lisis adicionales por serie para los controles de PCR. Hay que incluir un (1) control de PCR positivo y uno (1) negativo por cada ensayo con la prueba BD GeneOhm MRSA ACP. Se necesita un tubo de control de ADN (etiqueta con banda roja) de la prueba BD GeneOhm MRSA ACP por serie. Retirar el número necesario de tubos de su bolsa protectora, extraer el exceso de aire y cerrar las bolsas con el cierre rápido tras extraer los tubos. Comprobar que la bolsa protectora quede herméticamente cerrada. 1. Rotular cada tubo de lisis (alícuota de 20 µl) con la identificación adecuada. 2. Añadir 225 µl de tampón de muestras (tapón azul) al tubo de ADN de control. Comprobar que el pellet de ADN de control esté en el fondo del tubo. Insertar la punta de la micropipeta a través de la membrana del tapón. No insertar la punta a demasiada profundidad en el tapón. Dispensar tampón de muestras en el tubo. Guardar el resto del tampón de muestras para el control negativo. 3. Una vez reconstituido, agitar el tubo de ADN de control en vórtex durante 5 10 segundos. Hasta el momento de su procesamiento, colocar el tubo sobre hielo o sobre un bloque refrigerador diseñado para tubos de 1,5 ml. 4. Utilizando una micropipeta con puntas desechables nuevas por cada muestra y control, añadir 90 µl de la suspensión de muestra eluída directamente al tubo de lisis correspondiente pipeteando a través del septum o desenroscando el tapón. 5. Añadir 90 µl de control positivo (ADN reconstituido) a un tubo de lisis. Retirar con cuidado el tapón con septum del tubo de control positivo antes de pipetear el control positivo en el tubo de lisis. Después de pipetear, volver a cerrar el tubo de control positivo con el tapón con septum original. Conservar el tubo de control positivo por si fuera necesario repetir el análisis.. 6. Añadir 90 µl de control negativo (tampón de muestras) a un tubo de lisis. Los tubos de tampón de muestras (muestra, controles y CPM, en su caso) se pueden conservar a 2 8 C hasta 72 horas para realizar pruebas de seguimiento. 7. Incubar los tubos de lisis que contienen muestras y controles en un bloque térmico a 37 +/- 2 C durante 20 minutos (paso de lisis). Nota: es importante incubar los tubos en el intervalo de temperatura especificado. 8. Transferir los tubos de lisis a un bloque térmico a 99 +/- 2 C e incubarlos durante 5 minutos (paso de inactivación). Nota: es importante incubar los tubos en el intervalo de temperatura especificado. 9. Transferir los tubos de lisis a un bloque refrigerador (2 8 C) y dejarlos reposar durante 10 minutos. Si los lisados no van a ser utilizados en un plazo de 4 horas, cambiar el tapón con septum (en su caso) por un tapón a rosca y conservar los tubos a -20 C. 10. Consultar la ficha técnica de la prueba BD GeneOhm MRSA ACP para continuar el análisis. P0071(03)_ES - 6 -
7 Control de calidad Controles (positivos y negativos) de la prueba Los procedimientos de control de calidad están diseñados para controlar el rendimiento de la prueba BD GeneOhm MRSA ACP. El control negativo se utiliza para detectar la contaminación (o el arrastre) de los reactivos o del entorno por ADN o por amplicones de SARM. Hay que incluir un control positivo y uno negativo en cada serie de análisis. Preparar los controles según las instrucciones que se describen en la sección Lisis de las muestras de este documento.. Controles (positivos y negativos) de procesamiento de muestras Se recomienda utilizar controles de procesamiento de muestras (CPM) para ofrecer garantías de que no se produce una contaminación cruzada significativa y para controlar fallos sustanciales de los reactivos o de la metodología durante el procedimiento. Pueden analizarse cepas de control adicionales como CPM, en conformidad con las directrices o requisitos de la normativa local, estatal o federal, o de las organizaciones de acreditación. Se puede utilizar como CPM positivo una cepa de SARM de referencia (p. ej., ATCC 43300) o un aislado clínico de SARM bien caracterizado; si se dispone de las cepas de SARM MREJ tipo iii y vii, se pueden utilizar como CPM positivos adicionales, para controlar las sondas y cebadores de la prueba no directamente controlados en la misma. Como CPM negativo se puede utilizar una cepa de Staphylococcus aureus sensible a la meticilina (p. ej., ATCC 25923) o cualquier otro Staphylococcus no aureus (p. ej., Staphylococcus epidermidis ATCC 14990). Los CPM se preparan de la siguiente manera: incubar las colonias en agar sangre de carnero al 5% entre 18 y 24 horas. Resuspender las colonias aisladas en solución salina hasta una turbidez de 0,5 McFarland. Diluir con solución salina hasta obtener una suspensión de ~10 6 UFC/mL. Sumergir la torunda recomendada (véase la sección Materiales necesarios pero no suministrados ) en la suspensión bacteriana, exprimir el exceso de líquido y ponerla en un tubo de tampón de muestras debidamente identificado. Procesar y analizar como una muestra, junto con los correspondientes controles de PCR. Se puede obtener información adicional en la sección Preparación de las muestras y en la ficha técnica de la prueba BD GeneOhm MRSA ACP. Para obtener una orientación general acerca del control de calidad, el usuario puede consultar los documentos del CLSI MM3 3 y C24 4. Cultivo de muestras clínicas Para realizar pruebas de sensibilidad a antimicrobianos o tipado epidemiológico adicional, las muestras clínicas se pueden cultivar a partir del dispositivo de recogida (torunda) antes de llevar a cabo el procedimiento de preparación de las muestras (utilizando el método de extensión en placa) o después del procedimiento de preparación de las muestras (utilizando el método del caldo de enriquecimiento). Las torundas pueden conservarse en tubos de tampón de muestras cerrados a 2 8 C hasta 24 horas antes de cultivarlas. Método de extensión en placa Este método de cultivo puede llevarse a cabo con torundas de muestras antes del procedimiento de lisis de la muestra. 1. Retirar el dispositivo de recogida (torunda) de su tubo de transporte. 2. Inocular un medio sólido adecuado (p.ej. una placa de agar manitol sal o de BBL CHROMagar MRSA) extendiendo la muestra en el primer cuadrante de la placa. 3. Devolver la torunda a su tubo de transporte o romperla en un tubo de tampón de muestras (tapón azul) del kit de lisis BD GeneOhm MRSA ACP y continuar según las instrucciones de Preparación de las muestras. 4. Utilizando un asa o aguja estéril, extender el inóculo sobre los restantes cuadrantes. 5. Incubar la placa durante horas a 35 ± 2 ºC. 6. Identificar y confirmar las colonias de S. aureus y analizar su resistencia a la meticilina según las instrucciones de uso del fabricante de la placa. Caldo de enriquecimiento Este método de cultivo puede llevarse a cabo con las torundas que quedan en los tubos después de extraer la suspensión celular eluída, antes del paso de lisis de las muestras. Las torundas pueden conservarse a 2 8 C en tubos de tampón de muestras cerrados hasta 24 horas antes de cultivarlas. 1. Transferir la suspensión celular restante a un microtubo para su uso futuro, si fuera necesario. 2. Añadir 1,0 ml de caldo de enriquecimiento al tubo de tampón de muestras que contiene la torunda. Se recomienda TSB (caldo de triptona y soja) suplementado con NaCl al 6,5%. 3. Agitar el caldo de enriquecimiento inoculado en vórtex durante 2 5 segundos. 4. Incubar durante horas a 35 ± 2 ºC. Si no se observa ningún crecimiento, incubar durante 24 horas más. 5. Subcultivar en un medio sólido adecuado e incubar durante horas a 35 ± 2 ºC (p. ej. en una placa de agar sangre de carnero al 5%, agar manitol sal o BBL CHROMagar MRSA). 6. Identificar y confirmar las colonias de S. aureus y analizar su resistencia a la meticilina según las instrucciones de uso del fabricante de la placa. P0071(03)_ES - 7 -
8 Limitaciones del procedimiento Este producto está indicado para ser utilizado únicamente con la prueba BD GeneOhm MRSA ACP. Este producto está indicado para su utilización con muestras obtenidas mediante torunda nasal recogidas con los sistemas de recogida y transporte de muestras que se describen en la sección Materiales necesarios pero no suministrados. Su rendimiento con sistemas de recogida y transporte de muestras diferentes a los indicados no ha sido evaluado. Eficiencia de la lisis Se ha evaluado la eficiencia de la lisis con los diferentes dispositivo de recogida enumerado en la sección de Materiales necesarios pero no suministrados. Estos dispositivos de recogida en torunda se inocularon con concentraciones conocidas de tres (3) cepas de SARM. Con una alícuota extraída de la suspensión eluída de la torunda se realizó el procesamiento siguiendo las instrucciones de lisis de las muestras. Los lisados fueron inoculados en plagas de agar sangre, incubados durante horas y se realizó el recuento de UFC. El recuento de colonias varió entre 0 y UFC/placa. En la tabla siguiente se presenta un resumen del recuento de UFC obtenido con cada uno de los dispositivos de recogida utilizados y con cada una de las tres (3) cepas. Las eficiencias de la lisis más bajas y más altas que se observaron fueron del 99,7% y del 100%, respectivamente. Cepa de SARM 1 A B C Tipo de dispositivo de recogida (n = 18) Recuento inicial de UFC (límite inferior) Recuento inicial de UFC (límite superior) Recuento final de UFC después de la lisis (límite inferior) Recuento final de UFC después de la lisis (límite superior) Mínima eficiencia de la lisis (%) Máxima eficiencia de la lisis (%) Líquido de Amies ,9 100 Gel de Amies 7,26*10 5 1,02* ,9 100 Líquido de Stuart ,9 100 Líquido de Amies ,7 100 Gel de Amies 5,47*10 5 7,92* ,9 100 Líquido de Stuart ,9 100 Líquido de Amies 2 9,25*10 5 1,19* Gel de Amies Líquido de Stuart , A (ATCC 43300, MREJ Tipo ii), B (MREJ Tipo vii) y C (MREJ Tipo ii, PFGE USA 300), cepas de SARM caracterizadas previamente. 2 En dos casos se observó crecimiento confluyente en una (1) de las placas (n = 17 en lugar de 18); por tanto, no se pudieron realizar recuentos de colonias. 3 La eficiencia máxima de lisis se calculó de la siguiente manera: [(máximo recuento inicial de UFC observado antes de la lisis mínimo recuento después de la lisis)/máximo recuento inicial de UFC observado antes de la lisis] x La eficiencia mínima de lisis se calculó de la siguiente manera: [(mínimo recuento inicial de UFC observado antes de la lisis máximo recuento después de la lisis)/mínimo recuento inicial de UFC observado antes de la lisis] x 100. Referencias 1) Centers for Disease Control and Prevention. Biosafety in Microbiological and Biomedical Laboratories. Richmond JY and McKinney RW (eds) (1993). HHS Publication number (CDC) ) Clinical and Laboratory Standards Institute. Protection of Laboratory Workers from Instrument Biohazards and Infectious Disease Transmitted by Blood, Body Fluids and Tissue; Approved Guideline, Document M29 (Consultar la última edición). 3) Clinical and Laboratory Standards Institute. Molecular Diagnostic Methods for Infectious Diseases; Approved Guideline, Document MM3 (Consultar la última edición). 4) Clinical and Laboratory Standards Institute. Statistical Quality Control for Quantitative Measurements: Principles and Definitions; Approved Guideline, Document C24 (Consultar la última edición). P0071(03)_ES - 8 -
9 Índice de símbolos SÍMBOLO SIGNIFICADO SÍMBOLO SIGNIFICADO Fabricante Código del lote Número de catálogo Limites de temperatura Uso diagnóstico in vitro Protéjase de la luz y de la humedad Representante europeo autorizado Volver a cerrar las bolsas después de su uso Fecha de caducidad Consultar las instrucciones de uso Contiene cantidad suficiente para n pruebas Servicio de atención al cliente: Benex Limited Pottery Road Dun Laoghaire, Co. Dublin, Ireland GeneOhm Sciences Canada, Inc boul. du Parc-Technologique Québec, QC, Canada, G1P 4S5 BD, BD Logo and all other trademarks are property of Becton, Dickinson and Company BD. P0071(03)_ES - 9 -
1. OBTENCIÓN DE ADN DE BACTERIAS PATÓGENAS
 1. OBTENCIÓN DE ADN DE BACTERIAS PATÓGENAS Existen diferentes métodos para la obtención de ADN bacteriano que varían en duración y complejidad del procedimiento en función de la calidad del ADN que queramos
1. OBTENCIÓN DE ADN DE BACTERIAS PATÓGENAS Existen diferentes métodos para la obtención de ADN bacteriano que varían en duración y complejidad del procedimiento en función de la calidad del ADN que queramos
DANAGENE BLOOD DNA KIT
 Ref. 0601 100 ml Ref. 0602 200 ml DANAGENE BLOOD DNA KIT 1.INTRODUCCION DANAGENE BLOOD DNA Kit provee un método para la extracción de ADN genómico de alta calidad a partir de sangre total o médula ósea.
Ref. 0601 100 ml Ref. 0602 200 ml DANAGENE BLOOD DNA KIT 1.INTRODUCCION DANAGENE BLOOD DNA Kit provee un método para la extracción de ADN genómico de alta calidad a partir de sangre total o médula ósea.
Prueba BD GeneOhm TM VanR
 Prueba BD GeneOhm TM VanR 441250 48 PRUEBAS 441251 200 PRUEBAS P0025(01) -1- Fecha: 2012-04 Índice Uso previsto ------------------------------------------------------------------------------------------------------------------------------------
Prueba BD GeneOhm TM VanR 441250 48 PRUEBAS 441251 200 PRUEBAS P0025(01) -1- Fecha: 2012-04 Índice Uso previsto ------------------------------------------------------------------------------------------------------------------------------------
Prueba BD GeneOhm MRSA ACP Kit de amplificación
 Prueba Kit de amplificación REF. 441637 REF. 441639 48 pruebas 200 pruebas P0057(02)_ES Fecha: 2014-09 ÍNDICE USO PREVISTO... 3 RESUMEN Y EXPLICACIÓN... 3 PRINCIPIOS DEL PROCEDIMIENTO... 3 REACTIVOS...
Prueba Kit de amplificación REF. 441637 REF. 441639 48 pruebas 200 pruebas P0057(02)_ES Fecha: 2014-09 ÍNDICE USO PREVISTO... 3 RESUMEN Y EXPLICACIÓN... 3 PRINCIPIOS DEL PROCEDIMIENTO... 3 REACTIVOS...
PROCEDIMIENTO TECNICA DE COAGULASA EN TUBO PRT
 Página 1 de 7 1. OBJETIVO Comprobar la facultad de las unidades formadoras de colonias de S. aureus presentes en una muestra de alimento, de coagular el plasma de conejo por acción de la enzima coagulasa
Página 1 de 7 1. OBJETIVO Comprobar la facultad de las unidades formadoras de colonias de S. aureus presentes en una muestra de alimento, de coagular el plasma de conejo por acción de la enzima coagulasa
4. TIPADO GENÉTICO DE BACTERIAS PATÓGENAS MEDIANTE ELECTROFORESIS EN CAMPOS PULSADOS (PFGE) Materiales - Bacterias crecidas en placas de agar
 4. TIPADO GENÉTICO DE BACTERIAS PATÓGENAS MEDIANTE ELECTROFORESIS EN CAMPOS PULSADOS (PFGE) Materiales - Bacterias crecidas en placas de agar - Agarosa de grado molecular - Agarosa de bajo punto de fusión
4. TIPADO GENÉTICO DE BACTERIAS PATÓGENAS MEDIANTE ELECTROFORESIS EN CAMPOS PULSADOS (PFGE) Materiales - Bacterias crecidas en placas de agar - Agarosa de grado molecular - Agarosa de bajo punto de fusión
Protocolo de iniciación PCR. a tiempo real
 Protocolo de iniciación PCR a tiempo real CERTEST Biotec, S.L. Pol. Industrial Río Gállego II, Calle J, Nº 1, 50840, San Mateo de Gállego, Zaragoza (SPAIN) www.certest.es Protocolo de iniciación PCR a
Protocolo de iniciación PCR a tiempo real CERTEST Biotec, S.L. Pol. Industrial Río Gállego II, Calle J, Nº 1, 50840, San Mateo de Gállego, Zaragoza (SPAIN) www.certest.es Protocolo de iniciación PCR a
PROCEDIMIENTO DETECCIÓN Y ENUMERACIÓN POR NUMERO MAS PROBABLE (NMP) CON ETAPA DE PRE- ENRIQUECIMIENTO DE ENTEROBACTERIACEAE EN ALIMENTOS
 Página 1 de 5 1. OBJETIVO Estimar el número de Enterobacteriaceae presentes en el alimento. 2. CAMPO DE APLICACIÓN Y ALCANCE Aplicar este procedimiento a todas las muestras de alimentos de consumo humano
Página 1 de 5 1. OBJETIVO Estimar el número de Enterobacteriaceae presentes en el alimento. 2. CAMPO DE APLICACIÓN Y ALCANCE Aplicar este procedimiento a todas las muestras de alimentos de consumo humano
Hoja de protocolo del instrumento QIAsymphony SP
 Hoja de protocolo del instrumento QIAsymphony SP Protocolo VirusBlood200_V5_DSP Información general Para uso en diagnóstico in vitro. Este protocolo está indicado para la purificación de ADN viral a partir
Hoja de protocolo del instrumento QIAsymphony SP Protocolo VirusBlood200_V5_DSP Información general Para uso en diagnóstico in vitro. Este protocolo está indicado para la purificación de ADN viral a partir
Para uso diagnóstico in vitro. P0133(07) Para uso con el sistema BD MAX Español 4 I
 MAX MRSA 442953 Para uso diagnóstico in vitro P0133(07) Para uso con el sistema BD MAX 2016-10 Español 4 I USO PREVISTO El BD MAX MRSA assay (análisis BD MAX MRSA) se realiza en el sistema BD MAX y es
MAX MRSA 442953 Para uso diagnóstico in vitro P0133(07) Para uso con el sistema BD MAX 2016-10 Español 4 I USO PREVISTO El BD MAX MRSA assay (análisis BD MAX MRSA) se realiza en el sistema BD MAX y es
Petrifilm Recuento de Aerobios. Guía de Interpretación
 3 Petrifilm Recuento de Aerobios Guía de Interpretación 1 3M Petrifilm Recuento de Aerobios Recuento = 0 Es fácil interpretar la placa Petrifilm Recuento de Aerobios. La figura 2 nos muestra una placa
3 Petrifilm Recuento de Aerobios Guía de Interpretación 1 3M Petrifilm Recuento de Aerobios Recuento = 0 Es fácil interpretar la placa Petrifilm Recuento de Aerobios. La figura 2 nos muestra una placa
DANAGENE PLASMID MIDI/MAXI KIT
 REF.0702.4 25 Midis REF.0702.5 10 Maxis DANAGENE PLASMID MIDI/MAXI KIT 1. INTRODUCCION DANAGENE PLASMID Midi/Maxiprep Kit proporciona un método simple para purificar ADN plasmídico a partir de cultivos
REF.0702.4 25 Midis REF.0702.5 10 Maxis DANAGENE PLASMID MIDI/MAXI KIT 1. INTRODUCCION DANAGENE PLASMID Midi/Maxiprep Kit proporciona un método simple para purificar ADN plasmídico a partir de cultivos
Para uso diagnóstico in vitro. P0205(01) Para uso con el sistema BD MAX Español 4 U I
 MAX MRSA XT 443461 Para uso diagnóstico in vitro P0205(01) Para uso con el sistema BD MAX 2016-06 Español 4 U I USO PREVISTO La prueba BD MAX MRSA XT realizada en el sistema BD MAX es un test diagnóstico
MAX MRSA XT 443461 Para uso diagnóstico in vitro P0205(01) Para uso con el sistema BD MAX 2016-06 Español 4 U I USO PREVISTO La prueba BD MAX MRSA XT realizada en el sistema BD MAX es un test diagnóstico
ENUMERACIÓN DE ENTEROBACTERIACEAE EN ALIMENTOS SIN RESUSCITACIÓN. TÉCNICA RECUENTO EN PLACA
 PRT-712.03-040 Página 1 de 6 1. OBJETIVO Determinar el número de Enterobactereaceae presentes en un alimento. 2. CAMPO DE APLICACIÓN Y ALCANCE Aplicar este procedimiento a todas las muestras de alimentos
PRT-712.03-040 Página 1 de 6 1. OBJETIVO Determinar el número de Enterobactereaceae presentes en un alimento. 2. CAMPO DE APLICACIÓN Y ALCANCE Aplicar este procedimiento a todas las muestras de alimentos
Para uso diagnóstico in vitro. P0207(01) Para uso con el sistema BD MAX Español
 B MAX StaphSR 443419 Para uso diagnóstico in vitro P0207(01) Para uso con el sistema BD MAX 2016-07 Español 4 I USO PREVISTO El ensayo BD MAX StaphSR realizado en el BD MAX System (sistema BD MAX) es una
B MAX StaphSR 443419 Para uso diagnóstico in vitro P0207(01) Para uso con el sistema BD MAX 2016-07 Español 4 I USO PREVISTO El ensayo BD MAX StaphSR realizado en el BD MAX System (sistema BD MAX) es una
50 kits de recolección de muestras con torunda multitest Aptima (N.º de catálogo PRD-03546) Cada kit contiene:
 Uso previsto El kit de recolección de muestras con torunda se utiliza con los ensayos Aptima. El kit de recolección de muestras con torunda multitest Aptima se utiliza para que médico y paciente puedan
Uso previsto El kit de recolección de muestras con torunda se utiliza con los ensayos Aptima. El kit de recolección de muestras con torunda multitest Aptima se utiliza para que médico y paciente puedan
1. OBJETIVO Detectar enterotoxina A de C. perfringens por método de aglutinación pasiva en látex en cepas aisladas de alimentos
 PRT-712.04-080 Página 1 de 9 1. OBJETIVO Detectar enterotoxina A de C. perfringens por método de aglutinación pasiva en látex en cepas aisladas de alimentos 2. CAMPO DE APLICACIÓN Y ALCANCE Aplicar este
PRT-712.04-080 Página 1 de 9 1. OBJETIVO Detectar enterotoxina A de C. perfringens por método de aglutinación pasiva en látex en cepas aisladas de alimentos 2. CAMPO DE APLICACIÓN Y ALCANCE Aplicar este
Gelatina Ácido ascórbico Carbón
 Instrucciones de uso n Epower USO PREVISTO Los microorganismos Epower son preparaciones cuantitativas liofilizadas de microorganismos destinadas al uso en laboratorios industriales para fines de control
Instrucciones de uso n Epower USO PREVISTO Los microorganismos Epower son preparaciones cuantitativas liofilizadas de microorganismos destinadas al uso en laboratorios industriales para fines de control
PRACTICA Núm. 22 INVESTIGACION DE COLIFORMES TOTALES Y FECALES EN DESECHOS SOLIDOS Y COMPOSTA
 PRACTICA Núm. 22 INVESTIGACION DE COLIFORMES TOTALES Y FECALES EN DESECHOS SOLIDOS Y COMPOSTA I. OBJETIVO Determinar la presencia de coliformes totales y fecales en un desecho sólido por el método del
PRACTICA Núm. 22 INVESTIGACION DE COLIFORMES TOTALES Y FECALES EN DESECHOS SOLIDOS Y COMPOSTA I. OBJETIVO Determinar la presencia de coliformes totales y fecales en un desecho sólido por el método del
Diagnóstico molecular más allá de la simplicidad. Idylla. Sistema de diagnóstico molecular completamente automatizado
 Diagnóstico molecular más allá de la simplicidad Idylla TM Sistema de diagnóstico molecular completamente automatizado Idylla TM Nunca habia sido tan fácil volverse molecular Facilidad de uso El sistema
Diagnóstico molecular más allá de la simplicidad Idylla TM Sistema de diagnóstico molecular completamente automatizado Idylla TM Nunca habia sido tan fácil volverse molecular Facilidad de uso El sistema
NMP PARA LA DETERMINACION DE COLIFORMESY COLIFORMES FECALES EN AGUAS
 PRT-712.03-005 Página 1 de 6 1. OBJETIVO Este método es utilizado para estimar la densidad de bacterias del grupo coliformes y conocer la calidad sanitaria en aguas crudas 2. CAMPO DE APLICACIÓN Y ALCANCE
PRT-712.03-005 Página 1 de 6 1. OBJETIVO Este método es utilizado para estimar la densidad de bacterias del grupo coliformes y conocer la calidad sanitaria en aguas crudas 2. CAMPO DE APLICACIÓN Y ALCANCE
Ejemplos de recolección, conservación, envase y transporte de muestras de alimentos MANEJO EN EL MUESTRAS CONSERVACIÓN
 VI. Ejemplos de recolección, conservación, envase y transporte de muestras de alimentos RECOLECCIÓN Y Y DESECHO sólidos o mezcla de dos alimentos Realice cortes o tomar porciones de los alimentos utilizando
VI. Ejemplos de recolección, conservación, envase y transporte de muestras de alimentos RECOLECCIÓN Y Y DESECHO sólidos o mezcla de dos alimentos Realice cortes o tomar porciones de los alimentos utilizando
GUIA DE SOLUCIÓN DE ERRORES EN EL TAMIZAJE DE HEMOTRANSMISIBLES. Lic. TM. ANDRÉS LARA RODRÍGUEZ Hospital San Bartolomé
 GUIA DE SOLUCIÓN DE ERRORES EN EL TAMIZAJE DE HEMOTRANSMISIBLES Lic. TM. ANDRÉS LARA RODRÍGUEZ Hospital San Bartolomé Esquema de investigación en pruebas fallidas Revisar el procedimiento y determinar
GUIA DE SOLUCIÓN DE ERRORES EN EL TAMIZAJE DE HEMOTRANSMISIBLES Lic. TM. ANDRÉS LARA RODRÍGUEZ Hospital San Bartolomé Esquema de investigación en pruebas fallidas Revisar el procedimiento y determinar
INSTRUCCIONES DE USO
 INSTRUCCIONES DE USO Microorganismos Epower USO PREVISTO Los microorganismos Epower son preparaciones cuantitativas liofilizadas de microorganismos para realizar controles de calidad en laboratorios industriales.
INSTRUCCIONES DE USO Microorganismos Epower USO PREVISTO Los microorganismos Epower son preparaciones cuantitativas liofilizadas de microorganismos para realizar controles de calidad en laboratorios industriales.
50 kits de recolección de muestras con torunda multitest Aptima (N.º de catálogo PRD-03546) Cada kit contiene:
 Uso previsto El kit de recolección de muestras con torunda se utiliza con los ensayos Aptima. El kit de recolección de muestras con torunda multitest Aptima se utiliza para que médico y paciente puedan
Uso previsto El kit de recolección de muestras con torunda se utiliza con los ensayos Aptima. El kit de recolección de muestras con torunda multitest Aptima se utiliza para que médico y paciente puedan
Hoja de protocolo del instrumento QIAsymphony SP
 Hoja de protocolo del instrumento QIAsymphony SP PC_AXpH_HC2_V1_DSP protocol Indicaciones de uso Para el diagnóstico in vitro. Este protocolo se ha desarrollado para la preparación de muestras del cuello
Hoja de protocolo del instrumento QIAsymphony SP PC_AXpH_HC2_V1_DSP protocol Indicaciones de uso Para el diagnóstico in vitro. Este protocolo se ha desarrollado para la preparación de muestras del cuello
BUENAS PRÁCTICAS DE MUESTREO PARA LA RECOLECCION DE AGUA PARA EL ANALISIS MICROBIOLOGICO
 BUENAS PRÁCTICAS DE MUESTREO PARA LA RECOLECCION DE AGUA PARA EL ANALISIS MICROBIOLOGICO OBJETIVO Asegurar las condiciones de las tareas de toma de muestra de aguas a las que luego se les realizará análisis
BUENAS PRÁCTICAS DE MUESTREO PARA LA RECOLECCION DE AGUA PARA EL ANALISIS MICROBIOLOGICO OBJETIVO Asegurar las condiciones de las tareas de toma de muestra de aguas a las que luego se les realizará análisis
DEPARTAMENTO DE GENÉTICA UNIVERSIDAD DE GRANADA FUNDAMENTOS DE BIOLOGÍA APLICADA I 4º CURSO DE BIOLOGÍA
 DEPARTAMENTO DE GENÉTICA UNIVERSIDAD DE GRANADA FUNDAMENTOS DE BIOLOGÍA APLICADA I 4º CURSO DE BIOLOGÍA MÓDULO DE GENÉTICA TÉCNICAS MOLECULARES DE ANÁLISIS GENÉTICO AISLAMIENTO Y CLONACIÓN DE ADN SATÉLITE
DEPARTAMENTO DE GENÉTICA UNIVERSIDAD DE GRANADA FUNDAMENTOS DE BIOLOGÍA APLICADA I 4º CURSO DE BIOLOGÍA MÓDULO DE GENÉTICA TÉCNICAS MOLECULARES DE ANÁLISIS GENÉTICO AISLAMIENTO Y CLONACIÓN DE ADN SATÉLITE
EXTRACCIÓN DE ADN (Doyle & Doyle, 1987)
 EXTRACCIÓN DE ADN (Doyle & Doyle, 1987) MATERIALES Y REACTIVOS (Grado biología molecular a analítico) Cloroformo Alcohol Isoamilico Isopropanol. Etanol al 70%. Bloques de Hielo Microcentrifuga Bloque de
EXTRACCIÓN DE ADN (Doyle & Doyle, 1987) MATERIALES Y REACTIVOS (Grado biología molecular a analítico) Cloroformo Alcohol Isoamilico Isopropanol. Etanol al 70%. Bloques de Hielo Microcentrifuga Bloque de
EXTRACCIÓN DE ADN DE HONGOS FILAMENTOSOS
 EXTRACCIÓN DE ADN DE HONGOS FILAMENTOSOS Los hongos poseen un genoma complejo consistente en: ADN nuclear (n ADN) ADN mitocondrial (mt ADN) en algunos casos ADN plasmídico EXTRACCIÓN DE ADN DE HONGOS FILAMENTOSOS
EXTRACCIÓN DE ADN DE HONGOS FILAMENTOSOS Los hongos poseen un genoma complejo consistente en: ADN nuclear (n ADN) ADN mitocondrial (mt ADN) en algunos casos ADN plasmídico EXTRACCIÓN DE ADN DE HONGOS FILAMENTOSOS
TEMA 12. Pruebas de sensibilidad a los antimicrobianos
 TEMA 12 Pruebas de sensibilidad a los antimicrobianos Tema 12. Pruebas de sensibilidad a los antimicrobianos 1. Nacimiento de la era de los antibióticos 2. Pruebas de sensibilidad a los antimicrobianos
TEMA 12 Pruebas de sensibilidad a los antimicrobianos Tema 12. Pruebas de sensibilidad a los antimicrobianos 1. Nacimiento de la era de los antibióticos 2. Pruebas de sensibilidad a los antimicrobianos
Técnica para la obtención de la muestra
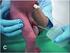 Técnica para la obtención de la muestra Luz Yanet Maldonado C Bacterióloga MSc. Microbiología Laboratorio Salud Publica Bogotá TIPO DE MUESTRA Pacientes hospitalizados (Niños): Aspirado nasofaríngeo diluyéndolo
Técnica para la obtención de la muestra Luz Yanet Maldonado C Bacterióloga MSc. Microbiología Laboratorio Salud Publica Bogotá TIPO DE MUESTRA Pacientes hospitalizados (Niños): Aspirado nasofaríngeo diluyéndolo
Antes de comenzar el procesamiento, lavarse las manos y colocarse gorro, y guantes.
 Directrices Banco de Leche Humana Itinerario al Ingresar al BLH: 1) Control de temperatura de freezer (menor a -20 ºC) y estufa (36 +/- 1ºC) y registro el cuaderno correspondiente 2) Limpieza y Desinfección
Directrices Banco de Leche Humana Itinerario al Ingresar al BLH: 1) Control de temperatura de freezer (menor a -20 ºC) y estufa (36 +/- 1ºC) y registro el cuaderno correspondiente 2) Limpieza y Desinfección
AdnaTest BreastCancerSelect
 AdnaTest BreastCancerSelect Enriquecimiento de células tumorales provenientes de sangre de pacientes con cáncer de mama para el análisis de la expresión génica Para uso de diagnóstico in vitro Manual T-1-508
AdnaTest BreastCancerSelect Enriquecimiento de células tumorales provenientes de sangre de pacientes con cáncer de mama para el análisis de la expresión génica Para uso de diagnóstico in vitro Manual T-1-508
PROCEDIMIENTO TECNICA NMP STAPHYLOCOCCUS AUREUS EN ALIMENTOS. BAM ONLINE 2001
 PRT-712.02-025 Página 1 de 9 1. OBJETIVO Estimar la densidad de bacterias S. aureus en matrices de alimento o agua como indicador sanitario 2. CAMPO DE APLICACIÓN Y ALCANCE El método de NMP es recomendado
PRT-712.02-025 Página 1 de 9 1. OBJETIVO Estimar la densidad de bacterias S. aureus en matrices de alimento o agua como indicador sanitario 2. CAMPO DE APLICACIÓN Y ALCANCE El método de NMP es recomendado
TRANSFERENCIAS ASÉPTICAS
 Introducción Objetivo Procedimiento Trabajo Práctico Nº 3 TRANSFERENCIAS ASÉPTICAS Resultados Observaciones Bibliografía INTRODUCCIÓN La inoculación de medios de cultivo y la manipulación de cultivos microbianos
Introducción Objetivo Procedimiento Trabajo Práctico Nº 3 TRANSFERENCIAS ASÉPTICAS Resultados Observaciones Bibliografía INTRODUCCIÓN La inoculación de medios de cultivo y la manipulación de cultivos microbianos
BBL Middlebrook 7H9 Broth with Glycerol
 BBL Middlebrook 7H9 Broth with Glycerol Rev. 12 Octubre 2015 PROCEDIMIENTOS DE CONTROL DE CALIDAD (Opcionales) I II INTRODUCCION Middlebrook 7H9 Broth with Glycerol (caldo Middlebrook 7H9 con glicerol)
BBL Middlebrook 7H9 Broth with Glycerol Rev. 12 Octubre 2015 PROCEDIMIENTOS DE CONTROL DE CALIDAD (Opcionales) I II INTRODUCCION Middlebrook 7H9 Broth with Glycerol (caldo Middlebrook 7H9 con glicerol)
PROCEDIMIENTO PARA REALIZAR CONCENTRACION DE VIRUS ENTERICOS EN MUESTRAS DE AGUA. PRT Página 1 de 5
 PRT-712.07.01-104 Página 1 de 5 1. OBJETIVO Realizar concentración viral desde muestras de agua para su posterior análisis de presencia de virus entéricos. 2. CAMPO DE APLICACIÓN Y ALCANCE Este procedimiento
PRT-712.07.01-104 Página 1 de 5 1. OBJETIVO Realizar concentración viral desde muestras de agua para su posterior análisis de presencia de virus entéricos. 2. CAMPO DE APLICACIÓN Y ALCANCE Este procedimiento
FICHA TÉCNICA: Rev. : Octubre /2009
 FICHA TÉCNICA: 771451 Rev. : Octubre /2009 Producto: THIOGLICOLLATE BROTH WITH RESAZURIN TUBO USO El Thioglicollate Broth With Resazurin es un medio indicado para el cultivo de gran variedad de micoorganismos,
FICHA TÉCNICA: 771451 Rev. : Octubre /2009 Producto: THIOGLICOLLATE BROTH WITH RESAZURIN TUBO USO El Thioglicollate Broth With Resazurin es un medio indicado para el cultivo de gran variedad de micoorganismos,
INSTRUCCIÓN TÉCNICA. Escrutinio de anticuerpos Irregulares o Coombs Indirecto DISTRIBUCIÓN: Jefe de la Unidad de Calidad SUMARIO DE MODIFICACIONES
 Página 1 de 6 DISTRIBUCIÓN: DEPARTAMENTO Dirección Hematología Enfermería RESPONSABLE Jefe de la Unidad de Calidad Jefe de la Unidad de Hematología Coordinadora de Enfermería REVISIÓN FECHA DESCRIPCIÓN
Página 1 de 6 DISTRIBUCIÓN: DEPARTAMENTO Dirección Hematología Enfermería RESPONSABLE Jefe de la Unidad de Calidad Jefe de la Unidad de Hematología Coordinadora de Enfermería REVISIÓN FECHA DESCRIPCIÓN
Anexo Conservar a 4 o C.
 Anexo 1 Purificación de ADN viral 1. Partir de un sobrenadante de un cultivo celular infectado y clarificado. 2. Concentrar las formas brotantes de los baculovirus por centrifugación (centrifugrar 1,5
Anexo 1 Purificación de ADN viral 1. Partir de un sobrenadante de un cultivo celular infectado y clarificado. 2. Concentrar las formas brotantes de los baculovirus por centrifugación (centrifugrar 1,5
CYP 2C9 A1075C CYP2C9*3
 CYP 2C9 A1075C Sistema para la detección de la mutación A1075C en el gene del citocromo P450 2C9. Valdense 3616. 11700. Montevideo. Uruguay. Teléfono (598) 2 336 83 01. Fax (598) 2 336 71 60. Info@atgen.com.uy
CYP 2C9 A1075C Sistema para la detección de la mutación A1075C en el gene del citocromo P450 2C9. Valdense 3616. 11700. Montevideo. Uruguay. Teléfono (598) 2 336 83 01. Fax (598) 2 336 71 60. Info@atgen.com.uy
PI, SYSCHECK, IVD, CE, SPANISH
 REV AUTHORED BY DATE LISA MCVICKER 6/13/2017 REV DRAFTED BY DATE LISA MCVICKER 6/13/2017 PROPRIETARY: This document contains proprietary data of Hologic, Inc. No disclosure, reproduction or use of any
REV AUTHORED BY DATE LISA MCVICKER 6/13/2017 REV DRAFTED BY DATE LISA MCVICKER 6/13/2017 PROPRIETARY: This document contains proprietary data of Hologic, Inc. No disclosure, reproduction or use of any
MANUAL DE NORMAS Y PROCEDIMIENTOS PROCEDIMIENTO: CONTROL DE CALIDAD INTERNO
 UNIDAD DE LABORATORIO 1 DE 8 I. INTRODUCCIÓN La Garantía de calidad es un conjunto de procedimientos utilizados para asegurar la calidad de los resultados finales, cubriendo con ello todas las fases del
UNIDAD DE LABORATORIO 1 DE 8 I. INTRODUCCIÓN La Garantía de calidad es un conjunto de procedimientos utilizados para asegurar la calidad de los resultados finales, cubriendo con ello todas las fases del
SSI DERMATOPHYTE PCR KIT PRUEBA PCR DERMATOFITO
 SSI DERMATOPHYTE PCR KIT PRUEBA PCR DERMATOFITO 2 Prueba de PCR para la detección de dermatofitos y Trichophyton rubrum Para uso diagnóstico in vitro Aplicación La prueba de PCR para dermatofitos en uñas
SSI DERMATOPHYTE PCR KIT PRUEBA PCR DERMATOFITO 2 Prueba de PCR para la detección de dermatofitos y Trichophyton rubrum Para uso diagnóstico in vitro Aplicación La prueba de PCR para dermatofitos en uñas
Prueba BD GeneOhm Cdiff
 Prueba BD GeneOhm Cdiff REF 441400 REF 441401 48 pruebas 200 pruebas P0047(02)_ES Fecha: 2014-09 ÍNDICE USO PREVISTO... 3 RESUMEN Y EXPLICACIÓN DE LA PRUEBA... 3 PRINCIPIOS DEL PROCEDIMIENTO... 3 REACTIVOS...
Prueba BD GeneOhm Cdiff REF 441400 REF 441401 48 pruebas 200 pruebas P0047(02)_ES Fecha: 2014-09 ÍNDICE USO PREVISTO... 3 RESUMEN Y EXPLICACIÓN DE LA PRUEBA... 3 PRINCIPIOS DEL PROCEDIMIENTO... 3 REACTIVOS...
Instrucciones de uso MBT Galaxy HCCA Matrix GPR
 Instrucciones de uso MBT Galaxy HCCA Matrix GPR Sustancia matriz purificada para uso en espectrometría de masas de desorción y ionización láser asistida por matriz y tiempo de vuelo (MALDI-TOF-MS). Para
Instrucciones de uso MBT Galaxy HCCA Matrix GPR Sustancia matriz purificada para uso en espectrometría de masas de desorción y ionización láser asistida por matriz y tiempo de vuelo (MALDI-TOF-MS). Para
WITNESS RELAXIN (plasma, serum) RLX RLX u d 9 n n ersio V X RLX L R -W IO B S
 WITNESS RELAXIN (plasma, serum) SBIO-W Version n 9 du 28.07.2010 WITNESS RELAXIN WITNESS RELAXIN GENERALIDADES El kit WITNESS RELAXIN permite diagnosticar la gestación en la perra y en la gata, y permite
WITNESS RELAXIN (plasma, serum) SBIO-W Version n 9 du 28.07.2010 WITNESS RELAXIN WITNESS RELAXIN GENERALIDADES El kit WITNESS RELAXIN permite diagnosticar la gestación en la perra y en la gata, y permite
RECOPILADO POR: EL PROGRAMA UNIVERSITARIO DE ALIMENTOS
 NMX-F-286-1992. ALIMENTOS. PREPARACIÓN Y DILUCIÓN DE MUESTRAS DE ALIMENTOS PARA ANÁLISIS MICROBIOLÓGICOS. FOODS. PREPARATION AND DILUTION OF FOOD SAMPLES FOR MICROBIOLOGICAL ANALYSIS. NORMAS MEXICANAS.
NMX-F-286-1992. ALIMENTOS. PREPARACIÓN Y DILUCIÓN DE MUESTRAS DE ALIMENTOS PARA ANÁLISIS MICROBIOLÓGICOS. FOODS. PREPARATION AND DILUTION OF FOOD SAMPLES FOR MICROBIOLOGICAL ANALYSIS. NORMAS MEXICANAS.
TECHNOLOGY. CROSSMATCH TEST canino. primer test inmunocromatografico para reaccion cruzada con antiglobulina canina especifica.
 CROSSMATCH TEST canino primer test inmunocromatografico para reaccion cruzada con antiglobulina canina especifica 20 minutos TECHNOLOGY - ahorra tiempo - facil manipulacion - resultados fiables - facil
CROSSMATCH TEST canino primer test inmunocromatografico para reaccion cruzada con antiglobulina canina especifica 20 minutos TECHNOLOGY - ahorra tiempo - facil manipulacion - resultados fiables - facil
Laboratorio Nacional de Salud Pública
 1. Tinción de Gram 2. Objeto y campo de aplicación La técnica de tinción de Gram se utiliza para la tinción de bacterias, levaduras y actinomicetos aerobios. Este procedimiento operativo estándar es aplicable
1. Tinción de Gram 2. Objeto y campo de aplicación La técnica de tinción de Gram se utiliza para la tinción de bacterias, levaduras y actinomicetos aerobios. Este procedimiento operativo estándar es aplicable
PCR gen 16S ARNr bacteriano
 PCR gen 16S ARNr bacteriano Ref. PCR16S 1. OBJETIVO DEL EXPERIMENTO El objetivo de este experimento es introducir a los estudiantes en los principios y la práctica de la Reacción en Cadena de la Polimerasa
PCR gen 16S ARNr bacteriano Ref. PCR16S 1. OBJETIVO DEL EXPERIMENTO El objetivo de este experimento es introducir a los estudiantes en los principios y la práctica de la Reacción en Cadena de la Polimerasa
DANAGENE RNA PURIFICATION KIT
 DANAGENE RNA PURIFICATION KIT REF.0801.1 100 EXTRACCIONES REF.0801.2 500 EXTRACCIONES 1.INTRODUCCION Este kit permite la permite la obtención de ARN total a partir de cultivos celulares, tejidos animales,
DANAGENE RNA PURIFICATION KIT REF.0801.1 100 EXTRACCIONES REF.0801.2 500 EXTRACCIONES 1.INTRODUCCION Este kit permite la permite la obtención de ARN total a partir de cultivos celulares, tejidos animales,
PRUEBAS DE SENSIBILIDAD A AGENTES ANTIMICROBIANOS
 PRACTICA Nº2 DE MALALTIES INFECCIOSES I PRUEBAS DE SENSIBILIDAD A AGENTES ANTIMICROBIANOS Introducción La determinación de la sensibilidad a los agentes antimicrobianos es una de las principales funciones
PRACTICA Nº2 DE MALALTIES INFECCIOSES I PRUEBAS DE SENSIBILIDAD A AGENTES ANTIMICROBIANOS Introducción La determinación de la sensibilidad a los agentes antimicrobianos es una de las principales funciones
LABORATORIO INFECCIONES INTRAHOSPITALARIAS- IIH CONTROL DE CALIDAD EXTERNO
 TALLER ANALISIS RESULTADOS PEEC BACTERIOLOGIA PROGRAMA: IDENTIFICACIÓN BACTERIANA Y SUSCEPTIBILIDAD ANTIMICROBIANA LABORATORIO INFECCIONES INTRAHOSPITALARIAS- IIH ACTIVIDADES ABRIL 2011 TM M. Soledad Prat.
TALLER ANALISIS RESULTADOS PEEC BACTERIOLOGIA PROGRAMA: IDENTIFICACIÓN BACTERIANA Y SUSCEPTIBILIDAD ANTIMICROBIANA LABORATORIO INFECCIONES INTRAHOSPITALARIAS- IIH ACTIVIDADES ABRIL 2011 TM M. Soledad Prat.
LABORATORIO INFECCIONES INTRAHOSPITALARIAS- IIH
 TALLER ANALISIS RESULTADOS PEEC BACTERIOLOGIA PROGRAMA: IDENTIFICACIÓN BACTERIANA Y SUSCEPTIBILIDAD ANTIMICROBIANA LABORATORIO INFECCIONES INTRAHOSPITALARIAS- IIH ACTIVIDADES ABRIL 2011 TM M. Soledad Prat.
TALLER ANALISIS RESULTADOS PEEC BACTERIOLOGIA PROGRAMA: IDENTIFICACIÓN BACTERIANA Y SUSCEPTIBILIDAD ANTIMICROBIANA LABORATORIO INFECCIONES INTRAHOSPITALARIAS- IIH ACTIVIDADES ABRIL 2011 TM M. Soledad Prat.
BBL Brain Heart Infusion BBL Brain Heart Infusion with 6.5% Sodium Chloride
 BBL Brain Heart Infusion BBL Brain Heart Infusion with 6.5% Sodium Chloride Rev. 12 Septiembre 2014 PROCEDIMIENTOS DE CONTROL DE CALIDAD I II INTRODUCCION Brain Heart Infusion (BHI) (infusión de cerebro
BBL Brain Heart Infusion BBL Brain Heart Infusion with 6.5% Sodium Chloride Rev. 12 Septiembre 2014 PROCEDIMIENTOS DE CONTROL DE CALIDAD I II INTRODUCCION Brain Heart Infusion (BHI) (infusión de cerebro
UNIVERSIDAD NACIONAL DEL NORDESTE Facultad de Ciencias Exactas y Naturales y Agrimensura Departamento de Biología - Área Zoología EMBRIOLOGÍA ANIMAL
 UNIVERSIDAD NACIONAL DEL NORDESTE Facultad de Ciencias Exactas y Naturales y Agrimensura Departamento de Biología - Área Zoología EMBRIOLOGÍA ANIMAL PROTOCOLO PARA OBTENCIÓN DE EMBRIONES DE POLLO EN LABORATORIO
UNIVERSIDAD NACIONAL DEL NORDESTE Facultad de Ciencias Exactas y Naturales y Agrimensura Departamento de Biología - Área Zoología EMBRIOLOGÍA ANIMAL PROTOCOLO PARA OBTENCIÓN DE EMBRIONES DE POLLO EN LABORATORIO
DETERMINACIÓN DEL MAPA DE UN PLÁSMIDO CON ENZIMAS DE RESTRICCIÓN
 DETERMINACIÓN DEL MAPA DE UN PLÁSMIDO CON ENZIMAS DE RESTRICCIÓN 6 grupos de estudiantes 1. OBJETIVO DEL EXPERIMENTO El objetivo de este experimento es desarrollar un conocimiento del mapaje de ADN determinando
DETERMINACIÓN DEL MAPA DE UN PLÁSMIDO CON ENZIMAS DE RESTRICCIÓN 6 grupos de estudiantes 1. OBJETIVO DEL EXPERIMENTO El objetivo de este experimento es desarrollar un conocimiento del mapaje de ADN determinando
TRABAJO PRÁCTICO N 6 FERTILIZANTES BIOLÓGICOS: DESARROLLO Y CONTROL DE CALIDAD DE INOCULANTES
 TRABAJO PRÁCTICO N 6 FERTILIZANTES BIOLÓGICOS: DESARROLLO Y CONTROL DE CALIDAD DE INOCULANTES Objetivos Conocer los parámetros para la selección de cepas. Conocer las metodologías y procedimientos microbiológicos
TRABAJO PRÁCTICO N 6 FERTILIZANTES BIOLÓGICOS: DESARROLLO Y CONTROL DE CALIDAD DE INOCULANTES Objetivos Conocer los parámetros para la selección de cepas. Conocer las metodologías y procedimientos microbiológicos
Hoja de protocolo del instrumento QIAsymphony SP
 Hoja de protocolo del instrumento QIAsymphony SP Protocolo DNA_Blood_200_V7_DSP Información general Para uso en diagnóstico in vitro. Este protocolo está indicado para la purificación de ADN mitocondrial
Hoja de protocolo del instrumento QIAsymphony SP Protocolo DNA_Blood_200_V7_DSP Información general Para uso en diagnóstico in vitro. Este protocolo está indicado para la purificación de ADN mitocondrial
NMP PARA LA DETERMINACION DE COLIFORMES Y ESCHERICHIA COLI EN ALIMENTOS PRT
 Página 1 de 8 1. OBJETIVO Estimar la densidad de bacterias del grupo coliformes, como indicador sanitario. 2. CAMPO DE APLICACIÓN Y ALCANCE Aplicar este procedimiento a todas las muestras de alimentos
Página 1 de 8 1. OBJETIVO Estimar la densidad de bacterias del grupo coliformes, como indicador sanitario. 2. CAMPO DE APLICACIÓN Y ALCANCE Aplicar este procedimiento a todas las muestras de alimentos
VERSIÓN PARA EQUIPOS COBAS c501/c502 DE ROCHE
 VERSIÓN PARA EQUIPOS COBAS c501/c502 DE ROCHE EQUIPO ADICIONAL NO SUMINISTRADO: La preparación de los reactivos requiere el empleo de micropipetas o sistemas que permitan dispensar los volúmenes especificados.
VERSIÓN PARA EQUIPOS COBAS c501/c502 DE ROCHE EQUIPO ADICIONAL NO SUMINISTRADO: La preparación de los reactivos requiere el empleo de micropipetas o sistemas que permitan dispensar los volúmenes especificados.
Técnicas de monitoreo para la detección de microorganismos en el medio ambiente
 Técnicas de monitoreo para la detección de microorganismos en el medio ambiente Gloria Alicia Figueroa Aguilar Condiciones Ambientales REQUISITO: El laboratorio debe asegurarse que las condiciones ambientales,
Técnicas de monitoreo para la detección de microorganismos en el medio ambiente Gloria Alicia Figueroa Aguilar Condiciones Ambientales REQUISITO: El laboratorio debe asegurarse que las condiciones ambientales,
Código: IDK-006 Ver: 1 MTHFR A1298C. Sistema para detección de la alteración A1298C en el gene de la Mutilen Tetrahidrofolato Reductasa
 Sistema para detección de la alteración A1298C en el gene de la Mutilen Tetrahidrofolato Reductasa Reg. MSP 21199 Valdense 3616. 11700. Montevideo. Uruguay. Teléfono (598) 2 336 83 01. Fax (598) 2 336
Sistema para detección de la alteración A1298C en el gene de la Mutilen Tetrahidrofolato Reductasa Reg. MSP 21199 Valdense 3616. 11700. Montevideo. Uruguay. Teléfono (598) 2 336 83 01. Fax (598) 2 336
TaqMan Roundup Ready Quantification Kit. Part No:
 TaqMan Roundup Ready Quantification Kit Part No: 4466335 1. Introducción Los organismos modificados genéticamente (OMG) se encuentran ampliamente distribuidos, siendo la soja y el maíz los vegetales que
TaqMan Roundup Ready Quantification Kit Part No: 4466335 1. Introducción Los organismos modificados genéticamente (OMG) se encuentran ampliamente distribuidos, siendo la soja y el maíz los vegetales que
Estudios microbiológicos.procedimientos. 1. Urocultivos
 Estudios microbiológicos.procedimientos 1. Urocultivos Se realizará el cultivo de orina a todas las muestras llegadas al laboratorio, que cumplan con los requisitos para la toma, conservación y transporte
Estudios microbiológicos.procedimientos 1. Urocultivos Se realizará el cultivo de orina a todas las muestras llegadas al laboratorio, que cumplan con los requisitos para la toma, conservación y transporte
Instrucciones de uso MBT Galaxy HCCA Matrix GPR
 Instrucciones de uso MBT Galaxy HCCA Matrix GPR Sustancia matriz purificada para uso en espectrometría de masas de desorción/ionización láser asistida por matriz y tiempo de vuelo (MALDI-TOF-MS). Los productos
Instrucciones de uso MBT Galaxy HCCA Matrix GPR Sustancia matriz purificada para uso en espectrometría de masas de desorción/ionización láser asistida por matriz y tiempo de vuelo (MALDI-TOF-MS). Los productos
TRABAJO PRÁCTICO Nº 11 DIAGNÓSTICO MICROBIOLÓGICO DIRECTO.
 TRABAJO PRÁCTICO Nº 11 DIAGNÓSTICO MICROBIOLÓGICO DIRECTO. En la práctica odontológica las lesiones bucales piógenas se tratan con antibióticos, generalmente administrados en forma empírica, cuando lo
TRABAJO PRÁCTICO Nº 11 DIAGNÓSTICO MICROBIOLÓGICO DIRECTO. En la práctica odontológica las lesiones bucales piógenas se tratan con antibióticos, generalmente administrados en forma empírica, cuando lo
AISLAMIENTO DE MICROORGANISMOS
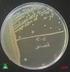 PRÁCTICA5 AISLAMIENTO DE MICROORGANISMOS Introducción En la naturaleza, la mayoría de los microorganismos no se encuentran aislados, sino integrados en poblaciones mixtas. Para llevar a cabo el estudio
PRÁCTICA5 AISLAMIENTO DE MICROORGANISMOS Introducción En la naturaleza, la mayoría de los microorganismos no se encuentran aislados, sino integrados en poblaciones mixtas. Para llevar a cabo el estudio
Frascos 50 ml (38 x 70 mm)
 Frascos 50 ml (38 x 70 mm) Material del tapón: polietileno. Volumen del frasco: 50 ml. descripción 409802 polipropileno alta transparencia 700 9,30 0,096 16 409852 polipropileno alta transparencia con
Frascos 50 ml (38 x 70 mm) Material del tapón: polietileno. Volumen del frasco: 50 ml. descripción 409802 polipropileno alta transparencia 700 9,30 0,096 16 409852 polipropileno alta transparencia con
Hoja de protocolo del instrumento QIAsymphony SP
 Hoja de protocolo del instrumento QIAsymphony SP Protocolo DNA_Buffy_Coat_200_V7_DSP Información general Para uso en diagnóstico in vitro. Este protocolo está indicado para la purificación de ADN mitocondrial
Hoja de protocolo del instrumento QIAsymphony SP Protocolo DNA_Buffy_Coat_200_V7_DSP Información general Para uso en diagnóstico in vitro. Este protocolo está indicado para la purificación de ADN mitocondrial
K ADN PuriPrep-GP kit. Extracción y purificación rápida de ADN a partir de: Gel de agarosa y Productos de PCR en solución
 K 1206 ADN PuriPrep-GP kit Extracción y purificación rápida de ADN a partir de: Gel de agarosa y Productos de PCR en solución Indice Presentación... 6 Importante... 6 Componentes del kit... 6 Condiciones
K 1206 ADN PuriPrep-GP kit Extracción y purificación rápida de ADN a partir de: Gel de agarosa y Productos de PCR en solución Indice Presentación... 6 Importante... 6 Componentes del kit... 6 Condiciones
PRÁCTICAS DE MICROBIOLOGÍA CLÍNICA (CURSO )
 PRÁCTICAS DE MICROBIOLOGÍA CLÍNICA (CURSO 2012 2013) PRÁCTICAS A REALIZAR ANÁLISIS CUALITATIVO DE ORINA PRUEBA DE BAUER KIRBY (ANTIBIOGRAMA) PRUEBA DE EPSILON (DETERMINACIÓN DE LA CMI) ANÁLISIS CUALITATIVO
PRÁCTICAS DE MICROBIOLOGÍA CLÍNICA (CURSO 2012 2013) PRÁCTICAS A REALIZAR ANÁLISIS CUALITATIVO DE ORINA PRUEBA DE BAUER KIRBY (ANTIBIOGRAMA) PRUEBA DE EPSILON (DETERMINACIÓN DE LA CMI) ANÁLISIS CUALITATIVO
Construcción de la biblioteca en cósmidos de Azospirillum brasilense CBG 497.
 Construcción de la biblioteca en cósmidos de Azospirillum brasilense CBG 497. Extracción de DNA genómico El DNA de A. brasilense CBG 497 se extrajo siguiendo el método descrito por la casa comercial distribuidora
Construcción de la biblioteca en cósmidos de Azospirillum brasilense CBG 497. Extracción de DNA genómico El DNA de A. brasilense CBG 497 se extrajo siguiendo el método descrito por la casa comercial distribuidora
Laboratorio Clínico Gendiag.exe, S.L. GENDIAG.LAB. Cartera Prestación Servicios
 Laboratorio Clínico Gendiag.exe, S.L. GENDIAG.LAB Cartera Prestación Servicios 10/10/2014 RESUMEN CARTERA SERVICIOS PRUEBA DESCRIPCIÓN TECNOLOGÍA (MÉTODO) Análisis (genotipado) de 113 marcadores genéticos
Laboratorio Clínico Gendiag.exe, S.L. GENDIAG.LAB Cartera Prestación Servicios 10/10/2014 RESUMEN CARTERA SERVICIOS PRUEBA DESCRIPCIÓN TECNOLOGÍA (MÉTODO) Análisis (genotipado) de 113 marcadores genéticos
PRÁCTICO N 4. Análisis de fertilidad del suelo
 PRÁCTICO N 4 Análisis de fertilidad del suelo OBJETIVOS Conocer las técnicas actuales de recuento de microorganismos. Conocer la importancia del monitoreo de abundancia, actividad y diversidad de los microorganismos
PRÁCTICO N 4 Análisis de fertilidad del suelo OBJETIVOS Conocer las técnicas actuales de recuento de microorganismos. Conocer la importancia del monitoreo de abundancia, actividad y diversidad de los microorganismos
INSTRUCCIONES DE USO
 1/4 INSTRUCCIONES DE USO (IMPROMINI TUBOS PARA LA RECOLECCION DE SANGRE CAPILAR PARA UN UNICO USO) Fabricante Guangzhou Improve Medical Instruments Co., Ltd Nombre del Producto Capillary Blood Collection
1/4 INSTRUCCIONES DE USO (IMPROMINI TUBOS PARA LA RECOLECCION DE SANGRE CAPILAR PARA UN UNICO USO) Fabricante Guangzhou Improve Medical Instruments Co., Ltd Nombre del Producto Capillary Blood Collection
BIOSEGURIDAD EN EL LABORATORIO DE MYCOBACTERIAS. Dr. Martin Yagui Moscoso
 BIOSEGURIDAD EN EL LABORATORIO DE MYCOBACTERIAS Dr. Martin Yagui Moscoso Contenido Brotes de TB en el laboratorio Riesgos de transmisión TB Barreras de contención Buenas Prácticas de Laboratorio Cabinas
BIOSEGURIDAD EN EL LABORATORIO DE MYCOBACTERIAS Dr. Martin Yagui Moscoso Contenido Brotes de TB en el laboratorio Riesgos de transmisión TB Barreras de contención Buenas Prácticas de Laboratorio Cabinas
Código: IDK-003 Ver: 1. Factor V Leiden
 Sistema para detección de la alteración G1691A en el gene que codifica para el Factor V de la coagulación humana Valdense 3616. 11700. Montevideo. Uruguay. Teléfono (598) 2 336 83 01. Fax (598) 2 336 71
Sistema para detección de la alteración G1691A en el gene que codifica para el Factor V de la coagulación humana Valdense 3616. 11700. Montevideo. Uruguay. Teléfono (598) 2 336 83 01. Fax (598) 2 336 71
NUEVO: tubo de 5,0 ml con tapa de rosca. El eslabón perdido. Eppendorf Tubes 5.0 ml sistema simple y seguro
 NUEVO: tubo de 5,0 ml con tapa de rosca El eslabón perdido 5.0 ml sistema simple y seguro 5mL_Tube_BRO_GB_2015.indd 1 27.11.15 14:04 2 En combinación con el amplio surtido de accesorios, los 5.0 ml son
NUEVO: tubo de 5,0 ml con tapa de rosca El eslabón perdido 5.0 ml sistema simple y seguro 5mL_Tube_BRO_GB_2015.indd 1 27.11.15 14:04 2 En combinación con el amplio surtido de accesorios, los 5.0 ml son
Código: KIT-005 Ver: 1 MTHFR C677T
 Sistema para detección de la alteración C677T en el gene que codifica para la Metilen-tetrahidrofolato reductasa humana 1 Valdense 3616. 11700. Montevideo. Uruguay. Teléfono (598) 2 336 83 01. Fax (598)
Sistema para detección de la alteración C677T en el gene que codifica para la Metilen-tetrahidrofolato reductasa humana 1 Valdense 3616. 11700. Montevideo. Uruguay. Teléfono (598) 2 336 83 01. Fax (598)
Código: IDX-016 Ver: 1 TOXO. Sistema para la detección de la presencia de ADN de Toxoplasma gondii. Reg. MSP 21205
 Sistema para la detección de la presencia de ADN de Toxoplasma gondii Reg. MSP 21205 Valdense 3616. 11700. Montevideo. Uruguay. Teléfono (598) 2 336 83 01. Fax (598) 2 336 71 60. info@atgen.com.uy www.atgen.com.uy
Sistema para la detección de la presencia de ADN de Toxoplasma gondii Reg. MSP 21205 Valdense 3616. 11700. Montevideo. Uruguay. Teléfono (598) 2 336 83 01. Fax (598) 2 336 71 60. info@atgen.com.uy www.atgen.com.uy
CONTROL DE CALIDAD DE MEDIOS DE CULTIVO. Maricela Esteban Méndez, Manuel Quintos Escalante, Alicia Herrera Benavides
 CONTROL DE CALIDAD DE MEDIOS DE CULTIVO Maricela Esteban Méndez, Manuel Quintos Escalante, Alicia Herrera Benavides Centro Interdisciplinario de Investigación para el Desarrollo Integral Regional Unidad
CONTROL DE CALIDAD DE MEDIOS DE CULTIVO Maricela Esteban Méndez, Manuel Quintos Escalante, Alicia Herrera Benavides Centro Interdisciplinario de Investigación para el Desarrollo Integral Regional Unidad
RECOPILADO POR: EL PROGRAMA UNIVERSITARIO DE ALIMENTOS
 NMX-F-187-1978. DETERMINACIÓN DEL NÚMERO MÁS PROBABLE DE GÉRMENES. METHOD OF TEST FOR GERMS MOST PROBABLE NUMBER. NORMAS MEXICANAS. DIRECCIÓN GENERAL DE NORMAS. PREFACIO En la elaboración de esta Norma
NMX-F-187-1978. DETERMINACIÓN DEL NÚMERO MÁS PROBABLE DE GÉRMENES. METHOD OF TEST FOR GERMS MOST PROBABLE NUMBER. NORMAS MEXICANAS. DIRECCIÓN GENERAL DE NORMAS. PREFACIO En la elaboración de esta Norma
COMO ABORDAR Y RESOLVER ASPECTOS PRÁCTICOS DE MICROBIOLOGÍA
 COMO ABORDAR Y RESOLVER ASPECTOS PRÁCTICOS DE MICROBIOLOGÍA 1. DILUCIONES Y CONCENTRACIONES. S LÍQUIDAS Y SÓLIDAS Inés Arana, Maite Orruño e Isabel Barcina Departamento Inmunología, Microbiología y Parasitología
COMO ABORDAR Y RESOLVER ASPECTOS PRÁCTICOS DE MICROBIOLOGÍA 1. DILUCIONES Y CONCENTRACIONES. S LÍQUIDAS Y SÓLIDAS Inés Arana, Maite Orruño e Isabel Barcina Departamento Inmunología, Microbiología y Parasitología
Instrucciones de uso. BAG Cycler Check. Kit de para la validación de la uniformidad de la temperatura en los termocicladores
 Instrucciones de uso BAG Cycler Check Kit de para la validación de la uniformidad de la temperatura en los termocicladores listo para usar, prealicuotado REF 7104 (10 tests) REF 71044 (4 tests) Contenidos
Instrucciones de uso BAG Cycler Check Kit de para la validación de la uniformidad de la temperatura en los termocicladores listo para usar, prealicuotado REF 7104 (10 tests) REF 71044 (4 tests) Contenidos
ScanGel ScanBrom ml
 ScanGel ScanBrom 86445 12 ml BROMELINA PARA PRUEBAS CRUZADAS IVD Todos los productos fabricados y comercializados por la sociedad Bio-Rad se hallan bajo un sistema de garantía de calidad desde la recepción
ScanGel ScanBrom 86445 12 ml BROMELINA PARA PRUEBAS CRUZADAS IVD Todos los productos fabricados y comercializados por la sociedad Bio-Rad se hallan bajo un sistema de garantía de calidad desde la recepción
Daniela Nieves Hernández Unidad de Metrología Soluciones Integrales y Metrología Aplicada
 Daniela Nieves Hernández Unidad de Metrología Soluciones Integrales y Metrología Aplicada Tipos de Micropipetas Micropipeta de Pistón con Cojín de Aire: Micropipeta de desplazamiento positivo: Micropipetas
Daniela Nieves Hernández Unidad de Metrología Soluciones Integrales y Metrología Aplicada Tipos de Micropipetas Micropipeta de Pistón con Cojín de Aire: Micropipeta de desplazamiento positivo: Micropipetas
Biplaca que se utiliza para evaluar la contaminación microbiológica de las superficies (Paredes, Techos, Equipos, Pisos, etc.) o Líquidos.
 BIPLACA HYCHECK Biplaca que se utiliza para evaluar la contaminación microbiológica de las superficies (Paredes, Techos, Equipos, Pisos, etc.) o Líquidos. Son estadísticamente comparables a una Torunda
BIPLACA HYCHECK Biplaca que se utiliza para evaluar la contaminación microbiológica de las superficies (Paredes, Techos, Equipos, Pisos, etc.) o Líquidos. Son estadísticamente comparables a una Torunda
SSI IMMUVIEW LEGIONELLA BLOOD TEST ANÁLISIS DE SANGRE IMMUVIEW LEGIONELLA
 SSI IMMUVIEW LEGIONELLA BLOOD TEST ANÁLISIS DE SANGRE IMMUVIEW LEGIONELLA Aplicación El análisis de sangre ImmuView Legionella de Statens Serum Institute se ha creado para el diagnóstico de una infección
SSI IMMUVIEW LEGIONELLA BLOOD TEST ANÁLISIS DE SANGRE IMMUVIEW LEGIONELLA Aplicación El análisis de sangre ImmuView Legionella de Statens Serum Institute se ha creado para el diagnóstico de una infección
Tissue_LC_200_V7_DSP y. Tissue_HC_200_V7_DSP. Sample to Insight. Agosto 2015 Hoja de protocolo del instrumento QIAsymphony SP
 Agosto 2015 Hoja de protocolo del instrumento QIAsymphony SP Tissue_LC_200_V7_DSP y Tissue_HC_200_V7_DSP Este documento es Hoja de protocolo del instrumento QIAsymphony SP para los protocolos Tissue_LC_200_V7_DSP
Agosto 2015 Hoja de protocolo del instrumento QIAsymphony SP Tissue_LC_200_V7_DSP y Tissue_HC_200_V7_DSP Este documento es Hoja de protocolo del instrumento QIAsymphony SP para los protocolos Tissue_LC_200_V7_DSP
PROCEDIMIENTO PARA LA DETERMINACIÓN DE HEMOGLOBINA MEDIANTE HEMOGLOBINOMETROS PORTATILES
 PROCEDIMIENTO PARA LA DETERMINACIÓN DE HEMOGLOBINA MEDIANTE HEMOGLOBINOMETROS PORTATILES 1 El procedimiento agrupa tres etapas: 1. Procedimiento previo a la punción capilar. 2. Procedimiento de la punción
PROCEDIMIENTO PARA LA DETERMINACIÓN DE HEMOGLOBINA MEDIANTE HEMOGLOBINOMETROS PORTATILES 1 El procedimiento agrupa tres etapas: 1. Procedimiento previo a la punción capilar. 2. Procedimiento de la punción
Indicadores Químicos y Biológicos para la esterilización térmica de cargas líquidas
 Indicadores Químicos y Biológicos para la esterilización térmica de cargas líquidas Terragene ofrece un método simple y eficaz para controlar con precisión el proceso de esterilización en la industria
Indicadores Químicos y Biológicos para la esterilización térmica de cargas líquidas Terragene ofrece un método simple y eficaz para controlar con precisión el proceso de esterilización en la industria
PRÁCTICA III. AISLAMIENTO DE MITOCONDRIAS: ACTIVIDAD MALATO DESHIDROGENASA
 PRÁCTICA III. AISLAMIENTO DE MITOCONDRIAS: ACTIVIDAD MALATO DESHIDROGENASA 1. Fundamento Teórico La mayoría de los procesos bioquímicos que producen energía química se realizan en orgánulos intracelulares
PRÁCTICA III. AISLAMIENTO DE MITOCONDRIAS: ACTIVIDAD MALATO DESHIDROGENASA 1. Fundamento Teórico La mayoría de los procesos bioquímicos que producen energía química se realizan en orgánulos intracelulares
UNIVERSIDAD NACIONAL MAYOR DE SAN MARCOS
 INFORME DE EVALUACIÓN ANTIBIOTICA N DE REGISTRO DEL ANÁLISIS: 690-05 SOLICITANTE: REFERENTE: AGROVET MARKET S.A. Umberto Calderón Ojeda IDENTIFICACION DE PRODUCTO Nombre Comercial: Principio Activo: Tilosina
INFORME DE EVALUACIÓN ANTIBIOTICA N DE REGISTRO DEL ANÁLISIS: 690-05 SOLICITANTE: REFERENTE: AGROVET MARKET S.A. Umberto Calderón Ojeda IDENTIFICACION DE PRODUCTO Nombre Comercial: Principio Activo: Tilosina
INSTRUCCIONES DE USO. Estándares Moleculares Helix Elite USO PREVISTO RESUMEN Y EXPLICACIÓN PRINCIPIOS COMPOSICIÓN
 INSTRUCCIONES DE USO Estándares Moleculares Helix Elite USO PREVISTO Los Estándares Moleculares sintéticos Helix Elite están diseñados para ser usados como material de control positivo en aplicaciones
INSTRUCCIONES DE USO Estándares Moleculares Helix Elite USO PREVISTO Los Estándares Moleculares sintéticos Helix Elite están diseñados para ser usados como material de control positivo en aplicaciones
OBTENCIÓN, PREPARACIÓN Y ENVÍO DE BIOPSIAS DE BAZO
 1 de 7 MANUAL DE PROCEDIMIENTOS OBTENCIÓN, PREPARACIÓN Y ENVÍO DE BIOPSIAS DE BAZO CONTROLADA Nº DESTINATARIO FECHA ENTREGA ENTREGADO POR Nombre Firma NO CONTROLADA ENTRADA EN REVISIÓN REALIZADO FECHA
1 de 7 MANUAL DE PROCEDIMIENTOS OBTENCIÓN, PREPARACIÓN Y ENVÍO DE BIOPSIAS DE BAZO CONTROLADA Nº DESTINATARIO FECHA ENTREGA ENTREGADO POR Nombre Firma NO CONTROLADA ENTRADA EN REVISIÓN REALIZADO FECHA
