Principio Activo: Gemcitabina clorhidrato Forma Farmacéutica: Polvo liofilizado estéril para Solución Inyectable
|
|
|
- Carla Pérez Rojo
- hace 7 años
- Vistas:
Transcripción
1 Gemcitabina 1000 mg Guarde este folleto, puede necesitar leerlo nuevamente. Si tiene cualquier duda o no está seguro de algo, pregunte a su médico o químico farmacéutico. Principio Activo: Gemcitabina clorhidrato Forma Farmacéutica: Polvo liofilizado estéril para Solución Inyectable Composición y Presentación: Cada frasco ampolla de Gemcitabina 1000 mg contiene: Gemcitabina (como clorhidrato) 1000 mg. Excipientes: Manitol, acetato de sodio trihidrato. Categoría: Antineoplásico. lndicaciones: Gemcitabina está indicado en el tratamiento de pacientes con diversos tipos de cáncer: - Cáncer Pulmonar de Células No-Pequeñas (No microcítico). La gemcitabina está indicada sola, o en combinación con cisplatino como tratamiento de primera línea en pacientes con cáncer pulmonar de células no pequeñas localmente avanzado o metastásico. - Cáncer de Páncreas: la gemcitabina está indicada como tratamiento de primera línea en pacientes con adenocarcinoma pancreático localmente avanzado a metastásico. Gemcitabina también está indicada para pacientes con cáncer pancreático refractario a 5- FU. - Cáncer de Ovario: la gemcitabina en combinación con cisplatino está indicada para el tratamiento de pacientes con carcinoma epitelial de ovario recurrente que han recaído después de un tratamiento mínimo de 6 meses con compuestos de platino. - Cáncer de Mama: Gemcitabina, en combinación está indicada para el tratamiento de pacientes con cáncer de mama con recurrencia local o metastásico, no resecable, que han recaído después de una quimioterapia adyuvante/neoadyuvante conteniendo alguna antraciclina. - Tracto biliar: Gemcitabina está indicado solo o en combinación, para el tratamiento de pacientes con cáncer de tracto biliar. - Cáncer cérvico-uteríno: Gemcitabina en combinación con cisplatino está indicado como tratamiento de primera línea en pacientes con cáncer cérvicouterino localmente avanzado y metastático. - Cáncer de vejiga: Gemcitabina está indicado sólo o en combinación con cisplatino para el tratamiento de pacientes con cáncer de vejiga avanzado a metastático. Posología:
2 Cáncer de pulmón no microcítico (de células no-pequeñas): - Adultos: la dosis recomendada de gemcitabina es de mg/m2 administrada por infusión intravenosa durante 30 minutos. Esta dosis debe repetirse una vez por semana durante tres semanas seguidas de una semana de descanso. Posteriormente se repite este ciclo de cuatro semanas. La reducción de la dosis se realiza según la toxicidad experimentada por el paciente. Gemcitabina en combinación con cisplatino: - Adultos: Gemcitabina en combinación con cisplatino fue investigado utilizando dos regímenes de dosis diferentes. Un régimen utiliza un esquema de 3 semanas y el otro régimen utiliza un esquema de 4 semanas. El esquema de tres semanas utiliza 1250 mg/ m2 de gemcitabina administrados en infusión intravenosa de 30 minutos, en los días 1 y 8 de cada ciclo de 21 días. La reducción de dosis en cada ciclo o dentro de cada ciclo se aplica basándose en el grado de toxicidad experimentada por el paciente. El esquema de cuatro semanas utiliza 1000 mg/ m2 de gemcitabina administrados en infusión intravenosa de 30 minutos, en los días 1, 8 y 15 de cada ciclo de 28 días. La reducción de dosis en cada ciclo o dentro de cada ciclo se aplica basándose en el grado de toxicidad experimentada por el paciente. Cáncer de vejiga: Gemcitabina solo: - Adultos: la dosis recomendada de gemcitabina es de 1250 mg/ m2. administrada mediante infusión intravenosa de 30 minutos. Esta dosis debe darse los días 1, 8 y 15 de un ciclo de 28' días. Este ciclo de 4 semanas debe luego repetirse. La reducción de la dosificación en cada ciclo o dentro del ciclo se aplica basándose en el grado de toxicidad experimentado por el paciente. Cáncer de Mama: Uso combinado de Gemcitabina con paclitaxel en adultos: se comienza utilizando paclitaxel (175 mg/ m2) administrado en el día 1 del ciclo, como infusión intravenosa, en aproximadamente 3 horas, seguida de gemcitabina (1250 mg/m2) como una infusión de 30 minutos en los días 1 y 8 de cada ciclo de 21 días. La dosis en cada ciclo o dentro de un mismo ciclo se puede reducir en función de la toxicidad experimentada por el paciente. Los pacientes deben tener una cuenta absoluta de granulocitos de al menos (xl06/ L) antes de iniciar la combinación de gemcitabina + paclitaxel. Uso como agente único en adultos: La dosis recomendada de gemcitabina es de 1,000 a 1,200 m9/ m2 administrada en una infusión durante 30 minutos, en los dias 1, 8 y 15 de cada ciclo de 28 días. Este ciclo de cuatro semanas debe repetirse. La dosis en cada ciclo o dentro de un mismo ciclo se puede reducir en función de la toxicidad experimentada por el paciente. Cáncer de ovario: Uso combinado en adultos: Gemcitabina en combinación con carboplatino. Se recomienda utilizar gemcitabina 1000 mg/ m2 administrada en los días 1 y 8 de cada ciclo de 21 días como una infusión intravenosa en 30 minutos. Después de la gemcitabina, se administrará el carboplatino en el día 1 de modo de conseguir un objetivo de área bajo la curva (AUC) de 4 mcg/ml/min.
3 La dosis en cada ciclo o dentro de un mismo ciclo se puede reducir en función de la toxicidad experimentada por el paciente. Los pacientes que reciben gemcitabina deben ser monitorizados antes de que les sea administrada cada dosis mediante recuentos de leucocitos, plaquetas y granulbcitos y, si fuera necesario, la dosis de gemcitabina puede ser reducida o suspendida en presencia de toxicidad hematológica. Se deben realizar, además, controles periódicos dela función hepática y renal, incluyendo transaminasas y creatinina sérica. Gemcitabina se tolera bien durante la infusión, habiéndose documentado sólo al unos casos de reacción en el lugar de inyección. No se han registrado casos de necrosis en la zona de inyección. Gemcitabina puede ser administrada fácilmente en régimen ambulatorio. Instrucciones de uso y manejo: El único diluyente aprobado para la reconstitución del clorhidrato de gemcitabina liofilizado, es el cloruro de sodio al 0.9% para inyección, sin preservativos. Debido a consideraciones de solubilidad, la concentración máxima de gemcitabina una vez reconstituida es de 40 mg/ml. La reconstitución a concentraciones mayores de 40 mg/ml. puede producir disolución incompleta y debe evitarse. Para su reconstitución, añada por lo menos 5 ml. de solución de cloruro de sodio al 0.9% para inyección al frasco de 200 mg o por lo menos 25 ml de solución de cloruro de sodio al 0.9% al frasco de 1 g. Agite para disolver. La cantidad apropiada de la droga puede ser administrada en la forma anterior o diluida aún más, con solución de cloruro de sodio al 0.9%. Los medicamentos parenterales deben ser inspeccionados visualmente para determinar la presencia de partículas o decoloración antes de su administración, en la medida en que la solución o el contenedor lo permitan. Es necesario observar los procedimientos de manipulación y disposición apropiados para los medicamentos oncológicos. El producto reconstituido con NaCl 09% puede mantenerse por 48 horas a temperatura ambiente: toda fracción de producto no utilizada debe ser incinerada. Infomación para su prescripción: Precauciones; Se ha demostrado un aumento de la toxicidad al prolongar el tiempo de infusión y al aumentar la frecuencia de las dosis. Gemcitabina tiene capacidad de producir supresión de la función medular, manifestándose como leucopenia, trombocitopenia y anemia. Sin embargo, la mielosupresión es de corta duración y normalmente no da lugar o necesidad de reducción de la dosis, siendo muy rara la suspensión de la medicación. Hipersensibilidad: se ha informado en raras ocasiones de algún caso de anafilaxis. En los pacientes bajo tratamiento con gemcitabina se requiere el monitoreo del recuento de plaquetas, leucocitos y granulocitos antes de cada dosis. Es necesario considerar la suspensión o la modificación de la terapia si se detecta una depresión de la médula inducida por el medicamento. Se deben evaluar en forma periódica con estudio de laboratorio las funciones renal y hepática.
4 Efectos sobre la capacidad para conducir y utilizar maquinaria: se han descrito casos de somnolencia de leve a moderada con el uso de emcitabina. Los pacientes deben evitar conducir o maneiar maquinarias hasta que se demuestre que no sufren somnolencia. Contraindioaciones: La gemcitabina está contraindicada en los pacientes con hipersensibilidad conocida al medicamento. Uso durante el embarazo: debe evitarse el uso de la Gemcitabina en mujeres embarazadas debido al riesgo potencial para el feto. Los estudios en animales de experimentación han mostrado toxicidad reproductora, por eiemplo, defectos de nacimiento y otros efectos sobre el desarrolo del embrión o del feto, el curso de la gestación o el desarrollo peri y postnatal. Usa durante la lactancia: debe evitarse el uso de la gemcitabina en muieres en periodo de lactancia debido al riesgo potencial para el niño. Advertencias: Carcinogénesis, mutagénesis, teratogénesis y sobre la fertilidad: Carcinogénesis. No se han realizado estudios a largo plazo en animales para evaluar su potencial carcinogónico. Mutogénesis: se ha producido daño citogénico por gemcitabina en un ensayo in vivo. La gemcitabina indujo mutación adelantada in vitro en un ensayo de linfoma en ratón (L5178Y). Efectos sobre la fertilidad: la gemcitabina causa una hipoespermatogénesis reversible, dependiente de la dosis y del esquema de administración en ratones machos. Aunque los estudios en animales han mostrado efecto sobre la fertilidad masculina, no se han observado efectos sobre la fertilidad femenina. Interacciones: Los estudios preclínicos y clínicos han demostrado que gemcitabina tiene actividad radiosensibilizante. En un estudio, se administró gemcitabina a una dosis de 1,000 m9/ m2 hasta por seis semanas consecutivas en forma concomitante con radioterapia torácica, en pacientes con cáncer de pulmón de células no pequeñas, se observó toxicidad significativa en forma de mucositis grave que potencialmente ponía en peligro la vida, especialmente esofagitis y neumonitis, en pacientes que recibieron altos volúmenes de radioterapia (volúmenes medios de tratamiento de 4,795 cm3). Los estudios realizados posteriormente han sugerido que es posible administrar gemcitabina a dosis menores con radioterapia concomitante con toxicidad predecible, como se estableció en un estudio de fase II en cáncer de pulmón de células no pequeñas. Efectos Adversos: Hematológicas: dado que gemcitabina es un supresor de la médula ósea, pueden aparecer anemia, leucopenia y trombocitopenia tras su administración. La mielosupresión suele ser de leve a moderada y más pronunciada en el recuento de granulocitos. Gastrointestinales: aproximadamente 2/3 de los pacientes presentan anomalías en las transaminasas hepáticas, pero éstas suelen ser leves, no progresivas y en muy raras
5 ocasiones es necesaria la suspensión del tratamiento. Se han comunicado náuseas y vómitos en l/3 de los pacientes. Este acontecimiento adverso requiere tratamiento en aproximádamente un 20% de los pacientes, raramente es limitante de la dosis y puede controlarse fácilmente con antieméticos. Renales: se han comunicado proteinuria y hematuria leves en aproximadamente la mitad de los pacientes, aunque raramente son clínicamente significativas y normalmente no se asocian a ningún cambio en la creatinina sérica o en el nitrógeno ureico san uíneo. No obstante, se han producido algunos casos de falla renal de etiología desconocida, por lo que gemcitabina debe ser administrada con precaución en pacientes con insuficiencia renal. En raras ocasiones, síndrome hemolítica-urémico (SHU) en que se debe suspender el tratamiento. Incluso después de suspender el tratamiento, puede aparecer la falla renal que puede ser irreversible y precisar diálisis. Alérgicas: se ha observado erupción cutánea en aproximadamente un 25% de las pacientes y está asociada a prurito en un 10% de los pacientes. La erupción es generalmente leve, no es limitante de dosis y responde a tratamiento local. En raras ocasiones han aparecido casos de descamación, vesiculación y ulceroción. Menos de un 1% de los pacientes han comunicado broncospasmo después de la infusión de gemcitabina que suele ser leve y transitorio, aunque puede ser necesario tratamiento parenteral. Aproximadamente un 10% de los pacientes han comunicado disnea en las horas siguientes a la administración de gemcitabina pero suele ser leve y de corta duración. Otros efectos: aproximadamente un 20% de los pacientes desarrollaron una sintomatología pseudogripal leve de corta duración, los síntomas más comunes son fiebre, dolor de cabeza dolor de espalda, escalofríos, mialgia y anorexia. También se han comunicado con frecuencia tos, rinitis, malestar general, sudor, insomnio y fiebre. En aproximadamente un 30% de los pacientes ha aparecido edema/edema periférico y edema facial. El edema/edema periférico suele ser de leve a moderada, y normalmente reversible después de suspender el tratamiento. En raras ocasiones, se han presentado síntomas pulmonares, que pueden llegar a ser graves como edema pulmonar, neumonitis intersticial o síndrome de distress respiratorio del adulto (SDRA) neumonitis intersticial (con infiltrados pulmonares asociados]. Si llegaran a presentarse, se debe considerar la posibilidad de interrumpir el tratamiento con gemcitabina. Los siguientes efectos adversos también se han comunicado frecuentemente: Alopecia (normalmente una mínima pérdida de cabello) en el 13% de los pacientes, somnolencia en un 10%, diarrea 8%, toxicidad bucal, que se maniliesta principalmente como ulceración y estomatitis, eritema en un 7%, y estreñimiento en un 6%. Se han comunicado algunos casos de hipotensión En los estudios realizados se han comunicado algunos casos de infarto de miocardio, insuficiencia cardiaca congestiva y arritmias, aunque no existe una evidencia clara de que gemcitabina cause toxicidad cardiaca También se han presentado casos de toxicidad por radiación, como se describe en las interacciones.
6 Sobredosis: Los sintomas de intoxicación son similares a los electos adversos descritos, destacándose la pérdida de glóbulos blancos. Destacan la mielosupresión, parestesia y rash severo. En el caso de una supuesta sobredosis, el paciente debe ser monitorizado, con recuentos sanguíneos frecuentes y recibiendo el tratamiento de mantenimiento necesario. Condiciones de almacenamiento: No manipular ni tomar contacto con la solución. Mantener lejos del alcance de los niños, en su envase original. Conservar en lugar seco a temperatura ambiente. No use este producto después de la fecha de vencimiento indicada en el envase. Desechar todos los materiales que han estado en contacto con el producto de acuerdo a las normas de seguridad para estos casos.
GENUTEN CITOSTÁTICO-ANTITUMORAL
 GENUTEN CITOSTÁTICO-ANTITUMORAL COMPOSICIÓN GENUTEN 200 mg. Cada frasco-ampolla contiene: Gemcitabina (como clorhidrato) 200 mg. Excipientes: Manitol, Acetato de sodio trihidrato, Hidróxido de sodio, Ácido
GENUTEN CITOSTÁTICO-ANTITUMORAL COMPOSICIÓN GENUTEN 200 mg. Cada frasco-ampolla contiene: Gemcitabina (como clorhidrato) 200 mg. Excipientes: Manitol, Acetato de sodio trihidrato, Hidróxido de sodio, Ácido
Polvo para solución inyectable para su reconstitución y administración por vía intravenosa.
 FT200899+3-B 1. DENOMINACIÓN DEL MEDICAMENTO GEMZAR Gemcitabina 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA GEMZAR 200 mg polvo para solución inyectable : cada vial contiene 200 mg de gemcitabina (DCI) (hidrocloruro).
FT200899+3-B 1. DENOMINACIÓN DEL MEDICAMENTO GEMZAR Gemcitabina 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA GEMZAR 200 mg polvo para solución inyectable : cada vial contiene 200 mg de gemcitabina (DCI) (hidrocloruro).
FOLLETO DE INFORMACION AL PACIENTE. ABRAXANE LIOFILIZADO PARA SUSPENSIÓN INYECTABLE 100 mg
 FOLLETO INFORMACION AL PACIENTE ABRAXANE LIOFILIZADO PARA SUSPENSIÓN INYECTABLE 100 mg NANOPARTICULAS DE PACLITAXEL LIGADO A ALBÚMINA Leer esta Información para el paciente antes de empezar a recibir ABRAXANE
FOLLETO INFORMACION AL PACIENTE ABRAXANE LIOFILIZADO PARA SUSPENSIÓN INYECTABLE 100 mg NANOPARTICULAS DE PACLITAXEL LIGADO A ALBÚMINA Leer esta Información para el paciente antes de empezar a recibir ABRAXANE
INFORMACION PARA PRESCRIBIR AMPLIA
 INFORMACION PARA PRESCRIBIR AMPLIA 1. Nombre Comercial: PAMIGEN 2. Nombre Genérico: GEMCITABINA 3. Forma Farmacéutica y Formulación: Solución Cada frasco ámpula con liofilizado contiene: Clorhidrato de
INFORMACION PARA PRESCRIBIR AMPLIA 1. Nombre Comercial: PAMIGEN 2. Nombre Genérico: GEMCITABINA 3. Forma Farmacéutica y Formulación: Solución Cada frasco ámpula con liofilizado contiene: Clorhidrato de
GEMCITABINA. 1000,0 mg. 24 meses
 RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO Nombre del producto: Forma farmacéutica: Fortaleza: Presentación: Titular del Registro Sanitario, país: Fabricante, país: GEMCITABINA Polvo liofilizado para
RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO Nombre del producto: Forma farmacéutica: Fortaleza: Presentación: Titular del Registro Sanitario, país: Fabricante, país: GEMCITABINA Polvo liofilizado para
Docetoxel solución concentrado inyectable 80 mg
 Docetoxel solución concentrado inyectable 80 mg Guarde este folleto, puede necesitar leerlo nuevamente. Si tiene cualquier duda o no está seguro de algo, pregunte a su médico o químico farmacéutico. Composición
Docetoxel solución concentrado inyectable 80 mg Guarde este folleto, puede necesitar leerlo nuevamente. Si tiene cualquier duda o no está seguro de algo, pregunte a su médico o químico farmacéutico. Composición
PROSPECTO: INFORMACIÓN PARA EL USUARIO. Gemcitabina Pharm V Solutions 1000 mg polvo para solución para perfusión EFG
 PROSPECTO: INFORMACIÓN PARA EL USUARIO Gemcitabina Pharm V Solutions 1000 mg polvo para solución para perfusión EFG Lea todo el prospecto detenidamente antes de empezar a usar el medicamento. - Conserve
PROSPECTO: INFORMACIÓN PARA EL USUARIO Gemcitabina Pharm V Solutions 1000 mg polvo para solución para perfusión EFG Lea todo el prospecto detenidamente antes de empezar a usar el medicamento. - Conserve
SODIOFOLIN 50 mg/ml solución para inyección o perfusión intravenosa
 L e a t o d o e l p r o s p e c t o d e t e n i d a m e n t e a n t e s d e e m p e z a r En este prospecto 1. Qué es Sodiofolin 50 mg/ml solución para inyección o perfusión intravenosa y para qué se utiliza
L e a t o d o e l p r o s p e c t o d e t e n i d a m e n t e a n t e s d e e m p e z a r En este prospecto 1. Qué es Sodiofolin 50 mg/ml solución para inyección o perfusión intravenosa y para qué se utiliza
PROSPECTO: INFORMACIÓN PARA EL USUARIO. Gemcitabina Kewl 1000 mg polvo para solución para perfusión EFG
 PROSPECTO: INFORMACIÓN PARA EL USUARIO Lea todo el prospecto detenidamente antes de empezar a usar el medicamento. - Conserve este prospecto, ya que puede tener que volver a leerlo. - Si tiene alguna duda,
PROSPECTO: INFORMACIÓN PARA EL USUARIO Lea todo el prospecto detenidamente antes de empezar a usar el medicamento. - Conserve este prospecto, ya que puede tener que volver a leerlo. - Si tiene alguna duda,
Resumen de las características del producto. 1 ml. Para consultar la lista completa de excipientes, ver sección 6.1.
 Resumen de las características del producto 1. NOMBRE DEL MEDICAMENTO Agua para preparaciones inyectables B.Braun Disolvente para uso parenteral 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Principio Activo
Resumen de las características del producto 1. NOMBRE DEL MEDICAMENTO Agua para preparaciones inyectables B.Braun Disolvente para uso parenteral 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Principio Activo
Prospecto: información para el usuario. Gemcitabina Hospira 1000 mg concentrado para solución para perfusión
 Prospecto: información para el usuario Gemcitabina Hospira 1000 mg concentrado para solución para perfusión Lea todo el prospecto detenidamente antes de empezar a usar este medicamento, porque contiene
Prospecto: información para el usuario Gemcitabina Hospira 1000 mg concentrado para solución para perfusión Lea todo el prospecto detenidamente antes de empezar a usar este medicamento, porque contiene
PP060912_2+1A (II28) PROSPECTO: INFORMACIÓN PARA EL USUARIO. Gemzar 200 mg polvo para solución para perfusión Gemcitabina
 PP060912_2+1A (II28) PROSPECTO: INFORMACIÓN PARA EL USUARIO Gemzar 200 mg polvo para solución para perfusión Gemcitabina Lea todo el prospecto detenidamente antes de empezar a usar este medicamento, porque
PP060912_2+1A (II28) PROSPECTO: INFORMACIÓN PARA EL USUARIO Gemzar 200 mg polvo para solución para perfusión Gemcitabina Lea todo el prospecto detenidamente antes de empezar a usar este medicamento, porque
FICHA TÉCNICA ECHINACIN MADAUS solución oral Echinacea purpurea
 FICHA TÉCNICA ECHINACIN MADAUS solución oral Echinacea purpurea 1. NOMBRE DEL MEDICAMENTO ECHINACIN MADAUS solución oral Echinacea purpurea 2. COMPOSICION CUALITATIVA Y CUANTITATIVA Cada ml contiene: Jugo
FICHA TÉCNICA ECHINACIN MADAUS solución oral Echinacea purpurea 1. NOMBRE DEL MEDICAMENTO ECHINACIN MADAUS solución oral Echinacea purpurea 2. COMPOSICION CUALITATIVA Y CUANTITATIVA Cada ml contiene: Jugo
Prospecto: información para el usuario. Gemcitabina Hospira 200 mg concentrado para solución para perfusión
 Prospecto: información para el usuario Gemcitabina Hospira 200 mg concentrado para solución para perfusión Lea todo el prospecto detenidamente antes de empezar a usar este medicamento, porque contiene
Prospecto: información para el usuario Gemcitabina Hospira 200 mg concentrado para solución para perfusión Lea todo el prospecto detenidamente antes de empezar a usar este medicamento, porque contiene
FOLLETO DE INFORMACIÓN AL PROFESIONAL GEMCIMIRA SOLUCIÓN INYECTABLE 1g/26,3 ml GEMCIMIRA SOLUCION INYECTABLE 200 mg/5,3 ml (Gemcitabina clorhidrato)
 FOLLETO DE INFORMACIÓN AL PROFESIONAL GEMCIMIRA SOLUCIÓN INYECTABLE 1g/26,3 ml GEMCIMIRA SOLUCION INYECTABLE 200 mg/5,3 ml (Gemcitabina clorhidrato) 1. NOMBRE DEL MEDICAMENTO GEMCIMIRA Solución Inyectable
FOLLETO DE INFORMACIÓN AL PROFESIONAL GEMCIMIRA SOLUCIÓN INYECTABLE 1g/26,3 ml GEMCIMIRA SOLUCION INYECTABLE 200 mg/5,3 ml (Gemcitabina clorhidrato) 1. NOMBRE DEL MEDICAMENTO GEMCIMIRA Solución Inyectable
PROSPECTO: INFORMACIÓN PARA EL USUARIO. Gemzar 200 mg polvo para solución para perfusión Gemcitabina
 PROSPECTO: INFORMACIÓN PARA EL USUARIO Gemzar 200 mg polvo para solución para perfusión Gemcitabina Lea todo el prospecto detenidamente antes de empezar a usar este medicamento, porque contiene información
PROSPECTO: INFORMACIÓN PARA EL USUARIO Gemzar 200 mg polvo para solución para perfusión Gemcitabina Lea todo el prospecto detenidamente antes de empezar a usar este medicamento, porque contiene información
FICHA TÉCNICA. 1. DENOMINACIÓN DEL MEDICAMENTO: GLUCOSAMINA GINELADIUS 625 mg comprimidos recubiertos con película
 FICHA TÉCNICA 1. DENOMINACIÓN DEL MEDICAMENTO: GLUCOSAMINA GINELADIUS 625 mg comprimidos recubiertos con película 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Un comprimido contiene 750 mg de Hidrocloruro
FICHA TÉCNICA 1. DENOMINACIÓN DEL MEDICAMENTO: GLUCOSAMINA GINELADIUS 625 mg comprimidos recubiertos con película 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Un comprimido contiene 750 mg de Hidrocloruro
Estadíos tumor maligno de cuello uterino
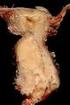 TUMOR MALIGNO DE CUELLO UTERINO Codificación CIE10 C53 tumor maligno del cuello del útero Problema: El cáncer cervical usualmente es un carcinoma de células escamosas (70% de todos los cánceres cervicales),
TUMOR MALIGNO DE CUELLO UTERINO Codificación CIE10 C53 tumor maligno del cuello del útero Problema: El cáncer cervical usualmente es un carcinoma de células escamosas (70% de todos los cánceres cervicales),
INFORMACION PARA PRESCRIBIR AMPLIA:
 INFORMACION PARA PRESCRIBIR AMPLIA: 1. Nombre Comercial: CARBOPLAT 2. Nombre Genérico: CARBOPLATINO 3. Forma Farmacéutica y Formulación: Solución Inyectable. Cada frasco ámpula con liofilizado contiene:
INFORMACION PARA PRESCRIBIR AMPLIA: 1. Nombre Comercial: CARBOPLAT 2. Nombre Genérico: CARBOPLATINO 3. Forma Farmacéutica y Formulación: Solución Inyectable. Cada frasco ámpula con liofilizado contiene:
FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO
 FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1. NOMBRE DEL MEDICAMENTO Gemcitabina ratiopharm 200 mg polvo para solución para perfusión EFG Gemcitabina ratiopharm 1 g polvo para solución
FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1. NOMBRE DEL MEDICAMENTO Gemcitabina ratiopharm 200 mg polvo para solución para perfusión EFG Gemcitabina ratiopharm 1 g polvo para solución
FOLLETO DE INFORMACIÓN AL PACIENTE DOLGENAL SOLUCIÓN INYECTABLE 30mg/1mL
 FOLLETO DE INFORMACIÓN AL PACIENTE DOLGENAL SOLUCIÓN INYECTABLE 30mg/1mL DOLGENAL Ketorolaco Trometamol 30 mg/1 ml Solución inyectable Vía de Administración: I.M. - I.V. Venta bajo receta médica en establecimientos
FOLLETO DE INFORMACIÓN AL PACIENTE DOLGENAL SOLUCIÓN INYECTABLE 30mg/1mL DOLGENAL Ketorolaco Trometamol 30 mg/1 ml Solución inyectable Vía de Administración: I.M. - I.V. Venta bajo receta médica en establecimientos
3. PROPIEDADES FARMACOLOGICAS Grupo farmacoterapéutico: Antineoplásicos, análogos de pirimidina. Código ATC: L01BC05
 1. NOMBRE DEL PRINCIPIO ACTIVO (DCI) GEMCITABINA 2. VIA DE ADMINISTRACION INTRAVENOSA 3. PROPIEDADES FARMACOLOGICAS Grupo farmacoterapéutico: Antineoplásicos, análogos de pirimidina. Código ATC: L01BC05
1. NOMBRE DEL PRINCIPIO ACTIVO (DCI) GEMCITABINA 2. VIA DE ADMINISTRACION INTRAVENOSA 3. PROPIEDADES FARMACOLOGICAS Grupo farmacoterapéutico: Antineoplásicos, análogos de pirimidina. Código ATC: L01BC05
Prospecto: información para el usuario. Gemcitabina Hetero 200 mg polvo para solución para perfusión EFG Gemcitabina hidrocloruro
 Prospecto: información para el usuario Gemcitabina Hetero 200 mg polvo para solución para perfusión EFG Gemcitabina hidrocloruro Lea todo el prospecto detenidamente antes de empezar a tomar este medicamento,
Prospecto: información para el usuario Gemcitabina Hetero 200 mg polvo para solución para perfusión EFG Gemcitabina hidrocloruro Lea todo el prospecto detenidamente antes de empezar a tomar este medicamento,
FICHA TÉCNICA. Excipientes con efecto conocido: 0,458 g de maltitol líquido (E965) y 1,830 g de isomalta (E953).
 1. NOMBRE DEL MEDICAMENTO FICHA TÉCNICA STREPSILS pastillas para chupar sabor limón 2.- COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Por pastilla para chupar: Amilmetacresol, 0,6 mg Alcohol 2,4 diclorobencílico,
1. NOMBRE DEL MEDICAMENTO FICHA TÉCNICA STREPSILS pastillas para chupar sabor limón 2.- COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Por pastilla para chupar: Amilmetacresol, 0,6 mg Alcohol 2,4 diclorobencílico,
Prospecto: Información para el usuario. Gemcitabina Aurovitas Spain mg concentrado para solución para perfusión
 Prospecto: Información para el usuario Gemcitabina Aurovitas Spain 1.000 mg concentrado para solución para perfusión Lea todo el prospecto detenidamente antes de empezar a usar este medicamento, porque
Prospecto: Información para el usuario Gemcitabina Aurovitas Spain 1.000 mg concentrado para solución para perfusión Lea todo el prospecto detenidamente antes de empezar a usar este medicamento, porque
Prospecto: Información para el usuario. Gemcitabina Aurovitas Spain 200 mg concentrado para solución para perfusión
 Prospecto: Información para el usuario Gemcitabina Aurovitas Spain 200 mg concentrado para solución para perfusión Lea todo el prospecto detenidamente antes de empezar a usar este medicamento, porque contiene
Prospecto: Información para el usuario Gemcitabina Aurovitas Spain 200 mg concentrado para solución para perfusión Lea todo el prospecto detenidamente antes de empezar a usar este medicamento, porque contiene
FICHA TÉCNICA. Normoreum 400 mg comprimidos recubiertos con película
 FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Normoreum 400 mg comprimidos recubiertos con película 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada comprimido contiene: Principios activos: 400 mg de extracto
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Normoreum 400 mg comprimidos recubiertos con película 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada comprimido contiene: Principios activos: 400 mg de extracto
RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO MONTEVIDEO, URUGUAY.
 RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO Nombre del producto: Forma farmacéutica: Fortaleza: Presentación: Titular del Registro Sanitario, país: Fabricante, país: OXALIPLATINO 100 mg Liofilizado para
RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO Nombre del producto: Forma farmacéutica: Fortaleza: Presentación: Titular del Registro Sanitario, país: Fabricante, país: OXALIPLATINO 100 mg Liofilizado para
FICHA TÉCNICA, ETIQUETADO Y PROSPECTO FICHA TÉCNICA
 1.3.1. FICHA TÉCNICA, ETIQUETADO Y PROSPECTO FICHA TÉCNICA MÓDULO 1. AGUA INYECCION GRIFOLS 1 1. NOMBRE DEL MEDICAMENTO Agua para Inyección Grifols 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Agua para preparaciones
1.3.1. FICHA TÉCNICA, ETIQUETADO Y PROSPECTO FICHA TÉCNICA MÓDULO 1. AGUA INYECCION GRIFOLS 1 1. NOMBRE DEL MEDICAMENTO Agua para Inyección Grifols 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Agua para preparaciones
Prospecto: información para el usuario
 Prospecto: información para el usuario Sugiran 20 microgramos polvo para solución para perfusión Alprostadil Lea todo el prospecto detenidamente antes de empezar a usar el medicamento. Conserve este prospecto,
Prospecto: información para el usuario Sugiran 20 microgramos polvo para solución para perfusión Alprostadil Lea todo el prospecto detenidamente antes de empezar a usar el medicamento. Conserve este prospecto,
ANASTROZOL COMPRIMIDOS RECUBIERTOS 1 mg. COMPOSICIÓN Cada comprimido recubierto contiene: Excipientes: Según lo aprobado en Registro
 ANASTROZOL COMPRIMIDOS RECUBIERTOS 1 mg COMPOSICIÓN Cada comprimido recubierto contiene: Anastrozol 1 mg Excipientes: Según lo aprobado en Registro CLASIFICACION TERAPEUTICA Antineoplásico INDICACIONES
ANASTROZOL COMPRIMIDOS RECUBIERTOS 1 mg COMPOSICIÓN Cada comprimido recubierto contiene: Anastrozol 1 mg Excipientes: Según lo aprobado en Registro CLASIFICACION TERAPEUTICA Antineoplásico INDICACIONES
CARBOPLATINO PHARMACIA 10 mg/ml concentrado para solución para perfusión EFG
 CARBOPLATINO PHARMACIA 10 mg/ml concentrado para solución para perfusión EFG COMPOSICIÓN Por ml: Principio activo: Carboplatino (D.C.I.) 10 mg Excipientes: Agua para inyección c.s. FORMA FARMACÉUTICA Y
CARBOPLATINO PHARMACIA 10 mg/ml concentrado para solución para perfusión EFG COMPOSICIÓN Por ml: Principio activo: Carboplatino (D.C.I.) 10 mg Excipientes: Agua para inyección c.s. FORMA FARMACÉUTICA Y
- Como disolvente de medicamentos en polvo o liofilizados, previamente a su administración. - Como diluyente de soluciones y/o medicamentos.
 FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Agua para preparaciones inyectables SERRACLINICS. 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada 100 ml contienen agua para preparaciones inyectables. ph: 5,0-7,0
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Agua para preparaciones inyectables SERRACLINICS. 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada 100 ml contienen agua para preparaciones inyectables. ph: 5,0-7,0
LABORATORIOS NORMON, S.A. AMBROXOL NORMON 15 mg/5 ml Jarabe EFG
 1. NOMBRE DEL MEDICAMENTO 2. COMPOSICION CUALITATIVA Y CUANTITATIVA Cada 5 ml de jarabe contienen: AMBROXOL (D.C.I.) hidrocloruro 15 mg Excipientes, ver apartado 6.1. 3. FORMA FARMACEUTICA Jarabe. 4. DATOS
1. NOMBRE DEL MEDICAMENTO 2. COMPOSICION CUALITATIVA Y CUANTITATIVA Cada 5 ml de jarabe contienen: AMBROXOL (D.C.I.) hidrocloruro 15 mg Excipientes, ver apartado 6.1. 3. FORMA FARMACEUTICA Jarabe. 4. DATOS
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO. Tusheel películas bucodispersables 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA
 FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Tusheel películas bucodispersables 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada película bucodispersable contiene 16 mg de extracto (como extracto seco) de hoja
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Tusheel películas bucodispersables 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada película bucodispersable contiene 16 mg de extracto (como extracto seco) de hoja
GUÍA DE ADMINISTRACIÓN Y DOSIFICACIÓN
 Pulmón* Riñón* Vejiga* GUÍA DE ADMINISTRACIÓN Y DOSIFICACIÓN AHORA A DOSIS FIJA OPDIVO está indicado para el tratamiento de: 1 Pulmón* Riñón* Vejiga* AHORA A DOSIS FIJA DOSIS EN RÉGIMEN DOSIS EN RÉGIMEN
Pulmón* Riñón* Vejiga* GUÍA DE ADMINISTRACIÓN Y DOSIFICACIÓN AHORA A DOSIS FIJA OPDIVO está indicado para el tratamiento de: 1 Pulmón* Riñón* Vejiga* AHORA A DOSIS FIJA DOSIS EN RÉGIMEN DOSIS EN RÉGIMEN
FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO
 FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1. NOMBRE DEL MEDICAMENTO Gemcitabina Hospira 200 mg Polvo para solución para perfusión EFG Gemcitabina Hospira 1 g Polvo para solución para
FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1. NOMBRE DEL MEDICAMENTO Gemcitabina Hospira 200 mg Polvo para solución para perfusión EFG Gemcitabina Hospira 1 g Polvo para solución para
FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO
 FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1. NOMBRE DEL MEDICAMENTO Gemcitabina Hospira 200 mg Polvo para solución para perfusión EFG Gemcitabina Hospira 1 g Polvo para solución para
FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1. NOMBRE DEL MEDICAMENTO Gemcitabina Hospira 200 mg Polvo para solución para perfusión EFG Gemcitabina Hospira 1 g Polvo para solución para
DRAGOXILO Suspensión Oral
 DRAGOXILO Suspensión Oral ANTIMICROBIANO DE AMPLIO ESPECTRO. Dragoxilo polvo para reconstituir suspensión oral, está indicado en el tratamiento de infecciones de la piel y tejidos blandos provocadas por
DRAGOXILO Suspensión Oral ANTIMICROBIANO DE AMPLIO ESPECTRO. Dragoxilo polvo para reconstituir suspensión oral, está indicado en el tratamiento de infecciones de la piel y tejidos blandos provocadas por
PROSPECTO: INFORMACION PARA EL USUARIO. MITOMYCIN-C 40 mg Polvo para solución inyectable Mitomicina
 PROSPECTO: INFORMACION PARA EL USUARIO MITOMYCIN-C 40 mg Polvo para solución inyectable Mitomicina Lea todo el prospecto detenidamente antes de empezar a usar el medicamento. - Conserve este prospecto
PROSPECTO: INFORMACION PARA EL USUARIO MITOMYCIN-C 40 mg Polvo para solución inyectable Mitomicina Lea todo el prospecto detenidamente antes de empezar a usar el medicamento. - Conserve este prospecto
FICHA TÉCNICA. Pacientes de edad avanzada No se requiere ajuste de dosis para el tratamiento de pacientes de edad avanzada.
 FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO GLUFAN 625 mg comprimidos recubiertos con película 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Un comprimido contiene 750 mg de hidrocloruro de glucosamina, equivalente
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO GLUFAN 625 mg comprimidos recubiertos con película 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Un comprimido contiene 750 mg de hidrocloruro de glucosamina, equivalente
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO. ACICLOVIR ACCORD INYECTABLE EFG Infusión intravenosa 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA
 FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO ACICLOVIR ACCORD INYECTABLE EFG Infusión intravenosa 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada vial contiene: Aciclovir (D.C.I.) (sódico) 250 mg 3. FORMA FARMACÉUTICA
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO ACICLOVIR ACCORD INYECTABLE EFG Infusión intravenosa 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada vial contiene: Aciclovir (D.C.I.) (sódico) 250 mg 3. FORMA FARMACÉUTICA
PROSPECTO: INFORMACIÓN PARA EL USUARIO. Folinato cálcico G.E.S. 50 mg polvo para solución inyectable EFG. Ácido Folínico
 PROSPECTO: INFORMACIÓN PARA EL USUARIO Folinato cálcico G.E.S. 50 mg polvo para solución inyectable EFG Ácido Folínico Lea todo el prospecto detenidamente antes de empezar a usar este medicamento, porque
PROSPECTO: INFORMACIÓN PARA EL USUARIO Folinato cálcico G.E.S. 50 mg polvo para solución inyectable EFG Ácido Folínico Lea todo el prospecto detenidamente antes de empezar a usar este medicamento, porque
FICHA TÉCNICA. Cada vial contiene hidrocloruro de gemcitabina equivalentes a 200 mg de gemcitabina.
 FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Gemzar 200 mg polvo para solución para perfusión. Gemzar 1.000 mg polvo para solución para perfusión. 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada vial contiene
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Gemzar 200 mg polvo para solución para perfusión. Gemzar 1.000 mg polvo para solución para perfusión. 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada vial contiene
FICHA TÉCNICA. Cada vial contiene hidrocloruro de gemcitabina equivalentes a 200 mg de gemcitabina.
 FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Gemzar 200 mg polvo para solución para perfusión. Gemzar 1.000 mg polvo para solución para perfusión. 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada vial contiene
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Gemzar 200 mg polvo para solución para perfusión. Gemzar 1.000 mg polvo para solución para perfusión. 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada vial contiene
Tratamiento en pacientes con cancer de mama no susceptible de cirugía, metastásico o localmente avanzado, en combinación con paclitaxel, siempre que
 1. DENOMINACIÓN DEL ESQUEMA: PACLITAXEL + GEMCITABINA 2. INDICACIÓN Tratamiento en pacientes con cancer de mama no susceptible de cirugía, metastásico o localmente avanzado, en combinación con paclitaxel,
1. DENOMINACIÓN DEL ESQUEMA: PACLITAXEL + GEMCITABINA 2. INDICACIÓN Tratamiento en pacientes con cancer de mama no susceptible de cirugía, metastásico o localmente avanzado, en combinación con paclitaxel,
FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO
 FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1. NOMBRE DEL MEDICAMENTO Gemcitabina medac 200 mg polvo para solución para perfusión EFG Gemcitabina medac 1000 mg polvo para solución para
FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1. NOMBRE DEL MEDICAMENTO Gemcitabina medac 200 mg polvo para solución para perfusión EFG Gemcitabina medac 1000 mg polvo para solución para
FICHA TÉCNICA. Niños entre 6 y 12 años de edad: 4 ml de jarabe, 2 veces al día, (equivalente a 66 mg diarios de extracto seco de hojas de hiedra).
 FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Cinfahelix jarabe. Extracto de Hedera helix L 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada ml de jarabe de Cinfahelix (equivalente a 1,18 g) contiene: 8,25 mg
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Cinfahelix jarabe. Extracto de Hedera helix L 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada ml de jarabe de Cinfahelix (equivalente a 1,18 g) contiene: 8,25 mg
FICHA TÉCNICA. Sorbitol líquido (no cristalizante); 1 ml de jarabe contiene 495,6 mg de sorbitol (E 420).
 FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Bisolvon Expectorante jarabe Extracto seco de hojas de hiedra 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Composición cualitativa y cuantitativa 1 ml de jarabe de
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Bisolvon Expectorante jarabe Extracto seco de hojas de hiedra 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Composición cualitativa y cuantitativa 1 ml de jarabe de
SIMETICONA 100 mg- CLORDIAZEPÓXIDO (CLORHIDRATO) 5 mg- METOCLOPRAMIDA (CLORHIDRATO) 5mg CAPSULAS
 SIMETICONA 100 mg- CLORDIAZEPÓXIDO (CLORHIDRATO) 5 mg- METOCLOPRAMIDA (CLORHIDRATO) 5mg CAPSULAS Lea cuidadosamente este folleto antes de la administración de este medicamento. Contiene información importante
SIMETICONA 100 mg- CLORDIAZEPÓXIDO (CLORHIDRATO) 5 mg- METOCLOPRAMIDA (CLORHIDRATO) 5mg CAPSULAS Lea cuidadosamente este folleto antes de la administración de este medicamento. Contiene información importante
Prospecto: información para el paciente. Carnicor 200 mg/ml solución inyectable L-carnitina
 Prospecto: información para el paciente Carnicor 200 mg/ml solución inyectable L-carnitina Lea todo el prospecto detenidamente antes de empezar a usar este medicamento, porque contiene información importante
Prospecto: información para el paciente Carnicor 200 mg/ml solución inyectable L-carnitina Lea todo el prospecto detenidamente antes de empezar a usar este medicamento, porque contiene información importante
FICHA TÉCNICA. Excipientes con efecto conocido 1,38 g de sacarosa y 1,10 g glucosa. Para consultar la lista completa de excipientes ver sección 6.1.
 1. NOMBRE DEL MEDICAMENTO FICHA TÉCNICA STREPSILS pastillas para chupar sabor menta 2.- COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Por pastilla para chupar: Amilmetacresol, 0,6 mg Alcohol 2,4-diclorobencílico,
1. NOMBRE DEL MEDICAMENTO FICHA TÉCNICA STREPSILS pastillas para chupar sabor menta 2.- COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Por pastilla para chupar: Amilmetacresol, 0,6 mg Alcohol 2,4-diclorobencílico,
FICHA TÉCNICA. Un ml de la solución para perfusión reconstituida contiene 38 mg de gemcitabina (como hidrocloruro).
 FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Gemcitabina SUN 200 mg polvo para solución para perfusión EFG. Gemcitabina SUN 1000 mg polvo para solución para perfusión EFG 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Gemcitabina SUN 200 mg polvo para solución para perfusión EFG. Gemcitabina SUN 1000 mg polvo para solución para perfusión EFG 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA
FICHA TÉCNICA. Un ml de la solución para perfusión reconstituida contiene 38 mg de gemcitabina.
 FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Gemcitabina Kabi 200 mg polvo para solución para perfusion EFG Gemcitabina Kabi 1000 mg polvo para solución para perfusion EFG Gemcitabina Kabi 2000 mg polvo para
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Gemcitabina Kabi 200 mg polvo para solución para perfusion EFG Gemcitabina Kabi 1000 mg polvo para solución para perfusion EFG Gemcitabina Kabi 2000 mg polvo para
FICHA TÉCNICA. Alivio de los síntomas del dolor agudo de garganta en adultos y niños mayores de 6 años.
 FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Geisil 0.6 mg / 1.2 mg pastillas para chupar sabor menta amilmetacresol / alcohol dichlorobencílico Geisil 0.6 mg / 1.2 mg pastillas para chupar sabor miel y limón
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Geisil 0.6 mg / 1.2 mg pastillas para chupar sabor menta amilmetacresol / alcohol dichlorobencílico Geisil 0.6 mg / 1.2 mg pastillas para chupar sabor miel y limón
COMPOSICIÓN CUALITATIVA Y CUANTITATIVA DE LA SUSTANCIA ACTIVA Y OTRAS SUSTANCIAS
 PROSPECTO NOMBRE O RAZON SOCIAL Y DOMICILIO O SEDE SOCIAL DEL TITULAR DE LA AUTORIZACIÓN DE COMERCIALIZACIÓN Y DEL FABRICANTE RESPONSABLE DE LA LIBERACIÓN DE LOS LOTES, EN CASO DE QUE SEAN DIFERENTES Titular
PROSPECTO NOMBRE O RAZON SOCIAL Y DOMICILIO O SEDE SOCIAL DEL TITULAR DE LA AUTORIZACIÓN DE COMERCIALIZACIÓN Y DEL FABRICANTE RESPONSABLE DE LA LIBERACIÓN DE LOS LOTES, EN CASO DE QUE SEAN DIFERENTES Titular
PROSPECTO. CEFTRIAXONA REIG JOFRÉ 1 g IM. Polvo y disolvente para solución inyectable. E.F.G. Ceftriaxona (D.C.I.)
 PROSPECTO Lea todo el prospecto detenidamente antes de empezar a usar el medicamento. - Conserve este prospecto. Puede tener que volver a leerlo. - Si tiene alguna duda, consulte a su médico o farmacéutico.
PROSPECTO Lea todo el prospecto detenidamente antes de empezar a usar el medicamento. - Conserve este prospecto. Puede tener que volver a leerlo. - Si tiene alguna duda, consulte a su médico o farmacéutico.
Cada ml de barniz de uñas medicamentoso contiene 280 mg de tioconazol.
 1. NOMBRE DEL MEDICAMENTO TROSID 280 mg/ml barniz de uñas medicamentoso 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada ml de barniz de uñas medicamentoso contiene 280 mg de tioconazol. Para consultar la
1. NOMBRE DEL MEDICAMENTO TROSID 280 mg/ml barniz de uñas medicamentoso 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada ml de barniz de uñas medicamentoso contiene 280 mg de tioconazol. Para consultar la
RESUMEN DE CARACTERÍSTICAS DEL PRODUCTO
 RESUMEN DE CARACTERÍSTICAS DEL PRODUCTO 1. DENOMINACIÓN DEL MEDICAMENTO VETERINARIO TOLFEDINE 4% 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA. INGREDIENTES ACTIVOS: Ácido tolfenámico... 4,00 g EXCIPIENTES:
RESUMEN DE CARACTERÍSTICAS DEL PRODUCTO 1. DENOMINACIÓN DEL MEDICAMENTO VETERINARIO TOLFEDINE 4% 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA. INGREDIENTES ACTIVOS: Ácido tolfenámico... 4,00 g EXCIPIENTES:
Prospecto: información para el paciente VEPESID 50 mg cápsulas de gelatina blanda. Etopósido
 Prospecto: información para el paciente VEPESID 50 mg cápsulas de gelatina blanda Etopósido Lea todo el prospecto detenidamente antes de empezar a tomar este medicamento porque contiene información importante
Prospecto: información para el paciente VEPESID 50 mg cápsulas de gelatina blanda Etopósido Lea todo el prospecto detenidamente antes de empezar a tomar este medicamento porque contiene información importante
FICHA TÉCNICA. La cantidad de principios activos presentes en 1 ml de ADDAMEL es de:
 FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO ADDAMEL concentrado para solución para perfusión 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA 1 ml de ADDAMEL contiene: Principio activo Cantidad Cloruro de cromo,
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO ADDAMEL concentrado para solución para perfusión 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA 1 ml de ADDAMEL contiene: Principio activo Cantidad Cloruro de cromo,
INFORMACIÓN PARA PRESCRIBIR AMPLIA. Seroalbúmina Humana 12.5 g 25 g Vehículo c.b.p. 50 ml 100 ml
 INFORMACIÓN PARA PRESCRIBIR AMPLIA IPP-A 1. DENOMINACIÓN DISTINTIVA ALBUMINA HUMANA GRIFOLS 2. DENOMINACIÓN GENÉRICA Seroalbúmina Humana 25% 3. FORMA FARMACÉUTICA Y FORMULACIÓN El frasco ámpula contiene:
INFORMACIÓN PARA PRESCRIBIR AMPLIA IPP-A 1. DENOMINACIÓN DISTINTIVA ALBUMINA HUMANA GRIFOLS 2. DENOMINACIÓN GENÉRICA Seroalbúmina Humana 25% 3. FORMA FARMACÉUTICA Y FORMULACIÓN El frasco ámpula contiene:
El contenido de iones de electrolitos por sobre reconstituido hasta 125 ml de solución es:
 1. NOMBRE DEL MEDICAMENTO Macrogol Sandoz 13,7 g polvo para solución oral 2 COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada sobre contiene los siguientes principios activos: Macrogol 3350 13,125 g Cloruro
1. NOMBRE DEL MEDICAMENTO Macrogol Sandoz 13,7 g polvo para solución oral 2 COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada sobre contiene los siguientes principios activos: Macrogol 3350 13,125 g Cloruro
1. DENOMINACION DEL ESQUEMA: CISPLATINO-GEMCITABINA
 1. DENOMINACION DEL ESQUEMA: CISPLATINO-GEMCITABINA 2. USO TERAPÉUTICO Primera línea de tratamiento en cancer de pulmón no microcítico con enfermedad metastásica avanzada (estadío IV) 3. ESQUEMA (1,2,3)
1. DENOMINACION DEL ESQUEMA: CISPLATINO-GEMCITABINA 2. USO TERAPÉUTICO Primera línea de tratamiento en cancer de pulmón no microcítico con enfermedad metastásica avanzada (estadío IV) 3. ESQUEMA (1,2,3)
FICHA TECNICA. Tratamiento de la intoxicación por Amanita phalloides.
 FICHA TECNICA 1 - NOMBRE DEL MEDICAMENTO Legalon SIL 2 - COMPOSICION CUALITATIVA Y CUANTITATIVA Un vial para infusión con 598,5 mg de producto liofilizado contiene: 528,5 mg de silibinina-c-2',3- dihidrogenosuccinato
FICHA TECNICA 1 - NOMBRE DEL MEDICAMENTO Legalon SIL 2 - COMPOSICION CUALITATIVA Y CUANTITATIVA Un vial para infusión con 598,5 mg de producto liofilizado contiene: 528,5 mg de silibinina-c-2',3- dihidrogenosuccinato
VIDAZA liofilizado para Suspensión Inyectable 100 mg AZACITIDINA. Para administración subcutánea y endovenosa FOLLETO DE INFORMACIÓN AL PACIENTE
 FOLLETO DE INFORMACIÓN AL PACIENTE VIDAZA liofilizado para Suspensión Inyectable 100 mg AZACITIDINA Para administración subcutánea y endovenosa COMPOSICIÓN: Cada vial contiene: Azacitidina..100 mg Manitol
FOLLETO DE INFORMACIÓN AL PACIENTE VIDAZA liofilizado para Suspensión Inyectable 100 mg AZACITIDINA Para administración subcutánea y endovenosa COMPOSICIÓN: Cada vial contiene: Azacitidina..100 mg Manitol
FICHA TÉCNICA. Concentración Cantidad de gemcitabina (como hidrocloruro)
 FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Gemcitabina Hospira 200 mg concentrado para solución para perfusión Gemcitabina Hospira 1000 mg concentrado para solución para perfusión Gemcitabina Hospira 2000
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Gemcitabina Hospira 200 mg concentrado para solución para perfusión Gemcitabina Hospira 1000 mg concentrado para solución para perfusión Gemcitabina Hospira 2000
FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO
 FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1. NOMBRE DEL MEDICAMENTO Agua para preparaciones inyectables Grifols Disolvente para uso parenteral 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA
FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1. NOMBRE DEL MEDICAMENTO Agua para preparaciones inyectables Grifols Disolvente para uso parenteral 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA
UNIDAD ONCOLÓGICA SOLCA TUNGURAHUA HOSPITAL Dr. Julio Enrique Paredes C.
 UNIDAD ONCOLÓGICA SOLCA TUNGURAHUA HOSPITAL Dr. Julio Enrique Paredes C. I CONGRESO INTERNACIONAL DE ONCOLOGÍA: Avances y Retos AVANCES RECIENTES EN LA ADMINISTRACION DE QUIMIOTERAPIA EN CANCER DE MAMA
UNIDAD ONCOLÓGICA SOLCA TUNGURAHUA HOSPITAL Dr. Julio Enrique Paredes C. I CONGRESO INTERNACIONAL DE ONCOLOGÍA: Avances y Retos AVANCES RECIENTES EN LA ADMINISTRACION DE QUIMIOTERAPIA EN CANCER DE MAMA
Vehículo para la dilución y reconstitución de medicamentos por vía parenteral.
 agencia española de medicamentos y productos sanitarios FICHA TECNICA NOMBRE DEL MEDICAMENTO Agua para inyección Meinsol, disolvente para uso parenteral COMPOSICION Agua para inyección 1 g por 1 ml. Para
agencia española de medicamentos y productos sanitarios FICHA TECNICA NOMBRE DEL MEDICAMENTO Agua para inyección Meinsol, disolvente para uso parenteral COMPOSICION Agua para inyección 1 g por 1 ml. Para
FICHA TÉCNICA. Gemcitabina Kewl mg: cada vial contiene hidrocloruro de gemcitabina equivalente a
 FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Gemcitabina Kewl 200 mg polvo para solución para perfusión EFG Gemcitabina Kewl 1000 mg polvo para solución para perfusión EFG 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Gemcitabina Kewl 200 mg polvo para solución para perfusión EFG Gemcitabina Kewl 1000 mg polvo para solución para perfusión EFG 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA
Información importante para el profesional sanitario sobre el tratamiento con LADEVINA
 Información importante para el profesional sanitario sobre el tratamiento con LADEVINA INTRODUCCION LADEVINA es un fármaco inmunomodulador. Estudios clínicos fase III, mostraron que en pacientes pretratados
Información importante para el profesional sanitario sobre el tratamiento con LADEVINA INTRODUCCION LADEVINA es un fármaco inmunomodulador. Estudios clínicos fase III, mostraron que en pacientes pretratados
FOLLETO DE INFORMACIÓN AL PROFESIONAL. CIMAherrr SOLUCIÓN INYECTABLE PARA PERFUSIÓN 50 mg/10 ml (NIMOTUZUMAB)
 RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO Nombre del producto: CIMAher (Nimotuzumab) Forma farmacéutica: Presentación: Inyección IV. Estuche con x frascos ampolla. Composición: Cada frasco ampolla contiene:
RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO Nombre del producto: CIMAher (Nimotuzumab) Forma farmacéutica: Presentación: Inyección IV. Estuche con x frascos ampolla. Composición: Cada frasco ampolla contiene:
CARBOPLATINO SANDOZ 450 mg/45 ml solución para perfusión EFG
 CARBOPLATINO SANDOZ 450 mg/45 ml solución para perfusión EFG Lea todo el prospecto detenidamente antes de empezar a usar el medicamento. - Conserve este prospecto, ya que puede tener que volver a leerlo.
CARBOPLATINO SANDOZ 450 mg/45 ml solución para perfusión EFG Lea todo el prospecto detenidamente antes de empezar a usar el medicamento. - Conserve este prospecto, ya que puede tener que volver a leerlo.
FICHA TÉCNICA. Cada ml de concentrado para solución para perfusión contiene 40 mg de gemcitabina (como hidrocloruro de gemcitabina).
 FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Gemcitabina Aurovitas 200 mg concentrado para solución para perfusión Gemcitabina Aurovitas 1.000 mg concentrado para solución para perfusión Gemcitabina Aurovitas
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Gemcitabina Aurovitas 200 mg concentrado para solución para perfusión Gemcitabina Aurovitas 1.000 mg concentrado para solución para perfusión Gemcitabina Aurovitas
FICHA TÉCNICA ADVERTENCIA TRIÁNGULO NEGRO 1. NOMBRE DEL MEDICAMENTO. Gotusal 13,7 g polvo para solución oral 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA
 ADVERTENCIA TRIÁNGULO NEGRO FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Gotusal 13,7 g polvo para solución oral 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada sobre contiene los siguientes principios activos:
ADVERTENCIA TRIÁNGULO NEGRO FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Gotusal 13,7 g polvo para solución oral 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada sobre contiene los siguientes principios activos:
Cloruro de sodio 0,9% Tecsolpar solución para perfusión. Ión sodio: 154 mmol/l (154 meq/l ), ión cloruro: 154 mmol/l ( 154 meq/l)
 1. NOMBRE DEL MEDICAMENTO Cloruro de sodio 0,9% Tecsolpar solución para perfusión 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada 100 ml de solución contienen: Cloruro de sodio 0,9 g Composición iónica:
1. NOMBRE DEL MEDICAMENTO Cloruro de sodio 0,9% Tecsolpar solución para perfusión 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada 100 ml de solución contienen: Cloruro de sodio 0,9 g Composición iónica:
FICHA TÉCNICA. Polisacárido Vi de Salmonella typhi (cepa Ty2)
 FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Typherix, solución inyectable en jeringa precargada Vacuna de polisacárido antitifoideo. 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada dosis de 0,5 ml de la vacuna
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Typherix, solución inyectable en jeringa precargada Vacuna de polisacárido antitifoideo. 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada dosis de 0,5 ml de la vacuna
Prospecto: información para el usuario. PARAPLATIN 450 mg/ 45 ml solución para perfusión Carboplatino
 Prospecto: información para el usuario PARAPLATIN 450 mg/ 45 ml solución para perfusión Carboplatino Lea todo el prospecto detenidamente antes de empezar a usar el medicamento. Conserve este prospecto,
Prospecto: información para el usuario PARAPLATIN 450 mg/ 45 ml solución para perfusión Carboplatino Lea todo el prospecto detenidamente antes de empezar a usar el medicamento. Conserve este prospecto,
FICHA TÉCNICA. Un mililitro de la solución reconstituida contiene 38 mg de gemcitabina (como hidrocloruro)
 FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Gemcitabina GP-Pharm 200 mg polvo para solución para perfusión EFG Gemcitabina GP-Pharm 1000 mg polvo para solución para perfusión EFG 2. COMPOSICIÓN CUALITATIVA
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Gemcitabina GP-Pharm 200 mg polvo para solución para perfusión EFG Gemcitabina GP-Pharm 1000 mg polvo para solución para perfusión EFG 2. COMPOSICIÓN CUALITATIVA
FICHA TÉCNICA. Una vez reconstituida, 1 ml de la solución contiene 38 mg/ml de gemcitabina.
 FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Gemcitabina Hetero 200 mg polvo para solución para perfusión EFG Gemcitabina Hetero 1.000 mg polvo para solución para perfusión EFG 2. COMPOSICIÓN CUALITATIVA Y
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Gemcitabina Hetero 200 mg polvo para solución para perfusión EFG Gemcitabina Hetero 1.000 mg polvo para solución para perfusión EFG 2. COMPOSICIÓN CUALITATIVA Y
FICHA TÉCNICA. Gemcitabina Accord 200 mg: un vial contiene hidrocloruro de gemcitabina equivalentes a 200 mg de gemcitabina.
 FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Gemcitabina Accord 200 mg polvo para solución para perfusión EFG Gemcitabina Accord 1000 mg polvo para solución para perfusión EFG 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Gemcitabina Accord 200 mg polvo para solución para perfusión EFG Gemcitabina Accord 1000 mg polvo para solución para perfusión EFG 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA
FICHA TÉCNICA. Gemcitabina Accord 200 mg: un vial contiene hidrocloruro de gemcitabina equivalentes a 200 mg de gemcitabina.
 FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Gemcitabina Accord 200 mg polvo para solución para perfusión EFG Gemcitabina Accord 1000 mg polvo para solución para perfusión EFG 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Gemcitabina Accord 200 mg polvo para solución para perfusión EFG Gemcitabina Accord 1000 mg polvo para solución para perfusión EFG 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA
FICHA TÉCNICA. MENCEVAX AC es una preparación liofilizada de polisacáridos purificados de Neisseria meningitidis (meningococo) de los grupos A y C.
 FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO. MENCEVAX AC Vacuna de polisacáridos meningocócicos, grupos A y C. 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA. MENCEVAX AC es una preparación liofilizada de polisacáridos
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO. MENCEVAX AC Vacuna de polisacáridos meningocócicos, grupos A y C. 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA. MENCEVAX AC es una preparación liofilizada de polisacáridos
Para consultar la lista completa de excipientes ver sección 6.1.
 1. NOMBRE DEL MEDICAMENTO bucomax pastillas para chupar sabor menta bucomax pastillas para chupar sabor fresa bucomax pastillas para chupar sabor miel y limón 2. COMPOSICION CUALITATIVA Y CUANTITATIVA
1. NOMBRE DEL MEDICAMENTO bucomax pastillas para chupar sabor menta bucomax pastillas para chupar sabor fresa bucomax pastillas para chupar sabor miel y limón 2. COMPOSICION CUALITATIVA Y CUANTITATIVA
