Regulación n y Control Productos Biológicos. & Biotecnológicos en Cuba. Papel del CECMED como ARN. VII eamí,
|
|
|
- Ángel Vargas Domínguez
- hace 8 años
- Vistas:
Transcripción
1 Regulación n y Control Productos Biológicos & Biotecnológicos en Cuba. Papel del CECMED como ARN VII eamí, de octubre, 2008 Cancún, n, México. M
2 Regulación n y Control de Productos Biológicos & Biotecnológicos en Cuba. Temas a tratar: Biológicos/Biotecnológicos. Características. La Biotecnología en Cuba. Regulación de medicamentos en Cuba. CECMED. Estructura y funciones. Regulación de productos Biológicos/Biotecnológicos. Proceso OMS de Precalificación ARN/Vacunas. Nuevos retos.
3 Biológicos/Biotecnológicos. Características. TERMINOLOGÍA En Cuba los productos Biológicos y Biotecnológicos son considerados bajo un mismo concepto: BIOLOGICOS
4 Biológicos/Biotecnológicos. Características. TERMINOLOGÍA Medicamento biológico: Medicamentos que se derivan de organismos vivos (desde microorganismos normales o genéticamente modificados a fluidos y tejidos derivados de diversas fuentes animales o humanas, presentando con frecuencia una estructura molecular compleja. Requieren consideraciones especiales de calidad debido a la naturaleza biológica de: los materiales de partida, el proceso de fabricación y/o los métodos de ensayo necesarios para caracterizar los lotes de estos productos. Comité Expertos en Biológicos. SIT 858. OMS
5 Biológicos/Biotecnológicos. Características. TERMINOLOGÍA Biológico: Producto utilizado para la prevención, tratamiento o diagnóstico de enfermedades (anticuerpos monoclonales) obtenidos a partir de organismos vivos o de sus tejidos. Productos biológicos: incluyen a los virus, sueros terapéuticos, toxinas, antitoxinas, vacunas, sangre, componentes o derivados de la sangre, productos alergénicos, hormonas, factores estimulantes de colonias, citoquinas, anticuerpos monoclonales, etc. Fuentes y métodos de producción: cultivo de células de microorganismos, extracción a partir de tejidos biológicos, técnicas del ADN recombinante, transgénesis, técnicas de hibridoma, propagación de microorganismos en embriones o animales, etc. Reglamento de Medicamentos. Cuba. 3ra. Versión. 2000
6 Biológicos/Biotecnológicos. Características Presentan problemas particulares con respecto a calidad, seguridad y eficacia. Alta complejidad molecular. Difíciles de caracterizar por métodos físico químicos. Ej. UK Biológicos: Sustancia usada en medicina que su pureza o potencia no pueden, en opinión de la Secretaria de Estado, ser adecuadamente evaluada por métodos físico químicos. Biological Standards Act Materiales de partida y/o procesos de producción varían según su naturaleza. Requieren métodos de ensayo para su caracterización: ensayos biológicos, potencia, inmunogenicidad, seguridad.
7 Biológicos/Biotecnológicos. Características Se diferencian de los medicamentos químicos: - Presentan problemas particulares con respecto a calidad, seguridad y eficacia. - Alta complejidad molecular. - Difíciles de caracterizar por métodos físico químicos. La consistencia de producción es de capital importancia. Cambios mayores y menores de producción pueden dar lugar a efectos adversos. Productos de diferentes lotes no difieren en su seguridad y eficacia demostrada en ensayos clínicos.
8 CNGM La Biotecnología a en Cuba CIM CIGB I. FINLAY CENIC IPK 52 instituciones CIE LIORAD NOVATEC CENPALAB BioCen CENSA AICA
9 La Biotecnología a en Cuba. Características Polo Científico del Oeste de la Habana. Instituciones 52 Trabajadores Universitarios Instituciones principales 10 Trabajadores > 5700 Profesionales I+D 1059 Doctores en Ciencias (PhD) 178
10 La Biotecnología a en Cuba Características Gobierno inversionista principal. Científicos y profesionales cubanos. Estrategia de ciclo cerrado: investigación/desarrollo/producción/comercialización. Colaboración nacional vs competencia individual Empresas comerciales / instituciones científicas y de producción. Principal prioridad: mercado nacional. Atención a oportunidades del mercado internacional Competencia internacional: calidad, volúmenes productivos, costo, novedad.
11 I n m u n o b i o l o g í c o s Productos IFN alfa y gamma IFN + Ribavirina SKr Egf Anti CD3 MAB (T3 mu ) Eritropoetin (EPO) G-CSF ACM in vitro p/ hemoclasificación (Labex) ACM in vitro p/ subp. Linfoides (Labex) Anti-EGF-R MAB (hr3) EPO sin Albúmina EGF Vaccine (NeuGc) NGM3 Vaccine Idiotypic Vaccine 1E10 Re 188 hr3 MAB (RAIT) Re 188 -C5 MAB (RAIT) Anti-CD6 MAB (T1 hu ) VSSP Muteinas IL-2 EGF/TGF Vaccine PanHer Vaccine Anti-anti-LDL ox Obt. Molécula Eval. Pre- Clinica Ens. Clín. Inicial Ens. Clín. Avanzado Registrado
12 I n m u n o b i o l o g í c o s Anti CD3 MAB (T3 q ) HER-1 Vaccine rec-p3 MAB rec-b7 MAB hu-14f7 MAB Anti-IL2 MAB Productos Obt. Molécula Eval. Pre- Clinica Pegilación de biomoléculas como: IFN, EPO, G-CSF Peg-Intron (Schering). IFN alfa 2b. 19/01/2001 Pegasys (Roche). IFN alfa 2a. 16/10/2002 Neulasta (Amgen). Pegfilgrastim o PEG-G-CSF. 31/01/2002 Peginterferon (Roche). IFN alfa 2a. 04/06/ (access data) Ens. Clín. Inicial Ens. Clín. Avanzado Registrado
13 Productos & Proyectos / Vacunas Vacunas Investigación Estudio Clínico Registro 1. Meningocóccica BC 2. Hepatitis B (HB) 3. Tetánica 4. Leptospirósica 5. Tifoídica (Vi) 6. Haemophilus influenzae Tipo b (Hib) 7. Diftérica - Tetánica (DT) niños 8. Difteria-Tetános-Pertussis (DTP) 9. Tetravalente (DTP-HB) 10. Pentavalente 4+1 (DTP-HB+Hib) 11. DT para adultos 12. Meningocóccica AC 13. Cólera atenuada 14. Meningocóccica C conjugada 15. Terapéutica antihepatitis B 16. Terapéutica antihepatitis C 17. HB Hib 18. Terapéutica antihepatitis B nasal
14 Productos & Proyectos / Vacunas Vacunas Investigación Desarrollo Estudio clínico 19. Pentavalente en un solo vial 20. DPT - Hib 21. Meningocóccica ACW Meningocóccica ACYW Meningocóccica recombinante 24. Dengue 25. Neumocóccica 26. Cólera inactivada 27. Leptospira 28. Tuberculosis 29. Pertussis acelular 30. Leishmania 31. Salmonella
15 Vacunas incluidas en el Programa Nacional de Inmunizaciones MMR AT TT BC BCG DT DTP Producción Nacional Polio HB Hib DTP-HB DTP-HB + Hib Importadas
16 REGULACIÓN N DE MEDICAMENTOS EN CUBA El Estado Cubano: Regula la calidad, seguridad y eficacia de los medicamentos al amparo de la Ley 41 de 1983, Ley de la Salud Pública y su Reglamento. Así mismo Acuerdo No Comité Ejecutivo del Consejo de Ministros/Atribuciones y funciones del MINSAP - Ejercer el control y la vigilancia sanitaria de todos los productos que pueden tener influencia sobre la salud humana. - Regular y Controlar la investigaciones en seres humanos. - Ejercer la evaluación, registro, regulación y control de los medicamentos, diagnosticadores y equipos médicos. Registro de Medicamentos = Autorización de Comercialización El Reglamento para el Registro de Medicamentos de uso humano en la República de Cuba. Resolución Ministerial No. 169/2000 Versión actualizada.
17 REGULACIÓN DE MEDICAMENTOS EN CUBA CATEGORIAS de los Medicamentos. Vigente Requisitos de Registro A. Sustancia químicamente definida, desconocida, nueva sustancia obtenida por síntesis química, fermentación, aislamiento de fuentes naturales, biotecnología, nuevos ésteres o sales de sustancias activas existentes en el mercado, nuevo en el país y en el mundo. B. Nueva asociación de principios activos conocidos en nuestro país y/o en el extranjero. C. Medicamentos con uno o más de un principio activo que se emplean por primera vez en Cuba, pero son de uso reconocido en el extranjero. D. Medicamentos con uso nacional establecido, elaborado con una nueva formulación y/o un nuevo fabricante.
18 REGULACIÓN DE MEDICAMENTOS EN CUBA CATEGORIAS de los Medicamentos. Propuesta Nuevos medicamentos: En su carácter más general comprenden todos los medicamentos terminados para el empleo en la medicina humana, tanto los que se utilizan por primera vez en Cuba, como los de uso conocido en el país y que se elaboren por un nuevo fabricante. De acuerdo a su grado de novedad se clasifican en las siguientes categorías:
19 REGULACIÓN DE MEDICAMENTOS EN CUBA CATEGORIAS de los Medicamentos. Propuesta Productos nuevos: Se agrupan en tres categorías: Categoría A: Medicamento o producto biológico de producción novedosos en el país y en el extranjero cuyo ingrediente farmacéutico activo no se encuentra aprobado en Cuba. Categoría B: Medicamento y producto biológico cuyo principio activo se encuentra aprobado en Cuba, pero se presenta una formulación de liberación modificada, una nueva vía de administración, nueva forma farmacéutica, nueva sal de un principio activo aprobado, nueva concentración que no se ajusta al rango posológico aprobado o una nueva asociación de principios activos aprobados. Categoría C: Medicamento de producción y producto biológico de importación, multiorigen cuyo ingrediente farmacéutico activo no se encuentra aprobado en Cuba, pero son de uso reconocido en otros países.
20 REGULACIÓN DE MEDICAMENTOS EN CUBA CATEGORIAS de los Medicamentos. Propuesta Productos conocidos: Se agrupan en dos categorías: Categoría D: Producto biológico de producción nacional cuyo principio activo se encuentra aprobado en Cuba, pero se presenta por un nuevo titular y/o fabricante. Categoría E: Medicamentos de producción nacional e importación y producto biológico de importación que se presenta con el mismo ingrediente farmacéutico activo, forma farmacéutica, dosis e indicaciones de otro producto ya registrado en Cuba.
21 Cuba: Regulación Sanitaria Ministerio de Salud Pública P BURÓ REGULATORIO PARA LA PROTECCIÓN N DE LA SALUD (BRPS) Agencia Nacional de Vigilancia Sanitaria encargada por el Ministerio de Salud Pública para garantizar la proteccion de la salud de la población ejerciendo el control sanitario sobre los productos y servicios objeto de vigilancia sanitaria. Resolución 228 / 96 Ministerio de Economía y Planificación Resolución 132 / 96 Ministerio de Salud Pública
22 MINISTRO DE SALUD PÚBLICAP BURÓ REGULATORIO PARA LA PROTECCIÓN N DE LA SALUD CECMED CDF CCEEM INHA Dependencias Provinciales
23 CENTRO PARA EL CONTROL ESTATAL DE LA CALIDAD DE LOS MEDICAMENTOS (CECMED) AUTORIDAD REGULADORA NACIONAL DE MEDICAMENTOS DE CUBA El CECMED: Creado el 21 de Abril de 1989 con el objetivo de centralizar y desarrollar las acciones para el control de calidad de los medicamentos. Mandato: Realizar una evaluación n integral de la relación n riesgo beneficio de los medicamentos.
24 REGULACIÓN DE MEDICAMENTOS EN CUBA ALCANCE Medicamentos / Productos Biológicos Diagnosticadores Sangre y hemoderivados Células, órganos y tejidos Terapia génica g Radiofármacos/productos radioactivos de uso médico. m Productos naturales y Homeopáticos Desinfectantes sanitarios
25 CECMED. Estructura La estructura de trabajo ha sido adaptada de acuerdo a las seis funciones básicas b de OMS Autorizaciones Sanitarias Inspección, Control & Vigilancia Registro Sanitario Evaluación n / Aprobación de Ensayos Clínicos Liberación n de Lotes Laboratorios de Control de Calidad Inspección n farmacéutica Vigilancia Postcomercialización
26 ESTRUCTURA FUNCIONAL CECMED DIRECCIÓN Gestión de la Calidad Dpto. de Secretaría, Archivo y Estadísticas Asesoría Legal Asesor Principal Subdirección Autorizaciones Sanitarias Subdirección Inspección, Control y Vigilancia Subdirección Gestión Estratégica Subdirección Aseguramiento Dpto. Biológicos Dpto. Medicamentos Dpto. Inspección Lab. Nac. de Control Vigilancia Dpto. Recursos Humanos Seguridad y Protección Dpto. Diagnosticadores Físico Químico Biológico Microbiológico Ciencia y Técnica Información, Informática y Comunicación Social Dpto. de Gestión Económica Administración y Servicios Planificación y Compras
27 REGULACIÓN DE MEDICAMENTOS EN CUBA CECMED. FUNCIONES BÁSICAS Sistema Regulador. Registro Sanitario/Autorización de comercialización. Liberación de Lotes de vacunas y biológicos. Autorización/Inspección y Control de Ensayos Clínicos. Inspección de Buenas Practicas y Licencias Sanitarias. Ensayos de Laboratorio/Físico-Químico, Microbiológicos y Biológicos. Vigilancia postcomercialización. Sistema Gestión de la Calidad ISO 9000:2000 Certificado por ONN/Cuba y AENOR/España
28 Regulación de productos Biológicos/Biotecnológicos Principios Básicos: Regulación apropiada para minimizar riesgos y maximizar beneficios. Proteger a pacientes y población contra efectos adversos inaceptables y productos ineficaces. Asegurar los beneficios científicos de la innovación tecnológica y el conocimiento. No obstaculizar el desarrollo. Medidas reguladoras desde la I + D. Etapas tempranas. Aplicación de Guías sobre producción y control de calidad (CECMED, OMS, ICH, EMEA, FDA) Decisiones basadas en criterios científicos.
29 Regulación de productos Biológicos/Biotecnológicos Base Legal y reglamentaria Reglamento para el Registro Sanitario de Medicamentos de Uso Humano; 2000 (en revisión). Reglamento para la Inspección n Farmacéutica Estatal; 2002 (revisado y actualizado). Requisitos para el Registro, Renovación n y Modificación n de Medicamentos de Uso Humano; 2000 (en revisión). Este documento cuenta con varios Anexos específicos, que aplican a cada tipo o clase de producto. Regulación n No /Requisitos para las solicitudes de inscripción n en el registro de medicamentos de uso humano de productos alergénicos. Regulación n No /Requerimientos para ensayos clínicos fase I y II con productos en investigación n destinados al tratamiento de cáncer c y sida.
30 Regulación de productos Biológicos/Biotecnológicos Base Legal y reglamentaria Regulación n No /Requisitos para la solicitud de autorización n y modificación n de ensayos clínicos (en revisión). Regulación n No /Requerimientos para el manejo y uso de productos en investigación n en los ensayos clínicos y responsabilidades de las partes. Regulación n No /Requisitos para la inscripción n en el registro de medicamentos de las vacunas suministradas por las Agencias de las Naciones Unidas. Regulación n No /Control de los eventos adversos consecutivos a la vacunación n (en revisión). Regulación n No /Requisitos y procedimientos para la liberación n de lotes de productos biológicos (revisada y actualizada).
31 Regulación de productos Biológicos/Biotecnológicos Base Legal y reglamentaria Marco de regulaciones relacionadas con la sangre y el plasma (hemoderivados). Regulación n No /Requerimientos de los estudios de estabilidad para el registro de productos farmacéuticos nuevos y conocidos. Regulación n No /Requerimientos de los estudios de estabilidad para el registro de nuevos ingredientes farmacéuticos activos. Regulación n No /Requerimientos de los estudios de estabilidad para el registro de productos biológicos y biotecnológicos. Regulación n No /Textos 1998/Textos para materiales de envase impresos e información n para medicamentos de uso humano de producción n nacional (en revisión). Regulación n No /Cambios al proceso de producción n de productos biológicos registrados. Comparación n de productos biológicos.
32 Regulación de productos Biológicos/Biotecnológicos Base Legal y reglamentaria Circular No /Adquisición n de vacunas (revisada y actualizada). Regulación n No /Requisitos Químicos micos-farmacéuticos y Biológicos para el Registro de Productos Biofarmacéuticos obtenidos a partir de plantas transgénicas. nicas. Regulación n No /Requerimientos para la notificación n y el reporte de eventos adversos graves e inesperados en los ensayos clínicos nicos. Otros documentos reguladores.
33 Regulación de productos Biológicos/Biotecnológicos PNOs (SOPs) Denominación Evaluación de la información administrativa, química farmacéutica y biológica de las solicitudes de trámites para el registro de los productos biológicos Metodología para la evaluación preclínica de solicitudes de modificación al Registro de Medicamentos Metodología para la evaluación preclínica de solicitudes de autorización de inicio y modificación de ensayo clínico Elaboración de los proyectos para las certificaciones de Inscripción, Renovación y Modificación de trámites en el Registro de productos biológicos Evaluación y codificación de formatos para textos y materiales de envase impresos e información de medicamentos en productos biológicos Elaboración del Plan de Evaluación de trámites de registro del Dpto. de Biológicos Control de la documentación en la Subdirección de SAS.
34 Recepción y entrega de trámites regulatorios Solicitud Evaluación preliminar Pago de cuota Aceptación Si No Notificación de rechazo Notificación a Subdirección SAS Entrega de documentos a evaluar Evaluación integral Recepción de documentación y dictamen CD CD Aceptación Emisión de Certificado Resolución de aceptación y Certificado Rechazo Resolución de rechazo o cancelación de registro
35 REGULACIÓN N DE VACUNAS. Metas de la OMS Asegurar que el 100% de las vacunas usadas en los Programas Nacionales de Inmunización n tienen CALIDAD asegurada. Definición n de VACUNAS CON CALIDAD ASEGURADA: Vacunas y productores precalificados OMS. Autoridad Reguladora Nacional (ARN) independiente. ARN totalmente funcional. Capacidad/investigar y resolver problemas relacionados a las vacunas.
36 Proceso OMS de Precalificación ARN / Vacunas EVALUACIÓN SEGÚN INDICADORES OMS Fecha Objetivo 2000 Evaluación n del CECMED como parte del proceso de precalificación n de la Vacuna Antihepatitis B recombinante 2002 Seguimiento 2003 Evaluación n integral de ARM para Vacunas 2004 Evaluación n integral de ARM para Medicamentos 2005 Seguimiento Resultados Desempeño Satisfactorio Todas las funciones están implementadas y la OMS reconoce la capacidad de regulación del CECMED Desempeño Satisfactorio Desempeño Satisfactorio Desempeño Satisfactorio Desempeño Satisfactorio
37 Impacto evaluación de OMS / CECMED Consolidación del CECMED como ARN y mayor soporte para todos los productos en el mercado cubano. Mayor apoyo gubernamental a las actividades del CECMED. Participación de especialistas del CECMED en curso de GTN/OMS. Capacidad de colaboración con OMS/OPS y otras ARNs: Participación de expertos del CECMED como parte del equipo OMS para evaluaciones de ARNs. Participación en elaboración y revisión de guías y herramientas de OMS. Participación de expertos del CECMED como parte de la Red OMS de ensayos clínicos.
38 Impacto evaluación de OMS / CECMED En colaboración n con OPS. Coordinación del Grupo de trabajo sobre vacunas de la Red Panamericana para la Armonización de la Reglamentación Farmacéutica. (PARF) Colaboración en el proceso de precalificación de Medicamentos. Contribución con OPS y las ARNs en Latinoamérica con cursos de entrenamiento de las funciones reguladoras básicas. (15 países / 68 participantes)
39 Ejemplos del impacto de las evaluaciones OMS en el desempeño regulador del CECMED Colaboración con OMS en la evaluación de otras ARNs Año ARN 2003 FDA, China 2003 Tailandia 2004 India 2004 COFEPRIS, México 2006 AIFA, Italia 2007 HPB, Canada
40 Regulación Biológicos/Biotecnológicos Desafíos Sistemas nuevos = resultados I + D. Ej. Productos derivados de plantas. AcM de Tabaco. Reconocimiento y trato adecuado a problemas científico /técnico en etapas tempranas de I + D de productos y técnicas. Garantizar bases de datos científicas disponibles sobre las cuales tomar decisiones. Posición regulatoria /avances científicos / dimensión internacional. ANR / Industria. Dialogo y concertación estratégica. Transferencia de Tecnologías. Ej. Cuba/Brasil (Comité Técnico Regulatorio/ANVISA-CECMED)
41 Regulación Biológicos/Biotecnológicos Desafíos Tecnologías emergentes/terapias de avanzada Genómica Farmacogenética Terapia Génica y celular Anticuerpos Monoclonales Vacunas Terapéuticas Convergencia agro farmacéutica Bioinformática Nanotecnologías Productos Biosimilares
42 MUCHAS GRACIAS
INNOVACION, RETOS Y COOPERACION.
 INNOVACION, RETOS Y COOPERACION. Viceministra Lina Domínguez Acosta Ministerio de Ciencia, Tecnología y Medio Ambiente República de Cuba lina@citma.cu MARZO /2011 Innovación Mudar o alterar algo, introduciendo
INNOVACION, RETOS Y COOPERACION. Viceministra Lina Domínguez Acosta Ministerio de Ciencia, Tecnología y Medio Ambiente República de Cuba lina@citma.cu MARZO /2011 Innovación Mudar o alterar algo, introduciendo
Reunión n de ARM: Regulación n de Productos Biológicos en Latino América y el Caribe Productos Biológicos / Biotecnológicos. gicos
 Reunión n de ARM: Regulación n de Prducts Bilógics en Latin América y el Caribe Prducts Bilógics / Bitecnlógics gics MSc. Rland Dminguez Mrales J. Dpt.. Bilógics Reunión n de ARM: Regulación n de Prducts
Reunión n de ARM: Regulación n de Prducts Bilógics en Latin América y el Caribe Prducts Bilógics / Bitecnlógics gics MSc. Rland Dminguez Mrales J. Dpt.. Bilógics Reunión n de ARM: Regulación n de Prducts
Medicamentos biológicos y biosimilares
 Medicamentos biológicos y biosimilares folleto biosimilares FILMAR.indd 1 24/10/12 10:09 En qué se diferencian los medicamentos biológicos de los medicamentos tradicionales? Introducción Gracias a la investigación
Medicamentos biológicos y biosimilares folleto biosimilares FILMAR.indd 1 24/10/12 10:09 En qué se diferencian los medicamentos biológicos de los medicamentos tradicionales? Introducción Gracias a la investigación
INTERCAMBIABILIDAD TERAPÉUTICA EN MOLECULAS PEQUEÑAS Y BIOLOGICAS
 INTERCAMBIABILIDAD TERAPÉUTICA EN MOLECULAS PEQUEÑAS Y BIOLOGICAS Oscar Armando García Vega MD, M Sc, Ph. D. Farmacología y Terapéutica Profesor Asociado Facultad de Medicina Universidad Nacional de Colombia
INTERCAMBIABILIDAD TERAPÉUTICA EN MOLECULAS PEQUEÑAS Y BIOLOGICAS Oscar Armando García Vega MD, M Sc, Ph. D. Farmacología y Terapéutica Profesor Asociado Facultad de Medicina Universidad Nacional de Colombia
REGISTRO SANITARIO DE PRODUCTOS BIOLÓGICOS/ BIOTECNOLÓGICOS
 REGISTRO SANITARIO DE PRODUCTOS BIOLÓGICOS/ BIOTECNOLÓGICOS REPÚBLICA DE PANAMÁ PRESENTADO POR: LICDA. KYRHIAM CASTILLO CHIAL MINISTERIO DE SALUD DIRECCIÓN N NACIONAL DE FARMACIAS Y DROGAS Registro Sanitario
REGISTRO SANITARIO DE PRODUCTOS BIOLÓGICOS/ BIOTECNOLÓGICOS REPÚBLICA DE PANAMÁ PRESENTADO POR: LICDA. KYRHIAM CASTILLO CHIAL MINISTERIO DE SALUD DIRECCIÓN N NACIONAL DE FARMACIAS Y DROGAS Registro Sanitario
Iniciativas del Ministerio de Salud de Canadá (HC) para el desarrollo de la capacidad reguladora. TALLER HC/OPS Antigua, Guatemala Marzo, 2014
 Iniciativas del Ministerio de Salud de Canadá (HC) para el desarrollo de la capacidad reguladora TALLER HC/OPS Antigua, Guatemala Marzo, 2014 HC y los Centros Colaboradores de la OMS para la Estandarización
Iniciativas del Ministerio de Salud de Canadá (HC) para el desarrollo de la capacidad reguladora TALLER HC/OPS Antigua, Guatemala Marzo, 2014 HC y los Centros Colaboradores de la OMS para la Estandarización
Medicamentos innovadores: La regulación en Cuba
 VIII ENCUENTRO DE AUTORIDADES COMPETENTES DE MEDICAMENTOS DE LOS PAISES IBEROAMERICANOS Medicamentos innovadores: La regulación en Cuba Dr. Rafael Pérez Cristiá Madrid 12-14 Mayo de 2010 DEFINICIONES CONTEXTO
VIII ENCUENTRO DE AUTORIDADES COMPETENTES DE MEDICAMENTOS DE LOS PAISES IBEROAMERICANOS Medicamentos innovadores: La regulación en Cuba Dr. Rafael Pérez Cristiá Madrid 12-14 Mayo de 2010 DEFINICIONES CONTEXTO
PAPEL DE LOS SISTEMAS INTEGRADOS DE GESTIÓN EN EL DESARROLLO DE MATERIALES DE REFERENCIA PARA LA INDUSTRIA FARMACÉUTICA
 PAPEL DE LOS SISTEMAS INTEGRADOS DE GESTIÓN EN EL DESARROLLO DE MATERIALES DE REFERENCIA PARA LA INDUSTRIA FARMACÉUTICA Autores: Mayra Castro Nodal 1, Janet Lora García 2, Ulises Jáuregui Haza 3. 1. Ingeniero
PAPEL DE LOS SISTEMAS INTEGRADOS DE GESTIÓN EN EL DESARROLLO DE MATERIALES DE REFERENCIA PARA LA INDUSTRIA FARMACÉUTICA Autores: Mayra Castro Nodal 1, Janet Lora García 2, Ulises Jáuregui Haza 3. 1. Ingeniero
FICHA TÉCNICA BIOTECNOLOGÍA PRODUCTIVA
 FICHA TÉCNICA BIOTECNOLOGÍA PRODUCTIVA Proyecto 000000000174102 Investigación y desarrollo tecnológico para la fabricación industrial en México de un anticuerpo monoclonal clave Y02-Ak desde el gen hasta
FICHA TÉCNICA BIOTECNOLOGÍA PRODUCTIVA Proyecto 000000000174102 Investigación y desarrollo tecnológico para la fabricación industrial en México de un anticuerpo monoclonal clave Y02-Ak desde el gen hasta
Certificación en Biotecnología Sanitaria (Curso Homologado con Titulación Universitaria + 20 Créditos tradicionales LRU)
 Certificación en Biotecnología Sanitaria (Curso Homologado con Titulación Universitaria + 20 Titulación certificada por EUROINNOVA BUSINESS SCHOOL Certificación en Biotecnología Sanitaria (Curso Homologado
Certificación en Biotecnología Sanitaria (Curso Homologado con Titulación Universitaria + 20 Titulación certificada por EUROINNOVA BUSINESS SCHOOL Certificación en Biotecnología Sanitaria (Curso Homologado
Comparador: Un producto de investigación o comercializado (por ejemplo control activo) o placebo utilizado conferencia en un estudio clínico.
 1. OBJETIVO Brindar los lineamientos necesarios para la presentación de solicitudes de importación de suministros y exportación de muestras biológicas para el desarrollo de protocolos de investigación.
1. OBJETIVO Brindar los lineamientos necesarios para la presentación de solicitudes de importación de suministros y exportación de muestras biológicas para el desarrollo de protocolos de investigación.
NORMATIVA TÉCNICA NUMERO 44-2004 Guatemala, Febrero 2005 Versión 3 DEPARTAMENTO DE REGULACION Y CONTROL DE PRODUCTOS FARMACEUTICOS Y AFINES
 NORMATIVA TÉCNICA NUMERO 44-2004 Guatemala, Febrero 2005 Versión 3 1 DEPARTAMENTO DE REGULACION Y CONTROL DE PRODUCTOS FARMACEUTICOS Y AFINES Que la Constitución Política de la República de Guatemala,
NORMATIVA TÉCNICA NUMERO 44-2004 Guatemala, Febrero 2005 Versión 3 1 DEPARTAMENTO DE REGULACION Y CONTROL DE PRODUCTOS FARMACEUTICOS Y AFINES Que la Constitución Política de la República de Guatemala,
fi' ~ ASUNTO: Comentarios al Proyecto de Decreto para el Registro Sanitario de Medicamentos Biológicos. Versión de Julio de 2014.
 ALLERCAN - - Bogotá, Julio 25 de 2014 fi' ~ Doctor: Alejandro Gaviria MINISTERIO DE SALUD Y PROTECCION SOCIAL La Ciudad.- I CC: Dra. Nancy Huertas Directora de Medicamentos y Tecnologías en Salud I I IMrnll
ALLERCAN - - Bogotá, Julio 25 de 2014 fi' ~ Doctor: Alejandro Gaviria MINISTERIO DE SALUD Y PROTECCION SOCIAL La Ciudad.- I CC: Dra. Nancy Huertas Directora de Medicamentos y Tecnologías en Salud I I IMrnll
EVALUACIÓN N PROTOCOLO RESUMEN DE PRODUCCIÓN N Y CONTROL PARA LA LIBERACIÓN N DE LOTE
 INSTITUTO NACIONAL DE HIGIENE RAFAEL RANGEL EVALUACIÓN N PROTOCOLO RESUMEN DE PRODUCCIÓN N Y CONTROL PARA LA LIBERACIÓN N DE LOTE Farmacéuticas: Ana Agatón Andreina Palacios Contenido Introducción Liberación
INSTITUTO NACIONAL DE HIGIENE RAFAEL RANGEL EVALUACIÓN N PROTOCOLO RESUMEN DE PRODUCCIÓN N Y CONTROL PARA LA LIBERACIÓN N DE LOTE Farmacéuticas: Ana Agatón Andreina Palacios Contenido Introducción Liberación
Anexo: Marco legal e institucional del registro de medicamentos en Chile
 Anexo: Marco legal e institucional del registro de medicamentos en Chile Contenido Definición de registro sanitario... 1 Información para el registro sanitario... 2 Tipos de registro sanitario... 4 Referencia
Anexo: Marco legal e institucional del registro de medicamentos en Chile Contenido Definición de registro sanitario... 1 Información para el registro sanitario... 2 Tipos de registro sanitario... 4 Referencia
ESCUELA DE TECNOLOGÍA DE ALIMENTOS PERFIL DEL PROFESIONAL EN TECNOLOGÍA/INGENIERÍA DE ALIMENTOS
 PERFIL DEL PROFESIONAL EN TECNOLOGÍA/INGENIERÍA DE ALIMENTOS Su quehacer profesional se enfoca en la investigación, desarrollo y aplicación de las ciencias físicas, químicas, biológicas y biotecnológicas,
PERFIL DEL PROFESIONAL EN TECNOLOGÍA/INGENIERÍA DE ALIMENTOS Su quehacer profesional se enfoca en la investigación, desarrollo y aplicación de las ciencias físicas, químicas, biológicas y biotecnológicas,
DECRETO NÚMERO DE 2013 HOJA N
 25.06.2013 MINISTERIO DE SALUD Y PROTECCIÓN SOCIAL ( ) G/TBT/NG N/COL/ Por el cual se reglamenta, para propósitos del registro sanitario, el procedimiento de evaluación de calidad, seguridad y eficaciaa
25.06.2013 MINISTERIO DE SALUD Y PROTECCIÓN SOCIAL ( ) G/TBT/NG N/COL/ Por el cual se reglamenta, para propósitos del registro sanitario, el procedimiento de evaluación de calidad, seguridad y eficaciaa
Sesión 4: Asegurar la Calidad del Producto en toda la Cadena de Suministro
 Sesión 4: Asegurar la Calidad del Producto en toda la Cadena de Suministro Fuente: PATH Posibles puntos de control para el aseguramiento de la calidad dentro de la cadena de suministro 1. Materias primas
Sesión 4: Asegurar la Calidad del Producto en toda la Cadena de Suministro Fuente: PATH Posibles puntos de control para el aseguramiento de la calidad dentro de la cadena de suministro 1. Materias primas
FARMACOPEA MERCOSUR: VACUNAS PARA USO HUMANO
 MERCOSUR/XLII SGT Nº 11/P.RES. Nº 09/14 FARMACOPEA MERCOSUR: VACUNAS PARA USO HUMANO VISTO: El Tratado de Asunción, el Protocolo de Ouro Preto y las Resoluciones N 31/11 y 22/14 del Grupo Mercado Común.
MERCOSUR/XLII SGT Nº 11/P.RES. Nº 09/14 FARMACOPEA MERCOSUR: VACUNAS PARA USO HUMANO VISTO: El Tratado de Asunción, el Protocolo de Ouro Preto y las Resoluciones N 31/11 y 22/14 del Grupo Mercado Común.
FUNCIONES DEL RESPONSABLE TECNICO DE IMPORTACIÓN/FABRICACIÓN DE PRODUCTOS COSMETICOS.
 FUNCIONES DEL RESPONSABLE TECNICO DE IMPORTACIÓN/FABRICACIÓN DE PRODUCTOS COSMETICOS. FUNDAMENTOS JURIDICOS ESPAÑOLES La Ley 14/1986, de 25 de abril, General de Sanidad, en su artículo 40, atribuye a la
FUNCIONES DEL RESPONSABLE TECNICO DE IMPORTACIÓN/FABRICACIÓN DE PRODUCTOS COSMETICOS. FUNDAMENTOS JURIDICOS ESPAÑOLES La Ley 14/1986, de 25 de abril, General de Sanidad, en su artículo 40, atribuye a la
Sistema de Vigilancia Vigente en Chile agosto de 2014
 Sistema de Vigilancia Vigente en Chile agosto de 2014 Ingeniero Biomédico Catalina Valdés León Subdepartamento Dispositivos Médicos Agencia Nacional de Medicamentos Temario Introducción Diversidad de los
Sistema de Vigilancia Vigente en Chile agosto de 2014 Ingeniero Biomédico Catalina Valdés León Subdepartamento Dispositivos Médicos Agencia Nacional de Medicamentos Temario Introducción Diversidad de los
ANTECEDENTES DE HECHO
 DIRECCIÓN Madrid, 23 de mayo de 2013 ASUNTO: RESOLUCIÓN POR LA QUE SE ESTABLECE LA CLASIFICACIÓN DEL USO TERAPÉUTICO NO SUSTITUTIVO DEL PLASMA AUTÓLOGO Y SUS FRACCIONES, COMPONENTES O DERIVADOS, COMO MEDICAMENTO
DIRECCIÓN Madrid, 23 de mayo de 2013 ASUNTO: RESOLUCIÓN POR LA QUE SE ESTABLECE LA CLASIFICACIÓN DEL USO TERAPÉUTICO NO SUSTITUTIVO DEL PLASMA AUTÓLOGO Y SUS FRACCIONES, COMPONENTES O DERIVADOS, COMO MEDICAMENTO
PROPUESTA PERFIL DE EGRESO BIOQUÍMICO UNIVERSIDAD DE CHILE
 PROPUESTA PERFIL DE EGRESO BIOQUÍMICO UNIVERSIDAD DE CHILE SÍNTESIS DEL PERFIL El Bioquímico de la Universidad de Chile es un profesional especialista en el conocimiento de la estructura y función molecular
PROPUESTA PERFIL DE EGRESO BIOQUÍMICO UNIVERSIDAD DE CHILE SÍNTESIS DEL PERFIL El Bioquímico de la Universidad de Chile es un profesional especialista en el conocimiento de la estructura y función molecular
MASTER EN GESTIÓN DE EMPRESAS BIOTECNOLÓGICAS DE LA SALUD MEMORIA DE VERIFICACIÓN Facultad de Farmacia
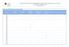 MAPA DE COMPETENCIAS POR MATERIAS Competencias Introducción y fundamentos Biotecnología de la Salud Departamentos transversales en bioempresas Marketing, estrategia y comercialización en biotecnología
MAPA DE COMPETENCIAS POR MATERIAS Competencias Introducción y fundamentos Biotecnología de la Salud Departamentos transversales en bioempresas Marketing, estrategia y comercialización en biotecnología
Medicamentos genéricos, una realidad en el campo de la oncología. Dra Q.F. Betzabé Rubio Lara San Pedro de Atacama CHILE-2013
 Medicamentos genéricos, una realidad en el campo de la oncología Dra Q.F. Betzabé Rubio Lara San Pedro de Atacama CHILE-2013 medicamento de marca Un medicamento de marca es aquél sintetizado por un laboratorio,
Medicamentos genéricos, una realidad en el campo de la oncología Dra Q.F. Betzabé Rubio Lara San Pedro de Atacama CHILE-2013 medicamento de marca Un medicamento de marca es aquél sintetizado por un laboratorio,
Preguntas que se hacen con frecuencia sobre los estudios clínicos
 Preguntas que se hacen con frecuencia sobre los estudios clínicos Son seguros? Todos los ensayos clínicos deben ser aprobados por el gobierno federal y deben cumplir con una reglamentación estricta que
Preguntas que se hacen con frecuencia sobre los estudios clínicos Son seguros? Todos los ensayos clínicos deben ser aprobados por el gobierno federal y deben cumplir con una reglamentación estricta que
Conclusiones y recomendaciones Primera parte: análisis situacional
 y recomendaciones Primera parte: análisis situacional Reunión regional de directores de programas de eliminación de lepra con los países que informan 100 o más casos nuevos por año (Argentina, Bolivia,
y recomendaciones Primera parte: análisis situacional Reunión regional de directores de programas de eliminación de lepra con los países que informan 100 o más casos nuevos por año (Argentina, Bolivia,
Ensayos Clínicos en Oncología
 Ensayos Clínicos en Oncología Qué son y para qué sirven? www.seom.org ESP 05/04 ON4 Con la colaboración de: Una parte muy importante de la Investigación en Oncología Médica se realiza a través de Ensayos
Ensayos Clínicos en Oncología Qué son y para qué sirven? www.seom.org ESP 05/04 ON4 Con la colaboración de: Una parte muy importante de la Investigación en Oncología Médica se realiza a través de Ensayos
PRESENTACIÓN. Lab Safety Consulting, S.L.U.
 PRESENTACIÓN se presenta como una empresa pionera en el ámbito nacional para ofrecer un servicio integral en todos los aspectos relacionados con la gestión de la seguridad e higiene y las buenas prácticas.
PRESENTACIÓN se presenta como una empresa pionera en el ámbito nacional para ofrecer un servicio integral en todos los aspectos relacionados con la gestión de la seguridad e higiene y las buenas prácticas.
Requisitos para optar a auditorias de BPM según RTCA 11.03.42:07 equivalente al Informe 32 de OMS
 Requisitos para optar a auditorias de BPM según RTCA 11.03.42:07 equivalente al Informe 32 de OMS Guatemala, 02 de octubre de 2012 M.Sc. Raúl Mendoza Paredes Inspecciones de establecimientos farmacéuticos
Requisitos para optar a auditorias de BPM según RTCA 11.03.42:07 equivalente al Informe 32 de OMS Guatemala, 02 de octubre de 2012 M.Sc. Raúl Mendoza Paredes Inspecciones de establecimientos farmacéuticos
Norma ISO 9001: 2008. Sistema de Gestión de la Calidad
 Norma ISO 9001: 2008 Sistema de Gestión de la Calidad Hemos recibido una solicitud de información a través de nuestra Web (www.grupoacms.com). Próximamente un comercial de ACMS se pondrá en contacto con
Norma ISO 9001: 2008 Sistema de Gestión de la Calidad Hemos recibido una solicitud de información a través de nuestra Web (www.grupoacms.com). Próximamente un comercial de ACMS se pondrá en contacto con
PLAN DE REFORMA DE GESTION DE LA DEUDA
 PERFIL DEL PAÍS, SITUACIÓN ACTUAL DE LA DEUDA. El Ministerio de Hacienda (MH) y el Banco Central de La República del Paraguay (BCP) han colaborado exitosamente para mejorar la gestión de la deuda pública
PERFIL DEL PAÍS, SITUACIÓN ACTUAL DE LA DEUDA. El Ministerio de Hacienda (MH) y el Banco Central de La República del Paraguay (BCP) han colaborado exitosamente para mejorar la gestión de la deuda pública
LINEAMIENTOS PARA LA TESTIFICACIÓN DE ALCANCES DE ACREDITACIÓN PARA ORGANISMOS DE CERTIFICACIÓN DE PRODUCTOS, PROCESOS O SERVICIOS INS-4.
 PÁGINA: 1 LINEAMIENTOS PARA LA TESTIFICACIÓN DE ORGANISMOS DE CERTIFICACIÓN DE PRODUCTOS, PROCESOS O SERVICIOS INS-4.1-01 PROCESO NIVEL 1: PROCESO NIVEL 2: 4. PROCESO EJECUCIÓN SERVICIOS DE CREDITACIÓN
PÁGINA: 1 LINEAMIENTOS PARA LA TESTIFICACIÓN DE ORGANISMOS DE CERTIFICACIÓN DE PRODUCTOS, PROCESOS O SERVICIOS INS-4.1-01 PROCESO NIVEL 1: PROCESO NIVEL 2: 4. PROCESO EJECUCIÓN SERVICIOS DE CREDITACIÓN
Curso. Introducción a la Administracion de Proyectos
 Curso Introducción a la Administracion de Proyectos Tema 5 Procesos del área de Integración INICIAR PLANEAR EJECUTAR CONTROL CERRAR Desarrollar el Acta de Proyecto Desarrollar el Plan de Proyecto Dirigir
Curso Introducción a la Administracion de Proyectos Tema 5 Procesos del área de Integración INICIAR PLANEAR EJECUTAR CONTROL CERRAR Desarrollar el Acta de Proyecto Desarrollar el Plan de Proyecto Dirigir
Guía de Normas de Correcta Fabricación de Medicamentos de Uso Humano y Veterinario. Capítulo 1. Sistema de Calidad Farmacéutico
 DEPARTAMENTO DE INSPECCIÓN Y CONTROL DE MEDICAMENTOS Guía de Normas de Correcta Fabricación de Medicamentos de Uso Humano y Veterinario Capítulo 1 Sistema de Calidad Farmacéutico Bases legales para la
DEPARTAMENTO DE INSPECCIÓN Y CONTROL DE MEDICAMENTOS Guía de Normas de Correcta Fabricación de Medicamentos de Uso Humano y Veterinario Capítulo 1 Sistema de Calidad Farmacéutico Bases legales para la
EXPEDIENTE DE MEDICAMENTO EN INVESTIGACIÓN (IMPD) PARA MEDICAMENTOS DE TERAPIA CELULAR: MÓDULO DE CALIDAD
 EXPEDIENTE DE MEDICAMENTO EN INVESTIGACIÓN (IMPD) PARA MEDICAMENTOS DE TERAPIA CELULAR: MÓDULO DE CALIDAD Susana Rojo División de Productos Biológicos y Biotecnología AEMPS La solicitud se hará preferentemente
EXPEDIENTE DE MEDICAMENTO EN INVESTIGACIÓN (IMPD) PARA MEDICAMENTOS DE TERAPIA CELULAR: MÓDULO DE CALIDAD Susana Rojo División de Productos Biológicos y Biotecnología AEMPS La solicitud se hará preferentemente
GESTIÓN DE LA CALIDAD EN LOS SERVICIOS ESPECIALIZADOS EN NUTRICIÓN E HIGIENE DE LOS ALIMENTOS
 Rev Cubana Aliment Nutr 1998;12(1):64-70 INFORMACIONES Instituto de Nutrición e Higiene de los Alimentos GESTIÓN DE LA CALIDAD EN LOS SERVICIOS ESPECIALIZADOS EN NUTRICIÓN E HIGIENE DE LOS ALIMENTOS Olga
Rev Cubana Aliment Nutr 1998;12(1):64-70 INFORMACIONES Instituto de Nutrición e Higiene de los Alimentos GESTIÓN DE LA CALIDAD EN LOS SERVICIOS ESPECIALIZADOS EN NUTRICIÓN E HIGIENE DE LOS ALIMENTOS Olga
Medicamento Biológico de Referencia Medicamentos Biosimilares
 Medicamento Biológico de Referencia (MBR): Producto innovador, con documentación completa e independiente que cumple las exigencias de la UE (EMA) en cuanto a calidad, seguridad, incluida inmunogenicidad,
Medicamento Biológico de Referencia (MBR): Producto innovador, con documentación completa e independiente que cumple las exigencias de la UE (EMA) en cuanto a calidad, seguridad, incluida inmunogenicidad,
PLANIFICACIÓN. PLANIFICACIÓN. OBJETIVOS, METAS Y PROGRAMAS PIG-07 HOTEL - RESTAURANTE. Fecha: Edición: 01 Página: 1/5.
 Página: 1/5 Elaborado por: Revisado por: Aprobado por: JAVIER ARRANZ LAPRIDA Página: 2/5 1. OBJETO El objetivo de este procedimiento es definir las actuaciones a llevar a cabo con respecto a la determinación
Página: 1/5 Elaborado por: Revisado por: Aprobado por: JAVIER ARRANZ LAPRIDA Página: 2/5 1. OBJETO El objetivo de este procedimiento es definir las actuaciones a llevar a cabo con respecto a la determinación
Actualización del Sistema de Registro Nacional
 Actualización del Sistema de Registro Nacional Subdirección General de Sanidad Ambiental y Salud Laboral Dirección General de Salud Pública, Calidad e Innovación Ministerio de Sanidad, Servicios Sociales
Actualización del Sistema de Registro Nacional Subdirección General de Sanidad Ambiental y Salud Laboral Dirección General de Salud Pública, Calidad e Innovación Ministerio de Sanidad, Servicios Sociales
GUÍA 14 Diseño de Planes y Programas. Descripción
 GUÍA 14 Diseño de Planes y Programas Descripción El Diseño de Planes y Programas tiene como objetivo elaborar la proyección de la institución a corto, mediano y largo plazo, e impulsar y guiar las actividades
GUÍA 14 Diseño de Planes y Programas Descripción El Diseño de Planes y Programas tiene como objetivo elaborar la proyección de la institución a corto, mediano y largo plazo, e impulsar y guiar las actividades
CIRCULAR No. 09/2002
 CIRCULAR No. 09/2002 A: Jefe del Programa Nacional de Inmunización del Ministerio de Salud Pública Unidad de Donaciones y Proyectos del Ministerio de Salud Pública Empresa Cubana Importadora y Exportadora
CIRCULAR No. 09/2002 A: Jefe del Programa Nacional de Inmunización del Ministerio de Salud Pública Unidad de Donaciones y Proyectos del Ministerio de Salud Pública Empresa Cubana Importadora y Exportadora
Certificación de Buenas Prácticas de Fabricación Productos Cosméticos UNE-EN-ISO 22716. Barcelona, 18 enero 2012
 Certificación de Buenas Prácticas de Fabricación Productos Cosméticos UNE-EN-ISO 22716 Barcelona, 18 enero 2012 AENOR Personas/ Pacientes Personas con necesidades, problemas de salud Organización/establecimiento
Certificación de Buenas Prácticas de Fabricación Productos Cosméticos UNE-EN-ISO 22716 Barcelona, 18 enero 2012 AENOR Personas/ Pacientes Personas con necesidades, problemas de salud Organización/establecimiento
AUD 008-2014. Estudio de Auditoría 008-2014 Verificación del Licenciamiento del Software equipo de MIDEPLAN Decreto Ejecutivo Nº 37549-JP
 AUD 008-2014 Estudio de Auditoría 008-2014 Verificación del Licenciamiento del Software equipo de MIDEPLAN Decreto Ejecutivo Nº 37549-JP JUNIO 2014 0 I.- INFORMACIÓN GENERAL 1.1 Nombre del Estudio Verificación
AUD 008-2014 Estudio de Auditoría 008-2014 Verificación del Licenciamiento del Software equipo de MIDEPLAN Decreto Ejecutivo Nº 37549-JP JUNIO 2014 0 I.- INFORMACIÓN GENERAL 1.1 Nombre del Estudio Verificación
POLITICA DE GESTION DE RIESGOS, ROLES Y RESPONSABLES. Departamento de Estudios y Gestión Estratégica
 POLITICA DE GESTION DE RIESGOS, ROLES Y RESPONSABLES Departamento de Estudios y Gestión Estratégica 2012 1 I. POLITICA DE GESTION DE RIESGOS La Comisión Nacional de Investigación Científica y Tecnológica
POLITICA DE GESTION DE RIESGOS, ROLES Y RESPONSABLES Departamento de Estudios y Gestión Estratégica 2012 1 I. POLITICA DE GESTION DE RIESGOS La Comisión Nacional de Investigación Científica y Tecnológica
\*J. MINISTERIO DE SALUD Y PROTECCiÓN SOCIAL 18 SEP 2014
 " REPÚBLICA DE COLOMBIA ~ \*J ------...,...;.:; dihnci~ III al IE'ia2.. I.CIiIIARlj JUIIIIII.... MINISTERIO DE SALUD Y PROTECCiÓN SOCIAL DECRETO NÚMERO 1782 DE 2014 18 SEP 2014 Por el cual se establecen
" REPÚBLICA DE COLOMBIA ~ \*J ------...,...;.:; dihnci~ III al IE'ia2.. I.CIiIIARlj JUIIIIII.... MINISTERIO DE SALUD Y PROTECCiÓN SOCIAL DECRETO NÚMERO 1782 DE 2014 18 SEP 2014 Por el cual se establecen
DOG Núm. 237 Lunes, 14 de diciembre de 2015 Pág. 46757
 DOG Núm. 237 Lunes, 14 de diciembre de 2015 Pág. 46757 III. OTRAS DISPOSICIONES UNIVERSIDAD DE SANTIAGO DE COMPOSTELA RESOLUCIÓN de 3 de diciembre de 2015 por la que se crea el fichero de datos de carácter
DOG Núm. 237 Lunes, 14 de diciembre de 2015 Pág. 46757 III. OTRAS DISPOSICIONES UNIVERSIDAD DE SANTIAGO DE COMPOSTELA RESOLUCIÓN de 3 de diciembre de 2015 por la que se crea el fichero de datos de carácter
IV JORNADA NACIONAL DE ANMAT FEDERAL
 IV JORNADA NACIONAL DE ANMAT FEDERAL AVANCES EN LA REGULACIÓN DE BANCOS DE SANGRE 25 de junio de 2013 Bioq. Patricia Aprea paprea@anmat.gov.ar BUENAS PRACTICAS DE MANUFACTURA DE MEDICAMENTOS ELEMENTO CLAVE
IV JORNADA NACIONAL DE ANMAT FEDERAL AVANCES EN LA REGULACIÓN DE BANCOS DE SANGRE 25 de junio de 2013 Bioq. Patricia Aprea paprea@anmat.gov.ar BUENAS PRACTICAS DE MANUFACTURA DE MEDICAMENTOS ELEMENTO CLAVE
RED MEXICANA DE MONITOREO DE ORGANISMOS GENÉTICAMENTE MODIFICADOS
 RED MEXICANA DE MONITOREO DE ORGANISMOS GENÉTICAMENTE MODIFICADOS La biotecnología moderna aplicada a la agricultura se utiliza desde hace 15 años como un componente para el desarrollo en países que quieren
RED MEXICANA DE MONITOREO DE ORGANISMOS GENÉTICAMENTE MODIFICADOS La biotecnología moderna aplicada a la agricultura se utiliza desde hace 15 años como un componente para el desarrollo en países que quieren
DISPOSICIONES GENERALES. En primer lugar se determina que la UNED contará para realizar sus funciones y competencias con:
 LA ESTRUCTURA ACADÉMICA DE LA UNED II. INSTITUTOS UNIVERSITARIOS DE INVESTIGACIÓN. CENTRO ADSCRITOS Y SERVICIOS DE ASISTENCIA A LA COMUNIDAD UNIVERSITARIA. En desarrollo del Capítulo I del Título II de
LA ESTRUCTURA ACADÉMICA DE LA UNED II. INSTITUTOS UNIVERSITARIOS DE INVESTIGACIÓN. CENTRO ADSCRITOS Y SERVICIOS DE ASISTENCIA A LA COMUNIDAD UNIVERSITARIA. En desarrollo del Capítulo I del Título II de
5 GESTION DE LOS PROVEEDORES. Módulo
 Módulo 5 GESTION DE LOS PROVEEDORES Consuelo Macías as Instituto de Hematología e Imunología Ministerio de Salud Pública Ciudad Habana Curso OPS Gestión n de Calidad para Laboratorios Antigua, Guatemala,
Módulo 5 GESTION DE LOS PROVEEDORES Consuelo Macías as Instituto de Hematología e Imunología Ministerio de Salud Pública Ciudad Habana Curso OPS Gestión n de Calidad para Laboratorios Antigua, Guatemala,
ANÁLISIS COMPARATIVO DE PROCESOS DE PRIORIZACIÓN EN SALUD
 ANÁLISIS COMPARATIVO DE PROCESOS DE PRIORIZACIÓN EN SALUD Ministerio de la Protección Social NICE International IECS Universidad de los Andes Banco Interamericano de Desarrollo Bogotá, 14 de abril, 2011
ANÁLISIS COMPARATIVO DE PROCESOS DE PRIORIZACIÓN EN SALUD Ministerio de la Protección Social NICE International IECS Universidad de los Andes Banco Interamericano de Desarrollo Bogotá, 14 de abril, 2011
PROCEDIMIENTO DE EVALUACIÓN Y ACREDITACIÓN DE LAS COMPETENCIAS PROFESIONALES CUESTIONARIO DE AUTOEVALUACIÓN PARA LAS TRABAJADORAS Y TRABAJADORES
 MINISTERIO DE EDUCACIÓN, CULTURA Y DEPORTE SECRETARÍA DE ESTADO DE EDUCACIÓN, FORMACIÓN PROFESIONAL Y UNIVERSIDADES DIRECCIÓN GENERAL DE FORMACIÓN PROFESIONAL INSTITUTO NACIONAL DE LAS CUALIFICACIONES
MINISTERIO DE EDUCACIÓN, CULTURA Y DEPORTE SECRETARÍA DE ESTADO DE EDUCACIÓN, FORMACIÓN PROFESIONAL Y UNIVERSIDADES DIRECCIÓN GENERAL DE FORMACIÓN PROFESIONAL INSTITUTO NACIONAL DE LAS CUALIFICACIONES
Principales Cambios de la ISO 9001:2015
 INTRODUCCIÓN La nueva versión disponible de ISO 9001:2015, actualmente en su versión DIS, muestra una gran cantidad de cambios respecto de su predecesora. Muchos de estos cambios están en línea con otros
INTRODUCCIÓN La nueva versión disponible de ISO 9001:2015, actualmente en su versión DIS, muestra una gran cantidad de cambios respecto de su predecesora. Muchos de estos cambios están en línea con otros
Datos sobre FSMA. Norma propuesta sobre las acreditaciones de los auditores externos. Sumario
 Datos sobre FSMA Norma propuesta sobre las acreditaciones de los auditores externos Sumario El 26 de julio de 2013, la FDA publicó para comentarios públicos su norma propuesta para establecer un programa
Datos sobre FSMA Norma propuesta sobre las acreditaciones de los auditores externos Sumario El 26 de julio de 2013, la FDA publicó para comentarios públicos su norma propuesta para establecer un programa
'No ORGANIZACIÓN ORGANIZACIÓN
 consejo directivo comité regional 'No ORGANIZACIÓN ORGANIZACIÓN PANAMERICANA MUNDIAL DE LA SALUD DE LA SALUD XXXIX Reunión Washington, D.C. Septiembre 1996 XLVIII Reunión Tema 2.6 del programa provisional
consejo directivo comité regional 'No ORGANIZACIÓN ORGANIZACIÓN PANAMERICANA MUNDIAL DE LA SALUD DE LA SALUD XXXIX Reunión Washington, D.C. Septiembre 1996 XLVIII Reunión Tema 2.6 del programa provisional
Dirección de Planificación y Desarrollo Descripción de Programas y Proyectos - Octubre - 2014
 Dirección de Planificación y Desarrollo Descripción de Programas y Proyectos - Octubre - 2014 Proveer el Data Center de equipo para la prevención y sofocación de incendios La Superintendencia de Valores
Dirección de Planificación y Desarrollo Descripción de Programas y Proyectos - Octubre - 2014 Proveer el Data Center de equipo para la prevención y sofocación de incendios La Superintendencia de Valores
RD 1591/2009 DOCUMENTO NO APLICABLE 2 1.9.2011 LIBRE
 TITULO DOCUMENTO OBLIGACIONES REGULATORIAS PARA EMPRESAS DISTRIBUIDORAS DE PRODUCTOS SANITARIOS EN ESPAÑA RD 1591/2009 EMPRESA DESTINATARIA EMPRESAS DISTRIBUIDORAS DE PRODUCTOSS SANITARIOS DOCUMENTOS ANEXOS
TITULO DOCUMENTO OBLIGACIONES REGULATORIAS PARA EMPRESAS DISTRIBUIDORAS DE PRODUCTOS SANITARIOS EN ESPAÑA RD 1591/2009 EMPRESA DESTINATARIA EMPRESAS DISTRIBUIDORAS DE PRODUCTOSS SANITARIOS DOCUMENTOS ANEXOS
Políticas públicas de Propiedad Intelectual e Innovación en Chile. La Habana, Cuba - 24 de abril 2014
 Políticas públicas de Propiedad Intelectual e Innovación en Chile La Habana, Cuba - 24 de abril 2014 Nuestra Economía La economía chilena se destaca por ser abierta, competitiva, orientada al libre comercio
Políticas públicas de Propiedad Intelectual e Innovación en Chile La Habana, Cuba - 24 de abril 2014 Nuestra Economía La economía chilena se destaca por ser abierta, competitiva, orientada al libre comercio
Unidad responsable: Servicio de Ordenación e Inspección Sanitaria
 PROGRAMA 511: ORDENACIÓN E INSPECCIÓN SANITARIAS Unidad responsable: Servicio de Ordenación e Inspección Sanitaria Objetivos/ Acciones/ Indicadores del programa 01. Establecer los requisitos técnico-sanitarios
PROGRAMA 511: ORDENACIÓN E INSPECCIÓN SANITARIAS Unidad responsable: Servicio de Ordenación e Inspección Sanitaria Objetivos/ Acciones/ Indicadores del programa 01. Establecer los requisitos técnico-sanitarios
SEMINARIO DE CAPACITACION EN DELITOS DE FALSIFICACIÓN DE PRODUCTOS. DE LAS FUNCIONES, COMPETENCIAS Y EL PROCESO SANCIONATORIO Junio 2013
 SEMINARIO DE CAPACITACION EN DELITOS DE FALSIFICACIÓN DE PRODUCTOS DE LAS FUNCIONES, COMPETENCIAS Y EL PROCESO SANCIONATORIO Junio 2013 COMPETENCIAS Ley 1122 de 2007. ARTÍCULO 34. SUPERVISIÓN EN ALGUNAS
SEMINARIO DE CAPACITACION EN DELITOS DE FALSIFICACIÓN DE PRODUCTOS DE LAS FUNCIONES, COMPETENCIAS Y EL PROCESO SANCIONATORIO Junio 2013 COMPETENCIAS Ley 1122 de 2007. ARTÍCULO 34. SUPERVISIÓN EN ALGUNAS
Convocatoria de Acciones de Apoyo a la Transferencia de Tecnología y Conocimiento
 4 de octubre de 2012 Convocatoria de Acciones de Apoyo a la Transferencia de Tecnología y Conocimiento El proyecto del programa CONSOLIDER INGENIO 2010 convoca acciones de apoyo para el desarrollo de proyectos
4 de octubre de 2012 Convocatoria de Acciones de Apoyo a la Transferencia de Tecnología y Conocimiento El proyecto del programa CONSOLIDER INGENIO 2010 convoca acciones de apoyo para el desarrollo de proyectos
TEMARIO. Sistemas de Gestión
 SISTEMAS DE GESTIÓN TEMARIO Sistemas de Gestión Sistema de Gestión Integrado Gestión de la Calidad Gestión Ambiental Gestión de la Salud y Seguridad Ocupacional Gestión de Energía Acuerdos de producción
SISTEMAS DE GESTIÓN TEMARIO Sistemas de Gestión Sistema de Gestión Integrado Gestión de la Calidad Gestión Ambiental Gestión de la Salud y Seguridad Ocupacional Gestión de Energía Acuerdos de producción
Elementos requeridos para crearlos (ejemplo: el compilador)
 Generalidades A lo largo del ciclo de vida del proceso de software, los productos de software evolucionan. Desde la concepción del producto y la captura de requisitos inicial hasta la puesta en producción
Generalidades A lo largo del ciclo de vida del proceso de software, los productos de software evolucionan. Desde la concepción del producto y la captura de requisitos inicial hasta la puesta en producción
PROGRAMA EFICIENCIA Y RENDICIÓN DE CUENTAS PROYECTO CAPACITACIÓN MECI ENTIDADES NIVEL NACIONAL
 PROGRAMA EFICIENCIA Y RENDICIÓN DE CUENTAS PROYECTO CAPACITACIÓN MECI ENTIDADES NIVEL NACIONAL 1 CONTENIDO 1. OBJETIVOS DE LA SESIÓN 2. COMO VAMOS? 3. DISEÑO E IMPLEMENTACIÓN ELEMENTOS INDICADORES Y MANUAL
PROGRAMA EFICIENCIA Y RENDICIÓN DE CUENTAS PROYECTO CAPACITACIÓN MECI ENTIDADES NIVEL NACIONAL 1 CONTENIDO 1. OBJETIVOS DE LA SESIÓN 2. COMO VAMOS? 3. DISEÑO E IMPLEMENTACIÓN ELEMENTOS INDICADORES Y MANUAL
POR EL TRABAJO SEGURO Y SALUDABLE EN EUSKADI
 POR EL TRABAJO SEGURO Y SALUDABLE EN EUSKADI Justificación Por qué es necesaria una Estrategia de Seguridad y Salud en el Trabajo de la CAE Para responder a la realidad de la prevención de los riesgos
POR EL TRABAJO SEGURO Y SALUDABLE EN EUSKADI Justificación Por qué es necesaria una Estrategia de Seguridad y Salud en el Trabajo de la CAE Para responder a la realidad de la prevención de los riesgos
Máster Universitario en Biotecnología Molecular y Celular de Plantas
 Máster Universitario en Biotecnología Molecular y Celular de Plantas 5.1. Descripción del Plan de Estudios El Plan de Estudios del Máster de Biotecnología Molecular y Celular de Plantas se estructura en
Máster Universitario en Biotecnología Molecular y Celular de Plantas 5.1. Descripción del Plan de Estudios El Plan de Estudios del Máster de Biotecnología Molecular y Celular de Plantas se estructura en
Nombre del Documento: Manual de Gestión de la Calidad. Referencia a punto de la norma ISO 9001:2000: 4.2.2 DIRECCIÓN GENERAL DE EVALUACIÓN
 Página 1 de 8 DIRECCIÓN GENERAL DE EVALUACIÓN 7.1 Planificación de la realización del servicio En la Dirección General de Evaluación (DGE) la planificación de la realización del servicio está sustentada
Página 1 de 8 DIRECCIÓN GENERAL DE EVALUACIÓN 7.1 Planificación de la realización del servicio En la Dirección General de Evaluación (DGE) la planificación de la realización del servicio está sustentada
PROGRAMA CONSOLIDACIÓN DE LA GESTIÓN FISCAL Y MUNICIPAL CREDITO BID-2032/BL-HO
 PROGRAMA CONSOLIDACIÓN DE LA GESTIÓN FISCAL Y MUNICIPAL CREDITO BID-2032/BL-HO MESA DE AYUDA I. Antecedentes 1. Generales del Proyecto El Gobierno de la República a través de la Secretaria de Finanzas
PROGRAMA CONSOLIDACIÓN DE LA GESTIÓN FISCAL Y MUNICIPAL CREDITO BID-2032/BL-HO MESA DE AYUDA I. Antecedentes 1. Generales del Proyecto El Gobierno de la República a través de la Secretaria de Finanzas
Asamblea Nacional Secretaría General TRÁMITE LEGISLATIVO 2014-2015
 Asamblea Nacional Secretaría General TRÁMITE LEGISLATIVO 2014-2015 ANTEPROYECTO DE LEY: 115 PROYECTO DE LEY: LEY: GACETA OFICIAL: TÍTULO: QUE REGULA EL EJERCICIO DE LA PROFESIÓN DE TÉCNICO ASISTENTE DE
Asamblea Nacional Secretaría General TRÁMITE LEGISLATIVO 2014-2015 ANTEPROYECTO DE LEY: 115 PROYECTO DE LEY: LEY: GACETA OFICIAL: TÍTULO: QUE REGULA EL EJERCICIO DE LA PROFESIÓN DE TÉCNICO ASISTENTE DE
OHSAS 18001: 2007. Sistema de Gestión de la Seguridad y Salud en el trabajo
 OHSAS 18001: 2007 Sistema de Gestión de la Seguridad y Salud en el trabajo El presente documento es la versión impresa de la página www.grupoacms.com Si desea más información sobre OHSAS 18001 u otras
OHSAS 18001: 2007 Sistema de Gestión de la Seguridad y Salud en el trabajo El presente documento es la versión impresa de la página www.grupoacms.com Si desea más información sobre OHSAS 18001 u otras
LISTA DE CHEQUEO REQUISITOS REGISTRO SANITARIO MEDICAMENTOS
 LISTA DE CHEQUEO REQUISITOS REGISTRO SANITARIO MEDICAMENTOS Los requisitos para registro sanitario son los siguientes: 7.1. Solicitud firmada y sellada por el Profesional Responsable conteniendo la información
LISTA DE CHEQUEO REQUISITOS REGISTRO SANITARIO MEDICAMENTOS Los requisitos para registro sanitario son los siguientes: 7.1. Solicitud firmada y sellada por el Profesional Responsable conteniendo la información
Modelos de gestión de proyectos informáticos
 Modelos de gestión de proyectos informáticos Informe SEIS 2005-2006 Xavier Pastor 25 de enero de 2007 Proyectos: Definición Características Temporalidad: inicio y final Productos, servicios o resultados
Modelos de gestión de proyectos informáticos Informe SEIS 2005-2006 Xavier Pastor 25 de enero de 2007 Proyectos: Definición Características Temporalidad: inicio y final Productos, servicios o resultados
REGLAMENTO DEL SISTEMA DE INVESTIGACIÓN, INNOVACIÓN, TRANSFERENCIA TECNOLÓGICA
 REGLAMENTO DEL SISTEMA DE INVESTIGACIÓN, INNOVACIÓN, TRANSFERENCIA TECNOLÓGICA EL HONORABLE CONSEJO GUBERNATIVO DEL INSTITUTO TECNOLÓGICO SUPERIOR BLUE HILL CONSIDERANDO: Que, de conformidad con la Constitución
REGLAMENTO DEL SISTEMA DE INVESTIGACIÓN, INNOVACIÓN, TRANSFERENCIA TECNOLÓGICA EL HONORABLE CONSEJO GUBERNATIVO DEL INSTITUTO TECNOLÓGICO SUPERIOR BLUE HILL CONSIDERANDO: Que, de conformidad con la Constitución
Norma ISO 14001: 2004
 Norma ISO 14001: 2004 Sistema de Gestión Ambiental El presente documento es la versión impresa de la página www.grupoacms.com Si desea más información sobre la Norma ISO 14001 u otras normas relacionadas
Norma ISO 14001: 2004 Sistema de Gestión Ambiental El presente documento es la versión impresa de la página www.grupoacms.com Si desea más información sobre la Norma ISO 14001 u otras normas relacionadas
AREA DE VIGILANCIA Y SEGURIDAD MANUAL SISTEMA INTEGRADO DE SEGURIDAD
 SISTEMA INTEGRADO DE SEGURIDAD PÁGINA 1 de 1 AREA DE VIGILANCIA Y SEGURIDAD SISTEMA INTEGRADO DE SEGURIDAD SISTEMA INTEGRADO DE SEGURIDAD PÁGINA 2 de 2 TABLA DE CONTENIDO 1. INTRODUCCIÓN... 3 2. OBJETIVO
SISTEMA INTEGRADO DE SEGURIDAD PÁGINA 1 de 1 AREA DE VIGILANCIA Y SEGURIDAD SISTEMA INTEGRADO DE SEGURIDAD SISTEMA INTEGRADO DE SEGURIDAD PÁGINA 2 de 2 TABLA DE CONTENIDO 1. INTRODUCCIÓN... 3 2. OBJETIVO
ALINEAMIENTO DE LOS PROCESOS DE DIGEMID PARA EL LOGRO DE LOS RESULTADOS INSTITUCIONALES. Octubre 2014
 ALINEAMIENTO DE LOS PROCESOS DE DIGEMID PARA EL LOGRO DE LOS RESULTADOS INSTITUCIONALES Octubre 2014 ERICA YUKIKO NISHIHARA DIRECTORA EJECUTIVA DE LA DIRECCION DE AUTORIZACIONES SANITARIAS- DIGEMID de
ALINEAMIENTO DE LOS PROCESOS DE DIGEMID PARA EL LOGRO DE LOS RESULTADOS INSTITUCIONALES Octubre 2014 ERICA YUKIKO NISHIHARA DIRECTORA EJECUTIVA DE LA DIRECCION DE AUTORIZACIONES SANITARIAS- DIGEMID de
Generalización del diseño y desarrollo tecnológico de una formulación inyectable de Ondansetron-4. aica. Empresa Laboratorios aica.
 Generalización del diseño y desarrollo tecnológico de una formulación inyectable de Ondansetron-4. aica Empresa Laboratorios aica. INTRODUCCIÓN La Empresa Laboratorios aica tiene como misión la Elaboración
Generalización del diseño y desarrollo tecnológico de una formulación inyectable de Ondansetron-4. aica Empresa Laboratorios aica. INTRODUCCIÓN La Empresa Laboratorios aica tiene como misión la Elaboración
GUÍA PROGRAMA ACCIONES ESPECIALES DE ALTO COSTE
 GUÍA PROGRAMA ACCIONES ESPECIALES DE ALTO COSTE Índice A. Objeto 3 B. Tipos de de proyectos / Requisitos 3 C. Beneficiarios 4 D. Periodo de ejecución y duración 4 E. Procedimiento 4 F. Plazo de presentación
GUÍA PROGRAMA ACCIONES ESPECIALES DE ALTO COSTE Índice A. Objeto 3 B. Tipos de de proyectos / Requisitos 3 C. Beneficiarios 4 D. Periodo de ejecución y duración 4 E. Procedimiento 4 F. Plazo de presentación
ACUERDO GUBERNATIVO No. 351-2006
 ACUERDO GUBERNATIVO No. 351-2006 Guatemala, 16 de junio de 2006. EL PRESIDENTE DE LA REPUBLICA CONSIDERANDO: De conformidad con la Constitución Política de la República de Guatemala la salud de los habitantes
ACUERDO GUBERNATIVO No. 351-2006 Guatemala, 16 de junio de 2006. EL PRESIDENTE DE LA REPUBLICA CONSIDERANDO: De conformidad con la Constitución Política de la República de Guatemala la salud de los habitantes
Requisitos Habilitación Servicio Vacunación
 Requisitos Habilitación Servicio Vacunación Anexo técnico No. 1 de la resolución 1043 de 2006, con las modificaciones de las resoluciones 2680 y 3763 de 2007 Por la cual se establecen las condiciones que
Requisitos Habilitación Servicio Vacunación Anexo técnico No. 1 de la resolución 1043 de 2006, con las modificaciones de las resoluciones 2680 y 3763 de 2007 Por la cual se establecen las condiciones que
COMITÉS Y UNIDADES DE FARMACOVIGILANCIA HOSPITALARIA FORO PARA UNIDADES DE FARMACOVIGILANCIA DE HOSPITALES Y CLINICAS
 COMITÉS Y UNIDADES DE FARMACOVIGILANCIA HOSPITALARIA FORO PARA UNIDADES DE FARMACOVIGILANCIA DE HOSPITALES Y CLINICAS 23 OCTUBRE 2013 SEGURIDAD DEL PACIENTE DAÑO ASOCIADO A LA ATENCION SANITARIA ATENCION
COMITÉS Y UNIDADES DE FARMACOVIGILANCIA HOSPITALARIA FORO PARA UNIDADES DE FARMACOVIGILANCIA DE HOSPITALES Y CLINICAS 23 OCTUBRE 2013 SEGURIDAD DEL PACIENTE DAÑO ASOCIADO A LA ATENCION SANITARIA ATENCION
Experiencias, Fortalezas y Debilidades del Sistema de Farmacovigilancia según Indicadores OPS
 REPÚBLICA DE NICARAGUA MINISTERIO DE SALUD DIRECCIÓN GENERAL DE REGULACIÓN SANITARIA DEPARTAMENTO DE FARMACOVIGILANCIA Experiencias, Fortalezas y Debilidades del Sistema de Farmacovigilancia según Indicadores
REPÚBLICA DE NICARAGUA MINISTERIO DE SALUD DIRECCIÓN GENERAL DE REGULACIÓN SANITARIA DEPARTAMENTO DE FARMACOVIGILANCIA Experiencias, Fortalezas y Debilidades del Sistema de Farmacovigilancia según Indicadores
EVALUACIÓN SOBRE LA PROPUESTA DE MODIFICACIÓN DE PLAN DE ESTUDIOS
 FECHA: 30/04/2015 EXPEDIENTE Nº: 2369/2009 ID TÍTULO: 2501468 EVALUACIÓN SOBRE LA PROPUESTA DE MODIFICACIÓN DE PLAN DE ESTUDIOS Denominación del Título Universidad solicitante Universidad/es participante/s
FECHA: 30/04/2015 EXPEDIENTE Nº: 2369/2009 ID TÍTULO: 2501468 EVALUACIÓN SOBRE LA PROPUESTA DE MODIFICACIÓN DE PLAN DE ESTUDIOS Denominación del Título Universidad solicitante Universidad/es participante/s
II ENCUENTRO DE ASOCIACIONES PROFESIONALES FARMACÉUTICAS
 II ENCUENTRO DE ASOCIACIONES PROFESIONALES FARMACÉUTICAS Punto de vista de los Farmacéuticos de Industria ( AEFI y Voc. Industria del COFM) Hemos hecho una revisión de los planes de estudio de las 6 universidades
II ENCUENTRO DE ASOCIACIONES PROFESIONALES FARMACÉUTICAS Punto de vista de los Farmacéuticos de Industria ( AEFI y Voc. Industria del COFM) Hemos hecho una revisión de los planes de estudio de las 6 universidades
INTERCAMBIABILIDAD. Adriana Martínez Martínez DIRECCIÓN EJECUTIVA DE AUTORIZACIÓN DE PRODUCTOS Y ESTABLECIMIENTOS. Dictaminadora Especializada
 INTERCAMBIABILIDAD Adriana Martínez Martínez Dictaminadora Especializada DIRECCIÓN EJECUTIVA DE AUTORIZACIÓN DE PRODUCTOS Y ESTABLECIMIENTOS 1 PRUEBAS DE INTERCAMBIABILIDAD Prueba A. Buenas prácticas de
INTERCAMBIABILIDAD Adriana Martínez Martínez Dictaminadora Especializada DIRECCIÓN EJECUTIVA DE AUTORIZACIÓN DE PRODUCTOS Y ESTABLECIMIENTOS 1 PRUEBAS DE INTERCAMBIABILIDAD Prueba A. Buenas prácticas de
Cells for Cells S.A. (C4C)
 Cells for Cells S.A. (C4C) Compañía biotecnológica chilena dedicada a la investigación, desarrollo y comercialización de terapias celulares innovativas en base a células madre adultas. Cells for Cells
Cells for Cells S.A. (C4C) Compañía biotecnológica chilena dedicada a la investigación, desarrollo y comercialización de terapias celulares innovativas en base a células madre adultas. Cells for Cells
Preguntas frecuentes. Preguntas frecuentes
 Preguntas frecuentes 1 Sobre los CIEES Qué son los CIEES? Son los Comités Interinstitucionales para la Evaluación de la Educación Superior, un organismo dedicado al aseguramiento de la calidad de la educación
Preguntas frecuentes 1 Sobre los CIEES Qué son los CIEES? Son los Comités Interinstitucionales para la Evaluación de la Educación Superior, un organismo dedicado al aseguramiento de la calidad de la educación
Bureau Veritas Certification. ISO 13485 Productos sanitarios. Sistemas de Gestión de la Calidad. Requisitos para fines reglamentarios
 Bureau Veritas Certification ISO 13485 Productos sanitarios. Sistemas de Gestión de la Calidad. Requisitos para fines reglamentarios ESCENARIO DE LA SITUACIÓN El sector sanitario es uno de los sectores
Bureau Veritas Certification ISO 13485 Productos sanitarios. Sistemas de Gestión de la Calidad. Requisitos para fines reglamentarios ESCENARIO DE LA SITUACIÓN El sector sanitario es uno de los sectores
REQUISITOS PARA EL CONTROL Y SEGUIMIENTO DE MARCAPASOS Y DESFIBRILADORES AUTOMÁTICOS IMPLANTABLES
 Ministerio de Salud Pública Centro de Control Estatal de Equipos Médicos Ciudad de la Habana Calle 4 #455.Vedado Tel. 832-5072 835 3889 Email rem@cceem.sld.cu CCEEM ER e -1.1 2008.11.22 REGULACION REQUISITOS
Ministerio de Salud Pública Centro de Control Estatal de Equipos Médicos Ciudad de la Habana Calle 4 #455.Vedado Tel. 832-5072 835 3889 Email rem@cceem.sld.cu CCEEM ER e -1.1 2008.11.22 REGULACION REQUISITOS
RESOLUCIÓN No. I-68 2003
 RESOLUCIÓN No. I-68 2003 POR CUANTO: El Decreto Ley No. 147 de 1994, modificó la integración de los organismos de la Administración central del estado y en su Artículo 4 estableció la creación de la Oficina
RESOLUCIÓN No. I-68 2003 POR CUANTO: El Decreto Ley No. 147 de 1994, modificó la integración de los organismos de la Administración central del estado y en su Artículo 4 estableció la creación de la Oficina
IDEAS PARA UN ANTEPROYECTO DEL PLAN VASCO DE FORMACION PROFESIONAL
 PVFP.J3 IDEAS PARA UN ANTEPROYECTO DEL PLAN VASCO DE FORMACION PROFESIONAL Esquema general J. Manzano INTRODUCCION * El acuerdo de la Comisión Delegada para Asuntos Económicos, por el que se aprueba la
PVFP.J3 IDEAS PARA UN ANTEPROYECTO DEL PLAN VASCO DE FORMACION PROFESIONAL Esquema general J. Manzano INTRODUCCION * El acuerdo de la Comisión Delegada para Asuntos Económicos, por el que se aprueba la
ADMINISTRACIÓN DE PROYECTOS
 QUITO INGENIERIA MECANICA ADMINISTRACIÓN DE PROYECTOS JUAN MARCELO IBUJES VILLACÍS ADMINISTRACIÓN DE PROYECTOS Contenido tomado de referencia de la Guía de los Fundamentos para la Dirección de Proyectos
QUITO INGENIERIA MECANICA ADMINISTRACIÓN DE PROYECTOS JUAN MARCELO IBUJES VILLACÍS ADMINISTRACIÓN DE PROYECTOS Contenido tomado de referencia de la Guía de los Fundamentos para la Dirección de Proyectos
SEMINARIO PARA PERIODISTAS
 SEMINARIO PARA PERIODISTAS Mitos y realidades d de los medicamentos genéricos éi Madrid, 5 de noviembre de 2009 La opinión de los farmacéuticos en cuanto a la prescripción de medicamentos Equivalencia
SEMINARIO PARA PERIODISTAS Mitos y realidades d de los medicamentos genéricos éi Madrid, 5 de noviembre de 2009 La opinión de los farmacéuticos en cuanto a la prescripción de medicamentos Equivalencia
01. Diseñar la ordenación de las enseñanzas de Formación Profesional.
 PROGRAMA 426: FORMACIÓN PROFESIONAL Unidad responsable: Servicio de Formación Profesional Objetivos/ Acciones/ Indicadores del programa 01. Diseñar la ordenación de las enseñanzas de Formación Profesional.
PROGRAMA 426: FORMACIÓN PROFESIONAL Unidad responsable: Servicio de Formación Profesional Objetivos/ Acciones/ Indicadores del programa 01. Diseñar la ordenación de las enseñanzas de Formación Profesional.
Agenda Regional para la Gestión de las Excretas y Aguas Residuales en Centroamérica y República Dominicana FOCARD-APS
 Secretaría General del Sistema de la Integración Centroamericana.. Agenda Regional para la Gestión de las Excretas y Aguas Residuales en Centroamérica y República Dominicana FOCARD-APS Ana de Cardoza Coordinadora
Secretaría General del Sistema de la Integración Centroamericana.. Agenda Regional para la Gestión de las Excretas y Aguas Residuales en Centroamérica y República Dominicana FOCARD-APS Ana de Cardoza Coordinadora
CONTROL DE DOCUMENTOS
 PR-SGIA-2 1 de 5 1. PROPÓSITO Este documento tiene por objeto establecer los lineamientos para el control administrativo y operativo de los documentos internos del Sistema de Gestión Integral de Panamericana
PR-SGIA-2 1 de 5 1. PROPÓSITO Este documento tiene por objeto establecer los lineamientos para el control administrativo y operativo de los documentos internos del Sistema de Gestión Integral de Panamericana
TECNOLOGICO DE ESTUDIOS SUPERIORES DE ECATEPEC CALIDAD DE SOFTWARE Guía para Examen Segundo Parcial Grupo 6501
 1. Qué incluye la ingeniería del software con SQA? Entrenamiento, soporte al consumidor instalación. 2. Menciona algunas características del software: Elemento lógico. Desarrollado no fabricado. No se
1. Qué incluye la ingeniería del software con SQA? Entrenamiento, soporte al consumidor instalación. 2. Menciona algunas características del software: Elemento lógico. Desarrollado no fabricado. No se
Medicamentos Seguros
 Medicamentos Seguros La Administración Nacional de Medicamentos, Alimentos y Tecnología Médica (ANMAT) es el organismo del Estado que, desde el año 1992, tiene como misión, función y responsabilidad primaria
Medicamentos Seguros La Administración Nacional de Medicamentos, Alimentos y Tecnología Médica (ANMAT) es el organismo del Estado que, desde el año 1992, tiene como misión, función y responsabilidad primaria
RESULTADOS DE APRENDIZAJE
 Política de equiparación de competencias de la carrera a resultados de. Área responsable: Carrera de Medicina.0 Página 1 de 5 CONTENIDO 1.- DEFINICIÓN... 2 2.- ALCANCE Y ÁMBITO DE APLICACIÓN... 2 3.- NORMA
Política de equiparación de competencias de la carrera a resultados de. Área responsable: Carrera de Medicina.0 Página 1 de 5 CONTENIDO 1.- DEFINICIÓN... 2 2.- ALCANCE Y ÁMBITO DE APLICACIÓN... 2 3.- NORMA
