Tema 4. ESTRUCTURA ATÓMICA Y SISTEMA PERIÓDICO
|
|
|
- Rosa Castillo Mendoza
- hace 7 años
- Vistas:
Transcripción
1 Tema 4. ESTRUCTURA ATÓMICA Y SISTEMA PERIÓDICO John Dalton (1808). La imagen del átomo expuesta por Dalton en su teoría atómica, es la de minúsculas partículas esféricas, indivisibles e inmutables, iguales entre sí en cada elemento químico. J.J. Thomson, 1897, el átomo debía de ser una esfera de materia cargada positivamente, en cuyo interior estaban incrustados los electrones. E. Rutherford, 1911, Dedujo que el átomo debía estar formado por una corteza con los electrones girando alrededor de un núcleo central cargado positivamente. Niels Bohr, 1913, Propuso un nuevo modelo atómico, según el cual los electrones giran alrededor del núcleo en unos niveles de energía bien definidos.
2 Problema: 1.- Electrones en movimiento alrededor del núcleo, emitirían radiación electromagnética perdiendo energía, y caerían sobre el núcleo átomos inestables. 2.- Electrones estacionarios, la atracción electrostática los arrojaría sobre el núcleo átomos inestables. Bases conceptuales del modelo mecano-cuántico del átomo - Interacción entre la luz y la materia. J.C. Maxwell (1873), la luz está constituida por ondas electromagnéticas. Campo eléctrico Amplitud Longitud de onda (λ) distancia entre puntos idénticos de ondas sucesivas. Amplitud distancia vertical desde el punto medio de la onda hasta el pico o el valle. Frecuencia (ν) número de ondas que pasan a través de un punto en un segundo (Hz = ciclos/s). Campo magnético λ Número de onda, υ es la inversa de la longitud de onda (1/λ) Para toda radiación electromagnética se cumple: λ. ν = c donde c, velocidad de la luz en el vacío = 3, m/s
3 Einstein (1905) la luz está constituida por partículas de energía llamadas fotones. Efecto fotoeléctrico: Emisión de electrones por un metal, al incidir sobre él radiación electromagnética de determinada υ. E fotón = h υ h (cte. de Planck) = 6, J.s Las partículas de luz chocan contra la superficie del metal intercambiando energía que puede liberar electrones. Louis de Broglie, 1924 (dualidad onda-corpúsculo). Toda partícula en movimiento lleva asociada una onda. λ = h mv Heisenberg, 1927 (principio de indeterminación). No es posible conocer simultaneamente y con precisión absoluta la posición y la velocidad de una partícula. x m v h 4π x: indeterminación en la posición. v: indeterminación en la velocidad. h 4π Calcula la longitud de onda asociada a un electrón que se mueve con una velocidad de 3, m/s. Si quieres conocer la posición del electrón con una precisión de 1 Å, cual será la indeterminación en su velocidad?
4 Calcula la longitud de onda asociada a una pelota de ping-pong de 2.5 g que se mueve a 15.6 m/s? Si quieres conocer la posición de la pelota con una precisión de 1 Å, cual será la indeterminación en su velocidad? Cuáles son las consecuencias de estos resultados? Ecuación de ondas de Schrodinger Esta ecuación de ondas (1926) describe las propiedades de partícula y onda de los cuerpos microscópicos. Cada electrón en un átomo está descrito por una función de ondas Ψ que permite conocer: 1. La energía del electrón. 2. La probabilidad de encontrarlo en una zona del espacio. Ψ Ψ Ψ Ψ 8π m ( ) E V Ψ = 0 x y z h Probabilidad de presencia del electrón en una región del espacio. Orbital Atómico: región del espacio donde la probabilidad de encontrar al electrón es del 99%.
5 Función de ondas para el electrón en un orbital atómico tipo p: 3 2 Zr Z r a 0 Z Ψ= cte e senθ cosφ a a 0 0 La resolución exacta de la ecuación de de ondas sólo es posible para el átomo de H. Para sistemas polielectrónicos son necesarias aproximaciones matemáticas que introducen un conjunto de parámetros numéricos llamados números cuánticos. Ψ = f (n, l, m, s) n (número cuántico principal): Su valor determina la energía y la distancia promedio del electrón al núcleo. n = 1, 2, 3, l (número cuántico secundario o acimutal): Su valor determina la energía y define la forma geométrica del orbital. l = 0, 1, (n-1) m (número cuántico magnético): Su valor determina la orientación espacial del orbital. m=-l, 0, +l s (número cuántico de espín): Este número cuántico está relacionado con el campo magnético creado por el electrón cuando gira sobre si mismo. s=± ½. Se simboliza por o por. s=+½ s=-½
6 Para el átomo de hidrógeno e hidrogenoides, se obtiene un valor de energía: E = - KZ 2 1 n 2 Ecuación de Bohr K= 1312 kj/mol e 4 4π 2 m r = n 2 2h 2 n=1 E - r=0.529 La energía necesaria para arrancar un electrón es positiva y al alejarnos del núcleo cada vez más pequeña Números cuánticos y orbitales atómicos n=1 l=0 orbital de forma esférica tipo s (1s) no existen subniveles de energía m=0 orientación única. + n=2 l=0 (2s) m=0 l=1 (2p) m=-1,0,+1 (tres orbitales degenerados) s Así sería un orbital tipo f: n=3 l=0 (3s) m=0 l=1 (3p) m=-1,0,+1 (tres orbitales degenerados) l=2 (3d) m=-2,-1,0,+1,+2 (cinco orbitales degenerados)
7 Números cuánticos, orbitales atómicos y electrones Principio Aufbau: los e - se incorporan al átomo, en estado fundamental de energía, por orden creciente de energía. Regla de Hund o de la máxima multiplicidad: en un átomo en estado fundamental de energía, los e - en orbitales degenerados tienen igual valor de espín (están desapareados). Principio de exclusión de Pauli: no pueden existir e - con los cuatro números cuánticos iguales. estado fundamental de energía? Niveles de energía de los orbitales atómicos = f(n,l) Efecto de apantallamiento: influencia de los e - presentes en el átomo, en la atracción núcleo-electrón. Z eff = Z - S S: cte de apantallamiento S=1 e - en n inferior. S<<1 e - en igual n. Efecto de penetración: Posibilidad del e - de situarse en las cercanías del núcleo. Para n=cte E(s)<E(p)<E(d) Para n=2 E(2s) < E(2p). qué ocurre entre 4d y 5s? Orden creciente de energía: 1s 2s 2p 3s 3p 4s 3d 4p 5s 4d 5p
8 Cuál es la configuración electrónica del sodio y del nitrógeno neutro en estado fundamental? La carga nuclear efectiva sobre el electrón más externo dónde es mayor? Comenta y/o corrige las siguientes afirmaciones: Según el principio de exclusión de Pauli, en cada uno de los orbitales atómicos f (l=3) pueden situarse, como máximo, tres electrones. La configuración electrónica 1s 2 2s 2 2p 6 sólo puede corresponder al neón. En un átomo de hidrógeno probablemente exista un nivel de energía con un valor E= -1, J. Pista: usa la ecuación de Bohr de la página 6. A continuación figuran configuraciones electrónicas de ocho elementos. Cuáles de ellas representan un átomo neutro, un catión o un anión? Especificar si el estado electrónico es fundamental, excitado o imposible. a) Li: 1s 2 2s 1 b) N: 1s 2 2p 4 c) H: 1s 2 2s 1 d) F: 1s 2 2s 2 2p 5 3s 1 e) C: 1s 2 2s 2 2p 1 2d 1 f) Ne: 1s 2 2s 1 2p 7 g) O: 1s 2 2s 2 2p 3 h) He: 1p 1
9 Metales alcalinos Tabla Periódica Gases nobles Metales alcalinotérreos Halógenos No metales 1 2 Metales de transición Lantánidos y Actínidos
10 Tabla periódica y estructura electrónica ns 1 (n-1)d 1 (n-1)d 5 (n-1)d 10 ns 2 ns 2 np 1 ns 2 np 3 ns2 np 6 (n-2)f 1 14 Indica el número de: a) electrones 2p en el nitrógeno, b) electrones 4s en el Rb, c) electrones 4d en el As, d) electrones 4f en el Au e) electrones desapareados en el Pb.
11 Propiedades periódicas: Radio atómico: Valor promedio de radio atómico del elemento en distintos compuestos. Al desplazarse en un período (aumenta Z en una unidad) se incorporan e - al mismo nivel n S<<1 Z eff = Z S el radio atómico debe... Al desplazarse en un grupo se incorporan e - a niveles n más altos S=1 la distancia promedio al núcleo.. Z eff = Z S el radio atómico debe... Ordenar las siguientes especies en función de su tamaño: Na +, Ne, F -, Mg 2+. Energía de ionización (EI): Energía necesaria para arrancar el e - más externo a un átomo en estado gaseoso. EI 1 : X(g) X + (g) + e - EI 2 : X + (g) X 2+ (g) + e - La EI aumenta al aumentar la energía necesaria para arrancar el e - más externo, al aumentar Z eff aumenta EI Derecha tabla periódica, Z eff elevadas altas EI tendencia a formar aniones. Izquierdatabla periódica, Z eff bajas bajas EI tendencia a formar cationes.
12 Afinidad electrónica (AE): Energía liberada cuando un átomo en estado gaseoso gana un e -. F(g) + e - F - g) AE = -328 kj F(1s 2 2s 2 2p 5 ) F - (1s 2 2s 2 2p 6 ) Li(g) + e - Li+(g) AE = kj Li(1s 2 2s 1 ) Li - (1s 2 2s 2 ) Derecha tabla elementos con AE alta (muy negativa) tendencia a formar aniones. Izquierda tabla elementos con AE baja (poco negativa) tendencia a formar cationes. Para los siguientes grupos de elementos, seleccione el que tenga la propiedad requerida: El átomo mayor: Mg, Mo, Bi, Br. La primera energía de ionización más pequeña: B, Sr, Br, Pb. La afinidad electrónica más negativa: As, B, Cl, K, Mg, S. Electronegatividad (EN): Tendencia de un átomo a atraer e - cuando está combinado con otros átomos. Electronegatividad baja (elementos electropositivos) baja EI y baja AE. Electronegatividad alta (elementos electronegativos) alta EI y alta AE. EN máxima (F) = 3,98
EXTRUCTURA ATOMICA ACTUAL
 ATOMOS Y ELEMENTOS TEMA 4 Química ATOMOS EXTRUCTURA ATOMICA ACTUAL PARTICULA UBICACION CARGA MASA PROTON NUCLEO + SI NEUTRON NUCLEO 0 SI ELECTRON ORBITAS - DESPRECIABLE La masa del átomo reside en el núcleo.
ATOMOS Y ELEMENTOS TEMA 4 Química ATOMOS EXTRUCTURA ATOMICA ACTUAL PARTICULA UBICACION CARGA MASA PROTON NUCLEO + SI NEUTRON NUCLEO 0 SI ELECTRON ORBITAS - DESPRECIABLE La masa del átomo reside en el núcleo.
Problemas de Química (1ero Grado de Química). Tema 2. ESTRUCTURA ATÓMICA Y PROPIEDADES PERIÓDICAS
 Problemas de Química (1ero Grado de Química). Tema 2. ESTRUCTURA ATÓMICA Y PROPIEDADES PERIÓDICAS 1. Para el isótopo del elemento con Z = 36 y número másico 84 indique: (a) su número de protones; (b) su
Problemas de Química (1ero Grado de Química). Tema 2. ESTRUCTURA ATÓMICA Y PROPIEDADES PERIÓDICAS 1. Para el isótopo del elemento con Z = 36 y número másico 84 indique: (a) su número de protones; (b) su
El átomo: sus partículas elementales
 El átomo: sus partículas elementales Los rayos catódicos estaban constituidos por partículas cargadas negativamente ( a las que se llamo electrones) y que la relación carga/masa de éstas partículas era
El átomo: sus partículas elementales Los rayos catódicos estaban constituidos por partículas cargadas negativamente ( a las que se llamo electrones) y que la relación carga/masa de éstas partículas era
Estudio del átomo: 1. Átomos e isótopos 2. Modelos Atómicos 3. Teoría cuántica. Ing. Sol de María Jiménez González
 Estudio del átomo: 1. Átomos e isótopos 2. Modelos Atómicos 3. Teoría cuántica 1 Núcleo: protones y neutrones Los electrones se mueven alrededor. Característica Partículas Protón Neutrón Electrón Símbolo
Estudio del átomo: 1. Átomos e isótopos 2. Modelos Atómicos 3. Teoría cuántica 1 Núcleo: protones y neutrones Los electrones se mueven alrededor. Característica Partículas Protón Neutrón Electrón Símbolo
MODELOS ATOMICOS. Solución Å; Ultravioleta; 1106 m/s
 MODELOS ATOMICOS 1. Calcular el valor del radio de la órbita que recorre el electrón del hidrogeno en su estado normal. Datos. h = 6 63 10 27 erg s, m(e ) = 9 1 10 28 gr, q(e ) = 4 8 10-10 u.e.e. Solución.
MODELOS ATOMICOS 1. Calcular el valor del radio de la órbita que recorre el electrón del hidrogeno en su estado normal. Datos. h = 6 63 10 27 erg s, m(e ) = 9 1 10 28 gr, q(e ) = 4 8 10-10 u.e.e. Solución.
LA TABLA PERIÓDICA. Cuestiones generales. Propiedades periódicas
 Cuestiones generales. LA TABLA PERIÓDICA. 1.- Indica el nombre, símbolo, nombre del grupo a que pertenece y periodo de los elementos de números atómicos 3, 9, 16, 19, 38 y 51. 2.- a) Indica el nombre,
Cuestiones generales. LA TABLA PERIÓDICA. 1.- Indica el nombre, símbolo, nombre del grupo a que pertenece y periodo de los elementos de números atómicos 3, 9, 16, 19, 38 y 51. 2.- a) Indica el nombre,
EJERCICIOS RESUELTOS DE TABLA PERIODICA
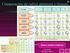 EJERCICIOS RESUELTOS DE TABLA PERIODICA 1. Indique Cuál es el modelo atómico que está actualmente vigente? El Modelo Mecano- cuántico 2. Cuáles fueron los principales hechos y/o descubrimientos que llevaron
EJERCICIOS RESUELTOS DE TABLA PERIODICA 1. Indique Cuál es el modelo atómico que está actualmente vigente? El Modelo Mecano- cuántico 2. Cuáles fueron los principales hechos y/o descubrimientos que llevaron
Estructura de la materia y Sistema Periódico
 Estructura de la materia y Sistema Periódico 1 - Respecto el número cuántico «n» que aparece en el modelo atómico de Bohr indicar de manera razonada cuáles de las siguientes frases son correctas y cuáles
Estructura de la materia y Sistema Periódico 1 - Respecto el número cuántico «n» que aparece en el modelo atómico de Bohr indicar de manera razonada cuáles de las siguientes frases son correctas y cuáles
Actividad: Cómo son las configuraciones electrónicas?
 Cómo son las configuraciones electrónicas de los elementos que forman una familia? Nivel: 2º Medio Subsector: Ciencias químicas Unidad temática: Actividad: Cómo son las configuraciones electrónicas? En
Cómo son las configuraciones electrónicas de los elementos que forman una familia? Nivel: 2º Medio Subsector: Ciencias químicas Unidad temática: Actividad: Cómo son las configuraciones electrónicas? En
TEMA 3 LA TABLA PERIÓDICA
 TEMA 3 LA TABLA PERIÓDICA Mª PILAR RUIZ OJEDA BORJA MUÑOZ LEOZ Contenidos: 1. Antecedentes de la Tabla Periódica 2. La TP y las configuraciones electrónicas 3. Radio atómico. Radio iónico 4. Energía de
TEMA 3 LA TABLA PERIÓDICA Mª PILAR RUIZ OJEDA BORJA MUÑOZ LEOZ Contenidos: 1. Antecedentes de la Tabla Periódica 2. La TP y las configuraciones electrónicas 3. Radio atómico. Radio iónico 4. Energía de
COLEGIO SAN JOSÉ - Hijas de María Auxiliadora C/ Emilio Ferrari, 87 - Madrid Departamento de Ciencias Naturales
 TEMA 1. ELEMENTOS Y COMPUESTOS EJERCICIOS Y SOLUCIONES 4. El sistema periódico 1. Escribe la configuración electrónica de los 3 primeros elementos alcalinotérreos y explica razonadamente si estos elementos
TEMA 1. ELEMENTOS Y COMPUESTOS EJERCICIOS Y SOLUCIONES 4. El sistema periódico 1. Escribe la configuración electrónica de los 3 primeros elementos alcalinotérreos y explica razonadamente si estos elementos
Tema 2_3. Átomos Polielectronicos y Sistema Periódico
 Tema 2_3. Átomos Polielectronicos y Sistema Periódico Caso más sencillo: átomo de helio (2 electrones) ĤΨ = EΨ ^ ^ Ĥ = T + V z r 12 x atracción del núcleo (+2e) sobre el electrón 1, a una distancia r 1
Tema 2_3. Átomos Polielectronicos y Sistema Periódico Caso más sencillo: átomo de helio (2 electrones) ĤΨ = EΨ ^ ^ Ĥ = T + V z r 12 x atracción del núcleo (+2e) sobre el electrón 1, a una distancia r 1
TEMA 2.- Estructura atómica. Sistema periódico. Propiedades periódicas
 TEMA 2.- Estructura atómica. Sistema periódico. Propiedades periódicas CUESTIONES 11.- Los átomos neutros X, Y, Z tienen las siguientes configuraciones: X = 1s 2 2s 2 p 1 ; Y = 1s 2 2s 2 p 5 ; Z = 1s 2
TEMA 2.- Estructura atómica. Sistema periódico. Propiedades periódicas CUESTIONES 11.- Los átomos neutros X, Y, Z tienen las siguientes configuraciones: X = 1s 2 2s 2 p 1 ; Y = 1s 2 2s 2 p 5 ; Z = 1s 2
Clase N 1. Modelo Atómico I
 Pre-Universitario Manuel Guerrero Ceballos Clase N 1 Modelo Atómico I ICAL ATACAMA Módulo Plan Común Modelos Atómicos Teoría Atómica De Dalton Los elementos están formados por partículas extremadamente
Pre-Universitario Manuel Guerrero Ceballos Clase N 1 Modelo Atómico I ICAL ATACAMA Módulo Plan Común Modelos Atómicos Teoría Atómica De Dalton Los elementos están formados por partículas extremadamente
Unidad 1 Estructura atómica de la materia. Teoría cuántica
 Unidad 1 Estructura atómica de la materia. Teoría cuántica 1.El átomo y la constitución de la materia DALTON NO ACEPTADO POR LOS FÍSICOS que creían en la idea de que los átomos se encontraban como disueltos
Unidad 1 Estructura atómica de la materia. Teoría cuántica 1.El átomo y la constitución de la materia DALTON NO ACEPTADO POR LOS FÍSICOS que creían en la idea de que los átomos se encontraban como disueltos
ESTRUCTURA ATÓMICA Y PROPIEDADES PERIÓDICAS
 ESTRUCTURA ATÓMICA Y PROPIEDADES PERIÓDICAS 1.- Escriba la configuración electrónica de los siguientes iones o elementos: 8 O -2, 9 F - y 10 Ne, e indique el período y grupo de los elementos correspondientes.
ESTRUCTURA ATÓMICA Y PROPIEDADES PERIÓDICAS 1.- Escriba la configuración electrónica de los siguientes iones o elementos: 8 O -2, 9 F - y 10 Ne, e indique el período y grupo de los elementos correspondientes.
El resultado es el Sistema Periódico. -En el sistema periódico los elementos están colocados por orden creciente de su número atómico (Z).
 Tema 2. La Tabla periódica -Desde hace tiempo los químicos han intentado ordenar los elementos de forma que queden agrupados aquellos que tienen propiedades químicas similares El resultado es el Sistema
Tema 2. La Tabla periódica -Desde hace tiempo los químicos han intentado ordenar los elementos de forma que queden agrupados aquellos que tienen propiedades químicas similares El resultado es el Sistema
LA TABLA PERIÓDICA. 1
 LA TABLA PERIÓDICA. 1 Clasificación de Mendeleiev Clasificó lo 63 elementos conocidos utilizando el criterio de masa atómica creciente, ya que no se conocía el concepto de número atómico puesto que no
LA TABLA PERIÓDICA. 1 Clasificación de Mendeleiev Clasificó lo 63 elementos conocidos utilizando el criterio de masa atómica creciente, ya que no se conocía el concepto de número atómico puesto que no
Universidad de San Carlos de Guatemala. Facultad de Ingeniería. Escuela de Ciencias. Departamento de Química. Catedrática: Tania de León.
 Universidad de San Carlos de Guatemala. Facultad de Ingeniería. Escuela de Ciencias. Departamento de Química. Catedrática: Tania de León. Química General. Código: 0348. Primer semestre. Hoja de trabajo.
Universidad de San Carlos de Guatemala. Facultad de Ingeniería. Escuela de Ciencias. Departamento de Química. Catedrática: Tania de León. Química General. Código: 0348. Primer semestre. Hoja de trabajo.
Tema II: Estructura atómica y tabla periódica
 República Bolivariana de Venezuela Ministerio del Poder Popular para la Educación U.E. Colegio Santo Tomás de Villanueva Departamento de Ciencias Cátedra: Química Orgánica 5 Año Tema II: Estructura atómica
República Bolivariana de Venezuela Ministerio del Poder Popular para la Educación U.E. Colegio Santo Tomás de Villanueva Departamento de Ciencias Cátedra: Química Orgánica 5 Año Tema II: Estructura atómica
3.1. Estructura atómica
 3.1. Estructura atómica Átomo Protones (+) Núcleo Neutrones (sin carga) Corteza Electrones (-) *Z Número atómico = Número de protones. Cuando el átomo está en estado neutro, Z también es equivalente al
3.1. Estructura atómica Átomo Protones (+) Núcleo Neutrones (sin carga) Corteza Electrones (-) *Z Número atómico = Número de protones. Cuando el átomo está en estado neutro, Z también es equivalente al
Tabla Periódica y Propiedades Periódicas
 Tabla Periódica y Propiedades Periódicas Primeras clasificaciones periódicas. Fines S. XVIII Metales y no metales. 1829, Döbereiner Tríadas de comportamiento químico similar. A principios del siglo XIX
Tabla Periódica y Propiedades Periódicas Primeras clasificaciones periódicas. Fines S. XVIII Metales y no metales. 1829, Döbereiner Tríadas de comportamiento químico similar. A principios del siglo XIX
FÍSICA y QUÍMICA. Número cuántico Secundario (SUBNIVEL) l. Número cuántico Magnético (ORBITAL, como si fuera una caja) m.
 TEMA 1: ESTRUCTURA DE LA MATERIA. MODELOS ATÓMICOS 1. Modelo Atómico de RUTHERFORD a. Modelo predecesor de Thomson. b. Modelo atómico de Rutherford. c. Virtudes y defectos del Modelo de Rutherford. 2.
TEMA 1: ESTRUCTURA DE LA MATERIA. MODELOS ATÓMICOS 1. Modelo Atómico de RUTHERFORD a. Modelo predecesor de Thomson. b. Modelo atómico de Rutherford. c. Virtudes y defectos del Modelo de Rutherford. 2.
La tabla periódica es la estrella orientadora para la exploración en el capo de la química, la física, la mineralogía y la técnica.
 SISTEMA PERIÓDICO DE LOS ELEMENTOS La tabla periódica es la estrella orientadora para la exploración en el capo de la química, la física, la mineralogía y la técnica. Niels Bohr Principio de exclusión
SISTEMA PERIÓDICO DE LOS ELEMENTOS La tabla periódica es la estrella orientadora para la exploración en el capo de la química, la física, la mineralogía y la técnica. Niels Bohr Principio de exclusión
INTERACTIVEBOOK - Física y Química 4º ESO McGraw-Hill Education Dalton 1.2. Thomson: Descubrimiento del electrón. 1.3.
 El modelo de átomo INTERACTIVEBOOK - Física y Química 4º ESO McGraw-Hill Education INDICE 1. El modelo de átomo 1.1. Dalton 1.2. Thomson: Descubrimiento del electrón. 1.3. Rutherford: 1.3.1. Radioactividad
El modelo de átomo INTERACTIVEBOOK - Física y Química 4º ESO McGraw-Hill Education INDICE 1. El modelo de átomo 1.1. Dalton 1.2. Thomson: Descubrimiento del electrón. 1.3. Rutherford: 1.3.1. Radioactividad
Modelo Pregunta 1A a) b) Septiembre Pregunta A1.- a) b) c) d) Junio Pregunta 1A a) b) c) d) Solución. Modelo Pregunta 1B.
 Modelo 2014. Pregunta 1A.- Cuando una muestra de átomos del elemento con Z = 19 se irradia con luz ultravioleta, se produce la emisión de electrones, formándose iones con carga +1. a) Escriba la configuración
Modelo 2014. Pregunta 1A.- Cuando una muestra de átomos del elemento con Z = 19 se irradia con luz ultravioleta, se produce la emisión de electrones, formándose iones con carga +1. a) Escriba la configuración
EL MODELO ATOMICO DE BOHR
 EL MODELO ATOMICO DE BOHR En 1913, Niels Bohr ideó un modelo atómico que explica perfectamente los espectros determinados experimentalmente para átomos hidrogenoides. Estos son sistemas formados solamente
EL MODELO ATOMICO DE BOHR En 1913, Niels Bohr ideó un modelo atómico que explica perfectamente los espectros determinados experimentalmente para átomos hidrogenoides. Estos son sistemas formados solamente
PROBLEMAS RESUELTOS SELECTIVIDAD ANDALUCÍA 2002 QUÍMICA TEMA 2: LA ESTRUCTURA DEL ÁTOMO
 PROBLEMAS RESUELTOS SELECTIVIDAD ANDALUCÍA 2002 QUÍMICA TEMA 2: LA ESTRUCTURA DEL ÁTOMO Junio, Ejercicio 2, Opción A Reserva 1, Ejercicio 2, Opción A Reserva 2, Ejercicio 3, Opción B Reserva 3, Ejercicio
PROBLEMAS RESUELTOS SELECTIVIDAD ANDALUCÍA 2002 QUÍMICA TEMA 2: LA ESTRUCTURA DEL ÁTOMO Junio, Ejercicio 2, Opción A Reserva 1, Ejercicio 2, Opción A Reserva 2, Ejercicio 3, Opción B Reserva 3, Ejercicio
Como esta formada la materia?
 Como esta formada la materia? Demócrito, filósofo griego que vivió en el siglo IV a. C. propuso que, si se dividía la materia en trozos cada vez más pequeños, debería llegarse a una porción que ya no podría
Como esta formada la materia? Demócrito, filósofo griego que vivió en el siglo IV a. C. propuso que, si se dividía la materia en trozos cada vez más pequeños, debería llegarse a una porción que ya no podría
J.J Thomson propone el primer modelo de átomo:
 MODELOS ATÓMICOS. DALTON En 1808, Dalton publicó sus ideas sobre el modelo atómico de la materia las cuales han servido de base a la química moderna. Los principios fundamentales de esta teoría son: 1.
MODELOS ATÓMICOS. DALTON En 1808, Dalton publicó sus ideas sobre el modelo atómico de la materia las cuales han servido de base a la química moderna. Los principios fundamentales de esta teoría son: 1.
MATERIA MOLÉCULAS ÁTOMOS PARTÍCULAS SUBATÓMICAS. Partícula Masa (g) Carga (Coulombs) Carga unitaria. Electrón
 MATERIA MOLÉCULAS ÁTOMOS PARTÍCULAS SUBATÓMICAS Partícula Masa (g) Carga (Coulombs) Carga unitaria Electrón 9.10939 10-28 -1.6022 10-19 -1 Protón 1.67262 10-24 +1.6022 10-19 +1 Neutrón 1.67493 10-24 0
MATERIA MOLÉCULAS ÁTOMOS PARTÍCULAS SUBATÓMICAS Partícula Masa (g) Carga (Coulombs) Carga unitaria Electrón 9.10939 10-28 -1.6022 10-19 -1 Protón 1.67262 10-24 +1.6022 10-19 +1 Neutrón 1.67493 10-24 0
PRIMERAS CLASIFICACIONES PERIÓDICAS
 LA TABLA PERIÓDICA PRIMERAS CLASIFICACIONES PERIÓDICAS Cuando a principios del siglo XIX se midieron las masas atómicas de una gran cantidad de elementos, se observó que ciertas propiedades variaban periódicamente
LA TABLA PERIÓDICA PRIMERAS CLASIFICACIONES PERIÓDICAS Cuando a principios del siglo XIX se midieron las masas atómicas de una gran cantidad de elementos, se observó que ciertas propiedades variaban periódicamente
TEMA II: ESTRUCTURA INTERNA DE LA MATERIA
 TEMA II: ESTRUCTURA INTERNA DE LA MATERIA 1.- El ión Calcio tiene 18 electrones y 20 neutrones. Calcular: a) Su número de Protones. Si el ión calcio (Ca 2+ ) tiene 18 e - su número de protones es 20. b)
TEMA II: ESTRUCTURA INTERNA DE LA MATERIA 1.- El ión Calcio tiene 18 electrones y 20 neutrones. Calcular: a) Su número de Protones. Si el ión calcio (Ca 2+ ) tiene 18 e - su número de protones es 20. b)
ESTRUCTURA DEL ÁTOMO - RESUMEN
 TEMA 1 ESTRUCTURA DEL ÁTOMO - RESUMEN 1. DESCUBRIMIENTO DE LA ESTRUCTURA ATÓMICA (ideas generales) Dalton: consideraba que un átomo no podía romperse en trozos más pequeños. El primer indicio de que el
TEMA 1 ESTRUCTURA DEL ÁTOMO - RESUMEN 1. DESCUBRIMIENTO DE LA ESTRUCTURA ATÓMICA (ideas generales) Dalton: consideraba que un átomo no podía romperse en trozos más pequeños. El primer indicio de que el
Sistema Periódico de los elementos. 2º Bachillerato
 Sistema Periódico de los elementos 2º Bachillerato Índice 1. Clasificación de los elementos 2. Núcleo atómico 3. Configuración electrónica 4. La tabla periódica 5. Propiedades periódicas Tamaño y radio
Sistema Periódico de los elementos 2º Bachillerato Índice 1. Clasificación de los elementos 2. Núcleo atómico 3. Configuración electrónica 4. La tabla periódica 5. Propiedades periódicas Tamaño y radio
- Dalton: TEORIA ATÓMICA ( inicio del SIGLO XIX) - Descubrimiento del electrónjoseph John Thomson ( )
 REPASO QUÍMICA 01 - Dalton: TEORIA ATÓMICA ( inicio del SIGLO XIX) - Descubrimiento del electrónjoseph John Thomson (1856-1940) Modelo de Thompson Modelo del budín de pasas - EN 1895 WILHELM RONTGEN Descubre
REPASO QUÍMICA 01 - Dalton: TEORIA ATÓMICA ( inicio del SIGLO XIX) - Descubrimiento del electrónjoseph John Thomson (1856-1940) Modelo de Thompson Modelo del budín de pasas - EN 1895 WILHELM RONTGEN Descubre
Solucionario Cuaderno Estrategias y Ejercitación Modelo atómico de la materia II: números cuánticos y configuración electrónica
 Solucionario Cuaderno Estrategias y Ejercitación Modelo atómico de la materia II: números cuánticos y configuración electrónica Química Técnico Profesional Intensivo SCUACTC002TC83-A16V1 Ítem Alternativa
Solucionario Cuaderno Estrategias y Ejercitación Modelo atómico de la materia II: números cuánticos y configuración electrónica Química Técnico Profesional Intensivo SCUACTC002TC83-A16V1 Ítem Alternativa
TEMA 2 TEMA PROPIEDADES PERIÓDICAS DE LOS PROPIEDADES PERIÓDICAS DE ELEMENT LOS
 Tema 2 La Tabla Periódica TEMA 2 PROPIEDADES PERIÓDICAS DE LOS ELEMENTOS 1. Períodos y grupos. La clasificación de Mendeléev. 2. Periodicidad de las estructuras electrónicas. 3. Periodicidad de las propiedades
Tema 2 La Tabla Periódica TEMA 2 PROPIEDADES PERIÓDICAS DE LOS ELEMENTOS 1. Períodos y grupos. La clasificación de Mendeléev. 2. Periodicidad de las estructuras electrónicas. 3. Periodicidad de las propiedades
TEMA 4 (I) ESTRUCTURA ATÓMICA.
 Estructura Atómica, Sistema Periódico y Enlace Químico. 1 TEMA 4 (I) ESTRUCTURA ATÓMICA. 1. DESCUBRIMIENTO DE LA ESTRUCTURA ATÓMICA. 1.- Qué experimentos condujeron a la idea del núcleo atómico? (3.12)
Estructura Atómica, Sistema Periódico y Enlace Químico. 1 TEMA 4 (I) ESTRUCTURA ATÓMICA. 1. DESCUBRIMIENTO DE LA ESTRUCTURA ATÓMICA. 1.- Qué experimentos condujeron a la idea del núcleo atómico? (3.12)
PROPIEDADES PERIÓDICAS DE LOS ELEMENTOS. LA TABLA PERIÓDICA.
 PROPIEDADES PERIÓDICAS DE LOS ELEMENTOS. LA TABLA PERIÓDICA. A partir de la posición de los elementos en la tabla periódica formando grupos y períodos podemos deducir la evolución de algunas propiedades
PROPIEDADES PERIÓDICAS DE LOS ELEMENTOS. LA TABLA PERIÓDICA. A partir de la posición de los elementos en la tabla periódica formando grupos y períodos podemos deducir la evolución de algunas propiedades
Configuración electrónica y Tabla Periódica
 Configuración electrónica y Tabla Periódica El modelo mecánico-cuántico de los átomos permite responder una de la preguntas centrales de la química: por qué los elementos se comportan como lo hacen? O
Configuración electrónica y Tabla Periódica El modelo mecánico-cuántico de los átomos permite responder una de la preguntas centrales de la química: por qué los elementos se comportan como lo hacen? O
QUÍMICA LICENCIATURA DE INGENIERÍA EN ENERGÍAS RENOVABLES
 QUÍMICA LICENCIATURA DE INGENIERÍA EN ENERGÍAS RENOVABLES 2013-1 Teoría: Dra. Karina Cuentas Gallegos Martes y jueves 10-12 hrs. Laboratorio: M.C. Mirna Guevara García Jueves 12-14 hrs. Curso de Química
QUÍMICA LICENCIATURA DE INGENIERÍA EN ENERGÍAS RENOVABLES 2013-1 Teoría: Dra. Karina Cuentas Gallegos Martes y jueves 10-12 hrs. Laboratorio: M.C. Mirna Guevara García Jueves 12-14 hrs. Curso de Química
QUÍMICA FUNDAMENTAL. Tabla Periódica
 QUÍMICA FUNDAMENTAL Tabla Periódica 1 TEMAS DE ESTUDIO Construcción de la Tabla Periódica con base en la configuración electrónica Propiedades periódicas de los elementos 2 ANTECEDENTES HISTÓRICOS: ELEMENTOS
QUÍMICA FUNDAMENTAL Tabla Periódica 1 TEMAS DE ESTUDIO Construcción de la Tabla Periódica con base en la configuración electrónica Propiedades periódicas de los elementos 2 ANTECEDENTES HISTÓRICOS: ELEMENTOS
El Modelo Moderno y resultados de nuestro interés
 CLASES 3 Y 4 ESTRUCTURA ELECTRÓNICA DE LOS ELEMENTOS AL ESTADO FUNDAMENTAL. TABLA PERIÓDICA. ELECTRONEGATIVIDAD. El Modelo Moderno y resultados de nuestro interés Así es como el Modelo Moderno (MM) reemplazó
CLASES 3 Y 4 ESTRUCTURA ELECTRÓNICA DE LOS ELEMENTOS AL ESTADO FUNDAMENTAL. TABLA PERIÓDICA. ELECTRONEGATIVIDAD. El Modelo Moderno y resultados de nuestro interés Así es como el Modelo Moderno (MM) reemplazó
PARTÍCULAS FUNDAMENTALES. NÚMEROS CUÁNTICOS. PROPIEDADES PERIÓDICAS.
 PARTÍCULAS FUNDAMENTALES. NÚMEROS CUÁNTICOS. PROPIEDADES PERIÓDICAS. PARTÍCULAS FUNDAMENTALES. CONCEPTOS PREVIOS De acuerdo con lo anterior, en un átomo hay tres partículas fundamentales: protones y neutrones,
PARTÍCULAS FUNDAMENTALES. NÚMEROS CUÁNTICOS. PROPIEDADES PERIÓDICAS. PARTÍCULAS FUNDAMENTALES. CONCEPTOS PREVIOS De acuerdo con lo anterior, en un átomo hay tres partículas fundamentales: protones y neutrones,
Teoría Cuántica y la estructura electrónica de los Átomos
 EN EL INTERIOR DEL ATOMO TEMA 3 Química General e Inorgánica A Teoría Cuántica y la estructura electrónica de los Átomos 1 LO QUE SABEMOS EXTRUCTURA ATOMICA ACTUAL PARTICULA UBICACION CARGA MASA PROTON
EN EL INTERIOR DEL ATOMO TEMA 3 Química General e Inorgánica A Teoría Cuántica y la estructura electrónica de los Átomos 1 LO QUE SABEMOS EXTRUCTURA ATOMICA ACTUAL PARTICULA UBICACION CARGA MASA PROTON
Contenido. 3.- Carga nuclear efectiva y reactividad. 4.- Propiedades periódicas:
 LA TABLA PERIÓDICA Contenido Primeras clasificaciones periódicas. 1.1. Sistema periódico de Mendeleiev. 2.- La tabla periódica. 2.1. Ley de Moseley. 3.- Carga nuclear efectiva y reactividad. 4.- Propiedades
LA TABLA PERIÓDICA Contenido Primeras clasificaciones periódicas. 1.1. Sistema periódico de Mendeleiev. 2.- La tabla periódica. 2.1. Ley de Moseley. 3.- Carga nuclear efectiva y reactividad. 4.- Propiedades
PROBLEMAS RESUELTOS SELECTIVIDAD ANDALUCÍA 2014
 PROBLEMAS RESUELTOS SELECTIVIDAD ANDALUCÍA 2014 QUÍMICA TEMA 2: LA ESTRUCTURA DEL ÁTOMO Junio, Ejercicio 2, Opción A Reserva 1, Ejercicio 2, Opción A Reserva 2, Ejercicio 3, Opción B Reserva 3, Ejercicio
PROBLEMAS RESUELTOS SELECTIVIDAD ANDALUCÍA 2014 QUÍMICA TEMA 2: LA ESTRUCTURA DEL ÁTOMO Junio, Ejercicio 2, Opción A Reserva 1, Ejercicio 2, Opción A Reserva 2, Ejercicio 3, Opción B Reserva 3, Ejercicio
La Tabla Periódica de los Elementos. Propiedades períodicas atómicas.
 La Tabla Periódica de los Elementos. Propiedades períodicas atómicas. Contenidos Descubrimiento de los elementos químicos. Desarrollo de la Tabla Periódica. Tabla Periódica y configuraciones electrónicas.
La Tabla Periódica de los Elementos. Propiedades períodicas atómicas. Contenidos Descubrimiento de los elementos químicos. Desarrollo de la Tabla Periódica. Tabla Periódica y configuraciones electrónicas.
Docente: Raquel Villafrades Torres. Química General
 Propiedades Periódicas Docente: Raquel Villafrades Torres Química General UPB Introducción Las propiedades periódicas son aquellas que varían de forma regular por la posición que ocupan los elementos en
Propiedades Periódicas Docente: Raquel Villafrades Torres Química General UPB Introducción Las propiedades periódicas son aquellas que varían de forma regular por la posición que ocupan los elementos en
Configuración Electrónica
 Configuración Electrónica La configuración electrónica de un átomo indica la forma como están distribuidos los electrones entre los distintos orbitales atómicos. Según el Principio de Exclusión de Pauli,
Configuración Electrónica La configuración electrónica de un átomo indica la forma como están distribuidos los electrones entre los distintos orbitales atómicos. Según el Principio de Exclusión de Pauli,
La tabla periódica. Julius Lothar Meyer. Dimitri Ivanovich Mendeleev
 La tabla periódica Julius Lothar Meyer Dimitri Ivanovich Mendeleev Silvia Ponce López ITESM, Julio 2007 Contenidos Organización de los elementos en la tabla periódica Propiedades periódicas: radio atómico,
La tabla periódica Julius Lothar Meyer Dimitri Ivanovich Mendeleev Silvia Ponce López ITESM, Julio 2007 Contenidos Organización de los elementos en la tabla periódica Propiedades periódicas: radio atómico,
Elementos ordenados según su número atómico (Z, número de p + ) Hay 18 PERÍODOS
 TABLA PERIÓDICA Elementos ordenados según su número atómico (Z, número de p + ) Columnas Filas GRUPOS PERÍODOS Familias de elementos con propiedades comunes Hay 18 División principal Elementos representativos
TABLA PERIÓDICA Elementos ordenados según su número atómico (Z, número de p + ) Columnas Filas GRUPOS PERÍODOS Familias de elementos con propiedades comunes Hay 18 División principal Elementos representativos
UNIVERSIDAD LIBRE FACULTAD DE INGENIERÌA DEPARTAMENTO DE CIENCIAS BÁSICAS GUIA DE CLASE No 4
 UNIVERSIDAD LIBRE FACULTAD DE INGENIERÌA DEPARTAMENTO DE CIENCIAS BÁSICAS GUIA DE CLASE No 4 NOMBRE DE LA ASIGNATURA: TÍTULO: DURACIÓN: BIBLIOGRAFÍA SUGERIDA: DOCENTES: Química General La Tabla Periódica
UNIVERSIDAD LIBRE FACULTAD DE INGENIERÌA DEPARTAMENTO DE CIENCIAS BÁSICAS GUIA DE CLASE No 4 NOMBRE DE LA ASIGNATURA: TÍTULO: DURACIÓN: BIBLIOGRAFÍA SUGERIDA: DOCENTES: Química General La Tabla Periódica
PROPIEDADES PERIÓDICAS DE LOS ELEMENTOS - (2015)
 PROPIEDADES PERIÓDICAS DE LOS ELEMENTOS - (2015) Serie A - RADIOS ATOMICOS, VOLUMENES ATÓMICOS, PROPIEDADES GENERALES Serie B - ENERGÍA DE IONIZACIÓN, AFINIDAD ELECTRÓNICA y ELECTRONEGATIVIDAD: Serie A:
PROPIEDADES PERIÓDICAS DE LOS ELEMENTOS - (2015) Serie A - RADIOS ATOMICOS, VOLUMENES ATÓMICOS, PROPIEDADES GENERALES Serie B - ENERGÍA DE IONIZACIÓN, AFINIDAD ELECTRÓNICA y ELECTRONEGATIVIDAD: Serie A:
Problemario de Talleres de Estructura de la Materia. DCBI/UAM-I. Obra Colectiva del. / Revisión octubre del 2012 UNIDAD 2
 UNIDAD 2 CAPAS ELECTRÓNICAS Y TAMAÑO DE LOS ÁTOMOS, ENERGÍA DE IONIZACIÓN Y AFINIDAD ELECTRÓNICA 1.- De acuerdo al modelo atómico propuesto por la mecánica cuántica, consideras que tiene sentido hablar
UNIDAD 2 CAPAS ELECTRÓNICAS Y TAMAÑO DE LOS ÁTOMOS, ENERGÍA DE IONIZACIÓN Y AFINIDAD ELECTRÓNICA 1.- De acuerdo al modelo atómico propuesto por la mecánica cuántica, consideras que tiene sentido hablar
QUÍMICA 2º BACH. TEMA 1. ESTRUCTURA ATÓMICA.
 Modelos atómicos QUÍMICA 2º BACH. TEMA 1. ESTRUCTURA ATÓMICA. Teoría atómica de Dalton: La materia está formada por átomos indivisibles. Los átomos de un elemento son distintos de los átomos de otro elemento
Modelos atómicos QUÍMICA 2º BACH. TEMA 1. ESTRUCTURA ATÓMICA. Teoría atómica de Dalton: La materia está formada por átomos indivisibles. Los átomos de un elemento son distintos de los átomos de otro elemento
PROBLEMAS RESUELTOS SELECTIVIDAD ANDALUCÍA 2010 QUÍMICA TEMA 2: LA ESTRUCTURA DEL ÁTOMO
 PROBLEMAS RESUELTOS SELECTIVIDAD ANDALUCÍA 010 QUÍMICA TEMA : LA ESTRUCTURA DEL ÁTOMO Junio, Ejercicio 3, Opción B Reserva 1, Ejercicio, Opción B Reserva, Ejercicio, Opción A Reserva 3, Ejercicio, Opción
PROBLEMAS RESUELTOS SELECTIVIDAD ANDALUCÍA 010 QUÍMICA TEMA : LA ESTRUCTURA DEL ÁTOMO Junio, Ejercicio 3, Opción B Reserva 1, Ejercicio, Opción B Reserva, Ejercicio, Opción A Reserva 3, Ejercicio, Opción
Configuración Electrónica
 Los subniveles se ordenan según el valor de n + l Distribución de los electrones en el átomo Número Orbitales que ocupan relativa A menor valor de n + l, menor energía (más estable) Válido sólo si l 3
Los subniveles se ordenan según el valor de n + l Distribución de los electrones en el átomo Número Orbitales que ocupan relativa A menor valor de n + l, menor energía (más estable) Válido sólo si l 3
EL ÁTOMO CONTENIDOS. ANTECEDENTES HISTÓRICOS. ( ) MODELOS ATÓMICOS. RAYOS CATÓDICOS. MODELO DE THOMSON.
 EL ÁTOMO CONTENIDOS. 1.- Antecedentes históricos.( ) 2.- Partículas subatómicas. ( ) 3.- Modelo atómico de Thomsom. 4.- Los rayos X. 5.- La radiactividad. 6.- Modelo atómico de Rutherford. 7.- Radiación
EL ÁTOMO CONTENIDOS. 1.- Antecedentes históricos.( ) 2.- Partículas subatómicas. ( ) 3.- Modelo atómico de Thomsom. 4.- Los rayos X. 5.- La radiactividad. 6.- Modelo atómico de Rutherford. 7.- Radiación
2. Cuál(es) de las siguientes propiedades periódicas aumenta(n) al incrementarse el número atómico en un grupo?
 Programa Estándar Anual Nº Guía práctica Teoría atómica III: tabla periódica y propiedades periódicas Ejercicios PSU 1. En un sistema periódico muy simplificado, como el que se muestra en la figura, los
Programa Estándar Anual Nº Guía práctica Teoría atómica III: tabla periódica y propiedades periódicas Ejercicios PSU 1. En un sistema periódico muy simplificado, como el que se muestra en la figura, los
- Marie Curie. - Joseph Thomson. - Ernest Rutherford. - Max Planck. - Albert Einstein. - Niels Bohr. - Louis de Broglie. - Werner Heisenberg
 - Marie Curie - Joseph Thomson - Ernest Rutherford - Max Planck - Albert Einstein - Niels Bohr - Louis de Broglie - Werner Heisenberg - Wolfgang Pauli - Arnorld Sommerfeld Autores (Orden Alfabético): Celia
- Marie Curie - Joseph Thomson - Ernest Rutherford - Max Planck - Albert Einstein - Niels Bohr - Louis de Broglie - Werner Heisenberg - Wolfgang Pauli - Arnorld Sommerfeld Autores (Orden Alfabético): Celia
El ÁTOMO de HIDRÓGENO
 El ÁTOMO de HIDRÓGENO Dr. Andres Ozols Dra. María Rebollo FIUBA 006 Dr. A. Ozols 1 ESPECTROS DE HIDROGENO espectros de emisión espectro de absorción Dr. A. Ozols ESPECTROS DE HIDROGENO Secuencias de las
El ÁTOMO de HIDRÓGENO Dr. Andres Ozols Dra. María Rebollo FIUBA 006 Dr. A. Ozols 1 ESPECTROS DE HIDROGENO espectros de emisión espectro de absorción Dr. A. Ozols ESPECTROS DE HIDROGENO Secuencias de las
PROBLEMAS RESUELTOS DE DISTRIBUCIÓN ELECTRONICA EN NIVELES, SUBNIVELES Y ORBITALES ATÓMICOS.
 PROBLEMAS RESUELTOS DE DISTRIBUCIÓN ELECTRONICA EN NIVELES, SUBNIVELES Y ORBITALES ATÓMICOS. 1. Explique que indica el número cuántico magnético y el número cuántico de espín. Número cuántico magnético:
PROBLEMAS RESUELTOS DE DISTRIBUCIÓN ELECTRONICA EN NIVELES, SUBNIVELES Y ORBITALES ATÓMICOS. 1. Explique que indica el número cuántico magnético y el número cuántico de espín. Número cuántico magnético:
INSTITUCION EDUCATIVA DIVERSIFICADO DE CHIA CIENCIAS NATURALES: QUIMICA ESTUDIO TABLA PERIODICA. GRADO DECIMO
 1 INSTITUCION EDUCATIVA DIVERSIFICADO DE CHIA CIENCIAS NATURALES: QUIMICA ESTUDIO TABLA PERIODICA. GRADO DECIMO CONTENIDOS 1.- Primeras clasificaciones periódicas. 1.1. Sistema periódico de Mendeleiev.
1 INSTITUCION EDUCATIVA DIVERSIFICADO DE CHIA CIENCIAS NATURALES: QUIMICA ESTUDIO TABLA PERIODICA. GRADO DECIMO CONTENIDOS 1.- Primeras clasificaciones periódicas. 1.1. Sistema periódico de Mendeleiev.
ESTRUCTURA ATÓMICA - PREGUNTAS DE TEST
 ESTRUCTURA ATÓMICA - PREGUNTAS DE TEST Serie A: PARTICULAS SUBATOMICAS: Serie B- ESPECTROS: Serie C- COMPOSICION DEL ÁTOMO Serie D- ESTRUCTURA ELECTRÓNICA Serie E- ATOMO DE THOMPSON Serie F- DEFECTO DE
ESTRUCTURA ATÓMICA - PREGUNTAS DE TEST Serie A: PARTICULAS SUBATOMICAS: Serie B- ESPECTROS: Serie C- COMPOSICION DEL ÁTOMO Serie D- ESTRUCTURA ELECTRÓNICA Serie E- ATOMO DE THOMPSON Serie F- DEFECTO DE
Tema 4: Propiedades periódicas de los elementos - 1 -
 Tema 4: Propiedades periódicas de los elementos - - BIBLIOGRAFÍA: * Estructura atómica y enlace químico J. Casabó i Gispert * Química. Curso Universitario B.M. Mahan y R.J. Myers * Química General R.H.
Tema 4: Propiedades periódicas de los elementos - - BIBLIOGRAFÍA: * Estructura atómica y enlace químico J. Casabó i Gispert * Química. Curso Universitario B.M. Mahan y R.J. Myers * Química General R.H.
ies menéndez tolosa 1 Escribe la combinación o combinaciones de números cuánticos correspondientes a: a) un electrón 1s y b) un electrón 4f.
 ies menéndez tolosa Escribe la combinación o combinaciones de números cuánticos correspondientes a: a) un electrón s y un electrón 4f. a) Un electrón s Situado en el er nivel n =, como es un orbital s
ies menéndez tolosa Escribe la combinación o combinaciones de números cuánticos correspondientes a: a) un electrón s y un electrón 4f. a) Un electrón s Situado en el er nivel n =, como es un orbital s
UNIDAD 1: EL ÁTOMO Y EL SISTEMA PERIÓDICO
 UNIDAD 1: EL ÁTOMO Y EL SISTEMA PERIÓDICO 1. PRIMERAS TEORÍAS ATÓMICAS Demócrito, filósofo griego que vivió en el siglo IV a. C. propuso que, si se dividía la materia en trozos cada vez más pequeños, debería
UNIDAD 1: EL ÁTOMO Y EL SISTEMA PERIÓDICO 1. PRIMERAS TEORÍAS ATÓMICAS Demócrito, filósofo griego que vivió en el siglo IV a. C. propuso que, si se dividía la materia en trozos cada vez más pequeños, debería
En la tabla periódica los elementos se clasifican periodos y grupos o familias.
 1 Curso: 1º medio Nombre alumno: Puntaje: Fecha: ACTIVIDAD ACUMULATIVA PROPIEDADES PERIÓDICAS Recordemos que: La primera tabla periódica o sistema periódico de los elementos fue presentada por Mendeleiev
1 Curso: 1º medio Nombre alumno: Puntaje: Fecha: ACTIVIDAD ACUMULATIVA PROPIEDADES PERIÓDICAS Recordemos que: La primera tabla periódica o sistema periódico de los elementos fue presentada por Mendeleiev
Capacidad de combinación. Capacidad de combinación La última capa de electrones de un átomo, se le conoce como capa de electrones de valencia
 Capacidad de combinación Para los elementos representativos, se define que el número de electrones de valencia de un elemento es igual al de la familia a la que pertenece Y está relacionado a la manera
Capacidad de combinación Para los elementos representativos, se define que el número de electrones de valencia de un elemento es igual al de la familia a la que pertenece Y está relacionado a la manera
PROBLEMAS RESUELTOS SELECTIVIDAD ANDALUCÍA 2015 QUÍMICA TEMA 2: LA ESTRUCTURA DEL ÁTOMO
 PROBLEMAS RESUELTOS SELECTIVIDAD ANDALUCÍA 2015 QUÍMICA TEMA 2: LA ESTRUCTURA DEL ÁTOMO Junio, Ejercicio 3, Opción B Reserva 1, Ejercicio 2, Opción B Reserva 2, Ejercicio 2, Opción A Reserva 3, Ejercicio
PROBLEMAS RESUELTOS SELECTIVIDAD ANDALUCÍA 2015 QUÍMICA TEMA 2: LA ESTRUCTURA DEL ÁTOMO Junio, Ejercicio 3, Opción B Reserva 1, Ejercicio 2, Opción B Reserva 2, Ejercicio 2, Opción A Reserva 3, Ejercicio
PARTÍCULAS DEL ÁTOMO MODELOS ATÓMICOS. TEMA 7 Pág. 155 libro nuevo
 PARTÍCULAS DEL ÁTOMO MODELOS ATÓMICOS TEMA 7 Pág. 155 libro nuevo DESCUBRIMIENTO DEL ÁTOMO. PARTÍCULAS SUBATÓMICAS En la antigua Grecia ya había dos teorías sobre la materia: Teoría Atomística (siglo IV
PARTÍCULAS DEL ÁTOMO MODELOS ATÓMICOS TEMA 7 Pág. 155 libro nuevo DESCUBRIMIENTO DEL ÁTOMO. PARTÍCULAS SUBATÓMICAS En la antigua Grecia ya había dos teorías sobre la materia: Teoría Atomística (siglo IV
b) La zona externa del átomo se llama CORTEZA. y ahí es donde se mueven los ELECTRONES
 PREGUNTAS DE RESPUESTA BREVE 1. Completa las siguientes frases relativas a los átomos de los elementos: a) La parte del átomo en donde se puede considerar que se concentra toda su masa es el NÚCLEO y ahí
PREGUNTAS DE RESPUESTA BREVE 1. Completa las siguientes frases relativas a los átomos de los elementos: a) La parte del átomo en donde se puede considerar que se concentra toda su masa es el NÚCLEO y ahí
1817: Döbreiner. Triadas de elementos con propiedades semejantes. 1865: Newlands. Ley de las octavas. Ordenó 55 elementos.
 Evolución histórica de la Tabla Periódica 1817: Döbreiner. Triadas de elementos con propiedades semejantes. 1865: Newlands. Ley de las octavas. Ordenó 55 elementos. 1869: Mendeleev y Meyer: las propiedades
Evolución histórica de la Tabla Periódica 1817: Döbreiner. Triadas de elementos con propiedades semejantes. 1865: Newlands. Ley de las octavas. Ordenó 55 elementos. 1869: Mendeleev y Meyer: las propiedades
Las que tienen relación con el de tamaño: LAS PROPIEDADES PERIÓDICAS. Se pueden separar en dos grupos: PERIODICIDAD
 LAS PROPIEDADES PERIÓDICAS Se pueden separar en dos grupos: 1- Las que tienen relación con el de tamaño: Los radios atómicos y los radios iónicos o cristalinos. La densidad. (ρ) El punto de fusión y ebullición.
LAS PROPIEDADES PERIÓDICAS Se pueden separar en dos grupos: 1- Las que tienen relación con el de tamaño: Los radios atómicos y los radios iónicos o cristalinos. La densidad. (ρ) El punto de fusión y ebullición.
Respuestas del Control 1. Curso Noviembre 2008
 NOMBRE y APELLIDOS... NOTA: En los cálculos numéricos tenga en cuenta la precisión de las constantes y de las magnitudes que se dan y dé el resultado con el número de cifras significativas adecuado. La
NOMBRE y APELLIDOS... NOTA: En los cálculos numéricos tenga en cuenta la precisión de las constantes y de las magnitudes que se dan y dé el resultado con el número de cifras significativas adecuado. La
Técnico Profesional QUÍMICA
 Programa Técnico Profesional QUÍMICA Teoría atómica III: tabla periódica y propiedades periódicas Nº Ejercicios PSU 1. En la tabla periódica, los elementos están ordenados según un valor creciente de su
Programa Técnico Profesional QUÍMICA Teoría atómica III: tabla periódica y propiedades periódicas Nº Ejercicios PSU 1. En la tabla periódica, los elementos están ordenados según un valor creciente de su
TEMA 2. ESTRUCTURA ATÓMICA Y CLASIFICACIÓN PERIÓDICA DE LOS ELEMENTOS
 TEMA 2. ESTRUCTURA ATÓMICA Y CLASIFICACIÓN PERIÓDICA DE LOS ELEMENTOS E1A.S2010 Indique el máximo número de electrones de un átomo que pueden tener los siguientes números cuánticos, asigne los restantes
TEMA 2. ESTRUCTURA ATÓMICA Y CLASIFICACIÓN PERIÓDICA DE LOS ELEMENTOS E1A.S2010 Indique el máximo número de electrones de un átomo que pueden tener los siguientes números cuánticos, asigne los restantes
ENLACE QUÍMICO Y ESTRUCTURA DE LA MATERIA
 PROBLEMAS DE LA ASIGNATURA: ENLACE QUÍMICO Y ESTRUCTURA DE LA MATERIA ÁREA DE QUÍMICA INORGÁNICA 1º CURSO. LICENCIATURA EN CIENCIAS QUÍMICAS CURSO 2006/2007 PROFESOR RESPONSABLE: - Dr. Luis Sánchez Granados
PROBLEMAS DE LA ASIGNATURA: ENLACE QUÍMICO Y ESTRUCTURA DE LA MATERIA ÁREA DE QUÍMICA INORGÁNICA 1º CURSO. LICENCIATURA EN CIENCIAS QUÍMICAS CURSO 2006/2007 PROFESOR RESPONSABLE: - Dr. Luis Sánchez Granados
Los problemas y cuestiones recogidos en este trabajo han sido enviados por:
 INTRODUCCIÓN El aprendizaje de la Química constituye un reto al que se enfrentan cada año los, cada vez más escasos, estudiantes de 2 de bachillerato que eligen las opciones de Ciencias, Ciencias de la
INTRODUCCIÓN El aprendizaje de la Química constituye un reto al que se enfrentan cada año los, cada vez más escasos, estudiantes de 2 de bachillerato que eligen las opciones de Ciencias, Ciencias de la
PORTAFOLIO DE EVIDENCIAS QUÍMICA I DE SEGUNDA OPORTUNIDAD I LEE DETENIDAMENTE CADA ENUNCIADO Y CONTESTA SEGÚN SE TE PIDA.
 PORTAFOLIO DE EVIDENCIAS QUÍMICA I DE SEGUNDA OPORTUNIDAD I LEE DETENIDAMENTE CADA ENUNCIADO Y CONTESTA SEGÚN SE TE PIDA. 1.- Ciencia que estudia las características y la composición de los materiales,
PORTAFOLIO DE EVIDENCIAS QUÍMICA I DE SEGUNDA OPORTUNIDAD I LEE DETENIDAMENTE CADA ENUNCIADO Y CONTESTA SEGÚN SE TE PIDA. 1.- Ciencia que estudia las características y la composición de los materiales,
Formativa para 2da. Oportunidad de Química I. 1er. Semestre Diciembre puntos. Nombre Grupo ETAPA I
 Formativa para 2da. Oportunidad de Química I. 1er. Semestre Diciembre 2016. 40 puntos Nombre Grupo ETAPA I LA QUÍMICA Y SU CONTRIBUCIÓN AL AVANCE DE LA CIENCIA Y LA TECNOLOGÍA. Define los siguientes Conceptos:
Formativa para 2da. Oportunidad de Química I. 1er. Semestre Diciembre 2016. 40 puntos Nombre Grupo ETAPA I LA QUÍMICA Y SU CONTRIBUCIÓN AL AVANCE DE LA CIENCIA Y LA TECNOLOGÍA. Define los siguientes Conceptos:
Corteza atómica: Estructura electrónica
 Corteza atómica: Estructura electrónica Aunque los conocimientos actuales sobre la estructura electrónica de los átomos son bastante complejos, las ideas básicas son las siguientes: 1. Existen 7 niveles
Corteza atómica: Estructura electrónica Aunque los conocimientos actuales sobre la estructura electrónica de los átomos son bastante complejos, las ideas básicas son las siguientes: 1. Existen 7 niveles
Modelo atómico de la materia.
 Modelo atómico de la materia. La Teoría Atómica se basa en la suposición (ratificada después por datos experimentales) de que la materia no es continua, sino que está formada por partículas distintas.
Modelo atómico de la materia. La Teoría Atómica se basa en la suposición (ratificada después por datos experimentales) de que la materia no es continua, sino que está formada por partículas distintas.
3 - Cómo podemos diferenciar un elemento químico de un compuesto, según la teoría de Dalton?
 TEORÍA ATÓMICA 1- A partir de los siguientes datos, cuántas veces es maor la masa del protón que la del electrón? Masa del protón =1,673 10-27 kg Masa del electrón =9,1 10-31 kg 2 - El modelo del átomo
TEORÍA ATÓMICA 1- A partir de los siguientes datos, cuántas veces es maor la masa del protón que la del electrón? Masa del protón =1,673 10-27 kg Masa del electrón =9,1 10-31 kg 2 - El modelo del átomo
Tabla Periódica y Propiedades Periódicas
 Tabla Periódica y Propiedades Periódicas 1. Las configuraciones electrónicas de los elementos nitrógeno y vanadio son respectivamente: Lo primero que debemos hacer es buscar en la Tabla Periódica los números
Tabla Periódica y Propiedades Periódicas 1. Las configuraciones electrónicas de los elementos nitrógeno y vanadio son respectivamente: Lo primero que debemos hacer es buscar en la Tabla Periódica los números
LiceoTolimense Química Séptimo 1 Periodo ESTRUCTURA INTERNA DE LA MATERIA
 ESTRUCTURA INTERNA DE LA MATERIA Lectura comprensiva Desde la antigüedad los filósofos se preguntaban de qué estaban formadas las cosas que los rodeaban. Primero pensaron que la materia era continua, es
ESTRUCTURA INTERNA DE LA MATERIA Lectura comprensiva Desde la antigüedad los filósofos se preguntaban de qué estaban formadas las cosas que los rodeaban. Primero pensaron que la materia era continua, es
PROBLEMAS Y CUESTIONES DE LAS OLIMPIADAS DE QUÍMICA
 PROBLEMAS Y CUESTIONES DE LAS OLIMPIADAS DE QUÍMICA (VOLUMEN 6: ESTRUCTURA ATÓMICA Y SISTEMA PERIÓDICO) SERGIO MENARGUES FERNANDO LATRE AMPARO GÓMEZ MARZO 2016 INTRODUCCIÓN El aprendizaje de la Química
PROBLEMAS Y CUESTIONES DE LAS OLIMPIADAS DE QUÍMICA (VOLUMEN 6: ESTRUCTURA ATÓMICA Y SISTEMA PERIÓDICO) SERGIO MENARGUES FERNANDO LATRE AMPARO GÓMEZ MARZO 2016 INTRODUCCIÓN El aprendizaje de la Química
PROBLEMAS RESUELTOS SELECTIVIDAD ANDALUCÍA 2007 QUÍMICA TEMA 2: LA ESTRUCTURA DEL ÁTOMO
 PROBLEMAS RESUELTOS SELECTIVIDAD ANDALUCÍA 2007 QUÍMICA TEMA 2: LA ESTRUCTURA DEL ÁTOMO Junio, Ejercicio 2, Opción A Reserva 1, Ejercicio 2, Opción A Reserva 2, Ejercicio 2, Opción B Reserva 3, Ejercicio
PROBLEMAS RESUELTOS SELECTIVIDAD ANDALUCÍA 2007 QUÍMICA TEMA 2: LA ESTRUCTURA DEL ÁTOMO Junio, Ejercicio 2, Opción A Reserva 1, Ejercicio 2, Opción A Reserva 2, Ejercicio 2, Opción B Reserva 3, Ejercicio
1. Uno de los grandes aciertos de los postulados de Mendeleiev respecto a la ordenación de los elementos fue:
 miniprueba Clase 04 Problemas 1. Uno de los grandes aciertos de los postulados de Mendeleiev respecto a la ordenación de los elementos fue: a. Designar un lugar fijo para el hidrogeno. b. Ordenar los elementos
miniprueba Clase 04 Problemas 1. Uno de los grandes aciertos de los postulados de Mendeleiev respecto a la ordenación de los elementos fue: a. Designar un lugar fijo para el hidrogeno. b. Ordenar los elementos
SEMANA 01 Estructura Atómica y Tabla Periódica. Licda. Lilian Judith Guzmán Melgar
 SEMANA 01 Estructura Atómica y Tabla Periódica Licda. Lilian Judith Guzmán Melgar 2016 ATOMO Es la partícula mas pequeña de un elemento que mantiene sus características. John Dalton formuló la TEORIA ATOMICA
SEMANA 01 Estructura Atómica y Tabla Periódica Licda. Lilian Judith Guzmán Melgar 2016 ATOMO Es la partícula mas pequeña de un elemento que mantiene sus características. John Dalton formuló la TEORIA ATOMICA
ÁTOMO..su historia y su estudio
 ÁTOMO.su historia y su estudio LOS GRIEGOS Y SU APORTE 2000 años antes de Cristo, la civilización griega representada por varios filósofos, ya se preguntaban acerca de qué estaba formado el universo?...
ÁTOMO.su historia y su estudio LOS GRIEGOS Y SU APORTE 2000 años antes de Cristo, la civilización griega representada por varios filósofos, ya se preguntaban acerca de qué estaba formado el universo?...
Unidad 7 LA TABLA PERIÓDICA.
 Unidad 7 LA TABLA PERIÓDICA. Primeras clasificaciones REPASO periódicas. Cuando a principios del siglo XIX se midieron las masas atómicas de una gran cantidad de elementos, se observó que ciertas propiedades
Unidad 7 LA TABLA PERIÓDICA. Primeras clasificaciones REPASO periódicas. Cuando a principios del siglo XIX se midieron las masas atómicas de una gran cantidad de elementos, se observó que ciertas propiedades
Unidad II Química I PERIODICIDAD QUÍMICA Y TABLA PERIÓDICA
 Unidad II Química I PERIODICIDAD QUÍMICA Y TABLA PERIÓDICA Gloria Angélica Fuentes Zenteno 1 Índice 2.3.1 Antecedentes 2.3.2 Componentes de la Tabla Periódica Nombre Símbolo Número y Masa atómica Estructura
Unidad II Química I PERIODICIDAD QUÍMICA Y TABLA PERIÓDICA Gloria Angélica Fuentes Zenteno 1 Índice 2.3.1 Antecedentes 2.3.2 Componentes de la Tabla Periódica Nombre Símbolo Número y Masa atómica Estructura
Contenidos LA TABLA PERIÓDICA. Primeras clasificaciones periódicas. Primeras clasificaciones periódicas. Triadas de Döbereiner (1829) (Enlace Web):
 Contenidos 2 LA TABLA PERIÓDICA. Unidad 7 1 1.- Primeras clasificaciones periódicas. 1.1. Sistema periódico de Mendeleiev. 2.- La tabla periódica. 2.1. Ley de Moseley. 3.- Carga nuclear efectiva y reactividad.
Contenidos 2 LA TABLA PERIÓDICA. Unidad 7 1 1.- Primeras clasificaciones periódicas. 1.1. Sistema periódico de Mendeleiev. 2.- La tabla periódica. 2.1. Ley de Moseley. 3.- Carga nuclear efectiva y reactividad.
PLAN DE EVALUACIÓN 2015
 PLAN DE EVALUACIÓN 2015 Año: 2015 Período: I Semestre Sub-sector: Química Nivel: NM1 Curso: I Medio Profesor: Alejandra Sotomaor A. Aprendizajes Esperados Indicadores Aprendizajes Evaluados Procedimientos
PLAN DE EVALUACIÓN 2015 Año: 2015 Período: I Semestre Sub-sector: Química Nivel: NM1 Curso: I Medio Profesor: Alejandra Sotomaor A. Aprendizajes Esperados Indicadores Aprendizajes Evaluados Procedimientos
Programa de Acceso Inclusivo, Equidad y Permanencia PAIEP U. de Santiago. Química
 Modelos atómicos Los filósofos de la antigüedad especularon sobre cómo estaba formada la materia. Demócrito (460-370 a.c) y otros filósofos anteriores a él, pensaban que el mundo material debería estar
Modelos atómicos Los filósofos de la antigüedad especularon sobre cómo estaba formada la materia. Demócrito (460-370 a.c) y otros filósofos anteriores a él, pensaban que el mundo material debería estar
Guía de Estudio para 1er Parcial Temas Selectos de Química
 Guía de Estudio para 1er Parcial Temas Selectos de Química 1. Menciona que científicos ordenaron los elementos conocidos en su época en triadas (grupos de tres), en octavas, por número atómico y quien
Guía de Estudio para 1er Parcial Temas Selectos de Química 1. Menciona que científicos ordenaron los elementos conocidos en su época en triadas (grupos de tres), en octavas, por número atómico y quien
IES Menéndez Tolosa Dpto Física y Química - Tabla periódica Propiedades periódicas. 1 Los átomos neutros, X, Y Z tienen la configuración electrónica:
 IES Menéndez Tolosa Dpto Física y Química - Tabla periódica Propiedades periódicas Los átomos neutros, X, Y Z tienen la configuración electrónica: X s s p Y s s p Z s s p 3s a) Indica el grupo y período
IES Menéndez Tolosa Dpto Física y Química - Tabla periódica Propiedades periódicas Los átomos neutros, X, Y Z tienen la configuración electrónica: X s s p Y s s p Z s s p 3s a) Indica el grupo y período
