29/08/2016. Unidad II: Estructura de la materia. El Átomo: Desde la concepción filosófica hasta la teoría atómica UNIDAD 2: ESTRUCTURA DE LA MATERIA
|
|
|
- Catalina Rodríguez Rey
- hace 6 años
- Vistas:
Transcripción
1 UNIDAD 2: ESTRUCTURA DE LA MATERIA Unidad II: Estructura de la materia. Teoría atómica de Dalton Modelos atómicos. Teoría atómica moderna. El átomo. Sus partículas fundamentales. Símbolo nuclear. Números atómico y másico. Isótopos Radiactividad. Partículas radiactivas. Radiación. Rastreadores químicos. Número cuántico. Definición. Número cuántico principal. Población electrónica (2n 2 ) Número cuántico orbital (l). Valores de l y tipos de orbital (s,p,d,f) Niveles y subniveles de energía. Cantidad de electrones en cada subnivel (bloques s,p,d,f) (ml y ms) Principio de exclusión de Pauli y regla de Hund. Diagrama de orbitales Los 10 primeros elementos : Desde la concepción filosófica hasta la teoría atómica Las imágenes muestran esculturas de Aristóteles de Estágira(384 a.c. 322 a.c.) y Demócrito de Abdera (460 a.c. 370 a. C.), quienes sostenían ideas contrarias con relación a la naturaleza de la materia. Sabe Ud. que postura defendían? UNIDAD 2: ESTRUCTURA DE LA MATERIA Desde los tiempos más remotos, el ser humano ha sentido curiosidad por conocer sobre la composición del universo que le rodea. Demócrito, un filósofo de la antigüedad, al igual que su mentor Leucipo, sostenía la creencia de que existía una partícula fundamental constitutiva de la materia que se caracterizaba por ser indivisible. A esta partícula la denominó Átomo, y a esta corriente de pensamiento se le llamó atomismo. UNIDAD 2: ESTRUCTURA DE LA MATERIA Empédocles, un filósofo presocrático del siglo V a.c, había sostenido la teoría de las cuatro raíces, la cual postulaba que todas las sustancias están compuestas por una mezcla de agua, aire, tierra y fuego. Aristóteles rechazaba el atomismo. Consideraba que la materia era continua y llamó elementos a las cuatro raíces de Empédocles. UNIDAD 2: ESTRUCTURA DE LA MATERIA Las ideas de Aristóteles perduraron por más de 2000 años. No fue sino hasta el siglo XVII cuando algunos hombres de ciencia como Robert Boyle e Isaac Newton retomaron las ideas atomistas de Leucipo y Demócrito. En 1804, John Dalton, Químico, Físico y Meteorólogo inglés propuso, a partir de los descubrimientos de Antoine Lavoisier y Joseph Proust, su teoría atómica, la cual presentaba los siguientes postulados: 1
2 Teoría Atómica de Dalton 1.- Los elementos químicos están formados por partículas muy pequeñas e indivisibles llamadas átomos. 2.- Todos los átomos de un elemento químico dado son idénticos en su masa y demás propiedades. 3.- Los átomos de diferentes elementos químicos son distintos, en particular sus masas. 4.- Los átomos son indestructibles y retienen su identidad en los cambios químicos. 5.- Los compuestos se forman cuando átomos de diferentes elementos se combinan entre sí, en una relación de números enteros y sencilla, formando entidades definidas (hoy llamadas moléculas). Si hoy, a pesar de los avances tecnológicos modernos que nos permiten obtener imágenes difusas de un átomo, aun no podemos decir que es posible verlos en el sentido estricto de la palabra, hace 100 años era más difícil todavía. Foto de unos 500 átomos de Niobio y Selenio ( ryandersonn/atoms-are-real/) 8 En ciencias, un modelo es una representación abstracta de un fenómeno complicado o poco conocido, de manera que cuando es comparado con el modelo (más simple y conocido) permite darle una explicación matemática. El modelo atómico de Dalton permitía explicar las leyes ponderales de la materia, como son la de conservación de la materia, la de proporciones múltiples y la de proporciones definidas Sin embargo, la teoría de Dalton no explicaba muchos fenómenos que fueron descubiertos desde fines del siglo XVII, como eran la conductividad de los metales, las celdas electroquímicas, la formación de iones, etc. En 1904 J. J. Thompson propuso el modelo del pudín de pasas, el primero que hacía referencia a las partículas subatómicas. Este modelo explicaba los fenómenos eléctricos de la materia pero no la fosforescencia, término con el que se confundió originalmente la radiactividad. En 1911, Ernest Rutherford propuso el modelo planetario del átomo. El mismo explicaba las radiaciones, pero no la existencia de los espectros atómicos, ni las discrepancias que éste modelo presentaba con las leyes de la Física clásica. Basado en el modelo anterior, Niels Bohr propuso en 1913 el modelo de Hidrógeno, con el que pudo explicar los espectros de absorción y emisión, así como el efecto fotoeléctrico, introduciendo el concepto de nivel de energía. El modelo de Bohr sólo era aplicable al átomo de hidrógeno, pues no podía explicar la existencia de electrones con distinto contenido energético en los niveles 2 en adelante. En 1916 Arnold Sommerfeld introduce variaciones al modelo de Bohr para generalizarlo. Por ejemplo, la posibilidad de que los electrones describan no sólo órbitas circulares, sino también elípticas. Es Sommerfeld quien introduce los conceptos de subnivel, orbital y spin en la actual descripción atómica. 2
3 El modelo de la nube de electrones, fundamento de la teoría atómica moderna, fue propuesto por Erwin Schrödinger y Werner Heinsenberg en Este modelo sustituye la noción de órbitas electrónicas precisas por la de regiones en el espacio donde con mayor probabilidad puede encontrarse un electrón (orbital). Este modelo se expresa matemáticamente mediante una compleja ecuación presentada más adelante, cuya solución denominada función de onda, mide la probabilidad de encontrar un electrón en el espacio. Cronología de la teoría atómica actual 1803: Dalton propone la primera teoría atómica. 1861: Maxwell desarrolla la teoría electromagnética 1896: Roentgen descubre la existencia de unos rayos de naturaleza desconocida (rayos X). 1896: Becquerel descubre la naturaleza radioactiva del uranio. 1897: J. J. Thompson descubre la existencia del electrón, y en 1904 propone el modelo del pudín de pasas. 1898: Los esposos Pierre y Marie Curie descubren el carácter radioactivo del Torio y el Uranio, así como los elementos Radio y Polonio. Cronología de la teoría atómica actual 1909: Millikan determina la carga del electrón. 1911: Rutherford prueba la existencia del protón. Corrige además el modelo de Thompson. 1913: Bohr propone el modelo del átomo de hidrógeno, corregido en 1916 por Summerfeld. 1926: Schrodinger y Heinsenberg proponen el modelo de la nube de electrones, base de la teoría atómica moderna. 1932: James Chadwick descubre la existencia del neutrón. El átomo es la partícula más pequeña de un elemento que aun mantiene las propiedades de ese elemento. Los átomos poseen un núcleo compuesto por protones y neutrones, y una nube electrónica formada por electrones. A los protones y neutrones se les llama nucleones, por estar localizados en el núcleo. Normalmente los átomos son eléctricamente neutros. El número de protones es único, constante y universal. Por ello, El número atómico (Z) se define como la cantidad de protones en el núcleo de todos los átomos de un elemento dado. El número de masa (A) se define como la suma de protones y neutrones en el núcleo de un tipo de átomos de un elemento dado
4 El símbolo nuclear de un elemento es una forma concisa de presentar el símbolo y los números de masa y atómico de un elemento. La diferencia entre los números de masa y atómico nos da el número de neutrones en el núcleo Contrario a la idea de Dalton, no todos los átomos de un elemento son idénticos. Los isótopos son átomos de un mismo elemento que poseen igual número de protones en el núcleo, pero diferente número de neutrones. Debido a que el número de masa varía entre los isótopos de un mismo elemento, la masa atómica se define como el promedio de los números de masa de todos los isótopos de un elemento. Generalmente este valor es muy influenciado por el número de masa del isótopo conocido más abundante en el universo. Radiactividad En 1896, mientras Henri Becquerel investigaba la fluorescencia de ciertos materiales, notó que unas sales de uranio con las que trabajaba, habían arruinado una película fotográfica guardada junto a ellas. Esto condujo a una estudiante doctoral de Becquerel Marie Curie y a su esposo Pierre, al descubrimiento de unos rayos y partículas que emiten algunos átomos cuyos núcleos son inestables. Esta emisión natural o artificial se conoce como radiactividad. La radiactividad consiste en la emisión de partículas alfa (α)(núcleos de Helio), beta (β)(electrones) y rayos gamma (γ). Radiactividad 4
5 Los Radioisótopos son isótopos radiactivos de un elemento. Por ejemplo, el 3 H es un isótopo radiactivo del 1 H. Las aplicaciones de los radioisótopos se basan en que un isótopo radiactivo es, desde el punto de vista físico y químico, exactamente igual a su isótopo no radiactivo y se comporta de la misma forma en cualquier proceso físico o químico en el cual participe. La ventaja es que se trata de un átomo marcado y puede ser seguido en todas sus reacciones químicas y/o biológicas gracias a las radiaciones que emite. Teniendo en cuenta estas características de los radioisótopos, se pueden emplear para tres aplicaciones: Como fuente de energía. En investigaciones científicas. En aplicaciones médicas. Aplicaciones como fuentes de energía En las Centrales nucleares se obtienen grandes cantidades de energía aprovechando la fisión de ciertos isótopos. Los isótopos más empleados en estas centrales son el uranio-235 y el plutonio-239. Otra de las formas de aprovechamiento de la energía nuclear, es en la fabricación de pilas de muy larga duración. Uno de los isótopos más empleados es el plutonio-238. Estas pilas se colocan en lugares de difícil acceso o que no pueden ser cambiadas con frecuencia, como por ejemplo: en marcapasos, en estaciones marítimas o en sondas espaciales. Aplicaciones en Investigación científica Los elementos, tal como se encuentran en la naturaleza, son una mezcla de isótopos. La masa atómica que aparece en la tabla periódica es el promedio de todas las masas isotópicas naturales, de ahí que no sean números enteros. Los isótopos se utilizan como rastreadores o marcadores, para saber en qué se transforma exactamente una sustancia en una reacción química. Por ejemplo, si tomamos un vaso de agua con sal (NaCl) que contenga al isótopo sodio-24, podemos observar que el sodio tarda sólo 75 segundos en llegar a la superficie de nuestra piel, por transpiración. Aplicaciones médicas Para diagnosticar algunas enfermedades se introduce en los enfermos una sustancia que contiene un isótopo radiactivo que emita radiación con poca energía. La sustancia se fija en el órgano que se desea estudiar y, así, se puede observar, por la radiación que emite. Por ejemplo, el tecnecio-99 se emplea en el diagnóstico de enfermedades óseas. Para ello se suministra con compuestos de fósforo que se fijan en los huesos. Para curar ciertos tipos de cáncer. Debido a que el cáncer hace que algunas células se reproduzcan rápidamente, los radioisótopos atacan a este proceso de reproducción celular. En esto consiste la radioterapia. Por ejemplo, el cobalto-60 y el yodo -131 son de los radioisótopos más empleados en la terapia contra el cáncer. 5
6 La solución de la ecuación de onda de Schrödinger da origen a cuatro tipos de valores llamados números cuánticos. Estos números constituyen la mejor forma de describir los electrones en un átomo. Los electrones orbitan alrededor del núcleo atómico en regiones denominadas niveles o capas de energía. El número cuántico principal (n) indica el número de nivel en el que se encuentra un electrón. Los niveles se identifican mediante números enteros positivos desde n = 1 para el nivel más cercano al núcleo, hasta n = 7 para el más alejado. El número máximo de electrones que puede haber en un nivel determinado viene dado por la expresión 2n 2, donde n es el número de nivel. 31 Los niveles de energía se dividen en subniveles. El número cuántico azimutal o del momento angular (l) indica el número de subnivel. Existen 4 tipos de subniveles, y entre n=1 y n=4 cada nivel tiene tantos subniveles como el número de nivel que le corresponde. Entre n=5 y n=7 el número de subniveles decrece desde 4 hasta 2. Los tipos de subnivel se representan mediante las letras s, p, d y f, y a éstas se les asignan los valores 0, 1, 2, y 3 respectivamente. Así como los niveles se subdividen en subniveles, éstos de dividen a su vez en orbitales. El número cuántico magnético (ml) o simplemente (m), llamado también orbital, se define como la posición más probable en la que podemos encontrar un electrón en un átomo. Cada tipo de subnivel tiene un número fijo de orbitales, así, un subnivel de tipo s posee un orbital; uno p posee tres, uno d posee cinco y uno f posee siete. 6
7 Los orbitales pertenecientes a un mismo subnivel se diferencian entre si mediante valores que son asignados a todos los orbitales del subnivel. Estos valores van desde (-l) hasta (+l) pasando por cero. Cada orbital es lo suficientemente grande para acomodar no más de dos electrones, los cuales deberán diferir, como veremos a continuación, en el valor del próximo número cuántico. El último número cuántico se denomina número cuántico de espín, (ms) o simplemente (s). Este indica la orientación del giro o rotación de los electrones dentro de un mismo orbital, y sólo puede tener dos valores posibles: ±½. Dos electrones en un mismo orbital sólo pueden coexistir si poseen distintos valores de espín, y se les denomina electrones apareados. La configuración electrónica es una descripción abreviada de la distribución de los electrones alrededor de los núcleos atómicos de un elemento utilizando los números cuánticos de esos electrones. La configuración se rige según el diagrama de Moeller, y se basa en una serie de reglas y principios que gobiernan la distribución electrónica, los cuales se mencionan a continuación: 7
8 El Principio de Incertidumbre de Heinsenberg: Es imposible saber exactamente dónde y a qué velocidad se mueve un electrón. La Regla de Hund: Al llenar orbitales de igual energía (los tres orbitales p, los cinco d, o los siete f) los electrones se distribuyen, siempre que sea posible, con sus espines paralelos, es decir, separados. El Principio de Exclusión de Pauli: Es imposible que dos átomos tengan el mismo grupo de números cuánticos. Provea la configuración electrónica de los elementos cuyos números atómicos son Z=6 y Z=16. Determine la identidad del elemento cuya configuración electrónica es 1s 2, 2s 2, 2p 4 Determine la configuración electrónica del Escandio (Z=21) Debido al solapamiento que ocurre entre los subniveles a partir del tercer nivel, necesitamos un recurso que nos permita determinar, en la mayoría de los casos, la configuración electrónica de un elemento con gran fiabilidad. Este recurso se conoce como el diagrama de Moeller Ejercicios Propuestos: Provea la configuración electrónica de los elementos cuyos números atómicos son Z=13, Z=33 y Z=53 Determine la configuración electrónica de los elementos con los primeros 10 valores de Z en la tabla periódica Determine la identidad del elemento cuya configuración electrónica aparece a continuación: 1s 2, 2s 2, 2p 6, 3s 2, 3p 6, 4s 2, 3d 10, 4p 6, 5s 2 45 Seleccione 2 elementos que pertenezcan a un mismo grupo o columna (1-2, 13-18) en la tabla periódica y encuentre su configuración electrónica. Existe alguna similitud en las configuraciones? De ser así, Cuál es o Cuáles son? Seleccione 2 elementos que pertenezcan a un mismo período o fila en la tabla periódica y encuentre su configuración electrónica. Existe alguna similitud en las configuraciones? De ser así, Cuál es o cuáles son? Determine la identidad de los elementos siguientes a partir de los 4 números cuánticos del último electrón de valencia de c/u de ellos: n=3, l=0, ml=0, ms=+½ n=5, l=1,ml=-1, ms=-½ N=5, l=2, ml=-2, ms=+½ FIN DE LA PRESENTACIÓN 8
LA ESTRUCTURA DEL ÁTOMO
 LA ESTRUCTURA DEL ÁTOMO 1 1.- EL ÁTOMO EN LA ANTIGÜEDAD Los filósofos griegos discutieron mucho acerca de la naturaleza de la materia y concluyeron que el mundo era más simple de lo que parecía. Algunas
LA ESTRUCTURA DEL ÁTOMO 1 1.- EL ÁTOMO EN LA ANTIGÜEDAD Los filósofos griegos discutieron mucho acerca de la naturaleza de la materia y concluyeron que el mundo era más simple de lo que parecía. Algunas
TEMA 7: ELEMENTOS Y COMPUESTOS
 TEMA 7: ELEMENTOS Y COMPUESTOS FÍSICA Y QUÍMICA 4º ESO IES ZOCO LAS PARTÍCULAS DEL ÁTOMO MODELO ATÓMICO DE DALTON Cada elemento químico se compone de partículas diminutas e indestructibles denominadas
TEMA 7: ELEMENTOS Y COMPUESTOS FÍSICA Y QUÍMICA 4º ESO IES ZOCO LAS PARTÍCULAS DEL ÁTOMO MODELO ATÓMICO DE DALTON Cada elemento químico se compone de partículas diminutas e indestructibles denominadas
Un modelo atómico, por lo tanto consiste en representar de manera grafica, la dimensión atómica de la materia. El objetivo de estos modelos es que el
 Modelos atómicos Debido a que no se podían ver los átomos los científicos crearon modelos para describirlos, éstos fueron evolucionando a lo largo de la historia a medida que se descubrieron nuevas cosas.
Modelos atómicos Debido a que no se podían ver los átomos los científicos crearon modelos para describirlos, éstos fueron evolucionando a lo largo de la historia a medida que se descubrieron nuevas cosas.
EXTRUCTURA ATOMICA ACTUAL
 ATOMOS Y ELEMENTOS TEMA 4 Química ATOMOS EXTRUCTURA ATOMICA ACTUAL PARTICULA UBICACION CARGA MASA PROTON NUCLEO + SI NEUTRON NUCLEO 0 SI ELECTRON ORBITAS - DESPRECIABLE La masa del átomo reside en el núcleo.
ATOMOS Y ELEMENTOS TEMA 4 Química ATOMOS EXTRUCTURA ATOMICA ACTUAL PARTICULA UBICACION CARGA MASA PROTON NUCLEO + SI NEUTRON NUCLEO 0 SI ELECTRON ORBITAS - DESPRECIABLE La masa del átomo reside en el núcleo.
FÍSICA Y QUÍMICA. TEMA 4: ESTRUCTURA DE LA MATERIA. https://www.youtube.com/watch?v=vkjfd4al1d8
 FÍSICA Y QUÍMICA. TEMA 4: ESTRUCTURA DE LA MATERIA https://www.youtube.com/watch?v=vkjfd4al1d8 1. TEORÍAS ATÓMICAS A lo largo de la historia han ido surgiendo diversas teorías y modelos para explicar la
FÍSICA Y QUÍMICA. TEMA 4: ESTRUCTURA DE LA MATERIA https://www.youtube.com/watch?v=vkjfd4al1d8 1. TEORÍAS ATÓMICAS A lo largo de la historia han ido surgiendo diversas teorías y modelos para explicar la
A. Lavoisier (mediciones de masas reaccionantes): la materia no se crea ni se destruye
 Características esenciales de las reacciones químicas A. Lavoisier (mediciones de masas reaccionantes): la materia no se crea ni se destruye Joseph Louis Proust (formación de CuCO 3 ): los elementos que
Características esenciales de las reacciones químicas A. Lavoisier (mediciones de masas reaccionantes): la materia no se crea ni se destruye Joseph Louis Proust (formación de CuCO 3 ): los elementos que
ESTRUCTURA DE LA MATERIA
 ESTRUCTURA DE LA MATERIA 1. Naturaleza de la materia (el átomo). 2. Modelos atómicos clásicos. 3. Modelo mecánico cuántico. 4. Mecánica ondulatoria de Schrödinger. 5. Números cuánticos. 6. Orbitales atómicos.
ESTRUCTURA DE LA MATERIA 1. Naturaleza de la materia (el átomo). 2. Modelos atómicos clásicos. 3. Modelo mecánico cuántico. 4. Mecánica ondulatoria de Schrödinger. 5. Números cuánticos. 6. Orbitales atómicos.
EL ÁTOMO. Departamento de Física y Química 3º ESO
 EL ÁTOMO Departamento de Física y Química 3º ESO 0. Mapa conceptual Metales No metales Tabla periódica Elementos Cationes Isótopos ÁTOMO Iones Aniones Protones Núcleo Neutrones Electrones Número atómico
EL ÁTOMO Departamento de Física y Química 3º ESO 0. Mapa conceptual Metales No metales Tabla periódica Elementos Cationes Isótopos ÁTOMO Iones Aniones Protones Núcleo Neutrones Electrones Número atómico
Tema 3 El Átomo. Modelos Atómicos y Configuraciones Electrónicas
 Física y Química 1º Bachillerato LOMCE FyQ 1 IES de Castuera Bloque 2 Aspectos Cuantitativos de la Química 2015 2016 Unidad Didáctica 3 Rev 01 El Átomo. Modelos Atómicos y Configuraciones Electrónicas
Física y Química 1º Bachillerato LOMCE FyQ 1 IES de Castuera Bloque 2 Aspectos Cuantitativos de la Química 2015 2016 Unidad Didáctica 3 Rev 01 El Átomo. Modelos Atómicos y Configuraciones Electrónicas
Demócrito. Modelo de Dalton. Modelo atómico de Thomson
 modelo atómico Demócrito Fue probablemente el primero en creer que la materia estaba constituida por partículas que denomino átomos, palabra que significa sin división, ya que consideraba el átomo como
modelo atómico Demócrito Fue probablemente el primero en creer que la materia estaba constituida por partículas que denomino átomos, palabra que significa sin división, ya que consideraba el átomo como
BLOQUE III Explicas el modelo atómico actual y sus aplicaciones
 Explicas el modelo atómico actual y sus aplicaciones Qué es un modelo atómico? Representación estructural de un átomo, cuyo fin es explicar sus propiedades y funcionamiento. Demócrito y Leucipo (Siglo
Explicas el modelo atómico actual y sus aplicaciones Qué es un modelo atómico? Representación estructural de un átomo, cuyo fin es explicar sus propiedades y funcionamiento. Demócrito y Leucipo (Siglo
Originales de. Primera Temporada. Capitulo 3 de 5
 Originales de +18 Capitulo 3 de 5 Primera Temporada Estructura Atómica. Historia de los modelos atómicos. Tabla Periódica. Estructura general de la tabla periódica Ing. Sergio Luppo 1 Teoría Atómica Siglo
Originales de +18 Capitulo 3 de 5 Primera Temporada Estructura Atómica. Historia de los modelos atómicos. Tabla Periódica. Estructura general de la tabla periódica Ing. Sergio Luppo 1 Teoría Atómica Siglo
M. Eugenia Villaseca R. Licenciada y Profesora de Biología PUCV
 M. Eugenia Villaseca R. Licenciada y Profesora de Biología PUCV Comprender la utilidad de los modelos atómicos y de la teoría atómica para explicar los procesos de transformación físico-química de la materia
M. Eugenia Villaseca R. Licenciada y Profesora de Biología PUCV Comprender la utilidad de los modelos atómicos y de la teoría atómica para explicar los procesos de transformación físico-química de la materia
Unidad I: El átomo; al interior de la materia
 Los misterios del átomo Unidad I: El átomo; al interior de la materia En la antigua Grecia se discutía si la materia podía ser dividida y subdividida indefinidamente hasta llegar a un punto en donde ya
Los misterios del átomo Unidad I: El átomo; al interior de la materia En la antigua Grecia se discutía si la materia podía ser dividida y subdividida indefinidamente hasta llegar a un punto en donde ya
Origen del Concepto Átomo MODELOS ATÓMICOS. Teoría o Modelo Atómico de Dalton (1808) Qué es un modelo en Ciencias?
 MODELOS ATÓMICOS Origen del Concepto Átomo Demócrito: Siglo IV (A.C.) Fundador de la Escuela Atomista los átomos son indivisibles (átomo), y se distinguen por forma, tamaño, orden y posición. Los átomos
MODELOS ATÓMICOS Origen del Concepto Átomo Demócrito: Siglo IV (A.C.) Fundador de la Escuela Atomista los átomos son indivisibles (átomo), y se distinguen por forma, tamaño, orden y posición. Los átomos
25 12 Mg. 1. En la especie el numero atómico corresponde a: A) 22 B) 12 C) 25 D) 13 E) ninguna de las anteriores.
 MINIPRUEBA CLASE 02 25 12 Mg 1. En la especie el numero atómico corresponde a: A) 22 B) 12 C) 25 D) 13 E) ninguna de las anteriores. 25 12 Mg Z 2. Se puede afirmar que: I) La masa del electrón es aproximadamente
MINIPRUEBA CLASE 02 25 12 Mg 1. En la especie el numero atómico corresponde a: A) 22 B) 12 C) 25 D) 13 E) ninguna de las anteriores. 25 12 Mg Z 2. Se puede afirmar que: I) La masa del electrón es aproximadamente
La Teoría atómica de Dalton se resume en los siguientes enunciados:
 1. EL ÁTOMO. Hasta ahora hemos estudiado cómo se presenta la materia y cómo se clasifica pero hay todavía muchas preguntas sin responder: cuál es la naturaleza de la materia?, cómo es por dentro?, Existe
1. EL ÁTOMO. Hasta ahora hemos estudiado cómo se presenta la materia y cómo se clasifica pero hay todavía muchas preguntas sin responder: cuál es la naturaleza de la materia?, cómo es por dentro?, Existe
Unidad II 2.1 Estructura del átomo
 Unidad II 2.1 Estructura del átomo Química general I Alfonso Rito Norma López 1 El átomo en la antigüedad Demócrito introdujo el concepto de átomo, como la constitución de la materia por partículas indivisibles.
Unidad II 2.1 Estructura del átomo Química general I Alfonso Rito Norma López 1 El átomo en la antigüedad Demócrito introdujo el concepto de átomo, como la constitución de la materia por partículas indivisibles.
Modelos atómicos. JOHN DALTON: Modelo atómico en forma de esfera
 M1 Modelos atómicos JOHN DALTON: Modelo atómico en forma de esfera Muchos años después de que se planteó la existencia de los átomos y que éstos eran la parte fundamental de todo lo que fuera materia,
M1 Modelos atómicos JOHN DALTON: Modelo atómico en forma de esfera Muchos años después de que se planteó la existencia de los átomos y que éstos eran la parte fundamental de todo lo que fuera materia,
Teoría atómica I: Modelos atómicos, estructura atómica y tipos de átomos. Teoría atómica II: Números cuánticos y configuración electrónica
 TEORÍA ATÓMICA Teoría atómica I: Modelos atómicos, estructura atómica y tipos de átomos Teoría atómica II: Números cuánticos y configuración electrónica Aprendizajes esperados Diferenciar los distintos
TEORÍA ATÓMICA Teoría atómica I: Modelos atómicos, estructura atómica y tipos de átomos Teoría atómica II: Números cuánticos y configuración electrónica Aprendizajes esperados Diferenciar los distintos
Estructura electrónica de los átomos
 Estructura electrónica de los átomos Partículas subatómicas Protón (p) 1,673 10-27 Kg + 1,602 10-19 C Goldstein (1886) Electrón (e) 9,109 10-31 Kg - 1,602 10-19 C Thomson (1897) Neutrón (n) 1,673 10-27
Estructura electrónica de los átomos Partículas subatómicas Protón (p) 1,673 10-27 Kg + 1,602 10-19 C Goldstein (1886) Electrón (e) 9,109 10-31 Kg - 1,602 10-19 C Thomson (1897) Neutrón (n) 1,673 10-27
La estructura atómica: el núcleo
 Tema 1 La estructura atómica: el núcleo Introducción. Modelos atómicos Composición del átomo. Partículas fundamentales Estructura del núcleo Estabilidad nuclear y energía de enlace nuclear Aplicaciones
Tema 1 La estructura atómica: el núcleo Introducción. Modelos atómicos Composición del átomo. Partículas fundamentales Estructura del núcleo Estabilidad nuclear y energía de enlace nuclear Aplicaciones
INTERACTIVEBOOK - Física y Química 4º ESO McGraw-Hill Education Dalton 1.2. Thomson: Descubrimiento del electrón. 1.3.
 El modelo de átomo INTERACTIVEBOOK - Física y Química 4º ESO McGraw-Hill Education INDICE 1. El modelo de átomo 1.1. Dalton 1.2. Thomson: Descubrimiento del electrón. 1.3. Rutherford: 1.3.1. Radioactividad
El modelo de átomo INTERACTIVEBOOK - Física y Química 4º ESO McGraw-Hill Education INDICE 1. El modelo de átomo 1.1. Dalton 1.2. Thomson: Descubrimiento del electrón. 1.3. Rutherford: 1.3.1. Radioactividad
Técnico Profesional QUÍMICA
 Convenio Programa Técnico Profesional QUÍMICA Modelos atómicos, estructura atómica y tipos de átomos Nº Ejercicios PSU 1. Rutherford, luego de realizar pruebas con una lámina de oro bombardeada por partículas
Convenio Programa Técnico Profesional QUÍMICA Modelos atómicos, estructura atómica y tipos de átomos Nº Ejercicios PSU 1. Rutherford, luego de realizar pruebas con una lámina de oro bombardeada por partículas
Prof. Jorge Rojo Carrascosa
 QUIMICA ESTRUCTURAL II Un átomo está constituido por un núcleo donde se encuentran los protones y los neutrones y rodeando al núcleo, se encuentran los electrones. La masa de los protones es 1000 veces
QUIMICA ESTRUCTURAL II Un átomo está constituido por un núcleo donde se encuentran los protones y los neutrones y rodeando al núcleo, se encuentran los electrones. La masa de los protones es 1000 veces
QUÍMICA I. TEMA 2: Estructura atómica. Tecnólogo Minero. E s q u e m a d e l a C l a s e
 QUÍMICA I TEMA 2: Estructura atómica Tecnólogo Minero E s q u e m a d e l a C l a s e Tema 2: Estructura atómica El átomo. Partículas atómicas. Número atómico, número másico. Isótopos. Estructura electrónica.
QUÍMICA I TEMA 2: Estructura atómica Tecnólogo Minero E s q u e m a d e l a C l a s e Tema 2: Estructura atómica El átomo. Partículas atómicas. Número atómico, número másico. Isótopos. Estructura electrónica.
ESTRUCTURA DE LA MATERIA VICENTE PUCHADES PUCHADES. SERVICIO DE RADIOFÍSICA Y PROTECCIÓN RADIOLÓGICA DEL HGU SANTA LUCÍA. CARTAGENA.
 ESTRUCTURA DE LA MATERIA VICENTE PUCHADES PUCHADES. SERVICIO DE RADIOFÍSICA Y PROTECCIÓN RADIOLÓGICA DEL HGU SANTA LUCÍA. CARTAGENA. INDICE Qué es la materia? Modelos de la materia Fuerzas Fundamentales
ESTRUCTURA DE LA MATERIA VICENTE PUCHADES PUCHADES. SERVICIO DE RADIOFÍSICA Y PROTECCIÓN RADIOLÓGICA DEL HGU SANTA LUCÍA. CARTAGENA. INDICE Qué es la materia? Modelos de la materia Fuerzas Fundamentales
TEORIA ATOMICA Y TABLA PERIODICA Licda. Lilian Judith Guzmán Melgar
 TEORIA ATOMICA Y TABLA PERIODICA Licda. Lilian Judith Guzmán Melgar 1 2019 ATOMO Es la partícula mas pequeña de un elemento que mantiene sus características. John Dalton formuló la TEORIA ATOMICA que propone:
TEORIA ATOMICA Y TABLA PERIODICA Licda. Lilian Judith Guzmán Melgar 1 2019 ATOMO Es la partícula mas pequeña de un elemento que mantiene sus características. John Dalton formuló la TEORIA ATOMICA que propone:
COMPLEJO EDUCACIONAL JOAQUIN EDWARDS BELLO PRUEBA REFORZAMIENTO 1 MEDIO EXAMENES LIBRES
 COMPLEJO EDUCACIONAL JOAQUIN EDWARDS BELLO PRUEBA REFORZAMIENTO 1 MEDIO EXAMENES LIBRES ASIGNATURA: UNIDAD: OBJETIVO (S): CONTENIDO (S): QUIMICA I - II Reconocer las partículas que componen el átomo. MODELO
COMPLEJO EDUCACIONAL JOAQUIN EDWARDS BELLO PRUEBA REFORZAMIENTO 1 MEDIO EXAMENES LIBRES ASIGNATURA: UNIDAD: OBJETIVO (S): CONTENIDO (S): QUIMICA I - II Reconocer las partículas que componen el átomo. MODELO
UNIDAD 1 LA ENERGÍA, LA MATERIA Y SUS CAMBIOS. 1.3 El sol, horno nuclear
 UNIDAD 1 LA ENERGÍA, LA MATERIA Y SUS CAMBIOS 1.3 El sol, horno nuclear RADIACTIVIDAD Y DESINTEGRACIÓN NUCLEAR HISTORIA DEL ÁTOMO Hace aproximadamente 2500 años, los filósofos griegos, afirmaron que la
UNIDAD 1 LA ENERGÍA, LA MATERIA Y SUS CAMBIOS 1.3 El sol, horno nuclear RADIACTIVIDAD Y DESINTEGRACIÓN NUCLEAR HISTORIA DEL ÁTOMO Hace aproximadamente 2500 años, los filósofos griegos, afirmaron que la
Nacimiento de las teorías. Nacimiento de las teorías. Introducción
 Introducción De qué esta formada cada una de las cosas que nos rodea? Por ejemplo: Podrías predecir de que están elaborados los objetos y sustancias representadas? Los tres objetos están compuesto de lo
Introducción De qué esta formada cada una de las cosas que nos rodea? Por ejemplo: Podrías predecir de que están elaborados los objetos y sustancias representadas? Los tres objetos están compuesto de lo
LA ESTRUCTURA ATÓMICA
 LA ESTRUCTURA ATÓMICA M en C Alicia Cea Bonilla 1 Teoría Atómica En 1808, John Dalton estableció las hipótesis sobre las que fundó su teoría atómica: a) Los elementos están formados por partículas pequeñas
LA ESTRUCTURA ATÓMICA M en C Alicia Cea Bonilla 1 Teoría Atómica En 1808, John Dalton estableció las hipótesis sobre las que fundó su teoría atómica: a) Los elementos están formados por partículas pequeñas
PROFESORES / TUTORES. Ignacio Torres Morales Medicina 2do año Catalina Gutiérrez Derecho 2do año
 QUIMICA COMUN PROFESORES / TUTORES Ignacio Torres Morales Medicina 2do año itorresm@udd.cl Catalina Gutiérrez Derecho 2do año cagutierreze@udd.cl MODELOS ATÓMICOS IDEAS GENERALES ANTECEDENTES Se establece
QUIMICA COMUN PROFESORES / TUTORES Ignacio Torres Morales Medicina 2do año itorresm@udd.cl Catalina Gutiérrez Derecho 2do año cagutierreze@udd.cl MODELOS ATÓMICOS IDEAS GENERALES ANTECEDENTES Se establece
Átomo. Posee protones y neutrones. Estos se llaman Nucleones. Alrededor giran los electrones en. forma de nube. Son eléctricamente neutro
 Átomo Posee protones y neutrones Estos se llaman Nucleones Alrededor giran los electrones en forma de nube Son eléctricamente neutro Por eso Z(número de Protones)=Ne(Número de Electrones) Átomo Su dimensión
Átomo Posee protones y neutrones Estos se llaman Nucleones Alrededor giran los electrones en forma de nube Son eléctricamente neutro Por eso Z(número de Protones)=Ne(Número de Electrones) Átomo Su dimensión
COLEGIO PERSONALIZADO PENSAMIENTO GUIA DE QUÌMICA GRADO 7 PERIODO 1 / 2017 Nombre grado. El átomo es la unidad o partícula más pequeña de un elemento.
 COLEGIO PERSONALIZADO PENSAMIENTO GUIA DE QUÌMICA GRADO 7 PERIODO 1 / 2017 Nombre grado El átomo es la unidad o partícula más pequeña de un elemento. Los filósofos griegos discutieron mucho sobre la naturaleza
COLEGIO PERSONALIZADO PENSAMIENTO GUIA DE QUÌMICA GRADO 7 PERIODO 1 / 2017 Nombre grado El átomo es la unidad o partícula más pequeña de un elemento. Los filósofos griegos discutieron mucho sobre la naturaleza
Tema 12. ESTRUCTURA DEL ÁTOMO. 1º Bachillerato Física y Química Santa María del Carmen Alicante
 Tema 12. ESTRUCTURA DEL ÁTOMO 1º Bachillerato Física y Química Santa María del Carmen Alicante 1. Los modelos atómicos DEMÓCRITO s Va.d.C. DALTON 1808 THOMSON 1904 RUTHERFORD 1911 BORH 1913 SOMMERFELD
Tema 12. ESTRUCTURA DEL ÁTOMO 1º Bachillerato Física y Química Santa María del Carmen Alicante 1. Los modelos atómicos DEMÓCRITO s Va.d.C. DALTON 1808 THOMSON 1904 RUTHERFORD 1911 BORH 1913 SOMMERFELD
Teoría atómica de Dalton (1803)
 EL ÁTOMO DIVISIBLE El átomo Desde los tiempos de la antigua Grecia,los pensadores se preguntaban cómo estaba constituida la materia en su interior? Demócrito (S.V a.c.) introduce el término de átomo como
EL ÁTOMO DIVISIBLE El átomo Desde los tiempos de la antigua Grecia,los pensadores se preguntaban cómo estaba constituida la materia en su interior? Demócrito (S.V a.c.) introduce el término de átomo como
ÁTOMO..su historia y su estudio
 ÁTOMO.su historia y su estudio LOS GRIEGOS Y SU APORTE 2000 años antes de Cristo, la civilización griega representada por varios filósofos, ya se preguntaban acerca de qué estaba formado el universo?...
ÁTOMO.su historia y su estudio LOS GRIEGOS Y SU APORTE 2000 años antes de Cristo, la civilización griega representada por varios filósofos, ya se preguntaban acerca de qué estaba formado el universo?...
Teoría atómica I: Modelos atómicos, estructura atómica y tipos de átomos
 PPTCANCBQMA03006V3 Clase Teoría atómica I: Modelos atómicos, estructura atómica y tipos de átomos Profesor: Nicolás Guzmán Las especies neutras tienen igual número de A) protones. B) neutrones. C) electrones.
PPTCANCBQMA03006V3 Clase Teoría atómica I: Modelos atómicos, estructura atómica y tipos de átomos Profesor: Nicolás Guzmán Las especies neutras tienen igual número de A) protones. B) neutrones. C) electrones.
Línea de tiempo: Modelos Atómicos
 Línea de tiempo: Modelos Atómicos Modelo de Thomson 1904 Budín de pasas Demócrito (450 a. c) Teoría Atómica de Dalton1808 Modelo de Rutherford 1911 Modelo Atómico de Bohr1913 Fuente de energía V o Q Bohr
Línea de tiempo: Modelos Atómicos Modelo de Thomson 1904 Budín de pasas Demócrito (450 a. c) Teoría Atómica de Dalton1808 Modelo de Rutherford 1911 Modelo Atómico de Bohr1913 Fuente de energía V o Q Bohr
Modelo de Thomson. Finalmente, el n 0 de protones = n 0 electrones.
 Se tuvo que esperar a los siglos XVI-XVII para poderse romper con la tradición alquimista, estableciéndose las bases del método científico y desapareciendo el hermetismo de los escritos, comunicándose
Se tuvo que esperar a los siglos XVI-XVII para poderse romper con la tradición alquimista, estableciéndose las bases del método científico y desapareciendo el hermetismo de los escritos, comunicándose
RECAPITULACIÓN. Planteado por John Dalton. Replantear unidad básica de la materia Átomo. Cada elemento se compone de un átomo en particular.
 QUIMICA COMUN RECAPITULACIÓN RECAPITULACIÓN Planteado por John Dalton. Replantear unidad básica de la materia Átomo. Cada elemento se compone de un átomo en particular. Los átomos se relacionan en proporciones
QUIMICA COMUN RECAPITULACIÓN RECAPITULACIÓN Planteado por John Dalton. Replantear unidad básica de la materia Átomo. Cada elemento se compone de un átomo en particular. Los átomos se relacionan en proporciones
2.- Los átomos de un mismo elemento son iguales en masa y propiedades. Y los átomos de elementos diferentes son diferentes en masa y propiedades.
 FICHA 1 TEMA 3: ESTRUCTURA DE LA MATERIA PRIMEROS MODELOS ATÓMICOS La discusión sobre la continuidad o discontinuidad de la materia viene desde muy antiguo. Ya en la antigua Grecia había varias corrientes
FICHA 1 TEMA 3: ESTRUCTURA DE LA MATERIA PRIMEROS MODELOS ATÓMICOS La discusión sobre la continuidad o discontinuidad de la materia viene desde muy antiguo. Ya en la antigua Grecia había varias corrientes
EL ÁTOMO CONTENIDOS. ANTECEDENTES HISTÓRICOS. ( ) MODELOS ATÓMICOS. RAYOS CATÓDICOS. MODELO DE THOMSON.
 EL ÁTOMO CONTENIDOS. 1.- Antecedentes históricos.( ) 2.- Partículas subatómicas. ( ) 3.- Modelo atómico de Thomsom. 4.- Los rayos X. 5.- La radiactividad. 6.- Modelo atómico de Rutherford. 7.- Radiación
EL ÁTOMO CONTENIDOS. 1.- Antecedentes históricos.( ) 2.- Partículas subatómicas. ( ) 3.- Modelo atómico de Thomsom. 4.- Los rayos X. 5.- La radiactividad. 6.- Modelo atómico de Rutherford. 7.- Radiación
LOS ÁTOMOS. En una reacción química, la masa total de los reactivos es igual a la masa total de las sustancias obtenidas tras el proceso.
 LOS ÁTOMOS 1. LEYES PONDERALES. MODELO ATÓMICO DE DALTON Se denominan leyes ponderales de las reacciones químicas aquellas que establecen las proporciones de los pesos en cualquier proceso químico. Son
LOS ÁTOMOS 1. LEYES PONDERALES. MODELO ATÓMICO DE DALTON Se denominan leyes ponderales de las reacciones químicas aquellas que establecen las proporciones de los pesos en cualquier proceso químico. Son
PARTÍCULAS DEL ÁTOMO MODELOS ATÓMICOS. TEMA 7 Pág. 155 libro nuevo Pág. 137 libro viejo
 PARTÍCULAS DEL ÁTOMO MODELOS ATÓMICOS TEMA 7 Pág. 155 libro nuevo Pág. 137 libro viejo DESCUBRIMIENTO DEL ÁTOMO. PARTÍCULAS SUBATÓMICAS En la antigua Grecia ya había dos teorías sobre la materia: Teoría
PARTÍCULAS DEL ÁTOMO MODELOS ATÓMICOS TEMA 7 Pág. 155 libro nuevo Pág. 137 libro viejo DESCUBRIMIENTO DEL ÁTOMO. PARTÍCULAS SUBATÓMICAS En la antigua Grecia ya había dos teorías sobre la materia: Teoría
GUIA TEÓRICA NÚMEROS CUÁNTICOS
 UNIVERSIDAD NACIONAL EXPERIMENTAL POLITECNICA ANTONIO JOSE DE SUCRE VICE RECTORADO PUERTO ORDAZ DEPARTAMENTO DE ESTUDIOS GENERALES SECCIÓN DE QUÍMICA Asignatura: QUÍMICA I GUIA TEÓRICA NÚMEROS CUÁNTICOS
UNIVERSIDAD NACIONAL EXPERIMENTAL POLITECNICA ANTONIO JOSE DE SUCRE VICE RECTORADO PUERTO ORDAZ DEPARTAMENTO DE ESTUDIOS GENERALES SECCIÓN DE QUÍMICA Asignatura: QUÍMICA I GUIA TEÓRICA NÚMEROS CUÁNTICOS
EL ÁTOMO 1. El átomo. 2. Modelos atómicos. 3. Núcleo atómico. 4. Espectros atómicos. 5. Modelo atómico cuántico.
 EL ÁTOMO 1. El átomo. 2. Modelos atómicos. 3. Núcleo atómico. 4. Espectros atómicos. 5. Modelo atómico cuántico. Química 1º bachillerato El átomo 1 El átomo no es una partícula indivisible, sino que está
EL ÁTOMO 1. El átomo. 2. Modelos atómicos. 3. Núcleo atómico. 4. Espectros atómicos. 5. Modelo atómico cuántico. Química 1º bachillerato El átomo 1 El átomo no es una partícula indivisible, sino que está
Integrantes :Natalia Castillo Carolina Cabello Laura Otálora Nicolás Osorio Asignatura : Química Curso : 2º año B
 Integrantes :Natalia Castillo Carolina Cabello Laura Otálora Nicolás Osorio Asignatura : Química Curso : 2º año B * Historia del Átomo: -El átomo en la antigüedad (pág. 3) -Leucipo y Demócrito (pág.4)
Integrantes :Natalia Castillo Carolina Cabello Laura Otálora Nicolás Osorio Asignatura : Química Curso : 2º año B * Historia del Átomo: -El átomo en la antigüedad (pág. 3) -Leucipo y Demócrito (pág.4)
PARTÍCULAS DEL ÁTOMO MODELOS ATÓMICOS. TEMA 7 Pág. 155 libro nuevo
 PARTÍCULAS DEL ÁTOMO MODELOS ATÓMICOS TEMA 7 Pág. 155 libro nuevo DESCUBRIMIENTO DEL ÁTOMO. PARTÍCULAS SUBATÓMICAS En la antigua Grecia ya había dos teorías sobre la materia: Teoría Atomística (siglo IV
PARTÍCULAS DEL ÁTOMO MODELOS ATÓMICOS TEMA 7 Pág. 155 libro nuevo DESCUBRIMIENTO DEL ÁTOMO. PARTÍCULAS SUBATÓMICAS En la antigua Grecia ya había dos teorías sobre la materia: Teoría Atomística (siglo IV
Clase N 1. Modelo Atómico I
 Pre-Universitario Manuel Guerrero Ceballos Clase N 1 Modelo Atómico I ICAL ATACAMA Módulo Plan Común Modelos Atómicos Teoría Atómica De Dalton Los elementos están formados por partículas extremadamente
Pre-Universitario Manuel Guerrero Ceballos Clase N 1 Modelo Atómico I ICAL ATACAMA Módulo Plan Común Modelos Atómicos Teoría Atómica De Dalton Los elementos están formados por partículas extremadamente
ESTRUCTURA ATOMICA DESARROLLO HISTORICO
 ESTRUCTURA ATOMICA DESARROLLO HISTORICO MODELOS ATOMICOS Átomo: Partícula más pequeña de un elemento que retiene sus propiedades. DEMOCRITO Y LEUCIPO. En el Siglo V A.C. dos Filósofos Griegos Leucipo y
ESTRUCTURA ATOMICA DESARROLLO HISTORICO MODELOS ATOMICOS Átomo: Partícula más pequeña de un elemento que retiene sus propiedades. DEMOCRITO Y LEUCIPO. En el Siglo V A.C. dos Filósofos Griegos Leucipo y
ESTRUCTURA DE LA MATERIA Y SISTEMA PERIÓDICO. Lola Castelao
 ESTRUCTURA DE LA MATERIA Y SISTEMA PERIÓDICO DALTON: el átomo es indivisible. MODELOS ATÓMICOS THOMSON: el átomo es una especie de pudín, formado por una masa cargada positivamente, dentro del cual se
ESTRUCTURA DE LA MATERIA Y SISTEMA PERIÓDICO DALTON: el átomo es indivisible. MODELOS ATÓMICOS THOMSON: el átomo es una especie de pudín, formado por una masa cargada positivamente, dentro del cual se
Estudio del átomo: 1. Átomos e isótopos 2. Modelos Atómicos 3. Teoría cuántica. Ing. Sol de María Jiménez González
 Estudio del átomo: 1. Átomos e isótopos 2. Modelos Atómicos 3. Teoría cuántica 1 Núcleo: protones y neutrones Los electrones se mueven alrededor. Característica Partículas Protón Neutrón Electrón Símbolo
Estudio del átomo: 1. Átomos e isótopos 2. Modelos Atómicos 3. Teoría cuántica 1 Núcleo: protones y neutrones Los electrones se mueven alrededor. Característica Partículas Protón Neutrón Electrón Símbolo
Capitulo 2 Los átomos y los elementos
 Capitulo 2 Los átomos y los elementos MODELOS ATOMICOS Modelo de Dalton Modelo de Thomson Modelo de Rutherford Modelo de Bohr La imagen del átomo expuesta por Dalton en su teoría atómica, para explicar
Capitulo 2 Los átomos y los elementos MODELOS ATOMICOS Modelo de Dalton Modelo de Thomson Modelo de Rutherford Modelo de Bohr La imagen del átomo expuesta por Dalton en su teoría atómica, para explicar
PREPARACIÓN PSU TEORÍA ATÓMICA PROF. ÁNGELA GAJARDO S. QUÍMICA ELECTIVO IV MEDIO 2016
 PREPARACIÓN PSU TEORÍA ATÓMICA PROF. ÁNGELA GAJARDO S. QUÍMICA ELECTIVO IV MEDIO 2016 I. ESTRUCTURA ATÓMICA 1.1 PARTÍCULAS SUBATÓMICAS Partícula subatómica Símbolo Carga fundamental (Q) Carga relativa
PREPARACIÓN PSU TEORÍA ATÓMICA PROF. ÁNGELA GAJARDO S. QUÍMICA ELECTIVO IV MEDIO 2016 I. ESTRUCTURA ATÓMICA 1.1 PARTÍCULAS SUBATÓMICAS Partícula subatómica Símbolo Carga fundamental (Q) Carga relativa
Surgió alrededor de 1925, como resultados de los trabajos realizados por diversos investigadores. Este modelo nos permite explicar la composición del
 Introducción al modelo mecano cuántico Surgió alrededor de 1925, como resultados de los trabajos realizados por diversos investigadores. Este modelo nos permite explicar la composición del átomo y algunos
Introducción al modelo mecano cuántico Surgió alrededor de 1925, como resultados de los trabajos realizados por diversos investigadores. Este modelo nos permite explicar la composición del átomo y algunos
La teoría atómica de Dalton (1808)
 EL ÁTOMO Evolución de los modelos atómicos, partículas atómicas, masa y número atómico, mol, elementos e isótopos, modelo atómico contemporáneo, números cuánticos, principio de aufbau, principio de Pauli,
EL ÁTOMO Evolución de los modelos atómicos, partículas atómicas, masa y número atómico, mol, elementos e isótopos, modelo atómico contemporáneo, números cuánticos, principio de aufbau, principio de Pauli,
LiceoTolimense Química Séptimo 1 Periodo ESTRUCTURA INTERNA DE LA MATERIA
 ESTRUCTURA INTERNA DE LA MATERIA Lectura comprensiva Desde la antigüedad los filósofos se preguntaban de qué estaban formadas las cosas que los rodeaban. Primero pensaron que la materia era continua, es
ESTRUCTURA INTERNA DE LA MATERIA Lectura comprensiva Desde la antigüedad los filósofos se preguntaban de qué estaban formadas las cosas que los rodeaban. Primero pensaron que la materia era continua, es
GUIA EJERCICIOS PSU TEORIA ATOMICA, NUMEROS CUANTICOS Y CONFIGURACION EDITORIAL SM
 GUIA EJERCICIOS PSU TEORIA ATOMICA, NUMEROS CUANTICOS Y CONFIGURACION EDITORIAL SM 1. Según el modelo mecanocuántico, dónde se pueden encontrar los electrones? A. En una posición definida en un momento
GUIA EJERCICIOS PSU TEORIA ATOMICA, NUMEROS CUANTICOS Y CONFIGURACION EDITORIAL SM 1. Según el modelo mecanocuántico, dónde se pueden encontrar los electrones? A. En una posición definida en un momento
Modelo Mecano Cuántico. Taller PSU Química 2018.
 Modelo Mecano Cuántico. Taller PSU Química 2018. Contenidos Mínimos Obligatorios Descripción básica de la Cuantización de la energía, organización y comportamiento de los electrones del átomo, utilizando
Modelo Mecano Cuántico. Taller PSU Química 2018. Contenidos Mínimos Obligatorios Descripción básica de la Cuantización de la energía, organización y comportamiento de los electrones del átomo, utilizando
LA TEORIA ATOMICA John Dalton
 LA TEORIA ATOMICA En 1808, un científico inglés, el profesor John Dalton, formuló una definición precisa de las unidades indivisibles con las que está formada la materia y que llamamos átomos 1766-1844
LA TEORIA ATOMICA En 1808, un científico inglés, el profesor John Dalton, formuló una definición precisa de las unidades indivisibles con las que está formada la materia y que llamamos átomos 1766-1844
SEMANA 01 Estructura Atómica y Tabla Periódica. Licda. Lilian Judith Guzmán Melgar
 SEMANA 01 Estructura Atómica y Tabla Periódica Licda. Lilian Judith Guzmán Melgar 2016 ATOMO Es la partícula mas pequeña de un elemento que mantiene sus características. John Dalton formuló la TEORIA ATOMICA
SEMANA 01 Estructura Atómica y Tabla Periódica Licda. Lilian Judith Guzmán Melgar 2016 ATOMO Es la partícula mas pequeña de un elemento que mantiene sus características. John Dalton formuló la TEORIA ATOMICA
NUCLEO ~ m NUCLEÓN ~ m. MATERIA ~ 10-9 m. ÁTOMO ~ m. Átomo. Protón
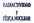 La materia está formada por átomos y moléculas que se unen para formar los sólidos. Cada átomo está compuesto de un núcleo con carga positiva y electrones que orbitan a su alrededor. El núcleo, a su vez,
La materia está formada por átomos y moléculas que se unen para formar los sólidos. Cada átomo está compuesto de un núcleo con carga positiva y electrones que orbitan a su alrededor. El núcleo, a su vez,
MODELOS ATÓMICOS. Obj. de la clase: Entender los modelos atómicos como un proceso de avance en la ciencia.
 MODELOS ATÓMICOS Obj. de la clase: Entender los modelos atómicos como un proceso de avance en la ciencia. MODELOS ATÓMICOS MODELO DE THOMSON, BUDÍN DE PASAS Modelo de fácil interpretación, pero carente
MODELOS ATÓMICOS Obj. de la clase: Entender los modelos atómicos como un proceso de avance en la ciencia. MODELOS ATÓMICOS MODELO DE THOMSON, BUDÍN DE PASAS Modelo de fácil interpretación, pero carente
Modelo atómico de la materia.
 Modelo atómico de la materia. La Teoría Atómica se basa en la suposición (ratificada después por datos experimentales) de que la materia no es continua, sino que está formada por partículas distintas.
Modelo atómico de la materia. La Teoría Atómica se basa en la suposición (ratificada después por datos experimentales) de que la materia no es continua, sino que está formada por partículas distintas.
cuestionario ASIGNATURA: QUIMICA PERIODO: 3 DOCENTE: LIC. DIEGO JAIMES FECHA: ESTUDIANTE: GRADO: 9
 cuestionario ASIGNATURA: QUIMICA PERIODO: 3 DOCENTE: LIC. DIEGO JAIMES FECHA: ESTUDIANTE: GRADO: 9 El siguiente esquema representa parte de la información que contiene la tabla periódica la corriente eléctrica.
cuestionario ASIGNATURA: QUIMICA PERIODO: 3 DOCENTE: LIC. DIEGO JAIMES FECHA: ESTUDIANTE: GRADO: 9 El siguiente esquema representa parte de la información que contiene la tabla periódica la corriente eléctrica.
02/06/2014. Química Plan Común
 Química Plan Común Limitaciones del Modelo Atómico de Rutherford Según el modelo atómico de Rutherford, los electrones se mueven en órbitas circulares y tienen una aceleración normal. Pero según los principios
Química Plan Común Limitaciones del Modelo Atómico de Rutherford Según el modelo atómico de Rutherford, los electrones se mueven en órbitas circulares y tienen una aceleración normal. Pero según los principios
Modelo atómico de Thomson
 Modelo atómico de Dalton. Ésta es la primera teoría científica que considera que la materia está dividida en átomos Modelo atómico de Thomson Introduce la idea de que el átomo puede dividirse en las llamadas
Modelo atómico de Dalton. Ésta es la primera teoría científica que considera que la materia está dividida en átomos Modelo atómico de Thomson Introduce la idea de que el átomo puede dividirse en las llamadas
Universidad de San Carlos de Guatemala. Facultad de Ingeniería. Escuela de Ciencias. Departamento de Química. Catedrática: Tania de León.
 Universidad de San Carlos de Guatemala. Facultad de Ingeniería. Escuela de Ciencias. Departamento de Química. Catedrática: Tania de León. Química General. Código: 0348. Primer semestre. Hoja de trabajo.
Universidad de San Carlos de Guatemala. Facultad de Ingeniería. Escuela de Ciencias. Departamento de Química. Catedrática: Tania de León. Química General. Código: 0348. Primer semestre. Hoja de trabajo.
ESTRUCTURA ATÓMICA DE LA MATERIA UNIDAD 2
 ESTRUCTURA ATÓMICA DE LA MATERIA UNIDAD 2 Qué ocurriría si dividiéramos un trozo de materia muchas veces? Llegaríamos hasta una parte indivisible o podríamos seguir dividiendo sin parar? Se establecieron
ESTRUCTURA ATÓMICA DE LA MATERIA UNIDAD 2 Qué ocurriría si dividiéramos un trozo de materia muchas veces? Llegaríamos hasta una parte indivisible o podríamos seguir dividiendo sin parar? Se establecieron
3 Estructura atómica de la materia
 3 Estructura atómica de la materia 1 Las leyes fundamentales de la química onservación de la masa y proporciones definidas uando hacemos reaccionar dos elementos químicos para formar un compuesto, se cumplen
3 Estructura atómica de la materia 1 Las leyes fundamentales de la química onservación de la masa y proporciones definidas uando hacemos reaccionar dos elementos químicos para formar un compuesto, se cumplen
24/02/2008. Aristóteles (384 a 322 A. C.) impone la teoría de los cuatro elementos: la llamó Ατομοσ (átomo)
 BREVE HISTORIA DE LA ESTRUCTURA DEL ÁTOMO Aristóteles (384 a 322 A. C.) impone la teoría de los cuatro elementos: Demócrito (Tracia, 460-357 ac.), propuso que, si se dividía la materia en trozos cada vez
BREVE HISTORIA DE LA ESTRUCTURA DEL ÁTOMO Aristóteles (384 a 322 A. C.) impone la teoría de los cuatro elementos: Demócrito (Tracia, 460-357 ac.), propuso que, si se dividía la materia en trozos cada vez
ESTRUCTURA ATÓMICA. 1. Modelos atómicos clásicos.
 1. Modelos atómicos clásicos. ESTRUCTURA ATÓMICA. En la antigua Grecia dos concepciones compitieron por dar una interpretación racional a cómo estaba formada la materia. Demócrito consideraba que la materia
1. Modelos atómicos clásicos. ESTRUCTURA ATÓMICA. En la antigua Grecia dos concepciones compitieron por dar una interpretación racional a cómo estaba formada la materia. Demócrito consideraba que la materia
1. Cuál de los siguientes pares de especies químicas son isoelectrónicas? a) Ne y Ar b) F - y Cl - c) Ne y F -
 E S T R U C T U R A A T Ó M I C A 1. Cuál de los siguientes pares de especies químicas son isoelectrónicas? a) Ne y Ar b) F - y Cl - c) Ne y F - 2. El número atómico de un elemento viene dado por: a) El
E S T R U C T U R A A T Ó M I C A 1. Cuál de los siguientes pares de especies químicas son isoelectrónicas? a) Ne y Ar b) F - y Cl - c) Ne y F - 2. El número atómico de un elemento viene dado por: a) El
Estructura íntima de la materia
 Estructura íntima de la materia El átomo clásico José Mauricio Rodas Rodríguez Curso de Química Inorgánica Licenciatura en Biología y Química Universidad de Caldas 22 de junio de 2015 1 / J.M. Rodas www.maurorodas.com
Estructura íntima de la materia El átomo clásico José Mauricio Rodas Rodríguez Curso de Química Inorgánica Licenciatura en Biología y Química Universidad de Caldas 22 de junio de 2015 1 / J.M. Rodas www.maurorodas.com
UNIDAD 1: PRINCIPIOS DE LA QUÍMICA
 UNIDAD 1: PRINCIPIOS DE LA QUÍMICA MODELO ATOMICO DE DALTON RAYOS CATÓDICOS (Thomsom) EL ELECTRÓN MODELO ATÓMICO DE THOMSOM RAYOS CANALES (Goldstein) EL PROTÓN Rutherford MODELO ATÓMICO DE RUTHERFORD Chadwick:
UNIDAD 1: PRINCIPIOS DE LA QUÍMICA MODELO ATOMICO DE DALTON RAYOS CATÓDICOS (Thomsom) EL ELECTRÓN MODELO ATÓMICO DE THOMSOM RAYOS CANALES (Goldstein) EL PROTÓN Rutherford MODELO ATÓMICO DE RUTHERFORD Chadwick:
- Dalton: TEORIA ATÓMICA ( inicio del SIGLO XIX) - Descubrimiento del electrónjoseph John Thomson ( )
 REPASO QUÍMICA 01 - Dalton: TEORIA ATÓMICA ( inicio del SIGLO XIX) - Descubrimiento del electrónjoseph John Thomson (1856-1940) Modelo de Thompson Modelo del budín de pasas - EN 1895 WILHELM RONTGEN Descubre
REPASO QUÍMICA 01 - Dalton: TEORIA ATÓMICA ( inicio del SIGLO XIX) - Descubrimiento del electrónjoseph John Thomson (1856-1940) Modelo de Thompson Modelo del budín de pasas - EN 1895 WILHELM RONTGEN Descubre
MODELO MECANO CUÁNTICO
 MODELO MECANO CUÁNTICO Primer Año A o Medio monica.ibanez@lbvm.cl Los átomos y su historia Obj. De hoy: 1. Recordar los modelos anteriores a la teoría a Cuántica. 2. Identificar las partículas subatómicas
MODELO MECANO CUÁNTICO Primer Año A o Medio monica.ibanez@lbvm.cl Los átomos y su historia Obj. De hoy: 1. Recordar los modelos anteriores a la teoría a Cuántica. 2. Identificar las partículas subatómicas
Atomos, Moléculas e Iones
 Atomo Atomos, Moléculas e Iones Basado en Capítulo 2 de Química (Chang, 2010) Dr. Hernández Castillo Grecia Demócrito Filosofía Química??? Materialismo monista atomos significaba indivisible Teoría Atómica
Atomo Atomos, Moléculas e Iones Basado en Capítulo 2 de Química (Chang, 2010) Dr. Hernández Castillo Grecia Demócrito Filosofía Química??? Materialismo monista atomos significaba indivisible Teoría Atómica
Atomos, Moléculas e Iones. Basado en Capítulo 2 de Química (Chang, 2010) Dr. Hernández Castillo
 Atomos, Moléculas e Iones Basado en Capítulo 2 de Química (Chang, 2010) Dr. Hernández Castillo Atomo Grecia Demócrito Filosofía Química??? Materialismo monista atomos significaba indivisible Teoría Atómica
Atomos, Moléculas e Iones Basado en Capítulo 2 de Química (Chang, 2010) Dr. Hernández Castillo Atomo Grecia Demócrito Filosofía Química??? Materialismo monista atomos significaba indivisible Teoría Atómica
Colegio Pasionista de Quilpué Departamento de Ciencias Ciencias Naturales 8 año básico 2015 Miss. Cecilia Rojas Olguín. El átomo.
 Colegio Pasionista de Quilpué Departamento de Ciencias Ciencias Naturales 8 año básico 2015 Miss. Cecilia Rojas Olguín El átomo 06 de Marzo 2015 Objetivos de la clase Comprender el Modelo corpuscular de
Colegio Pasionista de Quilpué Departamento de Ciencias Ciencias Naturales 8 año básico 2015 Miss. Cecilia Rojas Olguín El átomo 06 de Marzo 2015 Objetivos de la clase Comprender el Modelo corpuscular de
Con posterioridad el físico alemán Sommerfeld introdujo en el modelo la posibilidad de órbitas elípticas. Köningsberg, Munich, 1951
 4. El paso de una órbita a otra supone la absorción o emisión de radiación. El átomo sólo absorberá o emitirá la radiación justa para pasar de una órbita a otra. Las órbitas de los electrones son estables
4. El paso de una órbita a otra supone la absorción o emisión de radiación. El átomo sólo absorberá o emitirá la radiación justa para pasar de una órbita a otra. Las órbitas de los electrones son estables
MODELOS ATÓMICOS. Demócrito
 MODELOS ATÓMICOS Demócrito En enseñaban la teoría de que todas las cosas materiales del mundo que nos rodea estaban formadas por partículas pequeñas e indivisibles a las que llamó átomo (del griego: a=no,
MODELOS ATÓMICOS Demócrito En enseñaban la teoría de que todas las cosas materiales del mundo que nos rodea estaban formadas por partículas pequeñas e indivisibles a las que llamó átomo (del griego: a=no,
UNIDAD 2. Tema 2.1 Estructura del átomo. Partículas subatómicas. Número atómico, masa atómica, número de masa. Isótopos.
 UNIDAD 2 Tema 2.1 Estructura del átomo. Partículas subatómicas. Número atómico, masa atómica, número de masa. Isótopos. 1 Teoría atómica de la materia Demócrito (460-370 a.c.): el mundo material está formado
UNIDAD 2 Tema 2.1 Estructura del átomo. Partículas subatómicas. Número atómico, masa atómica, número de masa. Isótopos. 1 Teoría atómica de la materia Demócrito (460-370 a.c.): el mundo material está formado
PROPÓSITOS ASIGNATURA: GRADO: BLOQUE SABERES DECLARATIVOS. Química I. Primer Semestre. I. Estructura electrónica de los átomos.
 ASIGNATURA: Química I GRADO: Primer Semestre BLOQUE SABERES DECLARATIVOS PROPÓSITOS I. Estructura electrónica de los átomos. Define los conceptos de número atómico, masa atómica, número de masa e isótopo.
ASIGNATURA: Química I GRADO: Primer Semestre BLOQUE SABERES DECLARATIVOS PROPÓSITOS I. Estructura electrónica de los átomos. Define los conceptos de número atómico, masa atómica, número de masa e isótopo.
1 o Bachillerato. II. QUÍMICA Estructura de la Materia. Prof. Jorge Rojo Carrascosa
 FÍSICA Y QUÍMICA 1 o Bachillerato I. FÍSICA II. QUÍMICA Estructura de la Materia Prof. Jorge Rojo Carrascosa Índice general 1. ESTRUCTURA DE LA MATERIA 2 1.1. PARTÍCULAS SUBATÓMICAS.....................
FÍSICA Y QUÍMICA 1 o Bachillerato I. FÍSICA II. QUÍMICA Estructura de la Materia Prof. Jorge Rojo Carrascosa Índice general 1. ESTRUCTURA DE LA MATERIA 2 1.1. PARTÍCULAS SUBATÓMICAS.....................
Si nosotros observamos a nuestro alrededor podríamos predecir de qué esta formada cada una de las cosas que nos rodea?
 Introducción Si nosotros observamos a nuestro alrededor podríamos predecir de qué esta formada cada una de las cosas que nos rodea? Por ejemplo: Podrías predecir de que están elaborados los objetos y sustancias
Introducción Si nosotros observamos a nuestro alrededor podríamos predecir de qué esta formada cada una de las cosas que nos rodea? Por ejemplo: Podrías predecir de que están elaborados los objetos y sustancias
LOS ÁTOMOS Y LA ELECTRICIDAD (Ciencias Intermedia)
 LOS ÁTOMOS Y LA ELECTRICIDAD (Ciencias Intermedia) PROFESORA GILDA DIAZ MAT H AND S C I ENCE PAR T NERSHIP FOR T HE 21S T CENTURY ELEMENTARY AND MIDDLE S C HOOL MSP -21 ACADEMIA DE VERANO 7 DE JUNIO DE
LOS ÁTOMOS Y LA ELECTRICIDAD (Ciencias Intermedia) PROFESORA GILDA DIAZ MAT H AND S C I ENCE PAR T NERSHIP FOR T HE 21S T CENTURY ELEMENTARY AND MIDDLE S C HOOL MSP -21 ACADEMIA DE VERANO 7 DE JUNIO DE
Elemento Neutrones Protones Electrones
 PROBLEMAS DE ÁTOMOS 1. Argumenta cómo se explica la ley de conservación de la masa en las reacciones químicas mediante su teoría atómica de Dalton. Calcula cuánto carbono se necesita para reaccionar exactamente
PROBLEMAS DE ÁTOMOS 1. Argumenta cómo se explica la ley de conservación de la masa en las reacciones químicas mediante su teoría atómica de Dalton. Calcula cuánto carbono se necesita para reaccionar exactamente
QUIMICA Unidad N 3 : - ESTRUCTURA ATÓMICA
 QUIMICA Unidad N 3 : - ESTRUCTURA ATÓMICA Niels BOHR John DALTON 1 Profesora Mercedes Caratini - QUIMICA- ET 28 REPÚBLICA FRANCESA MODELO ATÓMICO ACTUAL El modelo atómico actual se construye a partir de
QUIMICA Unidad N 3 : - ESTRUCTURA ATÓMICA Niels BOHR John DALTON 1 Profesora Mercedes Caratini - QUIMICA- ET 28 REPÚBLICA FRANCESA MODELO ATÓMICO ACTUAL El modelo atómico actual se construye a partir de
LOS ÁTOMOS Y LA ELECTRICIDAD (Ciencias Superior)
 LOS ÁTOMOS Y LA ELECTRICIDAD (Ciencias Superior) PROFESORA GILDA DIAZ MAT H AND S C I ENCE PAR T NERSHIP FOR T HE 21S T CENTURY ELEMENTARY AND MIDDLE S C HOOL MSP -21 ACADEMIA DE VERANO 7 DE JUNIO DE 2016
LOS ÁTOMOS Y LA ELECTRICIDAD (Ciencias Superior) PROFESORA GILDA DIAZ MAT H AND S C I ENCE PAR T NERSHIP FOR T HE 21S T CENTURY ELEMENTARY AND MIDDLE S C HOOL MSP -21 ACADEMIA DE VERANO 7 DE JUNIO DE 2016
QUIMICA GENERAL. Docente : Raquel Villafrades Torres
 Universidad Pontificia Bolivariana QUIMICA GENERAL Docente : Raquel Villafrades Torres TEORIA ATOMICA DE DALTON (1808) BASES Ley de conservación de la masa: La masa total de las sustancias presentes después
Universidad Pontificia Bolivariana QUIMICA GENERAL Docente : Raquel Villafrades Torres TEORIA ATOMICA DE DALTON (1808) BASES Ley de conservación de la masa: La masa total de las sustancias presentes después
UNIDAD 1: EL ÁTOMO Y EL SISTEMA PERIÓDICO
 UNIDAD 1: EL ÁTOMO Y EL SISTEMA PERIÓDICO 1. PRIMERAS TEORÍAS ATÓMICAS Demócrito, filósofo griego que vivió en el siglo IV a. C. propuso que, si se dividía la materia en trozos cada vez más pequeños, debería
UNIDAD 1: EL ÁTOMO Y EL SISTEMA PERIÓDICO 1. PRIMERAS TEORÍAS ATÓMICAS Demócrito, filósofo griego que vivió en el siglo IV a. C. propuso que, si se dividía la materia en trozos cada vez más pequeños, debería
1. Dibuja un átomo neutro (cualquiera) y di el nombre de sus partículas y la carga de éstas, señalando estas partículas en el dibujo.
 Examen de la unidad 4 de Física y Química de 2º ESO D Nombre: Fecha: 1. Dibuja un átomo neutro (cualquiera) y di el nombre de sus partículas y la carga de éstas, señalando estas partículas en el dibujo.
Examen de la unidad 4 de Física y Química de 2º ESO D Nombre: Fecha: 1. Dibuja un átomo neutro (cualquiera) y di el nombre de sus partículas y la carga de éstas, señalando estas partículas en el dibujo.
Ponte en forma 1.- Realiza las actividades que se te solicitan a continuación: a) Completa el siguiente cuadro:
 RESPUESTAS BLOQUE III Ponte en forma 1.- Realiza las actividades que se te solicitan a continuación: a) Completa el siguiente cuadro: Tipo de raciación Partículas Carga eléctrica Masa(uma) Alfa α +2 4
RESPUESTAS BLOQUE III Ponte en forma 1.- Realiza las actividades que se te solicitan a continuación: a) Completa el siguiente cuadro: Tipo de raciación Partículas Carga eléctrica Masa(uma) Alfa α +2 4
Primeros modelos atómicos. Demócrito y Leucipo. Aristóteles
 Primeros modelos atómicos Demócrito y Leucipo Aristóteles Según la teoría atómica de la materia de Demócrito: Todas las cosas están compuestas de partículas diminutas, invisibles e indestructibles de materia
Primeros modelos atómicos Demócrito y Leucipo Aristóteles Según la teoría atómica de la materia de Demócrito: Todas las cosas están compuestas de partículas diminutas, invisibles e indestructibles de materia
Apuntes para la UNIDAD 2. Mtra. Norma M. López V. Junio, 2016
 Apuntes para la UNIDAD 2 Mtra. Norma M. López V. Junio, 2016 1 Teoría atómica de la materia Demócrito (460-370 a.c.): el mundo material está formado de pequeñas partículas indestructibles (átomos), desprovistas
Apuntes para la UNIDAD 2 Mtra. Norma M. López V. Junio, 2016 1 Teoría atómica de la materia Demócrito (460-370 a.c.): el mundo material está formado de pequeñas partículas indestructibles (átomos), desprovistas
