CONJUNTO DE ELECTRÓLISIS
|
|
|
- Jesús Olivares Herrera
- hace 6 años
- Vistas:
Transcripción
1 Manual de Instrucciones y Guía de Experimentos CONJUNTO DE ELECTRÓLISIS OBSERVACIÓN SOBRE LOS DERECHOS AUTORALES Este manual está protegido por las leyes de derechos autorales y todos los derechos están reservados. Está permitida y garantizada para instituciones de enseñanza, no obstante, la reproducción de cualquier parte de este manual para que se la suministre y utilice en los laboratorios pero no para su venta. Su reproducción bajo cualquier otra circunstancia, sin la debida autirización de la AZEHEB está terminantemente prohibida. GARANTÍA La AZEHEB garantiza este producto contra defectos de fabricación por un periodo de 3 años a partir de la fecha de envío al cliente. La AZEHEB reparará o cambiará el producto defectuoso si se constata que el defecto fue ocasionado por problemas en los materiales que lo componen o por fallas en su fabricación. Esta garantía no cubre problemas ocasionados por abuso o debidos al uso incorrecto del producto. La determinación de si el defecto del producto es resultado de una falla de fabricación o si fue ocasionado por uso indebido será llevada a cabo únicamente por la AZEHEB. Dirección: AZEHEB Laboratórios de Física R Arthur Bernardes, 137-2º andar CEP São João Del Rey - MG - Brasil Teléfono: exportacion@azeheb.com 1
2 2
3 COMPONENTES DEL CONJUNTO 05 electrodos tipo placa 100x20x1mm: aluminio, plomo, cobre, hierro, cinc; 05 electrodos tipo placa 100x40x1mm: aluminio, plomo, cobre, hierro, cinc; 04 electrodos tipo bastón Ø8x150mm: aluminio, cobre, hierro, carbono (Ø7x180mm); 01 beaker de vidrio de 400ml; 01 base de acero 18x10cm con varilla de aluminio 01 sistema para fijar los electrodos. Montajes Básicos 3
4 ELECTROQUÍMICA MATERIAL NECESARIO - Conjunto de electrólisis - Fuente de alimentación CC variable de 0 a 15V 3A - Cables de conexión. Experimento 1 PILA DE VOLTA PROCEDIMIENTOS 1. Monte el equipo como se muestra en el esquema/foto. 2. Vierta en el beaker 300ml de solución diluida de acido sulfúrico. 3. Fije las láminas de cinc y cobre al soporte. 4. Sumerja las láminas de cinc y cobre en la solución diluida de acido sulfúrico. 5. Con un voltímetro mida la fem entre las láminas de cinc y cobre. fem = 6. Con un amperímetro mida la intensidad de corriente máxima entre las láminas de cinc y cobre. I = 7. Altere el área de las láminas de cinc y cobre sumergida en la solución diluida de ácido sulfúrico y observe el comportamiento de la fem y de la corriente (cambie las láminas cinc y cobre por las mayores). fem = I = 8. Cómo se comportó la intensidad de corriente I y la fem (V)? 9. Observando las conexiones, se nota que la lámina de cinc es positiva o negativa? 10. Observando las conexiones notamos que la lámina de cobre es positiva o negativa? 4
5 11. Repita el experimento con diversos materiales, como por ejemplo, sustituyendo la lámina de cobre por una de plomo. 12. Para obtener una diferencia de potencial entre dos láminas de metal, qué condiciones es necesario satisfacer? 13. Las láminas de metal sumergidas en la solución reciben el nombre de. 14. El electrodo negativo se denomina. (ánodo/cátodo) 15. El electrodo positivo se denomina. (ánodo /cátodo) 16. Cuál de las láminas será consumida por la reacción química?. 17. La solución usada en la pila tiene el nombre de. 18. De qué depende la fem de una pila? 5
6 Experimento 2 BATERÍA DE PLOMO (Electrólisis de una solución diluida de ácido sulfúrico) PROCEDIMIENTOS 1. Monte el equipo como se muestra en el esquema/foto. 2. Vierta en el beaker 300ml de solución diluida de acido sulfúrico 25%. 3. Fije dos láminas de plomo al soporte. 4. Sumerja las láminas de plomo en la solución diluida de ácido sulfúrico. 5. Con un voltímetro mida la fem entre los electrodos de plomo. fem = 6. Para electrodos de la misma naturaleza la fuerza electromotriz es igual a. 7. Conecte los electros de plomo a la fuente de alimentación y aplique una tensión de 3,5V-CC durante 5 minutos. 6
7 8. Cuando la corriente elétrica circule entre los electros de plomo y la solución diluida de ácido sulfúrico, se formarán burbujas de gás en ambas placas. - En el electrodo cátodo (positiva) sucede el desprendimiento de: (hidrógeno u oxígeno) - En el electrodo ánodo (negativa) sucede el desprendimiento de: (hidrógeno u oxígeno) 9. Cuando la corriente circula por los electrodos y la solución diluida de ácido sulfúrico, la tensión indicada en el voltímetro es igual a 3,5V-CC. Si dicha corriente se interrumpe al desconectar la fuente de tensión, la lectura del voltímetro pasará a indicar. 10. Al retirar la fuente de alimentación aplicada a los electrodos de plomo, se establece una fem igual a la. Tal equipo se conoce como o acumulador de plomo. 11. Conecte en serie una bombilla de 2V y las placas de plomo del acumulador. Qué le sucede a la bombilla? 12. Repita el experimento para, una vez más, encender la bombilla. Este procedimiento indica que se debe volver a cargar la batería. 7
8 8
CONJUNTO COMPACTO DE ÓPTICA
 Manual de Instrucciones y Guía de Experimentos CONJUNTO COMPACTO DE ÓPTICA OBSERVACIÓN SOBRE LOS DERECHOS AUTORALES Este manual está protegido por las leyes de derechos autorales y todos los derechos están
Manual de Instrucciones y Guía de Experimentos CONJUNTO COMPACTO DE ÓPTICA OBSERVACIÓN SOBRE LOS DERECHOS AUTORALES Este manual está protegido por las leyes de derechos autorales y todos los derechos están
Manual de Instrucciones y Guía de Experimentos
 Manual de Instrucciones y Guía de Experimentos TUBO DE KUNDT OBSERVACIÓN SOBRE LOS DERECHOS AUTORALES Este manual está protegido por las leyes de derechos autorales y todos los derechos están reservados.
Manual de Instrucciones y Guía de Experimentos TUBO DE KUNDT OBSERVACIÓN SOBRE LOS DERECHOS AUTORALES Este manual está protegido por las leyes de derechos autorales y todos los derechos están reservados.
de todos los dados el correcto será el: a) A b) B c) C d) D
 Redox 3 41*. Uno de los experimentos que puedes hacer perfectamente en el laboratorio y que te permitiría recordar el proceso de la pila Daniell, sería sumergir una lámina o chapa de cinc en un vaso de
Redox 3 41*. Uno de los experimentos que puedes hacer perfectamente en el laboratorio y que te permitiría recordar el proceso de la pila Daniell, sería sumergir una lámina o chapa de cinc en un vaso de
Magnetismo y Electromagnetismo
 Manual de Instrucciones y Guía de Experimentos Magnetismo y Electromagnetismo OBSERVACIÓN SOBRE LOS DERECHOS AUTORALES Este manual está protegido por las leyes de derechos autorales y todos los derechos
Manual de Instrucciones y Guía de Experimentos Magnetismo y Electromagnetismo OBSERVACIÓN SOBRE LOS DERECHOS AUTORALES Este manual está protegido por las leyes de derechos autorales y todos los derechos
Unidad 6: ELECTROQUIMICA
 Unidad 6: ELECTROQUIMICA REACCIONES DE OXIDACION-REDUCCION Las reacciones redox son aquellas en las cuales hay intercambio de electrones entre las sustancias que intervienen en la reacción. Oxidación:
Unidad 6: ELECTROQUIMICA REACCIONES DE OXIDACION-REDUCCION Las reacciones redox son aquellas en las cuales hay intercambio de electrones entre las sustancias que intervienen en la reacción. Oxidación:
Electrólisis. Electrólisis 12/02/2015
 Electrólisis Dr. Armando Ayala Corona Electrólisis La electrolisis es un proceso mediante el cual se logra la disociación de una sustancia llamada electrolito, en sus iones constituyentes (aniones y cationes),
Electrólisis Dr. Armando Ayala Corona Electrólisis La electrolisis es un proceso mediante el cual se logra la disociación de una sustancia llamada electrolito, en sus iones constituyentes (aniones y cationes),
Corriente y Circuitos Eléctricos
 Módulo: Medición y Análisis de Circuitos Eléctricos Unidad 1 Unidades y Mediciones Eléctricas Responda en su cuaderno las siguientes preguntas: Cuestionario 1 1.- Defina los siguientes conceptos, indicando
Módulo: Medición y Análisis de Circuitos Eléctricos Unidad 1 Unidades y Mediciones Eléctricas Responda en su cuaderno las siguientes preguntas: Cuestionario 1 1.- Defina los siguientes conceptos, indicando
LA ELECTRÓLISIS DE DISOLUCIONES SALINAS (II)
 LA ELECTRÓLISIS DE DISOLUCIONES SALINAS (II) Se van a presentar tres electrólisis en diferentes condiciones y con distintos electrodos, a fin de observar la influencia de estas condiciones en sus resultados
LA ELECTRÓLISIS DE DISOLUCIONES SALINAS (II) Se van a presentar tres electrólisis en diferentes condiciones y con distintos electrodos, a fin de observar la influencia de estas condiciones en sus resultados
ELECTROQUÍMICA. 1- Concepto de potencial normal. Electrodo de referencia
 ELECTROQUÍMICA 1 Concepto de potencial normal. Electrodo de referencia 2 Se forma una pila con un electrodo de níquel y otro de plata. Indica el electrodo que eléctricamente es el polo positivo, el que
ELECTROQUÍMICA 1 Concepto de potencial normal. Electrodo de referencia 2 Se forma una pila con un electrodo de níquel y otro de plata. Indica el electrodo que eléctricamente es el polo positivo, el que
REACCIONES DE TRANSFERENCIA DE ELECTRONES (electrolisis)
 REACCIONES DE TRANSFERENCIA DE ELECTRONES (electrolisis) 1 2 Electrólisis Aplicando una f.e.m. adecuada se puede conseguir que tenga lugar una reacción redox en el sentido que no es espontánea. En una
REACCIONES DE TRANSFERENCIA DE ELECTRONES (electrolisis) 1 2 Electrólisis Aplicando una f.e.m. adecuada se puede conseguir que tenga lugar una reacción redox en el sentido que no es espontánea. En una
Pilas electrolíticas
 Pilas electrolíticas Apellidos, nombre Departamento Centro Atienza Boronat, Mª Julia (matien@qim.upv.es) Herrero Villén, Mª Asunción (maherrero@qim.upv.es) Morais Ezquerro, Sergi B. (smorais@qim.upv.es)
Pilas electrolíticas Apellidos, nombre Departamento Centro Atienza Boronat, Mª Julia (matien@qim.upv.es) Herrero Villén, Mª Asunción (maherrero@qim.upv.es) Morais Ezquerro, Sergi B. (smorais@qim.upv.es)
PROBLEMAS Y EJERCICIOS RESUELTOS SOBRE FUERZA ELECTROMOTRIZ, FUERZA CONTRAELECTROMOTRIZ, CIRCUITOD DE CORRIENTE CONTINUA A C B
 Ejercicio resuelto Nº 1 Dado el circuito de la figura adjunta: ε = 15 V A r i = 0,5 Ω B R 2 R 1 A C B R 3 R 4 R 1 = 2 Ω ; R 2 = 1 Ω ; R 3 = 2 Ω ; R 4 = 3 Ω Determinar: a) Intensidad de corriente que circula
Ejercicio resuelto Nº 1 Dado el circuito de la figura adjunta: ε = 15 V A r i = 0,5 Ω B R 2 R 1 A C B R 3 R 4 R 1 = 2 Ω ; R 2 = 1 Ω ; R 3 = 2 Ω ; R 4 = 3 Ω Determinar: a) Intensidad de corriente que circula
PROBLEMAS RESUELTOS SELECTIVIDAD ANDALUCÍA 2007 QUÍMICA TEMA 7: REACCIONES REDOX
 PROBLEMAS RESUELTOS SELECTIVIDAD ANDALUCÍA 007 QUÍMICA TEMA 7: REACCIONES REDOX Junio, Ejercicio 5, Opción A Reserva 1, Ejercicio 6, Opción B Reserva, Ejercicio, Opción A Reserva, Ejercicio 6, Opción B
PROBLEMAS RESUELTOS SELECTIVIDAD ANDALUCÍA 007 QUÍMICA TEMA 7: REACCIONES REDOX Junio, Ejercicio 5, Opción A Reserva 1, Ejercicio 6, Opción B Reserva, Ejercicio, Opción A Reserva, Ejercicio 6, Opción B
La Ley de Ohm establece una relación entre voltaje, V, aplicado a un conductor y corriente, I, circulando a través del mismo.
 FIS-1525 Ley de Ohm Objetivo Estudiar empíricamente la relación existente entre el voltaje aplicado a un conductor y la corriente eléctrica que circula. Probar el cumplimiento de la ley de Ohm para dos
FIS-1525 Ley de Ohm Objetivo Estudiar empíricamente la relación existente entre el voltaje aplicado a un conductor y la corriente eléctrica que circula. Probar el cumplimiento de la ley de Ohm para dos
TRABAJO PRÁCTICO N 6: ELECTRÓLISIS
 QUÍMICA GENERAL Y TECNOLÓGICA 2010 TRABAJO PRÁCTICO N 6: ELECTRÓLISIS Objetivo: Medición de la intensidad de corriente que circula por un sistema electrolítico y determinación del equivalente-gramo del
QUÍMICA GENERAL Y TECNOLÓGICA 2010 TRABAJO PRÁCTICO N 6: ELECTRÓLISIS Objetivo: Medición de la intensidad de corriente que circula por un sistema electrolítico y determinación del equivalente-gramo del
corriente) C Aquí q esta en Coulomb, t en segundos, I en Amperes (1A= 1 ) s
 UNA CORRIENTE i de electricidad existe en cualquier región donde sean transportadas cargas eléctricas desde un punto a otro punto de esa región.supóngase que la carga se mueve a través de un alambre.si
UNA CORRIENTE i de electricidad existe en cualquier región donde sean transportadas cargas eléctricas desde un punto a otro punto de esa región.supóngase que la carga se mueve a través de un alambre.si
LABORATORIO DE FÍSICA
 LABORATORIO DE FÍSICA OBJETIVO DE LA PRÁCTICA Fuente de c.c. MATERIAL Analizar el comportamiento y funcionamiento de diferentes diodos (silicio, germanio y Zener). Efecto válvula. Efecto rectificador.
LABORATORIO DE FÍSICA OBJETIVO DE LA PRÁCTICA Fuente de c.c. MATERIAL Analizar el comportamiento y funcionamiento de diferentes diodos (silicio, germanio y Zener). Efecto válvula. Efecto rectificador.
ELECTRICIDAD. La idea de corriente eléctrica es inseparable de la de un circuito cerrado. Si en algún lugar hay una ruptura, la corriente no circula.
 ELECTRICIDAD La idea de corriente eléctrica es inseparable de la de un circuito cerrado. Si en algún lugar hay una ruptura, la corriente no circula. Un circuito muy simple: pila, bombilla y cables y su
ELECTRICIDAD La idea de corriente eléctrica es inseparable de la de un circuito cerrado. Si en algún lugar hay una ruptura, la corriente no circula. Un circuito muy simple: pila, bombilla y cables y su
Tema 13: CORRIENTE ELÉCTRICA Y CIRCUITOS ELÉCTRICOS
 Tema 13: CORRIENTE ELÉCTRICA Y CIRCUITOS ELÉCTRICOS CORRIENTE ELÉCTRICA Y MOVIMIENTO DE CARGAS Problema 1: Una corriente de 3.6 A fluye a través de un faro de automóvil. Cuántos Culombios de carga fluyen
Tema 13: CORRIENTE ELÉCTRICA Y CIRCUITOS ELÉCTRICOS CORRIENTE ELÉCTRICA Y MOVIMIENTO DE CARGAS Problema 1: Una corriente de 3.6 A fluye a través de un faro de automóvil. Cuántos Culombios de carga fluyen
Unidad 7. Reacciones de transferencia de electrones. Oxidación- Reducción. Ajuste de reacciones de oxidación-reducción.
 Unidad 7. Reacciones de transferencia de electrones. Oxidación- Reducción Concepto de oxidación-reducción Número de oxidación Ajuste de reacciones de oxidación-reducción. Estequiometría Electroquímica
Unidad 7. Reacciones de transferencia de electrones. Oxidación- Reducción Concepto de oxidación-reducción Número de oxidación Ajuste de reacciones de oxidación-reducción. Estequiometría Electroquímica
ELECTRICIDAD. 1.- Circuito eléctrico
 ELECTRICIDAD 1.- Circuito eléctrico 2.- Generadores y/o acumuladores 3.- Conductores y aislantes 4.- Receptores 5.- Elementos de protección 6.- Elementos de maniobra 7.- Tipos de corriente eléctrica. Transformadores.
ELECTRICIDAD 1.- Circuito eléctrico 2.- Generadores y/o acumuladores 3.- Conductores y aislantes 4.- Receptores 5.- Elementos de protección 6.- Elementos de maniobra 7.- Tipos de corriente eléctrica. Transformadores.
REACCIONES DE TRANSFERENCIA DE ELECTRONES (Reacciones Redox)
 REACCIONES DE TRANSFERENCIA DE ELECTRONES (Reacciones Redox) 1 2 Tipos de reacciones redox (según su espontaneidad) Reacciones espontáneas: G
REACCIONES DE TRANSFERENCIA DE ELECTRONES (Reacciones Redox) 1 2 Tipos de reacciones redox (según su espontaneidad) Reacciones espontáneas: G
ELECTROQUIMICA CELDAS GALVANICAS, ELECTROLISIS Y ELECTROQUIMICA APLICADA
 ELECTROQUIMICA CELDAS GALVANICAS, ELECTROLISIS Y ELECTROQUIMICA APLICADA QUE ES LA ELECTROQUIMICA? Es la parte de la química que se encarga del estudio de las relaciones cualitativas y cuantitativas existentes
ELECTROQUIMICA CELDAS GALVANICAS, ELECTROLISIS Y ELECTROQUIMICA APLICADA QUE ES LA ELECTROQUIMICA? Es la parte de la química que se encarga del estudio de las relaciones cualitativas y cuantitativas existentes
APLICACIONES DE LA ENERGIA SOLAR FOTOVOLTAICA: PILAS DE COMBUSTIBLE
 APLICACIONES DE LA ENERGIA SOLAR FOTOVOLTAICA: PILAS DE COMBUSTIBLE 1.OBJETIVO Obtención de las curvas características de una célula solar y una ceda de combustible. 2.FUNDAMENTO TEORICO Células Solares
APLICACIONES DE LA ENERGIA SOLAR FOTOVOLTAICA: PILAS DE COMBUSTIBLE 1.OBJETIVO Obtención de las curvas características de una célula solar y una ceda de combustible. 2.FUNDAMENTO TEORICO Células Solares
LA ELECTRÓLISIS DEL AGUA
 LA ELECTRÓLISIS DEL AGUA Oxidación: 2H + +O +4e - 2 O(l) 4H (aq) 2 (g) Reducción: 2H 2 O(l) + 2e - H 2 (g) + 2OH - (aq) Reacción total en la celda 2H 2 O(l) 2H 2 (g) + O 2 (g) Nota: Obsérvese la diferencia
LA ELECTRÓLISIS DEL AGUA Oxidación: 2H + +O +4e - 2 O(l) 4H (aq) 2 (g) Reducción: 2H 2 O(l) + 2e - H 2 (g) + 2OH - (aq) Reacción total en la celda 2H 2 O(l) 2H 2 (g) + O 2 (g) Nota: Obsérvese la diferencia
TEMA 3 GENERADORES DE CORRIENTE CONTINUA
 TEMA 3 GENERADORES DE CORRIENTE CONTINUA En todo circuito eléctrico es necesaria una fuente de energía que sea capaz de poner en movimiento a los electrones, a la cual llamamos generador. Si existen dos
TEMA 3 GENERADORES DE CORRIENTE CONTINUA En todo circuito eléctrico es necesaria una fuente de energía que sea capaz de poner en movimiento a los electrones, a la cual llamamos generador. Si existen dos
Circuitos de corriente continua
 Capítulo 4: Circuitos de corriente continua Corriente promedio: carga que pasa por A por unidad de tiempo Corriente Instantánea [ I ] = C/s = A (Ampere) J = q n v d Ley de Ohm George Simon Ohm (1789-1854)
Capítulo 4: Circuitos de corriente continua Corriente promedio: carga que pasa por A por unidad de tiempo Corriente Instantánea [ I ] = C/s = A (Ampere) J = q n v d Ley de Ohm George Simon Ohm (1789-1854)
OXIDACIÓN REDUCCIÓN QCA 07 ANDALUCÍA
 .- Se realiza la electrolisis de litros de una disolución de nitrato de plata 0 M haciendo pasar una corriente eléctrica de 0 5 amperios durante 4 horas. Calcule: a) La masa de plata que se deposita en
.- Se realiza la electrolisis de litros de una disolución de nitrato de plata 0 M haciendo pasar una corriente eléctrica de 0 5 amperios durante 4 horas. Calcule: a) La masa de plata que se deposita en
Reacciones redox espontáneas
 Celda galvánica o voltaica o electroquímica Pila galvánica o voltaica o electroquímica Cuba galvánica o voltaica o electroquímica Cada una de las partes se denomina: semicelda o semipila o electrodo Pila
Celda galvánica o voltaica o electroquímica Pila galvánica o voltaica o electroquímica Cuba galvánica o voltaica o electroquímica Cada una de las partes se denomina: semicelda o semipila o electrodo Pila
TRABAJO PRÁCTICO N 10 PILAS-ELECTRÓLISIS
 TRABAJO PRÁCTICO N 10 PILAS-ELECTRÓLISIS Las celdas galvánicas (pilas) son dispositivos armados de tal forma que, usando reacciones redox espontáneas, generan energía eléctrica Ejemplo: Pila de Daniel:
TRABAJO PRÁCTICO N 10 PILAS-ELECTRÓLISIS Las celdas galvánicas (pilas) son dispositivos armados de tal forma que, usando reacciones redox espontáneas, generan energía eléctrica Ejemplo: Pila de Daniel:
PRÁCTICA Nº 9 y 10 CORROSIÓN I
 PRÁCTICA Nº 9 y 10 CORROSIÓN I OBJETO DE LA PRÁCTICA: CONCEPTO DE ÁNODO Y CÁTODO APLICACIÓN A TRES REACCIONES REDOX CONCEPTO DE ENERGÍA ELÉCTRICA ASOCIADA A CAMBIOS QUÍMICOS Y VICEVERSA REACCIÓN ESPONTÁNEA
PRÁCTICA Nº 9 y 10 CORROSIÓN I OBJETO DE LA PRÁCTICA: CONCEPTO DE ÁNODO Y CÁTODO APLICACIÓN A TRES REACCIONES REDOX CONCEPTO DE ENERGÍA ELÉCTRICA ASOCIADA A CAMBIOS QUÍMICOS Y VICEVERSA REACCIÓN ESPONTÁNEA
EFECTOS DE LA CORRIENTE ELÉCTRICA: TÉRMICO, MAGNÉTICO Y QUÍMICO
 EFECTOS DE LA CORRIENTE ELÉCTRICA: TÉRMICO, MAGNÉTICO Y QUÍMICO Marisol de la Fuente Mendoza IES LA CANAL DE NAVARRÉS Navarrés (Valencia) Introducción: Al hablar de los efectos de la corriente eléctrica,
EFECTOS DE LA CORRIENTE ELÉCTRICA: TÉRMICO, MAGNÉTICO Y QUÍMICO Marisol de la Fuente Mendoza IES LA CANAL DE NAVARRÉS Navarrés (Valencia) Introducción: Al hablar de los efectos de la corriente eléctrica,
El E.O. no tiene porqué ser la carga real que tiene un átomo, aunque a veces coincide.
 EQUILIBRIOS DE OXIDACIÓN-REDUCCIÓN (REDOX) 2º BACHILLERATO QUÍMICA 1.- Estado de oxidación. 2.- Concepto de oxidación y reducción. 3.- Ajuste de ecuaciones redox por el método del ión-electrón. 3.1. Reacciones
EQUILIBRIOS DE OXIDACIÓN-REDUCCIÓN (REDOX) 2º BACHILLERATO QUÍMICA 1.- Estado de oxidación. 2.- Concepto de oxidación y reducción. 3.- Ajuste de ecuaciones redox por el método del ión-electrón. 3.1. Reacciones
PRÁCTICA 18 ELECTROQUÍMICA 1.- FUNDAMENTO TEÓRICO.
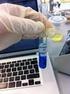 PRÁCTICA 18 ELECTROQUÍMICA 1.- FUNDAMENTO TEÓRICO. El concepto de Electroquímica implica transformaciones que requieren la presencia de electrodos. Dos electrodos sumergidos en un electrólito y unidos
PRÁCTICA 18 ELECTROQUÍMICA 1.- FUNDAMENTO TEÓRICO. El concepto de Electroquímica implica transformaciones que requieren la presencia de electrodos. Dos electrodos sumergidos en un electrólito y unidos
EXAMENES ELECTROTECNIA TEORIA
 EXAMENES En este archivo presento el tipo de exámenes propuesto en la asignatura de Electrotecnia en la fecha indicada, con las puntuaciones indicadas sobre un total de diez puntos. Según la guía académica
EXAMENES En este archivo presento el tipo de exámenes propuesto en la asignatura de Electrotecnia en la fecha indicada, con las puntuaciones indicadas sobre un total de diez puntos. Según la guía académica
PRÁCTICA 21 CÁLCULO DE LA CONSTANTE DE LOS GASES: VOLUMEN MOLAR DEL HIDRÓGENO. COMPARACIÓN CON EL MÉTODO HOFFMAN
 PRÁCTICA 1 CÁLCULO DE LA CONSTANTE DE LOS GASES: VOLUMEN MOLAR DEL HIDRÓGENO. COMPARACIÓN CON EL MÉTODO HOFFMAN OBJETIVOS Discernir entre un proceso redox que es espontáneo y otro que no lo es. Obtener,
PRÁCTICA 1 CÁLCULO DE LA CONSTANTE DE LOS GASES: VOLUMEN MOLAR DEL HIDRÓGENO. COMPARACIÓN CON EL MÉTODO HOFFMAN OBJETIVOS Discernir entre un proceso redox que es espontáneo y otro que no lo es. Obtener,
Batería de Mano. Batería de Mano
 E L E C T R I C I D A D Y M A G N E T I S M O Batería de Mano Batería de Mano ELECTRICIDAD Y MAGNETISMO La Electroquímica es una rama de la Química que estudia las transformaciones de energía química en
E L E C T R I C I D A D Y M A G N E T I S M O Batería de Mano Batería de Mano ELECTRICIDAD Y MAGNETISMO La Electroquímica es una rama de la Química que estudia las transformaciones de energía química en
ELECTRÓLISIS DEL AGUA FRANCISCO MORENO HUESO. 18 de noviembre de 2013
 18 de noviembre de 2013 Índice General 1 FUNDAMENTO TEÓRICO Índice General 1 FUNDAMENTO TEÓRICO 2 MATERIAL Y REACTIVOS Índice General 1 FUNDAMENTO TEÓRICO 2 MATERIAL Y REACTIVOS 3 PROCEDIMIENTO EXPERIMENTAL
18 de noviembre de 2013 Índice General 1 FUNDAMENTO TEÓRICO Índice General 1 FUNDAMENTO TEÓRICO 2 MATERIAL Y REACTIVOS Índice General 1 FUNDAMENTO TEÓRICO 2 MATERIAL Y REACTIVOS 3 PROCEDIMIENTO EXPERIMENTAL
Prueba experimental. Constante de Planck y comportamiento de un LED
 Prueba experimental. Constante de Planck y comportamiento de un LED Objetivo. Se va a construir un circuito eléctrico para alimentar LEDs de diferentes colores y obtener un valor aproximado de la constante
Prueba experimental. Constante de Planck y comportamiento de un LED Objetivo. Se va a construir un circuito eléctrico para alimentar LEDs de diferentes colores y obtener un valor aproximado de la constante
UNIDAD 10.- LAS UNIONES ENTRE ÁTOMOS. Cuestiones de evaluación inicial. 2.- Cuántos protones y cuantos neutrones tiene el Carbono?
 UNIDAD 10.- LAS UNIONES ENTRE ÁTOMOS Cuestiones de evaluación inicial 1.- Cuántos elementos químicos conoces? 2.- Cuántos protones y cuantos neutrones tiene el Carbono? 3.- Qué es el sistema periódico?
UNIDAD 10.- LAS UNIONES ENTRE ÁTOMOS Cuestiones de evaluación inicial 1.- Cuántos elementos químicos conoces? 2.- Cuántos protones y cuantos neutrones tiene el Carbono? 3.- Qué es el sistema periódico?
QUÍMICA. [ΔH afinidad Cl(g)] = -349 kj mol -1 (0,25 puntos) K + (g) + Cl - (g)
![QUÍMICA. [ΔH afinidad Cl(g)] = -349 kj mol -1 (0,25 puntos) K + (g) + Cl - (g) QUÍMICA. [ΔH afinidad Cl(g)] = -349 kj mol -1 (0,25 puntos) K + (g) + Cl - (g)](/thumbs/49/25837773.jpg) OPCIÓN A QUÍMICA. 1. (2,5 puntos) Construya el ciclo de Born-aber y calcule la energía de red (Δ red ) del KCl(s) a partir de los siguientes datos: Entalpía estándar de formación del KCl(s) [Δ f (KCl)]
OPCIÓN A QUÍMICA. 1. (2,5 puntos) Construya el ciclo de Born-aber y calcule la energía de red (Δ red ) del KCl(s) a partir de los siguientes datos: Entalpía estándar de formación del KCl(s) [Δ f (KCl)]
SENSOR DE OXIGENO Sensor de Oxígeno
 SENSOR DE OXIGENO Otro sensor especial utilizado solamente en los Sistemas de Control de Motores es el Sensor de Oxígeno. Este componente se monta en el tubo de escape de gases residuales de la combustión
SENSOR DE OXIGENO Otro sensor especial utilizado solamente en los Sistemas de Control de Motores es el Sensor de Oxígeno. Este componente se monta en el tubo de escape de gases residuales de la combustión
Los Circuitos Eléctricos
 Los Circuitos Eléctricos 1.- LA CORRIENTE ELÉCTRICA. La electricidad es un movimiento de electrones, partículas con carga eléctrica negativa que giran alrededor del núcleo de los átomos. En los materiales
Los Circuitos Eléctricos 1.- LA CORRIENTE ELÉCTRICA. La electricidad es un movimiento de electrones, partículas con carga eléctrica negativa que giran alrededor del núcleo de los átomos. En los materiales
Comprobar experimentalmente la ley de Ohm y las reglas de Kirchhoff. Determinar el valor de resistencias.
 38 6. LEY DE OHM. REGLAS DE KIRCHHOFF Objetivo Comprobar experimentalmente la ley de Ohm y las reglas de Kirchhoff. Determinar el valor de resistencias. Material Tablero de conexiones, fuente de tensión
38 6. LEY DE OHM. REGLAS DE KIRCHHOFF Objetivo Comprobar experimentalmente la ley de Ohm y las reglas de Kirchhoff. Determinar el valor de resistencias. Material Tablero de conexiones, fuente de tensión
ELECTROLISIS. Si a dos electrodos de una pila Daniel, en la que espontáneamente se verifica la reacción:
 ELECTROLISIS Si a dos electrodos de una pila Daniel, en la que espontáneamente se verifica la reacción: + + Zn + Cu Zn + Cu se aplica una diferencia de potencial progresivamente creciente que se oponga
ELECTROLISIS Si a dos electrodos de una pila Daniel, en la que espontáneamente se verifica la reacción: + + Zn + Cu Zn + Cu se aplica una diferencia de potencial progresivamente creciente que se oponga
Reacciones de transferencia de electrones
 Reacciones de transferencia de electrones Las reacciones de transferencia de electrones o reacciones de oxidación-reducción son aquellas en las que dos o más elementos cambian su número de oxidación. Número
Reacciones de transferencia de electrones Las reacciones de transferencia de electrones o reacciones de oxidación-reducción son aquellas en las que dos o más elementos cambian su número de oxidación. Número
TEMA 3 BATERÍAS, DÍNAMOS, MOTORES Y CONDENSADORES
 TEMA 3 BATERÍAS, DÍNAMOS, MOTORES Y CONDENSADORES III.1 Baterías III.2 Dínamos III.3 Motores de CC III.4 Rendimiento energético III.5 Condensadores eléctricos III.6 Acoplamiento de condensadores Cuestiones
TEMA 3 BATERÍAS, DÍNAMOS, MOTORES Y CONDENSADORES III.1 Baterías III.2 Dínamos III.3 Motores de CC III.4 Rendimiento energético III.5 Condensadores eléctricos III.6 Acoplamiento de condensadores Cuestiones
APUNTES DE TECNOLOGÍA
 APUNTES DE TECNOLOGÍA 4º E.S.O. TEMA 1 CIRCUITOS ELÉCTRICOS Alumno: Grupo: 4º 1 CORRIENTE ELÉCTRICA 1.-CIRCUITOS ELÉCTRICOS La corriente eléctrica es un flujo de electrones en el seno de un material conductor.
APUNTES DE TECNOLOGÍA 4º E.S.O. TEMA 1 CIRCUITOS ELÉCTRICOS Alumno: Grupo: 4º 1 CORRIENTE ELÉCTRICA 1.-CIRCUITOS ELÉCTRICOS La corriente eléctrica es un flujo de electrones en el seno de un material conductor.
GUÍA SUBPROGRAMA DE GESTIÓN INTEGRAL DE RESIDUOS SÓLIDOS
 GUÍA SUBPROGRAMA DE GESTIÓN INTEGRAL DE RESIDUOS SÓLIDOS 1. OBJETIVO GENERAL Implementar procesos y prácticas que permitan realizar un adecuado manejo y aprovechamiento de los residuos sólidos desde su
GUÍA SUBPROGRAMA DE GESTIÓN INTEGRAL DE RESIDUOS SÓLIDOS 1. OBJETIVO GENERAL Implementar procesos y prácticas que permitan realizar un adecuado manejo y aprovechamiento de los residuos sólidos desde su
ELECTROLISIS DEL AGUA POR
 ELECTROLISIS DEL AGUA POR TEORIA: La electrólisis del agua consiste en un proceso electroquímico en el cual el agua se divide en Hidrógeno y Oxígeno. La electrólisis consiste en pasar corriente eléctrica
ELECTROLISIS DEL AGUA POR TEORIA: La electrólisis del agua consiste en un proceso electroquímico en el cual el agua se divide en Hidrógeno y Oxígeno. La electrólisis consiste en pasar corriente eléctrica
PURIFICACIÓN DE CAOLÍN POR ELECTRÓLISIS. J. C. Flores, V. E. Reyes, F. Legorreta, L. E. Hernández
 PURIFICACIÓN DE CAOLÍN POR ELECTRÓLISIS J. C. Flores, V. E. Reyes, F. Legorreta, L. E. Hernández UAEH, carlosflores.segura@gmail.com, reyescruz16@yahoo.com, felegorreta@hotmail.com, laetitia106@hotmail.com
PURIFICACIÓN DE CAOLÍN POR ELECTRÓLISIS J. C. Flores, V. E. Reyes, F. Legorreta, L. E. Hernández UAEH, carlosflores.segura@gmail.com, reyescruz16@yahoo.com, felegorreta@hotmail.com, laetitia106@hotmail.com
DETERMINACION DE LA DENSIDAD
 DETERMINACION DE LA DENSIDAD GUÍA DE QUÍMICA EXPERIMENTO N 2 DETERMINANCION DE LA DENSIDAD DE SOLIDOS Y LÍQUIDOS OBJETIVOS: Que el estudiante: a) Desarrolle destrezas para determinar numéricamente las
DETERMINACION DE LA DENSIDAD GUÍA DE QUÍMICA EXPERIMENTO N 2 DETERMINANCION DE LA DENSIDAD DE SOLIDOS Y LÍQUIDOS OBJETIVOS: Que el estudiante: a) Desarrolle destrezas para determinar numéricamente las
TEMA VII. REACCIONES DE TRANSFERENCIA DE ELECTRONES.
 TEMA VII. REACCIONES DE TRANSFERENCIA DE ELECTRONES. 1. CONCEPTOS DE OXIDACIÓN-REDUCCIÓN. Concepto restringido: Oxidación es la reacción química en la que hay ganancia de oxígeno, y reducción, la reacción
TEMA VII. REACCIONES DE TRANSFERENCIA DE ELECTRONES. 1. CONCEPTOS DE OXIDACIÓN-REDUCCIÓN. Concepto restringido: Oxidación es la reacción química en la que hay ganancia de oxígeno, y reducción, la reacción
La electrólisis permite descomponer la Alúmina en aluminio y oxígeno.
 LA OBTENCIÓN DEL ALUMINIO. La primera fase de la obtención del aluminio consiste en aislar la Alúmina (óxido de aluminio) de estos minerales. Para ello lo primero es triturar la Bauxita para obtener un
LA OBTENCIÓN DEL ALUMINIO. La primera fase de la obtención del aluminio consiste en aislar la Alúmina (óxido de aluminio) de estos minerales. Para ello lo primero es triturar la Bauxita para obtener un
1.- Trabajar el sistema por el tiempo necesario para que el refractario alcance su máxima temperatura.
 INSTALACIÓN DE LOS SENSORES: Los controles primarios y programadores IC en sus diferentes modelos pueden trabajar con tres diferentes sistemas de detección de flama: A, R, ó H (al ordenar el control de
INSTALACIÓN DE LOS SENSORES: Los controles primarios y programadores IC en sus diferentes modelos pueden trabajar con tres diferentes sistemas de detección de flama: A, R, ó H (al ordenar el control de
Grado de Óptica y Optometría Asignatura: FÍSICA Curso: Práctica nº 5. MEDIDAS DE RESISTENCIAS, VOLTAJES Y CORRIENTES: MULTÍMETRO
 FCULTD DE CIENCIS UNIERSIDD DE LICNTE Grado de Óptica y Optometría signatura: FÍSIC Curso: 200- Práctica nº 5. MEDIDS DE RESISTENCIS, OLTJES Y CORRIENTES: MULTÍMETRO Material Fuente de alimentación de
FCULTD DE CIENCIS UNIERSIDD DE LICNTE Grado de Óptica y Optometría signatura: FÍSIC Curso: 200- Práctica nº 5. MEDIDS DE RESISTENCIS, OLTJES Y CORRIENTES: MULTÍMETRO Material Fuente de alimentación de
Circuitería Básica, Leyes de Kirchhoff y Equivalente Thévenin
 Circuitos de Corriente Continua Circuitería Básica, Leyes de Kirchhoff y Equivalente Thévenin 1. OBJETIVOS - Estudiar las asociaciones básicas de elementos resistivos en corriente continua: conexiones
Circuitos de Corriente Continua Circuitería Básica, Leyes de Kirchhoff y Equivalente Thévenin 1. OBJETIVOS - Estudiar las asociaciones básicas de elementos resistivos en corriente continua: conexiones
Acumuladores OPzS VR Baterías. Manual de operación
 Acumuladores OPzS VR Baterías Manual de operación 1. General El manual de operación es el documento que acredita los parámetros básicos y las especificaciones de las baterías OPzS garantizados por el fabricante,
Acumuladores OPzS VR Baterías Manual de operación 1. General El manual de operación es el documento que acredita los parámetros básicos y las especificaciones de las baterías OPzS garantizados por el fabricante,
ELECTROOBTENCIÓN DE ZINC UTILIZANDO CELDA DE ELECTRODIALISIS REACTIVA
 UNIVERSIDAD DE SANTIAGO DE CHILE FACULTAD DE INGENIERIA DEPARTAMENTO DE INGENIERIA METALURGICA ELECTROOBTENCIÓN DE ZINC UTILIZANDO CELDA DE ELECTRODIALISIS REACTIVA Profesor Dr. GERARDO CIFUENTES MOLINA
UNIVERSIDAD DE SANTIAGO DE CHILE FACULTAD DE INGENIERIA DEPARTAMENTO DE INGENIERIA METALURGICA ELECTROOBTENCIÓN DE ZINC UTILIZANDO CELDA DE ELECTRODIALISIS REACTIVA Profesor Dr. GERARDO CIFUENTES MOLINA
REACCIONES RED-OX QCA 01
 1.- Una muestra de un metal se disuelve en ácido clorhídrico y se realiza la electrólisis de la disolución. Cuando han pasado por la célula electrolítica 315 C, se encuentra que en el cátodo se han depositado
1.- Una muestra de un metal se disuelve en ácido clorhídrico y se realiza la electrólisis de la disolución. Cuando han pasado por la célula electrolítica 315 C, se encuentra que en el cátodo se han depositado
Si la intensidad de corriente y su dirección no cambian con el tiempo, entonces esa corriente se llama corriente continua.
 1.8. Corriente eléctrica. Ley de Ohm Clases de Electromagnetismo. Ariel Becerra Si un conductor aislado es introducido en un campo eléctrico entonces sobre las cargas libres q en el conductor va a actuar
1.8. Corriente eléctrica. Ley de Ohm Clases de Electromagnetismo. Ariel Becerra Si un conductor aislado es introducido en un campo eléctrico entonces sobre las cargas libres q en el conductor va a actuar
ALUMNO-A: CURSO: 2º ESO
 UNIDAD: ELECTRICIDAD. CONOCIENDO LA ELECTRICIDAD ALUMNO-A: CURSO: 2º ESO 1.- INTRODUCCIÓN Hoy en día la energía eléctrica es imprescindible, gracias a ella funcionan infinidad de aparatos, máquinas, fábricas,
UNIDAD: ELECTRICIDAD. CONOCIENDO LA ELECTRICIDAD ALUMNO-A: CURSO: 2º ESO 1.- INTRODUCCIÓN Hoy en día la energía eléctrica es imprescindible, gracias a ella funcionan infinidad de aparatos, máquinas, fábricas,
EMBELLECIMIENTO DE OBJETOS DE LA VIDA COTIDIANA
 EMBELLECIMIENTO DE OBJETOS DE LA VIDA COTIDIANA Hervilia Seco Lago 1, Julia Pérez Iglesias 2, José Mª. Fernández Solís 2, Victoria González Rodríguez 2, Elena González Soto 2, J. Manuel Castro Romero 2,
EMBELLECIMIENTO DE OBJETOS DE LA VIDA COTIDIANA Hervilia Seco Lago 1, Julia Pérez Iglesias 2, José Mª. Fernández Solís 2, Victoria González Rodríguez 2, Elena González Soto 2, J. Manuel Castro Romero 2,
ASOCIACIÓN DE RESISTORES
 ASOCIACIÓN DE RESISTORES Santiago Ramírez de la Piscina Millán Francisco Sierra Gómez Francisco Javier Sánchez Torres 1. INTRODUCCIÓN. Con esta práctica el alumno aprenderá a identificar los elementos
ASOCIACIÓN DE RESISTORES Santiago Ramírez de la Piscina Millán Francisco Sierra Gómez Francisco Javier Sánchez Torres 1. INTRODUCCIÓN. Con esta práctica el alumno aprenderá a identificar los elementos
TEMA 13: CIRCUITOS ELÉCTRICOS
 TEMA 13: CIRCUITOS ELÉCTRICOS 1 TEMA 13: CIRCUITOS ELÉCTRICOS 13.1.- QUÉ ES UN CIRCUITO ELÉCTRICO? Un circuito eléctrico es un conjunto de elementos conectados entre sí, por los que circula una corriente
TEMA 13: CIRCUITOS ELÉCTRICOS 1 TEMA 13: CIRCUITOS ELÉCTRICOS 13.1.- QUÉ ES UN CIRCUITO ELÉCTRICO? Un circuito eléctrico es un conjunto de elementos conectados entre sí, por los que circula una corriente
Objetivos. Equipo y materiales
 Laboratorio Circuitos DC Experimento 3: Fuentes de Voltaje Objetivos Conectar fuentes de voltaje fotovoltaicas en serie, paralelo y serie paralelo Medir corriente de carga en circuitos con fuentes de voltaje
Laboratorio Circuitos DC Experimento 3: Fuentes de Voltaje Objetivos Conectar fuentes de voltaje fotovoltaicas en serie, paralelo y serie paralelo Medir corriente de carga en circuitos con fuentes de voltaje
ELECTRÓLISIS. Electrólisis de sales fundidas
 El proceso por el cual se produce una reacción química a partir de una energía eléctrica se denomina electrólisis. Y se lleva a cabo en un dispositivo que se conoce como cuba o celda electrolítica. Este
El proceso por el cual se produce una reacción química a partir de una energía eléctrica se denomina electrólisis. Y se lleva a cabo en un dispositivo que se conoce como cuba o celda electrolítica. Este
Bloque IV: Electrolisis. Prof. Dr. Mª del Carmen Clemente Jul
 Bloque IV: Electrolisis Prof. Dr. Mª del Carmen Clemente Jul ELECTROLISIS PROCESO EN EL QUE SE UTILIZA LA ENERGÍA ELÉCTRICA PARA PROVOCAR UNA REACCIÓN QUÍMICA (REDOX) NO ESPONTÁNEA ELECTROLISIS DEL NaCl
Bloque IV: Electrolisis Prof. Dr. Mª del Carmen Clemente Jul ELECTROLISIS PROCESO EN EL QUE SE UTILIZA LA ENERGÍA ELÉCTRICA PARA PROVOCAR UNA REACCIÓN QUÍMICA (REDOX) NO ESPONTÁNEA ELECTROLISIS DEL NaCl
GUÍA DEL PROCESO Y PROCEDIMIENTO DE CALIBRACIÓN EN EL ALMACÉN
 1 GUÍA DEL PROCESO Y PROCEDIMIENTO DE CALIBRACIÓN EN EL ALMACÉN TABLA DE CONTENIDO Dispositivos que requieren calibración.... 4 Dispositivos autorizados de calibración.... 4 Prueba de Amperios del Probador
1 GUÍA DEL PROCESO Y PROCEDIMIENTO DE CALIBRACIÓN EN EL ALMACÉN TABLA DE CONTENIDO Dispositivos que requieren calibración.... 4 Dispositivos autorizados de calibración.... 4 Prueba de Amperios del Probador
TEMA 3: ELECTRICIDAD Y ELECTRÓNICA
 TEMA 3: ELECTRICIDAD Y ELECTRÓNICA Francisco Raposo Tecnología 3ºESO 1. INTRODUCCIÓN. LA CARGA ELÉCTRICA Los materiales están formados por átomos que se componen a su vez de: - Electrones: son carga eléctrica
TEMA 3: ELECTRICIDAD Y ELECTRÓNICA Francisco Raposo Tecnología 3ºESO 1. INTRODUCCIÓN. LA CARGA ELÉCTRICA Los materiales están formados por átomos que se componen a su vez de: - Electrones: son carga eléctrica
Sistemas de supervisión de las características y calidad del servicio asociadas al suministro de gas natural: Verificación de la normativa aplicable
 Sistemas de supervisión de las características y calidad del servicio asociadas al suministro de gas natural: Verificación de la normativa aplicable - Odorización en redes de distribución - Protección
Sistemas de supervisión de las características y calidad del servicio asociadas al suministro de gas natural: Verificación de la normativa aplicable - Odorización en redes de distribución - Protección
B Acumuladores de corriente eléctrica
 1 B Acumuladores de corriente eléctrica Condensadores Distintos tipos de condensadores. 2 3 Configuraciones para acoplar condensadores. Pilas y baterías a) Características de las pilas y baterías: Resistencia
1 B Acumuladores de corriente eléctrica Condensadores Distintos tipos de condensadores. 2 3 Configuraciones para acoplar condensadores. Pilas y baterías a) Características de las pilas y baterías: Resistencia
MALPICA TE EXPLICA TOQUES, TOQUES, PASELE JOVEN, TOQUEEEES!
 MALPICA TE EXPLICA SISTEMA ELECTRICO, Alternador, Marcha, Acumulador, (Formas de cambio de Batería y Pasar Corriente), Daños a Computadoras, Tipos de Computadoras y Vínculos entre las mismas. TOQUES, TOQUES,
MALPICA TE EXPLICA SISTEMA ELECTRICO, Alternador, Marcha, Acumulador, (Formas de cambio de Batería y Pasar Corriente), Daños a Computadoras, Tipos de Computadoras y Vínculos entre las mismas. TOQUES, TOQUES,
Co mo funcionan las baterı as?
 Co mo funcionan las baterı as? Imagine un mundo donde todo lo que funcione con electricidad tuviera que estar permanentemente enchufado: Linternas, audífonos, teléfonos móviles y otros dispositivos portátiles
Co mo funcionan las baterı as? Imagine un mundo donde todo lo que funcione con electricidad tuviera que estar permanentemente enchufado: Linternas, audífonos, teléfonos móviles y otros dispositivos portátiles
MANUAL TÉCNICO FILTRO DE POTENCIALES
 MANUAL TÉCNICO FILTRO DE POTENCIALES 1 Introducción a la Protección Catódica p. 2 2 Perjucios de la electrolisis p. 2 3 Filtro de Potenciales p. 4 4 Conexión del Filtro de Potenciales p. 5-1 - 1 Introducción
MANUAL TÉCNICO FILTRO DE POTENCIALES 1 Introducción a la Protección Catódica p. 2 2 Perjucios de la electrolisis p. 2 3 Filtro de Potenciales p. 4 4 Conexión del Filtro de Potenciales p. 5-1 - 1 Introducción
Conducción eléctrica en líquidos
 Conducción eléctrica en líquidos Objetivo El objetivo de este experimento es estudiar si los líquidos conducen o no la electricidad. Para aquellos que sí lo hacen, se propone verificar si satisfacen o
Conducción eléctrica en líquidos Objetivo El objetivo de este experimento es estudiar si los líquidos conducen o no la electricidad. Para aquellos que sí lo hacen, se propone verificar si satisfacen o
ESCUELA SUPERIOR POLITÉCNICA DEL LITORAL INSTITUTO DE CIENCIAS FÍSICAS I TÉRMINO FÍSICA C Segunda evaluación SOLUCIÓN
 ESCUELA SUPERIOR POLITÉCNICA DEL LITORAL INSTITUTO DE CIENCIAS FÍSICAS I TÉRMINO 2012-2013 FÍSICA C Segunda evaluación SOLUCIÓN Pregunta 1 (3 puntos) Un globo de caucho tiene en su interior una carga puntual.
ESCUELA SUPERIOR POLITÉCNICA DEL LITORAL INSTITUTO DE CIENCIAS FÍSICAS I TÉRMINO 2012-2013 FÍSICA C Segunda evaluación SOLUCIÓN Pregunta 1 (3 puntos) Un globo de caucho tiene en su interior una carga puntual.
E.8 Q. Guía de Química FUNCIONES QUÍMICAS. PROSERQUISA DE C.V. - Todos los Derechos Reservados
 FUNCIONES QUÍMICAS Guía de Química EXPERIMENTO N 8 IDENTIFICACIÓN DE FUNCIONES QUIMICAS OBJETVOS: Que el estudiante logre identificar experimentalmente las funciones químicas: Óxido, Ácido, Base y Sal.
FUNCIONES QUÍMICAS Guía de Química EXPERIMENTO N 8 IDENTIFICACIÓN DE FUNCIONES QUIMICAS OBJETVOS: Que el estudiante logre identificar experimentalmente las funciones químicas: Óxido, Ácido, Base y Sal.
SOLDADURA SOLDADURA DE FUSIÓN POR ARCO ELÉCTRICO
 SOLDADURA DEFINICIÓN Es la unión sólida de dos materiales o parte de un material mediante al fusión de sus bordes con calor proveniente de una fuente eléctrica o gaseosa, según el equipo que se emplee
SOLDADURA DEFINICIÓN Es la unión sólida de dos materiales o parte de un material mediante al fusión de sus bordes con calor proveniente de una fuente eléctrica o gaseosa, según el equipo que se emplee
JULIO 2012. FASE ESPECÍFICA. QUÍMICA.
 JULIO 2012. FASE ESPECÍFICA. QUÍMICA. OPCIÓN A 1. (2,5 puntos) Se añaden 10 mg de carbonato de estroncio sólido, SrCO 3 (s), a 2 L de agua pura. Calcule la cantidad de SrCO 3 (s) que queda sin disolver.
JULIO 2012. FASE ESPECÍFICA. QUÍMICA. OPCIÓN A 1. (2,5 puntos) Se añaden 10 mg de carbonato de estroncio sólido, SrCO 3 (s), a 2 L de agua pura. Calcule la cantidad de SrCO 3 (s) que queda sin disolver.
OBJETO DE ENSAYO: Equipo para corrección del factor de potencia
 LABORATORIO DE EQUIPOS ELÉCTRICOS UNIDAD DE ENERGÍA Informe de ensayos Nº B124-06-BJ-EE-01 Página 1 de 15 Ensayos de tipo OBJETO DE ENSAYO: Equipo para corrección del factor de potencia DESIGNACIÓN: EC
LABORATORIO DE EQUIPOS ELÉCTRICOS UNIDAD DE ENERGÍA Informe de ensayos Nº B124-06-BJ-EE-01 Página 1 de 15 Ensayos de tipo OBJETO DE ENSAYO: Equipo para corrección del factor de potencia DESIGNACIÓN: EC
A C E S. El sistema ACES no requiere manutención, gracias a la eliminación de los agujeros provocados de la corrosión. s.r.l.
 A C E S SISTEMA ELECTRÓNICO ANTICORROSIÓN EUROPEAN PATENT NR. 0630426 Sistema de protección catódica por corriente impresa ACES G2 para depósitos esmaltados de hasta 1.000 litros ACES para depósitos esmaltados
A C E S SISTEMA ELECTRÓNICO ANTICORROSIÓN EUROPEAN PATENT NR. 0630426 Sistema de protección catódica por corriente impresa ACES G2 para depósitos esmaltados de hasta 1.000 litros ACES para depósitos esmaltados
EL PRAE EN LA UNIDAD PEDAGÓGICA: UN COMPROMISO DE TODOS
 EL PRAE EN LA UNIDAD PEDAGÓGICA: UN COMPROMISO DE TODOS RECICLAJE DE PILAS JUSTIFICACIÓN Una batería o pila es un dispositivo que almacena energía química para ser liberada más tarde como electricidad.
EL PRAE EN LA UNIDAD PEDAGÓGICA: UN COMPROMISO DE TODOS RECICLAJE DE PILAS JUSTIFICACIÓN Una batería o pila es un dispositivo que almacena energía química para ser liberada más tarde como electricidad.
PROBLEMAS RESUELTOS SELECTIVIDAD ANDALUCÍA 2006 QUÍMICA TEMA 7: REACCIONES REDOX
 PROBLEMAS RESUELTOS SELECTIVIDAD ANDALUCÍA 006 QUÍMICA TEMA 7: REACCIONES REDOX Junio, Ejercicio, Opción A Junio, Ejercicio 6, Opción B Reserva 1, Ejercicio, Opción A Reserva 1, Ejercicio 6, Opción B Reserva,
PROBLEMAS RESUELTOS SELECTIVIDAD ANDALUCÍA 006 QUÍMICA TEMA 7: REACCIONES REDOX Junio, Ejercicio, Opción A Junio, Ejercicio 6, Opción B Reserva 1, Ejercicio, Opción A Reserva 1, Ejercicio 6, Opción B Reserva,
En el siguiente informe trataremos la ley de ohms desde una perspectiva practica.
 GUIA DE LABORATORIO NUMERO 1 USO DEL MULTITESTER LEY DE OHM (c) año 2001 INTRODUCCIÓN En el siguiente informe trataremos la ley de ohms desde una perspectiva practica. Con la ayuda de experiencias practicas
GUIA DE LABORATORIO NUMERO 1 USO DEL MULTITESTER LEY DE OHM (c) año 2001 INTRODUCCIÓN En el siguiente informe trataremos la ley de ohms desde una perspectiva practica. Con la ayuda de experiencias practicas
La electricidad. La electricidad se origina por la separación o movimiento de los electrones que forman los átomos.
 1 La electricidad Es el conjunto de fenómenos físicos relacionados con la presencia y flujo de cargas eléctricas. Se manifiesta en una gran variedad de fenómenos como los rayos, la electricidad estática,
1 La electricidad Es el conjunto de fenómenos físicos relacionados con la presencia y flujo de cargas eléctricas. Se manifiesta en una gran variedad de fenómenos como los rayos, la electricidad estática,
CIRCUITOS RESISTENCIAS RESISTENCIA INTERNA DE UNA BATERIA.
 CIRCUITOS RESISTENCIAS RESISTENCIA INTERNA DE UNA BATERIA. RESISTENCIAS EN SERIE: Cuando la corriente puede seguir una sola trayectoria al fluir a través de dos o más resistores conectados en línea, se
CIRCUITOS RESISTENCIAS RESISTENCIA INTERNA DE UNA BATERIA. RESISTENCIAS EN SERIE: Cuando la corriente puede seguir una sola trayectoria al fluir a través de dos o más resistores conectados en línea, se
SIMULACIÓN CON PROTEUS
 UNIVERSIDAD DEL VALLE ESCUELA DE INGENIERIA ELÉCTRICA Y ELÉCTRONICA CÁTEDRA DE PERCEPCIÓN Y SISTEMAS INTELIGENTES LABORATORIO 2: PROTEUS 1. OBJETIVOS SIMULACIÓN CON PROTEUS Introducir al estudiante en
UNIVERSIDAD DEL VALLE ESCUELA DE INGENIERIA ELÉCTRICA Y ELÉCTRONICA CÁTEDRA DE PERCEPCIÓN Y SISTEMAS INTELIGENTES LABORATORIO 2: PROTEUS 1. OBJETIVOS SIMULACIÓN CON PROTEUS Introducir al estudiante en
Programa de Responsabilidad Social
 Programa de Responsabilidad Social El objetivo del Programa de responsabilidad Social de Solartec Energía en movimiento es una feria rodante donde se expone a las comunidades rurales, escuelas y al publico
Programa de Responsabilidad Social El objetivo del Programa de responsabilidad Social de Solartec Energía en movimiento es una feria rodante donde se expone a las comunidades rurales, escuelas y al publico
REACCIONES DE TRANSFERENCIA DE ELECTRONES SEPTIEMBRE 2015
 REACCIONES DE TRANSFERENCIA DE ELECTRONES SEPTIEMBRE 2015 1- El permanganato de potasio actúa como oxidante en medio ácido, dando como producto Mn 2+. Por el contrario, como oxidante en medio básico el
REACCIONES DE TRANSFERENCIA DE ELECTRONES SEPTIEMBRE 2015 1- El permanganato de potasio actúa como oxidante en medio ácido, dando como producto Mn 2+. Por el contrario, como oxidante en medio básico el
MANUAL DE UTILIZACION
 MANUAL DE UTILIZACION SERIE XAP Modelos XAP-30 XAP-30P REV. 1A09M12 1 2 DETALLES TECNICOS Condiciones de trabajo * Alimentación: 4 x pilas secas tamaño C Alimentador AC/DC (DC 5,5V~ 8V, 200mA). * Temperatura
MANUAL DE UTILIZACION SERIE XAP Modelos XAP-30 XAP-30P REV. 1A09M12 1 2 DETALLES TECNICOS Condiciones de trabajo * Alimentación: 4 x pilas secas tamaño C Alimentador AC/DC (DC 5,5V~ 8V, 200mA). * Temperatura
Aplicar la ley de ohm, en el desarrollo de ejercicios..
 Corriente eléctrica Aplicar la ley de ohm, en el desarrollo de ejercicios.. En términos simples, la electricidad corresponde al movimiento de cargas eléctricas. Las cargas que pueden moverse son los electrones
Corriente eléctrica Aplicar la ley de ohm, en el desarrollo de ejercicios.. En términos simples, la electricidad corresponde al movimiento de cargas eléctricas. Las cargas que pueden moverse son los electrones
elab 3D Práctica 2 Diodos
 UNIVERSIDAD POLITÉCNICA DE MADRID ESCUELA TECNICA SUPERIOR DE INGENIERIA Y SISTEMAS DE TELECOMUNICACIÓN elab 3D Práctica 2 Diodos Curso 2013/2014 Departamento de Sistemas Electrónicos y de Control 1. Introducción
UNIVERSIDAD POLITÉCNICA DE MADRID ESCUELA TECNICA SUPERIOR DE INGENIERIA Y SISTEMAS DE TELECOMUNICACIÓN elab 3D Práctica 2 Diodos Curso 2013/2014 Departamento de Sistemas Electrónicos y de Control 1. Introducción
REACCIONES DE TRANSFERENCIA DE ELECTRONES
 REACCIONES DE TRANSFERENCIA DE ELECTRONES REACCIONES REDOX son aquellas en las que cambian el número de oxidación de algún elemento. En estas reacciones hay intercambio de electrones por lo que no se pueden
REACCIONES DE TRANSFERENCIA DE ELECTRONES REACCIONES REDOX son aquellas en las que cambian el número de oxidación de algún elemento. En estas reacciones hay intercambio de electrones por lo que no se pueden
ELECTROQUÍMICA. 1. Procesos electroquímicos (pila). 2. Potenciales normales de electrodo. 3. Ecuación de Nernst. 4. Electrolisis. 5. Leyes de Faraday.
 ELECTROQUÍMICA 1. Procesos electroquímicos (pila). 2. Potenciales normales de electrodo. 3. Ecuación de Nernst. 4. Electrolisis. 5. Leyes de Faraday. Química 2º bachillerato Electroquímica 1 0. CONOCIMIENTOS
ELECTROQUÍMICA 1. Procesos electroquímicos (pila). 2. Potenciales normales de electrodo. 3. Ecuación de Nernst. 4. Electrolisis. 5. Leyes de Faraday. Química 2º bachillerato Electroquímica 1 0. CONOCIMIENTOS
Fuente de alimentación de corriente continua (CC) de baja tensión y salidas múltiples Resistores fijos y variables Cables de conexión
 FISICA GENERAL III 2012 Guía de Trabajo Practico N o 8 Galvanómetro de las tangentes Ley de Faraday - Regla de Lenz R. Comes y R. Bürgesser Objetivos: Verificar, por medio de una brújula, que el campo
FISICA GENERAL III 2012 Guía de Trabajo Practico N o 8 Galvanómetro de las tangentes Ley de Faraday - Regla de Lenz R. Comes y R. Bürgesser Objetivos: Verificar, por medio de una brújula, que el campo
Conceptos Básicos de la Protección Catódica
 Charla de Seguridad Conceptos Básicos de la Protección Catódica Preparado por: Javier Cabezas C. Fecha: 28-04-10 Contenidos de la Presentación Qué es la Corrosión? Mecanismo de corrosión. Tipos de Corrosión.
Charla de Seguridad Conceptos Básicos de la Protección Catódica Preparado por: Javier Cabezas C. Fecha: 28-04-10 Contenidos de la Presentación Qué es la Corrosión? Mecanismo de corrosión. Tipos de Corrosión.
M A Y O A C T U A L I Z A D A
 U N I V E R S I D A D N A C I O N A L E X P E R I M E N T A L F R A N C I S C O D E M I R A N D A C O M P L E J O A C A D É M I C O E L S A B I N O Á R E A D E T E C N O L O G Í A D E P A R T A M E N T
U N I V E R S I D A D N A C I O N A L E X P E R I M E N T A L F R A N C I S C O D E M I R A N D A C O M P L E J O A C A D É M I C O E L S A B I N O Á R E A D E T E C N O L O G Í A D E P A R T A M E N T
CORRIENTE CONTINUA I : RESISTENCIA INTERNA DE UNA FUENTE
 eman ta zabal zazu Departamento de Física de la Materia Condensada universidad del país vasco euskal herriko unibertsitatea FACULTAD DE CIENCIA Y TECNOLOGÍA UNIVERSIDAD DEL PAÍS VASCO DEPARTAMENTO de FÍSICA
eman ta zabal zazu Departamento de Física de la Materia Condensada universidad del país vasco euskal herriko unibertsitatea FACULTAD DE CIENCIA Y TECNOLOGÍA UNIVERSIDAD DEL PAÍS VASCO DEPARTAMENTO de FÍSICA
