IMAGINACIÓN Y CREATIVIDAD EXPERIMENTOS SENCILLOS Y ECONÓMICOS
|
|
|
- Luis Miguel Muñoz Silva
- hace 8 años
- Vistas:
Transcripción
1 IMAGINACIÓN Y CREATIVIDAD EXPERIMENTOS SENCILLOS Y ECONÓMICOS
2 Universidad de Los Andes Facultad de Ciencias Departamento de Química IMAGINACIÓN Y CREATIVIDAD EXPERIMENTOS SENCILLOS Y ECONÓMICOS Yris Martínez Ricardo Hernández VI Escuela Venezolana para la Enseñanza de la Química Mérida, del 05 al 10 de Diciembre de 2004 ii
3 Imaginación y creatividad Experimentos sencillos y económicos VI ESCUELA VENEZOLANA PARA LA ENSEÑANZA DE LA QUÍMICA Edición 2004 El libro IMAGINACIÓN Y CREATIVIDAD EXPERIMENTOS SENCILLOS Y ECONÓMICOS, fue escrito especialmente como material de apoyo de uno de los cursos ofrecidos en la VI Escuela Venezolana para la Enseñanza de la Química. La Escuela es un programa organizado por CELCIEC-ULA, diseñada en base a Cursos de Actualización dirigidos a los docentes de Química de la Educación Básica, Media y Diversificada. Evaluación de la edición: Bernardo Fontal, Ricardo Contreras Comité organizador del VI Encuentro con la Química: Bernardo Fontal, Fernando Bellandi, Marisela Reyes, Ricardo Contreras Autor: Yris Martínez Ricardo Hernández Portada: Diseño y diagramación: ymartin@ula.ve rmhr@ula.ve Yanelly Gavidia Smart Service C.A. Se autoriza la reproducción parcial y total de esta obra, únicamente para fines de enseñanza, respetando los créditos del VI Escuela Venezolana para la Enseñanza de la Química y de los autores. Derechos reservados 2004, Universidad de Los Andes, Facultad de Ciencias, Departamento de Química, Laboratorio de Organometálicos La Hechicera, Mérida 5101, Venezuela. Tlf.: , Fax: , escueladequimica@hotmail.com Hecho en Venezuela Depósito legal: LF iii
4 Universidad de Los Andes Facultad de Ciencias Departamento de Química TABLA DE CONTENIDO Seguridad En El Laboratorio Cómo Realizar Experiencias Sencillas.? 1 Extintor Casero (Química General) 2 Convirtiendo Cobre En Oro. (Electroquímica) 3 Formación De Diferentes Compuestos Químicos (Química General) 4 Figuras De Plata. (Electroquímica) 5 Oxidación De Hierro Y Reducción De Cobre. (Electroquímica) 6 Formación De MgO. (Electroquímica) 7 Un Volcán En El Laboratorio. (Electroquímica) 8 Proceso De Corrosión. (Electroquímica) 9 Conductividad En Materiales. (Electroquímica) 10 Conductividad Y Electrolitos. (Electroquímica) 11 Electrólisis Celda De 1 Compartimiento. (Electroquímica) 12 Electrolisis Celda De 2 Compartimientos. (Electroquímica) 13 Cobreado De Monedas. (Electroquímica) 14 Celdas En Serie. (Electroquímica) 15 Electrólisis Del KI. (Electroquímica) 16 Electrólisis Del Agua. (Electroquímica) 17 Electrolisis Del Cloruro De Sodio. (Electroquímica) 18 Electrolisis Sencilla A. (Electroquímica) 19 Electrolisis Sencilla B. (Electroquímica) iv
5 Imaginación y creatividad Experimentos sencillos y económicos 20 Lápiz Eléctrico. (Electroquímica) 21 Reducción De Cobre Por Hidrólisis. (Electroquímica) 22 Cómo Es Una Batería?. (Electroquímica) 23 Batería De Limón.. (Electroquímica) 24 Reloj De Papa. (Electroquímica) 25 Batería Casera. (Electroquímica) 26 Limpieza De Materiales De Plata. (Electroquímica) 27 Alcoholimetro. (Electroquímica) 28 Sensor De CO2. (Electroquímica) 29 Indicador De Repollo Morado. (Química General) 30 Test De Respiración. (Química General) 31 Otro Indicador. (Química General) 32 Bibliografía v
6
7 Imaginación y creatividad Experimentos sencillos y económicos IMAGINACIÓN Y CREATIVIDAD EXPERIMENTOS SENCILLOS Y ECONÓMICOS SEGURIDAD EN ELL LLABORATTORI RIO O Cuando se trabaja en un laboratorio existe el peligro potencial de un ACCIDENTE, en virtud de las sustancias y elementos que se utilizan, y la posibilidad de cometer algún error al realizar un experimento. SUSTANCIA PELIGROSA + ERROR HUMANO = ACCIDENTE Por eso, cuando se trabaja en el laboratorio, deben tenerse presente una serie de reglas o consejos que disminuyen y en algunos casos logran evitar los accidentes. Manténgase informado de los riesgos y actitudes que debe tomar al manipular ciertas sustancias. Como primera regla, para empezar a trabajar: EL LUGAR DE TRABAJO DEBE ESTAR EN ORDEN Es conveniente no olvidar estas REGLAS / CONSEJOS: 1. INDICACIONES. El profesor debe dar a sus estudiantes todas las indicaciones de seguridad necesarias antes de realizar cada práctica 1. ESTUDIE CADA EXPERIENCIA ANTES DE CLASE Ahorrará tiempo y evitará errores y accidentes innecesarios 2. SEGURIDAD DE TODOS. El laboratorio es un lugar para trabajar con seriedad. Todos deben tomar conciencia de la importancia de trabajar con seguridad. 3. COMUNICAR LOS ACCIDENTES. Instruya al estudiante para que comunique con toda confianza, cualquier accidente al profesor o ayudante de laboratorio inmediatamente. 1
8 Universidad de Los Andes Facultad de Ciencias Departamento de Química 4. VERTIDO DE SUSTANCIAS. El trabajo debe hacerse con precaución. Este pendiente para actuar por si algo se derrama. 5. CALENTAMIENTO DE TUBOS DE ENSAYO. No se debe mirar al interior del tubo durante el calentamiento, ni apuntar durante el calentamiento la boca del tubo de ensayo hacia otro compañero es algo de lo que debe estar muy pendiente. 6. CALENTAMIENTO DE LÍQUIDOS EN TUBOS DE ENSAYO. No deben llenar los tubos, si no se toma esta precaución el vapor que asciende rápidamente y no podrá controlar proyecciones del contenido fuera del tubo. 7. OLOR DE LAS SUSTANCIAS. Antes de intentar percibir los olores de cualquier sustancia debe asegurarse con base en la literatura de la toxicidad del compuesto. Si es seguro, mueva con suavidad la mano desde la boca del recipiente hacia su nariz e inspire con precaución. No intente percibir olores si no tiene información de la sustancia contenida. 8. LIQUIDOS VOLÁTILES. Se deben almacenar en lugares frescos. Durante su trasvase o uso se deben evitar el uso de mecheros. 9. RECIPIENTES CON GRANDES VOLÚMENES DE SUSTANCIAS PELIGROSAS. Deben ser manipulados por el profesor o ayudante de laboratorio. 10. PREPARACIÓN DE ÁCIDOS DILUIDOS. Nunca agregue agua sobre un ácido. Agregue siempre el ácido concentrado, en pequeñas cantidades, sobre el agua y agite continuamente. 11. SUSTANCIAS CORROSIVAS. (Ácidos o álcalis concentrados). Manipule las mismas con máximo cuidado y empleando guantes protectores. 12. TRABAJO CON VIDRIO Al calentar material de vidrio permita que se enfríe antes de cualquier manipulación posterior o utilice una pinza o guante apropiado. 13. TAPONES Y CONEXIONES DE GOMA EN MATERIALES QUEBRADIZOS. Nunca fuerce dentro o fuera los conectores de goma en tubos de vidrio o cualquier otro material que se pueda quebrar. La glicerina o el detergente facilitan la tarea de quitar dichos nexos. 14. NUNCA COMER, BEBER O FUMAR ni dejar alimentos sobre el mesón del laboratorio. 2
9 Imaginación y creatividad Experimentos sencillos y económicos 15. VENTILACIÓN. Conviene trabajar siempre en un lugar bien ventilado. 16. ACCESO AL LABORATORIO. La puerta de acceso al laboratorio deberá abrir hacia afuera. Así, en caso de emergencia el desalojo del mismo se facilitará. 17. CABELLO LARGO. Se deberá atar el cabello largo para evitar accidentes con la llama del mechero. 18. NUNCA CALIENTE. Cosas en sistemas cerrados; la presión generada puede hacerlos explotar. 19. ARMADO DE EQUIPOS Se deberá usar soportes que se apoyen bien en la mesa. Especialmente se deben asegurar y vigilar continuamente los aparatos con centro de gravedad alto. 20. PRIMEROS AUXILIOS Es imprescindible contar con un adecuado equipo para primeros auxilios y conocer los pasos a seguir en cada caso luego de un accidente. En casos serios se deberá llamar a un especialista de la salud. 21. SUSTANCIAS CORROSIVAS EN CONTACTO CON PIEL y/u OJOS. Lavar inmediatamente con abundante agua. Consultar al especialista. Si el corrosivo es ácido, enjuáguese con solución de bicarbonato de sodio al 5% p/v. En el caso de un álcali, enjuáguese con vinagre (ácido acético) al 5% v/v 22. LIMPIEZA DEL MATERIAL Todo el material que se utiliza debe ser limpiado al finalizar, fin de evitar contaminaciones y/o reacciones no deseadas en posteriores experimentos. 3
10 Universidad de Los Andes Facultad de Ciencias Departamento de Química EXPERIMENTOS Cómo realizar experiencias sencillas.? Vivimos en un constante cambio, diariamente en la naturaleza ocurren cambios químicos y se forman nuevos compuestos. Los frutos se maduran, los alimentos que consumimos son producto de los cambios ocurridos en la cocción, los jugos se fermentan y se producen vinos, las plantas crecen, las sustancias que lanzamos al ambiente sufren transformaciones químicas y forman nuevas sustancias, algunas de las cuales son dañinas para los seres vivientes. Vivimos en un universo que está en constante cambio. Algunos de esos cambios de la materia son factibles de realizar mediante experiencias sencillas. Para hacer química, no necesariamente debemos contar con un laboratorio equipado con instrumentos muy sofisticados, algunos de estos pueden ser sustituidos por instrumentos y equipos caseros de fácil construcción. Con imaginación y creatividad se puede llegar a realizar experiencias sencillas y económicas que estimularían a penetrar el maravilloso mundo de la química. FFoorrmaacci ióónn Dee Difeerreennt teess Coomppuueesst tooss Quuí ímiccooss De forma general indicamos como obtener algunos componentes químicos con experimentos sencillos. El hidróxido de calcio se forma al agregar agua a la cal viva, el cloruro de zinc se forma de la reacción entre el zinc metálico y el ácido muriático (ácido clorhídrico), desprendiéndose hidrógeno en la reacción. El Cloruro de zinc puede ser formado a partir de pedazos de Zinc metálico (tomado de las baterías) al cual se le agrega poco a poco ácido muriático (HCL); Durante la reacción que ocurre es: Zn + 2HCL ZnCl 2 + H 2 se desprende hidrógeno y se forma la sal del metal. 4
11 Imaginación y creatividad Experimentos sencillos y económicos Otra experiencia que se podría practicar es quemar cintas de magnesio y luego agregar agua al residuo que se obtiene al quemar la cinta. (Hidróxido de magnesio) el cual es el principio activo en medicamentos para la acidez ya que este neutraliza la acción del ácido clorhídrico en el estómago produciendo cloruro de magnesio y agua. Un ejercicio interesante consiste en estudiar la reacción que ocurre al sumergir un huevo en vinagre. Qué compuesto se forma? Por qué? ácidos y bases caseros ácido o base ácido acético ácido acetil salicílico ácido ascórbico ácido sulfurico diluido ácido cítrico ácido clorhídrico ácido sulfúrico Hidróxido de sodio amoníaco (base) hidróxido de magnesio (base) donde se encuentra Vinagre Aspirina vitamina C Ácido de batería zumo de cítricos sal fumante para limpieza, jugos gástricos baterías de coches Destapa cañerías diablo rojo Algunos limpiadores caseros leche de magnesia (laxante y antiácido 5
12 Universidad de Los Andes Facultad de Ciencias Departamento de Química Otro compuesto químico que podemos obtener aprovechando recursos naturales, es el alcohol. En este caso el tratamiento es sencillo pero más laborioso. Se pueden utilizar los siguientes alimentos: una yuca rayada, o 2 papas rayadas, o una piña, o 3 trozos de caña de azúcar machacada, o 3 manzanas picadas, y 2litros de agua. El agua se pone a hervir y se deja enfriar en un botellón de vidrio, agregando luego cada uno de los componentes, los cuales deben ser mantenidos allí por espacio de 8 días. Mantenga por seguridad un pequeño orificio en la tapa para que escape el aire. De esta manera se obtiene el alcohol mediante el proceso de fermentación. Luego de ocho días se procede a la pasteurización, colocando el fermento en un depósito de aluminio y este a su vez se coloca en un baño de agua helada, matando así las bacterias que se producen. Finalmente se proceda a realizar una destilación a 80 para obtener el alcohol lo más puro posible. Existen alternativas que se pueden sugerir para realizar algunas actividades, en caso de no contar en la institución con un laboratorio químico bien dotado, por ejemplo: Fabricación de un mechero de alcohol en sustitución del mechero de Bunsen: con un frasco de compota (el cual resiste altas temperaturas), haciendo un hueco en la tapa por donde se pasa la mecha y se le agrega alcohol de 90. Un embudo puede realizarse a partir de una botella plástica de cuello largo y angosto cortada a la mitad. Vasos de precipitado sustituidos por frascos de compotas o de mayonesa. Los tubos de ensayo pueden ser frascos de medicinas pequeños. Los tubos de ensayo pueden ser sujetados por pinzas para colgar ropa (de madera. ) Probeta calibrada en centímetros cúbicos por un tetero con medidas. Mortero y pistilo de los usados en la cocina. Las jeringas desechables son muy apropiadas para diseñar aparatos o usarlas como instrumentos de medida, como por ejemplo mini buretas A los goteros de algunas medicinas también le podemos sacar buen provecho. 6
13 Imaginación y creatividad Experimentos sencillos y económicos Existen laxantes (chicles) cuyo principio activo es la fenoltaleina, estos pueden ser usados como indicadores. Además, en nuestro entorno tropical podemos encontrar flores de colores intensos que proporcionan, mediante extracción con alcohol etílico, compuestos coloreados con propiedades ácido-base que permiten usarlos como indicadores. Clavos de hierro, alambre de cobre, las agujas de las inyectadoras, el grafito que contienen la pilas, lápices de grafito, el metal que las recubre, latas de refrescos; entre otros pueden ser utilizados como conductores. Así, son muchos los materiales que con el ingenio y creatividad pueden ser utilizados para realizar diversas experiencias de laboratorio que permiten demostrar los principios básicos de la ciencia. No olvidemos que en nuestras casas, permanentemente estamos haciendo química. Nuestras abuelas acostumbran recetar remedios caseros cuando sentimos algún malestar; como ejemplos de ello teníamos que ante una picadura de hormiga o de una abeja se suele poner en la picadura bicarbonato, si es de una avispa se la trata con vinagre, si sentimos acidez nos dan leche de magnesia o bicarbonato, cuando se oxida una pieza de hierro la tratan con ácido muriático, una prenda de vestir con manchas de hierro es tratada con limón y sal expuesta luego al sol, los suelos demasiado ácidos los tratan con cal viva o cal apagada, si tienen poca acidez con azufre en polvo o sulfato de hierro (II). Así podemos seguir mencionando muchos ejemplos más. Un buen ejercicio sería analizar cada uno de los procesos descritos anteriormente, preguntándonos por ejemplo: (a) Por qué se produce la acidez en el estómago? (b) Si la acidez es por causa de de un ácido; Cómo deben ser los productos que se han de usar para tratar la acidez del estómago? (c) Qué sucede cuando se toma leche de magnesia? Algunas de las conclusiones a las que se puede llegar son: (a) El jugo gástrico contiene un ácido. (b) Las sustancias que se utilizan para tratar el exceso de acidez del estómago deben ser hidróxidos o bases. (c) La reacción de ácidos con bases causa la neutralización de los mismos. (d) La leche de magnesia debe ser una base dado que neutralizan la acidez. (e) La reacción que ocurre es una reacción de neutralización. 7
14 Universidad de Los Andes Facultad de Ciencias Departamento de Química EXPERIMENTO Nº1 EXTINTOR CASERO Este es un dispositivo que pudiera mantenerse siempre a la mano cuando estamos realizando practicas en las que exista la posibilidad de un incendio. Los extintores de fuego trabajan ahogando el fuego. Eliminan el oxígeno que el fuego necesita para arder y de esta manera detienen la combustión. Materiales: Bicarbonato, tapón de corcho de una botella de vino, pitillo, servilletas de papel, botella de refresco, vinagre, un hilo de los que se utilizan para coser PRROOCCEEDDI IIMMI IIEENNTTOO 1.- Abra la servilleta de papel, y coloque en ella 4 cucharaditas de bicarbonato (en el centro) y ciérrala por los extremos, en forma de bolsita, usando para ello el hilo (tiene que quedar bien sujeto). Después en la botella se agregan 5 mililitros vinagre. 2.- Al corcho se le hace un agujero en el centro, suficientemente amplio para que pueda entrar el pitillo. Si no se tiene un corcho, se puede utilizar el tapón de plástico de la botella tapando los huecos con plastilina o silicona. 3.- Seguidamente se toma la bolsita de bicarbonato y se mete en la botella de forma que cuelgue (con una parte del hilo fuera) evitando que toque el vinagre agregado previamente. 4.- Se introduce el pitillo en el corcho y con este se tapa la botella. El corcho se puede fijar cuidadosamente con cera derretida o silicona. Debe evitarse el contacto del 8
15 Imaginación y creatividad Experimentos sencillos y económicos vinagre con el bicarbonato si no va hacer utilizada inmediatamente, ya que la reacción entre el bicarbonato y el vinagre (ácido acético) genera gran cantidad de dióxido de carbono (CO 2 ) de acuerdo con la siguiente ecuación: NaHCO 3 + CH 3 COOH CH 3 COO - Na + + H 2 O +CO 2 La reacción química entre el bicarbonato de sodio y el vinagre produce dióxido de carbono. El gas produce presión contra el corcho y sale por el pitillo porque el gas de alguna manera tiene que abrirse paso. El dióxido de carbono es el gas que las personas y los animales expulsan cuando respiran. Puede que no parezca muy poderoso, pero este experimento muestra lo contrario! Cómo apaga una llama el dióxido de carbono? Las moléculas del CO 2 en contacto con la llama se agrupan alrededor de la llama y esta muere por no tener oxígeno. Por ultimo, para saber si el experimento funciona, encendemos una vela. Tapamos con el dedo el pitillo sujetando la botella al mismo tiempo, mezclamos el bicarbonato con el vinagre y agitamos, sin destapar el pitillo. Quitamos el dedo y proyectamos el gas que sale de la botella sobre la vela que se apaga. NOTA: Recuerda que se trata de un extintor casero y sólo sirve para apagar una llama pequeña. 9
16 Universidad de Los Andes Facultad de Ciencias Departamento de Química EXPERIMENTO Nº2 COONNVVI IIRRTTI IIEENNDDOO COOBBRREE EENN ORROO En este caso vamos a formar una aleación, la cual es una mezcla homogénea de dos o más metales (y excepcionalmente algún nometal) con características y propiedades metálicas superiores a la de los metales que la conforman en su estado puro; como ejemplo tenemos al bronce. Este es un experimento muy interesante en el se pretende convertir el metal base en oro, el que fue uno de los mayores retos de los alquimistas. Materiales: Una cápsula para evaporar, una moneda de cobre, zinc en polvo, una solución de hidróxido de sodio 6 M (24 g/100 cm 3 ) PRROOCCEEDDI IIMMI IIEENNTTOO 1.- Coloque 5 gramos de Zinc, en polvo o en virutas, en la cápsula y añada 25 ml de la solución de NaOH 6M y caliente con el mechero. Una reacción toma lugar al calentar formando inmediatamente Na 2 Zn(OH) Deje enfriar y añada la moneda de cobre que ha sido previamente pulida (para eliminar los óxidos superficiales). La moneda debe estar en contacto con el Zinc por 2 ó 3 minutos. 3.- Con una pinza remueva la moneda de la cápsula y lávela con abundante agua y séquela suave y cuidadosamente ya que si lo hace muy fuerte puede eliminar la fina cubierta. Usando nuevamente unas tenazas coloque la moneda a la llama hasta que se torne color oro. Enfríe y lave la moneda con agua. Por qué ocurre esto? Cuando la solución de hidróxido de sodio se pone en contacto con el Zinc la reacción que toma lugar es: Zn + 2NaOH +2H 2 0 Na 2 Zn(OH) 4 + H 2 10
17 Imaginación y creatividad Experimentos sencillos y económicos Cuando la moneda es colocada en la cápsula se forma una celda electroquímica: Zn Zn e - El zinc disuelto se deposita sobre la moneda de cobre, de acuerdo con la siguiente ecuación: Zn(OH) e - Zn + 2e - Cuando la moneda plateada es calentada el zinc se funde y a su vez algo de cobre se funde también lo que produce la aleación con ese bello color dorado que a muchos alquimistas engaño durante años. NOTA: El NaOH necesario para esta práctica, en caso de no tener el NaOH grado analítico puede ser sustituido utilizando algún producto para destapar cañerías, por ejemplo, Diablo rojo. CUIDADO: El NaOH es una base extremadamente agresiva!! Su efecto se neutraliza con vinagre. Por qué? EXPERIMENTO Nº3 FFI IIGGUURRAASS DDEE PLLAATTAA Otro experimento muy interesante es el que resulta de colocar una lamina de cobre en una solución de nitrato de plata. Si a esta lamina le das diferentes formas puedes obtener un bello diseño con unos cristales espectaculares, la parte interesante de este experimento radica en las reacciones que ocurren. La plata es reducida en el cobre y forma los cristales de plata. Una explicación esquemática del proceso que ocurre esta representada en la figura. 11
18 Universidad de Los Andes Facultad de Ciencias Departamento de Química Figura 1.- "Arbol de Navidad de Plata y Cobre" oxidación de hierro y reducción de cobre Algo similar ocurre cuando se usa un clavo de hierro en una solución se sulfato de cobre; rápidamente se deposita el cobre sobre el clavo de hierro. En estos casos el fenómeno que se observa es motivado por la reactividad de cada metal. En la "antigüedad" se decía que el hierro del clavo había sido "desplazado" por el Cu (II) presente en la solución. Lo que está ocurriendo en este caso es ni más ni menos que una auténtica reacción redox. Procedimiento: En el vaso de precipitación haz una solución de sulfato de cobre e introduce el clavo de hierro durante cinco minutos. Describe la reacción que ha ocurrido. 12
19 Imaginación y creatividad Experimentos sencillos y económicos Las ecuaciones de reducción involucradas en este experimento son: Fe e - ---> Fe 0 E 0 = V Cu e - ---> Cu 0 E 0 = V Como sabemos las reacciones ocurren espontáneamente si la energía libre del proceso ( G 0 ) tiene un valor negativo; es decir: G<0 Además sabemos que G 0 = -nfe 0 Donde n, es el número de electrones transferidos, F constante de Faraday, E es el potencial estándar de reducción. Por lo tanto si introducimos los valores de potencial estándar para las dos semi-celdas obtenemos: G o Cu+2/Cuo = -2. (96498 C./mol).(0.342 Volts) = ,74 Joules /mol <0 G o Fe+3/Feo = -2. (96498 C/mol).(-0.037Volts) = Joules/mol >0 Por lo tanto, de acuerdo con este resultado la reducción de Cu 2+ ocurriría espontáneamente, mientras que la correspondiente a Fe 3+ no lo hará. De esta manera, si sumamos las dos semi-reacciones cambiando el sentido de aquella correspondiente al hierro, obtenemos: 3(Cu e - ---> Cu 0 ) E 0 = V 2(Fe 0 ---> Fe e) E 0 = V 3Cu Fe 0 --->3Cu 0 + Fe 3+ ) E = V Sustituye el hierro por zinc y explica el proceso. La figura a continuación te servirá de ayuda. 13
20 Universidad de Los Andes Facultad de Ciencias Departamento de Química Figura 2.- Deposición espontánea de cobre sobre una barra de zinc Otros ejemplos similares que representan el mismo fenómeno, pero variando las reacciones involucradas por supuesto. Pueden ser ilustrados cuando colocamos un clavo de hierro en una solución que contiene 5% de SnCl 2. En otro experimento al colocar un trozo de Zinc en una solución al 5% de acetato de plomo, se observa que el proceso ocurre rápidamente pero los cristales bien definidos se observan luego de media hora. Las reacciones que explican el proceso son: Sn 2+ (ac) + 2Cl - (ac) + Fe(s) Sn(s) + Fe +2 (ac) + 2Cl - (ac) Pb 2+ (ac) + (CH 3 COO - ) 2(ac) + Zn Pb (s) + Zn +2 (ac) + (OCH 3 CO - ) 2(ac) FFOORRMMACCI A IIÓÓNN DDEE OOXXI IIDDOO DDEE MMAAGGNNEESSI IIOO Oxidación de magnesio con oxígeno: La distribución electrónica del magnesio es 1s 2 2s 2 2p 6 3s 2 en su estado metálico fundamental. Cuando el magnesio se oxida pierde los electrones de su última capa y por lo tanto tiene un número de oxidación de
21 Imaginación y creatividad Experimentos sencillos y económicos Materiales: Pinza, cinta de Mg, mechero. Procedimiento: 1.- Toma con una pinza un trozo de unos 3 cm de cinta de Mg. La cinta de magnesio tiene un color plomizo. 2.- Pon en contacto la cinta de magnesio con la llama del mechero. Al ponerse en contacto con el calor, la cinta de magnesio se oxida. Se obtiene el óxido de magnesio (MgO). La reacción es la siguiente: 2 Mg +O 2 ---> 2 MgO Ha ocurrido una reacción de oxidación-reducción. Mg ---> Mg 2+ : El magnesio se oxida; pierde dos electrones O 2 ---> O 2- : El oxígeno se reduce; gana dos electrones EXPERIMENTTO Nº º66 UNN VOOLLCÁÁNN C ENN ELL LLAABBOORRAATTOORRI IIOO Demostración de una reacción redox en fase sólida iniciada térmicamente y autocatalizada por el calor generado por ella misma Materiales: Fósforos, fuente, y espátula, dicromato de amonio PRROOCCEEDDI IIMMI IIEENNTTOO Forma una pequeña montaña con el dicromato de amonio sobre una fuente que te permita una fácil limpieza una vez finalizado el experimento. Desde el extremo superior de la montaña enciende el dicromato con un fósforo. 15
22 REACCIÓN: Universidad de Los Andes Facultad de Ciencias Departamento de Química (NH 4 ) 2 Cr 2 O 7 (s) > N 2 (g) + 4 H 2 O (líq) + Cr 2 O 3 (s) El dicromato es de color naranja fuerte y a medida que se va convirtiendo en Cr 2 O 3 va cambiando de color pasando a verde oscuro. Esta reacción es bastante sencilla e ilustrativa. El calor de la llama del fósforo inicia la reacción autocatalizada en la cual el cromo presente inicialmente como Cr (VI) toma 3 electrones que obtiene de la oxidación del grupo amonio donde el nitrógeno se encuentra en un estado de oxidación negativo (N 3- ). Las ecuaciones simplificadas correspondientes son las siguientes: 2Cr e - 2Cr 3+ 2N +6 - N 2 + 6e 2Cr N e - 2Cr 3+ + N 2 EXPERIMENTTO Nº º77 PRROOCCEESSOO DDEE CCOORRRROOSSI IIOONN La corrosión del hierro y el acero es un proceso común que es muy familiar para todos nosotros. En este experimento se puede observar como influyen las condiciones ambientales para que la corrosión se haga presente. Materiales: 3 Clavos, 3 tubos de ensayo, una gradilla, agua pura, agua pura hervida, aceite, cloruro de calcio 16
23 Imaginación y creatividad Experimentos sencillos y económicos Procedimiento: 1.- Monte un sistema como el de la figura y déjelo por una semana. Luego de la semana observe y analice cada caso. Luego del tiempo esperado se observa que el clavo del tubo número 1 (expuesto a la humedad y al aire) presenta corrosión, mientras que el número 2 (expuesto a la humedad) apenas si se observa algo de corrosión y número 3 (sin exposición a agentes que aceleren el proceso) por estar mas protegido de aire y en un ambiente anhidro no presenta corrosión. CCOONNDDUCCTTI U IIVVI IIDDADD A EENN MMAATTEERRI IIAALLEESS Con un pequeño circuito podemos ver que tan conductores pueden ser algunos materiales con los que trabajamos regularmente como son por ejemplo el lápiz que usas para escribir en tus clases, el borrador, clavos de acero, de hierro, trozos de aluminio etc. Materiales Una batería, varios bulbos eléctricos de diferentes tamaños o vatiaje, un vaso de vidrio o frasco de mayonesa, agua destilada, dos cables de cobre con caimanes, un tester. 17
24 Universidad de Los Andes Facultad de Ciencias Departamento de Química Procedimiento 1.- Usando los materiales nombrados anteriormente construye un circuito tal como esta detallado en la figura. Como puedes ver allí en donde esta la flecha el circuito esta abierto. Por lo cual no hay continuidad eléctrica entre la batería y la lámpara. 2.- Usando varios objetos, como los indicados anteriormente o algunos otros que tenga a mano, trata de completar el circuito y observar si la lámpara se enciende. Como podrás notar, al colocar los objetos metálicos, la bombilla se enciende con mucha facilidad y es más brillante en algunos caso que en otros. En otros casos no ocurre nada. Al usar grafito, trata de ver si la longitud o grosor afectan la intensidad de la luz. Usando este método podemos clasificar los materiales como conductores o no conductores (aislantes). Algunos de ellos tienen propiedades intermedias como el grafito. 18
25 Imaginación y creatividad Experimentos sencillos y económicos EXPERIMENTTO Nº º99 COONNDDUUCCTTI IIVVI IIDDAADD YY EELLEECCTTRROOLLIITOOSS IT La conductividad eléctrica, se define como la capacidad que tienen las sales inorgánicas en solución (electrolitos) para conducir la corriente eléctrica Que ocurre con el agua? Si modificamos el circuito anterior como lo muestra la figura podemos medir la conductividad del agua y de otras sustancias. Si tenemos a la mano un amperímetro podemos medir con mas precisión que con el bulbo aunque el bulbo es más demostrativo. Llene el contenedor con agua destilada y coloque los electrodos dentro del recipiente como lo muestra la figura sea cuidadoso de no tocar los electrodos uno con el otro. Si esta usando un amperímetro puede observar un pequeño flujo de corriente debido a la presencia de los iones H + y OH - por la disociación de las moléculas de agua. Agua pura Agua más un poco de sal Agua más suficiente sal Figura 3.- Comparando la conductividad con la concentración El agua destilada es un pobre conductor, por lo tanto podrías ayudarla colocando un poco de sal. Que ocurre? Porque la sal hace que el agua sea mas conductora? Es sencillo, los iones que se forman al disolver la sal en el agua es la clave en esta pregunta, ellos una vez disociados los iones se mueven hacia los electrodos dependiendo de la carga de cada uno de ellos, este movimiento hace que los electrones se muevan a través del circuito y producen entonces de esta manera la corriente eléctrica. Si añades más sal podrás ver algo interesante, recuerda que la 19
26 Universidad de Los Andes Facultad de Ciencias Departamento de Química conductividad de una solución esta directamente relacionada con la concentración de los iones en solución. Variaciones del solvente (etanol, kerosén, HCl, vinagre, agua con azúcar o jugo de limón), pueden ser introducidas en estos experimentos. El agua pura, prácticamente no conduce la corriente, sin embargo el agua con sales disueltas conduce la corriente eléctrica. Los iones cargados positiva y negativamente son los que conducen la corriente, y la cantidad conducida dependerá del número de iones presentes y de su movilidad. En la mayoría de las soluciones acuosas, entre mayor sea la cantidad de sales disueltas, mayor será la conductividad, este efecto continúa hasta que la solución está tan llena de iones que se restringe la libertad de movimiento y la conductividad puede disminuir en lugar de aumentas, dándose casos de dos diferentes concentraciones con la misma conductividad. Algunas sustancias se ionizan en forma más completa que otras y por lo mismo conducen mejor la corriente. Cada ácido, base o sal tienen su curva característica de concentración contra conductividad. Son conductores relativamente buenos los ácidos, bases y sales inorgánicas: HCl, NaOH, NaCl, Na 2 CO 3. Son conductores relativamente malos las moléculas de sustancias orgánicas que por la naturaleza de sus enlaces no son iónicas; como por ejemplo, la sacarosa, el benceno, los hidrocarburos, los carbohidratos. Estas sustancias, no se ionizan en el agua y por lo tanto no conducen la corriente eléctrica. Un aumento en la temperatura, disminuye la viscosidad del agua y permite que los iones se muevan más rápidamente, conduciendo más electricidad. EXPERIMENTTO O Nº1100 ELLEECCTRROOLLI T IISSI IISS CCEELLDDAA DDEE UUNN CCOOMMPPAARRTTI IIMMI IIEENNTTOO Como sabemos la electrólisis es el proceso en el que se utiliza una corriente eléctrica para producir un cambio químico. Aquí usaremos la corriente de una batería de 9 voltios para producir este cambio. 20
ELECTROLISIS DE UNA DISOLUCIÓN DE YODURO DE POTASIO. PILA ELECTROLÍTICA
 VIII 1 PRÁCTICA 8 ELECTROLISIS DE UNA DISOLUCIÓN DE YODURO DE POTASIO. PILA ELECTROLÍTICA En esta práctica estudiaremos algunos aspectos prácticos de las reacciones de oxidación reducción que no son espontáneas.
VIII 1 PRÁCTICA 8 ELECTROLISIS DE UNA DISOLUCIÓN DE YODURO DE POTASIO. PILA ELECTROLÍTICA En esta práctica estudiaremos algunos aspectos prácticos de las reacciones de oxidación reducción que no son espontáneas.
REACCIONES DE IONES METÁLICOS
 Actividad Experimental 4 REACCIONES DE IONES METÁLICOS Investigación previa -Investigar las medidas de seguridad para trabajar con amoniaco -Investigar las reglas de solubilidad de las sustancias químicas.
Actividad Experimental 4 REACCIONES DE IONES METÁLICOS Investigación previa -Investigar las medidas de seguridad para trabajar con amoniaco -Investigar las reglas de solubilidad de las sustancias químicas.
Electrólisis. Electrólisis 12/02/2015
 Electrólisis Dr. Armando Ayala Corona Electrólisis La electrolisis es un proceso mediante el cual se logra la disociación de una sustancia llamada electrolito, en sus iones constituyentes (aniones y cationes),
Electrólisis Dr. Armando Ayala Corona Electrólisis La electrolisis es un proceso mediante el cual se logra la disociación de una sustancia llamada electrolito, en sus iones constituyentes (aniones y cationes),
TRABAJO PRÁCTICO N 6: ELECTRÓLISIS
 QUÍMICA GENERAL Y TECNOLÓGICA 2010 TRABAJO PRÁCTICO N 6: ELECTRÓLISIS Objetivo: Medición de la intensidad de corriente que circula por un sistema electrolítico y determinación del equivalente-gramo del
QUÍMICA GENERAL Y TECNOLÓGICA 2010 TRABAJO PRÁCTICO N 6: ELECTRÓLISIS Objetivo: Medición de la intensidad de corriente que circula por un sistema electrolítico y determinación del equivalente-gramo del
REACCIONES DE TRANSFERENCIA DE ELECTRONES (electrolisis)
 REACCIONES DE TRANSFERENCIA DE ELECTRONES (electrolisis) 1 2 Electrólisis Aplicando una f.e.m. adecuada se puede conseguir que tenga lugar una reacción redox en el sentido que no es espontánea. En una
REACCIONES DE TRANSFERENCIA DE ELECTRONES (electrolisis) 1 2 Electrólisis Aplicando una f.e.m. adecuada se puede conseguir que tenga lugar una reacción redox en el sentido que no es espontánea. En una
SEPARACIÓN DE ALUMINIO A PARTIR DE MATERIAL DE DESECHO
 Actividad Experimental SEPARACIÓN DE ALUMINIO A PARTIR DE MATERIAL DE DESECHO Investigación previa 1.- Investigar las medidas de seguridad que hay que mantener al manipular KOH y H SO, incluyendo que acciones
Actividad Experimental SEPARACIÓN DE ALUMINIO A PARTIR DE MATERIAL DE DESECHO Investigación previa 1.- Investigar las medidas de seguridad que hay que mantener al manipular KOH y H SO, incluyendo que acciones
Unidad 7. Reacciones de transferencia de electrones. Oxidación- Reducción. Ajuste de reacciones de oxidación-reducción.
 Unidad 7. Reacciones de transferencia de electrones. Oxidación- Reducción Concepto de oxidación-reducción Número de oxidación Ajuste de reacciones de oxidación-reducción. Estequiometría Electroquímica
Unidad 7. Reacciones de transferencia de electrones. Oxidación- Reducción Concepto de oxidación-reducción Número de oxidación Ajuste de reacciones de oxidación-reducción. Estequiometría Electroquímica
Realizando una pequeña investigación
 Realizando una pequeña investigación 1. Introducción: Investigación realizada 1.1 Objetivo El Objetivo de esta investigación ha sido estudiar de qué factores depende la corrosión del hierro. 1.2 Hipótesis
Realizando una pequeña investigación 1. Introducción: Investigación realizada 1.1 Objetivo El Objetivo de esta investigación ha sido estudiar de qué factores depende la corrosión del hierro. 1.2 Hipótesis
EL PRAE EN LA UNIDAD PEDAGÓGICA: UN COMPROMISO DE TODOS
 EL PRAE EN LA UNIDAD PEDAGÓGICA: UN COMPROMISO DE TODOS RECICLAJE DE PILAS JUSTIFICACIÓN Una batería o pila es un dispositivo que almacena energía química para ser liberada más tarde como electricidad.
EL PRAE EN LA UNIDAD PEDAGÓGICA: UN COMPROMISO DE TODOS RECICLAJE DE PILAS JUSTIFICACIÓN Una batería o pila es un dispositivo que almacena energía química para ser liberada más tarde como electricidad.
ELECTRÓLISIS. Electrólisis de sales fundidas
 El proceso por el cual se produce una reacción química a partir de una energía eléctrica se denomina electrólisis. Y se lleva a cabo en un dispositivo que se conoce como cuba o celda electrolítica. Este
El proceso por el cual se produce una reacción química a partir de una energía eléctrica se denomina electrólisis. Y se lleva a cabo en un dispositivo que se conoce como cuba o celda electrolítica. Este
ELECTROQUÍMICA. químicas que se producen por acción de una corriente eléctrica.
 ELECTROQUÍMICA La electroquímica estudia los cambios químicos que producen una corriente eléctrica y la generación de electricidad mediante reacciones químicas. Es por ello, que el campo de la electroquímica
ELECTROQUÍMICA La electroquímica estudia los cambios químicos que producen una corriente eléctrica y la generación de electricidad mediante reacciones químicas. Es por ello, que el campo de la electroquímica
ELECTROQUIMICA CELDAS GALVANICAS, ELECTROLISIS Y ELECTROQUIMICA APLICADA
 ELECTROQUIMICA CELDAS GALVANICAS, ELECTROLISIS Y ELECTROQUIMICA APLICADA QUE ES LA ELECTROQUIMICA? Es la parte de la química que se encarga del estudio de las relaciones cualitativas y cuantitativas existentes
ELECTROQUIMICA CELDAS GALVANICAS, ELECTROLISIS Y ELECTROQUIMICA APLICADA QUE ES LA ELECTROQUIMICA? Es la parte de la química que se encarga del estudio de las relaciones cualitativas y cuantitativas existentes
PROBLEMAS QUÍMICA 2º BACHILLERATO
 PROBLEMAS QUÍMICA 2º BACHILLERATO ELECTRÓLISIS 1. A través de una cuba electrolítica que contiene una disolución de nitrato de cobalto (II) pasa una corriente eléctrica durante 30 minutos, depositándose
PROBLEMAS QUÍMICA 2º BACHILLERATO ELECTRÓLISIS 1. A través de una cuba electrolítica que contiene una disolución de nitrato de cobalto (II) pasa una corriente eléctrica durante 30 minutos, depositándose
JULIO 2012. FASE ESPECÍFICA. QUÍMICA.
 JULIO 2012. FASE ESPECÍFICA. QUÍMICA. OPCIÓN A 1. (2,5 puntos) Se añaden 10 mg de carbonato de estroncio sólido, SrCO 3 (s), a 2 L de agua pura. Calcule la cantidad de SrCO 3 (s) que queda sin disolver.
JULIO 2012. FASE ESPECÍFICA. QUÍMICA. OPCIÓN A 1. (2,5 puntos) Se añaden 10 mg de carbonato de estroncio sólido, SrCO 3 (s), a 2 L de agua pura. Calcule la cantidad de SrCO 3 (s) que queda sin disolver.
REACCIONES DE TRANSFERENCIA DE ELECTRONES MODELO 2016
 REACCIONES DE TRANSFERENCIA DE ELECTRONES MODELO 2016 1- Se lleva a cabo la electrolisis de una disolución acuosa de bromuro de sodio 1 M, haciendo pasar una corriente de 1,5 A durante 90 minutos. a) Ajuste
REACCIONES DE TRANSFERENCIA DE ELECTRONES MODELO 2016 1- Se lleva a cabo la electrolisis de una disolución acuosa de bromuro de sodio 1 M, haciendo pasar una corriente de 1,5 A durante 90 minutos. a) Ajuste
ELECTROQUÍMICA. 1. Procesos electroquímicos (pila). 2. Potenciales normales de electrodo. 3. Ecuación de Nernst. 4. Electrolisis. 5. Leyes de Faraday.
 ELECTROQUÍMICA 1. Procesos electroquímicos (pila). 2. Potenciales normales de electrodo. 3. Ecuación de Nernst. 4. Electrolisis. 5. Leyes de Faraday. Química 2º bachillerato Electroquímica 1 0. CONOCIMIENTOS
ELECTROQUÍMICA 1. Procesos electroquímicos (pila). 2. Potenciales normales de electrodo. 3. Ecuación de Nernst. 4. Electrolisis. 5. Leyes de Faraday. Química 2º bachillerato Electroquímica 1 0. CONOCIMIENTOS
EQUILIBRIO QUÍMICO: REACCIONES ÁCIDO-BASE
 Página: 1/7 DEPARTAMENTO ESTRELLA CAMPOS PRÁCTICO 8: EQUILIBRIO QUÍMICO: REACCIONES ÁCIDO-BASE Bibliografía: Química, La Ciencia Central, T.L. Brown, H. E. LeMay, Jr., B. Bursten; Ed. Prentice-Hall, Hispanoamérica,
Página: 1/7 DEPARTAMENTO ESTRELLA CAMPOS PRÁCTICO 8: EQUILIBRIO QUÍMICO: REACCIONES ÁCIDO-BASE Bibliografía: Química, La Ciencia Central, T.L. Brown, H. E. LeMay, Jr., B. Bursten; Ed. Prentice-Hall, Hispanoamérica,
UNIVERSIDAD TECNOLOGICA NACIONAL FACULTAD REGIONAL ROSARIO DEPARTAMENTO DE INGENIERIA QUIMICA CATEDRA DE QUIMICA GENERAL
 UNIVERSIDAD TECNOLOGICA NACIONAL FACULTAD REGIONAL ROSARIO DEPARTAMENTO DE INGENIERIA QUIMICA CATEDRA DE QUIMICA GENERAL ESTUDIO DE LA SOLUBILIDAD Y LOS FACTORES QUE LA AFECTAN OBJETIVOS 1. Interpretar
UNIVERSIDAD TECNOLOGICA NACIONAL FACULTAD REGIONAL ROSARIO DEPARTAMENTO DE INGENIERIA QUIMICA CATEDRA DE QUIMICA GENERAL ESTUDIO DE LA SOLUBILIDAD Y LOS FACTORES QUE LA AFECTAN OBJETIVOS 1. Interpretar
2.3 SISTEMAS HOMOGÉNEOS.
 2.3 SISTEMAS HOMOGÉNEOS. 2.3.1 DISOLUCIONES. Vemos que muchos cuerpos y sistemas materiales son heterogéneos y podemos observar que están formados por varias sustancias. En otros no podemos ver que haya
2.3 SISTEMAS HOMOGÉNEOS. 2.3.1 DISOLUCIONES. Vemos que muchos cuerpos y sistemas materiales son heterogéneos y podemos observar que están formados por varias sustancias. En otros no podemos ver que haya
Ácidos y bases (III) Disoluciones reguladoras Valoraciones ácido- base. Disoluciones reguladoras del ph
 Ácidos y bases (III) Disoluciones reguladoras Valoraciones ácido- base IES La Magdalena. Avilés. Asturias Disoluciones reguladoras del ph Si añadimos una pequeña cantidad de ácido o base a agua pura, el
Ácidos y bases (III) Disoluciones reguladoras Valoraciones ácido- base IES La Magdalena. Avilés. Asturias Disoluciones reguladoras del ph Si añadimos una pequeña cantidad de ácido o base a agua pura, el
Ablandamiento de agua mediante el uso de resinas de intercambio iónico.
 Ablandamiento de agua por intercambio iónica página 1 Ablandamiento de agua mediante el uso de resinas de intercambio iónico. (Fuentes varias) Algunos conceptos previos: sales, iones y solubilidad. Que
Ablandamiento de agua por intercambio iónica página 1 Ablandamiento de agua mediante el uso de resinas de intercambio iónico. (Fuentes varias) Algunos conceptos previos: sales, iones y solubilidad. Que
Prácticas de Análisis Instrumental
 Prácticas de Análisis Instrumental Asignatura: Análisis Instrumental Alumno: Daniel González Mancebo Practica 1. DETERMINACIÓN DE CONSTANTES DE EQUILIBRIO MEDIANTE ESPECTROFOTOMETRÍA UV- VISIBLE. Lo primero
Prácticas de Análisis Instrumental Asignatura: Análisis Instrumental Alumno: Daniel González Mancebo Practica 1. DETERMINACIÓN DE CONSTANTES DE EQUILIBRIO MEDIANTE ESPECTROFOTOMETRÍA UV- VISIBLE. Lo primero
La electrólisis CONTENIDOS. Electrolitos. Iones. Carga eléctrica negativa. www.codelcoeduca.cl
 La electrólisis Las moléculas de ciertos compuestos químicos, cuando se encuentran en disolución acuosa, presentan la capacidad de separarse en sus estructuras moleculares más simples y/o en sus átomos
La electrólisis Las moléculas de ciertos compuestos químicos, cuando se encuentran en disolución acuosa, presentan la capacidad de separarse en sus estructuras moleculares más simples y/o en sus átomos
PRÁCTICAS DE LABORATORIO QUÍMICA EN INGENIERÍA
 PRÁCTICAS DE LABORATORIO QUÍMICA EN INGENIERÍA DEPARTAMENTO DE QUÍMICA ORGÁNICA ESCUELA DE INGENIERÍAS INDUSTRIALES UNIVERSIDAD DE VALLADOLID CURSO 2014 2015 ÍNDICE Índice ii Introducción: Prácticas de
PRÁCTICAS DE LABORATORIO QUÍMICA EN INGENIERÍA DEPARTAMENTO DE QUÍMICA ORGÁNICA ESCUELA DE INGENIERÍAS INDUSTRIALES UNIVERSIDAD DE VALLADOLID CURSO 2014 2015 ÍNDICE Índice ii Introducción: Prácticas de
RECUBRIMIENTO ELECTROLITICO
 Cómo motivar a los estudiantes mediante actividades científicas atractivas RECUBRIMIENTO ELECTROLITICO Introducción: Esther Pérez Real COLEGIO ESCLAVAS DE MARIA Valencia Los procesos de recubrimientos
Cómo motivar a los estudiantes mediante actividades científicas atractivas RECUBRIMIENTO ELECTROLITICO Introducción: Esther Pérez Real COLEGIO ESCLAVAS DE MARIA Valencia Los procesos de recubrimientos
Fabricación de un panel solar casero
 Fabricación de un panel solar casero Qué es un panel solar? Es básicamente una caja que contiene un conjunto de células solares. Las células solares son las que hacen el trabajo real de convertir la luz
Fabricación de un panel solar casero Qué es un panel solar? Es básicamente una caja que contiene un conjunto de células solares. Las células solares son las que hacen el trabajo real de convertir la luz
Temas de electricidad II
 Temas de electricidad II CAMBIANDO MATERIALES Ahora volvemos al circuito patrón ya usado. Tal como se indica en la figura, conecte un hilo de cobre y luego uno de níquel-cromo. Qué ocurre con el brillo
Temas de electricidad II CAMBIANDO MATERIALES Ahora volvemos al circuito patrón ya usado. Tal como se indica en la figura, conecte un hilo de cobre y luego uno de níquel-cromo. Qué ocurre con el brillo
Ciencias Naturales 5º Primaria Tema 7: La materia
 1. La materia que nos rodea Propiedades generales de la materia Los objetos materiales tienes en común dos propiedades, que se llaman propiedades generales de la materia: Poseen masa. La masa es la cantidad
1. La materia que nos rodea Propiedades generales de la materia Los objetos materiales tienes en común dos propiedades, que se llaman propiedades generales de la materia: Poseen masa. La masa es la cantidad
Laboratorio N 3: Determinación de dureza en aguas -
 Laboratorio N 3: Determinación de dureza en aguas - Titulaciones complejométricas: Los ácidos aminopolicarboxílicos son excelentes agentes acomplejantes. El EDTA (ácido etilendiaminotetracético) el más
Laboratorio N 3: Determinación de dureza en aguas - Titulaciones complejométricas: Los ácidos aminopolicarboxílicos son excelentes agentes acomplejantes. El EDTA (ácido etilendiaminotetracético) el más
4.5. REACCIONES ÁCIDO-BASE.
 4.5. REACCIONES ÁCIDO-BASE. 4.5.1. ÁCIDOS, BASES Y SALES. Algunas sustancias tienen propiedades comunes y se pueden clasificar como del mismo tipo. El zumo de limón, el vinagre o la aspirina tienen un
4.5. REACCIONES ÁCIDO-BASE. 4.5.1. ÁCIDOS, BASES Y SALES. Algunas sustancias tienen propiedades comunes y se pueden clasificar como del mismo tipo. El zumo de limón, el vinagre o la aspirina tienen un
MANUAL TÉCNICO FILTRO DE POTENCIALES
 MANUAL TÉCNICO FILTRO DE POTENCIALES 1 Introducción a la Protección Catódica p. 2 2 Perjucios de la electrolisis p. 2 3 Filtro de Potenciales p. 4 4 Conexión del Filtro de Potenciales p. 5-1 - 1 Introducción
MANUAL TÉCNICO FILTRO DE POTENCIALES 1 Introducción a la Protección Catódica p. 2 2 Perjucios de la electrolisis p. 2 3 Filtro de Potenciales p. 4 4 Conexión del Filtro de Potenciales p. 5-1 - 1 Introducción
Química 2º Bach. Ácido-base 28/02/05
 Química 2º Bach. Ácido-base 28/02/05 DEPARTAMENTO DE FÍSICA E QUÍMICA Problemas Nombre: [3 PUNTOS / UNO] 1. Calcula el ph de una solución obtenida al disolver 20 L de amoníaco, medidos a 10 0 C y 2,0 atm
Química 2º Bach. Ácido-base 28/02/05 DEPARTAMENTO DE FÍSICA E QUÍMICA Problemas Nombre: [3 PUNTOS / UNO] 1. Calcula el ph de una solución obtenida al disolver 20 L de amoníaco, medidos a 10 0 C y 2,0 atm
Estudio de la evaporación
 Estudio de la evaporación Volumen del líquido Tipo de líquido Superficie del recipiente Altura del recipiente Forma del recipiente Presencia de una sal disuelta Introducción Todos hemos observado que una
Estudio de la evaporación Volumen del líquido Tipo de líquido Superficie del recipiente Altura del recipiente Forma del recipiente Presencia de una sal disuelta Introducción Todos hemos observado que una
www.fisicaeingenieria.es CARACTERÍSTICAS DE LOS ÁCIDOS Y LAS BASES
 CARACTERÍSTICAS DE LOS ÁCIDOS Y LAS BASES ÁCIDOS 1. Tienen sabor ácido como en el caso del ácido cítrico en la naranja. 2. Cambian el color del papel tornasol a rosado. 3. Son corrosivos. 4. Producen quemaduras
CARACTERÍSTICAS DE LOS ÁCIDOS Y LAS BASES ÁCIDOS 1. Tienen sabor ácido como en el caso del ácido cítrico en la naranja. 2. Cambian el color del papel tornasol a rosado. 3. Son corrosivos. 4. Producen quemaduras
Dar a conocer la capacidad de disolución del agua frente a otras sustancias.
 MINISTERIO DE EDUCACION Actividad 1: Agua en la vida II. Laboratorio: Solubilidad del agua 1. Tema: AGUA DISOLVENTE UNIVERSAL 2. Objetivo: Dar a conocer la capacidad de disolución del agua frente a otras
MINISTERIO DE EDUCACION Actividad 1: Agua en la vida II. Laboratorio: Solubilidad del agua 1. Tema: AGUA DISOLVENTE UNIVERSAL 2. Objetivo: Dar a conocer la capacidad de disolución del agua frente a otras
DISOLUCIONES Y ESTEQUIOMETRÍA
 DISOLUCIONES Y ESTEQUIOMETRÍA DISOLUCIONES 1.-/ Se disuelven 7 gramos de NaCl en 50 gramos de agua. Cuál es la concentración centesimal de la disolución? Sol: 12,28 % de NaCl 2.-/ En 20 ml de una disolución
DISOLUCIONES Y ESTEQUIOMETRÍA DISOLUCIONES 1.-/ Se disuelven 7 gramos de NaCl en 50 gramos de agua. Cuál es la concentración centesimal de la disolución? Sol: 12,28 % de NaCl 2.-/ En 20 ml de una disolución
BATERIA AUTOMOTRIZ. HECTOR CISTERNA MARTINEZ Profesor Técnico. Duoc UC, Ingenería Mecánica Automotriz y Autotrónica 16/11/2006
 BATERIA AUTOMOTRIZ HECTOR CISTERNA MARTINEZ Profesor Técnico 1 Introducción La batería es un acumulador de energía que cuando se le alimenta de corriente continua, transforma energía eléctrica en energía
BATERIA AUTOMOTRIZ HECTOR CISTERNA MARTINEZ Profesor Técnico 1 Introducción La batería es un acumulador de energía que cuando se le alimenta de corriente continua, transforma energía eléctrica en energía
SUAVIZACIÓN CONCEPTOS BÁSICOS
 SUAVIZACIÓN CONCEPTOS BÁSICOS Revisemos algunos conceptos que utilizarás para el diseño de los equipos del sistema de suavización, recuerda que muchos ya los has visto en cursos anteriores y que esto es
SUAVIZACIÓN CONCEPTOS BÁSICOS Revisemos algunos conceptos que utilizarás para el diseño de los equipos del sistema de suavización, recuerda que muchos ya los has visto en cursos anteriores y que esto es
PRACTICA No. 9 PREPARACION DE DISOLUCIONES
 1 UNIVERSIDAD DE SAN CARLOS DE GUATEMALA FACULTAD DE CIENCIAS QUÍMICAS Y FARMACIA ESCUELA DE QUÍMICA DEPARTAMENTO DE QUÍMICA GENERAL QUÍMICA GENERAL II PRACTICA No. 9 PREPARACION DE DISOLUCIONES INTRODUCCION:
1 UNIVERSIDAD DE SAN CARLOS DE GUATEMALA FACULTAD DE CIENCIAS QUÍMICAS Y FARMACIA ESCUELA DE QUÍMICA DEPARTAMENTO DE QUÍMICA GENERAL QUÍMICA GENERAL II PRACTICA No. 9 PREPARACION DE DISOLUCIONES INTRODUCCION:
OBTENCIÓN DE CARBONATO DE SODIO (P 5)
 OBTENCIÓN DE CARBONATO DE SODIO (P 5) Objetivos - Estudio descriptivo del carbonato de sodio y de sus usos industriales - Realización de la síntesis de carbonato de sodio y su comparación con el método
OBTENCIÓN DE CARBONATO DE SODIO (P 5) Objetivos - Estudio descriptivo del carbonato de sodio y de sus usos industriales - Realización de la síntesis de carbonato de sodio y su comparación con el método
EQUIPO PORTÁTIL PARA LA DETERMINACIÓN DE CLORO DISPONIBLE EN SOLUCIONES CONCENTRADAS DE HIPOCLORITO
 UNIDAD DE APOYO TÉCNICO PARA EL SANEAMIENTO BÁSICO DEL ÁREA RURAL EQUIPO PORTÁTIL PARA LA DETERMINACIÓN DE CLORO DISPONIBLE EN SOLUCIONES CONCENTRADAS DE HIPOCLORITO Centro Panamericano de Ingeniería Sanitaria
UNIDAD DE APOYO TÉCNICO PARA EL SANEAMIENTO BÁSICO DEL ÁREA RURAL EQUIPO PORTÁTIL PARA LA DETERMINACIÓN DE CLORO DISPONIBLE EN SOLUCIONES CONCENTRADAS DE HIPOCLORITO Centro Panamericano de Ingeniería Sanitaria
QUÍMICA. AgNO 3 (ac) Ag + (ac) + NO 3 - (ac) (0,25 puntos) 0,1 M 0,1 M 0,1 M. (0,25 puntos)
 OPCIÓN A QUÍMICA 1. (2,5 puntos) Se analiza una muestra de 10 ml de una disolución acuosa que contiene ión cloruro, Cl -, mediante la adición de una gota (0,2 ml) de disolución acuosa de nitrato de plata,
OPCIÓN A QUÍMICA 1. (2,5 puntos) Se analiza una muestra de 10 ml de una disolución acuosa que contiene ión cloruro, Cl -, mediante la adición de una gota (0,2 ml) de disolución acuosa de nitrato de plata,
II. METODOLOGÍA. El proceso de elaboración del biodiesel se constituye de siete pasos fundamentales: 6.1. DETERMINACIÓN DE LOS GRAMOS DE CATALIZADOR
 II. METODOLOGÍA 6. PROCESO DE ELABORACIÓN El proceso de elaboración del biodiesel se constituye de siete pasos fundamentales: 1. Determinación de los gramos de catalizador 2. Preparación del Metóxido de
II. METODOLOGÍA 6. PROCESO DE ELABORACIÓN El proceso de elaboración del biodiesel se constituye de siete pasos fundamentales: 1. Determinación de los gramos de catalizador 2. Preparación del Metóxido de
La separación de mezclas de las cuales existen dos tipos como son las homogéneas y heterogéneas
 Introducción En el tema operaciones fundamentales de laboratorio se dan una serie e pasos muy importantes para el desarrollo del programa de laboratorio por ejemplo podemos citar varios procedimientos
Introducción En el tema operaciones fundamentales de laboratorio se dan una serie e pasos muy importantes para el desarrollo del programa de laboratorio por ejemplo podemos citar varios procedimientos
Neutralización por Destilación ÍNDICE
 ÍNDICE Página Carátula 1 Índice 3 Introducción 4 Objetivos 5 Principios Teóricos 6 Neutralización 6 Producción de Amoniaco 7 Detalles Experimentales 8 Materiales y Reactivos 8 Procedimiento 9 Conclusiones
ÍNDICE Página Carátula 1 Índice 3 Introducción 4 Objetivos 5 Principios Teóricos 6 Neutralización 6 Producción de Amoniaco 7 Detalles Experimentales 8 Materiales y Reactivos 8 Procedimiento 9 Conclusiones
Completar: Un sistema material homogéneo constituido por un solo componente se llama.
 IES Menéndez Tolosa 3º ESO (Física y Química) 1 Completar: Un sistema material homogéneo constituido por un solo componente se llama. Un sistema material homogéneo formado por dos o más componentes se
IES Menéndez Tolosa 3º ESO (Física y Química) 1 Completar: Un sistema material homogéneo constituido por un solo componente se llama. Un sistema material homogéneo formado por dos o más componentes se
ELECTROLISIS DEL AGUA POR
 ELECTROLISIS DEL AGUA POR TEORIA: La electrólisis del agua consiste en un proceso electroquímico en el cual el agua se divide en Hidrógeno y Oxígeno. La electrólisis consiste en pasar corriente eléctrica
ELECTROLISIS DEL AGUA POR TEORIA: La electrólisis del agua consiste en un proceso electroquímico en el cual el agua se divide en Hidrógeno y Oxígeno. La electrólisis consiste en pasar corriente eléctrica
Informe del trabajo práctico nº7
 Informe del trabajo práctico nº7 Profesora : Lic. Graciela. Lic. Mariana. Alumnas: Romina. María Luján. Graciela. Mariana. Curso: Química orgánica 63.14 turno 1 OBJETIVOS Mostrar las propiedades que presentan
Informe del trabajo práctico nº7 Profesora : Lic. Graciela. Lic. Mariana. Alumnas: Romina. María Luján. Graciela. Mariana. Curso: Química orgánica 63.14 turno 1 OBJETIVOS Mostrar las propiedades que presentan
1. La magnitud 0,0000024mm expresada en notación científica es: a) 2,4 10 6 mm b) 2,4 10 5 mm c) 24 10 5 mm d) 24 10 6 mm
 Se responderá escribiendo un aspa en el recuadro correspondiente a la respuesta correcta o a la que con carácter más general suponga la contestación cierta más completa en la HOJA DE RESPUESTAS. Se facilitan
Se responderá escribiendo un aspa en el recuadro correspondiente a la respuesta correcta o a la que con carácter más general suponga la contestación cierta más completa en la HOJA DE RESPUESTAS. Se facilitan
TRABAJO PRÁCTICO N 10 PILAS-ELECTRÓLISIS
 TRABAJO PRÁCTICO N 10 PILAS-ELECTRÓLISIS Las celdas galvánicas (pilas) son dispositivos armados de tal forma que, usando reacciones redox espontáneas, generan energía eléctrica Ejemplo: Pila de Daniel:
TRABAJO PRÁCTICO N 10 PILAS-ELECTRÓLISIS Las celdas galvánicas (pilas) son dispositivos armados de tal forma que, usando reacciones redox espontáneas, generan energía eléctrica Ejemplo: Pila de Daniel:
LA ELECTRÓLISIS DEL AGUA
 LA ELECTRÓLISIS DEL AGUA Oxidación: 2H + +O +4e - 2 O(l) 4H (aq) 2 (g) Reducción: 2H 2 O(l) + 2e - H 2 (g) + 2OH - (aq) Reacción total en la celda 2H 2 O(l) 2H 2 (g) + O 2 (g) Nota: Obsérvese la diferencia
LA ELECTRÓLISIS DEL AGUA Oxidación: 2H + +O +4e - 2 O(l) 4H (aq) 2 (g) Reducción: 2H 2 O(l) + 2e - H 2 (g) + 2OH - (aq) Reacción total en la celda 2H 2 O(l) 2H 2 (g) + O 2 (g) Nota: Obsérvese la diferencia
GUIA DE MANEJO DE RESIDUOS QUÍMICOS
 La Universidad Autónoma de Occidente, mantendrá programas y operaciones para minimizar los efectos de las sustancias peligrosas y residuos peligrosos sobre el medio ambiente. Cuando se genere un residuo
La Universidad Autónoma de Occidente, mantendrá programas y operaciones para minimizar los efectos de las sustancias peligrosas y residuos peligrosos sobre el medio ambiente. Cuando se genere un residuo
Circuitos de corriente continua
 Capítulo 4: Circuitos de corriente continua Corriente promedio: carga que pasa por A por unidad de tiempo Corriente Instantánea [ I ] = C/s = A (Ampere) J = q n v d Ley de Ohm George Simon Ohm (1789-1854)
Capítulo 4: Circuitos de corriente continua Corriente promedio: carga que pasa por A por unidad de tiempo Corriente Instantánea [ I ] = C/s = A (Ampere) J = q n v d Ley de Ohm George Simon Ohm (1789-1854)
MANEJO DE REACTIVOS Y MEDICIONES DE MASA Y VOLUMEN
 Actividad Experimental 1 MANEJO DE REACTIVOS Y MEDICIONES DE MASA Y VOLUMEN Investigación previa 1. Investiga los siguientes aspectos de una balanza granataria y de una balanza digital: a. Características
Actividad Experimental 1 MANEJO DE REACTIVOS Y MEDICIONES DE MASA Y VOLUMEN Investigación previa 1. Investiga los siguientes aspectos de una balanza granataria y de una balanza digital: a. Características
Actividad: Qué es capilaridad?
 Qué es capilaridad? Nivel: 3º medio Subsector: Ciencias físicas Unidad temática: Ver video Capilaridad Actividad: Qué es capilaridad? Los fluidos son un conjunto de moléculas distribuidas al azar que se
Qué es capilaridad? Nivel: 3º medio Subsector: Ciencias físicas Unidad temática: Ver video Capilaridad Actividad: Qué es capilaridad? Los fluidos son un conjunto de moléculas distribuidas al azar que se
INTRODUCCIÓN AL TRABAJO DE LABORATORIO
 PRÁCTICA 1 INTRODUCCIÓN AL TRABAJO DE LABORATORIO OBJETIVOS 1. Manipular de manera adecuada el equipo de uso común en el laboratorio. 2. Ejecutar tareas básicas en la realización de experimentos. INTRODUCCIÓN
PRÁCTICA 1 INTRODUCCIÓN AL TRABAJO DE LABORATORIO OBJETIVOS 1. Manipular de manera adecuada el equipo de uso común en el laboratorio. 2. Ejecutar tareas básicas en la realización de experimentos. INTRODUCCIÓN
1.- La masa atómica de la plata es de 107'9 u. Cuántos gramos pesan 0'25 mol de plata?
 Unidad 6 1.- La masa atómica de la plata es de 107'9 u. Cuántos gramos pesan 0'25 mol de plata? Como la masa atómica de la plata es de 107'9 u, la masa de 1 mol de plata es de 107'9 g (la misma cifra pero
Unidad 6 1.- La masa atómica de la plata es de 107'9 u. Cuántos gramos pesan 0'25 mol de plata? Como la masa atómica de la plata es de 107'9 u, la masa de 1 mol de plata es de 107'9 g (la misma cifra pero
La electrólisis permite descomponer la Alúmina en aluminio y oxígeno.
 LA OBTENCIÓN DEL ALUMINIO. La primera fase de la obtención del aluminio consiste en aislar la Alúmina (óxido de aluminio) de estos minerales. Para ello lo primero es triturar la Bauxita para obtener un
LA OBTENCIÓN DEL ALUMINIO. La primera fase de la obtención del aluminio consiste en aislar la Alúmina (óxido de aluminio) de estos minerales. Para ello lo primero es triturar la Bauxita para obtener un
TEMA VII. REACCIONES DE TRANSFERENCIA DE ELECTRONES.
 TEMA VII. REACCIONES DE TRANSFERENCIA DE ELECTRONES. 1. CONCEPTOS DE OXIDACIÓN-REDUCCIÓN. Concepto restringido: Oxidación es la reacción química en la que hay ganancia de oxígeno, y reducción, la reacción
TEMA VII. REACCIONES DE TRANSFERENCIA DE ELECTRONES. 1. CONCEPTOS DE OXIDACIÓN-REDUCCIÓN. Concepto restringido: Oxidación es la reacción química en la que hay ganancia de oxígeno, y reducción, la reacción
CÁTEDRA: QUIMICA GUIA DE PROBLEMAS Nº 10
 CÁTEDRA: QUIMICA GUIA DE PROBLEMAS Nº 10 TEMA: ph, NEUTRALIZACIÓN Y EQUILIBRIO ÁCIDO BASE OBJETIVOS: Clasificar ácidos y bases de acuerdo al potencial de hidrógeno. PRERREQUISITOS: Tener conocimiento de
CÁTEDRA: QUIMICA GUIA DE PROBLEMAS Nº 10 TEMA: ph, NEUTRALIZACIÓN Y EQUILIBRIO ÁCIDO BASE OBJETIVOS: Clasificar ácidos y bases de acuerdo al potencial de hidrógeno. PRERREQUISITOS: Tener conocimiento de
HIDROSTANK. Catalogo 76.1
 HIDROSTANK TERMINODOUR: DESCRIPCIÓN TÉCNICA Catalogo 76.1 Terminodour TM, el Nuevo Concepto en Control de Olores. La tecnología de control de olor por ionización, de CSO Technik Hidrostank, está instalado
HIDROSTANK TERMINODOUR: DESCRIPCIÓN TÉCNICA Catalogo 76.1 Terminodour TM, el Nuevo Concepto en Control de Olores. La tecnología de control de olor por ionización, de CSO Technik Hidrostank, está instalado
Experiencias de laboratorio para el aprendizaje de la Química. Lic. Wagner Castro Castillo Lic. Nancy Rodríguez Coronado Lic. Amelia Calvo Rodríguez.
 Experiencias de laboratorio para el aprendizaje de la Química. Lic. Wagner Castro Castillo Lic. Nancy Rodríguez Coronado Lic. Amelia Calvo Rodríguez. Resumen: Existen muchas variantes que se involucran
Experiencias de laboratorio para el aprendizaje de la Química. Lic. Wagner Castro Castillo Lic. Nancy Rodríguez Coronado Lic. Amelia Calvo Rodríguez. Resumen: Existen muchas variantes que se involucran
Diseño Grafico: Ismael Camacho Sofía Alvarado. Sofía Alvarado. Preparación y Presentación de la receta: Ismael Camacho.
 Diseño Grafico: Ismael Camacho Sofía Alvarado Fotografia: Javier Peralta Sofía Alvarado Preparación y Presentación de la receta: Ismael Camacho Asistencia: Redacción: Sofía Alvarado Javier Peralta Sofía
Diseño Grafico: Ismael Camacho Sofía Alvarado Fotografia: Javier Peralta Sofía Alvarado Preparación y Presentación de la receta: Ismael Camacho Asistencia: Redacción: Sofía Alvarado Javier Peralta Sofía
REACCIONES DE TRANSFERENCIA DE ELECTRONES
 REACCIONES DE TRANSFERENCIA DE ELECTRONES REACCIONES REDOX son aquellas en las que cambian el número de oxidación de algún elemento. En estas reacciones hay intercambio de electrones por lo que no se pueden
REACCIONES DE TRANSFERENCIA DE ELECTRONES REACCIONES REDOX son aquellas en las que cambian el número de oxidación de algún elemento. En estas reacciones hay intercambio de electrones por lo que no se pueden
Mediciones Eléctricas
 Mediciones Eléctricas Grupos Electrógenos Mediciones Eléctricas Página 1 de 12 Tabla de Contenido Objetivo 1: Medidas de magnitudes eléctricas... 3 Objetivo 2: Generalidades sobre instrumentos de medición...
Mediciones Eléctricas Grupos Electrógenos Mediciones Eléctricas Página 1 de 12 Tabla de Contenido Objetivo 1: Medidas de magnitudes eléctricas... 3 Objetivo 2: Generalidades sobre instrumentos de medición...
EFECTOS DE LA CORRIENTE ELÉCTRICA: TÉRMICO, MAGNÉTICO Y QUÍMICO
 EFECTOS DE LA CORRIENTE ELÉCTRICA: TÉRMICO, MAGNÉTICO Y QUÍMICO Marisol de la Fuente Mendoza IES LA CANAL DE NAVARRÉS Navarrés (Valencia) Introducción: Al hablar de los efectos de la corriente eléctrica,
EFECTOS DE LA CORRIENTE ELÉCTRICA: TÉRMICO, MAGNÉTICO Y QUÍMICO Marisol de la Fuente Mendoza IES LA CANAL DE NAVARRÉS Navarrés (Valencia) Introducción: Al hablar de los efectos de la corriente eléctrica,
MANUAL DE INSTRUCCIONES OLLA ARROCERA ED-4588T
 MANUAL DE INSTRUCCIONES OLLA ARROCERA ED-4588T ESTIMADO CLIENTE Con el fin de que obtenga el mayor desempeño de su producto, por favor lea este manual de instrucciones cuidadosamente antes de comenzar
MANUAL DE INSTRUCCIONES OLLA ARROCERA ED-4588T ESTIMADO CLIENTE Con el fin de que obtenga el mayor desempeño de su producto, por favor lea este manual de instrucciones cuidadosamente antes de comenzar
4. Materiales y Métodos. Los equipos que a continuación se mencionan se encuentran en el laboratorio de
 39 4. Materiales y Métodos 4.1 Equipos Los equipos que a continuación se mencionan se encuentran en el laboratorio de Ingeniería Ambiental de la Universidad de las Américas Puebla y en el Laboratorio de
39 4. Materiales y Métodos 4.1 Equipos Los equipos que a continuación se mencionan se encuentran en el laboratorio de Ingeniería Ambiental de la Universidad de las Américas Puebla y en el Laboratorio de
RELACIÓN DE MATERIAL NECESARIO PARA LA REALIZACIÓN DE LAS PRÁCTICAS:
 RELACIÓN DE MATERIAL NECESARIO PARA LA REALIZACIÓN DE LAS PRÁCTICAS: Para la realización de las prácticas, necesitaremos el siguiente material: 1 5 m de cable de hilos de cobre de pequeña sección. Cartón
RELACIÓN DE MATERIAL NECESARIO PARA LA REALIZACIÓN DE LAS PRÁCTICAS: Para la realización de las prácticas, necesitaremos el siguiente material: 1 5 m de cable de hilos de cobre de pequeña sección. Cartón
PRÁCTICA Nº 5 REACCIONES DE POLIMERIZACIÓN. Objetivos
 PRÁCTICA Nº 5 REACCINES DE PLIMERIZACIÓN bjetivos - Realizar un ejemplo práctico de reacción de polimerización por condensación: Preparación de un poliéster. Preparación de una poliamida. - Resaltar la
PRÁCTICA Nº 5 REACCINES DE PLIMERIZACIÓN bjetivos - Realizar un ejemplo práctico de reacción de polimerización por condensación: Preparación de un poliéster. Preparación de una poliamida. - Resaltar la
TEMA 5: REACCIONES DE TRANSFERENCIA DE PROTONES EJERCICIOS DE SELECTIVIDAD 96/97
 TEMA 5: REACCIONES DE TRANSFERENCIA DE PROTONES EJERCICIOS DE SELECTIVIDAD 96/97 1. a) Cuántos gramos de hidróxido de potasio se necesitan para preparar 250 ml de una disolución acuosa de ph = 13? b) Calcule
TEMA 5: REACCIONES DE TRANSFERENCIA DE PROTONES EJERCICIOS DE SELECTIVIDAD 96/97 1. a) Cuántos gramos de hidróxido de potasio se necesitan para preparar 250 ml de una disolución acuosa de ph = 13? b) Calcule
ELECTRÓLISIS DEL AGUA FRANCISCO MORENO HUESO. 18 de noviembre de 2013
 18 de noviembre de 2013 Índice General 1 FUNDAMENTO TEÓRICO Índice General 1 FUNDAMENTO TEÓRICO 2 MATERIAL Y REACTIVOS Índice General 1 FUNDAMENTO TEÓRICO 2 MATERIAL Y REACTIVOS 3 PROCEDIMIENTO EXPERIMENTAL
18 de noviembre de 2013 Índice General 1 FUNDAMENTO TEÓRICO Índice General 1 FUNDAMENTO TEÓRICO 2 MATERIAL Y REACTIVOS Índice General 1 FUNDAMENTO TEÓRICO 2 MATERIAL Y REACTIVOS 3 PROCEDIMIENTO EXPERIMENTAL
PRÁCTICA NÚMERO 8 EL POLARÍMETRO Y LA ACTIVIDAD ÓPTICA
 PRÁCTICA NÚMERO 8 EL POLARÍMETRO Y LA ACTIVIDAD ÓPTICA I. Objetivos. 1. Estudiar el efecto que tienen ciertas sustancias sobre la luz polarizada. 2. Encontrar la gráfica y ecuación de la concentración
PRÁCTICA NÚMERO 8 EL POLARÍMETRO Y LA ACTIVIDAD ÓPTICA I. Objetivos. 1. Estudiar el efecto que tienen ciertas sustancias sobre la luz polarizada. 2. Encontrar la gráfica y ecuación de la concentración
PRÁCTICA 5. CALORIMETRÍA
 PRÁCTICA 5. CALORIMETRÍA INTRODUCCIÓN Al mezclar dos cantidades de líquidos a distinta temperatura se genera una transferencia de energía en forma de calor desde el más caliente al más frío. Dicho tránsito
PRÁCTICA 5. CALORIMETRÍA INTRODUCCIÓN Al mezclar dos cantidades de líquidos a distinta temperatura se genera una transferencia de energía en forma de calor desde el más caliente al más frío. Dicho tránsito
I. Objetivos 1. Determinar el cambio de entalpía de una reacción de metal de magnesio con ácido clorhídrico.
 UNIVERSIDAD INTERAMERICANA Recinto de Bayamón Departamento de Ciencias Naturales y Matemáticas Fundamentos de Química: CHEM 1111 Experimento No. 9: Cambio de entalpía de una reacción I. Objetivos 1. Determinar
UNIVERSIDAD INTERAMERICANA Recinto de Bayamón Departamento de Ciencias Naturales y Matemáticas Fundamentos de Química: CHEM 1111 Experimento No. 9: Cambio de entalpía de una reacción I. Objetivos 1. Determinar
EJERCICIOS PARA EXAMEN U6 Química 2º Bachiller
 2010 Reacciones de intercambio de Protones EJERCICIOS PARA EXAMEN U6 Química 2º Bachiller Recopilación de ejercicios preguntados en exámenes de cursos anteriores Mª Teresa Gómez Ruiz IES Politécnico Cartagena.
2010 Reacciones de intercambio de Protones EJERCICIOS PARA EXAMEN U6 Química 2º Bachiller Recopilación de ejercicios preguntados en exámenes de cursos anteriores Mª Teresa Gómez Ruiz IES Politécnico Cartagena.
Titulación Ácido Base
 Titulación Ácido Base Experimento 16 La titulación es el procedimiento utilizado para determinar el volumen de una solución que es necesario para reaccionar con una cierta cantidad de otra sustancia. En
Titulación Ácido Base Experimento 16 La titulación es el procedimiento utilizado para determinar el volumen de una solución que es necesario para reaccionar con una cierta cantidad de otra sustancia. En
1ª Parte. Debes Reciclar
 Avanza Lectura Fácil Guía para cuidar el medio ambiente Guía para cuidar el medio ambiente 1ª Parte. Debes Reciclar Financiado por: GUÍA PARA CUIDAR EL MEDIO AMBIENTE PRIMERA PARTE DEBES RECICLAR El medio
Avanza Lectura Fácil Guía para cuidar el medio ambiente Guía para cuidar el medio ambiente 1ª Parte. Debes Reciclar Financiado por: GUÍA PARA CUIDAR EL MEDIO AMBIENTE PRIMERA PARTE DEBES RECICLAR El medio
UNO MÁS UNO... IGUAL A DOS???
 UNO MÁS UNO... IGUAL A DOS??? Introducción La forma de afrontar un problema científico, ha ido cambiando a lo largo de la historia de la humanidad, los filósofos antiguos como Aristóteles (S IV a.c) usaban
UNO MÁS UNO... IGUAL A DOS??? Introducción La forma de afrontar un problema científico, ha ido cambiando a lo largo de la historia de la humanidad, los filósofos antiguos como Aristóteles (S IV a.c) usaban
LINEAS EQUIPOTENCIALES
 LINEAS EQUIPOTENCIALES Construcción de líneas equipotenciales. Visualización del campo eléctrico y del potencial eléctrico. Análisis del movimiento de cargas eléctricas en presencia de campos eléctricos.
LINEAS EQUIPOTENCIALES Construcción de líneas equipotenciales. Visualización del campo eléctrico y del potencial eléctrico. Análisis del movimiento de cargas eléctricas en presencia de campos eléctricos.
Limpieza y mantenimiento de armarios de acero inoxidable
 Limpieza y mantenimiento de armarios de acero inoxidable Limpieza de los armarios de acero inoxidable Los armarios de acero inoxidable Delvalle se deben limpiar por consideraciones estéticas y para preservar
Limpieza y mantenimiento de armarios de acero inoxidable Limpieza de los armarios de acero inoxidable Los armarios de acero inoxidable Delvalle se deben limpiar por consideraciones estéticas y para preservar
QUÉ HACER SI SE ROMPE UN TERMÓMETRO DE MERCURIO?
 QUÉ HACER SI SE ROMPE UN TERMÓMETRO DE MERCURIO? NOTA: Estas instrucciones también se aplican a los vertidos procedentes de otras fuentes, si la cantidad derramada es inferior o similar a la cantidad de
QUÉ HACER SI SE ROMPE UN TERMÓMETRO DE MERCURIO? NOTA: Estas instrucciones también se aplican a los vertidos procedentes de otras fuentes, si la cantidad derramada es inferior o similar a la cantidad de
EN BUSCA DE INDICADORES NATURALES
 EN BUSCA DE INDICADORES NATURALES Introducción: Ana Belén Domingo COLEGIO LA PURÍSIMA Torrent Los indicadores son sustancias que, mediante un cambio de color, nos ayudan a identificar si las sustancias
EN BUSCA DE INDICADORES NATURALES Introducción: Ana Belén Domingo COLEGIO LA PURÍSIMA Torrent Los indicadores son sustancias que, mediante un cambio de color, nos ayudan a identificar si las sustancias
UNIVERSIDADES PÚBLICAS DE LA COMUNIDAD DE MADRID PRUEBA DE ACCESO A LAS ENSEÑANZAS UNIVERSITARIAS OFICIALES DE GRADO. Modelo Curso 2010-2011
 UNIVERSIDADES PÚBLICAS DE LA COMUNIDAD DE MADRID PRUEBA DE ACCESO A LAS ENSEÑANZAS UNIVERSITARIAS OFICIALES DE GRADO MATERIA: QUÍMICA Modelo Curso 010-011 MODELO INSTRUCCIONES Y CRITERIOS GENERALES DE
UNIVERSIDADES PÚBLICAS DE LA COMUNIDAD DE MADRID PRUEBA DE ACCESO A LAS ENSEÑANZAS UNIVERSITARIAS OFICIALES DE GRADO MATERIA: QUÍMICA Modelo Curso 010-011 MODELO INSTRUCCIONES Y CRITERIOS GENERALES DE
CONTENIDO DE LA GUÍA OBJETIVO
 CONTENIDO DE LA GUÍA OBJETIVO Reconocer las características físicas y formas de emplear el material de laboratorio, con el cual se desarrollan diferentes actividades experimentales que permiten alcanzar
CONTENIDO DE LA GUÍA OBJETIVO Reconocer las características físicas y formas de emplear el material de laboratorio, con el cual se desarrollan diferentes actividades experimentales que permiten alcanzar
Materiales recopilados por la Ponencia Provincial de Química para Selectividad TEMA 1: QUÍMICA DESCRIPTIVA EJERCICIOS DE SELECTIVIDAD 96/97
 TEMA 1: QUÍMICA DESCRIPTIVA EJERCICIOS DE SELECTIVIDAD 96/97 1. De un recipiente que contiene 32 g de metano, se extraen 9 10 23 moléculas. a) Los moles de metano que quedan. b) Las moléculas de metano
TEMA 1: QUÍMICA DESCRIPTIVA EJERCICIOS DE SELECTIVIDAD 96/97 1. De un recipiente que contiene 32 g de metano, se extraen 9 10 23 moléculas. a) Los moles de metano que quedan. b) Las moléculas de metano
PRÁCTICA 1. PREPARACIÓN DE DISOLUCIONES.
 PRÁCTICA 1. PREPARACIÓN DE DISOLUCIONES. OBJETIVOS 1.- Familiarizarse con el material de laboratorio. 2.- Aprender a preparar disoluciones de una concentración determinada. 3.- Manejar las distintas formas
PRÁCTICA 1. PREPARACIÓN DE DISOLUCIONES. OBJETIVOS 1.- Familiarizarse con el material de laboratorio. 2.- Aprender a preparar disoluciones de una concentración determinada. 3.- Manejar las distintas formas
DEPARTAMENTO DE CIENCIAS BASICAS LABORATORIO DE BIOQUÍMICA 502504. GUÍA No: 3.2. DETERMINACIÓN DE PROTEINA BRUTA POR EL MÉTODO DE KJELDAHL
 1 DEPARTAMENTO DE CIENCIAS BASICAS LABORATORIO DE BIOQUÍMICA 502504 GUÍA No: 3.2. DETERMINACIÓN DE PROTEINA BRUTA POR EL MÉTODO DE KJELDAHL I. EL PROBLEMA Determinar el contenido de proteína bruta presente
1 DEPARTAMENTO DE CIENCIAS BASICAS LABORATORIO DE BIOQUÍMICA 502504 GUÍA No: 3.2. DETERMINACIÓN DE PROTEINA BRUTA POR EL MÉTODO DE KJELDAHL I. EL PROBLEMA Determinar el contenido de proteína bruta presente
ACTIVIDAD EXPERIMENTAL No. 2 TÉCNICAS COMUNES DEL LABORATORIO DE QUÍMICA.
 ACTIVIDAD EXPERIMENTAL No. 2 TÉCNICAS COMUNES DEL LABORATORIO DE QUÍMICA. Introducción: Cuando se inicia un curso en el que por primera vez se trabaja en un laboratorio escolar, es necesario que el alumno
ACTIVIDAD EXPERIMENTAL No. 2 TÉCNICAS COMUNES DEL LABORATORIO DE QUÍMICA. Introducción: Cuando se inicia un curso en el que por primera vez se trabaja en un laboratorio escolar, es necesario que el alumno
INSTRUCCIONES DE INSTALACIÓN Y RECARGA CISS HP CARTUCHO SERIE 1
 Antes de empezar Es muy importante que no realice ninguna acción hasta leer completamente las instrucciones. Léalas de forma detenida y completa!!! Es muy importante que compruebe que su impresora se encuentra
Antes de empezar Es muy importante que no realice ninguna acción hasta leer completamente las instrucciones. Léalas de forma detenida y completa!!! Es muy importante que compruebe que su impresora se encuentra
Tema 1: Sustancias puras, mezclas y disoluciones
 Tema 1: Sustancias puras, mezclas y disoluciones 1.- Tipos de materia Recordemos que materia es todo aquello que tiene masa y volumen. Toda la materia está formada por elementos químicos (recuerda la tabla
Tema 1: Sustancias puras, mezclas y disoluciones 1.- Tipos de materia Recordemos que materia es todo aquello que tiene masa y volumen. Toda la materia está formada por elementos químicos (recuerda la tabla
EXPERIMENTOS PARA HACER EN CASA 1. PUEDE EL CALOR MOVER EL AGUA. Materiales:
 EXPERIMENTOS PARA HACER EN CASA 1. PUEDE EL CALOR MOVER EL AGUA 1. Un recipiente transparente 2. Un frasco pequeño con tapa 3. Tinta o colorantes de cocina 4. Agua fría y caliente Llena el recipiente grande
EXPERIMENTOS PARA HACER EN CASA 1. PUEDE EL CALOR MOVER EL AGUA 1. Un recipiente transparente 2. Un frasco pequeño con tapa 3. Tinta o colorantes de cocina 4. Agua fría y caliente Llena el recipiente grande
sirve para medir volumen de líquidos y también para calentar y mezclar sustancias. es útil para medir volúmenes más pequeños de líquidos.
 NOMBRE USOS MEDIDAS ML O CM DIBUJO 2000, 1000 Vaso precipitado sirve para medir volumen de líquidos y también para calentar y mezclar sustancias. 900, 500 300, 200 150, 140 100, 80 2000, 1000 Probeta es
NOMBRE USOS MEDIDAS ML O CM DIBUJO 2000, 1000 Vaso precipitado sirve para medir volumen de líquidos y también para calentar y mezclar sustancias. 900, 500 300, 200 150, 140 100, 80 2000, 1000 Probeta es
http://www.rubenprofe.com.ar
 SOLUCIONES Objetivos: Mínimo: Definir las concentraciones Molar, normal, % m/m, % m/v y % v/v. Describir la forma de preparar soluciones de concentraciones definidas. Realizar cálculos con concentraciones
SOLUCIONES Objetivos: Mínimo: Definir las concentraciones Molar, normal, % m/m, % m/v y % v/v. Describir la forma de preparar soluciones de concentraciones definidas. Realizar cálculos con concentraciones
EXPERIMENTOS Nos. 3 y 4 FENÓMENOS ELECTROSTÁTICOS
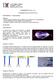 EXPERIMENTO 1: Electrostática EXPERIMENTOS Nos. 3 y 4 FENÓMENOS ELECTROSTÁTICOS Objetivos Obtener cargas de distinto signo mediante varios métodos y sus características Uso del electroscopio como detector
EXPERIMENTO 1: Electrostática EXPERIMENTOS Nos. 3 y 4 FENÓMENOS ELECTROSTÁTICOS Objetivos Obtener cargas de distinto signo mediante varios métodos y sus características Uso del electroscopio como detector
PRACTICA N 8 Cuantificación de nitrógeno total y determinación del contenido de proteína cruda Introducción:
 1 PRACTICA N 8 Cuantificación de nitrógeno total y determinación del contenido de proteína cruda I. Introducción: El nitrógeno es el elemento químico que permite diferenciar las proteínas de otros compuestos,
1 PRACTICA N 8 Cuantificación de nitrógeno total y determinación del contenido de proteína cruda I. Introducción: El nitrógeno es el elemento químico que permite diferenciar las proteínas de otros compuestos,
Introducción a la Química. Sistemas Materiales y Conceptos Fundamentales. Seminario de Problemas N 1
 Sistemas Materiales Introducción a la Química Seminario de Problemas N 1 1. Dibuja un esquema con los tres estados de la materia (sólido, líquido y gas) indicando el nombre de los cambios de estado. 2.
Sistemas Materiales Introducción a la Química Seminario de Problemas N 1 1. Dibuja un esquema con los tres estados de la materia (sólido, líquido y gas) indicando el nombre de los cambios de estado. 2.
Acción Enzimática: Actividad de la Catalasa
 Acción Enzimática: Actividad de la Catalasa Experimento 3 Muchos organismos pueden descomponer el peróxido de hidrógeno (H 2 O 2 ) por la acción de las enzimas. Las enzimas son proteínas globulares responsables
Acción Enzimática: Actividad de la Catalasa Experimento 3 Muchos organismos pueden descomponer el peróxido de hidrógeno (H 2 O 2 ) por la acción de las enzimas. Las enzimas son proteínas globulares responsables
De cualquier manera, solo estudiaremos en esta unidad los compuestos inorgánicos.
 Unidad 3 Ácidos, Hidróxidos y Sales: óxidos básicos, óxidos ácidos, hidróxidos, hidrácidos o ácidos binarios, ácidos ternarios, sales binarias, ternarias y cuaternarias. Formación y nomenclatura. Enlaces
Unidad 3 Ácidos, Hidróxidos y Sales: óxidos básicos, óxidos ácidos, hidróxidos, hidrácidos o ácidos binarios, ácidos ternarios, sales binarias, ternarias y cuaternarias. Formación y nomenclatura. Enlaces
MANUAL PARA ELABORAR LAMPARAS DE LAVA
 lava crea tu lampara de MANUAL PARA ELABORAR LAMPARAS DE LAVA índice: Lámpara de lava Materiales Recomendaciones Fabricación de la estructura de la lámpara Fabricación de la lava Preparación Terminado
lava crea tu lampara de MANUAL PARA ELABORAR LAMPARAS DE LAVA índice: Lámpara de lava Materiales Recomendaciones Fabricación de la estructura de la lámpara Fabricación de la lava Preparación Terminado
