Enzimas. Proteínas de forma globular. Catalizadores biológicos. Específicas para un substrato particular (Estéreo especificidad)
|
|
|
- Aarón Padilla Quiroga
- hace 6 años
- Vistas:
Transcripción
1 Enzimas
2 Enzimas Proteínas de forma globular. Catalizadores biológicos. Específicas para un substrato particular (Estéreo especificidad)
3 COO - C-H H-C COO - Fumarato (=,trans) COO - C-H C-H COO - Maleato (=,cis) + N H 3 + Aspartasa COO - H 3 + N-C-H COO - H-C- NH 3 + C-H 2 COO - C-H 2 COO - L-Aspartato D-Aspartato
4 Enzimas Proteínas de forma globular. Catalizadores biológicos. Específicas para un substrato particular (Estéreo especificidad) Aceleran reacciones químicas específicas ( ) Actúan en disolución acuosa, a ph y temp. óptimos
5 Enzima Temp. Ópt. ( o C) Mamíferos 37 Bacterias y algas aprox. 100 Bacterias Árticas aprox. 0 Bacterias en muestra de hielo antigua
6 Enzima ph óptimo Pepsina 1.5 Tripsina 7.7 Catalasa 7.6 Arginasa 9.7 Fumarasa 7.8 Ribonucleasa 7.8
7 Enzimas Proteínas de forma globular. Catalizadores biológicos. Específicas para un substrato particular (Estéreo especificidad) Aceleran reacciones químicas específicas ( ) Actúan en disolución acuosa, a ph y temp. óptimos Son las unidades funcionales del metabolismo celular
8
9 Enzimas Proteínas de forma globular. Catalizadores biológicos. Específicas para un substrato particular (Estéreo especificidad) Aceleran reacciones químicas específicas ( ) Actúan en disolución acuosa, a ph y temp. Óptimos Son las unidades funcionales del metabolismo celular Reacciones acopladas (catabolismo anabolismo)
10
11 Enzimas Proteínas de forma globular. Catalizadores biológicos. Específicas para un substrato particular (Estéreo especificidad) Aceleran reacciones químicas específicas ( ) Actúan en disolución acuosa, a ph y temp. Óptimos Son las unidades funcionales del metabolismo celular Reacciones acopladas (catabolismo anabolismo) Reguladoras de rutas metabólicas (Oligoméricas)
12 Enzima (gr). : fermento 1800 s fermentación del azúcar por levaduras Vitalistas Mecanicistas Eduard Buchner 1897 extracto de levadura 1926, James B. Summer Ureasa 1930 s John Howard Northrop Pepsina Tripsina Quimotripsina Carboxipeptidasa Enzima Amarillo viejo (flavoproteína NADPH)
13 Ribonucleasa Descubierta, bacteriólogo René Jules Dubo 1938 Aislada, químico Moses Kunitzen 1946 Sintetizada en residuos
14 Medicina Transaminasas Industria Química Penicilina Transformación de Alimentos Fermentaciones Quesos Vinos Agricultura Rhyzobium
15 Estructura globular Funcionalidad Hervir con HCl Tripsina Temperatura elevada ph extremo Inactiva
16 S: PM 250, 0.8 nm Ø E: PM , 7 nm Ø Cofactor Inorgánico: Fe 2+, Mn 2+, Zn 2+,etc. Grupo Prostético Orgánico: Coenzimas NAD, FAD, CoASH.
17 Apoenzima Holoenzima
18 Enzimas que requieren elementos inorgánicos Citocromo oxidasa Catalasa, peroxidasa Fe 2+, Fe +, Citocromo oxidasa Cu 2+ DNA polimerasa Anhídrasa carbónica Alcohol deshidrogensa Hexoquinasa Glucosa 6-fosfatasa Zn 2+ Mg 2+ Arginasa Mn 2+ Piruvato quinasa K +, Mg 2+ Ureasa Ni 2+ Nitrato reductasa Mo 2+
19 Coenzimas: Actúan como transportadores eventuales de átomos específicos o de grupos funcionales Coenzimas Pirofosfato de tiamina. Dinucleótido de flavina y adenina. Dinucleótido de nicotinamida y de adenina Coenzima A. Fosfato de Piridoxal. 5 -Desoxicobalamina (Coenzima B12) Biocitina. Tetrahidrofolato. Entidad transferida Aldehídos Átomos de hidrógeno Ion hidruro (H - ) Grupos acilo Grupos amino Átomos de H y grupos alquilo CO 2 Otros grupos monocarbonados
20
21 Coenzimas Adenosine Triphosphate (ATP) Coenzyme A (CoA) Nicotinamide Adenine Dinucleotide (NAD + ) Nicotinamide Adenine Dinucleotide Phosphate (NADP + ) Flavin Adenine Dinucleotide (FAD)
22 VITAMINAS C (ácido ascórbico) B1 (tiamina) B2 (riboflavina) B3 (ácido pantoténico) B5 (niacina) B6 (piridoxina) B12 (cobalamina) Biotina FUNCIONES Coenzima de algunas peptidasas. Interviene en la síntesis de colágeno Coenzima de las descarboxilasas y de las enzima que transfieren grupos aldehídos Constituyente de los coenzimas FAD y FMN Constituyente de la CoA Constituyente de las coenzimas NAD y NADP Interviene en las reacciones de transferencia de grupos aminos. Coenzima en la transferencia de grupos metilo. Coenzima de las enzimas que transfieren grupos carboxilo, en metabolismo de aminoácidos. Enfermedades carenciales Escorbuto Beriberi Dermatitis y lesiones en las mucosas Fatiga y trastornos del sueño Pelagra Depresión, anemia Anemia perniciosa Fatiga, dermatitis
23 Substrato Urea Arginina Enzima Ureasa Arginasa Pepsina Lis, Arg Tripsina Amilasa Rec A rec A gen HSP70 Proteína de choque térmico Caract. Comité de la Unión Internacional de Bioq. y Biol. Mol. (IUBMB)
24 Accepted name: EC alcohol dehydrogenase (NADP + ) Reaction: an alcohol + NADP + = an aldehyde + NADPH + H + Other na me(s): aldehyde reductase (NADPH2); NADP-alcohol dehydrogenase; NADP + - aldehyde reductase; NADP + -dependent aldehyde reductase; NADPHaldehyde reductase; NADPH-dependent aldehyde reductase; nonspecific succinic semialdehyde reductase; ALR 1; low-km aldehyde reductase; high-km aldehyde reductase; alcohol dehydrogenase (NADP + ) Systematic name: alcohol:nadp + oxidoreductase Comments: A zinc protein. Some members of this group oxidize only primary alcohols; others act also on secondary alcohols. May be identical with EC (L-glucuronate reductase), EC [mevaldate reductase (NADPH)] and EC [lactaldehyde reductase (NADPH)]. A-specific with respect to NADPH. Links to other da tabases: BRENDA, ERGO, EXPASY, IUBMB, KEGG, PDB, CAS registry number:
25 Clases de Enzimas: 1. Oxidorreductasas 2. Transferasas 3. Hidrolasas 4. Liasas 5. Isomerasas 6. Ligasas
26 EC 1.1 Acting on the CH-OH group of donors EC With NAD+ or NADP+ as acceptor EC alcohol dehydrogenase EC alcohol dehydrogenase (NADP+) EC homoserine dehydrogenase EC (R,R)-butanediol dehydrogenase EC acetoin dehydrogenase EC glycerol dehydrogenase EC With a cytochrome as acceptor EC now EC EC mannitol dehydrogenase (cytochrome) El segundo no. OH 1 Aldehído 2 CH-CH 3 Amino 4 EC With oxygen as acceptor EC deleted, included in EC EC now EC EC malate oxidase EC glucose oxidase EC With a disulfide as acceptor EC vitamin-k-epoxide reductase (warfarin-sensitive) EC With a quinone or similar compound as acceptor EC Deleted, see EC cellobiose dehydrogenase (acceptor) EC With other acceptors EC choline dehydrogenase EC hydroxyglutarate dehydrogenase
27 EC 1.2 Acting on the aldehyde or oxo group of donors EC With NAD+ or NADP+ as acceptor EC deleted, replaced by EC and EC EC formate dehydrogenase EC With a cytochrome as acceptor EC formate dehydrogenase (cytochrome) EC pyruvate dehydrogenase (cytochrome) EC With oxygen as acceptor EC aldehyde oxidase EC 1.3 Acting on the CH-CH group of donors EC With NAD+ or NADP+ as acceptor EC dihydrouracil dehydrogenase (NAD+) EC With a cytochrome as acceptor EC now EC EC now EC EC With oxygen as acceptor EC dihydroorotate oxidase EC now EC
28 Hexoquinasa Nombre formal: ATP, glucosa fosfotransferasa Nombre de la clase: Transferasa 7. Subclase ; Fosfotransferasa 1. Sub subclase: fosfotransferasas con un grupo OH como aceptor 1. Para la D-Glucosa como aceptor del grupo fosfato.
29 Clases de Enzimas: 1. Oxidorreductasas 2. Transferasas 3. Hidrolasas 4. Liasas 5. Isomerasas 6. Ligasas
30 Enzimas: No. Clase Tipo de reacción que catalizan Ejemplo 1 Oxidorreductasas De óxido reducción (transferencia de e-) Deshidrogenasas Peroxidasa Oxidasas Oxigenasas Reductasas Reducción: ganancia de electrones (hidrógeno o pérdida de oxígeno) Oxidación: pérdida de electrones (hidrógeno o ganancia de oxígeno). La Oxidación y la Reducción son reacciones acopladas (REDOX)
31 1. Oxido-reductasas ( Reacciones de oxido-reducción). Si una molécula se reduce, tiene que haber otra que se oxide Succinato Deshidrogenasa Citocromo c oxidasa.
32 Enzimas: No. Clase Tipo de reacción que catalizan 1 Oxidorreductasas De óxido reducción (transferencia de e-) Ejemplo Deshidrogenasas Peroxidasa Oxidasas Oxigenasas Reductasas 2 Transferasas Transferencia de grupos Kinasas Transaminasas
33 2. Transferasas (Transferencia de grupos funcionales) grupo aldehído grupo acilo grupo glucosilo grupo fosfato (kinasas)
34 Enzimas: No. Clase Tipo de reacción que catalizan 1 Oxidorreductasas De óxido reducción (transferencia de e-) Ejemplo Deshidrogenasas Peroxidasa Oxidasas Oxigenasas Reductasas 2 Transferasas Transferencia de grupos Kinasas Transaminasas 3 Hidrolasas Hidrólisis, con transferencia de grupos funcionales del agua Pirofosfatasa Tripsina Aldolasa
35 3. Hidrolasas (Reacciones de hidrólisis) Transforman polímeros en monómeros. Actúan sobre: enlace éster enlace glucosídico enlace peptídico enlace C-N
36 Enzimas: No. Clase Tipo de reacción que catalizan Ejemplo 1 Oxidorreductasas De óxido reducción (transferencia de e-) Deshidrogenasas Peroxidasa Oxidasas Oxigenasas Reductasas 2 Transferasas Transferencia de grupos Kinasas Transaminasas 3 Hidrolasas Hidrólisis, con transferencia de grupos funcionales del agua 4 Liasas Lisis de un substrato, generando un doble enlace, o Adición de un substrato a un doble enlace de un 2o. substrato Pirofosfatasa Tripsina Aldolasa (Sintasas) Descarboxilasa pirúvica
37 4. Liasas (Adición a los dobles enlaces) Entre C y C Entre C y O Entre C y N
38 Enzimas: No. Clase Tipo de reacción que catalizan 1 Oxidorreductasas De óxido reducción (transferencia de e-) Ejemplo Deshidrogenasas Peroxidasa Oxidasas Oxigenasas Reductasas 2 Transferasas Transferencia de grupos Kinasas Transaminasas 3 Hidrolasas Hidrólisis, con transferencia de grupos funcionales del agua 4 Liasas Lisis de un substrato, generando un doble enlace, o Adición de un substrato a un doble enlace de un 2o. substrato (Sintasa) Pirofosfatasa Tripsina Aldolasa (Sintasas) Descarboxilasa pirúvica 5 Isomerasas Transferencia de grupos en el interior de las moléculas para dar formas isómeras Mutasas Epimerasas Racemasas
39 5. Isomerasas (Reacciones de isomerización)
40 Enzimas: No. Clase Tipo de reacción que catalizan 1 Oxidorreductasas De óxido reducción (transferencia de e-) Ejemplo Deshidrogenasas Peroxidasa Oxidasas Oxigenasas Reductasas 2 Transferasas Transferencia de grupos Kinasas Transaminasas 3 Hidrolasas Hidrólisis, con transferencia de grupos funcionales del agua 4 Liasas Lisis de un substrato, generando un doble enlace, o Adición de un substrato a un doble enlace de un 2o. substrato (Sintasa) 5 Isomerasas Transferencia de grupos en el interior de las moléculas para dar formas isómeras 6 Ligasas Formación de enlaces C-C, C-S, C-O y C-N. Mediante reacciones de condensación, acopladas a la ruptura del ATP Pirofosfatasa Tripsina Aldolasa (Sintasas) Descarboxilasa pirúvica Mutasas Epimerasas Racemasas Sintetasas
41 6. Ligasas (Formación de enlaces, con aporte de ATP) Entre C y O Entre C y S Entre C y N Entre C y C
42 E + S SE E + P
43 Cómo detectar una enzima? 1. Actuación global de la reacción catalizada. 2. Utilizar un procedimiento analítico para la determinación de S que desaparece o los productos de la reacción que aparecen. 3. Si la enzima requiere cofactores (iónes metálicos o coenzimas). 4. La dependencia de la actividad enzimática con la [S] o sea K M del S. 5. El ph óptimo. 6. Un intervalo de temperatura en la que la enzima es estable y muestra actividad elevada.
44 1.0 Unidad de Actividad Enzimática Es la cantidad que transforma 1.0 mm (10-6 M) de S /min a 25 o C, en las condiciones de medida óptima. La Actividad Específica Es el no. de U de enzima / mg de proteína. Es una medida de la pureza de la enzima. Catalasa de Aspergillius niger U/mg de prot U U Catalasa de Hígado de bisonte U/mg de prot. 100 mg $ USD. 1 g $ USD.
45 El Número de Recambio de una Enzima Es el no. de moléculas de S transformadas / unidad de tiempo, por una molécula de enzima (o por un sólo sitio catalítico, cuando la E, es el limitante). Enzima. Anhidrasa carbónica b-amilasa b-galactosidasa Fosfoglucomutasa Moles de S, transf./ min. a o C
46 Ribozimas Moléculas de ARN que tienen la capacidad de actuar como catalizadores, (aceleran reacciones químicas específicas). Poseen un centro activo que se une específicamente a un sustrato y facilita su conversión en un producto. Menos versátiles que las enzimas proteicas. Implicadas en: Procesamiento o maduración del ARN y Síntesis de proteínas (ARNr, componentes del ribosoma cataliza la reacción de transpeptidación, o unión de los aminoácidos).
47
48 CINÉTICA ENZIMÁTICA
49 E + S SE E + P
50 PROPIEDADES GENERALES AUMENTAN LA VELOCIDAD DE REACCIÓN De 10 6 to veces vs sin enzima. Aún más rápido que los catalizadores químicos. CONDICIONES DE REACCIÓN Temperatura o C (algunas hasta 75 o C) ph neutro (5-9), la mayoría Presión atmosférica normal CAPACIDAD DE REGULACIÓN Por concentración de sustrato Por concentración de enzima Por inhibidores competitivos (semejantes al sustrato) Por inhibidores no competitivos (modificación covalente de la enzima) Por regulación alostérica ALTA ESPECIFICIDAD DE REACCIÓN Interacción estereoespecífica con el sustrato No hay productos colaterales
51 ALTA ESPECIFICIDAD DE REACCIÓN INTERACCIÓN ESTEREO ESPECÍFICA CON SU SUSTRATO
52 Los reactivos interaccionan con la enzima (sitio activo)
53 Cambia la configuración de la enzima
54 Substrato de glucosa Sitio de enlace La unión del sustrato produce un cambio conformacional de la enzima hexoquinasa (cinasa), la cual es monomérica.
55 Se realiza la reacción catalítica
56
57 Cinética enzimática V max K M K
58 K m de algunas enzimas ENZIMA SUSTRATO K m (mm) Catalasa H 2 O Hexoquinasa ATP 0.4 D-Glucosa 0.05 D-Fructosa 1.5 Anhidrasa carbónica HCO Quimotripsina Gliciltirosinilglicina N-Benzoiltirosinamida 2.5 b-galactosidasa D-Lactosa 4.0 Treonina deshidrogenasa L-Treonina 5.0
59 La K M es un parámetro de Actividad Enzimática La K M es inversamente proporcional con la actividad de la enzima. Valor de K M grande, baja actividad Valor de K M pequeño, alta actividad
60 Determinación Cuantitativa de la Cinética Enzimática 1. La reacción global 2. Procedimeinto analítico para determinar els que desaparece o el P que aparece 3. Sí el E requiere Cofactores (iónes o coenzimas) 4. La dependencia de la actividad enzimática con la [S] o se la K M del S. 5. El ph óptimo 6. Un intervalo de temperatura en la que la E es estable y muestra actividad elevada.
61 Actividad enzimática y variación del ph
62 Vo ph Enzima ph óptimo Pepsina 1.5 Tripsina 7.7 Catalasa 7.6 Arginasa 9.7 Fumarasa 7.8 Ribonucleasa 7.8 Vo Vo Vo Temperatura o C) Coenzima Tiempo (min)
63 1.0 Unidad de Actividad Enzimática (U): La cantidad que transforma 1.0 mmol (10-6 M) de S /min, a 25 0 C, en las condiciones de medida óptima. Actividad específica: Es el no. de U de una E / mg de proteína. Es decir: una medida de la pureza de la E. Al purificarla, el valor llega a un máximo y es estable. Número de recambio No. de moléculas de S transformadas /unidad de tiempo, por una molécula de E ( o por un solo sitio catalítico) Enzima No. de Recambio Anhidrasa carbónica B-Amilasa B-Galactosidasa Fosfoglucomutasa 1 240
64 Cuando: V o = Vmax Todos los sitios activos están ocupados y no hay moléculas de E libre. K M = [S] Sí... ½ Vmax K M representa la cantidad de sustrato necesaria para fijarse a la mitad de la E disponible y producir la mitad de la Vmax K M representa la concentración del sustrato en una célula
65 Inhibidores Reactivos químicos específicos que pueden inhibir a la mayor parte de las enzimas. Irreversibles INHIBIDORES Reversibles
66 Inhibidor Irreversible Fluorofosfato de diisopropilo (DFP) Acetilcolina Acetilcolinesterasa Acetato + Colina
67 Inhibidor Irreversible Acetilcolinesterasa Tripsina Elastasa Fosfoglucomutasa Cocoonasa (larvas de gusanos de seda Fluorofosfato de diisopropilo (DFP) Malatión
68 Fluorofosfato de diisopropilo (DFP) Serina Iodoacetamida Cisteína Histidina
69 Inhibidor Reversible La unión del inhibidor y la enzima es reversible. Al quitar el inhibidor del medio, se recupera la actividad. Hay 3 tipos: Competitiva No Competitiva Acompetitiva (Alostérica)
70 Antibióticos Insecticidas Hervicidas Venenos Diferentes Medicamentos Inhibición enzimática Dolor Inflamación Infecciones virales Cáncer
71 Inhibidores Competitivos Malonato Sulfas Deshidrogenasa del ácido succínico Infecciones microbianas Antihipertensores: Captopril y Enalopril Alopurinol Fluoruracilo Controla la gota Cáncer
72 Cinéticas de Inhibición Competitivo V max igual K M diferente 1 V No competitivo V max diferente K M igual No inhibitor 0 1/[S]
73
UNIVERSIDAD PERUANA CAYETANO HEREDIA CENTRO FORMATIVO PREUNIVERSITARIO BIOLOGÍA METABOLISMO
 UNIVERSIDAD PERUANA CAYETANO HEREDIA CENTRO FORMATIVO PREUNIVERSITARIO BIOLOGÍA METABOLISMO METABOLISMO Ciclo interdependendiente, intercambio de E y materia. AUTOTROFOS FOTOSINTETICOS HETEROTROFOS Procesos
UNIVERSIDAD PERUANA CAYETANO HEREDIA CENTRO FORMATIVO PREUNIVERSITARIO BIOLOGÍA METABOLISMO METABOLISMO Ciclo interdependendiente, intercambio de E y materia. AUTOTROFOS FOTOSINTETICOS HETEROTROFOS Procesos
CARACTERÍSTICAS DE LAS ENZIMAS
 BIOQUÍMICA I CARACTERÍSTICAS DE LAS ENZIMAS 1. Son los catalizadores de las reacciones químicas de los sistemas biológicos. 2. Tienen gran poder catalítico. 3. Poseen un elevado grado de especificidad
BIOQUÍMICA I CARACTERÍSTICAS DE LAS ENZIMAS 1. Son los catalizadores de las reacciones químicas de los sistemas biológicos. 2. Tienen gran poder catalítico. 3. Poseen un elevado grado de especificidad
Tema 7. Actividad enzimática
 Tema 7. Actividad enzimática Definición, clasificación y nomenclatura de las enzimas Coenzimas y cofactores Mecanismos de la catálisis enzimática Centro activo y especificidad Tipos de catálisis Generalidades
Tema 7. Actividad enzimática Definición, clasificación y nomenclatura de las enzimas Coenzimas y cofactores Mecanismos de la catálisis enzimática Centro activo y especificidad Tipos de catálisis Generalidades
LAS ENZIMAS ENZIMAS CLASIFICACIÓN ESTRUCTURA FUNCIÓN. Biocatalizadores. proteica. velocidad reacción. Energía activación. Inorgánica.
 LAS ENZIMAS ENZIMAS ESTRUCTURA puede ser FUNCIÓN CLASIFICACIÓN Holoenzima formada Estrictamente proteica Biocatalizadores actúan Ligasas Isomerasas Liasas Hidrolasas Transferasas Oxidorreductasas de naturaleza
LAS ENZIMAS ENZIMAS ESTRUCTURA puede ser FUNCIÓN CLASIFICACIÓN Holoenzima formada Estrictamente proteica Biocatalizadores actúan Ligasas Isomerasas Liasas Hidrolasas Transferasas Oxidorreductasas de naturaleza
ESTRUCTURA DE LA TRIOSAFOSFATO ISOMERASA esta proteína es una eficiente enzima involucrada en la vía glucolítica.
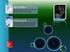 ESTRUCTURA DE LA TRIOSAFOSFATO ISOMERASA esta proteína es una eficiente enzima involucrada en la vía glucolítica. Características generales Cinética química Nomenclatura Centro activo Cofactores Factores
ESTRUCTURA DE LA TRIOSAFOSFATO ISOMERASA esta proteína es una eficiente enzima involucrada en la vía glucolítica. Características generales Cinética química Nomenclatura Centro activo Cofactores Factores
ENZIMAS APOENZIMAS: COENZIMAS:
 ENZIMAS En los seres vivos se están desarrollando continuamente una serie de reacciones químicas que, si se realizaran en un laboratorio, sólo podrían llevarse a cabo mediante altas temperaturas, descargas
ENZIMAS En los seres vivos se están desarrollando continuamente una serie de reacciones químicas que, si se realizaran en un laboratorio, sólo podrían llevarse a cabo mediante altas temperaturas, descargas
PROTEINAS COMO CATALIZADORES ENZIMAS
 PROTEINAS COMO CATALIZADORES ENZIMAS ENZIMAS son proteínas que catalizan reacciones químicas en los seres vivos. son catalizadores: sustancias que, sin consumirse en una reacción, aumentan notablemente
PROTEINAS COMO CATALIZADORES ENZIMAS ENZIMAS son proteínas que catalizan reacciones químicas en los seres vivos. son catalizadores: sustancias que, sin consumirse en una reacción, aumentan notablemente
Enzimas Departamento de Bioquímica Noviembre de 2005
 U.T.I. Biología Celular Enzimas Departamento de Bioquímica Noviembre de 2005 Enzimas A. Propiedades generales de las enzimas B. Principios fundamentales de su acción catalítica C. Introducción a la cinética
U.T.I. Biología Celular Enzimas Departamento de Bioquímica Noviembre de 2005 Enzimas A. Propiedades generales de las enzimas B. Principios fundamentales de su acción catalítica C. Introducción a la cinética
ENZIMAS I TEMA Introducción
 TEMA 7 ENZIMAS I 1. Introducción 2. Las enzimas como catalizadores 3. Nomenclatura y clasificación de enzimas 4. Cofactores enzimáticos 5. Modelos de actuación de las enzimas 1. Introducción La vida depende
TEMA 7 ENZIMAS I 1. Introducción 2. Las enzimas como catalizadores 3. Nomenclatura y clasificación de enzimas 4. Cofactores enzimáticos 5. Modelos de actuación de las enzimas 1. Introducción La vida depende
TEMA 4 (II). LAS ENZIMAS.
 TEMA 4 (II). LAS ENZIMAS. 1. Introducción. Las transformaciones que ocurren en los seres vivos son el resultado de un conjunto de reacciones químicas que constituyen el metabolismo celular. Estas reacciones
TEMA 4 (II). LAS ENZIMAS. 1. Introducción. Las transformaciones que ocurren en los seres vivos son el resultado de un conjunto de reacciones químicas que constituyen el metabolismo celular. Estas reacciones
Generalidades de ENZIMAS
 UNIVERSIDAD DE SAN CARLOS DE GUATEMALA FACULTAD DE CIENCIAS MÉDICAS FASE I, Unidad Didáctica: BIOQUÍMICA MÉDICA 2º AÑO CICLO ACADÉMICO 2,007 Generalidades de ENZIMAS Dr. Mynor Leiva 1 ENZIMAS Proteínas
UNIVERSIDAD DE SAN CARLOS DE GUATEMALA FACULTAD DE CIENCIAS MÉDICAS FASE I, Unidad Didáctica: BIOQUÍMICA MÉDICA 2º AÑO CICLO ACADÉMICO 2,007 Generalidades de ENZIMAS Dr. Mynor Leiva 1 ENZIMAS Proteínas
Universidad Nacional de la Patagonia S. J. B Facultad de Ciencias Naturales Química Biológica. Química Biológica TP 5 ENZIMAS, Introducción
 TP 5 ENZIMAS, Introducción Las funciones vitales de la célula no son más que una serie de reacciones químicas, que en conjunto determinan la existencia de una verdadera maraña de procesos y vías metabólicas.
TP 5 ENZIMAS, Introducción Las funciones vitales de la célula no son más que una serie de reacciones químicas, que en conjunto determinan la existencia de una verdadera maraña de procesos y vías metabólicas.
A + B [A + B] C + D E.A. Los principales biocatalizadores son: enzimas, vitaminas, hormonas y algunos oligoelementos (Fe, Cu, Zn, I, F, ).
![A + B [A + B] C + D E.A. Los principales biocatalizadores son: enzimas, vitaminas, hormonas y algunos oligoelementos (Fe, Cu, Zn, I, F, ). A + B [A + B] C + D E.A. Los principales biocatalizadores son: enzimas, vitaminas, hormonas y algunos oligoelementos (Fe, Cu, Zn, I, F, ).](/thumbs/30/14266899.jpg) TEMA 5: ENZIMAS 1. Concepto de biocatalizador En toda reacción química, los reactivos (A + B) se unen para dar los productos (C + D). En toda reacción existe un paso intermedio llamado complejo o estado
TEMA 5: ENZIMAS 1. Concepto de biocatalizador En toda reacción química, los reactivos (A + B) se unen para dar los productos (C + D). En toda reacción existe un paso intermedio llamado complejo o estado
Estructurales: dan forma a la proteína.
 1. Concepto de biocatalizador. Son sustancias que consiguen que las reacciones se realicen a gran velocidad a bajas temperaturas, ya que disminuyen la energía de activación de los reactivos. Pueden ser:
1. Concepto de biocatalizador. Son sustancias que consiguen que las reacciones se realicen a gran velocidad a bajas temperaturas, ya que disminuyen la energía de activación de los reactivos. Pueden ser:
D.-Cinética de las reacciones catalizadas enzimáticamente: cinética de Michaelis-Menten E.- Factores que afectan la actividad enzimática
 A.- Concepto de catálisis B.- Los enzimas como biocatalizadores: características de la actividad enzimática C.-Mecanismo de la actividad enzimática Concepto de centro activo D.-Cinética de las reacciones
A.- Concepto de catálisis B.- Los enzimas como biocatalizadores: características de la actividad enzimática C.-Mecanismo de la actividad enzimática Concepto de centro activo D.-Cinética de las reacciones
BIENVENIDOS A la unidad didáctica. Dr. MYNOR LEIVA E.
 BIENVENIDOS A la unidad didáctica Dr. MYNOR LEIVA E. Como esta organizada la unidad didáctica de bioquímica Oficina 214. Coordinador: Dr. Estuardo Pacheco. 10 catedráticos. 2 técnicos de laboratorio. (of
BIENVENIDOS A la unidad didáctica Dr. MYNOR LEIVA E. Como esta organizada la unidad didáctica de bioquímica Oficina 214. Coordinador: Dr. Estuardo Pacheco. 10 catedráticos. 2 técnicos de laboratorio. (of
CLASIFICACIÓN DE ENZIMAS
 Nomenclatura CLASIFICACIÓN DE ENZIMAS TEMA 15 Muchos se denominan utilizando el sufijo asa a continuación del nombre del sustrato Ej: Ureasa DNA polimerasa Existen también nombres que no se refieren al
Nomenclatura CLASIFICACIÓN DE ENZIMAS TEMA 15 Muchos se denominan utilizando el sufijo asa a continuación del nombre del sustrato Ej: Ureasa DNA polimerasa Existen también nombres que no se refieren al
ESTUDIOS CINÉTICOS SE MIDE LA VELOCIDAD DE LA REACCIÓN CATALIZADA. La velocidad de reacciones químicas: Para una reacción:
 ESTUDIOS CINÉTICOS SE MIDE LA VELOCIDAD DE LA REACCIÓN CATALIZADA La velocidad de reacciones químicas: Para una reacción: A B La velocidad depende de la concentración del reactante: v = k[a] k = constante
ESTUDIOS CINÉTICOS SE MIDE LA VELOCIDAD DE LA REACCIÓN CATALIZADA La velocidad de reacciones químicas: Para una reacción: A B La velocidad depende de la concentración del reactante: v = k[a] k = constante
1. Necesidad energética de las células. Concepto de metabolismo.
 1. Necesidad energética de las células. Concepto de metabolismo. Las células intercambian continuamente materia y energía con su entorno. La materia y energía son transformadas en su interior con objeto
1. Necesidad energética de las células. Concepto de metabolismo. Las células intercambian continuamente materia y energía con su entorno. La materia y energía son transformadas en su interior con objeto
1.- CONCEPTO DE ENZIMA
 ENZIMAS 1.- CONCEPTO DE ENZIMA Los enzimas son catalizadores muy potentes y eficaces, Químicamente son proteínas Actúan en pequeña cantidad y se recuperan indefinidamente No llevan a cabo reacciones energéticamente
ENZIMAS 1.- CONCEPTO DE ENZIMA Los enzimas son catalizadores muy potentes y eficaces, Químicamente son proteínas Actúan en pequeña cantidad y se recuperan indefinidamente No llevan a cabo reacciones energéticamente
REACCIONES METABÓLICAS
 REACCIONES METABÓLICAS Todas las reacciones químicas que tienen lugar en las células son reacciones metabolicas Todos los procesos vitales son consecuencia de reacciones metabólicas Algunas características
REACCIONES METABÓLICAS Todas las reacciones químicas que tienen lugar en las células son reacciones metabolicas Todos los procesos vitales son consecuencia de reacciones metabólicas Algunas características
Clase 4 Metabolismo bacteriano
 Clase 4 Metabolismo bacteriano Composición química de las bacterias. Fuentes de carbono y energía. Categorías nutricionales. Catabolismo y anabolismo. Reacciones de óxido-reducción, torre de electrones,
Clase 4 Metabolismo bacteriano Composición química de las bacterias. Fuentes de carbono y energía. Categorías nutricionales. Catabolismo y anabolismo. Reacciones de óxido-reducción, torre de electrones,
LA ENERGÍA EN LAS REACCIONES METABÓLICAS
 LA ENERGÍA EN LAS REACCIONES METABÓLICAS ENERGIA DE ACTIVACIÓN. CATALIZADORES ENERGIA DE ACTIVACIÓN. CATALIZADORES REACTIVOS PRODUCTOS ENERGIA DE ACTIVACIÓN. ENZIMAS Las ENZIMAS son proteínas que ACTÚAN
LA ENERGÍA EN LAS REACCIONES METABÓLICAS ENERGIA DE ACTIVACIÓN. CATALIZADORES ENERGIA DE ACTIVACIÓN. CATALIZADORES REACTIVOS PRODUCTOS ENERGIA DE ACTIVACIÓN. ENZIMAS Las ENZIMAS son proteínas que ACTÚAN
TEMA 11.- CINÉTICA ENZIMÁTICA
 TEMA 11.- CINÉTICA ENZIMÁTICA Introducción: Cinética enzimática. Ecuación de Michaelis-Menten. Ecuación de Lineweaver-Burk. Reacciones con múltiples substratos. Inhibición enzimática: - Reversible Competitiva.
TEMA 11.- CINÉTICA ENZIMÁTICA Introducción: Cinética enzimática. Ecuación de Michaelis-Menten. Ecuación de Lineweaver-Burk. Reacciones con múltiples substratos. Inhibición enzimática: - Reversible Competitiva.
ENZIMAS. Kuhne en el año de 1876 les llamó enzima a los catalizadores que producían
 ENZIMAS Dr. Santiago René Anzaldúa Arce. Kuhne en el año de 1876 les llamó enzima a los catalizadores que producían fermentaciones de diversos compuestos, La palabra enzima significa en la levadura, pues
ENZIMAS Dr. Santiago René Anzaldúa Arce. Kuhne en el año de 1876 les llamó enzima a los catalizadores que producían fermentaciones de diversos compuestos, La palabra enzima significa en la levadura, pues
Son CATALIZADORES, es decir, disminuyen la energía de activación de las reacciones químicas. Son PROTEÍNAS con estructura tridimensional, que poseen
 Son CATALIZADORES, es decir, disminuyen la energía de activación de las reacciones químicas. Son PROTEÍNAS con estructura tridimensional, que poseen un centro activo en el que se acopla el sustrato para
Son CATALIZADORES, es decir, disminuyen la energía de activación de las reacciones químicas. Son PROTEÍNAS con estructura tridimensional, que poseen un centro activo en el que se acopla el sustrato para
PROPEDÉUTICO DE ODONTOLOGÍA BIOQUÍMICA BÁSICA
 PROPEDÉUTICO DE ODONTOLOGÍA BIOQUÍMICA BÁSICA 2012 Dagmar Stojanovic de Malpica Ph D Escuela de Biología, Facultad de Ciencias, U.C.V. UNIDAD IV. ENZIMAS Relación entre el G o y la K eq en una reacción
PROPEDÉUTICO DE ODONTOLOGÍA BIOQUÍMICA BÁSICA 2012 Dagmar Stojanovic de Malpica Ph D Escuela de Biología, Facultad de Ciencias, U.C.V. UNIDAD IV. ENZIMAS Relación entre el G o y la K eq en una reacción
ENZIMAS. Las enzimas son proteínas con función catalítica
 ENZIMAS Las enzimas son proteínas con función catalítica Las enzimas son catalizadores biológicos que permiten que las reacciones metabólicas ocurran a gran velocidad en condiciones compatibles con la
ENZIMAS Las enzimas son proteínas con función catalítica Las enzimas son catalizadores biológicos que permiten que las reacciones metabólicas ocurran a gran velocidad en condiciones compatibles con la
METABOLISMO Y ENZIMAS
 DESAFÍO Nº 12 Profesora Verónica Abasto Córdova Biología 1 Medio Nombre del Estudiante : Curso : METABOLISMO Y ENZIMAS TIMBRE METABOLISMO En las clases anteriores, estudiamos los principios de la teoría
DESAFÍO Nº 12 Profesora Verónica Abasto Córdova Biología 1 Medio Nombre del Estudiante : Curso : METABOLISMO Y ENZIMAS TIMBRE METABOLISMO En las clases anteriores, estudiamos los principios de la teoría
EL CONTROL DE LAS ACTIVIDADES CELULARES
 EL CONTROL DE LAS ACTIVIDADES CELULARES LAS REACCIONES CELULARES BÁSICAS Todas las células llevan a cabo funciones vitales: Ingestión de nutrientes Eliminación de desperdicios Crecimiento Reproducción
EL CONTROL DE LAS ACTIVIDADES CELULARES LAS REACCIONES CELULARES BÁSICAS Todas las células llevan a cabo funciones vitales: Ingestión de nutrientes Eliminación de desperdicios Crecimiento Reproducción
ENZIMAS I TEMA 7. 1. Introducción
 TEMA 7 ENZIMAS I 1. Introducción 2. Las enzimas como catalizadores 3. Nomenclatura y clasificación de enzimas 4. Cofactores enzimáticos 5. Modelos de actuación de las enzimas 1. Introducción La vida depende
TEMA 7 ENZIMAS I 1. Introducción 2. Las enzimas como catalizadores 3. Nomenclatura y clasificación de enzimas 4. Cofactores enzimáticos 5. Modelos de actuación de las enzimas 1. Introducción La vida depende
Respiración Aeróbica y Anaeróbica, y Control
 Fisiología Vegetal Respiración Aeróbica y Anaeróbica, y Control Dra. Karen Peña R Respiración: Oxido-Reducción Organelos Glicólisis, Formación de acetil CoA, Ciclo de Krebs, Cadena Transportadora de Electrones,
Fisiología Vegetal Respiración Aeróbica y Anaeróbica, y Control Dra. Karen Peña R Respiración: Oxido-Reducción Organelos Glicólisis, Formación de acetil CoA, Ciclo de Krebs, Cadena Transportadora de Electrones,
Ciclo de Krebs Destino del piruvato. Descarboxilación oxidativa. Aspectos estructurales y mecanismos de la piruvato deshidrogenasa.
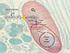 Ciclo de Krebs Destino del piruvato. Descarboxilación oxidativa. Aspectos estructurales y mecanismos de la piruvato deshidrogenasa. Relevancia del ciclo de Krebs dentro del metabolismo en general. Descripción
Ciclo de Krebs Destino del piruvato. Descarboxilación oxidativa. Aspectos estructurales y mecanismos de la piruvato deshidrogenasa. Relevancia del ciclo de Krebs dentro del metabolismo en general. Descripción
METABOLISMO DE PROTEINAS Y AMINOACIDOS
 sección III, metabolismo de proteínas y aminoácidos. Harper, bioquímica, 28a edición. ALFREDO ABADIA G. RESIDENTE III AÑO MD DE LA ACTIVIDAD FISICA Y EL DEPORTE FUCS-HISJ. METABOLISMO DE PROTEINAS Y AMINOACIDOS
sección III, metabolismo de proteínas y aminoácidos. Harper, bioquímica, 28a edición. ALFREDO ABADIA G. RESIDENTE III AÑO MD DE LA ACTIVIDAD FISICA Y EL DEPORTE FUCS-HISJ. METABOLISMO DE PROTEINAS Y AMINOACIDOS
Planta en desarrollo. Energía
 Respiración Planta en desarrollo Energía Respiración La característica más importante de la respiración es la liberación de energía susceptible de ser utilizada en cualquier ruta metabólica Ruta metabólica
Respiración Planta en desarrollo Energía Respiración La característica más importante de la respiración es la liberación de energía susceptible de ser utilizada en cualquier ruta metabólica Ruta metabólica
Enzimas y Cinética Enzimática
 Enzimas y Cinética Enzimática Temas Selectos de Bioquímica General Todas las reacciones químicas del metabolismo celular se realizan gracias a la acción de ciertas moléculas de origen proteico llamadas:
Enzimas y Cinética Enzimática Temas Selectos de Bioquímica General Todas las reacciones químicas del metabolismo celular se realizan gracias a la acción de ciertas moléculas de origen proteico llamadas:
Enzimas: conceptos básicos y cinéticos
 Enzimas: conceptos básicos y cinéticos ENZIMAS CATALIZADOR BIOLÓGICO Poder catalítico Especificidad S + E ES E + P S= Sustrato P= Producto ES= Complejo enzima-sustrato Enzyme Nonenzymatic half-life Uncatalyzed
Enzimas: conceptos básicos y cinéticos ENZIMAS CATALIZADOR BIOLÓGICO Poder catalítico Especificidad S + E ES E + P S= Sustrato P= Producto ES= Complejo enzima-sustrato Enzyme Nonenzymatic half-life Uncatalyzed
Biopolímero s (4831)
 Biopolímero s (4831) 4.3. Conceptos de catálisis química. 4.3.3. Ejemplos de tipos de catálisis. Aplicación a la catálisis enzimática Los iones metálicos como catalizadores Como se dijo anteriormente los
Biopolímero s (4831) 4.3. Conceptos de catálisis química. 4.3.3. Ejemplos de tipos de catálisis. Aplicación a la catálisis enzimática Los iones metálicos como catalizadores Como se dijo anteriormente los
En el APOENZIMA se distinguen tres tipos de aminoácidos:
 1. Concepto de biocatalizador. Son sustancias que consiguen que las reacciones se realicen a gran velocidad a bajas temperaturas, ya que disminuyen la energía de activación de los reactivos. Pueden ser:
1. Concepto de biocatalizador. Son sustancias que consiguen que las reacciones se realicen a gran velocidad a bajas temperaturas, ya que disminuyen la energía de activación de los reactivos. Pueden ser:
J. L. Sánchez Guillén. IES Pando - Oviedo Departamento de Biología y Geología
 J. L. Sánchez Guillén IES Pando - Oviedo Departamento de Biología y Geología METABOLISMO: Conjunto de procesos químicos que se producen en la célula, catalizados por enzimas y que tienen como objetivo
J. L. Sánchez Guillén IES Pando - Oviedo Departamento de Biología y Geología METABOLISMO: Conjunto de procesos químicos que se producen en la célula, catalizados por enzimas y que tienen como objetivo
Fosforilación a nivel de sustrato. Fosforilación Oxidativa (Fosforilación a nivel de Cadena Respiratoria).
 Fosforilación a nivel de sustrato Fosforilación Oxidativa (Fosforilación a nivel de Cadena Respiratoria). La Fosforilación a nivel de sustrato es un mecanismo poco habitual de formación de ATP FOSFOGLICERATO
Fosforilación a nivel de sustrato Fosforilación Oxidativa (Fosforilación a nivel de Cadena Respiratoria). La Fosforilación a nivel de sustrato es un mecanismo poco habitual de formación de ATP FOSFOGLICERATO
5) EL METABOLISMO CELULAR: GENERALIDADES. ENZIMAS
 5) EL METABOLISMO CELULAR: GENERALIDADES. ENZIMAS EL METABOLISMO: CONCEPTO La nutrición de las células supone una serie de complejos procesos químicos catalizados por enzimas que tienen como finalidad
5) EL METABOLISMO CELULAR: GENERALIDADES. ENZIMAS EL METABOLISMO: CONCEPTO La nutrición de las células supone una serie de complejos procesos químicos catalizados por enzimas que tienen como finalidad
Tema 10. Regulación de la actividad enzimática
 Tema 10. Regulación de la actividad enzimática Control de la actividad enzimática Regulación por cambios en la concentración de enzima Regulación alostérica Modificaciones covalentes reversibles Activación
Tema 10. Regulación de la actividad enzimática Control de la actividad enzimática Regulación por cambios en la concentración de enzima Regulación alostérica Modificaciones covalentes reversibles Activación
Similitudes y Diferencias entre los catalizadores inorgánico y las enzimas
 CINETICA ENZIATICA Enzimas: Determinan la pauta de las reacciones quimicas Intervienen en mecanismos de transduccion de Energia Estabilizan un estado de transicion Poseen alta especificidad de sustrato.
CINETICA ENZIATICA Enzimas: Determinan la pauta de las reacciones quimicas Intervienen en mecanismos de transduccion de Energia Estabilizan un estado de transicion Poseen alta especificidad de sustrato.
Es la capacidad de realizar un trabajo. En términos bioquímicos: representa la capacidad de cambio, ya que la vida depende de que la energía pueda
 Es la capacidad de realizar un trabajo. En términos bioquímicos: representa la capacidad de cambio, ya que la vida depende de que la energía pueda ser transformada de una forma a otra, cuyo estudio es
Es la capacidad de realizar un trabajo. En términos bioquímicos: representa la capacidad de cambio, ya que la vida depende de que la energía pueda ser transformada de una forma a otra, cuyo estudio es
TEMA 15: EL CONTROL BIOQUÍMICO: ENZIMAS Y VITAMINAS
 TEMA 15: EL CONTROL BIOQUÍMICO: ENZIMAS Y VITAMINAS 1. CONCEPTO DE BIOCATALIZADOR. ENZIMAS 2. COMPOSICIÓN QUÍMICA DE LAS ENZIMAS 3. CLASIFICACIÓN 4. PROPIEDADES 5. LA REACCIÓN ENZIMÁTICA 6. REGULACIÓN
TEMA 15: EL CONTROL BIOQUÍMICO: ENZIMAS Y VITAMINAS 1. CONCEPTO DE BIOCATALIZADOR. ENZIMAS 2. COMPOSICIÓN QUÍMICA DE LAS ENZIMAS 3. CLASIFICACIÓN 4. PROPIEDADES 5. LA REACCIÓN ENZIMÁTICA 6. REGULACIÓN
QUÍMICA BIOINORGÁNICA DEL ZINC
 QUÍMICA BIOINORGÁNICA DEL ZINC CARACTERÍSTICAS QUÍMICAS DE INTERÉS BIOLÓGICO ESTADO DE OXIDACIÓN ÚNICO: Zn(II) NO INTERVIENE EN REACCIONES REDOX pk a =9,6 NEUTRO PUEDE EXISTIR LIBRE EN EL PLASMA HUMANO
QUÍMICA BIOINORGÁNICA DEL ZINC CARACTERÍSTICAS QUÍMICAS DE INTERÉS BIOLÓGICO ESTADO DE OXIDACIÓN ÚNICO: Zn(II) NO INTERVIENE EN REACCIONES REDOX pk a =9,6 NEUTRO PUEDE EXISTIR LIBRE EN EL PLASMA HUMANO
BLOQUE I: LAS MOLÉCULAS DE LA VIDA ENZIMAS. 2. Mecanismo de acción y cinética enzimática.
 ENZIMAS 1. Concepto y estructura. 2. Mecanismo de acción y cinética enzimática. 3. Regulación de la actividad enzimática: temperatura, ph, inhibidores. 4. Bibliografía. 5. Preguntas selectividad. Imagen
ENZIMAS 1. Concepto y estructura. 2. Mecanismo de acción y cinética enzimática. 3. Regulación de la actividad enzimática: temperatura, ph, inhibidores. 4. Bibliografía. 5. Preguntas selectividad. Imagen
FOSFORILACIÓN OXIDATIVA
 FOSFORILACIÓN OXIDATIVA a) Reacciones de transferencia de electrones en las mitocondrias b) Síntesis de ATP LOCALIZACIÓN Y ESTRUCTURA DE LAS MITOCONDRIAS LA FOSFORILACIÓN OXIDATIVA SE LLEVA A CABO EN LA
FOSFORILACIÓN OXIDATIVA a) Reacciones de transferencia de electrones en las mitocondrias b) Síntesis de ATP LOCALIZACIÓN Y ESTRUCTURA DE LAS MITOCONDRIAS LA FOSFORILACIÓN OXIDATIVA SE LLEVA A CABO EN LA
RESULTADO DE APRENDIZAJE:
 Explicar las reacciones químicas del ciclo de Krebs y su regulación RESULTADO DE APRENDIZAJE: Relacionar el metabolismo de las distintas macromoléculas alrededor del Ciclo de Krebs Las reacciones se llevan
Explicar las reacciones químicas del ciclo de Krebs y su regulación RESULTADO DE APRENDIZAJE: Relacionar el metabolismo de las distintas macromoléculas alrededor del Ciclo de Krebs Las reacciones se llevan
TEMA IV. GLUCÓLISIS. 1.Generalidades 2.Reacciones de la glucólisis 3.Control de la glucólisis
 TEMA IV. GLUCÓLISIS 1.Generalidades 2.Reacciones de la glucólisis 3.Control de la glucólisis PRINCIPALES DESTINOS DE LA GLUCOSA SÍNTESIS DE GLUCÓGENO, ALMIDÓN, SACAROSA Reserva GLUCOSA Oxidación vía Pentosas
TEMA IV. GLUCÓLISIS 1.Generalidades 2.Reacciones de la glucólisis 3.Control de la glucólisis PRINCIPALES DESTINOS DE LA GLUCOSA SÍNTESIS DE GLUCÓGENO, ALMIDÓN, SACAROSA Reserva GLUCOSA Oxidación vía Pentosas
ENZIMAS Y VITAMINAS I.- ENZIMAS CENTRO DE ESTUDIOS MIRASIERRA
 ENZIMAS Y VITAMINAS I.- ENZIMAS 1.1.- Actividad enzimática 1.2.- Estructura de las enzimas 1.3.- Coenzimas 1.4.- Regulación de la actividad enzimática. 1.5.- Especificidad de las enzimas 1.6.- Enzimas
ENZIMAS Y VITAMINAS I.- ENZIMAS 1.1.- Actividad enzimática 1.2.- Estructura de las enzimas 1.3.- Coenzimas 1.4.- Regulación de la actividad enzimática. 1.5.- Especificidad de las enzimas 1.6.- Enzimas
Bioquímica Estructural y Metabólica. TEMA 5. Enzimología
 TEMA 5. Enzimas. Clasificación. Principios de la catálisis enzimá6ca. Energía de ac6vación. Velocidad de reacción y equilibrio de reacción. Ciné6ca enzimá6ca: ecuación de Michaelis- Menten. Ecuación de
TEMA 5. Enzimas. Clasificación. Principios de la catálisis enzimá6ca. Energía de ac6vación. Velocidad de reacción y equilibrio de reacción. Ciné6ca enzimá6ca: ecuación de Michaelis- Menten. Ecuación de
TEMA 12: EL METABOLISMO
 1 El metabolismo. TEMA 12: EL METABOLISMO 1.1 Concepto de metabolismo Metabolismo: Conjunto de reacciones químicas que se producen en el interior de las células y que conducen a la transformación de unas
1 El metabolismo. TEMA 12: EL METABOLISMO 1.1 Concepto de metabolismo Metabolismo: Conjunto de reacciones químicas que se producen en el interior de las células y que conducen a la transformación de unas
METABOLISMO CELULAR Metabolismo celular ruta vía metabólica ANABÓLICAS CATABÓLICAS
 METABOLISMO CELULAR Metabolismo celular: conjunto de reacciones químicas que se producen en la célula y que conducen a la transformación de unas biomoléculas en otras con el fin de obtener materia (nuevas
METABOLISMO CELULAR Metabolismo celular: conjunto de reacciones químicas que se producen en la célula y que conducen a la transformación de unas biomoléculas en otras con el fin de obtener materia (nuevas
Es la capacidad de realizar un trabajo. A pesar que existen varias formas de energía: química, luminosa, mecánica, etc., solo hay dos tipos básicos:
 Es la capacidad de realizar un trabajo. A pesar que existen varias formas de energía: química, luminosa, mecánica, etc., solo hay dos tipos básicos: Potencial: es la capacidad de realizar trabajo como
Es la capacidad de realizar un trabajo. A pesar que existen varias formas de energía: química, luminosa, mecánica, etc., solo hay dos tipos básicos: Potencial: es la capacidad de realizar trabajo como
1- DESCARBOXILACIÓN OXIDATIVA DEL PIRUVATO. 2- CICLO DE KREBS. Dr. Mynor A. Leiva Enríquez
 UNIVERSIDAD DE SAN CARLOS DE GUATEMALA FACULTAD DE CIENCIAS MÉDICAS FASE I, Unidad Didáctica: BIOQUÍMICA MÉDICA 2º AÑO, 2011 1- DESCARBOXILACIÓN OXIDATIVA DEL PIRUVATO. 2- CICLO DE KREBS. Dr. Mynor A.
UNIVERSIDAD DE SAN CARLOS DE GUATEMALA FACULTAD DE CIENCIAS MÉDICAS FASE I, Unidad Didáctica: BIOQUÍMICA MÉDICA 2º AÑO, 2011 1- DESCARBOXILACIÓN OXIDATIVA DEL PIRUVATO. 2- CICLO DE KREBS. Dr. Mynor A.
OXIDACIÓN DEL PIRUVATO Y CICLO DE KREBS (o ciclo del ácido cítrico, o ciclo de los ácidos tricarboxílicos)
 OXIDACIÓN DEL IRUVATO Y CICLO DE KREBS (o ciclo del ácido cítrico, o ciclo de los ácidos tricarboxílicos) Estos procesos oxidan completamente el piruvato hasta CO 2, es decir completan la oxidación total
OXIDACIÓN DEL IRUVATO Y CICLO DE KREBS (o ciclo del ácido cítrico, o ciclo de los ácidos tricarboxílicos) Estos procesos oxidan completamente el piruvato hasta CO 2, es decir completan la oxidación total
L(Leucina)- K(lisina) F(fenilalanina) Y(Tirosina) I(isoleucina) W(triptófano) T(treonina)
 L(Leucina)- K(lisina) F(fenilalanina) Y(Tirosina) I(isoleucina) W(triptófano) T(treonina) Para que el ciclo de krebs pueda iniciar es necesario que exista Acetil CoA, la formación de acetil
L(Leucina)- K(lisina) F(fenilalanina) Y(Tirosina) I(isoleucina) W(triptófano) T(treonina) Para que el ciclo de krebs pueda iniciar es necesario que exista Acetil CoA, la formación de acetil
En las células aerobias distintas vías catabólicas convergen en el ciclo de Krebs
 CICLO DE KREBS Material elaborado por: J. Monza, S. Doldán y S. Signorelli. En las células aerobias distintas vías catabólicas convergen en el ciclo de Krebs El ciclo de Krebs (de los ácidos tricarboxílicos
CICLO DE KREBS Material elaborado por: J. Monza, S. Doldán y S. Signorelli. En las células aerobias distintas vías catabólicas convergen en el ciclo de Krebs El ciclo de Krebs (de los ácidos tricarboxílicos
Los seres vivos y las células que los forman son sistemas abiertos, en equilibrio y que realizan un trabajo.
 Los seres vivos y las células que los forman son sistemas abiertos, en equilibrio y que realizan un trabajo. Sistema abierto Intercambio de materia y energía Equilibrio. Sus variables se mantienen dentro
Los seres vivos y las células que los forman son sistemas abiertos, en equilibrio y que realizan un trabajo. Sistema abierto Intercambio de materia y energía Equilibrio. Sus variables se mantienen dentro
Los mecanismos de las reacciones de la glucólisis son, en general, sustituciones nucleofílicas. Veamos algunos ejemplos:
 METABLISM DE AZÚAES III. Mecanismos de reacción Los mecanismos de las reacciones de la glucólisis son, en general, sustituciones nucleofílicas. Veamos algunos ejemplos:. Transferencia de grupo fosforilo
METABLISM DE AZÚAES III. Mecanismos de reacción Los mecanismos de las reacciones de la glucólisis son, en general, sustituciones nucleofílicas. Veamos algunos ejemplos:. Transferencia de grupo fosforilo
Catabolismo de la glucosa: respiración celular
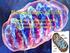 El Catabolismo 1 Catabolismo Obje/vo: obtención de energía (y almacenamiento en forma de ATP) Fuentes principales de E: glúcidos y lípidos Energía ATP para llevar a cabo ac/vidad celular o para sinte/zar
El Catabolismo 1 Catabolismo Obje/vo: obtención de energía (y almacenamiento en forma de ATP) Fuentes principales de E: glúcidos y lípidos Energía ATP para llevar a cabo ac/vidad celular o para sinte/zar
Metabolismo. Forma de obtención de carbono. Corresponde a la actividad. participan sistemas multienzimáticos (rutas metabólicas) RUTAS METABÓLICAS
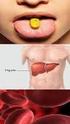 Facultad de Ciencias de la Salud BIO160 Bioquímica i General Metabolismo METABOLISMO Corresponde a la actividad coordinada que ocurre dentro de una célula, en la cual participan sistemas multienzimáticos
Facultad de Ciencias de la Salud BIO160 Bioquímica i General Metabolismo METABOLISMO Corresponde a la actividad coordinada que ocurre dentro de una célula, en la cual participan sistemas multienzimáticos
TEMA 1: CÉLULA. ACTIVIDAD ORIENTADORA 13. TÍTULO: METABOLISMO Y RESPIRACIÓN CELULAR
 TEMA 1: CÉLULA. ACTIVIDAD ORIENTADORA 13. TÍTULO: COMPONENTES MOLECULARES METABOLISMO Y RESPIRACIÓN CELULAR Autor: Dr. Daniel Sánchez Serrano Parte II TRANSPORTADORES DE LA CADENA DE HIDRÓGENO Coenzima
TEMA 1: CÉLULA. ACTIVIDAD ORIENTADORA 13. TÍTULO: COMPONENTES MOLECULARES METABOLISMO Y RESPIRACIÓN CELULAR Autor: Dr. Daniel Sánchez Serrano Parte II TRANSPORTADORES DE LA CADENA DE HIDRÓGENO Coenzima
GLUCOSA: EXCELENTE COMBUSTIBLE Y PRECURSOR VERSÁTIL
 GLICÓLISIS GLUCOSA: EXCELENTE COMBUSTIBLE Y PRECURSOR VERSÁTIL GLICÓLISIS (GLYCOS = AZÚCAR + LÍSIS = RUPTURA) FASE PREPARATORIA O FASE DE GASTO DE ENERGÍA (ATP) Inversión de ATP aumenta el contenido de
GLICÓLISIS GLUCOSA: EXCELENTE COMBUSTIBLE Y PRECURSOR VERSÁTIL GLICÓLISIS (GLYCOS = AZÚCAR + LÍSIS = RUPTURA) FASE PREPARATORIA O FASE DE GASTO DE ENERGÍA (ATP) Inversión de ATP aumenta el contenido de
CADENA RESPIRATORIA O CADENA DE TRANSPORTE DE ELECTRONES
 CADENA RESPIRATORIA O CADENA DE TRANSPORTE DE ELECTRONES El NADH y FADH2 obtenidos contienen un par de electrones que se transfieren al O2 con liberación de energía. La cadena respiratoria transporta los
CADENA RESPIRATORIA O CADENA DE TRANSPORTE DE ELECTRONES El NADH y FADH2 obtenidos contienen un par de electrones que se transfieren al O2 con liberación de energía. La cadena respiratoria transporta los
ENZIMAS. Catalizadores biológicos. Acción de otras células vivas (sin conexión con ellas)
 Enzimas (proteínas conjugadas) ENZIMAS Catalizadores biológicos Solubles en agua Interior de la célula Acción de otras células vivas (sin conexión con ellas) Intracelulares o constitutivas (acción en el
Enzimas (proteínas conjugadas) ENZIMAS Catalizadores biológicos Solubles en agua Interior de la célula Acción de otras células vivas (sin conexión con ellas) Intracelulares o constitutivas (acción en el
OXIDACIÓN DE LA GLUCOSA GLUCÓLISIS DECARBOXILACIÓN OXIDATIVA CICLO DE KREBS CADENA TRANSPORTADORA DE ELECTRONES
 OXIDACIÓN DE LA GLUCOSA GLUCÓLISIS DECARBOXILACIÓN OXIDATIVA CICLO DE KREBS CADENA TRANSPORTADORA DE ELECTRONES Reacciones de oxido-reducción Energía celular El ATP es el principal transportador de energía
OXIDACIÓN DE LA GLUCOSA GLUCÓLISIS DECARBOXILACIÓN OXIDATIVA CICLO DE KREBS CADENA TRANSPORTADORA DE ELECTRONES Reacciones de oxido-reducción Energía celular El ATP es el principal transportador de energía
La fosforilación oxidativa
 La fosforilación oxidativa arriba ) Bioenergética del transporte de electrones Transportadores de electrones en la mitocondria 4. Hierro. La reacción redox es la siguiente: Fe 2+ Fe 3+ + e - El átomo
La fosforilación oxidativa arriba ) Bioenergética del transporte de electrones Transportadores de electrones en la mitocondria 4. Hierro. La reacción redox es la siguiente: Fe 2+ Fe 3+ + e - El átomo
BIOQUÍMICA-1º de Medicina Dpto. Biología Molecular Jesús Navas ENZIMAS
 Tema 6. ENZIMAS. Clasificación. Principios de la catálisis enzimática. Energía de activación. Velocidad de reacción y equilibrio de reacción. Cinética enzimática: ecuación de Michaelis- Menten. Ecuación
Tema 6. ENZIMAS. Clasificación. Principios de la catálisis enzimática. Energía de activación. Velocidad de reacción y equilibrio de reacción. Cinética enzimática: ecuación de Michaelis- Menten. Ecuación
BIOSINTESIS DE AMINOÁCIDOS INTEGRANTES: ZACHARY FERNANDA CUELLAR CARDOZO PAOLA ANDREA CASTAÑO PAYA
 BIOSINTESIS DE AMINOÁCIDOS INTEGRANTES: ZACHARY FERNANDA CUELLAR CARDOZO PAOLA ANDREA CASTAÑO PAYA Aminoácidos Es una molécula orgánica con un grupo amino (-NH 2 ) y un grupo carboxilo (- COOH). Los aminoácidos
BIOSINTESIS DE AMINOÁCIDOS INTEGRANTES: ZACHARY FERNANDA CUELLAR CARDOZO PAOLA ANDREA CASTAÑO PAYA Aminoácidos Es una molécula orgánica con un grupo amino (-NH 2 ) y un grupo carboxilo (- COOH). Los aminoácidos
Click para ir al sitio web:
 Slide 1 / 63 New Jersey Center for Teaching and Learning Iniciativa de Ciencia Progresiva Este material está disponible gratuitamente en www.njctl.org y está pensado para el uso no comercial de estudiantes
Slide 1 / 63 New Jersey Center for Teaching and Learning Iniciativa de Ciencia Progresiva Este material está disponible gratuitamente en www.njctl.org y está pensado para el uso no comercial de estudiantes
III. Inhibición enzimática
 III. Inhibición enzimática Inhibidor: Efector que hace disminuir la actividad enzimática, a través de interacciones con el centro activo u otros centros específicos. Inhibidores Inhibidores Reversibles:
III. Inhibición enzimática Inhibidor: Efector que hace disminuir la actividad enzimática, a través de interacciones con el centro activo u otros centros específicos. Inhibidores Inhibidores Reversibles:
Metabolismo del C O L E S T E R O L
 UNIVERSIDAD DE SAN CARLOS DE GUATEMALA FACULTAD DE CIENCIAS MÉDICAS FASE I, BIOQUÍMICA MÉDICA 2º AÑO CICLO ACADÉMICO 2,011 Metabolismo del C O L E S T E R O L Dr. Mynor A. Leiva Enríquez Los lípidos que
UNIVERSIDAD DE SAN CARLOS DE GUATEMALA FACULTAD DE CIENCIAS MÉDICAS FASE I, BIOQUÍMICA MÉDICA 2º AÑO CICLO ACADÉMICO 2,011 Metabolismo del C O L E S T E R O L Dr. Mynor A. Leiva Enríquez Los lípidos que
VÍA DE PENTOSA FOSFATO
 UNIVERSIDAD DE SAN CARLOS DE GUATEMALA FACULTAD DE CIENCIAS MÉDICAS FASE I, UNIDAD DIDÁCTICA: BIOQUÍMICA MÉDICA 2º AÑO CICLO ACADÉMICO 2,013 VÍA DE PENTOSA FOSFATO DR. MYNOR A. LEIVA ENRÍQUEZ Fuente: Bioquímica,
UNIVERSIDAD DE SAN CARLOS DE GUATEMALA FACULTAD DE CIENCIAS MÉDICAS FASE I, UNIDAD DIDÁCTICA: BIOQUÍMICA MÉDICA 2º AÑO CICLO ACADÉMICO 2,013 VÍA DE PENTOSA FOSFATO DR. MYNOR A. LEIVA ENRÍQUEZ Fuente: Bioquímica,
Con relación a las enzimas que actúan en nuestro organismo, es correcto afirmar que
 Programa Estándar Anual Guía práctica Enzimas y metabolismo celular Biología Nº 1. 2. Ciencias Básicas Ejercicios PSU Cuál(es) de las siguientes reacciones químicas es (son) anabólica(s)? I) II) III) Replicación
Programa Estándar Anual Guía práctica Enzimas y metabolismo celular Biología Nº 1. 2. Ciencias Básicas Ejercicios PSU Cuál(es) de las siguientes reacciones químicas es (son) anabólica(s)? I) II) III) Replicación
RESPIRACIÓN AEROBIA Y ANAEROBIA
 RESPIRACIÓN AEROBIA Y ANAEROBIA Las células llevan a cabo diversos procesos para mantener su funcionamiento normal, muchos de los cuales requieren energía. La respiración celular es una serie de reacciones
RESPIRACIÓN AEROBIA Y ANAEROBIA Las células llevan a cabo diversos procesos para mantener su funcionamiento normal, muchos de los cuales requieren energía. La respiración celular es una serie de reacciones
Conversión del glucoso 6 fosfato en otras hexosas
 BIOSINTESIS DE LOS CARBOHIDRATOS TABLA DE CONTENIDO Introducción Justificación Objetivos Síntesis del glucoso fosfato a partir del ácido pirúvico Regulación de la ruta que va desde el piruvato al glucoso
BIOSINTESIS DE LOS CARBOHIDRATOS TABLA DE CONTENIDO Introducción Justificación Objetivos Síntesis del glucoso fosfato a partir del ácido pirúvico Regulación de la ruta que va desde el piruvato al glucoso
El catabolismo es la fase degradativa del metabolismo. El catabolismo es semejante en organismos autótrofos y heterótrofos.
 PROCESOS CATABÓLICOS El catabolismo es la fase degradativa del metabolismo El catabolismo es semejante en organismos autótrofos y heterótrofos. Son reacciones de oxidación y reducción acopladas En estas
PROCESOS CATABÓLICOS El catabolismo es la fase degradativa del metabolismo El catabolismo es semejante en organismos autótrofos y heterótrofos. Son reacciones de oxidación y reducción acopladas En estas
UNIDADES METABOLISMO
 UNIDADES 16-18 METABOLISMO DEFINICIÓN - CONJUNTO DE REACCIONES DE DEGRADACIÓN DE MOLÉCULAS ORGÁNICAS COMPLEJAS. - OCURRE EN TODOS LOS ORGANISMOS. - TIENE COMO FINALIDAD LA OBTENCIÓN DE ENERGÍA, PODER REDUCTOR
UNIDADES 16-18 METABOLISMO DEFINICIÓN - CONJUNTO DE REACCIONES DE DEGRADACIÓN DE MOLÉCULAS ORGÁNICAS COMPLEJAS. - OCURRE EN TODOS LOS ORGANISMOS. - TIENE COMO FINALIDAD LA OBTENCIÓN DE ENERGÍA, PODER REDUCTOR
METABOLISMO CELULAR. Es el conjunto de reacciones químicas a través de las cuales el organismo intercambia materia y energía con el medio
 METABOLISMO CELULAR Es el conjunto de reacciones químicas a través de las cuales el organismo intercambia materia y energía con el medio Reacciones Celulares Básicas. Los sistemas vivos convierten la energía
METABOLISMO CELULAR Es el conjunto de reacciones químicas a través de las cuales el organismo intercambia materia y energía con el medio Reacciones Celulares Básicas. Los sistemas vivos convierten la energía
Las moléculas de los seres vivos Control de la actividad celular Fuente de energía para las células:
 Las moléculas de los seres vivos Control de la actividad celular Fuente de energía para las células: 1. ATP 2. La respiración celular 3. La fermentación Proceso de fotosíntesis La fuente principal de energía
Las moléculas de los seres vivos Control de la actividad celular Fuente de energía para las células: 1. ATP 2. La respiración celular 3. La fermentación Proceso de fotosíntesis La fuente principal de energía
6. Enzimas - Actividades
 I.E.S. Flavio Irnitano El Saucejo (Sevilla) Curso 2.015 2.016 Departamento de Biología y Geología NIVEL: 2º Bachillerato MATERIA: BIOLOGÍA 6.1. Concepto y estructura. BLOQUE I. CUÁL ES LA COMPOSICIÓN DE
I.E.S. Flavio Irnitano El Saucejo (Sevilla) Curso 2.015 2.016 Departamento de Biología y Geología NIVEL: 2º Bachillerato MATERIA: BIOLOGÍA 6.1. Concepto y estructura. BLOQUE I. CUÁL ES LA COMPOSICIÓN DE
CARACTERIZACIÓN CINÉTICA DE LA ENZIMA FOSFATASA ÁCIDA DEL EXTRACTO CRUDO DE PAPA
 FACULTAD CIENCIAS SILVOAGROPECUARIAS LABORATORIO ASIGNATURA DE BIOQUÍMICA. PLAN COMÚN AGRONOMÍA E INGENIERÍA FORESTAL TRABAJO PRÁCTICO Nº3 CARACTERIZACIÓN CINÉTICA DE LA ENZIMA FOSFATASA ÁCIDA DEL EXTRACTO
FACULTAD CIENCIAS SILVOAGROPECUARIAS LABORATORIO ASIGNATURA DE BIOQUÍMICA. PLAN COMÚN AGRONOMÍA E INGENIERÍA FORESTAL TRABAJO PRÁCTICO Nº3 CARACTERIZACIÓN CINÉTICA DE LA ENZIMA FOSFATASA ÁCIDA DEL EXTRACTO
CATABOLISMO ESQUEMA METABOLISMO
 ESQUEMA METABOLISMO 1.- ENERGÉTICA CELULAR 1.1 Concepto de reacción espontánea y no espontánea Energía libre Reacciones espontáneas exoergónicas Reacciones no espontáneas endoergónicas Sistemas en equilibrio
ESQUEMA METABOLISMO 1.- ENERGÉTICA CELULAR 1.1 Concepto de reacción espontánea y no espontánea Energía libre Reacciones espontáneas exoergónicas Reacciones no espontáneas endoergónicas Sistemas en equilibrio
CONVERGENCIA METABÓLICA. En el catabolismo aerobio existen tres fases principales:
 CONVERGENCIA METABÓLICA Rutas catabólicas En el catabolismo aerobio existen tres fases principales: - Fase I.- Transformación de Macromoléculas en sus Monómeros correspondientes. 1) Polisacáridos Monosacáridos
CONVERGENCIA METABÓLICA Rutas catabólicas En el catabolismo aerobio existen tres fases principales: - Fase I.- Transformación de Macromoléculas en sus Monómeros correspondientes. 1) Polisacáridos Monosacáridos
Proteínas y Ácidos Nucleicos
 Proteínas y Ácidos Nucleicos Mapa conceptual Biomoléculas. Biomoléculas inorgánicas: Moléculas que no presentan carbono en su estructura. Biomoléculas orgánicas: Moléculas que presentan carbono en su estructura.
Proteínas y Ácidos Nucleicos Mapa conceptual Biomoléculas. Biomoléculas inorgánicas: Moléculas que no presentan carbono en su estructura. Biomoléculas orgánicas: Moléculas que presentan carbono en su estructura.
Flujo de energía. Light energy ECOSYSTEM. Photosynthesis in chloroplasts. Organic molecules + O 2 CO 2 + H 2 O. Cellular respiration in mitochondria
 Flujo de energía ECOSYSTEM Light energy CO 2 + H 2 O Photosynthesis in chloroplasts Cellular respiration in mitochondria Organic molecules + O 2 ATP powers most cellular work Heat energy ATP Rutas catabólicas
Flujo de energía ECOSYSTEM Light energy CO 2 + H 2 O Photosynthesis in chloroplasts Cellular respiration in mitochondria Organic molecules + O 2 ATP powers most cellular work Heat energy ATP Rutas catabólicas
Tema 1. Introducción
 Tema 1. Introducción - Bioquímica: concepto, y objetivos - Importancia de la Bioquímica en la Lic. De Farmacia - Composición química del cuerpo humano: Bioelementos Bioelementos primarios o principales
Tema 1. Introducción - Bioquímica: concepto, y objetivos - Importancia de la Bioquímica en la Lic. De Farmacia - Composición química del cuerpo humano: Bioelementos Bioelementos primarios o principales
METABOLISMO DEL NITRÓGENO
 METABLISM DEL NITRÓGEN Descomposición por microorganismos Compuesto rgánicos Nitrogenados ANIMALES Desechos orgánicos Amonificación CICL DEL NITRÓGEN N 3 Nitrificación Nitrosomonas Nitrosación N 2 Nitratación
METABLISM DEL NITRÓGEN Descomposición por microorganismos Compuesto rgánicos Nitrogenados ANIMALES Desechos orgánicos Amonificación CICL DEL NITRÓGEN N 3 Nitrificación Nitrosomonas Nitrosación N 2 Nitratación
ENZIMAS. Las enzimas son catalizadores específicos: cada enzima cataliza un solo tipo de reacción y, casi siempre, utiliza un único sustrato.
 ENZIMAS Las enzimas son proteínas que catalizan las reacciones químicas en los seres vivos. Catalizadores son sustancias que, sin consumirse en una reacción, aumentan su velocidad (Figura 1). Las enzimas
ENZIMAS Las enzimas son proteínas que catalizan las reacciones químicas en los seres vivos. Catalizadores son sustancias que, sin consumirse en una reacción, aumentan su velocidad (Figura 1). Las enzimas
Respiracion Celular Prof. Nerybelle Perez-Rosas 2011
 Respiracion Celular Prof. Nerybelle Perez-Rosas 2011 2 Respiracion Celular Podemos clasificar organismos basandonos en la forma en que obtienen energia. autotrofos: son capaces de producir sus propias
Respiracion Celular Prof. Nerybelle Perez-Rosas 2011 2 Respiracion Celular Podemos clasificar organismos basandonos en la forma en que obtienen energia. autotrofos: son capaces de producir sus propias
PLANIFICACIÓN DE ASIGNATURA
 PLANIFICACIÓN DE ASIGNATURA I IDENTIFICACION GENERAL DE LA ASIGNATURA CARRERA BIOQUÍMICA DEPARTAMENTO BiOLOGIA ASIGNATURA BIOQUIMICA I CÓDIGO PRERREQUISITOS Fisicoquímica II y Química Orgánica II CREDITOS
PLANIFICACIÓN DE ASIGNATURA I IDENTIFICACION GENERAL DE LA ASIGNATURA CARRERA BIOQUÍMICA DEPARTAMENTO BiOLOGIA ASIGNATURA BIOQUIMICA I CÓDIGO PRERREQUISITOS Fisicoquímica II y Química Orgánica II CREDITOS
Cloroplastos y Fotosíntesis
 Cloroplastos y Fotosíntesis Víctor Hugo Casco 2012 Labor Improbus Omnia Vincit (El Trabajo Tenaz Todo lo Puede) Funciones Los plástidos son los sitios donde se produce la fotosíntesis, allí se depositan
Cloroplastos y Fotosíntesis Víctor Hugo Casco 2012 Labor Improbus Omnia Vincit (El Trabajo Tenaz Todo lo Puede) Funciones Los plástidos son los sitios donde se produce la fotosíntesis, allí se depositan
Glucolisis y gluconeogénesis. Algunos aspectos puntuales Dr. Alfredo Rigalli
 Glucolisis y gluconeogénesis. Algunos aspectos puntuales Dr. Alfredo Rigalli Tabla de contenidos 1.Aspectos generales de glucólisis...1 2.Algunos aspectos particulares de la glucólisis...4 2.1.Glucokinase
Glucolisis y gluconeogénesis. Algunos aspectos puntuales Dr. Alfredo Rigalli Tabla de contenidos 1.Aspectos generales de glucólisis...1 2.Algunos aspectos particulares de la glucólisis...4 2.1.Glucokinase
TEMA 19. Ciclo del ácido cítrico (ciclo de los ácidos tricarboxílicos o de Krebs)
 . Ciclo del ácido cítrico (ciclo de los ácidos tricarboxílicos o de Krebs) Importancia del ciclo de Krebs como encrucijada metabólica. Formación del acetil-coenzima-a: el complejo piruvato deshidrogenasa.
. Ciclo del ácido cítrico (ciclo de los ácidos tricarboxílicos o de Krebs) Importancia del ciclo de Krebs como encrucijada metabólica. Formación del acetil-coenzima-a: el complejo piruvato deshidrogenasa.
MORFOFISIOLOGÍA HUMANA I. PRIMER SEMESTRE. PRIMER AÑO.
 MORFOFISIOLOGÍA HUMANA I. PRIMER SEMESTRE. PRIMER AÑO. TEMA 1: CÉLULA. ACTIVIDAD ORIENTADORA 13. TÍTULO: COMPONENTES MOLECULARES METABOLISMO Y RESPIRACIÓN CELULAR. SUMARIO 1. Transporte de electrones.
MORFOFISIOLOGÍA HUMANA I. PRIMER SEMESTRE. PRIMER AÑO. TEMA 1: CÉLULA. ACTIVIDAD ORIENTADORA 13. TÍTULO: COMPONENTES MOLECULARES METABOLISMO Y RESPIRACIÓN CELULAR. SUMARIO 1. Transporte de electrones.
Biología 2º Bachiller. Tema 13: Respiración y fotosíntesis
 Biología 2º Bachiller Tema 13: Respiración y fotosíntesis Qué vamos a ver en este tema?: Respiración aerobia: Oxidación de moléculas orgánicas para la obtención de energía Catabolismo de glúcidos: Oxidación
Biología 2º Bachiller Tema 13: Respiración y fotosíntesis Qué vamos a ver en este tema?: Respiración aerobia: Oxidación de moléculas orgánicas para la obtención de energía Catabolismo de glúcidos: Oxidación
