CENTRO DE INVESTIGACIÓN EN SANIDAD ANIMAL (CISA INIA)
|
|
|
- Emilia Moya Paz
- hace 6 años
- Vistas:
Transcripción
1 PROCEDIMIENTO PARA LA DETECCIÓN DEL VIRUS DE LA PESTE PORCINA AFRICANA (VPPA) MEDIANTE REACCIÓN EN CADENA DE LA Fecha de entrada en vigor: Diciembre 2008 REV. FECHA EPÍGRAFE/S CAUSA DEL CAMBIO Realizado Revisado Aprobado Fdo.: Jovita Fernández Pinero Responsable laboratorio diagnóstico molecular Fecha: Fdo.: Carmina Gallardo Responsable técnico del Laboratorio Nacional y Comunitario de PPA Fecha: Fdo.: Marisa Arias Neira Fecha: Directora Técnica del CISA PNT/CISA/PPA/PCR/1//2008
2 Hoja 2 de 10 ÍNDICE 1. OBJETO 2. ALCANCE 3. REFERENCIAS 3.1. DOCUMENTOS UTILIZADOS EN LA ELABORACIÓN 3.2. DOCUMENTOS A UTILIZAR CONJUNTAMENTE 4. GENERAL 5. DESCRIPCIÓN 5.1. EQUIPOS Y MATERIALES 5.2. PREPARACIÓN 5.3. REALIZACIÓN 5.4. TRATAMIENTO DE RESULTADOS 5.5. PUNTOS CRÍTICOS 5.6. MEDIDAS DE SEGURIDAD 5.7. CONTROL DE CALIDAD 6. ANEXOS
3 Hoja 3 de OBJETO El presente procedimiento tiene por objeto describir el método a seguir para la detección específica del ADN del virus de la Peste Porcina Africana (VPPA) en material clínico mediante la técnica de la reacción en cadena de la polimerasa (PCR) convencional. 2. ALCANCE Este procedimiento es de aplicación a cualquier tipo de muestra clínica de origen porcino (EDTA-sangre, suero, homogeneizados de tejido) y a sobrenadantes de cultivos celulares. Es particularmente útil para la detección del ADN de VPPA en muestras de tejido porcino en mal estado de conservación que no son adecuadas para técnicas de aislamiento viral o detección de antígeno, o cuando el virus ha podido ser inactivado antes de la llegada de las muestras al laboratorio. La técnica de la PCR es altamente sensible, siendo su límite de detección inferior a una partícula viral infectiva. 3. REFERENCIAS 3.1. DOCUMENTOS UTILIZADOS EN LA ELABORACIÓN Como referencia básica para la elaboración de este procedimiento se han tomado los criterios establecidos en los siguientes documentos: 1. Manual of Diagnostic Tests and Vaccines for Terrestrial Animals (mammals, birds and bees). Capítulo OIE, sexta edición, [ 2. Ensayos de comparación interlaboratorial organizados por el Laboratorio Comunitario de Referencia. 3. PG/LCV/001 Procedimiento para la elaboración de documentos, Edición M. Agüero, J. Fernández, L. Romero, C. Sánchez, M. Arias, J.M. Sánchez-Vizcaíno Highly Sensitive PCR Assay for Routine Diagnosis of African Swine Fever Virus in Clinical Samples. J. Clin. Microbiol., vol. 41, no. 9, p GENERAL La técnica de la reacción en cadena de la polimerasa (PCR) permite la detección específica del ADN del VPPA mediante la amplificación enzimática de un pequeño fragmento del genoma viral delimitado por una pareja de primers o cebadores específicos. La técnica de PCR requiere de la extracción previa del ADN del VPPA desde el material de origen a analizar, que será el molde de la reacción enzimática. Finalmente, el producto amplificado será detectado mediante electroforesis en geles de agarosa, tinción con bromuro de etidio (intercalante de ADN de doble cadena) y posterior visualización por irradiación con luz UV.
4 Hoja 4 de 10 La PCR es una técnica rápida, que puede completarse en pocas horas, y de elevada sensibilidad, pudiendo detectar la presencia de virus incluso antes de la aparición de los primeros signos clínicos en los animales infectados. El método descrito de PCR convencional para VPPA emplea una pareja de primers diseñada en una región altamente conservada del genoma viral, VP72, que asegura la detección de un amplio rango de aislados de VPPA. Los primers amplifican un fragmento de ADN de 257 pares de bases (pb), entre las posiciones de nucleótidos y de la cepa de referencia BA71V (nº de acceso a GenBank ASU18466). 5. DESCRIPCIÓN 5.1. EQUIPOS Y MATERIALES MATERIALES NECESARIOS Balanza electrónica Cámara fotográfica o videocámara con impresora Congelador de -20 Congelador -70 Cubeta para geles de agarosa horizontales y accesorios (bandejas, peines, conectores) Fuente de alimentación Gradillas Micropipetas automática monocanal de 1-10μl. Micropipetas automática monocanal de μl. Micropipetas automática monocanal de μl. Micropipetas automática monocanal de μl. Microcentrífuga de mesa Nevera de 4ºC Reloj cronómetro Termobloque Termociclador convencional Transiluminador de luz ultravioleta Vortex Material desechable: Guantes de nitrilo o látex Puntas de micropipeta de rangos y μl, estériles Puntas de micropipeta con filtros resistentes a aerosoles de rangos 1-20, y μl, estériles Tubos tipo eppendorf estériles, aptos para microcentrífuga, de volúmenes 0.2, 0.5, 1.5 y 2 ml REACTIVOS Reactivos para el paso de extracción de ADN: High Pure PCR Template Preparation Kit (Roche Diagnostics, ref. no ) Isopropanol absoluto Etanol absoluto H 2 O estéril, grado PCR.
5 Hoja 5 de 10 Tampón fosfato salino (PBS) ph 7,2 estéril ClNa [Merck ] ,0 g ClK [Merck ] ,2 g P0 4 H 2 K [Merck ] ,2 g P0 4 HNa 2 [Merck ] ,15 g H 2 0 destilada ml Conservación; temperatura ambiente Reactivos para el paso de amplificación de ADN: H 2 O estéril libre de nucleasas, grado PCR. Taq Gold DNA polimerasa, 10x PCR Buffer II y Cl 2 Mg de Applied Biosystems (Ref. N ). Deoxinucleótidos trifosfato (dntp) mix, conteniendo 10 mm de cada dntp, de Roche Diagnostics (Ref ). Primers a una concentración de uso de 20 pmol/µl: - secuencia primer PPA-1 5 -AGTTATGGGAAACCCGACCC-3 (primer forward); - secuencia primer PPA CCCTGAATCGGAGCATCCT-3 (primer reverse). Reactivos para el paso de detección del ADN amplificado: Agarosa MP 100 (Roche, Ref ). 10x tampón de carga: 0.2% xilencianol, 0.2% azul de bromofenol, 30% glicerol. Tampón de electroforesis TAE (50 ): Tris base (242 g); ácido acético glacial (57.1 ml); 0.5 M EDTA, ph 8.0 (100 ml); agua destilada (hasta 1 litro). Está disponible comercialmente en Applichem (Ref. A1691,1000) Bromuro de etidio, en solución con gotero (Amresco, Ref. E406-5ML) Marcador de peso molecular VI DNA (Roche Diagnostics, ref. no ) PREPARACIÓN Mediante la técnica de PCR descrita se pueden analizar distintos tipos de muestra como sobrenadantes de cultivo celular, sangre recogida en EDTA, suero y homogeneizados de tejidos, incluso cuando éstos últimos han sido conservados en condiciones no adecuadas y están putrefactos. Preparación de muestras: - Se recomienda en el caso de muestras de sangre-edta, analizar siempre las muestras sin diluir. - Para el análisis de muestras de órganos y tejidos, se debe preparar primero un homogeneizado del mismo en PBS estéril al 1/10. Posteriormente, centrifugar para clarificar a 12,000 g durante 5 minutos. Emplear para el análisis el fluido sobrenadante recuperado. Si éste no es muy claro, puede ser recomendable procesar una dilución 1/10 del sobrenadante en paralelo con el material no diluido REALIZACIÓN Método de extracción del ADN El método de extracción del ADN de VPPA que se describe emplea el kit comercial High Pure PCR Template Preparation Kit (Roche Diagnostics). Este sistema tiene la ventaja de poder ser utilizado para la extracción simultánea del ADN de VPPA y del ARN del virus de la Peste Porcina Clásica (VPPC), que va a facilitar la detección simultánea de ambos virus en una única reacción si se emplea un método de PCR múltiple (Agüero et al., 2004). Controles positivos y negativos de extracción: Se deben incluir al menos un control positivo y un control negativo en cada proceso de extracción. Las muestras controles serán homogeneizados de tejido 1/10, muestras de suero o sangre EDTA,
6 Hoja 6 de 10 correspondiendo al mismo tipo de material clínico que las muestras a analizar. El control negativo serán 200 µl de agua o material clínico negativo a VPPA; el control positivo serán 200 µl de homogeneizado, suero o sangre-edta positivo a VPPA. Es muy recomendable que el control positivo esté próximo al límite de detección de la técnica, que servirá para validar el rendimiento del método de extracción del ADN. Ambos controles serán incluidos en todo el procedimiento y procesados conjuntamente con las muestras a analizar. Protocolo de extracción de ADN con el High Pure PCR Template Preparation Kit: El High Pure PCR Template Preparation Kit incluye los siguientes reactivos: Binding Buffer, Proteinasa K, Inhibitor Removal Buffer, Wash Buffer, y los tubos con filtro de sílica y tubos colectores, necesarios para el proceso de extracción de ADN. Durante el proceso de extracción, las células son inicialmente lisadas durante una corta incubación con proteinasa K en presencia de una sal caotrópica (HCl guanidina), que inmediatamente inactiva todas las nucleasas. Los ácidos nucleicos se unen o adsorben selectivamente al filtro de fibra de vidrio (sílica) en un tubo de centrífuga especial. Los ácidos nucleicos permanecen unidos al filtro durante los siguientes pasos de lavado y centrifugado, donde se eliminan las moléculas celulares contaminantes, sales y proteínas. Finalmente, los ácidos nucleicos son eluidos del filtro añadiendo H 2 O estéril, grado PCR. Preparación de soluciones de trabajo: - Proteinasa K liofilizada: resuspender la proteinasa K en 4,5 ml de agua destilada estéril. Alicuotar en viales de 500 µl y mantener a -20ºC hasta su uso. - Inhibitor Removal Buffer: añadir 20 ml de etanol absoluto al vial original. Etiquetar y marcar la fecha en la botella. - Wash Buffer: añadir 80 ml de etanol absoluto al vial original. Etiquetar y marcar la fecha en la botella. Protocolo de extracción de ADN de VPPA: 1. Poner 200 μl/tubo de binding buffer. 2. Añadir 40 μl de Proteinasa K 20 mg/ml. 3. Añadir 200 μl de muestra. 4. Mezclar invirtiendo los tubos e incubar 10 min a 72ºC. Centrifugar unos segundos, un pulso de centrífuga, para eliminar restos de muestra en la tapa. 5. Añadir 100 μl de isopropanol. 6. Mezclar agitando en vortex. Centrifugar unos segundos, un pulso de centrífuga, para eliminar restos de muestra en la tapa. 7. Pasar la mezcla al High pure filter tube colocado sobre un tubo colector. Centrifugar 1 min a rpm (Con muestras de sangre, repetir el paso de centrifugación si queda muestra sobre el filtro). 8. Descartar el tubo colector y colocar el tubo columna sobre un nuevo tubo colector 9. Añadir 500 μl Inhibitor Removal buffer. Centrifugar 1 min a rpm 10. Descartar el tubo colector y colocar el tubo columna sobre un nuevo tubo colector. 11. Añadir 450 μl de Wash buffer. Centrifugar 1 min a rpm. 12. Descartar el tubo colector y colocar el tubo columna sobre un nuevo tubo colector. 13. Repetir el paso de lavado. 14. Centrifugar sobre un tubo vacío a rpm 10 seg. 15. Colocar la columna sobre un tubo de 1,5 ml con tapa. 16. Añadir 50 μl de agua destilada estéril, precalentada a 70ºC, asegurando que cubre totalmente el filtro (no emplear el buffer de elución incluido en el kit si se quiere extraer también ARN de VPPC). Centrifugar 1 min a rpm. 17. Recoger el eluido conteniendo el ADN y guardar a 20ºC hasta su uso (o a 4ºC si se va a emplear en 1-2 h desde su obtención).
7 Hoja 7 de Reacción de amplificación del ADN: Aspectos generales: - El ensayo amplifica un fragmento de ADN de 257pb dentro de la región VP72 del genoma de VPPA. - La PCR se realiza en un volumen final de 25 µl. - Tras la preparación de la mezcla de reacción, se añadirán 2 µl de ADN extraído a cada tubo de reacción. - Se deben incluir, en cada carrera de PCR, al menos un control positivo (2 µl de ADN de VPPA, a una dilución próxima al límite de detección de la técnica) y un control negativo de reacción (2 µl de agua destilada, grado PCR). Preparación de la mezcla de reacción: - En un tubo de microcentrífuga de 1.5 ml estéril, se preparará la mezcla de PCR, según se describe a continuación, para el número total de muestras a analizar (incluyendo los controles positivos y negativos de extracción y reacción) más, al menos, una muestra adicional (para compensar posibles errores de pipeteo). - Mezcla de PCR para una muestra: H 2 O estéril libre de nucleasas, grado PCR (17,375 µl), 10 PCR Buffer II (2,5 µl), cloruro de magnesio 25 mm (2 µl), dntp mix 10mM (0,5 µl), primer PPA-1 20 pmol/µl (0,25 µl), primer PPA-2 20 pmol/µl (0,25 µl), Taq Gold DNA polimerasa 5 U/µl (0,125 µl). - Añadir 23 µl de mezcla de PCR al número de tubos de PCR de 0,2 ml necesarios. Adición de la muestra: - Añadir 2 µl de ADN molde a cada tubo de PCR. - Incluir un control positivo (2 µl de ADN de VPPA, próximo al límite de detección de la técnica) y un control negativo de reacción (2 µl de agua destilada, grado PCR) en cada carrera de PCR. - Después de añadir la muestra, cerrar bien los tubos y dar un golpe de centrífuga para bajar la mezcla de PCR. Colocar los tubos en un termociclador automatizado provisto de tapa térmica y correr el programa de incubación detallado a continuación. Programa de incubación: Activación de TaqGold DNA po 95ºC min Desnaturalización ADN 95ºC seg Anillamiento primers 62ºC seg 40 ciclos Elongación 72ºC seg Paso extra de elongación 72ºC min Mantenimiento a 4 C Conservar los productos amplificados a 4ºC hasta proceder con la electroforesis Electroforesis en gel de agarosa: 1. En un matraz de 200 ml se pesan 2 gramos de agarosa. 2. Añadir 100 ml de tampón TAE 1X. 3. Calentar en el microondas hasta que la agarosa esté bien disuelta. 4. Añadir bromuro de etidio (BrEt) hasta concentración final 0,5 µg/ml. Agitar para que se reparta homogeneamente. 5. Preparar la bandeja sellando los extremos con cinta adhesiva y colocar los peines. Verter la agarosa disuelta sobre la bandeja. Esperar que gelifique (unos 20 minutos).
8 Hoja 8 de Retirar la cinta de los extremos. Poner la bandeja en la cubeta y añadir tampón TAE 1X conteniendo BrEt 0,5 µg/ml hasta que cubra el gel. Quitar los peines con cuidado. 7. Preparar las muestras añadiéndolas 2,5 µl de tampón de carga 10 X. Cargar 10 µl de cada muestra en los pocillos del gel. 8. Cargar 10 µl de marcador de peso molecular VI en el último pocillo de cada peine. 9. Conectar a la fuente de alimentación (las muestras migran hacia el polo positivo). Aplicar voltios y dejar correr el gel aproximadamente 40 minutos. 10. Colocar el gel sobre un transiluminador de luz UV para visualizar las bandas de ADN TRATAMIENTO DE RESULTADOS Una vez completada la electroforesis, examinar inmediatamente el gel en el transiluminador de luz ultravioleta. En una muestra positiva, se observará una banda clara que migrará paralelamente al producto de PCR del control positivo. Calcular el tamaño de los productos de PCR de las muestras analizadas y del control positivo en referencia al marcador de peso molecular. El producto amplificado del control positivo tiene un tamaño de 257 pares de bases (ver figura). En el control negativo no deben observarse bandas a la altura del control positivo. El procedimiento se considerará válido si los controles positivos de extracción y reacción dan una banda clara a la altura correspondiente al amplicón de VPPA y los controles negativos de extracción y reacción no muestran ningún patrón de bandas. Ensayo opcional: Se puede realizar un análisis de confirmación adicional mediante digestión de los productos amplificados con la enzima de restricción BsmA I. Para ello, se incubarán durante 2,5 horas a 55ºC, 5 µl de ADN amplificado en un volumen final de 20 µl de mezcla de digestión: 2 µl de 10x buffer, 1 µl de BsmA I (5U/µl) y 12 µl de agua destilada estéril. Una vez completado, correr las muestras en un gel de agarosa al 3% tal y como se ha descrito anteriormente. El patrón de restricción obtenido debe incluir dos fragmentos de tamaños y pares de bases en las muestras positivas PUNTOS CRÍTICOS Siendo una de las ventajas de la técnica de PCR su elevada sensibilidad, el punto crítico durante todo el proceso de análisis es el riesgo de contaminación de las muestras, y por tanto, los posibles falsos positivos que en este caso se obtendrían. La contaminación puede deberse al propio VPPA presente en las muestras que puedan ser positivas o en los controles positivos empleados en el proceso de extracción, o al ADN del VPPA resultante de la amplificación y manipulado durante el análisis de los amplicones de una PCR anterior mediante la electroforesis en gel de agarosa. Por ello, es imprescindible seguir y cumplir unas estrictas normas de trabajo para minimizar el riesgo de contaminación intrínseco a la técnica de PCR:
9 Hoja 9 de 10 Todos los pasos que implican el análisis de muestras por PCR se realizarán en espacios diferenciados, con equipamiento y material específico para cada uno: preparación de muestras, extracción de ADN, montaje de mezcla de PCR, análisis por electroforesis de los productos de PCR. Trabajar siempre con guantes de látex o nitrilo limpios en el laboratorio de PCR. Cada vez que el técnico, que esté realizando el análisis, acceda a una zona de PCR diferente, deberá cambiarse los guantes desechando los que tenía puestos. El material será de uso exclusivo para el paso del procedimiento para el que esté destinado por su situación/identificación. Utilizar una punta de pipeta diferente cada vez que se pipetee en un tubo conteniendo alguna muestra o ADN. Nunca se abrirán los tubos con producto amplificado en otro laboratorio que no sea el destinado exclusivamente al análisis de los mismos mediante electroforesis MEDIDAS DE SEGURIDAD Leer y seguir cuidadosamente el protocolo. Conservar los reactivos a la temperatura indicada antes y después de su utilización. No mezclar reactivos ni instrucciones de diferentes kits. Evitar cualquier contaminación de los reactivos. No utilizar los reactivos una vez superada la fecha de caducidad. No comer, beber ni fumar en el laboratorio. No pipetear los reactivos con la boca. Utilizar siempre guantes de látex o nitrilo. El bromuro de etidio es una sustancia cancerígena, principalmente cuando está en polvo. Asegurarse de pedirlo siempre en solución y con gotero. Manipularlo exclusivamente en el laboratorio destinado para ello siguiendo las normas de seguridad establecidas por el servicio de seguridad biológica (guantes, bata, manguitos, gafas de protección). En caso de contacto, lavar inmediatamente con agua abundante y avisar al servicio de seguridad biológica del centro. Avisar al mismo servicio si ocurre un vertido de algún reactivo conteniendo bromuro de etidio. El binding buffer, inhibitor removal buffer y wash buffer incluidos en el kit de extracción de ADN contienen derivados de guanidina que son irritantes, por lo que deben ser manipulados con precaución. En caso de contacto con piel, mucosas y/o ojos, lavar inmediatamente con agua abundante. Si ocurre un vertido accidental, diluir con agua antes de limpiar CONTROL DE CALIDAD Anualmente, el Laboratorio Comunitario de Referencia de PPA, CISA-INIA, Valdeolmos, Madrid, España, organiza un ensayo comparativo interlaboratorial (Interlaboratory Comparison Test, ILCT) para evaluar las técnicas de diagnóstico de PPA disponibles en los Laboratorios Nacionales de Referencia de los países miembros de la UE. El ILCT comprende un número de muestras clínicas ciegas que deben ser analizadas empleando las diferentes técnicas diagnósticas en uso en el laboratorio. El método de PCR convencional descrito en este procedimiento ha sido completamente validado a los largo de los V ensayos comparativos realizados hasta el momento.
10 Hoja 10 de ANEXOS Plantilla CISA/PPA/PCR/1/2008 Nº de registro CISA:... Fecha de entrada:... Tipo de muestras:..... Fecha análisis:... Técnico:. Hora:... Comentarios:.... Orden pipeteo REACTIVOS PCR MIX 1x VOLUMEN (reacción 25μl) Nx CONCENTRACIÓN FINAL 1 H 2 O 17,375μl 2 Buffer 10X 2,5μl 1X 3 Cl 2 Mg 25 mm 2μl 2 mm 4 dntps 10 mm 0,5μl 0,2 mm 5 Primer PPA-1 20 μm 0,25μl 0,2 μm 6 Primer PPA-2 20 μm 0,25μl 0,2 μm 7 Taq Gold 5 U/μl 0,125μl 0,025 U/μl Volumen PCR mix 23 μl 8 Adición de 2μl de ADN molde (muestras y controles de reacción) Identificación de muestras en tubos/placa Programa realizado:. Resultados:
SANIDAD ANIMAL (CISA INIA)
 Hoja 1 de 10 CENTRO DE PROCEDIMIENTO PARA LA DETECCIÓN DEL VIRUS DE LA PESTE PORCINA AFRICANA (VPPA) MEDIANTE REACCIÓN EN CADENA DE LA Fecha de entrada en vigor: Diciembre 2008 REV. FECHA EPÍGRAFE/S CAUSA
Hoja 1 de 10 CENTRO DE PROCEDIMIENTO PARA LA DETECCIÓN DEL VIRUS DE LA PESTE PORCINA AFRICANA (VPPA) MEDIANTE REACCIÓN EN CADENA DE LA Fecha de entrada en vigor: Diciembre 2008 REV. FECHA EPÍGRAFE/S CAUSA
1. OBJETO. 3.1. DOCUMENTOS UTILIZADOS EN LA ELABORACIÓN. 3.2. DOCUMENTOS (PNTs) A UTILIZAR CONJUNTAMENTE. 5.1. MATERIALES Y REACTIVOS.
 Página 1 de 5 CENTRO DE INVESTIGACION EN SANIDAD ANIMAL (CISA-INIA) Laboratorio de Referencia de la UE de PPA (EURL-ASF) Centro de Investigación en Sanidad Animal CISA-INIA, Valdeolmos 28130, Madrid, Spain.
Página 1 de 5 CENTRO DE INVESTIGACION EN SANIDAD ANIMAL (CISA-INIA) Laboratorio de Referencia de la UE de PPA (EURL-ASF) Centro de Investigación en Sanidad Animal CISA-INIA, Valdeolmos 28130, Madrid, Spain.
DETECCIÓN DEL GENOMA DEL VPPA MEDIANTE REACCIÓN EN CADENA DE LA POLIMERASA (PCR) CONVENCIONAL REV. 2013 1. OBJETO.
 Página 1 de 7 CONTENIDO CENTRO DE INVESTIGACION EN SANIDAD ANIMAL (CISA-INIA) Laboratorio de Referencia de la UE de PPA (EURL-ASF) Centro de Investigación en Sanidad Animal CISA-INIA, Valdeolmos 28130,
Página 1 de 7 CONTENIDO CENTRO DE INVESTIGACION EN SANIDAD ANIMAL (CISA-INIA) Laboratorio de Referencia de la UE de PPA (EURL-ASF) Centro de Investigación en Sanidad Animal CISA-INIA, Valdeolmos 28130,
PCR gen 16S ARNr bacteriano
 PCR gen 16S ARNr bacteriano Ref. PCR16S 1. OBJETIVO DEL EXPERIMENTO El objetivo de este experimento es introducir a los estudiantes en los principios y la práctica de la Reacción en Cadena de la Polimerasa
PCR gen 16S ARNr bacteriano Ref. PCR16S 1. OBJETIVO DEL EXPERIMENTO El objetivo de este experimento es introducir a los estudiantes en los principios y la práctica de la Reacción en Cadena de la Polimerasa
REACCIÓN EN CADENA DE LA POLIMERASA (PCR)
 REACCIÓN EN CADENA DE LA POLIMERASA (PCR) Microbiología General Microbiología M de los Alimentos Licenciatura en Bioquímica i Ingeniería en alimentos c Microbiología r 2015 Licenciatura en Biotecnología
REACCIÓN EN CADENA DE LA POLIMERASA (PCR) Microbiología General Microbiología M de los Alimentos Licenciatura en Bioquímica i Ingeniería en alimentos c Microbiología r 2015 Licenciatura en Biotecnología
SSI DERMATOPHYTE PCR KIT PRUEBA PCR DERMATOFITO
 SSI DERMATOPHYTE PCR KIT PRUEBA PCR DERMATOFITO 2 Prueba de PCR para la detección de dermatofitos y Trichophyton rubrum Para uso diagnóstico in vitro Aplicación La prueba de PCR para dermatofitos en uñas
SSI DERMATOPHYTE PCR KIT PRUEBA PCR DERMATOFITO 2 Prueba de PCR para la detección de dermatofitos y Trichophyton rubrum Para uso diagnóstico in vitro Aplicación La prueba de PCR para dermatofitos en uñas
REACCIÓN EN CADENA DE LA POLIMERASA (PCR) Microbiología de los Alimentos Ingeniería en alimentos
 REACCIÓN EN CADENA DE LA POLIMERASA (PCR) Microbiología de los Alimentos Ingeniería en alimentos 2015 Desarrollada por Kary Mullis en 1986 Técnica in vitro que permite amplificar enzimáticamente una región
REACCIÓN EN CADENA DE LA POLIMERASA (PCR) Microbiología de los Alimentos Ingeniería en alimentos 2015 Desarrollada por Kary Mullis en 1986 Técnica in vitro que permite amplificar enzimáticamente una región
DANAGENE BLOOD DNA KIT
 Ref. 0601 100 ml Ref. 0602 200 ml DANAGENE BLOOD DNA KIT 1.INTRODUCCION DANAGENE BLOOD DNA Kit provee un método para la extracción de ADN genómico de alta calidad a partir de sangre total o médula ósea.
Ref. 0601 100 ml Ref. 0602 200 ml DANAGENE BLOOD DNA KIT 1.INTRODUCCION DANAGENE BLOOD DNA Kit provee un método para la extracción de ADN genómico de alta calidad a partir de sangre total o médula ósea.
ESTUDIO DE POLIMORFISMOS ALU HUMANOS POR PCR
 ESTUDIO DE POLIMORFISMOS ALU HUMANOS POR PCR Ref. PCRALU 1. OBJETIVO DEL EXPERIMENTO El objetivo de este experimento es introducir a los estudiantes en los principios y práctica de la Reacción en Cadena
ESTUDIO DE POLIMORFISMOS ALU HUMANOS POR PCR Ref. PCRALU 1. OBJETIVO DEL EXPERIMENTO El objetivo de este experimento es introducir a los estudiantes en los principios y práctica de la Reacción en Cadena
IV Curso Avanzado WHO GSS 2006 Buenos Aires 15 al 24 de mayo de 2006
 IV Curso Avanzado WHO GSS 2006 Buenos Aires 15 al 24 de mayo de 2006 REACCION EN CADENA DE LA POLIMERASA (PCR) EN EL DIAGNOSTICO DE Campylobacter jejuni/coli Viernes 19 de mayo María Rosa Viñas Servicio
IV Curso Avanzado WHO GSS 2006 Buenos Aires 15 al 24 de mayo de 2006 REACCION EN CADENA DE LA POLIMERASA (PCR) EN EL DIAGNOSTICO DE Campylobacter jejuni/coli Viernes 19 de mayo María Rosa Viñas Servicio
Taller Ciencia para Jóvenes CIMAT 2012 Bachillerato julio 8 14 Cinvestav Campus Guanajuato
 Introducción Taller Ciencia para Jóvenes CIMAT 2012 Bachillerato julio 8 14 Cinvestav Campus Guanajuato Visita al CINVESTAV - Irapuato. 19 julio, 2012. Las bacterias son los organismos más abundantes que
Introducción Taller Ciencia para Jóvenes CIMAT 2012 Bachillerato julio 8 14 Cinvestav Campus Guanajuato Visita al CINVESTAV - Irapuato. 19 julio, 2012. Las bacterias son los organismos más abundantes que
REACCIÓN EN CADENA DE LA POLIMERASA (PCR)
 REACCIÓN EN CADENA DE LA POLIMERASA (PCR) Lic. en Bioquímica Lic. en Biotecnología Microbiología de los Alimentos 2016 Desarrollada por Kary Mullis en 1986 Técnica in vitro que permite amplificar enzimáticamente
REACCIÓN EN CADENA DE LA POLIMERASA (PCR) Lic. en Bioquímica Lic. en Biotecnología Microbiología de los Alimentos 2016 Desarrollada por Kary Mullis en 1986 Técnica in vitro que permite amplificar enzimáticamente
DETERMINACIÓN DEL MAPA DE UN PLÁSMIDO CON ENZIMAS DE RESTRICCIÓN
 DETERMINACIÓN DEL MAPA DE UN PLÁSMIDO CON ENZIMAS DE RESTRICCIÓN 6 grupos de estudiantes 1. OBJETIVO DEL EXPERIMENTO El objetivo de este experimento es desarrollar un conocimiento del mapaje de ADN determinando
DETERMINACIÓN DEL MAPA DE UN PLÁSMIDO CON ENZIMAS DE RESTRICCIÓN 6 grupos de estudiantes 1. OBJETIVO DEL EXPERIMENTO El objetivo de este experimento es desarrollar un conocimiento del mapaje de ADN determinando
EXTRACCIÓN DE ADN DE HONGOS FILAMENTOSOS
 EXTRACCIÓN DE ADN DE HONGOS FILAMENTOSOS Los hongos poseen un genoma complejo consistente en: ADN nuclear (n ADN) ADN mitocondrial (mt ADN) en algunos casos ADN plasmídico EXTRACCIÓN DE ADN DE HONGOS FILAMENTOSOS
EXTRACCIÓN DE ADN DE HONGOS FILAMENTOSOS Los hongos poseen un genoma complejo consistente en: ADN nuclear (n ADN) ADN mitocondrial (mt ADN) en algunos casos ADN plasmídico EXTRACCIÓN DE ADN DE HONGOS FILAMENTOSOS
PCR Múltiplex. Listeria monocytogenes
 PCR Múltiplex Listeria monocytogenes PCR-múltiplex En una sola reacción de PCR se amplifican al mismo tiempo 2 o más genes Condiciones similares de PCR para los genes amplificar: Desnaturalización Alineamiento
PCR Múltiplex Listeria monocytogenes PCR-múltiplex En una sola reacción de PCR se amplifican al mismo tiempo 2 o más genes Condiciones similares de PCR para los genes amplificar: Desnaturalización Alineamiento
Código: IDX-016 Ver: 1 TOXO. Sistema para la detección de la presencia de ADN de Toxoplasma gondii. Reg. MSP 21205
 Sistema para la detección de la presencia de ADN de Toxoplasma gondii Reg. MSP 21205 Valdense 3616. 11700. Montevideo. Uruguay. Teléfono (598) 2 336 83 01. Fax (598) 2 336 71 60. info@atgen.com.uy www.atgen.com.uy
Sistema para la detección de la presencia de ADN de Toxoplasma gondii Reg. MSP 21205 Valdense 3616. 11700. Montevideo. Uruguay. Teléfono (598) 2 336 83 01. Fax (598) 2 336 71 60. info@atgen.com.uy www.atgen.com.uy
Instrucciones de uso. BAG Cycler Check. Kit de para la validación de la uniformidad de la temperatura en los termocicladores
 Instrucciones de uso BAG Cycler Check Kit de para la validación de la uniformidad de la temperatura en los termocicladores listo para usar, prealicuotado REF 7104 (10 tests) REF 71044 (4 tests) Contenidos
Instrucciones de uso BAG Cycler Check Kit de para la validación de la uniformidad de la temperatura en los termocicladores listo para usar, prealicuotado REF 7104 (10 tests) REF 71044 (4 tests) Contenidos
APLICACIÓN DE LA PCR: DIAGNÓSTICO DE PARÁSITOS
 Prácticas docentes en la COD: 10-71 APLICACIÓN DE LA PCR: DIAGNÓSTICO DE PARÁSITOS FUNDAMENTO TEÓRICO La PCR es una técnica que permite llevar a cabo la síntesis in vitro de fragmentos de ADN. Está basada
Prácticas docentes en la COD: 10-71 APLICACIÓN DE LA PCR: DIAGNÓSTICO DE PARÁSITOS FUNDAMENTO TEÓRICO La PCR es una técnica que permite llevar a cabo la síntesis in vitro de fragmentos de ADN. Está basada
3. MATERIALES Y MÉTODOS
 3. MATERIALES Y MÉTODOS El proceso general llevado a cabo en la presente tesis se ilustra en el siguiente esquema: Exudado uretral/ cervical y/o biopsias Extracción del ADN PCR Digestión Algoritmo computacional:
3. MATERIALES Y MÉTODOS El proceso general llevado a cabo en la presente tesis se ilustra en el siguiente esquema: Exudado uretral/ cervical y/o biopsias Extracción del ADN PCR Digestión Algoritmo computacional:
ANEXOS. Anexo 1 Transformación mediante electroporación
 Anexo 1 Transformación mediante electroporación ANEXOS En este método de transformación de E. coli se requieren células electrocompetentes. La preparación de estas células consta de los siguientes pasos:
Anexo 1 Transformación mediante electroporación ANEXOS En este método de transformación de E. coli se requieren células electrocompetentes. La preparación de estas células consta de los siguientes pasos:
Anexo Conservar a 4 o C.
 Anexo 1 Purificación de ADN viral 1. Partir de un sobrenadante de un cultivo celular infectado y clarificado. 2. Concentrar las formas brotantes de los baculovirus por centrifugación (centrifugrar 1,5
Anexo 1 Purificación de ADN viral 1. Partir de un sobrenadante de un cultivo celular infectado y clarificado. 2. Concentrar las formas brotantes de los baculovirus por centrifugación (centrifugrar 1,5
DANAGENE RNA PURIFICATION KIT
 DANAGENE RNA PURIFICATION KIT REF.0801.1 100 EXTRACCIONES REF.0801.2 500 EXTRACCIONES 1.INTRODUCCION Este kit permite la permite la obtención de ARN total a partir de cultivos celulares, tejidos animales,
DANAGENE RNA PURIFICATION KIT REF.0801.1 100 EXTRACCIONES REF.0801.2 500 EXTRACCIONES 1.INTRODUCCION Este kit permite la permite la obtención de ARN total a partir de cultivos celulares, tejidos animales,
PROPIEDADES FISICOQUÍMICAS DE LOS ÁCIDOS NUCLEICOS. Es un ácido capaz de formar sales con iones cargados
 Extracción de ADN Genética molecular PROPIEDADES FISICOQUÍMICAS DE LOS ÁCIDOS NUCLEICOS Es un ácido capaz de formar sales con iones cargados positivamente (cationes). Es soluble en soluciones concentradas
Extracción de ADN Genética molecular PROPIEDADES FISICOQUÍMICAS DE LOS ÁCIDOS NUCLEICOS Es un ácido capaz de formar sales con iones cargados positivamente (cationes). Es soluble en soluciones concentradas
METODOLOGÍAS UTILIZADAS EN INVESTIGACIÓN BÁSICA Y APLICADA REACCION EN CADENA DE LA POLIMERASA (PCR)
 METODOLOGÍAS UTILIZADAS EN INVESTIGACIÓN BÁSICA Y APLICADA REACCION EN CADENA DE LA POLIMERASA (PCR) Centro de de Microscopía Electrónica Facultad de de Ciencias Médicas Universidad Nacional de de Córdoba
METODOLOGÍAS UTILIZADAS EN INVESTIGACIÓN BÁSICA Y APLICADA REACCION EN CADENA DE LA POLIMERASA (PCR) Centro de de Microscopía Electrónica Facultad de de Ciencias Médicas Universidad Nacional de de Córdoba
TECHNOLOGY. CROSSMATCH TEST canino. primer test inmunocromatografico para reaccion cruzada con antiglobulina canina especifica.
 CROSSMATCH TEST canino primer test inmunocromatografico para reaccion cruzada con antiglobulina canina especifica 20 minutos TECHNOLOGY - ahorra tiempo - facil manipulacion - resultados fiables - facil
CROSSMATCH TEST canino primer test inmunocromatografico para reaccion cruzada con antiglobulina canina especifica 20 minutos TECHNOLOGY - ahorra tiempo - facil manipulacion - resultados fiables - facil
UNIVERSIDAD NACIONAL AUTÓNOMA DE MÉXICO FACULTAD DE MEDICINA VETERINARIA Y ZOOTECNIA
 UNIVERSIDAD NACIONAL AUTÓNOMA DE MÉXICO FACULTAD DE MEDICINA VETERINARIA Y ZOOTECNIA. Estudio comparativo del diagnóstico del virus del PRRS por RT-PCR, PCR anidada y RT-PCR en tiempo real. Zoalli Angélica
UNIVERSIDAD NACIONAL AUTÓNOMA DE MÉXICO FACULTAD DE MEDICINA VETERINARIA Y ZOOTECNIA. Estudio comparativo del diagnóstico del virus del PRRS por RT-PCR, PCR anidada y RT-PCR en tiempo real. Zoalli Angélica
5. DETECCION DE GENES DE VIRULENCIA MEDIANTE HIBRIDACIÓN CON SONDAS DE ADN
 5. DETECCION DE GENES DE VIRULENCIA MEDIANTE HIBRIDACIÓN CON SONDAS DE ADN Materiales - Eppendorf de 1,5 ml estériles - Eppendorf de pared fina para PCR - Puntas de pipeta estériles desechables - Guantes
5. DETECCION DE GENES DE VIRULENCIA MEDIANTE HIBRIDACIÓN CON SONDAS DE ADN Materiales - Eppendorf de 1,5 ml estériles - Eppendorf de pared fina para PCR - Puntas de pipeta estériles desechables - Guantes
ELABORACIÓN N DE MEZCLA PARA PCR. Raquel Asunción Lima Cordón
 ELABORACIÓN N DE MEZCLA PARA PCR Raquel Asunción Lima Cordón PCR Polymerase Chain reaction (reacción en cadena de la polimerasa) Sintetizar muchas veces un fragmento de ADN PCR: simulación de lo que sucede
ELABORACIÓN N DE MEZCLA PARA PCR Raquel Asunción Lima Cordón PCR Polymerase Chain reaction (reacción en cadena de la polimerasa) Sintetizar muchas veces un fragmento de ADN PCR: simulación de lo que sucede
ELECTROFORESIS AVANZADA
 Ref. ELECAVANZADA (4 prácticas) 1. OBJETIVO DEL EXPERIMENTO ELECTROFORESIS AVANZADA El objetivo de este experimento es introducir a los alumnos en el conocimiento de la teoría electroforética y familiarizarse
Ref. ELECAVANZADA (4 prácticas) 1. OBJETIVO DEL EXPERIMENTO ELECTROFORESIS AVANZADA El objetivo de este experimento es introducir a los alumnos en el conocimiento de la teoría electroforética y familiarizarse
Construcción de la biblioteca en cósmidos de Azospirillum brasilense CBG 497.
 Construcción de la biblioteca en cósmidos de Azospirillum brasilense CBG 497. Extracción de DNA genómico El DNA de A. brasilense CBG 497 se extrajo siguiendo el método descrito por la casa comercial distribuidora
Construcción de la biblioteca en cósmidos de Azospirillum brasilense CBG 497. Extracción de DNA genómico El DNA de A. brasilense CBG 497 se extrajo siguiendo el método descrito por la casa comercial distribuidora
Materiales para la secuenciación de ADN
 Introduccion La Secuenciación Sanger es un método de secuenciación de ADN en el que el ADN diana se desnaturaliza y se hibrida con un cebador de oligonucleótidos, que se extiende entonces gracias a la
Introduccion La Secuenciación Sanger es un método de secuenciación de ADN en el que el ADN diana se desnaturaliza y se hibrida con un cebador de oligonucleótidos, que se extiende entonces gracias a la
38. Purificación de ADN plasmídico y electroforesis del mismo en gel de agarosa
 38. Purificación de ADN plasmídico y electroforesis del mismo en gel de agarosa José Luis Caballero Repullo, Enriqueta Moyano, Juan Muñoz Blanco Departamento de Bioquímica y Biología Molecular, Campus
38. Purificación de ADN plasmídico y electroforesis del mismo en gel de agarosa José Luis Caballero Repullo, Enriqueta Moyano, Juan Muñoz Blanco Departamento de Bioquímica y Biología Molecular, Campus
41. Comprobación de colonias transformantes mediante PCR y electroforesis
 41. Comprobación de colonias transformantes mediante PCR y electroforesis Aurora Galván Cejudo, Manuel Tejada, Antonio Camargo, José Javier Higuera, Vicente Mariscal, Emilio Fernández Reyes Departamento
41. Comprobación de colonias transformantes mediante PCR y electroforesis Aurora Galván Cejudo, Manuel Tejada, Antonio Camargo, José Javier Higuera, Vicente Mariscal, Emilio Fernández Reyes Departamento
PRÁCTICA III. AISLAMIENTO DE MITOCONDRIAS: ACTIVIDAD MALATO DESHIDROGENASA
 PRÁCTICA III. AISLAMIENTO DE MITOCONDRIAS: ACTIVIDAD MALATO DESHIDROGENASA 1. Fundamento Teórico La mayoría de los procesos bioquímicos que producen energía química se realizan en orgánulos intracelulares
PRÁCTICA III. AISLAMIENTO DE MITOCONDRIAS: ACTIVIDAD MALATO DESHIDROGENASA 1. Fundamento Teórico La mayoría de los procesos bioquímicos que producen energía química se realizan en orgánulos intracelulares
Manual de Uso (Ref /2)
 Fabricado por: BIOTOOLS B&M Labs, S.A. Valle de Tobalina - 52 - Nave 39 28021 Madrid España Tel. (34) 91 710 00 74 Fax (34) 93 843 78 84 e-mail: info@biotools.eu www.biotools.eu Diseñado para la purificación
Fabricado por: BIOTOOLS B&M Labs, S.A. Valle de Tobalina - 52 - Nave 39 28021 Madrid España Tel. (34) 91 710 00 74 Fax (34) 93 843 78 84 e-mail: info@biotools.eu www.biotools.eu Diseñado para la purificación
Detección de patógenos en alimentos, utilizando la técnica de PCR, reacción en cadena de la polimerasa.
 Detección de patógenos en alimentos, utilizando la técnica de PCR, reacción en cadena de la polimerasa. Lic. Esp. Mariano Diego Massari 1er Congreso Bioquímico Córdoba 2011 8ª Jornada de Actualización
Detección de patógenos en alimentos, utilizando la técnica de PCR, reacción en cadena de la polimerasa. Lic. Esp. Mariano Diego Massari 1er Congreso Bioquímico Córdoba 2011 8ª Jornada de Actualización
PROCEDIMIENTO DE EVALUACIÓN Y ACREDITACIÓN DE LAS COMPETENCIAS PROFESIONALES CUESTIONARIO DE AUTOEVALUACIÓN PARA LAS TRABAJADORAS Y TRABAJADORES
 MINISTERIO DE EDUCACIÓN SECRETARÍA DE ESTADO DE EDUCACIÓN Y FORMACIÓN PROFESIONAL DIRECCIÓN GENERAL DE FORMACIÓN PROFESIONAL INSTITUTO NACIONAL DE LAS CUALIFICACIONES PROCEDIMIENTO DE EVALUACIÓN Y ACREDITACIÓN
MINISTERIO DE EDUCACIÓN SECRETARÍA DE ESTADO DE EDUCACIÓN Y FORMACIÓN PROFESIONAL DIRECCIÓN GENERAL DE FORMACIÓN PROFESIONAL INSTITUTO NACIONAL DE LAS CUALIFICACIONES PROCEDIMIENTO DE EVALUACIÓN Y ACREDITACIÓN
Módulo 1 Biología Molecular Genética Molecular II 2009. Módulo 1. Amplificación de un fragmento de ADN genómico por PCR
 Módulo 1 Amplificación de un fragmento de ADN genómico por PCR En este primer módulo se amplificará por PCR, mediante el uso de oligonucleótidos específicos, un fragmento de ADN genómico de Aspergillus
Módulo 1 Amplificación de un fragmento de ADN genómico por PCR En este primer módulo se amplificará por PCR, mediante el uso de oligonucleótidos específicos, un fragmento de ADN genómico de Aspergillus
2. NIVEL MEDIO 1. NIVEL BASICO BIOLOGIA MOLECULAR 2.1 DNA SALIVA
 BIOLOGIA MOLECULAR Hemos elaborado un programa en 3 niveles, en función del tipo de estudiante y las posibilidades del centro educativo: 1. NIVEL BASICO 2. NIVEL MEDIO DANAEXTRACTOR KIT Práctica que constituye
BIOLOGIA MOLECULAR Hemos elaborado un programa en 3 niveles, en función del tipo de estudiante y las posibilidades del centro educativo: 1. NIVEL BASICO 2. NIVEL MEDIO DANAEXTRACTOR KIT Práctica que constituye
EXTRACCIÓN Y DETERMINACIÓN DE ÁCIDOS NUCLEICOS DE LA LEVADURA
 EXTRACCIÓN Y DETERMINACIÓN DE ÁCIDS NUCLEICS DE LA LEVADURA bjetivos: Al finalizar el trabajo práctico los cursantes estarán en capacidad de: - Extraer ARN a partir de células de levadura. - Realizar la
EXTRACCIÓN Y DETERMINACIÓN DE ÁCIDS NUCLEICS DE LA LEVADURA bjetivos: Al finalizar el trabajo práctico los cursantes estarán en capacidad de: - Extraer ARN a partir de células de levadura. - Realizar la
WITNESS RELAXIN (plasma, serum) RLX RLX u d 9 n n ersio V X RLX L R -W IO B S
 WITNESS RELAXIN (plasma, serum) SBIO-W Version n 9 du 28.07.2010 WITNESS RELAXIN WITNESS RELAXIN GENERALIDADES El kit WITNESS RELAXIN permite diagnosticar la gestación en la perra y en la gata, y permite
WITNESS RELAXIN (plasma, serum) SBIO-W Version n 9 du 28.07.2010 WITNESS RELAXIN WITNESS RELAXIN GENERALIDADES El kit WITNESS RELAXIN permite diagnosticar la gestación en la perra y en la gata, y permite
PCR en Tiempo Real. Introducción
 Introducción Página 1 de 6 Introducción general La reacción en cadena de la polimerasa, cuyas iniciales en inglés son PCR ("polymerase chain reaction"), es una técnica que fue desarrollada por Kary Mullis
Introducción Página 1 de 6 Introducción general La reacción en cadena de la polimerasa, cuyas iniciales en inglés son PCR ("polymerase chain reaction"), es una técnica que fue desarrollada por Kary Mullis
Técnicas moleculares.
 Técnicas moleculares. DMTV Carolina Acevedo Curso de Microbiología 2015 SÍNTESIS IN VITRO DE UNA GRAN CANTIDAD DE COPIAS DE UN SEGMENTO DE ADN EXISTENTE EN UNA MUESTRA. O sea. Amplificamos en forma exponencial
Técnicas moleculares. DMTV Carolina Acevedo Curso de Microbiología 2015 SÍNTESIS IN VITRO DE UNA GRAN CANTIDAD DE COPIAS DE UN SEGMENTO DE ADN EXISTENTE EN UNA MUESTRA. O sea. Amplificamos en forma exponencial
PROCEDIMIENTO DETECCIÓN Y ENUMERACIÓN POR NUMERO MAS PROBABLE (NMP) CON ETAPA DE PRE- ENRIQUECIMIENTO DE ENTEROBACTERIACEAE EN ALIMENTOS
 Página 1 de 5 1. OBJETIVO Estimar el número de Enterobacteriaceae presentes en el alimento. 2. CAMPO DE APLICACIÓN Y ALCANCE Aplicar este procedimiento a todas las muestras de alimentos de consumo humano
Página 1 de 5 1. OBJETIVO Estimar el número de Enterobacteriaceae presentes en el alimento. 2. CAMPO DE APLICACIÓN Y ALCANCE Aplicar este procedimiento a todas las muestras de alimentos de consumo humano
CURSO DE EXTENSIÓN TEÓRICO PRÁCTICO HERRAMIENTAS EFICIENTES PARA LA IDENTIFICACIÓN DE LEVADURAS DE INTERÉS AGROINDUSTRIAL
 LIBRO DE MEMORIAS 2 CURSO DE EXTENSIÓN TEÓRICO PRÁCTICO HERRAMIENTAS EFICIENTES PARA LA IDENTIFICACIÓN DE LEVADURAS DE INTERÉS AGROINDUSTRIAL Santiago de Cali, 23 al 28 de agosto de 2010 3 Libro de memorias
LIBRO DE MEMORIAS 2 CURSO DE EXTENSIÓN TEÓRICO PRÁCTICO HERRAMIENTAS EFICIENTES PARA LA IDENTIFICACIÓN DE LEVADURAS DE INTERÉS AGROINDUSTRIAL Santiago de Cali, 23 al 28 de agosto de 2010 3 Libro de memorias
MANUAL DE PRÁCTICAS DE LABORATORIO
 MANUAL DE PRÁCTICAS DE LABORATORIO INGENIERIA ENBIOTECNOLOGÍA INGENIERÍA GENÉTICA FICHA TECNICA FICHA TÉCNICA SEMINARIO DE BIOTECNOLOGÍA MÉDICO-FARMACÉUTICA Fecha: Nombre del catedrático: 10-Julio-2012
MANUAL DE PRÁCTICAS DE LABORATORIO INGENIERIA ENBIOTECNOLOGÍA INGENIERÍA GENÉTICA FICHA TECNICA FICHA TÉCNICA SEMINARIO DE BIOTECNOLOGÍA MÉDICO-FARMACÉUTICA Fecha: Nombre del catedrático: 10-Julio-2012
PLANIFICACIÓN DE ASIGNATURA
 PLANIFICACIÓN DE ASIGNATURA I IDENTIFICACION GENERAL DE LA ASIGNATURA CARRERA BIOQUIMICA DEPARTAMENTO BIOLOGIA ASIGNATURA BIOLOGIA MOLECULAR II CÓDIGO 1681 PRERREQUISITOS Biología Molecular I CREDITOS
PLANIFICACIÓN DE ASIGNATURA I IDENTIFICACION GENERAL DE LA ASIGNATURA CARRERA BIOQUIMICA DEPARTAMENTO BIOLOGIA ASIGNATURA BIOLOGIA MOLECULAR II CÓDIGO 1681 PRERREQUISITOS Biología Molecular I CREDITOS
ENFERMEDADES INFECCIOSAS GRADO EN VETERINARIA
 FACULTAD DE VETERINARIA DEPARTAMENTO DE SANIDAD ANIMAL ENFERMEDADES INFECCIOSAS GRADO EN VETERINARIA GUIÓN DE PRÁCTICAS DE LABORATORIO CURSO 2014 2015 MÓDULO: PORCINO Síndrome respiratorio y reproductor
FACULTAD DE VETERINARIA DEPARTAMENTO DE SANIDAD ANIMAL ENFERMEDADES INFECCIOSAS GRADO EN VETERINARIA GUIÓN DE PRÁCTICAS DE LABORATORIO CURSO 2014 2015 MÓDULO: PORCINO Síndrome respiratorio y reproductor
Conceptos generales de Biología Molecular. Extracción de DNA y Reacción en Cadena de la Polimerasa (PCR).
 Conceptos generales de Biología Molecular. Extracción de DNA y Reacción en Cadena de la Polimerasa (PCR). Olga Redondo González MIR 3 Análisis Clínicos Hospital Universitario de Guadalajara, 25 abril 2007
Conceptos generales de Biología Molecular. Extracción de DNA y Reacción en Cadena de la Polimerasa (PCR). Olga Redondo González MIR 3 Análisis Clínicos Hospital Universitario de Guadalajara, 25 abril 2007
PRÁCTICAS DE MICROBIOLOGIA CLINICA
 PRÁCTICAS DE MICROBIOLOGIA CLINICA Juan Carlos Rodríguez Hospital General Universitario de Alicante E-mail: rodriguez_juadia@gva.es http://microbiologia-alicante.umh.es CASO CLINICO: Rubéola Evolución
PRÁCTICAS DE MICROBIOLOGIA CLINICA Juan Carlos Rodríguez Hospital General Universitario de Alicante E-mail: rodriguez_juadia@gva.es http://microbiologia-alicante.umh.es CASO CLINICO: Rubéola Evolución
FRAGMENTO OLIGO 5-3 Hebra SECUENCIA 5' - - > 3' TAMAÑO (pb) F1. hmtl 569 L AACCAAACCCCAAAGACACC hmth2982 H CTGATCCAACATCGAGGTCG
 ANEXO 1 Protocolo para la PCR para la amplificación del mtdna en 10 fragmentos solapantes: Se prepara la siguiente mezcla: Tampón ( TRIS 100 mm, MgCl 2 12 mm, KCl 500 mm, ph 8,3): 10X dntps : 10 mm (cada
ANEXO 1 Protocolo para la PCR para la amplificación del mtdna en 10 fragmentos solapantes: Se prepara la siguiente mezcla: Tampón ( TRIS 100 mm, MgCl 2 12 mm, KCl 500 mm, ph 8,3): 10X dntps : 10 mm (cada
velocidades de movimiento mediante la aplicación de un campo eléctrico a través de una matriz porosa
 INTRODUCCIÓN En general, la electroforesis es una técnica que separa las moléculas en base a sus diferentes velocidades de movimiento mediante la aplicación de un campo eléctrico a través de una matriz
INTRODUCCIÓN En general, la electroforesis es una técnica que separa las moléculas en base a sus diferentes velocidades de movimiento mediante la aplicación de un campo eléctrico a través de una matriz
KIT PARA ESTUDIO MOLECULAR DE LA TRANSLOCACIÓN t(14;18) Nº CAT. MAD M-2/5 (20 DETERMINACIONES)
 KIT PARA ESTUDIO MOLECULAR DE LA TRANSLOCACIÓN t(14;18) Nº CAT. MAD-003997M-2/5 (20 DETERMINACIONES) El diagnóstico de los procesos linfoproliferativos se ha realizado tradicionalmente en base a las alteraciones
KIT PARA ESTUDIO MOLECULAR DE LA TRANSLOCACIÓN t(14;18) Nº CAT. MAD-003997M-2/5 (20 DETERMINACIONES) El diagnóstico de los procesos linfoproliferativos se ha realizado tradicionalmente en base a las alteraciones
Conceptos y técnicas en ecología fluvial
 Conceptos y técnicas en ecología fluvial Edición a cargo de: ARTURO ELOSEGI Profesor titular de Ecología en la Universidad del País Vasco SERGI SABATER Catedrático de Ecología en la Universidad de Girona
Conceptos y técnicas en ecología fluvial Edición a cargo de: ARTURO ELOSEGI Profesor titular de Ecología en la Universidad del País Vasco SERGI SABATER Catedrático de Ecología en la Universidad de Girona
12.359,04 IMPORTE MAXIMO LOTE 1: ,92 IMPORTE MAXIMO LOTE 2: IMPORTE MAXIMO LOTE 3: ,54 REACTIVOS PARA AISLAMIENTO DE ACIDOS NUCLEICOS
 HOSPITAL RAMON Y CAJAL RAZON SOCIAL: SUMINISTROS - PETICION DE OFERTAS C.I.F.: SERVICIO DE GENETICA MEDICA DOMICILIO: LOCALIDAD: TRAMITA: HOSPITAL RAMON Y CAJAL TELEFONO/FAX: Nº DE COMPRA: CONCURSO ABIERTO
HOSPITAL RAMON Y CAJAL RAZON SOCIAL: SUMINISTROS - PETICION DE OFERTAS C.I.F.: SERVICIO DE GENETICA MEDICA DOMICILIO: LOCALIDAD: TRAMITA: HOSPITAL RAMON Y CAJAL TELEFONO/FAX: Nº DE COMPRA: CONCURSO ABIERTO
Easy PDF Creator is professional software to create PDF. If you wish to remove this line, buy it now.
 Unidad Curricular: Virología y Micología Veterinaria 1 TRABAJO PRÁCTICO No. 3 AMPLIFICACIÓN DE GENES VIRALES Reacción en Cadena de la Polimerasa, conocida como PCR (por sus siglas en inglés: Polimerase
Unidad Curricular: Virología y Micología Veterinaria 1 TRABAJO PRÁCTICO No. 3 AMPLIFICACIÓN DE GENES VIRALES Reacción en Cadena de la Polimerasa, conocida como PCR (por sus siglas en inglés: Polimerase
PCR gen 18S ARNr humano
 PCR gen 18S ARNr humano Ref.PCR18S 1.OBJETIVO DEL EXPERIMENTO El objetivo de este experimento es introducir a los estudiantes en los principios y práctica de la Reacción en Cadena de la Polimerasa (PCR)
PCR gen 18S ARNr humano Ref.PCR18S 1.OBJETIVO DEL EXPERIMENTO El objetivo de este experimento es introducir a los estudiantes en los principios y práctica de la Reacción en Cadena de la Polimerasa (PCR)
Sistema Integrado de Gestión RECONOCIMIENTO Y PROPIEDADES DE LAS PROTEINAS PROGRAMAS DE DEPORTE Y FISIOTERAPIA GUIA PRÁCTICA N 6
 Sistema Integrado de Gestión RECONOCIMIENTO Y PROGRAMAS DE DEPORTE Y Versión 3 Proceso: Investigación - IV Octubre de 2013 Página 2 de 10 1. OBJETIVOS Reconocer algunas propiedades de las proteínas Determinar
Sistema Integrado de Gestión RECONOCIMIENTO Y PROGRAMAS DE DEPORTE Y Versión 3 Proceso: Investigación - IV Octubre de 2013 Página 2 de 10 1. OBJETIVOS Reconocer algunas propiedades de las proteínas Determinar
INSTRUCCIONES PARA AISLAMIENTO DE LEUCOCITOS A PARTIR DE SANGRE TOTAL
 INSTRUCCIONES PARA AISLAMIENTO DE LEUCOCITOS A PARTIR DE SANGRE TOTAL EL PRIMER PASO, ES LEER PRIMERO Y LUEGO SEGUIR TODAS LAS INSTRUCCIONES!!!!! ALFREDO URIBE ARDILA M.SC. REACTIVOS SOLUCION DEXTRAN-HEPARINA
INSTRUCCIONES PARA AISLAMIENTO DE LEUCOCITOS A PARTIR DE SANGRE TOTAL EL PRIMER PASO, ES LEER PRIMERO Y LUEGO SEGUIR TODAS LAS INSTRUCCIONES!!!!! ALFREDO URIBE ARDILA M.SC. REACTIVOS SOLUCION DEXTRAN-HEPARINA
PCR. Componentes del PCR. PCR Polymerase Chain Reaction (Reacción en Cadena de la Polimerasa)
 PCR PCR Polymerase Chain Reaction (Reacción en Cadena de la Polimerasa) Es una técnica de biología molecular descrita en 1986 por Kary Mullis. (Nobel de química en 1993) Necesidad de pruebas de diagnóstico
PCR PCR Polymerase Chain Reaction (Reacción en Cadena de la Polimerasa) Es una técnica de biología molecular descrita en 1986 por Kary Mullis. (Nobel de química en 1993) Necesidad de pruebas de diagnóstico
DETECCIÓN DE C. jejuni EN HAMBURGUESA DE POLLO POR PCR TRADICIONAL PRT-712.04-082
 Página 1 de 5 1. OBJETIVO Detectar la presencia de Campylobacter jejuni en hamburguesa de pollo mediante técnica de PCR. 2. CAMPO DE APLICACIÓN Y ALCANCE Aplicar este procedimiento a muestras de hamburguesa
Página 1 de 5 1. OBJETIVO Detectar la presencia de Campylobacter jejuni en hamburguesa de pollo mediante técnica de PCR. 2. CAMPO DE APLICACIÓN Y ALCANCE Aplicar este procedimiento a muestras de hamburguesa
A: Protocolo de Actuación para trabajos con Bromuro de Etidio.
 TRABAJOS CON BROMURO DE ETIDIO Y ACRILAMIDA. 1 A: Protocolo de Actuación para trabajos con Bromuro de Etidio. Objeto: Dar instrucciones de seguridad para todos los procedimientos que utilicen Bromuro de
TRABAJOS CON BROMURO DE ETIDIO Y ACRILAMIDA. 1 A: Protocolo de Actuación para trabajos con Bromuro de Etidio. Objeto: Dar instrucciones de seguridad para todos los procedimientos que utilicen Bromuro de
EXTRACCIÓN Y CUANTIFICACION DEL ARN DE LA LEVADURA
 EXTRACCIÓN Y CUANTIFICACION DEL ARN DE LA LEVADURA Objetivos: Al finalizar el trabajo práctico los cursantes estarán en capacidad de: - Extraer ARN a partir de células de levadura. - Realizar la hidrólisis
EXTRACCIÓN Y CUANTIFICACION DEL ARN DE LA LEVADURA Objetivos: Al finalizar el trabajo práctico los cursantes estarán en capacidad de: - Extraer ARN a partir de células de levadura. - Realizar la hidrólisis
1. OBJETO. 2. ALCANCE. 3.1. DOCUMENTOS UTILIZADOS EN LA ELABORACIÓN. 3.2. DOCUMENTOS (PNTs) A UTILIZAR CONJUNTAMENTE. 5.1. MATERIALES Y REACTIVOS.
 Página 1 de 9 1. OBJETO. CONTENIDO CENTRO DE INVESTIGACION EN SANIDAD ANIMAL (CISA-INIA) Laboratorio de Referencia de la UE de PPA (EURL-ASF) Centro de Investigación en Sanidad Animal CISA-INIA, Valdeolmos
Página 1 de 9 1. OBJETO. CONTENIDO CENTRO DE INVESTIGACION EN SANIDAD ANIMAL (CISA-INIA) Laboratorio de Referencia de la UE de PPA (EURL-ASF) Centro de Investigación en Sanidad Animal CISA-INIA, Valdeolmos
17.- Electroforesis de ácidos nucleicos en geles de agarosa. Aislamiento y caracterización electroforética de DNA plasmídico
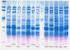 17.- Electroforesis de ácidos nucleicos en geles de agarosa. Aislamiento y caracterización electroforética de DNA plasmídico Carmen Alicia Padilla Peña, Jesús Diez Dapena, Emilia Martínez Galisteo, José
17.- Electroforesis de ácidos nucleicos en geles de agarosa. Aislamiento y caracterización electroforética de DNA plasmídico Carmen Alicia Padilla Peña, Jesús Diez Dapena, Emilia Martínez Galisteo, José
ELECTROFORESIS EN GELES DE AGAROSA. Agustín Garrido. agugarrido@hotmail.com
 1 ELECTROFORESIS EN GELES DE AGAROSA Agustín Garrido agugarrido@hotmail.com Introducción En este trabajo práctico se utilizó la técnica de electroforesis. Este proceso se basa en la migración de las moléculas
1 ELECTROFORESIS EN GELES DE AGAROSA Agustín Garrido agugarrido@hotmail.com Introducción En este trabajo práctico se utilizó la técnica de electroforesis. Este proceso se basa en la migración de las moléculas
RESULTADOS Y DISCUSIÓN
 RESULTADOS Y DISCUSIÓN Estimación de la Concentración Proteica del Filtrado de Cultivo de Mycobacterium tuberculosis H37Rv La curva estándar con la que se estimó la concentración proteica del filtrado
RESULTADOS Y DISCUSIÓN Estimación de la Concentración Proteica del Filtrado de Cultivo de Mycobacterium tuberculosis H37Rv La curva estándar con la que se estimó la concentración proteica del filtrado
QUE ES? Es la búsqueda de anticuerpos preformados contra los linfocitos de un posible donante en el suero de un paciente.
 CROSS MATCH QUE ES? Es la búsqueda de anticuerpos preformados contra los linfocitos de un posible donante en el suero de un paciente. Pueden estar específicamente dirigidos contra los antígenos HLA o contra
CROSS MATCH QUE ES? Es la búsqueda de anticuerpos preformados contra los linfocitos de un posible donante en el suero de un paciente. Pueden estar específicamente dirigidos contra los antígenos HLA o contra
1. OBJETO. 2. ALCANCE. 3. REFERENCIAS. 3.1. DOCUMENTOS UTILIZADOS EN LA ELABORACIÓN. 3.2. DOCUMENTOS (PNTs) A UTILIZAR CONJUNTAMENTE.
 Página 1 de 9 CONTENIDO CENTRO DE INVESTIGACIÓN EN SANIDAD ANIMAL (CISA-INIA) European Union Reference Laboratory for ASF, (EURL-ASF) Centro de Investigación en Sanidad Animal CISA-INIA, Valdeolmos 28130,
Página 1 de 9 CONTENIDO CENTRO DE INVESTIGACIÓN EN SANIDAD ANIMAL (CISA-INIA) European Union Reference Laboratory for ASF, (EURL-ASF) Centro de Investigación en Sanidad Animal CISA-INIA, Valdeolmos 28130,
Reacción en cadena de la Polimerasa (PCR)
 Explicación de TP Nº 3 Reacción en cadena de la Polimerasa (PCR) Química Biológica Patológica Bioq. Mariana L. Ferramola 2013 Definición de PCR Es la amplificación enzimática de un fragmento de interés
Explicación de TP Nº 3 Reacción en cadena de la Polimerasa (PCR) Química Biológica Patológica Bioq. Mariana L. Ferramola 2013 Definición de PCR Es la amplificación enzimática de un fragmento de interés
INTERPRETACIÓN DE GELES DE DNA DIGERIDOS CON ENZIMAS DE RESTRICCIÓN
 INTERPRETACIÓN DE GELES DE DNA DIGERIDOS CON ENZIMAS DE RESTRICCIÓN El empleo de las enzimas de restricción y los plásmidos es habitual en el laboratorio de Biología Molecular. Con este ejercicio se pretende
INTERPRETACIÓN DE GELES DE DNA DIGERIDOS CON ENZIMAS DE RESTRICCIÓN El empleo de las enzimas de restricción y los plásmidos es habitual en el laboratorio de Biología Molecular. Con este ejercicio se pretende
CUADERNO DE PRÁCTICAS GENETICA MOLECULAR HUMANA. Grado en Medicina
 DEPARTAMENTO DE BIOQUÍMICA Y BIOLOGÍA MOLECULAR III FACULTAD DE MEDICINA UNIVERSIDAD COMPLUTENSE DE MADRID CUADERNO DE PRÁCTICAS GENETICA MOLECULAR HUMANA Grado en Medicina CURSO ACADÉMICO 2014/2015 INDICE
DEPARTAMENTO DE BIOQUÍMICA Y BIOLOGÍA MOLECULAR III FACULTAD DE MEDICINA UNIVERSIDAD COMPLUTENSE DE MADRID CUADERNO DE PRÁCTICAS GENETICA MOLECULAR HUMANA Grado en Medicina CURSO ACADÉMICO 2014/2015 INDICE
Toma de Muestras Microbiológicas
 Toma de Muestras Microbiológicas MICROBIOLOGÍA CLÍNICA DIAGNÓSTICO DE ENFERMEDADES INFECCIOSAS MUESTRA AISLAMIENTO IDENTIFICACIÓN SENSIBILIDAD A ANTIMICROBIANOS Detección de anticuerpos, antígenos y ácidos
Toma de Muestras Microbiológicas MICROBIOLOGÍA CLÍNICA DIAGNÓSTICO DE ENFERMEDADES INFECCIOSAS MUESTRA AISLAMIENTO IDENTIFICACIÓN SENSIBILIDAD A ANTIMICROBIANOS Detección de anticuerpos, antígenos y ácidos
Investigando los genes FRAUDE CANINO
 FRAUDE CANINO Ahora vamos a actuar como policías científicos. No se trata de un caso humano, sino de perros. El protocolo seguido es similar al de la Huella Genética o Huella de ADN, es decir, vamos a
FRAUDE CANINO Ahora vamos a actuar como policías científicos. No se trata de un caso humano, sino de perros. El protocolo seguido es similar al de la Huella Genética o Huella de ADN, es decir, vamos a
Código: IDK-010 Ver: 1. Proteína G C825T. Sistema para la detección de la mutación C825T en el gene de la proteína G.
 C825T Sistema para la detección de la mutación C825T en el gene de la proteína G. Valdense 3616. 11700. Montevideo. Uruguay. Teléfono (598) 2 336 83 01. Fax (598) 2 336 71 60. Info@atgen.com.uy www.atgen.com.uy
C825T Sistema para la detección de la mutación C825T en el gene de la proteína G. Valdense 3616. 11700. Montevideo. Uruguay. Teléfono (598) 2 336 83 01. Fax (598) 2 336 71 60. Info@atgen.com.uy www.atgen.com.uy
MUESTREO Y DETERMINACIÓN DE LARVAS DE MEJILLÓN CEBRA
 MUESTREO Y DETERMINACIÓN DE LARVAS DE MEJILLÓN CEBRA Octubre 2006 ÍNDICE DE CONTENIDO 1. FUNDAMENTO DEL MÉTODO 2. MATERIAL NECESARIO 3. PREPARACIÓN DE LA MUESTRA 4. PROCEDIMIENTO OPERATIVO 5. IDENTIFICACIÓN
MUESTREO Y DETERMINACIÓN DE LARVAS DE MEJILLÓN CEBRA Octubre 2006 ÍNDICE DE CONTENIDO 1. FUNDAMENTO DEL MÉTODO 2. MATERIAL NECESARIO 3. PREPARACIÓN DE LA MUESTRA 4. PROCEDIMIENTO OPERATIVO 5. IDENTIFICACIÓN
TaqMan GMO Maize Quantification Kit. Part No: 4481972
 TaqMan GMO Maize Quantification Kit Part No: 4481972 1. Introducción Los organismos modificados genéticamente (OMG) se encuentran ampliamente distribuidos, siendo la soja y el maíz los vegetales que ocupan
TaqMan GMO Maize Quantification Kit Part No: 4481972 1. Introducción Los organismos modificados genéticamente (OMG) se encuentran ampliamente distribuidos, siendo la soja y el maíz los vegetales que ocupan
F-CGPEGI-CC-01/REV-00
 F-CGPEGI-CC-01/REV-00 UNIVERSIDAD AUTONOMA DE YUCATAN FACULTAD DE MEDICINA LABORATORIO DE CIENCIAS FISIOLOGICAS MANUAL DE PREPARACIÓN DE REACTIVOS RESPONSABLE DEL LABORATORIO DE CIENCIAS FISIOLOGICAS Q.
F-CGPEGI-CC-01/REV-00 UNIVERSIDAD AUTONOMA DE YUCATAN FACULTAD DE MEDICINA LABORATORIO DE CIENCIAS FISIOLOGICAS MANUAL DE PREPARACIÓN DE REACTIVOS RESPONSABLE DEL LABORATORIO DE CIENCIAS FISIOLOGICAS Q.
BIOLOGIA CELULAR Y MOLECULAR. LABORATORIO No 7: REACCION EN CADENA DE LA POLIMERASA (PCR)
 BIOLOGIA CELULAR Y MOLECULAR LABORATORIO No 7: REACCION EN CADENA DE LA POLIMERASA (PCR) 1. INTRODUCCIÓN La Reacción en Cadena de la Polimerasa (PCR) es una técnica in Vitro que imita la habilidad natural
BIOLOGIA CELULAR Y MOLECULAR LABORATORIO No 7: REACCION EN CADENA DE LA POLIMERASA (PCR) 1. INTRODUCCIÓN La Reacción en Cadena de la Polimerasa (PCR) es una técnica in Vitro que imita la habilidad natural
TÍTULO: Determinación colorimétrica de fenoles en agua por el método de la 4- aminoantipirina
 Página 1 de 6 1.- INTRODUCCIÓN Desde el punto de vista analítico el término fenol engloba este producto y sus homólogos inmediatamente superiores. El fenol se emplea como patrón y el resultado obtenido
Página 1 de 6 1.- INTRODUCCIÓN Desde el punto de vista analítico el término fenol engloba este producto y sus homólogos inmediatamente superiores. El fenol se emplea como patrón y el resultado obtenido
- Las mezclas de amplificación se presentan en formato monotest en tubos de PCR de 0.2 ó 0.5 ml, identificadas con diferentes colores.
 ! El diagnóstico de los linfomas malignos es una de las áreas que más dificultad reviste dentro de la histopatología. Si bien muchos casos se diagnostican a través de los datos histomorfológicos e inmunohistoquímicos,
! El diagnóstico de los linfomas malignos es una de las áreas que más dificultad reviste dentro de la histopatología. Si bien muchos casos se diagnostican a través de los datos histomorfológicos e inmunohistoquímicos,
DETERMINACIÓN DEL FACTOR Rh por PCR
 Ref.PCRRh DETERMINACIÓN DEL FACTOR Rh por PCR 1.OBJETIVO DEL EXPERIMENTO El objetivo de este experimento es introducir a los estudiantes en los principios y práctica de la Reacción en Cadena de la Polimerasa
Ref.PCRRh DETERMINACIÓN DEL FACTOR Rh por PCR 1.OBJETIVO DEL EXPERIMENTO El objetivo de este experimento es introducir a los estudiantes en los principios y práctica de la Reacción en Cadena de la Polimerasa
Caracteristicas del ADN. Se rompen con las siguientes condiciones -Temperaturas >90 - ph >10.5
 PCR Caracteristicas del ADN Se rompen con las siguientes condiciones -Temperaturas >90 C - ph >10.5 Baja astringencia tiene uniones parciales o imperfectas. Renaturalización Dependiendo de: -Contenido
PCR Caracteristicas del ADN Se rompen con las siguientes condiciones -Temperaturas >90 C - ph >10.5 Baja astringencia tiene uniones parciales o imperfectas. Renaturalización Dependiendo de: -Contenido
DIGESTIÓN DEL FAGO LAMBDA CON ENZIMAS DE RESTRICCIÓN
 DIGESTIÓN DEL FAGO LAMBDA CON ENZIMAS DE RESTRICCIÓN Ref.ER2 (4 PRÁCTICAS) 1. OBJETIVO DEL EXPERIMENTO El objetivo de este experimento es introducir los principios de la digestión del ADN con enzimas de
DIGESTIÓN DEL FAGO LAMBDA CON ENZIMAS DE RESTRICCIÓN Ref.ER2 (4 PRÁCTICAS) 1. OBJETIVO DEL EXPERIMENTO El objetivo de este experimento es introducir los principios de la digestión del ADN con enzimas de
PURIFICACIÓN Y DETERMINACIÓN DEL TAMAÑO DE PROTEÍNAS FLUORESCENTES VERDES Y AZULES
 PURIFICACIÓN Y DETERMINACIÓN DEL TAMAÑO DE PROTEÍNAS FLUORESCENTES VERDES Y AZULES 6 grupos de estudiantes 1. OBJETIVO DEL EXPERIMENTO En este experimento los estudiantes aprenderán a purificar parcialmente
PURIFICACIÓN Y DETERMINACIÓN DEL TAMAÑO DE PROTEÍNAS FLUORESCENTES VERDES Y AZULES 6 grupos de estudiantes 1. OBJETIVO DEL EXPERIMENTO En este experimento los estudiantes aprenderán a purificar parcialmente
TEMA 14. Métodos inmunológicos para la identificación microbiana
 TEMA 14 Métodos inmunológicos para la identificación microbiana Tema 14. Métodos inmunológicos para la identificación microbiana 1. Introducción 2. Detección de antígenos 2.1. Obtención de anticuerpos
TEMA 14 Métodos inmunológicos para la identificación microbiana Tema 14. Métodos inmunológicos para la identificación microbiana 1. Introducción 2. Detección de antígenos 2.1. Obtención de anticuerpos
Práctico: Genética bacteriana 2007.
 Práctico: Genética bacteriana 2007. Actividad integrada Departamento de Genética Departamento de Bacteriología y Virología. OBJETIVOS Objetivos generales El estudiante al terminar la actividad práctica
Práctico: Genética bacteriana 2007. Actividad integrada Departamento de Genética Departamento de Bacteriología y Virología. OBJETIVOS Objetivos generales El estudiante al terminar la actividad práctica
MICROBIOLOGÍA DE LOS ALIMENTOS 2015 INGENIERÍA EN ALIMENTOS LICENCIATURA EN BIOQUÍMICA TRABAJO PRÁCTICO N 1 REACCIÓN EN CADENA DE LA POLIMERASA (PCR)
 MICROBIOLOGÍA DE LOS ALIMENTOS 2015 INGENIERÍA EN ALIMENTOS LICENCIATURA EN BIOQUÍMICA TRABAJO PRÁCTICO N 1 REACCIÓN EN CADENA DE LA POLIMERASA (PCR) OBJETIVOS - Definir PCR, conocer los reactivos que
MICROBIOLOGÍA DE LOS ALIMENTOS 2015 INGENIERÍA EN ALIMENTOS LICENCIATURA EN BIOQUÍMICA TRABAJO PRÁCTICO N 1 REACCIÓN EN CADENA DE LA POLIMERASA (PCR) OBJETIVOS - Definir PCR, conocer los reactivos que
PROCEDIMIENTO DETERMINACIÓN DE ACIDOS GRASOS SATURADOS, MONOINSATURADOS, POLIINSATURADOS Y ACIDOS GRASOS TRANS Método Cromatografía Gaseosa (GC-FID)
 PRT-711.02-154 Página 1 de 6 1. OBJETIVO Determinar el perfil de los ácidos grasos, incluidos los isómeros de ácidos grasos trans (AGTs) en grasas y aceites de origen vegetal y animal. 2. CAMPO DE APLICACIÓN
PRT-711.02-154 Página 1 de 6 1. OBJETIVO Determinar el perfil de los ácidos grasos, incluidos los isómeros de ácidos grasos trans (AGTs) en grasas y aceites de origen vegetal y animal. 2. CAMPO DE APLICACIÓN
PRÁCTICA Nº 2 OPERACIONES COMUNES EN UN LABORATORIO
 PRÁCTICA Nº 2 OPERACIONES COMUNES EN UN LABORATORIO OBJETIVO Utilizar el material de laboratorio en las operaciones más comunes realizadas en un laboratorio de química. I. ASPECTOS TEÓRICOS Una vez conocido
PRÁCTICA Nº 2 OPERACIONES COMUNES EN UN LABORATORIO OBJETIVO Utilizar el material de laboratorio en las operaciones más comunes realizadas en un laboratorio de química. I. ASPECTOS TEÓRICOS Una vez conocido
Documentos de Referencia para Diagnóstico de Semilla de Papa de Canadá
 SECRETARIA DE AGRICULTURA, GANADERÍA. DESARROLLO RURAL, PESCA Y ALIMENTACIÓN Dirección General de Sanidad Vegetal Centro Nacional de Referencia Fitosanitaria Subdirección de Diagnóstico Fitosanitario Documentos
SECRETARIA DE AGRICULTURA, GANADERÍA. DESARROLLO RURAL, PESCA Y ALIMENTACIÓN Dirección General de Sanidad Vegetal Centro Nacional de Referencia Fitosanitaria Subdirección de Diagnóstico Fitosanitario Documentos
Proyecto de Fin de Cursos
 Universidad de la República Oriental del Uruguay Proyecto de Fin de Cursos ELECTROFORESIS EN GEL DE MOLÉCULAS DE ADN Noviembre de 2006 Carolina Etchart C.I. 3.757.708-8 Marcelo Lavagna C.I. 3.508.715-8
Universidad de la República Oriental del Uruguay Proyecto de Fin de Cursos ELECTROFORESIS EN GEL DE MOLÉCULAS DE ADN Noviembre de 2006 Carolina Etchart C.I. 3.757.708-8 Marcelo Lavagna C.I. 3.508.715-8
Protocolos de secuenciación de ADN
 1 Protocolos de secuenciación de ADN Introducción El método de secuenciación utilizado aquí es el desarrollado por Sanger en 1975. Este consiste en la incorporación de didesixinucleótidos marcados fluorescentemente
1 Protocolos de secuenciación de ADN Introducción El método de secuenciación utilizado aquí es el desarrollado por Sanger en 1975. Este consiste en la incorporación de didesixinucleótidos marcados fluorescentemente
Protocolo de laboratorio para purificación manual de ADN a partir de una muestra de 0,5 ml
 Protocolo de laboratorio para purificación manual de ADN a partir de una muestra de 0,5 ml Para la purificación de ADN genómico de todos los kits de colección Oragene y ORAcollect. Visite nuestro sitio
Protocolo de laboratorio para purificación manual de ADN a partir de una muestra de 0,5 ml Para la purificación de ADN genómico de todos los kits de colección Oragene y ORAcollect. Visite nuestro sitio
La Patología a Molecular y el Control de Calidad
 UNIDAD DIDÁCTICA 7: LOS PROCESOS EN ANATOMÍA PATOLÓGICA La Patología a Molecular y el Control de Calidad Asunción n Olmo Sevilla Master Diagnóstica S. L. Patología Molecular: Patología del futuro X Personal:
UNIDAD DIDÁCTICA 7: LOS PROCESOS EN ANATOMÍA PATOLÓGICA La Patología a Molecular y el Control de Calidad Asunción n Olmo Sevilla Master Diagnóstica S. L. Patología Molecular: Patología del futuro X Personal:
INSTRUCTIVO DETERMINACIÓN DE GRUPOS A,B,O Y RH-D
 1. OBJETIVO: Desarrollar la clasificación de Grupo y Rh a los usuarios del Hospital Regional de Arica Dr. Juan Noé Crevani, de acuerdo con los antígenos y anticuerpos presentes en la sangre, esto con el
1. OBJETIVO: Desarrollar la clasificación de Grupo y Rh a los usuarios del Hospital Regional de Arica Dr. Juan Noé Crevani, de acuerdo con los antígenos y anticuerpos presentes en la sangre, esto con el
PRACTICA # 1 DETERMINACION DE FOSFORO OLSEL Y BRAY P-1
 PRACTICA # 1 DETERMINACION DE FOSFORO OLSEL Y BRAY P-1 INTRODUCCIÓN El fósforo es un elemento esencial para la vida. Las plantas lo necesitan para crecer y desarrollar su potencial genético. Lamentablemente,
PRACTICA # 1 DETERMINACION DE FOSFORO OLSEL Y BRAY P-1 INTRODUCCIÓN El fósforo es un elemento esencial para la vida. Las plantas lo necesitan para crecer y desarrollar su potencial genético. Lamentablemente,
TRBAJO PRÁCTICO N 5: ph. Objetivo: Determinar el ph de soluciones ácidas y básicas de concentraciones diferentes.
 QUÍMICA GENERAL Y TECNOLÓGICA 2010 TRBAJO PRÁCTICO N 5: ph Objetivo: Determinar el ph de soluciones ácidas y básicas de concentraciones diferentes. Fundamentos Teóricos: La mayoría de las reacciones químicas
QUÍMICA GENERAL Y TECNOLÓGICA 2010 TRBAJO PRÁCTICO N 5: ph Objetivo: Determinar el ph de soluciones ácidas y básicas de concentraciones diferentes. Fundamentos Teóricos: La mayoría de las reacciones químicas
TRABAJO PRÁCTICO Nº 5: ÁCIDOS NUCLEICOS. DOCENTES: Dr. Andrés Ciochinni, Dra. Gabriela Niemirowicz. DESCRIPCIÓN DE LOS MÉTODOS A UTILIZAR
 TRABAJO PRÁCTICO Nº 5: ÁCIDOS NUCLEICOS DOCENTES: Dr. Andrés Ciochinni, Dra. Gabriela Niemirowicz. DESCRIPCIÓN DE LOS MÉTODOS A UTILIZAR Purificación de ácido desoxiribonucleico (ADN). El ADN es un polímero
TRABAJO PRÁCTICO Nº 5: ÁCIDOS NUCLEICOS DOCENTES: Dr. Andrés Ciochinni, Dra. Gabriela Niemirowicz. DESCRIPCIÓN DE LOS MÉTODOS A UTILIZAR Purificación de ácido desoxiribonucleico (ADN). El ADN es un polímero
TÉCNICAS GENÓMICAS. 2) Cuantificación del número de virus presentes en muestras de sangre o suero: carga vírica
 TÉCNICAS GENÓMICAS Utilidad/Objetivos: 1) Detección de microorganismos directamente en muestras clínicas identificando un fragmento específico del genoma del microorganismo concreto 2) Cuantificación del
TÉCNICAS GENÓMICAS Utilidad/Objetivos: 1) Detección de microorganismos directamente en muestras clínicas identificando un fragmento específico del genoma del microorganismo concreto 2) Cuantificación del
