ES A1 ESPAÑA 11. Número de publicación: Número de solicitud:
|
|
|
- Ana Belmonte Lagos
- hace 6 años
- Vistas:
Transcripción
1 19 OFICINA ESPAÑOLA DE PATENTES Y MARCAS ESPAÑA Número de publicación: Número de solicitud: Int. CI.: C12N 5/07 ( ) A01N 1/02 ( ) G01N 33/18 ( ) 12 SOLICITUD DE PATENTE A1 22 Fecha de presentación: 71 Solicitantes: Fecha de publicación de la solicitud: UNIVERSIDADE DE VIGO (100.0%) Campus Universitario s/n Vigo (Pontevedra) ES 72 Inventor/es: BEIRAS GARCÍA-SABELL, Ricardo ; BELLAS BEREIJO, Juan y PAREDES ROSENDO, Estefanía 54 Título: Procedimiento para la criopreservación de embriones de erizo de mar y bioensayo asociado 57 Resumen: Procedimiento para la criopreservación de embriones de erizo de mar y bioensayo asociado. El procedimiento se basa en el uso de un protocolo de criopreservación para blástulas de 8 horas de erizo de mar para poder almacenar en nitrógeno líquido embriones para su uso fuera de la temporada de reproducción natural de esta especie. Se ha desarrollado además, un bioensayo ecotoxicológico con embriones de erizo de mar criopreservados para la evaluación de la contaminación marina. El procedimiento objeto de esta patente permite el uso durante todo el año de embriones de erizo de mar tanto en bioensayos ecotoxicológicos como con aplicaciones en la industria de la acuicultura. ES A1
2 DESCRIPCIÓN PROCEDIMIENTO PARA LA CRIOPRESERVACION DE EMBRIONES DE ERIZO DE MAR Y BIOENSAYO ASOCIADO Sector de la tecnica El objeto de la presente invencion se refiere a un procedimiento de criopreservacion de 5 embriones de erizo de mar (Paracen tro tus lividus ) y su aplicacion en un bioensayo. El procedimiento se basa en el uso de un protocolo de criopreservacion especificamente disefiado para erizo de mar y este tipo celular (blastula de 8 horas) para poder almacenar en nitrogen liquido embriones para su uso fue de la temporada de reproduccion natural de esta especie. Protocolo de criopreservacion de embriones de erizo de mar con 10 aplicaciones en investigacion, acuicultura y ecotoxicologia. Desarrollo de un bioensayo con blastulas criopreservadas de erizo de mar para la evaluacion de la contaminacion marina. Estado de la tecnica Una gran variedad de organismos han sido criopreservados para su uso en biologia 15 experimental, medicina, acuicultura e investigacion. En particular, la criopreservacion de esperma y larvas de organismos marinos ha resultado de gran utilidad para el desarrollo de la acuicultura en los Altimos afios. Sin embargo, la mayor parte de estos estudios se han realizado con peces, y en menor medida con bivalvos como la ostra y el mejillon (Sansone et a l. 2002, Zhang et al. 2005, Adams e t a l. 2004, Di Mateo e t a l , Adams e t a l. 2011), mientras que solo se ha publicado informacion fragmentaria sobre erizos de mar endemicos de la zona del Pacifico (Asahina y Takahashi 1979 ; Gaknova e t a l y Naidenko et a l. 1991,1998; Barros e t a l y Adams e t a l. 2006). Por otra parte, la aplicacion de estas tecnicas se ha basado fundamentalmente en la criopreservacion de esperma, y en menor grado de larvas, ya sea por la mayor 25 sencillez del procedimiento, o por la mayor resistencia de dichos estados de desarrollo. Mientras que, debido a la dificultad del proceso de criopreservacion de estadios tempranos de desarrollo por su gran sensibilidad, la bibliografia publicada sobre el exito de criopreservacion de embriones tempranos de erizo de mar (desde ovocitos recien fertilizados a gastrulas) es minima (Naidenko e t a l. 1991, Paredes y Bellas 2009, Bellas 30 y Paredes 2011), y es precisamente la sensibilidad de estos estadios tempranos lo que 2
3 los convierte en los estados de desarrollo mas sensibles a la contaminacion y por tanto de interes en estudios ambientales. En acuicultura la criopreservacion de embriones tempranos (de estructura mas simple) supondria una alternativa a la criopreservacion de estadios larvarios mas complejos que 5 suelen presentar dafios/anormalidades en sus estructuras tras el proceso de criopreservacion. El desarrollo de estos protocolos de criopreservacion es especifico para las diferentes clases de organismos (radicalmente diferente para mamiferos, peces o invertebrados) y dentro de un mismo tipo de organismo es especifico para cada especie y cada tipo de estado de desarrollo. 10 No existen trabajos que hayan abordado la criopreservacion de gametos, embriones o larvas del erizo Paracentro tus lividus, mas and de aquellos publicados por nuestro grupo (Paredes y BeIlas, 2009, BeIlas y Paredes, 2011). Dichos estudios han abordado de forma preliminar alguna de las tareas iniciales en los estudios de criopreservacion, como el establecimiento de concentraciones adecuadas de agentes crioprotectores y de 15 sus combinaciones para diferentes estados embrionarios tempranos (Paredes y Bellas, 2009), y el estudio de factores que afectan al proceso de criopreservacion, como las tasas de congelacion, el proceso de 'seeding', o la inmersion en nitrogen liquido (Bellas y Paredes, 2011). Sin embargo, nunca ha sido publicado el proceso completo de criopreservacion para el que se quiere obtener esta patente. 20 El erizo de mar Paracen tro tus lividus (Lamarck, 1816), es un erizo regular de gran tamafio (hasta 7 cm de diametro), que presenta una distribucion amplia a lo largo del Mar Mediterraneo, las costas atlanticas europeas, noroeste de Rusia, Islandia, Marruecos y las Islas canarias (Hayward y Ryland, 1990; Boudouresque y Verlaque, 2007). Se trata de un erizo comestible de gran relevancia economica, pues es explotado 25 en algunos paises (p.ej. Esparia, Francia, Italia, Irlanda, Portugal, Croacia) por sus gonadas comestibles, que son muy apreciadas en gastronomia (Boudouresque y Verlaque, 2007). Ademas, suele desempefiar un importante papel ecologic en el funcionamiento, en la dinamica y en la estructura de los asentamientos bentonicos (Hayward y Ryland, 1990; Boudouresque y Verlaque, 2007). 30 Los bioensayos embrio-larvarios con invertebrados marinos han sido utilizados de rutina para la evaluacion y seguimiento de la contaminacion marina en todo el mundo 3
4 durante las Oltimas acacias (e.g. His e t a l. 1999, Kobayashi 1995, Beiras e t a l. 2003, Bellas 2008a, Duran and Beiras 2010), consisten en la exposicion de un grupo representativo de organismo a un rango de concentraciones de un compuesto quimico y registrar/cuantificar los efectos a lo largo de cierto periodo de tiempo. (Hoffman et a l , Wright and Welbourn 2002). La aplicacion de estas tecnicas biologicas con exit a nivel mundial ha permitido reconocer no solo sus beneficios si no tambien problemas asociados que estan limitando la utilizacion de estas tecnicas: la estacionalidad de la reproducci6n de las especies test produce una corta disponibilidad temporal de material biologic de calidad para los bioensayos (His e t a l. 1999). El diserio de un bioensayo 10 con embriones criopreservados, que pueden mantenerse almacenados en criobancos a lo largo del alio, asegura la accesibilidad a material biologic de calidad de forma continua. No tenemos conocimiento sobre ninguna patente sobre la criopreservacion del erizo de mar P. lividus, ni de ninguna otra especie de erizo, ni tampoco de la aplicacion de 15 embriones criopreservados de esta especie a tecnicas ecotoxicologicas o en acuicultura. Descripcion de la invencion El procedimiento de la presente invencion de criopreservacion de embriones tempranos (de estructura mas simple) supone una alternativa a la criopreservacion de estadios 20 larvarios mas complejos que suelen presentar datios/anormalidades en sus estructuras tras el proceso de criopreservacion. El uso de embriones tempranos criopreservados es una opci6n \Tali& a la criopreservacion de los gametos por separado, ya que aunque la criopreservacion de esperma se ha logrado satisfactoriamente, la criopreservacion de ovocitos aim permanece sin desarrollar. La posibilidad de la conservacion de material 25 biologic de calidad fuera de la temporada de reproduccion natural de una especie abre tanto la posibilidad de ampliar su uso a lo largo de todo el alio como la posibilidad de su uso en lugares que anteriormente no tenian acceso a este material biologic por encontrarse lejos de la costa o por no tener las instalaciones necesarias para el mantenimiento de los organismos adultos. 4
5 El proceso cuya patente se aborda aqui esta desarrollado en su totalidad, desde la obtencion de las blastulas de erizo de mar, la composicion y concentracion de crioprotector, la metodologia de adicion del crioprotector, el proceso de criopreservacion, temperatura de "seeding", hasta el proceso de descongelacion y 5 estudio de viabilidad. A pesar de que el desarrollo de un protocolo de criopreservacion es especifico de una especie y de un tipo celular concreto, hay estudios (Paredes et a l. 2013) que sugieren que podria darse la posibilidad que este protocolo disefiado para blastulas de P. lividus pudiese utilizarse para tipos celulares similares (blastulas y gastrulas) de otros erizos de mar (eg. Strongylocen tro tus spp., Te trap igus spp., 10 Evech inus spp. Hem icen tro tus spp. ). Se trata de un procedimiento novedoso en esta especie, con una amplia aplicacion en investigacion (reproducci6n, ecotoxicologia, criopreservacion, acuicultura) como industrial por su sinergia con otras tecnologias y aplicaciones en acuicultura y mon itoring medioambiental. El procedimiento de un bioensayo con embriones criopreservados de erizo de mar 15 mediante el protocolo de criopreservacion previamente descrito, que se aborda aqui es un alternativa at bioensayo embrio-larvario de erizo de mar estandar que ya es ampliamente utilizado para la evaluacion y seguimiento de la contaminacion marina, pero que esta sujeto a restricciones temporales debido a la estacionalidad de la reproducci6n de los organismos. 20 El bioensayo consiste en descongelar blastulas criopreservadas de erizo y una vez que se han eliminado los crioprotectores repartirlas en viales con diferentes concentraciones de un compuesto quimico. Tras un periodo de incubacion, el contenido de los viales se fija con formol al 40% para medir la respuesta a las dosis de contaminante en las larvas resultantes. Se calcula la Concentracion efectiva 50 (CE5o) como la concentracion que 25 induce una respuesta del 50% en los organismos expuestos. El uso de blastulas criopreservadas de erizo permite el acceso a material biologico sin restricciones estacionales y es mas sensible que el bioensayo embrio-larvario estandar to cual nos permite detectar concentraciones mas bajas de contaminantes. 5
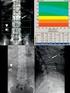
6 Breve descripcion de las figuras Para facilitar la comprension de la invencion, se anexan las siguientes figuras representativas: Tabla 1. Descripcion de los volamenes de adicion y retirada de los agentes 5 crioprotectores en 15 y 12 pasos equimolares respectivamente (con cada paso de adici6n la concentraci6n de crioprotector en los viales se incrementa en 0.1M, mientras que con cada paso de dilucion la concentraci6n de crioprotectores de la muestra se reduce en 0.125M). Figura 1. Crecimiento de larvas p lu teus de 4 brazos (96 horas de incubacion a 20 C sin 10 alimento) a partir de embriones criopreservados en diferentes meses del alio. Figura 2. Porcentaje de asentamiento larvario de larvas incubadas durante 20 dias procedentes de embriones criopreservados comparados con controles frescos para 2 parejas de erizos diferentes. Figura 3. Inhibicion del crecimiento larvario como resultado del bioensayo de toxicidad 15 del Plomo con embriones criopreservados (linea negra) en comparacion con el bioensayo embrio-larvario estandar (linea gris) para una misma pareja de erizo de mar, n= 35. Descripeion detallada de la invencion Como un ejemplo de realizacion preferida se describe el procedimiento de 20 criopreservacion de embriones de erizo de mar de Paracen tro tus lividus : 1.- Se obtienen los gametos directamente de las gonadas de una pareja de erizos de mar en epoca reproductiva con unas pipetas Se realiza una fertilizacion in vitro aliadiendo unos microlitros de esperma movil a una solucion de ovocitos en una probeta Se agita cuidadosamente unos segundos para favorecer la fertilizacion. Las blastulas se obtienen 25 por la incubacion de los ovocitos fertilizados durante 8 horas en oscuridad a la temperatura de 20 C. 2.- Elaboracion de los agentes crioprotectores: La solucion crioprotectora utilizada ha sido especificamente diseriada mediante pruebas de toxicidad y eficiencia crioprotectora 6
7 para este tipo celular y especie. La solucion crioprotectora consta de Dimetil sulfoxido 1.5M y Trealosa 0.04M de concentracion final en viales de congelacion preparados en una a disolucion al doble de concentracion final deseada en agua de mar artificial (ASW) a temperatura ambiente ( 19 ±1 C) Metodologia de adicion de los agentes crioprotectores: Se extraen las blastulas de los tanques utilizados para el cultivo usando filtracion en framed con filtro con maya de 20 micrometros. Se transfiere 1 ml de suspension de blastulas (de densidad deseada) a los viales de criopreservacion (volumen vial 2 ml). Se afiaden los agentes crioprotectores en 15 pasos equimolares (cada adici6n incrementa en 0.1M la concentracion en los 10 viales) de 1 minuto (volumenes detallados en tabla 1). Una vez finalizada la adicion de los agentes crioprotectores los viales estan listos para iniciar la criopreservacion (Volumen final son 2 ml, dilucion 1:1). Tabla 1. Descripcion de los volumenes de adicion y retirada de los agentes 15 crioprotectores en 15 y 12 pasos equimolares respectivamente (con cada paso la concentracion de crioprotector en los viales se incrementa en 0.1 M, mientras que con cada paso de dilucion la concentraci6n de crioprotectores en la muestra se reduce en M). Paso Ad ic ion de crioprotec tores ( ti L de soluc ion crioprotec tora ) 3 5 D i luc ion de crioprotectores OI L de ASW) Tiempo total 15 minutos 12 minutos 7
8 4.- Protocolo de criopreservacion: Los viales se introducen en una criocamara programable estilo Cryo logic Pty. L td. Australia y se sigue el protocolo de criopreservacion. La rampa de congelacion se programa para comenzar con una pausa a 5 4 C durante 2 min, enfriamiento a una tasa de 1 C min' hasta -12 C. En ese punto se hace el "seeding" durante una pausa de 2 min seguida de una tasa de congelacion de 1 C min' hasta alcanzar los 80 C. Tras una pausa final de 2 minutos los viales se sacan rapidamente de la criocamara y se introducen en nitrogeno liquido. 5.- El "seeding" consta de un golpecito seco con un objeto metalico y fi-io que se da a 10 los viales cuando alcanzan los -12 C para favorecer la congelacion de la solucion crioprotectora que contiene los embriones, en todos los viales en el misma temperatura. Este paso tiene que hacerse con rapidez para evitar fluctuaciones en la temperatura de los viales. 5.- El almacenamiento de los viales se hace en nitrogeno liquido a -196 C La descongelacion de los viales se hace por inmersion en un balm de agua a 17 ± 1 C (1.5-2 minutos). Una vez descongelada la solucion se transfiere a unos viales de 20 ml donde se procede a la dilucion de los crioprotectores. 7.- Retirada de los agentes crioprotectores: la dilucion de los crioprotectores se realiza con la adicion equimolar en 12 pasos de ASW (durante la dilucion cada paso reduce la 20 concentracion de crioprotectores en la muestra en M) a temperatura ambiente 19 ± 1 C (tabla 1). Una vez terminada la dilucion de los crioprotectores se filtran los embriones descongelados con una malla de 20 gm con ASW limpia y se concentran en una probeta con ASW para su uso. Resultados del proceso de criopreservacion 25 Hemos desarrollado un protocolo completo de criopreservacion de embriones de erizo de mar con una alta supervivencia que permite obtener un porcentaje alto de larvas normales que aunque pasan por un period de latencia post descongelacion, por lo cual su desamillo se ye un poco ralentizado, que dan lugar a larvas Ech inop lu teus de vida normal que pueden asentarse y producir juveniles. 8
9 Los embriones de erizo de mar criopreservados pasan por un proceso de latencia post descongelacion en la que el crecimiento es menor del 20% en las primeras 48 horas, alcanzando el estado de larva pluteus de 4 brazos a las 96 horas. El tamalio de la larva en ese momento sera normalmente del 50% comparado con 5 larvas de erizo no congeladas de 96 horas. El tamario larvario es del 20% el tamario de controles frescos a las 48 horas y mayor del 50% a las 96 horas. El 70% de las larvas criopreservadas sobreviven a un cultivo larvario completo de 20 dias de duraci6n en comparaci6n con controles. 10 El asentamiento medio de las larvas para producir juveniles es del 25% en comparacion con los controles. Uso de blastulas de erizo criopreservadas como bioensayo. Este bioensayo comprende las siguientes etapas: Una vez descongelados las blastulas de erizo de mar y eliminados los crioprotectores presentes por dilucion en 12 pasos equimolares (con cada paso de dilucion la concentracion de crioprotectores en la muestra se reduce en M). (tabla 1). 2.- Los embriones se filtran y se transfieren a viales que contienen las soluciones experimentales, en este ejemplo son de plomo, en una densidad de 80 embriones ml-i y 20 son incubados durante 96 horas hasta estado de larva pluteus de 4 brazos. 3.-Los viales se fijan con dos gotas de formol al 40% y se mide la longitud maxima de 35 larvas por vial como respuesta del bioensayo. En la figura 3, se muestran los resultados del bioensayo con embriones criopreservados (linea negra) en comparacion con el bioensayo embrio-larvario estandar (linea gris) para erizo de mar (Saco-Alvarez 25 et a l. 2010). 9
10 Resultados del bioensayo Los resultados indican que con el bioensayo de embriones criopreservados mediante el protocolo descrito previamente, se obtienen unas CE50 menores que con el bioensayo estandar (81 ug L-1, 425 ug L-', respectivamente), este bioensayo mas sensible puede 5 ser de mucha utilidad para la deteccion de concentraciones mas bajas de contaminantes en el medio ambiente (cuanto mas bajas depende del compuesto). Una vez conocida la comparaci6n entre ambos bioensayos se podran utilizar embriones criopreservados para la evaluacion de la contaminacion marina a lo largo de todo el alio con independencia de la temporada de reproduccion de la especie, lo cual habia representado hasta ahora 10 un handicap para esta herramienta. Este bioensayo con blastulas criopreservadas se ha probado utilizando, metales pesados, compuestos organicos y con elutriados de sedimentos portuarios. Aunque el ejemplo es con el plomo, este bioensayo es potencialmente utilizable con una amplisima gama de compuestos quimicos al igual que el bioensayo embrio-larvario estandar de erizo de 15 mar. 10
11 REIVINDICACIONES 1. Protocolo de criopreservacion para embriones de erizo de mar que comprende las siguientes etapas: a. Obtencion de embriones y proceso de fertilizacion e incubacion para 5 la obtencion de blastulas. b. Adicion de un agente crioprotector a traves de 15 pasos equimolares, de manera que cada adicion incrementa en 0,1 la concentracion en los viales, en una solucion crioprotectora diluida en agua de mar C. Criopreservacion utilizando rampas de congelacion incluyendo una 10 etapa de "seeding". d. Descongelacion y eliminacion de la solucion crioprotectora en 12 pasos equimolares en agua de mar. 2. Protocolo de criopreservacion para embriones de erizo de mar segun reivindicacion 1, caracterizado por: 15 a. Obtencion de blastulas segan la etapa a) se realiza por incubacion de ovocitos fertilizados durante 8 horas, en oscuridad, a 20 C. b. La solucion crioprotectora utilizada en la etapa b) esta compuesta por dimethilsulfoxido 1.5M y trealosa 0.04M (final) en agua de mar, preparada a doble concentraci6n de la final deseada. 20 c. La adici6n equimolar de la solucion crioprotectora segan la etapa b) se realiza utilizando una solucion a doble concentracion en pasos equimolares de 1 minuto, de manera que cada adicion incrementa en 0,1 la concentracion en los viales (dilucion final 1:1) a la temperatura 19 ±1 C. 25 d. Aplicar rampa de congelacion incluido "seeding segnn la etapa c)" primera rampa se inicia con pausa a 4 C durante 2 min, enfriamiento a una tasa de 1 C min-1 hasta la temperatura de "seeding" de -12 C con pausa de 2 minutos. A continuacion se alcanza la temperatura final de criopreservacion de -80 C enfriando a 1 C min-1. Tras pausa 30 final de 2 minutos los viales se retiran de la criocamara y se introducen en nitrogen liquido. e. Descongelacion de los viales segun la etapa d) por inmersi6n en bail de agua a 17 ± 1 C (1.5-2 minutos). 11
12 f. Retirada de los crioprotectores segnn etapa d) por dilucion total con agua de mar en pasos equimolares de 1 minuto. 3. Procedimiento segan reivindicaciones 1 y 2 para la criopreservacion de embriones de erizo de mar, preferentemente Paracen tro tus lividus Procedimiento segian reivindicaciones 1 y 2 aplicable para criopreservacion de embriones de otras especies de erizo de mar como Strongylocen tro tus spp., Tetrap igus spp., Evech inus spp. Hem icen tro tus spp.. 5. Bioensayo ecotoxicologico para evaluacion de la contaminacion marina con blastulas criopreservadas de erizo de mar siguiendo las reivindicaciones 1 y 10 2,que comprende las siguientes etapas: a. Descongelacion de embriones criopreservados y eliminacion del agente crioprotector en agua de mar en 12 pasos equimolares. b. Incubacion de embriones hasta estado de larva pluteus de 4 brazos en viales que contienen las soluciones experimentales de contaminantes 15 en una densidad de 80 embriones ml-1. c. Medir la respuesta a las dosis de contaminante mediante calculo de la concentracion efectiva 50 (CE50) que induce una respuesta del 50% en los organismos expuestos. 6. Bioensayo ecotoxicologico para evaluacion de la contaminacion marina con 20 blastulas criopreservadas de erizo que comprende las siguientes etapas descrito segnn reivindicacion 5, caracterizado por las siguientes etapas: a. Descongelacion segdn la etapa a) de los viales por immersion en bail de agua a 17 ± 1 C durante un intervalo minutos b. Retirada del agente crioprotector segnn etapa a) por dilucion con 25 agua de mar (concentracion) en pasos equimolares de 1 minuto. c. Incubacion de embriones segim etapa c) durante 96 horas a 20 C en oscuridad. d. Bioensayo segim etapa c) fijando los viales con dos gotas de formol al 40% y medir respuesta a la longitud maxima de 35 larvas por vial Uso de bioensayo segim reivindicaciones 5-6, para la evaluacion de toxicidad de compuestos inorganicos, organicos y elutriados en matrices de agua de mar. 8. Uso de un procedimiento segnn las reivindicaciones 1 y 2 para la aplicacion de embriones criopreservados en acuicultura. 12
13 13
14 14
15 OFICINA ESPAÑOLA DE PATENTES Y MARCAS ESPAÑA 21 N.º solicitud: Fecha de presentación de la solicitud: Fecha de prioridad: INFORME SOBRE EL ESTADO DE LA TECNICA 51 Int. Cl. : Ver Hoja Adicional DOCUMENTOS RELEVANTES Categoría 56 Documentos citados Reivindicaciones afectadas X A A A A BELLAS, J y PAREDES, E. Advances in the cryopreservation of sea-urchin embryos: Potential application in marine quality assessment. Cryobiology, 2011, vol. 62, páginas ODINTSOVA, N. et al. Cryopreservation of primary cell cultures of marine invertebrates. Cryoletters 2001, vol. 22, líneas ADAMS S. et al. The potential for cryopreserving larvae of the sea urchin, Evechinus chloroticus. Cryobiology, 2006, vol. 52, páginas GARMENDIA J.M. et al. Protocolo del test de toxicidad de sedimentos marinos con larvas de erizo de mar Paracentrotus lividus (Lamarck, 1816). Revista de Investigación Marina, 2009, vol. 11, página RU C1 (GRITSENKO A M) , Resumen de la base de datos EPODOC. Recuperado de EPOQUE [en línea] [recuperado el ] 1-8 1,2,4 1,2, Categoría de los documentos citados X: de particular relevancia Y: de particular relevancia combinado con otro/s de la misma categoría A: refleja el estado de la técnica O: referido a divulgación no escrita P: publicado entre la fecha de prioridad y la de presentación de la solicitud E: documento anterior, pero publicado después de la fecha de presentación de la solicitud El presente informe ha sido realizado para todas las reivindicaciones para las reivindicaciones nº: Fecha de realización del informe Examinador A. I. Polo Diez Página 1/5
16 INFORME DEL ESTADO DE LA TÉCNICA Nº de solicitud: CLASIFICACIÓN OBJETO DE LA SOLICITUD C12N5/07 ( ) A01N1/02 ( ) G01N33/18 ( ) Documentación mínima buscada (sistema de clasificación seguido de los símbolos de clasificación) C12N, A01N, G01N Bases de datos electrónicas consultadas durante la búsqueda (nombre de la base de datos y, si es posible, términos de búsqueda utilizados) INVENES, EPODOC, WPI, MEDLINE, BIOSIS, HCAPLUS Informe del Estado de la Técnica Página 2/5
17 OPINIÓN ESCRITA Nº de solicitud: Fecha de Realización de la Opinión Escrita: Declaración Novedad (Art. 6.1 LP 11/1986) Reivindicaciones 2, 4-6, 8 SI Reivindicaciones 1, 3, 7 NO Actividad inventiva (Art. 8.1 LP11/1986) Reivindicaciones SI Reivindicaciones 1-8 NO Se considera que la solicitud cumple con el requisito de aplicación industrial. Este requisito fue evaluado durante la fase de examen formal y técnico de la solicitud (Artículo 31.2 Ley 11/1986). Base de la Opinión.- La presente opinión se ha realizado sobre la base de la solicitud de patente tal y como se publica. Informe del Estado de la Técnica Página 3/5
18 OPINIÓN ESCRITA Nº de solicitud: Documentos considerados.- A continuación se relacionan los documentos pertenecientes al estado de la técnica tomados en consideración para la realización de esta opinión. Documento Número Publicación o Identificación Fecha Publicación D01 BELLAS, J y PAREDES, E Declaración motivada según los artículos 29.6 y 29.7 del Reglamento de ejecución de la Ley 11/1986, de 20 de marzo, de Patentes sobre la novedad y la actividad inventiva; citas y explicaciones en apoyo de esta declaración El objeto de la invención, según la primera reivindicación, es un procedimiento de criopreservación para embriones de erizo de mar que comprende las etapas de: a) Fertilización e incubación hasta la obtención de blástulas b) Adición de agentes crioprotectores en 15 pasos equimolares, con una solución crioprotectora en agua de mar c) Criopreservación utilizando rampas de congelación e incluyendo una etapa de seeding d) Descongelación y eliminación de la solución crioprotectora en 12 pasos equimolares. Las reivindicaciones 2 a 4 aportan detalles del procedimiento como los agentes crioprotectores utilizados, los tiempos de cada una de las etapas, etc. También es objeto de la invención el uso del procedimiento anterior para la aplicación a embriones criopreservados en acuicultura (reivindicación 8), un bioensayo ecotoxicológico en el que se utilizan las blástulas criopreservadas por el método anterior (reivindicaciones 5 y 6) y el uso del bioensayo para la evaluación de la toxicidad de compuestos (reivindicación 7). Novedad y actividad inventiva (art. 6.1 y 8.1 de L.P.) El documento D01 es un estudio para determinar las mejores condiciones de criopreservación para embriones de erizos de mar de la especie Paracentrotus lividus. El procedimiento más adecuado incluye: a) Obtención de los gametos, fertilización e incubación durante 7 horas para obtener las blástulas b) Introducción de las blástulas en viales de 2 ml con 1 ml de agua marina y adición de dimetilsufóxido (1,5 M) y trehalosa (0,04 M) como agentes crioprotectores. Los crioprotectores se añaden en 15 pasos equimolares. c) Mantenimiento a 4ºC durante 2 minutos y congelación a una razón de -1ºC/min hasta -12ºC. d) Inclusión de una etapa de seeding (2 minutos) e) Congelación hasta -80ºC a una velocidad de entre -1ºC/min. f) Introducción de las bástulas en nitrógeno líquido. La descongelación de las blástulas se realiza en baño de agua a 16ºC y eliminando la solución crioprotectora en 12 pasos equimolares con agua de mar. Las blástulas así tratadas se utilizan en bioensayos de contaminación, en los que se mide la longitud alcanzadas por las larvas pluteus de 4 brazos obtenidas a partir de las blástulas en 96 horas. Para ello se fijan las larvas con un 40% de formol y se mide la longitud de 35 de ellas. El procedimiento descrito en D01 es igual al que se define en las reivindicaciones 1, 3 y 7, por lo que estas reivindicaciones no son nuevas respecto al documento. Las reivindicaciones dependientes 2, 4-6, y 8 son nuevas pero no cumplen el requisito de actividad inventiva. La reivindicación 2, que se refiere al procedimiento de criopreservación de las blástulas, incluye pequeñas diferencias en cuanto a tiempos y temperaturas respecto al procedimiento descrito en D01. Sin embargo, dichas diferencias no aportan ningún efecto técnico a la invención, tratándose de meros ajustes del procedimiento descrito en D01, que un experto en la materia llevaría a cabo sin ejercer actividad inventiva. Informe del Estado de la Técnica Página 4/5
19 OPINIÓN ESCRITA Nº de solicitud: Las reivindicaciones 4 y 8, se refieren a posibilidades de llevar a cabo el procedimiento de criopreservación en otras especies de erizos y de utilizar los erizos criopreservados en acuicultura. En ausencia de ejemplos en la descripción relativos a estos procedimientos o usos, se considera que suponen una mera generalización dentro de las posibles aplicaciones y usos del procedimiento y carentes, por tanto, de actividad inventiva. En cuanto a las reivindicaciones 5 y 6 relativas al bioensayo para evaluar contaminación marina utilizando las blástulas criopreservadas, se considera que tampoco tienen actividad inventiva respecto a D01. El procedimiento para llevar a cabo el bioensayo ya estaba divulgado en esencia en D01 donde se aconsejaba extenderlo a 96 horas en lugar de 48 cuando se utilizan blástulas criopresenvadas y utilizar la longitud de las 35 primera larvas como parámetro indicador de la respuesta al contaminante. Aunque en D01 no se mencionan algunos detalles como la densidad de embriones utilizada en el bioensayo y el cálculo de la concentración efectiva EC 50, se considera que dichos detalles serían evidentes para un experto en la materia, que conociendo las enseñanzas de D01 tuviese que poner a punto el bioensayo divulgado en ese documento. Por tanto, en resumen, ninguna de las reivindicaciones 2, 4-6, y 8 cumplen el requisito de actividad inventiva a la vista de D01. Informe del Estado de la Técnica Página 5/5
ES R1 ESPAÑA 11. Número de publicación: Número de solicitud: B60K 15/04 ( ) B60K 15/05 ( )
 19 OFICIN ESPÑOL DE PTENTES Y MRCS ESPÑ 11 21 Número de publicación: 2 510 065 Número de solicitud: 201330552 51 Int. CI.: B60K 15/04 (2006.01) B60K 15/05 (2006.01) 12 INFORME SOBRE EL ESTDO DE L TÉCNIC
19 OFICIN ESPÑOL DE PTENTES Y MRCS ESPÑ 11 21 Número de publicación: 2 510 065 Número de solicitud: 201330552 51 Int. CI.: B60K 15/04 (2006.01) B60K 15/05 (2006.01) 12 INFORME SOBRE EL ESTDO DE L TÉCNIC
Información para la Oficina Internacional sobre la actividad inventiva y los requisitos relativos a la divulgación suficiente.
 Información para la Oficina Internacional sobre la actividad inventiva y los requisitos relativos a la divulgación suficiente. Actividad Inventiva i) Definición de experto en la materia: en la legislación
Información para la Oficina Internacional sobre la actividad inventiva y los requisitos relativos a la divulgación suficiente. Actividad Inventiva i) Definición de experto en la materia: en la legislación
11 Número de publicación: Número de solicitud: Int. Cl. 7 : B32B 31/ Inventor/es: Escolano Berna, María Gema
 19 OFICINA ESPAÑOLA DE PATENTES Y MARCAS ESPAÑA 11 Número de publicación: 2 220 170 21 Número de solicitud: 200200895 51 Int. Cl. 7 : B32B 31/14 B32B 7/04 12 SOLICITUD DE PATENTE A1 22 Fecha de presentación:
19 OFICINA ESPAÑOLA DE PATENTES Y MARCAS ESPAÑA 11 Número de publicación: 2 220 170 21 Número de solicitud: 200200895 51 Int. Cl. 7 : B32B 31/14 B32B 7/04 12 SOLICITUD DE PATENTE A1 22 Fecha de presentación:
ES A1. N. de publicación: ES PATENTES Y MARCAS. Número de solicitud: Int. Cl. 6 : B44D 5/00
 k 19 OFICINA ESPAÑOLA DE PATENTES Y MARCAS ESPAÑA 11 k N. de publicación: ES 2 092 431 21 k Número de solicitud: 9302574 51 k Int. Cl. 6 : B44D 5/00 k 12 SOLICITUD DE PATENTE A1 k 22 Fecha de presentación:
k 19 OFICINA ESPAÑOLA DE PATENTES Y MARCAS ESPAÑA 11 k N. de publicación: ES 2 092 431 21 k Número de solicitud: 9302574 51 k Int. Cl. 6 : B44D 5/00 k 12 SOLICITUD DE PATENTE A1 k 22 Fecha de presentación:
ES B1. Aviso: ESPAÑA 11. Número de publicación: Número de solicitud: A47B 91/06 ( ) A47C 7/00
 19 OFICINA ESPAÑOLA DE PATENTES Y MARCAS ESPAÑA 11 1 Número de publicación: 39 716 Número de solicitud: 0110069 51 Int. CI.: A47B 91/06 (006.01) A47C 7/00 (006.01) B60B 33/06 (006.01) B60B 33/08 (006.01)
19 OFICINA ESPAÑOLA DE PATENTES Y MARCAS ESPAÑA 11 1 Número de publicación: 39 716 Número de solicitud: 0110069 51 Int. CI.: A47B 91/06 (006.01) A47C 7/00 (006.01) B60B 33/06 (006.01) B60B 33/08 (006.01)
11 Número de publicación: Int. Cl. 7 : B31F 1/ Inventor/es: Gianni, Paolo. 74 Agente: Curell Suñol, Marcelino
 19 OFICINA ESPAÑOLA DE PATENTES Y MARCAS ESPAÑA 11 Número de publicación: 2 230 446 1 Int. Cl. 7 : B31F 1/07 12 TRADUCCIÓN DE PATENTE EUROPEA T3 86 Número de solicitud europea: 02076223.3 86 Fecha de presentación:
19 OFICINA ESPAÑOLA DE PATENTES Y MARCAS ESPAÑA 11 Número de publicación: 2 230 446 1 Int. Cl. 7 : B31F 1/07 12 TRADUCCIÓN DE PATENTE EUROPEA T3 86 Número de solicitud europea: 02076223.3 86 Fecha de presentación:
ES A1 ESPAÑA 11. Número de publicación: Número de solicitud: G01F 23/72 ( )
 19 OFICINA ESPAÑOLA DE PATENTES Y MARCAS ESPAÑA 11 21 Número de publicación: 2 406 608 Número de solicitud: 201101281 51 Int. CI.: G01F 23/72 (2006.01) 12 SOLICITUD DE PATENTE A1 22 Fecha de presentación:
19 OFICINA ESPAÑOLA DE PATENTES Y MARCAS ESPAÑA 11 21 Número de publicación: 2 406 608 Número de solicitud: 201101281 51 Int. CI.: G01F 23/72 (2006.01) 12 SOLICITUD DE PATENTE A1 22 Fecha de presentación:
Int. Cl. 7 : C02F 1/76
 k 19 OFICINA ESPAÑOLA DE PATENTES Y MARCAS ESPAÑA 11 k Número de publicación: 2 196 986 21 k Número de solicitud: 04 1 k Int. Cl. 7 : C02F 1/76 C02F 1/68 A23L 2/38 k 12 SOLICITUD DE PATENTE A1 22 kfecha
k 19 OFICINA ESPAÑOLA DE PATENTES Y MARCAS ESPAÑA 11 k Número de publicación: 2 196 986 21 k Número de solicitud: 04 1 k Int. Cl. 7 : C02F 1/76 C02F 1/68 A23L 2/38 k 12 SOLICITUD DE PATENTE A1 22 kfecha
11 Número de publicación: Int. Cl.: 72 Inventor/es: Isaksson, Jan y Nilsson, Bo. 74 Agente: Durán Moya, Carlos
 19 OFICINA ESPAÑOLA DE PATENTES Y MARCAS ESPAÑA 11 Número de publicación: 2 29 137 1 Int. Cl.: B27N 3/14 (06.01) 12 TRADUCCIÓN DE PATENTE EUROPEA T3 86 Número de solicitud europea: 03719044.4 86 Fecha
19 OFICINA ESPAÑOLA DE PATENTES Y MARCAS ESPAÑA 11 Número de publicación: 2 29 137 1 Int. Cl.: B27N 3/14 (06.01) 12 TRADUCCIÓN DE PATENTE EUROPEA T3 86 Número de solicitud europea: 03719044.4 86 Fecha
Criterios de la OEPM en la valoración de la Actividad Inventiva. Javier Vera Roa Madrid 28 de junio 2010
 Criterios de la OEPM en la valoración de la Actividad Inventiva Javier Vera Roa Madrid 28 de junio 2010 La invención patentable: requisitos de patentabilidad Ley de Patentes 11/1986 (art. 4.1) Novedad
Criterios de la OEPM en la valoración de la Actividad Inventiva Javier Vera Roa Madrid 28 de junio 2010 La invención patentable: requisitos de patentabilidad Ley de Patentes 11/1986 (art. 4.1) Novedad
INGENIERA DE PATENTES PROPIEDAD INTELECTUAL COLOMBIA
 PROYECTO MARÍA GUEVARA INGENIERA DE PATENTES PROPIEDAD INTELECTUAL COLOMBIA Diciembre de 2011 10 de septiembre 10 de 2010 FACTORES CLAVES A TENER EN CUENTA AL MOMENTO DE REDACTAR UNA SOLICITUD DE PATENTE
PROYECTO MARÍA GUEVARA INGENIERA DE PATENTES PROPIEDAD INTELECTUAL COLOMBIA Diciembre de 2011 10 de septiembre 10 de 2010 FACTORES CLAVES A TENER EN CUENTA AL MOMENTO DE REDACTAR UNA SOLICITUD DE PATENTE
ES A1 ESPAÑA 11. Número de publicación: Número de solicitud: A61M 39/26 ( ) F16L 37/30 ( )
 19 OFICINA ESPAÑOLA DE PATENTES Y MARCAS ESPAÑA 11 21 Número de publicación: 2 528 058 Número de solicitud: 201300731 51 Int. CI.: A61M 39/26 (2006.01) F16L 37/30 (2006.01) 12 SOLICITUD DE PATENTE A1 22
19 OFICINA ESPAÑOLA DE PATENTES Y MARCAS ESPAÑA 11 21 Número de publicación: 2 528 058 Número de solicitud: 201300731 51 Int. CI.: A61M 39/26 (2006.01) F16L 37/30 (2006.01) 12 SOLICITUD DE PATENTE A1 22
51 Int. CI.: H02K 1/27 H02K 7/14 ( ) PATENTE DE INVENCIÓN CON EXAMEN PREVIO
 19 OFICINA ESPAÑOLA DE PATENTES Y MARCAS ESPAÑA 11 Número de publicación: 21 2 378 634 Número de solicitud: 20113114 1 Int. CI.: B02C 17/24 (2006.01) H02K 1/27 (2006.01) H02K 7/14 (2006.01) 12 PATENTE
19 OFICINA ESPAÑOLA DE PATENTES Y MARCAS ESPAÑA 11 Número de publicación: 21 2 378 634 Número de solicitud: 20113114 1 Int. CI.: B02C 17/24 (2006.01) H02K 1/27 (2006.01) H02K 7/14 (2006.01) 12 PATENTE
Redacción de Reivindicaciones de Patentes de Productos Agroquímicos
 Redacción de Reivindicaciones de Patentes de Productos Agroquímicos Maria Carmen S. Brito Dannemann, Siemsen, Bigler & Ipanema Moreira ASIPI Asunción 17.03.2015 1 Temas tratados: - Reivindicaciones habituales
Redacción de Reivindicaciones de Patentes de Productos Agroquímicos Maria Carmen S. Brito Dannemann, Siemsen, Bigler & Ipanema Moreira ASIPI Asunción 17.03.2015 1 Temas tratados: - Reivindicaciones habituales
11 Número de publicación: Número de solicitud: Int. Cl. 7 : A61F 5/ Inventor/es: Moreno Galera, Ángel
 19 OFICINA ESPAÑOLA DE PATENTES Y MARCAS ESPAÑA 11 Número de publicación: 2 222 100 21 Número de solicitud: 200301599 51 Int. Cl. 7 : A61F 5/44 12 SOLICITUD DE PATENTE A1 22 Fecha de presentación: 09.07.2003
19 OFICINA ESPAÑOLA DE PATENTES Y MARCAS ESPAÑA 11 Número de publicación: 2 222 100 21 Número de solicitud: 200301599 51 Int. Cl. 7 : A61F 5/44 12 SOLICITUD DE PATENTE A1 22 Fecha de presentación: 09.07.2003
ES A1. Número de publicación: PATENTES Y MARCAS. Número de solicitud: Int. Cl. 7 : A01G 25/02
 k 19 OFICINA ESPAÑOLA DE PATENTES Y MARCAS ESPAÑA 11 k Número de publicación: 2 19 226 21 k Número de solicitud: 009900309 1 k Int. Cl. 7 : A01G 2/02 k 12 SOLICITUD DE PATENTE A1 k 22 Fecha de presentación:
k 19 OFICINA ESPAÑOLA DE PATENTES Y MARCAS ESPAÑA 11 k Número de publicación: 2 19 226 21 k Número de solicitud: 009900309 1 k Int. Cl. 7 : A01G 2/02 k 12 SOLICITUD DE PATENTE A1 k 22 Fecha de presentación:
Relativo al etiquetado energético de los acondicionadores de aire. 26 de Julio de de Enero de 2013
 Resumen del Reglamento Delegado UE nº 626/2011, por el que se complementa la Directiva 2010/30/UE del Parlamento Europeo y del Consejo en lo que respecta al ETIQUETADO ENERGÉTICO DE LOS ACONDICIONADORES
Resumen del Reglamento Delegado UE nº 626/2011, por el que se complementa la Directiva 2010/30/UE del Parlamento Europeo y del Consejo en lo que respecta al ETIQUETADO ENERGÉTICO DE LOS ACONDICIONADORES
Int. Cl. 6 : A61H 39/08
 k 19 OFICINA ESPAÑOLA DE PATENTES Y MARCAS ESPAÑA 11 k N. de publicación: ES 2 095 807 21 k Número de solicitud: 9500618 51 k Int. Cl. 6 : A61H 39/08 B65B 9/02 k 12 SOLICITUD DE PATENTE A1 22 kfecha de
k 19 OFICINA ESPAÑOLA DE PATENTES Y MARCAS ESPAÑA 11 k N. de publicación: ES 2 095 807 21 k Número de solicitud: 9500618 51 k Int. Cl. 6 : A61H 39/08 B65B 9/02 k 12 SOLICITUD DE PATENTE A1 22 kfecha de
9. CARTOGRAFÍA GEOQUÍMICA AMBIENTAL
 Página 123 de 148 9. CARTOGRAFÍA GEOQUÍMICA AMBIENTAL El sedimento, como muestra que representa una mezcla y un promedio de los materiales superficiales de la cuenca de drenaje, es susceptible de suministrar
Página 123 de 148 9. CARTOGRAFÍA GEOQUÍMICA AMBIENTAL El sedimento, como muestra que representa una mezcla y un promedio de los materiales superficiales de la cuenca de drenaje, es susceptible de suministrar
ES A1. Número de publicación: PATENTES Y MARCAS. Número de solicitud: Int. Cl. 7 : B44C 1/22
 k 19 OFICINA ESPAÑOLA DE PATENTES Y MARCAS ESPAÑA 11 k Número de publicación: 2 156 686 21 k Número de solicitud: 009802338 51 k Int. Cl. 7 : B44C 1/22 k 12 SOLICITUD DE PATENTE A1 k 22 Fecha de presentación:
k 19 OFICINA ESPAÑOLA DE PATENTES Y MARCAS ESPAÑA 11 k Número de publicación: 2 156 686 21 k Número de solicitud: 009802338 51 k Int. Cl. 7 : B44C 1/22 k 12 SOLICITUD DE PATENTE A1 k 22 Fecha de presentación:
Int. Cl. 7 : C02F 1/04
 k 19 OFICINA ESPAÑOLA DE PATENTES Y MARCAS ESPAÑA 11 k Número de publicación: 2 12 810 21 k Número de solicitud: 009800876 1 k Int. Cl. 7 : C02F 1/04 A23K 1/00 C0F 7/00 C02F 1/16 k 12 SOLICITUD DE PATENTE
k 19 OFICINA ESPAÑOLA DE PATENTES Y MARCAS ESPAÑA 11 k Número de publicación: 2 12 810 21 k Número de solicitud: 009800876 1 k Int. Cl. 7 : C02F 1/04 A23K 1/00 C0F 7/00 C02F 1/16 k 12 SOLICITUD DE PATENTE
ES A1. Número de publicación: PATENTES Y MARCAS. Número de solicitud: Int. Cl. 6 : A23C 19/09
 k 19 OFICINA ESPAÑOLA DE PATENTES Y MARCAS ESPAÑA 11 k Número de publicación: 2 125 839 21 k Número de solicitud: 9701342 51 k Int. Cl. 6 : A23C 19/09 k 12 SOLICITUD DE PATENTE A1 k 22 Fecha de presentación:
k 19 OFICINA ESPAÑOLA DE PATENTES Y MARCAS ESPAÑA 11 k Número de publicación: 2 125 839 21 k Número de solicitud: 9701342 51 k Int. Cl. 6 : A23C 19/09 k 12 SOLICITUD DE PATENTE A1 k 22 Fecha de presentación:
11 Número de publicación: Número de solicitud: Int. Cl. 7 : B08B 9/ Inventor/es: Blanc, Philippe
 19 OFICINA ESPAÑOLA DE PATENTES Y MARCAS ESPAÑA 11 Número de publicación: 2 228 220 21 Número de solicitud: 200201922 1 Int. Cl. 7 : B08B 9/08 12 SOLICITUD DE PATENTE A1 22 Fecha de presentación: 14.08.2002
19 OFICINA ESPAÑOLA DE PATENTES Y MARCAS ESPAÑA 11 Número de publicación: 2 228 220 21 Número de solicitud: 200201922 1 Int. Cl. 7 : B08B 9/08 12 SOLICITUD DE PATENTE A1 22 Fecha de presentación: 14.08.2002
Int. Cl. 7 : E06B 1/34
 k 19 OFICINA ESPAÑOLA DE PATENTES Y MARCAS ESPAÑA 11 k Número de publicación: 2 198 193 21 k Número de solicitud: 200102764 51 k Int. Cl. 7 : E06B 1/34 E06B 3/30 B32B 7/12 B23B 23/00 k 12 SOLICITUD DE
k 19 OFICINA ESPAÑOLA DE PATENTES Y MARCAS ESPAÑA 11 k Número de publicación: 2 198 193 21 k Número de solicitud: 200102764 51 k Int. Cl. 7 : E06B 1/34 E06B 3/30 B32B 7/12 B23B 23/00 k 12 SOLICITUD DE
Int. Cl. 6 : E04G 11/02
 k 19 OFICINA ESPAÑOLA DE PATENTES Y MARCAS ESPAÑA 11 k Número de publicación: 2 132 01 21 k Número de solicitud: 9602608 1 k Int. Cl. 6 : E04G 11/02 B2B 7/22 k 12 SOLICITUD DE PATENTE A1 22 kfecha de presentación:
k 19 OFICINA ESPAÑOLA DE PATENTES Y MARCAS ESPAÑA 11 k Número de publicación: 2 132 01 21 k Número de solicitud: 9602608 1 k Int. Cl. 6 : E04G 11/02 B2B 7/22 k 12 SOLICITUD DE PATENTE A1 22 kfecha de presentación:
ES A1 B65B 25/18 B65D 77/04 OFICINA ESPAÑOLA DE PATENTES Y MARCAS ESPAÑA. 11 Número de publicación:
 19 OFICINA ESPAÑOLA DE PATENTES Y MARCAS ESPAÑA 11 Número de publicación: 2 217 992 21 Número de solicitud: 200401536 51 Int. Cl. 7 : A21D 13/00 B65B 25/18 B65D 77/04 12 SOLICITUD DE PATENTE A1 22 Fecha
19 OFICINA ESPAÑOLA DE PATENTES Y MARCAS ESPAÑA 11 Número de publicación: 2 217 992 21 Número de solicitud: 200401536 51 Int. Cl. 7 : A21D 13/00 B65B 25/18 B65D 77/04 12 SOLICITUD DE PATENTE A1 22 Fecha
ES A1 B21D 39/04 OFICINA ESPAÑOLA DE PATENTES Y MARCAS ESPAÑA. 11 Número de publicación: Número de solicitud:
 19 OFICINA ESPAÑOLA DE PATENTES Y MARCAS ESPAÑA 11 Número de publicación: 2 224 824 21 Número de solicitud: 200202742 1 Int. Cl. 7 : F16L 13/14 B21D 39/04 12 SOLICITUD DE PATENTE A1 22 Fecha de presentación:
19 OFICINA ESPAÑOLA DE PATENTES Y MARCAS ESPAÑA 11 Número de publicación: 2 224 824 21 Número de solicitud: 200202742 1 Int. Cl. 7 : F16L 13/14 B21D 39/04 12 SOLICITUD DE PATENTE A1 22 Fecha de presentación:
11 Número de publicación: Número de solicitud: Int. Cl. 7 : A01G 27/ Inventor/es: Martínez Ruiz, Vicente
 19 OFICINA ESPAÑOLA DE PATENTES Y MARCAS ESPAÑA 11 Número de publicación: 2 242 498 21 Número de solicitud: 200301433 51 Int. Cl. 7 : A01G 27/04 A01G 29/00 12 SOLICITUD DE PATENTE A1 22 Fecha de presentación:
19 OFICINA ESPAÑOLA DE PATENTES Y MARCAS ESPAÑA 11 Número de publicación: 2 242 498 21 Número de solicitud: 200301433 51 Int. Cl. 7 : A01G 27/04 A01G 29/00 12 SOLICITUD DE PATENTE A1 22 Fecha de presentación:
ES A1. Número de publicación: PATENTES Y MARCAS. Número de solicitud: Int. Cl. 6 : B44C 1/17
 k 19 OFICINA ESPAÑOLA DE PATENTES Y MARCAS ESPAÑA 11 k Número de publicación: 2 137 098 21 k Número de solicitud: 009700112 51 k Int. Cl. 6 : B44C 1/17 k 12 SOLICITUD DE PATENTE A1 k 22 Fecha de presentación:
k 19 OFICINA ESPAÑOLA DE PATENTES Y MARCAS ESPAÑA 11 k Número de publicación: 2 137 098 21 k Número de solicitud: 009700112 51 k Int. Cl. 6 : B44C 1/17 k 12 SOLICITUD DE PATENTE A1 k 22 Fecha de presentación:
José Antonio Rojas Cerdeño Director de Calidad y Medio Ambiente Ormazabal Cotradis Transformadores
 EMPLEO DE LIQUIDOS DIELECTRICOS BIODEGRADABLES EN SUSTITUCION DE FLUIDOS CONVENCIONALES. LA EXPERIENCIA DEL BIOELECTRA EN TRANSFORMADORES ELÉCTRICOS DE DISTRIBUCION José Antonio Rojas Cerdeño Director
EMPLEO DE LIQUIDOS DIELECTRICOS BIODEGRADABLES EN SUSTITUCION DE FLUIDOS CONVENCIONALES. LA EXPERIENCIA DEL BIOELECTRA EN TRANSFORMADORES ELÉCTRICOS DE DISTRIBUCION José Antonio Rojas Cerdeño Director
ES A1. Número de publicación: PATENTES Y MARCAS. Número de solicitud: Int. Cl. 7 : A01G 31/06
 k 19 OFICINA ESPAÑOLA DE PATENTES Y MARCAS ESPAÑA 11 k Número de publicación: 2 194 69 21 k Número de solicitud: 200100048 1 k Int. Cl. 7 : A01G 31/06 k 12 SOLICITUD DE PATENTE A1 k 22 Fecha de presentación:
k 19 OFICINA ESPAÑOLA DE PATENTES Y MARCAS ESPAÑA 11 k Número de publicación: 2 194 69 21 k Número de solicitud: 200100048 1 k Int. Cl. 7 : A01G 31/06 k 12 SOLICITUD DE PATENTE A1 k 22 Fecha de presentación:
ES B1. Aviso: ESPAÑA 11. Número de publicación: Número de solicitud: B62M 11/00 ( ) B62M 11/10 (2006.
 19 OFICINA ESPAÑOLA DE PATENTES Y MARCAS ESPAÑA 11 21 Número de publicación: 2 402 009 Número de solicitud: 201131419 51 Int. CI.: B62M 11/00 (2006.01) B62M 11/10 (2006.01) 12 PATENTE DE INVENCIÓN B1 22
19 OFICINA ESPAÑOLA DE PATENTES Y MARCAS ESPAÑA 11 21 Número de publicación: 2 402 009 Número de solicitud: 201131419 51 Int. CI.: B62M 11/00 (2006.01) B62M 11/10 (2006.01) 12 PATENTE DE INVENCIÓN B1 22
ES A1. N. de publicación: ES PATENTES Y MARCAS. Número de solicitud: Int. Cl. 6 : A01K 97/04
 k 19 OFICINA ESPAÑOLA DE PATENTES Y MARCAS ESPAÑA 11 k N. de publicación: ES 2 079 314 21 k Número de solicitud: 9400293 51 k Int. Cl. 6 : A01K 97/04 k 12 SOLICITUD DE PATENTE A1 k 22 Fecha de presentación:
k 19 OFICINA ESPAÑOLA DE PATENTES Y MARCAS ESPAÑA 11 k N. de publicación: ES 2 079 314 21 k Número de solicitud: 9400293 51 k Int. Cl. 6 : A01K 97/04 k 12 SOLICITUD DE PATENTE A1 k 22 Fecha de presentación:
FÍSICA Y QUÍMICA 3º ESO. OBJETIVOS, CONTENIDOS Y CRITERIOS DE EVALUACIÓN 1ª Evaluación: Unidad 1. La medida y el método científico.
 FÍSICA Y QUÍMICA 3º ESO. OBJETIVOS, CONTENIDOS Y CRITERIOS DE EVALUACIÓN 1ª Evaluación: Unidad 1. La medida y el método científico. OBJETIVOS 1. Reconocer las etapas del trabajo científico y elaborar informes
FÍSICA Y QUÍMICA 3º ESO. OBJETIVOS, CONTENIDOS Y CRITERIOS DE EVALUACIÓN 1ª Evaluación: Unidad 1. La medida y el método científico. OBJETIVOS 1. Reconocer las etapas del trabajo científico y elaborar informes
Int. Cl. 6 : B44C 5/00
 k 19 OFICINA ESPAÑOLA DE PATENTES Y MARCAS ESPAÑA 11 k Número de publicación: 2 137 840 21 k Número de solicitud: 009700602 51 k Int. Cl. 6 : B44C 5/00 A44C 27/00 k 12 SOLICITUD DE PATENTE A1 22 kfecha
k 19 OFICINA ESPAÑOLA DE PATENTES Y MARCAS ESPAÑA 11 k Número de publicación: 2 137 840 21 k Número de solicitud: 009700602 51 k Int. Cl. 6 : B44C 5/00 A44C 27/00 k 12 SOLICITUD DE PATENTE A1 22 kfecha
11 Número de publicación: Número de solicitud: Int. Cl. 7 : B32B 17/ Inventor/es: Navarro Jiménez, Miguel
 19 OFICINA ESPAÑOLA DE PATENTES Y MARCAS ESPAÑA 11 Número de publicación: 2 219 126 21 Número de solicitud: 200102114 1 Int. Cl. 7 : B32B 17/10 12 SOLICITUD DE PATENTE A1 22 Fecha de presentación: 21.09.2001
19 OFICINA ESPAÑOLA DE PATENTES Y MARCAS ESPAÑA 11 Número de publicación: 2 219 126 21 Número de solicitud: 200102114 1 Int. Cl. 7 : B32B 17/10 12 SOLICITUD DE PATENTE A1 22 Fecha de presentación: 21.09.2001
Int. Cl. 7 : B27K 3/50
 k 19 OFICINA ESPAÑOLA DE PATENTES Y MARCAS ESPAÑA 11 k Número de publicación: 2 192 1 21 k Número de solicitud: 008 1 k Int. Cl. 7 : B27K 3/ C09D 133/08 k 12 SOLICITUD DE PATENTE A1 22 kfecha de presentación:
k 19 OFICINA ESPAÑOLA DE PATENTES Y MARCAS ESPAÑA 11 k Número de publicación: 2 192 1 21 k Número de solicitud: 008 1 k Int. Cl. 7 : B27K 3/ C09D 133/08 k 12 SOLICITUD DE PATENTE A1 22 kfecha de presentación:
Int. Cl. 7 : D21H 19/24
 k 19 OFICINA ESPAÑOLA DE PATENTES Y MARCAS ESPAÑA 11 k Número de publicación: 2 16 081 21 k Número de solicitud: 009901709 1 k Int. Cl. 7 : D21H 19/24 D21H 19/66 B32B 29/06 k 12 SOLICITUD DE PATENTE A1
k 19 OFICINA ESPAÑOLA DE PATENTES Y MARCAS ESPAÑA 11 k Número de publicación: 2 16 081 21 k Número de solicitud: 009901709 1 k Int. Cl. 7 : D21H 19/24 D21H 19/66 B32B 29/06 k 12 SOLICITUD DE PATENTE A1
PRÁCTICA Nº 2 OPERACIONES COMUNES EN UN LABORATORIO
 PRÁCTICA Nº 2 OPERACIONES COMUNES EN UN LABORATORIO OBJETIVO Utilizar el material de laboratorio en las operaciones más comunes realizadas en un laboratorio de química. I. ASPECTOS TEÓRICOS Una vez conocido
PRÁCTICA Nº 2 OPERACIONES COMUNES EN UN LABORATORIO OBJETIVO Utilizar el material de laboratorio en las operaciones más comunes realizadas en un laboratorio de química. I. ASPECTOS TEÓRICOS Una vez conocido
ES U. Número de publicación: PATENTES Y MARCAS. Número de solicitud: U Int. Cl. 6 : A23L 3/00
 k 19 OFICINA ESPAÑOLA DE PATENTES Y MARCAS ESPAÑA 11 k Número de publicación: 1 039 18 21 k Número de solicitud: U 970338 1 k Int. Cl. 6 : A23L 3/00 k 12 SOLICITUD DE MODELO DE UTILIDAD U k 22 Fecha de
k 19 OFICINA ESPAÑOLA DE PATENTES Y MARCAS ESPAÑA 11 k Número de publicación: 1 039 18 21 k Número de solicitud: U 970338 1 k Int. Cl. 6 : A23L 3/00 k 12 SOLICITUD DE MODELO DE UTILIDAD U k 22 Fecha de
ES A1 B29C 39/10 //B29K 75:00. Número de publicación: PATENTES Y MARCAS. Número de solicitud: Int. Cl.
 k 19 OFICINA ESPAÑOLA DE PATENTES Y MARCAS ESPAÑA 11 k Número de publicación: 2 156 736 21 k Número de solicitud: 009901276 51 k Int. Cl. 7 : A47B 96/20 B29C 39/10 //B29K 75:00 k 12 SOLICITUD DE PATENTE
k 19 OFICINA ESPAÑOLA DE PATENTES Y MARCAS ESPAÑA 11 k Número de publicación: 2 156 736 21 k Número de solicitud: 009901276 51 k Int. Cl. 7 : A47B 96/20 B29C 39/10 //B29K 75:00 k 12 SOLICITUD DE PATENTE
PROFESOR JANO
 Desarrollo embrionario del erizo de mar Paracentrotus lividus Iratxe Menchaca La präctica consistirä en estudiar el proceso de fecundaciån y primeras etapas del desarrollo embrionario del erizo de mar
Desarrollo embrionario del erizo de mar Paracentrotus lividus Iratxe Menchaca La präctica consistirä en estudiar el proceso de fecundaciån y primeras etapas del desarrollo embrionario del erizo de mar
ES U ESPAÑA 11. Número de publicación: Número de solicitud: E05B 13/00 ( )
 19 OFICINA ESPAÑOLA DE PATENTES Y MARCAS ESPAÑA 11 21 Número de publicación: 1 14 69 Número de solicitud: 20131137 1 Int. CI.: E0B 13/00 (2006.01) E0B 13/00 (2006.01) 12 SOLICITUD DE MODELO DE UTILIDAD
19 OFICINA ESPAÑOLA DE PATENTES Y MARCAS ESPAÑA 11 21 Número de publicación: 1 14 69 Número de solicitud: 20131137 1 Int. CI.: E0B 13/00 (2006.01) E0B 13/00 (2006.01) 12 SOLICITUD DE MODELO DE UTILIDAD
ES U. Número de publicación: PATENTES Y MARCAS. Número de solicitud: U Int. Cl. 7 : A01K 61/00
 k 19 OFICINA ESPAÑOLA DE PATENTES Y MARCAS ESPAÑA 11 k Número de publicación: 1 03 907 21 k Número de solicitud: U 02929 1 k Int. Cl. 7 : A01K 61/00 k 12 SOLICITUD DE MODELO DE UTILIDAD U k 22 Fecha de
k 19 OFICINA ESPAÑOLA DE PATENTES Y MARCAS ESPAÑA 11 k Número de publicación: 1 03 907 21 k Número de solicitud: U 02929 1 k Int. Cl. 7 : A01K 61/00 k 12 SOLICITUD DE MODELO DE UTILIDAD U k 22 Fecha de
Determinación de la concentración micelar crítica (cmc) y grado de disociación (α) de un tensioactivo iónico mediante medidas de conductividad
 Determinación de la concentración micelar crítica (cmc) y grado de disociación (α) de un tensioactivo iónico mediante medidas de conductividad OBJETIVO: Determinación de la concentración micelar crítica
Determinación de la concentración micelar crítica (cmc) y grado de disociación (α) de un tensioactivo iónico mediante medidas de conductividad OBJETIVO: Determinación de la concentración micelar crítica
INFORME SECTOR. AIDO ARTES GRÁFICAS. Análisis de ciclo de vida de libros impresos
 2011 INFORME SECTOR www.ecodisseny.net Análisis de ciclo de vida de libros impresos INDICE 1. INTRODUCCIÓN 2. ANÁLISIS DE CICLO DE VIDA 3. ANÁLISIS DE CICLO DE VIDA DEL LIBRO 2 1. INTRODUCCIÓN El cálculo
2011 INFORME SECTOR www.ecodisseny.net Análisis de ciclo de vida de libros impresos INDICE 1. INTRODUCCIÓN 2. ANÁLISIS DE CICLO DE VIDA 3. ANÁLISIS DE CICLO DE VIDA DEL LIBRO 2 1. INTRODUCCIÓN El cálculo
ES U ESPAÑA 11. Número de publicación: Número de solicitud: A45D 24/30 ( ) A61L 2/02 ( )
 19 OFICINA ESPAÑOLA DE PATENTES Y MARCAS ESPAÑA 11 21 Número de publicación: 1 143 89 Número de solicitud: 200432 1 Int. CI.: A4D 24/30 (2006.01) A61L 2/02 (2006.01) 12 SOLICITUD DE MODELO DE UTILIDAD
19 OFICINA ESPAÑOLA DE PATENTES Y MARCAS ESPAÑA 11 21 Número de publicación: 1 143 89 Número de solicitud: 200432 1 Int. CI.: A4D 24/30 (2006.01) A61L 2/02 (2006.01) 12 SOLICITUD DE MODELO DE UTILIDAD
PROGRAMACIÓN DEL RIEGO
 PROGRAMACIÓN DEL RIEGO Mª Dolores Fernández Fernández Estación Experimental Las Palmerillas (Fundación Cajamar) METODOS DE PROGRAMACION DEL RIEGO Cuánto y Cuándo regar Parámetros climáticos. Medida del
PROGRAMACIÓN DEL RIEGO Mª Dolores Fernández Fernández Estación Experimental Las Palmerillas (Fundación Cajamar) METODOS DE PROGRAMACION DEL RIEGO Cuánto y Cuándo regar Parámetros climáticos. Medida del
11 Número de publicación: Número de solicitud: Int. Cl. 7 : A61K 35/ Inventor/es: Aranda Samper, Eduardo
 19 OFICINA ESPAÑOLA DE PATENTES Y MARCAS ESPAÑA 11 Número de publicación: 2 211 321 21 Número de solicitud: 02878 1 Int. Cl. 7 : A61K /78 A61K 7/48 A61P 17/00 12 SOLICITUD DE PATENTE A1 22 Fecha de presentación:
19 OFICINA ESPAÑOLA DE PATENTES Y MARCAS ESPAÑA 11 Número de publicación: 2 211 321 21 Número de solicitud: 02878 1 Int. Cl. 7 : A61K /78 A61K 7/48 A61P 17/00 12 SOLICITUD DE PATENTE A1 22 Fecha de presentación:
11 Número de publicación: Número de solicitud: Int. Cl.: 74 Agente: Temiño Ceniceros, Ignacio
 19 OFICINA ESPAÑOLA DE PATENTES Y MARCAS ESPAÑA 11 Número de publicación: 2 331 168 21 Número de solicitud: 200800814 51 Int. Cl.: A23L 1/217 (2006.01) A23L 3/10 (2006.01) A23P 1/00 (2006.01) 12 PATENTE
19 OFICINA ESPAÑOLA DE PATENTES Y MARCAS ESPAÑA 11 Número de publicación: 2 331 168 21 Número de solicitud: 200800814 51 Int. Cl.: A23L 1/217 (2006.01) A23L 3/10 (2006.01) A23P 1/00 (2006.01) 12 PATENTE
ES B1. Aviso: ESPAÑA 11. Número de publicación: Número de solicitud: G01K 7/01 ( )
 19 OFICINA ESPAÑOLA DE PATENTES Y MARCAS ESPAÑA 11 21 Número de publicación: 2 42 299 Número de solicitud: 12273 1 Int. CI.: G01K 7/01 (06.01) 12 PATENTE DE INVENCIÓN B1 22 Fecha de presentación: 23.02.12
19 OFICINA ESPAÑOLA DE PATENTES Y MARCAS ESPAÑA 11 21 Número de publicación: 2 42 299 Número de solicitud: 12273 1 Int. CI.: G01K 7/01 (06.01) 12 PATENTE DE INVENCIÓN B1 22 Fecha de presentación: 23.02.12
ES U. Número de publicación: PATENTES Y MARCAS. Número de solicitud: U Int. Cl. 7 : A47J 42/38
 k 19 OFICINA ESPAÑOLA DE PATENTES Y MARCAS ESPAÑA 11 k Número de publicación: 1 03 97 21 k Número de solicitud: U 20030031 1 k Int. Cl. 7 : A47J 42/38 k 12 SOLICITUD DE MODELO DE UTILIDAD U k 22 Fecha
k 19 OFICINA ESPAÑOLA DE PATENTES Y MARCAS ESPAÑA 11 k Número de publicación: 1 03 97 21 k Número de solicitud: U 20030031 1 k Int. Cl. 7 : A47J 42/38 k 12 SOLICITUD DE MODELO DE UTILIDAD U k 22 Fecha
CAPITULO II REVISIÓN DE LITERATURA
 CAPITULO I 1. INTRODUCCIÓN... 1 1.1 EL PROBLEMA... 2 1.2 JUSTIFICACIÓN... 3 1.3 OBJETIVOS... 4 1.3.1 GENERAL... 4 1.3.2 ESPECÍFICOS... 4 1.4. PREGUNTA DIRECTRIZ... 4 CAPITULO II REVISIÓN DE LITERATURA
CAPITULO I 1. INTRODUCCIÓN... 1 1.1 EL PROBLEMA... 2 1.2 JUSTIFICACIÓN... 3 1.3 OBJETIVOS... 4 1.3.1 GENERAL... 4 1.3.2 ESPECÍFICOS... 4 1.4. PREGUNTA DIRECTRIZ... 4 CAPITULO II REVISIÓN DE LITERATURA
ES A1. Número de publicación: PATENTES Y MARCAS. Número de solicitud: Int. Cl. 7 : A23L 1/24
 k 19 OFICINA ESPAÑOLA DE PATENTES Y MARCAS ESPAÑA 11 k Número de publicación: 2 1 383 21 k Número de solicitud: 009802427 1 k Int. Cl. 7 : A23L 1/24 k 12 SOLICITUD DE PATENTE A1 k 22 Fecha de presentación:
k 19 OFICINA ESPAÑOLA DE PATENTES Y MARCAS ESPAÑA 11 k Número de publicación: 2 1 383 21 k Número de solicitud: 009802427 1 k Int. Cl. 7 : A23L 1/24 k 12 SOLICITUD DE PATENTE A1 k 22 Fecha de presentación:
Int. Cl. 6 : A01N 59/ kfecha de presentación: k Solicitante/s: Manuel Correa Negrín Arure, s/n, Valle Gran Rey-La Gomera,
 k 19 OFICINA ESPAÑOLA DE PATENTES Y MARCAS ESPAÑA 11 k Número de publicación: 2 129 37 21 k Número de solicitud: 9702434 1 k Int. Cl. 6 : A01N 9/14 A01N 6/00 k 12 SOLICITUD DE PATENTE A1 22 kfecha de presentación:.11.97
k 19 OFICINA ESPAÑOLA DE PATENTES Y MARCAS ESPAÑA 11 k Número de publicación: 2 129 37 21 k Número de solicitud: 9702434 1 k Int. Cl. 6 : A01N 9/14 A01N 6/00 k 12 SOLICITUD DE PATENTE A1 22 kfecha de presentación:.11.97
LEWATIT MonoPlus MP 500
 La Lewatit MonoPlus MP 500 es un intercambiador de aniones fuertemente básico de tipo I, macroporoso, con bolas de tamaño uniforme (monodispersas) a base de un copolímero de estireno divinilbenceno. Diseñado
La Lewatit MonoPlus MP 500 es un intercambiador de aniones fuertemente básico de tipo I, macroporoso, con bolas de tamaño uniforme (monodispersas) a base de un copolímero de estireno divinilbenceno. Diseñado
Comité de Ética de Experimentación Animal del Hospital Clínico San Carlos (CEEA)
 Comité de Ética de Experimentación Animal del Hospital Clínico San Carlos (CEEA) SOLICITUD DE INFORME DE AUTORIZACIÓN DE PROCEDIMIENTO EXPERIMENTAL DE ORGANISMOS GENETICAMENTE MODIFICADOS AL COMITÉ DE
Comité de Ética de Experimentación Animal del Hospital Clínico San Carlos (CEEA) SOLICITUD DE INFORME DE AUTORIZACIÓN DE PROCEDIMIENTO EXPERIMENTAL DE ORGANISMOS GENETICAMENTE MODIFICADOS AL COMITÉ DE
Int. Cl. 7 : B44C 3/12. k 71 Solicitante/s: José Vicente Boix Fenollosa. k 72 Inventor/es: Boix Fenollosa, José Vicente
 k 19 OFICINA ESPAÑOLA DE PATENTES Y MARCAS ESPAÑA 11 k Número de publicación: 2 156 712 21 k Número de solicitud: 009900427 51 k Int. Cl. 7 : B44C 3/12 k 12 SOLICITUD DE PATENTE A1 k 22 Fecha de presentación:
k 19 OFICINA ESPAÑOLA DE PATENTES Y MARCAS ESPAÑA 11 k Número de publicación: 2 156 712 21 k Número de solicitud: 009900427 51 k Int. Cl. 7 : B44C 3/12 k 12 SOLICITUD DE PATENTE A1 k 22 Fecha de presentación:
ES A1. Número de publicación: PATENTES Y MARCAS. Número de solicitud: Int. Cl. 7 : A23N 15/08
 k 19 OFICINA ESPAÑOLA DE PATENTES Y MARCAS ESPAÑA 11 k Número de publicación: 2 152 183 21 k Número de solicitud: 009900796 51 k Int. Cl. 7 : A23N 15/08 k 12 SOLICITUD DE PATENTE A1 k 22 Fecha de presentación:
k 19 OFICINA ESPAÑOLA DE PATENTES Y MARCAS ESPAÑA 11 k Número de publicación: 2 152 183 21 k Número de solicitud: 009900796 51 k Int. Cl. 7 : A23N 15/08 k 12 SOLICITUD DE PATENTE A1 k 22 Fecha de presentación:
11 Número de publicación: Int. Cl. 7 : A61K 39/ Inventor/es: Davelaar, Frans, Gerrit. 74 Agente: Curell Suñol, Marcelino
 19 OFICINA ESPAÑOLA DE PATENTES Y MARCAS ESPAÑA 11 Número de publicación: 2 224 294 1 Int. Cl. 7 : A61K 39/17 12 TRADUCCIÓN DE PATENTE EUROPEA T3 86 Número de solicitud europea: 9793833.7 86 Fecha de presentación:
19 OFICINA ESPAÑOLA DE PATENTES Y MARCAS ESPAÑA 11 Número de publicación: 2 224 294 1 Int. Cl. 7 : A61K 39/17 12 TRADUCCIÓN DE PATENTE EUROPEA T3 86 Número de solicitud europea: 9793833.7 86 Fecha de presentación:
DESCRIPCIÓN DEL RESULTADO DE INVESTIGACIÓN
 REF.: AGR_UAH_02 SECTOR INDUSTRIAL INVESTIGADOR DEPARTAMENTO DATOS DE CONTACTO PÁGINA WEB Agroalimentación Mª Luisa Marina Alegre Concepción García López Química Analítica, Química Física e Ingeniería
REF.: AGR_UAH_02 SECTOR INDUSTRIAL INVESTIGADOR DEPARTAMENTO DATOS DE CONTACTO PÁGINA WEB Agroalimentación Mª Luisa Marina Alegre Concepción García López Química Analítica, Química Física e Ingeniería
ES A1. Número de publicación: PATENTES Y MARCAS. Número de solicitud: Int. Cl. 6 : B28B 1/14
 k 19 OFICINA ESPAÑOLA DE PATENTES Y MARCAS ESPAÑA 11 k Número de publicación: 2 136 039 21 k Número de solicitud: 009800290 1 k Int. Cl. 6 : B28B 1/14 k 12 SOLICITUD DE PATENTE A1 k 22 Fecha de presentación:
k 19 OFICINA ESPAÑOLA DE PATENTES Y MARCAS ESPAÑA 11 k Número de publicación: 2 136 039 21 k Número de solicitud: 009800290 1 k Int. Cl. 6 : B28B 1/14 k 12 SOLICITUD DE PATENTE A1 k 22 Fecha de presentación:
LAS AGUAS RESIDUALES URBANAS
 LAS AGUAS RESIDUALES URBANAS Manhatan, New York Ciudadela del Machu Picchu, Perú Guayaquil, Ecuador Usos de las aguas residuales riego agrícola (cultivos y semilleros) riego de parques y jardines (campos
LAS AGUAS RESIDUALES URBANAS Manhatan, New York Ciudadela del Machu Picchu, Perú Guayaquil, Ecuador Usos de las aguas residuales riego agrícola (cultivos y semilleros) riego de parques y jardines (campos
ES A1. Número de publicación: PATENTES Y MARCAS. Número de solicitud: Int. Cl. 7 : B44C 1/22
 k 19 OFICINA ESPAÑOLA DE PATENTES Y MARCAS ESPAÑA 11 k Número de publicación: 2 161 189 21 k Número de solicitud: 200000431 51 k Int. Cl. 7 : B44C 1/22 k 12 SOLICITUD DE PATENTE A1 k 22 Fecha de presentación:
k 19 OFICINA ESPAÑOLA DE PATENTES Y MARCAS ESPAÑA 11 k Número de publicación: 2 161 189 21 k Número de solicitud: 200000431 51 k Int. Cl. 7 : B44C 1/22 k 12 SOLICITUD DE PATENTE A1 k 22 Fecha de presentación:
11 kn. de publicación: ES kint. Cl. 5 : A23L 1/16. k 72 Inventor/es: Guarneri, Roberto. k 74 Agente: Elzaburu Márquez, Fernando
 19 OFICINA ESPAÑOLA DE PATENTES Y MARCAS ESPAÑA 11 N. de publicación: ES 2 062 848 1 Int. Cl. : A23L 1/16 12 TRADUCCION DE PATENTE EUROPEA T3 86 Número de solicitud europea: 92876.7 86 Fecha de presentación
19 OFICINA ESPAÑOLA DE PATENTES Y MARCAS ESPAÑA 11 N. de publicación: ES 2 062 848 1 Int. Cl. : A23L 1/16 12 TRADUCCION DE PATENTE EUROPEA T3 86 Número de solicitud europea: 92876.7 86 Fecha de presentación
GUÍA DE CONTENIDOS MÍNIMOS DEL PLAN DE TRANSICIÓN TÉCNICA DE LOS SISTEMAS ATM/ANS
 ÍNDICE 1. OBJETO... 4 2. ÁMBITO DE APLICACIÓN... 4 3. ANTECEDENTES NORMATIVOS... 4 4. DOCUMENTACIÓN DE REFERENCIA... 6 5. CONTENIDOS MÍNIMOS A INCLUIR EN EL PLAN DE TRANSICIÓN TÉCNICA... 7 5.1. INICIO
ÍNDICE 1. OBJETO... 4 2. ÁMBITO DE APLICACIÓN... 4 3. ANTECEDENTES NORMATIVOS... 4 4. DOCUMENTACIÓN DE REFERENCIA... 6 5. CONTENIDOS MÍNIMOS A INCLUIR EN EL PLAN DE TRANSICIÓN TÉCNICA... 7 5.1. INICIO
Int. Cl. 5 : A23L 1/31
 k 19 OFICINA ESPAÑOLA DE PATENTES Y MARCAS ESPAÑA 11 k N. de publicación: ES 2 064 268 21 k Número de solicitud: 90526 51 k Int. Cl. 5 : A23L 1/31 k 12 SOLICITUD DE PATENTE A1 k 22 Fecha de presentación:
k 19 OFICINA ESPAÑOLA DE PATENTES Y MARCAS ESPAÑA 11 k N. de publicación: ES 2 064 268 21 k Número de solicitud: 90526 51 k Int. Cl. 5 : A23L 1/31 k 12 SOLICITUD DE PATENTE A1 k 22 Fecha de presentación:
II. INDICADORES DE EVALUACIÓN Y RELACIÓN CON COMPETENCIAS BÁSICAS CRITERIOS DE EVALUACIÓN
 1 11 1 1 CL CM CCyIMF CTIyCD CSyC CSyA CAA CAeIP CE UNIDAD DIDÁCTICA Nº PROPIEDADES DE LA MATERIA I. CONTENIDOS Materia, cuerpos materiales y sistemas materiales* Propiedades de la materia: intensivas
1 11 1 1 CL CM CCyIMF CTIyCD CSyC CSyA CAA CAeIP CE UNIDAD DIDÁCTICA Nº PROPIEDADES DE LA MATERIA I. CONTENIDOS Materia, cuerpos materiales y sistemas materiales* Propiedades de la materia: intensivas
ES A1. Número de publicación: PATENTES Y MARCAS. Número de solicitud: Int. Cl. 7 : B01D 61/02
 k 19 OFICINA ESPAÑOLA DE PATENTES Y MARCAS ESPAÑA 11 k Número de publicación: 2 198 186 21 k Número de solicitud: 200102121 1 k Int. Cl. 7 : B01D 61/02 k 12 SOLICITUD DE PATENTE A1 k 22 Fecha de presentación:
k 19 OFICINA ESPAÑOLA DE PATENTES Y MARCAS ESPAÑA 11 k Número de publicación: 2 198 186 21 k Número de solicitud: 200102121 1 k Int. Cl. 7 : B01D 61/02 k 12 SOLICITUD DE PATENTE A1 k 22 Fecha de presentación:
procedimiento específico
 procedimiento específico Medición de gases contaminantes [ex PGM-44.82-BAN] Código: Edición: 5 Responsable Elaborado Revisado Aprobado Medio Ambiente DANIEL P. CASSANO Prevención, Salud, Medio Ambiente
procedimiento específico Medición de gases contaminantes [ex PGM-44.82-BAN] Código: Edición: 5 Responsable Elaborado Revisado Aprobado Medio Ambiente DANIEL P. CASSANO Prevención, Salud, Medio Ambiente
Metodología Indagar I
 Metodología Indagar I ÁREA DE INTERÉS Explorar Decidir sobre FOCALIZACIÓN Indicar posibles cuestiones para indagar Decidir sobre CUESTIÓN PRINCIPAL Anticipar resultados Búsqueda de evidencia Mantenerse
Metodología Indagar I ÁREA DE INTERÉS Explorar Decidir sobre FOCALIZACIÓN Indicar posibles cuestiones para indagar Decidir sobre CUESTIÓN PRINCIPAL Anticipar resultados Búsqueda de evidencia Mantenerse
ES A1 B29C 70/30 //B29L 23:00. Número de publicación: PATENTES Y MARCAS. Número de solicitud: Int. Cl.
 k 19 OFICINA ESPAÑOLA DE PATENTES Y MARCAS ESPAÑA 11 k Número de publicación: 2 146 498 21 k Número de solicitud: 009601963 51 k Int. Cl. 7 : B29C 53/70 B29C 70/30 //B29L 23:00 k 12 SOLICITUD DE PATENTE
k 19 OFICINA ESPAÑOLA DE PATENTES Y MARCAS ESPAÑA 11 k Número de publicación: 2 146 498 21 k Número de solicitud: 009601963 51 k Int. Cl. 7 : B29C 53/70 B29C 70/30 //B29L 23:00 k 12 SOLICITUD DE PATENTE
ES A1. Número de publicación: PATENTES Y MARCAS. Número de solicitud: Int. Cl. 6 : A23G 1/00
 k 19 OFICINA ESPAÑOLA DE PATENTES Y MARCAS ESPAÑA 11 k Número de publicación: 2 141 023 21 k Número de solicitud: 00970 1 k Int. Cl. 6 : A23G 1/00 k 12 SOLICITUD DE PATENTE A1 k 22 Fecha de presentación:
k 19 OFICINA ESPAÑOLA DE PATENTES Y MARCAS ESPAÑA 11 k Número de publicación: 2 141 023 21 k Número de solicitud: 00970 1 k Int. Cl. 6 : A23G 1/00 k 12 SOLICITUD DE PATENTE A1 k 22 Fecha de presentación:
ES A2 ESPAÑA 11. Número de publicación: Número de solicitud: C22C 13/00 ( )
 19 OFICINA ESPAÑOLA DE PATENTES Y MARCAS ESPAÑA 11 21 Número de publicación: 2 418 279 Número de solicitud: 201131629 51 Int. CI.: C22C 13/00 (2006.01) 12 SOLICITUD DE PATENTE A2 22 Fecha de presentación:
19 OFICINA ESPAÑOLA DE PATENTES Y MARCAS ESPAÑA 11 21 Número de publicación: 2 418 279 Número de solicitud: 201131629 51 Int. CI.: C22C 13/00 (2006.01) 12 SOLICITUD DE PATENTE A2 22 Fecha de presentación:
Int. Cl. 5 : A23L 1/317
 k 19 OFICINA ESPAÑOLA DE PATENTES Y MARCAS ESPAÑA 11 k N. de publicación: ES 2 068 12 21 k Número de solicitud: 91421 1 k Int. Cl. : A23L 1/317 A23L 1/36 k 12 SOLICITUD DE PATENTE A1 22 kfecha de presentación:
k 19 OFICINA ESPAÑOLA DE PATENTES Y MARCAS ESPAÑA 11 k N. de publicación: ES 2 068 12 21 k Número de solicitud: 91421 1 k Int. Cl. : A23L 1/317 A23L 1/36 k 12 SOLICITUD DE PATENTE A1 22 kfecha de presentación:
RELACIONES CUANTITATIVAS PARA EL RELLENO DE PLAYAS
 LIBRO: TEMA: PUE. Puertos PARTE: 1. ESTUDIOS TÍTULO: 07. Estudios de Transporte Litoral CAPÍTULO: A. 009. Estimación del Relleno de Playas para Modificar su Perfil CONTENIDO Este Manual describe el procedimiento
LIBRO: TEMA: PUE. Puertos PARTE: 1. ESTUDIOS TÍTULO: 07. Estudios de Transporte Litoral CAPÍTULO: A. 009. Estimación del Relleno de Playas para Modificar su Perfil CONTENIDO Este Manual describe el procedimiento
Int. Cl. 7 : G01K 1/14
 k 19 OFICINA ESPAÑOLA DE PATENTES Y MARCAS ESPAÑA 11 k Número de publicación: 1 04 91 21 k Número de solicitud: U 00976 1 k Int. Cl. 7 : G01K 1/14 //A61B /01 k 12 SOLICITUD DE MODELO DE UTILIDAD U 22 kfecha
k 19 OFICINA ESPAÑOLA DE PATENTES Y MARCAS ESPAÑA 11 k Número de publicación: 1 04 91 21 k Número de solicitud: U 00976 1 k Int. Cl. 7 : G01K 1/14 //A61B /01 k 12 SOLICITUD DE MODELO DE UTILIDAD U 22 kfecha
ES U ESPAÑA 11. Número de publicación: Número de solicitud: A47D 1/10 ( ) B62J 9/00 ( )
 19 OFICINA ESPAÑOLA DE PATENTES Y MARCAS ESPAÑA 11 21 Número de publicación: 1 127 86 Número de solicitud: 201430977 1 Int. CI.: A47D 1/10 (2006.01) B62J 9/00 (2006.01) 12 SOLICITUD DE MODELO DE UTILIDAD
19 OFICINA ESPAÑOLA DE PATENTES Y MARCAS ESPAÑA 11 21 Número de publicación: 1 127 86 Número de solicitud: 201430977 1 Int. CI.: A47D 1/10 (2006.01) B62J 9/00 (2006.01) 12 SOLICITUD DE MODELO DE UTILIDAD
ES A1 ESPAÑA 11. Número de publicación: Número de solicitud: A61K 36/00 ( )
 19 OFICINA ESPAÑOLA DE PATENTES Y MARCAS ESPAÑA 11 21 Número de publicación: 2 74 40 Número de solicitud: 20163087 1 Int. CI.: A61K 36/00 (2006.01) 12 SOLICITUD DE PATENTE A1 22 Fecha de presentación:
19 OFICINA ESPAÑOLA DE PATENTES Y MARCAS ESPAÑA 11 21 Número de publicación: 2 74 40 Número de solicitud: 20163087 1 Int. CI.: A61K 36/00 (2006.01) 12 SOLICITUD DE PATENTE A1 22 Fecha de presentación:
11 knúmero de publicación: kint. Cl. 7 : G01C 9/26
 k 19 OFICINA ESPAÑOLA DE PATENTES Y MARCAS ESPAÑA 11 knúmero de publicación: 2 18 4 1 kint. Cl. 7 : G01C 9/26 G01C 2/00 B22F 3/11 12 k TRADUCCION DE PATENTE EUROPEA T3 86 knúmero de solicitud europea:
k 19 OFICINA ESPAÑOLA DE PATENTES Y MARCAS ESPAÑA 11 knúmero de publicación: 2 18 4 1 kint. Cl. 7 : G01C 9/26 G01C 2/00 B22F 3/11 12 k TRADUCCION DE PATENTE EUROPEA T3 86 knúmero de solicitud europea:
Procedimientos de reproducción asistida! 21. Capítulo 1. Descripción de procedimientos de reproducción asistida 2008! 22
 Tabla de contenidos Resumen! 18 Introducción! 19 Objetivos! 19 Procedimientos incluidos! 19 Novedades! 19 Estructura! 19 Información! 20 Origen de la información! 20 Cohorte! 20 Validación de los datos!
Tabla de contenidos Resumen! 18 Introducción! 19 Objetivos! 19 Procedimientos incluidos! 19 Novedades! 19 Estructura! 19 Información! 20 Origen de la información! 20 Cohorte! 20 Validación de los datos!
G2.- Competencia para aplicar los conocimientos adquiridos.
 Competencias generales El egresado del Título de Máster en Técnicas Avanzadas en Química adquirirá al menos las siguientes competencias generales, que desarrollan las competencias básicas previstas en
Competencias generales El egresado del Título de Máster en Técnicas Avanzadas en Química adquirirá al menos las siguientes competencias generales, que desarrollan las competencias básicas previstas en
RESUMEN DE LA POLÍTICA DE CONFLICTOS DE INTERÉS GRUPO CIMD
 RESUMEN DE LA POLÍTICA DE CONFLICTOS DE INTERÉS GRUPO CIMD Versión 31.10.2014 I. INTRODUCCIÓN La normativa vigente, legislación comunitaria MiFID (Directiva 2004/39/CE del Parlamento Europeo y de la Comisión
RESUMEN DE LA POLÍTICA DE CONFLICTOS DE INTERÉS GRUPO CIMD Versión 31.10.2014 I. INTRODUCCIÓN La normativa vigente, legislación comunitaria MiFID (Directiva 2004/39/CE del Parlamento Europeo y de la Comisión
ES A1. Número de publicación: PATENTES Y MARCAS. Número de solicitud: Int. Cl. 7 : A42B 3/04
 k 19 OFICINA ESPAÑOLA DE PATENTES Y MARCAS ESPAÑA 11 k Número de publicación: 2 145 666 21 k Número de solicitud: 009700221 51 k Int. Cl. 7 : A42B 3/04 k 12 SOLICITUD DE PATENTE A1 k 22 Fecha de presentación:
k 19 OFICINA ESPAÑOLA DE PATENTES Y MARCAS ESPAÑA 11 k Número de publicación: 2 145 666 21 k Número de solicitud: 009700221 51 k Int. Cl. 7 : A42B 3/04 k 12 SOLICITUD DE PATENTE A1 k 22 Fecha de presentación:
La concentración másica (C)
 La concentración másica (C) Apellidos, nombre Atarés Huerta, Lorena (loathue@tal.upv.es) Departamento Centro Departamento de Tecnología de Alimentos ETSIAMN (Universidad Politécnica de Valencia) 1 Resumen
La concentración másica (C) Apellidos, nombre Atarés Huerta, Lorena (loathue@tal.upv.es) Departamento Centro Departamento de Tecnología de Alimentos ETSIAMN (Universidad Politécnica de Valencia) 1 Resumen
PATENTES: REQUISITOS Y BASES DE DATOS
 PATENTES: REQUISITOS Y BASES DE DATOS Claves para la protección de nuevos productos y de tecnología Pablo López de Unceta pablo.lopez@oepm.es QUÉ ES UNA PATENTE? CONTRATO ADMINISTRACIÓN Concede un MONOPOLIO
PATENTES: REQUISITOS Y BASES DE DATOS Claves para la protección de nuevos productos y de tecnología Pablo López de Unceta pablo.lopez@oepm.es QUÉ ES UNA PATENTE? CONTRATO ADMINISTRACIÓN Concede un MONOPOLIO
Trabajo Profesional Ingeniería Civil Construcciones Ciclos de Proyectos
 Trabajo Profesional Ingeniería Civil Construcciones 74.99 Ciclos de Proyectos 1 Proyecto Es un esfuerzo temporal, que se lleva a cabo para crear un producto, servicio o resultado único, de modo de alcanzar
Trabajo Profesional Ingeniería Civil Construcciones 74.99 Ciclos de Proyectos 1 Proyecto Es un esfuerzo temporal, que se lleva a cabo para crear un producto, servicio o resultado único, de modo de alcanzar
CONTROL DE LECTURA QUE SON LAS AUDITORIAS AMBIENTALES Y PARA QUE SIRVEN?
 CONTROL DE LECTURA QUE SON LAS AUDITORIAS AMBIENTALES Y PARA QUE SIRVEN? AUDITORÍAS AMBIENTALES Auditoría Ambiental: Objetivo La auditoría evalúa el papel del seguimiento y el cumplimiento de las medidas
CONTROL DE LECTURA QUE SON LAS AUDITORIAS AMBIENTALES Y PARA QUE SIRVEN? AUDITORÍAS AMBIENTALES Auditoría Ambiental: Objetivo La auditoría evalúa el papel del seguimiento y el cumplimiento de las medidas
GRAFICOS DE CONTROL DATOS TIPO VARIABLES
 GRAFICOS DE CONTROL DATOS TIPO VARIABLES OBJETIVO DEL LABORATORIO El objetivo del presente laboratorio es que el estudiante conozca y que sea capaz de seleccionar y utilizar gráficos de control, para realizar
GRAFICOS DE CONTROL DATOS TIPO VARIABLES OBJETIVO DEL LABORATORIO El objetivo del presente laboratorio es que el estudiante conozca y que sea capaz de seleccionar y utilizar gráficos de control, para realizar
Dirección General de Salud Pública
 Dirección General de Salud Pública Se aplica a los siguientes productos de la pesca: - Peces vivos. - Pescado fresco o refrigerado o congelado. - Filetes y demás carne de pescado frescos, refrigerados
Dirección General de Salud Pública Se aplica a los siguientes productos de la pesca: - Peces vivos. - Pescado fresco o refrigerado o congelado. - Filetes y demás carne de pescado frescos, refrigerados
Aulas Virtuales IECSCYL. Manual de uso
 Aulas Virtuales IECSCYL Manual de uso Fundación Instituto de Estudios de Ciencias de la Salud de Castilla y León 1 ÍNDICE: 1. Acceso a las Aulas Virtuales del IECSCYL... 3 2. Inicio de Sesión... 4 2.1.
Aulas Virtuales IECSCYL Manual de uso Fundación Instituto de Estudios de Ciencias de la Salud de Castilla y León 1 ÍNDICE: 1. Acceso a las Aulas Virtuales del IECSCYL... 3 2. Inicio de Sesión... 4 2.1.
ES U. Número de publicación: PATENTES Y MARCAS. Número de solicitud: U Int. Cl. 7 : B05C 21/00
 k 19 OFICINA ESPAÑOLA DE PATENTES Y MARCAS ESPAÑA 11 k Número de publicación: 1 03 89 21 k Número de solicitud: U 00211 1 k Int. Cl. 7 : B0C 21/00 k 12 SOLICITUD DE MODELO DE UTILIDAD U k 22 Fecha de presentación:
k 19 OFICINA ESPAÑOLA DE PATENTES Y MARCAS ESPAÑA 11 k Número de publicación: 1 03 89 21 k Número de solicitud: U 00211 1 k Int. Cl. 7 : B0C 21/00 k 12 SOLICITUD DE MODELO DE UTILIDAD U k 22 Fecha de presentación:
51 Int. CI.: H04L 12/58 ( ) TRADUCCIÓN DE PATENTE EUROPEA
 19 OFICINA ESPAÑOLA DE PATENTES Y MARCAS ESPAÑA 11 Número de publicación: 2 4 383 1 Int. CI.: H04L 12/8 (06.01) 12 TRADUCCIÓN DE PATENTE EUROPEA T3 96 Fecha de presentación y número de la solicitud europea:
19 OFICINA ESPAÑOLA DE PATENTES Y MARCAS ESPAÑA 11 Número de publicación: 2 4 383 1 Int. CI.: H04L 12/8 (06.01) 12 TRADUCCIÓN DE PATENTE EUROPEA T3 96 Fecha de presentación y número de la solicitud europea:
LISTADO DE NORMAS TÉCNICAS DE CALZADO
 LISTADO DE NORMAS TÉCNICAS DE CALZADO NTP 241.024:2009 CALZADO. Etiquetado informativo para el consumidor. 2ª. Ed. Resumen: Establece los conceptos y criterios claros para un etiquetado informativo del
LISTADO DE NORMAS TÉCNICAS DE CALZADO NTP 241.024:2009 CALZADO. Etiquetado informativo para el consumidor. 2ª. Ed. Resumen: Establece los conceptos y criterios claros para un etiquetado informativo del
k 11 N. de publicación: ES k 21 Número de solicitud: k 51 Int. Cl. 5 : A01G 9/02
 k 19 OFICINA ESPAÑOLA DE PATENTES Y MARCAS ESPAÑA k 11 N. de publicación: ES 2 042 406 k 21 Número de solicitud: 9200656 k 51 Int. Cl. 5 : A01G 9/02 A01G 31/02 k 12 SOLICITUD DE PATENTE A1 22 kfecha de
k 19 OFICINA ESPAÑOLA DE PATENTES Y MARCAS ESPAÑA k 11 N. de publicación: ES 2 042 406 k 21 Número de solicitud: 9200656 k 51 Int. Cl. 5 : A01G 9/02 A01G 31/02 k 12 SOLICITUD DE PATENTE A1 22 kfecha de
SUBCONTRATAS, PROVEEDORES: BUENAS PRACTICAS MEDIOAMBIENTALES
 Página 1 de 7 PORTADA Este procedimiento es propiedad de PENTIA INGENIEROS, S.A. y podrá ser modificado, por las personas autorizadas, siempre que se estime conveniente. No genera ningún derecho de cliente,
Página 1 de 7 PORTADA Este procedimiento es propiedad de PENTIA INGENIEROS, S.A. y podrá ser modificado, por las personas autorizadas, siempre que se estime conveniente. No genera ningún derecho de cliente,
Int. Cl. 6 : A01N 43/40
 k 19 OFICINA ESPAÑOLA DE PATENTES Y MARCAS ESPAÑA 11 k Número de publicación: 2 9 866 21 k Número de solicitud: 90023 1 k Int. Cl. 6 : A01N 43/ //(A01N 43/ A01N 41:04 A01N 3:06) k 12 SOLICITUD DE PATENTE
k 19 OFICINA ESPAÑOLA DE PATENTES Y MARCAS ESPAÑA 11 k Número de publicación: 2 9 866 21 k Número de solicitud: 90023 1 k Int. Cl. 6 : A01N 43/ //(A01N 43/ A01N 41:04 A01N 3:06) k 12 SOLICITUD DE PATENTE
PRÁCTICA Nº 3 PROPIEDADES COLIGATIVAS: DETERMINACIÓN DE LA MASA MOLECULAR DE UN SOLUTO PROBLEMA POR CRIOSCOPIA
 PRÁCTICA Nº 3 PROPIEDADES COLIGATIVAS: DETERINACIÓN DE LA ASA OLECULAR DE UN SOLUTO PROBLEA POR CRIOSCOPIA OBJETIVOS: El objetivo de la práctica es el estudio del efecto que produce la adición de un soluto
PRÁCTICA Nº 3 PROPIEDADES COLIGATIVAS: DETERINACIÓN DE LA ASA OLECULAR DE UN SOLUTO PROBLEA POR CRIOSCOPIA OBJETIVOS: El objetivo de la práctica es el estudio del efecto que produce la adición de un soluto
Int. Cl. 7 : A47D 13/02
 k 19 OFICINA ESPAÑOLA DE PATENTES Y MARCAS ESPAÑA 11 k Número de publicación: 2 166 266 21 k Número de solicitud: 00990132 1 k Int. Cl. 7 : A47D 13/02 B60N 2/28 k 12 SOLICITUD DE PATENTE A1 22 kfecha de
k 19 OFICINA ESPAÑOLA DE PATENTES Y MARCAS ESPAÑA 11 k Número de publicación: 2 166 266 21 k Número de solicitud: 00990132 1 k Int. Cl. 7 : A47D 13/02 B60N 2/28 k 12 SOLICITUD DE PATENTE A1 22 kfecha de
Int. Cl. 6 : A61G 5/06. k 73 Titular/es: k 72 Inventor/es: k 74 Agente: Pons Ariño, Angel
 k 19 OFICINA ESPAÑOLA DE PATENTES Y MARCAS ESPAÑA 11 k Número de publicación: 2 132 020 21 k Número de solicitud: 009700823 51 k Int. Cl. 6 : A61G 5/06 B62B 5/02 B62B 9/02 k 12 PATENTEDEINVENCION B1 k
k 19 OFICINA ESPAÑOLA DE PATENTES Y MARCAS ESPAÑA 11 k Número de publicación: 2 132 020 21 k Número de solicitud: 009700823 51 k Int. Cl. 6 : A61G 5/06 B62B 5/02 B62B 9/02 k 12 PATENTEDEINVENCION B1 k
