CAP. 1:ESTRUCTURAS CRISTALINAS
|
|
|
- Amparo Quiroga Parra
- hace 6 años
- Vistas:
Transcripción
1 CAP. 1:ESTRUCTURAS CRISTALINAS Sólidos cristalinos: amorfos: Disposiciones periódicas en el espacio Disposición al azar Situaciones intermedias: (no periódicas pero ordenadas) Estructuras moduladas Casicristales (Nobel Química 2011: D Shechtman Cristales líquidos Sólido cristalino Sólido amorfo (vidrio) Casicristal (R. Penrose) Simetría pentagonal
2 PERIODICIDAD DE LOS CRISTALES Periodicidad: f(r') = f(r) si r' = r + T, con T = n 1 a + n 2 b + n 3 c a, b, c =" periodos fundamentales" (vectores de traslación mínimos) Celda unidad primitiva: paralelepípedo formado con a, b y c Volumen celda: V C = a b c Independiente de la elección de a, b, c "base": motivo que se repite periódicamente en el espacio.
3 Algunas propiedades/convenciones: * Las coordenadas de un punto P (x,y,z) se expresan SIEMPRE (aunque no se diga expresamente) en unidades de los periodos fundamentales, o parámetros de celda a, b,c: Es decir el vector de posición de P es realmente r = xa +yb +zc. * x,y,z son números sin dimensiones físicas. * Debido a la periodicidad, si se suman o restan entero arbitrarios a las coordenadas se obtiene un punto equivalente pro traslación casi siempre se dan valores de x,y,z entre 0 y 1. * a,b,c se dan casi siempre en angstroms (si no se dice nada): (1 Å = m). Alguna vez en nm (1 nm = 10-9 m)
4 Ejemplo real: [Fe(NC 5 H 5 ) 2 {Ag(CN) 2 }] Molécula Red y celda unidad (Z=2)
5 Ej. Escalera de caracol ELEMENTOS DE SIMETRIA PUNTUALES 1, 2, 3, 4 ó 6: Ejes de simetría de orden n: rotación de 2 π /n, (en los cristales sólo puede ser n = 1, 2, 3, 4, 6) m :Reflexión especular respecto de un plano. Ej1: plano x = 0 (x, y, z) (-x, y,z) Ej.2 plano x = x 0 (x, y, z) (2x 0 -x, y, z) -1 : Centro de inversión. ej.1 centro de inversión en (0,0,0) (x,y,z) (-x, -y, -z) ej2:centro de inversión en (x 0, y 0, z 0 ) (x, y, z) (2x 0 -x, 2y 0 -y, 2z 0 -z) -2, -3, -4 ó -6 Centros de rotoinversión de orden n: inversión + rotación de orden n. Elementos combinados de puntuales y traslaciones a, b, c, n, d: Planos de deslizamiento: Reflexión especular + traslación de 1/2 o 1/4 de periodo paralelamente al plano (la letra indica la dirección de desplazamiento) 2 1, 3 1, 3 2, 4 1, 4 2, 6 1, 6 2, 6 3, 6 4, 6 5 Ejes helicoidales de orden n m : Rotación de 2π/n + traslación de m/n de periodo, paralelamente al eje.
6 Ejemplo: elementos puntuales de simetría de un prisma de base triangular Ejes de simetría DOS de los Planos de reflexión especular
7 SISTEMAS CRISTALINOS I Celda unidad: paralelepípedo construido con los vectores a, b y c (el origen elegido arbitrariamente) Posición de un punto en la celda: x, y, z, en unidades de a, b y c: r = xa +yb +zc (0 x, y, z 1) Parámetros de celda: a, b, c, α, β, γ, : b c c a a = a, b = b, c = c, cosα =,cos β =, cosγ = bc ca Puntos de la red: vértices de la celda y otros equivalentes por traslación pura. Son puntos matemáticos NO ATOMOS! Red cristalina: conjunto de puntos de la red Grupo espacial: (hay 230) a b ab {elementos de simetría} = {traslaciones} {puntuales} {combinadas} Elementos de simetría puntuales o combinados SISTEMAS CRISTALINOS
8 Imposibilidad de estructuras periódicas con ejes de 5º orden o de órdenes mayores al 6º Sistema cúbico "pentagonal" trigonal hexagonal
9 SISTEMAS CRISTALINOS II: Elementos característicos de simetría Monoclínico Tetragonal Romboédrico Hexagonal y Trigonal Ortorrómbico
10 SISTEMAS CRISTALINOS III Sistema Simetría mínima Restricciones celda Centrados posibles Triclínico 1 o bien -1 ninguna P Monoclínico m a c n β = 90º P C A Ortorrómbico 3 ejes binarios o planos α = β = γ = 90º P A B C I F perpendiculares Tetragonal a = b y α = β = γ = 90º P I Trigonal a = b, α = β= 90º γ = 120º P R Hexagonal a = b, α = β= 90º γ = 120º P Romboédrico a = b = c y α = β = γ 90º (primitiva) a = b, α = β= 90º γ = 120º(hex) R Cúbico Tetragonal + romboédrico a = b = c y α = β = γ = 90º P I F
11 REDES DE BRAVAIS I Primitivas o tipo P: a, b, c son los periodos de traslación pura mínimos. Centradas: a, b, c se escogen mayores que los periodos mínimos para ver mejor la simetría. Red CENTRADA EN EL CUERPO o tipo I: f(x,y,z) = f(x+1/2, y+1/2, z+1/2) *** para TODO punto x y z de la celda! *** NO ES que haya un átomo en (0,0,0) y otro en (1/2,1/2,1/2) Puntos de la red en los vértices y en el centro de la celda Puede ocurrir en los sistemas Ortorrómbico, Tetragonal y Cúbico Grupo espacial: Ejemplos: I (orto) I 4/mmm (tetr), I m-3m (cúbico) Nombre del grupo: tipo de centrado+ algunos elementos puntuales o combinados de simetría) Cuando es cúbico también se llama bcc (body centered cubic)
12 Vectores de traslación primitivos en una bcc Red primitiva de una bcc
13 REDES DE BRAVAIS II Red CENTRADA EN UNA CARA: x, y, z de la celda se cumple: tipo A: f(x,y,z) = f( x, y+1/2, z+1/2) tipo B: f(x,y,z) = f(x+1/2, y, z+1/2) tipo C: f(x,y,z) = f(x+1/2, y+1/2, z) Puede ocurrir en los sistemas Monoclínico y Ortorrómbico Grupo espacial: Ejemplos: C 2/m (monoclínico) Bmab (ortorrómbico)
14 REDES DE BRAVAIS III Red centrada EN LAS CARAS, o tipo F: Centrada en las tres bases: x,y,z de la celda: f(x,y,z) = f( x, y+1/2, z+1/2) =f(x+1/, y,z+1/2) =f(x+1/2, y+1/2, z) Puntos de la red en los vértices y en el centro de cada cara de la celda Puede ocurrir en los sistemas Ortorrómbico y Cúbico Grupos espaciales: Ejemplos: F mmm (ortorrómbico) F m-3m (cúbico) Caso cúbico: se llama también fcc (face centered cubic)
15 Vectores de traslación y celda primitiva en una red fcc Celda romboédrica primitiva y relación con los ejes hexagonales
16 REDES DE BRAVAIS IV: el romboédrico Caso particular de trigonal(ver fig. anterior). TOMANDO EJES HEXAGONALES (lo más frecuente): x,y,z f(x,y,z) = f( x+2/3, y+1/3, z+1/3) = f(x+1/3, y+2/3,z+2/3) Puntos de la red en los vértices, en (2/3,1/3,1/3) y en (1/3,2/3,2/3) Puede ocurrir en los sistemas Ortorrómbico y Cúbico Grupos espaciales: Ejemplos: R-3m, R 3c La celda primitiva (EJES ROMBOÉDRIICOS ) se usa porque se compara con el cúbico. Relación entre la celda primitiva (romboédrica) y la hexagonal: a H = a R - b R b H = b R - c R c H = a R + b R + c R
17 RESUMEN DE LOS SISTEMAS CRISTALINOS
18 PLANOS CRISTALINOS: INDICES DE MILLER (hkl) Indican la orientación de un plano cualquiera en el cristal Se obtienen mediante la siguienteb regla: 1) Buscar los cortes con los ejes: n 1, n 2, n 3 (en unidades de los parámetros de celda a, b, c) no siempre enteros. Si el plano es paralelo a un eje se pone 2) Calcular los inversos 1/n 1, 1/n 2, 1/n 3 3) Multiplicarlos por un factor adecuado hasta obtener tres enteros, lo más pequeños posible h,k,l Ejemplo: 1) n 1 = 3, n 2 = 2, n 3 = 2 2) 1/3, 1/2, 1/2 3) Multiplicamos por 6: (h,k,l) = (2 3 3)
19
20 ESTRUCTURAS CRISTALINAS DE ELEMENTOS METALICOS CUBICA CENTRADA EN EL CUERPO (elegimos el origen en un átomo) bcc, con átomos en (0,0,0) y (1/2,1/2,1/2) Z = 2, SG Im-3m, Distancia vecinos: 3 d = 2 r = a = a 2 Fracción empaquetamiento: Vatomos/Vtotal =π 3/8 = Ejemplos: α-fe, Ba, K, Cr, metales halógenos (unos 13 casos en total a P y T ambiente) CUBICA COMPACTA: fcc, con átomos en (0,0,0), (1/2,1/2,0), (1/2,0,1/2) (0, 1/2,1/2) Z = 4, SG Fm-3m, Distancia vecinos: d = 2 r = 2 a = a 2 Fracción empaquetamiento: π 2/6 = Vol por átomo: a 3 /4 (ej: Å 3 para Al) Ejemplos: γ-fe, Al, Cu, Ag, Au, unos 25 ejemplos
21 HEXAGONAL COMPACTA átomos en (0,0,0), (2/3, 1/3, 1/2) Z = 2, SG, P-6m2 c / a = 8/ 3 = (ideal) 2 Distancia vecinos: d = 2 r = a = a 2 Fracción empaquetamiento: π 2/6 = Ejemplos: α-co, Be, Mg,Ti, Zr... unos 30 elementos EMPAQUETAMINTO EN CUB y HEX COMPACTAS Cúbica: ABCABC... Hexagonal: ABABAB...
22 ESTRUCTURA DE DIAMANTE fcc, átomos en (0,0,0), (1/4,1/4,1/4), + centrado F Z = 8, SG: Fd-3m, Distancia vecinos: ( 3)a/4 Fracción empaquetamiento: ( 3)π/16 = 0.34 Volumen por átomo: a 3 /8 (=5.64 Å 3 para C) Ejemplos: C, Si, Ge, Sn ESTRUCTURA DE GRAFITO (C puro) Hexagonal (0,0,0), (2/3,1/3,0), (no hcp) (0,0,1/2),(1/3, 2/3,1/2) Z = 4, SG P6 3 mc, a = , c = Distancia vecinos: plano d xy =a/ 3 =1.421 Å interplanos: d z = c/2 = A Volumen por átomo: 3a 2 c/8 = 8.80 Å 3
23 ESTRUCTURAS CRISTALINAS DE COMPUESTOS SIMPLES (pocas) CsCl (Pm-3m) CUBICA SIMPLE, no bcc NaCl (Fm-3m) Fluorita CaF 2 Rutilo TiO 2 Cincblenda: ZnS fcc pero diferente Perovskita (Pm-3m)
Física del Estado Sólido REDES CRISTALINAS. Dr. Andrés Ozols. Facultad de Ingeniería Universidad de Buenos Aires. Dr. A. Ozols 1
 Física del Estado Sólido REDES CRISTALINAS Dr. Andrés Ozols Facultad de Ingeniería Universidad de Buenos Aires 2009 Dr. A. Ozols 1 ÁTOMOS EN SÓLIDOS Dr. A. Ozols 2 ORDEN CRISTALINO y FORMA René Just Hauy
Física del Estado Sólido REDES CRISTALINAS Dr. Andrés Ozols Facultad de Ingeniería Universidad de Buenos Aires 2009 Dr. A. Ozols 1 ÁTOMOS EN SÓLIDOS Dr. A. Ozols 2 ORDEN CRISTALINO y FORMA René Just Hauy
LABORATORIO DE ESTADO SÓLIDO Y SEMICONDUCTORES 1.1. PRÁCTICA N o 1 REDES DE BRAVAIS Y ESTRUCTURAS CRISTALINAS
 LABORATORIO DE ESTADO SÓLIDO Y SEMICONDUCTORES 1.1 PRÁCTICA N o 1 REDES DE BRAVAIS Y ESTRUCTURAS CRISTALINAS 1. INTRODUCCIÓN 1.1 Red de Bravais y celda primitiva unidad Uno de los conceptos fundamentales
LABORATORIO DE ESTADO SÓLIDO Y SEMICONDUCTORES 1.1 PRÁCTICA N o 1 REDES DE BRAVAIS Y ESTRUCTURAS CRISTALINAS 1. INTRODUCCIÓN 1.1 Red de Bravais y celda primitiva unidad Uno de los conceptos fundamentales
Diagrama de correlación de enlaces moleculares Antienlace : rojo 1s similar a 2s
 Redes Cristalinas Ciencia de Materiales Ing. en Mecatrónica Otoño 2009 Lilia Meza Montes-IFUAP Diagrama de correlación de enlaces moleculares Antienlace : rojo 1s similar a 2s Sólidos cristalinos y amorfos
Redes Cristalinas Ciencia de Materiales Ing. en Mecatrónica Otoño 2009 Lilia Meza Montes-IFUAP Diagrama de correlación de enlaces moleculares Antienlace : rojo 1s similar a 2s Sólidos cristalinos y amorfos
Estructura de los Sólidos
 Estructura de los Sólidos Estructura Cristalina OBJETIVOS a) Definir sólidos cristalinos y amorfos b) Definir estructura cristalina c) Describir las diferentes estructuras cristalinas d) Utilizar índices
Estructura de los Sólidos Estructura Cristalina OBJETIVOS a) Definir sólidos cristalinos y amorfos b) Definir estructura cristalina c) Describir las diferentes estructuras cristalinas d) Utilizar índices
CRISTALOGRAFIA. Es un sólido compuesto de átomos, iones o moléculas ordenados de una cierta forma y que se repite en tres dimensiones.
 CRISTALOGRAFIA CRISTAL SÓLIDO MONOCRISTALINO SÓLIDO POLICRISTALINO Es un sólido compuesto de átomos, iones o moléculas ordenados de una cierta forma y que se repite en tres dimensiones. Región donde el
CRISTALOGRAFIA CRISTAL SÓLIDO MONOCRISTALINO SÓLIDO POLICRISTALINO Es un sólido compuesto de átomos, iones o moléculas ordenados de una cierta forma y que se repite en tres dimensiones. Región donde el
Capítulo 2 La estructura de los sólidos cristalinos
 Capítulo 2 La estructura de los sólidos cristalinos TEMA 2: La estructura de los sólidos cristalinos 1. Los enlaces interatómicos 2. La estructura cristalina 3. Estructuras de empaquetamiento compacto
Capítulo 2 La estructura de los sólidos cristalinos TEMA 2: La estructura de los sólidos cristalinos 1. Los enlaces interatómicos 2. La estructura cristalina 3. Estructuras de empaquetamiento compacto
Estructura Interna de los Materiales
 TEMA III Estructura Interna de los Materiales LECCIÓN 3 Estructura Cristalina y Amorfa 1 3.1 ESTADOS DE LA MATERIA Ciencia y Tecnología de los Materiales La materia puede presentarse en tres estados: gaseoso,
TEMA III Estructura Interna de los Materiales LECCIÓN 3 Estructura Cristalina y Amorfa 1 3.1 ESTADOS DE LA MATERIA Ciencia y Tecnología de los Materiales La materia puede presentarse en tres estados: gaseoso,
Contenido. 5. Estructura cristalina. Omar De la Peña-Seaman IFUAP Física del Estado Sólido Maestría (Física) 1/51 51
 Contenido 5. Estructura cristalina 1 / Omar De la Peña-Seaman IFUAP Física del Estado Sólido Maestría (Física) 1/51 51 Contenido: Tema 05 5. Estructura cristalina 5.1 Arreglo periódico de átomos: bases,
Contenido 5. Estructura cristalina 1 / Omar De la Peña-Seaman IFUAP Física del Estado Sólido Maestría (Física) 1/51 51 Contenido: Tema 05 5. Estructura cristalina 5.1 Arreglo periódico de átomos: bases,
Introducción a la Física del Estado Sólido
 Semana 1. Estructura cristalina. Definición de arreglos periódicos. Tipos de redes. Clasificación de simetrías. Índices de planos cristalinos. Ejemplos de estructuras cristalinas simples. Cristales no
Semana 1. Estructura cristalina. Definición de arreglos periódicos. Tipos de redes. Clasificación de simetrías. Índices de planos cristalinos. Ejemplos de estructuras cristalinas simples. Cristales no
3. La estructura de sólidos cristalinos 3.1 Conceptos fundamentales 3.2 Celda unitaria 3.3 Redes de Bravias 3.4 Estructuras cristalinas 3.
 Contenido 3. La estructura de sólidos cristalinos 3.1 Conceptos fundamentales 3.2 Celda unitaria 3.3 Redes de Bravias 3.4 Estructuras cristalinas 3.5 Volumen y densidad 3.6 Direcciones y planos cristalográficos
Contenido 3. La estructura de sólidos cristalinos 3.1 Conceptos fundamentales 3.2 Celda unitaria 3.3 Redes de Bravias 3.4 Estructuras cristalinas 3.5 Volumen y densidad 3.6 Direcciones y planos cristalográficos
LABORATORIO DE ESTADO SÓLIDO Y SEMICONDUCTORES 1.1. PRÁCTICA N o 1 REDES DE BRAVAIS Y ESTRUCTURAS CRISTALINAS
 LABORATORIO DE ESTADO SÓLIDO Y SEMICONDUCTORES 1.1 PRÁCTICA N o 1 REDES DE BRAVAIS Y ESTRUCTURAS CRISTALINAS 1. INTRODUCCIÓN 1.1 Red de Bravais y celda primitiva unidad Uno de los conceptos fundamentales
LABORATORIO DE ESTADO SÓLIDO Y SEMICONDUCTORES 1.1 PRÁCTICA N o 1 REDES DE BRAVAIS Y ESTRUCTURAS CRISTALINAS 1. INTRODUCCIÓN 1.1 Red de Bravais y celda primitiva unidad Uno de los conceptos fundamentales
GEOMETRÍA DE LOS CRISTALES I
 CAPÍTULO 4 GEOMETRÍA DE LOS CRISTALES I 4.1 REDES Conjuntos de puntos imaginarios que tienen una relación fija en el espacio constituyendo un armazón sobre el cual el cristal se construye. En la Figura
CAPÍTULO 4 GEOMETRÍA DE LOS CRISTALES I 4.1 REDES Conjuntos de puntos imaginarios que tienen una relación fija en el espacio constituyendo un armazón sobre el cual el cristal se construye. En la Figura
UNIDAD 1: LA MATERIA CRISTALINA
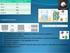 UNIDAD 1: LA MATERIA CRISTALINA CONCEPTOS MATERIA CRISTALINA: Aquella cuyas partículas están perfectamente ordenadas en el espacio, ocupando posiciones fijas y a distancias regulares unas de otras, formando
UNIDAD 1: LA MATERIA CRISTALINA CONCEPTOS MATERIA CRISTALINA: Aquella cuyas partículas están perfectamente ordenadas en el espacio, ocupando posiciones fijas y a distancias regulares unas de otras, formando
Capítulo 2 La estructura de los sólidos cristalinos
 Capítulo 2 La estructura de los sólidos cristalinos TEMA 2: La estructura de los sólidos cristalinos 1. Los enlaces interatómicos 2. La estructura cristalina 3. Estructuras cristalinas compactas 4. Direcciones
Capítulo 2 La estructura de los sólidos cristalinos TEMA 2: La estructura de los sólidos cristalinos 1. Los enlaces interatómicos 2. La estructura cristalina 3. Estructuras cristalinas compactas 4. Direcciones
MODIFICACIÓN DE LAS PROPIEDADES DE LOS METALES CONTENIDOS
 MODIFICACIÓN DE LAS PROPIEDADES DE LOS METALES CONTENIDOS Generalidades Estructura interna de los metales. Defectos en la estructura cristalina Soluciones sólidas Mecanismos de endurecimiento de los metales
MODIFICACIÓN DE LAS PROPIEDADES DE LOS METALES CONTENIDOS Generalidades Estructura interna de los metales. Defectos en la estructura cristalina Soluciones sólidas Mecanismos de endurecimiento de los metales
Tema 2.- Estructura de la Materia
 BLOQUE II.- ESTRUCTURA Estructura de la Materia * James F. Shackerlford Introducción a la Ciencia de Materiales para Ingenieros. Cuarta edición. Ed. Prentice Hall (1998) * Pat L. Mangonon Ciencia de Materiales:
BLOQUE II.- ESTRUCTURA Estructura de la Materia * James F. Shackerlford Introducción a la Ciencia de Materiales para Ingenieros. Cuarta edición. Ed. Prentice Hall (1998) * Pat L. Mangonon Ciencia de Materiales:
Estructuras Cristalinas. Julio Alberto Aguilar Schafer
 Estructuras Cristalinas Julio Alberto Aguilar Schafer Modelo del estado líquido los metales Modelo del paso del estado líquido al estado sólido de los metales Equilibrio líquido-vapor Presión de vapor
Estructuras Cristalinas Julio Alberto Aguilar Schafer Modelo del estado líquido los metales Modelo del paso del estado líquido al estado sólido de los metales Equilibrio líquido-vapor Presión de vapor
Tema 9. SOLIDOS COVALENTES
 Tema 9. SOLIDOS COVALENTES Introducción Estructuras de no-metales Boro Carbono Fósforo Arsénico, Antimonio y Bismuto Selenio y Telurio Estructuras de óxidos Estructuras basadas en tetraedros Estructuras
Tema 9. SOLIDOS COVALENTES Introducción Estructuras de no-metales Boro Carbono Fósforo Arsénico, Antimonio y Bismuto Selenio y Telurio Estructuras de óxidos Estructuras basadas en tetraedros Estructuras
Materia Condensada. Sistemas Complejos.
 Materia Condensada. Sistemas Complejos http://www.fisica.unlp.edu.ar/magnet/fisicamcsc.htm Sistemas Complejos (Física de no-equilibrio): Complejidad intrínseca (fundamental) aplicaciones dificultades derivaciones
Materia Condensada. Sistemas Complejos http://www.fisica.unlp.edu.ar/magnet/fisicamcsc.htm Sistemas Complejos (Física de no-equilibrio): Complejidad intrínseca (fundamental) aplicaciones dificultades derivaciones
Siete sistemas y catorce retículos
 ESTRUCTURA CRISTALINA - PERFECCION Siete sistemas y catorce retículos Celda unitaria c a b Constantes reticulares o parámetros reticulares Longitud de los bordes Ángulos entre los ejes cristalográficos
ESTRUCTURA CRISTALINA - PERFECCION Siete sistemas y catorce retículos Celda unitaria c a b Constantes reticulares o parámetros reticulares Longitud de los bordes Ángulos entre los ejes cristalográficos
Síntesis y Caracterización Estructural de los Materiales Ángel Carmelo Prieto Colorado
 Síntesis y Caracterización Estructural de los Materiales Ángel Carmelo Prieto Colorado Física de la Materia Condensada, Cristalografía y Mineralogía. Facultad de Ciencias. Universidad de Valladolid. Estructura
Síntesis y Caracterización Estructural de los Materiales Ángel Carmelo Prieto Colorado Física de la Materia Condensada, Cristalografía y Mineralogía. Facultad de Ciencias. Universidad de Valladolid. Estructura
Estructura Cristalina de Sólidos
 Estructura Cristalina de Sólidos Relación entre estructura periódica y propiedades Bibliografía: 1. Solid State Physics. Ashcroft and Mermin. 2. Solid State Chemistry. West. 3. Química del Estado Sólido.
Estructura Cristalina de Sólidos Relación entre estructura periódica y propiedades Bibliografía: 1. Solid State Physics. Ashcroft and Mermin. 2. Solid State Chemistry. West. 3. Química del Estado Sólido.
ESTRUCTURA DE LOS MATERIALES 2. 25/02/2012 Elaboró Ing. Efrén Giraldo T. 1
 ESTRUCTURA DE LOS MATERIALES 2 25/02/2012 Elaboró Ing. Efrén Giraldo T. 1 FACTOR DE EMPAQUETAMIENTO FEA = (No de átomos por celda. Vol de un átomo) / V (celda) 25/02/2012 Elaboró Ing. Efrén Giraldo T.
ESTRUCTURA DE LOS MATERIALES 2 25/02/2012 Elaboró Ing. Efrén Giraldo T. 1 FACTOR DE EMPAQUETAMIENTO FEA = (No de átomos por celda. Vol de un átomo) / V (celda) 25/02/2012 Elaboró Ing. Efrén Giraldo T.
Estructura cristalina: Índices de Miller. Y en términos de grado de compacidad? Volumen de átomos= Volumen de la celda= ( ) 3
 1 Cuántos átomos hay en una celda unidad? Vértices 1/8 Caras 1/2 Número total de átomos en la celda unidad: 8 en los vértices: 8 x 1/8 = 1 6 en las caras: 6 x 1/2 = 3 Total: 4 átomos Y en términos de grado
1 Cuántos átomos hay en una celda unidad? Vértices 1/8 Caras 1/2 Número total de átomos en la celda unidad: 8 en los vértices: 8 x 1/8 = 1 6 en las caras: 6 x 1/2 = 3 Total: 4 átomos Y en términos de grado
Consideraciones sobre estructuras representativas
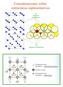 Consideraciones sobre estructuras representativas CONSIDERACIONES SOBRE ESTRUCTURAS REPRESENTATIVAS: En el empacamiento compacto hcp y ccp el número de coordinación es 12 Los elementos metálicos son los
Consideraciones sobre estructuras representativas CONSIDERACIONES SOBRE ESTRUCTURAS REPRESENTATIVAS: En el empacamiento compacto hcp y ccp el número de coordinación es 12 Los elementos metálicos son los
1.-La Cristalografía. 2.-Simetría
 1.-La Cristalografía La Cristalografía es la ciencia que se ocupa de los sólidos cristalinos y describe su estructura interna, es decir, como están distribuidos los átomos en su interior. También estudia
1.-La Cristalografía La Cristalografía es la ciencia que se ocupa de los sólidos cristalinos y describe su estructura interna, es decir, como están distribuidos los átomos en su interior. También estudia
Estructuras Cristalinas más usuales de Metales Puros (y de sus soluciones sólidas) Cristales metálicos
 Estructuras Cristalinas más usuales de Metales Puros (y de sus soluciones sólidas) Reglas generales Para un cristal al equilibrio químico, los átomos se ordenarán en forma regular y compacta, de manera
Estructuras Cristalinas más usuales de Metales Puros (y de sus soluciones sólidas) Reglas generales Para un cristal al equilibrio químico, los átomos se ordenarán en forma regular y compacta, de manera
ESTRUCTURAS CRISTALINAS (P2)
 ESTRUCTURAS CRISTALINAS (P2) Objetivos - Visualización de estructuras de sólidos mediante el uso de modelos - Estudio de redes cristalinas basadas en ordenamientos de esferas de igual tamaño - Identificación
ESTRUCTURAS CRISTALINAS (P2) Objetivos - Visualización de estructuras de sólidos mediante el uso de modelos - Estudio de redes cristalinas basadas en ordenamientos de esferas de igual tamaño - Identificación
TEMA 8 ESTRUCTURA CRISTALINA
 Tema 8. Estructura cristalina 1 TEMA 8 ESTRUCTURA CRISTALINA Los sólidos pueden clasificarse: 1.- Por su ordenación: 1a. Sólidos amorfos: tienen una estructura desordenada. Sus átomos o moléculas se colocan
Tema 8. Estructura cristalina 1 TEMA 8 ESTRUCTURA CRISTALINA Los sólidos pueden clasificarse: 1.- Por su ordenación: 1a. Sólidos amorfos: tienen una estructura desordenada. Sus átomos o moléculas se colocan
The problem of the structural biologist
 The problem of the structural biologist Biological function 3d structure of bio-molecules Structure and basic knowledge? Pure carbon: diamond Pure carbon: graphite The role of Crystallography Crystallography
The problem of the structural biologist Biological function 3d structure of bio-molecules Structure and basic knowledge? Pure carbon: diamond Pure carbon: graphite The role of Crystallography Crystallography
Módulo 3. Introducción a la cristalografía
 Módulo 3. Introducción a la cristalografía Poliedros cristalográficos recortables Un método muy recomendable para estudiar la forma y simetría de los cristales consiste en construir poliedros recortables.
Módulo 3. Introducción a la cristalografía Poliedros cristalográficos recortables Un método muy recomendable para estudiar la forma y simetría de los cristales consiste en construir poliedros recortables.
2. ESTRUCTURA DE LOS SÓLIDOS CRISTALINOS
 . ESTRUCTURA DE LOS SÓLIDOS CRISTALINOS MATERIALES 1/14 ÍNDICE 1. CONCEPTOS GENERALES. CELDILLA CRISTALINA. SISTEMAS CRISTALINOS. REDES DE BRAVAIS 4. DENSIDAD Y FACTOR DE EMPAQUETAMIENTO 5. ESTRUCTURAS
. ESTRUCTURA DE LOS SÓLIDOS CRISTALINOS MATERIALES 1/14 ÍNDICE 1. CONCEPTOS GENERALES. CELDILLA CRISTALINA. SISTEMAS CRISTALINOS. REDES DE BRAVAIS 4. DENSIDAD Y FACTOR DE EMPAQUETAMIENTO 5. ESTRUCTURAS
 Caso de varios vectores primitivos de un mismo arreglo. Base o Motivo: Átomo o conjunto de átomos que se asocian con un punto de la malla Malla o Lattice: Es un arreglo infinito de puntos en el espacio,
Caso de varios vectores primitivos de un mismo arreglo. Base o Motivo: Átomo o conjunto de átomos que se asocian con un punto de la malla Malla o Lattice: Es un arreglo infinito de puntos en el espacio,
Química Inorgánica-63.13- Dra.Silvia E. Jacobo. Sólidos. Estructuras Cristalinas
 Sólidos Estructuras Cristalinas Ordenamientos atómicos En gases no hay orden En líquidos hay orden de corto alcance En sólidos hay orden de largo alcance El ordenamiento está determinado por el tipo de
Sólidos Estructuras Cristalinas Ordenamientos atómicos En gases no hay orden En líquidos hay orden de corto alcance En sólidos hay orden de largo alcance El ordenamiento está determinado por el tipo de
Sólidos Arreglos y celdas unitarias. Ramón L. Hernández Castillo Enero 2012
 Sólidos Arreglos y celdas unitarias Ramón L. Hernández Castillo Enero 2012 Importancia de estudiar los sólidos cristalinos La mayoría de los compuestos inorgánicos son sólidos Casi todos los elementos
Sólidos Arreglos y celdas unitarias Ramón L. Hernández Castillo Enero 2012 Importancia de estudiar los sólidos cristalinos La mayoría de los compuestos inorgánicos son sólidos Casi todos los elementos
TEMA 1: ESTRUCTURA INTERNA DE LOS MATERIALES
 PERIODO Departamento de Tecnología. IES Nuestra Señora de la Almudena Mª Jesús Saiz TEMA 1: ESTRUCTURA INTERNA DE LOS MATERIALES El átomo: Toda la materia está compuesta por átomos y éstos por partículas
PERIODO Departamento de Tecnología. IES Nuestra Señora de la Almudena Mª Jesús Saiz TEMA 1: ESTRUCTURA INTERNA DE LOS MATERIALES El átomo: Toda la materia está compuesta por átomos y éstos por partículas
Estructura de sólidos
 Estructura de sólidos Química Inorgánica - 2006 Tipos de estructuras cristalinas cristal enlace características molecular covalente-baja energía cristales blandos, bajo p.f. red covalente covalente cristales
Estructura de sólidos Química Inorgánica - 2006 Tipos de estructuras cristalinas cristal enlace características molecular covalente-baja energía cristales blandos, bajo p.f. red covalente covalente cristales
Sobre la estructura periódica de los sólidos elementales
 Sobre la estructura periódica de los sólidos elementales Gonzalo Gutiérrez * gonzalo@fisica.ciencias.uchile.cl 3 Agosto 2004 Las diferentes propiedades de los materiales se reflejan con mucha claridad
Sobre la estructura periódica de los sólidos elementales Gonzalo Gutiérrez * gonzalo@fisica.ciencias.uchile.cl 3 Agosto 2004 Las diferentes propiedades de los materiales se reflejan con mucha claridad
TEMA 2: La Estructura de los sólidos cristalinos
 TEMA 2: La Estructura de los sólidos cristalinos 1. La plata solidifica en una estructura cúbica centrada en las caras (fcc). La masa atómica de la plata es 107.8682 y la longitud de la celda unidad, esto
TEMA 2: La Estructura de los sólidos cristalinos 1. La plata solidifica en una estructura cúbica centrada en las caras (fcc). La masa atómica de la plata es 107.8682 y la longitud de la celda unidad, esto
Estructura Atómica y Cristalina. Departamento de Tecnología IES San José
 1. INTRODUCCIÓN. Las propiedades y comportamiento de los materiales dependen, principalmente de su constitución y de su estructura. Por ello estudiaremos la disposición geométrica de los átomos y las interacciones
1. INTRODUCCIÓN. Las propiedades y comportamiento de los materiales dependen, principalmente de su constitución y de su estructura. Por ello estudiaremos la disposición geométrica de los átomos y las interacciones
4. El ClNa cristaliza en el sistema cúbico con parámetro [a]=5.631å. Calcular su densidad sabiendo que su masa molecular es 58.45 uma.
![4. El ClNa cristaliza en el sistema cúbico con parámetro [a]=5.631å. Calcular su densidad sabiendo que su masa molecular es 58.45 uma. 4. El ClNa cristaliza en el sistema cúbico con parámetro [a]=5.631å. Calcular su densidad sabiendo que su masa molecular es 58.45 uma.](/thumbs/28/12696458.jpg) Síntesis y Caracterización Estructural de los Materiales: Bases Cristalográficas. 1. Dibuje en las celdas fundamentales cúbicas adjuntas (a = 3 Å): a. Las filas reticulares de índices de Weiss [02-1],
Síntesis y Caracterización Estructural de los Materiales: Bases Cristalográficas. 1. Dibuje en las celdas fundamentales cúbicas adjuntas (a = 3 Å): a. Las filas reticulares de índices de Weiss [02-1],
Universidad de Murcia
 Universidad de Murcia CRISTALOGRAFÍA Control MURCIA 2011 2012 Francisco Cánovas Picón Índice Índice.............................................. 2 1. Problema 1.......................................
Universidad de Murcia CRISTALOGRAFÍA Control MURCIA 2011 2012 Francisco Cánovas Picón Índice Índice.............................................. 2 1. Problema 1.......................................
Tipos de estructuras. Introducción a la Ciencia de Materiales. M. Bizarro F. M. Sánchez
 Tipos de estructuras Empaquetamiento compacto Son estructuras formadas por átomos de igual tamaño que se unen mediante enlace metálico (esferas duras) A B A : A B C : FCC vs HCP El factor de empaquetamiento
Tipos de estructuras Empaquetamiento compacto Son estructuras formadas por átomos de igual tamaño que se unen mediante enlace metálico (esferas duras) A B A : A B C : FCC vs HCP El factor de empaquetamiento
Tema 4. Cristaloquímica. Descripción estructural y
 Tema 4. Cristaloquímica. Descripción estructural y estructuras tipos Qué objetivos tiene la Cristaloquímica? Las fases cristalinas son componentes esenciales de los materiales, y especificamente de los
Tema 4. Cristaloquímica. Descripción estructural y estructuras tipos Qué objetivos tiene la Cristaloquímica? Las fases cristalinas son componentes esenciales de los materiales, y especificamente de los
SÓLIDOS INORGÁNICOS. Tema 6. FUNDAMENTOS
 SÓLIDOS INORGÁNICOS Tema 6. Fundamentos Tema 7. Sólidos metálicos Tema 8. Sólidos iónicos Tema 9. Sólidos covalentes Tema 10. Sólidos moleculares Tema 11. Defectos y no-estequiometría Tema 12. Propiedades
SÓLIDOS INORGÁNICOS Tema 6. Fundamentos Tema 7. Sólidos metálicos Tema 8. Sólidos iónicos Tema 9. Sólidos covalentes Tema 10. Sólidos moleculares Tema 11. Defectos y no-estequiometría Tema 12. Propiedades
Estructura de los Sólidos
 Estructura de los Sólidos Estructura Cristalina OBJETIVOS a) Definir sólidos cristalinos y amorfos b) Definir estructura cristalina c) Describir las diferentes estructuras cristalinas d) Utilizar índices
Estructura de los Sólidos Estructura Cristalina OBJETIVOS a) Definir sólidos cristalinos y amorfos b) Definir estructura cristalina c) Describir las diferentes estructuras cristalinas d) Utilizar índices
PSU Matemática NM-4 Guía 23: Isometrías. Nombre: Curso: Fecha: -
 Centro Educacional San Carlos de Aragón. Dpto. Matemática. Prof. Ximena Gallegos H. PSU Matemática NM- Guía : Isometrías Nombre: Curso: Fecha: - Contenido: Isometrías. Aprendizaje Esperado: Analiza traslaciones
Centro Educacional San Carlos de Aragón. Dpto. Matemática. Prof. Ximena Gallegos H. PSU Matemática NM- Guía : Isometrías Nombre: Curso: Fecha: - Contenido: Isometrías. Aprendizaje Esperado: Analiza traslaciones
SÓLIDOS I. Tipos de sólidos. Sólidos cristalinos: los átomos, iones o moléculas se empaquetan en forma ordenada.
 SÓLIDOS I Tipos de sólidos Sólidos cristalinos: los átomos, iones o moléculas se empaquetan en forma ordenada. Sólidos amorfos: no presentan estructuras ordenadas. 1 Sólidos cristalinos Hay posiciones
SÓLIDOS I Tipos de sólidos Sólidos cristalinos: los átomos, iones o moléculas se empaquetan en forma ordenada. Sólidos amorfos: no presentan estructuras ordenadas. 1 Sólidos cristalinos Hay posiciones
Estructura atómica de superficies
 Estructura atómica de superficies El número de coordinación de los átomos en una superficie es mucho menor que el número de coordinación de los átomos en el sólido. Uno puede pensar que forma una superficie
Estructura atómica de superficies El número de coordinación de los átomos en una superficie es mucho menor que el número de coordinación de los átomos en el sólido. Uno puede pensar que forma una superficie
DEPARTAMENTO DE TECNOLOGÍA Actividades complementarias Curso: 1º Bach. Profesor: José Jiménez R. Tema 12: Materiales Metálicos: Metales ferrosos
 PARTAMENTO 1.- Determinar, en %, el factor de empaquetamiento de una: a) Red cúbica centrada en el cuerpo (BCC). b) Red cúbica centrada en las caras (FCC). 2.- El hierro a 20 ºC cristaliza en una red BCC
PARTAMENTO 1.- Determinar, en %, el factor de empaquetamiento de una: a) Red cúbica centrada en el cuerpo (BCC). b) Red cúbica centrada en las caras (FCC). 2.- El hierro a 20 ºC cristaliza en una red BCC
UNIDAD 3. MODIFICACIÓN DE LAS PROPIEDADES DE LOS METALES
 UNIDAD 3. MODIFICACIÓN DE LAS PROPIEDADES DE LOS METALES 1. GENERALIDADES... Pág. 49 2. ESTRUCTURA INTERNA DE LOS METALES... Pág. 49 2.1. Estructuras cristalinas... Pág. 49 2.2. Estructura cristalina cúbica
UNIDAD 3. MODIFICACIÓN DE LAS PROPIEDADES DE LOS METALES 1. GENERALIDADES... Pág. 49 2. ESTRUCTURA INTERNA DE LOS METALES... Pág. 49 2.1. Estructuras cristalinas... Pág. 49 2.2. Estructura cristalina cúbica
Introducción al Estado Sólido: El amarre fuerte (tight-binding, en inglés)
 Introducción al Estado Sólido: El amarre fuerte (tight-binding, en inglés) R. Baquero Departamento de Física Cinvestav setiembre 2008 amarre fuerte 1 Por qué estudiamos el método de amarre fuerte? Uno
Introducción al Estado Sólido: El amarre fuerte (tight-binding, en inglés) R. Baquero Departamento de Física Cinvestav setiembre 2008 amarre fuerte 1 Por qué estudiamos el método de amarre fuerte? Uno
a) La ecuación del plano que pasa por el punto ( 1, 1, 0 ). (3 puntos) b) La ecuación del plano que es paralelo a la recta r.
 PROBLEMAS DE SELECTIVIDAD. BLOQUE GEOMETRÍA 1. En el espacio se dan las rectas Obtener a) El valor de para el que las rectas r y s están contenidas en un plano. (4 puntos) b) La ecuación del plano que
PROBLEMAS DE SELECTIVIDAD. BLOQUE GEOMETRÍA 1. En el espacio se dan las rectas Obtener a) El valor de para el que las rectas r y s están contenidas en un plano. (4 puntos) b) La ecuación del plano que
Translaciones, giros, simetrías.
 Translaciones, giros, simetrías. Transformaciones geométricas Transformación geométrica es una aplicación del plano en el plano tal que a cada punto de un plano le hace corresponder otro punto del mismo
Translaciones, giros, simetrías. Transformaciones geométricas Transformación geométrica es una aplicación del plano en el plano tal que a cada punto de un plano le hace corresponder otro punto del mismo
CAPITULO 2 LA TABLA PERIODICA
 1.0079 1 H HIDROGENO 6.941 3 Li LITIO 22.989 11 Na SODIO 30.098 19 K POTASIO CAPITULO 2 LA TABLA PERIODICA ORDENAMIENTO ACTUAL GRUPOS Y PERIODOS PROPIEDADES PERIODICAS TAMAÑO POTENCIAL DE IONIZACION AFINIDAD
1.0079 1 H HIDROGENO 6.941 3 Li LITIO 22.989 11 Na SODIO 30.098 19 K POTASIO CAPITULO 2 LA TABLA PERIODICA ORDENAMIENTO ACTUAL GRUPOS Y PERIODOS PROPIEDADES PERIODICAS TAMAÑO POTENCIAL DE IONIZACION AFINIDAD
Problemas de exámenes de Geometría
 1 Problemas de exámenes de Geometría 1. Consideramos los planos π 1 : X = P+λ 1 u 1 +λ 2 u 2 y π 2 : X = Q+µ 1 v 1 +µ 2 v 2. Cuál de las siguientes afirmaciones es incorrecta? a) Si π 1 π 2 Ø, entonces
1 Problemas de exámenes de Geometría 1. Consideramos los planos π 1 : X = P+λ 1 u 1 +λ 2 u 2 y π 2 : X = Q+µ 1 v 1 +µ 2 v 2. Cuál de las siguientes afirmaciones es incorrecta? a) Si π 1 π 2 Ø, entonces
TEMA 4. IMPERFECIONES EN SÓLIDOS
 TEMA 4. IMPERFECIONES EN SÓLIDOS En el Tema 3 se ha descrito el SÓLIDO CRISTALINO mediante la aproximación del CRISTAL IDEAL, que tomamos como modelo de perfección cristalina Los sólidos cristalinos reales
TEMA 4. IMPERFECIONES EN SÓLIDOS En el Tema 3 se ha descrito el SÓLIDO CRISTALINO mediante la aproximación del CRISTAL IDEAL, que tomamos como modelo de perfección cristalina Los sólidos cristalinos reales
Aplicaciones de la teoría de grupos cristalográficos en cristaloquímica
 Aplicaciones de la teoría de grupos cristalográficos en cristaloquímica Manuales de químicas PROYECTO EDITORIAL CIENCIAS QUÍMICAS Director: Guillermo Calleja Pardo Áreas de publicación: QUÍMICA BÁSICA
Aplicaciones de la teoría de grupos cristalográficos en cristaloquímica Manuales de químicas PROYECTO EDITORIAL CIENCIAS QUÍMICAS Director: Guillermo Calleja Pardo Áreas de publicación: QUÍMICA BÁSICA
Corresponde a la operación que consiste en no hacer nada. Todos los objetos poseen al menos este elemento
 ELEMENTOS Y OPERACIONES DE SIMETRÍA Identidad (E) Corresponde a la operación que consiste en no hacer nada. Todos los objetos poseen al menos este elemento Eje de simetría (Cn) Eje que pasa por el objeto
ELEMENTOS Y OPERACIONES DE SIMETRÍA Identidad (E) Corresponde a la operación que consiste en no hacer nada. Todos los objetos poseen al menos este elemento Eje de simetría (Cn) Eje que pasa por el objeto
x-z = 0 x+y+2 = [2012] [EXT-B] Halla el punto simétrico del P(2,1,-5) respecto de la recta r definida por
![x-z = 0 x+y+2 = [2012] [EXT-B] Halla el punto simétrico del P(2,1,-5) respecto de la recta r definida por x-z = 0 x+y+2 = [2012] [EXT-B] Halla el punto simétrico del P(2,1,-5) respecto de la recta r definida por](/thumbs/55/35462313.jpg) x = 1+t 1. [014] [EXT-A] Considera los puntos A(1,1,) y B(1,-1,-) y la recta dada por y = t. z = 1 a) Halla la ecuación general del plano que que contiene a r y es paralelo a la recta que pasa por A y
x = 1+t 1. [014] [EXT-A] Considera los puntos A(1,1,) y B(1,-1,-) y la recta dada por y = t. z = 1 a) Halla la ecuación general del plano que que contiene a r y es paralelo a la recta que pasa por A y
ROCAS, MINERALES Y CRISTALES
 ROCAS, MINERALES Y CRISTALES LOS MINERALES Un mineral es un cuerpo sólido, natural, inorgánico, homogéneo en sus propiedades físico-químicas, de composición química fija (o variable dentro de límites estrechos)
ROCAS, MINERALES Y CRISTALES LOS MINERALES Un mineral es un cuerpo sólido, natural, inorgánico, homogéneo en sus propiedades físico-químicas, de composición química fija (o variable dentro de límites estrechos)
Fundamentos de óptica fotorrefractiva
 Fundamentos de óptica fotorrefractiva Prof. M.L. Calvo 11 y 12 de abril de 2011 ECUACIÓN DE ONDAS EN MEDIOS ANISÓTROPOS Y NO LINEALES El vector desplazamiento eléctrico cumple en estos medios: (, ) = ε
Fundamentos de óptica fotorrefractiva Prof. M.L. Calvo 11 y 12 de abril de 2011 ECUACIÓN DE ONDAS EN MEDIOS ANISÓTROPOS Y NO LINEALES El vector desplazamiento eléctrico cumple en estos medios: (, ) = ε
3.- ORDENAMIENTO ATÓMICO DE LOS SÓLIDOS
 3.- ORDENAMIENTO ATÓMICO DE LOS SÓLIDOS 3.1.- Orden de corto y largo alcance 3.2.- Estructuras cristalinas 3.3.- Puntos, direcciones y planos de una celda unitaria 3.4.- Las Celdas Tridimensionales 3.5.-
3.- ORDENAMIENTO ATÓMICO DE LOS SÓLIDOS 3.1.- Orden de corto y largo alcance 3.2.- Estructuras cristalinas 3.3.- Puntos, direcciones y planos de una celda unitaria 3.4.- Las Celdas Tridimensionales 3.5.-
Verifique los resultados analíticos mediante la resolución gráfica usando un software de Matemática.
 Álgebra Geometría Analítica Prof. Gisela Saslavsk Vectores en R en R 3. Rectas planos en el espacio Verifique los resultados analíticos mediante la resolución gráfica usando un software de Matemática..
Álgebra Geometría Analítica Prof. Gisela Saslavsk Vectores en R en R 3. Rectas planos en el espacio Verifique los resultados analíticos mediante la resolución gráfica usando un software de Matemática..
CAPI TULO 1 SEMICONDUCTORES Clasificación de la materia INTRODUCCIÓN
 CAPI TULO 1 SEMICONDUCTORES INTRODUCCIÓN En este capítulo estudiaremos las características de los materiales semiconductores, su clasificación, como se forman, que los hace atractivos para la industria
CAPI TULO 1 SEMICONDUCTORES INTRODUCCIÓN En este capítulo estudiaremos las características de los materiales semiconductores, su clasificación, como se forman, que los hace atractivos para la industria
ejerciciosyexamenes.com GEOMETRIA
 GEOMETRIA 1.- Dado el vector AB= (2,-1,3) y el punto B(3,1,2) halla las coordenadas del punto A. Sol: A =(1,2,-1) 2.- Comprobar si los vectores AB y CD son equipolentes, siendo A(1,2,-1), B(0,3,1), C(1,1,1)
GEOMETRIA 1.- Dado el vector AB= (2,-1,3) y el punto B(3,1,2) halla las coordenadas del punto A. Sol: A =(1,2,-1) 2.- Comprobar si los vectores AB y CD son equipolentes, siendo A(1,2,-1), B(0,3,1), C(1,1,1)
EJERCICIOS DE GEOMETRÍA
 EJERCICIOS DE GEOMETRÍA 1. Se consideran las rectas r x 2 = 0 x 2z = 1, s y + 3 = 0 y + z = 3 a) Estudiar la posición relativa de r y s. b) Hallar la mínima distancia entre ambas. Se pide: Sol: Se cruzan
EJERCICIOS DE GEOMETRÍA 1. Se consideran las rectas r x 2 = 0 x 2z = 1, s y + 3 = 0 y + z = 3 a) Estudiar la posición relativa de r y s. b) Hallar la mínima distancia entre ambas. Se pide: Sol: Se cruzan
Problemas métricos. Ángulo entre rectas y planos
 Problemas métricos Ángulo entre rectas y planos Ángulo entre dos rectas El ángulo que forman dos rectas es el ángulo agudo que determinan entre sí sus vectores directores. Dos rectas son perpendiculares
Problemas métricos Ángulo entre rectas y planos Ángulo entre dos rectas El ángulo que forman dos rectas es el ángulo agudo que determinan entre sí sus vectores directores. Dos rectas son perpendiculares
EJERCICIOS DE SELECTIVIDAD DE GEOMETRIA
 EJERCICIOS DE SELECTIVIDAD DE GEOMETRIA 2003 (4) Ejercicio 1. Considera los vectores u = (1,1,1), v = (2,2,a) y w = (2,0,0), (a) [1'25 puntos] Halla los valores de a para que los vectores u, v y w sean
EJERCICIOS DE SELECTIVIDAD DE GEOMETRIA 2003 (4) Ejercicio 1. Considera los vectores u = (1,1,1), v = (2,2,a) y w = (2,0,0), (a) [1'25 puntos] Halla los valores de a para que los vectores u, v y w sean
Llamamos potencia a todo producto de factores iguales. Por ejemplo: 3 4 =
 1. NÚMEROS NATURALES POTENCIAS DE UN NÚMERO NATURAL Llamamos potencia a todo producto de factores iguales. Por ejemplo: 3 4 = 3 3 3 3 El factor que se repite es la base, y el número de veces que se repite
1. NÚMEROS NATURALES POTENCIAS DE UN NÚMERO NATURAL Llamamos potencia a todo producto de factores iguales. Por ejemplo: 3 4 = 3 3 3 3 El factor que se repite es la base, y el número de veces que se repite
IMPERFECCIONES CRISTALINAS ANA QUIGUANTAR EDWIN RODRIGUES JEISON CORDOBA
 IMPERFECCIONES CRISTALINAS ANA QUIGUANTAR EDWIN RODRIGUES JEISON CORDOBA CORPORACION UNIVERSITARIA AUTONOMA DE NARIÑO FACULTAD DE INGENIERIA MECANICA SEGUNDO SEMESTRE CIENCIA DE LOS MATERIALES SAN JUAN
IMPERFECCIONES CRISTALINAS ANA QUIGUANTAR EDWIN RODRIGUES JEISON CORDOBA CORPORACION UNIVERSITARIA AUTONOMA DE NARIÑO FACULTAD DE INGENIERIA MECANICA SEGUNDO SEMESTRE CIENCIA DE LOS MATERIALES SAN JUAN
CONDUCTIVIDAD ELÉCTRICA I E
 CONDUCTVDAD LÉCTRCA La conductividad eléctrica de una substancia se define como la relación entre la intensidad de corriente eléctrica producida y el campo eléctrico que la produce: = el campo eléctrico
CONDUCTVDAD LÉCTRCA La conductividad eléctrica de una substancia se define como la relación entre la intensidad de corriente eléctrica producida y el campo eléctrico que la produce: = el campo eléctrico
4. Simetría y formas simples de cristales minerales
 4. Simetría y formas simples de cristales minerales La simetría rige al mundo de los cristales. Esto es una regularidad más general de las sustancias cristalinas. La simetría determina: 1) Las leyes de
4. Simetría y formas simples de cristales minerales La simetría rige al mundo de los cristales. Esto es una regularidad más general de las sustancias cristalinas. La simetría determina: 1) Las leyes de
Trabajo Práctico Nº 4 SACAROSA
 FUNDAMENTOS TEÓRICOS Trabajo Práctico Nº 4 SACAROSA PARTE A: PROPIEDADES COLIGATIVAS Si se disuelve un soluto en un líquido, hay ciertas propiedades de la solución que se irán modificando de acuerdo con
FUNDAMENTOS TEÓRICOS Trabajo Práctico Nº 4 SACAROSA PARTE A: PROPIEDADES COLIGATIVAS Si se disuelve un soluto en un líquido, hay ciertas propiedades de la solución que se irán modificando de acuerdo con
Tema 7. Metales. Empaquetamientos en 2D. El enlace metálico Teoría de bandas Conductividad eléctrica Semiconductividad
 Tema 7. Metales Empaquetamientos de esferas Empaquetamientos compactos Estructura de metales Aleaciones El enlace metálico Teoría de bandas Conductividad eléctrica Semiconductividad http://www.chem.ox.ac.uk/icl/heyes/structure_of_solids/strucsol.html
Tema 7. Metales Empaquetamientos de esferas Empaquetamientos compactos Estructura de metales Aleaciones El enlace metálico Teoría de bandas Conductividad eléctrica Semiconductividad http://www.chem.ox.ac.uk/icl/heyes/structure_of_solids/strucsol.html
1. Distancia entre puntos y rectas en el espacio. 3. Calcula la distancia existente entre las rectas: Solución: d(r, s) =
 7 Espacio métrico. Distancia entre puntos y rectas en el espacio Piensa y calcula Dados los puntos A, 4, ) y B5,, 4), halla las coordenadas del vector: AB AB,5,) Aplica la teoría. Calcula la distancia
7 Espacio métrico. Distancia entre puntos y rectas en el espacio Piensa y calcula Dados los puntos A, 4, ) y B5,, 4), halla las coordenadas del vector: AB AB,5,) Aplica la teoría. Calcula la distancia
UNIDAD: ÁLGEBRA Y FUNCIONES ECUACIÓN DE LA RECTA
 C u r s o : Matemática Material N 8 GUÍA TEÓRICO PRÁCTICA Nº 5 UNIDAD: ÁLGEBRA Y FUNCIONES ECUACIÓN DE LA RECTA SISTEMA CARTESIANO ORTOGONAL Para determinar la posición de los puntos de un plano usando
C u r s o : Matemática Material N 8 GUÍA TEÓRICO PRÁCTICA Nº 5 UNIDAD: ÁLGEBRA Y FUNCIONES ECUACIÓN DE LA RECTA SISTEMA CARTESIANO ORTOGONAL Para determinar la posición de los puntos de un plano usando
La presencia del estado sólido en la materia que nos rodea es constante. El arreglo de sus moléculas o iones es uniforme.
 2.7 ESTRUCTURA DE LOS MATERIALES. 2.7.1 ESTADO SÓLIDO (CRISTALINO). La presencia del estado sólido en la materia que nos rodea es constante. El arreglo de sus moléculas o iones es uniforme. En los gases
2.7 ESTRUCTURA DE LOS MATERIALES. 2.7.1 ESTADO SÓLIDO (CRISTALINO). La presencia del estado sólido en la materia que nos rodea es constante. El arreglo de sus moléculas o iones es uniforme. En los gases
5b. DIAGRAMA HIERRO-CARBONO
 5b. DIAGRAMA HIERRO-CARBONO MATERIALES 13/14 ÍNDICE ACERO DIAGRAMA Fe-C FASES EN EL DIAGRAMA PROPIEDADES MECANICAS DE LAS FASES 2 1. ACERO Constituyentes de las aleaciones Fe-C (fases) Ferrita : Solución
5b. DIAGRAMA HIERRO-CARBONO MATERIALES 13/14 ÍNDICE ACERO DIAGRAMA Fe-C FASES EN EL DIAGRAMA PROPIEDADES MECANICAS DE LAS FASES 2 1. ACERO Constituyentes de las aleaciones Fe-C (fases) Ferrita : Solución
Materiales: Estructura interna y propiedades
 Materiales: Estructura interna y propiedades Para satisfacer esa curiosidad que muestra el protagonista de nuestra historia, va a hacer como los detectives de algunas películas: mirar los materiales con
Materiales: Estructura interna y propiedades Para satisfacer esa curiosidad que muestra el protagonista de nuestra historia, va a hacer como los detectives de algunas películas: mirar los materiales con
1. Halla la ecuación de la recta r, sabiendo que pasa por A(1,-2) y B(-1,2)
 1. Halla la ecuación de la recta r, sabiendo que pasa por A(1,-2) y B(-1,2) 2. Halla la ecuación de la recta r, sabiendo que es paralela a y=2x-3 y pasa por el punto (1,3). 3. Halla la ecuación de la recta
1. Halla la ecuación de la recta r, sabiendo que pasa por A(1,-2) y B(-1,2) 2. Halla la ecuación de la recta r, sabiendo que es paralela a y=2x-3 y pasa por el punto (1,3). 3. Halla la ecuación de la recta
Química del Estado Sólido
 Química del Estado Sólido Por qué un curso de química de sólidos?? 2x2x2 celdas de una perovskita distorsionada Celda unitaria del YBa2Cu3O7 Existe un aspecto económico que es muy importante y mueve muchas
Química del Estado Sólido Por qué un curso de química de sólidos?? 2x2x2 celdas de una perovskita distorsionada Celda unitaria del YBa2Cu3O7 Existe un aspecto económico que es muy importante y mueve muchas
Facultad de Tecnología y Cs Aplicadas Licenciatura en Geología CUADERNO DOCENTE 2015 MINERALOGIA I CRISTALOGRAFIA Y OPTICA MINERAL
 Facultad de Tecnología y Cs Aplicadas CUADERNO DOCENTE 2015 MINERALOGIA I CRISTALOGRAFIA Y OPTICA MINERAL Universidad Nacional de Catamarca Secretaría de Ciencia y Tecnología -Editorial Científica Universitaria-
Facultad de Tecnología y Cs Aplicadas CUADERNO DOCENTE 2015 MINERALOGIA I CRISTALOGRAFIA Y OPTICA MINERAL Universidad Nacional de Catamarca Secretaría de Ciencia y Tecnología -Editorial Científica Universitaria-
Guía n 0: Herramientas de Física y Matemáticas
 Guía n 0: Herramientas de Física y Matemáticas Problema Dadas dos partículas en el espacio ubicadas en los puntos de coordenadas p = (0,5, 2) y p 2 = (2,3,). Hallar el vector posición de la partícula respecto
Guía n 0: Herramientas de Física y Matemáticas Problema Dadas dos partículas en el espacio ubicadas en los puntos de coordenadas p = (0,5, 2) y p 2 = (2,3,). Hallar el vector posición de la partícula respecto
TEMAS 6 Y 7 RECTAS Y PLANOS EN EL ESPACIO
 Temas 6 y 7 Rectas y planos en el espacio Matemáticas II - 2º Bachillerato 1 TEMAS 6 Y 7 RECTAS Y PLANOS EN EL ESPACIO RECTAS Y PLANOS EJERCICIO 1 : Halla el volumen del tetraedro determinado por los ejes
Temas 6 y 7 Rectas y planos en el espacio Matemáticas II - 2º Bachillerato 1 TEMAS 6 Y 7 RECTAS Y PLANOS EN EL ESPACIO RECTAS Y PLANOS EJERCICIO 1 : Halla el volumen del tetraedro determinado por los ejes
LA CIRCUNFERENCIA. La circunferencia es la sección producida por un plano perpendicular al eje.
 LA CIRCUNFERENCIA La circunferencia es la sección producida por un plano perpendicular al eje. β = 90º La circunferencia es un caso particular de elipse. Se llama circunferencia al lugar geométrico de
LA CIRCUNFERENCIA La circunferencia es la sección producida por un plano perpendicular al eje. β = 90º La circunferencia es un caso particular de elipse. Se llama circunferencia al lugar geométrico de
Elementos de análisis
 Elementos de análisis El estudio universitario del electromagnetismo en Física II requiere del uso de elementos de análisis en varias variables que el alumno adquirirá en la asignatura Análisis Matemático
Elementos de análisis El estudio universitario del electromagnetismo en Física II requiere del uso de elementos de análisis en varias variables que el alumno adquirirá en la asignatura Análisis Matemático
GRUPOS PUNTUALES. 4.- Si un plano de simetría contiene un eje de orden n, existen n planos que contienen el eje. formando entre ellos ángulos de
 GRUPOS PUNTUALES Existen algunas relaciones entre elementos de simetría que pueden ser útiles a la hora de deducir cuales son los conjuntos de estos que forman grupo. 1.- Todos los elementos de simetría
GRUPOS PUNTUALES Existen algunas relaciones entre elementos de simetría que pueden ser útiles a la hora de deducir cuales son los conjuntos de estos que forman grupo. 1.- Todos los elementos de simetría
Piden: Dato: Piden: Dato: Piden: Dato:
 SEMANA 1 PRISMAS Y PIRÁMIDE 1. Calcule el número de caras de un prisma donde el número de vértices más el número de aristas es 50. A) 10 B) 0 C) 0 D) 1 E) 18 Sea n el número de lados de la base del prisma:
SEMANA 1 PRISMAS Y PIRÁMIDE 1. Calcule el número de caras de un prisma donde el número de vértices más el número de aristas es 50. A) 10 B) 0 C) 0 D) 1 E) 18 Sea n el número de lados de la base del prisma:
En la figura 1.1 puede verse el cuarzo cristalino y no cristalino respectivamente.
 TEMA 3.- ESTRUCTURA CRISTALINA. 1.- Introducción. Conceptos fundamentales. Se han descrito los enlaces atómicos determinados por la configuración electrónica de los átomos individuales. Ahora se va a tratar
TEMA 3.- ESTRUCTURA CRISTALINA. 1.- Introducción. Conceptos fundamentales. Se han descrito los enlaces atómicos determinados por la configuración electrónica de los átomos individuales. Ahora se va a tratar
IES EL PILES SELECTIVIDAD OVIEDO DPTO. MATEMÁTICAS Geometría
 P.A.U. de. (Oviedo). (junio 994) Dados los puntos A (,0, ), B (,, ), C (,6, a), se pide: i) hallar para qué valores del parámetro a están alineados, ii) hallar si existen valores de a para los cuales A,
P.A.U. de. (Oviedo). (junio 994) Dados los puntos A (,0, ), B (,, ), C (,6, a), se pide: i) hallar para qué valores del parámetro a están alineados, ii) hallar si existen valores de a para los cuales A,
TEMA 7 Las formas y las medidas que nos rodean. 2. Repaso a las figuras planas elementales
 TEMA 7 Las formas y las medidas que nos rodean 1. Introducción 1.1. Qué es la geometría? Es una rama de la matemática que se ocupa del estudio de las propiedades de las figuras geométricas en el plano
TEMA 7 Las formas y las medidas que nos rodean 1. Introducción 1.1. Qué es la geometría? Es una rama de la matemática que se ocupa del estudio de las propiedades de las figuras geométricas en el plano
MÓDULO Nº 3. Nivelación. Matemática Módulo Nº3. Contenidos. Polígonos Circunferencia y Círculo Volúmenes
 MÓDULO Nº 3 Nivelación Matemática 2005 Módulo Nº3 Contenidos Polígonos Circunferencia y Círculo Volúmenes Nivelación Polígonos Polígono Regular: Son aquellos polígonos que tienen todos sus lados y ángulos
MÓDULO Nº 3 Nivelación Matemática 2005 Módulo Nº3 Contenidos Polígonos Circunferencia y Círculo Volúmenes Nivelación Polígonos Polígono Regular: Son aquellos polígonos que tienen todos sus lados y ángulos
Tema 2 Estructuras Cristalinas
 Tema 2 Estructuras Cristalinas Para poder comprender las propiedades de los materiales, y poder por tanto seleccionar el material idóneo para una aplicación específica, se hace necesario comprender la
Tema 2 Estructuras Cristalinas Para poder comprender las propiedades de los materiales, y poder por tanto seleccionar el material idóneo para una aplicación específica, se hace necesario comprender la
Cristal. Estado Sólido. Estructura Cristalina. Red. Celdas. Red
 Estdo Sólido Estructurs Cristlins Cristl Un cristl es un rreglo periódico de átomos o grupos de átomos que es construido por l repetición infinit de estructurs unitris idéntics en el espcio. L estructur
Estdo Sólido Estructurs Cristlins Cristl Un cristl es un rreglo periódico de átomos o grupos de átomos que es construido por l repetición infinit de estructurs unitris idéntics en el espcio. L estructur
UNIVERSIDADES DE ANDALUCÍA PRUEBA DE ACCESO A LA UNIVERSIDAD
 Opción A Ejercicio 1.- Sea f : R R definida por f(x) = x 3 +ax 2 +bx+c. a) [1 75 puntos] Halla a,b y c para que la gráfica de f tenga un punto de inflexión de abscisa x = 1 2 y que la recta tangente en
Opción A Ejercicio 1.- Sea f : R R definida por f(x) = x 3 +ax 2 +bx+c. a) [1 75 puntos] Halla a,b y c para que la gráfica de f tenga un punto de inflexión de abscisa x = 1 2 y que la recta tangente en
Capítulo 1 Vectores. 26 Problemas de selección - página 13 (soluciones en la página 99)
 Capítulo 1 Vectores 26 Problemas de selección - página 13 (soluciones en la página 99) 21 Problemas de desarrollo - página 22 (soluciones en la página 100) 11 1.A PROBLEMAS DE SELECCIÓN Sección 1.A Problemas
Capítulo 1 Vectores 26 Problemas de selección - página 13 (soluciones en la página 99) 21 Problemas de desarrollo - página 22 (soluciones en la página 100) 11 1.A PROBLEMAS DE SELECCIÓN Sección 1.A Problemas
Qué es la textura de un policristal? Introducción a la textura: Conceptos básicos
 Qué es la textura de un policristal? Introducción a la textura: Conceptos básicos (la textura cristaloráfica, como yo lo entiendo) Gaspar Gónzález-Doncel CENIM, C.S.I.C. ggd@cenim.csic.es Esquema a seguir
Qué es la textura de un policristal? Introducción a la textura: Conceptos básicos (la textura cristaloráfica, como yo lo entiendo) Gaspar Gónzález-Doncel CENIM, C.S.I.C. ggd@cenim.csic.es Esquema a seguir
ÁLGEBRA LINEAL II Práctica
 ÁLGEBRA LINEAL II Práctica 3.1-3.2 Geometría afín. (Curso 2013 2014) 1. En un espacio afín real de dimensión 3, se consideran dos sistemas de referencia R = O, ē 1, ē 2, ē 3 } y R = P, ū 1, ū 2, ū 3 },
ÁLGEBRA LINEAL II Práctica 3.1-3.2 Geometría afín. (Curso 2013 2014) 1. En un espacio afín real de dimensión 3, se consideran dos sistemas de referencia R = O, ē 1, ē 2, ē 3 } y R = P, ū 1, ū 2, ū 3 },

 ᒬ 01) En el triángulo ABC de la figura AD = BD;
ᒬ 01) En el triángulo ABC de la figura AD = BD;