DETERMINACIÓN DE ESTRUCTURAS CRISTALINAS II 5.1. MÉTODO ANALÍTICO PARA EL INDEXADO DE PATRONES DE CRISTALES NO CÚBICOS
|
|
|
- Lidia Toro Espejo
- hace 6 años
- Vistas:
Transcripción
1 CAPÍTULO 5 DETERMINACIÓN DE ESTRUCTURAS CRISTALINAS II 5.. MÉTODO ANALÍTICO PARA EL INDEXADO DE PATRONES DE CRISTALES NO CÚBICOS Los métodos analíticos de indexado requiere manipulaciones aritméticas de los valores observados sen en un intento de hallar ciertas relaciones entre ellas. Puesto que cada sistema cristalino se caracteriza por relaciones particulares entre los valores de sen, el reconocimiento de estas relaciones identifica el sistema cristalino y conduce a la solución de los índices de las líneas. Para el Sistema cristalino Hexagonal - de constantes de red a y c - el espaciado d de los planos individuales de la red cristalina, con índices (hk ), se obtiene de la forma cuadrática: 4 h h k k (5.) c d hk 3 a De la ecuación (5.) y la ley de Bragg, con n, se obtiene la ecuación cuadrática de Bragg: 4 (h h k k ) sen (5.) 4 3 a c Los valores del sen deben obedecer la relación: donde: A y C sen A (h h k k ) C (5.3) son constantes para cualquier patrón. El problema es hallar estas 3a 4 c constantes, puesto que ellas permitirán determinar los parámetros a y c de la celda y harán posible que se calculen los índices de las líneas. El valor de A se obtiene a partir de las líneas hk0. Cuando 0, la ecuación (5.3) se convierte en sen A (h h k k ). Los valores permitidos de (h hk k ) se determinan de una Tabla de Formas Cuadráticas de los índices de Miller, como la que se incluye en el Apéndice ; estos valores son, 3, 4, 7, 9,, 3, etc. Por lo tanto, las líneas hk0 deben tener valores de sen en la proporción de estos enteros y A será algún número como, /3, /4, /7, /9, etc., veces los valores del sen de estas líneas. Determinado el valor de A se puede hallar el parámetro a de la celda. El valor de C se obtiene de las otras líneas del patrón y el uso de la ecuación (5.3) en la forma: (5.4) sen A (h h k k ) C Las diferencias representadas por el lado izquierdo de la ecuación (5.4) se establecen para diversos valores asumidos de h y k, en un intento de hallar un conjunto consistente de valores de C, los cuales deben estar es la proporción, 4, 9, 6, etc. Una vez que estos valores se encuentran, puede calcularse C. Determinado el valor de C se puede hallar el parámetro c de la celda. Para el Sistema cristalino Tetragonal, - de constantes de red a y c - el espaciado d de los planos individuales de la red cristalina, con índices (hk ), se obtiene de la forma cuadrática: 7
2 (h k ) (5.5) d hk a c De la ecuación (5.5) y la ley de Bragg, con n, se obtiene la ecuación cuadrática de Bragg: (h k ) sen (5.6) 4 a c Los valores de sen deben obedecer a la relación: donde: A y C sen A (h k ) C (5.7), son constantes para cualquier patrón. El problema es hallar estas 4a 4 c constantes, puesto que ellas permitirán determinar los parámetros a y c de la celda y harán posible que se calculen los índices de las líneas. El valor de A se obtiene a partir de las líneas hk0. Cuando 0, la ecuación (5.7) se convierte en sen A (h k ). Los valores permitidos de (h k ) son,, 4, 5, 8, 9, 0, etc. Por lo tanto, las líneas hk0 deben tener valores de sen en la proporción de estos enteros, y A será algún número como, /, /4, /5, /8, etc., veces los valores del sen de estas líneas. Determinado el valor de A se puede hallar el parámetro a de la celda. El valor de C se obtiene de las otras líneas del patrón y el uso de la ecuación (5.7) en la forma (5.8) sen A (h k ) C Las diferencias representadas por el lado izquierdo de la ecuación (5.8) se establecen para diversos valores asumidos de h y k, en un intento de hallar un conjunto consistente de valores de C, los cuales deben estar es la proporción, 4, 9, 6, etc. Una vez que estos valores se encuentran, puede calcularse C. Determinado el valor de C se puede hallar el parámetro c de la celda. Las sustancias cristalinas Monoclínicas y Triclínicas producen patrones de polvo de gran complejidad debido a que el número de constantes independientes involucradas es ahora cuatro y seis, respectivamente. Todavía no se ha creado algún método exitoso, analítico o gráfico para indexar tales patrones. Se puede concluir que el patrón de polvo de una sustancia que tiene más de dos parámetros de celda independientemente variables es extremadamente difícil, si no imposible de resolver. Las estructuras de tales sustancias se determinan casi siempre examinando un monocristal de la sustancia. 5.. EFECTO DE LA DISTORSIÓN DE LA CELDA EN EL PATRÓN DE POLVO Cuando la celda unitaria de la sustancia se distorsiona en diversas formas, existen muchas más líneas en el patrón de una sustancia de baja simetría - tal como la triclínica - que en el patrón de una sustancia de alta simetría - tal como la cúbica - y se puede tomar como regla general que cualquier distorsión de la celda unidad que disminuya su simetría, en el sentido de introducir parámetros variables adicionales, incrementará el número de líneas en el patrón de polvo. 73
3 El incremento en el número de líneas se debe fundamentalmente a la introducción de nuevos espaciados en los planos, originados por la distorsión no uniforme. Así, por ejemplo, en la celda cúbica los planos (00), (00) y (00) tienen el miso espaciado y solamente se forma una línea en el patrón, llamada línea 00; pero esta línea se divide en dos cuando la celda llega a ser tetragonal, cuando se distorsiona a través de un solo eje, puesto que ahora el espaciado de los planos (00) difiere de los otros dos. Si por distorsión la celda llega a ser ortorrómbica, los tres espaciados son diferentes y se formarán tres líneas DETERMINACIÓN DEL NÚMERO DE ÁTOMOS EN UNA CELDA UNITARIA Después de establecer la forma y el tamaño de la celda unidad, se debe hallar el número de átomos en la celda, debido a que el número de átomos debe conocerse antes que sus posiciones puedan ser determinadas. Para hallar este número, se usa el hecho que el volumen V de la celda unidad, calculada a partir de los parámetros de la red, multiplicada por la densidad de la sustancia es igual al peso de todos los átomos en la celda. Así tenemos que para una masa m de átomos o moléculas contenidas en la celda unidad, su m NM densidad es dada por: (5.9) V N0V donde: N es el número de átomos o moléculas en la celda unidad, N 0 es el Número de Avogadro y M es el peso molecular. Luego, el número de átomos por celda se puede calcular a partir de N y la composición de la fase. Si la sustancia es un elemento de peso atómico A, entonces la ecuación (5.9) se convierte en: N A N 0 V, donde N es el número de átomos por celda unidad. Cuando se determina en esta forma, el número de átomos por celda es siempre un entero, dentro del error experimental DETERMINACIÓN DE POSICIONES ATÓMICAS Para hallar las posiciones de un número conocido de átomos en una celda unidad de forma y tamaño conocidos, se debe usar las intensidades relativas observadas de los haces difractados, puesto que estas intensidades son determinadas por las posiciones de los átomos. Para hallar las posiciones atómicas, sin embargo, se debe proceder por prueba y error, porque no existe método conocido de calcular directamente las posiciones atómicas a partir de las intensidades observadas. Para ver porqué es esto así, consideraremos las dos ecuaciones básicas involucradas, a saber: cos I F p (5.0) sen cos que proporciona las intensidades relativas de los haces reflejados y N F fn e i (hu n kv n w n ) (5.) que proporciona el valor del factor de estructura F para la reflexión hk en términos de las posiciones atómicas uvw. 74
4 Puesto que la intensidad relativa I, el factor de multiplicidad p y el ángulo de Bragg se conocen para cada línea del patrón, se puede hallar el valor de F para cada reflexión de la ecuación (5.0). Pero F mide solamente la amplitud relativa de cada reflexión, mientras que para usar la ecuación (5.), para calcular las posiciones atómicas, se debe conocer el valor de F, el cual mide la amplitud y la fase de una reflexión relativa a la otra. Esta es la esencia del problema. Las intensidades de dos haces reflejados son proporcionales a los cuadrados de sus amplitudes pero independientes de sus fases relativas. Puesto que todo lo que se puede medir es la intensidad, se puede determinar la amplitud pero no la fase, lo cual significa que no se puede calcular el factor de estructura sino solamente su valor absoluto. Las posiciones atómicas, por lo tanto, se pueden determinar solamente por prueba y error. Se asume un conjunto de posiciones atómicas, se calculan las intensidades correspondientes a esas posiciones y las intensidades calculadas se comparan con las observadas, el proceso se repite hasta que se alcanza una concordancia satisfactoria EJEMPLO DE DETERMINACIÓN DE ESTRUCTURA El patrón de difracción de una muestra en polvo de CdTe se obtuvo usando una cámara Debye-Scherrer y radiación K de Cu. Los valores observados del sen para las primeras 6 líneas se listan en la Tabla 5-, junto con las intensidades relativas de las líneas estimadas visualmente. Este patrón puede indexarse sobre la base de una celda unidad cúbica y los índices de las líneas observadas se dan en la Tabla. El parámetro de red, calculado del valor de sen para la línea de más alto ángulo, es de 6.46 A. La densidad medida de la muestra fue de 5.8 g/cm3 y su peso molecular es 40.0 g/mol. La aplicación de la ecuación (5.9) da el número de N0V moléculas por celda unidad: N. M Reemplazando los valores, se tiene: Tabla 5- Línea Intensidad fuerte muy fuerte muy fuerte muy débil fuerte débil débil débil muy fuerte fuerte sen hk , , , 553 (5.8 g / cm3 )( molec / mol)( cm) g / mol En este punto, se conoce que la celda unidad del CdTe es cúbica y que contiene 4 moléculas de CdTe, esto es, 4 átomos de Cd y 4 átomos de Te. Se debe ahora considerar los posibles arreglos de estos átomos en la celda unidad. Examinando los índices listados en la Tabla 5- se observa que los índices son todos no mezclados, por lo que la red de Bravais debe ser cara centrada. Sin embargo se observa, además, que no están presentes todos los posibles conjuntos de índices no mezclados: 00, 40, 600, 44, 6 y 640 no se encuentran en el patrón. Pero estas reflexiones pueden ser demasiado débiles para ser observadas y el hecho de que ellas no aparezcan no invalida la conclusión de que la red es cara centrada. Existen dos estructuras cúbicas caras centradas del tipo AB, esto es, que contienen dos átomos diferentes en iguales proporciones y N 75
5 ambas contienen cuatro moléculas por celda unidad: estas son la estructura NaCl, de enlace iónico y la forma blenda de zinc del ZnS, de enlace covalente. El siguiente paso es calcular las intensidades difractadas relativas para cada estructura y compararlas con el experimento, para determinar cual de estas estructuras es la correcta. Si el CdTe tiene la estructura del NaCl entonces su factor de estructura para índices no mezclados es dado por: F 6 (f Cd f Te ), si (h k ) es par F 6 (f Cd f Te ), si (h k ) es impar (5.) Por otro lado, si la estructura ZnS es correcta, entonces el factor de estructura para índices no mezclados es dado por: F 6 (f Cd f Te ), si (h k ) es impar F 6 (f Cd f Te ), si (h k ) es un impar múltiplo de (5.3) F 6 (f Cd f Te ), si (h k ) es un par múltiplo de. Si antes de realizar un cálculo detallado de intensidades difractadas relativas por medio de la ecuación (5.0), casi se puede descartar la estructura NaCl como una posibilidad simplemente inspeccionando las ecuaciones (5.). Los números atómicos del Cadmio y el Teluro son 48 y 5, respectivamente, así que los valores de (f Cd f Te ) es varios cientos más grande que el valor de (f Cd f Te ), para todos los valores del sen /. Entonces, si el CdTe tiene la estructura del NaCl, la reflexión debería ser muy débil y la reflexión 00 muy fuerte. En la Tabla 5-, la reflexión es fuerte y la 00 no se observa. Evidencia posterior que la estructura NaCl es incorrecta se da en la cuarta columna de la Tabla 5-, donde las intensidades calculadas de las primeras ocho posibles líneas se listan: no existe concordancia entre estos valores y las intensidades observadas. Por otro lado, si se asume la estructura ZnS, los cálculos de intensidad conducen a los valores listados en la quinta columna. La concordancia entre estos valores y las intensidades observadas es excelente, excepto para un poco menor inconsistencia entre las reflexiones a bajo ángulo y que se debe a que se ha despreciado el factor de absorción. En particular, se nota que la estructura ZnS cuenta satisfactoriamente para todas las reflexiones perdidas (00, 40, etc.) puesto que las intensidades calculadas de estas reflexiones son todas extremadamente bajas. Se puede concluir, por lo tanto, que el CdTe tiene la estructura de la forma blenda de zinc del ZnS. Antes de que una estructura sea mostrada que está en concordancia con la data de difracción, es recomendable calcular las distancias interatómicas incluidas en esa estructura. Este cálculo no sólo es de interés por si mismo, sino que sirve para revelar cualquier error que pudo haberse cometido, puesto que existe obviamente algo incorrecto con una estructura propuesta si ubica ciertos átomos juntos lo que es imposible. En nuestro caso, el vecino más próximo al átomo de Cd en 000 es el átomo de Te en ¼ ¼ ¼. La distancia interatómica Cd-Te es por lo tanto 3 a / 4.80 A. Para comparar, se puede calcular una distancia interatómica Cd-Te teórica prondo las distancias de aproximación de los átomos más próximos en los elementos puros. Para hacer esto, consideramos los átomos como esferas rígidas en contacto e ignoramos los efectos del número de coordinación y el tipo de enlace sobre el tamaño del átomo. 76
6 Tabla 5-3 Línea hk Intensidad observada , , , , fuerte muy fuerte muy fuerte muy débil fuerte débil débil débil muy fuerte fuerte 4 5 Intensidad calculada Estructura NaCl Estructura ZnS Estas distancias de aproximación son.98 A en el Cadmio puro y.87 A en el Teluro puro, el promedio es.93 A. La distancia interatómica observada Cd-Te es.80 A, casi el 4.5% más pequeño que el valor calculado; esta diferencia es razonable y puede ser debido al enlace covalente que caracteriza esta estructura. 77
7 LABORATORIO N DETERMINACIÓN DE ESTRUCTURAS HEXAGONALES OBJETIVOS. Registrar la intensidad de los rayos X difractados por una muestra en polvo de zinc como una función del ángulo de difracción. Calcular las constantes de red del zinc a partir de las posiciones angulares de las líneas individuales de Bragg. Asignar las reflexiones de Bragg a los correspondientes planos de la red del zinc y determinar el tipo de red de Bravais. Determinar el número de átomos en la celda unitaria del zinc. TEORÍA.Cuando rayos x de longitud de onda inciden sobre un conjunto de planos de la red de un cristal de espaciado d bajo un ángulo de inclinación, entonces los rayos reflejados sólo serán sujetos a interferencia constructiva cuando se satisface la condición de Bragg, esto es: d sen Donde n es el orden de difracción. () d Cuando existe sólo un átomo en la celda unidad, entonces todas las reflexiones que ocurren satisfacen d sen d sen las condiciones de Bragg, ver Figura. Cuando Figura.- Condición de Bragg para existen N átomos en una celda unidad, sin embargo, reflexión constructiva de los rayos X por entonces la amplitud total de los rayos x dispersados los planos de un cristal. por la celda es descrita por el factor de estructura F, que se calcula totalizando los factores de dispersión atómica f de los N átomos individuales, teniendo en cuenta sus fases. En general, para el factor de estructura F, se cumple que: N Fhk f n e i (hu n kv n w n ) () donde h, k, son los índices de Miller de los planos reflectantes de la red cristalina y, u n, v n, w n son las coordenadas de los átomos en fracciones de las longitudes particulares de las aristas de la celda unidad. Como en general F es un número complejo, la intensidad total dispersada es descrita por Fhk. La celda unitaria de un sistema hexagonal con la mayor densidad de empaquetamiento de esferas contiene dos átomos con posiciones 0,0,0 y /3,/3,/. De acuerdo a la ecuación (), por consiguiente, el factor de estructura F para este tipo de red cristalina es dada por: (3) F f{e i (0) e i[(/3) h (/3) k (/) ]} La Tabla N proporciona las reglas de selección para el factor de estructura F, considerando que n 0,,,3, 4,... 78
8 Para el sistema cristalino hexagonal, de constantes de red a y c, el espaciado d de los planos individuales de la red cristalina, con índices (hk ), se obtiene de la forma cuadrática: 4 h h k k (4) c d hk 3 a Tabla N.- Reglas de selección para el factor de estructura F de sistemas hexagonales h k 3n Impar De las ecuaciones (4) y (), con n, se obtiene la ecuación n Par cuadrática de Bragg: 3n Impar 4 (h h k k ) sen (5) 4 3 3n Par a c Para la evaluación del registro de difracción, la ecuación (5) se puede escribir como: sen A (h h k k ) C Donde se ha considerado que: A y C F 0 4f 3f f (6). 3a 4 c El valor de A se obtiene a partir de las líneas hk0. Cuando 0, la ecuación (6) se convierte sen A (h h k k ) en: (7) Los valores permitidos de (h hk k ) se determinan de una Tabla de Formas Cuadráticas de los índices de Miller, como la que se incluye en el Apéndice ; estos valores se reproducen en la Tabla N. Por lo tanto, las líneas hk0 deben tener valores de sen en la proporción de estos enteros y A será algún número como, /3, /4, /7, /9, etc., veces los valores del sen de estas líneas. Determinado el valor de A se puede hallar el parámetro a de la celda. Tabla N.- Combinaciones permitidas h, k. hk h hk k El valor de C se obtiene de las otras líneas del patrón y el uso de la ecuación (6) en la forma: (8) sen A (h h k k ) C Las diferencias representadas por el lado izquierdo de la ecuación (8) se establecen para diversos valores asumidos de h y k, en un intento de hallar un conjunto consistente de valores de C, los cuales deben estar es la proporción, 4, 9, 6, etc. Una vez que estos valores se encuentran, puede calcularse C. Determinado el valor de C se puede hallar el parámetro c de la celda. Cuando no se usa filtro para la monocromatización de los rayos X, el hecho de que líneas muy intensas resultantes de la radiación K - estén acompañadas por líneas secundarias resultantes de la radiación más débil K - debe tomarse en consideración cuando se evalúan las líneas individualmente. Los pares de líneas K y K se pueden identificar de la ecuación () si consideramos que: (K ) sen 54.8 pm. (K ) sen 39. pm (9) 79
9 Por otro lado, para una masa m de átomos o moléculas contenidas en un volumen V de la celda m NM unidad, se tiene que su densidad es dada por:. V N0V Luego, el número N de átomos o moléculas en la celda unidad es: N N 0 ( 3 a c / ) (0) M Donde: N 0 es el Número de Avogadro, a y c son las constantes de la red y M es el peso atómico. EQUIPOS Y MATERIALES.Unidad de rayos X Goniómetro Tubo de rayos X con ánodo de Cu Tubo contador tipo B Cristal de LiF(00) d m Soporte universal de cristales Portamuestra de polvo Diafragma tubular de mm de diámetro Diafragma tubular con hoja de níquel Polvo de zinc Cuchara con extremo en forma de espátula Vaselina Mortero y pistilo Computador personal PROCEDIMIENTO.I. Preparación de la muestra. Preparar la muestra en polvo, echando una suficiente cantidad de polvo de zinc en el mortero y molerla hasta lograr pulverizarla.. Transferir un poco de polvo de zinc a una hoja de papel y usar la espátula para amasarla hasta lograr una pasta firme. Para lograr la concentración más alta posible del material, usar muy poca vaselina, sólo una punta de la espátula. 3. Llevar la muestra en pasta relativamente sólida dentro del espécimen para muestras de polvo y aplanarla al mismo nivel. Usar el soporte universal de cristales para sujetar la muestra. II. Calibración del goniómetro 4. Instalar el tubo de rayos X con ánodo de cobre e insertar en el orificio de salida del haz el diafragma tubular de mm de diámetro. 5. Montar el cristal de LiF en el soporte del goniómetro y, considerando que teóricamente la reflexión más intensa 00 del cristal se ubica a un ángulo de.6º, calibrar el goniómetro como se indicó en el Laboratorio. III. Obtención del Registro de difracción 6. Montar el experimento como se muestra en la Figura, fijando la línea de marca del bloque del goniómetro en la posición 4.5. Para obtener un buen ángulo de resolución empuje el soporte del tubo contador a la parte posterior. 7. Fijar el diafragma tubular de mm de diámetro en la salida del tubo de rayos X y montar la muestra de zinc en el soporte del goniómetro. Cerrar y asegurar la puerta. 8. Encender la unidad de rayos X y la computadora y abrir el programa measure. Seleccionar del menú Archivo/Nueva medida o presionar el botón de registro rojo en el panel de botones. 9. En el cuadro de diálogo introducir los siguientes valores: 80
10 Tipo de medida : espectro Corriente de emisión : ma Registro de datos : ángulo del cristal Tiempo de integración : s Tensión constante : 35 kv Modo rotación : acoplado : Cristal : Zn Ángulo de arranque : 0º Absorbedor : sin absorbedor Ángulo de parada : 60º Filtro : sin filtro Incremento del ángulo : 0,º 0. Seleccionar Continuar y en el cuadro de diálogo que aparece seleccionar iniciar medida. Cuando termine el registro, archivar el espectro obtenido y apagar el equipo de rayos X.. Fijar el diafragma tubular con hoja de Níquel en la salida del tubo de rayos X y montar la muestra de zinc en el soporte del goniómetro. Cerrar y asegurar la puerta. Figura.- Montaje experimental para la obtención del registro. Encender la unidad de rayos X y la computadora y abrir el programa measure. Seleccionar del menú Archivo/Nueva medida o presionar el botón de registro rojo en el panel de botones. 3. En el cuadro de diálogo introducir los siguientes valores: Tipo de medida : espectro Corriente de emisión : ma Registro de datos : ángulo del cristal Tiempo de integración : s Tensión constante : 35 kv Modo rotación : acoplado : Cristal : Zn Ángulo de arranque : 0º Absorbedor : sin absorbedor Ángulo de parada : 60º Filtro : Ni Incremento del ángulo : 0,º 4. Seleccionar Continuar y en el cuadro de diálogo que aparece seleccionar iniciar medida. Cuando termine el registro, archivar el espectro obtenido y apagar el equipo de rayos X. CUESTIONARIO.. Observar el registro de difracción del Zinc, obtenido sin filtro, y registrar en la Tabla N 3 los valores de correspondientes a cada pico de difracción. Determinar los valores de sen en cada caso para identificar los picos de difracción K y K usando la ecuación (9). 8
11 . Usar el registro de difracción del Zinc, obtenido con filtro de Níquel, para corroborar que la identificación de los picos de difracción K ha sido correcta. Qué observa respecto a la intensidad los picos? Qué ocurre con la detección de las reflexiones a grandes ángulos de difracción? 3. Completar la Tabla Nº 3 y buscar los cocientes que sean aproximadamente iguales entre si, o a los valores de sen, ya que puede asumirse que los picos correspondientes tienen índices con 0. Asignar los índices de Miller a estos picos, tomando como referencia las combinaciones permitidas h, k que se listan en la Tabla Nº. Tabla Nº 3 Pico i sen i sen i sen i / 3 sen i / 4 sen i / 7 hk Pror los valores de los cocientes identificados aproximadamente iguales para determinar el valor de A. 5. A partir de la ecuación A / 3a, determinar la constante de red a, usando los valores de A y (K ) 54.8 pm. 6. Completar la Tabla Nº 4 y buscar valores C que estén a una razón, 4, 9, 6, etc. Asignar los índices de Miller a estos picos, tomando como referencia las combinaciones permitidas h, k que se listan en la Tabla N. Tabla N 4 Pico i sen i sen i A sen i 3A sen i 4A hk
12 7. Usando la ecuación (8) determinar los valores correspondientes de C y determinar su valor promedio. 8. A partir de la ecuación C / 4 c, determinar la constante de red c, usando los valores de C y (K ) 54.8 pm. 9. Considerando los valores aceptados de a 66.3pm y c 49.5 pm para las dos constantes de la red hexagonal del zinc, determinar el error relativo en la determinación experimental de estos parámetros. 0. Demostrar que para una celda unitaria hexagonal de parámetros a y c su volumen es dado 3 por V a c.. Considerando que la densidad del zinc es 7.4 g/cm3 y que su peso atómico es gramos, usando la ecuación (0) determinar el número de átomos en la celda unitaria de la red del zinc.. Del análisis de sus resultados, determinar el tipo de red de Bravais que le corresponde al zinc y representarla en un dibujo. 83
13 LABORATORIO N DETERMINACIÓN DE ESTRUCTURAS TETRAGONALES OBJETIVOS. Registrar la intensidad de los rayos X difractados por una muestra en polvo de dióxido de plomo (PbO ) como una función del ángulo de difracción. Calcular las constantes de red del PbO partir de las posiciones angulares de las líneas individuales de Bragg. Asignar las reflexiones de Bragg a los correspondientes planos de la red del PbO y determinar el tipo de red de Bravais. Determinar el número de átomos en la celda unitaria del PbO. TEORÍA.Cuando rayos x de longitud de onda inciden sobre un conjunto de planos de la red de un cristal de espaciado d bajo un ángulo de inclinación, entonces los rayos reflejados sólo serán sujetos a interferencia constructiva cuando se satisface la condición de Bragg, esto es: d sen () Donde n es el orden de difracción. Cuando existe sólo un átomo en la celda unidad, entonces todas las reflexiones que ocurren satisfacen las condiciones de Bragg. Cuando existen N átomos en una celda unidad, sin embargo, entonces la amplitud total de los rayos x dispersados por la celda es descrita por el factor de estructura F, que se calcula totalizando los factores de dispersión atómica f de los N átomos individuales, teniendo en cuenta sus fases. En general, para el factor de estructura F, se cumple que: N Fhk f n e i (hu n kv n w n ) () donde h, k, son los índices de Miller de los planos reflectantes de la red cristalina y, u n, v n, w n son las coordenadas de los átomos en fracciones de las longitudes particulares de las aristas de la celda unidad. Como en general F es un número complejo, la intensidad total dispersada es descrita por Fhk. La celda unitaria de un sistema tetragonal puede ser simple, esto es, tener sólo un átomo en el origen de la red. Adicionalmente a esto, pueden existir otras variantes: celdas unidad caras centradas y cuerpo centrado. Solamente la última, que contiene dos átomos o moléculas en las coordenadas 0,0,0 y /,/,/ será considerada aquí. De acuerdo a la ecuación (), por consiguiente, el factor de estructura F para este tipo de red cristalina es dada por: F f{e i (0) e i[(/) h (/) k (/) ]} Cuando h k n, con n,, 3, 4..., la suma es impar, así que F 0. Si h k n, la suma es par, entonces F f y Fhk (3) 4f. 84
14 Para el sistema cristalino tetragonal, de constantes de red a y c, el espaciado d de los planos individuales de la red cristalina, con índices (hk ), se obtiene de la forma cuadrática: h k (4) d hk a c De las ecuaciones (4) y (), con n, se obtiene la ecuación cuadrática de Bragg: h k sen (5) 4 a c Para la evaluación del registro de difracción, la ecuación (5) se puede escribir como: sen A (h k ) C (6) y C. 4a 4c El valor de A se obtiene a partir de las líneas hk0. Cuando 0, la ecuación (6) se convierte Donde se ha considerado que: A sen A (h k ) en: (7) Los valores permitidos de (h k ) son,, 4, 5, 8, 9, 0, etc., ver Tabla. Tabla N.- Combinaciones permitidas h, k. hk h k Por lo tanto, las líneas hk0 deben tener valores de sen en la proporción de estos enteros, y A será algún número como, /, /4, /5, /8, /9, /0, etc., veces los valores del sen de estas líneas. Determinado el valor de A se puede hallar el parámetro a de la celda. El valor de C se obtiene de las otras líneas del patrón y el uso de la ecuación (6) en la forma: (8) sen A (h k ) C Las diferencias representadas por el lado izquierdo de la ecuación (8) se establecen para diversos valores asumidos de h y k, en un intento de hallar un conjunto consistente de valores de C, los cuales deben estar es la proporción, 4, 9, 6, etc. Una vez que estos valores se encuentran, puede calcularse C. Determinado el valor de C se puede hallar el parámetro c de la celda. Cuando no se usa filtro para la monocromatización de los rayos X, el hecho de que líneas muy intensas resultantes de la radiación K - estén acompañadas por líneas secundarias resultantes de la radiación más débil K - debe tomarse en consideración cuando se evalúan las líneas individualmente. Los pares de líneas K y K se pueden identificar de la ecuación () si consideramos que: (K ) sen 54.8 pm. (9) (K ) sen 39. pm Por otro lado, para una masa m de átomos o moléculas contenidas en un volumen V de la celda m NM unidad, se tiene que su densidad es dada por:. V N0V Luego, el número N de átomos o moléculas en la celda unidad es: N N 0 (a c) M (0) 85
15 Donde: N 0 es el Número de Avogadro, a y c son las constantes de la red y M es el peso molecular. EQUIPOS Y MATERIALES.Unidad de rayos X Goniómetro Tubo de rayos X con ánodo de Cu Tubo contador tipo B Cristal de LiF(00) d m Soporte universal de cristales Portamuestra de polvo Diafragma tubular de mm de diámetro Diafragma tubular con hoja de níquel Polvo de PbO Cuchara con extremo en forma de espátula Vaselina Mortero y pistilo Computador personal PROCEDIMIENTO.I. Preparación de la muestra. Preparar la muestra en polvo, echando una suficiente cantidad de polvo de PbO en el mortero y molerla hasta lograr pulverizarla.. Transferir un poco de polvo de PbO a una hoja de papel y usar la espátula para amasarla hasta lograr una pasta firme. Para lograr la concentración más alta posible del material, usar muy poca vaselina, sólo una punta de la espátula. 3. Llevar la muestra en pasta relativamente sólida dentro del espécimen para muestras de polvo y aplanarla al mismo nivel. Usar el soporte universal de cristales para sujetar la muestra. II. Calibración del goniómetro 4. Instalar el tubo de rayos X con ánodo de cobre e insertar en el orificio de salida del haz el diafragma tubular de mm de diámetro. 5. Montar el cristal de LiF en el soporte del goniómetro y, considerando que teóricamente la reflexión más intensa 00 del cristal se ubica a un ángulo de.6º, calibrar el goniómetro como se indicó en el Laboratorio. III. Obtención del Registro de difracción 6. Montar el experimento como se muestra en la Figura, fijando la línea de marca del bloque del goniómetro en la posición 4.5. Para obtener un buen ángulo de resolución empuje el soporte del tubo contador a la parte posterior. 7. Fijar el diafragma tubular de mm de diámetro en la salida del tubo de rayos X y montar la muestra de PbO en el soporte del goniómetro. Cerrar y asegurar la puerta. 8. Encender la unidad de rayos X y la computadora y abrir el programa measure. Seleccionar del menú Archivo/Nueva medida o presionar el botón de registro rojo en el panel de botones. 9. En el cuadro de diálogo introducir los siguientes valores: Tipo de medida : espectro Corriente de emisión : ma Registro de datos : ángulo del cristal Tiempo de integración : s Tensión constante : 35 kv Modo rotación : acoplado : Cristal : PbO Ángulo de arranque : 0º Absorbedor : sin absorbedor Ángulo de parada : 45º Filtro : sin filtro Incremento del ángulo : 0,º 86
16 0. Seleccionar Continuar y en el cuadro de diálogo que aparece seleccionar iniciar medida. Cuando termine el registro, archivar el espectro obtenido y apagar el equipo de rayos X.. Fijar el diafragma tubular con hoja de Níquel en la salida del tubo de rayos X y montar la muestra de PbO en el soporte del goniómetro. Cerrar y asegurar la puerta. Figura.- Montaje experimental para la obtención del registro. Encender la unidad de rayos X y la computadora y abrir el programa measure. Seleccionar del menú Archivo/Nueva medida o presionar el botón de registro rojo en el panel de botones. 3. En el cuadro de diálogo introducir los siguientes valores: Tipo de medida : espectro Corriente de emisión : ma Registro de datos : ángulo del cristal Tiempo de integración : s Tensión constante : 35 kv Modo rotación : acoplado : Cristal : PbO Ángulo de arranque : 0º Absorbedor : sin absorbedor Ángulo de parada : 45º Filtro : Ni Incremento del ángulo : 0,º 4. Seleccionar Continuar y en el cuadro de diálogo que aparece seleccionar iniciar medida. Cuando termine el registro, archivar el espectro obtenido y apagar el equipo de rayos X. CUESTIONARIO.. Observar el registro de difracción del PbO, obtenido sin filtro, y registrar en la Tabla N los valores de correspondientes a cada pico de difracción. Determinar los valores de sen en cada caso para identificar los picos de difracción K y K usando la ecuación (9).. Usar el registro de difracción del PbO, obtenido con filtro de Níquel, para corroborar que la identificación de los picos de difracción K ha sido correcta. Qué observa respecto a la intensidad los picos? Qué ocurre con la detección de las reflexiones a grandes ángulos de difracción? 87
17 3. Completar la Tabla Nº 3 y buscar los cocientes que sean aproximadamente iguales entre si, o a los valores de sen, ya que puede asumirse que los picos correspondientes tienen índices con 0. Asignar los índices de Miller a estos picos, tomando como referencia las combinaciones permitidas h, k que se listan en la Tabla Nº. Tabla Nº i Pico sen i sen i sen i / sen i / 4 sen i / 5 sen i / 8 hk Pror los valores de los cocientes identificados que sean aproximadamente iguales para determinar el valor de A. 5. A partir de la ecuación A / 4 a, determinar la constante de red a del PbO, usando los valores de A y (K ) 54.8 pm. 6. Completar la Tabla Nº 3 y buscar valores C que estén a una razón, 4, 9, 6, etc. Asignar los índices de Miller a estos picos, tomando como referencia las combinaciones permitidas h, k que se listan en la Tabla N. Tabla N 3 Pico i sen i sen i A sen i A sen i 4A sen i 5A sen i 8A hk
18 7. Usando la ecuación (8) determinar los valores correspondientes de C y determinar su valor promedio. 8. A partir de la ecuación C / 4 c, determinar la constante de red c del PbO, usando los valores de C y (K ) 54.8 pm. 9. Considerando los valores aceptados de a 66.3pm y c 49.5 pm para las dos constantes de la red tetragonal del PbO, determinar el error relativo en la determinación experimental de estos parámetros. 0. Considerando que la densidad del PbO es g/cm3 y que su peso molecular es 39.9 gramos, usando la ecuación (0) determinar el número de átomos en la celda unitaria de la red del PbO.. Del análisis de sus resultados, determinar el tipo de red de Bravais que le corresponde al PbO y representarla en un dibujo. 89
DETERMINACIÓN DE ESTRUCTURAS CRISTALINAS I. La determinación de una estructura desconocida se realiza en tres etapas principales:
 CAPÍTULO 4 DETERMINACIÓN DE ESTRUCTURAS CRISTALINAS I 4.. INTRODUCCIÓN El método que se adopta para la determinación de las estructuras cristalinas es esencialmente la de prueba y error. Sobre la base
CAPÍTULO 4 DETERMINACIÓN DE ESTRUCTURAS CRISTALINAS I 4.. INTRODUCCIÓN El método que se adopta para la determinación de las estructuras cristalinas es esencialmente la de prueba y error. Sobre la base
PROPIEDADES DE LOS RAYOS X I
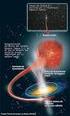 CAPÍTULO.. RADIACIÓN ELECTROMAGNÉTICA Los rayos X son radiación electromagnética de la misma aturaleza que la luz pero de longitud de onda mucho más corta. La unidad de medida en la región de los rayos
CAPÍTULO.. RADIACIÓN ELECTROMAGNÉTICA Los rayos X son radiación electromagnética de la misma aturaleza que la luz pero de longitud de onda mucho más corta. La unidad de medida en la región de los rayos
MEDIDAS DIFRACTOMÉTRICAS 1.1. ASPECTOS GENERALES DEL DIFRACTÓMETRO DE RAYOS X
 CAPÍTULO 1 MEDIDAS DIFRACTOMÉTRICAS 1.1. ASPECTOS GENERALES DEL DIFRACTÓMETRO DE RAYOS X Los aspectos esenciales de un difractómetro se muestran en la Figura 1.1. Una muestra cristalina sólida o en polvo
CAPÍTULO 1 MEDIDAS DIFRACTOMÉTRICAS 1.1. ASPECTOS GENERALES DEL DIFRACTÓMETRO DE RAYOS X Los aspectos esenciales de un difractómetro se muestran en la Figura 1.1. Una muestra cristalina sólida o en polvo
Contenido. 5. Estructura cristalina. Omar De la Peña-Seaman IFUAP Física del Estado Sólido Maestría (Física) 1/51 51
 Contenido 5. Estructura cristalina 1 / Omar De la Peña-Seaman IFUAP Física del Estado Sólido Maestría (Física) 1/51 51 Contenido: Tema 05 5. Estructura cristalina 5.1 Arreglo periódico de átomos: bases,
Contenido 5. Estructura cristalina 1 / Omar De la Peña-Seaman IFUAP Física del Estado Sólido Maestría (Física) 1/51 51 Contenido: Tema 05 5. Estructura cristalina 5.1 Arreglo periódico de átomos: bases,
Practica nº n 5: Fenómenos de Difracción.
 Facultad de Farmacia Universidad de Granada Departamento de Química Física Practica nº n 5: Fenómenos de Difracción. OBJETIVOS 1.Observar los fenómenos de difracción Rendija simple Rendija doble 2.Calcular
Facultad de Farmacia Universidad de Granada Departamento de Química Física Practica nº n 5: Fenómenos de Difracción. OBJETIVOS 1.Observar los fenómenos de difracción Rendija simple Rendija doble 2.Calcular
Estado Sólido. Estado Sólido. Estado Sólido. Estado Sólido - + Sólidos cristalinos y sólidos amorfos
 Sólidos cristalinos y sólidos amorfos Sólidos cristalinos: presentan un ordenamiento regular en el espacio Sólidos amorfos: no presentan el ordenamiento típico de los cristalinos Región cristalina Región
Sólidos cristalinos y sólidos amorfos Sólidos cristalinos: presentan un ordenamiento regular en el espacio Sólidos amorfos: no presentan el ordenamiento típico de los cristalinos Región cristalina Región
Pontificia Universidad Católica de Chile Facultad de Física. Estática
 Pontificia Universidad Católica de Chile Facultad de Física Estática La estática es una rama de la Mecánica Clásica que estudia los sistemas mecánicos que están en equilibrio debido a la acción de distintas
Pontificia Universidad Católica de Chile Facultad de Física Estática La estática es una rama de la Mecánica Clásica que estudia los sistemas mecánicos que están en equilibrio debido a la acción de distintas
Estructura de los Sólidos
 Estructura de los Sólidos Estructura Cristalina OBJETIVOS a) Definir sólidos cristalinos y amorfos b) Definir estructura cristalina c) Describir las diferentes estructuras cristalinas d) Utilizar índices
Estructura de los Sólidos Estructura Cristalina OBJETIVOS a) Definir sólidos cristalinos y amorfos b) Definir estructura cristalina c) Describir las diferentes estructuras cristalinas d) Utilizar índices
Estructura cristalina: Índices de Miller. Y en términos de grado de compacidad? Volumen de átomos= Volumen de la celda= ( ) 3
 1 Cuántos átomos hay en una celda unidad? Vértices 1/8 Caras 1/2 Número total de átomos en la celda unidad: 8 en los vértices: 8 x 1/8 = 1 6 en las caras: 6 x 1/2 = 3 Total: 4 átomos Y en términos de grado
1 Cuántos átomos hay en una celda unidad? Vértices 1/8 Caras 1/2 Número total de átomos en la celda unidad: 8 en los vértices: 8 x 1/8 = 1 6 en las caras: 6 x 1/2 = 3 Total: 4 átomos Y en términos de grado
Tutoría 2: Experimentos de difracción
 Tutoría 2: Experimentos de difracción T2.1 Introducción En esta tutoría trataremos la cuestión fundamental de cómo conocemos donde se sitúan los átomos en un sólido. La demostración realizada se basa en
Tutoría 2: Experimentos de difracción T2.1 Introducción En esta tutoría trataremos la cuestión fundamental de cómo conocemos donde se sitúan los átomos en un sólido. La demostración realizada se basa en
Diagrama de correlación de enlaces moleculares Antienlace : rojo 1s similar a 2s
 Redes Cristalinas Ciencia de Materiales Ing. en Mecatrónica Otoño 2009 Lilia Meza Montes-IFUAP Diagrama de correlación de enlaces moleculares Antienlace : rojo 1s similar a 2s Sólidos cristalinos y amorfos
Redes Cristalinas Ciencia de Materiales Ing. en Mecatrónica Otoño 2009 Lilia Meza Montes-IFUAP Diagrama de correlación de enlaces moleculares Antienlace : rojo 1s similar a 2s Sólidos cristalinos y amorfos
CRISTALOGRAFIA. Es un sólido compuesto de átomos, iones o moléculas ordenados de una cierta forma y que se repite en tres dimensiones.
 CRISTALOGRAFIA CRISTAL SÓLIDO MONOCRISTALINO SÓLIDO POLICRISTALINO Es un sólido compuesto de átomos, iones o moléculas ordenados de una cierta forma y que se repite en tres dimensiones. Región donde el
CRISTALOGRAFIA CRISTAL SÓLIDO MONOCRISTALINO SÓLIDO POLICRISTALINO Es un sólido compuesto de átomos, iones o moléculas ordenados de una cierta forma y que se repite en tres dimensiones. Región donde el
Estructuras Cristalinas más usuales de Metales Puros (y de sus soluciones sólidas) Cristales metálicos
 Estructuras Cristalinas más usuales de Metales Puros (y de sus soluciones sólidas) Reglas generales Para un cristal al equilibrio químico, los átomos se ordenarán en forma regular y compacta, de manera
Estructuras Cristalinas más usuales de Metales Puros (y de sus soluciones sólidas) Reglas generales Para un cristal al equilibrio químico, los átomos se ordenarán en forma regular y compacta, de manera
 Caso de varios vectores primitivos de un mismo arreglo. Base o Motivo: Átomo o conjunto de átomos que se asocian con un punto de la malla Malla o Lattice: Es un arreglo infinito de puntos en el espacio,
Caso de varios vectores primitivos de un mismo arreglo. Base o Motivo: Átomo o conjunto de átomos que se asocian con un punto de la malla Malla o Lattice: Es un arreglo infinito de puntos en el espacio,
ESTEQUIOMETRIA. H 2 SO Na Na 2 SO 4 + H 2 Acido sulfúrico Sodio Sulfato de sodio Hidrógeno
 ESTEQUIOMETRIA 1.- Se hace reaccionar 4,00 g de ácido sulfúrico con sodio metálico en condiciones estequiométricas. a) Cuántos moles de sulfato de sodio se obtienen? b) Cuántas moléculas de hidrógeno se
ESTEQUIOMETRIA 1.- Se hace reaccionar 4,00 g de ácido sulfúrico con sodio metálico en condiciones estequiométricas. a) Cuántos moles de sulfato de sodio se obtienen? b) Cuántas moléculas de hidrógeno se
DEPARTAMENTO DE TECNOLOGÍA Actividades complementarias Curso: 1º Bach. Profesor: José Jiménez R. Tema 12: Materiales Metálicos: Metales ferrosos
 PARTAMENTO 1.- Determinar, en %, el factor de empaquetamiento de una: a) Red cúbica centrada en el cuerpo (BCC). b) Red cúbica centrada en las caras (FCC). 2.- El hierro a 20 ºC cristaliza en una red BCC
PARTAMENTO 1.- Determinar, en %, el factor de empaquetamiento de una: a) Red cúbica centrada en el cuerpo (BCC). b) Red cúbica centrada en las caras (FCC). 2.- El hierro a 20 ºC cristaliza en una red BCC
ANÁLISIS CUANTITATIVO POR WDFRX
 ANÁLISIS CUANTITATIVO POR WDFRX El análisis cuantitativo se obtiene mediante la medida de las intensidades de las energías emitidas por la muestra. Siendo la intensidad de la emisión (número de fotones)
ANÁLISIS CUANTITATIVO POR WDFRX El análisis cuantitativo se obtiene mediante la medida de las intensidades de las energías emitidas por la muestra. Siendo la intensidad de la emisión (número de fotones)
Siete sistemas y catorce retículos
 ESTRUCTURA CRISTALINA - PERFECCION Siete sistemas y catorce retículos Celda unitaria c a b Constantes reticulares o parámetros reticulares Longitud de los bordes Ángulos entre los ejes cristalográficos
ESTRUCTURA CRISTALINA - PERFECCION Siete sistemas y catorce retículos Celda unitaria c a b Constantes reticulares o parámetros reticulares Longitud de los bordes Ángulos entre los ejes cristalográficos
Estequiometria estequio metría
 La estequiometria es el concepto usado para designar a la parte de la química que estudia las relaciones cuantitativas de las sustancias y sus reacciones. En su origen etimológico, se compone de dos raíces,
La estequiometria es el concepto usado para designar a la parte de la química que estudia las relaciones cuantitativas de las sustancias y sus reacciones. En su origen etimológico, se compone de dos raíces,
TEMA 2 CONCEPTOS BÁSICOS Cálculos estequiométricos
 TEMA 2 CONCEPTOS BÁSICOS Cálculos estequiométricos ÍNDICE 1. Ecuaciones (reacciones) químicas 2. Cálculos estequiométricos. Reactivo limitante y reacciones consecutivas 3. Pureza de un reactivo 4. Rendimiento
TEMA 2 CONCEPTOS BÁSICOS Cálculos estequiométricos ÍNDICE 1. Ecuaciones (reacciones) químicas 2. Cálculos estequiométricos. Reactivo limitante y reacciones consecutivas 3. Pureza de un reactivo 4. Rendimiento
DIRECCIÓN DE LOS HACES DIFRACTADOS
 CAPÍTULO 6 6.1 DIFRACCIÓN DE RAYOS X Cuando los rayos X son dispersados por el entorno ordenado de un cristal, tienen lugar interferencias - tanto constructivas como destructivas - entre los rayos dispersados
CAPÍTULO 6 6.1 DIFRACCIÓN DE RAYOS X Cuando los rayos X son dispersados por el entorno ordenado de un cristal, tienen lugar interferencias - tanto constructivas como destructivas - entre los rayos dispersados
TRAZADO DE LÍNEAS EQUIPOTENCIALES
 TRAZADO DE LÍNEAS EQUIPOTENCIALES Nota: Traer, por comisión, dos hojas de papel carbónico de x 30 cm c/u, una hoja A3 o similar de 5 x 30 cm un pendrive o cualquier otro tipo de dispositivo estándar de
TRAZADO DE LÍNEAS EQUIPOTENCIALES Nota: Traer, por comisión, dos hojas de papel carbónico de x 30 cm c/u, una hoja A3 o similar de 5 x 30 cm un pendrive o cualquier otro tipo de dispositivo estándar de
ESTRUCTURAS CRISTALINAS (P2)
 ESTRUCTURAS CRISTALINAS (P2) Objetivos - Visualización de estructuras de sólidos mediante el uso de modelos - Estudio de redes cristalinas basadas en ordenamientos de esferas de igual tamaño - Identificación
ESTRUCTURAS CRISTALINAS (P2) Objetivos - Visualización de estructuras de sólidos mediante el uso de modelos - Estudio de redes cristalinas basadas en ordenamientos de esferas de igual tamaño - Identificación
C: GASES Y PRESIÓN DE VAPOR DEL AGUA
 hecho el vacío. Calcula a) Cantidad de gas que se tiene ; b) la presión en los dos recipientes después de abrir la llave de paso y fluir el gas de A a B, si no varía la temperatura. C) Qué cantidad de
hecho el vacío. Calcula a) Cantidad de gas que se tiene ; b) la presión en los dos recipientes después de abrir la llave de paso y fluir el gas de A a B, si no varía la temperatura. C) Qué cantidad de
COMO USAR EL APARATO DE RAYOS X
 COMO USAR EL APARATO DE RAYOS X INTRODUCCIÓN Software propio para el Aparato de rayos X El aparato de rayos X registra tasas de impulsos en función de los ajustes angulares del blanco y del sensor. El
COMO USAR EL APARATO DE RAYOS X INTRODUCCIÓN Software propio para el Aparato de rayos X El aparato de rayos X registra tasas de impulsos en función de los ajustes angulares del blanco y del sensor. El
Tema 2 Estructuras Cristalinas
 Tema 2 Estructuras Cristalinas Para poder comprender las propiedades de los materiales, y poder por tanto seleccionar el material idóneo para una aplicación específica, se hace necesario comprender la
Tema 2 Estructuras Cristalinas Para poder comprender las propiedades de los materiales, y poder por tanto seleccionar el material idóneo para una aplicación específica, se hace necesario comprender la
Estequiometría y Leyes Ponderales
 Estequiometría y Leyes Ponderales Equipo de Educación en Química Verde Centro Interdisciplinario de Líquidos Iónicos Programa de Educación Continua para el Magisterio Introducción Leyes fundamentales de
Estequiometría y Leyes Ponderales Equipo de Educación en Química Verde Centro Interdisciplinario de Líquidos Iónicos Programa de Educación Continua para el Magisterio Introducción Leyes fundamentales de
Determinación de la Masa Molar del Magnesio
 Determinación de la Masa Molar del Magnesio Introducción teórica Como en muchas reacciones químicas, los reactivos o sus productos o ambos son gases, es más común medir éstos en función del volumen usando
Determinación de la Masa Molar del Magnesio Introducción teórica Como en muchas reacciones químicas, los reactivos o sus productos o ambos son gases, es más común medir éstos en función del volumen usando
Parte I. Escoge la mejor contestación 1) Cuál es la unidad básica para medir cantidades de sustancias? a. Depende del tipo de sustancia que quieras
 Parte I. Escoge la mejor contestación 1) Cuál es la unidad básica para medir cantidades de sustancias? a. Depende del tipo de sustancia que quieras medir b. Litros c. Moles d. Kilogramos 2) Cuál es la
Parte I. Escoge la mejor contestación 1) Cuál es la unidad básica para medir cantidades de sustancias? a. Depende del tipo de sustancia que quieras medir b. Litros c. Moles d. Kilogramos 2) Cuál es la
LIGHT SCATTERING MEASUREMENTS FROM SMALL DIELECTRIC PARTICLES
 LIGHT SCATTERING MEASUREMENTS FROM SMALL DIELECTRIC PARTICLES M.Sc. Abner Velazco Dr. Abel Gutarra abnervelazco@yahoo.com Laboratorio de Materiales Nanoestructurados Facultad de ciencias Universidad Nacional
LIGHT SCATTERING MEASUREMENTS FROM SMALL DIELECTRIC PARTICLES M.Sc. Abner Velazco Dr. Abel Gutarra abnervelazco@yahoo.com Laboratorio de Materiales Nanoestructurados Facultad de ciencias Universidad Nacional
GUÍA DE EJERCICIOS CONCEPTOS FUNDAMENTALES
 GUÍA DE EJERCICIOS CONCEPTOS FUNDAMENTALES Área Resultados de aprendizaje Identifica, conecta y analiza conceptos básicos de química para la resolución de ejercicios, desarrollando pensamiento lógico y
GUÍA DE EJERCICIOS CONCEPTOS FUNDAMENTALES Área Resultados de aprendizaje Identifica, conecta y analiza conceptos básicos de química para la resolución de ejercicios, desarrollando pensamiento lógico y
PORTAFOLIO DE EVIDENCIAS QUÍMICA I DE SEGUNDA OPORTUNIDAD I LEE DETENIDAMENTE CADA ENUNCIADO Y CONTESTA SEGÚN SE TE PIDA.
 PORTAFOLIO DE EVIDENCIAS QUÍMICA I DE SEGUNDA OPORTUNIDAD I LEE DETENIDAMENTE CADA ENUNCIADO Y CONTESTA SEGÚN SE TE PIDA. 1.- Ciencia que estudia las características y la composición de los materiales,
PORTAFOLIO DE EVIDENCIAS QUÍMICA I DE SEGUNDA OPORTUNIDAD I LEE DETENIDAMENTE CADA ENUNCIADO Y CONTESTA SEGÚN SE TE PIDA. 1.- Ciencia que estudia las características y la composición de los materiales,
- Leyes ponderales: Las leyes ponderales relacionan las masas de las sustancias que intervienen en una reacción química.
 FÍSICA Y QUÍMICA 4ºESO COLEGIO GIBRALJAIRE CÁLCULOS QUÍMICOS 1.- LA REACCIÓN QUÍMICA. LEYES PONDERALES Una reacción química es el proceso en el que, mediante una reorganización de enlaces y átomos, una
FÍSICA Y QUÍMICA 4ºESO COLEGIO GIBRALJAIRE CÁLCULOS QUÍMICOS 1.- LA REACCIÓN QUÍMICA. LEYES PONDERALES Una reacción química es el proceso en el que, mediante una reorganización de enlaces y átomos, una
Práctica Módulo de torsión
 Práctica Módulo de torsión Objetivo eterminar el módulo de torsión de varillas de distintos materiales por los métodos estático y dinámico. Material Aparato de torsión representado en la figura, varillas
Práctica Módulo de torsión Objetivo eterminar el módulo de torsión de varillas de distintos materiales por los métodos estático y dinámico. Material Aparato de torsión representado en la figura, varillas
b. No debe reaccionar con ninguno de los componentes de la mezcla.
 ANÁLISIS CUALITATIVO Una vez obtenido un cromatograma satisfactorio se procede a realizar la identificación de los componentes de la muestra empleando alguna de las siguientes técnicas. 1. Técnica cualitativa
ANÁLISIS CUALITATIVO Una vez obtenido un cromatograma satisfactorio se procede a realizar la identificación de los componentes de la muestra empleando alguna de las siguientes técnicas. 1. Técnica cualitativa
En la figura 1 se observan los cambios de polaridad (positivo y negativo) y las variaciones en amplitud de una onda de ca.
 Página 1 de 7 TENSION ALTERNA En la figura 1 se observan los cambios de polaridad (positivo y negativo) y las variaciones en amplitud de una onda de ca. Puede definirse un voltaje alterno como el que varía
Página 1 de 7 TENSION ALTERNA En la figura 1 se observan los cambios de polaridad (positivo y negativo) y las variaciones en amplitud de una onda de ca. Puede definirse un voltaje alterno como el que varía
CONDUCTIVIDAD ELÉCTRICA I E
 CONDUCTVDAD LÉCTRCA La conductividad eléctrica de una substancia se define como la relación entre la intensidad de corriente eléctrica producida y el campo eléctrico que la produce: = el campo eléctrico
CONDUCTVDAD LÉCTRCA La conductividad eléctrica de una substancia se define como la relación entre la intensidad de corriente eléctrica producida y el campo eléctrico que la produce: = el campo eléctrico
Red de difracción (medida de λ del láser) Fundamento
 Red de difracción (medida de λ del láser) Fundamento Si sobre una superficie transparente marcamos en un gran número de rayas paralelas y equidistantes tendremos una red de difracción. El número de rayas
Red de difracción (medida de λ del láser) Fundamento Si sobre una superficie transparente marcamos en un gran número de rayas paralelas y equidistantes tendremos una red de difracción. El número de rayas
QUÍMICA. La MATERIA REPRESENTACIÓN. Observación Datos Ley Hipótesis Teoría DEFINICIONES BÁSICAS. Propiedades
 QUÍMICA La MATERIA Relación constante TEORÍA EXPERIMENTACIÓN Ciencia básica - Estructura - Composición - Propiedades - Transformaciones REPRESENTACIÓN OBSERVACIÓN mundo macroscópico Técnica sistemática
QUÍMICA La MATERIA Relación constante TEORÍA EXPERIMENTACIÓN Ciencia básica - Estructura - Composición - Propiedades - Transformaciones REPRESENTACIÓN OBSERVACIÓN mundo macroscópico Técnica sistemática
UNIVERSIDAD DE ANTIOQUIA FACULTAD DE QUÍMICA FARMACÉUTICA LABORATORIO DE QUÍMICA GENERAL Profesor: Jaime O. Pérez
 UNIVERSIDAD DE ANTIOQUIA FACULTAD DE QUÍMICA FARMACÉUTICA LABORATORIO DE QUÍMICA GENERAL Profesor: Jaime O. Pérez Práctica: Determinación de Densidades. Fecha: 24 de noviembre de 2009 DEYMER GÓMEZ CORREA:
UNIVERSIDAD DE ANTIOQUIA FACULTAD DE QUÍMICA FARMACÉUTICA LABORATORIO DE QUÍMICA GENERAL Profesor: Jaime O. Pérez Práctica: Determinación de Densidades. Fecha: 24 de noviembre de 2009 DEYMER GÓMEZ CORREA:
DEPARTAMENTO DE INGENIERIA QUÍMICA CÁTEDRA DE FISICOQUÍMICA TRABAJO PRÁCTICO DE LABORATORIO Nº 4
 Universidad Tecnológica Nacional Facultad Regional La Plata DEPARTAMENTO DE INGENIERIA QUÍMICA CÁTEDRA DE FISICOQUÍMICA TRABAJO PRÁCTICO DE LABORATORIO Nº 4 Descenso crioscópico Objeto de la experiencia:
Universidad Tecnológica Nacional Facultad Regional La Plata DEPARTAMENTO DE INGENIERIA QUÍMICA CÁTEDRA DE FISICOQUÍMICA TRABAJO PRÁCTICO DE LABORATORIO Nº 4 Descenso crioscópico Objeto de la experiencia:
CANTIDAD DE SUSTANCIA. EL MOL. Física y Química 3º de E.S.O. IES Isidra de Guzmán
 CANTIDAD DE SUSTANCIA. EL MOL Física y Química 3º de E.S.O. IES Isidra de Guzmán Introducción Es fácil contar los garbanzos que hay en un puñado de esta legumbre. Hay que tener más paciencia para contar
CANTIDAD DE SUSTANCIA. EL MOL Física y Química 3º de E.S.O. IES Isidra de Guzmán Introducción Es fácil contar los garbanzos que hay en un puñado de esta legumbre. Hay que tener más paciencia para contar
Equipos Cantidad Observacion Calibrador 1 Tornillo micrometrico 1 Cinta metrica 1 Esferas 3 Calculadora 1
 No 1 LABORATORIO DE FISICA PARA LAS CIENCIAS DE LA VIDA DEPARTAMENTO DE FISICA Y GEOLOGIA UNIVERSIDAD DE PAMPLONA FACULTAD DE CIENCIAS BÁSICAS Objetivos Realizar mediciones de magnitudes de diversos objetos
No 1 LABORATORIO DE FISICA PARA LAS CIENCIAS DE LA VIDA DEPARTAMENTO DE FISICA Y GEOLOGIA UNIVERSIDAD DE PAMPLONA FACULTAD DE CIENCIAS BÁSICAS Objetivos Realizar mediciones de magnitudes de diversos objetos
PRÁCTICO 3: SOLUCIONES
 Curso de Laboratorio Página: 1/6 DEPARTAMENTO ESTRELLA CAMPOS PRÁCTICO 3: SOLUCIONES Bibliografía: Química, La Ciencia Central, T.L. Brown, H.E.LeMay, Jr., B.Bursten; Ed. Prentice-Hall Hispanoamericana,
Curso de Laboratorio Página: 1/6 DEPARTAMENTO ESTRELLA CAMPOS PRÁCTICO 3: SOLUCIONES Bibliografía: Química, La Ciencia Central, T.L. Brown, H.E.LeMay, Jr., B.Bursten; Ed. Prentice-Hall Hispanoamericana,
PRÁCTICA Nº 3 PROPIEDADES COLIGATIVAS: DETERMINACIÓN DE LA MASA MOLECULAR DE UN SOLUTO PROBLEMA POR CRIOSCOPIA
 PRÁCTICA Nº 3 PROPIEDADES COLIGATIVAS: DETERINACIÓN DE LA ASA OLECULAR DE UN SOLUTO PROBLEA POR CRIOSCOPIA OBJETIVOS: El objetivo de la práctica es el estudio del efecto que produce la adición de un soluto
PRÁCTICA Nº 3 PROPIEDADES COLIGATIVAS: DETERINACIÓN DE LA ASA OLECULAR DE UN SOLUTO PROBLEA POR CRIOSCOPIA OBJETIVOS: El objetivo de la práctica es el estudio del efecto que produce la adición de un soluto
 TALLER: TEMAS IMPORTANTES DE QUIMICA http://cap7-teoriacuantica.blogspot.com/p/s-isoelectronicos.html Refuerzo, ver video: http://www.quimitube.com/videos/comparacion-radio-ionicoiones-isoelectronico/
TALLER: TEMAS IMPORTANTES DE QUIMICA http://cap7-teoriacuantica.blogspot.com/p/s-isoelectronicos.html Refuerzo, ver video: http://www.quimitube.com/videos/comparacion-radio-ionicoiones-isoelectronico/
Las sustancias reaccionan entre sí. REACCIÓN QUÍMICA: proceso en el cual una o varias sustancias cambian para formar sustancias nuevas
 Las sustancias reaccionan entre sí. REACCIÓN QUÍMICA: proceso en el cual una o varias sustancias cambian para formar sustancias nuevas LEY DE LAVOISIER: Los átomos no se crean ni se destruyen durante cualquier
Las sustancias reaccionan entre sí. REACCIÓN QUÍMICA: proceso en el cual una o varias sustancias cambian para formar sustancias nuevas LEY DE LAVOISIER: Los átomos no se crean ni se destruyen durante cualquier
TEMA 2: LEYES Y CONCEPTOS BÁSICOS EN QUÍMICA
 1. SUSTANCIAS PURAS Y MEZCLAS 2. LEYES PONDERALES DE LAS COMBINACIONES QUÍMICAS 2.1. LEY DE CONSERVACIÓN DE LA MATERIA Enunciada en 1783 por Lavoisier: La materia ni se crea ni se destruye, únicamente
1. SUSTANCIAS PURAS Y MEZCLAS 2. LEYES PONDERALES DE LAS COMBINACIONES QUÍMICAS 2.1. LEY DE CONSERVACIÓN DE LA MATERIA Enunciada en 1783 por Lavoisier: La materia ni se crea ni se destruye, únicamente
Profesora: Teresa Esparza Araña LA CANTIDAD DE SUSTANCIA EN QUÍMICA. UNIDAD 6: Los gases ideales
 Departamento de Física y Química Profesora: Teresa Esparza Araña CEAD P. Félix Pérez Parrilla LA CANTIDAD DE SUSTANCIA EN QUÍMICA UNIDAD 6: Los gases ideales 1. LOS GASES SEGÚN LA TEORÍA CINÉTICA DE LA
Departamento de Física y Química Profesora: Teresa Esparza Araña CEAD P. Félix Pérez Parrilla LA CANTIDAD DE SUSTANCIA EN QUÍMICA UNIDAD 6: Los gases ideales 1. LOS GASES SEGÚN LA TEORÍA CINÉTICA DE LA
MEDIDA DE LA DENSIDAD DE UN CUERPO. DETERMINACIÓN DE π
 1 Objetivos Departamento de Física Curso cero MEDIDA DE LA DENSIDAD DE UN CUERPO. DETERMINACIÓN DE π Utilización de un calibre en la determinación de las dimensiones de un objeto y de una balanza digital
1 Objetivos Departamento de Física Curso cero MEDIDA DE LA DENSIDAD DE UN CUERPO. DETERMINACIÓN DE π Utilización de un calibre en la determinación de las dimensiones de un objeto y de una balanza digital
todoesquimica.bligoo.cl
 todoesquimica.bligoo.cl Ley de conservación de la masa (Lavoisier) Ley de proporciones definidas (Proust) Ley de proporciones múltiples (Dalton). Ley de proporciones recíprocas (Ritcher) Ley de volúmenes
todoesquimica.bligoo.cl Ley de conservación de la masa (Lavoisier) Ley de proporciones definidas (Proust) Ley de proporciones múltiples (Dalton). Ley de proporciones recíprocas (Ritcher) Ley de volúmenes
Laboratorio de Física para Ingeniería
 Laboratorio de para Ingeniería 1. Al medir la longitud de un cilindro se obtuvieron las siguientes medidas: x [cm] 8,45 8,10 8,40 8,55 8,45 8,30 Al expresar la medida en la forma x = x + x resulta: (a)
Laboratorio de para Ingeniería 1. Al medir la longitud de un cilindro se obtuvieron las siguientes medidas: x [cm] 8,45 8,10 8,40 8,55 8,45 8,30 Al expresar la medida en la forma x = x + x resulta: (a)
TEMA 2: La Estructura de los sólidos cristalinos
 TEMA 2: La Estructura de los sólidos cristalinos 1. La plata solidifica en una estructura cúbica centrada en las caras (fcc). La masa atómica de la plata es 107.8682 y la longitud de la celda unidad, esto
TEMA 2: La Estructura de los sólidos cristalinos 1. La plata solidifica en una estructura cúbica centrada en las caras (fcc). La masa atómica de la plata es 107.8682 y la longitud de la celda unidad, esto
Capítulo 2 La estructura de los sólidos cristalinos
 Capítulo 2 La estructura de los sólidos cristalinos TEMA 2: La estructura de los sólidos cristalinos 1. Los enlaces interatómicos 2. La estructura cristalina 3. Estructuras de empaquetamiento compacto
Capítulo 2 La estructura de los sólidos cristalinos TEMA 2: La estructura de los sólidos cristalinos 1. Los enlaces interatómicos 2. La estructura cristalina 3. Estructuras de empaquetamiento compacto
MEDICIÓN Y PROPAGACIÓN DE ERRORES. Comprender el proceso de medición y expresar correctamente el resultado de una medida realizada.
 LABORATORIO Nº 1 MEDICIÓN Y PROPAGACIÓN DE ERRORES I. LOGROS Comprender el proceso de medición y expresar correctamente el resultado de una medida realizada. Aprender a calcular el error propagado e incertidumbre
LABORATORIO Nº 1 MEDICIÓN Y PROPAGACIÓN DE ERRORES I. LOGROS Comprender el proceso de medición y expresar correctamente el resultado de una medida realizada. Aprender a calcular el error propagado e incertidumbre
CLASE Nº 2 ESTEQUIOMETRÍA
 UNIVERSIDAD NACIONAL EXPERIMENTAL POLITECNICA ANTONIO JOSÉ DE SUCRE VICERRECTORADO BARQUISIMETO DEPARTAMENTO DE INGENIERÍA QUÍMICA QUÍMICA GENERAL CLASE Nº 2 ESTEQUIOMETRÍA 1 Estequiometría Leyes que rigen
UNIVERSIDAD NACIONAL EXPERIMENTAL POLITECNICA ANTONIO JOSÉ DE SUCRE VICERRECTORADO BARQUISIMETO DEPARTAMENTO DE INGENIERÍA QUÍMICA QUÍMICA GENERAL CLASE Nº 2 ESTEQUIOMETRÍA 1 Estequiometría Leyes que rigen
Primaria Sexto Grado Matemáticas (con QuickTables)
 Primaria Sexto Grado Matemáticas (con QuickTables) Este curso cubre los conceptos mostrados a continuación. El estudiante navega por trayectos de aprendizaje basados en su nivel de preparación. Usuarios
Primaria Sexto Grado Matemáticas (con QuickTables) Este curso cubre los conceptos mostrados a continuación. El estudiante navega por trayectos de aprendizaje basados en su nivel de preparación. Usuarios
Unidad V. 5.1 Recta tangente y recta normal a una curva en un punto. Curvas ortogonales.
 Unidad V Aplicaciones de la derivada 5.1 Recta tangente y recta normal a una curva en un punto. Curvas ortogonales. Una tangente a una curva es una recta que toca la curva en un solo punto y tiene la misma
Unidad V Aplicaciones de la derivada 5.1 Recta tangente y recta normal a una curva en un punto. Curvas ortogonales. Una tangente a una curva es una recta que toca la curva en un solo punto y tiene la misma
ESTRUCTURA DE LOS MATERIALES 2. 25/02/2012 Elaboró Ing. Efrén Giraldo T. 1
 ESTRUCTURA DE LOS MATERIALES 2 25/02/2012 Elaboró Ing. Efrén Giraldo T. 1 FACTOR DE EMPAQUETAMIENTO FEA = (No de átomos por celda. Vol de un átomo) / V (celda) 25/02/2012 Elaboró Ing. Efrén Giraldo T.
ESTRUCTURA DE LOS MATERIALES 2 25/02/2012 Elaboró Ing. Efrén Giraldo T. 1 FACTOR DE EMPAQUETAMIENTO FEA = (No de átomos por celda. Vol de un átomo) / V (celda) 25/02/2012 Elaboró Ing. Efrén Giraldo T.
Difracción e Interferencia: Experimento de Young
 Universidad Nacional Autónoma de Honduras Facultad de Ciencias Escuela de Física Difracción e Interferencia: Experimento de Young Elaborado por: Sofía D. Escobar, Miguel A. Serrano y Jorge A. Pérez Introducción
Universidad Nacional Autónoma de Honduras Facultad de Ciencias Escuela de Física Difracción e Interferencia: Experimento de Young Elaborado por: Sofía D. Escobar, Miguel A. Serrano y Jorge A. Pérez Introducción
Master en Análisis Forense
 Master en Análisis Forense Evidencias físicas Métodos Cristalográficos de Caracterización en AF Tema 3.- Difracción de Rayos X Dr. José Luis Pizarro Dpto. Mineralogía y Petrología Fac. Ciencia y Tecnología
Master en Análisis Forense Evidencias físicas Métodos Cristalográficos de Caracterización en AF Tema 3.- Difracción de Rayos X Dr. José Luis Pizarro Dpto. Mineralogía y Petrología Fac. Ciencia y Tecnología
FLORIDA Secundaria. 1º BACH MATEMÁTICAS CCSS -1- BLOQUE ESTADÍSTICA: ESTADÍSTICA VARIABLE UNIDIMENSIONAL. Estadística variable unidimensional
 FLORIDA Secundaria. 1º BACH MATEMÁTICAS CCSS -1- Estadística variable unidimensional 1. Conceptos de Estadística 2. Distribución de frecuencias 2.1. Tablas de valores con variables continuas 3. Parámetros
FLORIDA Secundaria. 1º BACH MATEMÁTICAS CCSS -1- Estadística variable unidimensional 1. Conceptos de Estadística 2. Distribución de frecuencias 2.1. Tablas de valores con variables continuas 3. Parámetros
FIZ Física Contemporánea
 FIZ1111 - Física Contemporánea Interrogación N o 3 17 de Junio de 2008, 18 a 20 hs Nombre completo: hrulefill Sección: centering Buenas Malas Blancas Nota Table 1. Instrucciones - Marque con X el casillero
FIZ1111 - Física Contemporánea Interrogación N o 3 17 de Junio de 2008, 18 a 20 hs Nombre completo: hrulefill Sección: centering Buenas Malas Blancas Nota Table 1. Instrucciones - Marque con X el casillero
1.- La materia y clasificación. La materia es cualquier cosa que ocupa un espacio y tiene masas Estados: sólido, líquido, gaseoso
 La Química La Química se encarga del estudio de las propiedades de la materia y de los cambios que en ella se producen. La Química es una ciencia cuantitativa y requiere el uso de mediciones. Las cantidades
La Química La Química se encarga del estudio de las propiedades de la materia y de los cambios que en ella se producen. La Química es una ciencia cuantitativa y requiere el uso de mediciones. Las cantidades
2- Describa y deduzca las expresiones matemáticas correspondientes al experimento de la doble rendija de Young.
 ASIGNATURA FISICA II AÑO 2012 GUIA NRO. 14 INTERFERENCIA, DIFRACCION Y POLARIZACION Bibliografía Obligatoria (mínima) Capítulos 37 y 38 Física de Serway Tomo II PREGUNTAS SOBRE LA TEORIA Las preguntas
ASIGNATURA FISICA II AÑO 2012 GUIA NRO. 14 INTERFERENCIA, DIFRACCION Y POLARIZACION Bibliografía Obligatoria (mínima) Capítulos 37 y 38 Física de Serway Tomo II PREGUNTAS SOBRE LA TEORIA Las preguntas
Ecuación de estado del gas ideal
 Prácticas de laboratorio de Física I Ecuación de estado del gas ideal Curso 2010/11 1 Objetivos Comprobación de la ecuación de estado del gas ideal experimentalmente Construcción de curvas a presión, temperatura
Prácticas de laboratorio de Física I Ecuación de estado del gas ideal Curso 2010/11 1 Objetivos Comprobación de la ecuación de estado del gas ideal experimentalmente Construcción de curvas a presión, temperatura
ESPECTROS ATÓMICOS. a) Obtener las curvas características para los espectros de emisión del sodio, helio, hidrógeno y mercurio.
 ESPECTROS ATÓMICOS OBJETIVOS a) Obtener las curvas características para los espectros de emisión del sodio, helio, hidrógeno y mercurio. b) Mediante las curvas características obtenidas, determinar las
ESPECTROS ATÓMICOS OBJETIVOS a) Obtener las curvas características para los espectros de emisión del sodio, helio, hidrógeno y mercurio. b) Mediante las curvas características obtenidas, determinar las
UNIDAD 1: LA MATERIA CRISTALINA
 UNIDAD 1: LA MATERIA CRISTALINA CONCEPTOS MATERIA CRISTALINA: Aquella cuyas partículas están perfectamente ordenadas en el espacio, ocupando posiciones fijas y a distancias regulares unas de otras, formando
UNIDAD 1: LA MATERIA CRISTALINA CONCEPTOS MATERIA CRISTALINA: Aquella cuyas partículas están perfectamente ordenadas en el espacio, ocupando posiciones fijas y a distancias regulares unas de otras, formando
Estequiometría. Química General I 2013
 Estequiometría Química General I 2013 Estequiometría Es el estudio cuantitativo de reactivos y productos en una reacción química. Conceptos importantes Masa atómica Mol Peso molecular Masa atómica En química
Estequiometría Química General I 2013 Estequiometría Es el estudio cuantitativo de reactivos y productos en una reacción química. Conceptos importantes Masa atómica Mol Peso molecular Masa atómica En química
SÓLIDOS INORGÁNICOS. Tema 6. FUNDAMENTOS
 SÓLIDOS INORGÁNICOS Tema 6. Fundamentos Tema 7. Sólidos metálicos Tema 8. Sólidos iónicos Tema 9. Sólidos covalentes Tema 10. Sólidos moleculares Tema 11. Defectos y no-estequiometría Tema 12. Propiedades
SÓLIDOS INORGÁNICOS Tema 6. Fundamentos Tema 7. Sólidos metálicos Tema 8. Sólidos iónicos Tema 9. Sólidos covalentes Tema 10. Sólidos moleculares Tema 11. Defectos y no-estequiometría Tema 12. Propiedades
Balance Global de Energía
 Balance Global de Energía Balance de energía 1a Ley de la Termodinámica El balance básico global se establece entre la energía proveniente del sol y la energía regresada al espacio por emisión de la radiación
Balance Global de Energía Balance de energía 1a Ley de la Termodinámica El balance básico global se establece entre la energía proveniente del sol y la energía regresada al espacio por emisión de la radiación
Departamento de Física Aplicada I. Escuela Politécnica Superior. Universidad de Sevilla. Física II
 Física II Osciloscopio y Generador de señales Objetivos: Familiarizar al estudiante con el manejo del osciloscopio y del generador de señales. Medir las características de una señal eléctrica alterna (periodo
Física II Osciloscopio y Generador de señales Objetivos: Familiarizar al estudiante con el manejo del osciloscopio y del generador de señales. Medir las características de una señal eléctrica alterna (periodo
Campo Magnético en un alambre recto.
 Campo Magnético en un alambre recto. A.M. Velasco (133384) J.P. Soler (133380) O.A. Botina (133268) Departamento de física, facultad de ciencias, Universidad Nacional de Colombia Resumen. Se hizo pasar
Campo Magnético en un alambre recto. A.M. Velasco (133384) J.P. Soler (133380) O.A. Botina (133268) Departamento de física, facultad de ciencias, Universidad Nacional de Colombia Resumen. Se hizo pasar
Ley de enfriamiento de Newton considerando reservorios finitos
 Ley de enfriamiento de Newton considerando reservorios finitos María ecilia Molas, Florencia Rodriguez Riou y Débora Leibovich Facultad de Ingeniería, iencias Exactas y Naturales Universidad Favaloro,.
Ley de enfriamiento de Newton considerando reservorios finitos María ecilia Molas, Florencia Rodriguez Riou y Débora Leibovich Facultad de Ingeniería, iencias Exactas y Naturales Universidad Favaloro,.
Determinación de constantes de ionización
 Capítulo 5. Determinación de constantes de ionización Se determinaron las constantes de ionización de diversos compuestos mediante curvas de titulación ácido-base empleando métodos espectrofotométricos
Capítulo 5. Determinación de constantes de ionización Se determinaron las constantes de ionización de diversos compuestos mediante curvas de titulación ácido-base empleando métodos espectrofotométricos
Apuntes Disoluciones
 Una disolución es una mezcla homogénea (los componentes no se pueden distinguir a simple vista) de dos a más sustancias. En las disoluciones hay que distinguir el soluto, el disolvente y la propia disolución
Una disolución es una mezcla homogénea (los componentes no se pueden distinguir a simple vista) de dos a más sustancias. En las disoluciones hay que distinguir el soluto, el disolvente y la propia disolución
UNIVERSIDAD CATOLICA ANDRES BELLO FACULTAD DE INGENIERIA DEPARTAMENTO DE FÍSICA LABORATORIO DE FÍSICA II TELECOMUNICACIONES OPTICA FISICA
 UNIVERSIDAD CATOICA ANDRES BEO FACUTAD DE INGENIERIA DEPARTAMENTO DE FÍSICA ABORATORIO DE FÍSICA II TEECOMUNICACIONES OPTICA FISICA Una onda es una perturbación física de algún tipo que se propaga en el
UNIVERSIDAD CATOICA ANDRES BEO FACUTAD DE INGENIERIA DEPARTAMENTO DE FÍSICA ABORATORIO DE FÍSICA II TEECOMUNICACIONES OPTICA FISICA Una onda es una perturbación física de algún tipo que se propaga en el
Reflexión de la luz MATERIALES MONTAJE
 Reflexión de la luz Espejos planos Estamos acostumbrados a usar los espejos sin plantearnos que ocurre con los rayos de luz que inciden sobre ellos. Vamos a estudiar el comportamiento de la luz primero
Reflexión de la luz Espejos planos Estamos acostumbrados a usar los espejos sin plantearnos que ocurre con los rayos de luz que inciden sobre ellos. Vamos a estudiar el comportamiento de la luz primero
GEOMETRÍA DE LOS CRISTALES I
 CAPÍTULO 4 GEOMETRÍA DE LOS CRISTALES I 4.1 REDES Conjuntos de puntos imaginarios que tienen una relación fija en el espacio constituyendo un armazón sobre el cual el cristal se construye. En la Figura
CAPÍTULO 4 GEOMETRÍA DE LOS CRISTALES I 4.1 REDES Conjuntos de puntos imaginarios que tienen una relación fija en el espacio constituyendo un armazón sobre el cual el cristal se construye. En la Figura
Síntesis y Caracterización Estructural de los Materiales Ángel Carmelo Prieto Colorado
 Síntesis y Caracterización Estructural de los Materiales Ángel Carmelo Prieto Colorado Física de la Materia Condensada, Cristalografía y Mineralogía. Facultad de Ciencias. Universidad de Valladolid. Estructura
Síntesis y Caracterización Estructural de los Materiales Ángel Carmelo Prieto Colorado Física de la Materia Condensada, Cristalografía y Mineralogía. Facultad de Ciencias. Universidad de Valladolid. Estructura
Magnitud: cualidad que se puede medir. Ej. Longitud y temperatura de una varilla
 Curso nivelación I Presentación Magnitudes y Medidas El método científico que se aplica en la Física requiere la observación de un fenómeno natural y después la experimentación es decir, reproducir ese
Curso nivelación I Presentación Magnitudes y Medidas El método científico que se aplica en la Física requiere la observación de un fenómeno natural y después la experimentación es decir, reproducir ese
4.1. Polinomios y teoría de ecuaciones
 CAPÍTULO 4 Polinomios y teoría de ecuaciones 4.1. Polinomios y teoría de ecuaciones Un polinomio real en x, o simplemente polinomio en x es una expresión algebraica de la forma a n x n + a n 1 x n 1 +
CAPÍTULO 4 Polinomios y teoría de ecuaciones 4.1. Polinomios y teoría de ecuaciones Un polinomio real en x, o simplemente polinomio en x es una expresión algebraica de la forma a n x n + a n 1 x n 1 +
CENTRO DE GRAVEDAD Y CENTROIDE. Considerando el sistema de n partículas fijo dentro de una región del espacio,
 CENTRO DE GRAVEDAD Y CENTROIDE Centro de gravedad y centro de masa para un sistema de partículas Centro de gravedad Considerando el sistema de n partículas fijo dentro de una región del espacio, Los pesos
CENTRO DE GRAVEDAD Y CENTROIDE Centro de gravedad y centro de masa para un sistema de partículas Centro de gravedad Considerando el sistema de n partículas fijo dentro de una región del espacio, Los pesos
GUÍAS DE LOS LABORATORIO DE FÍSICA I Y LABORATORIO DE FÍSICA GENERAL
 UNIVERSIDAD NACIONAL EXPERIMENTAL FRANCISCO DE MIRANDA COMPLEJO ACADÉMICO EL SABINO AREA DE TECNOLOGIA DEPARTAMENTO DE FÍSICA Y MATEMATICA COORDINACION DE LABORATORIOS DE FÍSICA GUÍAS DE LOS LABORATORIO
UNIVERSIDAD NACIONAL EXPERIMENTAL FRANCISCO DE MIRANDA COMPLEJO ACADÉMICO EL SABINO AREA DE TECNOLOGIA DEPARTAMENTO DE FÍSICA Y MATEMATICA COORDINACION DE LABORATORIOS DE FÍSICA GUÍAS DE LOS LABORATORIO
GUÍA DE DISCUSIÓN DE PROBLEMAS 4 TEMA DIFUSIÓN EN MATERIALES DE INGENIERÍA
 UNIVERSIDAD DON BOSCO FACULTAD DE INGENIERÍA ESCUELA DE INGENIERÍA MECÁNICA Asignatura: "Ciencia de los Materiales" I- SECCION DE PREGUNTAS: GUÍA DE DISCUSIÓN DE PROBLEMAS 4 TEMA DIFUSIÓN EN MATERIALES
UNIVERSIDAD DON BOSCO FACULTAD DE INGENIERÍA ESCUELA DE INGENIERÍA MECÁNICA Asignatura: "Ciencia de los Materiales" I- SECCION DE PREGUNTAS: GUÍA DE DISCUSIÓN DE PROBLEMAS 4 TEMA DIFUSIÓN EN MATERIALES
RELACIÓN CARGA - MASA DEL ELECTRÓN
 Práctica 5 RELACIÓN CARGA - MASA DEL ELECTRÓN OBJETIVO Determinar la relación carga-masa del electrón (e/m e ), a partir de las trayectorias observadas de un haz de electrones que cruza una región en la
Práctica 5 RELACIÓN CARGA - MASA DEL ELECTRÓN OBJETIVO Determinar la relación carga-masa del electrón (e/m e ), a partir de las trayectorias observadas de un haz de electrones que cruza una región en la
II Unidad Diagramas en bloque de transmisores /receptores
 1 Diagramas en bloque de transmisores /receptores 10-04-2015 2 Amplitud modulada AM Frecuencia modulada FM Diagramas en bloque de transmisores /receptores Amplitud modulada AM En la modulación de amplitud
1 Diagramas en bloque de transmisores /receptores 10-04-2015 2 Amplitud modulada AM Frecuencia modulada FM Diagramas en bloque de transmisores /receptores Amplitud modulada AM En la modulación de amplitud
AÑO: HORAS CÁTEDRA SEMANALES:...3 horas... CURSO: cuarto año bachiller Decreto 6680/56
 Escuela del caminante Instituto Privado Incorporado a la Enseñanza Oficial AÑO: 2014 ASIGNATURA:... QUIMICA HORAS CÁTEDRA SEMANALES:...3 horas... CURSO: cuarto año bachiller Decreto 6680/56 PROFESOR/A:...Guillermo
Escuela del caminante Instituto Privado Incorporado a la Enseñanza Oficial AÑO: 2014 ASIGNATURA:... QUIMICA HORAS CÁTEDRA SEMANALES:...3 horas... CURSO: cuarto año bachiller Decreto 6680/56 PROFESOR/A:...Guillermo
CLASIFICACIÓN DE LA MATERIA
 1. Clasificación de la materia por su aspecto CLASIFICACIÓN DE LA MATERIA La materia homogénea es la que presenta un aspecto uniforme, en la cual no se pueden distinguir a simple vista sus componentes.
1. Clasificación de la materia por su aspecto CLASIFICACIÓN DE LA MATERIA La materia homogénea es la que presenta un aspecto uniforme, en la cual no se pueden distinguir a simple vista sus componentes.
Derivadas Parciales (parte 2)
 40 Derivadas Parciales (parte 2) Ejercicio: Si donde y. Determinar Solución: Consideraremos ahora la situación en la que, pero cada una de las variables e es función de dos variables y. En este caso tiene
40 Derivadas Parciales (parte 2) Ejercicio: Si donde y. Determinar Solución: Consideraremos ahora la situación en la que, pero cada una de las variables e es función de dos variables y. En este caso tiene
Los pesos de las partículas pueden reemplazarse por una única (equivalente) resultante con un punto de aplicación G bien definido.
 UNIDAD 2 EQUILIBRIO DE CUERPOS RÍGIDOS. CENTROS DE GRAVEDAD GENERALIDADES.- El centro de gravedad es aquel que localiza el peso resultante de un sistema de partículas y el centro de masas de un sistema
UNIDAD 2 EQUILIBRIO DE CUERPOS RÍGIDOS. CENTROS DE GRAVEDAD GENERALIDADES.- El centro de gravedad es aquel que localiza el peso resultante de un sistema de partículas y el centro de masas de un sistema
Introducción. Flujo Eléctrico.
 Introducción La descripción cualitativa del campo eléctrico mediante las líneas de fuerza, está relacionada con una ecuación matemática llamada Ley de Gauss, que relaciona el campo eléctrico sobre una
Introducción La descripción cualitativa del campo eléctrico mediante las líneas de fuerza, está relacionada con una ecuación matemática llamada Ley de Gauss, que relaciona el campo eléctrico sobre una
CAPITULO 6. Análisis Dimensional y Semejanza Dinámica
 CAPITULO 6. Análisis Dimensional y Semejanza Dinámica Debido a que son pocos los flujos reales que pueden ser resueltos con exactitud sólo mediante métodos analíticos, el desarrollo de la mecánica de fluidos
CAPITULO 6. Análisis Dimensional y Semejanza Dinámica Debido a que son pocos los flujos reales que pueden ser resueltos con exactitud sólo mediante métodos analíticos, el desarrollo de la mecánica de fluidos
FORMAS MÁS COMUNES DE EXPRESAR LA CONCENTRACIÓN:
 CÁTEDRA: QUÍMICA GUÍA DE PROBLEMAS Nº 4 TEMA: ESTEQUIOMETRÍA DE SOLUCIONES OBJETIVOS: Resolver problemas basados en la estequiometría de las soluciones, ampliando los conocimientos para ser aplicados criteriosamente
CÁTEDRA: QUÍMICA GUÍA DE PROBLEMAS Nº 4 TEMA: ESTEQUIOMETRÍA DE SOLUCIONES OBJETIVOS: Resolver problemas basados en la estequiometría de las soluciones, ampliando los conocimientos para ser aplicados criteriosamente
Relación entre mol y constante de Avogadro
 Relación entre mol y constante de Avogadro Los químicos trabajan con aspectos cuantitativos que pueden ser vistos y tocados, es decir, cantidades macroscópicas, tales como masa en gramos y volumen en litros,
Relación entre mol y constante de Avogadro Los químicos trabajan con aspectos cuantitativos que pueden ser vistos y tocados, es decir, cantidades macroscópicas, tales como masa en gramos y volumen en litros,
I. Objetivos. II. Introducción.
 Universidad de Sonora División de Ciencias Exactas y Naturales Departamento de Física Laboratorio de Mecánica II Práctica #: Dinámica rotacional: Cálculo del Momento de Inercia I. Objetivos. Medir el momento
Universidad de Sonora División de Ciencias Exactas y Naturales Departamento de Física Laboratorio de Mecánica II Práctica #: Dinámica rotacional: Cálculo del Momento de Inercia I. Objetivos. Medir el momento
4. Identificar un isótopo radiactivo del carbono e indicar su uso. 5. Cuál es la configuración electrónica del vanadio?
 ESTRUCTURA ATÓMICA 1. Qué afirmación sobre el número de electrones, protones y neutrones del átomo es correcta? A El número de neutrones menos el número de electrones es cero. B. El número de protones
ESTRUCTURA ATÓMICA 1. Qué afirmación sobre el número de electrones, protones y neutrones del átomo es correcta? A El número de neutrones menos el número de electrones es cero. B. El número de protones
Concepto de mol. Concepto de mol. Número de Avogadro
 Concepto de mol Concepto de mol. Número de Avogadro La masa de los átomos es muy pequeña. Si se toma como ejemplo el átomo de calcio, cuyo radio es de 2.10-8 cm, para completar una distancia de un centímetro
Concepto de mol Concepto de mol. Número de Avogadro La masa de los átomos es muy pequeña. Si se toma como ejemplo el átomo de calcio, cuyo radio es de 2.10-8 cm, para completar una distancia de un centímetro
MÉTODOS DE DIFRACCIÓN DE RAYOS X
 MÉTODOS DE DIFRACCIÓN DE RAYOS X Métodos de Difracción de rayos X. Cuando el haz de rayos X incide sobre un cristal, es decir, sobre una agrupación de átomos periódicamente ordenados en el espacio, entre
MÉTODOS DE DIFRACCIÓN DE RAYOS X Métodos de Difracción de rayos X. Cuando el haz de rayos X incide sobre un cristal, es decir, sobre una agrupación de átomos periódicamente ordenados en el espacio, entre
Estructura Interna de los Materiales
 TEMA III Estructura Interna de los Materiales LECCIÓN 3 Estructura Cristalina y Amorfa 1 3.1 ESTADOS DE LA MATERIA Ciencia y Tecnología de los Materiales La materia puede presentarse en tres estados: gaseoso,
TEMA III Estructura Interna de los Materiales LECCIÓN 3 Estructura Cristalina y Amorfa 1 3.1 ESTADOS DE LA MATERIA Ciencia y Tecnología de los Materiales La materia puede presentarse en tres estados: gaseoso,
