MINERALES, compuestos, elementos, átomos e isótopos
|
|
|
- Ricardo Revuelta Márquez
- hace 6 años
- Vistas:
Transcripción
1 MINERALES, compuestos, elementos, átomos e isótopos
2 Los minerales son los constituyentes de las rocas. Los términos mineral, compuesto, elemento, átomo e isótopo, se refieren a diferentes niveles de organización de la materia. El siguiente nivel de organización superior a mineral, desde el punto de vista de Ciencias de la Tierra (Geología), es el de ROCAS 2
3 Mineral Compuesto o elemento de ocurrencia natural Inorgánico, Sólido, Con una composición química específica, Que posee una estructura interna ordenada de átomos como consecuencia de esta estructura interna presenta una forma cristalina característica (sólido) y, propiedades físicas características. 3
4 Ejemplos de qué es y qué no es mineral Diamante vs. diamante sintético Diamante vs. Carbón Hielo vs. Agua El petróleo es mineral?, la resina es mineral? Mineraloide.- Compuesto sólido natural sin composición química específica y sin estructura cristalina (amorfo). Ejemplo: vidrio, resina, opalo 4
5 Polimorfo. Compuesto que bajo diferentes condiciones organiza su estructura cristalina de diferente manera. Ejemplos Calcita vs. Aragonita, diferentes minerales de misma composición: CaCO 3 Diamante vs. Grafito, diferentes minerales de misma composición: C (Carbono) Pirita vs. Marcasita, diferentes minerales de misma composición: FeS 2 Cuarzo vs Cristobalita vs. Tridimita, diferentes minerales de misma composición: SiO 2 5
6 ÁTOMO La más pequeña división de la materia que retiene las características químicas de un elemento. Se representa como un sistema solar en miniatura con un núcleo de protones y neutrones y hasta 7 capas de electrones orbitando alrededor del núcleo a) Protones.- partículas cargadas positivamente con masa de 1 AMU b) Neutrones.- partículas eléctricamente neutras con masa de 1 AMU c) Electrones.- partículas de tamaño infinitesimal con carga eléctrica negativa. 6
7 Número Atómico = Número de Protones (= # electrones) Este número da la identidad de cada ELEMENTO De No. Atómico 0 al 92 corresponden a elementos que ocurren naturalmente (el 61 es excepción; los 43, 85 y 87 son muy inestables, solo están en espectro estelar) Del 92 en adelante NO ocurren naturalmente, cuando se logra producirlos, son inestables 7
8 8
9 Masa Atómica = de Protones + Neutrones del núcleo. Un mismo elemento puede tener diferente masa atómica, en virtud a que el número de neutrones puede variar. Cada una de estas variaciones es un ISÓTOPO Ejemplo: la mayoría del H es de ma = 1 (1 protón); el deuterio es ma = 2 (1 protón, 1 neutrón) y el tritio es ma = 3 (1 protón, 2 neutrones) Entre más protones en el núcleo, hay más electrones y más capas orbitales. En cada capa hay hasta un # determinado de electrones; en la última el máximo es 8 electrones Elementos con 8 electrones en última capa son: gases inertes y son los más estables. El resto de los elementos tiene < de 8 electrones en última capa, por lo que son químicamente reactivos. 9
10 10
11 Compuestos Los Átomos de los elementos reaccionan unos con otros y forman compuestos. Con estas reacciones se llenan las últimas capas de los átomos, con lo cual quedan químicamente estables. En este proceso los átomos: a) ganan electrones: Aniones.- ion cargado negativamente (# electrones > # proton) b) pierden electrones: Cationes.- ion cargado positivamente (# electrones < # protones) Átomos con 1,2 ó 3 electrones en última órbita tienden a perderlos Átomos con 4 ó más electrones en última órbita tienden a ganarlos Ejemplos: el Na con # atóm = 11 con 11 electrones: 2, 8 y 1, es catión con Na 1+ El Cl con # atóm = 17 con 17 electrones: 2, 8, 7, es anión con Cl 1-11
12 12
13 Tipo De Uniones Atómicas La forma como se unen los átomos de los compuestos, condiciona en gran medida el arreglo interno ordenado de átomos que ocurre en los minerales Iónica. Electrón externo de un átomo se da a otro para completar sus 8 electrones de la última capa Ejemplo: el NaCl, LiF Característica importante: solubles en agua 13
14 Covalente. Unión más fuerte: electrones de ambos átomos son compartidos. La verdadera unión covalente solo se da con átomos del mismo elemento Ejemplo: Diamante Característica: casi NO son solubles en agua 14
15 Otros tipos de uniones atómicas Metálica. Similares a uniones covalentes apretadas, porque la unión ocurre en capas más internas de energía y los electrones externos van de un lado a otro con facilidad Presentan propiedades como conductividad eléctrica, térmica Van der Waals. Atracción electrostática débil entre subunidades que tienen una cierta unión iónica o covalente Ejemplo: grafito, talco Iones Complejos. Iones combinados que actúan como si fueran un solo ion, formando pares fuertemente unidos. Ejemplo: CO 3 2- SO 4 2- NO 3 1- SiO
16 Estructura cristalina de los minerales Los Átomos individuales ordenados de los minerales se encuentran juntos en una red: Látice Cristalino. En esta red cada átomo o ión, se localiza en el mismo lugar específico Si ocupan lugares al azar estructura amorfa Esta organización interna solo puede darse en un Sólido Estados de la Materia. Sólido, (baja ºT ó alta ºT y baja P) Líquido y Gaseoso (alta ºT ó baja ºT y alta P) 16
17 Sistemas Cristalinos Existen 6 (7) Sistemas Cristalinos: Isométrico, tetragonal, hexagonal, trigonal, ortorrómbico, monoclínico, triclínico. Los cuáles se subdividen en 32 clases en total. Están caracterizados por su forma exterior (ángulos entre caras) pero principalmente por: sus elementos de simetría: Eje de simetría: su longitud relativa y ángulos entre estos ejes; Planos de simetría y Centro de simetría. Sistema Cristalino Ejes Ángulos entre ejes Isométrico (Cúbico ó Regular) a = b = c α = β = γ = 90º; Tetragonal a = b c α = β = γ = 90º Hexagonal a = b c α = β = 90º; γ = 120º 17
18 Hexagonal a = b c α = β = 90º; γ = 120º Trigonal (o Romboédrico) a = b = c α = β = γ 90º Ortorrómbico a b c a α = β = γ = 90º Monoclínico a b c a α = γ = 90º; β 90º Triclínico a b c a α β γ (Todos distintos de 90º) 18
19 PROPIEDADES FÍSICAS DE LOS MINERALES Color.- Propiedad más conspicua pero menos confiable. Depende del grado de absorción de la luz. Las pequeñas impurezas pueden cambiar el color. Raya.- Color del polvo al rayarse. En algunos casos es diagnóstico como la hematita Lustre.- Apariencia de la superficie bajo luz reflejada: Metálico, No Metálico (perlado, sedoso, vítreo, terroso, adamantino) Dureza.- Resistencia a ser rayado. Se usa escala de Mohs del 1 al 10; 1 = yeso (el más suave), 10 = diamante (el más duro) Clivaje.- Muy diagnóstica. Tendencia a romperse a lo largo de ciertos planos (débiles) Fractura.- En minerales sin clivaje. Planos en los que se rompe cuando se golpean (ej. concoidal) Peso Específico.- masa del sólido ó mineral / masa de agua de igual volumen que el sólido o mineral. Aumenta con el incremento del número atómico. (la mayoría está entre 2.5 y 3) Reacción al ácido.- burbujeo al HCl Ej.: CaCO 3 +2HCl CO 2 +H2O+Ca 2 +2Cl2 Forma.- ángulos entre caras, reflejo de estructura cristalina. Sabor.- Con precaución, útil para halita (NaCl), y silvita (KCl) 19
20 Color.- Propiedad conspicua pero poco indicativa. Ve los diferentes colores que puede tener el Cuarzo debido a sus impurezas Raya.- Aunque el color de un mineral varía, el color de la raya es una propiedad más característica 20
21 Dureza 21
22 Lustre 22
23 Clivaje y Fractura Clivaje: Tendencia a romperse a lo largo de ciertos planos (débiles) 23
24 Peso específico la mayoría de los minerales está entre 2.5 y 3 24
25 Reacción al ácido Sabor 25
26 CLASIFICACION DE MINERALES. Dada la composición de los elementos de la corteza terrestre, los minerales pueden clasificarse de forma muy general en dos: 1. Silicatos. 2. No Silicatos. Los primeros (constituidos por el anión SiO 2 ) están subdivididos con base en el contenido de su principal catión: Fe y los segundos de acuerdo con sus aniones constitutivos. 26
27 (a) Silicatos. Constituidos por tetraedros de sílice (SiO 2 ), estructura básica, dispuestos en diversos arreglos i) Ferromagnesianos arreglos de tetraedros aislados (grupo del olivino), arreglos de cadenas sencillas (grupo de piroxenos), cadenas dobles (grupo de anfíboles), arreglos en capas (micas oscuras: biotita) ii) No Ferromagnesianos en capas (micas claras: muscovita) en redes tridimensionales (grupo de los feldespatos y el cuarzo) (b) No Silicatos Constituidos por varios grupos de acuerdo con sus aniones Elementos nativos (Au, Ag, Cu) Óxidos (O 2- ) e Hidróxidos (OH - ) ej. hematita (Fe 2 O 3 ) y brucita (Mg [OH] 2 ) Haluros cloruros (Cl - ), fluoruros (F - ), bromuros (Br - ), yoduros (I - ), ej. halita (NaCl) Carbonatos (CO 2-3 ) ej calcita CaCO 3 Sulfatos (SO 2-4 ) ej. yeso (CaSO 4 2H 2 O), Sulfuros y sulfosales (S) ej pirita (FeS 2 ), Fosfatos (PO 4 ), Arsenatos, Vanadatos y Boratos ej apatito (Ca 5 (PO 4 ) 3 (OH,F,Cl), Orgánicos (no son verdaderos minerales) ej. ámbar 27
28 Estructura básica de los silicatos: tetraedro de silicio-oxígeno oxígeno Funciona como un ion: SiO4 con carga de 4- Y forma compuestos químicos neutros con la adición de iones cargados positivamente: cationes 28
29 29
30 FORMACIÓN DE MINERALES Todos los minerales que observamos en las rocas tienen determinada temperatura de formación (la transición de fase líquida a sólida), que va desde la temperatura ambiente (como los minerales formados en las rocas sedimentarias) hasta altas temperaturas (como las de una lava o magma al enfriarse). De tal manera que la presencia de cada mineral es indicativo de las condiciones de formación de la roca. En las rocas ígneas este orden de formación de minerales de acuerdo a su temperatura se conoce como Serie de Bowen. En las rocas metamórficas los minerales se usan como índice para conocer la temperatura y presión a la que se formaron tales rocas 30
31 31
32 32
33 IDENTIFICACION DE MINERALES + Observación de propiedades físicas en muestras de mano. + Microscopio Petrográfico.- Láminas delgadas vistas con luz transmitida y reflejada, se observan propiedades ópticas de los minerales características para su identificación (estas propiedades son consecuencia de su estructura interna): Reflexión y refracción, Dispersión, Birrefringencia, Isotropía y Anisotropía, Pleocroismo + Mediante la difracción de Rayos X + Microscopio electrónico y de barrido.- Se observa la forma y estructura de los minerales. Identificación de Elementos: + Espectrómetros, + Fluorescencia de rayos X 33
Suelos formados por viento (Loess)
 Suelos formados por viento (Loess) Procesos generales de formación de los suelos (continuación). Los elementos más facilmente lixiviables son las sales (carbonatos, cloruros, sulfatos, nitratos, bicarbonatos).
Suelos formados por viento (Loess) Procesos generales de formación de los suelos (continuación). Los elementos más facilmente lixiviables son las sales (carbonatos, cloruros, sulfatos, nitratos, bicarbonatos).
Capítulo 2: Los Minerales. Geología Física
 Capítulo 2: Los Minerales Geología Física La materia y su composición TODO lo que tenga masa y ocupe espacio es materia La materia se presenta en uno de tres estados o fases, todos ellos importantes para
Capítulo 2: Los Minerales Geología Física La materia y su composición TODO lo que tenga masa y ocupe espacio es materia La materia se presenta en uno de tres estados o fases, todos ellos importantes para
MINERALOGÍA Profesora: Priscilla Guzmán C.
 MINERALOGÍA Profesora: Priscilla Guzmán C. Habilidades Conocimiento. Comprensión. Aplicación. Contenidos Definición de mineral. Propiedades físicas y químicas de los minerales. Definición de roca y clasificación.
MINERALOGÍA Profesora: Priscilla Guzmán C. Habilidades Conocimiento. Comprensión. Aplicación. Contenidos Definición de mineral. Propiedades físicas y químicas de los minerales. Definición de roca y clasificación.
UNIDAD 1: LA MATERIA CRISTALINA
 UNIDAD 1: LA MATERIA CRISTALINA CONCEPTOS MATERIA CRISTALINA: Aquella cuyas partículas están perfectamente ordenadas en el espacio, ocupando posiciones fijas y a distancias regulares unas de otras, formando
UNIDAD 1: LA MATERIA CRISTALINA CONCEPTOS MATERIA CRISTALINA: Aquella cuyas partículas están perfectamente ordenadas en el espacio, ocupando posiciones fijas y a distancias regulares unas de otras, formando
NOCIONES ELEMENTALES DE MINERALES
 NOCIONES ELEMENTALES DE MINERALES ROCA Agregado de uno o más minerales Minerales: juntos, mezclados, pero reteniendo sus propiedades individuales formadas por más de un mineral, algunos minerales por sí
NOCIONES ELEMENTALES DE MINERALES ROCA Agregado de uno o más minerales Minerales: juntos, mezclados, pero reteniendo sus propiedades individuales formadas por más de un mineral, algunos minerales por sí
FÍSICA Y QUÍMICA Solucionario ELECTRONES Y ENLACES
 FÍSICA Y QUÍMICA Solucionario ELECTRONES Y ENLACES 1.* Indicad cuántos electrones tienen en la última capa cada uno de estos elementos. a) C 4 f) O 6 k) K 1 b) F 7 g) P 5 l) S 6 c) Ne 8 h) H 1 m) He 8
FÍSICA Y QUÍMICA Solucionario ELECTRONES Y ENLACES 1.* Indicad cuántos electrones tienen en la última capa cada uno de estos elementos. a) C 4 f) O 6 k) K 1 b) F 7 g) P 5 l) S 6 c) Ne 8 h) H 1 m) He 8
FÍSICA Y QUÍMICA - 3º ESO ESTRUCTURA ATOMICA Y ENLACE 2
 FÍSICA Y QUÍMICA - 3º ESO ESTRUCTURA ATOMICA Y ENLACE 2 1. Define y explica los siguientes conceptos: número atómico, número másico e isótopos de un elemento químico. 2. Copia el siguiente párrafo y complétalo:
FÍSICA Y QUÍMICA - 3º ESO ESTRUCTURA ATOMICA Y ENLACE 2 1. Define y explica los siguientes conceptos: número atómico, número másico e isótopos de un elemento químico. 2. Copia el siguiente párrafo y complétalo:
Estructura de sólidos
 Estructura de sólidos Química Inorgánica - 2006 Tipos de estructuras cristalinas cristal enlace características molecular covalente-baja energía cristales blandos, bajo p.f. red covalente covalente cristales
Estructura de sólidos Química Inorgánica - 2006 Tipos de estructuras cristalinas cristal enlace características molecular covalente-baja energía cristales blandos, bajo p.f. red covalente covalente cristales
ENLACE QUÍMICO 2º BACH EJERCICIOS DE ENLACE QUÍMICO DEL LIBRO 28. H-CHO H C = O : CH 3 OH H C O H H H H C O C H H H CH 3 OCH 3
 EJERCICIOS DE ENLACE QUÍMICO DEL LIBRO 28. -CO C = O : C 3 O C O C 3 OC 3 C O C a) La longitud de enlace CO es menor en el formaldehido, ya que tiene un doble enlace. b) El metanol puede formar enlaces
EJERCICIOS DE ENLACE QUÍMICO DEL LIBRO 28. -CO C = O : C 3 O C O C 3 OC 3 C O C a) La longitud de enlace CO es menor en el formaldehido, ya que tiene un doble enlace. b) El metanol puede formar enlaces
Los minerales son sustancias químicas y como tales, tienen una composición
 4.2. MINERALES. Los minerales son sustancias químicas y como tales, tienen una composición química fija. Están formados siempre por los mismos elementos y en la misma proporción. Los minerales siempre
4.2. MINERALES. Los minerales son sustancias químicas y como tales, tienen una composición química fija. Están formados siempre por los mismos elementos y en la misma proporción. Los minerales siempre
LA CORTEZA TERRESTRE
 LA CORTEZA TERRESTRE La corteza es la capa superficial sólida de la geosfera, es una capa muy delgada, pues su espesor oscila entre los 60 km en los continentes y los 7 km en los fondos oceánicos. Tipos
LA CORTEZA TERRESTRE La corteza es la capa superficial sólida de la geosfera, es una capa muy delgada, pues su espesor oscila entre los 60 km en los continentes y los 7 km en los fondos oceánicos. Tipos
5ª UNIDAD ELEMENTOS Y COMPUESTOS
 5ª UNIDAD ELEMENTOS Y COMPUESTOS 3º E.S.O. Grupo Apellidos: Nombre: INTRODUCCIÓN Comenzamos recordando los conceptos más importantes del tema anterior: Cómo son los átomos? Cómo están distribuidos los
5ª UNIDAD ELEMENTOS Y COMPUESTOS 3º E.S.O. Grupo Apellidos: Nombre: INTRODUCCIÓN Comenzamos recordando los conceptos más importantes del tema anterior: Cómo son los átomos? Cómo están distribuidos los
FÍSICA Y QUÍMICA 3º ESO ACTIVIDADES DE RECUPERACIÓN
 FÍSICA Y QUÍMICA 3º ESO ACTIVIDADES DE RECUPERACIÓN (PARTE 2) CURSO 2012/13 Nombre y apellidos: 1 LA CIENCIA Y SU MÉTODO. MEDIDA DE MAGNITUDES LOS ÁTOMOS Y SU COMPLEJIDAD 1. Qué explica el modelo atómico
FÍSICA Y QUÍMICA 3º ESO ACTIVIDADES DE RECUPERACIÓN (PARTE 2) CURSO 2012/13 Nombre y apellidos: 1 LA CIENCIA Y SU MÉTODO. MEDIDA DE MAGNITUDES LOS ÁTOMOS Y SU COMPLEJIDAD 1. Qué explica el modelo atómico
Una mezcla es un compuesto formado por varias sustancias con distintas propiedades
 COMPOSICIÓN DE LA MATERIA Mezclas homogéneas y heterogéneas Una mezcla es un compuesto formado por varias sustancias con distintas propiedades Algunos sistemas materiales como la leche a simple vista parecen
COMPOSICIÓN DE LA MATERIA Mezclas homogéneas y heterogéneas Una mezcla es un compuesto formado por varias sustancias con distintas propiedades Algunos sistemas materiales como la leche a simple vista parecen
Minerales: Clasificación y Propiedades de los Minerales. Hernán Santos, Ph.D. Departamento de Geología Recinto Universitario de Mayagüez
 Minerales: Clasificación y Propiedades de los Minerales Hernán Santos, Ph.D. Departamento de Geología Recinto Universitario de Mayagüez 1 Qué es un Mineral? Un mineral es un sólido inorgánico que ocurre
Minerales: Clasificación y Propiedades de los Minerales Hernán Santos, Ph.D. Departamento de Geología Recinto Universitario de Mayagüez 1 Qué es un Mineral? Un mineral es un sólido inorgánico que ocurre
TEMA 8 SISTEMA PERIÓDICO Y ENLACES
 TEMA 8 SISTEMA PERIÓDICO Y ENLACES 1. LA TABLA PERIÓDICA Elementos químicos son el conjunto de átomos que tienen en común su número atómico, Z. Hoy conocemos 111 elementos diferentes. Los elementos que
TEMA 8 SISTEMA PERIÓDICO Y ENLACES 1. LA TABLA PERIÓDICA Elementos químicos son el conjunto de átomos que tienen en común su número atómico, Z. Hoy conocemos 111 elementos diferentes. Los elementos que
1. Los elementos químicos
 RESUMEN de la UNIDAD 3. ELEMENTOS Y COMPUESTOS 1. Los elementos químicos La materia está formada por partículas denominadas átomos que, a su vez, están formados por otras partículas más pequeñas: protones,
RESUMEN de la UNIDAD 3. ELEMENTOS Y COMPUESTOS 1. Los elementos químicos La materia está formada por partículas denominadas átomos que, a su vez, están formados por otras partículas más pequeñas: protones,
TEMA 17. LOS MINERALES
 TEMA 17. LOS MINERALES Lee atentamente. 1. LOS MINERALES: MATERIA AMORFA Y MATERIA CRISTALINA La capa más externa de la Tierra se llama Litosfera. Los elementos químicos que forman parte de la Tierra reciben
TEMA 17. LOS MINERALES Lee atentamente. 1. LOS MINERALES: MATERIA AMORFA Y MATERIA CRISTALINA La capa más externa de la Tierra se llama Litosfera. Los elementos químicos que forman parte de la Tierra reciben
Niveles de Organización Conceptos, átomos y enlaces
 Niveles de Organización Conceptos, átomos y enlaces Cómo se organiza la materia viva? NIVELES DE ORGANIZACIÓN ÁTOMO MOLÉCULA (ELEMENTO- COMPUESTO) MACROMOLÉCULA CÉLULA TEJIDO ÓRGANO SISTEMA ORGANISMO MULTICELULAR
Niveles de Organización Conceptos, átomos y enlaces Cómo se organiza la materia viva? NIVELES DE ORGANIZACIÓN ÁTOMO MOLÉCULA (ELEMENTO- COMPUESTO) MACROMOLÉCULA CÉLULA TEJIDO ÓRGANO SISTEMA ORGANISMO MULTICELULAR
MINERALES Y ROCAS PROCESOS DE FORMACIÓN ROCAS ÍGNEAS
 II Unidad MINERALES Y ROCAS PROCESOS DE FORMACIÓN ROCAS ÍGNEAS Carla Navea G. Magma Es un material móvil, caliente, constituido por fases sólidas, gaseosas y liquidas, es decir, es un sistema multicomponente,
II Unidad MINERALES Y ROCAS PROCESOS DE FORMACIÓN ROCAS ÍGNEAS Carla Navea G. Magma Es un material móvil, caliente, constituido por fases sólidas, gaseosas y liquidas, es decir, es un sistema multicomponente,
Los elementos químicos
 Los elementos químicos Física y Química Las primeras clasificaciones de los elementos Oxford University Press España, S. A. Física y Química 3º ESO 2 Un elemento químico es un tipo de materia constituido
Los elementos químicos Física y Química Las primeras clasificaciones de los elementos Oxford University Press España, S. A. Física y Química 3º ESO 2 Un elemento químico es un tipo de materia constituido
ByG 1º Bto. Tema 2 Los materiales terrestres: minerales.
 ByG 1º Bto. Tema 2 Los materiales terrestres: minerales. 1. Los cristales. El ser humano siempre se ha sentido atraído por los colores, el brillo y la forma de los cristales que aparecen en las rocas.
ByG 1º Bto. Tema 2 Los materiales terrestres: minerales. 1. Los cristales. El ser humano siempre se ha sentido atraído por los colores, el brillo y la forma de los cristales que aparecen en las rocas.
Características de electrones protones y neutrones
 Características de electrones protones y neutrones Carga eléctrica Masa Espín SI (C) Atómica SI(g) Atómica (uma) Protón +1,6021 10-19 +1 1,6725 10-24 1,0073 1/2 neutrón 0 0 1,6748 10-24 1,0087 1/2 electrón
Características de electrones protones y neutrones Carga eléctrica Masa Espín SI (C) Atómica SI(g) Atómica (uma) Protón +1,6021 10-19 +1 1,6725 10-24 1,0073 1/2 neutrón 0 0 1,6748 10-24 1,0087 1/2 electrón
PORTAFOLIO DE EVIDENCIAS QUÍMICA I DE SEGUNDA OPORTUNIDAD I LEE DETENIDAMENTE CADA ENUNCIADO Y CONTESTA SEGÚN SE TE PIDA.
 PORTAFOLIO DE EVIDENCIAS QUÍMICA I DE SEGUNDA OPORTUNIDAD I LEE DETENIDAMENTE CADA ENUNCIADO Y CONTESTA SEGÚN SE TE PIDA. 1.- Ciencia que estudia las características y la composición de los materiales,
PORTAFOLIO DE EVIDENCIAS QUÍMICA I DE SEGUNDA OPORTUNIDAD I LEE DETENIDAMENTE CADA ENUNCIADO Y CONTESTA SEGÚN SE TE PIDA. 1.- Ciencia que estudia las características y la composición de los materiales,
Los minerales. Has observado las arenas de las playas de México?. Para los que hemos tenido
 Los minerales Sabes cómo se forman los minerales? Introducción Has observado las arenas de las playas de México?. Para los que hemos tenido la oportunidad de visitar las playas de la costas del pacífico,
Los minerales Sabes cómo se forman los minerales? Introducción Has observado las arenas de las playas de México?. Para los que hemos tenido la oportunidad de visitar las playas de la costas del pacífico,
Sistemática de minerales. 2. Silicatos
 Sistemática de minerales 2. Silicatos Silicatos Enlace Si-O Geometría: tetraedros Estabilidad máxima Posibilidad polimerización Grupos de Silicatos Nesosilicatos [SiO4] -4 Grupos de Silicatos Sorosilicatos
Sistemática de minerales 2. Silicatos Silicatos Enlace Si-O Geometría: tetraedros Estabilidad máxima Posibilidad polimerización Grupos de Silicatos Nesosilicatos [SiO4] -4 Grupos de Silicatos Sorosilicatos
ROCAS, MINERALES Y CRISTALES
 1º Bachillerato ROCAS, MINERALES Y CRISTALES Calcita DEFINICIÓN DE MINERAL Cuerpo sólido, natural, inorgánico, homogéneo en sus propiedades físico-químicas, de composición química fija (o variable dentro
1º Bachillerato ROCAS, MINERALES Y CRISTALES Calcita DEFINICIÓN DE MINERAL Cuerpo sólido, natural, inorgánico, homogéneo en sus propiedades físico-químicas, de composición química fija (o variable dentro
PROPIEDADES FÍSICAS DE LOS MINERALES
 PROPIEDADES FÍSICAS DE LOS MINERALES INTRODUCCIÓN La identificación de un mineral, basándose en la estructura interna y la composición química, es difícil sin la ayuda de ensayos y aparatos sofisticados.
PROPIEDADES FÍSICAS DE LOS MINERALES INTRODUCCIÓN La identificación de un mineral, basándose en la estructura interna y la composición química, es difícil sin la ayuda de ensayos y aparatos sofisticados.
3. El sistema periódico de los elementos. 3. El sistema periódico de los elementos. 3. El sistema periódico de los elementos
 3. El sistema periódico de los elementos Clasificación de los elementos químicos en el siglo XIX: los químicos de la época tenían una idea vaga de los átomos; no conocían p + ni e -. Clasificaban los elementos
3. El sistema periódico de los elementos Clasificación de los elementos químicos en el siglo XIX: los químicos de la época tenían una idea vaga de los átomos; no conocían p + ni e -. Clasificaban los elementos
Física y Química 3º E.S.O. 2013/14
 Física y Química 3º E.S.O. 2013/14 TEMA 3: La materia. Propiedades eléctricas y el átomo 1.- En la siguiente sopa de letras puedes encontrar los nombres de 13 elementos químicos. A O M O L P B A C E E
Física y Química 3º E.S.O. 2013/14 TEMA 3: La materia. Propiedades eléctricas y el átomo 1.- En la siguiente sopa de letras puedes encontrar los nombres de 13 elementos químicos. A O M O L P B A C E E
Tema 7 Mineralogía. Turmalina Vanadinita. Willemita
 1 Tema 7 Mineralogía Turmalina Vanadinita Willemita 2 Por qué estudiar los minerales y las rocas? El mundo en que vivimos depende de ellos... Por qué estudiar los minerales y las rocas? Cada persona del
1 Tema 7 Mineralogía Turmalina Vanadinita Willemita 2 Por qué estudiar los minerales y las rocas? El mundo en que vivimos depende de ellos... Por qué estudiar los minerales y las rocas? Cada persona del
CRISTALES Y MI ERALES
 CRISTALES Y MI ERALES ÁTOMOS, ELEME TOS, MI ERALES, CRISTALES Y ROCAS Un átomo es la partícula más pequeña de un elemento químico que tiene las características del elemento. Formado por protones, neutrones
CRISTALES Y MI ERALES ÁTOMOS, ELEME TOS, MI ERALES, CRISTALES Y ROCAS Un átomo es la partícula más pequeña de un elemento químico que tiene las características del elemento. Formado por protones, neutrones
Las que tienen relación con el de tamaño: LAS PROPIEDADES PERIÓDICAS. Se pueden separar en dos grupos: PERIODICIDAD
 LAS PROPIEDADES PERIÓDICAS Se pueden separar en dos grupos: 1- Las que tienen relación con el de tamaño: Los radios atómicos y los radios iónicos o cristalinos. La densidad. (ρ) El punto de fusión y ebullición.
LAS PROPIEDADES PERIÓDICAS Se pueden separar en dos grupos: 1- Las que tienen relación con el de tamaño: Los radios atómicos y los radios iónicos o cristalinos. La densidad. (ρ) El punto de fusión y ebullición.
MINERALES Y ROCAS. POLIMORFISMO. Dos minerales o más son polimorfos cuando presentan la misma composición química y distinto sistema cristalino.
 MINERALES Y ROCAS QUÉ ES UN MINERAL? Un mineral es un sólido de composición química y estructura cristalina determinadas, que se ha formado de modo natural. Frecuentemente los minerales forman granos pequeños
MINERALES Y ROCAS QUÉ ES UN MINERAL? Un mineral es un sólido de composición química y estructura cristalina determinadas, que se ha formado de modo natural. Frecuentemente los minerales forman granos pequeños
La presencia del estado sólido en la materia que nos rodea es constante. El arreglo de sus moléculas o iones es uniforme.
 2.7 ESTRUCTURA DE LOS MATERIALES. 2.7.1 ESTADO SÓLIDO (CRISTALINO). La presencia del estado sólido en la materia que nos rodea es constante. El arreglo de sus moléculas o iones es uniforme. En los gases
2.7 ESTRUCTURA DE LOS MATERIALES. 2.7.1 ESTADO SÓLIDO (CRISTALINO). La presencia del estado sólido en la materia que nos rodea es constante. El arreglo de sus moléculas o iones es uniforme. En los gases
Elementos ordenados según su número atómico (Z, número de p + ) Hay 18 PERÍODOS
 TABLA PERIÓDICA Elementos ordenados según su número atómico (Z, número de p + ) Columnas Filas GRUPOS PERÍODOS Familias de elementos con propiedades comunes Hay 18 División principal Elementos representativos
TABLA PERIÓDICA Elementos ordenados según su número atómico (Z, número de p + ) Columnas Filas GRUPOS PERÍODOS Familias de elementos con propiedades comunes Hay 18 División principal Elementos representativos
La geosfera. Biología y Geología 1.º ESO
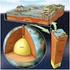 La geosfera Biología y Geología 1.º ESO El origen del universo Acreción de planetesimales Diferenciación por densidades Biología y Geología 1.º ESO 2 Las capas de la geosfera Corteza continental Más de
La geosfera Biología y Geología 1.º ESO El origen del universo Acreción de planetesimales Diferenciación por densidades Biología y Geología 1.º ESO 2 Las capas de la geosfera Corteza continental Más de
Ciencias del Mar. Meteorización de las Rocas. Oceanografía Química. Meteorización de las rocas
 Ciencias del Mar Meteorización de las Rocas Oceanografía Química Meteorización de las rocas La meteorización es el proceso de transformaciones físicas y químicas de las rocas parentales y minerales primarios
Ciencias del Mar Meteorización de las Rocas Oceanografía Química Meteorización de las rocas La meteorización es el proceso de transformaciones físicas y químicas de las rocas parentales y minerales primarios
OBJETIVO.- Diferenciar los distintos tipos de enlace químico para establecer las propiedades de cada compuesto.
 OBJETIVO.- Diferenciar los distintos tipos de enlace químico para establecer las propiedades de cada compuesto. 1. Generalidades de los enlaces químicos Los enlaces químicos, son las fuerzas que mantienen
OBJETIVO.- Diferenciar los distintos tipos de enlace químico para establecer las propiedades de cada compuesto. 1. Generalidades de los enlaces químicos Los enlaces químicos, son las fuerzas que mantienen
Departamento de Física y Química. Ies Dr. Rodríguez Delgado. Ronda Nivel 1º Bachillerato
 Departamento de Física y Química. Ies Dr. Rodríguez Delgado. Ronda Nivel 1º Bachillerato Planteamiento del problema 1. La mina de un lápiz se compone de grafito y arcilla. El grafito es una sustancia simple
Departamento de Física y Química. Ies Dr. Rodríguez Delgado. Ronda Nivel 1º Bachillerato Planteamiento del problema 1. La mina de un lápiz se compone de grafito y arcilla. El grafito es una sustancia simple
La geosfera. La geosfera. Biología y Geología 1.º ESO
 La geosfera Biología y Geología 1.º ESO El origen del universo Acreción de planetesimales Diferenciación por densidades Oxford University Press España, S. A. Biología y Geología 1.º ESO 2 Las capas de
La geosfera Biología y Geología 1.º ESO El origen del universo Acreción de planetesimales Diferenciación por densidades Oxford University Press España, S. A. Biología y Geología 1.º ESO 2 Las capas de
Explicación de las propiedades y los estados de agregación en los compuestos químicos en función de los tipos de enlace. vs.
 Explicación de las propiedades y los estados de agregación en los compuestos químicos en función de los tipos de enlace. vs. Usar las propiedades y los estados de agregación en los compuestos químicos
Explicación de las propiedades y los estados de agregación en los compuestos químicos en función de los tipos de enlace. vs. Usar las propiedades y los estados de agregación en los compuestos químicos
Unidad 3 Curso: Química General 1 Mtra. Norma Mónica López.
 Unidad 3 Curso: Química General 1 Mtra. Norma Mónica López. Interacciones eléctricas De atracción +, - De repulsión +, + ó -,- Entre Átomos de una misma molécula Moléculas vecinas 2 ENLACE QUÍMICO Siempre
Unidad 3 Curso: Química General 1 Mtra. Norma Mónica López. Interacciones eléctricas De atracción +, - De repulsión +, + ó -,- Entre Átomos de una misma molécula Moléculas vecinas 2 ENLACE QUÍMICO Siempre
TEMA 1: ESTRUCTURA INTERNA DE LOS MATERIALES
 PERIODO Departamento de Tecnología. IES Nuestra Señora de la Almudena Mª Jesús Saiz TEMA 1: ESTRUCTURA INTERNA DE LOS MATERIALES El átomo: Toda la materia está compuesta por átomos y éstos por partículas
PERIODO Departamento de Tecnología. IES Nuestra Señora de la Almudena Mª Jesús Saiz TEMA 1: ESTRUCTURA INTERNA DE LOS MATERIALES El átomo: Toda la materia está compuesta por átomos y éstos por partículas
LA LA ESTRUCTURA DE LA MATERIA. 1.-Desarrollo histórico del concepto de átomo. Teoría de Demócrito. Teoría de Dalton. Componentes del átomo
 ANEXO AL TEMA 4 LA LA ESTRUCTURA DE LA MATERIA 1.-Desarrollo histórico del concepto de átomo Teoría de Demócrito Teoría de Dalton Modelo actual Componentes del átomo Concepto de ión 2.-Elememtos y compuestos
ANEXO AL TEMA 4 LA LA ESTRUCTURA DE LA MATERIA 1.-Desarrollo histórico del concepto de átomo Teoría de Demócrito Teoría de Dalton Modelo actual Componentes del átomo Concepto de ión 2.-Elememtos y compuestos
PRÁCTICA: RECONOCIMIENTO DE MINERALES
 PRÁCTICA: RECONOCIMIENTO DE MINERALES OBJETIVO Identificar minerales a partir de la observación directa de sus propiedades físicas principales. CONCEPTOS BÁSICOS Un mineral es una sustancia inorgánica
PRÁCTICA: RECONOCIMIENTO DE MINERALES OBJETIVO Identificar minerales a partir de la observación directa de sus propiedades físicas principales. CONCEPTOS BÁSICOS Un mineral es una sustancia inorgánica
Química Inorgánica Bloque d 1. BLOQUE d
 Química Inorgánica Bloque d 1 BLOQUE d Los elementos del bloque d están ubicados entre los grupos 2 y 13 de la tabla periódica y se los suele llamar metales de transición. elemento de transición: es un
Química Inorgánica Bloque d 1 BLOQUE d Los elementos del bloque d están ubicados entre los grupos 2 y 13 de la tabla periódica y se los suele llamar metales de transición. elemento de transición: es un
IES Atenea (S.S. de los Reyes) Departamento de Física y Química. PAU Química. Septiembre Fase específica OPCIÓN A
 1 PAU Química. Septiembre 2010. Fase específica OPCIÓN A Cuestión 1A. Considere las sustancias: cloruro de potasio, agua, cloro y sodio. a) Indique el tipo de enlace que presenta cada una de ellas. b)
1 PAU Química. Septiembre 2010. Fase específica OPCIÓN A Cuestión 1A. Considere las sustancias: cloruro de potasio, agua, cloro y sodio. a) Indique el tipo de enlace que presenta cada una de ellas. b)
Tema 5: El átomo y sus uniones.
 Tema 5: El átomo y sus uniones. 1. Teoría Atómica de Dalton. En 1803, John Dalton expone su Teoría Atómica que se basa en los siguientes puntos: Los elementos químicos están formados por partículas muy
Tema 5: El átomo y sus uniones. 1. Teoría Atómica de Dalton. En 1803, John Dalton expone su Teoría Atómica que se basa en los siguientes puntos: Los elementos químicos están formados por partículas muy
Física y Química 3º ESO
 1. Física y Química. Ciencias de la medida forman parte de las necesitan Ciencias de la naturaleza medir las propiedades de los cuerpos que se dividen en para lo cual se emplean lo que siempre conlleva
1. Física y Química. Ciencias de la medida forman parte de las necesitan Ciencias de la naturaleza medir las propiedades de los cuerpos que se dividen en para lo cual se emplean lo que siempre conlleva
IES Atenea (S.S. de los Reyes) Departamento de Física y Química. PAU Química. Septiembre 2006 PRIMERA PARTE
 1 PAU Química. Septiembre 2006 PRIMERA PARTE Cuestión 1. La configuración electrónica del último nivel energético de un elemento es 4s 2 4p 3. De acuerdo con este dato: a) Deduzca la situación de dicho
1 PAU Química. Septiembre 2006 PRIMERA PARTE Cuestión 1. La configuración electrónica del último nivel energético de un elemento es 4s 2 4p 3. De acuerdo con este dato: a) Deduzca la situación de dicho
SOLUCIONARIO Guía Estándar Anual
 SOLUCIONARIO Guía Estándar Anual El enlace químico SGUICES004CB33-A16V1 Ítem Alternativa Habilidad 1 E Reconocimiento 2 B Aplicación 3 C Comprensión 4 D Comprensión 5 D Aplicación 6 D Aplicación 7 D Comprensión
SOLUCIONARIO Guía Estándar Anual El enlace químico SGUICES004CB33-A16V1 Ítem Alternativa Habilidad 1 E Reconocimiento 2 B Aplicación 3 C Comprensión 4 D Comprensión 5 D Aplicación 6 D Aplicación 7 D Comprensión
ESTRUCTURA DE LA MATERIA QCA 05 ANDALUCÍA
 1.- a) Escriba la configuración electrónica de los elementos A, B y C, cuyos números atómicos son 33, 35 y 37, respectivamente. b) Indique el grupo y el periodo al que pertenecen. c) Razone que elemento
1.- a) Escriba la configuración electrónica de los elementos A, B y C, cuyos números atómicos son 33, 35 y 37, respectivamente. b) Indique el grupo y el periodo al que pertenecen. c) Razone que elemento
Materia: FÍSICA Y QUÍMICA Curso
 ACTIVIDADES DE REFUERZO FÍSICA Y QUÍMICA 3º ESO. JUNIO 2015. 1.- Realizar las configuraciones electrónicas de todos los elementos de los tres primeros periodos de la tabla periódica. 2.- Razonar cuales
ACTIVIDADES DE REFUERZO FÍSICA Y QUÍMICA 3º ESO. JUNIO 2015. 1.- Realizar las configuraciones electrónicas de todos los elementos de los tres primeros periodos de la tabla periódica. 2.- Razonar cuales
A su vez, una molécula está compuesta por átomos. Cada uno de ellos posee unas propiedades diferentes en el interior de la molécula que constituyen.
 Constitución de la materia. Supongamos que cualquier sustancia de la naturaleza la dividimos en partes cada vez más pequeñas, conservando cada una de ellas las propiedades de la sustancia inicial. Si seguimos
Constitución de la materia. Supongamos que cualquier sustancia de la naturaleza la dividimos en partes cada vez más pequeñas, conservando cada una de ellas las propiedades de la sustancia inicial. Si seguimos
QUÍMICA. La MATERIA REPRESENTACIÓN. Observación Datos Ley Hipótesis Teoría DEFINICIONES BÁSICAS. Propiedades
 QUÍMICA La MATERIA Relación constante TEORÍA EXPERIMENTACIÓN Ciencia básica - Estructura - Composición - Propiedades - Transformaciones REPRESENTACIÓN OBSERVACIÓN mundo macroscópico Técnica sistemática
QUÍMICA La MATERIA Relación constante TEORÍA EXPERIMENTACIÓN Ciencia básica - Estructura - Composición - Propiedades - Transformaciones REPRESENTACIÓN OBSERVACIÓN mundo macroscópico Técnica sistemática
Colegio San Lorenzo - Copiapó - Región de Atacama Per Laborem ad Lucem
 TEMARIO EXAMENES QUIMICA 2012 7º BASICO Descubrimiento del átomo: Quién lo descubrió y su significado Estructura atómica: Partes del átomo, características del núcleo y la corteza, cálculo del protón,
TEMARIO EXAMENES QUIMICA 2012 7º BASICO Descubrimiento del átomo: Quién lo descubrió y su significado Estructura atómica: Partes del átomo, características del núcleo y la corteza, cálculo del protón,
IES Atenea (S.S. de los Reyes) Departamento de Física y Química. PAU Química. Junio 2008 PRIMERA PARTE
 1 PAU Química. Junio 2008 PRIMERA PARTE Cuestión 1. Dados los elementos Na, C, Si y Ne: a) Escriba sus configuraciones electrónicas. Cuántos electrones desapareados presenta cada uno en su estado fundamental?
1 PAU Química. Junio 2008 PRIMERA PARTE Cuestión 1. Dados los elementos Na, C, Si y Ne: a) Escriba sus configuraciones electrónicas. Cuántos electrones desapareados presenta cada uno en su estado fundamental?
Astrofísica del Sistema Solar
 Astrofísica del Sistema Solar Unidad 3: Superficies Planetarias los planetas terrestres y cuerpos menores presentan una superficie. todas ellas presentan propiedades geológicas únicas. la reflectividad
Astrofísica del Sistema Solar Unidad 3: Superficies Planetarias los planetas terrestres y cuerpos menores presentan una superficie. todas ellas presentan propiedades geológicas únicas. la reflectividad
UNIDAD 10.- LAS UNIONES ENTRE ÁTOMOS. Cuestiones de evaluación inicial. 2.- Cuántos protones y cuantos neutrones tiene el Carbono?
 UNIDAD 10.- LAS UNIONES ENTRE ÁTOMOS Cuestiones de evaluación inicial 1.- Cuántos elementos químicos conoces? 2.- Cuántos protones y cuantos neutrones tiene el Carbono? 3.- Qué es el sistema periódico?
UNIDAD 10.- LAS UNIONES ENTRE ÁTOMOS Cuestiones de evaluación inicial 1.- Cuántos elementos químicos conoces? 2.- Cuántos protones y cuantos neutrones tiene el Carbono? 3.- Qué es el sistema periódico?
LECCIÓN Nº 03 TABLA PERIÓDICA
 LECCIÓN Nº 03 TABLA PERIÓDICA OBJETIVO ESPECÍFICO: Conocer las características estructurales y propiedades de las partículas subatómicas(electrón, protón y neutrón), modelos Reconocer Número atómico y
LECCIÓN Nº 03 TABLA PERIÓDICA OBJETIVO ESPECÍFICO: Conocer las características estructurales y propiedades de las partículas subatómicas(electrón, protón y neutrón), modelos Reconocer Número atómico y
UNIDAD 3. MODIFICACIÓN DE LAS PROPIEDADES DE LOS METALES
 UNIDAD 3. MODIFICACIÓN DE LAS PROPIEDADES DE LOS METALES 1. GENERALIDADES... Pág. 49 2. ESTRUCTURA INTERNA DE LOS METALES... Pág. 49 2.1. Estructuras cristalinas... Pág. 49 2.2. Estructura cristalina cúbica
UNIDAD 3. MODIFICACIÓN DE LAS PROPIEDADES DE LOS METALES 1. GENERALIDADES... Pág. 49 2. ESTRUCTURA INTERNA DE LOS METALES... Pág. 49 2.1. Estructuras cristalinas... Pág. 49 2.2. Estructura cristalina cúbica
PROBLEMAS RESUELTOS SELECTIVIDAD ANDALUCÍA 2010 QUÍMICA TEMA 3: ENLACES QUÍMICOS
 PROBLEMAS RESUELTOS SELECTIVIDAD ANDALUCÍA 010 QUÍMICA TEMA : ENLACES QUÍMICOS Junio, Ejercicio, Opción A Reserva 1, Ejercicio, Opción A Reserva, Ejercicio, Opción B Reserva, Ejercicio, Opción B Septiembre,
PROBLEMAS RESUELTOS SELECTIVIDAD ANDALUCÍA 010 QUÍMICA TEMA : ENLACES QUÍMICOS Junio, Ejercicio, Opción A Reserva 1, Ejercicio, Opción A Reserva, Ejercicio, Opción B Reserva, Ejercicio, Opción B Septiembre,
Colección de problemas Unidad 2
 Facultad de Química, UNAM Curso: Química General I Colección de problemas Unidad 2 1. Describe una contribución importante a la ciencia hecha por cada uno de los científicos siguientes: Dalton, Thomson,
Facultad de Química, UNAM Curso: Química General I Colección de problemas Unidad 2 1. Describe una contribución importante a la ciencia hecha por cada uno de los científicos siguientes: Dalton, Thomson,
b) La zona externa del átomo se llama CORTEZA. y ahí es donde se mueven los ELECTRONES
 PREGUNTAS DE RESPUESTA BREVE 1. Completa las siguientes frases relativas a los átomos de los elementos: a) La parte del átomo en donde se puede considerar que se concentra toda su masa es el NÚCLEO y ahí
PREGUNTAS DE RESPUESTA BREVE 1. Completa las siguientes frases relativas a los átomos de los elementos: a) La parte del átomo en donde se puede considerar que se concentra toda su masa es el NÚCLEO y ahí
INTRODUCCIÓN A LA QUÍMICA
 INTRODUCCIÓN A LA QUÍMICA TRABAJO PRÁCTICO N 1 4 Año A, B, C, D 2.015 Prof. María Laura Sepúlveda Broky INTRODUCCIÓN A LA QUÍMICA Prof. María Laura Sepúlveda Broky 1)A- Realizar un esquema de la Tabla
INTRODUCCIÓN A LA QUÍMICA TRABAJO PRÁCTICO N 1 4 Año A, B, C, D 2.015 Prof. María Laura Sepúlveda Broky INTRODUCCIÓN A LA QUÍMICA Prof. María Laura Sepúlveda Broky 1)A- Realizar un esquema de la Tabla
Tema 1.3 Estados de agregación de la materia. Tema 1.4 Composición de la materia
 Tema 1.3 Estados de agregación de la materia Tema 1.4 Composición de la materia 1 MATERIA Todo aquello que ocupa un lugar en el espacio, tiene una energía medible y está sujeto a cambios en el tiempo y
Tema 1.3 Estados de agregación de la materia Tema 1.4 Composición de la materia 1 MATERIA Todo aquello que ocupa un lugar en el espacio, tiene una energía medible y está sujeto a cambios en el tiempo y
María Eugenia Mendoza Álvarez Instituto de Física BUAP
 María Eugenia Mendoza Álvarez Instituto de Física BUAP febrero 2014 Contenido Introducción El reino mineral: definiciones y clasificación Procesos de formación de los minerales Evolución mineral 2 El reino
María Eugenia Mendoza Álvarez Instituto de Física BUAP febrero 2014 Contenido Introducción El reino mineral: definiciones y clasificación Procesos de formación de los minerales Evolución mineral 2 El reino
PROYECTO PLATAFORMA VIRTUAL PRUEBA SABER 11 COLEGIO ANDRES BELLO
 PROYECTO PLATAFORMA VIRTUAL PRUEBA SABER 11 COLEGIO ANDRES BELLO QUÍMICA PROFESORA: ADRIANA GUTIERREZ RIVAS GRADO 11 SAN JOSE DE CÚCUTA 20/07/12 1451. El elemento Q reacciona con el oxígeno formando el
PROYECTO PLATAFORMA VIRTUAL PRUEBA SABER 11 COLEGIO ANDRES BELLO QUÍMICA PROFESORA: ADRIANA GUTIERREZ RIVAS GRADO 11 SAN JOSE DE CÚCUTA 20/07/12 1451. El elemento Q reacciona con el oxígeno formando el
ENLACES QUÍMICOS. Los enlaces químicos, son las fuerzas que mantienen unidos a los átomos.
 1. Generalidades de los enlaces químicos ENLACES QUÍMICOS Los enlaces químicos, son las fuerzas que mantienen unidos a los átomos. Cuando los átomos se enlazan entre sí, ceden, aceptan o comparten electrones.
1. Generalidades de los enlaces químicos ENLACES QUÍMICOS Los enlaces químicos, son las fuerzas que mantienen unidos a los átomos. Cuando los átomos se enlazan entre sí, ceden, aceptan o comparten electrones.
Profesor(a): C.D. María Isabel Pérez Aguilar
 Área Académica: Biología Básica Tema: Bioelementos Profesor(a): C.D. María Isabel Pérez Aguilar Periodo: Enero- Julio 2012 Abstract Bioelements Bioelements are the essential components of life. This topic
Área Académica: Biología Básica Tema: Bioelementos Profesor(a): C.D. María Isabel Pérez Aguilar Periodo: Enero- Julio 2012 Abstract Bioelements Bioelements are the essential components of life. This topic
PROGRAMA DE LA MATERIA GEOLOGIA GENERAL
 PROGRAMA DE LA MATERIA GEOLOGIA GENERAL MODULO 1 MODULO 2 MODULO 3 Formación del universo y el planeta GEODINAMICA INTERNA Geodinámica externa Geología Histórica Aplicación de la Geología a la búsqueda
PROGRAMA DE LA MATERIA GEOLOGIA GENERAL MODULO 1 MODULO 2 MODULO 3 Formación del universo y el planeta GEODINAMICA INTERNA Geodinámica externa Geología Histórica Aplicación de la Geología a la búsqueda
CRISTALOQUÍMICA TEMA 9 POLIMORFISMO Y TRANSFORMACIONES POLIMÓRFICAS. TRANSFORMACIONES ORDEN - DESORDEN ÍNDICE
 CRISTALOQUÍMICA TEMA 9 POLIMORFISMO Y TRANSFORMACIONES POLIMÓRFICAS. TRANSFORMACIONES ORDEN - DESORDEN 9.1 Introducción 9.2 Estabilidad y equilibrio ÍNDICE 9.3 Concepto de polimorfismo y de transformación
CRISTALOQUÍMICA TEMA 9 POLIMORFISMO Y TRANSFORMACIONES POLIMÓRFICAS. TRANSFORMACIONES ORDEN - DESORDEN 9.1 Introducción 9.2 Estabilidad y equilibrio ÍNDICE 9.3 Concepto de polimorfismo y de transformación
Profesor: Carlos Gutiérrez Arancibia. Temas a tratar: - - Sustancias Puras - Mezclas - Enlaces Químicos - Fuerzas Intermoleculares
 Profesor: Carlos Gutiérrez Arancibia Temas a tratar: - - Sustancias Puras - Mezclas - Enlaces Químicos - Fuerzas Intermoleculares A. Sustancia Pura: SUSTANCIAS PURAS Y MEZCLAS Una sustancia pura es un
Profesor: Carlos Gutiérrez Arancibia Temas a tratar: - - Sustancias Puras - Mezclas - Enlaces Químicos - Fuerzas Intermoleculares A. Sustancia Pura: SUSTANCIAS PURAS Y MEZCLAS Una sustancia pura es un
FORMACION DE MINERALES
 Minerales Metalicos FORMACION DE MINERALES El magma se considera como la fuente primaria de los minerales que forma las menas. En él se encuentran diseminados, en pequeñas cantidades, la mayoría de los
Minerales Metalicos FORMACION DE MINERALES El magma se considera como la fuente primaria de los minerales que forma las menas. En él se encuentran diseminados, en pequeñas cantidades, la mayoría de los
0,225. 0, ,15 0,92
 1.- El ácido clorhídrico reacciona con el mármol (carbonato de calcio) formando cloruro de calcio, dióxido de carbono gas y agua. a) Escribe y ajusta la reacción química. (0,5 p) b) Halla el volumen de
1.- El ácido clorhídrico reacciona con el mármol (carbonato de calcio) formando cloruro de calcio, dióxido de carbono gas y agua. a) Escribe y ajusta la reacción química. (0,5 p) b) Halla el volumen de
1º ESO. Ciencias de la naturaleza. Actividades de recuperación 1ª parte. Instituto Español de Andorra. Alumno/a: Curso actual:
 Instituto Español de Andorra Departamento de Biología y Geología Ciencias de la naturaleza 1º ESO Actividades de recuperación 1ª parte Alumno/a: Curso actual: Página 1 de 10 ATENCIÓN Utiliza este cuadernillo
Instituto Español de Andorra Departamento de Biología y Geología Ciencias de la naturaleza 1º ESO Actividades de recuperación 1ª parte Alumno/a: Curso actual: Página 1 de 10 ATENCIÓN Utiliza este cuadernillo
Departamento de Física y Química. 2.- Deduce el número de neutrones, protones y electrones de los átomos siguientes:
 1.- Para el átomo de Galio, 69 31Ga ; deduce el número de protones, electrones y neutrones. 2.- Deduce el número de neutrones, protones y electrones de los átomos siguientes: U ; Hg ; Th ; He; Ne 235 200
1.- Para el átomo de Galio, 69 31Ga ; deduce el número de protones, electrones y neutrones. 2.- Deduce el número de neutrones, protones y electrones de los átomos siguientes: U ; Hg ; Th ; He; Ne 235 200
Tema 2: MINERALOGÍA. - Concepto de mineral y cristal - Propiedades y características - Clasificación de los minerales (Strunz)
 Tema 2: MINERALOGÍA - Concepto de mineral y cristal - Propiedades y características - Clasificación de los minerales (Strunz) Concepto de mineral y cristal: Mineral: Sólido homogéneo por naturaleza con
Tema 2: MINERALOGÍA - Concepto de mineral y cristal - Propiedades y características - Clasificación de los minerales (Strunz) Concepto de mineral y cristal: Mineral: Sólido homogéneo por naturaleza con
GEOLOGÍA BÁSICA PARA EL CURSO DE AGRONOMÍA I
 Prof. Donato García López GEOLOGÍA BÁSICA PARA EL CURSO DE AGRONOMÍA I GEOLOGÍA es una palabra del idioma griego, que se puede traducir al español de la manera siguiente: geo = tierra y logos = tratado.
Prof. Donato García López GEOLOGÍA BÁSICA PARA EL CURSO DE AGRONOMÍA I GEOLOGÍA es una palabra del idioma griego, que se puede traducir al español de la manera siguiente: geo = tierra y logos = tratado.
ACTIVIDADES Tema 10. 2. Qué relación hay entre los minerales y las rocas? Los minerales se mezclan para formar las rocas.
 ACTIVIDADES Tema 10 1. Escribe en tu cuaderno una definición de mineral en la que se especifiquen las tres características que lo identifican. Un mineral es un sólido creado por la combinación química
ACTIVIDADES Tema 10 1. Escribe en tu cuaderno una definición de mineral en la que se especifiquen las tres características que lo identifican. Un mineral es un sólido creado por la combinación química
Sistema Periódico de los elementos. 2º Bachillerato
 Sistema Periódico de los elementos 2º Bachillerato Índice 1. Clasificación de los elementos 2. Núcleo atómico 3. Configuración electrónica 4. La tabla periódica 5. Propiedades periódicas Tamaño y radio
Sistema Periódico de los elementos 2º Bachillerato Índice 1. Clasificación de los elementos 2. Núcleo atómico 3. Configuración electrónica 4. La tabla periódica 5. Propiedades periódicas Tamaño y radio
Capítulo 2 La estructura de los sólidos cristalinos
 Capítulo 2 La estructura de los sólidos cristalinos TEMA 2: La estructura de los sólidos cristalinos 1. Los enlaces interatómicos 2. La estructura cristalina 3. Estructuras de empaquetamiento compacto
Capítulo 2 La estructura de los sólidos cristalinos TEMA 2: La estructura de los sólidos cristalinos 1. Los enlaces interatómicos 2. La estructura cristalina 3. Estructuras de empaquetamiento compacto
Universidad de Murcia
 Universidad de Murcia CRISTALOGRAFÍA Control MURCIA 2011 2012 Francisco Cánovas Picón Índice Índice.............................................. 2 1. Problema 1.......................................
Universidad de Murcia CRISTALOGRAFÍA Control MURCIA 2011 2012 Francisco Cánovas Picón Índice Índice.............................................. 2 1. Problema 1.......................................
PROPIEDADES QUÍMICAS DEL SUELO
 PROPIEDADES QUÍMICAS DEL SUELO DEFINICIONES Ión: Átomos o moléculas que pierden o ganan electrones por lo cual adquieren una determinada carga; si ganan adquieren carga negativa: aniones (Cl -, NO 3- );
PROPIEDADES QUÍMICAS DEL SUELO DEFINICIONES Ión: Átomos o moléculas que pierden o ganan electrones por lo cual adquieren una determinada carga; si ganan adquieren carga negativa: aniones (Cl -, NO 3- );
2.1.- ESTRUCTURA DEL ÁTOMO
 2.1.- ESTRUCTURA DEL ÁTOMO El átomo está formado por un núcleo, que contiene nuetrones y protones, el que a su vez esta rodeado por electrones. La carga eléctrica de un átomo es nula. Número atómico es
2.1.- ESTRUCTURA DEL ÁTOMO El átomo está formado por un núcleo, que contiene nuetrones y protones, el que a su vez esta rodeado por electrones. La carga eléctrica de un átomo es nula. Número atómico es
Fuerzas Intermoleculares. Materia Condensada.
 Fuerzas Intermoleculares. Materia Condensada. Contenidos Introducción. Tipos de fuerzas intermoleculares. Fuerzas ion-dipolo Fuerzas ion-dipolo inducido Fuerzas de van der Waals Enlace de hidrógeno Tipos
Fuerzas Intermoleculares. Materia Condensada. Contenidos Introducción. Tipos de fuerzas intermoleculares. Fuerzas ion-dipolo Fuerzas ion-dipolo inducido Fuerzas de van der Waals Enlace de hidrógeno Tipos
COMPUESTOS BINARIOS: están formados por átomos de dos elementos diferentes. Se escribe primero el menos electronegativo. (NaCl cloruro de sodio).
 NOMENCLATURA La Química se apoya en la organización La Unión Internacional de Química Pura y Aplicada (IUPAC) para establecer las reglas para nombrar los compuestos. Esta parte de la química se llama nomenclatura.
NOMENCLATURA La Química se apoya en la organización La Unión Internacional de Química Pura y Aplicada (IUPAC) para establecer las reglas para nombrar los compuestos. Esta parte de la química se llama nomenclatura.
Guía de Estudio para 1er Parcial Temas Selectos de Química
 Guía de Estudio para 1er Parcial Temas Selectos de Química 1. Menciona que científicos ordenaron los elementos conocidos en su época en triadas (grupos de tres), en octavas, por número atómico y quien
Guía de Estudio para 1er Parcial Temas Selectos de Química 1. Menciona que científicos ordenaron los elementos conocidos en su época en triadas (grupos de tres), en octavas, por número atómico y quien
ENLACE QUÍMICO. TEMA 3 Pág. 271 libro (Unidad 13)
 ENLACE QUÍMICO TEMA 3 Pág. 271 libro (Unidad 13) CONCEPTO DE ENLACE QUÍMICO Concepto de enlace químico Propiedades de sustancias puras se deben a: Elementos de las que están constituidas Tipo de enlace
ENLACE QUÍMICO TEMA 3 Pág. 271 libro (Unidad 13) CONCEPTO DE ENLACE QUÍMICO Concepto de enlace químico Propiedades de sustancias puras se deben a: Elementos de las que están constituidas Tipo de enlace
UNIDAD 1 La materia y sus cambios
 UNIDAD 1 La materia y sus cambios Tema 1.2 Composición de la materia. Sustancias y mezclas. Mezclas homogéneas, heterogéneas y coloides. Introducción a las disoluciones: no saturadas, saturadas y sobresaturadas.
UNIDAD 1 La materia y sus cambios Tema 1.2 Composición de la materia. Sustancias y mezclas. Mezclas homogéneas, heterogéneas y coloides. Introducción a las disoluciones: no saturadas, saturadas y sobresaturadas.
GUÍA PARA EXAMEN DE REGULARIZACIÓN DE QUÍMICA 1
 GUÍA PARA EXAMEN DE REGULARIZACIÓN DE QUÍMICA 1 1.- Ciencia que estudia la composición, estructura de la materia y sus transformaciones. R= Química 2.-Es todo lo que tiene masa y posee inercia R= Materia
GUÍA PARA EXAMEN DE REGULARIZACIÓN DE QUÍMICA 1 1.- Ciencia que estudia la composición, estructura de la materia y sus transformaciones. R= Química 2.-Es todo lo que tiene masa y posee inercia R= Materia
Átomos polielectrónicos Espín y configuraciones electrónicas Número y masa atómicos (isótopos) Tabla periódica y configuraciones electrónicas
 ESTRUCTURA ELECTRÓNICA Espín y configuraciones electrónicas Número y masa atómicos (isótopos) Tabla periódica y configuraciones electrónicas Átomos con un solo electrón: La energía depende solamente del
ESTRUCTURA ELECTRÓNICA Espín y configuraciones electrónicas Número y masa atómicos (isótopos) Tabla periódica y configuraciones electrónicas Átomos con un solo electrón: La energía depende solamente del
ROCAS, MINERALES Y CRISTALES
 ROCAS, MINERALES Y CRISTALES LOS MINERALES Un mineral es un cuerpo sólido, natural, inorgánico, homogéneo en sus propiedades físico-químicas, de composición química fija (o variable dentro de límites estrechos)
ROCAS, MINERALES Y CRISTALES LOS MINERALES Un mineral es un cuerpo sólido, natural, inorgánico, homogéneo en sus propiedades físico-químicas, de composición química fija (o variable dentro de límites estrechos)
Solucionario Cuaderno Estrategias y Ejercitación Modelo atómico de la materia I: estructura atómica, modelos atómicos y tipos de átomos
 Solucionario Cuaderno Estrategias y Ejercitación Modelo atómico de la materia I: estructura atómica, modelos atómicos y tipos de átomos Química Técnico Profesional Intensivo SCUACTC001TC83-A16V1 Ítem Alternativa
Solucionario Cuaderno Estrategias y Ejercitación Modelo atómico de la materia I: estructura atómica, modelos atómicos y tipos de átomos Química Técnico Profesional Intensivo SCUACTC001TC83-A16V1 Ítem Alternativa
Ciclo roca suelo. Ciclo erosivo. Propiedades fisico - quimico de los minerales arcillosos. Estructura de los minerales arcillosos CICLO ROCA SUELO
 Ciclo roca suelo Ciclo erosivo Propiedades fisico - quimico de los minerales arcillosos Estructura de los minerales arcillosos Indice CICLO ROCA SUELO Según la ASTM : ² Suelo : Sedimentos u otras acumulaciones
Ciclo roca suelo Ciclo erosivo Propiedades fisico - quimico de los minerales arcillosos Estructura de los minerales arcillosos Indice CICLO ROCA SUELO Según la ASTM : ² Suelo : Sedimentos u otras acumulaciones
LA FORMACIÓN DE MINERALES Y ROCAS
 Ó LA FORMACIÓN DE MINERALES Y ROCAS LA FORMACIÓN DE MINERALES Y ROCAS CONTENIDOS: 1. La composición de la Tierra 1. 1. Las rocas que componen la Tierra 1. 2. Qué es un mineral? 1. 3. Los cristales 1. 4.
Ó LA FORMACIÓN DE MINERALES Y ROCAS LA FORMACIÓN DE MINERALES Y ROCAS CONTENIDOS: 1. La composición de la Tierra 1. 1. Las rocas que componen la Tierra 1. 2. Qué es un mineral? 1. 3. Los cristales 1. 4.
Ejercicios resueltos de 3º de E.S.O.
 Ejercicios resueltos de 3º de E.S.O. Estructura de la materia. Modelos atómicos Ejercicio resuelto nº 1 Si el número másico de un átomo es A = 30 y tiene 12 protones, calcula su número de neutrones. Resolución
Ejercicios resueltos de 3º de E.S.O. Estructura de la materia. Modelos atómicos Ejercicio resuelto nº 1 Si el número másico de un átomo es A = 30 y tiene 12 protones, calcula su número de neutrones. Resolución
