Conclusiones científicas y motivos de las conclusiones
|
|
|
- Mario Sosa Ortega
- hace 6 años
- Vistas:
Transcripción
1 Anexo II Conclusiones científicas y motivos para la modificación de las condiciones de las autorizaciones de comercialización y explicación pormenorizada de las diferencias con respecto a la recomendación del PRAC 289
2 Conclusiones científicas y motivos de las conclusiones El CHMP consideró la siguiente recomendación del PRAC de fecha 10 de octubre de 2013 relativa a los anticonceptivos hormonales combinados que contienen clormadinona, desogestrel, dienogest, drospirenona, etonogestrel, gestodeno, norelgestromina, norgestimato o nomegestrol. 1 Resumen general de la evaluación científica Los medicamentos que contienen clormadinona, desogestrel, dienogest, drospirenona, etonogestrel, gestodeno, norelgestromina, norgestimato o nomegestrol están autorizados en la Unión Europea como anticonceptivos hormonales combinados (AHC). Estos medicamentos se combinan con dosis variables de etinilestadiol (EE) o con estradiol (E2). En febrero de 2103, la agencia francesa de medicamentos (ANSM) inició un procedimiento de arbitraje de conformidad con el artículo 31 de la Directiva 2001/83/CE, basándose en que la relación riesgo/beneficio de estos anticonceptivos hormonales combinados era ahora desfavorable para la indicación de anticoncepción autorizada actualmente, debido al incremento del riesgo de tromboembolia (TE) y, por consiguiente, era de interés para la Unión remitir el asunto al PRAC. Se solicitó al PRAC que emitiera una opinión sobre si la indicación de medicamentos que contienen clormadinona, desogestrel, dienogest, drospirenona, etonogestrel, gestodeno, norelgestromina, norgestimato o nomegestrol combinados con un estrógeno (etinilestradiol o estradiol) se debía restringir y/o se debían tomar otras medidas reguladoras. El PRAC revisó todos los datos disponibles procedentes de estudios clínicos, estudios farmacoepidemiológicos, bibliografía publicada, experiencia posterior a la comercialización, incluidas las respuestas presentadas por los titulares de la autorización de comercialización (TAC) tanto por escrito como mediante explicaciones orales, así como los puntos de vista de una reunión de expertos ad hoc sobre la eficacia y la seguridad de los AHC, en especial en lo relacionado con el riesgo de tromboembolia. Los acontecimientos tromboembólicos son acontecimientos adversos que se suelen producir en una vena de la pierna (trombosis venosa profunda, TVP). Cuando no se hace un diagnóstico y no se inicia un tratamiento o cuando no se pueden identificar síntomas claros de trombosis, el coágulo se puede desplazar hacia arriba y llegar a los pulmones (embolia pulmonar, EP) o al cerebro (embolia cerebral, EC). Es posible que se realicen diagnósticos erróneos ya que la TE cursa con síntomas difusos y es un acontecimiento raro en la población de mujeres jóvenes sanas. En general, los acontecimientos tromboembólicos venosos (TEV) pueden ser mortales en el 1-2 % de los casos. Entre los factores de riesgo conocidos de TEV se incluyen antecedentes de TEV, embarazo, traumatismo, cirugía, inmovilización (p. ej., después de una intervención quirúrgica o tras un vuelo largo), obesidad y tabaquismo (es decir, todas las situaciones de un estado protrombótico). Además, ciertos defectos trombofílicos hereditarios aumentan el riesgo. Por consiguiente, en la información sobre el producto de estos medicamentos se recomienda comprobar los antecedentes personales y familiares de TEV antes de prescribir AHC. En muchos estudios se ha evaluado el riesgo de TEV y sus complicaciones (trombosis venosa profunda, embolia pulmonar) entre usuarias de diferentes AHC. La revisión actual ha confirmado la información anterior de que el nivel de riesgo de TEV con los AHC que contienen dosis bajas de etinilestradiol (etinilestradiol <50 µg) es pequeño, pero sí se observaron diferencias en este riesgo entre la mayoría de los productos según el tipo de progestágeno que contienen. Basándose en todos los datos disponibles, el PRAC concluyó que el riesgo de TEV es diferente según el medicamento, siendo los de menos riesgo aquellos que contienen los progestágenos levonorgestrel, noretisterona y norgestimato. Actualmente no se dispone de suficientes datos de algunos medicamentos (esto es, clormadinona, 290
3 dienogest, nomegestrol) para establecer el riesgo en comparación con los medicamentos de menor riesgo. En el caso de la clormadinona, esta cuestión se investigará mediante un estudio de seguridad posterior a la autorización, que se tratará más adelante en este documento. Con respecto al dienogest y al nomegestrol actualmente se están realizando estudios y los resultados se presentarán en cuanto estén disponibles. El riesgo de TEV con los AHC difiere de un medicamento a otro según el tipo de progestágeno que contengan. Tras evaluar todos los datos disponibles, el PRAC concluyó que: la incidencia estimada del riesgo es menor con los AHC que contienen los progestágenos levonorgestrel, norgestimato y noretisterona: se ha estimado que cada año se producen entre 5 y 7 casos de TEV por cada mujeres que emplean estos medicamentos, la incidencia estimada del riesgo es mayor con los progestágenos etonogestrel y norelgestromina, de 6 y 12 casos anuales por cada mujeres, la incidencia estimada del riesgo también es mayor con los progestágenos gestodeno, desogestrel, drospirenona, de 9 y 12 casos anuales por cada mujeres, para los AHC que contienen clormadinona, dienogest y nomegestrol, los datos disponibles no bastan para conocer el riesgo y compararlo con el de los otros AHC. A efectos comparativos, en mujeres no usuarias de AHC y que no están embarazadas se producen aproximadamente 2 casos de TEV anuales por cada mujeres. Se ha demostrado que el riesgo de TEV es mayor durante el primer año de uso de los anticonceptivos hormonales o cuando se reanuda su ingesta tras un periodo sin usarlos de al menos un mes (Dinger et al,. 2007, Sidney et al., 2013). Después de un riesgo inicial mayor durante el primer año de uso, este disminuye a un nivel menor constante. Asimismo, el riesgo de TEV es mayor en presencia de factores de riesgo intrínsecos. Considerando que los factores de riesgo de TEV cambian con el tiempo, el PRAC observó que el riesgo de cada persona se debe reevaluar periódicamente. Se sabe que el riesgo de tromboembolia arterial (TEA) (infarto de miocardio, accidente cerebrovascular) también aumenta con el uso de ACH, aunque no se dispone de pruebas de la existencia de diferencias entre los AHC en su riesgo relativo de TEA. Por consiguiente, según las pruebas disponibles, el PRAC reconoció que los beneficios asociados al uso de AHC son mucho mayores que el riesgo de acontecimientos adversos graves en la mayoría de las mujeres. No se ha evidenciado la existencia de diferencias entre estos medicamentos en cuanto a los efectos beneficiosos. No obstante, el PRAC recomendó establecer medidas de minimización de riesgo de rutina, como reforzar el texto de la información sobre el producto para reflejar los conocimientos actuales sobre los riesgos (tasa de incidencia), así como los síntomas de TEV y TEA, y aclarar las situaciones para las que estos medicamentos están contraindicados. En concreto, estos medicamentos deben estar contraindicados en pacientes con múltiples factores de riesgo, en pacientes sometidas a una intervención quirúrgica mayor con inmovilización prolongada, en pacientes que fuman y en pacientes con antecedentes o predisposición hereditaria a sufrir tromboembolias. Además, se recomendó proporcionar información con diligencia para comunicar el resultado de esta revisión y para destacar el riesgo de acontecimientos tromboembólicos mediante una comunicación directa a los profesionales sanitarios (DHPC). Además, el PRAC solicitó un estudio de seguridad posterior a la autorización con el fin de caracterizar mejor el riesgo relativo de acontecimientos tromboembólicos producidos por la clormadinona en comparación con los medicamentos que contienen levonorgestrel. Relación riesgo/beneficio 291
4 Habiendo considerado todo lo anterior, el PRAC concluyó que la relación riesgo/beneficio de los medicamentos identificados en el Anexo I en la indicación de anticoncepción sigue siendo favorable, supeditada a la inclusión en la información sobre el producto de las restricciones, advertencias y otros cambios acordados. Además, los titulares de la autorización de comercialización de la clormadinona deben realizar un estudio de seguridad posterior a la autorización. Motivos para la modificación de las condiciones de las autorizaciones de comercialización Considerando que: el PRAC examinó el procedimiento conforme al artículo 31 de la Directiva 2001/83/CE sobre medicamentos que contienen anticonceptivos hormonales combinados. el PRAC revisó todos los datos disponibles procedentes de estudios clínicos, estudios farmacoepidemiológicos, bibliografía publicada, experiencia posterior a la comercialización, incluidas las respuestas presentadas por los titulares de la autorización de comercialización (TAC), tanto por escrito como mediante explicaciones orales, sobre la eficacia y la seguridad de los medicamentos que contienen anticonceptivos hormonales combinados, en especial en lo relacionado con el riesgo de tromboembolia. El PRAC confirmó el riesgo conocido de tromboembolia de los medicamentos que contienen anticonceptivos hormonales combinados y recomendó que se indicaran con claridad en el etiquetado los síntomas de acontecimientos tromboembólicos, así como los factores de riesgo de los acontecimientos tromboembólicos. el PRAC consideró que, a la luz de los datos de seguridad disponibles actualmente, la relación riesgo/beneficio de los anticonceptivos hormonales combinados es favorable, supeditada a las restricciones, advertencias y otras modificaciones en la información sobre el producto. En concreto, estos medicamentos deben estar contraindicados en pacientes con múltiples factores de riesgo (sobrepeso, tabaquismo, hipertensión, edad avanzada, etc.), en pacientes sometidas a una intervención quirúrgica mayor con inmovilización prolongada y en pacientes con antecedentes o predisposición hereditaria a sufrir trombosis venosa. Otras modificaciones en la información sobre el producto contribuirán a informar mejor a los profesionales sanitarios y a las mujeres en riesgo de tromboembolia. el PRAC opina que los beneficios de los medicamentos que contienen anticonceptivos hormonales combinados siguen siendo mayores que los riesgos en la indicación de anticoncepción. el PRAC consideró necesarios más datos sobre los anticonceptivos hormonales combinados que contienen clormadinona e impuso la realización de un estudio de seguridad posterior a la autorización (PASS) para evaluar el riesgo relativo de acontecimientos tromboembólicos debidos a estos medicamentos en comparación con los anticonceptivos que contienen levonorgestrel. Como consecuencia, el PRAC concluyó que la relación riesgo/beneficio de los medicamentos identificados en el Anexo I en la indicación de anticoncepción sigue siendo favorable, supeditada a las condiciones, restricciones, advertencias y otros cambios acordados en la información sobre el producto y a medidas de minimización del riesgo adicionales. 292
5 2 Explicación pormenorizada de las diferencias con respecto a la recomendación del PRAC Después de revisar la recomendación del PRAC, el CHMP aceptó las conclusiones científicas generales y los motivos de la recomendación. Sin embargo, el CHMP consideró necesario modificar la sección Fertilidad, embarazo y lactancia del RCP de modo que refleje el incremento del riesgo de TEV en el periodo posparto para garantizar la consistencia de la sección sobre advertencias del RCP. Por consiguiente, en la sección Embarazo del RCP se insertó la siguiente frase: «Se debe tener en cuenta el incremento de riesgo de TEV durante el periodo posparto a la hora de reanudar [denominación de fantasía] (ver secciones 4.2 y 4.4.).» No se consideraron necesarias más modificaciones. Dictamen del CHMP El CHMP, después de considerar la recomendación del PRAC de fecha 10 de octubre de 2013 de conformidad con lo dispuesto en la Directiva 2001/83/CE, artículo 107 duodecies, apartado 3, adoptó la posición de que deben modificarse las autorizaciones de comercialización de los anticonceptivos hormonales combinados que contienen clormadinona, desogestrel, dienogest, drospirenona, etonogestrel, gestodeno, norgestimato. Las modificaciones en las secciones pertinentes del Resumen de las Características del Producto y el prospecto se indican en el Anexo III. Las autorizaciones de comercialización para los anticonceptivos hormonales combinados que contienen clormadinona están sujetas a las condiciones indicadas en el Anexo IV. 293
Anexo II. Conclusiones científicas y motivos para la modificación de los términos de las autorizaciones de comercialización
 Anexo II Conclusiones científicas y motivos para la modificación de los términos de las autorizaciones de comercialización 12 Conclusiones científicas y motivos para la modificación de los términos de
Anexo II Conclusiones científicas y motivos para la modificación de los términos de las autorizaciones de comercialización 12 Conclusiones científicas y motivos para la modificación de los términos de
Anexo IV. Conclusiones científicas y motivos para la modificación de las condiciones de las autorizaciones de comercialización
 Anexo IV Conclusiones científicas y motivos para la modificación de las condiciones de las autorizaciones de comercialización 267 Conclusiones científicas El CHMP estudió la siguiente recomendación del
Anexo IV Conclusiones científicas y motivos para la modificación de las condiciones de las autorizaciones de comercialización 267 Conclusiones científicas El CHMP estudió la siguiente recomendación del
Recomendaciones para minimizar el riesgo de tromboembolismo asociado a anticonceptivos hormonales combinados.
 Esta sección proporciona herramientas para los profesionales que se desempeñan en farmacia comunitaria y que requieren de información actualizada sobre temas de su interés. En esta edición, entregaremos
Esta sección proporciona herramientas para los profesionales que se desempeñan en farmacia comunitaria y que requieren de información actualizada sobre temas de su interés. En esta edición, entregaremos
Anexo II. Conclusiones científicas y motivos para el dictamen positivo presentados por la Agencia Europea de Medicamentos
 Anexo II Conclusiones científicas y motivos para el dictamen positivo presentados por la Agencia Europea de Medicamentos 4 Conclusiones científicas Resumen general de la evaluación científica de Seasonique
Anexo II Conclusiones científicas y motivos para el dictamen positivo presentados por la Agencia Europea de Medicamentos 4 Conclusiones científicas Resumen general de la evaluación científica de Seasonique
Anexo I. Conclusiones científicas y motivos para la modificación de las condiciones de la(s) autorización(es) de comercialización.
 Anexo I Conclusiones científicas y motivos para la modificación de las condiciones de la(s) autorización(es) de comercialización. Conclusiones científicas Teniendo en cuenta lo dispuesto en el Informe
Anexo I Conclusiones científicas y motivos para la modificación de las condiciones de la(s) autorización(es) de comercialización. Conclusiones científicas Teniendo en cuenta lo dispuesto en el Informe
Anticoncepción en mujeres con antecedentes de tromboembolismo venoso
 Anticoncepción en mujeres con antecedentes de tromboembolismo venoso Asesoramiento para las mujeres con antecedentes de tromboembolismo venoso que requieren anticonceptivos o terapia de reemplazo hormonal.
Anticoncepción en mujeres con antecedentes de tromboembolismo venoso Asesoramiento para las mujeres con antecedentes de tromboembolismo venoso que requieren anticonceptivos o terapia de reemplazo hormonal.
Día Mundial de la Trombosis DÍA MUNDIAL DE LA TROMBOSIS 13 DE OCTUBRE
 Día Mundial de la Trombosis Qué es la Trombosis? La TROMBOSIS es un coágulo sanguíneo que se forma en las arterias o venas y bloquea la llegada de sangre y oxígeno. Constituye el principal factor responsable
Día Mundial de la Trombosis Qué es la Trombosis? La TROMBOSIS es un coágulo sanguíneo que se forma en las arterias o venas y bloquea la llegada de sangre y oxígeno. Constituye el principal factor responsable
Anexo II. Conclusiones científicas y motivos para la modificación de las condiciones de las autorizaciones de comercialización sujeta a condiciones
 Anexo II Conclusiones científicas y motivos para la modificación de las condiciones de las autorizaciones de comercialización sujeta a condiciones 24 Conclusiones científicas y motivos para la modificación
Anexo II Conclusiones científicas y motivos para la modificación de las condiciones de las autorizaciones de comercialización sujeta a condiciones 24 Conclusiones científicas y motivos para la modificación
Historia Clínica Antecedentes Familiares
 Historia Clínica Antecedentes Familiares Diabetes Cáncer Hipertensión arterial Trombosis venosa Infarto agudo de miocardio Tromboembolismo pulmonar Otros antecedentes Cardiovasculares Historia Clínica
Historia Clínica Antecedentes Familiares Diabetes Cáncer Hipertensión arterial Trombosis venosa Infarto agudo de miocardio Tromboembolismo pulmonar Otros antecedentes Cardiovasculares Historia Clínica
INN Nombre inventado Concentración Forma farmacéutica. Caustinerf Arsenical
 Estado Miembro (en EEA) Autorización de Comercialización Titular INN Nombre inventado Concentración Forma farmacéutica Vía de administración Lituania Septodont 58, rue du Pont de Creteil clorhidrato de
Estado Miembro (en EEA) Autorización de Comercialización Titular INN Nombre inventado Concentración Forma farmacéutica Vía de administración Lituania Septodont 58, rue du Pont de Creteil clorhidrato de
Anexo I. Conclusiones científicas y motivos para la modificación de las condiciones de la(s) autorización(es) de comercialización
 Anexo I Conclusiones científicas y motivos para la modificación de las condiciones de la(s) autorización(es) de comercialización 1 Conclusiones científicas Teniendo en cuenta lo dispuesto en el Informe
Anexo I Conclusiones científicas y motivos para la modificación de las condiciones de la(s) autorización(es) de comercialización 1 Conclusiones científicas Teniendo en cuenta lo dispuesto en el Informe
MANEJO DEL TRATAMIENTO ANTICOAGULANTE ORAL (TACO) EN PACIENTES HOSPITALIZADOS en Hospital Dr. Rafael Avaria Valenzuela de Curanilahue
 JUNIO 21 MANEJO DEL TRATAMIENTO ANTICOAGULANTE ORAL (TACO) EN PACIENTES HOSPITALIZADOS en Hospital Dr. Rafael Avaria Valenzuela de Curanilahue Resolución N : O99O DEL 24/06/21 Página 1 de 13 JUNIO 21 Indice
JUNIO 21 MANEJO DEL TRATAMIENTO ANTICOAGULANTE ORAL (TACO) EN PACIENTES HOSPITALIZADOS en Hospital Dr. Rafael Avaria Valenzuela de Curanilahue Resolución N : O99O DEL 24/06/21 Página 1 de 13 JUNIO 21 Indice
COMUNICACIÓN DIRIGIDA A PROFESIONALES SANITARIOS
 COMUNICACIÓN DIRIGIDA A PROFESIONALES SANITARIOS Actualización de la indicación, contraindicaciones y advertencias de los medicamentos que contienen acetato de ciproterona 2 mg /etinilestradiol 35 mcg
COMUNICACIÓN DIRIGIDA A PROFESIONALES SANITARIOS Actualización de la indicación, contraindicaciones y advertencias de los medicamentos que contienen acetato de ciproterona 2 mg /etinilestradiol 35 mcg
Anexo III. Modificaciones a las secciones relevantes de la ficha técnica o resumen de las características del producto y los prospectos
 Anexo III Modificaciones a las secciones relevantes de la ficha técnica o resumen de las características del producto y los prospectos Nota: Estas modificaciones a las secciones relevantes de la Ficha
Anexo III Modificaciones a las secciones relevantes de la ficha técnica o resumen de las características del producto y los prospectos Nota: Estas modificaciones a las secciones relevantes de la Ficha
FARMACOVIGILANCIA PRESCRIPCIÓN RAZONADA DE MEDICAMENTOS. Esther Salgueiro 10, 17 de Marzo de 2015
 FARMACOVIGILANCIA PRESCRIPCIÓN RAZONADA DE MEDICAMENTOS 10, 17 de Marzo de 2015 Esther Salgueiro (salgueiroesther@uniovi.es) FASES DEL DESARROLLO DE MEDICAMENTOS ENSAYO CLÍNICO CONTROLADO/ PRÁCTICA CLÍNICA
FARMACOVIGILANCIA PRESCRIPCIÓN RAZONADA DE MEDICAMENTOS 10, 17 de Marzo de 2015 Esther Salgueiro (salgueiroesther@uniovi.es) FASES DEL DESARROLLO DE MEDICAMENTOS ENSAYO CLÍNICO CONTROLADO/ PRÁCTICA CLÍNICA
ANEXO CONDICIONES O RESTRICCIONES A IMPLEMENTAR EN LOS ESTADOS MIEMBROS EN RELACIÓN CON LA UTILIZACIÓN SEGURA Y EFICAZ DEL MEDICAMENTO
 ANEXO CONDICIONES O RESTRICCIONES A IMPLEMENTAR EN LOS ESTADOS MIEMBROS EN RELACIÓN CON LA UTILIZACIÓN SEGURA Y EFICAZ DEL MEDICAMENTO CONDICIONES O RESTRICCIONES A IMPLEMENTAR EN LOS ESTADOS MIEMBROS
ANEXO CONDICIONES O RESTRICCIONES A IMPLEMENTAR EN LOS ESTADOS MIEMBROS EN RELACIÓN CON LA UTILIZACIÓN SEGURA Y EFICAZ DEL MEDICAMENTO CONDICIONES O RESTRICCIONES A IMPLEMENTAR EN LOS ESTADOS MIEMBROS
11 Número de publicación: Int. Cl. 7 : A61K 31/ Inventor/es: Grubb, Gary, S. 74 Agente: Curell Suñol, Marcelino
 19 OFICINA ESPAÑOLA DE PATENTES Y MARCAS ESPAÑA 11 Número de publicación: 2 236 243 1 Int. Cl. 7 : A61K 31/00 12 TRADUCCIÓN DE PATENTE EUROPEA T3 86 Número de solicitud europea: 01941933.2 86 Fecha de
19 OFICINA ESPAÑOLA DE PATENTES Y MARCAS ESPAÑA 11 Número de publicación: 2 236 243 1 Int. Cl. 7 : A61K 31/00 12 TRADUCCIÓN DE PATENTE EUROPEA T3 86 Número de solicitud europea: 01941933.2 86 Fecha de
PROTOCOLO DE ACTUACIÓN EN URGENCIAS ANTE LA SOSPECHA DE TROMBOEMBOLISMO PULMONAR (TEP)
 Página 1 de 7 PROTOCOLO DE ACTUACIÓN EN URGENCIAS ANTE LA SOSPECHA DE Página 2 de 7 El tromboembolismo pulmonar es el resultado de la obstrucción de la circulación arterial pulmonar por un émbolo procedente,
Página 1 de 7 PROTOCOLO DE ACTUACIÓN EN URGENCIAS ANTE LA SOSPECHA DE Página 2 de 7 El tromboembolismo pulmonar es el resultado de la obstrucción de la circulación arterial pulmonar por un émbolo procedente,
SOCIEDAD MEXICANA DE TROMBOSIS Y HEMOSTASIA INSTITUTO NACIONAL DE CARDIOLOGÍA IGNACIO CHÁVEZ
 SOCIEDAD MEXICANA DE TROMBOSIS Y HEMOSTASIA INSTITUTO NACIONAL DE CARDIOLOGÍA IGNACIO CHÁVEZ DÍA MUNDIAL CONTRA LA TROMBOSIS 13 de octubre de 2016 EVITE COÁGULOS EVITE LOS COÁGULOS MORTALES CONOZCA LOS
SOCIEDAD MEXICANA DE TROMBOSIS Y HEMOSTASIA INSTITUTO NACIONAL DE CARDIOLOGÍA IGNACIO CHÁVEZ DÍA MUNDIAL CONTRA LA TROMBOSIS 13 de octubre de 2016 EVITE COÁGULOS EVITE LOS COÁGULOS MORTALES CONOZCA LOS
FARMACOVIGILANCIA. Nota informativa de la AEMPS publicada con fecha 15 de enero de Ref: MUH (FV), 02/2013 y 03/2013
 FARMACOVIGILANCIA Notificación electrónica de sospechas de Reacciones Adversas a Medicamentos por parte de los profesionales sanitarios y los ciudadanos Nota informativa de la AEMPS publicada con fecha
FARMACOVIGILANCIA Notificación electrónica de sospechas de Reacciones Adversas a Medicamentos por parte de los profesionales sanitarios y los ciudadanos Nota informativa de la AEMPS publicada con fecha
El síndrome de anticuerpos antifosfolípidos
 El síndrome de anticuerpos antifosfolípidos El síndrome de anticuerpos antifosfolípidos afecta cinco veces más a mujeres que a hombres. El síndrome de anticuerpos antifosfolípidos (llamado por lo general
El síndrome de anticuerpos antifosfolípidos El síndrome de anticuerpos antifosfolípidos afecta cinco veces más a mujeres que a hombres. El síndrome de anticuerpos antifosfolípidos (llamado por lo general
Resumen general de la evaluación científica de los supositorios que contienen derivados terpénicos (ver Anexo I)
 ANEXO II CONCLUSIONES CIENTÍFICAS Y MOTIVOS DE LA REVOCACIÓN O MODIFICACIÓN DE LAS SECCIONES PERTINENTES DE LOS RESÚMENES DE LAS CARACTERÍSTICAS DEL PRODUCTO, ETIQUETADOS Y PROSPECTOS PRESENTADOS POR LA
ANEXO II CONCLUSIONES CIENTÍFICAS Y MOTIVOS DE LA REVOCACIÓN O MODIFICACIÓN DE LAS SECCIONES PERTINENTES DE LOS RESÚMENES DE LAS CARACTERÍSTICAS DEL PRODUCTO, ETIQUETADOS Y PROSPECTOS PRESENTADOS POR LA
POSICIONAMIENTO DE LA SEEP EN RELACIÓN A LOS BIOSIMILARES DE LA HORMONA DE CRECIMIENTO E INSULINAS.
 POSICIONAMIENTO DE LA SEEP EN RELACIÓN A LOS BIOSIMILARES DE LA HORMONA DE CRECIMIENTO E INSULINAS. Los fármacos biosimilares son fármacos biológicos aprobados por la Agencia Europea del Medicamento (EMA)
POSICIONAMIENTO DE LA SEEP EN RELACIÓN A LOS BIOSIMILARES DE LA HORMONA DE CRECIMIENTO E INSULINAS. Los fármacos biosimilares son fármacos biológicos aprobados por la Agencia Europea del Medicamento (EMA)
Anexo II. Conclusiones científicas
 Anexo II Conclusiones científicas 200 Conclusiones científicas Consiguientemente a la evaluación de un informe periódico de seguridad (IPS) sobre los medicamentos que contienen ambroxol, elaborado conforme
Anexo II Conclusiones científicas 200 Conclusiones científicas Consiguientemente a la evaluación de un informe periódico de seguridad (IPS) sobre los medicamentos que contienen ambroxol, elaborado conforme
51 Int. CI.: A61K 31/519 (2006.01) A61P 15/18 (2006.01) A61K 31/567 (2006.01) A61K 31/57 (2006.01) TRADUCCIÓN DE PATENTE EUROPEA.
 19 OFICINA ESPAÑOLA DE PATENTES Y MARCAS ESPAÑA 11 Número de publicación: 2 432 378 1 Int. CI.: A61K 31/19 (06.01) A61P 1/18 (06.01) A61K 31/67 (06.01) A61K 31/7 (06.01) 12 TRADUCCIÓN DE PATENTE EUROPEA
19 OFICINA ESPAÑOLA DE PATENTES Y MARCAS ESPAÑA 11 Número de publicación: 2 432 378 1 Int. CI.: A61K 31/19 (06.01) A61P 1/18 (06.01) A61K 31/67 (06.01) A61K 31/7 (06.01) 12 TRADUCCIÓN DE PATENTE EUROPEA
ANTICONCEPCIÓN HORMONAL COMBINADA
 ANTICONCEPCIÓN HORMONAL COMBINADA Soledad Díaz Instituto Chileno de Medicina Reproductiva 2014 ICMER CONTENIDO DE ESTA PRESENTACIÓN Descripción de los métodos hormonales combinados de uso regular. Evaluación
ANTICONCEPCIÓN HORMONAL COMBINADA Soledad Díaz Instituto Chileno de Medicina Reproductiva 2014 ICMER CONTENIDO DE ESTA PRESENTACIÓN Descripción de los métodos hormonales combinados de uso regular. Evaluación
Resumen general de la evaluación científica de los medicamentos que contienen nimesulida para uso sistémico (Ver Anexo I)
 Anexo II Conclusiones científicas y motivos de la modificación de los resúmenes de las características del producto y los prospectos presentados por la EMA 41 Conclusiones científicas Resumen general de
Anexo II Conclusiones científicas y motivos de la modificación de los resúmenes de las características del producto y los prospectos presentados por la EMA 41 Conclusiones científicas Resumen general de
PROGRAMA DE PREVENCIÓN DE EMBARAZOS DE ISOTRETINOÍNA
 GUÍA DEL FARMACÉUTICO PARA LA DISPENSACIÓN DE ISOTRETINOÍNA PROGRAMA DE PREVENCIÓN DE EMBARAZOS DE ISOTRETINOÍNA Información sobre prevención de riesgos autorizada por la Agencia Española de Medicamentos
GUÍA DEL FARMACÉUTICO PARA LA DISPENSACIÓN DE ISOTRETINOÍNA PROGRAMA DE PREVENCIÓN DE EMBARAZOS DE ISOTRETINOÍNA Información sobre prevención de riesgos autorizada por la Agencia Española de Medicamentos
ANEXO III MODIFICACIONES AL RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO Y AL PROSPECTO
 ANEXO III MODIFICACIONES AL RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO Y AL PROSPECTO Estas modificaciones del SPC (ficha técnica) y prospecto entran en vigor en el momento de la Decisión de la Comisión.
ANEXO III MODIFICACIONES AL RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO Y AL PROSPECTO Estas modificaciones del SPC (ficha técnica) y prospecto entran en vigor en el momento de la Decisión de la Comisión.
Comunicación dirigida a los profesionales sanitarios
 Comunicación dirigida a los profesionales sanitarios Metoclopramida (Primperan, Metoclopramida EFG): Actualización de indicaciones y posología para minimizar el riesgo de efectos adversos (principalmente
Comunicación dirigida a los profesionales sanitarios Metoclopramida (Primperan, Metoclopramida EFG): Actualización de indicaciones y posología para minimizar el riesgo de efectos adversos (principalmente
Recomendaciones del PRAC sobre las señales para la actualización de la información sobre el producto
 23 April 2015 EMA/PRAC/273926/2015 Pharmacovigilance Risk Assessment Committee Recomendaciones del PRAC sobre las señales para la actualización de la información sobre el producto Adoptado por el PRAC
23 April 2015 EMA/PRAC/273926/2015 Pharmacovigilance Risk Assessment Committee Recomendaciones del PRAC sobre las señales para la actualización de la información sobre el producto Adoptado por el PRAC
(Texto pertinente a efectos del EEE)
 L 119/4 Diario Oficial de la Unión Europea 7.5.2011 REGLAMENTO (UE) N o 440/2011 DE LA COMISIÓN de 6 de mayo de 2011 sobre la autorización y la denegación de autorización de determinadas declaraciones
L 119/4 Diario Oficial de la Unión Europea 7.5.2011 REGLAMENTO (UE) N o 440/2011 DE LA COMISIÓN de 6 de mayo de 2011 sobre la autorización y la denegación de autorización de determinadas declaraciones
ANTICONCEPCIÓN HORMONAL COMBINADA
 ANTICONCEPCIÓN HORMONAL COMBINADA Dra. Soledad Díaz, Dr. Octavio Peralta Instituto Chileno de Medicina Reproductiva 2016 ICMER CONTENIDO DE ESTA PRESENTACIÓN Descripción de los métodos hormonales combinados
ANTICONCEPCIÓN HORMONAL COMBINADA Dra. Soledad Díaz, Dr. Octavio Peralta Instituto Chileno de Medicina Reproductiva 2016 ICMER CONTENIDO DE ESTA PRESENTACIÓN Descripción de los métodos hormonales combinados
Anexo II. Conclusiones científicas y motivos para la denegación presentados por la Agencia Europea de Medicamentos
 Anexo II Conclusiones científicas y motivos para la denegación presentados por la Agencia Europea de Medicamentos 5 Conclusiones científicas Resumen general de la evaluación científica de Etinilestradiol-Drospirenona
Anexo II Conclusiones científicas y motivos para la denegación presentados por la Agencia Europea de Medicamentos 5 Conclusiones científicas Resumen general de la evaluación científica de Etinilestradiol-Drospirenona
Forma farmacéutica. Estado miembro. Vía de administración. Concentra ción. Especie de destino. Solicitante Nombre Sustancia activa
 Anexo I Relación de los nombres, formas farmacéuticas y dosis de los medicamentos veterinarios, y de las especies animales, vías de y solicitantes en los estados miembros 1/9 Estado miembro Solicitante
Anexo I Relación de los nombres, formas farmacéuticas y dosis de los medicamentos veterinarios, y de las especies animales, vías de y solicitantes en los estados miembros 1/9 Estado miembro Solicitante
LEFLUNOMIDA. Información sobre seguridad para los profesionales sanitarios
 LEFLUNOMIDA Información sobre seguridad para los profesionales sanitarios Leflunomida es un fármaco antirreumático modificador de la enfermedad" (FARME) indicado para el tratamiento de pacientes adultos
LEFLUNOMIDA Información sobre seguridad para los profesionales sanitarios Leflunomida es un fármaco antirreumático modificador de la enfermedad" (FARME) indicado para el tratamiento de pacientes adultos
1. Enfermedad tromboembólica venosa (ETEV) en paciente anciano y/o insuficiencia renal crónica (IRC)
 1. Enfermedad tromboembólica venosa (ETEV) en paciente anciano y/o insuficiencia renal crónica (IRC) Escasez de estudios clínicos aleatorizados. Tanto la insuficiencia renal (IR) como el bajo peso y la
1. Enfermedad tromboembólica venosa (ETEV) en paciente anciano y/o insuficiencia renal crónica (IRC) Escasez de estudios clínicos aleatorizados. Tanto la insuficiencia renal (IR) como el bajo peso y la
Etiologia. La trombosis venosa se define como la presencia de un trombo o coágulo de sangre en una vena, sea cual sea su localización.
 TROMBOSIS VENOSA Universidad Abierta Interamericana Facultad de Medicina Carrera Licenciatura en Enfermería Materia: Ciencias Biológicas IV Prof.: Alejandro Vázquez Alumno: Miranda Lino Etiologia La trombosis
TROMBOSIS VENOSA Universidad Abierta Interamericana Facultad de Medicina Carrera Licenciatura en Enfermería Materia: Ciencias Biológicas IV Prof.: Alejandro Vázquez Alumno: Miranda Lino Etiologia La trombosis
CUESTIONARIO PREVIO DE LA PRACTICA No.6 EFECTOS TERAPEUTICOS Y ADVERSOS PRODUCIDOS DE LOS ANTICONCEPTIVOS " Profesoras : Semestre:
 UNIVERSIDAD NACIONAL AUTÓNOMA DE MÉXICO FACULTAD DE ESTUDIOS SUPERIORES CUAUTITLÁN DEPARTAMENO DE CIENCIAS BIOLÓGICAS SECCIÓN BIOQUIMICA Y FARMACOLOGIA HUMANA LABORATORIO DE FARMACOLOGIA ESPECIAL CUESTIONARIO
UNIVERSIDAD NACIONAL AUTÓNOMA DE MÉXICO FACULTAD DE ESTUDIOS SUPERIORES CUAUTITLÁN DEPARTAMENO DE CIENCIAS BIOLÓGICAS SECCIÓN BIOQUIMICA Y FARMACOLOGIA HUMANA LABORATORIO DE FARMACOLOGIA ESPECIAL CUESTIONARIO
CONSEJO DE LA UNIÓN EUROPEA. Bruselas, 25 de enero de 2011 (25.01) (OR. en) 5610/11 DENLEG 7
 CONSEJO DE LA UNIÓN EUROPEA Bruselas, 25 de enero de 2011 (25.01) (OR. en) 5610/11 DENLEG 7 NOTA DE TRANSMISIÓN Emisor: Comisión Europea Fecha de recepción: 21 de enero de 2011 Destinatario: Secretaría
CONSEJO DE LA UNIÓN EUROPEA Bruselas, 25 de enero de 2011 (25.01) (OR. en) 5610/11 DENLEG 7 NOTA DE TRANSMISIÓN Emisor: Comisión Europea Fecha de recepción: 21 de enero de 2011 Destinatario: Secretaría
EL EMBOLISMO PULMONAR EN LAS MUJERES QUE USAN ANTICONCEPTIVOS HORMONALES
 EL EMBOLISMO PULMONAR EN LAS MUJERES QUE USAN ANTICONCEPTIVOS HORMONALES ANTICONCEPTIVOS HORMONALES (ACO) Vía a oral: Etinilestradiol 20, 25, 30 mcgr + Progestágenos genos de 2ª 2 generación n (levonorgestrel(
EL EMBOLISMO PULMONAR EN LAS MUJERES QUE USAN ANTICONCEPTIVOS HORMONALES ANTICONCEPTIVOS HORMONALES (ACO) Vía a oral: Etinilestradiol 20, 25, 30 mcgr + Progestágenos genos de 2ª 2 generación n (levonorgestrel(
CONSENTIMIENTO INFORMADO PARA REPARACION DE FISTULA ARTERIO-VENOSA / PRÓTESIS VASCULAR 1.- IDENTIFICACIÓN DEL PACIENTE/ REPRESENTANTE LEGAL
 CONSENTIMIENTO INFORMADO PARA REPARACION DE FISTULA ARTERIO-VENOSA / PRÓTESIS VASCULAR 1.- IDENTIFICACIÓN DEL PACIENTE/ REPRESENTANTE LEGAL Don(ña) Nombre:...Apellidos de.años, Rut N. Don /Doña Nombre:...
CONSENTIMIENTO INFORMADO PARA REPARACION DE FISTULA ARTERIO-VENOSA / PRÓTESIS VASCULAR 1.- IDENTIFICACIÓN DEL PACIENTE/ REPRESENTANTE LEGAL Don(ña) Nombre:...Apellidos de.años, Rut N. Don /Doña Nombre:...
Definición TROMBOEMBOLIA PULMONAR. Epidemiología. >40 años >riesgo y se duplica con cada década posterior.
 Definición? TROMBOEMBOLIA PULMONAR Evelyn Aldana RII Medicina Interna Epidemiología Es la tercera enfermedad cardiovascular mas frecuente, incidencia anual global 100-200/100000 habitantes. Se estima que
Definición? TROMBOEMBOLIA PULMONAR Evelyn Aldana RII Medicina Interna Epidemiología Es la tercera enfermedad cardiovascular mas frecuente, incidencia anual global 100-200/100000 habitantes. Se estima que
PROTOCOLO ANTICONCEPCIÓN HORMONAL
 Torrelavega, marzo 2013 PROTOCOLO ANTICONCEPCIÓN HORMONAL CONSEJO CONTRACEPTIVO Objetivos: Proporcionar información sobre los diferentes métodos o Mecanismo de acción o Eficacia o Duración o Reversibilidad
Torrelavega, marzo 2013 PROTOCOLO ANTICONCEPCIÓN HORMONAL CONSEJO CONTRACEPTIVO Objetivos: Proporcionar información sobre los diferentes métodos o Mecanismo de acción o Eficacia o Duración o Reversibilidad
Forma farmacéutica Vía de administración. Contenido (Concentración) Estado miembro. Nombre. Dinamarca. Vantas 50 mg Implante Subcutánea 50 mg
 ANEXO I RELACIÓN DE LOS NOMBRES DEL MEDICAMENTO, FORMA FARMACÉUTICA, DOSIS, VÍA DE ADMINISTRACIÓN, SOLICITANTE, TITULAR DE LA AUTORIZACIÓN DE COMERCIALIZACIÓN EN LOS ESTADOS MIEMBROS Estado miembro Dinamarca
ANEXO I RELACIÓN DE LOS NOMBRES DEL MEDICAMENTO, FORMA FARMACÉUTICA, DOSIS, VÍA DE ADMINISTRACIÓN, SOLICITANTE, TITULAR DE LA AUTORIZACIÓN DE COMERCIALIZACIÓN EN LOS ESTADOS MIEMBROS Estado miembro Dinamarca
Anticoncepción en la mujer diabética
 Anticoncepción en la mujer diabética XIII Congreso Latinoamericano de Diabetes (ALAD-007) al 6 de Noviembre 007 Dr. Felipe Santana Pérez, MSc Instituto Nacional de Endocrinología, La Habana, Cuba. Por
Anticoncepción en la mujer diabética XIII Congreso Latinoamericano de Diabetes (ALAD-007) al 6 de Noviembre 007 Dr. Felipe Santana Pérez, MSc Instituto Nacional de Endocrinología, La Habana, Cuba. Por
ANTICONCEPCIÓN HORMONAL COMBINADA. Historia. Historia
 MÓDULO 2: ASPECTOS TEÓRICOS DE LOS MÉTODOS ANTICONCEPTIVOS ANTICONCEPCIÓN HORMONAL COMBINADA Dra. Mª Jesús Alonso Llamazares Todos los contenidos de este curso (diapositivas, material docente, página web,
MÓDULO 2: ASPECTOS TEÓRICOS DE LOS MÉTODOS ANTICONCEPTIVOS ANTICONCEPCIÓN HORMONAL COMBINADA Dra. Mª Jesús Alonso Llamazares Todos los contenidos de este curso (diapositivas, material docente, página web,
EVRA Parche transdérmico de norelgestromin/etinilestradiol
 EVRA Parche transdérmico de norelgestromin/etinilestradiol Industria alemana Venta bajo receta FÓRMULA CUALITATIVA Y CUANTITATIVA Cada parche transdérmico de 20 cm 2 contiene 6 mg de norelgestromin (NGMN)
EVRA Parche transdérmico de norelgestromin/etinilestradiol Industria alemana Venta bajo receta FÓRMULA CUALITATIVA Y CUANTITATIVA Cada parche transdérmico de 20 cm 2 contiene 6 mg de norelgestromin (NGMN)
el nuevo marco normativo para la realización de ensayos clínicos
 el nuevo marco normativo para la realización de ensayos clínicos (con medicamentos) César Hernández García Jefe Departamento Medicamentos de Uso Humano Agencia Española de Medicamentos y Productos Sanitarios.
el nuevo marco normativo para la realización de ensayos clínicos (con medicamentos) César Hernández García Jefe Departamento Medicamentos de Uso Humano Agencia Española de Medicamentos y Productos Sanitarios.
ENFERMEDAD TROMBOEMBÓLICA VENOSA EN EL EMBARAZO Y EL PUERPERIO
 ENFERMEDAD TROMBOEMBÓLICA VENOSA EN EL EMBARAZO Y EL PUERPERIO Milagros Cruz Martínez UGC Obstetricia y Ginecología. Hospital Universitario San Cecilio. Granada INTRODUCCIÓN La enfermedad tromboembólica
ENFERMEDAD TROMBOEMBÓLICA VENOSA EN EL EMBARAZO Y EL PUERPERIO Milagros Cruz Martínez UGC Obstetricia y Ginecología. Hospital Universitario San Cecilio. Granada INTRODUCCIÓN La enfermedad tromboembólica
METODOLOGÍA ANTECEDENTES
 Dictamen de la Segunda Comisión de Trabajo, el que DICTAMEN DE LA SEGUNDA COMISIÓN DE TRABAJO, EL QUE CONTIENE PUNTO DE ACUERDO QUE EXHORTA A LA SECRETARÍA DE SALUD PARA QUE, EN COORDINACIÓN CON SUS HOMÓLOGAS
Dictamen de la Segunda Comisión de Trabajo, el que DICTAMEN DE LA SEGUNDA COMISIÓN DE TRABAJO, EL QUE CONTIENE PUNTO DE ACUERDO QUE EXHORTA A LA SECRETARÍA DE SALUD PARA QUE, EN COORDINACIÓN CON SUS HOMÓLOGAS
TROMBOEMBOLISMO PULMONAR
 TROMBOEMBOLISMO PULMONAR AHOGAMIENTO INCOMPLETO Concepto: El troemboembolismo pulmonar se puede conceptuar como la expresión clínica del enclavamiento de un trombo hemático en el árbol pulmonar. Es la
TROMBOEMBOLISMO PULMONAR AHOGAMIENTO INCOMPLETO Concepto: El troemboembolismo pulmonar se puede conceptuar como la expresión clínica del enclavamiento de un trombo hemático en el árbol pulmonar. Es la
SOCIEDAD MEXICANA DE TROMBOSIS Y HEMOSTASIA INSTITUTO NACIONAL DE CARDIOLOGÍA IGNACIO CHÁVEZ
 SOCIEDAD MEXICANA DE TROMBOSIS Y HEMOSTASIA INSTITUTO NACIONAL DE CARDIOLOGÍA IGNACIO CHÁVEZ DÍA MUNDIAL CONTRA LA TROMBOSIS 13 de octubre de 2016 EVITE COÁGULOS LA TROMBOSIS COMO PRIORIDAD A NIVEL MUNDIAL
SOCIEDAD MEXICANA DE TROMBOSIS Y HEMOSTASIA INSTITUTO NACIONAL DE CARDIOLOGÍA IGNACIO CHÁVEZ DÍA MUNDIAL CONTRA LA TROMBOSIS 13 de octubre de 2016 EVITE COÁGULOS LA TROMBOSIS COMO PRIORIDAD A NIVEL MUNDIAL
Información importante para el profesional sanitario sobre el tratamiento con LADEVINA
 Información importante para el profesional sanitario sobre el tratamiento con LADEVINA INTRODUCCION LADEVINA es un fármaco inmunomodulador. Estudios clínicos fase III, mostraron que en pacientes pretratados
Información importante para el profesional sanitario sobre el tratamiento con LADEVINA INTRODUCCION LADEVINA es un fármaco inmunomodulador. Estudios clínicos fase III, mostraron que en pacientes pretratados
Anticoncepción de emergencia. Nota descriptiva N 244 Febrero de 2016
 Nota descriptiva N 244 Febrero de 2016 Datos y cifras La anticoncepción de emergencia puede prevenir la mayoría de los embarazos cuando se usa después de una relación sexual. Se puede recurrir a la anticoncepción
Nota descriptiva N 244 Febrero de 2016 Datos y cifras La anticoncepción de emergencia puede prevenir la mayoría de los embarazos cuando se usa después de una relación sexual. Se puede recurrir a la anticoncepción
Enfermedades Cardiovasculares y Salud del Corazón
 Enfermedades Cardiovasculares y Salud del Corazón Qué son enfermedades cardiovasculares? Las Enfermedades Cardiovasculares(ECVs) son un grupo de desordenes en el corazón y los vasos sanguíneos que incluyen
Enfermedades Cardiovasculares y Salud del Corazón Qué son enfermedades cardiovasculares? Las Enfermedades Cardiovasculares(ECVs) son un grupo de desordenes en el corazón y los vasos sanguíneos que incluyen
Enfermedad Tromboembólica: Estudio de Trombofilia Cuándo y a Quién?
 Dr. Mauricio Duhalde N. Hematólogo. Jefe Servicio Banco de Sangre. Clínica Las Condes. Trombofilia puede ser definida como una anormalidad heredada o adquirida de la hemostasia que predispone a trombosis.
Dr. Mauricio Duhalde N. Hematólogo. Jefe Servicio Banco de Sangre. Clínica Las Condes. Trombofilia puede ser definida como una anormalidad heredada o adquirida de la hemostasia que predispone a trombosis.
PROSPECTO: INFORMACIÓN PARA EL USUARIO. CITICOLINA Normon 1000 mg solución inyectable EFG
 PROSPECTO: INFORMACIÓN PARA EL USUARIO CITICOLINA Normon 1000 mg solución inyectable EFG Lea todo el prospecto detenidamente antes de empezar a tomar el medicamento, porque contiene información importante
PROSPECTO: INFORMACIÓN PARA EL USUARIO CITICOLINA Normon 1000 mg solución inyectable EFG Lea todo el prospecto detenidamente antes de empezar a tomar el medicamento, porque contiene información importante
ANEXO I FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO
 ANEXO I FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1 Este medicamento está sujeto a seguimiento adicional, lo que agilizará la detección de nueva información sobre su seguridad. Se invita
ANEXO I FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1 Este medicamento está sujeto a seguimiento adicional, lo que agilizará la detección de nueva información sobre su seguridad. Se invita
Contenido Qué es la tromboembolia venosa (TEV)? 4 Qué es la trombosis venosa profunda (TVP)? 5 Qué es la embolia pulmonar (EP)? 6 Signos y síntomas de
 Ayudar a tratar la trombosis venosa profunda y la embolia pulmonar, así como a prevenir las reapariciones Este folleto está dirigido a pacientes adultos a los que se les ha recetado ELIQUIS (apixaban)
Ayudar a tratar la trombosis venosa profunda y la embolia pulmonar, así como a prevenir las reapariciones Este folleto está dirigido a pacientes adultos a los que se les ha recetado ELIQUIS (apixaban)
ANEXO III MODIFICACIONES DEL RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO Y DEL PROSPECTO
 ANEXO III MODIFICACIONES DEL RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO Y DEL PROSPECTO 42 RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO DE LOS MEDICAMENTOS QUE CONTENGAN CABERGOLINA 4.2 Posología y forma
ANEXO III MODIFICACIONES DEL RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO Y DEL PROSPECTO 42 RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO DE LOS MEDICAMENTOS QUE CONTENGAN CABERGOLINA 4.2 Posología y forma
Historia. Fisiopatología. Sistema venoso profundo. JOHN JAIRO BERRêO C. - ADELMA SOFêA HOYOS
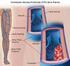 35 JOHN JAIRO BERRêO C. - ADELMA SOFêA HOYOS Historia La terapia anticoagulante ingresó en el arsenal clínico a partir del aislamiento de un glucosaminoglicano del hígado de un canino, que fue denominado
35 JOHN JAIRO BERRêO C. - ADELMA SOFêA HOYOS Historia La terapia anticoagulante ingresó en el arsenal clínico a partir del aislamiento de un glucosaminoglicano del hígado de un canino, que fue denominado
DIRECTRICES PARA LA RESOLUCIÓN DE VARIACIONES DE ADECUACIÓN AL RD 1345/2007 Y OTRAS VARIACIONES COEXISTENTES EN EL TIEMPO
 DIRECTRICES PARA LA RESOLUCIÓN DE VARIACIONES DE ADECUACIÓN AL RD 1345/2007 Y OTRAS VARIACIONES COEXISTENTES EN EL TIEMPO Antecedentes 21 de mayo de 2010 La Disposición transitoria tercera del Real Decreto
DIRECTRICES PARA LA RESOLUCIÓN DE VARIACIONES DE ADECUACIÓN AL RD 1345/2007 Y OTRAS VARIACIONES COEXISTENTES EN EL TIEMPO Antecedentes 21 de mayo de 2010 La Disposición transitoria tercera del Real Decreto
Evaluación y consejería en anticoncepción: seguridad en la prescripción y criterios de elegibilidad
 Evaluación y consejería en anticoncepción: seguridad en la prescripción y criterios de elegibilidad Dra. Cristina irribarra Ávila Ginecóloga obstetra Prof. agregado Universidad de Chile Residente maternidad
Evaluación y consejería en anticoncepción: seguridad en la prescripción y criterios de elegibilidad Dra. Cristina irribarra Ávila Ginecóloga obstetra Prof. agregado Universidad de Chile Residente maternidad
Taller de capacitación en las Normas de Atención en Planificación Familiar
 Taller de capacitación en las Normas de Atención en Planificación Familiar METODOS HORMONALES Anticonceptivos Orales Combinados. Anticonceptivos Orales de Progestina sola. Inyectable Mensual Inyectable
Taller de capacitación en las Normas de Atención en Planificación Familiar METODOS HORMONALES Anticonceptivos Orales Combinados. Anticonceptivos Orales de Progestina sola. Inyectable Mensual Inyectable
El especialista explicó que existen dos tipos de ACV:
 El accidente cerebrovascular (ACV) es una emergencia porque hay muy poco tiempo para tratarlo y revertirlo: desde que se empiezan a tener los síntomas, el lapso para actuar es de entre 3 y 6 horas. Por
El accidente cerebrovascular (ACV) es una emergencia porque hay muy poco tiempo para tratarlo y revertirlo: desde que se empiezan a tener los síntomas, el lapso para actuar es de entre 3 y 6 horas. Por
NUEVO PARCHE ANTICONCEPTIVO: Lo que siempre le has pedido
 NUEVO PARCHE ANTICONCEPTIVO: Lo que siempre le has pedido Dra. E. De la Viuda García Hospital Universitario de Guadalajara Universidad de Alcalá HM Gabinete Médico Velázquez Justificación 77% no en todas
NUEVO PARCHE ANTICONCEPTIVO: Lo que siempre le has pedido Dra. E. De la Viuda García Hospital Universitario de Guadalajara Universidad de Alcalá HM Gabinete Médico Velázquez Justificación 77% no en todas
AEMPS, 22 de abril de 2016
 AEMPS, 22 de abril de 2016 La hipercolesterolemia es la alteración lipídica más frecuente y constituye uno de los principales factores de riesgo de enfermedad cardiovascular, la primera causa de muerte
AEMPS, 22 de abril de 2016 La hipercolesterolemia es la alteración lipídica más frecuente y constituye uno de los principales factores de riesgo de enfermedad cardiovascular, la primera causa de muerte
Anexo IV. Conclusiones científicas y motivos para la modificación de los términos de las autorizaciones de comercialización
 Anexo IV Conclusiones científicas y motivos para la modificación de los términos de las autorizaciones de comercialización 28 Conclusiones científicas Resumen general de la evaluación científica de los
Anexo IV Conclusiones científicas y motivos para la modificación de los términos de las autorizaciones de comercialización 28 Conclusiones científicas Resumen general de la evaluación científica de los
Taller de actualización. en anticoncepción 2016
 Curso de actualización en Taller de actualización ginecología y anticoncepción en en anticoncepción 2016 atención primaria introducción Raquel Rodríguez Rodríguez 1994 Conferencia Internacional de Población
Curso de actualización en Taller de actualización ginecología y anticoncepción en en anticoncepción 2016 atención primaria introducción Raquel Rodríguez Rodríguez 1994 Conferencia Internacional de Población
TÍTULO: ANTICONCEPTIVOS HORMONALES Y TROMBOSIS
 Fecha: /0/0 Nombre: Dra. Jessica Nogueira García R Tipo de Sesión: Revisión de guías clínicas TÍTULO: ANTICONCEPTIVOS HORMONALES Y TROMBOSIS GUIA 0 SEC ( Sociedad Española de Contracepción) y SETH ( Sociedad
Fecha: /0/0 Nombre: Dra. Jessica Nogueira García R Tipo de Sesión: Revisión de guías clínicas TÍTULO: ANTICONCEPTIVOS HORMONALES Y TROMBOSIS GUIA 0 SEC ( Sociedad Española de Contracepción) y SETH ( Sociedad
Trombólisis para la TVP
 Trombólisis para la TVP Trombosis venosa profunda Una trombosis venosa profunda (TVP) es un coágulo de sangre que se forma en una vena profunda. Se trata de una afección grave que ocurre con mayor frecuencia
Trombólisis para la TVP Trombosis venosa profunda Una trombosis venosa profunda (TVP) es un coágulo de sangre que se forma en una vena profunda. Se trata de una afección grave que ocurre con mayor frecuencia
Síndrome Antifosfolípido
 Síndrome Antifosfolípido El síndrome de anticuerpos antifosfolípidos es una enfermedad autoinmune de identificación reciente que se presenta principalmente en la población joven femenina. En estas personas,
Síndrome Antifosfolípido El síndrome de anticuerpos antifosfolípidos es una enfermedad autoinmune de identificación reciente que se presenta principalmente en la población joven femenina. En estas personas,
PROTOCOLOS SEGO/SEC ANTICONCEPCIÓN HORMONAL Y RIESGO CARDIOVASCULAR
 PROTOCOLOS SEGO/SEC ANTICONCEPCIÓN HORMONAL Y RIESGO CARDIOVASCULAR Dr José Vicente González Navarro. Servicio Ginecología Hospital Clínico Universitario Lozano Blesa. Zaragoza. INTRODUCCIÓN A pesar de
PROTOCOLOS SEGO/SEC ANTICONCEPCIÓN HORMONAL Y RIESGO CARDIOVASCULAR Dr José Vicente González Navarro. Servicio Ginecología Hospital Clínico Universitario Lozano Blesa. Zaragoza. INTRODUCCIÓN A pesar de
PROCEDIMIENTO ESPECÍFICO. USO de IMPLANÓN COD. PE-OBS-27
 PROCEDIMIENTO ESPECÍFICO USO de IMPLANÓN COD. PE-OBS-27 Elaborado por: Manuel Lozano Sanchez RU Obstetricia y Ginecología Fecha 01/05/2013 Revisado por: Enrique Pérez Trueba Unidad de Calidad Fecha: 15/06/2013
PROCEDIMIENTO ESPECÍFICO USO de IMPLANÓN COD. PE-OBS-27 Elaborado por: Manuel Lozano Sanchez RU Obstetricia y Ginecología Fecha 01/05/2013 Revisado por: Enrique Pérez Trueba Unidad de Calidad Fecha: 15/06/2013
11 Número de publicación: 2 205 252. 51 Int. Cl. 7 : A61K 31/565, A61K 31/566. 72 Inventor/es: Gast, Michael, Jay. 74 Agente: Curell Suñol, Marcelino
 19 OFICINA ESPAÑOLA DE PATENTES Y MARCAS ESPAÑA 11 Número de publicación: 2 22 1 Int. Cl. 7 : A61K 31/6, A61K 31/66 A61K 31/67, A61K 31/7 A61P 1/18 // (A61K 31/7, A61K 31:6 12 TRADUCCIÓN DE PATENTE EUROPEA
19 OFICINA ESPAÑOLA DE PATENTES Y MARCAS ESPAÑA 11 Número de publicación: 2 22 1 Int. Cl. 7 : A61K 31/6, A61K 31/66 A61K 31/67, A61K 31/7 A61P 1/18 // (A61K 31/7, A61K 31:6 12 TRADUCCIÓN DE PATENTE EUROPEA
COMUNICACIÓN SOBRE RIESGOS D.E MEDICAMENTOS PARA PROFESIONALES SANITARIOS NOT A INFORMA
 I Carrt' Km.2.200 28220 Majadahonda-Pozuelo MAJADAHONDA - TEL: 915967711 FAX: 91 596 7891 :m ; agencia española de medicamentos y.\", ", productos sanitarios SUBDIRECCI6N GENERAL COMUNICACIÓN SOBRE RIESGOS
I Carrt' Km.2.200 28220 Majadahonda-Pozuelo MAJADAHONDA - TEL: 915967711 FAX: 91 596 7891 :m ; agencia española de medicamentos y.\", ", productos sanitarios SUBDIRECCI6N GENERAL COMUNICACIÓN SOBRE RIESGOS
ALUMNA ROSA Mª VELA BLANCO TUTORES EMILIO GARCIA-JIMENEZ ANA Mª VICENTE MARTINEZ FELIPE HERENCIA SALABERT
 ALUMNA ROSA Mª VELA BLANCO TUTORES EMILIO GARCIA-JIMENEZ ANA Mª VICENTE MARTINEZ FELIPE HERENCIA SALABERT MASTER ATENCION FARMACEUTICA UNIVERSIDAD DE GRANADA 0-0 INDICE INTRODUCCION...5 I. ANTICONCEPTIVOS
ALUMNA ROSA Mª VELA BLANCO TUTORES EMILIO GARCIA-JIMENEZ ANA Mª VICENTE MARTINEZ FELIPE HERENCIA SALABERT MASTER ATENCION FARMACEUTICA UNIVERSIDAD DE GRANADA 0-0 INDICE INTRODUCCION...5 I. ANTICONCEPTIVOS
El nuevo Reglamento 536/2014 de ensayos clínicos
 El nuevo Reglamento 536/2014 de ensayos clínicos Mariantonia Serrano Castro Departamento de Medicamentos de Uso Humano Agencia Española de Medicamentos y Productos Sanitarios Jornada formativa del Programa
El nuevo Reglamento 536/2014 de ensayos clínicos Mariantonia Serrano Castro Departamento de Medicamentos de Uso Humano Agencia Española de Medicamentos y Productos Sanitarios Jornada formativa del Programa
Grupo Nº 19: Planificación Familiar
 Grupo Nº 19: Planificación Familiar Contenido TABLA Grupo Nº 19: Planificación Familiar... 2 CETROELIX... 2 DESOGESTREL Y ETINILESTRADIOL... 2 ETONOGESTREL... 3 LEVONORGESTREL... 3 LEVONORGESTREL Y ETINILESTRADIOL...
Grupo Nº 19: Planificación Familiar Contenido TABLA Grupo Nº 19: Planificación Familiar... 2 CETROELIX... 2 DESOGESTREL Y ETINILESTRADIOL... 2 ETONOGESTREL... 3 LEVONORGESTREL... 3 LEVONORGESTREL Y ETINILESTRADIOL...
T019 FALLOS DE LA AHO Carmen Coll Capdevilla. T020 APORTA ALGO NOVEDOSO LA REDUCCIÓN DE DOSIS DE EE DE LOS ACTUALES AHO? J.
 T019 FALLOS DE LA AHO Carmen Coll Capdevilla T020 APORTA ALGO NOVEDOSO LA REDUCCIÓN DE DOSIS DE EE DE LOS ACTUALES AHO? J. Haya Palazuelos 96 Mucho han cambiado los anticonceptivos desde que en 1959 Gregory
T019 FALLOS DE LA AHO Carmen Coll Capdevilla T020 APORTA ALGO NOVEDOSO LA REDUCCIÓN DE DOSIS DE EE DE LOS ACTUALES AHO? J. Haya Palazuelos 96 Mucho han cambiado los anticonceptivos desde que en 1959 Gregory
11 Número de publicación: 2 223 081. 51 Int. Cl. 7 : A61K 31/57. 72 Inventor/es: Gast, Michael, Jay. 74 Agente: Curell Suñol, Marcelino
 19 OFICINA ESPAÑOLA DE PATENTES Y MARCAS ESPAÑA 11 Número de publicación: 2 223 081 1 Int. Cl. 7 : A61K 31/7 A61K 31/6 A61P 1/18 // (A61K 31/7 A61K 31:6) 12 TRADUCCIÓN DE PATENTE EUROPEA T3 86 Número de
19 OFICINA ESPAÑOLA DE PATENTES Y MARCAS ESPAÑA 11 Número de publicación: 2 223 081 1 Int. Cl. 7 : A61K 31/7 A61K 31/6 A61P 1/18 // (A61K 31/7 A61K 31:6) 12 TRADUCCIÓN DE PATENTE EUROPEA T3 86 Número de
Los anticonceptivos. y el riesgo de eventos trombóticos. Definiciones básicas
 / ACTUALIDAD Los anticonceptivos y el riesgo de eventos trombóticos Revisión editorial a cargo del comité científico de Farmaproyectos Ltda., bajo la coordinación de Jorge Vargas, MD, Esp. Farmacología,
/ ACTUALIDAD Los anticonceptivos y el riesgo de eventos trombóticos Revisión editorial a cargo del comité científico de Farmaproyectos Ltda., bajo la coordinación de Jorge Vargas, MD, Esp. Farmacología,
FICHA TÉCNICA. Comprimidos recubiertos con película. Comprimidos recubiertos con película de color blanco o marfil, redondo, biconvexo.
 FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Danielle 2 mg/0,03 mg comprimidos recubiertos con película EFG 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada comprimido recubierto con película contiene 2 mg de
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Danielle 2 mg/0,03 mg comprimidos recubiertos con película EFG 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada comprimido recubierto con película contiene 2 mg de
DIRECCION REGULACION DE LA SALUD CENTRO NACIONAL DE FARMACOVIGILANCIA
 DIRECCION REGULACION DE LA SALUD CENTRO NACIONAL DE FARMACOVIGILANCIA Comunicación sobre cambios en la información de seguridad de Sibutramina para profesionales sanitarios Mayo de 2010 NOTA INFORMATIVA
DIRECCION REGULACION DE LA SALUD CENTRO NACIONAL DE FARMACOVIGILANCIA Comunicación sobre cambios en la información de seguridad de Sibutramina para profesionales sanitarios Mayo de 2010 NOTA INFORMATIVA
Reducción de Sodio y Grasa en productos cárnicos y su efecto en la salud
 Reducción de Sodio y Grasa en productos cárnicos y su efecto en la salud MSC. ING. GIOVANNA CASTAÑEDA SAAVEDRA Contenido Resumen La sal ( Cloruro de Sodio Nacl ) es vital para el funcionamiento de nuestro
Reducción de Sodio y Grasa en productos cárnicos y su efecto en la salud MSC. ING. GIOVANNA CASTAÑEDA SAAVEDRA Contenido Resumen La sal ( Cloruro de Sodio Nacl ) es vital para el funcionamiento de nuestro
XVIII Jornadas de Medicina Interna. Actualizaciones en Medicina de la Mujer
 XVIII Jornadas de Medicina Interna Actualizaciones en Medicina de la Mujer Anticoncepción Hormonal Riesgos y Beneficios Moderador: Dr. Panelistas: Mauricio Tapia M. Dra. María José Miranda G Dr. Pablo
XVIII Jornadas de Medicina Interna Actualizaciones en Medicina de la Mujer Anticoncepción Hormonal Riesgos y Beneficios Moderador: Dr. Panelistas: Mauricio Tapia M. Dra. María José Miranda G Dr. Pablo
Medicamentos biológicos y biosimilares
 Medicamentos biológicos y biosimilares Guía breve para el paciente Qué son los medicamentos biológicos? Los medicamentos biológicos son moléculas grandes y complejas, que se obtienen a partir de organismos
Medicamentos biológicos y biosimilares Guía breve para el paciente Qué son los medicamentos biológicos? Los medicamentos biológicos son moléculas grandes y complejas, que se obtienen a partir de organismos
Anexo II. Conclusiones científicas y motivos para la modificación de los términos de las autorizaciones de comercialización
 Anexo II Conclusiones científicas y motivos para la modificación de los términos de las autorizaciones de comercialización 367 Conclusiones científicas y motivos para la modificación de los términos de
Anexo II Conclusiones científicas y motivos para la modificación de los términos de las autorizaciones de comercialización 367 Conclusiones científicas y motivos para la modificación de los términos de
ANTICONCEPCIÓN EN MUJERES CON PATOLOGÍA VASCULAR CEREBRAL
 ANTICONCEPCIÓN EN MUJERES CON PATOLOGÍA VASCULAR CEREBRAL Dr. Eduardo López-Arregui Clínica Euskalduna. Bilbao. cambiando actitudes 9º Congreso S.E.C. Sevilla. PATOLOGÍA VASCULAR CEREBRAL * HIPOXIA......ISQUEMIA......INFARTO
ANTICONCEPCIÓN EN MUJERES CON PATOLOGÍA VASCULAR CEREBRAL Dr. Eduardo López-Arregui Clínica Euskalduna. Bilbao. cambiando actitudes 9º Congreso S.E.C. Sevilla. PATOLOGÍA VASCULAR CEREBRAL * HIPOXIA......ISQUEMIA......INFARTO
NUEVOS ANTICOAGULANTES ORALES. David Muñoz S. Urgencias. H. Galdakao
 NUEVOS ANTICOAGULANTES ORALES David Muñoz S. Urgencias. H. Galdakao USO DE LOS ACO Profilaxis Primaria y Secundaria de los fenómenos embólicos sistémicos en la Fibrilación Auricular. Profilaxis Primaria
NUEVOS ANTICOAGULANTES ORALES David Muñoz S. Urgencias. H. Galdakao USO DE LOS ACO Profilaxis Primaria y Secundaria de los fenómenos embólicos sistémicos en la Fibrilación Auricular. Profilaxis Primaria
51 Int. CI.: A61K 31/567 ( ) G04F 1/00 ( ) A61K 31/565 ( ) A61K 31/57 ( ) A61J 7/04 ( ) TRADUCCIÓN DE PATENTE EUROPEA
 19 OFICINA ESPAÑOLA DE PATENTES Y MARCAS ESPAÑA 11 Número de publicación: 2 61 823 1 Int. CI.: A61K 31/67 (06.01) G04F 1/00 (06.01) A61K 31/6 (06.01) A61K 31/7 (06.01) A61J 7/04 (06.01) 12 TRADUCCIÓN DE
19 OFICINA ESPAÑOLA DE PATENTES Y MARCAS ESPAÑA 11 Número de publicación: 2 61 823 1 Int. CI.: A61K 31/67 (06.01) G04F 1/00 (06.01) A61K 31/6 (06.01) A61K 31/7 (06.01) A61J 7/04 (06.01) 12 TRADUCCIÓN DE
Experiencia Clínica con Dienogest 2mg continuo
 Experiencia Clínica con Dienogest 2mg continuo Dr. Luis Auge PROFESOR TITULAR DE GINECOLOGÍA, FACULTAD DE MEDICINA. U.B.A. DIRECTOR INSTITUTO DE GINECOLOGÍA Y FERTILIDAD EX PRESIDENTE DE LA SOCIEDAD ARGENTINA
Experiencia Clínica con Dienogest 2mg continuo Dr. Luis Auge PROFESOR TITULAR DE GINECOLOGÍA, FACULTAD DE MEDICINA. U.B.A. DIRECTOR INSTITUTO DE GINECOLOGÍA Y FERTILIDAD EX PRESIDENTE DE LA SOCIEDAD ARGENTINA
riesgos con Xolair. Información sobre Xolair (omalizumab)
 La FDA aprueba cambios en la etiqueta del medicamento para el asma Xolair (omalizumab), los que incluyen la descripción de un riesgo ligeramente mayor de acontecimientos adversos cardíacos y cerebrales
La FDA aprueba cambios en la etiqueta del medicamento para el asma Xolair (omalizumab), los que incluyen la descripción de un riesgo ligeramente mayor de acontecimientos adversos cardíacos y cerebrales
CONTROVERSIAS HIPERTENSION PULMONAR
 CONTROVERSIAS HIPERTENSION PULMONAR Mª Carmen Torreiro Penas Hospital Xeral-Calde Lugo Eficacia/precio de los fármacos f aprobados? Es necesario evaluar los fármacos f aprobados? TRATAMIENTO Importantes
CONTROVERSIAS HIPERTENSION PULMONAR Mª Carmen Torreiro Penas Hospital Xeral-Calde Lugo Eficacia/precio de los fármacos f aprobados? Es necesario evaluar los fármacos f aprobados? TRATAMIENTO Importantes
FARMACOS QUE ACTUAN EN EL SISTEMA REPRODUCTOR
 FARMACOS QUE ACTUAN EN EL SISTEMA REPRODUCTOR CLASE DE FARMACOS Durante la adolescencia inicias la toma de decisiones importantes, algunas de las cuales pueden influir a todo lo largo de tu vida. La elección
FARMACOS QUE ACTUAN EN EL SISTEMA REPRODUCTOR CLASE DE FARMACOS Durante la adolescencia inicias la toma de decisiones importantes, algunas de las cuales pueden influir a todo lo largo de tu vida. La elección
Ma. Soledad Quesada M Centro Nacional de Información de Medicamentos, UCR
 Análisis del estado de salud y comportamientos de los pacientes con diabetes mellitus encuestados en la Encuesta Nacional de Salud 2006, Centro Centroamericano de Población-Universidad de Costa Rica Ma.
Análisis del estado de salud y comportamientos de los pacientes con diabetes mellitus encuestados en la Encuesta Nacional de Salud 2006, Centro Centroamericano de Población-Universidad de Costa Rica Ma.
FOLLETO DE INFORMACIÓN AL PROFESIONAL LISVY PARCHE TRANSDÉRMICO
 1. NOMBRE DEL MEDICAMENTO Lisvy parche transdérmico, 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada parche transdérmico de 11 cm 2 contiene 2,10 mg de gestodeno y 0,55 mg de etinilestradiol. Cada parche
1. NOMBRE DEL MEDICAMENTO Lisvy parche transdérmico, 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada parche transdérmico de 11 cm 2 contiene 2,10 mg de gestodeno y 0,55 mg de etinilestradiol. Cada parche
4.8. LA PRESIÓN ARTERIAL
 4.8. LA PRESIÓN ARTERIAL 10/11/10 ALF- FUNDAMENTOS BIOLÓGICOS 10/11 1 La presión arterial es la fuerza que ejerce la sangre sobre las paredes de las arterias. Es medida en mm. de mercurio (Hg). 10/11/10
4.8. LA PRESIÓN ARTERIAL 10/11/10 ALF- FUNDAMENTOS BIOLÓGICOS 10/11 1 La presión arterial es la fuerza que ejerce la sangre sobre las paredes de las arterias. Es medida en mm. de mercurio (Hg). 10/11/10
PROTOCOLO : PROFILAXIS DE TROMBOEMBOLISMO
 PROTOCOLO : PROFILAXIS DE TROMBOEMBOLISMO Dr. Oscar Diaz Cambronero Servicio de Anestesia Reanimacion y Tratamiento del Dolor Consorcio Hospital General Universitario de Valencia INTRODUCCION La enfermedad
PROTOCOLO : PROFILAXIS DE TROMBOEMBOLISMO Dr. Oscar Diaz Cambronero Servicio de Anestesia Reanimacion y Tratamiento del Dolor Consorcio Hospital General Universitario de Valencia INTRODUCCION La enfermedad
