LABORATORIO DE MICROBIOLOGÍA EXPERIMENTAL Grupo 02 (10:00 13:00 hrs) Semestre Profesores: Guadalupe Tsuzuki Reyes y Rosalba Esquivel-Cote
|
|
|
- Alfonso Lagos Plaza
- hace 5 años
- Vistas:
Transcripción
1 Sema na 3 Semana 2 Semana 1 LABORATORIO DE EXPERIMENTAL Grupo 02 (10:00 13:00 hrs) Semestre Profesores: Guadalupe Tsuzuki Reyes y Rosalba Esquivel-Cote CALENDARIO DE ACTIVIDADES PROTOCOLO / UNIDAD Lunes 5 AGOSTO Miércoles 7 AGOSTO Presentación. Organización. Forma de evaluación. 1. BUENAS PRÁCTICAS DE LABORATORIO Explicación acerca del Formato para entregar Reportes AUDIOVISUAL 11:00 a.m. Revisión de los siguientes videos: Técnica aséptica Trabajo en el laboratorio Y el reglamento? Conseguir candado y material básico para limpieza para siguiente clase. Lectura del manual de higiene y seguridad para discutir en clase. P1 Bioseguridad. Análisis del reglamento de seguridad e higiene. Cuestionario del Reglamento de Bioseguridad e Higiene. Traer candado y material básico para limpieza Conseguir una letra muy pequeña y asimétrica (a, e, f, t, r, p) recortada de periódico o revista, para siguiente clase. Traer pulque (200 ml/grupo) Microscopio Uso del microscopio Frotis Tinción simple PROTOCOLO / UNIDAD Lunes 12 AGOSTO Miércoles 14 AGOSTO P2.1 Uso y cuidado del microscopio de campo claro. Presentación del microscopio. Enfoque de letra asimétrica. P2.2 Preparaciones microbiológicas. P2.2.3 Preparaciones fijas. P2.2.4 Tinción simple Manejo de la zona aséptica. Traer una letra muy pequeña y asimétrica. 200 ml de pulque Organizar material en gavetas (20 min) P2.2 Preparaciones microbiológicas. P2.2.5a y P2.2.5b Tinciones diferenciales (Tinción Gram y Ziehl-Neelsen). Reporte 1: Bioseguridad en el Laboratorio de Microbiología Cuestionario del artículo Laboratorios de bioseguridad nivel 3 y 4 Tinción de Gram Tinción de Ziehl Neelsen Conseguir pulque para la siguiente semana. Poner el domingo antes, azúcar (1 cucharada sopera/1000ml) y no tapar herméticamente. Tinción de endospora Tinción negativa de cápsula PROTOCOLO / UNIDAD Lunes 19 AGOSTO Miércoles 21 AGOSTO P2.2 Preparaciones microbiológicas. P2.2 Preparaciones microbianas P2.2.6a Tinción selectiva (tinción de endospora). Concluir con tinciones diferenciales,
2 Semana 4 P2.2.6b Tinción negativa (tinción de cápsula). Pulque (100 ml) selectiva y negativa P2.3 Esterilización y preparación de medios de cultivo. Pedir y lavar material de vidrio. Enjuagar con agua destilada. Secado en horno. Pulque (100 ml) Conseguir latas de conserva forradas por afuera y por dentro con papel estraza para la siguiente clase. Preparación de material para su esterilización PROTOCOLO / UNIDAD Lunes 26 AGOSTO Miércoles 28 AGOSTO P2.3 Esterilización y preparación de medios de cultivo. Preparar material de vidrio para su esterilización, previamente lavado (poner filtro y envolver pipetas y cajas Petri). Preparar medios de cultivo y tubos con SSI. Esterilización. Utilizar controles biológicos. REPORTE 2: Uso y cuidado del microscopio de campo claro. Preparaciones fijas, tinciones simple, diferenciales, selectiva y negativa. Traer latas forradas con papel estraza. P2.3 Esterilización y preparación de medios de cultivo. Lectura e interpretación de resultados. P2.3 Control de calidad de esterilización, (controles biológicos), Zona y Técnica aséptica. Inoculación de control biológico y placas técnica aséptica. Conseguir un alimento enmohecido para el miércoles 4 de septiembre. Investigar las características macroscópicas y microscópicas de las actinobacterias (en una cuartilla). Siembra en tubo por estría Siembra por extensión superficial Siembra por picadura Siembra en medio líquido Siembra por estría en placa A partir de la siguiente semana, los laboratoristas del L 1A, no proporcionarán el siguiente material: asas bacteriológicas, gradillas, mecheros, portaobjetos y cubreobjetos
3 Semana 6 Semana 5 PROTOCOLO / UNIDAD Lunes 2 SEPTIEMBRE Miércoles 4 SEPTIEMBRE P2.3 Control de calidad de esterilización, (controles biológicos), Zona y Técnica aséptica. Lectura e interpretación de resultados. 3. ESTUDIO DE CULTIVOS BACTERIANOS PUROS 4. ESTUDIO MICROSCÓPICO Y CULTIVO DE HONGOS P3.1 Técnicas de cultivo de bacterias no filamentosas y actinobacterias: Inoculación. Tinción de Gram a partir de cepas. Características macroscópicas y microscópicas de las actinobacterias. Siembra con asa micológica P3.1 Técnicas de cultivo de bacterias no filamentosas y actinobacterias: Lectura e interpretación de resultados (desarrollo de bacterias no filamentosas). Tinción de Gram a partir de los cultivos obtenidos. P4.1 Técnica de cultivo de hongos. Inoculación de hongos (mohos y levaduras) a partir de cultivos puros y de una muestra natural. Observación por impronta. Alimento (vegetal, pan o tortilla) enmohecido Conseguir material para la instalación de la columna de Winogradsky, el miércoles 11 de septiembre. Investigar las características morfológicas de los hongos filamentosos. Hacer un modelo. PROTOCOLO / UNIDAD Lunes 9 SEPTIEMBRE Miércoles 11 SEPTIEMBRE (0) P2.2.1 Preparaciones microbiológicas (Preparaciones húmedas a partir de muestras de agua de florero, lago). 3. ESTUDIO DE CULTIVOS BACTERIANOS PUROS 4. ESTUDIO MICROSCÓPICO Y CULTIVO DE HONGOS EN UN MICROAMBIENTE P3.1 Técnicas de cultivo de bacterias: Lectura e interpretación de resultados (desarrollo de bacterias filamentosas). Tinción de Gram a partir de los cultivos obtenidos. P4.1 Técnica de cultivo de hongos. Lectura e interpretación de resultados. Observación por impronta a partir de cultivos puros y de la muestra natural. EXPOSICIÓN POR EQUIPO DE MODELOS de las características morfológicas de hongos filamentosos REPORTE 3: Esterilización y control de calidad. Revisar los videos de las técnicas : Preparaciones húmedas Tinciones vitales Observación de protozoarios y algas ESTUDIO DE PROTOZOARIOS Y ALGAS Características básicas de protozoarios y algas 9.2 Instalación de la Columna de Winogradsky. Observación macroscópica de la apariencia de la Columna, y microscópica de la diversidad microbiana (bacterias, hongos, protozoarios y algas). Primera observación. Toma de fotos. Material para instalar la columna de Winogradsky Cuestionario del Artículo Winogradsky Column. Preparar tubos con SSIE y conseguir cajas de Petri de plástico estériles desechables para el miércoles 18 de septiembre
4 Semana 9 Semana 8 Semana 7 PROTOCOLO / UNIDAD Lunes 16 SEPTIEMBRE Miércoles 18 SEPTIEMBRE (1) 5. TÉCNICAS DE AISLAMIENTO DE NO HAY LABORES P5.1 Técnicas de aislamiento de microorganismos. Aislamiento de: bacteria G+, G-, esporulada, levaduras y/o actinobacterias, a partir de un cultivo mixto. 9.2 Observación macroscópica y microscópica de la Columna de Winogradsky. Segunda observación. Toma de fotos. REPORTE 4: Cultivo de bacterias, hongos, estudio de protozoarios y algas. I. Desde Buenas prácticas de laboratorio hasta Cultivo de Bacterias y Hongos. PROTOCOLO / UNIDAD Lunes 23 SEPTIEMBRE Miércoles 25 SEPTIEMBRE (2) P5.1 Técnicas de aislamiento de microorganismos. Lectura e interpretación de resultados P5.1 Técnicas de aislamiento de microorganismos. (comparación de la diversidad de colonias Lectura de resultados (comprobación de pureza de 5. TÉCNICAS DE AISLAMIENTO desarrolladas en los diferentes medios de cultivo y colonias desarrolladas en los medios de cultivo, DE condiciones de incubación, tinción Gram, simple o selección de colonias). Impronta. Selección de colonias). Resiembra en medio general. Aislamiento primario. Cuestionario del Artículo Microbial Safari 9.2 Observación macroscópica y microscópica de la Columna de Winogradsky. Tercera observación. Toma de fotos. Esterilizar pipetas Pasteur para siguiente clase PROTOCOLO / UNIDAD Lunes 30 SEPTIEMBRE Miércoles 2 OCTUBRE (4) P5.1 Técnicas de aislamiento de microorganismos. Lectura de resultados (comprobación de pureza de 5. TÉCNICAS DE AISLAMIENTO colonias desarrolladas en los medios de cultivo, DE selección de colonias). Conservación de cepa pura 6. NUTRICIÓN MICROBIANA Y CARACTERIZACIÓN ES oxígeno (cepas de referencia). Inoculación de microorganismos en medio mineral con diferentes fuentes de C. Lectura e interpretación de resultados 48 hrs. 9.2 Observación macroscópica y microscópica de la Columna de Winogradsky. Cuarta observación. Toma de fotos. MAESTRAS: Pedir a los alumnos $90.00 p/equipo para la compra de la Tira Api para el 7 de octubre
5 Semana 11 Semana 10 PROTOCOLO / UNIDAD Lunes 7 OCTUBRE Miércoles 9 OCTUBRE (5) 6. NUTRICIÓN MICROBIANA Y CARACTERIZACIÓN Lectura e interpretación de resultados 7 días. 9.2 Observación macroscópica y microscópica de la Columna de Winogradsky. Quinta observación. Toma de fotos. microbiana. Inoculación de microorganismos que participan en los ciclos biogeoquímicos (N, P, S) y con actividad antagónica. REPORTE 5: Aislamiento de microorganismos. Pagar Tiras Api microbiana. Lectura de resultados de 48 horas. RETIRAR COLUMNAS WINOGRADSKY II. Desde. Buenas prácticas de laboratorio hasta Nutrición microbiana y caracterización fisiológica de bacterias. Esterilizar pipetas Pasteur, serológicas y tubos con SSI para la inoculación de tiras Api. Viernes 11: Resembrar cepa Gram negativa (aislada) e Incubar en gaveta. PROTOCOLO / UNIDAD Lunes 14 OCTUBRE Miércoles 16 OCTUBRE (6) Lectura e interpretación de resultados 14 días. 6. NUTRICIÓN MICROBIANA Y CARACTERIZACIÓN P6.2 Uso de pruebas bioquímicas y técnicas rápidas para la caracterización fisiológica de bacterias (Pruebas en tubos y cajas e Inoculación de tiras Api) Siembra en diferentes medios de cultivo e inoculación de tiras Api. microbiana. Lectura de resultados de 7 días. Martes 15: Refrigerar tiras Api P6.2 Uso de pruebas bioquímicas y técnicas rápidas para la caracterización fisiológica de bacterias Lectura e interpretación de resultados de pruebas en tubos y cajas. Revelar tiras Api Conseguir un frasco (del Valle, 350mL) de vidrio, limpio, para el 21 de octubre. Conseguir leche bronca (cruda) y pasteurizada (producto nuevo y sin abrir) para el lunes 23 de octubre. Viernes 18: Resembrar cepa Gram positiva (aislada) e Incubar en gaveta.
6 Semana 13 Semana 12 PROTOCOLO / UNIDAD Lunes 21 OCTUBRE Miércoles 23 OCTUBRE Lectura e interpretación de resultados 21 días.. 6. NUTRICIÓN MICROBIANA Y CARACTERIZACIÓN 7. TÉCNICAS PARA LA ENUMERACIÓN DE P6.2 Uso de pruebas bioquímicas y técnicas rápidas para la caracterización fisiológica de bacterias (Sistema Vitek2) P7.5 Análisis microbiológico del agua (NMP). Inoculación en Caldo Lactosado P7.2 Método turbidimétrico Densimat. Graficar resultados microbiana. Lectura de resultados 14 días. Frasco (del Valle, 350mL) limpio de vidrio y colocar TIOSULFATO DE SODIO (0.5%). Esterilizar y llevar a casa para traer muestra de agua. Esterilizar un matraz Erlenmeyer (90 ml SSI), pipetas serológicas (1 ml) y tubos ensayo (9 ml SSI). Conseguir cajas de Petri de plástico estériles desechables para lunes 28 de octubre. Preparar y esterilizar tres pipetas (1mL) y dos tubos vacíos con tapón de rosca para siguiente clase. Entrega de resultados de Sistema Vitek2 P7.5 Análisis microbiológico del agua (NMP). Lectura e interpretación de resultados. Resiembra a partir de tubos con caldo lactosado a tubos con CBVB y caldo EC. P7.1 Método de RedOx con azul de metileno (Reductasas en leche) P7.4 Técnica de Filtración Preparar y esterilizar equipo Millipore para filtración Leche bronca (cruda) y pasteurizada (producto nuevo y sin abrir, aprox 250mL). Esterilizar tubo con SSIE (BQ de P7.5) para siguiente clase. Conseguir muestra de suelo (100g) para siguiente clase. Jueves 24: Registrar tubos + en CBVB y en caldo EC. Inocular en placa EMB a partir de EC. Viernes 25: Inocular en placa GN a partir de EMB. Incubar en gaveta PROTOCOLO / UNIDAD Lunes 28 OCTUBRE Miércoles 30 OCTUBRE P7.5 Análisis microbiológico del agua Revelar pruebas Bioquímicas. 7. TÉCNICAS PARA LA ENUMERACIÓN DE NOTA: 1 de Noviembre no hay labores. P7.5 Análisis microbiológico del agua Inocular pruebas Bioquímicas. P7.3 Técnica de dilución y vertido en placa (UFC). Inoculación P7.4 Técnica de Filtración Filtración e inoculación microbiana. Lectura de resultados 21 días. Muestra de agua (250mL aprox) en frasco de vidrio estéril. Muestra de suelo (100 g) P7.3 Técnica de dilución y vertido en placa (UFC). Lectura de resultados P7.4 Técnica de Filtración Lectura de resultados REPORTE 6: Nutrición microbiana y requerimientos de
7 Semana 16 Semana 15 Semana 14 PROTOCOLO / UNIDAD Lunes 4 NOVIEMBRE Miércoles 6 NOVIEMBRE P8.1 Determinación del efecto de ph, P8.1 Determinación del efecto de ph, 8. CONDICIONES temperatura y concentración de solutos. temperatura y concentración de solutos. AMBIENTALES PARA EL Inocular dos cepas de referencia. Lectura de resultados. DESARROLLO, INHIBICIÓN Y P8.2 Determinación del efecto letal y mutagénico P8.2 Determinación del efecto letal y mutagénico DESTRUCCIÓN DE LOS de las radicaciones UV de las radicaciones UV Inocular dos cepas de referencia. Lectura de resultados. REPORTE 7: Uso de pruebas bioquímicas y técnicas rápidas para la caracterización fisiológica LAVAR Y ENTREGAR MATERIAL ADEUDADO de bacterias. Conseguir agentes químicos (limpiadores, desinfectantes, antisépticos, etc.), 30 discos de papel filtro (estériles en una caja de Petri de vidrio), 4 hisopos estériles y 8 cajas de Petri de plástico estériles desechables para lunes 11 de noviembre. PROTOCOLO / UNIDAD Lunes 11 NOVIEMBRE Miércoles 13 NOVIEMBRE 8. CONDICIONES P8.3 Determinación del efecto de agentes P8.3 Determinación del efecto de agentes químicos AMBIENTALES PARA EL químicos en el crecimiento microbiano. en el crecimiento microbiano. DESARROLLO, INHIBICIÓN Y Lectura de halos de inhibición Inoculación de dos cepas de referencia mediante la DESTRUCCIÓN DE LOS Resiembra de tubos + en placas (Efecto de técnica de Difusión en Placa. estreptomicina) Traer 8 cajas de Petri desechables estériles y agentes químicos (limpiadores, desinfectantes, antisépticos, etc.) LAVAR Y ENTREGAR MATERIAL ADEUDADO REPORTE 8: Técnicas para la enumeración de microorganismos. III (FINAL) Jueves 14: Lectura de placas (Efecto de estreptomicina) PROTOCOLO / UNIDAD Lunes 18 NOVIEMBRE Miércoles 20 NOVIEMBRE NO HAY LABORES EXPOSICIÓN-REPORTE Integración y discusión de resultados obtenidos en la Unidad IX (Columna de Winogradsky). Microorganismos que participan en los ciclos biogeoquímicos (N, P, S) CONCLUSIONES DEL CURSO REPORTE 9: Condiciones ambientales para el desarrollo, inhibición y destrucción de los microorganismos.
LABORATORIO DE MICROBIOLOGÍA EXPERIMENTAL Grupo 2 (10:00 13:00 hrs) Semestre Profesores: Guadalupe Tsuzuki Reyes y Rosalba Esquivel-Cote
 Semana 2 Semana 1 LABORATORIO DE EXPERIMENTAL Grupo 2 (10:00 13:00 hrs) Semestre 2013-2 Profesores: Guadalupe Tsuzuki Reyes y Rosalba Esquivel-Cote CALENDARIO DE ACTIVIDADES UNIDAD Lunes 28 ENERO Miércoles
Semana 2 Semana 1 LABORATORIO DE EXPERIMENTAL Grupo 2 (10:00 13:00 hrs) Semestre 2013-2 Profesores: Guadalupe Tsuzuki Reyes y Rosalba Esquivel-Cote CALENDARIO DE ACTIVIDADES UNIDAD Lunes 28 ENERO Miércoles
Unidad 5. Técnicas de aislamiento de microorganismos Práctica 6. Técnicas de aislamiento de microorganismos.
 Unidad 5. Técnicas de aislamiento de microorganismos Práctica 6. Técnicas de aislamiento de microorganismos. Objetivos Explicar el fundamento de diferentes medios de cultivo y condiciones de incubación
Unidad 5. Técnicas de aislamiento de microorganismos Práctica 6. Técnicas de aislamiento de microorganismos. Objetivos Explicar el fundamento de diferentes medios de cultivo y condiciones de incubación
PRÁCTICA 5. Aislamiento de Microorganismos (1ª Sesión)
 PRÁCTICA 5. Aislamiento de Microorganismos (1ª Sesión) Objetivos Al finalizar esta práctica el alumno será capaz de: Explicar el fundamento de diferentes medios de cultivo y condiciones de incubación para
PRÁCTICA 5. Aislamiento de Microorganismos (1ª Sesión) Objetivos Al finalizar esta práctica el alumno será capaz de: Explicar el fundamento de diferentes medios de cultivo y condiciones de incubación para
PRÁCTICAS DEL LABORATORIO DE MICROBIOLOGÍA GENERAL Trimestre 14-I
 PRÁCTICAS DEL LABORATORIO DE MICROBIOLOGÍA GENERAL Trimestre 14-I P # 1 P # 2 P # 3 P # 4 P # 5 P # 6 Uso y cuidados en el manejo del Microscopio Esterilización de materiales y medios Técnicas de Tinción
PRÁCTICAS DEL LABORATORIO DE MICROBIOLOGÍA GENERAL Trimestre 14-I P # 1 P # 2 P # 3 P # 4 P # 5 P # 6 Uso y cuidados en el manejo del Microscopio Esterilización de materiales y medios Técnicas de Tinción
PRÁCTICA 5.1 Aislamiento de Microorganismos
 PRÁCTICA 5.1 Aislamiento de Microorganismos Objetivos Al finalizar esta práctica el alumno será capaz de: Explicar el fundamento de diferentes medios de cultivo y condiciones de incubación para el aislamiento
PRÁCTICA 5.1 Aislamiento de Microorganismos Objetivos Al finalizar esta práctica el alumno será capaz de: Explicar el fundamento de diferentes medios de cultivo y condiciones de incubación para el aislamiento
Unidad 6. Nutrición microbiana y caracterización de bacterias. Práctica 9 Metabolismo de bacterias.
 Unidad 6. Nutrición microbiana y caracterización de bacterias. Práctica 9 Metabolismo de bacterias. Objetivos Relacionar la actividad metabólica de los microorganismos con los cambios producidos en diferentes
Unidad 6. Nutrición microbiana y caracterización de bacterias. Práctica 9 Metabolismo de bacterias. Objetivos Relacionar la actividad metabólica de los microorganismos con los cambios producidos en diferentes
PRÁCTICA 8. CONDICIONES AMBIENTALES PARA EL DESARROLLO, INHIBICIÓN Y DESTRUCCIÓN DE LOS MICROORGANISMOS
 PRÁCTICA 8. CONDICIONES AMBIENTALES PARA EL DESARROLLO, INHIBICIÓN Y DESTRUCCIÓN DE LOS MICROORGANISMOS Objetivos Al finalizar este ejercicio el alumno será capaz de: Explicar el efecto de factores físicos
PRÁCTICA 8. CONDICIONES AMBIENTALES PARA EL DESARROLLO, INHIBICIÓN Y DESTRUCCIÓN DE LOS MICROORGANISMOS Objetivos Al finalizar este ejercicio el alumno será capaz de: Explicar el efecto de factores físicos
UNIVERSIDAD AUTONOMA DE TAMAULIPAS
 R-RS-01-25-03 UNIVERSIDAD AUTONOMA DE TAMAULIPAS UNIDAD ACADÉMICA MULTIDISCIPLINARIA REYNOSA-AZTLÁN NOMBRE DE LA CARRERA LICENCIADO EN NUTRICION Y CIENCIA DE LOS ALIMENTOS NOMBRE DE LA ASIGNATURA LABORATORIO
R-RS-01-25-03 UNIVERSIDAD AUTONOMA DE TAMAULIPAS UNIDAD ACADÉMICA MULTIDISCIPLINARIA REYNOSA-AZTLÁN NOMBRE DE LA CARRERA LICENCIADO EN NUTRICION Y CIENCIA DE LOS ALIMENTOS NOMBRE DE LA ASIGNATURA LABORATORIO
Dr. Oscar Gutiérrez Coronado Microbiologia Práctica No. 1 Preparación y esterilización de materiales y medios de cultivo
 Dr. Oscar Gutiérrez Coronado Microbiologia Práctica No. 1 Preparación y esterilización de materiales y medios de cultivo Objetivos. Que el alumno conozca los principios generales de las técnicas de esterilización
Dr. Oscar Gutiérrez Coronado Microbiologia Práctica No. 1 Preparación y esterilización de materiales y medios de cultivo Objetivos. Que el alumno conozca los principios generales de las técnicas de esterilización
PRACTICA Núm. 22 INVESTIGACION DE COLIFORMES TOTALES Y FECALES EN DESECHOS SOLIDOS Y COMPOSTA
 PRACTICA Núm. 22 INVESTIGACION DE COLIFORMES TOTALES Y FECALES EN DESECHOS SOLIDOS Y COMPOSTA I. OBJETIVO Determinar la presencia de coliformes totales y fecales en un desecho sólido por el método del
PRACTICA Núm. 22 INVESTIGACION DE COLIFORMES TOTALES Y FECALES EN DESECHOS SOLIDOS Y COMPOSTA I. OBJETIVO Determinar la presencia de coliformes totales y fecales en un desecho sólido por el método del
GUÍA DE LABORATORIO Nº 1 MEDIOS DE CULTIVO. OBJETIVO Comprender la utilidad de los medios de cultivo en el trabajo microbiológico.
 GUÍA DE LABORATORIO Nº 1 MEDIOS DE CULTIVO OBJETIVO Comprender la utilidad de los medios de cultivo en el trabajo microbiológico. MATERIALES Placas de agar sangre y agar McConkey. Tubos con agar TSI, agar
GUÍA DE LABORATORIO Nº 1 MEDIOS DE CULTIVO OBJETIVO Comprender la utilidad de los medios de cultivo en el trabajo microbiológico. MATERIALES Placas de agar sangre y agar McConkey. Tubos con agar TSI, agar
Materiales. Cultivos puros de bacterias: Streptomyces griseus Streptomyces erythraeus
 Unidad 3. Estudio de cultivos bacterianos puros y Unidad 4. Estudio microscópico y cultivo de hongos, algas y protozoarios Práctica 6. Técnicas de siembra y cultivo de actinomicetos y hongos Objetivos
Unidad 3. Estudio de cultivos bacterianos puros y Unidad 4. Estudio microscópico y cultivo de hongos, algas y protozoarios Práctica 6. Técnicas de siembra y cultivo de actinomicetos y hongos Objetivos
PRACTICA Núm. 12 AISLAMIENTO DE 2 MICROORGANISMOS Y OBTENCION DE UN CULTIVO AXENICO
 PRACTICA Núm. 12 AISLAMIENTO DE 2 MICROORGANISMOS Y OBTENCION DE UN CULTIVO AXENICO I. OBJETIVO Aislar dos microorganismos por la técnica de siembra de dilución por estría en placa de agar y obtener un
PRACTICA Núm. 12 AISLAMIENTO DE 2 MICROORGANISMOS Y OBTENCION DE UN CULTIVO AXENICO I. OBJETIVO Aislar dos microorganismos por la técnica de siembra de dilución por estría en placa de agar y obtener un
PRÁCTICA Esterilización y Preparación de Medios de Cultivo (1ª sesión)
 Objetivos PRÁCTICA Esterilización y Preparación de Medios de Cultivo (1ª sesión) Al finalizar este ejercicio el alumno será capaz de: Explicar el concepto de esterilización y su aplicación en microbiología.
Objetivos PRÁCTICA Esterilización y Preparación de Medios de Cultivo (1ª sesión) Al finalizar este ejercicio el alumno será capaz de: Explicar el concepto de esterilización y su aplicación en microbiología.
- Mencionar las Normas de Bioseguridad y precauciones necesarias para trabajar en el laboratorio microbiológico.
 Microbiología General e Inmunología Año 2012 Trabajo Práctico Nº1 Objetivos: Que el alumno sea capaz de: - Mencionar las Normas de Bioseguridad y precauciones necesarias para trabajar en el laboratorio
Microbiología General e Inmunología Año 2012 Trabajo Práctico Nº1 Objetivos: Que el alumno sea capaz de: - Mencionar las Normas de Bioseguridad y precauciones necesarias para trabajar en el laboratorio
Asignaturas antecedentes y subsecuentes
 PROGRAMA DE ESTUDIOS Microbiología General Área a la que pertenece: AREA SUSTANTIVA PROFESIONAL Horas teóricas: 3 Horas practicas: 3 Créditos: 9 Clave: F0219 Ninguna. Asignaturas antecedentes y subsecuentes
PROGRAMA DE ESTUDIOS Microbiología General Área a la que pertenece: AREA SUSTANTIVA PROFESIONAL Horas teóricas: 3 Horas practicas: 3 Créditos: 9 Clave: F0219 Ninguna. Asignaturas antecedentes y subsecuentes
Objetivo Describir el efecto de los factores ambientales, su concentración, así como de agentes químicos en el crecimiento de los microorganismos.
 Unidad 8. Condiciones ambientales para el desarrollo, inhibición y destrucción de microorganismos. Práctica 8. Crecimiento Microbiano. Efecto de los factores ambientales y químicos Objetivo Describir el
Unidad 8. Condiciones ambientales para el desarrollo, inhibición y destrucción de microorganismos. Práctica 8. Crecimiento Microbiano. Efecto de los factores ambientales y químicos Objetivo Describir el
LABORATORIO DE MICROBIOLOGÍA EXPERIMENTAL Grupo 02 (10:00 13:00 hrs) Semestre Profesores: Rosalba Esquivel-Cote y Hugo A.
 LABORATORIO DE MICROBIOLOGÍA EXPERIMENTAL Grupo 02 (10:00 13:00 hrs) Semestre 2011-1 Profesores: Rosalba Esquivel-Cote y Hugo A. Hernández Pérez CALENDARIO DE ACTIVIDADES Semana 1 UNIDAD Lunes 9 de Agosto
LABORATORIO DE MICROBIOLOGÍA EXPERIMENTAL Grupo 02 (10:00 13:00 hrs) Semestre 2011-1 Profesores: Rosalba Esquivel-Cote y Hugo A. Hernández Pérez CALENDARIO DE ACTIVIDADES Semana 1 UNIDAD Lunes 9 de Agosto
Cultivo Puro. Técnicas de aislamiento Mantenimiento y preservación de cultivos puros Morfología macroscópica Morfología microscópica
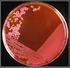 Cultivo Puro Técnicas de aislamiento Mantenimiento y preservación de cultivos puros Morfología macroscópica Morfología microscópica Definición El cultivo puro representa las condiciones artificiales para
Cultivo Puro Técnicas de aislamiento Mantenimiento y preservación de cultivos puros Morfología macroscópica Morfología microscópica Definición El cultivo puro representa las condiciones artificiales para
En la naturaleza los microorganismos se encuentran en poblaciones mixtas de varios tipos. Para todos los estudios llevados a cabo en el laboratorio
 En la naturaleza los microorganismos se encuentran en poblaciones mixtas de varios tipos. Para todos los estudios llevados a cabo en el laboratorio de microbiología se requiere un cultivo axénico, es decir,
En la naturaleza los microorganismos se encuentran en poblaciones mixtas de varios tipos. Para todos los estudios llevados a cabo en el laboratorio de microbiología se requiere un cultivo axénico, es decir,
PROCEDIMIENTO DETECCIÓN Y ENUMERACIÓN POR NUMERO MAS PROBABLE (NMP) CON ETAPA DE PRE- ENRIQUECIMIENTO DE ENTEROBACTERIACEAE EN ALIMENTOS
 Página 1 de 5 1. OBJETIVO Estimar el número de Enterobacteriaceae presentes en el alimento. 2. CAMPO DE APLICACIÓN Y ALCANCE Aplicar este procedimiento a todas las muestras de alimentos de consumo humano
Página 1 de 5 1. OBJETIVO Estimar el número de Enterobacteriaceae presentes en el alimento. 2. CAMPO DE APLICACIÓN Y ALCANCE Aplicar este procedimiento a todas las muestras de alimentos de consumo humano
PRÁCTICAS DE MICROBIOLOGÍA CLÍNICA (CURSO )
 PRÁCTICAS DE MICROBIOLOGÍA CLÍNICA (CURSO 2012 2013) PRÁCTICAS A REALIZAR ANÁLISIS CUALITATIVO DE ORINA PRUEBA DE BAUER KIRBY (ANTIBIOGRAMA) PRUEBA DE EPSILON (DETERMINACIÓN DE LA CMI) ANÁLISIS CUALITATIVO
PRÁCTICAS DE MICROBIOLOGÍA CLÍNICA (CURSO 2012 2013) PRÁCTICAS A REALIZAR ANÁLISIS CUALITATIVO DE ORINA PRUEBA DE BAUER KIRBY (ANTIBIOGRAMA) PRUEBA DE EPSILON (DETERMINACIÓN DE LA CMI) ANÁLISIS CUALITATIVO
UNIVERSIDAD DE CIENCIAS Y ARTES DE CHIAPAS
 1 FACULTAD DE CIENCIAS DE LA NUTRICIÓN Y ALIMENTOS LICENCIATURA EN NUTRIOLOGÍA MANUAL DE PRÁCTICAS PARA LA EXPERIENCIA ACADÉMICA MICROBIOLOGÍA DE ALIMENTOS ELABORO: M. EN C. GILBER VELA GUTIÉRREZ Y M.
1 FACULTAD DE CIENCIAS DE LA NUTRICIÓN Y ALIMENTOS LICENCIATURA EN NUTRIOLOGÍA MANUAL DE PRÁCTICAS PARA LA EXPERIENCIA ACADÉMICA MICROBIOLOGÍA DE ALIMENTOS ELABORO: M. EN C. GILBER VELA GUTIÉRREZ Y M.
1ª sesión. Unidad 2. Técnicas básicas de microbiología. Práctica 2. Esterilización y preparación de medios de cultivo
 Unidad 2. Técnicas básicas de microbiología. Práctica 2. Esterilización y preparación de medios de cultivo Objetivos Explicar el concepto de esterilización y su utilidad en microbiología. Preparar correctamente
Unidad 2. Técnicas básicas de microbiología. Práctica 2. Esterilización y preparación de medios de cultivo Objetivos Explicar el concepto de esterilización y su utilidad en microbiología. Preparar correctamente
V. Campos y S. Lisperguer / Manual de Laboratorio
 V. Campos y S. Lisperguer / Manual de Laboratorio 1 2 V. Campos y S. Lisperguer / Manual de Laboratorio V. Campos y S. Lisperguer / Manual de Laboratorio 3 a b c Manual de Laboratorio Microbiología Dr.
V. Campos y S. Lisperguer / Manual de Laboratorio 1 2 V. Campos y S. Lisperguer / Manual de Laboratorio V. Campos y S. Lisperguer / Manual de Laboratorio 3 a b c Manual de Laboratorio Microbiología Dr.
TÉCNICO SUPERIOR UNIVERSITARIO EN PROCESOS ALIMENTARIOS EN COMPETENCIAS PROFESIONALES ASIGNATURA DE MICROBIOLOGÍA
 TÉCNICO SUPERIOR UNIVERSITARIO EN PROCESOS ALIMENTARIOS EN COMPETENCIAS PROFESIONALES ASIGNATURA DE MICROBIOLOGÍA 1. Competencias Industrializar materias primas a través de procesos tecnológicos, para
TÉCNICO SUPERIOR UNIVERSITARIO EN PROCESOS ALIMENTARIOS EN COMPETENCIAS PROFESIONALES ASIGNATURA DE MICROBIOLOGÍA 1. Competencias Industrializar materias primas a través de procesos tecnológicos, para
RECOPILADO POR: EL PROGRAMA UNIVERSITARIO DE ALIMENTOS
 NMX-F-187-1978. DETERMINACIÓN DEL NÚMERO MÁS PROBABLE DE GÉRMENES. METHOD OF TEST FOR GERMS MOST PROBABLE NUMBER. NORMAS MEXICANAS. DIRECCIÓN GENERAL DE NORMAS. PREFACIO En la elaboración de esta Norma
NMX-F-187-1978. DETERMINACIÓN DEL NÚMERO MÁS PROBABLE DE GÉRMENES. METHOD OF TEST FOR GERMS MOST PROBABLE NUMBER. NORMAS MEXICANAS. DIRECCIÓN GENERAL DE NORMAS. PREFACIO En la elaboración de esta Norma
TÉCNICO SUPERIOR UNIVERSITARIO EN PROCESOS ALIMENTARIOS
 TÉCNICO SUPERIOR UNIVERSITARIO EN PROCESOS ALIMENTARIOS HOJA DE ASIGNATURA CON DESGLOSE DE UNIDADES TEMÁTICAS 1. Nombre de la asignatura Microbiología. 2. Competencias a la que contribuye la asignatura
TÉCNICO SUPERIOR UNIVERSITARIO EN PROCESOS ALIMENTARIOS HOJA DE ASIGNATURA CON DESGLOSE DE UNIDADES TEMÁTICAS 1. Nombre de la asignatura Microbiología. 2. Competencias a la que contribuye la asignatura
1ª sesión. Unidad 2. Técnicas básicas de microbiología. Práctica 4. Esterilización y preparación de medios de cultivo
 Unidad 2. Técnicas básicas de microbiología. Práctica 4. Esterilización y preparación de medios de cultivo Objetivos Explicar el concepto de esterilización y su utilidad en microbiología. Preparar correctamente
Unidad 2. Técnicas básicas de microbiología. Práctica 4. Esterilización y preparación de medios de cultivo Objetivos Explicar el concepto de esterilización y su utilidad en microbiología. Preparar correctamente
Semana 2. ECOLOGÍA MICROBIANA
 Semana 2. ECOLOGÍA MICROBIANA LUNES 14 DE MAYO PRACTICA # 1A. Columna de Winogradsky 1 matraz aforado de 100 ml 1 matraz Erlenmeyer de 500 ml 1 probeta de 250 ml 1 varilla de vidrio 1 vaso de precipitados
Semana 2. ECOLOGÍA MICROBIANA LUNES 14 DE MAYO PRACTICA # 1A. Columna de Winogradsky 1 matraz aforado de 100 ml 1 matraz Erlenmeyer de 500 ml 1 probeta de 250 ml 1 varilla de vidrio 1 vaso de precipitados
PRÁCTICO N 3. Técnicas para la observación, aislamiento y conservación de microorganismos
 PRÁCTICO N 3 Técnicas para la observación, aislamiento y conservación de microorganismos Objetivos Conocer el manejo del microscopio óptico, sus partes y utilidad en el laboratorio de microbiología. Conocer
PRÁCTICO N 3 Técnicas para la observación, aislamiento y conservación de microorganismos Objetivos Conocer el manejo del microscopio óptico, sus partes y utilidad en el laboratorio de microbiología. Conocer
PROCEDIMIENTO TECNICA NMP STAPHYLOCOCCUS AUREUS EN ALIMENTOS. BAM ONLINE 2001
 PRT-712.02-025 Página 1 de 9 1. OBJETIVO Estimar la densidad de bacterias S. aureus en matrices de alimento o agua como indicador sanitario 2. CAMPO DE APLICACIÓN Y ALCANCE El método de NMP es recomendado
PRT-712.02-025 Página 1 de 9 1. OBJETIVO Estimar la densidad de bacterias S. aureus en matrices de alimento o agua como indicador sanitario 2. CAMPO DE APLICACIÓN Y ALCANCE El método de NMP es recomendado
PRÁCTICA 2.3 Esterilización y Preparación de Medios de Cultivo
 PRÁCTICA 2.3 Esterilización y Preparación de Medios de Cultivo Objetivos Al finalizar este ejercicio el alumno será capaz de: Explicar el concepto de esterilización y su utilidad en microbiología. Preparar
PRÁCTICA 2.3 Esterilización y Preparación de Medios de Cultivo Objetivos Al finalizar este ejercicio el alumno será capaz de: Explicar el concepto de esterilización y su utilidad en microbiología. Preparar
Procedimiento de Muestreo [25] Recipientes de muestreo: Los recipientes de muestro utilizados fueron de
![Procedimiento de Muestreo [25] Recipientes de muestreo: Los recipientes de muestro utilizados fueron de Procedimiento de Muestreo [25] Recipientes de muestreo: Los recipientes de muestro utilizados fueron de](/thumbs/81/84303382.jpg) Apéndice A Procedimiento de Muestreo [25] Recipientes de muestreo: Los recipientes de muestro utilizados fueron de plástico y de vidrio, adecuados para el manejo durante el trabajo de campo y durante el
Apéndice A Procedimiento de Muestreo [25] Recipientes de muestreo: Los recipientes de muestro utilizados fueron de plástico y de vidrio, adecuados para el manejo durante el trabajo de campo y durante el
GUÍA OBSERVACIÓN DE MICROORGANISMOS Y USO DE TINCIONES
 ESCUELA DE SALUD GUÍA OBSERVACIÓN DE MICROORGANISMOS Y USO DE TINCIONES DIRIGIDO A ALUMNOS DE: Técnico de laboratorio Clínico y Banco de Sangre Técnico de Enfermería Técnico de Radiodiagnóstico y Radioterapia
ESCUELA DE SALUD GUÍA OBSERVACIÓN DE MICROORGANISMOS Y USO DE TINCIONES DIRIGIDO A ALUMNOS DE: Técnico de laboratorio Clínico y Banco de Sangre Técnico de Enfermería Técnico de Radiodiagnóstico y Radioterapia
PRÁCTICA No. 4 Métodos de cultivo y descripción morfológica de hongos Introducción
 PRÁCTICA No. 4 Métodos de cultivo y descripción morfológica de hongos Objetivos. Que el alumno aprenda las técnicas de cultivo y manipulación de diferentes tipos de hongos. Que el estudiante conozca las
PRÁCTICA No. 4 Métodos de cultivo y descripción morfológica de hongos Objetivos. Que el alumno aprenda las técnicas de cultivo y manipulación de diferentes tipos de hongos. Que el estudiante conozca las
Unidad 2. Técnicas básicas de microbiología Práctica 5. Preparaciones Microbiológicas
 Unidad 2. Técnicas básicas de microbiología Práctica 5. Preparaciones Microbiológicas Objetivos Realizar diferentes preparaciones microbiológicas a partir de muestras naturales y cultivos puros. Describir
Unidad 2. Técnicas básicas de microbiología Práctica 5. Preparaciones Microbiológicas Objetivos Realizar diferentes preparaciones microbiológicas a partir de muestras naturales y cultivos puros. Describir
UNIVERSIDAD AUTÓNOMA CHAPINGO DEPARTAMENTO DE INGENIERÍA AGROINDUSTRIAL FICHA CURRICULAR
 UNIVERSIDAD AUTÓNOMA CHAPINGO DEPARTAMENTO DE INGENIERÍA AGROINDUSTRIAL FICHA CURRICULAR 1. Datos Generales: Departamento Nombre del Programa Licenciatura Línea curricular Tecnológica Asignatura Biología
UNIVERSIDAD AUTÓNOMA CHAPINGO DEPARTAMENTO DE INGENIERÍA AGROINDUSTRIAL FICHA CURRICULAR 1. Datos Generales: Departamento Nombre del Programa Licenciatura Línea curricular Tecnológica Asignatura Biología
TÉCNICO SUPERIOR UNIVERSITARIO EN AGRICULTURA SUSTENTABLE Y PROTEGIDA EN COMPETENCIAS PROFESIONALES ASIGNATURA DE MICROBIOLOGÍA AGRÍCOLA
 TÉCNICO SUPERIOR UNIVERSITARIO EN AGRICULTURA SUSTENTABLE Y PROTEGIDA EN COMPETENCIAS PROFESIONALES ASIGNATURA DE MICROBIOLOGÍA AGRÍCOLA 1. Competencias Desarrollar el proceso de producción agrícola a
TÉCNICO SUPERIOR UNIVERSITARIO EN AGRICULTURA SUSTENTABLE Y PROTEGIDA EN COMPETENCIAS PROFESIONALES ASIGNATURA DE MICROBIOLOGÍA AGRÍCOLA 1. Competencias Desarrollar el proceso de producción agrícola a
TRABAJO PRÁCTICO N 6 FERTILIZANTES BIOLÓGICOS: DESARROLLO Y CONTROL DE CALIDAD DE INOCULANTES
 TRABAJO PRÁCTICO N 6 FERTILIZANTES BIOLÓGICOS: DESARROLLO Y CONTROL DE CALIDAD DE INOCULANTES Objetivos Conocer los parámetros para la selección de cepas. Conocer las metodologías y procedimientos microbiológicos
TRABAJO PRÁCTICO N 6 FERTILIZANTES BIOLÓGICOS: DESARROLLO Y CONTROL DE CALIDAD DE INOCULANTES Objetivos Conocer los parámetros para la selección de cepas. Conocer las metodologías y procedimientos microbiológicos
PLANIFICACIÓN DE SESIÓN DE APRENDIZAJE
 PLANIFICACIÓN DE SESIÓN DE APRENDIZAJE GRADO UNIDAD SESIÓN HORAS CUARTO 2 6/9 3 TÍTULO DE LA SESIÓN La energía que impulsa la vida APRENDIZAJES ESPERADOS COMPETENCIAS CAPACIDADES INDICADORES Indaga, mediante
PLANIFICACIÓN DE SESIÓN DE APRENDIZAJE GRADO UNIDAD SESIÓN HORAS CUARTO 2 6/9 3 TÍTULO DE LA SESIÓN La energía que impulsa la vida APRENDIZAJES ESPERADOS COMPETENCIAS CAPACIDADES INDICADORES Indaga, mediante
CURSO BUENAS PRÁCTICAS EN EL LABORATORIO DE MICROBIOLOGÍA ALIMENTARIA
 CURSO BUENAS PRÁCTICAS EN EL LABORATORIO DE MICROBIOLOGÍA ALIMENTARIA DESTINATARIOS Este curso está dirigido a Titulados Universitarios, Diplomados Universitarios, Técnicos de formación profesional que
CURSO BUENAS PRÁCTICAS EN EL LABORATORIO DE MICROBIOLOGÍA ALIMENTARIA DESTINATARIOS Este curso está dirigido a Titulados Universitarios, Diplomados Universitarios, Técnicos de formación profesional que
Unidad 2. Técnicas básicas de microbiología Práctica 3. Preparaciones Microbiológicas
 Unidad 2. Técnicas básicas de microbiología Práctica 3. Preparaciones Microbiológicas Objetivos Realizar diferentes preparaciones microbiológicas a partir de muestras naturales y cultivos puros. Describir
Unidad 2. Técnicas básicas de microbiología Práctica 3. Preparaciones Microbiológicas Objetivos Realizar diferentes preparaciones microbiológicas a partir de muestras naturales y cultivos puros. Describir
PREPARACIONES Y TINCIONES
 PREPARACIONES Y TINCIONES PREPARACIONES En fresco Temporales: Microcultivos de hongos, preparaciones de tejidos Fijas: Gram, Ziehl Nielsen, Sheaffer y fulton, SEM, TEM, naranja de acridina. CONTRASTE DE
PREPARACIONES Y TINCIONES PREPARACIONES En fresco Temporales: Microcultivos de hongos, preparaciones de tejidos Fijas: Gram, Ziehl Nielsen, Sheaffer y fulton, SEM, TEM, naranja de acridina. CONTRASTE DE
PARTE EXPERIMENTAL 1 MATERIALES, EQUIPOS Y REACTIVOS 1.1 MATERIAL Y EQUIPOS
 II PARTE EXPERIMENTAL El presente trabajo se realizó en el laboratorio del Centro Latino Americano de Enseñanza e Investigación de Bacteriología Alimentaria (CLEIBA), con sede en la Facultad de Farmacia
II PARTE EXPERIMENTAL El presente trabajo se realizó en el laboratorio del Centro Latino Americano de Enseñanza e Investigación de Bacteriología Alimentaria (CLEIBA), con sede en la Facultad de Farmacia
Microbiología. Carrera: AGF Participantes Representante de las academias de Ingeniería Agronomía de los Institutos Tecnológicos.
 1.- DATOS DE LA ASIGNATURA Nombre de la asignatura: Carrera: Clave de la asignatura: Horas teoría-horas práctica-créditos Microbiología Ingeniería en Agronomía AGF - 0631 2 4 8 2. HISTORIA DEL PROGRAMA
1.- DATOS DE LA ASIGNATURA Nombre de la asignatura: Carrera: Clave de la asignatura: Horas teoría-horas práctica-créditos Microbiología Ingeniería en Agronomía AGF - 0631 2 4 8 2. HISTORIA DEL PROGRAMA
ENUMERACIÓN DE ENTEROBACTERIACEAE EN ALIMENTOS SIN RESUSCITACIÓN. TÉCNICA RECUENTO EN PLACA
 PRT-712.03-040 Página 1 de 6 1. OBJETIVO Determinar el número de Enterobactereaceae presentes en un alimento. 2. CAMPO DE APLICACIÓN Y ALCANCE Aplicar este procedimiento a todas las muestras de alimentos
PRT-712.03-040 Página 1 de 6 1. OBJETIVO Determinar el número de Enterobactereaceae presentes en un alimento. 2. CAMPO DE APLICACIÓN Y ALCANCE Aplicar este procedimiento a todas las muestras de alimentos
Técnicas de monitoreo para la detección de microorganismos en el medio ambiente
 Técnicas de monitoreo para la detección de microorganismos en el medio ambiente Gloria Alicia Figueroa Aguilar Condiciones Ambientales REQUISITO: El laboratorio debe asegurarse que las condiciones ambientales,
Técnicas de monitoreo para la detección de microorganismos en el medio ambiente Gloria Alicia Figueroa Aguilar Condiciones Ambientales REQUISITO: El laboratorio debe asegurarse que las condiciones ambientales,
ING. IRMA CASTILLO CARMONA CLISERIA RENDON DORANTES TECNICAS DE CULTIVOS VEGETALES FECHA: 19 DE MARZO DE 2013
 ING. IRMA CASTILLO CARMONA CLISERIA RENDON DORANTES TECNICAS DE CULTIVOS VEGETALES FECHA: 19 DE MARZO DE 2013 GENERALIDADES Solución Formulación MEDIO DE CULTIVO Los medios de cultivo constituyen un elemento
ING. IRMA CASTILLO CARMONA CLISERIA RENDON DORANTES TECNICAS DE CULTIVOS VEGETALES FECHA: 19 DE MARZO DE 2013 GENERALIDADES Solución Formulación MEDIO DE CULTIVO Los medios de cultivo constituyen un elemento
PRACTICAS ADECUADAS EN EL LABORATORIO DE MICROBIOLOGIA CAPITULO 1117, 1051 (USP 40) Farmacopea Nacional de los Estados Unidos Mexicanos (FEUM)
 PRACTICAS ADECUADAS EN EL LABORATORIO DE MICROBIOLOGIA CAPITULO 1117, 1051 (USP 40) Farmacopea Nacional de los Estados Unidos Mexicanos (FEUM) Norma Oficial Mexicana NOM-059-SSA1-2015 INSTALACIONES Áreas
PRACTICAS ADECUADAS EN EL LABORATORIO DE MICROBIOLOGIA CAPITULO 1117, 1051 (USP 40) Farmacopea Nacional de los Estados Unidos Mexicanos (FEUM) Norma Oficial Mexicana NOM-059-SSA1-2015 INSTALACIONES Áreas
NMX-BB-040-SCFI-1999 MÉTODOS GENERALES DE ANÁLISIS - DETERMINACIÓN DE LA ACTIVIDAD ANTIMICROBIANA EN PRODUCTOS GERMICIDAS
 MÉTODOS GENERALES DE ANÁLISIS - DETERMINACIÓN DE LA ACTIVIDAD ANTIMICROBIANA EN PRODUCTOS GERMICIDAS GENERAL METHODS FOR ANALYSIS - ANTIMICROBIAL ACTIVITY DETERMINATION TO GERMICIDAL PRODUCTS PREFACIO
MÉTODOS GENERALES DE ANÁLISIS - DETERMINACIÓN DE LA ACTIVIDAD ANTIMICROBIANA EN PRODUCTOS GERMICIDAS GENERAL METHODS FOR ANALYSIS - ANTIMICROBIAL ACTIVITY DETERMINATION TO GERMICIDAL PRODUCTS PREFACIO
PM 8b Técnicas de siembra -1- 7e&1,&$6'(6,(0%5$
 PM 8b Técnicas de siembra -1-7e&1,&$6'(6,(0%5$ 2%-(7,926(63(&Ë),&26 Proporcionar los medios adecuados para que los alumnos trabajen en condiciones de esterilidad. Manejar el material que se empleará en
PM 8b Técnicas de siembra -1-7e&1,&$6'(6,(0%5$ 2%-(7,926(63(&Ë),&26 Proporcionar los medios adecuados para que los alumnos trabajen en condiciones de esterilidad. Manejar el material que se empleará en
Objetivos. S Determinar la presencia de bacterias coliformes en una muestra de agua
 Análisis del agua S Objetivos S Determinar la presencia de bacterias coliformes en una muestra de agua Introducción S Las tres pruebas básicas para determinar la presencia de bacterias coliformes (asociada
Análisis del agua S Objetivos S Determinar la presencia de bacterias coliformes en una muestra de agua Introducción S Las tres pruebas básicas para determinar la presencia de bacterias coliformes (asociada
Título de la gráfica: Crecimiento/ No crecimiento
 Resultados de la semana anterior (TSB) Título de la gráfica: # tubo TSB 1-24 Crecimiento/ No crecimiento Descripción del crecimiento Resultados de la semana anterior (TSA slant) Título de la gráfica: tubo
Resultados de la semana anterior (TSB) Título de la gráfica: # tubo TSB 1-24 Crecimiento/ No crecimiento Descripción del crecimiento Resultados de la semana anterior (TSA slant) Título de la gráfica: tubo
GUÍA REALIZACIÓN DE CULTIVOS MICROBIOLÓGICOS
 ESCUELA DE SALUD GUÍA REALIZACIÓN DE CULTIVOS MICROBIOLÓGICOS DIRIGIDO A ALUMNOS DE: Técnico de laboratorio Clínico y Banco de Sangre Técnico de Enfermería Técnico de Radiodiagnóstico y Radioterapia Informática
ESCUELA DE SALUD GUÍA REALIZACIÓN DE CULTIVOS MICROBIOLÓGICOS DIRIGIDO A ALUMNOS DE: Técnico de laboratorio Clínico y Banco de Sangre Técnico de Enfermería Técnico de Radiodiagnóstico y Radioterapia Informática
FICHAS DE PRÁCTICAS DE BIOLOGÍA 4º ESO BIOLOGÍA
 FICHAS DE PRÁCTICAS DE BIOLOGÍA 4º ESO BIOLOGÍA UNIDAD DIDÁCTICA : CÉLULAS Y TEJIDOS 01.- Células animales y vegetales Duración Estimada: 1h 40 min Capacidad Terminal Observación de células animales y
FICHAS DE PRÁCTICAS DE BIOLOGÍA 4º ESO BIOLOGÍA UNIDAD DIDÁCTICA : CÉLULAS Y TEJIDOS 01.- Células animales y vegetales Duración Estimada: 1h 40 min Capacidad Terminal Observación de células animales y
FICHA TECNICA DE PRODUCTO N. 285
 FICHA TECNICA DE PRODUCTO N. 285 ALCOHOL ETÍLICO AL 99,9% V/V. 51102710 GRADO REACTIVO. FICHA DE DATOS DE SEGURIDAD (FDS) FRASCO X LITRO FECHA DE VENCIMIENTO MINIMA DE 2 AÑOS A PARTIR DE LA ENTREGA. MARCA
FICHA TECNICA DE PRODUCTO N. 285 ALCOHOL ETÍLICO AL 99,9% V/V. 51102710 GRADO REACTIVO. FICHA DE DATOS DE SEGURIDAD (FDS) FRASCO X LITRO FECHA DE VENCIMIENTO MINIMA DE 2 AÑOS A PARTIR DE LA ENTREGA. MARCA
Objetivos Describir los efectos de diferentes factores físicos en el crecimiento de bacterias.
 Unidad 8. Condiciones ambientales para el desarrollo, inhibición y destrucción de microorganismos. Práctica 8. Efecto de los factores ambientales y químicos Objetivos Describir los efectos de diferentes
Unidad 8. Condiciones ambientales para el desarrollo, inhibición y destrucción de microorganismos. Práctica 8. Efecto de los factores ambientales y químicos Objetivos Describir los efectos de diferentes
Bioseguridad en el Laboratorio de Microbiología
 Bioseguridad en el Laboratorio de Microbiología Objetivos Al finalizar la práctica el estudiante será capaz de: Aplicar las reglas básicas de higiene y seguridad para los laboratorios del área microbiológica.
Bioseguridad en el Laboratorio de Microbiología Objetivos Al finalizar la práctica el estudiante será capaz de: Aplicar las reglas básicas de higiene y seguridad para los laboratorios del área microbiológica.
Universidad Nacional de Ingeniería UNI Norte. Métodos de detección de contaminación microbiana
 Universidad Nacional de Ingeniería UNI Norte Curso: Un enfoque práctico para la inocuidad de los alimentos Métodos de detección de contaminación microbiana iciar el explorador Internet Explorer.lnk Facilitadoras
Universidad Nacional de Ingeniería UNI Norte Curso: Un enfoque práctico para la inocuidad de los alimentos Métodos de detección de contaminación microbiana iciar el explorador Internet Explorer.lnk Facilitadoras
PRACTICA Núm. 18 INVESTIGACION DE COLIFORMES TOTALES Y FECALES EN AGUA RESIDUAL
 I. OBJETIVO PRACTICA Núm. 18 INVESTIGACION DE COLIFORMES TOTALES Y FECALES EN AGUA RESIDUAL Determinar la presencia de coliformes totales y fecales en agua residual por el método del Número Más Probable,
I. OBJETIVO PRACTICA Núm. 18 INVESTIGACION DE COLIFORMES TOTALES Y FECALES EN AGUA RESIDUAL Determinar la presencia de coliformes totales y fecales en agua residual por el método del Número Más Probable,
UNIVERSIDAD JUAREZ AUTONOMA DE TABASCO DIVISIÓN ACADEMICA DE CIENCIAS BIOLOGICAS LICENCIATURA EN ECOLOGIA
 UNIVERSIDAD JUAREZ AUTONOMA TABASCO DIVISIÓN ACAMICA CIENCIAS BIOLOGICAS LICENCIATURA EN ECOLOGIA ASIGNATURA: MICROBIOLOGÍA AREA : SUSTANTIVA PROFESIONAL HORAS TEÓRICAS: 2 HORAS PRÁCTICAS: 4 CRÉDITOS:
UNIVERSIDAD JUAREZ AUTONOMA TABASCO DIVISIÓN ACAMICA CIENCIAS BIOLOGICAS LICENCIATURA EN ECOLOGIA ASIGNATURA: MICROBIOLOGÍA AREA : SUSTANTIVA PROFESIONAL HORAS TEÓRICAS: 2 HORAS PRÁCTICAS: 4 CRÉDITOS:
Medición del crecimiento Microbiano
 Medición del crecimiento Microbiano Determinación del número de microorganismos en una muestra. Determinación de la actividad metabólica, biomasa y proteínas. Métodos para el conteo de microorganismos
Medición del crecimiento Microbiano Determinación del número de microorganismos en una muestra. Determinación de la actividad metabólica, biomasa y proteínas. Métodos para el conteo de microorganismos
USP FEUM ÍFICO CIENT Límites microbianos ENCUENTRO MEMORIAS
 Límites microbianos Origen de técnicas de cultivo en medios sólidos En 1881 dentro del Congreso Médico Internacional en Londres, Robert Koch describió un método de cultivo de microorganismos empleando
Límites microbianos Origen de técnicas de cultivo en medios sólidos En 1881 dentro del Congreso Médico Internacional en Londres, Robert Koch describió un método de cultivo de microorganismos empleando
PRACTICA Núm. 19 DETERMINACION DE ESTREPTOCOCOS FECALES EN AGUA
 PRACTICA Núm. 19 DETERMINACION DE ESTREPTOCOCOS FECALES EN AGUA I. OBJETIVO Investigar la presencia de Estreptococos fecales en una muestra de agua mediante la técnica del Número Más Probable (NMP) usando
PRACTICA Núm. 19 DETERMINACION DE ESTREPTOCOCOS FECALES EN AGUA I. OBJETIVO Investigar la presencia de Estreptococos fecales en una muestra de agua mediante la técnica del Número Más Probable (NMP) usando
NMP PARA LA DETERMINACION DE COLIFORMESY COLIFORMES FECALES EN AGUAS
 PRT-712.03-005 Página 1 de 6 1. OBJETIVO Este método es utilizado para estimar la densidad de bacterias del grupo coliformes y conocer la calidad sanitaria en aguas crudas 2. CAMPO DE APLICACIÓN Y ALCANCE
PRT-712.03-005 Página 1 de 6 1. OBJETIVO Este método es utilizado para estimar la densidad de bacterias del grupo coliformes y conocer la calidad sanitaria en aguas crudas 2. CAMPO DE APLICACIÓN Y ALCANCE
Materiales. Cultivos puros de hongos: Saccharomyces cerevisiae Rhodototula sp Penicillum sp Aspergillus niger Rhizopous sp Alternaria sp Fusarium sp
 Unidad 3. Estudio de cultivos bacterianos puros y Unidad 4. Estudio microscópico y cultivo de hongos algas y protozoarios Práctica 5. Técnicas de siembra y cultivo de bacterias y hongos Objetivos Aplicar
Unidad 3. Estudio de cultivos bacterianos puros y Unidad 4. Estudio microscópico y cultivo de hongos algas y protozoarios Práctica 5. Técnicas de siembra y cultivo de bacterias y hongos Objetivos Aplicar
1 MATERIALES Y MÉTODOS
 1 MATERIALES Y MÉTODOS 1.1 ESQUEMA DE TRABAJO Toma de muestras mesofílicos aerobios por cuenta en placa (UFC*). coniformes fecales mediante NMP * Vibrio cholerae O1 Salmonella Staphyloccoccus aureus *NMP,
1 MATERIALES Y MÉTODOS 1.1 ESQUEMA DE TRABAJO Toma de muestras mesofílicos aerobios por cuenta en placa (UFC*). coniformes fecales mediante NMP * Vibrio cholerae O1 Salmonella Staphyloccoccus aureus *NMP,
UNIVERSIDAD DE CIENCIAS Y ARTES DE CHIAPAS
 FACULTAD DE CIENCIAS DE LA NUTRICIÓN Y ALIMENTOS LICENCIATURA EN NUTRIOLOGÍA MANUAL DE PRÁCTICAS PARA LA EXPERIENCIA ACADÉMICA MICROBIOLOGÍA Y PARASITOLOGÍA ELABORO: Q.F.B. MARÍA DOLORES TOLEDO MEZA ACTUALIZÓ:
FACULTAD DE CIENCIAS DE LA NUTRICIÓN Y ALIMENTOS LICENCIATURA EN NUTRIOLOGÍA MANUAL DE PRÁCTICAS PARA LA EXPERIENCIA ACADÉMICA MICROBIOLOGÍA Y PARASITOLOGÍA ELABORO: Q.F.B. MARÍA DOLORES TOLEDO MEZA ACTUALIZÓ:
TÉCNICAS PARA LA ENUMERACIÓN DE MICROORGANISMOS.
 TÉCNICAS PARA LA ENUMERACIÓN DE MICROORGANISMOS. ANÁLISIS MICROBIOLÓGICO DEL AGUA Y OTRAS MUESTRAS. Objetivos Al finalizar este ejercicio el alumno será capaz de: Explicar el fundamento de la técnicas
TÉCNICAS PARA LA ENUMERACIÓN DE MICROORGANISMOS. ANÁLISIS MICROBIOLÓGICO DEL AGUA Y OTRAS MUESTRAS. Objetivos Al finalizar este ejercicio el alumno será capaz de: Explicar el fundamento de la técnicas
Aislamiento de Microorganismos (1ª Sesión)
 Aislamiento de Microorganismos (1ª Sesión) Objetivos Al finalizar esta práctica el alumno será capaz de: Explicar el fundamento de diferentes medios de cultivo y condiciones de incubación para el aislamiento
Aislamiento de Microorganismos (1ª Sesión) Objetivos Al finalizar esta práctica el alumno será capaz de: Explicar el fundamento de diferentes medios de cultivo y condiciones de incubación para el aislamiento
Clostridium perfringens
 Clostridium perfringens Introducción Cuando se lanza un producto alimentario al mercado se deben tener en cuenta varios parámetros que le otorgan calidad al producto, uno de ellos es la inocuidad. Los
Clostridium perfringens Introducción Cuando se lanza un producto alimentario al mercado se deben tener en cuenta varios parámetros que le otorgan calidad al producto, uno de ellos es la inocuidad. Los
PROCEDIMIENTO TECNICA DE COAGULASA EN TUBO PRT
 Página 1 de 7 1. OBJETIVO Comprobar la facultad de las unidades formadoras de colonias de S. aureus presentes en una muestra de alimento, de coagular el plasma de conejo por acción de la enzima coagulasa
Página 1 de 7 1. OBJETIVO Comprobar la facultad de las unidades formadoras de colonias de S. aureus presentes en una muestra de alimento, de coagular el plasma de conejo por acción de la enzima coagulasa
MÉTODOS BÁSICOS DE ENUMERACIÓN DE POBLACIONES BACTERIANAS
 MÉTODOS BÁSICOS DE ENUMERACIÓN DE POBLACIONES BACTERIANAS ACTIVIDADES. SOLUCIONES PROPUESTAS Inés Arana, Maite Orruño Departamento Inmunología, Microbiología y Parasitología Universidad del País Vasco/Euskal
MÉTODOS BÁSICOS DE ENUMERACIÓN DE POBLACIONES BACTERIANAS ACTIVIDADES. SOLUCIONES PROPUESTAS Inés Arana, Maite Orruño Departamento Inmunología, Microbiología y Parasitología Universidad del País Vasco/Euskal
PRACTICA Núm. 6 TINCION DE FLAGELOS BACTERIANOS POR EL METODO DE LEIFSON
 PRACTICA Núm. 6 TINCION DE FLAGELOS BACTERIANOS POR EL METODO DE LEIFSON I. OBJETIVO Demostrar la presencia de flagelos mediante tinción y observar la movilidad que presentan algunas bacterias diferenciándola
PRACTICA Núm. 6 TINCION DE FLAGELOS BACTERIANOS POR EL METODO DE LEIFSON I. OBJETIVO Demostrar la presencia de flagelos mediante tinción y observar la movilidad que presentan algunas bacterias diferenciándola
AISLAMIENTO DE MICROORGANISMOS
 PRÁCTICA5 AISLAMIENTO DE MICROORGANISMOS Introducción En la naturaleza, la mayoría de los microorganismos no se encuentran aislados, sino integrados en poblaciones mixtas. Para llevar a cabo el estudio
PRÁCTICA5 AISLAMIENTO DE MICROORGANISMOS Introducción En la naturaleza, la mayoría de los microorganismos no se encuentran aislados, sino integrados en poblaciones mixtas. Para llevar a cabo el estudio
NMP PARA LA DETERMINACION DE COLIFORMES Y Escherichia coli EN ALIMENTOS BASADO EN BAM on line
 COLIFORMES Y Escherichia coli EN ME-712.02-004 Página 1 de 9 1. OBJETIVO Estimar la densidad de bacterias del grupo coliformes, como indicador sanitario en alimentos. 2. CAMPO DE APLICACIÓN Y ALCANCE Aplicar
COLIFORMES Y Escherichia coli EN ME-712.02-004 Página 1 de 9 1. OBJETIVO Estimar la densidad de bacterias del grupo coliformes, como indicador sanitario en alimentos. 2. CAMPO DE APLICACIÓN Y ALCANCE Aplicar
SÍNTESIS DE LA PROGRAMACIÓN
 www.iesanctipetri.com Modelo MD7501PR05 Rev.: 1 Página 1 de 6 CURSO ACADÉMICO GRUPO MÓDULO PROFESOR/A 2017/2018 2ºLCB- A y B Microbiología clínica D. Manuel Prado Fernández D. José Nacente Aleu RESULTADOS
www.iesanctipetri.com Modelo MD7501PR05 Rev.: 1 Página 1 de 6 CURSO ACADÉMICO GRUPO MÓDULO PROFESOR/A 2017/2018 2ºLCB- A y B Microbiología clínica D. Manuel Prado Fernández D. José Nacente Aleu RESULTADOS
PRÁCTICA 6.1 Nutrición Microbiana y Requerimientos de Oxígeno
 PRÁCTICA 6.1 Nutrición Microbiana y Requerimientos de Oxígeno Objetivos Determinar las características nutricionales de diferentes microorganismos considerando las fuentes de carbono, energía y nitrógeno.
PRÁCTICA 6.1 Nutrición Microbiana y Requerimientos de Oxígeno Objetivos Determinar las características nutricionales de diferentes microorganismos considerando las fuentes de carbono, energía y nitrógeno.
Microbiología. Trabajo Práctico 3. Cultivo e identificación de bacterias. GRACIELA NATALIA PUCCI
 Microbiología Trabajo Práctico 3. Cultivo e identificación de bacterias. GRACIELA NATALIA PUCCI Objetivos: Reconocer los distintos medios de cultivo utilizados para la recuperación de bacterias, y comprender
Microbiología Trabajo Práctico 3. Cultivo e identificación de bacterias. GRACIELA NATALIA PUCCI Objetivos: Reconocer los distintos medios de cultivo utilizados para la recuperación de bacterias, y comprender
PROCEDIMIENTO RECUENTO MOHOS Y LEVADURAS EN ALIMENTOS NORMA ISO 7954
 PRT- 712.02-031 Página 1 de 9 1. OBJETIVO Conocer el número de Mohos y Levaduras que contiene un alimento. 2. CAMPO DE APLICACIÓN Y ALCANCE Este procedimiento se aplica a todos los alimentos de consumos
PRT- 712.02-031 Página 1 de 9 1. OBJETIVO Conocer el número de Mohos y Levaduras que contiene un alimento. 2. CAMPO DE APLICACIÓN Y ALCANCE Este procedimiento se aplica a todos los alimentos de consumos
PRACTICA N 02: PROCESOS FERMENTATIVOS: PRODUCCION DE PROTEÍNA UNICELULAR O BIOMASA
 PRACTICA N 02: PROCESOS FERMENTATIVOS: PRODUCCION DE PROTEÍNA UNICELULAR O BIOMASA Capacidades a lograr: 1. Conoce y aplica técnicas de siembra, cultivo y cuantificación del proceso fermentativo para producción
PRACTICA N 02: PROCESOS FERMENTATIVOS: PRODUCCION DE PROTEÍNA UNICELULAR O BIOMASA Capacidades a lograr: 1. Conoce y aplica técnicas de siembra, cultivo y cuantificación del proceso fermentativo para producción
Bioseguridad en el Laboratorio de Microbiología
 Objetivos Bioseguridad en el Laboratorio de Microbiología Al finalizar la práctica el estudiante será capaz de: Analizar la importancia que tienen las reglas básicas de higiene y seguridad, tanto en las
Objetivos Bioseguridad en el Laboratorio de Microbiología Al finalizar la práctica el estudiante será capaz de: Analizar la importancia que tienen las reglas básicas de higiene y seguridad, tanto en las
Análisis Microbiológico de aguas.
 Análisis Microbiológico de aguas. Laboratorio. Dolores Garvi Higueras. sedceroya@us.es www.aguapedia.org Índice. 1. Legislación 2. Toma de muestras 3. Medios de cultivo 4. Esterilización 5. Material 6.
Análisis Microbiológico de aguas. Laboratorio. Dolores Garvi Higueras. sedceroya@us.es www.aguapedia.org Índice. 1. Legislación 2. Toma de muestras 3. Medios de cultivo 4. Esterilización 5. Material 6.
PRÁCTICAS DEL LABORATORIO DE MICROBIOLOGÍA: BACTERIOLOGÍA Y MICOLOGÍA
 PRÁCTICAS DEL LABORATORIO DE MICROBIOLOGÍA: BACTERIOLOGÍA Y MICOLOGÍA Mª PAZ MERINO JIMÉNEZ MIREIA LLINARES MARCELO PRÁCTICAS DEL LABORATORIO DE MICROBIOLOGÍA: BACTERIOLOGÍA Y MICOLOGÍA A mi padre. M.
PRÁCTICAS DEL LABORATORIO DE MICROBIOLOGÍA: BACTERIOLOGÍA Y MICOLOGÍA Mª PAZ MERINO JIMÉNEZ MIREIA LLINARES MARCELO PRÁCTICAS DEL LABORATORIO DE MICROBIOLOGÍA: BACTERIOLOGÍA Y MICOLOGÍA A mi padre. M.
ESTRATEGIAS PARA EL CONTROL HIGIENICO SANITARIO DE ALIMENTARIAS. 21 Mayo de 2015
 ESTRATEGIAS PARA EL CONTROL HIGIENICO SANITARIO DE SUPERFICIES EN INDUSTRIAS ALIMENTARIAS. METODOS DIRECTOS E INDIRECTOS 21 Mayo de 2015 CRITERIOS MICROBIOLOGICOS PARA EL CONTROL AMBIENTAL INDICADORES
ESTRATEGIAS PARA EL CONTROL HIGIENICO SANITARIO DE SUPERFICIES EN INDUSTRIAS ALIMENTARIAS. METODOS DIRECTOS E INDIRECTOS 21 Mayo de 2015 CRITERIOS MICROBIOLOGICOS PARA EL CONTROL AMBIENTAL INDICADORES
Los pasos a seguir para la toma de material a partir de abscesos de origen bucal son:
 Trabajos Prácticos Nº 6 y 7 Diagnóstico microbiológico directo Objetivos. Describir la importancia de la toma de muestra en el diagnóstico etiológico de un absceso de origen bucal. Describir los requisitos
Trabajos Prácticos Nº 6 y 7 Diagnóstico microbiológico directo Objetivos. Describir la importancia de la toma de muestra en el diagnóstico etiológico de un absceso de origen bucal. Describir los requisitos
Trabajo Práctico Nº4: Análisis Bacteriológico del Agua. Lic Soria José
 Trabajo Práctico Nº4: Análisis Bacteriológico del Agua Lic Soria José Las fuentes del Agua Se considera agua potable de suministro público y agua potable de uso domiciliario la que es apta para la alimentación
Trabajo Práctico Nº4: Análisis Bacteriológico del Agua Lic Soria José Las fuentes del Agua Se considera agua potable de suministro público y agua potable de uso domiciliario la que es apta para la alimentación
Laboratorio Lavado y Arreglo de material
 1 de 5 TABLA DE CONTENIDO INDICE PÁGINA 1. PROCESO 2 2. RESPONSABLES 2 3. OBJETIVO GENERAL 2 4. ALCANCE 2 5. MARCO LEGAL 2 6. DESCRIPCIÓN DE LA ACTIVIDAD 3 7. INSUMOS, REACTIVOS Y EQUIPOS 4 8.1 Insumos
1 de 5 TABLA DE CONTENIDO INDICE PÁGINA 1. PROCESO 2 2. RESPONSABLES 2 3. OBJETIVO GENERAL 2 4. ALCANCE 2 5. MARCO LEGAL 2 6. DESCRIPCIÓN DE LA ACTIVIDAD 3 7. INSUMOS, REACTIVOS Y EQUIPOS 4 8.1 Insumos
UNIVERSIDAD DE PUERTO RICO EN HUMACAO DEPARTAMENTO DE BIOLOGÍA PRONTUARIO DEL LABORATORIO DE MICROBIOLOGÍA GENERAL BIOL 3707
 UNIVERSIDAD DE PUERTO RICO EN HUMACAO DEPARTAMENTO DE BIOLOGÍA PRONTUARIO DEL LABORATORIO DE MICROBIOLOGÍA GENERAL BIOL 3707 Actualizado por: DR. HÉCTOR L. AYALA DEL RÍO 2005 UPR-H Departamento de Biología-BIOL
UNIVERSIDAD DE PUERTO RICO EN HUMACAO DEPARTAMENTO DE BIOLOGÍA PRONTUARIO DEL LABORATORIO DE MICROBIOLOGÍA GENERAL BIOL 3707 Actualizado por: DR. HÉCTOR L. AYALA DEL RÍO 2005 UPR-H Departamento de Biología-BIOL
UNIVERSIDAD DE EL SALVADOR FACULTAD DE QUÍMICA Y FARMACIA
 1 UNIVERSIDAD DE EL SALVADOR MANUAL PARA LA CONSERVACIÓN DE CEPAS BACTERIANAS DE TRABAJO SAN SALVADOR, EL SALVADOR, CENTRO AMERICA UNIVERSIDAD DE EL SALVADOR DEPARTAMENTO DE BIOQUIMICA Y Código CONTAMINACIÓN
1 UNIVERSIDAD DE EL SALVADOR MANUAL PARA LA CONSERVACIÓN DE CEPAS BACTERIANAS DE TRABAJO SAN SALVADOR, EL SALVADOR, CENTRO AMERICA UNIVERSIDAD DE EL SALVADOR DEPARTAMENTO DE BIOQUIMICA Y Código CONTAMINACIÓN
Por qué en un resultado positivo siempre cambia a amarillo intenso pero solo algunos emiten fluorescencia?
 Biología 3725 L COLILERT Por qué en un resultado positivo siempre cambia a amarillo intenso pero solo algunos emiten fluorescencia? ENTEROLERT Cuál es el propósito de utilizar enterolert, que nos dice
Biología 3725 L COLILERT Por qué en un resultado positivo siempre cambia a amarillo intenso pero solo algunos emiten fluorescencia? ENTEROLERT Cuál es el propósito de utilizar enterolert, que nos dice
Laboratorio de Agroindustria II. Calidad de Leche
 Laboratorio de Agroindustria II. Calidad de Leche Medio de cultivo: Caldo lactosado biliado verde brillante (Brilliant Green Bile Lactose: BGBL) Composición - Peptona 10 g. - Lactosa 10 g. - Bilis de buey
Laboratorio de Agroindustria II. Calidad de Leche Medio de cultivo: Caldo lactosado biliado verde brillante (Brilliant Green Bile Lactose: BGBL) Composición - Peptona 10 g. - Lactosa 10 g. - Bilis de buey
TEMA 12. Pruebas de sensibilidad a los antimicrobianos
 TEMA 12 Pruebas de sensibilidad a los antimicrobianos Tema 12. Pruebas de sensibilidad a los antimicrobianos 1. Nacimiento de la era de los antibióticos 2. Pruebas de sensibilidad a los antimicrobianos
TEMA 12 Pruebas de sensibilidad a los antimicrobianos Tema 12. Pruebas de sensibilidad a los antimicrobianos 1. Nacimiento de la era de los antibióticos 2. Pruebas de sensibilidad a los antimicrobianos
GUIAS PRACTICAS PARA LOS LABORATORIOS DE BACTERIOLOGIA CLINICA
 GUIAS PRACTICAS PARA LOS LABORATORIOS DE GUIAS PRACTICAS PARA LOS LABORATORIOS DE Duración: 80 horas Precio: consultar euros. Modalidad: A distancia Metodología: El Curso será desarrollado con una metodología
GUIAS PRACTICAS PARA LOS LABORATORIOS DE GUIAS PRACTICAS PARA LOS LABORATORIOS DE Duración: 80 horas Precio: consultar euros. Modalidad: A distancia Metodología: El Curso será desarrollado con una metodología
