10.8. Balances de carga y materia
|
|
|
- Asunción Gómez Rodríguez
- hace 9 años
- Vistas:
Transcripción
1 10.8. Balances de carga y materia La determinación de la concentración de todas las especies en equilibrio de la disolución acuosa diluida de ácidos y bases se resume a un problema de N ecuaciones no lineales con N incógnitas, más la condición que no puede haber ninguna concentración negativa, lo que permite elegir una, entre todas las posibles soluciones. A la hora de resolver un problema de este tipo, lo primero que debemos hacer es escribir una lista de todas las moléculas e iones en disolución, excepto el disolvente, que es el agua, cuya concentración, M, es conocida (consideramos que en un litro de disolución diluida hay un kilogramo de agua, de peso molecular 18, lo que conduce a una concentración 1000/18=55.55 M). El resto de especies están todas en concentración muy diluida y constituyen la lista de incógnitas a determinar, empezando por los protones e hidroxilos, más todas las especies que se forman en la disolución. Pues bien, una vez escrita la lista, contamos las especies cuya concentración desconocemos. El resultado es el número de incógnitas. Debemos ahora escribir tantas ecuaciones como incógnitas tenemos. La primera de 14 las ecuaciones es el producto iónico del agua: K w = 10 = [ H ][ OH ]. A continuación escribimos todas las ecuaciones de equilibrio, cuyas respectivas constantes vendrán dadas en el enunciado del problema o debemos buscar en tablas. Seguidamente escribiremos el balance de cargas. Obviamente, sólo existe un balance de de cargas que nos dice que, puesto que la disolución es electro-neutra, habrá tantas carga positivas como negativas. Volveremos más tarde sobre como escribir la ecuación de este balance. Contamos ahora cuantas ecuaciones hemos escrito y por tanto cuantas nos quedan hasta llegar al número de incógnitas. El número resultante coincide con el número de balances de materia que podemos establecer y que más tarde volveremos sobre el detalle de cómo plantearlos. Con esto hemos escrito tantas ecuaciones como incógnitas teníamos. Como el sistema de ecuaciones no es lineal habrá más de una solución. Ahora bien, entre todas las soluciones sólo habrá una que tendrá sentido y es la que debemos escoger. Típicamente sólo encontraremos una en que todas las concentraciones son positivas. Volvamos sobre los balances de materia. Se establece uno por cada ácido y uno por cada base que añadimos en disolución, entendiendo que una sal está compuesta de ácidos y bases. Con esto último quiere decirse que si tenemos, por ejemplo, una disolución de acetato amónico CH 3 COONH 4 o simplemente AcNH 4, tenemos en realidad la base anión acetato Ac y el ácido catión amonio N 4. Consideremos un primer ejemplo sencillo: la disolución de un ácido débil, por ejemplo de ácido acético AcH. Empezamos con la lista de incógnitas. En primer lugar está el agua que genera protones e hidroxilos OH y en segundo y último lugar está el ácido acético que por ser un ácido débil se disocia parcialmente dando lugar a acetato, Ac, más protones. Esto viene esquematizado en la figura siguiente.
2 HAc Ac OH En este caso hay cuatro incógnitas (HAc, Ac,, OH ). Entre las ecuaciones tenemos el producto iónico 14 del agua: K w = 10 = [ H ][ OH ], el equilibrio de disociación del ácido acético, K a [ Ac ][ H ] =, [ HAc] y el balance de cargas, esto es, el que la suma de cargas positivas es igual al de negativas. En este caso: número de iones = número de iones Ac número iones OH. Si dividimos ambos miembros por el número de Avogadro obtenemos la ecuación equivalente: número de moles = número de moles Ac número moles OH. Si finalmente dividimos por el volumen, encontramos concentraciones: [ H ] = [ Ac ] [OH ]. Podremos ahora establecer tantos balances de materia como ecuaciones necesitemos, hasta tener tantas como incógnitas. En este caso sólo una, pues tenemos la disolución de una sola especie (en nuestro caso ácida). La figura ejemplifica como debemos plantear el balance material. Representamos allí por un cuadro grande los moles de ácido acético que añadimos inicialmente para preparar un litro de disolución y por un círculo el agua. Cuando se alcanza el equilibrio, el acético se disocia, de manera que parte del acético inicial desaparece (el cuadro oscuro) dando lugar a sendos cuadros de Ac y. También el agua genera algunos protones e hidroxilos, pero no sabemos cuantos. Por ello, el balance material, que equivale a decir que debemos restituir el cuadro eliminado, sólo lo podemos establecer sumando las concentraciones de AcH y 0. Ac - en equilibrio: [ HAc] = [ HAc] [ Ac ] Pasemos a un caso un poco más complicado: la disolución de un ácido diprótico, como por ejemplo el ácido sulfhídrico H 2 S. La lista de especies en disolución es:, OH, H 2 S, HS, S =. Hay pues cinco incógnitas y deberá haber cinco ecuaciones. En primer lugar tenemos el producto iónico del agua. A continuación, las dos ecuaciones de disociación del ácido sulfhídrico y por último el balance de cargas. Queda pues una incógnita
3 por cubrir, que lo haremos con un balance material correspondiente a la única especie que hemos añadido para hacer la disolución. H 2 S HS OH S = De nuevo la figura nos da la clave para establecer el balance. Cuando se establece el equilibrio parte del H 2 S desaparece (cuadro negro mayor) para formar la correspondiente cantidad de HS (cuadro blanco mediano) y. El HS, a su vez, se disocia y parte desaparece (cuadro negro pequeño) para formar la correspondiente cantidad de S = (cuadro blanco pequeño) y. Como antes, el agua aporta también protones e hidroxilos en una cantidad desconocida que no permite tomar estas especies a la hora de hacer balances (restituir el cuadro = 2 0 = 2. inicial). El balance material queda pues: [ H S ] [ H S ] [ HS ] [ S ] Veamos ahora el balance de cargas. Hemos de contar por una parte las cargas positivas, que en este caso sólo son protones, y por otra las negativas, que aparecen en las especies siguientes OH, HS y S =. Ahora, y esto es importante, debemos recordar que estamos contando número de cargas y no número de especies que las llevan. Por ello, el número de cargas negativas será [ OH ] [ HS ] 2 [ S ]. Es decir contamos dos veces el número de especies que llevan dos cargas. Podemos hacer un símil. Supongamos que tenemos A monocicletas (de una rueda) y B bicicletas (de dos ruedas). El numero total de ruedas será A2B, ya que habrá una rueda por cada monocicleta pero dos por cada bicicleta. Y si hubiese coches, contaríamos cuatro veces cada coche, que tiene cuatro ruedas! Pasemos a un caso un poco más complicado aún: Hemos preparado la disolución añadiendo un ácido y una base. Por ejemplo acético y amoniaco. La lista de especies en disolución es:, OH, HAc, Ac, NH 4 OH, NH4. Tenemos pues seis incógnitas. Entre las ecuaciones tenemos el producto iónico del agua, a continuación, una ecuación de disociación del ácido acético otra del amoniaco y, por último, el balance de cargas. Total cuatro ecuaciones y tenemos seis incógnitas. Habrá pues dos balances, que se corresponden a las dos especies que hemos añadido al agua para formar la disolución. =
4 HAc NH 4 OH Ac OH OH La figura visualiza los dos balances: [ HAc ] 0 = [ HAc ] [ Ac ] y [ NH OH ] [ NH OH ] [ N ] En cuanto al balance de carga: [ H ] [ NH4 ] = [OH ] [ Ac ]. 4 0 = 4 4. Pasemos a otro caso, la disolución de una sal. Hemos preparado la disolución de acetato amónico AcNH 4. El acetato amónico es una sal soluble que se disuelve completamente generando un ácido, el catión amonio N 4, y una base, el anión acetato Ac. Ambas especies son débiles, en el sentido que reaccionan parcialmente con el agua generando protones e hidroxilos, siendo que la mayoría de compuesto queda por reaccionar: NH 4 H 2O HNH 4 O H Ac H 2O HAc OH Vemos pues que las especies que se generan en disolución son las mismas que en el caso anterior, con la única diferencia que las concentraciones iniciales de acetato y amonio son iguales entre si e iguales a los moles de acetato amónico que hemos disuelto en el litro de disolución, [ AcNH4 ] 0 = [ Ac ] 0 = [ NH4 ] 0. Los balances materiales son: [ Ac ] = [ Ac ] [ HAc] y N ] = [ N ] [ NH OH ]. 0 El balance de carga es el mismo: [ H ] [ NH4 ] = [OH ] [ Ac ]. El grafico siguiente visualiza las ecuaciones de balance. [
5 Ac NH 4 NH 4 OH HAc OH Para acabar plantearemos un último problema cuyo interés radica en su balance material. Es el caso de la disolución de ácido fluorhídrico en cuya disolución suceden los siguientes equilibrios: HF cuya constante de equilibrio es k a = y HF F HF 2 con una constate k 2 = 5. H F HF F OH La lista de especies en disolución es:, OH, HF, F, HF 2. Total cinco incógnitas. En cuanto a ecuaciones, tenemos el producto iónico del agua, las dos ecuaciones de equilibrio del fluorhídrico y el balance de cargas. Queda pues una incógnita. Habrá pues un balance material, correspondiente a la única especie que hemos añadido para hacer la disolución. Para hacer bien este balance debemos recordar el símil del coche y las ruedas. El balance es: [ HF ] 0 = [ HF ] [ F ] 2 [ HF2 ], puesto que en el dímero hay dos átomos flúor. En la figura se ve que debemos contar dos veces el cuadro pequeño blanco para que, sumado a los otros dos cuadros, se obtenga el cuadro blanco original.
EJERCICIOS PARA EXAMEN U6 Química 2º Bachiller
 2010 Reacciones de intercambio de Protones EJERCICIOS PARA EXAMEN U6 Química 2º Bachiller Recopilación de ejercicios preguntados en exámenes de cursos anteriores Mª Teresa Gómez Ruiz IES Politécnico Cartagena.
2010 Reacciones de intercambio de Protones EJERCICIOS PARA EXAMEN U6 Química 2º Bachiller Recopilación de ejercicios preguntados en exámenes de cursos anteriores Mª Teresa Gómez Ruiz IES Politécnico Cartagena.
Ecuaciones de primer grado con dos incógnitas
 Ecuaciones de primer grado con dos incógnitas Si decimos: "las edades de mis padres suman 120 años", podemos expresar esta frase algebraicamente de la siguiente forma: Entonces, Denominamos x a la edad
Ecuaciones de primer grado con dos incógnitas Si decimos: "las edades de mis padres suman 120 años", podemos expresar esta frase algebraicamente de la siguiente forma: Entonces, Denominamos x a la edad
1. - DEFINICION DE LOS ÁCIDOS Y DE LAS BASES 2. - REACCIONES ENTRE LOS ACIDOS Y LAS BASES CH 3 COOH + NH 3 CH 3 COO - + NH 4 H 2 O OH - + H +
 1 1. - DEFINICION DE LOS ÁCIDOS Y DE LAS BASES Se define un ácido como cualquier ión o molécula capaz de ceder protones. Por lo contrario, una base es cualquier ión o molécula capaz de fijar protones.
1 1. - DEFINICION DE LOS ÁCIDOS Y DE LAS BASES Se define un ácido como cualquier ión o molécula capaz de ceder protones. Por lo contrario, una base es cualquier ión o molécula capaz de fijar protones.
Fracción másica y fracción molar. Definiciones y conversión
 Fracción másica y fracción ar. Definiciones y conversión Apellidos, nombre Atarés Huerta, Lorena (loathue@tal.upv.es) Departamento Centro Departamento de Tecnología de Alimentos ETSIAMN (Universidad Politécnica
Fracción másica y fracción ar. Definiciones y conversión Apellidos, nombre Atarés Huerta, Lorena (loathue@tal.upv.es) Departamento Centro Departamento de Tecnología de Alimentos ETSIAMN (Universidad Politécnica
Divisibilidad y números primos
 Divisibilidad y números primos Divisibilidad En muchos problemas es necesario saber si el reparto de varios elementos en diferentes grupos se puede hacer equitativamente, es decir, si el número de elementos
Divisibilidad y números primos Divisibilidad En muchos problemas es necesario saber si el reparto de varios elementos en diferentes grupos se puede hacer equitativamente, es decir, si el número de elementos
TEMA 5: REACCIONES DE TRANSFERENCIA DE PROTONES EJERCICIOS DE SELECTIVIDAD 96/97
 TEMA 5: REACCIONES DE TRANSFERENCIA DE PROTONES EJERCICIOS DE SELECTIVIDAD 96/97 1. a) Cuántos gramos de hidróxido de potasio se necesitan para preparar 250 ml de una disolución acuosa de ph = 13? b) Calcule
TEMA 5: REACCIONES DE TRANSFERENCIA DE PROTONES EJERCICIOS DE SELECTIVIDAD 96/97 1. a) Cuántos gramos de hidróxido de potasio se necesitan para preparar 250 ml de una disolución acuosa de ph = 13? b) Calcule
ÁCIDO BASE QCA 04 ANDALUCÍA
 ÁCIDO BASE QCA 4 ANDAUCÍA 1.- Un ácido monoprótico, HA, en disolución acuosa de concentración, se encuentra ionizado en un 5 %. Calcule: a) El ph de la disolución. b) a constante de ionización del ácido..-
ÁCIDO BASE QCA 4 ANDAUCÍA 1.- Un ácido monoprótico, HA, en disolución acuosa de concentración, se encuentra ionizado en un 5 %. Calcule: a) El ph de la disolución. b) a constante de ionización del ácido..-
Tema 7: Solubilidad. (Fundamentos de Química, Grado en Física) Equilibrio químico Enero Mayo, 2011 1 / 24
 Tema 7: Solubilidad. Producto de solubilidad. Efecto del ion común en la solubilidad. Limitaciones al producto de solubilidad: K ps. Criterios para la precipitación de la sal. Precipitación fraccionada.
Tema 7: Solubilidad. Producto de solubilidad. Efecto del ion común en la solubilidad. Limitaciones al producto de solubilidad: K ps. Criterios para la precipitación de la sal. Precipitación fraccionada.
QUÉ ES LA RENTABILIDAD Y CÓMO MEDIRLA. La rentabilidad mide la eficiencia con la cual una empresa utiliza sus recursos financieros.
 QUÉ ES LA RENTABILIDAD Y CÓMO MEDIRLA La rentabilidad mide la eficiencia con la cual una empresa utiliza sus recursos financieros. Qué significa esto? Decir que una empresa es eficiente es decir que no
QUÉ ES LA RENTABILIDAD Y CÓMO MEDIRLA La rentabilidad mide la eficiencia con la cual una empresa utiliza sus recursos financieros. Qué significa esto? Decir que una empresa es eficiente es decir que no
Solubilidad. y se representa por.
 Solubilidad Solubilidad. La solubilidad mide la cantidad máxima de soluto capaz de disolverse en una cantidad definida de disolvente, a una temperatura determinada, y formar un sistema estable que se denomina
Solubilidad Solubilidad. La solubilidad mide la cantidad máxima de soluto capaz de disolverse en una cantidad definida de disolvente, a una temperatura determinada, y formar un sistema estable que se denomina
Cómo?: Resolviendo el sistema lineal homógeneo que satisfacen las componentes de cualquier vector de S. x4 = x 1 x 3 = x 2 x 1
 . ESPACIOS VECTORIALES Consideremos el siguiente subconjunto de R 4 : S = {(x, x 2, x 3, x 4 )/x x 4 = 0 x 2 x 4 = x 3 a. Comprobar que S es subespacio vectorial de R 4. Para demostrar que S es un subespacio
. ESPACIOS VECTORIALES Consideremos el siguiente subconjunto de R 4 : S = {(x, x 2, x 3, x 4 )/x x 4 = 0 x 2 x 4 = x 3 a. Comprobar que S es subespacio vectorial de R 4. Para demostrar que S es un subespacio
UNIDAD 1. LOS NÚMEROS ENTEROS.
 UNIDAD 1. LOS NÚMEROS ENTEROS. Al final deberás haber aprendido... Interpretar y expresar números enteros. Representar números enteros en la recta numérica. Comparar y ordenar números enteros. Realizar
UNIDAD 1. LOS NÚMEROS ENTEROS. Al final deberás haber aprendido... Interpretar y expresar números enteros. Representar números enteros en la recta numérica. Comparar y ordenar números enteros. Realizar
Matrices equivalentes. El método de Gauss
 Matrices equivalentes. El método de Gauss Dada una matriz A cualquiera decimos que B es equivalente a A si podemos transformar A en B mediante una combinación de las siguientes operaciones: Multiplicar
Matrices equivalentes. El método de Gauss Dada una matriz A cualquiera decimos que B es equivalente a A si podemos transformar A en B mediante una combinación de las siguientes operaciones: Multiplicar
Ácidos y bases (III) Disoluciones reguladoras Valoraciones ácido- base. Disoluciones reguladoras del ph
 Ácidos y bases (III) Disoluciones reguladoras Valoraciones ácido- base IES La Magdalena. Avilés. Asturias Disoluciones reguladoras del ph Si añadimos una pequeña cantidad de ácido o base a agua pura, el
Ácidos y bases (III) Disoluciones reguladoras Valoraciones ácido- base IES La Magdalena. Avilés. Asturias Disoluciones reguladoras del ph Si añadimos una pequeña cantidad de ácido o base a agua pura, el
Ablandamiento de agua mediante el uso de resinas de intercambio iónico.
 Ablandamiento de agua por intercambio iónica página 1 Ablandamiento de agua mediante el uso de resinas de intercambio iónico. (Fuentes varias) Algunos conceptos previos: sales, iones y solubilidad. Que
Ablandamiento de agua por intercambio iónica página 1 Ablandamiento de agua mediante el uso de resinas de intercambio iónico. (Fuentes varias) Algunos conceptos previos: sales, iones y solubilidad. Que
PREGUNTAS DE TEST SOBRE ÁCIDOS Y BASES
 PREGUNTAS DE TEST SOBRE ÁCIDOS Y BASES A GENERALIDADES B DEFINICION DE ph C ACIDOS Y BASES FUERTES D ACIDOS Y BASES DEBILES: E DISOLUCIONES DE SALES: F DISOLUCIONES TAMPON: G VALORACIONES ACIDOBASE: H
PREGUNTAS DE TEST SOBRE ÁCIDOS Y BASES A GENERALIDADES B DEFINICION DE ph C ACIDOS Y BASES FUERTES D ACIDOS Y BASES DEBILES: E DISOLUCIONES DE SALES: F DISOLUCIONES TAMPON: G VALORACIONES ACIDOBASE: H
www.fisicaeingenieria.es CARACTERÍSTICAS DE LOS ÁCIDOS Y LAS BASES
 CARACTERÍSTICAS DE LOS ÁCIDOS Y LAS BASES ÁCIDOS 1. Tienen sabor ácido como en el caso del ácido cítrico en la naranja. 2. Cambian el color del papel tornasol a rosado. 3. Son corrosivos. 4. Producen quemaduras
CARACTERÍSTICAS DE LOS ÁCIDOS Y LAS BASES ÁCIDOS 1. Tienen sabor ácido como en el caso del ácido cítrico en la naranja. 2. Cambian el color del papel tornasol a rosado. 3. Son corrosivos. 4. Producen quemaduras
Prácticas de Análisis Instrumental
 Prácticas de Análisis Instrumental Asignatura: Análisis Instrumental Alumno: Daniel González Mancebo Practica 1. DETERMINACIÓN DE CONSTANTES DE EQUILIBRIO MEDIANTE ESPECTROFOTOMETRÍA UV- VISIBLE. Lo primero
Prácticas de Análisis Instrumental Asignatura: Análisis Instrumental Alumno: Daniel González Mancebo Practica 1. DETERMINACIÓN DE CONSTANTES DE EQUILIBRIO MEDIANTE ESPECTROFOTOMETRÍA UV- VISIBLE. Lo primero
Lección 4: Suma y resta de números racionales
 GUÍA DE MATEMÁTICAS II Lección : Suma y resta de números racionales En esta lección recordaremos cómo sumar y restar números racionales. Como los racionales pueden estar representados como fracción o decimal,
GUÍA DE MATEMÁTICAS II Lección : Suma y resta de números racionales En esta lección recordaremos cómo sumar y restar números racionales. Como los racionales pueden estar representados como fracción o decimal,
SUAVIZACIÓN CONCEPTOS BÁSICOS
 SUAVIZACIÓN CONCEPTOS BÁSICOS Revisemos algunos conceptos que utilizarás para el diseño de los equipos del sistema de suavización, recuerda que muchos ya los has visto en cursos anteriores y que esto es
SUAVIZACIÓN CONCEPTOS BÁSICOS Revisemos algunos conceptos que utilizarás para el diseño de los equipos del sistema de suavización, recuerda que muchos ya los has visto en cursos anteriores y que esto es
Ejercicio de estadística para 3º de la ESO
 Ejercicio de estadística para 3º de la ESO Unibelia La estadística es una disciplina técnica que se apoya en las matemáticas y que tiene como objetivo la interpretación de la realidad de una población
Ejercicio de estadística para 3º de la ESO Unibelia La estadística es una disciplina técnica que se apoya en las matemáticas y que tiene como objetivo la interpretación de la realidad de una población
Datos del autor. Nombres y apellido: Germán Andrés Paz. Lugar de nacimiento: Rosario (Código Postal 2000), Santa Fe, Argentina
 Datos del autor Nombres y apellido: Germán Andrés Paz Lugar de nacimiento: Rosario (Código Postal 2000), Santa Fe, Argentina Correo electrónico: germanpaz_ar@hotmail.com =========0========= Introducción
Datos del autor Nombres y apellido: Germán Andrés Paz Lugar de nacimiento: Rosario (Código Postal 2000), Santa Fe, Argentina Correo electrónico: germanpaz_ar@hotmail.com =========0========= Introducción
Aproximación local. Plano tangente. Derivadas parciales.
 Univ. de Alcalá de Henares Ingeniería de Telecomunicación Cálculo. Segundo parcial. Curso 004-005 Aproximación local. Plano tangente. Derivadas parciales. 1. Plano tangente 1.1. El problema de la aproximación
Univ. de Alcalá de Henares Ingeniería de Telecomunicación Cálculo. Segundo parcial. Curso 004-005 Aproximación local. Plano tangente. Derivadas parciales. 1. Plano tangente 1.1. El problema de la aproximación
1.3 Números racionales
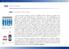 1.3 1.3.1 El concepto de número racional Figura 1.2: Un reparto no equitativo: 12 5 =?. Figura 1.3: Un quinto de la unidad. Con los números naturales y enteros es imposible resolver cuestiones tan simples
1.3 1.3.1 El concepto de número racional Figura 1.2: Un reparto no equitativo: 12 5 =?. Figura 1.3: Un quinto de la unidad. Con los números naturales y enteros es imposible resolver cuestiones tan simples
1. MEDIDAS DE TENDENCIA CENTRAL
 1. MEDIDAS DE TENDENCIA CENTRAL Lo importante en una tendencia central es calcular un valor central que actúe como resumen numérico para representar al conjunto de datos. Estos valores son las medidas
1. MEDIDAS DE TENDENCIA CENTRAL Lo importante en una tendencia central es calcular un valor central que actúe como resumen numérico para representar al conjunto de datos. Estos valores son las medidas
BASES Y DIMENSIÓN. Propiedades de las bases. Ejemplos de bases.
 BASES Y DIMENSIÓN Definición: Base. Se llama base de un espacio (o subespacio) vectorial a un sistema generador de dicho espacio o subespacio, que sea a la vez linealmente independiente. β Propiedades
BASES Y DIMENSIÓN Definición: Base. Se llama base de un espacio (o subespacio) vectorial a un sistema generador de dicho espacio o subespacio, que sea a la vez linealmente independiente. β Propiedades
EJERCICIOS DE MATEMÁTICAS I HOJA 4. Ejercicio 1. Se consideran los vectores
 EJERCICIOS DE MATEMÁTICAS I HOJA 4 Ejercicio 1. Se consideran los vectores u 1 = (1, 1, 0, 1), u 2 = (0, 2, 1, 0), u 3 = ( 1, 1, 1, 1), u 4 = (2, 2, 1, 0) de R 4. Expresa, si es posible, los vectores u
EJERCICIOS DE MATEMÁTICAS I HOJA 4 Ejercicio 1. Se consideran los vectores u 1 = (1, 1, 0, 1), u 2 = (0, 2, 1, 0), u 3 = ( 1, 1, 1, 1), u 4 = (2, 2, 1, 0) de R 4. Expresa, si es posible, los vectores u
Sistemas de ecuaciones lineales
 Sistemas de ecuaciones lineales Índice general 1. Sistemas de ecuaciones lineales 2 2. Método de sustitución 5 3. Método de igualación 9 4. Método de eliminación 13 5. Conclusión 16 1 Sistemas de ecuaciones
Sistemas de ecuaciones lineales Índice general 1. Sistemas de ecuaciones lineales 2 2. Método de sustitución 5 3. Método de igualación 9 4. Método de eliminación 13 5. Conclusión 16 1 Sistemas de ecuaciones
El sistema decimal, es aquél en el que se combinan 10 cifras (o dígitos) del 0 al 9 para indicar una cantidad específica.
 5.2 SISTEMAS DE NUMERACIÓN. DECIMAL El sistema decimal, es aquél en el que se combinan 10 cifras (o dígitos) del 0 al 9 para indicar una cantidad específica. La base de un sistema indica el número de caracteres
5.2 SISTEMAS DE NUMERACIÓN. DECIMAL El sistema decimal, es aquél en el que se combinan 10 cifras (o dígitos) del 0 al 9 para indicar una cantidad específica. La base de un sistema indica el número de caracteres
Sistemas de dos ecuaciones lineales con dos incógnitas
 Sistemas de dos ecuaciones lineales con dos incógnitas Una ecuación lineal con dos incógnitas es una epresión de la forma a b c donde a, b c son los coeficientes (números) e son las incógnitas. Gráficamente
Sistemas de dos ecuaciones lineales con dos incógnitas Una ecuación lineal con dos incógnitas es una epresión de la forma a b c donde a, b c son los coeficientes (números) e son las incógnitas. Gráficamente
La lección de hoy es sobre Resolver Ecuaciones. El cuál es la expectativa para el aprendizaje del estudiante SEI.2.A1.1
 SEI.2.A1.1-Solving Equations-Student Learning Expectation. La lección de hoy es sobre Resolver Ecuaciones. El cuál es la expectativa para el aprendizaje del estudiante SEI.2.A1.1 En esta lección aprenderemos
SEI.2.A1.1-Solving Equations-Student Learning Expectation. La lección de hoy es sobre Resolver Ecuaciones. El cuál es la expectativa para el aprendizaje del estudiante SEI.2.A1.1 En esta lección aprenderemos
Tema 2. Espacios Vectoriales. 2.1. Introducción
 Tema 2 Espacios Vectoriales 2.1. Introducción Estamos habituados en diferentes cursos a trabajar con el concepto de vector. Concretamente sabemos que un vector es un segmento orientado caracterizado por
Tema 2 Espacios Vectoriales 2.1. Introducción Estamos habituados en diferentes cursos a trabajar con el concepto de vector. Concretamente sabemos que un vector es un segmento orientado caracterizado por
CÁTEDRA: QUIMICA GUIA DE PROBLEMAS Nº 10
 CÁTEDRA: QUIMICA GUIA DE PROBLEMAS Nº 10 TEMA: ph, NEUTRALIZACIÓN Y EQUILIBRIO ÁCIDO BASE OBJETIVOS: Clasificar ácidos y bases de acuerdo al potencial de hidrógeno. PRERREQUISITOS: Tener conocimiento de
CÁTEDRA: QUIMICA GUIA DE PROBLEMAS Nº 10 TEMA: ph, NEUTRALIZACIÓN Y EQUILIBRIO ÁCIDO BASE OBJETIVOS: Clasificar ácidos y bases de acuerdo al potencial de hidrógeno. PRERREQUISITOS: Tener conocimiento de
VI Olimpiada de Informática del estado de Guanajuato Solución Examen Teórico
 I.- En todos los problemas siguientes de esta sección, encuentra qué número (o números) debe seguir según la sucesión, y explica el por qué. 1) 1, 4, 27, 256,? (5 puntos) R = 3125 Observa que 1=1 1, 4=2
I.- En todos los problemas siguientes de esta sección, encuentra qué número (o números) debe seguir según la sucesión, y explica el por qué. 1) 1, 4, 27, 256,? (5 puntos) R = 3125 Observa que 1=1 1, 4=2
La Lección de Hoy es Distancia entre dos puntos. El cuál es la expectativa para el aprendizaje del estudiante CGT.5.G.1
 La Lección de Hoy es Distancia entre dos puntos El cuál es la expectativa para el aprendizaje del estudiante CGT.5.G.1 La formula de la distancia dada a dos pares es: d= (x 2 -x 1 ) 2 + (y 2 -y 1 ) 2 De
La Lección de Hoy es Distancia entre dos puntos El cuál es la expectativa para el aprendizaje del estudiante CGT.5.G.1 La formula de la distancia dada a dos pares es: d= (x 2 -x 1 ) 2 + (y 2 -y 1 ) 2 De
Trabajo Práctico N o 1
 1 Trabajo Práctico N o 1 Soluciones y diluciones OBJETIVOS - Conocer todas las formas de indicar la concentración química de una solución. - Ser capaz de calcular la concentración de una solución a partir
1 Trabajo Práctico N o 1 Soluciones y diluciones OBJETIVOS - Conocer todas las formas de indicar la concentración química de una solución. - Ser capaz de calcular la concentración de una solución a partir
Funciones más usuales 1
 Funciones más usuales 1 1. La función constante Funciones más usuales La función constante Consideremos la función más sencilla, por ejemplo. La imagen de cualquier número es siempre 2. Si hacemos una
Funciones más usuales 1 1. La función constante Funciones más usuales La función constante Consideremos la función más sencilla, por ejemplo. La imagen de cualquier número es siempre 2. Si hacemos una
LÍMITES Y CONTINUIDAD DE FUNCIONES
 Capítulo 9 LÍMITES Y CONTINUIDAD DE FUNCIONES 9.. Introducción El concepto de ite en Matemáticas tiene el sentido de lugar hacia el que se dirige una función en un determinado punto o en el infinito. Veamos
Capítulo 9 LÍMITES Y CONTINUIDAD DE FUNCIONES 9.. Introducción El concepto de ite en Matemáticas tiene el sentido de lugar hacia el que se dirige una función en un determinado punto o en el infinito. Veamos
UNIDAD 6. POLINOMIOS CON COEFICIENTES ENTEROS
 UNIDAD 6. POLINOMIOS CON COEFICIENTES ENTEROS Unidad 6: Polinomios con coeficientes enteros. Al final deberás haber aprendido... Expresar algebraicamente enunciados sencillos. Extraer enunciados razonables
UNIDAD 6. POLINOMIOS CON COEFICIENTES ENTEROS Unidad 6: Polinomios con coeficientes enteros. Al final deberás haber aprendido... Expresar algebraicamente enunciados sencillos. Extraer enunciados razonables
QUÉ ES UN NÚMERO DECIMAL?
 QUÉ ES UN NÚMERO DECIMAL? Un número decimal representa un número que no es entero, es decir, los números decimales se utilizan para representar a los números que se encuentran entre un número entero y
QUÉ ES UN NÚMERO DECIMAL? Un número decimal representa un número que no es entero, es decir, los números decimales se utilizan para representar a los números que se encuentran entre un número entero y
Sistemas de numeración
 Sistemas de numeración Un sistema de numeración es un conjunto de símbolos y reglas que permiten representar datos numéricos. Los sistemas de numeración actuales son sistemas posicionales, que se caracterizan
Sistemas de numeración Un sistema de numeración es un conjunto de símbolos y reglas que permiten representar datos numéricos. Los sistemas de numeración actuales son sistemas posicionales, que se caracterizan
UNIDAD 3: SOLUCIONES
 UNIDAD 3: SOLUCIONES 1 Las soluciones son mezclas homogéneas. Estas constan de dos o más componentes en una única fase, por ejemplo agua con sal de cocina, o azúcar en agua Para estudiar o trabajar con
UNIDAD 3: SOLUCIONES 1 Las soluciones son mezclas homogéneas. Estas constan de dos o más componentes en una única fase, por ejemplo agua con sal de cocina, o azúcar en agua Para estudiar o trabajar con
EJERCICIOS RESUELTOS SOBRE ERRORES DE REDONDEO
 EJERCICIOS RESUELTOS SOBRE ERRORES DE REDONDEO 1º) Considérese un número estrictamente positivo del sistema de números máquina F(s+1, m, M, 10). Supongamos que tal número es: z = 0.d 1 d...d s 10 e Responde
EJERCICIOS RESUELTOS SOBRE ERRORES DE REDONDEO 1º) Considérese un número estrictamente positivo del sistema de números máquina F(s+1, m, M, 10). Supongamos que tal número es: z = 0.d 1 d...d s 10 e Responde
E4B.S2007. a) HCl + H 2 O Cl + H 3 O + ácido1 base2 base1 ácido2. b) NH 3 + H 2 O NH 4 + + OH base1 ácido2 ácido1 base2
 TEMA 6. ACIDOS Y BASES E1B.S009 Para las especies CN, HF y CO 3, en disolución acuosa: a) Escriba, según corresponda, la fórmula del ácido o de la base conjugados. b) Justifique, mediante la reacción correspondiente,
TEMA 6. ACIDOS Y BASES E1B.S009 Para las especies CN, HF y CO 3, en disolución acuosa: a) Escriba, según corresponda, la fórmula del ácido o de la base conjugados. b) Justifique, mediante la reacción correspondiente,
ECUACION DE DEMANDA. El siguiente ejemplo ilustra como se puede estimar la ecuación de demanda cuando se supone que es lineal.
 ECUACION DE DEMANDA La ecuación de demanda es una ecuación que expresa la relación que existe entre q y p, donde q es la cantidad de artículos que los consumidores están dispuestos a comprar a un precio
ECUACION DE DEMANDA La ecuación de demanda es una ecuación que expresa la relación que existe entre q y p, donde q es la cantidad de artículos que los consumidores están dispuestos a comprar a un precio
Lección 24: Lenguaje algebraico y sustituciones
 LECCIÓN Lección : Lenguaje algebraico y sustituciones En lecciones anteriores usted ya trabajó con ecuaciones. Las ecuaciones expresan una igualdad entre ciertas relaciones numéricas en las que se desconoce
LECCIÓN Lección : Lenguaje algebraico y sustituciones En lecciones anteriores usted ya trabajó con ecuaciones. Las ecuaciones expresan una igualdad entre ciertas relaciones numéricas en las que se desconoce
Esta es la forma vectorial de la recta. Si desarrollamos las dos posibles ecuaciones, tendremos las ecuaciones paramétricas de la recta:
 Todo el mundo sabe que dos puntos definen una recta, pero los matemáticos son un poco diferentes y, aún aceptando la máxima universal, ellos prefieren decir que un punto y un vector nos definen una recta.
Todo el mundo sabe que dos puntos definen una recta, pero los matemáticos son un poco diferentes y, aún aceptando la máxima universal, ellos prefieren decir que un punto y un vector nos definen una recta.
QUIMICA ANALÍTICA (63.05) SOLUCIONES REGULADORAS DE ph 63.05.12. Lic. Ana María Martín
 QUIMICA ANALÍTICA (63.05) SOLUCIONES REGULADORAS DE ph 63.05.12 Lic. Ana María Martín Lic. Ana María Martín Introducción SOLUCIONES REGULADORAS DE ph Muchas de las reacciones químicas que se producen en
QUIMICA ANALÍTICA (63.05) SOLUCIONES REGULADORAS DE ph 63.05.12 Lic. Ana María Martín Lic. Ana María Martín Introducción SOLUCIONES REGULADORAS DE ph Muchas de las reacciones químicas que se producen en
Conductividad en disoluciones electrolíticas.
 Conductividad en disoluciones electrolíticas. 1.- Introducción 2.- Conductores 3.- Definición de magnitudes 3.1- Conductividad específica 3.2 Conductividad molar " 4. Variación de la conductividad (, ")
Conductividad en disoluciones electrolíticas. 1.- Introducción 2.- Conductores 3.- Definición de magnitudes 3.1- Conductividad específica 3.2 Conductividad molar " 4. Variación de la conductividad (, ")
E 1 E 2 E 2 E 3 E 4 E 5 2E 4
 Problemas resueltos de Espacios Vectoriales: 1- Para cada uno de los conjuntos de vectores que se dan a continuación estudia si son linealmente independientes, sistema generador o base: a) (2, 1, 1, 1),
Problemas resueltos de Espacios Vectoriales: 1- Para cada uno de los conjuntos de vectores que se dan a continuación estudia si son linealmente independientes, sistema generador o base: a) (2, 1, 1, 1),
Electrólisis. Electrólisis 12/02/2015
 Electrólisis Dr. Armando Ayala Corona Electrólisis La electrolisis es un proceso mediante el cual se logra la disociación de una sustancia llamada electrolito, en sus iones constituyentes (aniones y cationes),
Electrólisis Dr. Armando Ayala Corona Electrólisis La electrolisis es un proceso mediante el cual se logra la disociación de una sustancia llamada electrolito, en sus iones constituyentes (aniones y cationes),
Profr. Efraín Soto Apolinar. Factorización
 Factorización La factorización es la otra parte de la historia de los productos notables. Esto es, ambas cosas se refieren a las mismas fórmulas, pero en los productos notables se nos daba una operación
Factorización La factorización es la otra parte de la historia de los productos notables. Esto es, ambas cosas se refieren a las mismas fórmulas, pero en los productos notables se nos daba una operación
EJERCICIOS DEL TEMA 1
 EJERCICIOS DEL TEMA 1 Introducción a los ordenadores 1) Averigua y escribe el código ASCII correspondiente, tanto en decimal como en binario, a las letras de tu nombre y apellidos. Distinguir entre mayúsculas/minúsculas,
EJERCICIOS DEL TEMA 1 Introducción a los ordenadores 1) Averigua y escribe el código ASCII correspondiente, tanto en decimal como en binario, a las letras de tu nombre y apellidos. Distinguir entre mayúsculas/minúsculas,
Índice Introducción Números Polinomios Funciones y su Representación. Curso 0: Matemáticas y sus Aplicaciones Tema 1. Números, Polinomios y Funciones
 Curso 0: Matemáticas y sus Aplicaciones Tema 1. Números, Polinomios y Funciones Leandro Marín Dpto. de Matemática Aplicada Universidad de Murcia 2012 1 Números 2 Polinomios 3 Funciones y su Representación
Curso 0: Matemáticas y sus Aplicaciones Tema 1. Números, Polinomios y Funciones Leandro Marín Dpto. de Matemática Aplicada Universidad de Murcia 2012 1 Números 2 Polinomios 3 Funciones y su Representación
A continuación voy a colocar las fuerzas que intervienen en nuestro problema.
 ísica EL PLANO INCLINADO Supongamos que tenemos un plano inclinado. Sobre él colocamos un cubo, de manera que se deslice sobre la superficie hasta llegar al plano horizontal. Vamos a suponer que tenemos
ísica EL PLANO INCLINADO Supongamos que tenemos un plano inclinado. Sobre él colocamos un cubo, de manera que se deslice sobre la superficie hasta llegar al plano horizontal. Vamos a suponer que tenemos
A VUELTAS CON EL MOL
 A VUELTAS CON EL MOL El concepto de mol es algo íntimamente ligado a la teoría atómico-molecular de la materia y al Número de Avogadro. Es necesario, por tanto, tener una idea clara de lo que es un átomo
A VUELTAS CON EL MOL El concepto de mol es algo íntimamente ligado a la teoría atómico-molecular de la materia y al Número de Avogadro. Es necesario, por tanto, tener una idea clara de lo que es un átomo
EQUILIBRIO ÁCIDO-BASE
 EQUIIBRIO ÁCIDO-BASE Electrolito y no electrolito os electrolitos son sustancias (ácidos, bases y sales) que al disolverse en agua o fundidos, pueden conducir la corriente eléctrica. os electrolitos pueden
EQUIIBRIO ÁCIDO-BASE Electrolito y no electrolito os electrolitos son sustancias (ácidos, bases y sales) que al disolverse en agua o fundidos, pueden conducir la corriente eléctrica. os electrolitos pueden
Combina, prueba, tantea PÁGINA 14
 PÁGINA 14 Pág. 1 3 Si escribes todos los números impares entre el 55 y el 555, cuántas veces habrás usado la cifra 6? Un número impar entre el 55 y el 555 solo puede tener un 6 en la cifra de las decenas.
PÁGINA 14 Pág. 1 3 Si escribes todos los números impares entre el 55 y el 555, cuántas veces habrás usado la cifra 6? Un número impar entre el 55 y el 555 solo puede tener un 6 en la cifra de las decenas.
1. Cuál es la constante de acidez de un ácido monoprótico HA, sabiendo que una disolución 0,2 M está disociada un 1 %.
 Problemas 1. Cuál es la constante de acidez de un ácido monoprótico HA, sabiendo que una disolución 0,2 M está disociada un 1 %. (septiembre 95) 2. Cuál es la concentración molar de una disolución de ácido
Problemas 1. Cuál es la constante de acidez de un ácido monoprótico HA, sabiendo que una disolución 0,2 M está disociada un 1 %. (septiembre 95) 2. Cuál es la concentración molar de una disolución de ácido
Cajón de Ciencias. Problemas resueltos de sistemas de ecuaciones
 Problemas resueltos de sistemas de ecuaciones 1) En una granja se crían gallinas y conejos. En total hay 50 cabezas y 134 patas Cuántos animales hay de cada clase? 2) En un taller hay vehículos de 4 y
Problemas resueltos de sistemas de ecuaciones 1) En una granja se crían gallinas y conejos. En total hay 50 cabezas y 134 patas Cuántos animales hay de cada clase? 2) En un taller hay vehículos de 4 y
MÉTODOS DE ELIMINACIÓN Son tres los métodos de eliminación más utilizados: Método de igualación, de sustitución y de suma o resta.
 ECUACIONES SIMULTÁNEAS DE PRIMER GRADO CON DOS INCÓGNITAS. Dos o más ecuaciones con dos incógnitas son simultáneas cuando satisfacen iguales valores de las incógnitas. Para resolver ecuaciones de esta
ECUACIONES SIMULTÁNEAS DE PRIMER GRADO CON DOS INCÓGNITAS. Dos o más ecuaciones con dos incógnitas son simultáneas cuando satisfacen iguales valores de las incógnitas. Para resolver ecuaciones de esta
1. HABILIDAD MATEMÁTICA
 HABILIDAD MATEMÁTICA SUCESIONES, SERIES Y PATRONES. HABILIDAD MATEMÁTICA Una serie es un conjunto de números, literales o dibujos ordenados de tal manera que cualquiera de ellos puede ser definido por
HABILIDAD MATEMÁTICA SUCESIONES, SERIES Y PATRONES. HABILIDAD MATEMÁTICA Una serie es un conjunto de números, literales o dibujos ordenados de tal manera que cualquiera de ellos puede ser definido por
a < b y se lee "a es menor que b" (desigualdad estricta) a > b y se lee "a es mayor que b" (desigualdad estricta)
 Desigualdades Dadas dos rectas que se cortan, llamadas ejes (rectangulares si son perpendiculares, y oblicuos en caso contrario), un punto puede situarse conociendo las distancias del mismo a los ejes,
Desigualdades Dadas dos rectas que se cortan, llamadas ejes (rectangulares si son perpendiculares, y oblicuos en caso contrario), un punto puede situarse conociendo las distancias del mismo a los ejes,
Estos elementos mecánicos suelen ir montados sobre los ejes de transmisión, que son piezas cilíndricas sobre las cuales se colocan los mecanismos.
 MECANISMOS A. Introducción. Un mecanismo es un dispositivo que transforma el movimiento producido por un elemento motriz (fuerza de entrada) en un movimiento deseado de salida (fuerza de salida) llamado
MECANISMOS A. Introducción. Un mecanismo es un dispositivo que transforma el movimiento producido por un elemento motriz (fuerza de entrada) en un movimiento deseado de salida (fuerza de salida) llamado
TIEMPO -DÍAS -HORAS CONCEPTO GENERAL DEL TIEMPO
 TIEMPO -DÍAS -HORAS CONCEPTO GENERAL DEL TIEMPO Para medir el tiempo se necesita un fenómeno periódico, que se repita continuamente y con la misma fase, lo que sucede con fenómenos astronómicos basado
TIEMPO -DÍAS -HORAS CONCEPTO GENERAL DEL TIEMPO Para medir el tiempo se necesita un fenómeno periódico, que se repita continuamente y con la misma fase, lo que sucede con fenómenos astronómicos basado
1. Números Reales 1.1 Clasificación y propiedades
 1. Números Reales 1.1 Clasificación y propiedades 1.1.1 Definición Número real, cualquier número racional o irracional. Los números reales pueden expresarse en forma decimal mediante un número entero,
1. Números Reales 1.1 Clasificación y propiedades 1.1.1 Definición Número real, cualquier número racional o irracional. Los números reales pueden expresarse en forma decimal mediante un número entero,
UNIVERSIDADES PÚBLICAS DE LA COMUNIDAD DE MADRID PRUEBA DE ACCESO A LAS ENSEÑANZAS UNIVERSITARIAS OFICIALES DE GRADO. Modelo Curso 2010-2011
 UNIVERSIDADES PÚBLICAS DE LA COMUNIDAD DE MADRID PRUEBA DE ACCESO A LAS ENSEÑANZAS UNIVERSITARIAS OFICIALES DE GRADO MATERIA: QUÍMICA Modelo Curso 010-011 MODELO INSTRUCCIONES Y CRITERIOS GENERALES DE
UNIVERSIDADES PÚBLICAS DE LA COMUNIDAD DE MADRID PRUEBA DE ACCESO A LAS ENSEÑANZAS UNIVERSITARIAS OFICIALES DE GRADO MATERIA: QUÍMICA Modelo Curso 010-011 MODELO INSTRUCCIONES Y CRITERIOS GENERALES DE
Subespacios vectoriales en R n
 Subespacios vectoriales en R n Víctor Domínguez Octubre 2011 1. Introducción Con estas notas resumimos los conceptos fundamentales del tema 3 que, en pocas palabras, se puede resumir en técnicas de manejo
Subespacios vectoriales en R n Víctor Domínguez Octubre 2011 1. Introducción Con estas notas resumimos los conceptos fundamentales del tema 3 que, en pocas palabras, se puede resumir en técnicas de manejo
Resortes y fuerzas. Analiza la siguiente situación. Ley de Hooke. 2do Medio > Física Ley de Hooke. Qué aprenderé?
 2do Medio > Física Ley de Hooke Resortes y fuerzas Analiza la siguiente situación Aníbal trabaja en una fábrica de entretenimientos electrónicos. Es el encargado de diseñar algunas de las máquinas que
2do Medio > Física Ley de Hooke Resortes y fuerzas Analiza la siguiente situación Aníbal trabaja en una fábrica de entretenimientos electrónicos. Es el encargado de diseñar algunas de las máquinas que
PARTE 3 ECUACIONES DE EQUIVALENCIA FINANCIERA T E M A S
 PARTE 3 ECUACIONES DE EQUIVALENCIA FINANCIERA Valor del dinero en el tiempo Conceptos de capitalización y descuento Ecuaciones de equivalencia financiera Ejercicio de reestructuración de deuda T E M A
PARTE 3 ECUACIONES DE EQUIVALENCIA FINANCIERA Valor del dinero en el tiempo Conceptos de capitalización y descuento Ecuaciones de equivalencia financiera Ejercicio de reestructuración de deuda T E M A
Descomposición factorial de polinomios
 Descomposición factorial de polinomios Contenidos del tema Introducción Sacar factor común Productos notables Fórmula de la ecuación de segundo grado Método de Ruffini y Teorema del Resto Combinación de
Descomposición factorial de polinomios Contenidos del tema Introducción Sacar factor común Productos notables Fórmula de la ecuación de segundo grado Método de Ruffini y Teorema del Resto Combinación de
Jubilación en la Ley del IMSS
 Jubilación en la Ley del IMSS Ley del Seguro Social Ley del Seguro Social 1973 Ley Vigente del Seguro Social (1997) Artículo Tercero Transitorio. Los asegurados inscritos con anterioridad a la entrada
Jubilación en la Ley del IMSS Ley del Seguro Social Ley del Seguro Social 1973 Ley Vigente del Seguro Social (1997) Artículo Tercero Transitorio. Los asegurados inscritos con anterioridad a la entrada
TEMA 8: SISTEMA DE COSTES POR PROCESOS. INDICE. 1.- Caracteristicas generales de los sistemas de costes por procesos.
 Costes y Sistemas de Costes. Profesor: Jose Ignacio González Gómez. Página 1 de 6 TEMA 8: SISTEMA DE COSTES POR PROCESOS. INDICE 1.- CARACTERISTICAS GENERALES DE LOS SIS TEMAS DE COSTES POR PROCESOS...1
Costes y Sistemas de Costes. Profesor: Jose Ignacio González Gómez. Página 1 de 6 TEMA 8: SISTEMA DE COSTES POR PROCESOS. INDICE 1.- CARACTERISTICAS GENERALES DE LOS SIS TEMAS DE COSTES POR PROCESOS...1
ELECTRÓLISIS. Electrólisis de sales fundidas
 El proceso por el cual se produce una reacción química a partir de una energía eléctrica se denomina electrólisis. Y se lleva a cabo en un dispositivo que se conoce como cuba o celda electrolítica. Este
El proceso por el cual se produce una reacción química a partir de una energía eléctrica se denomina electrólisis. Y se lleva a cabo en un dispositivo que se conoce como cuba o celda electrolítica. Este
gsoluto %p/p = 100 gdedisolución
 I. Presentación de la guía: ASIGNATURA: QUIMICA AGROPECUARIA (RB8002) TALLER N 3: CONCENTRACION DE DISOLUCIONES Competencia: El alumno será capaz de resolver problemas con disoluciones en unidades físicas
I. Presentación de la guía: ASIGNATURA: QUIMICA AGROPECUARIA (RB8002) TALLER N 3: CONCENTRACION DE DISOLUCIONES Competencia: El alumno será capaz de resolver problemas con disoluciones en unidades físicas
PROBLEMAS RESUELTOS SELECTIVIDAD ANDALUCÍA 2009 QUÍMICA TEMA 4: ENERGÍA DE LAS REACCIONES QUÍMICAS
 PROBLEMAS RESUELTOS SELECTIVIDAD ANDALUCÍA 9 QUÍMICA TEMA 4: ENERGÍA DE LAS REACCIONES QUÍMICAS Junio, Ejercicio 6, Opción A Reserva 1, Ejercicio 5, Opción B Reserva, Ejercicio 4, Opción A Reserva, Ejercicio
PROBLEMAS RESUELTOS SELECTIVIDAD ANDALUCÍA 9 QUÍMICA TEMA 4: ENERGÍA DE LAS REACCIONES QUÍMICAS Junio, Ejercicio 6, Opción A Reserva 1, Ejercicio 5, Opción B Reserva, Ejercicio 4, Opción A Reserva, Ejercicio
1 1 0 1 x 1 0 1 1 1 1 0 1 + 1 1 0 1 0 0 0 0 1 1 0 1 1 0 0 0 1 1 1 1
 5.1.3 Multiplicación de números enteros. El algoritmo de la multiplicación tal y como se realizaría manualmente con operandos positivos de cuatro bits es el siguiente: 1 1 0 1 x 1 0 1 1 1 1 0 1 + 1 1 0
5.1.3 Multiplicación de números enteros. El algoritmo de la multiplicación tal y como se realizaría manualmente con operandos positivos de cuatro bits es el siguiente: 1 1 0 1 x 1 0 1 1 1 1 0 1 + 1 1 0
1. Funciones de varias variables: representaciones gráficas, límites y continuidad.
 GRADO DE INGENIERÍA AEROESPACIAL. CURSO 0.. Funciones de varias variables: representaciones gráficas, límites y continuidad. En el análisis de los problemas de la ciencia y de la técnica, las cantidades
GRADO DE INGENIERÍA AEROESPACIAL. CURSO 0.. Funciones de varias variables: representaciones gráficas, límites y continuidad. En el análisis de los problemas de la ciencia y de la técnica, las cantidades
Tabla 4.1. Reglas de solubilidad para compuestos iónicos a 25ºC
 La disolución y la precipitación de compuestos son fenómenos que se presentan corrientemente en la naturaleza. Por ejemplo la preparación de muchos productos químicos industriales, como el Na 2 CO 3, está
La disolución y la precipitación de compuestos son fenómenos que se presentan corrientemente en la naturaleza. Por ejemplo la preparación de muchos productos químicos industriales, como el Na 2 CO 3, está
SESION 4. 1. El comando Integrate 2. Aproximación de integrales definidas 3. Integración de funciones racionales
 SESION. El comando Integrate. Aproimación de integrales definidas. Integración de funciones racionales . El comando Integrate El cálculo de integrales definidas e indefinidas en MATHEMATICA es sencillo
SESION. El comando Integrate. Aproimación de integrales definidas. Integración de funciones racionales . El comando Integrate El cálculo de integrales definidas e indefinidas en MATHEMATICA es sencillo
Los números racionales
 Los números racionales Los números racionales Los números fraccionarios o fracciones permiten representar aquellas situaciones en las que se obtiene o se debe una parte de un objeto. Todas las fracciones
Los números racionales Los números racionales Los números fraccionarios o fracciones permiten representar aquellas situaciones en las que se obtiene o se debe una parte de un objeto. Todas las fracciones
EQUILIBRIO QUÍMICO: REACCIONES ÁCIDO-BASE
 Página: 1/7 DEPARTAMENTO ESTRELLA CAMPOS PRÁCTICO 8: EQUILIBRIO QUÍMICO: REACCIONES ÁCIDO-BASE Bibliografía: Química, La Ciencia Central, T.L. Brown, H. E. LeMay, Jr., B. Bursten; Ed. Prentice-Hall, Hispanoamérica,
Página: 1/7 DEPARTAMENTO ESTRELLA CAMPOS PRÁCTICO 8: EQUILIBRIO QUÍMICO: REACCIONES ÁCIDO-BASE Bibliografía: Química, La Ciencia Central, T.L. Brown, H. E. LeMay, Jr., B. Bursten; Ed. Prentice-Hall, Hispanoamérica,
OPCIÓN A. moléculas 1 mol. moléculas 2 átomos. moléculas. = 0,166 10 22 moles.
 OPCIÓN A CUESTIÓN 4.- Se tienen tres depósitos cerrados A, B y C de igual olumen y que se encuentran a la misma temperatura. En ellos se introducen, respectiamente, 0 g de H (g), 7 moles de O (g) y 0 3
OPCIÓN A CUESTIÓN 4.- Se tienen tres depósitos cerrados A, B y C de igual olumen y que se encuentran a la misma temperatura. En ellos se introducen, respectiamente, 0 g de H (g), 7 moles de O (g) y 0 3
1.4.- D E S I G U A L D A D E S
 1.4.- D E S I G U A L D A D E S OBJETIVO: Que el alumno conozca y maneje las reglas empleadas en la resolución de desigualdades y las use para determinar el conjunto solución de una desigualdad dada y
1.4.- D E S I G U A L D A D E S OBJETIVO: Que el alumno conozca y maneje las reglas empleadas en la resolución de desigualdades y las use para determinar el conjunto solución de una desigualdad dada y
TABLA DE DECISION. Consideremos la siguiente tabla, expresada en forma genérica, como ejemplo y establezcamos la manera en que debe leerse.
 TABLA DE DECISION La tabla de decisión es una herramienta que sintetiza procesos en los cuales se dan un conjunto de condiciones y un conjunto de acciones a tomar según el valor que toman las condiciones.
TABLA DE DECISION La tabla de decisión es una herramienta que sintetiza procesos en los cuales se dan un conjunto de condiciones y un conjunto de acciones a tomar según el valor que toman las condiciones.
MINERALIZACIÓN. Conductividad eléctrica (µs/cm) Mineralización. 100-200 Débil 200-700 Media 700 a 1000 Importante
 MINERALIZACIÓN CONDUCTIVIDAD ELÉCTRICA DUREZA ALCALINIDAD IONES (SHÖLLER) CONDUCTIVIDAD ELÉCTRICA La conductividad eléctrica es la capacidad de un agua para conducir electricidad; se mide como la conductividad
MINERALIZACIÓN CONDUCTIVIDAD ELÉCTRICA DUREZA ALCALINIDAD IONES (SHÖLLER) CONDUCTIVIDAD ELÉCTRICA La conductividad eléctrica es la capacidad de un agua para conducir electricidad; se mide como la conductividad
TEMA 5 RESOLUCIÓN DE CIRCUITOS
 TEMA 5 RESOLUCIÓN DE CIRCUITOS RESOLUCIÓN DE CIRCUITOS POR KIRCHHOFF Para poder resolver circuitos por Kirchhoff debemos determinar primeros los conceptos de malla, rama y nudo. Concepto de malla: Se llama
TEMA 5 RESOLUCIÓN DE CIRCUITOS RESOLUCIÓN DE CIRCUITOS POR KIRCHHOFF Para poder resolver circuitos por Kirchhoff debemos determinar primeros los conceptos de malla, rama y nudo. Concepto de malla: Se llama
Unidad IV: Cinética química
 63 Unidad IV: Cinética química El objetivo de la cinética química es el estudio de las velocidades de las reacciones químicas y de los factores de los que dependen dichas velocidades. De estos factores,
63 Unidad IV: Cinética química El objetivo de la cinética química es el estudio de las velocidades de las reacciones químicas y de los factores de los que dependen dichas velocidades. De estos factores,
Cap. 24 La Ley de Gauss
 Cap. 24 La Ley de Gauss Una misma ley física enunciada desde diferentes puntos de vista Coulomb Gauss Son equivalentes Pero ambas tienen situaciones para las cuales son superiores que la otra Aquí hay
Cap. 24 La Ley de Gauss Una misma ley física enunciada desde diferentes puntos de vista Coulomb Gauss Son equivalentes Pero ambas tienen situaciones para las cuales son superiores que la otra Aquí hay
1. Lección 5 - Comparación y Sustitución de capitales
 Apuntes: Matemáticas Financieras 1. Lección 5 - Comparación y Sustitución de capitales 1.1. Comparación de Capitales Se dice que dos capitales son equivalentes cuando tienen el mismo valor en la fecha
Apuntes: Matemáticas Financieras 1. Lección 5 - Comparación y Sustitución de capitales 1.1. Comparación de Capitales Se dice que dos capitales son equivalentes cuando tienen el mismo valor en la fecha
Profr. Efraín Soto Apolinar. La función lineal. y = a 0 + a 1 x. y = m x + b
 La función lineal Una función polinomial de grado uno tiene la forma: y = a 0 + a 1 x El semestre pasado estudiamos la ecuación de la recta. y = m x + b En la notación de funciones polinomiales, el coeficiente
La función lineal Una función polinomial de grado uno tiene la forma: y = a 0 + a 1 x El semestre pasado estudiamos la ecuación de la recta. y = m x + b En la notación de funciones polinomiales, el coeficiente
SOLUCIONES A LOS EJERCICIOS DE LA UNIDAD
 Pág. Página 9 PRACTICA Sistemas lineales Comprueba si el par (, ) es solución de alguno de los siguientes sistemas: x + y 5 a) x y x y 5 x + y 8 El par (, ) es solución de un sistema si al sustituir x
Pág. Página 9 PRACTICA Sistemas lineales Comprueba si el par (, ) es solución de alguno de los siguientes sistemas: x + y 5 a) x y x y 5 x + y 8 El par (, ) es solución de un sistema si al sustituir x
Funciones polinomiales de grados 3 y 4
 Funciones polinomiales de grados 3 y 4 Ahora vamos a estudiar los casos de funciones polinomiales de grados tres y cuatro. Vamos a empezar con sus gráficas y después vamos a estudiar algunos resultados
Funciones polinomiales de grados 3 y 4 Ahora vamos a estudiar los casos de funciones polinomiales de grados tres y cuatro. Vamos a empezar con sus gráficas y después vamos a estudiar algunos resultados
Inversión C D= -400 F1= 200 F2= 600
 EJEMPLO PAYBACK VAN TIR Para realizar este ejercicio me baso en los datos que se dan para el mismo en la página 358 nº 1 pero incluyo el tercer flujo de caja en el segundo para tener un ejemplo que me
EJEMPLO PAYBACK VAN TIR Para realizar este ejercicio me baso en los datos que se dan para el mismo en la página 358 nº 1 pero incluyo el tercer flujo de caja en el segundo para tener un ejemplo que me
AXIOMAS DE CUERPO (CAMPO) DE LOS NÚMEROS REALES
 AXIOMASDECUERPO(CAMPO) DELOSNÚMEROSREALES Ejemplo: 6 INECUACIONES 15 VA11) x y x y. VA12) x y x y. Las demostraciones de muchas de estas propiedades son evidentes de la definición. Otras se demostrarán
AXIOMASDECUERPO(CAMPO) DELOSNÚMEROSREALES Ejemplo: 6 INECUACIONES 15 VA11) x y x y. VA12) x y x y. Las demostraciones de muchas de estas propiedades son evidentes de la definición. Otras se demostrarán
Física de los Procesos Biológicos Curso 2005/6
 Bibliografía: ísica, Kane, Tema 8 ísica de los Procesos Biológicos Curso 2005/6 Grupo 3 TEMA 2 BIOMECÁNICA 2.1 SÓIDO DEORMABE Parte 1 Introducción Vamos a estudiar como los materiales se deforman debido
Bibliografía: ísica, Kane, Tema 8 ísica de los Procesos Biológicos Curso 2005/6 Grupo 3 TEMA 2 BIOMECÁNICA 2.1 SÓIDO DEORMABE Parte 1 Introducción Vamos a estudiar como los materiales se deforman debido
Negro x Zafiro: Todos Negros. Negro x Zafiro: 1/2 Negros y ½ Zafiro. Negro x Zafiro: ½ Negros y ½ Platino. Zafiro x Zafiro: Todos Zafiro
 En el visón, el color de pelo es negro, platino (azul grisáceo) o zafiro (azul muy claro). En los cruzamientos que se detallan se obtuvieron los siguientes resultados en F1: Negro x afiro: Todos Negros.
En el visón, el color de pelo es negro, platino (azul grisáceo) o zafiro (azul muy claro). En los cruzamientos que se detallan se obtuvieron los siguientes resultados en F1: Negro x afiro: Todos Negros.
Hasta ahora hemos estudiado potencias pertenecientes a distintos campos numéricos. n N, ( a 0 ) m a. m Z, n N
 EXPONENCIALES Y LOGARITMOS FUNCIÓN EXPONENCIAL Hasta ahora hemos estudiado potencias pertenecientes a distintos campos numéricos. Potencias de eponente natural: a n = a. a. a... a n N n veces Potencias
EXPONENCIALES Y LOGARITMOS FUNCIÓN EXPONENCIAL Hasta ahora hemos estudiado potencias pertenecientes a distintos campos numéricos. Potencias de eponente natural: a n = a. a. a... a n N n veces Potencias
