SOLUCIÓN (b) 8. (a) 2. (a) 29. (b) 30. (c) 22. (d) 23. (b) 24. (a) 25. (b) 26. (d) 27. (c) 28. (a)
|
|
|
- Beatriz Fernández de la Fuente
- hace 7 años
- Vistas:
Transcripción
1 29. Si la presión externa del ambiente que rodea a un líquido aumenta, qué le pasa a la temperatura a la que hierve? a) disminuye b) aumenta c) no cambia d) no se puede saber 30. Las gotas de agua que se acumulan en las paredes de una lata de refresco fría, provienen de: a) del interior de la lata (el agua atraviesa los microorificios que hay en la lata y que no se ven) b) del agua que hay en el frigorífico (se manchó con el hielo que siempre se cría en el frigorífico) c) del vapor de agua del aire (el agua se condensa al contacto con una superficie fría) SOLUCIÓN (b) 8. (a) 2. (a) 9. (c) 3. (a) 10. (c) 4. (c) 11. (d) 5. (a) 12. (a) 6. (b) 13. (b) 7. (c) 14. (d) 15. (c) 16. (b) 17. (c) 18. (c) 19. (b) 20. (b) 21. (b) 22. (d) 23. (b) 24. (a) 25. (b) 26. (d) 27. (c) 28. (a) 29. (b) 30. (c) TEMA 3 1. Una sustancia que está formada por un sólo componente es: a) una mezcla b) un compuesto c) un elemento d) una sustanica pura 2. Una sustancia que está formada por más de un componente es: a) una mezcla b) un compuesto c) un elemento d) una sustancia pura 3. Es cierto que una mezcla: a) puede ser homogénea b) puede ser heterogénea c) está formada por más de un componente 4. Las sustancias puras son: a) elementos y compuestos b) compuestos y mezclas puras c) compuestos puros 5. A un laboratorio llega una sustancia para ser analizada. Después de muchos estudios se llega a la conclusión de que esa sustancia no puede ser separada en otras sustancias de ninguna de las maneras posibles que existen en un laboratorio: a) se trata de una mezcla pura b) se trata de una sustancia pura y es un elemento químico c) se trata de una sustancia pura y es un compuesto químico 9
2 6. Una sustancia se envió al laboratorio para ser analizada. No se logró separar en otras sustancias por procedimientos físicos (como filtrar, destilar...), pero se pudo separar en otras sustancias mediante reacciones químicas. Es cierto que: a) se trata de una mezcla pura b) se trata de una sustancia pura y es un elemento químico c) se trata de una sustancia pura y es un compuesto químico 7. Un elemento químico se puede definir como: a) una sustancia pura que sí puede descomponerse en otras sustancias puras mediante algún procedimiento b) una sustanica pura que puede descomponerse a veces en otras sustancias puras mediante algún procedimiento c) una sustancia pura que no puede separarse en otras sustancias puras por ningún procedimiento 8. Un compuesto puede definirse como: a) una mezcla de elementos b) una clase de sustancia pura que puede ser separada en otras sustancias puras mediante procedimientos químicos (por ejemplo, reacciones químicas) c) una clase de sustancia pura que no puede ser separada en otras sustancias puras mediante procedimientos (por ejemplo, reacciones químicas) 9. Una mezcla heterogénea: a) hay partes de la mezcla con propiedades distintas b) todas las partes de la mezcla tienen las mismas propiedades c) todas las partes de la mezcla tienen igual densidad d) todas las partes de la mezcla tienen igual temperatura 10. Es cierto que una mezcla homogénea: a) es una clase especial de sustancia pura b) tiene las mismas propiedades en todas sus partes c) es una clase diferente de compuesto 11. Es cierto que una disolución: a) es una clase especial de compuesto b) es una clase especial de mezcla heterogénea c) está formada exclusivamente por mezcla de elementos químicos 12. Es cierto que la pura leche de vaca: a) es una sustancia muy pura b) es una mezcla homogénea c) sólo es pura según la marca 13. La siguiente mezcla es homogénea: a) turrón de almendra b) aire c) arena y agua d) cerveza con espuma 14. La siguiente mezcla es heterogénea: a) copa de cava con muchas burbujas b) agua embotellada c) leche de vaca d) bronce 10
3 15. Es cierto que las mezclas: a) no se pueden separar si son mezclas homogéneas b) se pueden separar por procedimientos físicos c) están hechas por componentes que pierden sus propiedades al ser separados 16. La filtración o tamizado: a) sirve para separar mezclas homogéneas b) se basa en que las partículas que forman la mezcla tienen tamaño diferente c) sirve para separar mezclas como agua y sal 17. La destilación es un método de separación de mezclas que se basa: a) las sustancias mezcladas tienen temperaturas de fusión diferentes b) las sustancias mezcladas tienen temperatura de sublimación diferentes c) las sustancias mezcladas tienen temperaturas de ebullición distintas 18. Los procesos que suceden en la destilación son: a) evaporación y condensación del vapor b) condensación del líquido y evaporación del vapor c) sublimación y condensación del vapor 19. Mediante un movimiento giratorio a gran velocidad, una mezcla de un sólido y un líquido, que no son miscibles, pueden separarse. Esta técnica de separación de mezclas se denomina: a) destilación b) cromatografía c) decantación 20. La centrifugación no se puede usar: a) para separar dos líquidos como agua y alcohol b) para separar arena y agua c) para separar las células de la sangre del plasma sanguíneo 21. Una mezcla de dos líquidos no miscibles como el aceite y el agua pueden separarse mediante: a) centrifugación b) tamizado c) cromatografía d) decantación 22. Una mezcla de limaduras de hierro y arena llegan a una fábrica. En la fábrica sólo necesitan las limaduras de hierro, cómo las separan de la arena? a) por disolución selectiva b) por separación magnética c) cribado d) decantación 23. Una mezcla formada por sal y agua puede separarse por: a) cristalización b) separación magnética c) cribado d) decantación 11
4 24. En un vaso de precipitados existe una mezcla de aceite, sal y arena. Los pasos correctos para conseguir separar cada uno de los componentes serían: a) filtar, añadir a agua a la mezcla de sólidos y volver a filtrar; finalmente,evaporar el agua b) añadir agua, filtrar y destilar; finalmente, evaporar el agua c) añadir agua, centrifugar; finalmente, evaporar el agua d) ninguna es correcta 25. La densidad de una sustancia pura: a) es la relación entre la masa y el volumen que esa masa ocupa b) es una propiedad característica de esa sustancia c) es siempre la misma d) todas son correctas 26. La densidad de una mezcla: a) es la relación entre la masa y el volumen que esa masa ocupa b) su valor se modifica según la composición de la mezcla c) puede utilizarse para afirmar que una sustancia es una mezcla 27. En un experimento realizado en el laboratorio, una sustancia sólida desconocida fue sometida a calentamiento. Durante el paso de sólido a líquido la temperatura permaneció constante a 75ºC. Con estos datos estamos seguros de que: a) se trata de una mezcla b) se trata de una sustancia pura c) se trata de un elemento d) se trata de un compuesto 28. Una sustancia líquida desconocida fue calentada hasta que comenzó a hervir. Durante el proceso la temperatura pasó de 98ºC a 101ºC. Con estos datos estamos seguros de que: a) se trata de una mezcla b) se trata de una sustancia pura c) se trata de un elemento d) se trata de un compuesto 29. En el proceso de cristalización, se consiguen obtener cristales grandes si la evaporación se realiza: a) rápidamente b) lentamente c) a velocidad intermedia 30. Los componentes de una disolución son: a) disolventes b) solutos c) disolvente y soluto 31. Al componente de una disolución que se encuentra en mayor proporción se le denomina: a) disolvente b) disoluto c) soluto 32. Al componente de una disolución que se encuentra en menor proporción se le denomina: a) disoluto b) disolvente c) soluto 12
5 33. En el agua del mar: a) el disolvente es el agua b) hay solutos que son sales c) hay solutos que son gases 34. Con relación a las disoluciones, es cierto que: a) las aleaciones, como el bronce, también se conocen como disoluciones sólidas b) es poco frecuente que un gas se disuelva en un sólido c) los solutos y los disolventes pueden estar en cualquier estado de agregación 35. Cuando se echa una gota de alcohol en agua: a) el disolvente es el alcohol b) el disolvente es el agua c) la mezcla es heterogénea 36. Cuando se echa una gota de agua en alcohol: a) el disolvente es el alcohol b) el disolvente es el agua c) la mezcla es heterogénea 37. Con relación al aire húmedo, no es cierta la siguiente afirmación: a) es una mezcla homogénea b) es una mezcla heterogénea c) la disolución se encuentra en estado gaseoso d) se podría considerar al aire como el disolvente y al agua como el soluto 38. Se añade sal, azúcar y agua en un vaso. Se puede afirmar que: a) no llegarán a mezclarse del todo b) seguro que la mezcla es heterogénea, porque la sal y el azúcar juntos no se disuelven bien en agua c) seguro que la mezcla es homogénea 39. La cantidad de soluto que hay disuelto en una cantidad de disolvente o de disolución es una forma de: a) calcular el tanto por ciento en masa b) calcular el tanto por ciento en volumen c) expresar la composición de una mezcla 40. El % en masa de un componente de una mezcla puede calcularse: a) dividiendo la masa de ese componente entre el total de la mezcla y multiplicando por cien b) dividiendo la masa de la mezcla entre la masa de ese componente y multiplicando por cien c) diviendo la masa de ese componente entre la masa del disolvente y multiplicando por cien 41. Se mezclan 30 g de sal y 70 g de azúcar. La composición de la mezcla es de: a) 70% en masa de azúcar b) 0,3% en masa de sal c) 0,7% en masa de azúcar 42. La mezcla de 50 g de agua, 5 g de sal y 15 g de bicarbonato tiene la siguiente composición: a) 10,2% de agua c) 21,4% de bicarbonato b) 5,1% de sal 13
6 43. El % en volumen suele usarse para expresar la composición: a) de mezcla de sólidos b) de mezcla de líquidos c) de mezcla se sal en aire 44. Con relación a la siguiente afirmación, "El grado alcohólico de una bebida representa el % en volumen de alcohol en esa bebida", hay que decir: a) es cierta sólo para bebidas de baja graduación como cerveza o vino b) es cierta sólo para bebidas de alta graduación como ginebra c) siempre es cierta 45. Se mezclan 125 cm3 de alcohol puro con 375 cm3 de agua. La composición de esa mezcla puede expresarse: a) 0,375% en volumen de agua b) 1,25% en volumen de alcohol c) 3,75% en volumen de agua d) 25% en volumen de alcohol 46. Una persona toma 330 cm3 de una cerveza de 4,5º de alcohol. Esa persona ha ingerido la siguiente cantidad de alcohol puro: a) 4,5 cm3 de alcohol puro b) 3,30 cm3 de alcohol puro c) 14,85 cm3 de alcohol puro 47. Es cierto que otra forma de expresar la composición de una mezcla, sobre todo si es una disolución acuosa, es: a) dividir la masa del soluto entre el volumen de la mezcla b) dividir la masa del soluto entre el volumen de la disolución c) dividir la masa del soluto entre el volumen del conjunto soluto y disolvente 48. Cuando a 15g de sal se añade agua hasta que el volumen es de 2 litros, se obtiene una concentración de: a) 75% b) 7,5 g/l c) 0,88% 49. La cantidad máxima de una sustancia que se puede disolver en un determinado disolvente se conoce con el nombre de: a) concentración máxima b) máxima mezcla c) solubilidad 50. La solubilidad de una sustancia en un determinado disolvente depende de: a) la temperatura b) la concentración c) el calor 51. La solubilidad del azúcar en agua: a) es mayor cuando la temperatura es menor b) es mayor cuando la temperatura es alta c) no depende de la temperatura sino de la cantidad de azúcar que se eche 14
7 52. Es cierto que los gases: a) se disuelven más en un líquido a temperatura elevada b) se disuelven menos en un líquido a temperatura elevada c) no se disuelven en agua 53. Es cierto que los gases de la bebidas: a) están disueltos pero mezclados b) se disuelven más a temperatura elevada c) se disuelven más a temperaturas bajas 54. Cuando se ha conseguido disolver la máxima cantidad de soluto posible, se obtiene una disolución: a) insaturada b) maximalista c) sobresaturada 55. Una disolución en la que existe gran cantidad de soluto se dice que es: a) concentrada b) diluida c) semiconcentrada 56. Una disolución con muy poca cantidad de soluto se dice que es: a) concentrada b) diluida c) semiconcentrada 57. La solubilidad de los gases en los líquidos también dependen de la presión. Así, cuando la presión aumenta: a) la solubilidad disminuye b) la solubilidad aumenta c) la solubilidad se mantiene constante 58. Una disolución saturada puede que sea diluida: a) cierto, porque hay sustancia que se disuelven muy poco en un disolvente b) falso, porque saturada quiere decir concentrada c) falso, porque un disolvente es un buen disolvente 59. Una disolución saturada puede ser concentrada: a) cierto, porque hay sustancias que se disuelven mucho en un disolvente b) falto, porque hay sustancias que se disuelven poco en un disolvente c) cierto, porque saturada siempre quiere decir concentrada 60. Una gráfica en donde se representa la solubilidad (eje y) en función de la temperatura (eje x), recibe el nombre de: a) curvas de temperatura b) curvas de solubilidad creciente c) curvas de solubilidad d) curvas de solubilidad decreciente 61. Es lo mismo solubilidad que velocidad de disolución? a) sí, porque una sustancia muy soluble también se disuelve muy rápido b) sí, porque una sustancia que tarda en disolverse es poco soluble c) no, porque la rapidez con que se disuelve una sustancia depende de factores como la temperatura, agitación o 15
8 grado de pulverización de la muestra 62. Se dice que dos líquidos son inmiscibles entre sí, cuando: a) se disuelven el uno en el otro b) no se disuelven el uno en el otro c) las partículas que forman los líquidos se entremeten las unas entre las otras Clave (b) (d) 2. (a) 3. (d) 4. (a) 5. (b) 6. (c) 7. (c) 8. (b) 9. (a) 10. (b) 11. (d) 12. (b) 13. (b) 14. (a) 15. (b) 16. (b) 17. (c) 18. (a) 19. (d) 20. (a) 21. (d) 22. (b) 23. (a) 24. (a) 25. (d) 26. (d) 27. (b) 28. (a) 29. (b) 30. (c) 31. (a) 32. (c) 33. (d) 34. (d) 35. (b) 36. (a) 37. (b) 38. (d) 39. (c) 40. (a) 41. (a) 42. (c) 43. (b) 44. (c) 45. (d) 46. (c) 47. (d) 48. (b) 49. (c) 50. (a) 51. (b) 52. (b) 53. (c) 54. (d) 55. (a) 56. (b) 57. (b) 58. (a) 59. (a) 60. (c) 61. (c) 62. (b) TEMA 4 1. Que la materia estuviera hecha de partículas muy pequeñas a) se probó científicamente en el siglo XX b) esta idea ya había sido propuesta por filósofos griegos hace unos 2500 años c) el gran filósofo griego Aristóteles estaba en contra 2. La teoría atómica de Dalton afirma: a) los átomos son partículas indivisibles b) los átomos están hechos de protones, neutrones y electrones c) los átomos están hehcos de electrones y de protones 3. Respecto a los átomos de un mismo elemento químico: a) según Dalton todos son iguales b) es posible que siendo átomos de un mismo elemento químico no sean iguales porque tengan masas distintas c) tienen las mismas propiedades químicas 4. Un compuesto es una sustancia pura que está formada: a) por la unión de átomos b) por la unión de moléculas c) por la unión de átomos y moléculas, según el compuesto que se trate 5. Los nombres que aparecen en la tabla periódica a) se refieren a elementos químicos conocidos b) se refieren a las clases de átomos diferentes que forman la materia que se conoce c) se refieren a un tipo de sustancia pura denominada elementos químicos 16
TEMA 3. CLASIFICACIÓN DE LA MATERIA.
 TEMA 3. CLASIFICACIÓN DE LA MATERIA. FÍSICA Y QUÍMICA 3º ESO 1. CLASIFICACIÓN DE LA MATERIA SUSTANCIAS PURAS. Son las que tienen siempre las mismas propiedades físicas y químicas. - Elemento. Es una sustancia
TEMA 3. CLASIFICACIÓN DE LA MATERIA. FÍSICA Y QUÍMICA 3º ESO 1. CLASIFICACIÓN DE LA MATERIA SUSTANCIAS PURAS. Son las que tienen siempre las mismas propiedades físicas y químicas. - Elemento. Es una sustancia
FÍSICA Y QUÍMICA 3ºESO
 TEMA 3. CLASIFICACIÓN DE LA MATERIA. FÍSICA Y QUÍMICA 3ºESO 1. CLASIFICACIÓN DE LA MATERIA SUSTANCIAS PURAS. Son las que tienen siempre las mismas propiedades físicas y químicas. Por ejemplo siempre tienen
TEMA 3. CLASIFICACIÓN DE LA MATERIA. FÍSICA Y QUÍMICA 3ºESO 1. CLASIFICACIÓN DE LA MATERIA SUSTANCIAS PURAS. Son las que tienen siempre las mismas propiedades físicas y químicas. Por ejemplo siempre tienen
PCPI Ámbito Científico-Tecnológico LA MATERIA
 LA MATERIA La materia es todo aquello que ocupa lugar en el espacio y tiene masa. Un sistema material es una porción de materia que, para su estudio, aislamos del resto. La materia está formada por partículas
LA MATERIA La materia es todo aquello que ocupa lugar en el espacio y tiene masa. Un sistema material es una porción de materia que, para su estudio, aislamos del resto. La materia está formada por partículas
Tema 13: La materia Ciencias Naturales 1º ESO página 1. Materia es todo aquello que posee masa y ocupa un volumen. Está formada de partículas muy
 Tema 13: La materia Ciencias Naturales 1º ESO página 1 TEMA 13: LA MATERIA, BASE DEL UNIVERSO 1. Qué es materia? Materia es todo aquello que posee masa y ocupa un volumen. Está formada de partículas muy
Tema 13: La materia Ciencias Naturales 1º ESO página 1 TEMA 13: LA MATERIA, BASE DEL UNIVERSO 1. Qué es materia? Materia es todo aquello que posee masa y ocupa un volumen. Está formada de partículas muy
LA MATERIA, SUS PROPIEDADE, ESTADOS Y DIFERENTES CLASES DE SUSTANCIAS
 LA MATERIA, SUS PROPIEDADE, ESTADOS Y DIFERENTES CLASES DE SUSTANCIAS 1.- Todos los objetos y cuerpos están formados por alguna sustancia. Las sustancias puede ser distintas, pero todo es materia. La materia
LA MATERIA, SUS PROPIEDADE, ESTADOS Y DIFERENTES CLASES DE SUSTANCIAS 1.- Todos los objetos y cuerpos están formados por alguna sustancia. Las sustancias puede ser distintas, pero todo es materia. La materia
ESTADOS DE LA MATERIA. CAMBIOS DE ESTADO.
 ESTADOS DE LA MATERIA. CAMBIOS DE ESTADO. Propiedades generales y específicas. Densidad. Estados de agregación de la materia. Cambios de estado. Diferencias entre evaporación y ebullición. Temperatura
ESTADOS DE LA MATERIA. CAMBIOS DE ESTADO. Propiedades generales y específicas. Densidad. Estados de agregación de la materia. Cambios de estado. Diferencias entre evaporación y ebullición. Temperatura
2 Sustancias puras y mezclas
 2 Sustancias puras y mezclas Sustancias puras Llamamos sustancia pura a cualquier material que tiene unas propiedades características que la distinguen claramente de otras. Algunas de estas propiedades
2 Sustancias puras y mezclas Sustancias puras Llamamos sustancia pura a cualquier material que tiene unas propiedades características que la distinguen claramente de otras. Algunas de estas propiedades
qwertyuiopasdfghjklzxcvbnmqwerty uiopasdfghjklzxcvbnmqwertyuiopasd fghjklzxcvbnmqwertyuiopasdfghjklzx cvbnmqwertyuiopasdfghjklzxcvbnmq
 qwertyuiopasdfghjklzxcvbnmqwerty uiopasdfghjklzxcvbnmqwertyuiopasd fghjklzxcvbnmqwertyuiopasdfghjklzx cvbnmqwertyuiopasdfghjklzxcvbnmq ACTIVIDADES DE RECUPERACIÓN DE FÍSICA Y QUÍMICA 3º ESO 2º TRIMESTRE
qwertyuiopasdfghjklzxcvbnmqwerty uiopasdfghjklzxcvbnmqwertyuiopasd fghjklzxcvbnmqwertyuiopasdfghjklzx cvbnmqwertyuiopasdfghjklzxcvbnmq ACTIVIDADES DE RECUPERACIÓN DE FÍSICA Y QUÍMICA 3º ESO 2º TRIMESTRE
MEZCLAS Y METODOS http://biologiaudes.wordpress.com/periodo-4/mezclas-y-metodos-deseparacion/de SEPARACION
 MEZCLAS Y METODOS http://biologiaudes.wordpress.com/periodo-4/mezclas-y-metodos-deseparacion/de SEPARACION Las Mezclas Son materiales que contienen dos o más sustancias simple, que pueden ser separadas
MEZCLAS Y METODOS http://biologiaudes.wordpress.com/periodo-4/mezclas-y-metodos-deseparacion/de SEPARACION Las Mezclas Son materiales que contienen dos o más sustancias simple, que pueden ser separadas
Tema 3: Ecuaciones químicas y concentraciones
 Tema 3: Ecuaciones químicas y concentraciones Definición de disolución. Clases de disoluciones. Formas de expresar la concentración de una disolución. Proceso de dilución. Solubilidad. Diagramas de fases
Tema 3: Ecuaciones químicas y concentraciones Definición de disolución. Clases de disoluciones. Formas de expresar la concentración de una disolución. Proceso de dilución. Solubilidad. Diagramas de fases
Disoluciones químicas
 Disoluciones químicas Recordemos. Qué son las disoluciones químicas? Mezcla homogénea, constituida por dos o más componentes Soluciones = disoluciones COMPONENTES DE UNA DISOLUCION SOLUTO: Es la sustancia
Disoluciones químicas Recordemos. Qué son las disoluciones químicas? Mezcla homogénea, constituida por dos o más componentes Soluciones = disoluciones COMPONENTES DE UNA DISOLUCION SOLUTO: Es la sustancia
27. (b) 28. (a) 29. (b) 30. (c) 31. (a) 32. (c) 33. (d) 34. (d) 35. (b) 36. (a) 37. (b) 38. (d) 39. (c) TEMA 4
 grado de pulverización de la muestra 62. Se dice que dos líquidos son inmiscibles entre sí, cuando: a) se disuelven el uno en el otro b) no se disuelven el uno en el otro c) las partículas que forman los
grado de pulverización de la muestra 62. Se dice que dos líquidos son inmiscibles entre sí, cuando: a) se disuelven el uno en el otro b) no se disuelven el uno en el otro c) las partículas que forman los
Actividad: Mezcla homogénea o heterogénea?
 Mezcla homogénea o heterogénea? Nivel: 2º Medio Subsector: Ciencias químicas Unidad temática: Actividad: Mezcla homogénea o heterogénea? Cuál es la diferencia entre una mezcla homogénea y una heterogénea?
Mezcla homogénea o heterogénea? Nivel: 2º Medio Subsector: Ciencias químicas Unidad temática: Actividad: Mezcla homogénea o heterogénea? Cuál es la diferencia entre una mezcla homogénea y una heterogénea?
SEPARACIÓN DE LOS COMPONENTES DE UNA MEZCLA OBJETIVOS: Establecer los fundamentos teóricos de los proceso de separación.
 PRÁCTICA Nº 2 SEPARACIÓN DE LOS COMPONENTES DE UNA MEZCLA OBJETIVOS: Establecer los fundamentos teóricos de los proceso de separación. Separar los componentes de una muestra problema. Realizar la destilación
PRÁCTICA Nº 2 SEPARACIÓN DE LOS COMPONENTES DE UNA MEZCLA OBJETIVOS: Establecer los fundamentos teóricos de los proceso de separación. Separar los componentes de una muestra problema. Realizar la destilación
Solubilidad. Material de apoyo, Segundo Medio monica.ibanez@lbvm. onica.ibanez@lbvm.clcl 15:21
 Solubilidad Material de apoyo, Segundo Medio monica.ibanez@lbvm. onica.ibanez@lbvm.clcl Obj. de hoy: Señalar que es Solubilidad y los factores que la afectan. Qué es algo SOLUBLE? La Solubilidad corresponde
Solubilidad Material de apoyo, Segundo Medio monica.ibanez@lbvm. onica.ibanez@lbvm.clcl Obj. de hoy: Señalar que es Solubilidad y los factores que la afectan. Qué es algo SOLUBLE? La Solubilidad corresponde
La materia. Clasificación de la materia
 27 de marzo de 2005 Contenidos 1 Introducción La materia 2 La materia Qué es la materia? Materia es todo aquello que tiene masa y posee volumen. La materia Qué es la materia? Materia es todo aquello que
27 de marzo de 2005 Contenidos 1 Introducción La materia 2 La materia Qué es la materia? Materia es todo aquello que tiene masa y posee volumen. La materia Qué es la materia? Materia es todo aquello que
2. Ordena las letras para obtener los nombres de los cambios de estado que se definen en cada casilla.
 1. Observa las figuras, lee los textos y responde: Un trozo de mármol no varía su forma si lo cambiamos de posición. Su volumen tampoco cambia aunque lo apretemos con la mano. Podemos cambiar la forma
1. Observa las figuras, lee los textos y responde: Un trozo de mármol no varía su forma si lo cambiamos de posición. Su volumen tampoco cambia aunque lo apretemos con la mano. Podemos cambiar la forma
TEMA 1: LA CIENCIA Y SU MÉTODO. MEDIDA DE MAGNITUDES
 Nombre Grupo TEMA 1: LA CIENCIA Y SU MÉTODO. MEDIDA DE MAGNITUDES 5. Realiza cálculos y expresa las siguientes cantidades en unidades del Sistema Internacional. a) 237 mm b) 50 horas 1. Cuándo una hipótesis
Nombre Grupo TEMA 1: LA CIENCIA Y SU MÉTODO. MEDIDA DE MAGNITUDES 5. Realiza cálculos y expresa las siguientes cantidades en unidades del Sistema Internacional. a) 237 mm b) 50 horas 1. Cuándo una hipótesis
Materia. Definición, propiedades, cambios de la materia y energía, clasificación de la materia.
 TEMA 02 Materia. Definición, propiedades, cambios de la materia y energía, clasificación de la materia. -.-.-.-.-.-.-.-.-..-..-..-..-..-..-.-..-..-..-..-..-.-..-.-..-.-.-.-..-.-...-..-.-..-.-..-.-..-.-..-.-..-.-..-.-..-.-
TEMA 02 Materia. Definición, propiedades, cambios de la materia y energía, clasificación de la materia. -.-.-.-.-.-.-.-.-..-..-..-..-..-..-.-..-..-..-..-..-.-..-.-..-.-.-.-..-.-...-..-.-..-.-..-.-..-.-..-.-..-.-..-.-..-.-
1.2 LA MATERIA Y LOS CAMBIOS
 1.2 LA MATERIA Y LOS CAMBIOS Por equipo definir que es átomo, molécula y de que están formados Equipo Átomo Molécula 1 2 3 4 5 6 7 8 ÁTOMO 1. Un átomo es eléctricamente neutro. tiene el mismo número
1.2 LA MATERIA Y LOS CAMBIOS Por equipo definir que es átomo, molécula y de que están formados Equipo Átomo Molécula 1 2 3 4 5 6 7 8 ÁTOMO 1. Un átomo es eléctricamente neutro. tiene el mismo número
LA MATERIA SISTEMAS MATERIALES CAMBIOS PROPIEDADES POSEE SE TRANSFORMA FORMA. pueden ser. pueden ser. pueden ser QUÍMICOS FÍSICOS
 LA MATERIA POSEE FORMA SE TRANSFORMA PROPIEDADES SISTEMAS MATERIALES CAMBIOS pueden ser pueden ser pueden ser GENERALES PARTICULARES ESPECIFÍCAS HOMOGÉNEOS HETEROGÉNEOS FÍSICOS QUÍMICOS MASA VOLUMEN TEMPERATURA
LA MATERIA POSEE FORMA SE TRANSFORMA PROPIEDADES SISTEMAS MATERIALES CAMBIOS pueden ser pueden ser pueden ser GENERALES PARTICULARES ESPECIFÍCAS HOMOGÉNEOS HETEROGÉNEOS FÍSICOS QUÍMICOS MASA VOLUMEN TEMPERATURA
MEZCLAS Y DISOLUCIONES
 Unidades Didácticas Adaptadas 1 MEZCLAS Y DISOLUCIONES Qué vamos a estudiar en este tema?. Aquí tienes el esquema. 1. Las sustancias puras y las mezclas. 2. Observamos las mezclas a nuestro alrededor!
Unidades Didácticas Adaptadas 1 MEZCLAS Y DISOLUCIONES Qué vamos a estudiar en este tema?. Aquí tienes el esquema. 1. Las sustancias puras y las mezclas. 2. Observamos las mezclas a nuestro alrededor!
QUÍMICA I. TEMA 1: Estado Físico de la materia
 QUÍMICA I TEMA 1: Estado Físico de la materia Tecnólogo Minero - 2014 E s q u e m a d e l a C l a s e Tema 1: Estado físico de la materia La materia Clasificación de la materia Estado Sólido, liquido y
QUÍMICA I TEMA 1: Estado Físico de la materia Tecnólogo Minero - 2014 E s q u e m a d e l a C l a s e Tema 1: Estado físico de la materia La materia Clasificación de la materia Estado Sólido, liquido y
MEZCLAS Y DISOLUCIONES. Física y Química 3º de E.S.O. IES Isidra de Guzmán
 MEZCLAS Y DISOLUCIONES Física y Química 3º de E.S.O. IES Isidra de Guzmán Introducción Ya sabes que los sistemas materiales se pueden clasificar según su composición en sustancias puras y mezclas. Las
MEZCLAS Y DISOLUCIONES Física y Química 3º de E.S.O. IES Isidra de Guzmán Introducción Ya sabes que los sistemas materiales se pueden clasificar según su composición en sustancias puras y mezclas. Las
1. Las propiedades de los gases
 1. Las propiedades de los gases Para establecer por qué las diferentes sustancias tienen unas propiedades características de cada una de ellas (densidades, puntos de cambios de estado, solubilidad en agua,
1. Las propiedades de los gases Para establecer por qué las diferentes sustancias tienen unas propiedades características de cada una de ellas (densidades, puntos de cambios de estado, solubilidad en agua,
Materia: Todo aquello que existe en el universo, que posee masa y está ocupando un lugar en el
 LA QUÍMICA La química estudia la naturaleza de la materia, su composición, propiedades, transformaciones que sufre y las leyes que gobiernan esos cambios. Materia: Todo aquello que existe en el universo,
LA QUÍMICA La química estudia la naturaleza de la materia, su composición, propiedades, transformaciones que sufre y las leyes que gobiernan esos cambios. Materia: Todo aquello que existe en el universo,
Tema 7. Las mezclas. Introducción
 Tema 7. Las mezclas Introducción Ya sabes que los sistemas materiales se pueden clasificar según su composición en sustancias puras y mezclas. Las sustancias puras son los elementos y los compuestos que
Tema 7. Las mezclas Introducción Ya sabes que los sistemas materiales se pueden clasificar según su composición en sustancias puras y mezclas. Las sustancias puras son los elementos y los compuestos que
Física y Química - 3º ESO
 C O L L E G I S A N A N T O N I O D E P A D U A F R A N C I S C A N S L C A R C A I X E N T C U R S 2 0 1 1 / 2 0 1 2 Física y Química - 3º ESO Tema 1 La ciencia y su método. Medida de magnitudes. Anexo
C O L L E G I S A N A N T O N I O D E P A D U A F R A N C I S C A N S L C A R C A I X E N T C U R S 2 0 1 1 / 2 0 1 2 Física y Química - 3º ESO Tema 1 La ciencia y su método. Medida de magnitudes. Anexo
SISTEMAS MATERIALES. Departamento de Física y Química 2º ESO
 SISTEMAS MATERIALES Departamento de Física y Química 2º ESO 0. Mapa conceptual MATERIA Sustancias puras Mezclas Heterogéneas Homogéneas Sistemas coloidales Técnicas de separación Disoluciones Soluto Disolvente
SISTEMAS MATERIALES Departamento de Física y Química 2º ESO 0. Mapa conceptual MATERIA Sustancias puras Mezclas Heterogéneas Homogéneas Sistemas coloidales Técnicas de separación Disoluciones Soluto Disolvente
Curso 2014/15 Física y Química 3º ESO ACTIVIDADES DE REFUERZO PRIMER TRIMESTRE Nombre: Apellidos:
 Curso 2014/15 Física y Química 3º ESO ACTIVIDADES DE REFUERZO PRIMER TRIMESTRE Nombre: Apellidos: Fecha de entrega: día del examen de recuperación. 1. Contesta brevemente las siguientes preguntas relacionadas
Curso 2014/15 Física y Química 3º ESO ACTIVIDADES DE REFUERZO PRIMER TRIMESTRE Nombre: Apellidos: Fecha de entrega: día del examen de recuperación. 1. Contesta brevemente las siguientes preguntas relacionadas
TEMA 3: MEZCLAS, DISOLUCIONES Y SUSTANCIAS PURAS
 TEMA 3: MEZCLAS, DISOLUCIONES Y SUSTANCIAS PURAS 1. LA MATERIA Y SU ASPECTO Los sistemas materiales, formados por una o varias sustancias, pueden clasificarse en: - Sistemas materiales heterogéneos: presentan
TEMA 3: MEZCLAS, DISOLUCIONES Y SUSTANCIAS PURAS 1. LA MATERIA Y SU ASPECTO Los sistemas materiales, formados por una o varias sustancias, pueden clasificarse en: - Sistemas materiales heterogéneos: presentan
qwertyuiopasdfghjklzxcvbnmqwerty uiopasdfghjklzxcvbnmqwertyuiopasd fghjklzxcvbnmqwertyuiopasdfghjklzx cvbnmqwertyuiopasdfghjklzxcvbnmq
 qwertyuiopasdfghjklzxcvbnmqwerty uiopasdfghjklzxcvbnmqwertyuiopasd fghjklzxcvbnmqwertyuiopasdfghjklzx cvbnmqwertyuiopasdfghjklzxcvbnmq Actividades de recuperación de 2º trimestre 3º ESO wertyuiopasdfghjklzxcvbnmqwertyui
qwertyuiopasdfghjklzxcvbnmqwerty uiopasdfghjklzxcvbnmqwertyuiopasd fghjklzxcvbnmqwertyuiopasdfghjklzx cvbnmqwertyuiopasdfghjklzxcvbnmq Actividades de recuperación de 2º trimestre 3º ESO wertyuiopasdfghjklzxcvbnmqwertyui
Se entiende por disolución toda mezcla homogénea de dos o más componentes en proporción variable.
 6. DISOLUCIONES 6.1. Generalidades Se entiende por disolución toda mezcla homogénea de dos o más componentes en proporción variable. Las disoluciones objeto de nuestro estudio serán binarias, en las que
6. DISOLUCIONES 6.1. Generalidades Se entiende por disolución toda mezcla homogénea de dos o más componentes en proporción variable. Las disoluciones objeto de nuestro estudio serán binarias, en las que
CLASIFICACIÓN DE LA MATERIA
 1. Clasificación de la materia por su aspecto CLASIFICACIÓN DE LA MATERIA La materia homogénea es la que presenta un aspecto uniforme, en la cual no se pueden distinguir a simple vista sus componentes.
1. Clasificación de la materia por su aspecto CLASIFICACIÓN DE LA MATERIA La materia homogénea es la que presenta un aspecto uniforme, en la cual no se pueden distinguir a simple vista sus componentes.
DISOLUCIONES. Molécula de agua (disolvente) iones solvatados
 DISOLUCIONES Una disolución es una mezcla homogénea (los componentes no se pueden distinguir a simple vista) de dos a más sustancias. En las disoluciones hay que distinguir el soluto, el disolvente y la
DISOLUCIONES Una disolución es una mezcla homogénea (los componentes no se pueden distinguir a simple vista) de dos a más sustancias. En las disoluciones hay que distinguir el soluto, el disolvente y la
La materia se puede definir como todo aquello que tiene masa y ocupa un volumen.
 Tema 2: LA MATERIA Que es la materia? La materia se puede definir como todo aquello que tiene masa y ocupa un volumen. Clasificación de la materia (criterio: separación) Mezclas Sustancias puras Composición
Tema 2: LA MATERIA Que es la materia? La materia se puede definir como todo aquello que tiene masa y ocupa un volumen. Clasificación de la materia (criterio: separación) Mezclas Sustancias puras Composición
Teoría cinética de la materia
 Teoría cinética de la materia Hechos y observaciones Movimiento browniano de granos de polen en agua Descubrimiento accidental Reproducible con partículas inertes Los sólidos se disuelven Los sólidos se
Teoría cinética de la materia Hechos y observaciones Movimiento browniano de granos de polen en agua Descubrimiento accidental Reproducible con partículas inertes Los sólidos se disuelven Los sólidos se
Las disoluciones son mezclas homogéneas. Están compuestas por un soluto y un disolvente.
 Liceo Confederación Suiza Guía de aprendizaje Agosto,2014 SECTOR: Química PROFESORA: Genny Astudillo Castillo UNIDAD TEMÁTICA o DE APRENDIZAJE: Disoluciones NIVEL/CURSO:2 Medio CONTENIDO: -Conceptos Básicos
Liceo Confederación Suiza Guía de aprendizaje Agosto,2014 SECTOR: Química PROFESORA: Genny Astudillo Castillo UNIDAD TEMÁTICA o DE APRENDIZAJE: Disoluciones NIVEL/CURSO:2 Medio CONTENIDO: -Conceptos Básicos
1. MATERIA Y SU ASPECTO
 1. MATERIA Y SU ASPECTO El aspecto de un sistema material puede variar según el método de observación. Algunos sistemas materiales como la leche, la sangre o la mantequilla a simple vista parecen uniformes,
1. MATERIA Y SU ASPECTO El aspecto de un sistema material puede variar según el método de observación. Algunos sistemas materiales como la leche, la sangre o la mantequilla a simple vista parecen uniformes,
Contenido de Física y Química Conceptos y ejercicios - 13-14
 Contenido de Física y Química Conceptos y ejercicios - 13-14 Concepto Teoría (Conceptos) Práctica (Ejercicios) Óxidos básicos (M+O) Nomenclatura. Tablas de formulación. Óxidos ácidos (NM+O) Nomenclatura.
Contenido de Física y Química Conceptos y ejercicios - 13-14 Concepto Teoría (Conceptos) Práctica (Ejercicios) Óxidos básicos (M+O) Nomenclatura. Tablas de formulación. Óxidos ácidos (NM+O) Nomenclatura.
TRABAJO FINAL CURSO EVALUACIONES EXTERNAS INTERNACIONALES DEL SISTEMA EDUCATIVO. Fecha: 31/05/2014. Autor: Idoia Alkorta.
 TRABAJO FINAL CURSO EVALUACIONES EXTERNAS INTERNACIONALES DEL SISTEMA EDUCATIVO Fecha: 31/05/2014 Autor: Idoia Alkorta Página 1 de 20 Contenido 1. Matriz de especificaciones.... 3 2. Estímulos e ítems....
TRABAJO FINAL CURSO EVALUACIONES EXTERNAS INTERNACIONALES DEL SISTEMA EDUCATIVO Fecha: 31/05/2014 Autor: Idoia Alkorta Página 1 de 20 Contenido 1. Matriz de especificaciones.... 3 2. Estímulos e ítems....
UNIDAD 4. La materia: propiedades eléctricas y el átomo
 PRUEBAS EXTRAORDINARIA DE FÍSICA Y QUÍMICA DE 3º y 4º ESO 1.- CONTENIDOS MÍNIMOS 3º DE LA ESO UNIDAD 1. La ciencia, la materia y su medida 1. Diferenciar ciencia y pseudociencia. 2. Distinguir entre propiedades
PRUEBAS EXTRAORDINARIA DE FÍSICA Y QUÍMICA DE 3º y 4º ESO 1.- CONTENIDOS MÍNIMOS 3º DE LA ESO UNIDAD 1. La ciencia, la materia y su medida 1. Diferenciar ciencia y pseudociencia. 2. Distinguir entre propiedades
Soluciones y solubilidad Capítulo 3
 Soluciones y solubilidad Capítulo 3 Editorial Contexto 010 - www.editorialcontexto.com.uy - 9019493 Una solución es todo sistema homogéneo formado por más de una sustancia. Al mencionar soluciones es necesario
Soluciones y solubilidad Capítulo 3 Editorial Contexto 010 - www.editorialcontexto.com.uy - 9019493 Una solución es todo sistema homogéneo formado por más de una sustancia. Al mencionar soluciones es necesario
UNIDAD 5: LOS ÁTOMOS Y LAS MOLÉCULAS
 UNIDAD 5: LOS ÁTOMOS Y LAS MOLÉCULAS Lee atentamente: 1. LA MISMA SUSTANCIA EN LOS TRES ESTADOS Todos los cuerpos están formados por sustancias: las personas, los coches, los muebles, el aire, etc. Todas
UNIDAD 5: LOS ÁTOMOS Y LAS MOLÉCULAS Lee atentamente: 1. LA MISMA SUSTANCIA EN LOS TRES ESTADOS Todos los cuerpos están formados por sustancias: las personas, los coches, los muebles, el aire, etc. Todas
4. TEORÍA ATÓMICO-MOLECULAR
 4. TEORÍA ATÓMICO-MOLECULAR Sustancias que reaccionan 1. Explica qué son los procesos o cambios físicos y pon ejemplos de ellos. Los procesos o cambios físicos no producen modificaciones en la naturaleza
4. TEORÍA ATÓMICO-MOLECULAR Sustancias que reaccionan 1. Explica qué son los procesos o cambios físicos y pon ejemplos de ellos. Los procesos o cambios físicos no producen modificaciones en la naturaleza
FÍSICA Y QUÍMICA 1º Bachillerato Ejercicios: Sistemas Físicos y Químicos
 1(7) Ejercicio nº 1 Una muestra de sulfuro de hierro de 60,5 g contiene 28 g de azufre. Cuál es la fórmula empírica de dicho compuesto? Ejercicio nº 2 150 g de un compuesto contienen 45,65 g de nitrógeno
1(7) Ejercicio nº 1 Una muestra de sulfuro de hierro de 60,5 g contiene 28 g de azufre. Cuál es la fórmula empírica de dicho compuesto? Ejercicio nº 2 150 g de un compuesto contienen 45,65 g de nitrógeno
CIENCIAS DE LA NATURALEZA 1º ESO BLOQUE FÍSICA / QUÍMICA
 CIENCIAS DE LA NATURALEZA 1º ESO BLOQUE FÍSICA / QUÍMICA El último bloque de la asignatura de ciencias de la naturaleza corresponde al estudio de los conceptos más básicos de física y química. La FÍSICA
CIENCIAS DE LA NATURALEZA 1º ESO BLOQUE FÍSICA / QUÍMICA El último bloque de la asignatura de ciencias de la naturaleza corresponde al estudio de los conceptos más básicos de física y química. La FÍSICA
ÁREA DE INGENIERÍA QUÍMICA Prof. Isidoro García García. Operaciones Básicas de Transferencia de Materia. Tema 1
 ÁREA DE INGENIERÍA QUÍMICA Operaciones Básicas de Transferencia de Materia Los procesos químicos modifican las condiciones de una determinada cantidad de materia: modificando su masa o composición modificando
ÁREA DE INGENIERÍA QUÍMICA Operaciones Básicas de Transferencia de Materia Los procesos químicos modifican las condiciones de una determinada cantidad de materia: modificando su masa o composición modificando
UNIDAD 3: LA MATERIA Y SUS ESTADOS DE AGREGACIÓN
 UNIDAD 3: LA MATERIA Y SUS ESTADOS DE AGREGACIÓN MATERIA Es todo aquello que ocupa un lugar en el espacio y tiene la característica de tener masa. SÓLIDOS LÍQUIDOS Algoritmo para reconocer cada uno: SEPARACIÓN
UNIDAD 3: LA MATERIA Y SUS ESTADOS DE AGREGACIÓN MATERIA Es todo aquello que ocupa un lugar en el espacio y tiene la característica de tener masa. SÓLIDOS LÍQUIDOS Algoritmo para reconocer cada uno: SEPARACIÓN
Materia: es aquello que ocupa un lugar en el espacio y cuyas propiedades percibimos por los sentidos. Es diversa y discontinua.
 Sistemas materiales Materia: es aquello que ocupa un lugar en el espacio y cuyas propiedades percibimos por los sentidos. Es diversa y discontinua. Mezcla Heterogénea: unión de dos o más sustancias de
Sistemas materiales Materia: es aquello que ocupa un lugar en el espacio y cuyas propiedades percibimos por los sentidos. Es diversa y discontinua. Mezcla Heterogénea: unión de dos o más sustancias de
PRUEBA DE ACCESO A LA UNIVERSIDAD PARA MAYORES DE 25 AÑOS PRUEBA ESPECÍFICA QUÍMICA
 PRUEBA DE ACCESO A LA UNIVERSIDAD PARA MAYORES DE 5 AÑOS QUÍMICA 1.- Cómo se nombra este compuesto? Seleccione la respuesta correcta a) -in-propano b) butano c) butino d) 1-in-propano CH C CH CH.- Una
PRUEBA DE ACCESO A LA UNIVERSIDAD PARA MAYORES DE 5 AÑOS QUÍMICA 1.- Cómo se nombra este compuesto? Seleccione la respuesta correcta a) -in-propano b) butano c) butino d) 1-in-propano CH C CH CH.- Una
3. C 2. 4. Un recipiente tiene la siguiente etiqueta
 2 AC - 002-112 PREGUNTAS DE SELECCÓN MÚLTPLE CON ÚNCA RESPUESTA - (TPO ) Estas preguntas constan de un enunciado y cuatro posibilidades de respuesta, entre las cuales usted debe escoger la que considere
2 AC - 002-112 PREGUNTAS DE SELECCÓN MÚLTPLE CON ÚNCA RESPUESTA - (TPO ) Estas preguntas constan de un enunciado y cuatro posibilidades de respuesta, entre las cuales usted debe escoger la que considere
Clasificación de la materia
 Clasificación de la materia Sustancias Puras Son caracterizados por su composición y propiedades definidas y constantes bajo condiciones determinadas. Sustancias puras: Elementos Son sustancias puras formadas
Clasificación de la materia Sustancias Puras Son caracterizados por su composición y propiedades definidas y constantes bajo condiciones determinadas. Sustancias puras: Elementos Son sustancias puras formadas
La Materia y la energía. Javiera Mujica Nivelación de estudios CREA
 La Materia y la energía Javiera Mujica Nivelación de estudios CREA La materia La materia es todo lo que tiene masa y ocupa un lugar en el espacio. La materia es cuantificable La cantidad de materia de
La Materia y la energía Javiera Mujica Nivelación de estudios CREA La materia La materia es todo lo que tiene masa y ocupa un lugar en el espacio. La materia es cuantificable La cantidad de materia de
CONCENTRACIÓN DE LAS DISOLUCIONES
 CONCENTRACIÓN DE LAS DISOLUCIONES NOMBRE DEL ALUMNO: PROFESOR: GRUPO: 2. Espacio sugerido: Laboratorio de usos múltiples. 3. Desempeño y habilidades: 4. Marco Teórico: 1. Obtiene, registra y sistematiza
CONCENTRACIÓN DE LAS DISOLUCIONES NOMBRE DEL ALUMNO: PROFESOR: GRUPO: 2. Espacio sugerido: Laboratorio de usos múltiples. 3. Desempeño y habilidades: 4. Marco Teórico: 1. Obtiene, registra y sistematiza
Física y Química: guía interactiva para la resolución de ejercicios
 Física y Química: guía interactiva para la resolución de ejercicios CLASIFICACIÓN DE LA MATERIA I.E.S. Élaios Departamento de Física y Química EJERCICIO 1 (a) En un vaso tenemos alcohol que calentamos
Física y Química: guía interactiva para la resolución de ejercicios CLASIFICACIÓN DE LA MATERIA I.E.S. Élaios Departamento de Física y Química EJERCICIO 1 (a) En un vaso tenemos alcohol que calentamos
OBJETIVOS Y METODOS DE LA QUIMICA. CLASIFICACIÓN DE LA MATERIA. OBJETIVOS Y METODOS DE LA QUIMICA.
 OBJETIVOS Y METODOS DE LA QUIMICA. CLASIFICACIÓN DE LA MATERIA. OBJETIVOS Y METODOS DE LA QUIMICA. Para reflexionar: la Química forma parte de las Ciencias Naturales, cuyo objetivo último es mejorar las
OBJETIVOS Y METODOS DE LA QUIMICA. CLASIFICACIÓN DE LA MATERIA. OBJETIVOS Y METODOS DE LA QUIMICA. Para reflexionar: la Química forma parte de las Ciencias Naturales, cuyo objetivo último es mejorar las
La Materia y sus Transformaciones
 La Materia y sus Transformaciones Los estados de la materia La materia se presenta en la Naturaleza en tres estados distintos: sólido, líquido y gaseoso. La Temperatura La temperatura es un medida que
La Materia y sus Transformaciones Los estados de la materia La materia se presenta en la Naturaleza en tres estados distintos: sólido, líquido y gaseoso. La Temperatura La temperatura es un medida que
TRANSFORMACIONES QUÍMICAS 1.- SUSTANCIAS PURAS, ELEMENTOS Y COMPUESTOS
 TRANSFORMACIONES QUÍMICAS - Sustancias puras, elementos y compuestos. - Leyes ponderales de la Química. - Teoría atómica de Dalton. - Hipótesis de Avogadro. - Masas atómica y molecular. Mol. - Leyes de
TRANSFORMACIONES QUÍMICAS - Sustancias puras, elementos y compuestos. - Leyes ponderales de la Química. - Teoría atómica de Dalton. - Hipótesis de Avogadro. - Masas atómica y molecular. Mol. - Leyes de
TEORÍA CINÉTICA. CAMBIOS DE ESTADO 3ºESO
 1. ESTADOS DE AGREGACIÓN DE LA MATERIA La materia se puede encontrar en la naturaleza en tres estados de agregación o estados físicos: sólido, líquido y gaseoso. Estos estados poseen unas propiedades que
1. ESTADOS DE AGREGACIÓN DE LA MATERIA La materia se puede encontrar en la naturaleza en tres estados de agregación o estados físicos: sólido, líquido y gaseoso. Estos estados poseen unas propiedades que
COLEGIO ROSARIO DE SANTODOMINGO BANCO DE PREGUNTAS QUÍMICA GRADO 6-2012
 COLEGIO ROSARIO DE SANTODOMINGO BANCO DE PREGUNTAS QUÍMICA GRADO 6-2012 1. Para que un cuerpo flote su nsidad be ser menor que la medio en don está flotando. La nsidad está relacionada con la cantidad
COLEGIO ROSARIO DE SANTODOMINGO BANCO DE PREGUNTAS QUÍMICA GRADO 6-2012 1. Para que un cuerpo flote su nsidad be ser menor que la medio en don está flotando. La nsidad está relacionada con la cantidad
Departamento Ciencias. Física y Química MATERIA. se clasifica en. SUSTANCIAS PURAS pueden ser. por métodos. físicos originan. Compuestos.
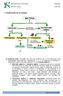 1. Clasificación de la materia MATERIA se clasifica en MEZCLAS pueden ser por métodos físicos originan SUSTANCIAS PURAS pueden ser Heterogéneas Homogéneas Compuestos como las Disoluciones formados por
1. Clasificación de la materia MATERIA se clasifica en MEZCLAS pueden ser por métodos físicos originan SUSTANCIAS PURAS pueden ser Heterogéneas Homogéneas Compuestos como las Disoluciones formados por
Ley de conservación de la masa (Ley de Lavoisier) La suma de las masas de los reactivos es igual a la suma de las masas de los productos de la
 Prof.- Juan Sanmartín 4º E.S.O ESO 1 3 Ley de conservación de la masa (Ley de Lavoisier) La suma de las masas de los reactivos es igual a la suma de las masas de los productos de la reacción, es decir,
Prof.- Juan Sanmartín 4º E.S.O ESO 1 3 Ley de conservación de la masa (Ley de Lavoisier) La suma de las masas de los reactivos es igual a la suma de las masas de los productos de la reacción, es decir,
LA MATERIA Y SU DIVERSIDAD
 LA MATERIA Y SU DIVERSIDAD La materia es todo aquello que tiene masa y ocupa un espacio, es decir, tiene volumen. Propiedades generales La masa y el volumen, son comunes a toda la materia y no nos sirven
LA MATERIA Y SU DIVERSIDAD La materia es todo aquello que tiene masa y ocupa un espacio, es decir, tiene volumen. Propiedades generales La masa y el volumen, son comunes a toda la materia y no nos sirven
2. Estados de agregación de la materia: sólido, líquido y gaseoso.
 TEMA 3. La materia. Estados de agregación de la materia: sólido, líquido y gaseoso. Teoría cinética y cambios de estado. Sustancias puras y mezclas. Métodos de separación de mezclas. Disoluciones. 1. La
TEMA 3. La materia. Estados de agregación de la materia: sólido, líquido y gaseoso. Teoría cinética y cambios de estado. Sustancias puras y mezclas. Métodos de separación de mezclas. Disoluciones. 1. La
Gabriel Villalobos Profesor de Física y Química de secundaria MEZCLAS
 MEZCLAS Gabriel Villalobos 1. Sistemas materiales homogéneos y heterogéneos Clasificación Desde un punto de vista experimental. Podemos clasificar la materia que nos encontramos en la naturaleza entre:
MEZCLAS Gabriel Villalobos 1. Sistemas materiales homogéneos y heterogéneos Clasificación Desde un punto de vista experimental. Podemos clasificar la materia que nos encontramos en la naturaleza entre:
QUIM 3004 PROBLEMAS RESUELTOS - PROPIEDADES COLIGATIVAS
 UNIVERSIDAD DE PUERTO RICO EN HUMACAO DEPARTAMENTO DE QUÍMICA (http://www.uprh.edu/~quimgen) QUIM 3004 PROBLEMAS RESUELTOS - PROPIEDADES COLIGATIVAS Ejemplo #1 PRESIÓN DE VAPOR DE UNA DISOLUCIÓN DE COMPONENTES
UNIVERSIDAD DE PUERTO RICO EN HUMACAO DEPARTAMENTO DE QUÍMICA (http://www.uprh.edu/~quimgen) QUIM 3004 PROBLEMAS RESUELTOS - PROPIEDADES COLIGATIVAS Ejemplo #1 PRESIÓN DE VAPOR DE UNA DISOLUCIÓN DE COMPONENTES
ALGUNAS PROPIEDADES DE LA MATERIA: SOLUBILIDAD Y DENSIDAD
 Práctico 2 Página: 1/6 DEPARTAMENTO ESTRELLA CAMPOS PRÁCTICO 2: ALGUNAS PROPIEDADES DE LA MATERIA: SOLUBILIDAD Y DENSIDAD Bibliografía: Química, La Ciencia Central, T.L. Brown, H.E.LeMay, Jr., B.Bursten;
Práctico 2 Página: 1/6 DEPARTAMENTO ESTRELLA CAMPOS PRÁCTICO 2: ALGUNAS PROPIEDADES DE LA MATERIA: SOLUBILIDAD Y DENSIDAD Bibliografía: Química, La Ciencia Central, T.L. Brown, H.E.LeMay, Jr., B.Bursten;
Experimental Intercolegial. Mezclas
 Prueba experimental intercolegial 25 de junio de 2010 Experimental Intercolegial Mezclas Introducción En nuestra vida, diariamente tenemos contacto con algún tipo de mezcla, como por ejemplo, el aire que
Prueba experimental intercolegial 25 de junio de 2010 Experimental Intercolegial Mezclas Introducción En nuestra vida, diariamente tenemos contacto con algún tipo de mezcla, como por ejemplo, el aire que
Todo lo que vemos es materia
 Todo lo que vemos es materia CLASIFICACIÓN DE LA MATERIA La materia se presenta en la naturaleza en forma de sustancias puras y mezclas, de modo que podemos establecer la siguiente clasificación: CLASIFICACIÓN
Todo lo que vemos es materia CLASIFICACIÓN DE LA MATERIA La materia se presenta en la naturaleza en forma de sustancias puras y mezclas, de modo que podemos establecer la siguiente clasificación: CLASIFICACIÓN
Ejercicios y respuestas del apartado: Estados de la materia. Cambios de estado.
 Ejercicios y respuestas del apartado: Estados de la materia. Cambios de estado. 2 de 9 Sobre las propiedades de la materia. Sobre las propiedades de la materia 1. Señala la afirmación correcta. a) El volumen
Ejercicios y respuestas del apartado: Estados de la materia. Cambios de estado. 2 de 9 Sobre las propiedades de la materia. Sobre las propiedades de la materia 1. Señala la afirmación correcta. a) El volumen
PROBLEMAS MEZCLAS Y DISOLUCIONES
 PROBLEMAS MEZCLAS Y DISOLUCIONES 1. Clasifica como homogéneos o heterogéneos los siguientes sistemas materiales: un trozo de cobre, agua salada, hierro oxidado, una ensalada. 2. Al mezclar dos sistemas
PROBLEMAS MEZCLAS Y DISOLUCIONES 1. Clasifica como homogéneos o heterogéneos los siguientes sistemas materiales: un trozo de cobre, agua salada, hierro oxidado, una ensalada. 2. Al mezclar dos sistemas
Estados de la materia y cambios de fase
 3 Año de Química: Sistemas Materiales Prof. Javier Ponce Qué es Ciencia? Ciencia (en latíns cientia, de scire, conocer ), término que en su sentido más amplio se emplea para referirse al conocimiento sistematizado
3 Año de Química: Sistemas Materiales Prof. Javier Ponce Qué es Ciencia? Ciencia (en latíns cientia, de scire, conocer ), término que en su sentido más amplio se emplea para referirse al conocimiento sistematizado
La materia MATERIA. se encuentra
 La materia La materia se puede encontrar en la naturaleza como sustancia pura o formando mezclas. En el caso del cobre, éste se encuentra en rocas formando mezclas con otros minerales. Para separar el
La materia La materia se puede encontrar en la naturaleza como sustancia pura o formando mezclas. En el caso del cobre, éste se encuentra en rocas formando mezclas con otros minerales. Para separar el
LIQUIDOS. Propiedades:
 LIQUIDOS Los líquidos se caracterizan por su volumen fijo y forma variable. Las fuerzas intermoleculares son mayores que en los gases, pero al igual que en estos, sus partículas están en movimiento constante.
LIQUIDOS Los líquidos se caracterizan por su volumen fijo y forma variable. Las fuerzas intermoleculares son mayores que en los gases, pero al igual que en estos, sus partículas están en movimiento constante.
UNIDAD DIDÁCTICA: MEZCLAS Y DISOLUCIONES
 Unidades Didácticas Adaptadas: MEZCLAS Y DISOLUCIONES 1 UNIDAD DIDÁCTICA: MEZCLAS Y DISOLUCIONES Qué vamos a estudiar en este tema?. Aquí tienes el esquema. 1. Las sustancias puras y las mezclas. 2. Observamos
Unidades Didácticas Adaptadas: MEZCLAS Y DISOLUCIONES 1 UNIDAD DIDÁCTICA: MEZCLAS Y DISOLUCIONES Qué vamos a estudiar en este tema?. Aquí tienes el esquema. 1. Las sustancias puras y las mezclas. 2. Observamos
SOLUCIONES. Lic. Sandra Williams Pinto Profesora de Química Colegio Instituto de Humanidades Alfredo Silva Santiago (Concepción)
 SOLUCIONES Dr. José Francisco Acuña Elgueta Docente de Química Facultad de Agronomía Universidad de Concepción Lic. Sandra Williams Pinto Profesora de Química Colegio Instituto de Humanidades Alfredo Silva
SOLUCIONES Dr. José Francisco Acuña Elgueta Docente de Química Facultad de Agronomía Universidad de Concepción Lic. Sandra Williams Pinto Profesora de Química Colegio Instituto de Humanidades Alfredo Silva
Tema 3 CLASIFICACIÓN DE LA MATERIA
 Clasificación de la materia 1 Tema 3 CLASIFICACIÓN DE LA MATERIA 1. ÁTOMOS Y MOLÉCULAS... 1 2. SUSTANCIAS PURAS Y MEZCLAS.... 2 2.1. SUSTANCIAS PURAS... 2 2.2. MEZCLAS... 2 3. SEPARACIÓN DE LOS COMPONENTES
Clasificación de la materia 1 Tema 3 CLASIFICACIÓN DE LA MATERIA 1. ÁTOMOS Y MOLÉCULAS... 1 2. SUSTANCIAS PURAS Y MEZCLAS.... 2 2.1. SUSTANCIAS PURAS... 2 2.2. MEZCLAS... 2 3. SEPARACIÓN DE LOS COMPONENTES
Una mezcla es un compuesto formado por varias sustancias con distintas propiedades
 COMPOSICIÓN DE LA MATERIA Mezclas homogéneas y heterogéneas Una mezcla es un compuesto formado por varias sustancias con distintas propiedades Algunos sistemas materiales como la leche a simple vista parecen
COMPOSICIÓN DE LA MATERIA Mezclas homogéneas y heterogéneas Una mezcla es un compuesto formado por varias sustancias con distintas propiedades Algunos sistemas materiales como la leche a simple vista parecen
Apuntes Disoluciones
 Una disolución es una mezcla homogénea (los componentes no se pueden distinguir a simple vista) de dos a más sustancias. En las disoluciones hay que distinguir el soluto, el disolvente y la propia disolución
Una disolución es una mezcla homogénea (los componentes no se pueden distinguir a simple vista) de dos a más sustancias. En las disoluciones hay que distinguir el soluto, el disolvente y la propia disolución
CRISTALIZACIÓN Es una operación unitaria de gran importancia en la Industria Química, como método de purificación y de obtención de materiales cristal
 CRISTALIZACIÓN CRISTALIZACIÓN Es una operación unitaria de gran importancia en la Industria Química, como método de purificación y de obtención de materiales cristalinos que tienen múltiples aplicaciones.
CRISTALIZACIÓN CRISTALIZACIÓN Es una operación unitaria de gran importancia en la Industria Química, como método de purificación y de obtención de materiales cristalinos que tienen múltiples aplicaciones.
1. a) Define Sustancia pura: Es aquella que tiene la misma composición y las mismas propiedades. b) Define Disolución: Es una mezcla homogénea.
 Tema 3. LA MATERIA Y SU ASPECTO MEZCLAS Y SUSTANCIAS PURAS 1. a) Define Sustancia pura: Es aquella que tiene la misma composición y las mismas propiedades. b) Define Disolución: Es una mezcla homogénea.
Tema 3. LA MATERIA Y SU ASPECTO MEZCLAS Y SUSTANCIAS PURAS 1. a) Define Sustancia pura: Es aquella que tiene la misma composición y las mismas propiedades. b) Define Disolución: Es una mezcla homogénea.
UNIDADES DE CONCENTRACIÓN
 Colegio San Esteban Diácono Departamento de Ciencias Química IIº Medio Prof. Juan Pastrián / Sofía Ponce de León UNIDADES DE CONCENTRACIÓN 1. Porcentaje masa/masa (%m/m) Cantidad en masa (g) de un componente
Colegio San Esteban Diácono Departamento de Ciencias Química IIº Medio Prof. Juan Pastrián / Sofía Ponce de León UNIDADES DE CONCENTRACIÓN 1. Porcentaje masa/masa (%m/m) Cantidad en masa (g) de un componente
Materia es todo aquello que tiene masa y ocupa un lugar en el espacio (tiene volumen). La ciencia que estudia la materia es la Química.
 Alfonso García Materia es todo aquello que tiene masa y ocupa un lugar en el espacio (tiene volumen). La ciencia que estudia la materia es la Química. Un sistema material es una porción de materia. Ejemplos:
Alfonso García Materia es todo aquello que tiene masa y ocupa un lugar en el espacio (tiene volumen). La ciencia que estudia la materia es la Química. Un sistema material es una porción de materia. Ejemplos:
Disolu ciones. Contenidos
 Disolu ciones Contenidos 1) Soluciones a) Definiciones. i) Soluto Solvente ii) Solubilidad. Factores de los que depende iii) Curvas de solubilidad b) Concentración de las soluciones i) Expresión de las
Disolu ciones Contenidos 1) Soluciones a) Definiciones. i) Soluto Solvente ii) Solubilidad. Factores de los que depende iii) Curvas de solubilidad b) Concentración de las soluciones i) Expresión de las
TEMA 2: LA MATERIA: CÓMO SE PRESENTA?
 TEMA 2: LA MATERIA: CÓMO SE PRESENTA? 1.- La materia: sustancias puras y mezclas. 1.1.- Recordatorio. 1.2.- Sustancias puras. 1.3.- Mezclas. 1.4.- Cómo distinguir un coloide de una mezcla homogénea. 2.-
TEMA 2: LA MATERIA: CÓMO SE PRESENTA? 1.- La materia: sustancias puras y mezclas. 1.1.- Recordatorio. 1.2.- Sustancias puras. 1.3.- Mezclas. 1.4.- Cómo distinguir un coloide de una mezcla homogénea. 2.-
La materia y sus propiedades
 SECCIÓN 1.2 La materia y sus propiedades Todo lo que te rodea está formado por materia. Los libros, los escritorios, las computadoras, los árboles y los edificios están formados por materia, al igual que
SECCIÓN 1.2 La materia y sus propiedades Todo lo que te rodea está formado por materia. Los libros, los escritorios, las computadoras, los árboles y los edificios están formados por materia, al igual que
Temperatura. Temperatura. La temperatura es la energía cinética promedio de las partículas. Calor. El calor es una transferencia de energía
 Temperatura Temperatura La temperatura es la energía cinética promedio de las partículas Calor El calor es una transferencia de energía Diferencias entre calor y temperatura Todos sabemos que cuando calentamos
Temperatura Temperatura La temperatura es la energía cinética promedio de las partículas Calor El calor es una transferencia de energía Diferencias entre calor y temperatura Todos sabemos que cuando calentamos
TEMA 1. LA MATERIA Y SU ESTUDIO ACTIVIDADES
 TEMA 1. LA MATERIA Y SU ESTUDIO ACTIVIDADES 1. Lee el siguiente texto sobre el método científico y contesta a las preguntas Galileo inventó un telescopio con el que observó el planeta Júpiter y cuatro
TEMA 1. LA MATERIA Y SU ESTUDIO ACTIVIDADES 1. Lee el siguiente texto sobre el método científico y contesta a las preguntas Galileo inventó un telescopio con el que observó el planeta Júpiter y cuatro
TEMA 3: Composición de la Materia
 TEMA 3: Composición de la Materia 1. Mezclas homogéneas y heterogéneas Una mezcla es una composición de varias sustancias con distintas propiedades. Distinguimos dos tipos de mezclas: Mezclas homogéneas:
TEMA 3: Composición de la Materia 1. Mezclas homogéneas y heterogéneas Una mezcla es una composición de varias sustancias con distintas propiedades. Distinguimos dos tipos de mezclas: Mezclas homogéneas:
DISOLUCIONES. Líquido (H 2 O)
 DISOLUCIONES IES La Magdalena. Avilés. Asturias Una disolución es una mezcla homogénea (los componentes no se pueden distinguir a simple vista) de dos a más sustancias. En las disoluciones hay que distinguir
DISOLUCIONES IES La Magdalena. Avilés. Asturias Una disolución es una mezcla homogénea (los componentes no se pueden distinguir a simple vista) de dos a más sustancias. En las disoluciones hay que distinguir
Tema 4: Sustancias puras y mezclas
 Tema 4: Sustancias puras y mezclas Esquema de trabajo: 1. Sustancias puras: Tipos: elementos y compuestos. 2. Mezclas: Tipos: Homogénea y heterogénea 3. Disoluciones Concepto Componentes Tipos de disoluciones
Tema 4: Sustancias puras y mezclas Esquema de trabajo: 1. Sustancias puras: Tipos: elementos y compuestos. 2. Mezclas: Tipos: Homogénea y heterogénea 3. Disoluciones Concepto Componentes Tipos de disoluciones
DEPARTAMENTO DE BIOLOGÍA Y GEOLOGÍA
 DEPARTAMENTO DE BIOLOGÍA Y GEOLOGÍA CIENCIAS DE LA NATURALEZA DE 1º ESO EJERCICIOS DE RECUPERACIÓN NOMBRE CURSO.. Para recuperar el primer trimestre de Ciencias de la Naturaleza de 1º de ESO deberás: Realizar
DEPARTAMENTO DE BIOLOGÍA Y GEOLOGÍA CIENCIAS DE LA NATURALEZA DE 1º ESO EJERCICIOS DE RECUPERACIÓN NOMBRE CURSO.. Para recuperar el primer trimestre de Ciencias de la Naturaleza de 1º de ESO deberás: Realizar
Materia. Mezclas Son aquellas que están formados por 2 o más sustancias.
 Qué es la materia? Materia Sustancias Puras Son aquellas que tienen una composición y propiedades DEFINIDAS. Mezclas Son aquellas que están formados por 2 o más sustancias. Elementos No se pueden separar
Qué es la materia? Materia Sustancias Puras Son aquellas que tienen una composición y propiedades DEFINIDAS. Mezclas Son aquellas que están formados por 2 o más sustancias. Elementos No se pueden separar
oluciones del apartado «Resuelve problemas»
 S oluciones del apartado «Resuelve problemas» Pág. 1 19 Un café con azúcar es una mezcla homogénea o heterogénea? Es una disolución de sólidos (café y azúcar) en agua. 20 Un material formado por moléculas
S oluciones del apartado «Resuelve problemas» Pág. 1 19 Un café con azúcar es una mezcla homogénea o heterogénea? Es una disolución de sólidos (café y azúcar) en agua. 20 Un material formado por moléculas
DISOLUCIONES. Finalmente se incluye un cuestionario on line para que alumno pruebe sus conocimientos.
 Introducción general Objetivos y destinatarios DISOLUCIONES El material está destinado como complemento de estudio en lo concerniente al tema Soluciones para alumnos que cursen Química en la Carrera de
Introducción general Objetivos y destinatarios DISOLUCIONES El material está destinado como complemento de estudio en lo concerniente al tema Soluciones para alumnos que cursen Química en la Carrera de
MODULO DE QUIMICA DISOLUCIONES
 1 LICEO DE MÚSICA- COPIAPÓ Educar a través de la música para el desarrollo integral de los estudiantes MODULO DE QUIMICA DISOLUCIONES PROFESOR: MARIA ANGELICA MORALES GOMEZ Nombre:...Curso... 2 OBJETIVOS:
1 LICEO DE MÚSICA- COPIAPÓ Educar a través de la música para el desarrollo integral de los estudiantes MODULO DE QUIMICA DISOLUCIONES PROFESOR: MARIA ANGELICA MORALES GOMEZ Nombre:...Curso... 2 OBJETIVOS:
PENDIENTES 3ºE.S.O. FÍSICA Y QUÍMICA ACTIVIDADES DE RECUPERACIÓN
 PENDIENTES 3ºE.S.O. FÍSICA Y QUÍMICA ACTIVIDADES DE RECUPERACIÓN 1) Razona si los procesos siguientes son físicos o químicos: a. La fermentación del azúcar. b. Formación de hielo. c. Destrucción de la
PENDIENTES 3ºE.S.O. FÍSICA Y QUÍMICA ACTIVIDADES DE RECUPERACIÓN 1) Razona si los procesos siguientes son físicos o químicos: a. La fermentación del azúcar. b. Formación de hielo. c. Destrucción de la
Universidad de Los Andes Facultad de Ingeniería Escuela de Ingeniería Química Dpto. de Operaciones Unitarias y Proyectos CRISTALIZACIÓN
 Universidad de Los Andes Facultad de Ingeniería Escuela de Ingeniería Química Dpto. de Operaciones Unitarias y Proyectos CRISTALIZACIÓN Prof. Yoana Castillo yoanacastillo@ula.ve CONTENIDO Cristalización.
Universidad de Los Andes Facultad de Ingeniería Escuela de Ingeniería Química Dpto. de Operaciones Unitarias y Proyectos CRISTALIZACIÓN Prof. Yoana Castillo yoanacastillo@ula.ve CONTENIDO Cristalización.
