Tema 14 11/02/2005. Tema 8. Mecánica Cuántica. 8.1 Fundamentos de la mecánica cuántica
|
|
|
- Marta Cano Marín
- hace 7 años
- Vistas:
Transcripción
1 Tema 14 11/0/005 Tema 8 Mecánica Cuántica 8.1 Fundamentos de la mecánica cuántica 8. La ecuación de Schrödinger 8.3 Significado físico de la función de onda 8.4 Soluciones de la ecuación de Schrödinger para el átomo de hidrógeno 8.5 Números cuánticos 8.6 Orbitales atómicos 11/0/005 Bases Físicas y Químicas del Medio Ambiente. Tema /0/005 Bases Físicas y Químicas del Medio Ambiente. Tema Fundamentos de la mecánica cuántica A finales del siglo XIX se habían acumulado una serie de resultados experimentales que no era posible explicar con la teoría existente (Mecánica clásica) RADIACIÓN DE CUERPO NEGRO La radiación del cuerpo negro es la que emite un cuerpo cuando se calienta. Los objetos calientes emiten luz de diferentes colores. Ejemplos: Nacimiento de la mecánica cuántica Planck, Einstein, Bohr, De Broglie, Schrödinger, Heisenberg... Rojo oscuro: Elemento calefactor de un horno eléctrico. Blanco: Filamento de una bombilla eléctrica. 11/0/005 Bases Físicas y Químicas del Medio Ambiente. Tema /0/005 Bases Físicas y Químicas del Medio Ambiente. Tema 8 4 Espectro de la radiación emitida por un cuerpo caliente Intensidad Predicciones de la Resultado mecánica clásica experimental 7000 K Cuanto mayor es T, menor 5000 K es λ máxima. Longitud de onda 11/0/005 Bases Físicas y Químicas del Medio Ambiente. Tema 8 5 La intensidad de la luz varía con la longitud de onda con un máximo a una cierta λ determinada por la T de la fuente La física clásica no podía proporcionar una completa explicación de la emisión de la luz por los sólidos calientes, conocida como la RADIACIÓN DEL CUERPO NEGRO. El Sol y el resto de estrellas se comporta muy aproximadamente como un cuerpo negro La teoría clásica predice que la intensidad de la radiación emitida debería aumentar indefinidamente 11/0/005 Bases Físicas y Químicas del Medio Ambiente. Tema 8 6 1
2 Tema 14 11/0/005 En 1900, Planck, para explicar que la intensidad no aumenta indefinidamente al disminuir la frecuencia, hizo una propuesta revolucionaria: la energía como la materia, es discontinua. Esta es la diferencia esencial entre la FÍSICA CLÁSICA y la nueva TEORÍA CUÁNTICA. El postulado de Planck puede resumirse por la ecuación: E =energía de un cuanto de radiación electromagnética E = h ν h= constante de Planck ν = frecuencia 11/0/005 Bases Físicas y Químicas del Medio Ambiente. Tema 8 7 Ni la materia ni la radiación son continuas, están divididas en partículas de materia (partículas subatómicas) o de energía (fotones). Esta hipótesis explica: Los espectros de emisión de los elementos (H, He...) El efecto fotoeléctrico La radiación de cuerpo negro La capcidad calorífica de los sólidos a bajas temperaturas 11/0/005 Bases Físicas y Químicas del Medio Ambiente. Tema 8 8 La mecánica cuántica establece límites a la información que podemos tener de un sistema. Principio de Incertidumbre (Heisenberg, 197) x p h/ 4π Es una limitación de la naturaleza Error en la medida Error en la medida de la posición del momento 11/0/005 Bases Físicas y Químicas del Medio Ambiente. Tema La ecuación de Schrödinger Sabemos que la radiación se puede comportar como partículas o como ondas, y lo mismo ocurre con la materia (difracción de electrones) Las ondas de materia son ONDAS ESTACIONARIAS La ecuación de propagación de las ondas de la materia es la ecuación de Schrödinger 11/0/005 Bases Físicas y Químicas del Medio Ambiente. Tema 8 10 Función de onda Energía total del sistema Un e - o cualquier otra partícula que posea propiedades de onda podría ser descrita mediante una función matemática denominada FUNCIÓN DE ONDA ψ. Las funciones de onda son las soluciones de la ecuación de Schrödinger 11/0/005 Bases Físicas y Químicas del Medio Ambiente. Tema 8 11 H ( Ψ( = E Ψ( Operador hamiltoniano (equivalente cuántico a la suma de las energías cinética y potencial clásicas). La ecuación de Schrödinger es el equivalente a la conservación de la energía mecánica clásica E es lo que hay que comparar con la energía experimental del sistema. En Mecánica Cuántica a las magnitudes mensurables experimentalmente se les llama OBSERVABLES 11/0/005 Bases Físicas y Químicas del Medio Ambiente. Tema 8 1
3 Tema 14 11/0/005 En una dimensión ( la ec Schrödinger se escribe Energía cinética m d T( = m d x V( H ( x ) Ψ ( x ) Energía potencial d Ψ( + V ( Ψ( = E d x = h π Operador energía potencial = E Ψ ( x ) Ψ( Operador energía cinética La ec de Schrödinger es una ecuación diferencial que se puede resolver en algunos casos aplicando métodos matemáticos. Solo algunas de esas soluciones tienen sentido físico En principio nosotros sabemos (o suponemos) como son los operadores energía cinética y energía potencial (interacciones eléctricas entre las partículas, ley de Coulomb) y RESOLVIENDO la ecuación de Schrödinger se obtienen E y ψ. 11/0/005 Bases Físicas y Químicas del Medio Ambiente. Tema /0/005 Bases Físicas y Químicas del Medio Ambiente. Tema Significado físico de la función de onda En una onda convencional el cuadrado de la función de onda es proporcional a la intensidad de la radiación. En una onda de materia el cuadrado de la función de onda da la probabilidad de encontrar materia en ese determinado punto. x z r Ψ( r Probabilidad de encontrar ) d V = la partícula en un pequeño y volumen dv 11/0/005 Bases Físicas y Químicas del Medio Ambiente. Tema /0/005 Bases Físicas y Químicas del Medio Ambiente. Tema Soluciones de la ecuación de Schrödinger para el átomo de hidrógeno z Las funciones de onda se m analizan en función de las (x, y,z) 3 coordenadas (x, y, z) M y + x necesarias para definir p un punto con respecto El átomo de hidrógeno al núcleo. consta de un protón en el centro y un electrón girando a su alrededor 11/0/005 Bases Físicas y Químicas del Medio Ambiente. Tema 8 17 e - El átomo de H es uno de los pocos sistemas para el cual se puede resolver la ec. de Schrödinger EXACTAMENTE ( pero podemos resolverla para otros muchos átomos de una manera aproximada) Las soluciones de la ecuación de Schrodinger para el átomo de H proporcionan las funciones de onda para el e - en el átomo de H. Estas funciones de onda se llaman ORBITALES. Es decir, un orbital es la función de ondas de un solo electrón 11/0/005 Bases Físicas y Químicas del Medio Ambiente. Tema
4 Tema 14 11/0/005 Función de onda para el átomo de hidrógeno Ψ = Ψ( r) = Ψ( x, y, z) Depende de r(x,y,z) 8.5 Números cuánticos Cuando resolvemos la ecuación de Schrödinger para el átomo de H vemos que solo tiene solución para posibles m Ψ Ψ Ψ V ( r) Ψ = E x y z masa del electrón Ψ valores de energía. E = - R n Constante de Rydberg Z e V ( r) = 4πε r 0 Interacción Coulombica electrón-núcleo n es un número entero (1,,3...) que llamamos número cuántico. 11/0/005 Bases Físicas y Químicas del Medio Ambiente. Tema /0/005 Bases Físicas y Químicas del Medio Ambiente. Tema 8 0 Cada valor de n caracteriza un nivel de energía del átomo de hidrógeno. n se denomina número cuántico principal EN EL ÁTOMO DE HIDRÓGENO la energía depende SOLAMENTE de n En los demás átomos la energía depende de otros números cuánticos El valor de la energía para n = 1 es el estado fundamental del sistema El resto de los estados (n 1) se llaman estados excitados Se puede pasar de un estado excitado a otro o al estado fundamental liberando energía 11/0/005 Bases Físicas y Químicas del Medio Ambiente. Tema /0/005 Bases Físicas y Químicas del Medio Ambiente. Tema 8 E n E = R 1 1 n 1 n Al resolver la ec de Schrödinger no solo obtenemos las energías sino las funciones de onda ψ. Esas ψ son los ORBITALES ATÓMICOS que n 1 están definidos por TRES números cuánticos. La fórmula que explica qué líneas aparecen en los espectros de emisión es una consecuencia de cómo son las soluciones de la ecuación de Schrödinger 11/0/005 Bases Físicas y Químicas del Medio Ambiente. Tema 8 3 n (número cuántico principal) n = 1,,3... l (número cuántico secundario) l = 0,1,... n-1 Determina las regiones de máxima probabilidad de encontrar al electrón y está relacionado con el momento angular m l (número cuántico magnético) m l = -l, ,+l Determina la orientación en el espacio de un orbital. 11/0/005 Bases Físicas y Químicas del Medio Ambiente. Tema 8 4 4
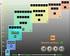
5 Tema 14 11/0/ Orbitales atómicos Orbitales atómicos CAPA SUBCAPA ORBITAL Todos los orbitales con el mismo valor de n se encuentran en la MISMA CAPA Las capas se numeran de acuerdo a n Todos los orbitales con los mismos valores de n y l pertenecen a la MISMA SUBCAPA Las subcapas se definen mediante letras 11/0/005 Bases Físicas y Químicas del Medio Ambiente. Tema /0/005 Bases Físicas y Químicas del Medio Ambiente. Tema 8 6 CAPA n = 4 11/0/005 Bases Físicas y Químicas del Medio Ambiente. Tema 8 7 Nº cuánticos posibles para n =4 n l =n-1 ml = -l...+l Tipo de orbital n = 4 l = 0 l = 1 m l = 1 m l = -1 e - 6 e - l = m l = 10 e - m l = 1 m l = -1 m l = - l = 3 m l = 3 m l = m l = 1 m l = -1 m l = - m l = -3 4 s 4 p x 4 p y 4 p z 4 d xy 4 d xz 4 d yz 4 d x-y 4 d z 11/0/005 Bases Físicas y Químicas del Medio Ambiente. Tema e - Orbitales s Nube electrónica Probabilidad Poseen simetría esférica Orbitales p 11/0/005 Bases Físicas y Químicas del Medio Ambiente. Tema /0/005 Bases Físicas y Químicas del Medio Ambiente. Tema
6 Tema 14 11/0/005 Orbitales d Para definir EL ELECTRÓN DENTRO DE LOS ORBITALES se necesita un cuarto número cuántico Número cuántico de espín s = m s = +1/ m s = -1/ Está relacionado con las propiedades magnéticas intrínsecas del electrón 11/0/005 Bases Físicas y Químicas del Medio Ambiente. Tema /0/005 Bases Físicas y Químicas del Medio Ambiente. Tema 8 3 El experimento de Stern-Gerlach Número cuántico de spin Sirvió para detectar el espín del electrón IMÁN Haz de átomos de Ag N m s = +1/ El experimento de Stern y Gerlach en 190 reveló la necesidad de un cuarto número cuántico, asociado a un momento Angular intrínseco al electrón S=1/ Dos estados posibles rendija S m s = -1/ El haz se desdobla en m s =+1/ m s =-1/ 11/0/005 Bases Físicas y Químicas del Medio Ambiente. Tema /0/005 Bases Físicas y Químicas del Medio Ambiente. Tema 8 34 Spin del electrón Las funciones de onda de un solo electrón al considerar el spin se llaman spin orbitales. Podemos relacionar el spin con un momento angular intrínseco del electrón PROBABILIDAD Funciones de distribución radial Proporcionan la probabilidad de encontrar al electrón en función de la distancia electrón-núcleo: p 1s s Distancia a 0 11/0/005 Bases Físicas y Químicas del Medio Ambiente. Tema /0/005 Bases Físicas y Químicas del Medio Ambiente. Tema
EXTRUCTURA ATOMICA ACTUAL
 ATOMOS Y ELEMENTOS TEMA 4 Química ATOMOS EXTRUCTURA ATOMICA ACTUAL PARTICULA UBICACION CARGA MASA PROTON NUCLEO + SI NEUTRON NUCLEO 0 SI ELECTRON ORBITAS - DESPRECIABLE La masa del átomo reside en el núcleo.
ATOMOS Y ELEMENTOS TEMA 4 Química ATOMOS EXTRUCTURA ATOMICA ACTUAL PARTICULA UBICACION CARGA MASA PROTON NUCLEO + SI NEUTRON NUCLEO 0 SI ELECTRON ORBITAS - DESPRECIABLE La masa del átomo reside en el núcleo.
Unidad 1 Estructura atómica de la materia. Teoría cuántica
 Unidad 1 Estructura atómica de la materia. Teoría cuántica 1.El átomo y la constitución de la materia DALTON NO ACEPTADO POR LOS FÍSICOS que creían en la idea de que los átomos se encontraban como disueltos
Unidad 1 Estructura atómica de la materia. Teoría cuántica 1.El átomo y la constitución de la materia DALTON NO ACEPTADO POR LOS FÍSICOS que creían en la idea de que los átomos se encontraban como disueltos
MATERIA MOLÉCULAS ÁTOMOS PARTÍCULAS SUBATÓMICAS. Partícula Masa (g) Carga (Coulombs) Carga unitaria. Electrón
 MATERIA MOLÉCULAS ÁTOMOS PARTÍCULAS SUBATÓMICAS Partícula Masa (g) Carga (Coulombs) Carga unitaria Electrón 9.10939 10-28 -1.6022 10-19 -1 Protón 1.67262 10-24 +1.6022 10-19 +1 Neutrón 1.67493 10-24 0
MATERIA MOLÉCULAS ÁTOMOS PARTÍCULAS SUBATÓMICAS Partícula Masa (g) Carga (Coulombs) Carga unitaria Electrón 9.10939 10-28 -1.6022 10-19 -1 Protón 1.67262 10-24 +1.6022 10-19 +1 Neutrón 1.67493 10-24 0
FÍSICA y QUÍMICA. Número cuántico Secundario (SUBNIVEL) l. Número cuántico Magnético (ORBITAL, como si fuera una caja) m.
 TEMA 1: ESTRUCTURA DE LA MATERIA. MODELOS ATÓMICOS 1. Modelo Atómico de RUTHERFORD a. Modelo predecesor de Thomson. b. Modelo atómico de Rutherford. c. Virtudes y defectos del Modelo de Rutherford. 2.
TEMA 1: ESTRUCTURA DE LA MATERIA. MODELOS ATÓMICOS 1. Modelo Atómico de RUTHERFORD a. Modelo predecesor de Thomson. b. Modelo atómico de Rutherford. c. Virtudes y defectos del Modelo de Rutherford. 2.
INTERACTIVEBOOK - Física y Química 4º ESO McGraw-Hill Education Dalton 1.2. Thomson: Descubrimiento del electrón. 1.3.
 El modelo de átomo INTERACTIVEBOOK - Física y Química 4º ESO McGraw-Hill Education INDICE 1. El modelo de átomo 1.1. Dalton 1.2. Thomson: Descubrimiento del electrón. 1.3. Rutherford: 1.3.1. Radioactividad
El modelo de átomo INTERACTIVEBOOK - Física y Química 4º ESO McGraw-Hill Education INDICE 1. El modelo de átomo 1.1. Dalton 1.2. Thomson: Descubrimiento del electrón. 1.3. Rutherford: 1.3.1. Radioactividad
Universidad de San Carlos de Guatemala. Facultad de Ingeniería. Escuela de Ciencias. Departamento de Química. Catedrática: Tania de León.
 Universidad de San Carlos de Guatemala. Facultad de Ingeniería. Escuela de Ciencias. Departamento de Química. Catedrática: Tania de León. Química General. Código: 0348. Primer semestre. Hoja de trabajo.
Universidad de San Carlos de Guatemala. Facultad de Ingeniería. Escuela de Ciencias. Departamento de Química. Catedrática: Tania de León. Química General. Código: 0348. Primer semestre. Hoja de trabajo.
J.J Thomson propone el primer modelo de átomo:
 MODELOS ATÓMICOS. DALTON En 1808, Dalton publicó sus ideas sobre el modelo atómico de la materia las cuales han servido de base a la química moderna. Los principios fundamentales de esta teoría son: 1.
MODELOS ATÓMICOS. DALTON En 1808, Dalton publicó sus ideas sobre el modelo atómico de la materia las cuales han servido de base a la química moderna. Los principios fundamentales de esta teoría son: 1.
El átomo: sus partículas elementales
 El átomo: sus partículas elementales Los rayos catódicos estaban constituidos por partículas cargadas negativamente ( a las que se llamo electrones) y que la relación carga/masa de éstas partículas era
El átomo: sus partículas elementales Los rayos catódicos estaban constituidos por partículas cargadas negativamente ( a las que se llamo electrones) y que la relación carga/masa de éstas partículas era
QUÍMICA 2º BACH. TEMA 1. ESTRUCTURA ATÓMICA.
 Modelos atómicos QUÍMICA 2º BACH. TEMA 1. ESTRUCTURA ATÓMICA. Teoría atómica de Dalton: La materia está formada por átomos indivisibles. Los átomos de un elemento son distintos de los átomos de otro elemento
Modelos atómicos QUÍMICA 2º BACH. TEMA 1. ESTRUCTURA ATÓMICA. Teoría atómica de Dalton: La materia está formada por átomos indivisibles. Los átomos de un elemento son distintos de los átomos de otro elemento
Radiación. Cuerpo Negro Espectros Estructura del Atomo Espectroscopia Efecto Doppler. L. Infante 1
 Radiación Cuerpo Negro Espectros Estructura del Atomo Espectroscopia Efecto Doppler L. Infante 1 Cuerpo Negro: Experimento A medida que el objeto se calienta, se hace más brillante ya que emite más radiación
Radiación Cuerpo Negro Espectros Estructura del Atomo Espectroscopia Efecto Doppler L. Infante 1 Cuerpo Negro: Experimento A medida que el objeto se calienta, se hace más brillante ya que emite más radiación
Programa de Acceso Inclusivo, Equidad y Permanencia PAIEP U. de Santiago. Química
 Modelos atómicos Los filósofos de la antigüedad especularon sobre cómo estaba formada la materia. Demócrito (460-370 a.c) y otros filósofos anteriores a él, pensaban que el mundo material debería estar
Modelos atómicos Los filósofos de la antigüedad especularon sobre cómo estaba formada la materia. Demócrito (460-370 a.c) y otros filósofos anteriores a él, pensaban que el mundo material debería estar
ESTRUCTURA DEL ÁTOMO - RESUMEN
 TEMA 1 ESTRUCTURA DEL ÁTOMO - RESUMEN 1. DESCUBRIMIENTO DE LA ESTRUCTURA ATÓMICA (ideas generales) Dalton: consideraba que un átomo no podía romperse en trozos más pequeños. El primer indicio de que el
TEMA 1 ESTRUCTURA DEL ÁTOMO - RESUMEN 1. DESCUBRIMIENTO DE LA ESTRUCTURA ATÓMICA (ideas generales) Dalton: consideraba que un átomo no podía romperse en trozos más pequeños. El primer indicio de que el
Estudio del átomo: 1. Átomos e isótopos 2. Modelos Atómicos 3. Teoría cuántica. Ing. Sol de María Jiménez González
 Estudio del átomo: 1. Átomos e isótopos 2. Modelos Atómicos 3. Teoría cuántica 1 Núcleo: protones y neutrones Los electrones se mueven alrededor. Característica Partículas Protón Neutrón Electrón Símbolo
Estudio del átomo: 1. Átomos e isótopos 2. Modelos Atómicos 3. Teoría cuántica 1 Núcleo: protones y neutrones Los electrones se mueven alrededor. Característica Partículas Protón Neutrón Electrón Símbolo
Teoría Cuántica y la estructura electrónica de los Átomos
 EN EL INTERIOR DEL ATOMO TEMA 3 Química General e Inorgánica A Teoría Cuántica y la estructura electrónica de los Átomos 1 LO QUE SABEMOS EXTRUCTURA ATOMICA ACTUAL PARTICULA UBICACION CARGA MASA PROTON
EN EL INTERIOR DEL ATOMO TEMA 3 Química General e Inorgánica A Teoría Cuántica y la estructura electrónica de los Átomos 1 LO QUE SABEMOS EXTRUCTURA ATOMICA ACTUAL PARTICULA UBICACION CARGA MASA PROTON
PLAN DE EVALUACIÓN 2015
 PLAN DE EVALUACIÓN 2015 Año: 2015 Período: I Semestre Sub-sector: Química Nivel: NM1 Curso: I Medio Profesor: Alejandra Sotomaor A. Aprendizajes Esperados Indicadores Aprendizajes Evaluados Procedimientos
PLAN DE EVALUACIÓN 2015 Año: 2015 Período: I Semestre Sub-sector: Química Nivel: NM1 Curso: I Medio Profesor: Alejandra Sotomaor A. Aprendizajes Esperados Indicadores Aprendizajes Evaluados Procedimientos
La Ecuación de Schrödinger
 La Ecuación de Schrödinger Dr. Héctor René VEGA CARRILLO Notas del curso de Física Moderna Unidad Académica de Ingeniería Eléctrica Universidad Autónoma de Zacatecas Buzón electrónico: fermineutron@yahoo.com
La Ecuación de Schrödinger Dr. Héctor René VEGA CARRILLO Notas del curso de Física Moderna Unidad Académica de Ingeniería Eléctrica Universidad Autónoma de Zacatecas Buzón electrónico: fermineutron@yahoo.com
GUÍA DIDACTICA CURSO FÍSICA 2º BACHILLERATO. PROFESOR: Alicia Blanco Pozos
 GUÍA DIDACTICA FÍSICA 2º BACHILLERATO CURSO 2016-17 PROFESOR: Alicia Blanco Pozos CONTENIDOS Los contenidos se organizan en 13 unidades didácticas distribuidos en cinco bloques de conocimiento: BLOQUE
GUÍA DIDACTICA FÍSICA 2º BACHILLERATO CURSO 2016-17 PROFESOR: Alicia Blanco Pozos CONTENIDOS Los contenidos se organizan en 13 unidades didácticas distribuidos en cinco bloques de conocimiento: BLOQUE
INDICE 22. La carga eléctrica Resumen, preguntas, problemas 23. El campo eléctrico Resumen, preguntas, problemas Resumen, preguntas, problemas
 INDICE 22. La carga eléctrica 22-1. las propiedades de la materia con carga 646 22-2. la conservación y cuantización de la carga 652 22-3. la ley de Colulomb 654 22-4. las fuerzas en las que intervienen
INDICE 22. La carga eléctrica 22-1. las propiedades de la materia con carga 646 22-2. la conservación y cuantización de la carga 652 22-3. la ley de Colulomb 654 22-4. las fuerzas en las que intervienen
Ejercicios de Física cuántica y nuclear. PAU (PAEG)
 1. Las longitudes de onda del espectro visible están comprendidas, aproximadamente, entre 390 nm en el violeta y 740 nm en el rojo. Qué intervalo aproximado de energías, en ev, corresponde a los fotones
1. Las longitudes de onda del espectro visible están comprendidas, aproximadamente, entre 390 nm en el violeta y 740 nm en el rojo. Qué intervalo aproximado de energías, en ev, corresponde a los fotones
Robert A. MILLIKAN ( )
 Robert A. MILLIKAN (1906 1914) Modelo atómico de Rutherford - Todo átomo está formado por un núcleo y corteza. - El núcleo, muy pesado, y de muy pequeño tamaño, formado por un número de protones igual
Robert A. MILLIKAN (1906 1914) Modelo atómico de Rutherford - Todo átomo está formado por un núcleo y corteza. - El núcleo, muy pesado, y de muy pequeño tamaño, formado por un número de protones igual
ESTRUCTURA DE LA MATERIA
 ESTRUCTURA DE LA MATERIA CONTENIDOS. 1.- Radiación electromagnética y espectros atómicos. 1.1. Espectros atómicos. 1.2. Series espectrales. 1.3. Ley de Rygberg ( ). 2.- Orígenes de la teoría cuántica.
ESTRUCTURA DE LA MATERIA CONTENIDOS. 1.- Radiación electromagnética y espectros atómicos. 1.1. Espectros atómicos. 1.2. Series espectrales. 1.3. Ley de Rygberg ( ). 2.- Orígenes de la teoría cuántica.
Las estructura electrónica de los átomos
 Las estructura electrónica de los átomos Al preguntarnos por las diferencias entre las propiedades químicas y físicas de los elementos, así como, su forma de enlazarse y la forma en la cual emiten o absorben
Las estructura electrónica de los átomos Al preguntarnos por las diferencias entre las propiedades químicas y físicas de los elementos, así como, su forma de enlazarse y la forma en la cual emiten o absorben
MODELOS ATOMICOS. Solución Å; Ultravioleta; 1106 m/s
 MODELOS ATOMICOS 1. Calcular el valor del radio de la órbita que recorre el electrón del hidrogeno en su estado normal. Datos. h = 6 63 10 27 erg s, m(e ) = 9 1 10 28 gr, q(e ) = 4 8 10-10 u.e.e. Solución.
MODELOS ATOMICOS 1. Calcular el valor del radio de la órbita que recorre el electrón del hidrogeno en su estado normal. Datos. h = 6 63 10 27 erg s, m(e ) = 9 1 10 28 gr, q(e ) = 4 8 10-10 u.e.e. Solución.
DIVISIÓN DE CIENCIAS BÁSICAS DEPARTAMENTO DE FÍSICA PROGRAMA DE ASIGNATURA
 CENTRO UNIVERSITARIO DE CIENCIAS EXACTAS E INGENIERÍAS DIVISIÓN DE CIENCIAS BÁSICAS DEPARTAMENTO DE FÍSICA PROGRAMA DE ASIGNATURA NOMBRE DE LA MATERIA FÍSICA MODERNA CLAVE DE MATERIA FS 301 DEPARTAMENTO
CENTRO UNIVERSITARIO DE CIENCIAS EXACTAS E INGENIERÍAS DIVISIÓN DE CIENCIAS BÁSICAS DEPARTAMENTO DE FÍSICA PROGRAMA DE ASIGNATURA NOMBRE DE LA MATERIA FÍSICA MODERNA CLAVE DE MATERIA FS 301 DEPARTAMENTO
BLOQUE 4.1 ÓPTICA FÍSICA
 BLOQUE 4.1 ÓPTICA FÍSICA 1. NATURALEZA DE LA LUZ Hasta ahora hemos considerado a la luz como algo que transporta energía de un lugar a otro. Por otra parte, sabemos que existen dos formas básicas de transportar
BLOQUE 4.1 ÓPTICA FÍSICA 1. NATURALEZA DE LA LUZ Hasta ahora hemos considerado a la luz como algo que transporta energía de un lugar a otro. Por otra parte, sabemos que existen dos formas básicas de transportar
QUÍMICA LICENCIATURA DE INGENIERÍA EN ENERGÍAS RENOVABLES
 QUÍMICA LICENCIATURA DE INGENIERÍA EN ENERGÍAS RENOVABLES 2013-1 Teoría: Dra. Karina Cuentas Gallegos Martes y jueves 10-12 hrs. Laboratorio: M.C. Mirna Guevara García Jueves 12-14 hrs. Curso de Química
QUÍMICA LICENCIATURA DE INGENIERÍA EN ENERGÍAS RENOVABLES 2013-1 Teoría: Dra. Karina Cuentas Gallegos Martes y jueves 10-12 hrs. Laboratorio: M.C. Mirna Guevara García Jueves 12-14 hrs. Curso de Química
EL ÁTOMO CONTENIDOS. ANTECEDENTES HISTÓRICOS. ( ) MODELOS ATÓMICOS. RAYOS CATÓDICOS. MODELO DE THOMSON.
 EL ÁTOMO CONTENIDOS. 1.- Antecedentes históricos.( ) 2.- Partículas subatómicas. ( ) 3.- Modelo atómico de Thomsom. 4.- Los rayos X. 5.- La radiactividad. 6.- Modelo atómico de Rutherford. 7.- Radiación
EL ÁTOMO CONTENIDOS. 1.- Antecedentes históricos.( ) 2.- Partículas subatómicas. ( ) 3.- Modelo atómico de Thomsom. 4.- Los rayos X. 5.- La radiactividad. 6.- Modelo atómico de Rutherford. 7.- Radiación
LA ESTRUCTURA ELECTRÓNICA DE LOS ÁTOMOS
 LA ESTRUCTURA ELECTRÓNICA DE LOS ÁTOMOS 1.- La descripción macroscópica del Universo. El desarrollo de la Física hasta finales del siglo XIX permite una descripción de nuestro entorno cotidiano que se
LA ESTRUCTURA ELECTRÓNICA DE LOS ÁTOMOS 1.- La descripción macroscópica del Universo. El desarrollo de la Física hasta finales del siglo XIX permite una descripción de nuestro entorno cotidiano que se
PROGRAMA DE: FISICA MODERNA II IDENTIFICACION DE LA ASIGNATURA CODIGO OPTICO:
 UNIVERSIDAD DEL ZULIA FACULTAD EXPERIMENTAL DE CIENCIAS D.E.B.S. COORDINACION ACADEMICA DE LA FEC DEPARTAMENTO DE FISICA UNIDAD ACADÉMICA FÍSICA CUÁNTICA PROGRAMA DE: FISICA MODERNA II IDENTIFICACION DE
UNIVERSIDAD DEL ZULIA FACULTAD EXPERIMENTAL DE CIENCIAS D.E.B.S. COORDINACION ACADEMICA DE LA FEC DEPARTAMENTO DE FISICA UNIDAD ACADÉMICA FÍSICA CUÁNTICA PROGRAMA DE: FISICA MODERNA II IDENTIFICACION DE
ESTRUCTURA DEL ÁTOMO. MODELOS DE RUTHERFORD Y DE BOHR-SOMMERFELD
 ESTRUCTURA DEL ÁTOMO. MODELOS DE RUTHERFORD Y DE BOHR-SOMMERFELD De todas las partículas subatómicas elementales, ay tres que interesan fundamentalmente, pues son necesarias para construir un modelo atómico
ESTRUCTURA DEL ÁTOMO. MODELOS DE RUTHERFORD Y DE BOHR-SOMMERFELD De todas las partículas subatómicas elementales, ay tres que interesan fundamentalmente, pues son necesarias para construir un modelo atómico
Thompson (1898) Rutherford (1911) Bohr (1913) Schrödinger (1926) NUMEROS CUANTICOS
 Thompson (1898) Modelo Atómico Rutherford (1911) Bohr (1913) Propiedad corpuscular de las onda (PLANCK) Propiedad ondulatoria de las partículas (De Broglie) Schrödinger (1926) Números cuánticos 1 NUMEROS
Thompson (1898) Modelo Atómico Rutherford (1911) Bohr (1913) Propiedad corpuscular de las onda (PLANCK) Propiedad ondulatoria de las partículas (De Broglie) Schrödinger (1926) Números cuánticos 1 NUMEROS
Como esta formada la materia?
 Como esta formada la materia? Demócrito, filósofo griego que vivió en el siglo IV a. C. propuso que, si se dividía la materia en trozos cada vez más pequeños, debería llegarse a una porción que ya no podría
Como esta formada la materia? Demócrito, filósofo griego que vivió en el siglo IV a. C. propuso que, si se dividía la materia en trozos cada vez más pequeños, debería llegarse a una porción que ya no podría
Con posterioridad el físico alemán Sommerfeld introdujo en el modelo la posibilidad de órbitas elípticas. Köningsberg, Munich, 1951
 4. El paso de una órbita a otra supone la absorción o emisión de radiación. El átomo sólo absorberá o emitirá la radiación justa para pasar de una órbita a otra. Las órbitas de los electrones son estables
4. El paso de una órbita a otra supone la absorción o emisión de radiación. El átomo sólo absorberá o emitirá la radiación justa para pasar de una órbita a otra. Las órbitas de los electrones son estables
! Parte I. " Introducción " Bases experimentales de la Mecánica Cuántica. ! Parte II
 Módulo 865- Enlace Químico y Estructura de la Materia Responsable: Juan José Borrás (juan.j.borras@uv.es) Curso 7-8 Grupo D- Aula F9 http://www.uv.es/~borrasj Tema Estructura electrónica del átomo Parte
Módulo 865- Enlace Químico y Estructura de la Materia Responsable: Juan José Borrás (juan.j.borras@uv.es) Curso 7-8 Grupo D- Aula F9 http://www.uv.es/~borrasj Tema Estructura electrónica del átomo Parte
I.E.S. Virgen del Puerto Química 2º Bachillerato 2016/2017
 UD. 1 ESTRUCTURA ATÓMICA 1. INTRODUCCIÓN Dalton Thomson Rutherford Bohr Schrödinger (El concepto de átomo surge en la Grecia clásica, pero hasta principios del siglo XIX no se formula la primera teoría
UD. 1 ESTRUCTURA ATÓMICA 1. INTRODUCCIÓN Dalton Thomson Rutherford Bohr Schrödinger (El concepto de átomo surge en la Grecia clásica, pero hasta principios del siglo XIX no se formula la primera teoría
Clase N 1. Modelo Atómico I
 Pre-Universitario Manuel Guerrero Ceballos Clase N 1 Modelo Atómico I ICAL ATACAMA Módulo Plan Común Modelos Atómicos Teoría Atómica De Dalton Los elementos están formados por partículas extremadamente
Pre-Universitario Manuel Guerrero Ceballos Clase N 1 Modelo Atómico I ICAL ATACAMA Módulo Plan Común Modelos Atómicos Teoría Atómica De Dalton Los elementos están formados por partículas extremadamente
PARTÍCULAS DEL ÁTOMO MODELOS ATÓMICOS. TEMA 7 Pág. 155 libro nuevo
 PARTÍCULAS DEL ÁTOMO MODELOS ATÓMICOS TEMA 7 Pág. 155 libro nuevo DESCUBRIMIENTO DEL ÁTOMO. PARTÍCULAS SUBATÓMICAS En la antigua Grecia ya había dos teorías sobre la materia: Teoría Atomística (siglo IV
PARTÍCULAS DEL ÁTOMO MODELOS ATÓMICOS TEMA 7 Pág. 155 libro nuevo DESCUBRIMIENTO DEL ÁTOMO. PARTÍCULAS SUBATÓMICAS En la antigua Grecia ya había dos teorías sobre la materia: Teoría Atomística (siglo IV
1. Estructura Atómica
 1. Estructura Atómica 1.1 Modelos atómicos: de Dalton a Rutherford 1.1.1 Modelo atómico de Dalton 1.1.2 Modelo atómico de Thomson 1.1.3 Modelo atómico de Rutherford 1.2 Modelo atómico de Bohr 1.2.1 Espectro
1. Estructura Atómica 1.1 Modelos atómicos: de Dalton a Rutherford 1.1.1 Modelo atómico de Dalton 1.1.2 Modelo atómico de Thomson 1.1.3 Modelo atómico de Rutherford 1.2 Modelo atómico de Bohr 1.2.1 Espectro
ÁTOMO..su historia y su estudio
 ÁTOMO.su historia y su estudio LOS GRIEGOS Y SU APORTE 2000 años antes de Cristo, la civilización griega representada por varios filósofos, ya se preguntaban acerca de qué estaba formado el universo?...
ÁTOMO.su historia y su estudio LOS GRIEGOS Y SU APORTE 2000 años antes de Cristo, la civilización griega representada por varios filósofos, ya se preguntaban acerca de qué estaba formado el universo?...
- Marie Curie. - Joseph Thomson. - Ernest Rutherford. - Max Planck. - Albert Einstein. - Niels Bohr. - Louis de Broglie. - Werner Heisenberg
 - Marie Curie - Joseph Thomson - Ernest Rutherford - Max Planck - Albert Einstein - Niels Bohr - Louis de Broglie - Werner Heisenberg - Wolfgang Pauli - Arnorld Sommerfeld Autores (Orden Alfabético): Celia
- Marie Curie - Joseph Thomson - Ernest Rutherford - Max Planck - Albert Einstein - Niels Bohr - Louis de Broglie - Werner Heisenberg - Wolfgang Pauli - Arnorld Sommerfeld Autores (Orden Alfabético): Celia
TEORIA ELECTROMAGNETICA CLASE 10 SOLUCIONES DE LA ECUACION DE ONDA
 TEORIA ELECTROMAGNETICA CLASE 10 SOLUCIONES DE LA ECUACION DE ONDA Onda Electromagnética ESTA FORMADA POR UN PAR DE CAMPOS (UNO ELECTRICO Y OTRO MAGNETICO) QUE VARIAN CON LA POSICION Y EL TIEMPO ESA ONDA
TEORIA ELECTROMAGNETICA CLASE 10 SOLUCIONES DE LA ECUACION DE ONDA Onda Electromagnética ESTA FORMADA POR UN PAR DE CAMPOS (UNO ELECTRICO Y OTRO MAGNETICO) QUE VARIAN CON LA POSICION Y EL TIEMPO ESA ONDA
Capítulo 2. Fundamentos de la Química Cuántica.
 Capítulo.. Objetivos: Introducción de la naturaleza dual (onda-partícula) de la materia Introducción del concepto de función de onda Familiarizar al alumno con los conceptos más básicos de la mecánica
Capítulo.. Objetivos: Introducción de la naturaleza dual (onda-partícula) de la materia Introducción del concepto de función de onda Familiarizar al alumno con los conceptos más básicos de la mecánica
TEMA 4 La Materia: Propiedades. eléctricas y el átomo
 TEMA 4 La Materia: Propiedades eléctricas y el átomo La mente curiosa de un científico le hace preguntarse incluso por aquellos que no ve? Pero esas preguntas nacen de aquellos fenómenos que apreciamos
TEMA 4 La Materia: Propiedades eléctricas y el átomo La mente curiosa de un científico le hace preguntarse incluso por aquellos que no ve? Pero esas preguntas nacen de aquellos fenómenos que apreciamos
PRUEBAS DE ACCESO A LA UNIVERSIDAD MATERIAS DE MODALIDAD: FASES GENERAL Y ESPECÍFICA
 PRUEBAS DE ACCESO A LA UNIVERSIDAD MATERIAS DE MODALIDAD: FASES GENERAL Y ESPECÍFICA CURSO 013 014 CONVOCATORIA: PROBLEMAS OPCIÓN A MATERIA: FÍSICA De las dos opciones propuestas, sólo hay que desarrollar
PRUEBAS DE ACCESO A LA UNIVERSIDAD MATERIAS DE MODALIDAD: FASES GENERAL Y ESPECÍFICA CURSO 013 014 CONVOCATORIA: PROBLEMAS OPCIÓN A MATERIA: FÍSICA De las dos opciones propuestas, sólo hay que desarrollar
Comportamiento Electrónico de los Materiales. Tema 1. Fundamentos Físicos de la Estructura Electrónica del Átomo
 Comportamiento Electrónico de los Materiales Tema 1. Fundamentos Físicos de la Estructura Electrónica del Átomo 1.1 Fundamentos de la Estructura Atómica de la Materia1. 1.1.1 Historia: Se tiene conocimiento
Comportamiento Electrónico de los Materiales Tema 1. Fundamentos Físicos de la Estructura Electrónica del Átomo 1.1 Fundamentos de la Estructura Atómica de la Materia1. 1.1.1 Historia: Se tiene conocimiento
XIII OLIMPIADA CHILENA DE FISICA 2005 Sociedad Chilena de Física
 XIII OLIMPIADA CHILENA DE FISICA 2005 Sociedad Chilena de Física PRUEBA EXPERIMENTAL A NOMBRE: RUT: CURSO: NUMERO TOTAL DE PAGINAS ESCRITAS: PUNTAJE TOTAL La constante de Planck de la física cuántica y
XIII OLIMPIADA CHILENA DE FISICA 2005 Sociedad Chilena de Física PRUEBA EXPERIMENTAL A NOMBRE: RUT: CURSO: NUMERO TOTAL DE PAGINAS ESCRITAS: PUNTAJE TOTAL La constante de Planck de la física cuántica y
Solucionario Cuaderno Estrategias y Ejercitación Modelo atómico de la materia II: números cuánticos y configuración electrónica
 Solucionario Cuaderno Estrategias y Ejercitación Modelo atómico de la materia II: números cuánticos y configuración electrónica Química Técnico Profesional Intensivo SCUACTC002TC83-A16V1 Ítem Alternativa
Solucionario Cuaderno Estrategias y Ejercitación Modelo atómico de la materia II: números cuánticos y configuración electrónica Química Técnico Profesional Intensivo SCUACTC002TC83-A16V1 Ítem Alternativa
MODELOS ATÓMICOS. Ya ves que se empezó pronto con el estudio de la composición de la materia.
 MODELOS ATÓMICOS El primero en hablar de la estructura de la materia fue Demócrito de Abdera, 460 a. C-370 a. C. Consideraba que la materia estaba compuesta por pequeñas partículas indivisibles e indestructibles.
MODELOS ATÓMICOS El primero en hablar de la estructura de la materia fue Demócrito de Abdera, 460 a. C-370 a. C. Consideraba que la materia estaba compuesta por pequeñas partículas indivisibles e indestructibles.
Modelo atómico de la materia.
 Modelo atómico de la materia. La Teoría Atómica se basa en la suposición (ratificada después por datos experimentales) de que la materia no es continua, sino que está formada por partículas distintas.
Modelo atómico de la materia. La Teoría Atómica se basa en la suposición (ratificada después por datos experimentales) de que la materia no es continua, sino que está formada por partículas distintas.
ÁTOMO ~ m NÚCLEO ~ mnucleón < m. MATERIA ~ 10-9 m. Átomo FÍSICA MATERIALES PARTÍCULAS
 ESTRUCTURA DE LA MATERIA Grupo D CURSO 20011 2012 EL NÚCLEO ATÓMICO DE QUÉ ESTÁN HECHAS LAS COSAS? MATERIA ~ 10-9 m Átomo FÍSICA MATERIALES ÁTOMO ~ 10-10 m NÚCLEO ~ 10-14 mnucleón < 10-15 m Electrón Protón
ESTRUCTURA DE LA MATERIA Grupo D CURSO 20011 2012 EL NÚCLEO ATÓMICO DE QUÉ ESTÁN HECHAS LAS COSAS? MATERIA ~ 10-9 m Átomo FÍSICA MATERIALES ÁTOMO ~ 10-10 m NÚCLEO ~ 10-14 mnucleón < 10-15 m Electrón Protón
TEMA 2 ESTRUCTURA ELECTRÓNICA DE LOS ÁTOMOS
 TEMA 2 ESTRUCTURA ELECTRÓNICA DE LOS ÁTOMOS MARÍA PILAR RUIZ OJEDA BORJA MUÑOZ LEOZ Contenidos: 1. Introducción 2. Modelo de Thomson 3. Modelo de Rutherford 4. La luz y las ondas electromagnéticas 5. Dispersión
TEMA 2 ESTRUCTURA ELECTRÓNICA DE LOS ÁTOMOS MARÍA PILAR RUIZ OJEDA BORJA MUÑOZ LEOZ Contenidos: 1. Introducción 2. Modelo de Thomson 3. Modelo de Rutherford 4. La luz y las ondas electromagnéticas 5. Dispersión
Puntos de ebullición.
 1.-Indica el tipo de enlace de los siguientes hidruros. Ayundándote de la siguiente tabla comenta la polaridad de los enlaces. Hidruro % carácter iónico HF 43 HCl 17 HBr 11 HI 6 Representa gráficamente
1.-Indica el tipo de enlace de los siguientes hidruros. Ayundándote de la siguiente tabla comenta la polaridad de los enlaces. Hidruro % carácter iónico HF 43 HCl 17 HBr 11 HI 6 Representa gráficamente
EJERCICIOS RESUELTOS DE TABLA PERIODICA
 EJERCICIOS RESUELTOS DE TABLA PERIODICA 1. Indique Cuál es el modelo atómico que está actualmente vigente? El Modelo Mecano- cuántico 2. Cuáles fueron los principales hechos y/o descubrimientos que llevaron
EJERCICIOS RESUELTOS DE TABLA PERIODICA 1. Indique Cuál es el modelo atómico que está actualmente vigente? El Modelo Mecano- cuántico 2. Cuáles fueron los principales hechos y/o descubrimientos que llevaron
Interacción de neutrones con la materia. Laura C. Damonte 2014
 Interacción de neutrones con la materia Laura C. Damonte 2014 Interacción de neutrones con la materia La interacción de los neutrones con la materia tiene interés tanto experimental y teórico como también
Interacción de neutrones con la materia Laura C. Damonte 2014 Interacción de neutrones con la materia La interacción de los neutrones con la materia tiene interés tanto experimental y teórico como también
PROBLEMAS RESUELTOS DE DISTRIBUCIÓN ELECTRONICA EN NIVELES, SUBNIVELES Y ORBITALES ATÓMICOS.
 PROBLEMAS RESUELTOS DE DISTRIBUCIÓN ELECTRONICA EN NIVELES, SUBNIVELES Y ORBITALES ATÓMICOS. 1. Explique que indica el número cuántico magnético y el número cuántico de espín. Número cuántico magnético:
PROBLEMAS RESUELTOS DE DISTRIBUCIÓN ELECTRONICA EN NIVELES, SUBNIVELES Y ORBITALES ATÓMICOS. 1. Explique que indica el número cuántico magnético y el número cuántico de espín. Número cuántico magnético:
Corteza atómica: Estructura electrónica
 Corteza atómica: Estructura electrónica Aunque los conocimientos actuales sobre la estructura electrónica de los átomos son bastante complejos, las ideas básicas son las siguientes: 1. Existen 7 niveles
Corteza atómica: Estructura electrónica Aunque los conocimientos actuales sobre la estructura electrónica de los átomos son bastante complejos, las ideas básicas son las siguientes: 1. Existen 7 niveles
M. Eugenia Villaseca R. Licenciada y Profesora de Biología PUCV
 M. Eugenia Villaseca R. Licenciada y Profesora de Biología PUCV Comprender la utilidad de los modelos atómicos y de la teoría atómica para explicar los procesos de transformación físico-química de la materia
M. Eugenia Villaseca R. Licenciada y Profesora de Biología PUCV Comprender la utilidad de los modelos atómicos y de la teoría atómica para explicar los procesos de transformación físico-química de la materia
ESTRUCTURA DE LA MATERIA VICENTE PUCHADES PUCHADES. SERVICIO DE RADIOFÍSICA Y PROTECCIÓN RADIOLÓGICA DEL HGU SANTA LUCÍA. CARTAGENA.
 ESTRUCTURA DE LA MATERIA VICENTE PUCHADES PUCHADES. SERVICIO DE RADIOFÍSICA Y PROTECCIÓN RADIOLÓGICA DEL HGU SANTA LUCÍA. CARTAGENA. INDICE Qué es la materia? Modelos de la materia Fuerzas Fundamentales
ESTRUCTURA DE LA MATERIA VICENTE PUCHADES PUCHADES. SERVICIO DE RADIOFÍSICA Y PROTECCIÓN RADIOLÓGICA DEL HGU SANTA LUCÍA. CARTAGENA. INDICE Qué es la materia? Modelos de la materia Fuerzas Fundamentales
Un modelo atómico, por lo tanto consiste en representar de manera grafica, la dimensión atómica de la materia. El objetivo de estos modelos es que el
 Modelos atómicos Debido a que no se podían ver los átomos los científicos crearon modelos para describirlos, éstos fueron evolucionando a lo largo de la historia a medida que se descubrieron nuevas cosas.
Modelos atómicos Debido a que no se podían ver los átomos los científicos crearon modelos para describirlos, éstos fueron evolucionando a lo largo de la historia a medida que se descubrieron nuevas cosas.
PRUEBAS DE ACCESO A LA UNIVERSIDAD MATERIAS DE MODALIDAD: FASES GENERAL Y ESPECÍFICA
 PRUEBAS DE ACCESO A LA UNIVERSIDAD MATERIAS DE MODALIDAD: FASES GENERAL Y ESPECÍFICA CURSO 2012-2013 CONVOCATORIA: JULIO MATERIA: FÍSICA De las dos opciones propuestas, sólo hay que desarrollar una opción
PRUEBAS DE ACCESO A LA UNIVERSIDAD MATERIAS DE MODALIDAD: FASES GENERAL Y ESPECÍFICA CURSO 2012-2013 CONVOCATORIA: JULIO MATERIA: FÍSICA De las dos opciones propuestas, sólo hay que desarrollar una opción
ESTRUCTURA ATÓMICA - PREGUNTAS DE TEST
 ESTRUCTURA ATÓMICA - PREGUNTAS DE TEST Serie A: PARTICULAS SUBATOMICAS: Serie B- ESPECTROS: Serie C- COMPOSICION DEL ÁTOMO Serie D- ESTRUCTURA ELECTRÓNICA Serie E- ATOMO DE THOMPSON Serie F- DEFECTO DE
ESTRUCTURA ATÓMICA - PREGUNTAS DE TEST Serie A: PARTICULAS SUBATOMICAS: Serie B- ESPECTROS: Serie C- COMPOSICION DEL ÁTOMO Serie D- ESTRUCTURA ELECTRÓNICA Serie E- ATOMO DE THOMPSON Serie F- DEFECTO DE
Antecedentes de Química. Autora: Violeta Luz María Bravo Hernández
 Antecedentes de Química Autora: Violeta Luz María Bravo Hernández CONTENIDO 1. Descubrimiento del electrón, protón y neutrón. 2. Modelo atómico de Thomson. 3. Modelo atómico de Rutherford. 4. Modelo atómico
Antecedentes de Química Autora: Violeta Luz María Bravo Hernández CONTENIDO 1. Descubrimiento del electrón, protón y neutrón. 2. Modelo atómico de Thomson. 3. Modelo atómico de Rutherford. 4. Modelo atómico
LiceoTolimense Química Séptimo 1 Periodo ESTRUCTURA INTERNA DE LA MATERIA
 ESTRUCTURA INTERNA DE LA MATERIA Lectura comprensiva Desde la antigüedad los filósofos se preguntaban de qué estaban formadas las cosas que los rodeaban. Primero pensaron que la materia era continua, es
ESTRUCTURA INTERNA DE LA MATERIA Lectura comprensiva Desde la antigüedad los filósofos se preguntaban de qué estaban formadas las cosas que los rodeaban. Primero pensaron que la materia era continua, es
Problemas. Cuestiones. Física 2º Bach. Física moderna 20/05/09 DEPARTAMENTO DE FÍSICA E QUÍMICA. Nombre: [2 PUNTOS /UNO]
![Problemas. Cuestiones. Física 2º Bach. Física moderna 20/05/09 DEPARTAMENTO DE FÍSICA E QUÍMICA. Nombre: [2 PUNTOS /UNO] Problemas. Cuestiones. Física 2º Bach. Física moderna 20/05/09 DEPARTAMENTO DE FÍSICA E QUÍMICA. Nombre: [2 PUNTOS /UNO]](/thumbs/49/25535199.jpg) Física 2º Bach. Física moderna 20/05/09 DEPARTAMENTO DE FÍSICA E QUÍMICA Problemas Nombre: [2 PUNTOS /UNO] 1. Al iluminar una célula fotoeléctrica con radiación electromagnética de longitud de onda 185
Física 2º Bach. Física moderna 20/05/09 DEPARTAMENTO DE FÍSICA E QUÍMICA Problemas Nombre: [2 PUNTOS /UNO] 1. Al iluminar una célula fotoeléctrica con radiación electromagnética de longitud de onda 185
Tema 2: Estructura Atómica y radiación atómica
 Tema : Estructura Atómica y radiación atómica 1. Naturaleza atómica de la materia 1.1. Teoría atómica de Dalton Desde el mundo antiguo han existido teorías filosóficas acerca de la composición de la materia
Tema : Estructura Atómica y radiación atómica 1. Naturaleza atómica de la materia 1.1. Teoría atómica de Dalton Desde el mundo antiguo han existido teorías filosóficas acerca de la composición de la materia
El Modelo Moderno y resultados de nuestro interés
 CLASES 3 Y 4 ESTRUCTURA ELECTRÓNICA DE LOS ELEMENTOS AL ESTADO FUNDAMENTAL. TABLA PERIÓDICA. ELECTRONEGATIVIDAD. El Modelo Moderno y resultados de nuestro interés Así es como el Modelo Moderno (MM) reemplazó
CLASES 3 Y 4 ESTRUCTURA ELECTRÓNICA DE LOS ELEMENTOS AL ESTADO FUNDAMENTAL. TABLA PERIÓDICA. ELECTRONEGATIVIDAD. El Modelo Moderno y resultados de nuestro interés Así es como el Modelo Moderno (MM) reemplazó
FÍSICA MATEMÁTICA I. Espacios de Hilbert y Operadores Lineales. María Cruz Boscá Dpto. Física Atómica y Nuclear Universidad de Granada
 FÍSICA MATEMÁTICA I Espacios de Hilbert y Operadores Lineales María Cruz Boscá Dpto. Física Atómica y Nuclear Universidad de Granada Para qué? Principios del s. XX: -diversos fenómenos (cuerpo negro, espectroscopía,
FÍSICA MATEMÁTICA I Espacios de Hilbert y Operadores Lineales María Cruz Boscá Dpto. Física Atómica y Nuclear Universidad de Granada Para qué? Principios del s. XX: -diversos fenómenos (cuerpo negro, espectroscopía,
2.- Los átomos de un mismo elemento son iguales en masa y propiedades. Y los átomos de elementos diferentes son diferentes en masa y propiedades.
 FICHA 1 TEMA 3: ESTRUCTURA DE LA MATERIA PRIMEROS MODELOS ATÓMICOS La discusión sobre la continuidad o discontinuidad de la materia viene desde muy antiguo. Ya en la antigua Grecia había varias corrientes
FICHA 1 TEMA 3: ESTRUCTURA DE LA MATERIA PRIMEROS MODELOS ATÓMICOS La discusión sobre la continuidad o discontinuidad de la materia viene desde muy antiguo. Ya en la antigua Grecia había varias corrientes
Unidad. Formas en que se presenta la energía. Física y Química 4. ESO. La energía. Energía interna. Energía mecánica. Energía electromagnética
 La energía Puede ser de tres tipos mecánica interna electromagnética Se presenta como Se presenta como Se presenta como química térmica nuclear cinética potencial elástica luminosa o radiante potencial
La energía Puede ser de tres tipos mecánica interna electromagnética Se presenta como Se presenta como Se presenta como química térmica nuclear cinética potencial elástica luminosa o radiante potencial
Núcleo Atómico. El núcleo es una masa muy compacta formada por protones y neutrones.
 Núcleo Atómico Profesor: Robinson Pino H. 1 COMPONENTES DEL NÚCLEO ATÓMICO El núcleo es una masa muy compacta formada por protones y neutrones. PROTÓN PROTÓN(p + ) Es una partícula elemental con carga
Núcleo Atómico Profesor: Robinson Pino H. 1 COMPONENTES DEL NÚCLEO ATÓMICO El núcleo es una masa muy compacta formada por protones y neutrones. PROTÓN PROTÓN(p + ) Es una partícula elemental con carga
Universidad Central del Ecuador Facultad de Ciencias Químicas Fundamentos Espectroscópicos
 Universidad Central del Ecuador Facultad de Ciencias Químicas Fundamentos Espectroscópicos INTEGRANTES: * Nazate Amuy Ana * Veloz Hidalgo Polet TEMA: Combinación Lineal de Orbitales Atómicos ORBITAL ATÓMICO
Universidad Central del Ecuador Facultad de Ciencias Químicas Fundamentos Espectroscópicos INTEGRANTES: * Nazate Amuy Ana * Veloz Hidalgo Polet TEMA: Combinación Lineal de Orbitales Atómicos ORBITAL ATÓMICO
Tercero: una reacción química incluye sólo la separación combinación o reordenamiento de átomos sin crearlos o destruirlos.
 Coomppoonneennt teess ffuunnddaameennt taalleess ddeell áát toomoo El filósofo griego demócrito en el siglo V a.c. propuso la idea de que la materia estaba formada por partículas muy pequeñas indivisibles
Coomppoonneennt teess ffuunnddaameennt taalleess ddeell áát toomoo El filósofo griego demócrito en el siglo V a.c. propuso la idea de que la materia estaba formada por partículas muy pequeñas indivisibles
Física cuántica I - Colección de ejercicios cortos
 Física cuántica I - Colección de ejercicios cortos http://teorica.fis.ucm.es En las siguientes cuestiones una y sólo una de las cuatro respuestas ofrecidas es correcta. Dígase cuál. Es conveniente hacer
Física cuántica I - Colección de ejercicios cortos http://teorica.fis.ucm.es En las siguientes cuestiones una y sólo una de las cuatro respuestas ofrecidas es correcta. Dígase cuál. Es conveniente hacer
El interior del átomo
 PLANIFICACIÓN DE SESIÓN DE APRENDIZAJE GRADO UNIDAD SESIÓN HORAS 3.º 1 7/8 2 TÍTULO DE LA SESIÓN: El interior del átomo APRENDIZAJES ESPERADOS COMPETENCIA CAPACIDAD INDICADOR Explica el mundo físico, Comprende
PLANIFICACIÓN DE SESIÓN DE APRENDIZAJE GRADO UNIDAD SESIÓN HORAS 3.º 1 7/8 2 TÍTULO DE LA SESIÓN: El interior del átomo APRENDIZAJES ESPERADOS COMPETENCIA CAPACIDAD INDICADOR Explica el mundo físico, Comprende
Estas partículas son estudiadas por J.J. Thomson que las caracterizó determinando el tipo de carga que poseían y su relación carga/masa.
 página 1/12 Partículas en el átomo Los experimentos de Volta y más tarde otros que pusieron de manifiesto la existencia de partículas cargadas en la materia llevaron a la investigación que obligó a replantearse
página 1/12 Partículas en el átomo Los experimentos de Volta y más tarde otros que pusieron de manifiesto la existencia de partículas cargadas en la materia llevaron a la investigación que obligó a replantearse
Integrantes :Natalia Castillo Carolina Cabello Laura Otálora Nicolás Osorio Asignatura : Química Curso : 2º año B
 Integrantes :Natalia Castillo Carolina Cabello Laura Otálora Nicolás Osorio Asignatura : Química Curso : 2º año B * Historia del Átomo: -El átomo en la antigüedad (pág. 3) -Leucipo y Demócrito (pág.4)
Integrantes :Natalia Castillo Carolina Cabello Laura Otálora Nicolás Osorio Asignatura : Química Curso : 2º año B * Historia del Átomo: -El átomo en la antigüedad (pág. 3) -Leucipo y Demócrito (pág.4)
Modelos atómicos. El valor de la energía de estos niveles de energía está en función de un número n, denominado número cuántico principal 18 J.
 MODELO ATÓMICO DE BOHR (1913) El modelo atómico de Rutherfod tuvo poca vigencia, ya que inmediatamente a su publicación, se le puso una objeción que no supo rebatir: según la teoría del electromagnetismo
MODELO ATÓMICO DE BOHR (1913) El modelo atómico de Rutherfod tuvo poca vigencia, ya que inmediatamente a su publicación, se le puso una objeción que no supo rebatir: según la teoría del electromagnetismo
TEMA 2 LA CORTEZA ELECTRÓNICA
 Orígenes de la teoría cuántica TEMA 2 LA CORTEZA ELECTRÓNICA Había una grave dificultad con el modelo del átomo de Rutherford. De acuerdo con todos los principios de la física conocidos en 1911, el átomo
Orígenes de la teoría cuántica TEMA 2 LA CORTEZA ELECTRÓNICA Había una grave dificultad con el modelo del átomo de Rutherford. De acuerdo con todos los principios de la física conocidos en 1911, el átomo
Colegio Pasionista de Quilpué Departamento de Ciencias Ciencias Naturales 8 año básico 2015 Miss. Cecilia Rojas Olguín. El átomo.
 Colegio Pasionista de Quilpué Departamento de Ciencias Ciencias Naturales 8 año básico 2015 Miss. Cecilia Rojas Olguín El átomo 06 de Marzo 2015 Objetivos de la clase Comprender el Modelo corpuscular de
Colegio Pasionista de Quilpué Departamento de Ciencias Ciencias Naturales 8 año básico 2015 Miss. Cecilia Rojas Olguín El átomo 06 de Marzo 2015 Objetivos de la clase Comprender el Modelo corpuscular de
Interacciones Eléctricas La Ley de Coulomb
 Interacciones Eléctricas La Ley de Coulomb 1. Introducción La Electrostática se ocupa del estudio de las interacciones entre cargas eléctricas en reposo. Las primeras experiencias relativas a los fenómenos
Interacciones Eléctricas La Ley de Coulomb 1. Introducción La Electrostática se ocupa del estudio de las interacciones entre cargas eléctricas en reposo. Las primeras experiencias relativas a los fenómenos
El e c t r o m a g n e t i s m o. Eduardo Bonda Álvaro Suárez Marcelo Vachetta
 El e c t r o m a g n e t i s m o Cuántica y Relatividad Eduardo Bonda Álvaro Suárez Marcelo Vachetta índice Índice Prólogo...9 Capítulo 1 - Campo Eléctrico...11 Introducción... 11 Elektron... 11 Carga
El e c t r o m a g n e t i s m o Cuántica y Relatividad Eduardo Bonda Álvaro Suárez Marcelo Vachetta índice Índice Prólogo...9 Capítulo 1 - Campo Eléctrico...11 Introducción... 11 Elektron... 11 Carga
TEMAS SELECTOS DE FÍSICA CONTEMPORÁNEA. 1. Introducción a la mecánica cuántica Nanotecnología 18
 TEMAS SELECTOS DE FÍSICA CONTEMPORÁNEA 3 horas a la semana 6 créditos 3 horas teóricas y 0 de laboratorio OBJETIVO: Que el alumno adquiera conceptos básicos de física contemporánea y que construya una
TEMAS SELECTOS DE FÍSICA CONTEMPORÁNEA 3 horas a la semana 6 créditos 3 horas teóricas y 0 de laboratorio OBJETIVO: Que el alumno adquiera conceptos básicos de física contemporánea y que construya una
MODELOS ATÓMICOS REALIZADO POR: NICOLÁS CASTELLANO SUÁREZ. Nº2, 4ºesoB. Física y Química
 MODELOS ATÓMICOS REALIZADO POR: NICOLÁS CASTELLANO SUÁREZ. Nº2, 4ºesoB Física y Química 2 Índice: Introducción..3 Modelo atómico de Dalton..4 Modelo atómico de Thomson.5 Modelo atómico de Rutherford..6
MODELOS ATÓMICOS REALIZADO POR: NICOLÁS CASTELLANO SUÁREZ. Nº2, 4ºesoB Física y Química 2 Índice: Introducción..3 Modelo atómico de Dalton..4 Modelo atómico de Thomson.5 Modelo atómico de Rutherford..6
A su vez, una molécula está compuesta por átomos. Cada uno de ellos posee unas propiedades diferentes en el interior de la molécula que constituyen.
 Constitución de la materia. Supongamos que cualquier sustancia de la naturaleza la dividimos en partes cada vez más pequeñas, conservando cada una de ellas las propiedades de la sustancia inicial. Si seguimos
Constitución de la materia. Supongamos que cualquier sustancia de la naturaleza la dividimos en partes cada vez más pequeñas, conservando cada una de ellas las propiedades de la sustancia inicial. Si seguimos
UNIDAD 1: EL ÁTOMO Y EL SISTEMA PERIÓDICO
 UNIDAD 1: EL ÁTOMO Y EL SISTEMA PERIÓDICO 1. PRIMERAS TEORÍAS ATÓMICAS Demócrito, filósofo griego que vivió en el siglo IV a. C. propuso que, si se dividía la materia en trozos cada vez más pequeños, debería
UNIDAD 1: EL ÁTOMO Y EL SISTEMA PERIÓDICO 1. PRIMERAS TEORÍAS ATÓMICAS Demócrito, filósofo griego que vivió en el siglo IV a. C. propuso que, si se dividía la materia en trozos cada vez más pequeños, debería
PROBLEMAS RESUELTOS SELECTIVIDAD ANDALUCÍA 2002 QUÍMICA TEMA 2: LA ESTRUCTURA DEL ÁTOMO
 PROBLEMAS RESUELTOS SELECTIVIDAD ANDALUCÍA 2002 QUÍMICA TEMA 2: LA ESTRUCTURA DEL ÁTOMO Junio, Ejercicio 2, Opción A Reserva 1, Ejercicio 2, Opción A Reserva 2, Ejercicio 3, Opción B Reserva 3, Ejercicio
PROBLEMAS RESUELTOS SELECTIVIDAD ANDALUCÍA 2002 QUÍMICA TEMA 2: LA ESTRUCTURA DEL ÁTOMO Junio, Ejercicio 2, Opción A Reserva 1, Ejercicio 2, Opción A Reserva 2, Ejercicio 3, Opción B Reserva 3, Ejercicio
Ejercicios de Física cuántica y nuclear. PAEG
 1. Las longitudes de onda del espectro visible están comprendidas, aproximadamente, entre 390 nm en el violeta y 740 nm en el rojo. Qué intervalo aproximado de energías, en ev, corresponde a los fotones
1. Las longitudes de onda del espectro visible están comprendidas, aproximadamente, entre 390 nm en el violeta y 740 nm en el rojo. Qué intervalo aproximado de energías, en ev, corresponde a los fotones
IEO-394 Semiconductores. Juan E. Martínez P. Docente. UdeA
 IEO-394 Semiconductores Juan E. Martínez P. Docente. UdeA Bandas de Energía Y Corrientes de Portadores en Semiconductores. PARTICION DE LOS NIVELES DE ENERGIA A medida que se traen juntos N átomos Cada
IEO-394 Semiconductores Juan E. Martínez P. Docente. UdeA Bandas de Energía Y Corrientes de Portadores en Semiconductores. PARTICION DE LOS NIVELES DE ENERGIA A medida que se traen juntos N átomos Cada
PORTAFOLIO DE EVIDENCIAS QUÍMICA I DE SEGUNDA OPORTUNIDAD I LEE DETENIDAMENTE CADA ENUNCIADO Y CONTESTA SEGÚN SE TE PIDA.
 PORTAFOLIO DE EVIDENCIAS QUÍMICA I DE SEGUNDA OPORTUNIDAD I LEE DETENIDAMENTE CADA ENUNCIADO Y CONTESTA SEGÚN SE TE PIDA. 1.- Ciencia que estudia las características y la composición de los materiales,
PORTAFOLIO DE EVIDENCIAS QUÍMICA I DE SEGUNDA OPORTUNIDAD I LEE DETENIDAMENTE CADA ENUNCIADO Y CONTESTA SEGÚN SE TE PIDA. 1.- Ciencia que estudia las características y la composición de los materiales,
Colegio Alberto Pérez Institución Teresiana Departamento de Ciencias Química Profesora Caterina González Poblete. Núcleo. (protones y neutrones)
 Colegio Alberto Pérez Institución Teresiana Departamento de Ciencias Química Profesora Caterina González Poblete EL ÁTOMO Núcleo Envoltura (electrones) (protones y neutrones) El átomo, como lo conocemos
Colegio Alberto Pérez Institución Teresiana Departamento de Ciencias Química Profesora Caterina González Poblete EL ÁTOMO Núcleo Envoltura (electrones) (protones y neutrones) El átomo, como lo conocemos
PARTÍCULAS FUNDAMENTALES. NÚMEROS CUÁNTICOS. PROPIEDADES PERIÓDICAS.
 PARTÍCULAS FUNDAMENTALES. NÚMEROS CUÁNTICOS. PROPIEDADES PERIÓDICAS. PARTÍCULAS FUNDAMENTALES. CONCEPTOS PREVIOS De acuerdo con lo anterior, en un átomo hay tres partículas fundamentales: protones y neutrones,
PARTÍCULAS FUNDAMENTALES. NÚMEROS CUÁNTICOS. PROPIEDADES PERIÓDICAS. PARTÍCULAS FUNDAMENTALES. CONCEPTOS PREVIOS De acuerdo con lo anterior, en un átomo hay tres partículas fundamentales: protones y neutrones,
Slide 1 / 33. Slide 2 / 33. Slide 3 / El número atómico es equivalente a cuál de los siguientes? A El número de neutrones del átomo.
 Slide 1 / 33 Slide 2 / 33 3 El número atómico es equivalente a cuál de los siguientes? Slide 3 / 33 A El número de neutrones del átomo. B El número de protones del átomo C El número de nucleones del átomo.
Slide 1 / 33 Slide 2 / 33 3 El número atómico es equivalente a cuál de los siguientes? Slide 3 / 33 A El número de neutrones del átomo. B El número de protones del átomo C El número de nucleones del átomo.
Observa la imagen de la derecha. Puedes identificar el núcleo y la nube de electrones? Qué crees que representan las esferas azules, rojas y grises?
 reflexiona Nuestro mundo está lleno de diversidad. Existe una variedad asombrosa en todos los materiales, sustancias y seres vivos que existen en la Tierra. Observa la imagen de la derecha. Incluso en
reflexiona Nuestro mundo está lleno de diversidad. Existe una variedad asombrosa en todos los materiales, sustancias y seres vivos que existen en la Tierra. Observa la imagen de la derecha. Incluso en
TEMA 1 EL ÁTOMO Miguel Alcaraz Baños Objetivos generales
 TEMA 1 EL ÁTOMO Miguel Alcaraz Baños Objetivos generales 1. Describir las partes del átomo y enumerar los componentes más importantes. 2. Enunciar que es el numero atómico Z. 3. Explicar qué propiedades
TEMA 1 EL ÁTOMO Miguel Alcaraz Baños Objetivos generales 1. Describir las partes del átomo y enumerar los componentes más importantes. 2. Enunciar que es el numero atómico Z. 3. Explicar qué propiedades
Problemas adicionales de Física Cuántica (2010/2011)
 Problemas adicionales de Física Cuántica (2010/2011) Mª del Rocío Calero Fernández-Cortés María Jesús Jiménez Donaire Ejercicio 3.- La potencia (en forma de ondas gravitacionales) emitida por un sistema
Problemas adicionales de Física Cuántica (2010/2011) Mª del Rocío Calero Fernández-Cortés María Jesús Jiménez Donaire Ejercicio 3.- La potencia (en forma de ondas gravitacionales) emitida por un sistema
PROPÓSITOS ASIGNATURA: GRADO: BLOQUE SABERES DECLARATIVOS. Química I. Primer Semestre. I. Estructura electrónica de los átomos.
 ASIGNATURA: Química I GRADO: Primer Semestre BLOQUE SABERES DECLARATIVOS PROPÓSITOS I. Estructura electrónica de los átomos. Define los conceptos de número atómico, masa atómica, número de masa e isótopo.
ASIGNATURA: Química I GRADO: Primer Semestre BLOQUE SABERES DECLARATIVOS PROPÓSITOS I. Estructura electrónica de los átomos. Define los conceptos de número atómico, masa atómica, número de masa e isótopo.
INDICE. Volumen 1 Mecánica
 INDICE Volumen 1 Mecánica 1 1. Unidades cantidades físicas y vectores 1.1. La naturaleza de la física 2 1.2. Como resolver problemas en física 3 1.3. Estándares y unidades 5 1.4. Consistencia y conversiones
INDICE Volumen 1 Mecánica 1 1. Unidades cantidades físicas y vectores 1.1. La naturaleza de la física 2 1.2. Como resolver problemas en física 3 1.3. Estándares y unidades 5 1.4. Consistencia y conversiones
Prueba experimental. Constante de Planck y comportamiento de un LED
 Prueba experimental. Constante de Planck y comportamiento de un LED Objetivo. Se va a construir un circuito eléctrico para alimentar LEDs de diferentes colores y obtener un valor aproximado de la constante
Prueba experimental. Constante de Planck y comportamiento de un LED Objetivo. Se va a construir un circuito eléctrico para alimentar LEDs de diferentes colores y obtener un valor aproximado de la constante
LAS LEYES DE LA RADIACIÓN EN LA TIERRA Y EN EL ESPACIO OBJETIVO RESUMEN. GENERACIÓN DE LINEAS: Leyes de Kirchhoff
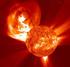 LAS LEYES DE LA RADIACIÓN EN LA TIERRA Y EN EL ESPACIO OBJETIVO Aproximarnos a los procesos que absorben y generan radiación electromagnética en la Tierra y en el espacio. Basada en presentación de Tabaré
LAS LEYES DE LA RADIACIÓN EN LA TIERRA Y EN EL ESPACIO OBJETIVO Aproximarnos a los procesos que absorben y generan radiación electromagnética en la Tierra y en el espacio. Basada en presentación de Tabaré
Radiación electromagnética Naturaleza de la luz Teoría cuántica Espectros atómicos Modelo de Bohr
 ESTRUCTURA ELECTRÓNICA Número de Avogadro Radiación electromagnética Naturaleza de la luz Teoría cuántica Espectros atómicos Modelo de Bohr Número de Avogadro Amadeo Avogadro (1776-1856, italiano) Descubrió
ESTRUCTURA ELECTRÓNICA Número de Avogadro Radiación electromagnética Naturaleza de la luz Teoría cuántica Espectros atómicos Modelo de Bohr Número de Avogadro Amadeo Avogadro (1776-1856, italiano) Descubrió
