Teoría atómica I: Modelos atómicos, estructura atómica y tipos de átomos. Teoría atómica II: Números cuánticos y configuración electrónica
|
|
|
- Óscar Padilla Páez
- hace 6 años
- Vistas:
Transcripción
1 TEORÍA ATÓMICA
2 Teoría atómica I: Modelos atómicos, estructura atómica y tipos de átomos Teoría atómica II: Números cuánticos y configuración electrónica
3 Aprendizajes esperados Diferenciar los distintos modelos atómicos. Definir términos y conceptos utilizados en teoría atómica. Conocer el concepto de número atómico y de número másico. Establecer el número de partículas subatómicas en un átomo. Diferenciar isótopos, isóbaros e isótonos. Conocer los números cuánticos. Trabajar con la configuración electrónica. Relacionar los números cuánticos con la configuración electrónica.
4 Pregunta oficial PSU Las especies neutras S y Cl tienen igual número de A) protones. B) neutrones. C) electrones. D) protones + electrones. E) protones + neutrones. Fuente: DEMRE U. DE CHILE. Proceso de admisión 2008
5 Pregunta oficial PSU La configuración electrónica del átomo de sodio en su estado fundamental es 1s 2 2s 2 2p 6 3s 1. Al respecto, cuántos niveles de energía están ocupados completamente? A) 1 B) 2 C) 3 D) 4 E) 11 Fuente : DEMRE - U. DE CHILE, Proceso de admisión 2012
6 Temas a estudiar 1. Modelos atómicos 2. Estructura atómica 3. Tipos de átomos 4. Números cuánticos 5. Configuración electrónica 6. Reglas que rigen la configuración electrónica
7 1. Modelos atómicos 1.1 Teoría atómica de Dalton Postulados: Los elementos están formados por partículas extremadamente pequeñas llamadas átomos. Todos los átomos de un mismo elemento son idénticos, tienen igual tamaño, masa y propiedades químicas. Los átomos de un elemento son diferentes a los átomos de todos los demás elementos. Los compuestos están formados por átomos de más de un elemento. En cualquier compuesto, la relación del número de átomos entre dos de los elementos presentes siempre es un número entero o una fracción sencilla. Una reacción química implica sólo la separación, combinación o reordenamiento de los átomos; nunca supone la creación o destrucción de los mismos.
8 1. Modelos atómicos 1.2 Modelo atómico de Thomson Thomson propuso el primer modelo atómico. Premio Nobel de Física, 1906 En su modelo los átomos están formados por una esfera uniforme cargada positivamente, en la cual se encuentran incrustados los electrones, de carga negativa. Descubrió el electrón. Midió la relación carga/masa del electrón. Joseph John Thomson ( ) Físico británico Base del descubrimiento: Electrón Modelo atómico de Thomson, también llamado budín de pasas
9 1. Modelos atómicos 1.3 Modelo atómico de Rutherford Rutherford propuso el modelo nuclear del átomo. Premio Nobel de Química, 1908 En su modelo la mayor parte de la masa del átomo y toda su carga positiva, se concentra en una región muy pequeña a la que llamó núcleo. Los electrones están moviéndose constantemente alrededor del núcleo. La mayor parte del átomo es espacio vacío. Ernest Rutherford ( ) Físico y químico neozelandés Base del descubrimiento: Núcleo
10 1. Modelos atómicos 1.4 Modelo atómico de Bohr El electrón del átomo de hidrógeno gira alrededor del núcleo en orbitas circulares estacionarias Premio Nobel de Física, 1922 Los electrones solo pueden existir en ciertas orbitas discretas. Los electrones están restringidos a ciertos estados cuantizados. Es conocido como el modelo planetario. Niels Bohr ( ) Físico danés Base del descubrimiento: Órbitas cuantizadas
11 1. Modelos atómicos 1.5 Modelo mecánico cuántico Premio Nobel de Física, 1933 La energía presente en los electrones los lleva a comportarse como ondas (comportamiento dual). Los electrones se mueven alrededor del núcleo en zonas de mayor probabilidad. Plantea una ecuación de onda, la cual, conduce a una cuantificación de la energía que depende de ciertos números enteros, estos son los números cuánticos. Werner Heisenberg ( ) Físico alemán Erwin Schrödinger ( ) Físico austriaco Premio Nobel de Física, 1929 Premio Nobel de Física, 1932 Principio de incertidumbre de Heisenberg: Es imposible medir simultáneamente de forma precisa la posición y el momento lineal (velocidad) de una partícula. Louis-Victor de Broglie ( ) Físico francés
12 2. Estructura atómica 2.1 El átomo El átomo es la unidad de materia más pequeña. No es posible dividir un átomo mediante procesos químicos. El átomo está compuesto por un núcleo, en el que se concentra casi toda su masa, rodeado por una nube de electrones. El núcleo atómico está formado por protones, con carga positiva y neutrones, eléctricamente neutros. Los electrones, cargados negativamente, permanecen ligados al núcleo mediante la fuerza electromagnética.
13 2. Estructura atómica 2.2 Partículas subatómicas Partícula Masa (g) Masa (uma) Carga (C) Carga (ev) Masa (relación) Símbolo Protón x x p + Neutrón x n Electrón x x /1840 e -
14 2. Estructura atómica 2.3 Núcleo atómico Número atómico (Z): Número de protones del átomo. Indica el elemento al que pertenece el átomo. ZX A Número másico (A): Suma de protones y neutrones del átomo. Indica la masa del átomo
15 2. Estructura atómica 2.4 Átomos e iones Átomo negativo Átomo con mayor número de electrones que de protones. e - > p + denominados aniones. Átomo neutro Átomo con número de electrones igual al de protones. e - = p + Átomo positivo Átomo con menor número de electrones que de protones. e - < p + denominados cationes.
16 Ejemplos Mg protones neutrones electrones Br protones neutrones electrones O protones neutrones electrones Ti protones neutrones electrones
17 3. Tipos de átomos 3.1 Isótopos Corresponden a átomos que tienen el mismo número atómico pero diferente número másico. Por ejemplo, existen tres isótopos de hidrógeno. Se conocen como hidrógeno, deuterio y tritio. Solo 21 elementos poseen un solo isótopo natural
18 3. Tipos de átomos 3.2 Isóbaros Se denominan isóbaros a los distintos núcleos atómicos con el mismo número másico (A), pero diferente número atómico (Z). Las especies químicas son distintas, pero la cantidad de protones y neutrones es tal que, a pesar de ser distinta entre los dos isóbaros, la suma es la misma.
19 3. Tipos de átomos 3.3 Isótonos Son átomos diferentes, por lo tanto, tienen diferente número atómico, también tienen diferente número másico, pero, tienen el mismo número de neutrones. Número de protones difiere entre átomos.
20 3. Tipos de átomos Regla nemotécnica ISÓTONOS ISÓBAROS ISÓTOPOS igual número de Neutrones (N) igual número Másico (A) igual número de Protones (P) ISÓTONOS ISÓBAROS ISÓTOPOS
21 Ejemplos 1 1 H 3 1H isótopos 14 7 N 12 5B isótonos Ag 107 Pd 46 isóbaros 12 6 C 14 6C isótopos
22 Introducción Schrodinger propuso una ecuación que contiene términos de ondas y partículas para los electrones. Resolviendo la ecuación obtenemos funciones de onda; su cuadrado nos indica la probabilidad en que los electrones se encuentran distribuidos. Las variables de esta función son los números cuánticos. La ecuación de Schrodinger permite obtener orbitales y su energía.
23 4. Números cuánticos De la ecuación de Schrodinger emergen naturalmente tres números. Número cuántico principal, n Indica la energía de los orbitales. Es el mismo asignado por Bohr para las órbitas, cuanto más pequeño el número, más cerca del núcleo. Número cuántico del momento angular o azimutal, l Indica la forma de los orbitales. Depende del valor de n, desde 0 hasta (n 1). Número cuántico magnético, m o m l Valor l Tipo orbital s p d f Indica la orientación espacial de los orbitales. Presenta valores enteros desde l hasta +l, incluyendo el 0.
24 4. Números cuánticos 4.1 Número cuántico principal Número principal o energético (n) Indica la distancia entre el núcleo y el electrón. Permite establecer el tamaño del orbital. Se visualiza en la forma de capas alrededor del núcleo. n = 1, 2, 3, 4,
25 4. Números cuánticos 4.2 Número cuántico secundario Número secundario o de momentum angular (l) Indica la forma tridimensional de los orbitales. Se visualiza en la forma de subcapas dentro de cada nivel energético. Puede existir más de un l por nivel energético. l = 0 (s), 1 (p), 2 (d).(n-1) l siempre es menor que n
26 4. Números cuánticos 4.2 Número cuántico secundario Orbital s
27 4. Números cuánticos 4.2 Número cuántico secundario Orbital p Los tres orbitales p corresponden a valores de m de 1, 0 y +1, respectivamente. Se encuentran en los ejes cartesianos x, y, z. Al aumentar n, se hacen más grandes.
28 4. Números cuánticos 4.2 Número cuántico secundario Orbital d
29 4. Números cuánticos 4.2 Número cuántico secundario Orbital tipo Valor l Nº orbitales (2l + 1) Nº electrones s p d f
30 4. Números cuánticos Relación entre números cuánticos n y l n = 4 l = 0, 1, 2, 3 4s 4p 4d 4f n = 3 l = 0, 1, 2 3s 3p 3d n = 2 l = 0, 1 2s 2p n = 1 l = 0 1s
31 4. Números cuánticos 4.3 Número cuántico terciario Número terciario o magnético (m) Indica la orientación en el espacio del orbital. Se establece sobre un eje de coordenadas. m = -l,,0,,+l
32 4. Números cuánticos 4.3 Número cuántico terciario Orbital tipo s 0 Orbital tipo p Orbital tipo d Orbital tipo f
33 4. Números cuánticos 4.4 Número cuántico de espín Número de espín Indica el sentido de rotación del electrón sobre su eje. Es independiente de los otros números cuánticos. Puede adoptar dos valores. s = +1/2 o 1/2
34 5. Configuración electrónica Permite la completa descripción de la estructura de la electrósfera. Corresponde a una versión resumida de los números cuánticos de todos los electrones presentes en un átomo. Indica el número cuántico principal (n) 3p 1 Indica la cantidad de electrones existentes en un tipo de orbital Indica el número cuántico secundario (l) Números cuánticos n = 3 l =1 m = -1 s = +1/2 incompleto
35 5. Configuración electrónica 5.1 Orden de llenado 1s 2s 3s 4s 5s 6s 7s 2p 3p 4p 5p 6p 7p 3d 4d 5d 6d 4f 5f
36 5. Configuración electrónica 5.2 Configuración electrónica abreviada Las configuraciones electrónicas se pueden escribir abreviadas, utilizando la configuración del gas noble más cercano. Ejemplo: Na (Z=11): [Ne]3s 1 Li (Z=3): [He]2s 1 Electrones internos entre corchetes Electrones de valencia fuera de conf. de gas noble Gases nobles: Elementos que tienen la capa p llena adquiriendo una gran estabilidad. Estos gases en su mayoría son inertes. He (Z=2) Ne (Z=10) Ar (Z=18) Kr (Z=36)
37 5. Configuración electrónica 5.3 Incremento energético en el orden de llenado
38 Ejemplos Configuración electrónica para 11 electrones 11Na 1s 2 2s 2 2p 6 3s 1 Números cuánticos n = 3 l = 0 m = 0 s = +½
39 6. Reglas que rigen la configuración electrónica 6.1 Principio de exclusión de Pauli Si queremos colocar más de un electrón en un mismo orbital debemos cambiar el número cuántico de espín (s). Ejemplo: Se tienen dos elementos: Na y Mg. Premio Nobel de Física,1945 Na (Z=11): 1s 2 2s 2 2p 6 3s 1 Los cuatro números cuánticos son: n l m s /2 Mg (Z=12): 1s 2 2s 2 2p 6 3s 2 Los cuatro números cuánticos son: n l m s /2 En un átomo no pueden existir dos electrones con el mismo conjunto de números cuánticos Se cumple el principio de exclusión de Pauli
40 6. Reglas que rigen la configuración electrónica 6.2 Principio de Aufbau Primero debe llenarse el orbital 1s (hasta un máximo de dos electrones, esto de acuerdo con el número cuántico l). Después se llena el orbital 2s (también con dos electrones como máximo). La subcapa 2p tiene tres orbitales degenerados en energía, denominados, según su posición tridimensional, 2p x, 2p y, 2p z. Así, los tres orbitales 2p puede llenarse hasta con seis electrones, dos en cada uno. Los electrones se agregan al átomo partiendo del orbital de menor energía, hasta que todos los electrones están ubicados en un orbital apropiado.
41 6. Reglas que rigen la configuración electrónica 6.3 Regla de máxima multiplicidad de Hund Las partículas subatómicas son más estables (tienen menor energía) cuando presentan electrones desapareados (espines paralelos) que cuando esos electrones están apareados (espines opuestos o antiparalelos). Elementos N electrones Diagrama orbitales Configuración electrónica Li 3 1s 2 2s 1 Be 4 1s 2 2s 2 B 5 1s 2 2s 2 2p x 1 C 6 1s 2 2s 2 2p x1 2p y 1 Friedrich Hund ( ) Físico alemán N Ne s 2 2s 2 2p x1 2p y1 2p 1 z 1s 2 2s 2 2p x2 2p y2 2p 2 z Na 11 1s 2 2s 2 2p 6 3s 1
42 Pregunta oficial PSU Las especies neutras S y Cl tienen igual número de A) protones. B) neutrones. C) electrones. D) protones + electrones. E) protones + neutrones. E Comprensión Fuente: DEMRE U. DE CHILE.
43 Pregunta oficial PSU La configuración electrónica del átomo de sodio en su estado fundamental es 1s 2 2s 2 2p 6 3s 1. Al respecto, cuántos niveles de energía están ocupados completamente? A) 1 B) 2 C) 3 D) 4 E) 11 B Comprensión Fuente : DEMRE - U. DE CHILE, Proceso de admisión 2012.
Clase N 1. Modelo Atómico I
 Pre-Universitario Manuel Guerrero Ceballos Clase N 1 Modelo Atómico I ICAL ATACAMA Módulo Plan Común Modelos Atómicos Teoría Atómica De Dalton Los elementos están formados por partículas extremadamente
Pre-Universitario Manuel Guerrero Ceballos Clase N 1 Modelo Atómico I ICAL ATACAMA Módulo Plan Común Modelos Atómicos Teoría Atómica De Dalton Los elementos están formados por partículas extremadamente
Solucionario Cuaderno Estrategias y Ejercitación Modelo atómico de la materia II: números cuánticos y configuración electrónica
 Solucionario Cuaderno Estrategias y Ejercitación Modelo atómico de la materia II: números cuánticos y configuración electrónica Química Técnico Profesional Intensivo SCUACTC002TC83-A16V1 Ítem Alternativa
Solucionario Cuaderno Estrategias y Ejercitación Modelo atómico de la materia II: números cuánticos y configuración electrónica Química Técnico Profesional Intensivo SCUACTC002TC83-A16V1 Ítem Alternativa
Estudio del átomo: 1. Átomos e isótopos 2. Modelos Atómicos 3. Teoría cuántica. Ing. Sol de María Jiménez González
 Estudio del átomo: 1. Átomos e isótopos 2. Modelos Atómicos 3. Teoría cuántica 1 Núcleo: protones y neutrones Los electrones se mueven alrededor. Característica Partículas Protón Neutrón Electrón Símbolo
Estudio del átomo: 1. Átomos e isótopos 2. Modelos Atómicos 3. Teoría cuántica 1 Núcleo: protones y neutrones Los electrones se mueven alrededor. Característica Partículas Protón Neutrón Electrón Símbolo
Configuración Electrónica
 Configuración Electrónica La configuración electrónica de un átomo indica la forma como están distribuidos los electrones entre los distintos orbitales atómicos. Según el Principio de Exclusión de Pauli,
Configuración Electrónica La configuración electrónica de un átomo indica la forma como están distribuidos los electrones entre los distintos orbitales atómicos. Según el Principio de Exclusión de Pauli,
EXTRUCTURA ATOMICA ACTUAL
 ATOMOS Y ELEMENTOS TEMA 4 Química ATOMOS EXTRUCTURA ATOMICA ACTUAL PARTICULA UBICACION CARGA MASA PROTON NUCLEO + SI NEUTRON NUCLEO 0 SI ELECTRON ORBITAS - DESPRECIABLE La masa del átomo reside en el núcleo.
ATOMOS Y ELEMENTOS TEMA 4 Química ATOMOS EXTRUCTURA ATOMICA ACTUAL PARTICULA UBICACION CARGA MASA PROTON NUCLEO + SI NEUTRON NUCLEO 0 SI ELECTRON ORBITAS - DESPRECIABLE La masa del átomo reside en el núcleo.
Modelo atómico de la materia.
 Modelo atómico de la materia. La Teoría Atómica se basa en la suposición (ratificada después por datos experimentales) de que la materia no es continua, sino que está formada por partículas distintas.
Modelo atómico de la materia. La Teoría Atómica se basa en la suposición (ratificada después por datos experimentales) de que la materia no es continua, sino que está formada por partículas distintas.
- Dalton: TEORIA ATÓMICA ( inicio del SIGLO XIX) - Descubrimiento del electrónjoseph John Thomson ( )
 REPASO QUÍMICA 01 - Dalton: TEORIA ATÓMICA ( inicio del SIGLO XIX) - Descubrimiento del electrónjoseph John Thomson (1856-1940) Modelo de Thompson Modelo del budín de pasas - EN 1895 WILHELM RONTGEN Descubre
REPASO QUÍMICA 01 - Dalton: TEORIA ATÓMICA ( inicio del SIGLO XIX) - Descubrimiento del electrónjoseph John Thomson (1856-1940) Modelo de Thompson Modelo del budín de pasas - EN 1895 WILHELM RONTGEN Descubre
El átomo: sus partículas elementales
 El átomo: sus partículas elementales Los rayos catódicos estaban constituidos por partículas cargadas negativamente ( a las que se llamo electrones) y que la relación carga/masa de éstas partículas era
El átomo: sus partículas elementales Los rayos catódicos estaban constituidos por partículas cargadas negativamente ( a las que se llamo electrones) y que la relación carga/masa de éstas partículas era
LiceoTolimense Química Séptimo 1 Periodo ESTRUCTURA INTERNA DE LA MATERIA
 ESTRUCTURA INTERNA DE LA MATERIA Lectura comprensiva Desde la antigüedad los filósofos se preguntaban de qué estaban formadas las cosas que los rodeaban. Primero pensaron que la materia era continua, es
ESTRUCTURA INTERNA DE LA MATERIA Lectura comprensiva Desde la antigüedad los filósofos se preguntaban de qué estaban formadas las cosas que los rodeaban. Primero pensaron que la materia era continua, es
Con posterioridad el físico alemán Sommerfeld introdujo en el modelo la posibilidad de órbitas elípticas. Köningsberg, Munich, 1951
 4. El paso de una órbita a otra supone la absorción o emisión de radiación. El átomo sólo absorberá o emitirá la radiación justa para pasar de una órbita a otra. Las órbitas de los electrones son estables
4. El paso de una órbita a otra supone la absorción o emisión de radiación. El átomo sólo absorberá o emitirá la radiación justa para pasar de una órbita a otra. Las órbitas de los electrones son estables
PARTÍCULAS DEL ÁTOMO MODELOS ATÓMICOS. TEMA 7 Pág. 155 libro nuevo
 PARTÍCULAS DEL ÁTOMO MODELOS ATÓMICOS TEMA 7 Pág. 155 libro nuevo DESCUBRIMIENTO DEL ÁTOMO. PARTÍCULAS SUBATÓMICAS En la antigua Grecia ya había dos teorías sobre la materia: Teoría Atomística (siglo IV
PARTÍCULAS DEL ÁTOMO MODELOS ATÓMICOS TEMA 7 Pág. 155 libro nuevo DESCUBRIMIENTO DEL ÁTOMO. PARTÍCULAS SUBATÓMICAS En la antigua Grecia ya había dos teorías sobre la materia: Teoría Atomística (siglo IV
QUIMICA GENERAL. Docente : Raquel Villafrades Torres
 Universidad Pontificia Bolivariana QUIMICA GENERAL Docente : Raquel Villafrades Torres TEORIA ATOMICA DE DALTON (1808) BASES Ley de conservación de la masa: La masa total de las sustancias presentes después
Universidad Pontificia Bolivariana QUIMICA GENERAL Docente : Raquel Villafrades Torres TEORIA ATOMICA DE DALTON (1808) BASES Ley de conservación de la masa: La masa total de las sustancias presentes después
Thompson (1898) Rutherford (1911) Bohr (1913) Schrödinger (1926) NUMEROS CUANTICOS
 Thompson (1898) Modelo Atómico Rutherford (1911) Bohr (1913) Propiedad corpuscular de las onda (PLANCK) Propiedad ondulatoria de las partículas (De Broglie) Schrödinger (1926) Números cuánticos 1 NUMEROS
Thompson (1898) Modelo Atómico Rutherford (1911) Bohr (1913) Propiedad corpuscular de las onda (PLANCK) Propiedad ondulatoria de las partículas (De Broglie) Schrödinger (1926) Números cuánticos 1 NUMEROS
b) La zona externa del átomo se llama CORTEZA. y ahí es donde se mueven los ELECTRONES
 PREGUNTAS DE RESPUESTA BREVE 1. Completa las siguientes frases relativas a los átomos de los elementos: a) La parte del átomo en donde se puede considerar que se concentra toda su masa es el NÚCLEO y ahí
PREGUNTAS DE RESPUESTA BREVE 1. Completa las siguientes frases relativas a los átomos de los elementos: a) La parte del átomo en donde se puede considerar que se concentra toda su masa es el NÚCLEO y ahí
3 - Cómo podemos diferenciar un elemento químico de un compuesto, según la teoría de Dalton?
 TEORÍA ATÓMICA 1- A partir de los siguientes datos, cuántas veces es maor la masa del protón que la del electrón? Masa del protón =1,673 10-27 kg Masa del electrón =9,1 10-31 kg 2 - El modelo del átomo
TEORÍA ATÓMICA 1- A partir de los siguientes datos, cuántas veces es maor la masa del protón que la del electrón? Masa del protón =1,673 10-27 kg Masa del electrón =9,1 10-31 kg 2 - El modelo del átomo
MODELOS ATOMICOS. Solución Å; Ultravioleta; 1106 m/s
 MODELOS ATOMICOS 1. Calcular el valor del radio de la órbita que recorre el electrón del hidrogeno en su estado normal. Datos. h = 6 63 10 27 erg s, m(e ) = 9 1 10 28 gr, q(e ) = 4 8 10-10 u.e.e. Solución.
MODELOS ATOMICOS 1. Calcular el valor del radio de la órbita que recorre el electrón del hidrogeno en su estado normal. Datos. h = 6 63 10 27 erg s, m(e ) = 9 1 10 28 gr, q(e ) = 4 8 10-10 u.e.e. Solución.
Guía de Estudio para 1er Parcial Temas Selectos de Química
 Guía de Estudio para 1er Parcial Temas Selectos de Química 1. Menciona que científicos ordenaron los elementos conocidos en su época en triadas (grupos de tres), en octavas, por número atómico y quien
Guía de Estudio para 1er Parcial Temas Selectos de Química 1. Menciona que científicos ordenaron los elementos conocidos en su época en triadas (grupos de tres), en octavas, por número atómico y quien
Colegio Alberto Pérez Institución Teresiana Departamento de Ciencias Química Profesora Caterina González Poblete. Núcleo. (protones y neutrones)
 Colegio Alberto Pérez Institución Teresiana Departamento de Ciencias Química Profesora Caterina González Poblete EL ÁTOMO Núcleo Envoltura (electrones) (protones y neutrones) El átomo, como lo conocemos
Colegio Alberto Pérez Institución Teresiana Departamento de Ciencias Química Profesora Caterina González Poblete EL ÁTOMO Núcleo Envoltura (electrones) (protones y neutrones) El átomo, como lo conocemos
2.- Los átomos de un mismo elemento son iguales en masa y propiedades. Y los átomos de elementos diferentes son diferentes en masa y propiedades.
 FICHA 1 TEMA 3: ESTRUCTURA DE LA MATERIA PRIMEROS MODELOS ATÓMICOS La discusión sobre la continuidad o discontinuidad de la materia viene desde muy antiguo. Ya en la antigua Grecia había varias corrientes
FICHA 1 TEMA 3: ESTRUCTURA DE LA MATERIA PRIMEROS MODELOS ATÓMICOS La discusión sobre la continuidad o discontinuidad de la materia viene desde muy antiguo. Ya en la antigua Grecia había varias corrientes
Actividad: Cómo son las configuraciones electrónicas?
 Cómo son las configuraciones electrónicas de los elementos que forman una familia? Nivel: 2º Medio Subsector: Ciencias químicas Unidad temática: Actividad: Cómo son las configuraciones electrónicas? En
Cómo son las configuraciones electrónicas de los elementos que forman una familia? Nivel: 2º Medio Subsector: Ciencias químicas Unidad temática: Actividad: Cómo son las configuraciones electrónicas? En
ÁTOMO..su historia y su estudio
 ÁTOMO.su historia y su estudio LOS GRIEGOS Y SU APORTE 2000 años antes de Cristo, la civilización griega representada por varios filósofos, ya se preguntaban acerca de qué estaba formado el universo?...
ÁTOMO.su historia y su estudio LOS GRIEGOS Y SU APORTE 2000 años antes de Cristo, la civilización griega representada por varios filósofos, ya se preguntaban acerca de qué estaba formado el universo?...
Un modelo atómico, por lo tanto consiste en representar de manera grafica, la dimensión atómica de la materia. El objetivo de estos modelos es que el
 Modelos atómicos Debido a que no se podían ver los átomos los científicos crearon modelos para describirlos, éstos fueron evolucionando a lo largo de la historia a medida que se descubrieron nuevas cosas.
Modelos atómicos Debido a que no se podían ver los átomos los científicos crearon modelos para describirlos, éstos fueron evolucionando a lo largo de la historia a medida que se descubrieron nuevas cosas.
UNIDAD 1: EL ÁTOMO Y EL SISTEMA PERIÓDICO
 UNIDAD 1: EL ÁTOMO Y EL SISTEMA PERIÓDICO 1. PRIMERAS TEORÍAS ATÓMICAS Demócrito, filósofo griego que vivió en el siglo IV a. C. propuso que, si se dividía la materia en trozos cada vez más pequeños, debería
UNIDAD 1: EL ÁTOMO Y EL SISTEMA PERIÓDICO 1. PRIMERAS TEORÍAS ATÓMICAS Demócrito, filósofo griego que vivió en el siglo IV a. C. propuso que, si se dividía la materia en trozos cada vez más pequeños, debería
Tema II: Estructura atómica y tabla periódica
 República Bolivariana de Venezuela Ministerio del Poder Popular para la Educación U.E. Colegio Santo Tomás de Villanueva Departamento de Ciencias Cátedra: Química Orgánica 5 Año Tema II: Estructura atómica
República Bolivariana de Venezuela Ministerio del Poder Popular para la Educación U.E. Colegio Santo Tomás de Villanueva Departamento de Ciencias Cátedra: Química Orgánica 5 Año Tema II: Estructura atómica
Configuración Electrónica
 Los subniveles se ordenan según el valor de n + l Distribución de los electrones en el átomo Número Orbitales que ocupan relativa A menor valor de n + l, menor energía (más estable) Válido sólo si l 3
Los subniveles se ordenan según el valor de n + l Distribución de los electrones en el átomo Número Orbitales que ocupan relativa A menor valor de n + l, menor energía (más estable) Válido sólo si l 3
Tercero: una reacción química incluye sólo la separación combinación o reordenamiento de átomos sin crearlos o destruirlos.
 Coomppoonneennt teess ffuunnddaameennt taalleess ddeell áát toomoo El filósofo griego demócrito en el siglo V a.c. propuso la idea de que la materia estaba formada por partículas muy pequeñas indivisibles
Coomppoonneennt teess ffuunnddaameennt taalleess ddeell áát toomoo El filósofo griego demócrito en el siglo V a.c. propuso la idea de que la materia estaba formada por partículas muy pequeñas indivisibles
QUÍMICA 2º BACH. TEMA 1. ESTRUCTURA ATÓMICA.
 Modelos atómicos QUÍMICA 2º BACH. TEMA 1. ESTRUCTURA ATÓMICA. Teoría atómica de Dalton: La materia está formada por átomos indivisibles. Los átomos de un elemento son distintos de los átomos de otro elemento
Modelos atómicos QUÍMICA 2º BACH. TEMA 1. ESTRUCTURA ATÓMICA. Teoría atómica de Dalton: La materia está formada por átomos indivisibles. Los átomos de un elemento son distintos de los átomos de otro elemento
Colegio Pasionista de Quilpué Departamento de Ciencias Ciencias Naturales 8 año básico 2015 Miss. Cecilia Rojas Olguín. El átomo.
 Colegio Pasionista de Quilpué Departamento de Ciencias Ciencias Naturales 8 año básico 2015 Miss. Cecilia Rojas Olguín El átomo 06 de Marzo 2015 Objetivos de la clase Comprender el Modelo corpuscular de
Colegio Pasionista de Quilpué Departamento de Ciencias Ciencias Naturales 8 año básico 2015 Miss. Cecilia Rojas Olguín El átomo 06 de Marzo 2015 Objetivos de la clase Comprender el Modelo corpuscular de
Programa de Acceso Inclusivo, Equidad y Permanencia PAIEP U. de Santiago. Química
 Modelos atómicos Los filósofos de la antigüedad especularon sobre cómo estaba formada la materia. Demócrito (460-370 a.c) y otros filósofos anteriores a él, pensaban que el mundo material debería estar
Modelos atómicos Los filósofos de la antigüedad especularon sobre cómo estaba formada la materia. Demócrito (460-370 a.c) y otros filósofos anteriores a él, pensaban que el mundo material debería estar
Ordenando Electrones. De qué forma? 2do Medio > Química Configuración Electrónica. Analiza la siguiente situación:
 do Medio > Química Ordenando Electrones Analiza la siguiente situación: Uno de los mayores logros de la ciencia de la primera mitad del siglo XX se dio en el área de la física, y fue el desarrollo de la
do Medio > Química Ordenando Electrones Analiza la siguiente situación: Uno de los mayores logros de la ciencia de la primera mitad del siglo XX se dio en el área de la física, y fue el desarrollo de la
3.1. Estructura atómica
 3.1. Estructura atómica Átomo Protones (+) Núcleo Neutrones (sin carga) Corteza Electrones (-) *Z Número atómico = Número de protones. Cuando el átomo está en estado neutro, Z también es equivalente al
3.1. Estructura atómica Átomo Protones (+) Núcleo Neutrones (sin carga) Corteza Electrones (-) *Z Número atómico = Número de protones. Cuando el átomo está en estado neutro, Z también es equivalente al
PORTAFOLIO DE EVIDENCIAS QUÍMICA I DE SEGUNDA OPORTUNIDAD I LEE DETENIDAMENTE CADA ENUNCIADO Y CONTESTA SEGÚN SE TE PIDA.
 PORTAFOLIO DE EVIDENCIAS QUÍMICA I DE SEGUNDA OPORTUNIDAD I LEE DETENIDAMENTE CADA ENUNCIADO Y CONTESTA SEGÚN SE TE PIDA. 1.- Ciencia que estudia las características y la composición de los materiales,
PORTAFOLIO DE EVIDENCIAS QUÍMICA I DE SEGUNDA OPORTUNIDAD I LEE DETENIDAMENTE CADA ENUNCIADO Y CONTESTA SEGÚN SE TE PIDA. 1.- Ciencia que estudia las características y la composición de los materiales,
ESTRUCTURA ATÓMICA - PREGUNTAS DE TEST
 ESTRUCTURA ATÓMICA - PREGUNTAS DE TEST Serie A: PARTICULAS SUBATOMICAS: Serie B- ESPECTROS: Serie C- COMPOSICION DEL ÁTOMO Serie D- ESTRUCTURA ELECTRÓNICA Serie E- ATOMO DE THOMPSON Serie F- DEFECTO DE
ESTRUCTURA ATÓMICA - PREGUNTAS DE TEST Serie A: PARTICULAS SUBATOMICAS: Serie B- ESPECTROS: Serie C- COMPOSICION DEL ÁTOMO Serie D- ESTRUCTURA ELECTRÓNICA Serie E- ATOMO DE THOMPSON Serie F- DEFECTO DE
ESTRUCTURA DEL ÁTOMO - RESUMEN
 TEMA 1 ESTRUCTURA DEL ÁTOMO - RESUMEN 1. DESCUBRIMIENTO DE LA ESTRUCTURA ATÓMICA (ideas generales) Dalton: consideraba que un átomo no podía romperse en trozos más pequeños. El primer indicio de que el
TEMA 1 ESTRUCTURA DEL ÁTOMO - RESUMEN 1. DESCUBRIMIENTO DE LA ESTRUCTURA ATÓMICA (ideas generales) Dalton: consideraba que un átomo no podía romperse en trozos más pequeños. El primer indicio de que el
Estructura de la materia y Sistema Periódico
 Estructura de la materia y Sistema Periódico 1 - Respecto el número cuántico «n» que aparece en el modelo atómico de Bohr indicar de manera razonada cuáles de las siguientes frases son correctas y cuáles
Estructura de la materia y Sistema Periódico 1 - Respecto el número cuántico «n» que aparece en el modelo atómico de Bohr indicar de manera razonada cuáles de las siguientes frases son correctas y cuáles
MODELOS ATOMICOS. Conoce algo acerca de los Modelos Atómicos? Te Invito A Que Eches Un Vistazo AL Libro!
 MODELOS ATOMICOS Conoce algo acerca de los Modelos Atómicos? Te Invito A Que Eches Un Vistazo AL Libro! POR: Yariza Lombo Caterine Ortiz Natalia Salazar Yesika Novoa F_76336 Qué es el átomo? Definimos
MODELOS ATOMICOS Conoce algo acerca de los Modelos Atómicos? Te Invito A Que Eches Un Vistazo AL Libro! POR: Yariza Lombo Caterine Ortiz Natalia Salazar Yesika Novoa F_76336 Qué es el átomo? Definimos
ESTRUCTURA ATÓMICA Y PROPIEDADES PERIÓDICAS
 ESTRUCTURA ATÓMICA Y PROPIEDADES PERIÓDICAS 1.- Escriba la configuración electrónica de los siguientes iones o elementos: 8 O -2, 9 F - y 10 Ne, e indique el período y grupo de los elementos correspondientes.
ESTRUCTURA ATÓMICA Y PROPIEDADES PERIÓDICAS 1.- Escriba la configuración electrónica de los siguientes iones o elementos: 8 O -2, 9 F - y 10 Ne, e indique el período y grupo de los elementos correspondientes.
FÍSICA y QUÍMICA. Número cuántico Secundario (SUBNIVEL) l. Número cuántico Magnético (ORBITAL, como si fuera una caja) m.
 TEMA 1: ESTRUCTURA DE LA MATERIA. MODELOS ATÓMICOS 1. Modelo Atómico de RUTHERFORD a. Modelo predecesor de Thomson. b. Modelo atómico de Rutherford. c. Virtudes y defectos del Modelo de Rutherford. 2.
TEMA 1: ESTRUCTURA DE LA MATERIA. MODELOS ATÓMICOS 1. Modelo Atómico de RUTHERFORD a. Modelo predecesor de Thomson. b. Modelo atómico de Rutherford. c. Virtudes y defectos del Modelo de Rutherford. 2.
Unidad 1 Estructura atómica de la materia. Teoría cuántica
 Unidad 1 Estructura atómica de la materia. Teoría cuántica 1.El átomo y la constitución de la materia DALTON NO ACEPTADO POR LOS FÍSICOS que creían en la idea de que los átomos se encontraban como disueltos
Unidad 1 Estructura atómica de la materia. Teoría cuántica 1.El átomo y la constitución de la materia DALTON NO ACEPTADO POR LOS FÍSICOS que creían en la idea de que los átomos se encontraban como disueltos
Observa la imagen de la derecha. Puedes identificar el núcleo y la nube de electrones? Qué crees que representan las esferas azules, rojas y grises?
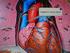 reflexiona Nuestro mundo está lleno de diversidad. Existe una variedad asombrosa en todos los materiales, sustancias y seres vivos que existen en la Tierra. Observa la imagen de la derecha. Incluso en
reflexiona Nuestro mundo está lleno de diversidad. Existe una variedad asombrosa en todos los materiales, sustancias y seres vivos que existen en la Tierra. Observa la imagen de la derecha. Incluso en
El Modelo Moderno y resultados de nuestro interés
 CLASES 3 Y 4 ESTRUCTURA ELECTRÓNICA DE LOS ELEMENTOS AL ESTADO FUNDAMENTAL. TABLA PERIÓDICA. ELECTRONEGATIVIDAD. El Modelo Moderno y resultados de nuestro interés Así es como el Modelo Moderno (MM) reemplazó
CLASES 3 Y 4 ESTRUCTURA ELECTRÓNICA DE LOS ELEMENTOS AL ESTADO FUNDAMENTAL. TABLA PERIÓDICA. ELECTRONEGATIVIDAD. El Modelo Moderno y resultados de nuestro interés Así es como el Modelo Moderno (MM) reemplazó
- Marie Curie. - Joseph Thomson. - Ernest Rutherford. - Max Planck. - Albert Einstein. - Niels Bohr. - Louis de Broglie. - Werner Heisenberg
 - Marie Curie - Joseph Thomson - Ernest Rutherford - Max Planck - Albert Einstein - Niels Bohr - Louis de Broglie - Werner Heisenberg - Wolfgang Pauli - Arnorld Sommerfeld Autores (Orden Alfabético): Celia
- Marie Curie - Joseph Thomson - Ernest Rutherford - Max Planck - Albert Einstein - Niels Bohr - Louis de Broglie - Werner Heisenberg - Wolfgang Pauli - Arnorld Sommerfeld Autores (Orden Alfabético): Celia
M. Eugenia Villaseca R. Licenciada y Profesora de Biología PUCV
 M. Eugenia Villaseca R. Licenciada y Profesora de Biología PUCV Comprender la utilidad de los modelos atómicos y de la teoría atómica para explicar los procesos de transformación físico-química de la materia
M. Eugenia Villaseca R. Licenciada y Profesora de Biología PUCV Comprender la utilidad de los modelos atómicos y de la teoría atómica para explicar los procesos de transformación físico-química de la materia
Tema 5: El átomo y sus uniones.
 Tema 5: El átomo y sus uniones. 1. Teoría Atómica de Dalton. En 1803, John Dalton expone su Teoría Atómica que se basa en los siguientes puntos: Los elementos químicos están formados por partículas muy
Tema 5: El átomo y sus uniones. 1. Teoría Atómica de Dalton. En 1803, John Dalton expone su Teoría Atómica que se basa en los siguientes puntos: Los elementos químicos están formados por partículas muy
La estructura atómica: el núcleo
 Tema 1 La estructura atómica: el núcleo Introducción. Modelos atómicos Composición del átomo. Partículas fundamentales Estructura del núcleo Estabilidad nuclear y energía de enlace nuclear Aplicaciones
Tema 1 La estructura atómica: el núcleo Introducción. Modelos atómicos Composición del átomo. Partículas fundamentales Estructura del núcleo Estabilidad nuclear y energía de enlace nuclear Aplicaciones
Como esta formada la materia?
 Como esta formada la materia? Demócrito, filósofo griego que vivió en el siglo IV a. C. propuso que, si se dividía la materia en trozos cada vez más pequeños, debería llegarse a una porción que ya no podría
Como esta formada la materia? Demócrito, filósofo griego que vivió en el siglo IV a. C. propuso que, si se dividía la materia en trozos cada vez más pequeños, debería llegarse a una porción que ya no podría
LA MATERIA. Características de los átomos
 LA MATERIA Características de los átomos Años más tarde del modelo atómico de Rutherford (1911) se descubrió una nueva partícula en el núcleo, el neutrón. Esta fue descubierta por Chadwick en 1932, y se
LA MATERIA Características de los átomos Años más tarde del modelo atómico de Rutherford (1911) se descubrió una nueva partícula en el núcleo, el neutrón. Esta fue descubierta por Chadwick en 1932, y se
Tabla Periódica y Propiedades Periódicas
 Tabla Periódica y Propiedades Periódicas 1. Las configuraciones electrónicas de los elementos nitrógeno y vanadio son respectivamente: Lo primero que debemos hacer es buscar en la Tabla Periódica los números
Tabla Periódica y Propiedades Periódicas 1. Las configuraciones electrónicas de los elementos nitrógeno y vanadio son respectivamente: Lo primero que debemos hacer es buscar en la Tabla Periódica los números
Tema 2_3. Átomos Polielectronicos y Sistema Periódico
 Tema 2_3. Átomos Polielectronicos y Sistema Periódico Caso más sencillo: átomo de helio (2 electrones) ĤΨ = EΨ ^ ^ Ĥ = T + V z r 12 x atracción del núcleo (+2e) sobre el electrón 1, a una distancia r 1
Tema 2_3. Átomos Polielectronicos y Sistema Periódico Caso más sencillo: átomo de helio (2 electrones) ĤΨ = EΨ ^ ^ Ĥ = T + V z r 12 x atracción del núcleo (+2e) sobre el electrón 1, a una distancia r 1
Unidad I: Propiedades Periódicas: Masa y Enlace
 Unidad I: Propiedades Periódicas: Masa y Enlace 1. Nociones de teoría atómica moderna 2. Propiedades periódicas de los elementos 3. Enlace iónico y covalente 4. Masas atómicas y moleculares 1. Nociones
Unidad I: Propiedades Periódicas: Masa y Enlace 1. Nociones de teoría atómica moderna 2. Propiedades periódicas de los elementos 3. Enlace iónico y covalente 4. Masas atómicas y moleculares 1. Nociones
Sistema Periódico de los elementos. 2º Bachillerato
 Sistema Periódico de los elementos 2º Bachillerato Índice 1. Clasificación de los elementos 2. Núcleo atómico 3. Configuración electrónica 4. La tabla periódica 5. Propiedades periódicas Tamaño y radio
Sistema Periódico de los elementos 2º Bachillerato Índice 1. Clasificación de los elementos 2. Núcleo atómico 3. Configuración electrónica 4. La tabla periódica 5. Propiedades periódicas Tamaño y radio
Qué estudiamos en Química Orgánica? ÁTOMOS Y ELECTRONES! ENLACE QUÍMICO
 Química Orgánica I Qué estudiamos en Química Orgánica? Cómo los compuestos orgánicos reaccionan: Rompimiento y formación de enlaces. Enlaces que se forman cuando átomos comparten electrones, enlaces que
Química Orgánica I Qué estudiamos en Química Orgánica? Cómo los compuestos orgánicos reaccionan: Rompimiento y formación de enlaces. Enlaces que se forman cuando átomos comparten electrones, enlaces que
Corteza atómica: Estructura electrónica
 Corteza atómica: Estructura electrónica Aunque los conocimientos actuales sobre la estructura electrónica de los átomos son bastante complejos, las ideas básicas son las siguientes: 1. Existen 7 niveles
Corteza atómica: Estructura electrónica Aunque los conocimientos actuales sobre la estructura electrónica de los átomos son bastante complejos, las ideas básicas son las siguientes: 1. Existen 7 niveles
J.J Thomson propone el primer modelo de átomo:
 MODELOS ATÓMICOS. DALTON En 1808, Dalton publicó sus ideas sobre el modelo atómico de la materia las cuales han servido de base a la química moderna. Los principios fundamentales de esta teoría son: 1.
MODELOS ATÓMICOS. DALTON En 1808, Dalton publicó sus ideas sobre el modelo atómico de la materia las cuales han servido de base a la química moderna. Los principios fundamentales de esta teoría son: 1.
EL ÁTOMO CONTENIDOS. ANTECEDENTES HISTÓRICOS. ( ) MODELOS ATÓMICOS. RAYOS CATÓDICOS. MODELO DE THOMSON.
 EL ÁTOMO CONTENIDOS. 1.- Antecedentes históricos.( ) 2.- Partículas subatómicas. ( ) 3.- Modelo atómico de Thomsom. 4.- Los rayos X. 5.- La radiactividad. 6.- Modelo atómico de Rutherford. 7.- Radiación
EL ÁTOMO CONTENIDOS. 1.- Antecedentes históricos.( ) 2.- Partículas subatómicas. ( ) 3.- Modelo atómico de Thomsom. 4.- Los rayos X. 5.- La radiactividad. 6.- Modelo atómico de Rutherford. 7.- Radiación
PROBLEMAS RESUELTOS DE DISTRIBUCIÓN ELECTRONICA EN NIVELES, SUBNIVELES Y ORBITALES ATÓMICOS.
 PROBLEMAS RESUELTOS DE DISTRIBUCIÓN ELECTRONICA EN NIVELES, SUBNIVELES Y ORBITALES ATÓMICOS. 1. Explique que indica el número cuántico magnético y el número cuántico de espín. Número cuántico magnético:
PROBLEMAS RESUELTOS DE DISTRIBUCIÓN ELECTRONICA EN NIVELES, SUBNIVELES Y ORBITALES ATÓMICOS. 1. Explique que indica el número cuántico magnético y el número cuántico de espín. Número cuántico magnético:
PROBLEMAS RESUELTOS SELECTIVIDAD ANDALUCÍA 2010 QUÍMICA TEMA 2: LA ESTRUCTURA DEL ÁTOMO
 PROBLEMAS RESUELTOS SELECTIVIDAD ANDALUCÍA 010 QUÍMICA TEMA : LA ESTRUCTURA DEL ÁTOMO Junio, Ejercicio 3, Opción B Reserva 1, Ejercicio, Opción B Reserva, Ejercicio, Opción A Reserva 3, Ejercicio, Opción
PROBLEMAS RESUELTOS SELECTIVIDAD ANDALUCÍA 010 QUÍMICA TEMA : LA ESTRUCTURA DEL ÁTOMO Junio, Ejercicio 3, Opción B Reserva 1, Ejercicio, Opción B Reserva, Ejercicio, Opción A Reserva 3, Ejercicio, Opción
Teoría Cuántica y la estructura electrónica de los Átomos
 EN EL INTERIOR DEL ATOMO TEMA 3 Química General e Inorgánica A Teoría Cuántica y la estructura electrónica de los Átomos 1 LO QUE SABEMOS EXTRUCTURA ATOMICA ACTUAL PARTICULA UBICACION CARGA MASA PROTON
EN EL INTERIOR DEL ATOMO TEMA 3 Química General e Inorgánica A Teoría Cuántica y la estructura electrónica de los Átomos 1 LO QUE SABEMOS EXTRUCTURA ATOMICA ACTUAL PARTICULA UBICACION CARGA MASA PROTON
Enseñanza - Aprendizaje
 El primer modelo atómico con bases científicas, fue formulado por John Dalton descubrió a los átomos en 1804. Pensaba que eran las partículas más pequeñas de la materia, que no podían ser divididas en
El primer modelo atómico con bases científicas, fue formulado por John Dalton descubrió a los átomos en 1804. Pensaba que eran las partículas más pequeñas de la materia, que no podían ser divididas en
U N A M. Facultad de Ingeniería MODELO ATÓMICO DE J. J. THOMSON MODELO ATÓMICO DE ERNEST RUTHERFORD DESCUBRIMIENTO DEL PROTÓN Y DEL NEUTRON
 MODELO ATÓMICO DE J. J. THOMSON MODELO ATÓMICO DE ERNEST RUTHERFORD DESCUBRIMIENTO DEL PROTÓN Y DEL NEUTRON M. C. Q. Alfredo Velásquez Márquez Modelo Atómico de J. J. Thomson Electrones de Carga Negativa
MODELO ATÓMICO DE J. J. THOMSON MODELO ATÓMICO DE ERNEST RUTHERFORD DESCUBRIMIENTO DEL PROTÓN Y DEL NEUTRON M. C. Q. Alfredo Velásquez Márquez Modelo Atómico de J. J. Thomson Electrones de Carga Negativa
MATERIA MOLÉCULAS ÁTOMOS PARTÍCULAS SUBATÓMICAS. Partícula Masa (g) Carga (Coulombs) Carga unitaria. Electrón
 MATERIA MOLÉCULAS ÁTOMOS PARTÍCULAS SUBATÓMICAS Partícula Masa (g) Carga (Coulombs) Carga unitaria Electrón 9.10939 10-28 -1.6022 10-19 -1 Protón 1.67262 10-24 +1.6022 10-19 +1 Neutrón 1.67493 10-24 0
MATERIA MOLÉCULAS ÁTOMOS PARTÍCULAS SUBATÓMICAS Partícula Masa (g) Carga (Coulombs) Carga unitaria Electrón 9.10939 10-28 -1.6022 10-19 -1 Protón 1.67262 10-24 +1.6022 10-19 +1 Neutrón 1.67493 10-24 0
EL ÁTOMO Modelos Atómicos
 EL ÁTOMO Modelos Atómicos Cómo está formada la materia en su interior? Desde los tiempos de la antigua Grecia,los pensadores venían haciéndose esta pregunta, acerca de cómo estaba constituida la materia
EL ÁTOMO Modelos Atómicos Cómo está formada la materia en su interior? Desde los tiempos de la antigua Grecia,los pensadores venían haciéndose esta pregunta, acerca de cómo estaba constituida la materia
MODELOS ATÓMICOS 2ª PARTE
 MODELOS ATÓMICOS 2ª PARTE Teoría Atómica de Joseph John Thomson Diseño Experimental de Joseph John Thomson (1856-1940) Utiliza Tubos de Rayos Catódicos, en los cuales estudia el comportamiento de los gases
MODELOS ATÓMICOS 2ª PARTE Teoría Atómica de Joseph John Thomson Diseño Experimental de Joseph John Thomson (1856-1940) Utiliza Tubos de Rayos Catódicos, en los cuales estudia el comportamiento de los gases
Integrantes :Natalia Castillo Carolina Cabello Laura Otálora Nicolás Osorio Asignatura : Química Curso : 2º año B
 Integrantes :Natalia Castillo Carolina Cabello Laura Otálora Nicolás Osorio Asignatura : Química Curso : 2º año B * Historia del Átomo: -El átomo en la antigüedad (pág. 3) -Leucipo y Demócrito (pág.4)
Integrantes :Natalia Castillo Carolina Cabello Laura Otálora Nicolás Osorio Asignatura : Química Curso : 2º año B * Historia del Átomo: -El átomo en la antigüedad (pág. 3) -Leucipo y Demócrito (pág.4)
Colegio San Lorenzo - Copiapó - Región de Atacama Per Laborem ad Lucem
 TEMARIO EXAMENES QUIMICA 2012 7º BASICO Descubrimiento del átomo: Quién lo descubrió y su significado Estructura atómica: Partes del átomo, características del núcleo y la corteza, cálculo del protón,
TEMARIO EXAMENES QUIMICA 2012 7º BASICO Descubrimiento del átomo: Quién lo descubrió y su significado Estructura atómica: Partes del átomo, características del núcleo y la corteza, cálculo del protón,
LA TABLA PERIÓDICA. Cuestiones generales. Propiedades periódicas
 Cuestiones generales. LA TABLA PERIÓDICA. 1.- Indica el nombre, símbolo, nombre del grupo a que pertenece y periodo de los elementos de números atómicos 3, 9, 16, 19, 38 y 51. 2.- a) Indica el nombre,
Cuestiones generales. LA TABLA PERIÓDICA. 1.- Indica el nombre, símbolo, nombre del grupo a que pertenece y periodo de los elementos de números atómicos 3, 9, 16, 19, 38 y 51. 2.- a) Indica el nombre,
PROBLEMAS RESUELTOS SELECTIVIDAD ANDALUCÍA 2015 QUÍMICA TEMA 2: LA ESTRUCTURA DEL ÁTOMO
 PROBLEMAS RESUELTOS SELECTIVIDAD ANDALUCÍA 2015 QUÍMICA TEMA 2: LA ESTRUCTURA DEL ÁTOMO Junio, Ejercicio 3, Opción B Reserva 1, Ejercicio 2, Opción B Reserva 2, Ejercicio 2, Opción A Reserva 3, Ejercicio
PROBLEMAS RESUELTOS SELECTIVIDAD ANDALUCÍA 2015 QUÍMICA TEMA 2: LA ESTRUCTURA DEL ÁTOMO Junio, Ejercicio 3, Opción B Reserva 1, Ejercicio 2, Opción B Reserva 2, Ejercicio 2, Opción A Reserva 3, Ejercicio
Repartido nº3 Estructura electrónica y Tabla Periódica
 La periferia: Recordamos: Repartido nº3 Estructura electrónica y Tabla Periódica En la periferia se encuentran los electrones. La cantidad de electrones de un átomo equivale a la cantidad de protones,
La periferia: Recordamos: Repartido nº3 Estructura electrónica y Tabla Periódica En la periferia se encuentran los electrones. La cantidad de electrones de un átomo equivale a la cantidad de protones,
Modelos atómicos: Dalton, Thomson, Rutherford, Bohr y Mecánica Cuántica. Clasificación de los elementos y propiedades periódicas
 Modelos atómicos: Dalton, Thomson, Rutherford, Bohr y Mecánica Cuántica Clasificación de los elementos y propiedades periódicas Modelos atómicos: Átomo de Dalton NOMBRE EN QUÉ CONSISTE QUÉ EXPLICA QUÉ
Modelos atómicos: Dalton, Thomson, Rutherford, Bohr y Mecánica Cuántica Clasificación de los elementos y propiedades periódicas Modelos atómicos: Átomo de Dalton NOMBRE EN QUÉ CONSISTE QUÉ EXPLICA QUÉ
Los problemas y cuestiones recogidos en este trabajo han sido enviados por:
 INTRODUCCIÓN El aprendizaje de la Química constituye un reto al que se enfrentan cada año los, cada vez más escasos, estudiantes de 2 de bachillerato que eligen las opciones de Ciencias, Ciencias de la
INTRODUCCIÓN El aprendizaje de la Química constituye un reto al que se enfrentan cada año los, cada vez más escasos, estudiantes de 2 de bachillerato que eligen las opciones de Ciencias, Ciencias de la
Estructura Atómica. Lic. Raúl Hernández Mazariegos
 Área de Química 2008 Estructura Atómica Lic. Raúl Hernández Mazariegos http://rhermazariegos.wordpress.com/ http://raulher.wordpress.com http://raulherqg.wordpress.com http://medicina.usac.edu.gt/quimica/
Área de Química 2008 Estructura Atómica Lic. Raúl Hernández Mazariegos http://rhermazariegos.wordpress.com/ http://raulher.wordpress.com http://raulherqg.wordpress.com http://medicina.usac.edu.gt/quimica/
1. Cuál de los siguientes enunciados es uno de los postulados correspondientes al modelo atómico de Bohr?
 Programa Estándar Anual Nº Guía práctica: Teoría atómica I: modelos atómicos, estructura atómica y tipos de átomos Ejercicios PSU 1. Cuál de los siguientes enunciados es uno de los postulados correspondientes
Programa Estándar Anual Nº Guía práctica: Teoría atómica I: modelos atómicos, estructura atómica y tipos de átomos Ejercicios PSU 1. Cuál de los siguientes enunciados es uno de los postulados correspondientes
PSU QUIMICA 2010 RAOV - CYQ
 1 PSU QUIMICA 2010 RAOV - CYQ 2 NUMERO ATOMICO Y NUMERO MASICO 1.- Si los átomos A, B y C presentan la siguiente cantidad de partículas subatómicas: A.- 12 protones, 14 neutrones, 12 electrones B.- 12
1 PSU QUIMICA 2010 RAOV - CYQ 2 NUMERO ATOMICO Y NUMERO MASICO 1.- Si los átomos A, B y C presentan la siguiente cantidad de partículas subatómicas: A.- 12 protones, 14 neutrones, 12 electrones B.- 12
TABLA PERIODICA Y PERIOCIDAD
 ENSAYO QUIMICA MODELOS ATOMICOS Y TABLA PERIODICA El mundo que hoy habitamos tiene infinidades de elementos que lo conforman, los océanos, la tierra, una mesa o hasta nosotros mismos estamos formados por
ENSAYO QUIMICA MODELOS ATOMICOS Y TABLA PERIODICA El mundo que hoy habitamos tiene infinidades de elementos que lo conforman, los océanos, la tierra, una mesa o hasta nosotros mismos estamos formados por
ETIMOLOGÍA DEL ÁTOMO. A = Sin Tomo = División TEORÍAS Y MODELOS ATÓMICOS
 ETIMOLOGÍA DEL ÁTOMO A = Sin Tomo = División TEORÍAS Y MODELOS ATÓMICOS 1. TEORÍA GRIEGA: En Grecia los pensadores filósofos por año 460 a. C. fueron los primeros en hablar que todos los cuerpos estaban
ETIMOLOGÍA DEL ÁTOMO A = Sin Tomo = División TEORÍAS Y MODELOS ATÓMICOS 1. TEORÍA GRIEGA: En Grecia los pensadores filósofos por año 460 a. C. fueron los primeros en hablar que todos los cuerpos estaban
Problemas de Química (1ero Grado de Química). Tema 2. ESTRUCTURA ATÓMICA Y PROPIEDADES PERIÓDICAS
 Problemas de Química (1ero Grado de Química). Tema 2. ESTRUCTURA ATÓMICA Y PROPIEDADES PERIÓDICAS 1. Para el isótopo del elemento con Z = 36 y número másico 84 indique: (a) su número de protones; (b) su
Problemas de Química (1ero Grado de Química). Tema 2. ESTRUCTURA ATÓMICA Y PROPIEDADES PERIÓDICAS 1. Para el isótopo del elemento con Z = 36 y número másico 84 indique: (a) su número de protones; (b) su
El resultado es el Sistema Periódico. -En el sistema periódico los elementos están colocados por orden creciente de su número atómico (Z).
 Tema 2. La Tabla periódica -Desde hace tiempo los químicos han intentado ordenar los elementos de forma que queden agrupados aquellos que tienen propiedades químicas similares El resultado es el Sistema
Tema 2. La Tabla periódica -Desde hace tiempo los químicos han intentado ordenar los elementos de forma que queden agrupados aquellos que tienen propiedades químicas similares El resultado es el Sistema
Capítulo 2. Átomos, moléculas y iones
 Capítulo 2 Átomos, moléculas y iones En este capítulo se estudian los conceptos de átomos, moléculas y iones: la construcción de bloques de toda materia. Al terminar este capítulo, el estudiante podrá:
Capítulo 2 Átomos, moléculas y iones En este capítulo se estudian los conceptos de átomos, moléculas y iones: la construcción de bloques de toda materia. Al terminar este capítulo, el estudiante podrá:
Hecho por: Patricia Arroyo Gamallo nº 2 4ºeso C
 Hecho por: Patricia Arroyo Gamallo nº 2 4ºeso C La materia es todo aquello que tiene masa, ocupa un lugar en el espacio y es cuantificable (se puede medir).la Química es la ciencia que estudia su naturaleza,
Hecho por: Patricia Arroyo Gamallo nº 2 4ºeso C La materia es todo aquello que tiene masa, ocupa un lugar en el espacio y es cuantificable (se puede medir).la Química es la ciencia que estudia su naturaleza,
Colegio CEMEP Proyecto Nº 2 Química. 1º Media. Enero-Febrero Profesor Melvyn García
 Colegio CEMEP Proyecto Nº 2 Química. 1º Media. Enero-Febrero Profesor Melvyn García Propósito 1 Analizar la teoría atómica y el átomo como partícula fundamental de la materia. Qué es un modelo atómico?
Colegio CEMEP Proyecto Nº 2 Química. 1º Media. Enero-Febrero Profesor Melvyn García Propósito 1 Analizar la teoría atómica y el átomo como partícula fundamental de la materia. Qué es un modelo atómico?
Radiación. Cuerpo Negro Espectros Estructura del Atomo Espectroscopia Efecto Doppler. L. Infante 1
 Radiación Cuerpo Negro Espectros Estructura del Atomo Espectroscopia Efecto Doppler L. Infante 1 Cuerpo Negro: Experimento A medida que el objeto se calienta, se hace más brillante ya que emite más radiación
Radiación Cuerpo Negro Espectros Estructura del Atomo Espectroscopia Efecto Doppler L. Infante 1 Cuerpo Negro: Experimento A medida que el objeto se calienta, se hace más brillante ya que emite más radiación
Ponte en forma 1.- Realiza las actividades que se te solicitan a continuación: a) Completa el siguiente cuadro:
 RESPUESTAS BLOQUE III Ponte en forma 1.- Realiza las actividades que se te solicitan a continuación: a) Completa el siguiente cuadro: Tipo de raciación Partículas Carga eléctrica Masa(uma) Alfa α +2 4
RESPUESTAS BLOQUE III Ponte en forma 1.- Realiza las actividades que se te solicitan a continuación: a) Completa el siguiente cuadro: Tipo de raciación Partículas Carga eléctrica Masa(uma) Alfa α +2 4
Problemario de Talleres de Estructura de la Materia. DCBI/UAM-I. Obra Colectiva del. / Revisión octubre del 2012 UNIDAD 2
 UNIDAD 2 CAPAS ELECTRÓNICAS Y TAMAÑO DE LOS ÁTOMOS, ENERGÍA DE IONIZACIÓN Y AFINIDAD ELECTRÓNICA 1.- De acuerdo al modelo atómico propuesto por la mecánica cuántica, consideras que tiene sentido hablar
UNIDAD 2 CAPAS ELECTRÓNICAS Y TAMAÑO DE LOS ÁTOMOS, ENERGÍA DE IONIZACIÓN Y AFINIDAD ELECTRÓNICA 1.- De acuerdo al modelo atómico propuesto por la mecánica cuántica, consideras que tiene sentido hablar
Modelo atómico de Dalton(1808)
 El átomo Modelos atómicos Como no se podían ver los átomos los científicos crearon modelos para describirlos, éstos fueron evolucionando a lo largo de la historia a medida que se descubrieron nuevas cosas.
El átomo Modelos atómicos Como no se podían ver los átomos los científicos crearon modelos para describirlos, éstos fueron evolucionando a lo largo de la historia a medida que se descubrieron nuevas cosas.
ALUMNO: AUTORA: Prof. Ma. Laura Sanchez
 ALUMNO: AUTORA: Prof. Ma. Laura Sanchez 1.1 Evolución de las teorías atómicas Desde la antigüedad se ha discutido acerca de cómo está formada la materia, especialmente si es infinitamente divisible, o
ALUMNO: AUTORA: Prof. Ma. Laura Sanchez 1.1 Evolución de las teorías atómicas Desde la antigüedad se ha discutido acerca de cómo está formada la materia, especialmente si es infinitamente divisible, o
Núcleo Atómico. El núcleo es una masa muy compacta formada por protones y neutrones.
 Núcleo Atómico Profesor: Robinson Pino H. 1 COMPONENTES DEL NÚCLEO ATÓMICO El núcleo es una masa muy compacta formada por protones y neutrones. PROTÓN PROTÓN(p + ) Es una partícula elemental con carga
Núcleo Atómico Profesor: Robinson Pino H. 1 COMPONENTES DEL NÚCLEO ATÓMICO El núcleo es una masa muy compacta formada por protones y neutrones. PROTÓN PROTÓN(p + ) Es una partícula elemental con carga
LA TABLA PERIÓDICA. 1
 LA TABLA PERIÓDICA. 1 Clasificación de Mendeleiev Clasificó lo 63 elementos conocidos utilizando el criterio de masa atómica creciente, ya que no se conocía el concepto de número atómico puesto que no
LA TABLA PERIÓDICA. 1 Clasificación de Mendeleiev Clasificó lo 63 elementos conocidos utilizando el criterio de masa atómica creciente, ya que no se conocía el concepto de número atómico puesto que no
PLAN DE EVALUACIÓN 2015
 PLAN DE EVALUACIÓN 2015 Año: 2015 Período: I Semestre Sub-sector: Química Nivel: NM1 Curso: I Medio Profesor: Alejandra Sotomaor A. Aprendizajes Esperados Indicadores Aprendizajes Evaluados Procedimientos
PLAN DE EVALUACIÓN 2015 Año: 2015 Período: I Semestre Sub-sector: Química Nivel: NM1 Curso: I Medio Profesor: Alejandra Sotomaor A. Aprendizajes Esperados Indicadores Aprendizajes Evaluados Procedimientos
La tabla periódica es la estrella orientadora para la exploración en el capo de la química, la física, la mineralogía y la técnica.
 SISTEMA PERIÓDICO DE LOS ELEMENTOS La tabla periódica es la estrella orientadora para la exploración en el capo de la química, la física, la mineralogía y la técnica. Niels Bohr Principio de exclusión
SISTEMA PERIÓDICO DE LOS ELEMENTOS La tabla periódica es la estrella orientadora para la exploración en el capo de la química, la física, la mineralogía y la técnica. Niels Bohr Principio de exclusión
Capacidad de combinación. Capacidad de combinación La última capa de electrones de un átomo, se le conoce como capa de electrones de valencia
 Capacidad de combinación Para los elementos representativos, se define que el número de electrones de valencia de un elemento es igual al de la familia a la que pertenece Y está relacionado a la manera
Capacidad de combinación Para los elementos representativos, se define que el número de electrones de valencia de un elemento es igual al de la familia a la que pertenece Y está relacionado a la manera
Las estructura electrónica de los átomos
 Las estructura electrónica de los átomos Al preguntarnos por las diferencias entre las propiedades químicas y físicas de los elementos, así como, su forma de enlazarse y la forma en la cual emiten o absorben
Las estructura electrónica de los átomos Al preguntarnos por las diferencias entre las propiedades químicas y físicas de los elementos, así como, su forma de enlazarse y la forma en la cual emiten o absorben
I. Relaciona la columna de la izquierda con la de la derecha escribiendo dentro del paréntesis la letra que corresponda a la respuesta correcta.
 AUTOEVALUACIÓN I. Relaciona la columna de la izquierda con la de la derecha escribiendo dentro del paréntesis la letra que corresponda a la respuesta correcta. 1.-Es un ejemplo de sustancia pura ( ) 2.-El
AUTOEVALUACIÓN I. Relaciona la columna de la izquierda con la de la derecha escribiendo dentro del paréntesis la letra que corresponda a la respuesta correcta. 1.-Es un ejemplo de sustancia pura ( ) 2.-El
Contenido. 3.- Carga nuclear efectiva y reactividad. 4.- Propiedades periódicas:
 LA TABLA PERIÓDICA Contenido Primeras clasificaciones periódicas. 1.1. Sistema periódico de Mendeleiev. 2.- La tabla periódica. 2.1. Ley de Moseley. 3.- Carga nuclear efectiva y reactividad. 4.- Propiedades
LA TABLA PERIÓDICA Contenido Primeras clasificaciones periódicas. 1.1. Sistema periódico de Mendeleiev. 2.- La tabla periódica. 2.1. Ley de Moseley. 3.- Carga nuclear efectiva y reactividad. 4.- Propiedades
LA LA ESTRUCTURA DE LA MATERIA. 1.-Desarrollo histórico del concepto de átomo. Teoría de Demócrito. Teoría de Dalton. Componentes del átomo
 ANEXO AL TEMA 4 LA LA ESTRUCTURA DE LA MATERIA 1.-Desarrollo histórico del concepto de átomo Teoría de Demócrito Teoría de Dalton Modelo actual Componentes del átomo Concepto de ión 2.-Elememtos y compuestos
ANEXO AL TEMA 4 LA LA ESTRUCTURA DE LA MATERIA 1.-Desarrollo histórico del concepto de átomo Teoría de Demócrito Teoría de Dalton Modelo actual Componentes del átomo Concepto de ión 2.-Elememtos y compuestos
5ª UNIDAD ELEMENTOS Y COMPUESTOS
 5ª UNIDAD ELEMENTOS Y COMPUESTOS 3º E.S.O. Grupo Apellidos: Nombre: INTRODUCCIÓN Comenzamos recordando los conceptos más importantes del tema anterior: Cómo son los átomos? Cómo están distribuidos los
5ª UNIDAD ELEMENTOS Y COMPUESTOS 3º E.S.O. Grupo Apellidos: Nombre: INTRODUCCIÓN Comenzamos recordando los conceptos más importantes del tema anterior: Cómo son los átomos? Cómo están distribuidos los
Ejercicios resueltos de 3º de E.S.O.
 Ejercicios resueltos de 3º de E.S.O. Estructura de la materia. Modelos atómicos Ejercicio resuelto nº 1 Si el número másico de un átomo es A = 30 y tiene 12 protones, calcula su número de neutrones. Resolución
Ejercicios resueltos de 3º de E.S.O. Estructura de la materia. Modelos atómicos Ejercicio resuelto nº 1 Si el número másico de un átomo es A = 30 y tiene 12 protones, calcula su número de neutrones. Resolución
ies menéndez tolosa 1 Escribe la combinación o combinaciones de números cuánticos correspondientes a: a) un electrón 1s y b) un electrón 4f.
 ies menéndez tolosa Escribe la combinación o combinaciones de números cuánticos correspondientes a: a) un electrón s y un electrón 4f. a) Un electrón s Situado en el er nivel n =, como es un orbital s
ies menéndez tolosa Escribe la combinación o combinaciones de números cuánticos correspondientes a: a) un electrón s y un electrón 4f. a) Un electrón s Situado en el er nivel n =, como es un orbital s
PROBLEMAS RESUELTOS SELECTIVIDAD ANDALUCÍA 2014
 PROBLEMAS RESUELTOS SELECTIVIDAD ANDALUCÍA 2014 QUÍMICA TEMA 2: LA ESTRUCTURA DEL ÁTOMO Junio, Ejercicio 2, Opción A Reserva 1, Ejercicio 2, Opción A Reserva 2, Ejercicio 3, Opción B Reserva 3, Ejercicio
PROBLEMAS RESUELTOS SELECTIVIDAD ANDALUCÍA 2014 QUÍMICA TEMA 2: LA ESTRUCTURA DEL ÁTOMO Junio, Ejercicio 2, Opción A Reserva 1, Ejercicio 2, Opción A Reserva 2, Ejercicio 3, Opción B Reserva 3, Ejercicio
MODELOS ATÓMICOS REALIZADO POR: NICOLÁS CASTELLANO SUÁREZ. Nº2, 4ºesoB. Física y Química
 MODELOS ATÓMICOS REALIZADO POR: NICOLÁS CASTELLANO SUÁREZ. Nº2, 4ºesoB Física y Química 2 Índice: Introducción..3 Modelo atómico de Dalton..4 Modelo atómico de Thomson.5 Modelo atómico de Rutherford..6
MODELOS ATÓMICOS REALIZADO POR: NICOLÁS CASTELLANO SUÁREZ. Nº2, 4ºesoB Física y Química 2 Índice: Introducción..3 Modelo atómico de Dalton..4 Modelo atómico de Thomson.5 Modelo atómico de Rutherford..6
CONTENIDO T1 EL ÁTOMO Y EL SISTEMA PERIÓDICO...3 T2 EL ENLACE QUÍMICO...7 T3 FORMULACIÓN Y NOMENCLATURA INORGÁNICA...13
 CONTENIDO T1 EL ÁTOMO Y EL SISTEMA PERIÓDICO...3 T2 EL ENLACE QUÍMICO...7 T3 FORMULACIÓN Y NOMENCLATURA INORGÁNICA...13 T4 REACCIONES QUÍMICAS: Cálculos, Energías y Velocidades...19 T5 ESTUDIO DEL MOVIMIENTO...25
CONTENIDO T1 EL ÁTOMO Y EL SISTEMA PERIÓDICO...3 T2 EL ENLACE QUÍMICO...7 T3 FORMULACIÓN Y NOMENCLATURA INORGÁNICA...13 T4 REACCIONES QUÍMICAS: Cálculos, Energías y Velocidades...19 T5 ESTUDIO DEL MOVIMIENTO...25
