1 o Bachillerato. II. QUÍMICA Sistemas Materiales Propiedades Coligativas. Prof. Jorge Rojo Carrascosa
|
|
|
- Amparo Ríos Herrera
- hace 5 años
- Vistas:
Transcripción
1 FÍSICA Y QUÍMICA 1 o Bachillerato I. FÍSICA II. QUÍMICA Sistemas Materiales Propiedades Coligativas Prof. Jorge Rojo Carrascosa
2 Índice general 1. SISTEMAS MATERIALES TIPOS DE SISTEMAS MATERIALES MAPA CONCEPTUAL SISTEMAS MATERIALES METODOS DE SEPARACIÓN METODOS DE SEPARACIÓN MECÁNICOS METODOS DE SEPARACIÓN FÍSICOS DISOLUCIONES FORMAS CUANTITATIVAS DE EXPRESAR LA CONCEN- TRACIÓN DE UNA DISOLUCIÓN PORCENTAJE EN MASA PORCENTAJE EN VOLUMEN GRAMOS POR LITRO FRACCIÓN MOLAR MOLARIDAD MOLALIDAD SOLUBILIDAD PROPIEDADES COLIGATIVAS DE LAS DISOLUCIONES PRESIÓN OSMÓTICA DISMINUCIÓN DE LA PRESIÓN DE VAPOR ASCENSO EBULLOSCÓPICO DESCENSO CRIOSCÓPICO PROBLEMAS RESUELTOS
3 Capítulo 1 SISTEMAS MATERIALES La materia presenta dos tipos de propiedades, las propiedades extensivas y las propiedades intensivas. Las propiedades extensivas dependen de la cantidad y forma de la materia. Por ejemplo: peso, volumen, longitud, energía potencial, calor,..., sin embargo, las propiedades intensivas tienen que ver más con la estructura química interna de la materia, como la temperatura, punto de fusión, punto de ebullición, calor específico, concentración, índice de refracción,... Las propiedades intensivas pueden servir para identificar y caracterizar una sustancia pura, es decir, aquella que está compuesta por un solo tipo de molécula, como, por ejemplo, el agua, que está formada solo por moléculas de agua (H 2 O), o el azúcar, que solo la conforman moléculas de sacarosa (C 12 H 22 O 11 ) TIPOS DE SISTEMAS MATERIALES Un sistema químico consiste en cualquier combinación de componentes químicos que es objeto de estudio y/o análisis con fines específicos. Los sistemas pueden ser abierto, cerrados o aislados. En química se denomina fase a toda materia o masa homogénea del sistema que estamos estudiando, por lo tanto, las sustancias puras y mezclas homogéneas, cada una constituye una sola fase, de aquí que puedan existir mezclas homogéneas o heterogénes dependiendo de la existencia de una o más fases respectivamente. La interfase es el medio que separa dos fases(puede ser monofásico, difásico, trifásico, etc.). Los componentes son las diferentes sustancias que están presentes en el sistema y los constituyentes son los diferentes elementos que forman las diferentes sustancias que dan lugar a un sistema químico. Una disolución de sal en agua, por ejemplo, es un sistema químico homogéneo (ve- 2
4 mos un fase) en el que los componentes son la sal y el agua y los constituyentes son el sodio, cloro, hidrógeno y oxígeno. Los componentes químicos de un sistema pueden presentarse en sus fases sólida, líquida o gaseosa. Un sistema no puede contener más de una fase gaseosa, pero sí puede tener varias fases líquidas y sólidas. Una aleación de cobre y níquel, por ejemplo, contiene dos fases sólidas; una mezcla de tetracloruro de carbono y agua tiene dos fases líquidas MAPA CONCEPTUAL SISTEMAS MATERIALES El siguiente mapa conceptual nos muestra como podemos distinguir y separar cualquier sistema químico. DEPARTAMENTO DE FÍSICA Y QUÍMICA 3
5 Figura 1.1: Sistemas materiales DEPARTAMENTO DE FÍSICA Y QUÍMICA 4
6 METODOS DE SEPARACIÓN En los métodos de separación mecánicos se suelen separar separar mezclas con componentes de gran tamaño. No existen cambios de fases en las mezclas, por ejemplo, el filtrado de una mezcla de agua y arena a través de un tamiz (tamizado). Sin embargo, en los métodos físicos se aprovechan las propiedades físicas de las mezclas para separar sus componentes (diferencias en el punto de ebullición o sublimación) y suelen darse cambios de fase. Por ejemplo, la destilación del alcohol que se separa de la mezcla fermentada de agua y fruta azucarada. Algunos métodos de separación son: METODOS DE SEPARACIÓN MECÁNICOS Filtración: este método consiste en hacer pasar el sistema formado por un sólido y un líquido a través de una pared porosa llamada filtro, que generalmente se coloca en un embudo. La fase sólida es retenida y el líquido atraviesa el filtro. Decantación: Permite separar un sólido de un líquido o dos líquidos que no se mezclen, o no miscibles, de diferente peso específico. La fase de mayor peso específico se deposita en el fondo del recipiento (sedimenta) y la otra sobrenada, facilitando la separación. Centrifugación: Se utilizan centrifugadoras para separar sólidos de líquidos. Al girar a gran velocidad la fase más densa, generalmente la sólida, se deposita en el fondo del recipiente y posteriormente se separa por decantación. Cristalización: Metodo de separación físico por medio del cual se separa un componente de una disolución liquida transfiriéndolo a la fase sólida en forma de cristales que precipitan. Se suelen preparar disoluciones a una temperatura para posteriomente ir enfriando lentamente para conseguir la precipitación de cristales METODOS DE SEPARACIÓN FÍSICOS Destilación: Consiste en calentar un líquido hasta que sus componentes más volátiles pasan a la fase de vapor y, a continuación, enfriar el vapor para recuperar dichos componentes en forma líquida por medio de la condensación. Cromatografía: es una técnica de separación de sustancias que se basa en las diferentes velocidades con que se mueve cada una de ellas a través de un medio poroso arrastradas por un disolvente en movimiento. DEPARTAMENTO DE FÍSICA Y QUÍMICA 5
7 1.2. DISOLUCIONES Una disolución es una mezcla homogénea de dos a más sustancias puras llamadas componentes de la disolución. Estos componentes reciben el nombre de soluto y disolvente, siendo el soluto el componente en menor proporción y el disolvente el componente que se encuentra en mayor proporción. Las disoluciones en las que el disolvente es el agua se conocen con el nombre de disoluciones acuosas. De manera cualitativa, podemos encontrar según la concentración de soluto disuelto las siguientes disoluciones: Disoluciones Diluidas: Concentración de soluto muy inferior a la máxima. Disoluciones Concentradas: Concentración cercana a la máxima admitida. Disoluciones Saturadas: Son aquellas en las que no se admite mayor cantidad de soluto en el disolvente,la concentración es máxima y dependedel disolvente y de las condiciones de presión y teemperatura FORMAS CUANTITATIVAS DE EXPRESAR LA CONCENTRACIÓN DE UNA DISOLUCIÓN En química, y muchas otras disciplinas científicas, es muy importante conocer la proporción relativa entre el soluto y la cantidad total de disolución, siendo esta proporción conocida como concentración. Por tanto, expresada matemáticamente, la concentración de una disolución de forma genérica vendrá dada por: cantidad de soluto Concentración = cantidad de disolución Cuantitativamente existen distintas formas de expresar la concentración, PORCENTAJE EN MASA Se define como la masa en gramos de soluto disueltos por cada 100 gramos de disolución. % masa = masa(g) soluto masa(g) soluto + masa(g) disolvente PORCENTAJE EN VOLUMEN Se define como el volumen de soluto o de disolvente, ambos expresados en ml, que hay en 100 ml de disolución. Se emplea en disoluciones de liquidos o gases puros. DEPARTAMENTO DE FÍSICA Y QUÍMICA 6
8 % vol = V (ml) soluto V (ml) disolvente 100 ó % vol = V (ml) disolución V (ml) disolución GRAMOS POR LITRO Se define como la masa en gramos de soluto que hay por cada litro de disolución. g/l = FRACCIÓN MOLAR masa(g) soluto V (L) disolución Se define como la relación del número de moles de soluto (o disolvente) y el número de moles totales de la disolución. La suma de las fracciones molares de todos los componentes es 1. x A = n A n A + n B MOLARIDAD Esta es la forma más común en Química para expresar la concentración de una disolución. Para saber aplicarla bien hay que referirnos a dos conceptos previos. Peso atómico o masa atómica relativa: Estas expresiones se corresponden con la razón de la masa media por átomo del elemento a 1/12 de la masa de un átomo de 12 C. El valor de cada elemento viene tabulado en el sistema periódico, así por ejemplo, para el C es 12 g/mol, para el O 2 32 g/mol, para el HCl es 36,5 g/mol,.... De igual forma, la unidad de masa atómica (u) (peso atómico o molecular) equivale a 1, kg. Mol: El mol es la unidad que mide la cantidad de sustancia en el S.I. de unidades, se define como la cantidad de sustancia (átomos, moléculas, iones,... ) que contiene tantos entidades como átomos hay exactamente en 12 gramos de carbono 12. El número de entidades elementales existentes en un mol es una constante que no depende del tipo de partícula considerado. Esta cantidad se llama número de avogadro, N A, y equivale a 6, El número de moles (n) de un elemento o compuesto presentes en una cantidad de sustancia de masa en gramos (m), es, n = m peso atómico o molecular(g/mol) DEPARTAMENTO DE FÍSICA Y QUÍMICA 7
9 Con estos dos conceptos, ya estamos en condiciones de conocer y aplicar correctamente el concepto de Molaridad. La Molaridad se define como el número de moles de soluto disueltos por litro de disolución. Matemáticamente, MOLALIDAD M = moles de soluto V (L) disolución Cantidad de soluto por cada kilogramo de disolvente. Es una magnitud independiente de la temperatura. m = 1.3. SOLUBILIDAD n soluto m disolvente (kg) La solubilidad es un concepto físico que mide la capacidad máxima para disolverse un soluto en un disolvente determinado y a una temperatura determinada. El concepto de solubilidad lleva implicito el termino de disolución saturada. Solubilidad (g soluto /100 g H 2 O) Disolución sobresaturada Disolución saturada Disolución diluida Temperatura (Kelvin) Solubilidad del KCl en H 2 O Como vemos en la gráfica de solubilidad del KCl en H 2 O podemos observar como la solubilidad depende de la temperatura y no sólo eso, también estamos en condiciones DEPARTAMENTO DE FÍSICA Y QUÍMICA 8
10 de entender los conceptos de disolución diluida o insaturada, disolución saturada y disolución sobresaturada. Cuando tenemos una disolución sobresaturada es cuando aparece un precipitado, es decir, la disolución contiene más soluto del que puede existir y por tanto, precipita. Hasta una disolución saturada tenemos tan sólo un estado, sin embargo al pasar a una disolución sobresaturada tenemos dos estados, el liquido con dos componentes (por ejemplo, KCl y H 2 O) y otro sólido (KCl). La concentración se suele expresar como, [s] moles litro o gramos litro Como hemos visto, la solubilidad depende de la Temperatura, pero también depende de la natureza del disolvente y del soluto, y de la presión. Por ejemplo, en agua se disuelve la sal pero no así el aceite. En general, la solubilidad de los sólidos en un líquido aumenta con el incremento de la temperatura pero sin embargo, la de los gases en un líquido, disminuye si se aumenta la temperatura. En la siguiente curva de solubilidad podemos ver como es la disolución de distintas sales en 100 gramos de agua. DEPARTAMENTO DE FÍSICA Y QUÍMICA 9
11 1.4. PROPIEDADES COLIGATIVAS DE LAS DI- SOLUCIONES Con la disolución, las propiedades de las sustancias que lo forman son diferentes a las que presentan cuando son sustancias puras. Se habla de propiedades coligativas cuando las disoluciones dependen exclusivamente de la concentración del soluto que forma la disolución. Existen cuatro propiedades: PRESIÓN OSMÓTICA La ósmosis es un fenómeno de difusión a través de una membrana semipermeable por donde pasan las moleculas de disolvente desde la disolución más diluida a la más concentrada. La difusión se mantiene hasta alcanzar el equilibrio osmótico entre ambas disoluciones. Las moléculas de soluto no puden atravesar la membrana semipermeable. Por tanto, se define la presión osmótica, π, como la presión que es necesaria aplicar a una disolución para detener el flujo de disolvente a través de una membrana semipermeable que la separa del disolvente puro. La presión osmótica es directamente proporcional a la concentración de la disolución, expresada en mol m 3 ; π = crt siendo R, la constante de los gases en unidades del S.I. y T la temperartura en Kelvin DISMINUCIÓN DE LA PRESIÓN DE VAPOR La presión de vapor es aquella que se encuentra en equilibrio entre la presión del gas y del líquido. Sin embargo, en una disolución, con soluto no volátil ni iónico, se observa un descenso relativo de la presión de vapor de la disolución respecto a la del disolvente puro directamente proporcional a la fracción molar del soluto. Esta ley es conocida como Ley de Raoult, p = p 0 p = χp 0 siendo p la disminución de la presión de vapor, p 0 la presión de vapor del disolvente puro, p la presión de vapor de la disolución y χ la fracción molar del soluto. DEPARTAMENTO DE FÍSICA Y QUÍMICA 10
12 ASCENSO EBULLOSCÓPICO La disminución de la presión de vapor provoca que para alcanzar el punto de ebullición (deben igualarse la presión de vapor y la atmosférica) sea necesario un mayor aporte de energía. Es decir, la temperatura de ebullición de la disolución es mayor que la del disolvente puro. T e = k e m donde T e es el ascenso ebulloscópico, m es la molalidad de la disolución y K e es la constante ebulloscópica del disolvente, sus unidades son K kg mol DESCENSO CRIOSCÓPICO De igual manera se produce una disminución del punto de fusión en la disolución ya que se necesita una menor temperatura para que el sistema se solidifique. T f = k c m donde T f es el descenso crioscópico, m es la molalidad de la disolución y K c es la constante crioscópica del disolvente, sus unidades son K kg mol 1. DEPARTAMENTO DE FÍSICA Y QUÍMICA 11
13 1.5. PROBLEMAS RESUELTOS 1. Se deja una disolución de KCl en un frasco, en el que, por estar mal cerrado, al cabo de unas semanas se produce un precipitado. Cómo es la disolución que hay sobre el precipitado? Al haberse formado un precipitado la disolución se encuentra saturada de cloruro potásico. 2. Si sabemos que a una determinada temperatura la solubilidad del cloruro de sodio en agua es de 35 g en 100 cm 3 y tenemos una disolución de cloruro de sodio a esa temperatura que contiene 352 g por litro de agua, cómo es la disolución? Para poder comparar nuestra disolución con la saturada, tenemos que cambiar las unidades. 35 g 100 cm 103 cm l = 350 g l En la comparación observamos que tenemos más cantidad de soluto en nuestra disolución que en la saturada, por tanto, está sobresaturada y se habrá formado un precipitado. 3. Un ácido hipocloroso concentrado de densidad 1,6 g/ml tiene una pureza del 90 %. Calcula: a) su concentración en g/l. b) Su molaridad. c) El volumen de esta disolución necesario para preparar 200 ml de una nueva disolución 0,1 M. P.m (HClO)=52,5 g/mol. a) A partir de los datos de densidad de la disolución podemos hallar la concentración en g/l del ácido. 1, 6 g ácido 1 ml ml l = 1440 g l b) Para hallar la molaridad hay que hallar primero el número de moles de ácido. Esto podemos hacerlo desde la concentración hallada en el apartado anterior. DEPARTAMENTO DE FÍSICA Y QUÍMICA 12
14 1440 g ácido 1 l 1 mol ácido 52, 5 g ácido = 2, 74 Molar c) Vamos a preparar una dilución, por tanto, la cantidad en moles que necesitamos para preparar esta nueva disolución es la misma cantidad que debemos recoger en el volumen que nos piden, es decir M A V A = M B V B V A = M B V B M A = 7, ml = 7, 3 l 4. En 40 g de agua se disuelven 5 g de H 2 S (Pm=34 g/mol). La densidad de la disolución formada es 1,08 g/cm3. Calcula: a) su concentración en tanto por ciento en masa. b) su molalidad. c) su molaridad. a) Al tener la masa de ambos, %masa = 5 g H 2 S 100 = 11, 11 % 45 g disolución b) Para hallar la molalidad hay que hallar primero el número de moles del ácido.n = 5 = 0, m = 0, 15 g ácido 0, 04 kg = 3, 67 molal c) Para hallar la molaridad tenemos que conocer cuál es el volumen de la disolución. d = m v v = m d = 45 1, 8 M = moles volumen(l) = 41, 66 cm3 = 3, 53 Molar 5. La presión de vapor del agua a 60 C es 149,4 mmhg. Si deseamos preparar una disolución donde la presión de vapor disminuya a 140 mmhg. Determine la masa de glucosa (C 6 H 12 O 6 ) que debe disolverse en 150 g de agua para lograr dicho efecto. Aplicando la Ley de Raoult podemos determinar la fracción molar de glucosa y posteriormente la masa de glucosa. DEPARTAMENTO DE FÍSICA Y QUÍMICA 13
15 P = χ g P 0 = n g (n g + n a ) P 0 n g = 0, 55 siendo 180 g/mol el peso molecular de la glucosa, nos queda una masa de, n = masa peso molecular m = 99 gramos 6. Si al disolver 20 g de urea (masa molar 60 g/mol) en 200 g de disolvente se observa que el punto de ebullición de la disolución es de 90 C, determine el punto de ebullición de un disolvente puro cuya constante ebulloscópica es 0,61 C/molal, Al añadir un soluto en un disolvente se produce un aumento del punto de ebullición. Matematicamente se expresa si la molalidad de la urea es, T = K e m T disolución T 0 disolvente = K e m m = 20/60 0, 2 = 1, 67 molal T 0 disolvente = T disolución K e m = 88, 98 o C DEPARTAMENTO DE FÍSICA Y QUÍMICA 14
DISOLUCIONES. Las disoluciones son mezclas homogéneas de dos o más sustancias (componentes) en proporciones variables.
 DISOLUCIONES Las disoluciones son mezclas homogéneas de dos o más sustancias (componentes) en proporciones variables. Soluto es la sustancia que se encuentra en menor proporción. Disolvente es la sustancia
DISOLUCIONES Las disoluciones son mezclas homogéneas de dos o más sustancias (componentes) en proporciones variables. Soluto es la sustancia que se encuentra en menor proporción. Disolvente es la sustancia
CLASIFICACIÓN DE LA MATERIA
 1. Clasificación de la materia por su aspecto CLASIFICACIÓN DE LA MATERIA La materia homogénea es la que presenta un aspecto uniforme, en la cual no se pueden distinguir a simple vista sus componentes.
1. Clasificación de la materia por su aspecto CLASIFICACIÓN DE LA MATERIA La materia homogénea es la que presenta un aspecto uniforme, en la cual no se pueden distinguir a simple vista sus componentes.
INTRODUCCIÓN DISOLUCIONES
 QUIMICA COMUN INTRODUCCIÓN DISOLUCIONES EBULLICIÓN V/S EVAPORACIÓN Ambos conceptos tienen relación con la presión de vapor. La presión de vapor es la fuerza que tienen las moléculas de un líquido para
QUIMICA COMUN INTRODUCCIÓN DISOLUCIONES EBULLICIÓN V/S EVAPORACIÓN Ambos conceptos tienen relación con la presión de vapor. La presión de vapor es la fuerza que tienen las moléculas de un líquido para
FyQ 1. IES de Castuera Bloque 2 Aspectos Cuantitativos de la Química Unidad Didáctica 2
 Física y Química 1º Bachillerato LOMCE FyQ 1 IES de Castuera Bloque 2 Aspectos Cuantitativos de la Química 2015 2016 Unidad Didáctica 2 Rev 01 Las Disoluciones. Métodos Actuales para el Análisis de Sustancias
Física y Química 1º Bachillerato LOMCE FyQ 1 IES de Castuera Bloque 2 Aspectos Cuantitativos de la Química 2015 2016 Unidad Didáctica 2 Rev 01 Las Disoluciones. Métodos Actuales para el Análisis de Sustancias
Tema 2: Disoluciones. Tipos de disoluciones. Composición de las disoluciones: formas de expresión. Diluciones. Propiedades coligativas.
 Tema 2: Disoluciones Tipos de disoluciones. Composición de las disoluciones: formas de expresión. Diluciones. Propiedades coligativas. Presión de vapor. Presión osmótica. Aumento ebulloscópico y descenso
Tema 2: Disoluciones Tipos de disoluciones. Composición de las disoluciones: formas de expresión. Diluciones. Propiedades coligativas. Presión de vapor. Presión osmótica. Aumento ebulloscópico y descenso
TEMA 3 LAS DISOLUCIONES
 TEMA 3 LAS DISOLUCIONES 1.- DISOLUCIÓN: COMPONENTES Y TIPOS DE DISOLUCIONES 1.1- EL PROCESO DE DISOLUCIÓN - FACTORES QUE AFECTAN AL PROCESO DE DISOLUCIÓN 1.2-LA CONCENTRACIÓN - % EN MASA -% EN VOLUMEN
TEMA 3 LAS DISOLUCIONES 1.- DISOLUCIÓN: COMPONENTES Y TIPOS DE DISOLUCIONES 1.1- EL PROCESO DE DISOLUCIÓN - FACTORES QUE AFECTAN AL PROCESO DE DISOLUCIÓN 1.2-LA CONCENTRACIÓN - % EN MASA -% EN VOLUMEN
Tema 4: Sustancias puras y mezclas
 Tema 4: Sustancias puras y mezclas Esquema de trabajo: 1. Sustancias puras: Tipos: elementos y compuestos. 2. Mezclas: Tipos: Homogénea y heterogénea 3. Disoluciones Concepto Componentes Tipos de disoluciones
Tema 4: Sustancias puras y mezclas Esquema de trabajo: 1. Sustancias puras: Tipos: elementos y compuestos. 2. Mezclas: Tipos: Homogénea y heterogénea 3. Disoluciones Concepto Componentes Tipos de disoluciones
Tema 2: Disoluciones. Tipos de disoluciones. Composición de las disoluciones: formas de expresión. Diluciones. Propiedades coligativas.
 Tema 2: Disoluciones Tipos de disoluciones. Composición de las disoluciones: formas de expresión. Diluciones. Propiedades coligativas. Presión de vapor. Presión osmótica. Aumento ebulloscópico y descenso
Tema 2: Disoluciones Tipos de disoluciones. Composición de las disoluciones: formas de expresión. Diluciones. Propiedades coligativas. Presión de vapor. Presión osmótica. Aumento ebulloscópico y descenso
Universidad de La Frontera Fac. Ing.Cs. y Adm. Dpto. Cs. Químicas. Soluciones. Prof. Josefina Canales
 Universidad de La Frontera Fac. Ing.Cs. y Adm. Dpto. Cs. Químicas Soluciones Prof. Josefina Canales Una disolución es una mezcla homogénea de dos o más sustancias. Soluto El más pequeño (en masa) de los
Universidad de La Frontera Fac. Ing.Cs. y Adm. Dpto. Cs. Químicas Soluciones Prof. Josefina Canales Una disolución es una mezcla homogénea de dos o más sustancias. Soluto El más pequeño (en masa) de los
III. D ISOLU L CIONES E
 III. DISOLUCIONES III. DISOLUCIONES Índice 1. Disoluciones 2. Solubilidad 3. Factores que favorecen la disolución de las sustancias 4. Propiedades coligativas de las disoluciones 5. Suspensiones y disoluciones
III. DISOLUCIONES III. DISOLUCIONES Índice 1. Disoluciones 2. Solubilidad 3. Factores que favorecen la disolución de las sustancias 4. Propiedades coligativas de las disoluciones 5. Suspensiones y disoluciones
El aire de la atmósfera (78% N 2 ; 21% O 2 ; 1% Ar, He, CO 2 y vapor de agua) y el agua del mar son ejemplos de soluciones.
 SOLUCIONES la materia se presenta, con mayor frecuencia, en forma de mezcla de sustancias puras. dentro de éstas mezclas hay que distinguir las: I) mezclas propiamente dichas II) y las soluciones. El aire
SOLUCIONES la materia se presenta, con mayor frecuencia, en forma de mezcla de sustancias puras. dentro de éstas mezclas hay que distinguir las: I) mezclas propiamente dichas II) y las soluciones. El aire
QUÍMICA APLICADA. TEMA 5. Sistemas dispersos. Ingeniería Técnica Naval
 Sistemas dispersos QUÍMICA APLICADA. TEMA 5 Ingeniería Técnica Naval 1 I. Introducción........................... II. Disoluciones.......................... 3 III. Solubilidad...........................
Sistemas dispersos QUÍMICA APLICADA. TEMA 5 Ingeniería Técnica Naval 1 I. Introducción........................... II. Disoluciones.......................... 3 III. Solubilidad...........................
M A T E R I A L E S SOLUCIONES
 M A T E R I A L E S SOLUCIONES I Componentes Mayor proporción solvente Menor proporción soluto Concentración: indica la cantidad de soluto presente en una dada cantidad de solvente o una dada cantidad
M A T E R I A L E S SOLUCIONES I Componentes Mayor proporción solvente Menor proporción soluto Concentración: indica la cantidad de soluto presente en una dada cantidad de solvente o una dada cantidad
PSU MÓDULO COMÚN QUÍMICA PROPIEDADES COLIGATIVAS
 DEPARTAMENTO DE CIENCIAS PSU_MÓDULO COMÚN DE QUÍMICA PSU MÓDULO COMÚN QUÍMICA PROPIEDADES COLIGATIVAS Corresponden a las nuevas propiedades del solvente, debido que el soluto altera al solvente puro en
DEPARTAMENTO DE CIENCIAS PSU_MÓDULO COMÚN DE QUÍMICA PSU MÓDULO COMÚN QUÍMICA PROPIEDADES COLIGATIVAS Corresponden a las nuevas propiedades del solvente, debido que el soluto altera al solvente puro en
Aprendizajes esperados
 Disoluciones II Aprendizajes esperados Identificar diluciones. Identificar los factores que afectan la solubilidad. Definir propiedades coligativas. Pregunta oficial PSU Al bajar gradualmente la temperatura,
Disoluciones II Aprendizajes esperados Identificar diluciones. Identificar los factores que afectan la solubilidad. Definir propiedades coligativas. Pregunta oficial PSU Al bajar gradualmente la temperatura,
UNIDAD EDUCATIVA COLEGIO SAN ANTONIO DEL TUY OCUMARE DEL TUY, ESTADO MIRANDA
 UNIDAD EDUCATIVA COLEGIO SAN ANTONIO DEL TUY OCUMARE DEL TUY, ESTADO MIRANDA CURSO: 4 TO AÑO PROFESOR: CARLOS M. LANDAETA H. GUÍA N 2: SOLUCIONES. UNIDADES DE CONCENTRACIÓN. LEY DE RAOULT Y PROPIEDADES
UNIDAD EDUCATIVA COLEGIO SAN ANTONIO DEL TUY OCUMARE DEL TUY, ESTADO MIRANDA CURSO: 4 TO AÑO PROFESOR: CARLOS M. LANDAETA H. GUÍA N 2: SOLUCIONES. UNIDADES DE CONCENTRACIÓN. LEY DE RAOULT Y PROPIEDADES
Tema 7. Las mezclas. Introducción
 Tema 7. Las mezclas Introducción Ya sabes que los sistemas materiales se pueden clasificar según su composición en sustancias puras y mezclas. Las sustancias puras son los elementos y los compuestos que
Tema 7. Las mezclas Introducción Ya sabes que los sistemas materiales se pueden clasificar según su composición en sustancias puras y mezclas. Las sustancias puras son los elementos y los compuestos que
SISTEMAS MATERIALES. Departamento de Física y Química 2º ESO
 SISTEMAS MATERIALES Departamento de Física y Química 2º ESO 0. Mapa conceptual MATERIA Sustancias puras Mezclas Heterogéneas Homogéneas Sistemas coloidales Técnicas de separación Disoluciones Soluto Disolvente
SISTEMAS MATERIALES Departamento de Física y Química 2º ESO 0. Mapa conceptual MATERIA Sustancias puras Mezclas Heterogéneas Homogéneas Sistemas coloidales Técnicas de separación Disoluciones Soluto Disolvente
RECAPITULACIÓN < ,5 ~ 107,5 ~ 104,5 ~ Ángulos
 QUIMICA COMUN RECAPITULACIÓN RECAPITULACIÓN RECAPITULACIÓN Ángulos 180 120 < 120 109,5 ~ 107,5 ~ 104,5 ~ RECAPITULACIÓN MOLÉCULAS TIPO GEOMETRÍA ÁNGULO DE ENLACE CO 2 / HCN AX 2 Lineal 180 BI 3 / AlCl
QUIMICA COMUN RECAPITULACIÓN RECAPITULACIÓN RECAPITULACIÓN Ángulos 180 120 < 120 109,5 ~ 107,5 ~ 104,5 ~ RECAPITULACIÓN MOLÉCULAS TIPO GEOMETRÍA ÁNGULO DE ENLACE CO 2 / HCN AX 2 Lineal 180 BI 3 / AlCl
1 UNIVERSIDAD DON BOSCO DEPARTAMENTO DE CIENCIAS BÁSICAS QUÍMICA GENERAL Y QUÍMICA I CICLO I-2009 UNIDAD 4: SOLUCIONES
 1 UNIVERSIDAD DON BOSCO DEPARTAMENTO DE CIENCIAS BÁSICAS QUÍMICA GENERAL Y QUÍMICA I CICLO I-2009 DISCUSIÓN DE PROBLEMAS Nº 4 UNIDAD 4: SOLUCIONES OBJETIVOS: El estudiante al finalizar esta discusión de
1 UNIVERSIDAD DON BOSCO DEPARTAMENTO DE CIENCIAS BÁSICAS QUÍMICA GENERAL Y QUÍMICA I CICLO I-2009 DISCUSIÓN DE PROBLEMAS Nº 4 UNIDAD 4: SOLUCIONES OBJETIVOS: El estudiante al finalizar esta discusión de
MEZCLAS Y DISOLUCIONES. Física y Química 3º de E.S.O. IES Isidra de Guzmán
 MEZCLAS Y DISOLUCIONES Física y Química 3º de E.S.O. IES Isidra de Guzmán Introducción Ya sabes que los sistemas materiales se pueden clasificar según su composición en sustancias puras y mezclas. Las
MEZCLAS Y DISOLUCIONES Física y Química 3º de E.S.O. IES Isidra de Guzmán Introducción Ya sabes que los sistemas materiales se pueden clasificar según su composición en sustancias puras y mezclas. Las
Tema 5: Disoluciones. (Químic General) Disoluciones 6 de noviembre de / 38
 Tema 5: Disoluciones Tipos de disoluciones. Concentración. Solubilidad de gases. Diagramas de fases de dos componentes. Propiedades coligativas: presión osmótica, disminución del punto de fusión y aumento
Tema 5: Disoluciones Tipos de disoluciones. Concentración. Solubilidad de gases. Diagramas de fases de dos componentes. Propiedades coligativas: presión osmótica, disminución del punto de fusión y aumento
Bioquímica Tema 2: Soluciones. Unidades Año: 2013
 TEMA 2: SOLUCIONES Al estudio de las soluciones se le asigna gran importancia, teniendo en cuenta que la mayoría de las reacciones químicas ocurren entre soluciones, particularmente en medios acuosos.
TEMA 2: SOLUCIONES Al estudio de las soluciones se le asigna gran importancia, teniendo en cuenta que la mayoría de las reacciones químicas ocurren entre soluciones, particularmente en medios acuosos.
CÁTEDRA: QUÍMICA GUÍA DE PROBLEMAS Nº6
 CÁTEDRA: QUÍMICA GUÍA DE PROBLEMAS Nº6 TEMA: PROPIEDADES COLIGATIVAS OBJETIVOS: Aplicar las propiedades coligativas para el cálculo de masas molares de solutos y de las propiedades físicas de las soluciones.
CÁTEDRA: QUÍMICA GUÍA DE PROBLEMAS Nº6 TEMA: PROPIEDADES COLIGATIVAS OBJETIVOS: Aplicar las propiedades coligativas para el cálculo de masas molares de solutos y de las propiedades físicas de las soluciones.
SOLUCIONARIO Guía Estándar Anual
 SOLUCIONARIO Guía Estándar Anual Disoluciones III: solubilidad y propiedades coligativas SGUICES045CB33-A16V1 Ítem Alternativa Habilidad 1 D Comprensión 2 B Reconocimiento 3 E Reconocimiento 4 D Reconocimiento
SOLUCIONARIO Guía Estándar Anual Disoluciones III: solubilidad y propiedades coligativas SGUICES045CB33-A16V1 Ítem Alternativa Habilidad 1 D Comprensión 2 B Reconocimiento 3 E Reconocimiento 4 D Reconocimiento
Profesor: Carlos Gutiérrez Arancibia
 Objetivo: Reconocer las propiedades coligativas de las disoluciones estableciendo comparaciones y diferencias entre el comportamiento del disolvente puro y de la disolución. Profesor: Carlos Gutiérrez
Objetivo: Reconocer las propiedades coligativas de las disoluciones estableciendo comparaciones y diferencias entre el comportamiento del disolvente puro y de la disolución. Profesor: Carlos Gutiérrez
LA MATERIA. - Masa - Volumen -Energía - Carga eléctrica. Propiedades generales
 TEMA 2 La Materia LA MATERIA Propiedades generales - Masa - Volumen -Energía - Carga eléctrica Propiedades características - Densidad - Punto de fusión - Punto de ebullición -Conductividad eléctrica -
TEMA 2 La Materia LA MATERIA Propiedades generales - Masa - Volumen -Energía - Carga eléctrica Propiedades características - Densidad - Punto de fusión - Punto de ebullición -Conductividad eléctrica -
Disoluciones y cálculos de concentraciones
 Disoluciones y cálculos de concentraciones Disoluciones Una disolución es una mezcla homogénea (los componentes no se pueden distinguir a simple vista) de dos o más sustancias en proporciones variables.
Disoluciones y cálculos de concentraciones Disoluciones Una disolución es una mezcla homogénea (los componentes no se pueden distinguir a simple vista) de dos o más sustancias en proporciones variables.
Disoluciones. Mezclas: Asociación de dos o más sustancias distintas.
 Mezclas: Asociación de dos o más sustancias distintas. Mezclas heterogéneas: en las que sus componentes no están uniformemente distribuidos y conservan sus propiedades individuales. Se clasifican como
Mezclas: Asociación de dos o más sustancias distintas. Mezclas heterogéneas: en las que sus componentes no están uniformemente distribuidos y conservan sus propiedades individuales. Se clasifican como
SOLUCIONES. Coordinadora de Enseñanza de Bioquímica y Biología Molecular. Fac. de Medicina. UNAM
 SOLUCIONES M. en C. Alicia Cea Bonilla Coordinadora de Enseñanza de Bioquímica y Biología Molecular. Fac. de Medicina. UNAM 1 Qué es una solución? Es una mezcla homogénea de dos o más sustancias. La sustancia
SOLUCIONES M. en C. Alicia Cea Bonilla Coordinadora de Enseñanza de Bioquímica y Biología Molecular. Fac. de Medicina. UNAM 1 Qué es una solución? Es una mezcla homogénea de dos o más sustancias. La sustancia
Todo lo que vemos es materia
 Todo lo que vemos es materia CLASIFICACIÓN DE LA MATERIA La materia se presenta en la naturaleza en forma de sustancias puras y mezclas, de modo que podemos establecer la siguiente clasificación: CLASIFICACIÓN
Todo lo que vemos es materia CLASIFICACIÓN DE LA MATERIA La materia se presenta en la naturaleza en forma de sustancias puras y mezclas, de modo que podemos establecer la siguiente clasificación: CLASIFICACIÓN
Disoluciones. Tema 8. Una disolución es una mezcla homogénea de dos o más sustancias. disolución
 Disoluciones Tema 8 Química General e Inorgánica A Una disolución es una mezcla homogénea de dos o más sustancias disolución soluto disolvente El soluto es la sustancia que se encuentra en menor cantidad
Disoluciones Tema 8 Química General e Inorgánica A Una disolución es una mezcla homogénea de dos o más sustancias disolución soluto disolvente El soluto es la sustancia que se encuentra en menor cantidad
PROPIEDADES COLIGATIVAS DE LAS SOLUCIONES
 PROPIEDADES COLIGATIVAS DE LAS SOLUCIONES Los estudios teóricos y experimentales han permitido establecer, que los líquidos poseen propiedades físicas características. Entre ellas cabe mencionar: la densidad,
PROPIEDADES COLIGATIVAS DE LAS SOLUCIONES Los estudios teóricos y experimentales han permitido establecer, que los líquidos poseen propiedades físicas características. Entre ellas cabe mencionar: la densidad,
Materia: es aquello que ocupa un lugar en el espacio y cuyas propiedades percibimos por los sentidos. Es diversa y discontinua.
 Sistemas materiales Materia: es aquello que ocupa un lugar en el espacio y cuyas propiedades percibimos por los sentidos. Es diversa y discontinua. Mezcla Heterogénea: unión de dos o más sustancias de
Sistemas materiales Materia: es aquello que ocupa un lugar en el espacio y cuyas propiedades percibimos por los sentidos. Es diversa y discontinua. Mezcla Heterogénea: unión de dos o más sustancias de
INSTITUCION EDUCATIVA LA PRESENTACION NOMBRE ALUMNA: CIENCIAS NATURALES Y EDUCACIÓN AMBIENTAL ASIGNATURA: QUÍMICA NOTA
 INDICADORES DE DESEMPEÑO INSTITUCION EDUCATIVA LA PRESENTACION NOMBRE ALUMNA: AREA : CIENCIAS NATURALES Y EDUCACIÓN AMBIENTAL ASIGNATURA: QUÍMICA NOTA DOCENTE: LEADY RODRIGUEZ TIPO DE GUIA: CONCEPTUAL
INDICADORES DE DESEMPEÑO INSTITUCION EDUCATIVA LA PRESENTACION NOMBRE ALUMNA: AREA : CIENCIAS NATURALES Y EDUCACIÓN AMBIENTAL ASIGNATURA: QUÍMICA NOTA DOCENTE: LEADY RODRIGUEZ TIPO DE GUIA: CONCEPTUAL
Materia. Mezclas Son aquellas que están formados por 2 o más sustancias.
 Qué es la materia? Materia Sustancias Puras Son aquellas que tienen una composición y propiedades DEFINIDAS. Mezclas Son aquellas que están formados por 2 o más sustancias. Elementos No se pueden separar
Qué es la materia? Materia Sustancias Puras Son aquellas que tienen una composición y propiedades DEFINIDAS. Mezclas Son aquellas que están formados por 2 o más sustancias. Elementos No se pueden separar
Propiedades de soluciones líquidas
 Soluciones Propiedades de soluciones líquidas Es una mezcla homogénea de dos o mas sustancias químicas tal que el tamaño molecular de la partículas sea inferior a 10-9 m. Cuando el tamaño de partícula
Soluciones Propiedades de soluciones líquidas Es una mezcla homogénea de dos o mas sustancias químicas tal que el tamaño molecular de la partículas sea inferior a 10-9 m. Cuando el tamaño de partícula
SUSTANCIA QUÍMICA mercurio oxígeno
 ELEMENTO O SUSTANCIA ELEMENTAL: Sustancia formada por un mismo tipo de átomos, por ejemplo: Hg, H 2, Cu, O 2 SUSTANCIA QUÍMICA mercurio oxígeno COMPUESTO O SUSTANCIA COMPUESTA: Sustancia formada por dos
ELEMENTO O SUSTANCIA ELEMENTAL: Sustancia formada por un mismo tipo de átomos, por ejemplo: Hg, H 2, Cu, O 2 SUSTANCIA QUÍMICA mercurio oxígeno COMPUESTO O SUSTANCIA COMPUESTA: Sustancia formada por dos
Propiedades de soluciones líquidas
 Propiedades de soluciones líquidas Dra. Patricia Satti, UNRN PROPIEDADES DE LAS SOLUCIONES Soluciones Es una mezcla homogénea de dos o mas sustancias químicas tal que el tamaño molecular de la partículas
Propiedades de soluciones líquidas Dra. Patricia Satti, UNRN PROPIEDADES DE LAS SOLUCIONES Soluciones Es una mezcla homogénea de dos o mas sustancias químicas tal que el tamaño molecular de la partículas
PROPIEDADES COLIGATIVAS DE LAS SOLUCIONES
 PROPIEDADES COLIGATIVAS DE LAS SOLUCIONES Propiedades Coligativas Son aquellas propiedades físicas de las soluciones que dependen más bien de la cantidad de soluto que de su naturaleza. Cuatro son las
PROPIEDADES COLIGATIVAS DE LAS SOLUCIONES Propiedades Coligativas Son aquellas propiedades físicas de las soluciones que dependen más bien de la cantidad de soluto que de su naturaleza. Cuatro son las
Soluciones y unidades de concentración
 MATERIA Soluciones y unidades de concentración MEZCLAS SISTEMAS HETEROGÉNEOS Leche Arena Sal y azúcar SISTEMAS HOMOGÉNEOS Sal en agua Aire Acero COMPUESTOS Agua Etanol Benceno SUSTANCIAS PURAS ELEMENTOS
MATERIA Soluciones y unidades de concentración MEZCLAS SISTEMAS HETEROGÉNEOS Leche Arena Sal y azúcar SISTEMAS HOMOGÉNEOS Sal en agua Aire Acero COMPUESTOS Agua Etanol Benceno SUSTANCIAS PURAS ELEMENTOS
Soluciones y unidades de concentración
 Soluciones y unidades de concentración Dra. Dra. Patricia Patricia Satti, Satti, UNRN UNRN MATERIA MEZCLAS SUSTANCIAS PURAS SISTEMAS HETEROGÉNEOS Leche Arena Sal y azúcar SISTEMAS HOMOGÉNEOS Sal en agua
Soluciones y unidades de concentración Dra. Dra. Patricia Patricia Satti, Satti, UNRN UNRN MATERIA MEZCLAS SUSTANCIAS PURAS SISTEMAS HETEROGÉNEOS Leche Arena Sal y azúcar SISTEMAS HOMOGÉNEOS Sal en agua
SOLUCIONES SOLIDA LIQUIDA GASEOSA. mezclas homogéneas de dos sustancias: SEGÚN EL ESTADO FISICO DEL SOLVENTE
 Soluciones SOLUCIONES mezclas homogéneas de dos sustancias: SOLUTO SOLVENTE SEGÚN EL ESTADO FISICO DEL SOLVENTE SOLIDA LIQUIDA GASEOSA Cuando un sólido se disuelve en un líquido las partículas que lo
Soluciones SOLUCIONES mezclas homogéneas de dos sustancias: SOLUTO SOLVENTE SEGÚN EL ESTADO FISICO DEL SOLVENTE SOLIDA LIQUIDA GASEOSA Cuando un sólido se disuelve en un líquido las partículas que lo
TEMA 3: MEZCLAS, DISOLUCIONES Y SUSTANCIAS PURAS
 TEMA 3: MEZCLAS, DISOLUCIONES Y SUSTANCIAS PURAS 1. LA MATERIA Y SU ASPECTO Los sistemas materiales, formados por una o varias sustancias, pueden clasificarse en: - Sistemas materiales heterogéneos: presentan
TEMA 3: MEZCLAS, DISOLUCIONES Y SUSTANCIAS PURAS 1. LA MATERIA Y SU ASPECTO Los sistemas materiales, formados por una o varias sustancias, pueden clasificarse en: - Sistemas materiales heterogéneos: presentan
EJERCIOS DE CONCENTRACIÓN DE SOLUCIONES
 Preuniversitario Liceo de Aplicación Química 4º 2010 Profesora Paola Lizama V. GUÍA 4: DISOLUCIONES EJERCIOS DE CONCENTRACIÓN DE SOLUCIONES 01.- Calcular la cantidad de sosa cáustica (NaOH) y de agua que
Preuniversitario Liceo de Aplicación Química 4º 2010 Profesora Paola Lizama V. GUÍA 4: DISOLUCIONES EJERCIOS DE CONCENTRACIÓN DE SOLUCIONES 01.- Calcular la cantidad de sosa cáustica (NaOH) y de agua que
QUÉ SON LAS DISOLUCIONES?
 LICEO FEMENINO MERCEDES NARIÑO IED ÁREA CIENCIAS NATURALES Y ED. AMBIENTAL- QUÍMICA GRADO 10 DISOLUCIONES DOCENTES: VERONICA PINZÓN - JUAN GABRIEL PERILLA Propósito General: Reconocer la presencia, comportamiento,
LICEO FEMENINO MERCEDES NARIÑO IED ÁREA CIENCIAS NATURALES Y ED. AMBIENTAL- QUÍMICA GRADO 10 DISOLUCIONES DOCENTES: VERONICA PINZÓN - JUAN GABRIEL PERILLA Propósito General: Reconocer la presencia, comportamiento,
MEZCLAS Y DISOLUCIONES - CUESTIONES Y EJERCICIOS
 MEZCLAS Y DISOLUCIONES - CUESTIONES Y EJERCICIOS Concentración de una disolución 1º.- Calcula la masa de nitrato de hierro (II), Fe(NO 3 ) 2, existente en 100 ml de disolución acuosa al 6 % en masa. Dato:
MEZCLAS Y DISOLUCIONES - CUESTIONES Y EJERCICIOS Concentración de una disolución 1º.- Calcula la masa de nitrato de hierro (II), Fe(NO 3 ) 2, existente en 100 ml de disolución acuosa al 6 % en masa. Dato:
PROPIEDADES COLIGATIVAS DE LAS SOLUCIONES
 PROPIEDADES COLIGATIVAS DE LAS SOLUCIONES Los estudios teóricos y experimentales han permitido establecer, que los líquidos poseen propiedades físicas características. Entre ellas cabe mencionar: la densidad,
PROPIEDADES COLIGATIVAS DE LAS SOLUCIONES Los estudios teóricos y experimentales han permitido establecer, que los líquidos poseen propiedades físicas características. Entre ellas cabe mencionar: la densidad,
QUÉ SON LAS DISOLUCIONES?
 LICEO FEMENINO MERCEDES NARIÑO IED ÁREA CIENCIAS NATURALES Y ED. AMBIENTAL- QUÍMICA GRADO 11 DISOLUCIONES Prof. Juan Gabriel Perilla Jiménez Propósito General: Reconocer la presencia, comportamiento, importancia
LICEO FEMENINO MERCEDES NARIÑO IED ÁREA CIENCIAS NATURALES Y ED. AMBIENTAL- QUÍMICA GRADO 11 DISOLUCIONES Prof. Juan Gabriel Perilla Jiménez Propósito General: Reconocer la presencia, comportamiento, importancia
TEMA 3: DISOLUCIONES
 TEMA 3: DISOLUCIONES 1. Las disoluciones Las disoluciones son mezclas homogéneas de dos o más sustancias. Esto quiere decir que cualquier porción que tomemos de ella tiene la misma composición y propiedades.
TEMA 3: DISOLUCIONES 1. Las disoluciones Las disoluciones son mezclas homogéneas de dos o más sustancias. Esto quiere decir que cualquier porción que tomemos de ella tiene la misma composición y propiedades.
Sustituir fotografía. Sustituir texto
 Soluciones Sustituir fotografía Sustituir texto Tipos de soluciones. Hidrólisis. Solubilidad y el efecto de la temperatura. Unidades de concentración: Expresiones físicas de concentración (%m/m, %m/v,
Soluciones Sustituir fotografía Sustituir texto Tipos de soluciones. Hidrólisis. Solubilidad y el efecto de la temperatura. Unidades de concentración: Expresiones físicas de concentración (%m/m, %m/v,
HOJA DE PROBLEMAS 5: ENUNCIADOS
 Tema: SISTEMAS DISPERSOS HOJA DE PROBLEMAS 5: ENUNCIADOS 1. ( ) Calcule la molaridad de un disolución preparada disolviendo 23.4 g de sulfato de sodio hasta obtener 125 ml de disolución. 2. ( ) Cuantos
Tema: SISTEMAS DISPERSOS HOJA DE PROBLEMAS 5: ENUNCIADOS 1. ( ) Calcule la molaridad de un disolución preparada disolviendo 23.4 g de sulfato de sodio hasta obtener 125 ml de disolución. 2. ( ) Cuantos
DISOLUCIONES. Finalmente se incluye un cuestionario on line para que alumno pruebe sus conocimientos.
 Introducción general Objetivos y destinatarios DISOLUCIONES El material está destinado como complemento de estudio en lo concerniente al tema Soluciones para alumnos que cursen Química en la Carrera de
Introducción general Objetivos y destinatarios DISOLUCIONES El material está destinado como complemento de estudio en lo concerniente al tema Soluciones para alumnos que cursen Química en la Carrera de
So S l o u l c u i c o i n o e n s e
 Soluciones SOLUCIONES mezclas homogéneas de dos sustancias: SOLUTO SOLVENTE SEGÚN EL ESTADO FISICO DEL SOLVENTE SOLIDA LIQUIDA GASEOSA Cuando un sólido se disuelve en un líquido las partículas que lo
Soluciones SOLUCIONES mezclas homogéneas de dos sustancias: SOLUTO SOLVENTE SEGÚN EL ESTADO FISICO DEL SOLVENTE SOLIDA LIQUIDA GASEOSA Cuando un sólido se disuelve en un líquido las partículas que lo
TEMA 2: LA MATERIA: CÓMO SE PRESENTA?
 TEMA 2: LA MATERIA: CÓMO SE PRESENTA? 1.- La materia: sustancias puras y mezclas. 1.1.- Recordatorio. 1.2.- Sustancias puras. 1.3.- Mezclas. 1.4.- Cómo distinguir un coloide de una mezcla homogénea. 2.-
TEMA 2: LA MATERIA: CÓMO SE PRESENTA? 1.- La materia: sustancias puras y mezclas. 1.1.- Recordatorio. 1.2.- Sustancias puras. 1.3.- Mezclas. 1.4.- Cómo distinguir un coloide de una mezcla homogénea. 2.-
EJERCICIOS RESUELTOS DISOLUCIONES
 EJERIIOS RESUELTOS DISOLUIONES 1.- Se disuelven 20 g de NaOH en 560 g de agua. alcula a) la concentración de la en % en masa y b) su molalidad. Ar(Na) 2. Ar(O)16. Ar(H)1. NaOH 20 a) % NaOH.100 % NaOH.100
EJERIIOS RESUELTOS DISOLUIONES 1.- Se disuelven 20 g de NaOH en 560 g de agua. alcula a) la concentración de la en % en masa y b) su molalidad. Ar(Na) 2. Ar(O)16. Ar(H)1. NaOH 20 a) % NaOH.100 % NaOH.100
QUIMICA Unidad N 1: - PARTE B SOLUCIONES MAGNITUDES ATÓMICO-MOLECULAR. Profesora Mercedes Caratini - QUIMICA- ET 28 REPÚBLICA FRANCESA
 QUIMICA Unidad N 1: - PARTE B SOLUCIONES MAGNITUDES ATÓMICO-MOLECULAR Profesora Mercedes Caratini - QUIMICA- ET 28 REPÚBLICA FRANCESA 1 SOLUCIONES Una solución es un sistema homogéneo, en el cual las partículas
QUIMICA Unidad N 1: - PARTE B SOLUCIONES MAGNITUDES ATÓMICO-MOLECULAR Profesora Mercedes Caratini - QUIMICA- ET 28 REPÚBLICA FRANCESA 1 SOLUCIONES Una solución es un sistema homogéneo, en el cual las partículas
PRÁCTICA # 01 PREPARACIÓN DE DISOLUCIONES
 REPÚBLICA BOLIVARIANA DE VENEZUELA MINISTERIO DEL PODER POPULAR PARA LA DEFENSA AVIACIÓN MILITAR VENEZOLANA U.E.A.M LIBERTADOR ASIGNATURA: QUÍMICA PROF(A): ANGÉLICA RODRÍGUEZ MARBELIS MELENDEZ CURSO: 4to
REPÚBLICA BOLIVARIANA DE VENEZUELA MINISTERIO DEL PODER POPULAR PARA LA DEFENSA AVIACIÓN MILITAR VENEZOLANA U.E.A.M LIBERTADOR ASIGNATURA: QUÍMICA PROF(A): ANGÉLICA RODRÍGUEZ MARBELIS MELENDEZ CURSO: 4to
TEMA 7. DISOLUCIONES Y PROPIEDADES COLIGATIVAS
 TEMA 7. DISOLUCIONES Y PROPIEDADES COLIGATIVAS 1. Una solución saturada A) Contiene más soluto que disolvente. B) Contiene más disolvente que soluto. C) Contiene el mismo número de moles de soluto que
TEMA 7. DISOLUCIONES Y PROPIEDADES COLIGATIVAS 1. Una solución saturada A) Contiene más soluto que disolvente. B) Contiene más disolvente que soluto. C) Contiene el mismo número de moles de soluto que
Repaso de Sistemas de concentración molar
 Repaso de Sistemas de concentración molar Prof. José A. Pérez Química Analítica 1 Unidades de Concentración molaridad, molalidad, % masa, % volumen, %masa/volumen, partes por mil (ppmil), partes por millón
Repaso de Sistemas de concentración molar Prof. José A. Pérez Química Analítica 1 Unidades de Concentración molaridad, molalidad, % masa, % volumen, %masa/volumen, partes por mil (ppmil), partes por millón
La materia se puede definir como todo aquello que tiene masa y ocupa un volumen.
 Tema 2: LA MATERIA Que es la materia? La materia se puede definir como todo aquello que tiene masa y ocupa un volumen. Clasificación de la materia (criterio: separación) Mezclas Sustancias puras Composición
Tema 2: LA MATERIA Que es la materia? La materia se puede definir como todo aquello que tiene masa y ocupa un volumen. Clasificación de la materia (criterio: separación) Mezclas Sustancias puras Composición
LOGO. Soluciones. M. C. Rita Paz Samaniego
 LOGO Soluciones M. C. Rita Paz Samaniego Contenido Qué es una solución Terminología de solubilidad Solubilidad de compuestos Unidades de concentración de soluciones Qué es una solución? Una solución es
LOGO Soluciones M. C. Rita Paz Samaniego Contenido Qué es una solución Terminología de solubilidad Solubilidad de compuestos Unidades de concentración de soluciones Qué es una solución? Una solución es
UNIVERSIDAD DE CÓRDOBA FACULTAD DE EDUCACIÓN Y CIENCIAS HUMANAS LICENCIATURA EN CIENCIAS NATURALES Y EDUCACION AMBIENTAL V SEMESTRE
 Química Analítica UNIVERSIDAD DE CÓRDOBA FACULTAD DE EDUCACIÓN Y CIENCIAS HUMANAS LICENCIATURA EN CIENCIAS NATURALES Y EDUCACION AMBIENTAL V SEMESTRE 2015 Una solución es una mezcla homogénea de dos o
Química Analítica UNIVERSIDAD DE CÓRDOBA FACULTAD DE EDUCACIÓN Y CIENCIAS HUMANAS LICENCIATURA EN CIENCIAS NATURALES Y EDUCACION AMBIENTAL V SEMESTRE 2015 Una solución es una mezcla homogénea de dos o
Para la solución de algunos de los ejercicios propuestos, se adjunta una parte del sistema periódico hasta el elemento Nº 20.
 Programa Estándar Anual Nº Guía práctica Disoluciones I: mezclas, disoluciones y unidades porcentuales de concentración Ejercicios PSU Para la solución de algunos de los ejercicios propuestos, se adjunta
Programa Estándar Anual Nº Guía práctica Disoluciones I: mezclas, disoluciones y unidades porcentuales de concentración Ejercicios PSU Para la solución de algunos de los ejercicios propuestos, se adjunta
Por qué es importante conocer. componentes de una disolución química?
 Por qué es importante conocer la proporción de los componentes de una disolución química? Qué será más conveniente cuando calentamos agua para cocinar algún alimento: agregar sal antes o después que hierva
Por qué es importante conocer la proporción de los componentes de una disolución química? Qué será más conveniente cuando calentamos agua para cocinar algún alimento: agregar sal antes o después que hierva
Departamento Ciencias. Física y Química MATERIA. se clasifica en. SUSTANCIAS PURAS pueden ser. por métodos. físicos originan. Compuestos.
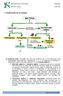 1. Clasificación de la materia MATERIA se clasifica en MEZCLAS pueden ser por métodos físicos originan SUSTANCIAS PURAS pueden ser Heterogéneas Homogéneas Compuestos como las Disoluciones formados por
1. Clasificación de la materia MATERIA se clasifica en MEZCLAS pueden ser por métodos físicos originan SUSTANCIAS PURAS pueden ser Heterogéneas Homogéneas Compuestos como las Disoluciones formados por
Profesor: Carlos Gutiérrez Arancibia
 Profesor: Carlos Gutiérrez Arancibia Temas a tratar: - Sustancias puras - Mezclas - Disoluciones - Procesos de Disoluciones - Solubilidad - Factores que afectan la solubilidad - Unidades de Concentraciones
Profesor: Carlos Gutiérrez Arancibia Temas a tratar: - Sustancias puras - Mezclas - Disoluciones - Procesos de Disoluciones - Solubilidad - Factores que afectan la solubilidad - Unidades de Concentraciones
UNIDAD DIDÁCTICA LA MATERIA
 UNIDAD DIDÁCTICA INTRODUCCIÓN LA MATERIA En esta unidad comenzamos el estudio de la Química. Es necesario recordar una serie de conceptos como son: - Densidad: cociente entre la masa de un cuerpo y el
UNIDAD DIDÁCTICA INTRODUCCIÓN LA MATERIA En esta unidad comenzamos el estudio de la Química. Es necesario recordar una serie de conceptos como son: - Densidad: cociente entre la masa de un cuerpo y el
Soluciones. Instituto Espíritu Santo Química. Diferentes estados de soluto y solventes
 Instituto Espíritu Santo Química Soluciones Las soluciones son sistemas homogéneos fraccionables formados por dos o más sustancias puras. Los componentes de una solución pueden estar en estado sólido,
Instituto Espíritu Santo Química Soluciones Las soluciones son sistemas homogéneos fraccionables formados por dos o más sustancias puras. Los componentes de una solución pueden estar en estado sólido,
TEMA 3: Composición de la Materia
 TEMA 3: Composición de la Materia 1. Mezclas homogéneas y heterogéneas Una mezcla es una composición de varias sustancias con distintas propiedades. Distinguimos dos tipos de mezclas: Mezclas homogéneas:
TEMA 3: Composición de la Materia 1. Mezclas homogéneas y heterogéneas Una mezcla es una composición de varias sustancias con distintas propiedades. Distinguimos dos tipos de mezclas: Mezclas homogéneas:
CONTENIDOS MÍNIMOS Y CRITERIOS DE EVALUACIÓN
 4 La materia: estados de agregación. Objetivos Observar el aspecto y otras características de la materia, en sus diversos estados de agregación: sólido, líquido y gaseoso. Distinguir y aplicar a ejercicios
4 La materia: estados de agregación. Objetivos Observar el aspecto y otras características de la materia, en sus diversos estados de agregación: sólido, líquido y gaseoso. Distinguir y aplicar a ejercicios
Fundamentos de Química. Horario de Tutorías
 Fundamentos de Química Segundo Cuatrimestre Horario de Tutorías Martes 12:00-14:00 16:00-19:00 Edificio 24B.Tercera Planta 14/02/2006 Tema 11: Propiedades de las disoluciones 11.1 Definición de disolución
Fundamentos de Química Segundo Cuatrimestre Horario de Tutorías Martes 12:00-14:00 16:00-19:00 Edificio 24B.Tercera Planta 14/02/2006 Tema 11: Propiedades de las disoluciones 11.1 Definición de disolución
PREPARACIÓN DE SOLUCIONES
 PRÁCTICA 4 PREPARACIÓN DE SOLUCIONES OBJETIVOS: Determinar las concentraciones físicas y químicas de las soluciones Preparar soluciones a partir de reactivos sólidos y líquidos I. FUNDAMENTO TEÓRICO. Las
PRÁCTICA 4 PREPARACIÓN DE SOLUCIONES OBJETIVOS: Determinar las concentraciones físicas y químicas de las soluciones Preparar soluciones a partir de reactivos sólidos y líquidos I. FUNDAMENTO TEÓRICO. Las
Apuntes Disoluciones
 Una disolución es una mezcla homogénea (los componentes no se pueden distinguir a simple vista) de dos a más sustancias. En las disoluciones hay que distinguir el soluto, el disolvente y la propia disolución
Una disolución es una mezcla homogénea (los componentes no se pueden distinguir a simple vista) de dos a más sustancias. En las disoluciones hay que distinguir el soluto, el disolvente y la propia disolución
Los átomos no se crean ni se destruyen en una reacción química, solo se redistribuyen.
 LEYES PONDERALES 1. Ley de conservación de la masa o de Lavoisier En cualquier reacción química que ocurra en un sistema cerrado, la masa total de las sustancias existentes se conserva. O lo que es lo
LEYES PONDERALES 1. Ley de conservación de la masa o de Lavoisier En cualquier reacción química que ocurra en un sistema cerrado, la masa total de las sustancias existentes se conserva. O lo que es lo
Clasificación de la materia
 Clasificación de la materia Sustancias Puras Son caracterizados por su composición y propiedades definidas y constantes bajo condiciones determinadas. Sustancias puras: Elementos Son sustancias puras formadas
Clasificación de la materia Sustancias Puras Son caracterizados por su composición y propiedades definidas y constantes bajo condiciones determinadas. Sustancias puras: Elementos Son sustancias puras formadas
DISOLUCIONES DILUIDAS IDEALES. LEY DE HENRY. MODELO DE LA DISOLUCIÓN DILUIDA IDEAL
 DISOLUCIONES DILUIDAS IDEALES. LEY DE HENRY. Muchas disoluciones se desvían bastante del modelo de disolución ideal. or ello resulta útil definir otro modelo: MODELO DE LA DISOLUCIÓN DILUIDA IDEAL 1) Descripción
DISOLUCIONES DILUIDAS IDEALES. LEY DE HENRY. Muchas disoluciones se desvían bastante del modelo de disolución ideal. or ello resulta útil definir otro modelo: MODELO DE LA DISOLUCIÓN DILUIDA IDEAL 1) Descripción
Tema 6: Disoluciones. Propiedades coligativas
 Tema 6: Disoluciones. Propiedades coligativas 1-Una solución saturada A) Contiene más soluto que solvente. B) Contiene más solvente que soluto. C) Contiene el mismo número de moles de soluto que de solvente.
Tema 6: Disoluciones. Propiedades coligativas 1-Una solución saturada A) Contiene más soluto que solvente. B) Contiene más solvente que soluto. C) Contiene el mismo número de moles de soluto que de solvente.
Solución. Propiedades Físicas de las Disoluciones. Tipos de soluciones (tabla 12.1) 8/20/2010. Mezcla homogénea de 2 ó mas sustancias
 8/2/21 Propiedades Físicas de las Disoluciones Basado en Capítulo 12 de Química (Chang, 9 na edición, 27) Ramón L. Hernández Castillo, Ph.D Solución Mezcla homogénea de 2 ó mas sustancias Soluto sustancia(s)
8/2/21 Propiedades Físicas de las Disoluciones Basado en Capítulo 12 de Química (Chang, 9 na edición, 27) Ramón L. Hernández Castillo, Ph.D Solución Mezcla homogénea de 2 ó mas sustancias Soluto sustancia(s)
1. MATERIA Y SU ASPECTO
 1. MATERIA Y SU ASPECTO El aspecto de un sistema material puede variar según el método de observación. Algunos sistemas materiales como la leche, la sangre o la mantequilla a simple vista parecen uniformes,
1. MATERIA Y SU ASPECTO El aspecto de un sistema material puede variar según el método de observación. Algunos sistemas materiales como la leche, la sangre o la mantequilla a simple vista parecen uniformes,
Teoría Disoluciones Fórmula empírica y molecular Física y Química. 1º bachiller DISOLUCIONES
 Teoría Disoluciones Fórmula empírica y molecular Física y Química. 1º bachiller 18-1-2015 CONCEPTO DE DISOLUCIÓN DISOLUCIONES Una disolución es una mezcla homogénea de sustancias en igual o distintos estados
Teoría Disoluciones Fórmula empírica y molecular Física y Química. 1º bachiller 18-1-2015 CONCEPTO DE DISOLUCIÓN DISOLUCIONES Una disolución es una mezcla homogénea de sustancias en igual o distintos estados
Escuela del Petróleo - Química
 Escuela del Petróleo - Química 2012 1 Unidad 2 1) Sistema Materiales 2) Materiales Homogéneos y Heterogéneos. a. Separación de las fases b. Sustancia Pura 3) extensivas e intensivas 4) Sistemas dispersos
Escuela del Petróleo - Química 2012 1 Unidad 2 1) Sistema Materiales 2) Materiales Homogéneos y Heterogéneos. a. Separación de las fases b. Sustancia Pura 3) extensivas e intensivas 4) Sistemas dispersos
DISOLUCIONES UNIDAD IV. Licda. Miriam Marroquín Leiva
 DISOLUCIONES UNIDAD IV 1 DISOLUCIÓN Es una mezcla homogénea de dos o más sustancias; el soluto y el disolvente. Es un término utilizado para describir un sistema en el cual una o más sustancias están mezcladas
DISOLUCIONES UNIDAD IV 1 DISOLUCIÓN Es una mezcla homogénea de dos o más sustancias; el soluto y el disolvente. Es un término utilizado para describir un sistema en el cual una o más sustancias están mezcladas
A continuación se detallan cada una de las propiedades coligativas:
 PREGUNTA (Técnico Profesional) Se prepara una solución con 2 mol de agua y 0,5 mol de un electrolito no volátil. Al respecto, cuál es la presión de vapor a 25 ºC de esta solución, si la presión del agua
PREGUNTA (Técnico Profesional) Se prepara una solución con 2 mol de agua y 0,5 mol de un electrolito no volátil. Al respecto, cuál es la presión de vapor a 25 ºC de esta solución, si la presión del agua
Química Analítica QQ 201 II PERIODO 2017 SECCIONES: 10am 11am. Ing. Alexis Rodríguez Horas de consulta: Lun-Mie: 11am-12pm
 Química Analítica QQ 201 II PERIODO 2017 SECCIONES: 10am 11am Ing. Alexis Rodríguez Horas de consulta: Lun-Mie: 11am-12pm OBJETIVO: Conocer los conceptos básicos de la química analítica y principios fundamentales
Química Analítica QQ 201 II PERIODO 2017 SECCIONES: 10am 11am Ing. Alexis Rodríguez Horas de consulta: Lun-Mie: 11am-12pm OBJETIVO: Conocer los conceptos básicos de la química analítica y principios fundamentales
TERMODINÁMICA DE SOLUCIONES Q.F. ALEX SILVA ARAUJO
 TERMODINÁMICA DE SOLUCIONES Q.F. ALEX SILVA ARAUJO SOLUCIÓN Sistema homogéneo constituido por 2 o más sustancias, cuya composición puede variar continuamente dentro de ciertos límites. Soluto: el o los
TERMODINÁMICA DE SOLUCIONES Q.F. ALEX SILVA ARAUJO SOLUCIÓN Sistema homogéneo constituido por 2 o más sustancias, cuya composición puede variar continuamente dentro de ciertos límites. Soluto: el o los
Disoluciones. Qué masa de KI necesitamos para preparar 500 ml de una disolución de KI 2.80 M? Pm KI volumen de KI moles KI gramos KI M KI
 Disoluciones La concentración de una disolución es la cantidad de soluto presente en una cantidad dad de disolvente o disolución. moles de soluto M = molaridad = litros de disolución Qué masa de KI necesitamos
Disoluciones La concentración de una disolución es la cantidad de soluto presente en una cantidad dad de disolvente o disolución. moles de soluto M = molaridad = litros de disolución Qué masa de KI necesitamos
INSTITUCION EDUCATIVA LA PRESENTACION
 INSTITUCION EDUCATIVA LA PRESENTACION NOMBRE ALUMNA: AREA : CIENCIAS NATURALES Y EDUCACION AMBIENTAL ASIGNATURA: QUIMICA DOCENTE: OSCAR GIRALDO HERNANDEZ TIPO DE GUIA: CONCEPTUAL - EJERCITACION PERIODO
INSTITUCION EDUCATIVA LA PRESENTACION NOMBRE ALUMNA: AREA : CIENCIAS NATURALES Y EDUCACION AMBIENTAL ASIGNATURA: QUIMICA DOCENTE: OSCAR GIRALDO HERNANDEZ TIPO DE GUIA: CONCEPTUAL - EJERCITACION PERIODO
Disoluciones químicas
 Disoluciones químicas Contenidos 1.- Las disoluciones. Clasificación. 2.- Concentración de una disolución 2.1. Porcentaje en masa (% en masa) 2.2. Porcentaje en volumen (% en volumen) 2.3. Concentración
Disoluciones químicas Contenidos 1.- Las disoluciones. Clasificación. 2.- Concentración de una disolución 2.1. Porcentaje en masa (% en masa) 2.2. Porcentaje en volumen (% en volumen) 2.3. Concentración
Apuntes Disoluciones. Fórmula empírica y molecular. Propiedades coligativas Física y Química. 1º bachiller
 Apuntes Disoluciones. Fórmula empírica y molecular. Propiedades coligativas Física y Química. 1º bachiller 27-10-2016 DISOLUCIONES CONCEPTO DE DISOLUCIÓN Una disolución es una mezcla homogénea de sustancias
Apuntes Disoluciones. Fórmula empírica y molecular. Propiedades coligativas Física y Química. 1º bachiller 27-10-2016 DISOLUCIONES CONCEPTO DE DISOLUCIÓN Una disolución es una mezcla homogénea de sustancias
Problemas resueltos de propiedades coligativas.
 Problemas resueltos de propiedades coligativas. Propiedades aditivas: las propiedades son aditivas cuando son iguales a la suma de los valores aislados de sus componentes Propiedades constitutivas: una
Problemas resueltos de propiedades coligativas. Propiedades aditivas: las propiedades son aditivas cuando son iguales a la suma de los valores aislados de sus componentes Propiedades constitutivas: una
HOJA DE PROBLEMAS 1: ENUNCIADOS
 Tema: DISOLUCIONES HOJA DE PROBLEMAS 1: ENUNCIADOS 1. ( ) Una disolución acuosa de AgNO 3 con una composición del 12 % en peso tiene una densidad de 1.1080 g/cm 3 a 20 C y 1 atm. Calcule la fracción molar,
Tema: DISOLUCIONES HOJA DE PROBLEMAS 1: ENUNCIADOS 1. ( ) Una disolución acuosa de AgNO 3 con una composición del 12 % en peso tiene una densidad de 1.1080 g/cm 3 a 20 C y 1 atm. Calcule la fracción molar,
TEMA 6 MEZCLAS Y DISOLUCIONES
 TEMA 6 MEZCLAS Y DISOLUCIONES 1 Contenidos: 1. Tipos de disoluciones 2. El proceso de disolución 3. Formas de expresar la concentración. 4. Solubilidad. Factores que afectan a la solubilidad 5. Propiedades
TEMA 6 MEZCLAS Y DISOLUCIONES 1 Contenidos: 1. Tipos de disoluciones 2. El proceso de disolución 3. Formas de expresar la concentración. 4. Solubilidad. Factores que afectan a la solubilidad 5. Propiedades
Unidad III CLASE Nº 4. Propiedades Coligativas
 UNIVERSIDD NCIONL EXPERIMENTL POLITECNIC NTONIO JOSÉ DE SUCRE VICERRECTORDO RQUISIMETO DEPRTMENTO DE INGENIERÍ QUÍMIC QUÍMIC GENERL Unidad III CLSE Nº 4 Preparación de soluciones y Propiedades Coligativas
UNIVERSIDD NCIONL EXPERIMENTL POLITECNIC NTONIO JOSÉ DE SUCRE VICERRECTORDO RQUISIMETO DEPRTMENTO DE INGENIERÍ QUÍMIC QUÍMIC GENERL Unidad III CLSE Nº 4 Preparación de soluciones y Propiedades Coligativas
MOL. Nº AVOGADRO DISOLUCIONES. TEMA 4 Pág. 198 libro (Unidad 10)
 MOL. Nº AVOGADRO DISOLUCIONES TEMA 4 Pág. 198 libro (Unidad 10) CONCEPTOS PREVIOS Supuestos de Dalton Teoría atómica de Dalton Elementos consitudios por átomos, partícuals separads e indivisibles Átomos
MOL. Nº AVOGADRO DISOLUCIONES TEMA 4 Pág. 198 libro (Unidad 10) CONCEPTOS PREVIOS Supuestos de Dalton Teoría atómica de Dalton Elementos consitudios por átomos, partícuals separads e indivisibles Átomos
GUÍA DE EJERCICIOS DISOLUCIONES
 GUÍA DE EJERCICIOS DISOLUCIONES Área Química Resultados de aprendizaje Conocer el concepto de disolución y calcular la concentración de esta en ejercicios, de forma lógica. Contenidos 1. Definición de
GUÍA DE EJERCICIOS DISOLUCIONES Área Química Resultados de aprendizaje Conocer el concepto de disolución y calcular la concentración de esta en ejercicios, de forma lógica. Contenidos 1. Definición de
Tema 2: Disoluciones. Tipos de disoluciones. Composición de las disoluciones: formas de expresión. Diluciones. Propiedades coligativas.
 Tema 2: Disoluciones Tipos de disoluciones. Composición de las disoluciones: formas de expresión. Diluciones. Propiedades coligativas. Presión de vapor. Presión osmótica. Aumento ebulloscópico y descenso
Tema 2: Disoluciones Tipos de disoluciones. Composición de las disoluciones: formas de expresión. Diluciones. Propiedades coligativas. Presión de vapor. Presión osmótica. Aumento ebulloscópico y descenso
DISOLUCIONES. Líquido (H 2 O)
 DISOLUCIONES Una disolución es una mezcla homogénea (los componentes no se pueden distinguir a simple vista) de dos a más sustancias. En las disoluciones hay que distinguir el soluto, el disolvente y la
DISOLUCIONES Una disolución es una mezcla homogénea (los componentes no se pueden distinguir a simple vista) de dos a más sustancias. En las disoluciones hay que distinguir el soluto, el disolvente y la
2. Métodos de separación de los componentes de una mezcla.
 TEMA 3: Mezclas, disoluciones y sustancias puras. 1. Clasificación de la materia. 2. Métodos de separación de los componentes de una mezcla. 3. Disoluciones. a) Definición. b) Cómo se preparan. c) Concentración.
TEMA 3: Mezclas, disoluciones y sustancias puras. 1. Clasificación de la materia. 2. Métodos de separación de los componentes de una mezcla. 3. Disoluciones. a) Definición. b) Cómo se preparan. c) Concentración.
