CELDAS ELECTROQUIMICAS
|
|
|
- Mercedes Méndez Fidalgo
- hace 8 años
- Vistas:
Transcripción
1 CELDAS ELECTROQUIMICAS
2 CLASIFICACION DE LAS CELDAS CELDAS ELECTROQUIMICAS Son aquellas en las cuales la energía eléctrica que procede de una fuente externa provee reacciones químicas no espontáneas. CELDAS ELECTROLITICAS, GALVANICAS O VOLTAICAS Son aquellas en las cuales las reacciones químicas espontáneas producen energía eléctrica (electricidad) la cual sale a un circuito eléctrico.
3 Constituyentes de la celda Catodo,, sin importar el tipo de celda (electrolítica ó voltaica) se define como el electrodo en el cual se produce la reducción porque algunas especies ganan electrones. Este posee carga negativa y a el migran los iones o cargas positivas.
4 Anodo,, sin importar el tipo de celda (electrolítica ó voltaica) se define como el electrodo en el cual se produce la oxidación porque algunas especies pierden electrones. Este posee carga positiva y a el migran los iones o cargas negativas.
5 Puente salino: Es un tubo con un electrolito en un gel que está conectado a las dos semiceldas de una celda galvánica; el puente salino permite el flujo de iones, pero evita la mezcla de las disoluciones diferentes que podría permitir la reacción directa de los reactivos de la celda.
6
7 Modelo de celda
8 Una pila voltáica aprovecha la electricidad de una reacción química espontánea para encender una bombilla (foco). Las tiras de cinc y cobre, dentro de disoluciones de ácido sulfúrico diluido y sulfato de cobre respectivamente, actúan como electrodos.
9 Celda de Volta Semireacción de oxidación Zn(s) Zn 2+ (ac) + 2 e- Semireacción de reducción Cu 2+ (ac) + 2 e- Cu(s) Reacción global: Zn 2+ (ac) Cu 2+ (ac) + Zn(s) Cu(s) +
10 Notación para una celda Galvánica Zn(s) Zn 2+ (ac) Cu 2+ (ac) Cu(s) En esta notación la semicelda de oxidación, es decir donde va el ánodo siempre se coloca a la izquierda y la semicelda de reducción o cátodo se coloca a la derecha. Los dos electrodos están conectados eléctricamente por medio de un puente salino el cual se indica con dos barras.
11 Zn(s) Zn 2+ (ac) Cu 2+ (ac) Cu(s) anodo puente salino cátodo Los terminales de la celda están en los extremos en esta notación, y una sola barra vertical, indica un limite entre las dos fases, digamos entre un terminal sólido y la solución del electrodo.
12 Zn(s) Zn 2+ (ac) terminal del ánodo disolución límite de la fase Si uno tiene un electrodo donde uno de los componentes es un gas, como el caso del electrodo de hidrógeno:
13 Electrodo de H 2
14 Electrodo de Hidrógeno 2 H + (ac) +2 e- H 2 (g) notación para el hidrógeno: H + (ac) H 2 (g) Pt Para escribir este electrodo como un ánodo, simplemente se invierte la notación: Pt H 2 (g) H + (ac)
15 Electrodo de Hidrógeno
16 POTENCIAL ESTANDAR DE LOS ELECTRODOS Tensión eléctrica: se trata de V, y se mide en voltios (V) ó milivoltios (mv). Fuerza electromotriz o potencial de la celda: se trata de E, y de igual manera se mide en voltios (V) ó milivoltios (mv).
17 Fuerza electromotriz La Fuerza electromotriz (F.E.M.),es una característica de cada generador eléctrico, y se define como el trabajo que el generador realiza para pasar la unidad de carga positiva del polo negativo al positivo por el interior del generador. Esto se justifica en el hecho de que cuando circula esta unidad de carga positiva por el circuito exterior al generador, desde el polo positivo al negativo, al llegar a este polo negativo es necesario realizar un trabajo o sea, un consumo de energía (mecánica, química, etc,) para el transporte de dicha carga por el interior desde un punto de menor potencial (polo negativo) a otro de mayor potencial (polo positivo) La F.E.M. se mide en voltios lo mismo que el potencial eléctrico
18 Fuerza electromotriz Se define como fuerza electromotriz (fem) la máxima diferencia de potencial entre dos electrodos de una celda galvánica. E celda La fem de una celda es una medida entonces de la fuerza directriz de la reacción de la celda. Esta reacción se efectúa en la celda en semireacciones separadas:
19 fem contribución del ánodo cuyo valor depende de la semireacción de oxidación para perder electrones contribución del cátodo cuyo valor depende de la semireacción de reducción para ganar electrones A estas contribuciones las llamaremos: Potencial de oxidación y potencial de reducción
20 Celdas electroquímicas
21
22
23 E oxidación = - E reducción Consideremos la siguiente celda: Zn(s) Zn 2+ (ac) Cu 2+ (ac) Cu(s) La fem de esta celda es entonces la suma de los dos potenciales, oxidación n y reducción: Cu 2+ (ac) + Zn(s) Zn 2+ (ac) + Cu(s) E celda = E Cu + (- E Zn ) = E Cu -E Zn es decir: E celda = E cátodo E ánodo
24 Potenciales estándares del electrodo (fem estándar) E celda o La fem estándar ( ): de una celda galvánica que opera bajo condiciones de estado estándar (concentraciones de soluto son cada una 1 M, presión de gas 1 atm, temperatura especificada, usualmente 25 C).
25 Los potenciales estándar de las semireacciones, no son valores absolutos sino que tienen referencia. Por convención, la referencia escogida es el electrodo estándar de hidrógeno. Por convención internacional para el electrodo de H 2 : H + (ac) H 2 (g) Pt 2 H e- H 2 (g, 1atm) E o = 0 V
26 Si uno desea escribir entonces los potenciales estándares de otras semireacciones, debe escribir la celda anterior como un ánodo, es decir el electrodo de hidrógeno será el ánodo: Pt, H 2 (g, 1 atm) H + (1 M) otra celda (ánodo) (cátodo)
27 Ejemplo: Midiendo el potencial estándar de la pareja Cu 2+ /Cu E celda = E cátodo E ánodo E celda = E derecha E izquierda E celda = E Cu 2+ /Cu E H + /H E celda = E Cu 2+ /Cu 0.0 V E celda = V Este valor positivo del potencial estándar dice que los iones Cu 2+, son más fácilmente reducibles a Cu que los H + a H 2 (g).
28 Consideremos otro ejemplo: Pt, H 2 (g, 1 atm) H + (1 M) Zn 2+ (1M) Zn (s) E = V E celda = E Zn 2+ /Zn 0.0 V E celda = V El valor negativo del potencial estándar de electrodo nos dice que el Zn 2+ (ac) es más fácil reducirlo a Zn(s) que los H + a H 2 (g).
29
30
31 PREDICCION DE LA ESPONTANEIDAD DE UNA REACCION A PARTIR DE LA fem Trabajo eléctrico máximo de una celda galvánica se define como: W máximo = - n F x E celda sus unidades son: volt x coul (1 V = 1 J/C ó bien 1 J = 1 V x C) Este trabajo eléctrico está relacionado con el cambio de energía libre a través de la siguiente ecuación: o bien: ΔG = ω = n F ΔG = n F elec E celda E celda
32 Celdas para medir ph
33 Celdas k ps
34
35
36
37 1. Sí G < 0 la reacción procede espontáneamente, por tanto Ecelda es positivo. 2. Sí E celda es positivo, la reacción va de izquierda a derecha y se dice que es espontánea. 3. Sí Sí E celda es negativo, la reacción va de derecha a izquierda y se dice que es no espontánea. 4. Sí E celda es igual a cero, el sistema está en equilibrio. 5. Cuando la celda de reacción está escrita al revés, tanto G como Ecelda cambian de signo.
38 CALCULO DE CONSTANTES DE EQUILIBRIO A PARTIR DE LA fem La variación de energía libre, está relacionada con la constante de equilibrio a partir de la siguiente ecuación: ΔG = R T ln K eq Sí combinamos esta ecuación con la de la de energía libre de la celda, tenemos: ΔG = n F E = R T ln celda K eq
39 de lo cual deducimos que: E o celda = R T ln K n F eq R = (L) (atm)/(gmol)(k) al sustituir los valores de R y F a 25 C tenemos la ecuación: o E celda = log K n Si tenemos una reacción, el cambio de energía libre, ΔG, está relacionado con el cambio de energía libre estándar ΔG, por la siguiente ecuación:
40 Si tenemos una reacción, el cambio de energía libre, G, está relacionado con el cambio de energía libre estándar G, por la siguiente ecuación: o ΔG = ΔG + R T ln Q donde Q es el cociente termodinámico de la reacción. Esta ecuación se puede aplicar a una celda galvánica. En este caso las concentraciones y las presiones del gas son las que existen en la celda en un instante determinado.
41 Sí se consideran: ΔG = n F o ΔG = n F E celda o E celda y estas ecuaciones se sustituyen en: o ΔG = ΔG + R T ln Q o n F Ecelda = n F Ecelda + R T ln Q
42 rearreglando nos queda: o bien: R T Ecelda = E o celda ln Q n F R T Ecelda = E o celda lg Q n F Sí se sustituye 298 K (25 C) en esta ecuación y se colocan los valores de R y F, nos quedará finalmente: Ecelda = E o celda lg Q n valores en volt
43 Ejemplo: Determine el E celda de la siguiente celda: Cátodo 2 [Fe 3+ (1 M) + e Fe 2+ (1 M)] Anodo Cu (s) Cu 2+ (1 M) + 2 e Cu (s) + 2 Fe 3+ (1 M) 2 Fe 2+ (1 M) + Cu 2+ (1 M)
44 E celda = E cátodo E ánodo E celda = E Fe 3+ /Fe 2+ E Cu 2+ /Cu E celda = = V ahora suponga: Cu (s) + 2 Fe 3+ (0.2 M) 2 Fe 2+ (0.1 M) + Cu 2+ (0.5 M) los datos son: E celda = V; n = 2 ; [Fe 2+ ]= 0.10 M; [Fe 3+ ]= 0.20 M; [Cu 2+ ]= 0.50 M
45 Ecelda = E o celda lg Q n E celda = lg [ ][ ] Cu Fe [ ] 3+ 2 Fe E celda = V
46 CELDAS DE CONCENTRACION Supongamos: Cátodo Cu 2+ (1 M) + 2 e Cu (s) Cu (s) Cu 2+ (1 M) + 2 e Cu 2+ (1 M) Cu 2+ (1 M)
47 E celda = E cátodo E ánodo E celda = E Cu 2+ /Cu E Cu 2+ /Cu E celda = = 0.00 V En este caso el problema es que hay uno de los electrodos que está al revés y por ello E da 0.0 V. Cuando se tengan similares concentraciones el resultado será el esperado.
48 Veamos la misma celda pero con otras concentraciones: Supongamos: Cu 2+ (1.5 M) + 2 e Cu 2+ (0.025 M) Nos piden E celda =? los datos son: E celda = 0.00 V Ecelda = E o celda lg n Q n = 2 [ 2+ Cu ] = [ Cu ] = Q
49 E celda = lg = V Una celda de concentración es aquella que contiene o puede contener un mismo tipo de iones en diferentes concentraciones.
50 Pilas o acumuladores
51
52
53 BATERIA ELECTRICA Se llama ordinariamente pila eléctrica a un dispositivo que genera energía eléctrica por un proceso químico transitorio, tras de lo cual cesa su actividad y han de renovarse sus elementos constituyentes, puesto que sus características resultan alteradas durante el mismo. Se trata de un generador primario. Esta energía resulta accesible mediante dos terminales que tiene la pila, llamados polos, electrodos o bornes. Uno de ellos es el polo positivo o ánodo y el otro es el polo negativo o cátodo.
54 BATERIA ELECTRICA También se usa incorrectamente como sinónimo de pila el término batería, la diferencia es que la pila no ha sido diseñada para poderse recargar y por el contrario, la batería si que puede considerarse un dispositivo recargable o acumulador eléctrico. En este caso, se trata de generadores eléctricos secundarios.
55 BATERIA ELECTRICA Tanto pila como batería son términos provenientes de los primeros tiempos de la electricidad, en los que se juntaban varios elementos o celdas (en el primer caso uno encima de otro, "apilados", y en el segundo adosados lateralamente, "en batería"), como se sigue haciendo actualmente, para así aumentar la magnitud de los fenómenos eléctricos y poder estudiarlos sistemáticamente. Las pilas actuales están formadas a veces por un único elemento (como sucede con las de 1,5 V que, por tanto, no son baterías en sentido estricto) y otras veces por un apilamiento o batería de ellos (caso de las de 9 V, p. ej., que constan de seis celdas).
56 BATERIA ELECTRICA La estructura fundamental de una pila consiste en piezas de dos metales diferentes introducidas en un líquido conductor de la electricidad o electrolito. El funcionamiento de una pila se basa en el potencial de contacto entre un metal y un electrolito, esto es, el potencial que se produce al poner en contacto un metal con un líquido.
57 PROPIEDADES ELECTRICAS DE UNA PILA Una vez fijada la tensión, la ley de Ohm determina la corriente que circulará por la carga y consecuentemente el trabajo que podrá realizarse, siempre naturalmente que esté dentro de las posibilidades de la pila, que no son infinitas, viniendo limitadas fundamentalmente por el tamaño de los electrodos (lo que determina el tamaño externo de la pila completa) y por su separación. Símbolo de una pila (izquierda); modelo eléctrico simplificado (centro); modelo más elaborado (derecha).
58 PROPIEDADES ELECTRICAS DE UNA PILA Estos condicionamientos físicos se representan en el modelo de generador como una resistencia interna por la que pasaría la corriente de un generador ideal, es decir, de uno que pudiese suministrar una corriente infinita al voltaje predeterminado. Conforme la célula se va gastando, su resistencia interna va aumentando, lo que hace que la tensión disponible sobre la carga vaya disminuyendo, hasta que resulte insuficiente para los fines deseados, momento en el que es necesario reemplazarla. Para dar una idea, una pila nueva de las ordinarias de 1,5 V tiene una resistencia interna de unos 0,35 Ω, mientras que una vez agotada puede tener varios.
59 PROPIEDADES ELECTRICAS DE UNA PILA Esta es la razón de que la mera medición de la tensión con un voltímetro no sirva para indicar el estado de una pila; en circuito abierto incluso una pila gastada puede indicar 1,4 V, dada la carga insignificante que representa la resistencia de entrada del voltímetro, pero, si la medición se hace con la carga que habitualmente soporte, la lectura bajará a 1,0 V o menos, momento en que esa pila ha dejado de tener utilidad. Las actuales pilas alcalinas tienen una curva de descarga más suave que las previas de carbón; su resistencia interna aumenta proporcionalmente más despacio.
60 Capacidad total La capacidad total de una pila se mide en amperios/hora (A h); es el número máximo de amperios que el elemento puede suministrar en una hora. Es cifra que no suele conocerse, ya que no es muy esclarecedora, por variar con la intensidad solicitada y con la temperatura. Cuando se extrae una gran corriente de manera continuada, la pila entrega menos potencia total que si la carga es más suave. También en esto las pilas alcalinas son mejores. Una de tipo D tiene una capacidad de entre 9 Ah (con una carga de 1 A) y 12 Ah (con una carga de 1 ma), mientras que los correspondientes valores para una de carbón-zinc son 1 y 7,5, respectivamente.
61 Las baterías secundarias o recargables Actualmente existen dos tipos de baterías recargables que dominan el mercado: las baterías de plomo y las de níquelcadmio. Las baterías de plomo reinan en nuestros automóviles pero sólo destinadas a cubrir las necesidades de arranque, iluminación e ignición (no tienen suficiente energía para mover el coche). Las baterías de níquel-cadmio a falta de mejores baterías, se emplean en artículos de electrónica de consumo como videocámaras y ordenadores o teléfonos móviles.
62 Que tecnología es la ideal para el desarrollo de nuevas baterías recargables?. En general, cada tecnología tiene características que se ajustan mejor a ciertas aplicaciones, y existen asimismo numerosos y variados tipos de baterías que se pueden considerar hoy en día en estado de desarrollo.
63 Baterías: Sodio/azufre Zinc/aire Hidruro metálico/óxido de níquel Baterías de litio Todas tienen ventajas e inconvenientes que se intentan evitar con diseños adecuados pero las baterías de litio, junto quizá a las de hidruro metálico son las que van encontrando un mayor consenso en cuanto a su potencial y un mayor esfuerzo en su investigación y desarrollo a nivel mundial.
64 Baterías de Litio Cuando un ánodo de litio metálico se combina con cátodos de ciertos óxidos de metales de transición las celdas electroquímicas reversibles que resultan presentan valores de voltaje superiores al de otros sistemas; ello contribuye a una alta densidad de energía. Además de sus características técnicas, la tecnología de litio es de las más versátiles y puede llegar a encontrar aplicaciones comerciales en muy distintos ámbitos, desde los que requieren pequeñas y delgadas microbaterías hasta baterías de alta capacidad y reducido peso para automóviles.
65 En las baterías de ion-litio el ánodo no está formado por litio metálico sino por otro material mucho más seguro, como por ejemplo el grafito, capaz de intercalar (o almacenar) iones de litio en una forma menos reactiva que la del litio metálico, sin un notable detrimento de su densidad energética.
66 Batería de litio La siguiente figura indica esquemáticamente el funcionamiento a nivel atómico de este tipo de baterías.
67 DURANTE LA DESCARGA: Los iones litio (amarillos) cambian espontáneamente del electrodo negativo (negro) al electrolito (azul) y de éste al electrodo positivo (rojo). El electrolito permite el paso de iones pero no de electrones. Al mismo tiempo, los electrones fluyen espontáneamente del electrodo negativo al positivo a través del único camino que les dejamos libre: a través de nuestro circuito eléctrico. A medida que avanza la descarga, el potencial (E) de cada electrodo cambia de forma que su diferencia disminuye y cae por tanto el voltaje de la celda (DeltaE) a medida que sacamos carga eléctrica (Q) de la batería.
68 DURANTE LA CARGA: Bombeamos electrones en el electrodo negativo y los extraemos del positivo. Hacemos por tanto el electrodo negativo más negativo y el positivo más positivo y aumentamos así la diferencia de potencial entre ellos, o, lo que es lo mismo, el voltaje de la celda. Este proceso fuerza también a los iones litio a salir del electrodo positivo y a intercalarse en el negativo.
69 Las baterías recargables de ión-litio que empiezan ya a aparecer en el mercado están compuestas de cátodos de Li- CoO 2, electrolitos poliméricos y ánodos de grafito altamente densificados y con poca superficie para minimizar los fenómenos de pasivación que también les afectan. Se pueden recargar hasta 2500 veces y gracias a su bajo precio constituyen la mejor alternativa en el mercado de la electrónica de consumo.
70
71
72
73
74
75
76 Aplicaciones de las reacciones REDOX Fotografía en blanco y negro Ag + Br - + luz Ag + Br 0 + e Ag+ + e Ag 0 OH O 2 Ag Ag 0 OH O O OH 2- SO 3 + SO 3 + H 2O O OH H+ OH - + H 2O AgBr + 2 Na 2S 2O 3 NaBr + Na 3Ag(S 2O 3) 2
77 Aplicaciones de las reacciones REDOX Combustible sólido: Propulsores sólidos para cohetes 12% aluminio en polvo 74% de perclorato de amonio 12% de un polímero aglutinante 8 Al 3 NH ClO 4AlO 3NH Cl
78 Aplicaciones de las reacciones REDOX Redox en un horno de fundición Para obtener el hierro metálico se debe separar del mineral del hierro, por lo general la hematita, Fe 2 O 3 Este proceso se lleva a cabo en un alto horno por medio de reacciones redox: CaCO 3 (s) CaO (s) + CO 2(g) CO (g) 2 + C(s) 2 CO(g) Fe (s) + 3O (s) + 3CO(g) 2Fe (l) + 3CO 2 (g)
79 Aplicaciones de las reacciones REDOX Detección de alcohol Se utiliza este método de oxidación de alcoholes primarios en la prueba del analizador del aliento H CH 3CH 2 OH + K 2Cr 2O7 R C + O rojo naranja H K Cr O O C OH Cr verde
80 FUNCIONAMIENTO
81 FUNCIONAMIENTO Así, al introducir una placa de zinc (Zn) en agua, el zinc se disuelve algo en forma de iones Zn ++ que pasan al líquido; esta emisión de iones hace que la placa adquiera una carga negativa respecto al líquido, pues tiene ahora un exceso de electrones, creándose entre ambos una diferencia de potencial. Los iones que están en el líquido ejercen una presión osmótica, que se opone a la continuación de la disolución, la cual se detendrá cuando se alcance un valor determinado, llamado tensión de disolución. Cuando se cierra el circuito externo, los electrones del zinc retornan a través de él al polo opuesto, mientras que en el interior del electrolito se reanuda la corriente de iones que circula en sentido contrario. La imagen precedente muestra el esquema electroquímico de una celda Daniell, que se describe luego con más detalle. (Incidentalmente, obsérvese que las denominaciones de ánodo y cátodo se utilizan sobre la base del flujo de electrones por el circuito externo y no en el sentido habitual, según el cual la corriente va del polo positivo al negativo.)
82 Características, propiedades y forma de utilización de las pilas Tensión, voltaje o fuerza electromotriz El voltaje que produce un elemento electroquímico viene determinado completamente por la naturaleza de las sustancias de los electrodos y del electrolito (o de los electrolitos), así como por su concentración. Walther Nernst obtuvo el premio Nobel de química de 1920 por haber formulado cuantitativamente y demostrado las leyes que rigen este fenómeno. La conexión de elementos en serie permite multiplicar esta tensión básica cuanto se quiera.
83 WALTHER NERNST Walther Nernst Walther Hermann Nernst (Briesen, Prusia, 25 de junio de Ober-Zibelle, Alemania, 18 de noviembre de 1941); fisico y químico alemán, premio Nobel de Química en Sus trabajos ayudaron a establecer la moderna física-química. Trabajó en los campos de la electroquímica, termodinámica, química del estado sólido y fotoquímica. Sus descubrimientos incluyen la ecuación de Nerst. Estudió en las universidades de Zürich, Berlín, Graz y Wurzburgo. Tras trabajar algún tiempo en Leipzig, desde 1891 ejerció como profesor de física en la Universidad de Gotinga, en donde, en 1895, fundó el Instituto de Química, Física y Electroquímica. Posteriormente, en 1905 se trasladó a la Universidad de Berlín como profesor y director del Instituto de Química Física de dicha universidad. En 1922 fue nombrado presidente del Instituto Fisicotécnico de Berlín-Charlottenburg, cargo que dejó en Desde entonces se dedicó al estudio de la electoacústica y astrofísica. Desarrolló el llamado "teorema del calor", según el cual la entropía de una materia tiende a anularse cuando su temperatura se aproxima al cero absoluto, y que constituye la tercera ley de la termodinámica. Por este desarrollo, en 1920 fue galardonado con el premio Nobel de Química. Desarrolló también una teoría osmótica para explicar y determinar el potencial de los electrodos de una pila de concentración y formuló la ley de distribución de una materia entre dos fases dadas. Inventó la llamada lámpara de Nernst, cuyo filamento (constituido por óxidos de circonio e itrio) se hace conductor al calentarse, pudiendo alcanzar temperaturas superiores en más de 1000 C a las de otras lámparas, más eficaz que las antiguas lámparas de arco de carbón y que suele emplearse como fuente de rayos infrarrojos. Inventó también una microbalanza así como un piano eléctrico, en el que utilizó amplifcadores de radio.
84 PROPIEDADES ELECTRICAS DE UNA PILA Las propiedades puramente eléctricas de una pila se representan mediante el modelo adjunto. En su forma más sencilla está formado por una fuente de tensión perfecta (es decir, con resistencia interna nula) en serie con un resistor que representa la resistencia interna. El condensador de la versión más compleja es enormemente grande y su carga simula la descarga de la pila. Además de ello entre los terminales también aparece una capacitancia, que no suele tener importancia en las aplicaciones de corriente continua.
Unidad 7. Reacciones de transferencia de electrones. Oxidación- Reducción. Ajuste de reacciones de oxidación-reducción.
 Unidad 7. Reacciones de transferencia de electrones. Oxidación- Reducción Concepto de oxidación-reducción Número de oxidación Ajuste de reacciones de oxidación-reducción. Estequiometría Electroquímica
Unidad 7. Reacciones de transferencia de electrones. Oxidación- Reducción Concepto de oxidación-reducción Número de oxidación Ajuste de reacciones de oxidación-reducción. Estequiometría Electroquímica
ELECTROQUÍMICA. 1. Procesos electroquímicos (pila). 2. Potenciales normales de electrodo. 3. Ecuación de Nernst. 4. Electrolisis. 5. Leyes de Faraday.
 ELECTROQUÍMICA 1. Procesos electroquímicos (pila). 2. Potenciales normales de electrodo. 3. Ecuación de Nernst. 4. Electrolisis. 5. Leyes de Faraday. Química 2º bachillerato Electroquímica 1 0. CONOCIMIENTOS
ELECTROQUÍMICA 1. Procesos electroquímicos (pila). 2. Potenciales normales de electrodo. 3. Ecuación de Nernst. 4. Electrolisis. 5. Leyes de Faraday. Química 2º bachillerato Electroquímica 1 0. CONOCIMIENTOS
Electrólisis. Electrólisis 12/02/2015
 Electrólisis Dr. Armando Ayala Corona Electrólisis La electrolisis es un proceso mediante el cual se logra la disociación de una sustancia llamada electrolito, en sus iones constituyentes (aniones y cationes),
Electrólisis Dr. Armando Ayala Corona Electrólisis La electrolisis es un proceso mediante el cual se logra la disociación de una sustancia llamada electrolito, en sus iones constituyentes (aniones y cationes),
ELECTROQUIMICA CELDAS GALVANICAS, ELECTROLISIS Y ELECTROQUIMICA APLICADA
 ELECTROQUIMICA CELDAS GALVANICAS, ELECTROLISIS Y ELECTROQUIMICA APLICADA QUE ES LA ELECTROQUIMICA? Es la parte de la química que se encarga del estudio de las relaciones cualitativas y cuantitativas existentes
ELECTROQUIMICA CELDAS GALVANICAS, ELECTROLISIS Y ELECTROQUIMICA APLICADA QUE ES LA ELECTROQUIMICA? Es la parte de la química que se encarga del estudio de las relaciones cualitativas y cuantitativas existentes
ELECTRÓLISIS. Electrólisis de sales fundidas
 El proceso por el cual se produce una reacción química a partir de una energía eléctrica se denomina electrólisis. Y se lleva a cabo en un dispositivo que se conoce como cuba o celda electrolítica. Este
El proceso por el cual se produce una reacción química a partir de una energía eléctrica se denomina electrólisis. Y se lleva a cabo en un dispositivo que se conoce como cuba o celda electrolítica. Este
REACCIONES DE TRANSFERENCIA DE ELECTRONES (electrolisis)
 REACCIONES DE TRANSFERENCIA DE ELECTRONES (electrolisis) 1 2 Electrólisis Aplicando una f.e.m. adecuada se puede conseguir que tenga lugar una reacción redox en el sentido que no es espontánea. En una
REACCIONES DE TRANSFERENCIA DE ELECTRONES (electrolisis) 1 2 Electrólisis Aplicando una f.e.m. adecuada se puede conseguir que tenga lugar una reacción redox en el sentido que no es espontánea. En una
ELECTROQUÍMICA. químicas que se producen por acción de una corriente eléctrica.
 ELECTROQUÍMICA La electroquímica estudia los cambios químicos que producen una corriente eléctrica y la generación de electricidad mediante reacciones químicas. Es por ello, que el campo de la electroquímica
ELECTROQUÍMICA La electroquímica estudia los cambios químicos que producen una corriente eléctrica y la generación de electricidad mediante reacciones químicas. Es por ello, que el campo de la electroquímica
La electricidad. La electricidad se origina por la separación o movimiento de los electrones que forman los átomos.
 1 La electricidad Es el conjunto de fenómenos físicos relacionados con la presencia y flujo de cargas eléctricas. Se manifiesta en una gran variedad de fenómenos como los rayos, la electricidad estática,
1 La electricidad Es el conjunto de fenómenos físicos relacionados con la presencia y flujo de cargas eléctricas. Se manifiesta en una gran variedad de fenómenos como los rayos, la electricidad estática,
Capítulo 1 GESTIÓN DE LA ALIMENTACIÓN
 Capítulo 1 GESTIÓN DE LA ALIMENTACIÓN 1 Introducción En un robot autónomo la gestión de la alimentación es fundamental, desde la generación de energía hasta su consumo, ya que el robot será más autónomo
Capítulo 1 GESTIÓN DE LA ALIMENTACIÓN 1 Introducción En un robot autónomo la gestión de la alimentación es fundamental, desde la generación de energía hasta su consumo, ya que el robot será más autónomo
Circuitos de corriente continua
 Capítulo 4: Circuitos de corriente continua Corriente promedio: carga que pasa por A por unidad de tiempo Corriente Instantánea [ I ] = C/s = A (Ampere) J = q n v d Ley de Ohm George Simon Ohm (1789-1854)
Capítulo 4: Circuitos de corriente continua Corriente promedio: carga que pasa por A por unidad de tiempo Corriente Instantánea [ I ] = C/s = A (Ampere) J = q n v d Ley de Ohm George Simon Ohm (1789-1854)
EL PRAE EN LA UNIDAD PEDAGÓGICA: UN COMPROMISO DE TODOS
 EL PRAE EN LA UNIDAD PEDAGÓGICA: UN COMPROMISO DE TODOS RECICLAJE DE PILAS JUSTIFICACIÓN Una batería o pila es un dispositivo que almacena energía química para ser liberada más tarde como electricidad.
EL PRAE EN LA UNIDAD PEDAGÓGICA: UN COMPROMISO DE TODOS RECICLAJE DE PILAS JUSTIFICACIÓN Una batería o pila es un dispositivo que almacena energía química para ser liberada más tarde como electricidad.
TRABAJO PRÁCTICO N 6: ELECTRÓLISIS
 QUÍMICA GENERAL Y TECNOLÓGICA 2010 TRABAJO PRÁCTICO N 6: ELECTRÓLISIS Objetivo: Medición de la intensidad de corriente que circula por un sistema electrolítico y determinación del equivalente-gramo del
QUÍMICA GENERAL Y TECNOLÓGICA 2010 TRABAJO PRÁCTICO N 6: ELECTRÓLISIS Objetivo: Medición de la intensidad de corriente que circula por un sistema electrolítico y determinación del equivalente-gramo del
Tema 13: CORRIENTE ELÉCTRICA Y CIRCUITOS ELÉCTRICOS
 Tema 13: CORRIENTE ELÉCTRICA Y CIRCUITOS ELÉCTRICOS CORRIENTE ELÉCTRICA Y MOVIMIENTO DE CARGAS Problema 1: Una corriente de 3.6 A fluye a través de un faro de automóvil. Cuántos Culombios de carga fluyen
Tema 13: CORRIENTE ELÉCTRICA Y CIRCUITOS ELÉCTRICOS CORRIENTE ELÉCTRICA Y MOVIMIENTO DE CARGAS Problema 1: Una corriente de 3.6 A fluye a través de un faro de automóvil. Cuántos Culombios de carga fluyen
ELECTROLISIS DE UNA DISOLUCIÓN DE YODURO DE POTASIO. PILA ELECTROLÍTICA
 VIII 1 PRÁCTICA 8 ELECTROLISIS DE UNA DISOLUCIÓN DE YODURO DE POTASIO. PILA ELECTROLÍTICA En esta práctica estudiaremos algunos aspectos prácticos de las reacciones de oxidación reducción que no son espontáneas.
VIII 1 PRÁCTICA 8 ELECTROLISIS DE UNA DISOLUCIÓN DE YODURO DE POTASIO. PILA ELECTROLÍTICA En esta práctica estudiaremos algunos aspectos prácticos de las reacciones de oxidación reducción que no son espontáneas.
Figura 1 Fotografía de varios modelos de multímetros
 El Multímetro El multímetro ó polímetro es un instrumento que permite medir diferentes magnitudes eléctricas. Así, en general, todos los modelos permiten medir: - Tensiones alternas y continuas - Corrientes
El Multímetro El multímetro ó polímetro es un instrumento que permite medir diferentes magnitudes eléctricas. Así, en general, todos los modelos permiten medir: - Tensiones alternas y continuas - Corrientes
Electrón: partícula más pequeña de un átomo, que no se encuentra en el núcleo y que posee carga eléctrica negativa.
 Electricidad: flujo o corriente de electrones. Electrón: partícula más pequeña de un átomo, que no se encuentra en el núcleo y que posee carga eléctrica negativa. Elementos básicos de un circuito: generador,
Electricidad: flujo o corriente de electrones. Electrón: partícula más pequeña de un átomo, que no se encuentra en el núcleo y que posee carga eléctrica negativa. Elementos básicos de un circuito: generador,
Polo positivo: mayor potencial. Polo negativo: menor potencial
 CORRIENTE ELÉCTRICA Es el flujo de carga a través de un conductor Aunque son los electrones los responsables de la corriente eléctrica, está establecido el tomar la dirección de la corriente eléctrica
CORRIENTE ELÉCTRICA Es el flujo de carga a través de un conductor Aunque son los electrones los responsables de la corriente eléctrica, está establecido el tomar la dirección de la corriente eléctrica
Si la intensidad de corriente y su dirección no cambian con el tiempo, entonces esa corriente se llama corriente continua.
 1.8. Corriente eléctrica. Ley de Ohm Clases de Electromagnetismo. Ariel Becerra Si un conductor aislado es introducido en un campo eléctrico entonces sobre las cargas libres q en el conductor va a actuar
1.8. Corriente eléctrica. Ley de Ohm Clases de Electromagnetismo. Ariel Becerra Si un conductor aislado es introducido en un campo eléctrico entonces sobre las cargas libres q en el conductor va a actuar
Energía eléctrica. Elementos activos I
 La corriente eléctrica con mucha chispa Elementos activos y pasivos Circuitos eléctricos Corriente continua y alterna, las chispas de nuestras casas Almacenamiento y producción de energía eléctrica ehículos
La corriente eléctrica con mucha chispa Elementos activos y pasivos Circuitos eléctricos Corriente continua y alterna, las chispas de nuestras casas Almacenamiento y producción de energía eléctrica ehículos
ENERGÍA Y ELECTRICIDAD Circuitos eléctricos
 Física y Química: guía interactiva para la resolución de ejercicios ENERGÍA Y ELECTRICIDAD I.E.S. Élaios Departamento de Física y Química EJERCICIO 1 El cuadro siguiente muestra distintos materiales. Clasifica
Física y Química: guía interactiva para la resolución de ejercicios ENERGÍA Y ELECTRICIDAD I.E.S. Élaios Departamento de Física y Química EJERCICIO 1 El cuadro siguiente muestra distintos materiales. Clasifica
Información importante. 1. El potencial eléctrico. Preuniversitario Solidario. 1.1. Superficies equipotenciales.
 1.1 Superficies equipotenciales. Preuniversitario Solidario Información importante. Aprendizajes esperados: Es guía constituye una herramienta que usted debe manejar para poder comprender los conceptos
1.1 Superficies equipotenciales. Preuniversitario Solidario Información importante. Aprendizajes esperados: Es guía constituye una herramienta que usted debe manejar para poder comprender los conceptos
Reacciones de oxido reducción
 Reacciones de oxido reducción Oxidación pérdida de electrones Reducción ganancia de electrones Las reacciones de oxido reducción tienen lugar mediante intercambio de electrones Ej.: Zn(s) + 2 H + (ac)
Reacciones de oxido reducción Oxidación pérdida de electrones Reducción ganancia de electrones Las reacciones de oxido reducción tienen lugar mediante intercambio de electrones Ej.: Zn(s) + 2 H + (ac)
ELEMENTOS DE UN CIRCUITO Unidad 1. Conceptos básicos de electricidad
 ELEMENTOS DE UN CIRCUITO Unidad 1. Conceptos básicos de electricidad Qué elementos componen un circuito eléctrico? En esta unidad identificaremos los elementos fundamentales de un circuito eléctrico, nomenclatura
ELEMENTOS DE UN CIRCUITO Unidad 1. Conceptos básicos de electricidad Qué elementos componen un circuito eléctrico? En esta unidad identificaremos los elementos fundamentales de un circuito eléctrico, nomenclatura
Temas de electricidad II
 Temas de electricidad II CAMBIANDO MATERIALES Ahora volvemos al circuito patrón ya usado. Tal como se indica en la figura, conecte un hilo de cobre y luego uno de níquel-cromo. Qué ocurre con el brillo
Temas de electricidad II CAMBIANDO MATERIALES Ahora volvemos al circuito patrón ya usado. Tal como se indica en la figura, conecte un hilo de cobre y luego uno de níquel-cromo. Qué ocurre con el brillo
JULIO 2012. FASE ESPECÍFICA. QUÍMICA.
 JULIO 2012. FASE ESPECÍFICA. QUÍMICA. OPCIÓN A 1. (2,5 puntos) Se añaden 10 mg de carbonato de estroncio sólido, SrCO 3 (s), a 2 L de agua pura. Calcule la cantidad de SrCO 3 (s) que queda sin disolver.
JULIO 2012. FASE ESPECÍFICA. QUÍMICA. OPCIÓN A 1. (2,5 puntos) Se añaden 10 mg de carbonato de estroncio sólido, SrCO 3 (s), a 2 L de agua pura. Calcule la cantidad de SrCO 3 (s) que queda sin disolver.
Centro de Bachillerato Tecnológico Industrial y de Servicios nº 137. Submódulo: Prueba Circuitos Eléctricos y Electrónicos Para Sistemas de Control
 Centro de Bachillerato Tecnológico Industrial y de Servicios nº 137 Submódulo: Prueba Circuitos Eléctricos y Electrónicos Para Sistemas de Control Profr. Ing. Cesar Roberto Cruz Pablo Enrique Lavín Lozano
Centro de Bachillerato Tecnológico Industrial y de Servicios nº 137 Submódulo: Prueba Circuitos Eléctricos y Electrónicos Para Sistemas de Control Profr. Ing. Cesar Roberto Cruz Pablo Enrique Lavín Lozano
TEMA VII. REACCIONES DE TRANSFERENCIA DE ELECTRONES.
 TEMA VII. REACCIONES DE TRANSFERENCIA DE ELECTRONES. 1. CONCEPTOS DE OXIDACIÓN-REDUCCIÓN. Concepto restringido: Oxidación es la reacción química en la que hay ganancia de oxígeno, y reducción, la reacción
TEMA VII. REACCIONES DE TRANSFERENCIA DE ELECTRONES. 1. CONCEPTOS DE OXIDACIÓN-REDUCCIÓN. Concepto restringido: Oxidación es la reacción química en la que hay ganancia de oxígeno, y reducción, la reacción
FUENTES DE ALIMENTACION
 FUENTES DE ALIMENTACION INTRODUCCIÓN Podemos definir fuente de alimentación como aparato electrónico modificador de la electricidad que convierte la tensión alterna en una tensión continua. Remontándonos
FUENTES DE ALIMENTACION INTRODUCCIÓN Podemos definir fuente de alimentación como aparato electrónico modificador de la electricidad que convierte la tensión alterna en una tensión continua. Remontándonos
JULIO 2012. FASE GENERAL QUÍMICA
 OPCIÓN A JULIO 2012. FASE GENERAL QUÍMICA 1. (2,5 puntos) A partir de los siguientes datos de energías de ruptura de enlaces (ED): Molécula Enlaces ED (kj mol -1 ) H 2 H H 436 N 2 N N 946 NH 3 N-H 389
OPCIÓN A JULIO 2012. FASE GENERAL QUÍMICA 1. (2,5 puntos) A partir de los siguientes datos de energías de ruptura de enlaces (ED): Molécula Enlaces ED (kj mol -1 ) H 2 H H 436 N 2 N N 946 NH 3 N-H 389
Escuela 4-016 Ing. Marcelo Antonio Arboit - Junín
 Un transformador se compone de dos arrollamientos aislados eléctricamente entre sí y devanados sobre un mismo núcleo de hierro. Una corriente alterna que circule por uno de los arrollamientos crea en el
Un transformador se compone de dos arrollamientos aislados eléctricamente entre sí y devanados sobre un mismo núcleo de hierro. Una corriente alterna que circule por uno de los arrollamientos crea en el
TEMA 2. CIRCUITOS ELÉCTRICOS.
 TEMA 2. CIRCUITOS ELÉCTRICOS. 1. INTRODUCCIÓN. A lo largo del presente tema vamos a estudiar los circuitos eléctricos, para lo cual es necesario recordar una serie de conceptos previos tales como la estructura
TEMA 2. CIRCUITOS ELÉCTRICOS. 1. INTRODUCCIÓN. A lo largo del presente tema vamos a estudiar los circuitos eléctricos, para lo cual es necesario recordar una serie de conceptos previos tales como la estructura
Mediciones Eléctricas
 Mediciones Eléctricas Grupos Electrógenos Mediciones Eléctricas Página 1 de 12 Tabla de Contenido Objetivo 1: Medidas de magnitudes eléctricas... 3 Objetivo 2: Generalidades sobre instrumentos de medición...
Mediciones Eléctricas Grupos Electrógenos Mediciones Eléctricas Página 1 de 12 Tabla de Contenido Objetivo 1: Medidas de magnitudes eléctricas... 3 Objetivo 2: Generalidades sobre instrumentos de medición...
Conceptos de Electricidad Básica (1ª Parte)
 Con este artículo sobre la electricidad básica tenemos la intención de iniciar una serie de publicaciones periódicas que aparecerán en esta página Web de forma trimestral. Estos artículos tienen la intención
Con este artículo sobre la electricidad básica tenemos la intención de iniciar una serie de publicaciones periódicas que aparecerán en esta página Web de forma trimestral. Estos artículos tienen la intención
Reacciones de transferencia de electrones
 Reacciones de transferencia de electrones Las reacciones de transferencia de electrones o reacciones de oxidación-reducción son aquellas en las que dos o más elementos cambian su número de oxidación. Número
Reacciones de transferencia de electrones Las reacciones de transferencia de electrones o reacciones de oxidación-reducción son aquellas en las que dos o más elementos cambian su número de oxidación. Número
3. 1 Generalidades y clasificación de los generadores. Según sea la energía absorbida, los generadores pueden ser:
 CAPITULO 3 GNRADORS LÉCTRICOS 3. 1 Generalidades y clasificación de los generadores. Se llama generador eléctrico todo aparato o máquina capaz de producir o generar energía eléctrica a expensas de otra
CAPITULO 3 GNRADORS LÉCTRICOS 3. 1 Generalidades y clasificación de los generadores. Se llama generador eléctrico todo aparato o máquina capaz de producir o generar energía eléctrica a expensas de otra
ELECTRICIDAD. La idea de corriente eléctrica es inseparable de la de un circuito cerrado. Si en algún lugar hay una ruptura, la corriente no circula.
 ELECTRICIDAD La idea de corriente eléctrica es inseparable de la de un circuito cerrado. Si en algún lugar hay una ruptura, la corriente no circula. Un circuito muy simple: pila, bombilla y cables y su
ELECTRICIDAD La idea de corriente eléctrica es inseparable de la de un circuito cerrado. Si en algún lugar hay una ruptura, la corriente no circula. Un circuito muy simple: pila, bombilla y cables y su
Supercondensadores: Una Alternativa Limpia Y Eficiente De Almacenamiento De Energía
 Septiembre 2012 Supercondensadores: Una Alternativa Limpia Y Eficiente De Almacenamiento De Energía IM. María Guadalupe Reveles Miranda Estudiante de Maestría Unidad de Energía Renovable Centro de Investigación
Septiembre 2012 Supercondensadores: Una Alternativa Limpia Y Eficiente De Almacenamiento De Energía IM. María Guadalupe Reveles Miranda Estudiante de Maestría Unidad de Energía Renovable Centro de Investigación
Los Circuitos Eléctricos
 Los Circuitos Eléctricos 1.- LA CORRIENTE ELÉCTRICA. La electricidad es un movimiento de electrones, partículas con carga eléctrica negativa que giran alrededor del núcleo de los átomos. En los materiales
Los Circuitos Eléctricos 1.- LA CORRIENTE ELÉCTRICA. La electricidad es un movimiento de electrones, partículas con carga eléctrica negativa que giran alrededor del núcleo de los átomos. En los materiales
ELECTRICIDAD BÁSICA EN REPARACIÓN DE AUTOMÓVILES
 ELECTRICIDAD BÁSICA EN REPARACIÓN DE AUTOMÓVILES 1) CONCEPTOS BÁSICOS DE ELECTRICIDAD 1.1 TEORÍA ELECTRÓNICA Los físicos distinguen cuatro diferentes tipos de fuerzas que son comunes en todo el Universo.
ELECTRICIDAD BÁSICA EN REPARACIÓN DE AUTOMÓVILES 1) CONCEPTOS BÁSICOS DE ELECTRICIDAD 1.1 TEORÍA ELECTRÓNICA Los físicos distinguen cuatro diferentes tipos de fuerzas que son comunes en todo el Universo.
BATERIA AUTOMOTRIZ. HECTOR CISTERNA MARTINEZ Profesor Técnico. Duoc UC, Ingenería Mecánica Automotriz y Autotrónica 16/11/2006
 BATERIA AUTOMOTRIZ HECTOR CISTERNA MARTINEZ Profesor Técnico 1 Introducción La batería es un acumulador de energía que cuando se le alimenta de corriente continua, transforma energía eléctrica en energía
BATERIA AUTOMOTRIZ HECTOR CISTERNA MARTINEZ Profesor Técnico 1 Introducción La batería es un acumulador de energía que cuando se le alimenta de corriente continua, transforma energía eléctrica en energía
POTENCIAL CRITICO: Energía mínima para hacer saltar un electrón desde su orbital normal al inmediato superior expresado en ev.
 MECANISMOS DE CONDUCCION ELECTRICA EN GASES Para estudiar el proceso de conducción en gases tenemos que considerar que el gas se encuentra contenido en una ampolla de vidrio, la cual está ocupada únicamente
MECANISMOS DE CONDUCCION ELECTRICA EN GASES Para estudiar el proceso de conducción en gases tenemos que considerar que el gas se encuentra contenido en una ampolla de vidrio, la cual está ocupada únicamente
TEMA 1: LA ELECTRICIDAD
 TEMA 1: LA ELECTRICIDAD 1.- Producción y consumo de la electricidad Existen muchas formas de producir electricidad. Las podemos separar en energías no renovables y energías renovables. Las energías no
TEMA 1: LA ELECTRICIDAD 1.- Producción y consumo de la electricidad Existen muchas formas de producir electricidad. Las podemos separar en energías no renovables y energías renovables. Las energías no
La energía y sus transformaciones
 La energía y sus transformaciones Índice 1 Definición de energía 2 Energías renovables y no renovables 2.1 Energías no renovables 2.2 Energías renovables 3 Transformaciones energéticas 4 Conservación de
La energía y sus transformaciones Índice 1 Definición de energía 2 Energías renovables y no renovables 2.1 Energías no renovables 2.2 Energías renovables 3 Transformaciones energéticas 4 Conservación de
CÁLCULO SECCIÓN CABLEADO DE ALIMENTACIÓN
 CÁLCULO SECCIÓN CABLEADO DE ALIMENTACIÓN V 1.0 SEPTIEMBRE 2005 Corriente máxima en el cable (A) CÁLCULO DE LA SECCIÓN MÍNIMA DEL CABLEADO DE ALIMENTACIÓN Longitud del cable en metros 0 1.2 1.2 2.1 2.1
CÁLCULO SECCIÓN CABLEADO DE ALIMENTACIÓN V 1.0 SEPTIEMBRE 2005 Corriente máxima en el cable (A) CÁLCULO DE LA SECCIÓN MÍNIMA DEL CABLEADO DE ALIMENTACIÓN Longitud del cable en metros 0 1.2 1.2 2.1 2.1
CAPÍTULO COMPONENTES EL DIODO SEMICONDUCTORES: 1.1 INTRODUCCIÓN
 CAPÍTULO 1 COMPONENTES SEMICONDUCTORES: EL DIODO 1.1 INTRODUCCIÓN E n el capítulo 5 del tomo III se presentó una visión general de los componentes semiconductores básicos más frecuentes en electrónica,
CAPÍTULO 1 COMPONENTES SEMICONDUCTORES: EL DIODO 1.1 INTRODUCCIÓN E n el capítulo 5 del tomo III se presentó una visión general de los componentes semiconductores básicos más frecuentes en electrónica,
Entonces el trabajo de la fuerza eléctrica es : =F d (positivo porque la carga se desplaza en el sentido en que actúa la fuerza (de A a B)
 Consideremos la siguiente situación. Una carga Q que genera un campo eléctrico uniforme, y sobre este campo eléctrico se ubica una carga puntual q.de tal manara que si las cargas son de igual signo la
Consideremos la siguiente situación. Una carga Q que genera un campo eléctrico uniforme, y sobre este campo eléctrico se ubica una carga puntual q.de tal manara que si las cargas son de igual signo la
La electrólisis permite descomponer la Alúmina en aluminio y oxígeno.
 LA OBTENCIÓN DEL ALUMINIO. La primera fase de la obtención del aluminio consiste en aislar la Alúmina (óxido de aluminio) de estos minerales. Para ello lo primero es triturar la Bauxita para obtener un
LA OBTENCIÓN DEL ALUMINIO. La primera fase de la obtención del aluminio consiste en aislar la Alúmina (óxido de aluminio) de estos minerales. Para ello lo primero es triturar la Bauxita para obtener un
CORRIENTE CONTÍNUA (II) GENERADORES Y MOTORES
 CORRENTE CONTÍNU () GENERORES Y OTORES ES La agdalena. vilés. sturias En un circuito se pueden intercalar, además de resistencias, elementos activos tales como generadores y motores. Los generadores (o
CORRENTE CONTÍNU () GENERORES Y OTORES ES La agdalena. vilés. sturias En un circuito se pueden intercalar, además de resistencias, elementos activos tales como generadores y motores. Los generadores (o
SISTEMA MONOFÁSICO Y TRIFÁSICO DE C.A Unidad 1 Magnetismo, electromagnetismo e Inducción electromagnética.
 SISTEMA MONOFÁSICO Y TRIFÁSICO DE C.A Unidad 1 Magnetismo, electromagnetismo e Inducción electromagnética. A diferencia de los sistemas monofásicos de C.A., estudiados hasta ahora, que utilizan dos conductores
SISTEMA MONOFÁSICO Y TRIFÁSICO DE C.A Unidad 1 Magnetismo, electromagnetismo e Inducción electromagnética. A diferencia de los sistemas monofásicos de C.A., estudiados hasta ahora, que utilizan dos conductores
ELECTRICIDAD Secundaria
 ELECTRICIDAD Secundaria Carga eléctrica. Los átomos que constituyen la materia están formados por otras partículas todavía más pequeñas, llamadas protones, neutrones y electrones. Los protones y los electrones
ELECTRICIDAD Secundaria Carga eléctrica. Los átomos que constituyen la materia están formados por otras partículas todavía más pequeñas, llamadas protones, neutrones y electrones. Los protones y los electrones
Fundamentos de Electricidad de C.C.
 LEY DE OHM El flujo de los electrones a través de un circuito se parece en muchas cosas al flujo del agua en las tuberías. Por tanto, se puede comprender la acción de una corriente eléctrica comparando
LEY DE OHM El flujo de los electrones a través de un circuito se parece en muchas cosas al flujo del agua en las tuberías. Por tanto, se puede comprender la acción de una corriente eléctrica comparando
CIRCUITO ELÉCTRICO ELEMENTAL
 CIRCUITO ELÉCTRICO ELEMENTL Elementos que integran un circuito elemental. Los elementos necesarios para el armado de un circuito elemental son los que se indican en la figura siguiente; Figura 1 Extremo
CIRCUITO ELÉCTRICO ELEMENTL Elementos que integran un circuito elemental. Los elementos necesarios para el armado de un circuito elemental son los que se indican en la figura siguiente; Figura 1 Extremo
FISICA DE LOS PROCESOS BIOLOGICOS
 FISICA DE LOS PROCESOS BIOLOGICOS BIOELECTROMAGNETISMO 1. Cuál es la carga total, en coulombios, de todos los electrones que hay en 3 moles de átomos de hidrógeno? -289481.4 Coulombios 2. Un átomo de hidrógeno
FISICA DE LOS PROCESOS BIOLOGICOS BIOELECTROMAGNETISMO 1. Cuál es la carga total, en coulombios, de todos los electrones que hay en 3 moles de átomos de hidrógeno? -289481.4 Coulombios 2. Un átomo de hidrógeno
CAPITULO II CARACTERISTICAS DE LOS INSTRUMENTOS DE MEDICION
 CAPITULO II CARACTERISTICAS DE LOS INSTRUMENTOS DE MEDICION Como hemos dicho anteriormente, los instrumentos de medición hacen posible la observación de los fenómenos eléctricos y su cuantificación. Ahora
CAPITULO II CARACTERISTICAS DE LOS INSTRUMENTOS DE MEDICION Como hemos dicho anteriormente, los instrumentos de medición hacen posible la observación de los fenómenos eléctricos y su cuantificación. Ahora
Examen de problemas. PROBLEMA 1 Considere la siguiente reacción: C(s) + CO 2 (g) 2CO(g)
 PROBLEMA 1 Considere la siguiente reacción: C(s) + CO 2 (g) 2CO(g) a) A partir de qué temperatura es espontánea o dejará de serlo? Suponga que r Hº y r Sº no dependen de la temperatura. b) Calcule el valor
PROBLEMA 1 Considere la siguiente reacción: C(s) + CO 2 (g) 2CO(g) a) A partir de qué temperatura es espontánea o dejará de serlo? Suponga que r Hº y r Sº no dependen de la temperatura. b) Calcule el valor
La Absorción del Agua
 La Absorción del Agua Importancia del Agua en las Plantas Es el cons5tuyente principal del protoplasma celular, en ocasiones representa hasta el 95% del peso total de la planta. Es el solvente en el que
La Absorción del Agua Importancia del Agua en las Plantas Es el cons5tuyente principal del protoplasma celular, en ocasiones representa hasta el 95% del peso total de la planta. Es el solvente en el que
Máster Universitario en Profesorado
 Máster Universitario en Profesorado Complementos para la formación disciplinar en Tecnología y procesos industriales Aspectos básicos de la Tecnología Eléctrica Contenido (II) SEGUNDA PARTE: corriente
Máster Universitario en Profesorado Complementos para la formación disciplinar en Tecnología y procesos industriales Aspectos básicos de la Tecnología Eléctrica Contenido (II) SEGUNDA PARTE: corriente
Experimento 5 COMBINACIONES DE RESISTENCIAS. Objetivos. Introducción. Figura 1 Circuito con dos resistencias en serie
 Experimento 5 COMBINACIONES DE RESISTENCIAS Objetivos 1. Construir circuitos con baterías, resistencias, y cables conductores, 2. Analizar circuitos con combinaciones de resistencias en serie para verificar
Experimento 5 COMBINACIONES DE RESISTENCIAS Objetivos 1. Construir circuitos con baterías, resistencias, y cables conductores, 2. Analizar circuitos con combinaciones de resistencias en serie para verificar
Tema 6: Equilibrio químico.
 Tema 6: Equilibrio químico. Equilibrio en las recciones químicas. Constante de equilibrio. Propiedades de las constantes de equilibrio. Constantes de equilibrio K c y K p. Equilibrio en mezclas heterogéneas.
Tema 6: Equilibrio químico. Equilibrio en las recciones químicas. Constante de equilibrio. Propiedades de las constantes de equilibrio. Constantes de equilibrio K c y K p. Equilibrio en mezclas heterogéneas.
LÍMITES Y CONTINUIDAD DE FUNCIONES
 Capítulo 9 LÍMITES Y CONTINUIDAD DE FUNCIONES 9.. Introducción El concepto de ite en Matemáticas tiene el sentido de lugar hacia el que se dirige una función en un determinado punto o en el infinito. Veamos
Capítulo 9 LÍMITES Y CONTINUIDAD DE FUNCIONES 9.. Introducción El concepto de ite en Matemáticas tiene el sentido de lugar hacia el que se dirige una función en un determinado punto o en el infinito. Veamos
El generador de Van de Graaff
 Cuando se introduce un conductor cargado dentro de otro hueco y se ponen en contacto, toda la carga del primero pasa al segundo, cualquiera que sea la carga inicial del conductor hueco Teóricamente, el
Cuando se introduce un conductor cargado dentro de otro hueco y se ponen en contacto, toda la carga del primero pasa al segundo, cualquiera que sea la carga inicial del conductor hueco Teóricamente, el
Tema 7. MOTORES ELÉCTRICOS DE CORRIENTE CONTINUA
 Tema 7. MOTORES ELÉCTRICOS DE CORRIENTE CONTINUA 1. MAGNETISMO Y ELECTRICIDAD...2 Fuerza electromotriz inducida (Ley de inducción de Faraday)...2 Fuerza electromagnética (2ª Ley de Laplace)...2 2. LAS
Tema 7. MOTORES ELÉCTRICOS DE CORRIENTE CONTINUA 1. MAGNETISMO Y ELECTRICIDAD...2 Fuerza electromotriz inducida (Ley de inducción de Faraday)...2 Fuerza electromagnética (2ª Ley de Laplace)...2 2. LAS
Electricidad y electrónica - Diplomado
 CONOCIMIENTOS DE CONCEPTOS Y PRINCIPIOS Circuitos Eléctricos: principios, conceptos, tipos, características Unidades Básicas de los circuitos eléctricos: conceptos, tipos, características Leyes fundamentales
CONOCIMIENTOS DE CONCEPTOS Y PRINCIPIOS Circuitos Eléctricos: principios, conceptos, tipos, características Unidades Básicas de los circuitos eléctricos: conceptos, tipos, características Leyes fundamentales
TECNOLOGIA RESUMEN DEL TEMA 3 (NOCIONES DE ELECTRICIDAD Y MAGNETISMO)
 TECNOLOGIA RESUMEN DEL TEMA 3 (NOCIONES DE ELECTRICIDAD Y MAGNETISMO) Existen 2 clases de electrización, la positiva (que se representa con + ), y la negativa (que se representa con - ). Hay una partícula
TECNOLOGIA RESUMEN DEL TEMA 3 (NOCIONES DE ELECTRICIDAD Y MAGNETISMO) Existen 2 clases de electrización, la positiva (que se representa con + ), y la negativa (que se representa con - ). Hay una partícula
Bloque IV: Electrolisis. Prof. Dr. Mª del Carmen Clemente Jul
 Bloque IV: Electrolisis Prof. Dr. Mª del Carmen Clemente Jul ELECTROLISIS PROCESO EN EL QUE SE UTILIZA LA ENERGÍA ELÉCTRICA PARA PROVOCAR UNA REACCIÓN QUÍMICA (REDOX) NO ESPONTÁNEA ELECTROLISIS DEL NaCl
Bloque IV: Electrolisis Prof. Dr. Mª del Carmen Clemente Jul ELECTROLISIS PROCESO EN EL QUE SE UTILIZA LA ENERGÍA ELÉCTRICA PARA PROVOCAR UNA REACCIÓN QUÍMICA (REDOX) NO ESPONTÁNEA ELECTROLISIS DEL NaCl
A VUELTAS CON EL MOL
 A VUELTAS CON EL MOL El concepto de mol es algo íntimamente ligado a la teoría atómico-molecular de la materia y al Número de Avogadro. Es necesario, por tanto, tener una idea clara de lo que es un átomo
A VUELTAS CON EL MOL El concepto de mol es algo íntimamente ligado a la teoría atómico-molecular de la materia y al Número de Avogadro. Es necesario, por tanto, tener una idea clara de lo que es un átomo
Instrumentación y Ley de OHM
 Instrumentación y Ley de OHM A) INSTRUMENTACIÓN 1. OBJETIVOS. 1. Conocer el manejo de instrumentos y materiales de uso corriente en los experimentos de electricidad y magnetismo. 2. Conocer el área de
Instrumentación y Ley de OHM A) INSTRUMENTACIÓN 1. OBJETIVOS. 1. Conocer el manejo de instrumentos y materiales de uso corriente en los experimentos de electricidad y magnetismo. 2. Conocer el área de
LA ELECTRÓLISIS DEL AGUA
 LA ELECTRÓLISIS DEL AGUA Oxidación: 2H + +O +4e - 2 O(l) 4H (aq) 2 (g) Reducción: 2H 2 O(l) + 2e - H 2 (g) + 2OH - (aq) Reacción total en la celda 2H 2 O(l) 2H 2 (g) + O 2 (g) Nota: Obsérvese la diferencia
LA ELECTRÓLISIS DEL AGUA Oxidación: 2H + +O +4e - 2 O(l) 4H (aq) 2 (g) Reducción: 2H 2 O(l) + 2e - H 2 (g) + 2OH - (aq) Reacción total en la celda 2H 2 O(l) 2H 2 (g) + O 2 (g) Nota: Obsérvese la diferencia
corriente) C Aquí q esta en Coulomb, t en segundos, I en Amperes (1A= 1 ) s
 UNA CORRIENTE i de electricidad existe en cualquier región donde sean transportadas cargas eléctricas desde un punto a otro punto de esa región.supóngase que la carga se mueve a través de un alambre.si
UNA CORRIENTE i de electricidad existe en cualquier región donde sean transportadas cargas eléctricas desde un punto a otro punto de esa región.supóngase que la carga se mueve a través de un alambre.si
UD 4.-ELECTRICIDAD 1. EL CIRCUITO ELÉCTRICO
 DPTO. TECNOLOGÍA (ES SEFAAD) UD 4.-ELECTCDAD UD 4.- ELECTCDAD. EL CCUTO ELÉCTCO. ELEMENTOS DE UN CCUTO 3. MAGNTUDES ELÉCTCAS 4. LEY DE OHM 5. ASOCACÓN DE ELEMENTOS 6. TPOS DE COENTE 7. ENEGÍA ELÉCTCA.
DPTO. TECNOLOGÍA (ES SEFAAD) UD 4.-ELECTCDAD UD 4.- ELECTCDAD. EL CCUTO ELÉCTCO. ELEMENTOS DE UN CCUTO 3. MAGNTUDES ELÉCTCAS 4. LEY DE OHM 5. ASOCACÓN DE ELEMENTOS 6. TPOS DE COENTE 7. ENEGÍA ELÉCTCA.
REACCIONES DE TRANSFERENCIA DE ELECTRONES MODELO 2016
 REACCIONES DE TRANSFERENCIA DE ELECTRONES MODELO 2016 1- Se lleva a cabo la electrolisis de una disolución acuosa de bromuro de sodio 1 M, haciendo pasar una corriente de 1,5 A durante 90 minutos. a) Ajuste
REACCIONES DE TRANSFERENCIA DE ELECTRONES MODELO 2016 1- Se lleva a cabo la electrolisis de una disolución acuosa de bromuro de sodio 1 M, haciendo pasar una corriente de 1,5 A durante 90 minutos. a) Ajuste
FICHA DE CONSULTA DE EXCURSIÓN POR LA RED ELÉCTRICA
 FICHA DE CONSULTA Sumario 1. Glosario 1.1. Siglas 3 1.2. Términos 3 2. Paneles solares 2.1. Qué es un panel solar? 4 2.2. Cómo funciona un panel solar? 6 2 1. Glosario 1.1. Siglas 1.2. Términos W/m² Watts
FICHA DE CONSULTA Sumario 1. Glosario 1.1. Siglas 3 1.2. Términos 3 2. Paneles solares 2.1. Qué es un panel solar? 4 2.2. Cómo funciona un panel solar? 6 2 1. Glosario 1.1. Siglas 1.2. Términos W/m² Watts
PRÁCTICA Nº 1: EL VOLTÍMETRO Y EL AMPERÍMETRO
 PRÁCTICA Nº 1: EL VOLTÍMETRO Y EL AMPERÍMETRO Objetivos: Utilización de un voltímetro y de un amperímetro, caracterización de aparatos analógicos y digitales, y efecto de carga. Material: Un voltímetro
PRÁCTICA Nº 1: EL VOLTÍMETRO Y EL AMPERÍMETRO Objetivos: Utilización de un voltímetro y de un amperímetro, caracterización de aparatos analógicos y digitales, y efecto de carga. Material: Un voltímetro
Seminario de Electricidad Básica
 Seminario de Electricidad Básica Qué es la Electricidad? Es una forma de energía natural que puede ser producida artificialmente y que se caracteriza por su poder de transformación; ya que se puede convertir
Seminario de Electricidad Básica Qué es la Electricidad? Es una forma de energía natural que puede ser producida artificialmente y que se caracteriza por su poder de transformación; ya que se puede convertir
Tema 7: Solubilidad. (Fundamentos de Química, Grado en Física) Equilibrio químico Enero Mayo, 2011 1 / 24
 Tema 7: Solubilidad. Producto de solubilidad. Efecto del ion común en la solubilidad. Limitaciones al producto de solubilidad: K ps. Criterios para la precipitación de la sal. Precipitación fraccionada.
Tema 7: Solubilidad. Producto de solubilidad. Efecto del ion común en la solubilidad. Limitaciones al producto de solubilidad: K ps. Criterios para la precipitación de la sal. Precipitación fraccionada.
FÍSICA Y QUÍMICA 3º ESO ACTIVIDADES DE RECUPERACIÓN
 FÍSICA Y QUÍMICA 3º ESO ACTIVIDADES DE RECUPERACIÓN (PARTE 2) CURSO 2011/12 Nombre y apellidos: 1 LA CIENCIA Y SU MÉTODO. MEDIDA DE MAGNITUDES LOS ÁTOMOS Y SU COMPLEJIDAD 1. Qué explica el modelo atómico
FÍSICA Y QUÍMICA 3º ESO ACTIVIDADES DE RECUPERACIÓN (PARTE 2) CURSO 2011/12 Nombre y apellidos: 1 LA CIENCIA Y SU MÉTODO. MEDIDA DE MAGNITUDES LOS ÁTOMOS Y SU COMPLEJIDAD 1. Qué explica el modelo atómico
ELECTROLISIS. Si a dos electrodos de una pila Daniel, en la que espontáneamente se verifica la reacción:
 ELECTROLISIS Si a dos electrodos de una pila Daniel, en la que espontáneamente se verifica la reacción: + + Zn + Cu Zn + Cu se aplica una diferencia de potencial progresivamente creciente que se oponga
ELECTROLISIS Si a dos electrodos de una pila Daniel, en la que espontáneamente se verifica la reacción: + + Zn + Cu Zn + Cu se aplica una diferencia de potencial progresivamente creciente que se oponga
TEMA 2: Representación de la Información en las computadoras
 TEMA 2: Representación de la Información en las computadoras Introducción Una computadora es una máquina que procesa información y ejecuta programas. Para que la computadora ejecute un programa, es necesario
TEMA 2: Representación de la Información en las computadoras Introducción Una computadora es una máquina que procesa información y ejecuta programas. Para que la computadora ejecute un programa, es necesario
Unidad 6: ELECTROQUIMICA
 Unidad 6: ELECTROQUIMICA REACCIONES DE OXIDACION-REDUCCION Las reacciones redox son aquellas en las cuales hay intercambio de electrones entre las sustancias que intervienen en la reacción. Oxidación:
Unidad 6: ELECTROQUIMICA REACCIONES DE OXIDACION-REDUCCION Las reacciones redox son aquellas en las cuales hay intercambio de electrones entre las sustancias que intervienen en la reacción. Oxidación:
En la 3ª entrega de este trabajo nos centraremos en la relación entre magnitudes eléctricas, hecho que explica la famosa Ley de Ohm.
 3º parte En la 3ª entrega de este trabajo nos centraremos en la relación entre magnitudes eléctricas, hecho que explica la famosa Ley de Ohm. ELEMENTOS DEL CIRCUITO ELÉCTRICO Para poder relacionar las
3º parte En la 3ª entrega de este trabajo nos centraremos en la relación entre magnitudes eléctricas, hecho que explica la famosa Ley de Ohm. ELEMENTOS DEL CIRCUITO ELÉCTRICO Para poder relacionar las
Tema 5. Oxidación Reducción. Prof(a). María Angélica Sánchez Palacios
 Tema 5. Oxidación Reducción Prof(a). María Angélica Sánchez Palacios Los procesos electroquímicos consisten en reacciones de oxido-reducción en las cuales: - La energía liberada por una reacción espontánea
Tema 5. Oxidación Reducción Prof(a). María Angélica Sánchez Palacios Los procesos electroquímicos consisten en reacciones de oxido-reducción en las cuales: - La energía liberada por una reacción espontánea
PLAN DE RECUPERACIÓN DE MATERIAS PENDIENTES
 PLAN DE RECUPERACIÓN DE MATERIAS PENDIENTES ACTIVIDADES DE RECUPERACIÓN DE LA ASIGNATURA DE TECNOLOGÍA 3 ESO Los alumnos que tienen pendiente la asignatura de Tecnología de 3º de la ESO encontrándose en
PLAN DE RECUPERACIÓN DE MATERIAS PENDIENTES ACTIVIDADES DE RECUPERACIÓN DE LA ASIGNATURA DE TECNOLOGÍA 3 ESO Los alumnos que tienen pendiente la asignatura de Tecnología de 3º de la ESO encontrándose en
TEMA 3 GENERADORES DE CORRIENTE CONTINUA
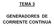 TEMA 3 GENERADORES DE CORRIENTE CONTINUA En todo circuito eléctrico es necesaria una fuente de energía que sea capaz de poner en movimiento a los electrones, a la cual llamamos generador. Si existen dos
TEMA 3 GENERADORES DE CORRIENTE CONTINUA En todo circuito eléctrico es necesaria una fuente de energía que sea capaz de poner en movimiento a los electrones, a la cual llamamos generador. Si existen dos
INTRODUCCIÓN. En el mundo actual, el manejo y acceso de la información para tenerla y manejarla en el
 INTRODUCCIÓN Antecedentes En el mundo actual, el manejo y acceso de la información para tenerla y manejarla en el lugar y momento adecuados se ha hecho esencial para poder ser un profesional o empresa
INTRODUCCIÓN Antecedentes En el mundo actual, el manejo y acceso de la información para tenerla y manejarla en el lugar y momento adecuados se ha hecho esencial para poder ser un profesional o empresa
LINEAS EQUIPOTENCIALES
 LINEAS EQUIPOTENCIALES Construcción de líneas equipotenciales. Visualización del campo eléctrico y del potencial eléctrico. Análisis del movimiento de cargas eléctricas en presencia de campos eléctricos.
LINEAS EQUIPOTENCIALES Construcción de líneas equipotenciales. Visualización del campo eléctrico y del potencial eléctrico. Análisis del movimiento de cargas eléctricas en presencia de campos eléctricos.
Figura 1. Tipos de capacitores 1
 CAPACITOR EN CIRCUITO RC OBJETIVO: REGISTRAR GRÁFICAMENTE LA DESCARGA DE UN CAPACITOR Y DETERMINAR EXPERIMENTALMENTE LA CONSTANTE DE TIEMPO RC DEL CAPACITOR. Ficha 12 Figura 1. Tipos de capacitores 1 Se
CAPACITOR EN CIRCUITO RC OBJETIVO: REGISTRAR GRÁFICAMENTE LA DESCARGA DE UN CAPACITOR Y DETERMINAR EXPERIMENTALMENTE LA CONSTANTE DE TIEMPO RC DEL CAPACITOR. Ficha 12 Figura 1. Tipos de capacitores 1 Se
Componentes Pasivos. CATEDRA: Mediciones Electricas I Y II. Facultad de Ciencias Exactas y Tecnología UNIVERSIDAD NACINAL DE TUCUMÁN
 Componentes Pasivos CATEDRA: Mediciones Electricas I Y II Facultad de Ciencias Exactas y Tecnología UNIVERSIDAD NACINAL DE TUCUMÁN Año 2011 Resistencias Resistencia es la oposición que presenta un conductor
Componentes Pasivos CATEDRA: Mediciones Electricas I Y II Facultad de Ciencias Exactas y Tecnología UNIVERSIDAD NACINAL DE TUCUMÁN Año 2011 Resistencias Resistencia es la oposición que presenta un conductor
Cap. 24 La Ley de Gauss
 Cap. 24 La Ley de Gauss Una misma ley física enunciada desde diferentes puntos de vista Coulomb Gauss Son equivalentes Pero ambas tienen situaciones para las cuales son superiores que la otra Aquí hay
Cap. 24 La Ley de Gauss Una misma ley física enunciada desde diferentes puntos de vista Coulomb Gauss Son equivalentes Pero ambas tienen situaciones para las cuales son superiores que la otra Aquí hay
Desulfatación para Baterías de Plomo-Ácido y NiCd
 Tecnología de Regeneración de Baterías *Según el BCI (Battery Council International) 80% de los fallos en las baterías ocurren por la sulfatación Desulfatación para Baterías de Plomo-Ácido y NiCd Tl:(34)
Tecnología de Regeneración de Baterías *Según el BCI (Battery Council International) 80% de los fallos en las baterías ocurren por la sulfatación Desulfatación para Baterías de Plomo-Ácido y NiCd Tl:(34)
MODULO Nº12 TRANSISTORES MOSFET
 MODULO Nº12 TRANSISTORES MOSFET UNIDAD: CONVERTIDORES CC - CC TEMAS: Transistores MOSFET. Parámetros del Transistor MOSFET. Conmutación de Transistores MOSFET. OBJETIVOS: Comprender el funcionamiento del
MODULO Nº12 TRANSISTORES MOSFET UNIDAD: CONVERTIDORES CC - CC TEMAS: Transistores MOSFET. Parámetros del Transistor MOSFET. Conmutación de Transistores MOSFET. OBJETIVOS: Comprender el funcionamiento del
RECUBRIMIENTO ELECTROLITICO
 Cómo motivar a los estudiantes mediante actividades científicas atractivas RECUBRIMIENTO ELECTROLITICO Introducción: Esther Pérez Real COLEGIO ESCLAVAS DE MARIA Valencia Los procesos de recubrimientos
Cómo motivar a los estudiantes mediante actividades científicas atractivas RECUBRIMIENTO ELECTROLITICO Introducción: Esther Pérez Real COLEGIO ESCLAVAS DE MARIA Valencia Los procesos de recubrimientos
Aire acondicionado y refrigeración
 Aire acondicionado y refrigeración CONCEPTO: El acondicionamiento del aire es el proceso que enfría, limpia y circula el aire, controlando, además, su contenido de humedad. En condiciones ideales logra
Aire acondicionado y refrigeración CONCEPTO: El acondicionamiento del aire es el proceso que enfría, limpia y circula el aire, controlando, además, su contenido de humedad. En condiciones ideales logra
El E.O. no tiene porqué ser la carga real que tiene un átomo, aunque a veces coincide.
 EQUILIBRIOS DE OXIDACIÓN-REDUCCIÓN (REDOX) 2º BACHILLERATO QUÍMICA 1.- Estado de oxidación. 2.- Concepto de oxidación y reducción. 3.- Ajuste de ecuaciones redox por el método del ión-electrón. 3.1. Reacciones
EQUILIBRIOS DE OXIDACIÓN-REDUCCIÓN (REDOX) 2º BACHILLERATO QUÍMICA 1.- Estado de oxidación. 2.- Concepto de oxidación y reducción. 3.- Ajuste de ecuaciones redox por el método del ión-electrón. 3.1. Reacciones
MEDICIONES ELECTRICAS II
 Año:... Alumno:... Comisión:... MEDICIONES ELECTRICAS II Trabajo Práctico N 3 Tema: MEDICION DE FASE CONTRASTE DE COFIMETRO. Conceptos Fundamentales El período de una señal senoidal se corresponde con
Año:... Alumno:... Comisión:... MEDICIONES ELECTRICAS II Trabajo Práctico N 3 Tema: MEDICION DE FASE CONTRASTE DE COFIMETRO. Conceptos Fundamentales El período de una señal senoidal se corresponde con
PREGUNTAS FRECUENTES
 PREGUNTAS FRECUENTES ÍNDICE Qué son los Repartidores de costes de calefacción? Montaje y funcionamiento de los repartidores Base de datos de radiadores existentes. Precio de los Repartidores de Costes
PREGUNTAS FRECUENTES ÍNDICE Qué son los Repartidores de costes de calefacción? Montaje y funcionamiento de los repartidores Base de datos de radiadores existentes. Precio de los Repartidores de Costes
La electrólisis CONTENIDOS. Electrolitos. Iones. Carga eléctrica negativa. www.codelcoeduca.cl
 La electrólisis Las moléculas de ciertos compuestos químicos, cuando se encuentran en disolución acuosa, presentan la capacidad de separarse en sus estructuras moleculares más simples y/o en sus átomos
La electrólisis Las moléculas de ciertos compuestos químicos, cuando se encuentran en disolución acuosa, presentan la capacidad de separarse en sus estructuras moleculares más simples y/o en sus átomos
TEMA ELECTRÓNICA 3º ESO TECNOLOGÍA
 3º ESO Tecnologías Tema Electrónica página 1 de 11 TEMA ELECTRÓNICA 3º ESO TECNOLOGÍA Índice de contenido 1 Electrónica...2 2 Pilas en los circuitos electrónicos...2 3 DIODO...2 4 LED (diodo emisor de
3º ESO Tecnologías Tema Electrónica página 1 de 11 TEMA ELECTRÓNICA 3º ESO TECNOLOGÍA Índice de contenido 1 Electrónica...2 2 Pilas en los circuitos electrónicos...2 3 DIODO...2 4 LED (diodo emisor de
Corriente continua y corriente alterna
 Electricidad ENTREGA 1 Corriente continua y corriente alterna Elaborado por Jonathan Caballero La corriente o intensidad eléctrica es el flujo de carga por unidad de tiempo que recorre un material. Se
Electricidad ENTREGA 1 Corriente continua y corriente alterna Elaborado por Jonathan Caballero La corriente o intensidad eléctrica es el flujo de carga por unidad de tiempo que recorre un material. Se
Nota Técnica Abril 2014
 LÁMPARAS LED QUE QUEDAN SEMIENCENDIDAS O PARPADEAN: En ocasiones ocurre que al realizar una sustitución en donde antes teníamos una halógena por una lámpara LED, la nueva lámpara se queda semiencendida
LÁMPARAS LED QUE QUEDAN SEMIENCENDIDAS O PARPADEAN: En ocasiones ocurre que al realizar una sustitución en donde antes teníamos una halógena por una lámpara LED, la nueva lámpara se queda semiencendida
