PROBLEMAS DE INGENIERÍA TÉRMICA
|
|
|
- María del Carmen Gutiérrez Poblete
- hace 7 años
- Vistas:
Transcripción
1 PROBLEMAS DE INGENIERÍA TÉRMICA Pedro Fernández Díez Carlos Renedo Estébanez Pedro R. FernándezGarcía
2 PROBLEMAS SOBRE COMBUSTIÓN Combustión.-
3 En los cálculos estequiométricos hay que distinguir continuamente entre el balance de la masa, que se debe mantener, y las variaciones moleculares de sus ecuaciones. Por ejemplo, en la ecuación de combustión: CO + 1 O CO el cambio molecular se expresa por kg-mol CO + 1 kg-mol O kg-mol CO es decir, se ha producido una reducción molecular de, kg-mol, a kg-mol al pasar del estado reactivo al estado producto. Sin embargo, por el principio de conservación de la masa, debe existir un estricto balance entre los kilos de reactivos y productos. Puesto que los números anteriores representan los valores respectivos de n CO, n O, y n CO, la ecuación de la masa se puede poner en la forma: n M (CO) + n M (O ) n M (CO ) es decir: kg-mol (CO) x 8 ( kg kg-mol ) CO + 1 kg-mol (O ) x 3 ( kg kg-mol ) O kg-mol (CO ) x 44 ( 56 kg CO + 3 kg O 88 kg CO (en equilibrio, puesto que ) 93 Para el benceno se tiene: (C 6 H 6 ) + 15 (O ) 1 (CO ) + 6 (H O) en la que: n (reactivos) kg-mol n (productos) kg-mol kg kg-mol ) CO es decir, existe un incremento molecular, mientras que se mantiene el balance de la masa puesto que en este caso se puede poner: ( x 78) kg C 6 H 6 + (15 x 3) kg O (1 x 44) kg CO + (6 x 18) kg H O es decir ó A veces se obtiene un balance simultáneo en masa y volumen; por ejemplo en la reacción: CO + H O CO + H el número de reactivos y de productos es igual a kg-mol.... Combustión.-3
4 1.- Una caldera utiliza un combustible gaseoso con el siguiente análisis volumétrico: H 48% ; CH 4,5% ; CO 19% ; N 6% ; CO 4,5%. El aire que se suministra excede en un 5% al suministro de aire estequiométrico, y con esta proporción aire/combus-tible, la combustión es completa. Calcular para 100 kg-mol de combustible los porcentajes de los gases de la chimenea analizados en las siguientes situaciones: (a) sobre una base volumétrica para los gases "secos" de la chimenea (b) sobre una base de la masa para el total de gases "húmedos" de la chimenea. H + O H O Ecuaciones químicas básicas de la combustión: CH 4 + O CO + H O CO + O CO El combustible está formado por: Para la combustión estequiométrica: 48 kg-mol de H ;,5 kg-mol de CH 4 ; 19 kg-mol de CO 6 kg-mol de N ; 4,50 kg/mol de CO 48 kg-mol de H necesitan 4 kg-mol de O,5 kg-mol de CH 4 necesitan 45 kg-mol de O 19 kg-mol de CO necesitan 9,5 kg-mol de O por lo que el requerimiento estequiométrico de oxígeno para el combustible es de: ,5 78,5 kg-mol de O por 100 kg-mol de combustible Como el suministro de aire excede en un 5% a las necesidades estequiométricas fi que el oxígeno suministrado también es un 5% superior al calculado para la combustión estequiométrica, por lo que lo que: Suministro de oxígeno: 1,5 x 78,5 98,1 kg-mol Suministro de nitrógeno: 3,76 x 98,1 369,1 kg-mol 368, ,9 kg-mol de N por 100 kg-mol de combustible kg-mol de H O por 100 kg-mol de combustible Productos de la combustión: 4,5 +, kg-mol de CO por 100 kg-mol de combustible 398,1-78,5 19,6 kg-mol de O por 100 kg-mol de combustible n Análisis seco (se excluye el agua) M (kg/kg-mol) Nitrógeno 374,9 8 x(n) 374,9/440,5 0,851 85,1% Anhidrido carbónico x(co) 46/440,5 0, ,44% Oxígeno 19,6 3 x(o) 19,6/440,5 0,0445 4,45% Total ,5 Análisis húmedo n M (kg/kg-mol) n M (kg-mol) x n / Σ n Nitrógeno 374, /148 0,708 70,8% Vapor de agua /148 0,119 11,9% Anhidrido carbónico /148 0, ,65% Oxígeno 19, /148 0,043 4,3% Total ,5 148 % masa (n M)/ Σ(n M).- Un combustible derivado del petróleo cuyo análisis gravimétrico es: C 86% ; H 1% ; O 1% ; S 1% se quema con aire que excede en un 70% del mínimo para la combustión completa teórica. Determinar por 1 kg de combustible: a) La masa de aire que se suministra por kg de combustible b) El análisis volumétrico de los gases después de la combustión. Combustión.-4
5 Ecuaciones químicas básicas de la combustión: 1 kg H + (3/4) kg O 9 kg H O 1 kg C + (3/1) kg O (44/1) kg CO 1 kg S + 1 kg O kg SO por lo que el oxígeno estequiométrico por kg de combustible es: ( 3 1 x 0,86) C + {( 3 4 x 0,1) - 0,01} O + (1 x 0,01) S 3,53 por lo que: Masa de aire Masa combustible H + O H O ; 4 kg H + 3 kg O 36 kg H O C + O CO ; 1 kg C + 3 kg O 44 kg CO S + O SO ; 3 kg S + 3 kg O 64 kg SO kg O { Masa de aire 1 + 0,7 1,7 } 1,7 x 3,53 kg O x 0,33 kg O 3,73 Gases de la combustión por 1 kg de combustible: ( 44 1 x 0,86) CO + ( 36 4 x 0,1) H kg O + ( x 0,01) SO + (3,53 x 0,7) O + (0,767 x 3,73) N ( ) 3,153 kg CO + 1,08 kg H O + 0,0 kg SO +,77 kg O + 18, kg N G (kg) M (kg/kg-mol) G/M (kg-mol) Nitrógeno 18, 8 0,65 0,65/0,853 0, ,18% Vapor de agua 1, ,06 0,06/0,853 0,0703 7,03% Anhidrido carbónico 3, ,0717 0,60717/0,853 0,084 8,4% Oxígeno,77 3 0,071 0,071/0,853 0,0834 8,34% Anhidrido sulfuroso 0,0 64 0,0003 0,0003/0,853 0,0004 0,04% Total... 4,73 kg 0,853 kg-mol x (G/M)/ Σ(G/M) Los porcentajes en volumen son: N 76,18 ; H O 7,03 ; CO 8,4 ; O 8,34 ; SO 0, Calcular los análisis volumétricos secos de los gases desprendidos de la combustión del alcohol etílico C H 6 O con concentraciones de mezcla de 90% y 10%. Se puede considerar que no existe oxígeno libre en el escape con la mezcla rica en combustible y que la combustión es completa con la mezcla débil en combustible. Reacción química: C H 6 O + 3 O CO + 3 H O 46 kg C H 6 O + 96 kg O 88 kg CO + 54 kg H O Relación de masa estequiométrica aire combustible G aire G comb La concentración de la mezcla se define en la forma: CM kg O 0,33 kg O 8,96 aire estequiométrico suministrado aire real suministrado MEZCLA DEL 90% DE CONCENTRACIÓN G aire 8,96 G comb 0,9 9,96 (mezcla pobre) C H 6 O + 9,96 x 0,33 x 46 3 O + 9,96 x 0,33 x 46 3 x 79 1 N CO + 3 H O + a O + b N C H 6 O + 3,336 O + 1,55 N CO + 3 H O + a O + b N Oxígeno 0,5 + 3, Equilibrio atómico: + a a 0,336 Nitrógeno 1,55 b Combustión.-5
6 El volumen total de los productos secos es: n + 0,336 +1,55 14,886 kg-mol, por lo que: x CO n CO x 100 n 14,886 13,44% ; x O n O 0,336 x 100,6% ; x n 14,886 N n N n 1,55 x ,886 84,3% MEZCLA DEL 10% DE CONCENTRACIÓN G aire 8,96 G comb 1, 7,47 7,47 x 0,33 x 46 C H 6 O + O 3 + (mezcla rica) 7,47 x 0,33 x 46 3 C H 6 O +,5 O + 9,41 N a CO + b CO + c H O + d N x 79 1 N a CO + b CO + c H O + d N Carbono a + b Equilibrio atómico: Hidrógeno 3 c a 1 ; b 1 ; c 3 Oxígeno 0,5 +,5 a + b + c El volumen total de los productos secos es: n ,41 11,41 kg-mol, por lo que: x CO n CO 1 x 100 n 11,41 8,76% ; x CO n CO 1 x 100 n 11,41 8,76% ; x N n N 9,41 x 100 8,47% n 11, Un combustible tiene de masa 84% de carbono y 16% de hidrógeno. Después de quemar el combustible con aire, el análisis volumétrico seco de los productos es: CO 10% ; CO 1% ; O 5,35%. Determinar el tanto por ciento de aire suministrado en exceso. Por cada kg de combustible se obtienen 0,84 kg de C y 0,16 kg de H. Si se suministran X kg-mol de aire (que contiene 0,1 X kg-mol de O y 0,79 X kg-mol de N ) por kg de combustible, la ecuación de la combustión en kg-mol es: 0,84 kg C kg-mol C 1 kg C + 0,16 kg H kg-mol H kg H + 0,1 X kg-mol O + 0,79 X kg-mol N Equilibrio atómico: a kg-mol CO + b kg-mol CO Carbono 0,84/1 a + b 0,07 Hidrógeno 0,16/ c 0,08 Oxígeno 0,1 X a + (b + c)/ + d Nitrógeno 0,79 X e + c kg-mol H O + d kg-mol O + e kg-mol N que junto con las ecuaciones de los balances volumétricos: a b x CO x CO 10% 1% 10 ; a d x CO x O completan el sistema de 6 ecuaciones, y 6 incógnitas cuyas soluciones son: b 0, Balance del carbono: 0,07 a + b { a 10 b } 10 b + b 11 b a 0,06364 Balance del oxígeno: 0,1 X a + b + c 0, d d 5,35 a 10 0, ,08 5,35 x 0, , ,35 1,87 + 0, ,14087 X 0,6708 kg-mol aire Como M aire 9 La relación estequiométrica es: kg-mol aire, resulta: G aire G comb 0,6708 kg-mol aire x 9 kg-mol aire 19,45 Combustión.-6
7 {0,84 G aire G comb estequiométrica existiendo un exceso de aire kg C 3 x 1 19,45-15,11 15,11 kg O kg C } + {0,16 0,33 kg O 0,87 8,7% kg H x 8 kg O kg H } 15, Una máquina utiliza un combustible gaseoso de composición volumétrica: CO 6% ; H 9% ; CH 4 38% ; CO 6% ; O 1% ; N 0%, que se quema con aire en un motor, siendo la relación volumétrica aire/combustible 7/1. Determinar la composición volumétrica de los gases de escape considerando no existe CO. Para 1 kg-mol de combustible, la ecuación química correspondiente es: 0,6 CO + 0,09 H + 0,38 CH 4 + 0,06 CO + 0,01 O + 0,0 N + (0,1 x 7) O + (0,79 x 7) N Equilibrio atómico: a CO + b H O + c O + d N Carbono 0,6 + 0,38 + 0,06 a 0,7 Hidrógeno 0,09 + 0,76 b 0,85 Oxígeno 0,13 + 0,06 + 0,01 + 1,47 a + (b / ) + c 0,7 + (0,85/ ) + c c 0,565 Nitrógeno 0, + 5,53 d 5,73 El volumen total es: n 0,7 + 0,85 +0, ,73 7,85 kg-mol, por lo que: x CO n CO 0,7 n 7, ,95% x ; x H O n H O 0,85 x ,86%; n 7,85 x O n O 0,545 n 7, ,96% x ; x N n N 5,73 x ,3% n 7, Determinar la relación de la masa estequiométrica aire/combustible para una gasolina de composición química parecida a la del hexano C 6 H 14 y el análisis volumétrico de los gases (húmedos) desprendidos en la combustión en las siguientes situaciones: a) Está presente todo el vapor de agua b) Los gases se enfrían a 1,0135 bar y 18ºC. a) La ecuación química correspondiente es C 6 H ,5 O + ( 9,5 79 x 1 ) N 6 CO + 7 H O + ( 9,5 79 x 1 ) N C 6 H ,5 O + 35,7 N 6 CO + 7 H O + 35,7 N La relación de la masa estequiométrica aire/combustible viene dada por: G aire kg-mol O 9,5 kg-mol comb 3 kg O x x x 15,17 G comb estequiométrica kg-mol comb 86 kg-mol O 0,33 kg O n ,7 48,7 kg-mol kg-mol comb x CO n CO 6 x 100 n 48,7 1,3% ; x H O n H O 7 x 100 n 48,7 14,4% ; x N n N n b) La presión del vapor de agua a 18ºC es de 0,006 bar, por lo que: x H O n H O p H O 0,006 x 100,03% n p 1, ,7 x ,7 73,3% Combustión.-7
8 n n H O + 6 CO + 35,7 N n H O 0,003 n 0,003 (n H O + 41,7) n H O 0,85 kg-mol 0, ,7 4,57 kg-mol x CO n CO 6 n 4,57 x ,1% ; x N n N 35,7 x ,90% n 4, Una muestra de gas combustible tiene el siguiente análisis volumétrico seco: CO 9,3% ; O 30,3% ; N 60,4% Cuando la mezcla de gas húmedo se enfría a 1,0 bar el vapor de agua del gas condensa a 50ºC. Determinar: a) Las presiones parciales de los constituyentes a 1,0 bar y 50ºC b) Si se considera que el combustible está formado totalmente por carbono e hidrógeno y que el vapor de agua de los gases de la combustión procede completamente de la combustión del hidrógeno del combustible, calcular los porcentajes en masa, del carbono e hidrógeno del combustible. n p H O } H 50ºC 0,133 bar O p n total x H O p total x H O 0,133 0,103 10,3% humedad 1, n H O 0,103 (n H O + n CO + n O + n N ) 0,103 n H O + 0,103 n sequedad 0,897 n H O 0,103 n sequedad n H O 0,115 n sequedad n humedad n H O + n sequedad 0,115 n sequedad + n sequedad 1,115 n sequedad deduciéndose las siguientes presiones parciales: n p CO } CO 50ºC p n total n CO p total humedad 1,115 n sequedad p O } 50ºC n O n humedad p total n O 1,115 p total n sequedad 0,093 x 1, 1,115 0,303 x 1, 1,115 0,1 bar 0,36 bar p N } 50ºC n N n humedad p total n N 1,115 p total n sequedad 0,604 x 1, 1,115 0,65 bar o también: p N } 50ºC 1, - (0,1 + 0, ,36) 0,65 bar Si llamamos Y al porcentaje de la masa de carbono del combustible y se suministran X kg-mol de aire por kg de combustible, resulta Y 1 C Y Equilibrio atómico: p CO n CO p total n p H O p total por lo que: n H O n H + X H O + 3,76 X N a CO + b H O + c O +d N a b Y/1 (1 - Y)/ 0,0834 0,1075 Carbono a Y/1 Hidrógeno b (1 - Y)/ Oxígeno X a + (b /) + c Nitrógeno 3,76 X d a a + b + c + d 0,1 1, 0,0834 b a + b + c + d 0,133 0,1075 1, 0,8117 Y 0,897 Combustión.-8
9 8.- Una caldera quema 8 Tm/ de petróleo con una dosificación de 1 kg de combustible por 0 kg de aire; los gases salen de la chimenea a una velocidad de 4,5 m/seg; el coeficiente global de pérdidas térmicas debido al paso de los gases a través de la chimenea es de 14 Kcal/hm ºC. La temperatura del medio exterior es de 0ºC. El coeficiente de gasto es, ϕ 0,3 El peso específico de los gases es, γ gases 1,315 kg/m 3 ; El peso específico del aire es, γ aire 1,88 kg/m 3 Determinar, en condiciones de gasto máximo: a) La altura H de la chimenea y la depresión existente en la misma si se supone circulación natural b) La sección transversal S de la chimenea c) El volumen de los gases evacuados RESOLUCION a) Altura de la chimenea y depresión existente en la misma, si se supone circulación natural v sal 4,5 m seg h cf g H T int - T ext T ext (con h cf en Kcal hm ºC ) Como se supone gasto máximo T int T ext x (0 + 73) 586ºK 4,5 m seg g H ,58 g H H 15,5 m Depresión existente en la chimenea si se supone circulación natural Depresión natural: Δp H (γ gases - γ aire ) 15,5 x (1,315-1,88) b)sección transversal S de la chimenea G comb (1 + ε G aire - G cenizas ) 94 ϕ S Kg ( ) 3600 seg 94 x 0,3 x S c) Volumen de los gases evacuados H (T int - T ext ) T int 15,5 (586-93) 586 V humos S x v 13,49 m x 4,5 m seg x 60 seg min m 3 minuto Kg m Kg 0,4185 m S 13,49 m ; d 4,144 m ******* 9.- Una caldera debe producir kg/ de vapor saturado a la presión de 0 kg/cm y temperatura de saturación T s 11,4ºC, tomando el agua de alimentación a 15ºC, y quemando hulla de potencia calorífica 7800 Kcal/kg, de composición: C 0,78 ; H 0,055 ; O 0,07 ; cenizas 0,07 ; humedad 0,03 El coeficiente de transmisión de calor para el agua es, h C agua 5000 Kcal/h.m.ºC El coeficiente de transmisión de calor para los humos es, h C humos 40 Kcal/h.m.ºC El coeficiente de conductividad del hierro es, k 50 Kcal/m.h.ºC Espesor de la caldera, e 10 mm Coeficiente de exceso de aire, ε 1,4 Calor específico medio de los humos, c p(humos) 0,7 Kcal/kgºC Temperatura de la sala de calderas, 0ºC Pérdidas por radiación al exterior, δ 0,1 Determinar a) El peso de los gases producidos por cada kg de carbón b) La temperatura media de los gases de la cámara de combustión c) La temperatura de los humos al principio de la superficie de calefacción d) La cantidad de combustible quemado por e) El coeficiente complejo U de transmisión del calor Combustión.-9
10 f) La temperatura de los gases al final de la superficie de calefacción. g) La superficie de calefacción RESOLUCION a) Peso de los gases producidos por cada kg de carbón: G gases 1 + 4,34 ε (,67 C + 8 H + S - O) - G cenizas 1 + ε G aire - G cenizas G aire 4,34 (,67 C + 8 H + S - O) G gases 1 + (1,4 x 10,47) - 0,07 15,59 Kg Kg aire 1 Kg combustible Kg gases 1 Kg combustible 4,34 x {(,67 x 0,78) + (8 x 0,05) + 0-0,07} 10,47 Kg aire 1 Kg combustible b) Temperatura media de los gases de la cámara de combustión (T ext es la temperatura del medio exterior 0ºC): (1 - δ) P ci (1 + ε G aire - G cen ) c p(humos) (T caldera - T ext ) δ es el tanto por uno de las pérdidas por radiación al exterior (1-0,1) x 7800 Kcal (1 - δ) P T caldera ci 1 Kg comb + T (1 + ε G aire - G cenizas ) c ext + 0ºC 1687ºC p(humos) Kg gases 15,59 1 Kg comb x 0,7 Kcal Kg gases ºC c) Temperatura de los humos al principio de la superficie de calefacción.- En esta situación no hay pérdidas por radiación: 7800 Kcal T humos P ci 1 Kg comb + T (1 + ε G aire - G cenizas ) c ext + 0ºC 1873ºC p(humos) Kg gases 15,59 1 Kg comb x 0,7 Kcal Kg gases ºC d) La cantidad de combustible quemado por Kg vapor Kg vapor (i vapor sat - i agua alimentación ) 7800 Kcal Kg comb G comb η 7800 (668,5-15) Kcal Kg vapor 7800 Kcal Kg comb G comb x 0,9 e) Coeficiente U de transmisión del calor (pared plana) U e 1 39,37 h Chumos k + 1 h Cvapor , Kcal hm ºC Kcal Kg comb G comb (1 - δ) G comb 931 Kg comb f) Temperatura de los gases al final de la superficie de calefacción (A es la superficie de calefacción). - U A T final T sat + ( T inicial - T sat ) exp ( ) G aire c p( humos) G comb g) Superficie A de calefacción Q kg vapor - 39,37 A 11,4ºC + ( ,4)ºC exp( ) 11, ,6 exp (- 0,01 A) 15,59 x 0,7 x 931 ( i vapor - i agua alim. ) Kcal kg vapor (668,5-15) 6, Kcal Q U A ΔT - ΔT 1 ln ΔT ΔT 1 por lo que: ΔT ,4 1661,6 ΔT 1 T final - 15 T final 11, ,6 exp (- 0,01 A) 39,37 A (1676,6 - T final ) 6, (ln 39, ,6 T final - 15 ) Kcal m hºc A 1661,6 - T final ,6 ln T final , Kcal Combustión.-10
11 conforman un sistema de dos ecuaciones con dos incógnitas, cuya solución es: A 173,7 m y T final 500ºC ********* 10.- En una instalación térmica se han de quemar 1,8 Tm/ de un combustible líquido, de composición química, C 1 H 3, en exceso de aire, ε 1,5. Determinar a) La potencia calorífica superior e inferior de este combustible b) El aire necesario para la combustión, teniendo en cuenta el exceso de aire. c) La sección transversal y la altura de la chimenea que ha de evacuar los gases de la combustión, siendo la relación, diámetro/altura 1/0, en condiciones de tiro máximo, sabiendo que la temperatura y presión de la atmósfera son 15ºC, y 760 mm de Hg respectivamente. El coeficiente de velocidad es,ϕ 0,5. RESOLUCION a)potencia calorífica superior e inferior de este combustible 0,86 x Potencia calorífica superior del combustible: P cs ,138 x Potencia calorífica inferior del combustible: P ci Kcal/ b) Aire necesario para la combustión, teniendo en cuenta el exceso de aire C 1 H ,75 O 1 CO + 11,5 H O {(1 x 1) + 3} C 1 H ,75 (16 x ) O 1 (1 + 3) CO + 11,5 ( + 16) H O {167} C 1 H 3 + {568} O {58} CO + {07} H O Aire: 1% O ; 79% N ; Nitrógeno 79 x ,7 (unidades en peso de N 1 ) 167 es a 568 N º de kg de O por 1 kg de combustible: G como 1 es a G O 3,401 O por lo que: 1 es a 0,1 k O como G aire es a 3,401 G aire 16,196 kg O Kcal Como hay un exceso de aire (1,5) serán necesarios, 16,196 x 1,5 4,3 por 1 ustible. c) La sección transversal y la altura de la chimenea que ha de evacuar los gases de la combustión, siendo la relación, diámetro/altura 1/0, en condiciones de tiro máximo, sabiendo que la temperatura y presión de la atmósfera son 15ºC, y 760 mm de Hg respectivamente. El coeficiente de velocidad es,ϕ 0,5. G comb (1 + ε G aire - G cenizas ) ϕ S H (T int - T ext ) T int T int T ext x ( ) 576ºK ; T ext ºK 1800 ( kg/ ) (1 + 4,3-0 ) 3600 π D H 18,7 4 D H 1 0 H 0 D 94 x 0,5 S π D 4 H (576-88) D 18,7 S H 18,7 D 1,934 m H 0 D 38,7 m ******* 11.- Un hidrocarburo líquido tiene la siguiente composición química en masa, C 84,7% ; H 15,5%, y se le hace arder, inyectándole en un hogar de una caldera, con un 50% de exceso de aire. Determinar a) La composición química de los humos producidos Combustión.-11
12 b) La potencia calorífica superior e inferior de este combustible c) Cómo variará el poder calorífico superior, si la humedad del combustible aumenta hasta el 1%? d) Si los humos producidos tienen una temperatura de 80ºC cuando se les introduce en la chimenea, y se sabe que el coeficiente de gasto de la misma es, ϕ 0,, cuál será la relación que deberá existir entre la sección transversal S de la chimenea, y su altura H, sabiendo que la temperatura del medio ambiente es de 0ºC? RESOLUCION a) Composición química de los humos producidos 100 gramos de hidrocarburo se componen de: 84,7 1 7,05 moles de C ; 15,3 7,65 moles de H Ecuaciones de la combustión: C + O CO H + 1 O H O La combustión teórica de 100 gramos de hidrocarburo necesita: Para el C: 7,05 moles de O producen 7,05 moles de CO Para el H : 7,65 moles de O producen 7,65 moles de H O por lo que es necesario utilizar. 7,05 + 3,85 10,875 moles de O, lo cual supone que en los humos habrá un contenido de N dado por: 10,875 x ,91 moles de N Como la combustión se realiza con un 50% de exceso de aire, resulta que: Oxígeno: 10,875 x 0,5 5,437 moles que pasan a los humos Aire: Nitrógeno: 40,91 x 0,5 0,455 moles que habrá que sumar a los 40,91 61,36 moles Los porcentajes de humos húmedos de la combustión real de 100 gramos de hidrocarburo son: Composición en volumen de los humos: De otra forma: C x 84,7 H y 15,3 C x + H y 100 CO 7,05 moles CO 7,05/81,505 8,65% O 5,44 moles O 5,44/81,505 6,67% H O 7,65 moles H O 7,65/81,505 9,38% N 61,365 moles N 61,35/81,505 75,3% 1 x + y 100 Fórmula aproximada, (C 7,05 H 15,3 ) n ó C 1 H 6 CO 1,87 C 1,583 O mín 1,87 C + 5,6 H,44 m 3 kg O comb O en exceso (ε - 1) O mín 0,5 x,44 1, H O 11, H 1,713 N 79 1 O 13,76 Humos 18,76 m 3 Kg comb x 7,058 y 15,3 m 3 ; Composición en volumen de los humos: CO kg 1,583 x 100 8,65% comb 18,76 m 3 ; Comp. en vol. humos: O 1, x 100 6,67% 18,76 m 3 ; Composición en volumen de los humos: H O 1,713 x 100 9,38% 18,76 m 3 ; Composición en volumen de los humos: N kg 13,76 x ,3% comb 18,76 b) Potencia calorífica superior e inferior de este combustible P c sup 8080 C H S Como la fórmula aproximada es, C 1 H 6, tendremos, para 1 mol: C 1 x gramos/mol ; H 6 gramos/mol ; Total, 170 gramos/mol Combustión.-1
13 por lo que: C x ,847 ; H x , P c sup (8.080 x 0,847) + ( x 0,153) Kcal Kg P c inf P c sup - {(9 x H x ) + w} x (9 x 0, ) x Kcal Kg c) Variación del poder calorífico superior, si la humedad del combustible aumenta hasta el 1% Composición química con 1% de humedad: Potencia calorífica superior: x 1-0,1 1 C 84,7% x 0,88 74,536% H 15,37% x 0,88 13,464% Humedad: 1% Kcal Kg Potencia calorífica inferior: x 0, Kcal Kg un total del 100% d) Si los humos producidos tienen una temperatura de 80ºC cuando se les introduce en la chimenea, y se sabe que el coeficiente de gasto de la misma es ϕ 0,, cuál será la relación que deberá existir entre la sección transversal S de la chimenea, y su altura H, sabiendo que la temperatura del medio ambiente es de 0ºC? Kg de aire G aire 4,3 {(,67 x 0,847) + (8 x 0,153)} x 1,5,69 Kg combustible G comb (1 + ε G aire - G cenizas ) ϕ S H (T int - T ext ) T int G comb (1 +,69-0) x 0, S H (80-0) 80 siendo G comb el nº de kg/ de combustible a quemar. 0,01 G comb S H ********* Combustión.-13
BALANCE TÉRMICO EN CALDERAS
 BALANCE TÉRMICO EN CALDERAS 1. Definición: Es el registro de la distribución de energía en un equipo. Puede registrarse en forma de tablas o gráficos, lo que permite una mejor visualización de la situación.
BALANCE TÉRMICO EN CALDERAS 1. Definición: Es el registro de la distribución de energía en un equipo. Puede registrarse en forma de tablas o gráficos, lo que permite una mejor visualización de la situación.
Análisis esquemático simplificado de una torre de enfriamiento.
 Análisis esquemático simplificado de una torre de enfriamiento. En el diagrama el aire con una humedad Y 2 y temperatura t 2 entra por el fondo de la torre y la abandona por la parte superior con una humedad
Análisis esquemático simplificado de una torre de enfriamiento. En el diagrama el aire con una humedad Y 2 y temperatura t 2 entra por el fondo de la torre y la abandona por la parte superior con una humedad
ANEXO 9: ESTUDIO DE LA INCENERACIÓN
 ANEXO 9: ESTUDIO DE LA INCENERACIÓN 108 1.8. ESTUDIO Y RESULTADOS DE LA INCINERACIÓN DE LOS RESIDUOS. 1.8.1. Cantidad teórica de aire en combustión neutra Si tenemos en cuenta que los principales elementos
ANEXO 9: ESTUDIO DE LA INCENERACIÓN 108 1.8. ESTUDIO Y RESULTADOS DE LA INCINERACIÓN DE LOS RESIDUOS. 1.8.1. Cantidad teórica de aire en combustión neutra Si tenemos en cuenta que los principales elementos
QUÍMICA 2º Bachillerato Ejercicios: Cálculos en Química
 1(8) Ejercicio nº 1 Se dispone de tres recipientes que contienen 1 litro de metano gas, dos litros de nitrógeno gas y 1,5 litros de ozono gas, respectivamente, en las mismas condiciones de presión y temperatura.
1(8) Ejercicio nº 1 Se dispone de tres recipientes que contienen 1 litro de metano gas, dos litros de nitrógeno gas y 1,5 litros de ozono gas, respectivamente, en las mismas condiciones de presión y temperatura.
EJERCICIOS DE EQUILIBRIO QUÍMICO.
 EJERCICIOS DE EQUILIBRIO QUÍMICO. 1º. A partir de 150 g de acético se desean obtener 166 g de acetato de etilo. Calcular los gramos de etanol que se necesitan sabiendo que la K c de la reacción de esterificación
EJERCICIOS DE EQUILIBRIO QUÍMICO. 1º. A partir de 150 g de acético se desean obtener 166 g de acetato de etilo. Calcular los gramos de etanol que se necesitan sabiendo que la K c de la reacción de esterificación
CONCEPTOS BÁSICOS EN QUÍMICA
 CONCEPTOS BÁSICOS EN QUÍMICA MOLES, ÁTOMOS Y MOLÉCULAS 1.-/ Calcule la masa molar de las siguientes sustancias: a) Disulfuro de carbono. b) Óxido de nitrógeno (III). c) Hidróxido de berilio. d) Carbonato
CONCEPTOS BÁSICOS EN QUÍMICA MOLES, ÁTOMOS Y MOLÉCULAS 1.-/ Calcule la masa molar de las siguientes sustancias: a) Disulfuro de carbono. b) Óxido de nitrógeno (III). c) Hidróxido de berilio. d) Carbonato
EJERCICIOS DE TERMODINÁMICA
 EJERCICIOS DE TERMODINÁMICA. La descomposición del tetraóxido de nitrógeno ( N O 4 NO4( NO( ocurre espontáneamente a temperaturas altas. Los datos termodinámicos a 98ºK se incluyen en la tabla adjunta.
EJERCICIOS DE TERMODINÁMICA. La descomposición del tetraóxido de nitrógeno ( N O 4 NO4( NO( ocurre espontáneamente a temperaturas altas. Los datos termodinámicos a 98ºK se incluyen en la tabla adjunta.
Estequiometría. En química, la estequiometría (del griego "στοιχειον"
 Estequiometría En química, la estequiometría (del griego "στοιχειον" = stoicheion (elemento) y "μετρον"=métron, (medida) es el cálculo de las relaciones cuantitativas entre reactivos y productos en el
Estequiometría En química, la estequiometría (del griego "στοιχειον" = stoicheion (elemento) y "μετρον"=métron, (medida) es el cálculo de las relaciones cuantitativas entre reactivos y productos en el
9. PROCESO DE COMBUSTIÓN
 9. PROCESO DE COMBUSTIÓN La gran mayoría de los procesos de generación de energía, implica la utilización de algunas fuentes de energía, las cuales al combustionarse producen reacciones químicas como es
9. PROCESO DE COMBUSTIÓN La gran mayoría de los procesos de generación de energía, implica la utilización de algunas fuentes de energía, las cuales al combustionarse producen reacciones químicas como es
FÍSICA Y QUÍMICA 1º Bachillerato Ejercicios: Sistemas Físicos y Químicos
 1(7) Ejercicio nº 1 Una muestra de sulfuro de hierro de 60,5 g contiene 28 g de azufre. Cuál es la fórmula empírica de dicho compuesto? Ejercicio nº 2 150 g de un compuesto contienen 45,65 g de nitrógeno
1(7) Ejercicio nº 1 Una muestra de sulfuro de hierro de 60,5 g contiene 28 g de azufre. Cuál es la fórmula empírica de dicho compuesto? Ejercicio nº 2 150 g de un compuesto contienen 45,65 g de nitrógeno
Método del polo de operación (III) - Extracción
 Método del polo de operación (III) - Extracción Problemas Se desea tratar 1000 kg /h de un lodo que contiene 0,20 fracción másica de aceite (A), sin benceno (C). El solvente que entra a 662 kg/h es benceno
Método del polo de operación (III) - Extracción Problemas Se desea tratar 1000 kg /h de un lodo que contiene 0,20 fracción másica de aceite (A), sin benceno (C). El solvente que entra a 662 kg/h es benceno
Tema 2. Estequiometría
 Tema 2. Estequiometría Masas Atómicas Escala del carbono 12 Masas atómicas relativas Concepto de mol Relaciones de masa de las fórmulas químicas Composición centesimal Fórmula empírica. Fórmula molecular
Tema 2. Estequiometría Masas Atómicas Escala del carbono 12 Masas atómicas relativas Concepto de mol Relaciones de masa de las fórmulas químicas Composición centesimal Fórmula empírica. Fórmula molecular
TEMA 4: BALANCES DE ENERGÍA. IngQui-4 [1]
![TEMA 4: BALANCES DE ENERGÍA. IngQui-4 [1] TEMA 4: BALANCES DE ENERGÍA. IngQui-4 [1]](/thumbs/40/22050892.jpg) TEMA 4: BALANCES DE ENERGÍA IngQui-4 [1] OBJETIVOS! Aplicar la ecuación de conservación al análisis de la energía involucrada en un sistema.! Recordar las componentes de la energía (cinética, potencial
TEMA 4: BALANCES DE ENERGÍA IngQui-4 [1] OBJETIVOS! Aplicar la ecuación de conservación al análisis de la energía involucrada en un sistema.! Recordar las componentes de la energía (cinética, potencial
Butano(g) -124,7 Dióxido de carbono(g) -393 Agua(l) -286
 1.- Dada la reacción de combustión del butano: Butano(g) + oxígeno (g) ======== dióxido de carbono(gas) + agua (gas) Sabiendo que es una reacción exotérmica, indica si a la misma temperatura, el calor
1.- Dada la reacción de combustión del butano: Butano(g) + oxígeno (g) ======== dióxido de carbono(gas) + agua (gas) Sabiendo que es una reacción exotérmica, indica si a la misma temperatura, el calor
EXAMEN TEÓRICO PARA LA OBTENCIÓN DEL CARNÉ DE OPERADOR INDUSTRIAL DE CALDERAS NOMBRE Y APELLIDOS:
 EXAMEN TEÓRICO PARA LA OBTENCIÓN DEL CARNÉ DE OPERADOR INDUSTRIAL DE CALDERAS NOMBRE Y APELLIDOS: DNI.: Madrid, 14 de marzo de 2015 FIRMA DEL INTERESADO OBSERVACIONES IMPORTANTES: - Para cada pregunta
EXAMEN TEÓRICO PARA LA OBTENCIÓN DEL CARNÉ DE OPERADOR INDUSTRIAL DE CALDERAS NOMBRE Y APELLIDOS: DNI.: Madrid, 14 de marzo de 2015 FIRMA DEL INTERESADO OBSERVACIONES IMPORTANTES: - Para cada pregunta
PROBLEMAS DE INGENIERÍA TÉRMICA
 PROBLEMAS DE INGENIERÍA TÉRMICA pferadezdiez.es Pedro Ferádez Díez Carlos Reedo Estébaez Pedro R. FerádezGarcía PROBLEMAS SOBRE COMBUSTIÓN pferadezdiez.es E los cálculos estequiométricos hay que distiguir
PROBLEMAS DE INGENIERÍA TÉRMICA pferadezdiez.es Pedro Ferádez Díez Carlos Reedo Estébaez Pedro R. FerádezGarcía PROBLEMAS SOBRE COMBUSTIÓN pferadezdiez.es E los cálculos estequiométricos hay que distiguir
Ejercicios de repaso
 Ejercicios de repaso 1. (2001) Tenemos 250 ml de una disolución de KOH 0 2 M. a) Cuántos moles de KOH hay disueltos? b) Cuántos gramos de KOH hay disueltos? c) Describa el procedimiento e indique el material
Ejercicios de repaso 1. (2001) Tenemos 250 ml de una disolución de KOH 0 2 M. a) Cuántos moles de KOH hay disueltos? b) Cuántos gramos de KOH hay disueltos? c) Describa el procedimiento e indique el material
FÍSICA Y QUÍMICA 1º Bachillerato Ejercicios: Estequiometría
 1(7) Ejercicio nº 1 El acetileno o etino (C 2 H 2 ) arde en el aire con llama muy luminosa. a) Qué volumen de acetileno, medido en c.n. será preciso utilizar si en esta reacción se han obtenido 100 litros
1(7) Ejercicio nº 1 El acetileno o etino (C 2 H 2 ) arde en el aire con llama muy luminosa. a) Qué volumen de acetileno, medido en c.n. será preciso utilizar si en esta reacción se han obtenido 100 litros
TEMA 12. PSICROMETRÍA
 Termodinámica Aplicada Ingeniería Química TEMA 12. PSICROMETRÍA TEMA 12: PSICROMETRÍA BLOQUE II. Análisis termodinámico de procesos industriales PROCESOS INDUSTRIALES ANÁLISIS PROCESOS CALOR TRABAJO POTENCIA
Termodinámica Aplicada Ingeniería Química TEMA 12. PSICROMETRÍA TEMA 12: PSICROMETRÍA BLOQUE II. Análisis termodinámico de procesos industriales PROCESOS INDUSTRIALES ANÁLISIS PROCESOS CALOR TRABAJO POTENCIA
QUIM 3004 PROBLEMAS RESUELTOS - PROPIEDADES COLIGATIVAS
 UNIVERSIDAD DE PUERTO RICO EN HUMACAO DEPARTAMENTO DE QUÍMICA (http://www.uprh.edu/~quimgen) QUIM 3004 PROBLEMAS RESUELTOS - PROPIEDADES COLIGATIVAS Ejemplo #1 PRESIÓN DE VAPOR DE UNA DISOLUCIÓN DE COMPONENTES
UNIVERSIDAD DE PUERTO RICO EN HUMACAO DEPARTAMENTO DE QUÍMICA (http://www.uprh.edu/~quimgen) QUIM 3004 PROBLEMAS RESUELTOS - PROPIEDADES COLIGATIVAS Ejemplo #1 PRESIÓN DE VAPOR DE UNA DISOLUCIÓN DE COMPONENTES
TIPOS DE REACCIONES QUIMICAS
 Liceo Polivalente Juan Antonio Ríos Quinta Normal Unidad temática: Disoluciones Químicas. GUÍA DE APRENDIZAJE Nº 6 2º MEDIO SOLUCIONES 2ª parte Objetivo General:Conocer conceptos de las disoluciones en
Liceo Polivalente Juan Antonio Ríos Quinta Normal Unidad temática: Disoluciones Químicas. GUÍA DE APRENDIZAJE Nº 6 2º MEDIO SOLUCIONES 2ª parte Objetivo General:Conocer conceptos de las disoluciones en
TEORICO-PRÁCTICO N 5: LEYES DE LOS GASES IDEALES
 TEORICO-PRÁCTICO N 5: LEYES DE LOS GASES IDEALES FUNDAMENTO TEÓRICO: La materia puede estar en tres estados: sólido, líquido y gaseoso. Los gases, no tienen forma ni volumen fijo, las fuerzas que mantienen
TEORICO-PRÁCTICO N 5: LEYES DE LOS GASES IDEALES FUNDAMENTO TEÓRICO: La materia puede estar en tres estados: sólido, líquido y gaseoso. Los gases, no tienen forma ni volumen fijo, las fuerzas que mantienen
Problemas de Química (1ero Grado de Química). Tema 1.
 Problemas de Química (1ero Grado de Química). Tema 1. CÁLCULOS BÁSICOS 1. Expresa en notación científica, indicando en cada caso el número de cifras significativas: a) 258292 b) 1804, 5289 c) 0, 48 d)
Problemas de Química (1ero Grado de Química). Tema 1. CÁLCULOS BÁSICOS 1. Expresa en notación científica, indicando en cada caso el número de cifras significativas: a) 258292 b) 1804, 5289 c) 0, 48 d)
UDELAR Tecnología y Servicios Industriales 1
 (2017) Ejercicio 1 Determinar composición de humos, gasto de aire y gasto de humos húmedos y semihúmedos en las siguientes combustiones estequiométricas: a) Fuel oil de composición en peso: C = 84,4% H
(2017) Ejercicio 1 Determinar composición de humos, gasto de aire y gasto de humos húmedos y semihúmedos en las siguientes combustiones estequiométricas: a) Fuel oil de composición en peso: C = 84,4% H
Facultad de Ciencias Fisicomatemáticas e Ingeniería VAPOR - EXERGÍA
 Cátedra: Termodinámica - Ing. Civil e Ing. Ambiental Docente/s: Ing. José Contento / Ing. Jorge Rosasco Guía de trabajos prácticos Nº 6 VAPOR - EXERGÍA.- En un recipiente de paredes rígidas y adiabáticas,
Cátedra: Termodinámica - Ing. Civil e Ing. Ambiental Docente/s: Ing. José Contento / Ing. Jorge Rosasco Guía de trabajos prácticos Nº 6 VAPOR - EXERGÍA.- En un recipiente de paredes rígidas y adiabáticas,
GUÍA DE EJERCICIOS DE ESTEQUIOMETRÍA. 1. Igualar las siguientes ecuaciones mediante el método algebraico.
 1 GUÍA DE EJERCICIOS DE ESTEQUIOMETRÍA 1. Igualar las siguientes ecuaciones mediante el método algebraico. a) P 4 + KOH + H 2 O KH 2 PO 2 + PH 3 b) Co 2+ + NH 4 + + NH 3 + O 2 H 2 O + (Co(NH 3 ) 6 ) 3+
1 GUÍA DE EJERCICIOS DE ESTEQUIOMETRÍA 1. Igualar las siguientes ecuaciones mediante el método algebraico. a) P 4 + KOH + H 2 O KH 2 PO 2 + PH 3 b) Co 2+ + NH 4 + + NH 3 + O 2 H 2 O + (Co(NH 3 ) 6 ) 3+
H2SO4 (aq)+ NaOH (aq) Na2SO4 (aq)+ H2O (líq)
 1. Calcular la pureza (en %) de una muestra de carburo de calcio (CaC 2) sabiendo que al tratar 2,056 g de éste con agua se obtiene hidróxido de calcio y 656 ml de acetileno (C2H2) medidos a 22º C y 730
1. Calcular la pureza (en %) de una muestra de carburo de calcio (CaC 2) sabiendo que al tratar 2,056 g de éste con agua se obtiene hidróxido de calcio y 656 ml de acetileno (C2H2) medidos a 22º C y 730
UNIDAD: 7 ESTEQUIOMETRÍA
 UNIDAD: 7 ESTEQUIOMETRÍA CONCEPTOS BÁSICOS DE ESTEQUIOMETRÍA RECOPILÓ: QUIM. GABRIEL JIMENEZ ZERON TOMADO DEL TEMA ESTEQUIOMETRIA www.wikipedia.org Estequiometría El termino estequiometría proviene del
UNIDAD: 7 ESTEQUIOMETRÍA CONCEPTOS BÁSICOS DE ESTEQUIOMETRÍA RECOPILÓ: QUIM. GABRIEL JIMENEZ ZERON TOMADO DEL TEMA ESTEQUIOMETRIA www.wikipedia.org Estequiometría El termino estequiometría proviene del
RELACIÓN DE PROBLEMAS. DISOLUCIONES Y PROPIEDADES COLIGATIVAS.
 RELACIÓN DE PROBLEMAS. Y PROPIEDADES COLIGATIVAS. 1.- Se disuelven 150 gramos de etanol (CH 3 CH 2 OH), de densidad 0,8 g /cm 3, en agua hasta completar 0,5 litros de disolución. Calcular el porcentaje
RELACIÓN DE PROBLEMAS. Y PROPIEDADES COLIGATIVAS. 1.- Se disuelven 150 gramos de etanol (CH 3 CH 2 OH), de densidad 0,8 g /cm 3, en agua hasta completar 0,5 litros de disolución. Calcular el porcentaje
4. TEORÍA ATÓMICO-MOLECULAR
 4. TEORÍA ATÓMICO-MOLECULAR Sustancias que reaccionan 1. Explica qué son los procesos o cambios físicos y pon ejemplos de ellos. Los procesos o cambios físicos no producen modificaciones en la naturaleza
4. TEORÍA ATÓMICO-MOLECULAR Sustancias que reaccionan 1. Explica qué son los procesos o cambios físicos y pon ejemplos de ellos. Los procesos o cambios físicos no producen modificaciones en la naturaleza
1010 DEPARTAMENTO DE FÍSICA Y QUÍMICA 2º Bachillerato QUÍMICA
 1.- La constante de equilibrio, K p, para la siguiente reacción química: C 2 H 4 (g) + H 2 (g) C 2 H 6 (g), vale 5 x 10 17, a 25º C. Calcula, a la misma temperatura, el valor de K c. Solución: K c = 1,22
1.- La constante de equilibrio, K p, para la siguiente reacción química: C 2 H 4 (g) + H 2 (g) C 2 H 6 (g), vale 5 x 10 17, a 25º C. Calcula, a la misma temperatura, el valor de K c. Solución: K c = 1,22
(g) CO 2. (g) + 2 H 2. Procediendo en la misma forma con la segunda ecuación, obtenemos: (g) 3 CO 2. (g) + 4 H 2
 Para ajustar el oxígeno, escribiremos otro dos delante de la molécula de oxígeno gaseoso en los reactivos. De este modo, la ecuación ajustada del primer proceso es: CH (g) + 2 O 2 (g) CO 2 (g) + 2 H 2
Para ajustar el oxígeno, escribiremos otro dos delante de la molécula de oxígeno gaseoso en los reactivos. De este modo, la ecuación ajustada del primer proceso es: CH (g) + 2 O 2 (g) CO 2 (g) + 2 H 2
FÓRMULAS EMPÍRICA Y MOLECULAR
 FÓRMULAS EMPÍRICA Y MOLECULAR 1.- Un cierto compuesto X está formado por un 33,3% del elemento A y un 66,7% del elemento B. Cuántos gramos de X se formarán cuando se mezclan 3,98 gramos de A con 6,23 gramos
FÓRMULAS EMPÍRICA Y MOLECULAR 1.- Un cierto compuesto X está formado por un 33,3% del elemento A y un 66,7% del elemento B. Cuántos gramos de X se formarán cuando se mezclan 3,98 gramos de A con 6,23 gramos
PROBLEMAS RESUELTOS SELECTIVIDAD ANDALUCÍA 2015 QUÍMICA TEMA 4: ENERGÍA DE LAS REACCIONES QUÍMICAS
 PROBLEMAS RESUELTOS SELECTIVIDAD ANDALUCÍA 15 QUÍMICA TEMA 4: ENERGÍA DE LAS REACCIONES QUÍMICAS Junio, Ejercicio 6, Opción B Reserva 1, Ejercicio 3, Opción B Reserva, Ejercicio 6, Opción A Reserva 3,
PROBLEMAS RESUELTOS SELECTIVIDAD ANDALUCÍA 15 QUÍMICA TEMA 4: ENERGÍA DE LAS REACCIONES QUÍMICAS Junio, Ejercicio 6, Opción B Reserva 1, Ejercicio 3, Opción B Reserva, Ejercicio 6, Opción A Reserva 3,
misma naturaleza, de las entradas de aire parásito en la cámara de combustión, etc. Suele oscilar, en nuestro caso, entre un 15% y un 25%.
 51 4.- LA COMBUSTIÓN DE SUBSTANCIAS ORGÁNICAS 4.1.- CRITERIOS DE TIPO QUÍMICO Los combustibles generalmente utilizados en los hornos de elaboración de vidrios industriales, están formados por mezclas de
51 4.- LA COMBUSTIÓN DE SUBSTANCIAS ORGÁNICAS 4.1.- CRITERIOS DE TIPO QUÍMICO Los combustibles generalmente utilizados en los hornos de elaboración de vidrios industriales, están formados por mezclas de
1.- Se disuelven 180 gramos de NaOH en 400 gramos de agua, resultando un volumen de 432,836 ml. Determinar:
 1.- Se disuelven 180 gramos de NaOH en 400 gramos de agua, resultando un volumen de 432,836 ml. Determinar: a. La densidad de la disolución b. La concentración de NaOH en gramos por litro c. La concentración
1.- Se disuelven 180 gramos de NaOH en 400 gramos de agua, resultando un volumen de 432,836 ml. Determinar: a. La densidad de la disolución b. La concentración de NaOH en gramos por litro c. La concentración
EJERCICIOS DE TERMOQUÍMICA.
 EJERCICIOS DE TERMOQUÍMICA. 1º.- A temperatura ambiente, el calor de formación del dióxido de carbono es de -94.030 cal/mol, y el calor de combustión del monóxido de carbono es de -67.410 cal/mol. Calcular
EJERCICIOS DE TERMOQUÍMICA. 1º.- A temperatura ambiente, el calor de formación del dióxido de carbono es de -94.030 cal/mol, y el calor de combustión del monóxido de carbono es de -67.410 cal/mol. Calcular
Química 2º Bachillerato Termoquímica
 I. E. S. Atenea. Departamento de Física y Química 1 Química 2º Bachillerato Termoquímica 1. Calcular la variación de energía interna para la reacción de combustión del benceno (C 6 H 6 ) si el proceso
I. E. S. Atenea. Departamento de Física y Química 1 Química 2º Bachillerato Termoquímica 1. Calcular la variación de energía interna para la reacción de combustión del benceno (C 6 H 6 ) si el proceso
Tema 0. Conceptos Básicos en Química. Química Átomo: números másicos y atómicos Mol Fórmulas Reacciones químicas Gases Disoluciones
 Tema 0. Conceptos Básicos en Química Química Átomo: números másicos y atómicos Mol Fórmulas Reacciones químicas Gases Disoluciones Qué es la Química? Ciencia que trata de la composición y propiedades de
Tema 0. Conceptos Básicos en Química Química Átomo: números másicos y atómicos Mol Fórmulas Reacciones químicas Gases Disoluciones Qué es la Química? Ciencia que trata de la composición y propiedades de
Quemadores. Ahorro energético con seguridad. Combustión Quemadores digitales Emisiones de NOx Variación de velocidad Control de O2 Caso práctico
 Quemadores Ahorro energético con seguridad Combustión Quemadores digitales Emisiones de NOx Variación de velocidad Control de O2 Caso práctico 1 Combustión Combustión eficiente y segura 2 COMBUSTIÓN: Equilibrio
Quemadores Ahorro energético con seguridad Combustión Quemadores digitales Emisiones de NOx Variación de velocidad Control de O2 Caso práctico 1 Combustión Combustión eficiente y segura 2 COMBUSTIÓN: Equilibrio
Unidades de masa atómica
 Unidades de masa atómica La estructura química y las fórmulas químicas sirven para estudiar las relaciones de masa de átomos y moléculas. Estas relaciones ayudan a explicar la composición de los compuestos
Unidades de masa atómica La estructura química y las fórmulas químicas sirven para estudiar las relaciones de masa de átomos y moléculas. Estas relaciones ayudan a explicar la composición de los compuestos
UDELAR Tecnología y Servicios Industriales 1
 Ejercicio 1 Determinar composición de humos, gasto de aire y gasto de humos húmedos y semihúmedos en las siguientes combustiones estequiométricas: a) Fuel oil de composición en peso: C = 84,4% H = 11%
Ejercicio 1 Determinar composición de humos, gasto de aire y gasto de humos húmedos y semihúmedos en las siguientes combustiones estequiométricas: a) Fuel oil de composición en peso: C = 84,4% H = 11%
Las ecuaciones químicas
 Las reacciones químicas se representan escribiendo las fórmulas de los reactivos en el primer miembro de una ecuación y las de los productos en el segundo. El signo igual se sustituye por una flecha (
Las reacciones químicas se representan escribiendo las fórmulas de los reactivos en el primer miembro de una ecuación y las de los productos en el segundo. El signo igual se sustituye por una flecha (
de una reacción n en la cual, tanto reactivos como productos están n en condiciones estándar (p = 1 atm; ; T = 298 K = 25 ºC;
 Entalpía a estándar de la reacción Es el incremento entálpico de una reacción n en la cual, tanto reactivos como productos están n en condiciones estándar (p = 1 atm; ; T = 298 K = 25 ºC; conc.. = 1 M).
Entalpía a estándar de la reacción Es el incremento entálpico de una reacción n en la cual, tanto reactivos como productos están n en condiciones estándar (p = 1 atm; ; T = 298 K = 25 ºC; conc.. = 1 M).
Ejercicios de QUÍMICA (2ºBachillerato) Tema 0. REVISIÓN DE CONCEPTOS BÁSICOS [1]
![Ejercicios de QUÍMICA (2ºBachillerato) Tema 0. REVISIÓN DE CONCEPTOS BÁSICOS [1] Ejercicios de QUÍMICA (2ºBachillerato) Tema 0. REVISIÓN DE CONCEPTOS BÁSICOS [1]](/thumbs/40/20756584.jpg) Ejercicios de QUÍMICA (2ºBachillerato) Tema 0. REVISIÓN DE CONCEPTOS BÁSICOS [1] [1]. Calcula: (a) La masa de un átomo de potasio. (b) El número de átomos de fósforo que hay en 2 g de este elemento. (c)
Ejercicios de QUÍMICA (2ºBachillerato) Tema 0. REVISIÓN DE CONCEPTOS BÁSICOS [1] [1]. Calcula: (a) La masa de un átomo de potasio. (b) El número de átomos de fósforo que hay en 2 g de este elemento. (c)
Ley de conservación de la masa (Ley de Lavoisier) La suma de las masas de los reactivos es igual a la suma de las masas de los productos de la
 Prof.- Juan Sanmartín 4º E.S.O ESO 1 3 Ley de conservación de la masa (Ley de Lavoisier) La suma de las masas de los reactivos es igual a la suma de las masas de los productos de la reacción, es decir,
Prof.- Juan Sanmartín 4º E.S.O ESO 1 3 Ley de conservación de la masa (Ley de Lavoisier) La suma de las masas de los reactivos es igual a la suma de las masas de los productos de la reacción, es decir,
Reactivos limitantes UNIDAD 3: ESTEQUIOMETRÍA
 Reactivos limitantes En muchos procesos industriales la cantidad de productos que se obtenga dependerá de la cantidad de materias iniciales con las que se cuente. Por ejemplo, si deseas fabricar bicicletas,
Reactivos limitantes En muchos procesos industriales la cantidad de productos que se obtenga dependerá de la cantidad de materias iniciales con las que se cuente. Por ejemplo, si deseas fabricar bicicletas,
EL MOL. MOL: cantidad de materia que tiene 6,022.10 23 partículas, es decir, el número de Avogadro de partículas
 EL MOL MOL: cantidad de materia que tiene 6,022.10 23 partículas, es decir, el número de Avogadro de partículas MOL DE ATOMOS: 6,022.10 23 átomos MOL DE MOLÉCULAS 6,022.10 23 moléculas 1 mol de átomos
EL MOL MOL: cantidad de materia que tiene 6,022.10 23 partículas, es decir, el número de Avogadro de partículas MOL DE ATOMOS: 6,022.10 23 átomos MOL DE MOLÉCULAS 6,022.10 23 moléculas 1 mol de átomos
si con 24 g de magnesio reaccionan 6 g de oxígeno pues con 6 g reaccionarán x
 Hoja número 1. 1) Si 24 g de magnesio se combinan exactamente con 16 g de oxígeno para formar óxido de magnesio, a) cuántos gramos de óxido se habrán formado?; b) a partir de 6 g de magnesio cuántos gramos
Hoja número 1. 1) Si 24 g de magnesio se combinan exactamente con 16 g de oxígeno para formar óxido de magnesio, a) cuántos gramos de óxido se habrán formado?; b) a partir de 6 g de magnesio cuántos gramos
Departamento de Formación formacion.iad.ctcd@juntadeandalucia.es DOCUMENTACIÓN
 Departamento de Formación formacion.iad.ctcd@juntadeandalucia.es DOCUMENTACIÓN 200607101 APLICACIÓN DE LAS ENERGÍAS RENOVABLES EN LAS INSTALACIONES TÉRMICAS DE PISCINAS CUBIERTAS Dimensionamiento de las
Departamento de Formación formacion.iad.ctcd@juntadeandalucia.es DOCUMENTACIÓN 200607101 APLICACIÓN DE LAS ENERGÍAS RENOVABLES EN LAS INSTALACIONES TÉRMICAS DE PISCINAS CUBIERTAS Dimensionamiento de las
Se entiende por disolución toda mezcla homogénea de dos o más componentes en proporción variable.
 6. DISOLUCIONES 6.1. Generalidades Se entiende por disolución toda mezcla homogénea de dos o más componentes en proporción variable. Las disoluciones objeto de nuestro estudio serán binarias, en las que
6. DISOLUCIONES 6.1. Generalidades Se entiende por disolución toda mezcla homogénea de dos o más componentes en proporción variable. Las disoluciones objeto de nuestro estudio serán binarias, en las que
ESTEQUIOMETRÍA I. ÁTOMO Mínima porción de materia que posee aún las propiedades del elemento.
 ESTEQUIOMETRÍA I Preparado por: José del c. Mondragón C. El término estequiometría deriva del griego steicheion, que significa primer principio o elemento y de metron, que significa medida. La estequiometría
ESTEQUIOMETRÍA I Preparado por: José del c. Mondragón C. El término estequiometría deriva del griego steicheion, que significa primer principio o elemento y de metron, que significa medida. La estequiometría
UNIVERSIDAD LIBRE FACULTAD DE INGENIERÌA DEPARTAMENTO DE CIENCIAS BÁSICAS GUIA DE CLASE No 8
 UNIVERSIDAD LIBRE FACULTAD DE INGENIERÌA DEPARTAMENTO DE CIENCIAS BÁSICAS GUIA DE CLASE No 8 NOMBRE DE LA ASIGNATURA TÍTULO DURACIÓN BIBLIOGRAFÍA SUGERIDA DOCENTES Química General UNIDADES QUÍMICAS Y ESTEQUIOMETRÍA
UNIVERSIDAD LIBRE FACULTAD DE INGENIERÌA DEPARTAMENTO DE CIENCIAS BÁSICAS GUIA DE CLASE No 8 NOMBRE DE LA ASIGNATURA TÍTULO DURACIÓN BIBLIOGRAFÍA SUGERIDA DOCENTES Química General UNIDADES QUÍMICAS Y ESTEQUIOMETRÍA
ENERGÍA DE LAS REACCIONES QUÍMICAS. TERMOQUÍMICA
 ENERGÍA DE LAS REACCIONES QUÍMICAS. TERMOQUÍMICA Problemas 1. El calor de combustión del ácido acético(l) es 874 kj/mol. Sabiendo que las entalpías de formación estándar del CO 2 (g), H 2 O(l) son respectivamente:
ENERGÍA DE LAS REACCIONES QUÍMICAS. TERMOQUÍMICA Problemas 1. El calor de combustión del ácido acético(l) es 874 kj/mol. Sabiendo que las entalpías de formación estándar del CO 2 (g), H 2 O(l) son respectivamente:
UNA ONG ESPERA TU RESPUESTA, ATIÉNDELA PARA QUE PUEDA AYUDAR A OTROS OPCIÓN A
 UNA ONG ESPERA TU RESPUESTA, ATIÉNDELA PARA QUE PUEDA AYUDAR A OTROS OPCIÓN A CUESTIÓN.- Cuál de las siguientes reacciones nunca será espontánea independientemente del valor de la temperatura?, cuál será
UNA ONG ESPERA TU RESPUESTA, ATIÉNDELA PARA QUE PUEDA AYUDAR A OTROS OPCIÓN A CUESTIÓN.- Cuál de las siguientes reacciones nunca será espontánea independientemente del valor de la temperatura?, cuál será
Interacción aire - agua. Termómetro húmedo
 Interacción aire - agua. Termómetro húmedo Objetivos de la práctica! Obtener experimentalmente la denominada temperatura húmeda.! Estudiar las magnitudes psicrométricas de dos corrientes de aire húmedo,
Interacción aire - agua. Termómetro húmedo Objetivos de la práctica! Obtener experimentalmente la denominada temperatura húmeda.! Estudiar las magnitudes psicrométricas de dos corrientes de aire húmedo,
Fundamentos de Química 1er Curso de los Grados en Ingeniería de los Recursos Energéticos y de los Recursos Mineros 1
 Departamento de Ingeniería Química y Química Inorgánica Universidad de Cantabria (SPAIN) Fundamentos de Química 1er Curso de los Grados en Ingeniería de los Recursos Energéticos y de los Recursos Mineros
Departamento de Ingeniería Química y Química Inorgánica Universidad de Cantabria (SPAIN) Fundamentos de Química 1er Curso de los Grados en Ingeniería de los Recursos Energéticos y de los Recursos Mineros
1. Introducción: la leyes de la Termodinámica (Gianc. 17.1)
 Tema 2: Termodinámica 1. Introducción: las leyes de la termodinámica. 2. Equilibrio y temperatura. 3. Gases y temperatura absoluta 4. Gases ideales y disoluciones. 5. Energía interna y velocidades moleculares.
Tema 2: Termodinámica 1. Introducción: las leyes de la termodinámica. 2. Equilibrio y temperatura. 3. Gases y temperatura absoluta 4. Gases ideales y disoluciones. 5. Energía interna y velocidades moleculares.
Formas de expresar la concentración de disoluciones. Química General II 2011
 Formas de expresar la concentración de disoluciones Química General II 2011 Concentración de las disoluciones Es la cantidad de soluto presente en cierta cantidad de disolución. Fracción que se busca Porcentaje
Formas de expresar la concentración de disoluciones Química General II 2011 Concentración de las disoluciones Es la cantidad de soluto presente en cierta cantidad de disolución. Fracción que se busca Porcentaje
Cantidad de sustancia. Gases. Disoluciones.
 1. ÁTOMOS Y MOLÉCULAS. MOLES 1.1. En 68 gramos de amoniaco, calcular: a) el número de moléculas de amoniaco; b) el número de átomos que hay en total; c) el número de moléculas de hidrógeno y nitrógeno.
1. ÁTOMOS Y MOLÉCULAS. MOLES 1.1. En 68 gramos de amoniaco, calcular: a) el número de moléculas de amoniaco; b) el número de átomos que hay en total; c) el número de moléculas de hidrógeno y nitrógeno.
Tema 13: La materia Ciencias Naturales 1º ESO página 1. Materia es todo aquello que posee masa y ocupa un volumen. Está formada de partículas muy
 Tema 13: La materia Ciencias Naturales 1º ESO página 1 TEMA 13: LA MATERIA, BASE DEL UNIVERSO 1. Qué es materia? Materia es todo aquello que posee masa y ocupa un volumen. Está formada de partículas muy
Tema 13: La materia Ciencias Naturales 1º ESO página 1 TEMA 13: LA MATERIA, BASE DEL UNIVERSO 1. Qué es materia? Materia es todo aquello que posee masa y ocupa un volumen. Está formada de partículas muy
Ud 5: Cálculos en circuitos neumáticos.
 4 Ud 5: Cálculos en circuitos neumáticos. Presión absoluta y relativa. Presión relativa, es el valor de la presión indicado por un manómetro, tomando como referencia cero la presión atmosférica ( Pat )
4 Ud 5: Cálculos en circuitos neumáticos. Presión absoluta y relativa. Presión relativa, es el valor de la presión indicado por un manómetro, tomando como referencia cero la presión atmosférica ( Pat )
de aire. Determinar la composicion de la mezcla resultante. Cuál es el porcentaje en exceso de aire, suponiendo conversion completa?
 C A P Í T U L O 2 Dada la importancia que tienen los procesos de combustión en la generación de contaminantes, en este capítulo se han incluido algunos ejercicios relacionados con la combustión estequiométrica.
C A P Í T U L O 2 Dada la importancia que tienen los procesos de combustión en la generación de contaminantes, en este capítulo se han incluido algunos ejercicios relacionados con la combustión estequiométrica.
Transformaciones de las energías
 Transformaciones de las energías 1. Introducción La energía se puede definir como la capacidad para realizar trabajo. En el momento actual y debido al alto bienestar de la sociedad, el consumo de energía
Transformaciones de las energías 1. Introducción La energía se puede definir como la capacidad para realizar trabajo. En el momento actual y debido al alto bienestar de la sociedad, el consumo de energía
PROBLEMAS RESUELTOS SELECTIVIDAD ANDALUCÍA 2009 QUÍMICA TEMA 4: ENERGÍA DE LAS REACCIONES QUÍMICAS
 PROBLEMAS RESUELTOS SELECTIVIDAD ANDALUCÍA 9 QUÍMICA TEMA 4: ENERGÍA DE LAS REACCIONES QUÍMICAS Junio, Ejercicio 6, Opción A Reserva 1, Ejercicio 5, Opción B Reserva, Ejercicio 4, Opción A Reserva, Ejercicio
PROBLEMAS RESUELTOS SELECTIVIDAD ANDALUCÍA 9 QUÍMICA TEMA 4: ENERGÍA DE LAS REACCIONES QUÍMICAS Junio, Ejercicio 6, Opción A Reserva 1, Ejercicio 5, Opción B Reserva, Ejercicio 4, Opción A Reserva, Ejercicio
UNIDADES DE CONCENTRACIÓN
 Colegio San Esteban Diácono Departamento de Ciencias Química IIº Medio Prof. Juan Pastrián / Sofía Ponce de León UNIDADES DE CONCENTRACIÓN 1. Porcentaje masa/masa (%m/m) Cantidad en masa (g) de un componente
Colegio San Esteban Diácono Departamento de Ciencias Química IIº Medio Prof. Juan Pastrián / Sofía Ponce de León UNIDADES DE CONCENTRACIÓN 1. Porcentaje masa/masa (%m/m) Cantidad en masa (g) de un componente
2
 1 2 3 4 5 6 7 8 9 10 11 12 13 EJERCICIOS TERMOQUÍMICA TEORÍA 1. a) Define energía interna (U). b) Qué es una variable de estado. c) Qué es una variable intensiva y extensiva. 2. a) Que es la entalpía.
1 2 3 4 5 6 7 8 9 10 11 12 13 EJERCICIOS TERMOQUÍMICA TEORÍA 1. a) Define energía interna (U). b) Qué es una variable de estado. c) Qué es una variable intensiva y extensiva. 2. a) Que es la entalpía.
Alternativas de Ahorro en Plantas Térmicas.
 Alternativas de Ahorro en Plantas Térmicas. 1. Introducción El objetivo de este artículo es llamar la atención sobre las interesantes alternativas existentes, para reducir los costos operacionales en Plantas
Alternativas de Ahorro en Plantas Térmicas. 1. Introducción El objetivo de este artículo es llamar la atención sobre las interesantes alternativas existentes, para reducir los costos operacionales en Plantas
DIVERTIDISIMOS EJERCICIOS PARA NAVIDAD (I)
 COLEGIO HISPANO-INGLÉS DIVERTIDISIMOS EJERCICIOS PARA NAVIDAD (I) NOMBRE: DPTO.FÍSICA-QUÍMICA CURSO:1º DE BACH A y B 1.- Un hidrocarburo gaseoso contenido en un matraz de 500 ml en condiciones normales
COLEGIO HISPANO-INGLÉS DIVERTIDISIMOS EJERCICIOS PARA NAVIDAD (I) NOMBRE: DPTO.FÍSICA-QUÍMICA CURSO:1º DE BACH A y B 1.- Un hidrocarburo gaseoso contenido en un matraz de 500 ml en condiciones normales
Descripción de los 3 estados de la materia. Química General II Estado Gaseoso
 Descripción de los 3 estados de la materia Química General II Estado Gaseoso Clasificación de los Estados de la Materia. Gases Líquidos Sólidos 1. Carecen de forma definida, llenan completamente el recipiente.
Descripción de los 3 estados de la materia Química General II Estado Gaseoso Clasificación de los Estados de la Materia. Gases Líquidos Sólidos 1. Carecen de forma definida, llenan completamente el recipiente.
TERMODINÁMICA 1. En la fermentación de la glucosa (C6H12O6) se obtiene etanol (C2H5OH) y CO2. Si la entalpía de combustión de la glucosa es de 15.
 TERMODINÁMICA 1. En la fermentación de la glucosa (C6H12O6) se obtiene etanol (C2H5OH) y CO2. Si la entalpía de combustión de la glucosa es de 15.63 kj/g y la del etanol es de 29.72 kj/g, a) Calcular la
TERMODINÁMICA 1. En la fermentación de la glucosa (C6H12O6) se obtiene etanol (C2H5OH) y CO2. Si la entalpía de combustión de la glucosa es de 15.63 kj/g y la del etanol es de 29.72 kj/g, a) Calcular la
Resolución de Cuestiones
 La cantidad en Química 1 Cuestión 1 Resolución de Cuestiones Sabiendo que la masa molecular de hidrógeno es 2 y la del oxígeno 32, conteste razonadamente a las siguientes cuestiones: a) Qué ocupará más
La cantidad en Química 1 Cuestión 1 Resolución de Cuestiones Sabiendo que la masa molecular de hidrógeno es 2 y la del oxígeno 32, conteste razonadamente a las siguientes cuestiones: a) Qué ocupará más
CAPÍTULO FUNDICIÓN Y COLADA
 FUNDICIÓN Y COLADA CAPÍTULO 1 1.1. Definición 1.. Conceptos de colada 1.. Cálculo del tiempo de llenado y de solidificación 1.4. Cálculo de mazarotas 1.5. Cálculo de moldes 1.6. Cálculo de la presión de
FUNDICIÓN Y COLADA CAPÍTULO 1 1.1. Definición 1.. Conceptos de colada 1.. Cálculo del tiempo de llenado y de solidificación 1.4. Cálculo de mazarotas 1.5. Cálculo de moldes 1.6. Cálculo de la presión de
PIU SABATINO SERIE I QUÍMICA COORDINACIÓN DE QUÍMICA Y LABORATORIOS
 PIU SABATINO SERIE I QUÍMICA COORDINACIÓN DE QUÍMICA Y LABORATORIOS 1. De acuerdo a la posición de los elementos en la tabla periódica, cuál de los siguientes compuestos será el más iónico? a) NaCl b)
PIU SABATINO SERIE I QUÍMICA COORDINACIÓN DE QUÍMICA Y LABORATORIOS 1. De acuerdo a la posición de los elementos en la tabla periódica, cuál de los siguientes compuestos será el más iónico? a) NaCl b)
TEMA 5 CINÉTICA QUÍMICA
 TEMA 5 CINÉTICA QUÍMICA ÍNDICE 1. Cinética Química 2. Orden de reacción 3. Mecanismo de las reacciones químicas 4. Factores que influyen en la velocidad de reacción 5. Teoría de las reacciones químicas
TEMA 5 CINÉTICA QUÍMICA ÍNDICE 1. Cinética Química 2. Orden de reacción 3. Mecanismo de las reacciones químicas 4. Factores que influyen en la velocidad de reacción 5. Teoría de las reacciones químicas
PROBLEMAS RESUELTOS SELECTIVIDAD ANDALUCÍA 2009 QUÍMICA TEMA 1: LA TRANSFORMACIÓN QUÍMICA
 PROBLEMAS RESUELTOS SELECTIVIDAD ANDALUCÍA 009 QUÍMICA TEMA 1: LA TRANSFORMACIÓN QUÍMICA Junio, Ejercicio 4, Opción A Reserva 1, Ejercicio 6, Opción A Reserva 1, Ejercicio, Opción B Reserva, Ejercicio,
PROBLEMAS RESUELTOS SELECTIVIDAD ANDALUCÍA 009 QUÍMICA TEMA 1: LA TRANSFORMACIÓN QUÍMICA Junio, Ejercicio 4, Opción A Reserva 1, Ejercicio 6, Opción A Reserva 1, Ejercicio, Opción B Reserva, Ejercicio,
PROBLEMAS RESUELTOS SELECTIVIDAD ANDALUCÍA 2015 QUÍMICA TEMA 1: LA TRANSFORMACIÓN QUÍMICA
 PROBLEMAS RESUELTOS SELECTIVIDAD ANDALUCÍA 015 QUÍMICA TEMA 1: LA TRANSFORMACIÓN QUÍMICA Junio, Ejercicio, Opción B Reserva 1, Ejercicio 5, Opción A Reserva 1, Ejercicio 5, Opción B Reserva, Ejercicio
PROBLEMAS RESUELTOS SELECTIVIDAD ANDALUCÍA 015 QUÍMICA TEMA 1: LA TRANSFORMACIÓN QUÍMICA Junio, Ejercicio, Opción B Reserva 1, Ejercicio 5, Opción A Reserva 1, Ejercicio 5, Opción B Reserva, Ejercicio
EJERCICIOS TECNOLOGÍA INDUSTRIAL I EJERCICIO 1
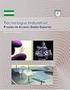 EJERCICIOS TECNOLOGÍA INDUSTRIAL I EJERCICIO 1 EJERCICIO 2 En el siguiente circuito calcular: 1. La intensidad de corriente total 2. La intensidad que circula por cada rama 3. La energía disipada por la
EJERCICIOS TECNOLOGÍA INDUSTRIAL I EJERCICIO 1 EJERCICIO 2 En el siguiente circuito calcular: 1. La intensidad de corriente total 2. La intensidad que circula por cada rama 3. La energía disipada por la
GASES - PREGUNTAS DE TEST
 GASES - PREGUNTAS DE TEST A - CONCEPTOS GENERALES B - LEYES GENERALES DE LOS GASES IDEALES: C- LEY DE GRAHAM DE LA DIFUSIÓN D- TEORÍA CINÉTICA A - CONCEPTO DE GAS-VAPOR A-1 - Un vapor es A - Cualquier
GASES - PREGUNTAS DE TEST A - CONCEPTOS GENERALES B - LEYES GENERALES DE LOS GASES IDEALES: C- LEY DE GRAHAM DE LA DIFUSIÓN D- TEORÍA CINÉTICA A - CONCEPTO DE GAS-VAPOR A-1 - Un vapor es A - Cualquier
CONTENIDOS BÁSICOS. HIPÓTESIS DE AVOGADRO, CANTIDAD DE MATERIA, LEY DE LOS GASES IDEALES.
 CONTENIDOS BÁSICOS. HIPÓTESIS DE AVOGADRO, CANTIDAD DE MATERIA, LEY DE LOS GASES IDEALES. CUESTIONES E1S2013 La fórmula molecular del azúcar común o azúcar de mesa (sacarosa) es C12H22O11. Indique razonadamente
CONTENIDOS BÁSICOS. HIPÓTESIS DE AVOGADRO, CANTIDAD DE MATERIA, LEY DE LOS GASES IDEALES. CUESTIONES E1S2013 La fórmula molecular del azúcar común o azúcar de mesa (sacarosa) es C12H22O11. Indique razonadamente
PROCESOS DE COMBUSTIÓN
 1 ACTIVIDAD DE APRENDIZAJE Nº 05 PROCESOS DE COMBUSTIÓN I. COMBUSTIÓN La combustión no es más que una reacción química de oxidación, en la que normalmente se va a liberar una gran cantidad de calor (energía).
1 ACTIVIDAD DE APRENDIZAJE Nº 05 PROCESOS DE COMBUSTIÓN I. COMBUSTIÓN La combustión no es más que una reacción química de oxidación, en la que normalmente se va a liberar una gran cantidad de calor (energía).
RECOMENDACIÓN UIT-R P.836-1 VAPOR DE AGUA: DENSIDAD EN LA SUPERFICIE Y CONTENIDO DE COLUMNA TOTAL. (Cuestión UIT-R 201/3)
 Rec. UIT-R P.836-1 1 RECOMENDACIÓN UIT-R P.836-1 VAPOR DE AGUA: DENSIDAD EN LA SUPERFICIE Y CONTENIDO DE COLUMNA TOTAL (Cuestión UIT-R 201/3) Rec. UIT-R P.836-1 (1992-1997) La Asamblea de Radiocomunicaciones
Rec. UIT-R P.836-1 1 RECOMENDACIÓN UIT-R P.836-1 VAPOR DE AGUA: DENSIDAD EN LA SUPERFICIE Y CONTENIDO DE COLUMNA TOTAL (Cuestión UIT-R 201/3) Rec. UIT-R P.836-1 (1992-1997) La Asamblea de Radiocomunicaciones
Los gases de la combustión
 Los gases de la combustión El incremento de todo tipo de combustión es un agente contaminante del ambiente con concentraciones siempre mayores de polución. La formación de humos, la lluvia ácida y el aumento
Los gases de la combustión El incremento de todo tipo de combustión es un agente contaminante del ambiente con concentraciones siempre mayores de polución. La formación de humos, la lluvia ácida y el aumento
Principios del corte Oxicorte
 Aspectos Químicos del Corte por Oxígeno Principios del corte Oxicorte El corte por oxígeno se basa en la capacidad del oxígeno para combinarse con el hierro cuando éste se calienta hasta su temperatura
Aspectos Químicos del Corte por Oxígeno Principios del corte Oxicorte El corte por oxígeno se basa en la capacidad del oxígeno para combinarse con el hierro cuando éste se calienta hasta su temperatura
Universidad Nacional Experimental Politécnica Antonio José de Sucre Vicerrectorado Barquisimeto Departamento de Ingeniería Química Ingeniería Química
 Universidad Nacional Experimental Politécnica Antonio José de Sucre Vicerrectorado Barquisimeto Departamento de Ingeniería Química Ingeniería Química Guía de Ejercicios. Unidad II. Prof: Juan E. Rodríguez
Universidad Nacional Experimental Politécnica Antonio José de Sucre Vicerrectorado Barquisimeto Departamento de Ingeniería Química Ingeniería Química Guía de Ejercicios. Unidad II. Prof: Juan E. Rodríguez
Química 2º Bacharelato
 Química 2º Bacharelato DEPARTAMENTO DE FÍSICA E QUÍMICA Termodinámica química 13/12/07 Nombre: Problemas 1. a) Calcula qué calor se desprende en la combustión de 20,0 cm 3 de etanol líquido a presión atmosférica
Química 2º Bacharelato DEPARTAMENTO DE FÍSICA E QUÍMICA Termodinámica química 13/12/07 Nombre: Problemas 1. a) Calcula qué calor se desprende en la combustión de 20,0 cm 3 de etanol líquido a presión atmosférica
DIFERENCIA ENTRE FLUIDOS Y SÓLIDOS
 DIFERENCIA ENTRE FLUIDOS Y SÓLIDOS Se le llama fluido a toda aquella sustancia continua que puede fluir. Los fluidos pueden ser gaseosos y líquidos. Esta es la diferencia fundamental entre un sólido, cuya
DIFERENCIA ENTRE FLUIDOS Y SÓLIDOS Se le llama fluido a toda aquella sustancia continua que puede fluir. Los fluidos pueden ser gaseosos y líquidos. Esta es la diferencia fundamental entre un sólido, cuya
TEMA 10. CICLOS DE POTENCIA DE GAS Y OTROS CICLOS DE POTENCIA
 Termodinámica Aplicada Ingeniería Química TEMA 10. CICLOS DE POTENCIA DE GAS Y OTROS CICLOS DE POTENCIA TEMA 10: CICLOS DE POTENCIA DE GAS Y OTROS CICLOS BLOQUE II. Análisis termodinámico de procesos industriales
Termodinámica Aplicada Ingeniería Química TEMA 10. CICLOS DE POTENCIA DE GAS Y OTROS CICLOS DE POTENCIA TEMA 10: CICLOS DE POTENCIA DE GAS Y OTROS CICLOS BLOQUE II. Análisis termodinámico de procesos industriales
CLASE 10 BALANCE DE MASA CON REACCIONES QÚÍMICAS Y COMBUSTIÓN
 CLASE 10 BALANCE DE MASA CON REACCIONES QÚÍMICAS Y COMBUSTIÓN Universidad de la Costa, C.U.C. Programa de Ingeniería Ambiental Asignatura: Diseño de Plantas Industriales PROFESOR: JORGE ENRIQUE CALDERÓN
CLASE 10 BALANCE DE MASA CON REACCIONES QÚÍMICAS Y COMBUSTIÓN Universidad de la Costa, C.U.C. Programa de Ingeniería Ambiental Asignatura: Diseño de Plantas Industriales PROFESOR: JORGE ENRIQUE CALDERÓN
PRÁCTICA 16 ESTEQUIOMETRÍA DE LAS REACCIONES QUÍMICAS 1.- FUNDAMENTO TEÓRICO.
 PRÁCTICA 16 ESTEQUIOMETRÍA DE LAS REACCIONES QUÍMICAS 1.- FUNDAMENTO TEÓRICO. En esta práctica se dirigirá la atención hacia el concepto de reacción química. Toda reacción es una transformación de la materia
PRÁCTICA 16 ESTEQUIOMETRÍA DE LAS REACCIONES QUÍMICAS 1.- FUNDAMENTO TEÓRICO. En esta práctica se dirigirá la atención hacia el concepto de reacción química. Toda reacción es una transformación de la materia
Tema 3: Ecuaciones químicas y concentraciones
 Tema 3: Ecuaciones químicas y concentraciones Definición de disolución. Clases de disoluciones. Formas de expresar la concentración de una disolución. Proceso de dilución. Solubilidad. Diagramas de fases
Tema 3: Ecuaciones químicas y concentraciones Definición de disolución. Clases de disoluciones. Formas de expresar la concentración de una disolución. Proceso de dilución. Solubilidad. Diagramas de fases
TRABAJO PRÁCTICO N 2 DETERMINACIÓN DE DENSIDADES
 0 TRABAJO PRÁCTICO N 2 DETERMINACIÓN DE DENSIDADES a) Determinación de la densidad de hidrógeno Objetivos Determinar la densidad de un gas Conceptos Gases ideales, presión de vapor, rendimiento, pureza,
0 TRABAJO PRÁCTICO N 2 DETERMINACIÓN DE DENSIDADES a) Determinación de la densidad de hidrógeno Objetivos Determinar la densidad de un gas Conceptos Gases ideales, presión de vapor, rendimiento, pureza,
UNIVERSIDAD NACIONAL EXPERIMENTAL POLITECNICA ANTONIO JOSÉ DE SUCRE VICERRECTORADO BARQUISIMETO DEPARTAMENTO DE INGENIERÍA QUÍMICA QUÍMICA GENERAL
 UNIERSIDAD NACIONAL EXERIMENAL OLIECNICA ANONIO JOSÉ DE SUCRE ICERRECORADO BARQUISIMEO DEARAMENO DE INGENIERÍA QUÍMICA QUÍMICA GENERAL UNIDAD I CLASE Nº EL ESADO GASEOSO GAS REAL Gas erfecto: es aquel
UNIERSIDAD NACIONAL EXERIMENAL OLIECNICA ANONIO JOSÉ DE SUCRE ICERRECORADO BARQUISIMEO DEARAMENO DE INGENIERÍA QUÍMICA QUÍMICA GENERAL UNIDAD I CLASE Nº EL ESADO GASEOSO GAS REAL Gas erfecto: es aquel
EJERCICIOS RESUELTOS DE EQUILIBRIO QUIMICO
 EJERIIOS RESUELTOS DE EQUILIBRIO QUIMIO 1. uando el cloruro amónico se calienta a 75º en un recipiente cerrado de 1,0 litro, se descompone dando lugar a cloruro de hidrógeno gaseoso y amoniaco gaseoso
EJERIIOS RESUELTOS DE EQUILIBRIO QUIMIO 1. uando el cloruro amónico se calienta a 75º en un recipiente cerrado de 1,0 litro, se descompone dando lugar a cloruro de hidrógeno gaseoso y amoniaco gaseoso
ESTABLECE FUENTES ESTACIONARIAS A LAS QUE LES SON APLICABLES LAS NORMAS DE EMISIÓN DE MONÓXIDO DE CARBONO CO) Y DIÓXIDO DE AZUFRE (SO2)
 Resolución Exenta 2.063 SEREMI Región Metrpolitana, Ministerio Salud Promulgación: 26.01.2005 Publicación Diario Oficial: 02.02.2005 Original: ESTABLECE FUENTES ESTACIONARIAS A LAS QUE LES SON APLICABLES
Resolución Exenta 2.063 SEREMI Región Metrpolitana, Ministerio Salud Promulgación: 26.01.2005 Publicación Diario Oficial: 02.02.2005 Original: ESTABLECE FUENTES ESTACIONARIAS A LAS QUE LES SON APLICABLES
TEMA 5: RECURSOS NATURALES
 TEMA 5: RECURSOS NATURALES ÍNDICE 1. DEFINICIÓN RECURSO NATURAL Qué es un recurso natural? De dónde se obtienen los recursos naturales? Qué consecuencias tiene su explotación? IMPACTO AMBIENTAL 2. TIPOS
TEMA 5: RECURSOS NATURALES ÍNDICE 1. DEFINICIÓN RECURSO NATURAL Qué es un recurso natural? De dónde se obtienen los recursos naturales? Qué consecuencias tiene su explotación? IMPACTO AMBIENTAL 2. TIPOS
Balances de Masa. CI4102 Ingeniería Ambiental Profesor Marcelo Olivares A.
 Balances de Masa CI4102 Ingeniería Ambiental Profesor Marcelo Olivares A. Principio de Conservacion de Masa El concepto de continuidad o de conservación de masa es uno de los más fundamentales en ingeniería....la
Balances de Masa CI4102 Ingeniería Ambiental Profesor Marcelo Olivares A. Principio de Conservacion de Masa El concepto de continuidad o de conservación de masa es uno de los más fundamentales en ingeniería....la
IES Atenea (S.S. de los Reyes) Departamento de Física y Química. PAU Química. Septiembre 2010. Fase general OPCIÓN A
 1 PAU Química. Septiembre 2010. Fase general OPCIÓN A Cuestión 1A. Considerando el elemento alcalinotérreo del tercer periodo y el segundo elemento del grupo de los halógenos: a) Escriba sus configuraciones
1 PAU Química. Septiembre 2010. Fase general OPCIÓN A Cuestión 1A. Considerando el elemento alcalinotérreo del tercer periodo y el segundo elemento del grupo de los halógenos: a) Escriba sus configuraciones
El agua calentada en microondas se enfría más rápido?
 El agua calentada en microondas se enfría más rápido? Primera parte Experiencia de Laboratorio, Física experimental II, 2009 Larregain, Pedro pedrolarregain@yahoo.com Machado, Alejandro machado.alejandro@yahoo.com
El agua calentada en microondas se enfría más rápido? Primera parte Experiencia de Laboratorio, Física experimental II, 2009 Larregain, Pedro pedrolarregain@yahoo.com Machado, Alejandro machado.alejandro@yahoo.com
