Determinación de propiedades de transporte en membranas de intercambio iónico
|
|
|
- Eduardo Alvarado Crespo
- hace 6 años
- Vistas:
Transcripción
1 Recuperación de metales por técnicas electroquímicas y procesos de membranas para la producción de materiales nanoestructurados Determinación de propiedades de transporte en membranas de Valentín Pérez Herranz Departamento de Ingeniería Química y Nuclear. Instituto de Seguridad Industrial, Radiofísica y Medioambiental. Universidad Politécnica de Valencia.
2 Recuperación de metales por técnicas electroquímicas y procesos de membranas para la producción de materiales nanoestructurados Universidad Politécnica de Valencia Tres campus, en Valencia, Gandía y Alcoy. 13 Escuelas y Facultades 42 Departamentos 23 Institutos de Investigación 4 Institutos Mixtos o Concertados 12 Centros de Investigación Alumnos
3 Recuperación de metales por técnicas electroquímicas y procesos de membranas para la producción de materiales nanoestructurados DEPARTAMENTO DE INGENIERÍA QUÍMICA Y NUCLEAR Encargado de coordinar las enseñanzas de una o varias áreas de conocimiento y de apoyar las iniciativas docentes o investigadoras del profesorado. Elabora los programas de las asignaturas que imparte, y propone las metodologías docentes y los sistemas de evaluación. ÁREA DE INGENIERÍA QUÍMICA (44 profesores) Ingeniería Química Ingeniería Industrial ÁREA DE INGENIERÍA NUCLEAR (12 profesores) Ingeniería Energética Ingeniería Industrial
4 Recuperación de metales por técnicas electroquímicas y procesos de membranas para la producción de materiales nanoestructurados MASTER EN SEGURIDAD INDUSTRIAL Y MEDIO AMBIENTE Módulo Obligatorio (18 ECTS) Módulo de Medio Ambiente Industrial (18 ECTS) Complementos Formativos (12 ECTS) Prácticas en Empresa (12 ECTS) Movilidad (12 ECTS) Módulo de Seguridad Nuclear (18 ECTS) Complementos Formativos (12 ECTS) Trabajo Fin de Master (12 ECTS) DOCTORADO: INGENIERÍA Y PRODUCCIÓN INDUSTRIAL
5 Recuperación de metales por técnicas electroquímicas y procesos de membranas para la producción de materiales nanoestructurados INSTITUTO DE SEGURIDAD INDUSTRIAL, RADIOFÍSICA Y MEDIOAMBIENTAL (ISIRYM) SEGURIDAD NUCLEAR Y BIOINGENIERÍA DE LA RADIACIÓN IONIZANTE (20 Investigadores) PROCESOS DE MEMBRANA, TRATAMIENTO DE EFLUENTES LÍQUIDOS Y OPTIMIZACIÓN (20 Investigadores) INGENIERÍA ELECTROQUÍMICA Y CORROSIÓN (20 Investigadores)
6 Recuperación de metales por técnicas electroquímicas y procesos de membranas para la producción de materiales nanoestructurados LINEAS DE INVESTIGACIÓN Corrosión estática y dinámica Corrosión de aceros inoxidables altamente aleados a elevadas temperaturas Biocorrosión-biotribocorrosión Generación de hidrógeno y pilas de combustible Revalorización de efluentes industriales mediante técnicas electroquímicas
7 1. Introducción. 2. Principio de exclusión de Donnan. 3. Números de transferencia o de transporte. 4. Polarización por concentración y densidad de corriente límite.
8 1. INTRODUCCIÓN Determinación de propiedades de transporte en membranas de Membranas de Intercambio Iónico. Son polímeros con grupos ácido o base disociables en la cadena polimérica. Membranas Catiónicas. Contienen grupos aniónicos fijos en una matriz polimérica que están en equilibrio con cationes móviles en el sistema de poros del polímero de tal forma que se mantiene la electroneutralidad. Contienen grupos como: -SO 3-, -COO -, PO 3 2-, PO 3 H -, C 6 H 4 O -, etc. Membranas Aniónicas. Contienen grupos catiónicos fijos en una matriz polimérica que están en equilibrio con aniones móviles en el sistema de poros del polímero. Contienen grupos como: -NH 3+, -NRH 2+, -NR 3+, -PR 3+, -SR 2+.
9 1. INTRODUCCIÓN Determinación de propiedades de transporte en membranas de Membranas Catiónicas. Membranas Aniónicas. C + C + C + C + C + + C + - C + C A + - C + C + C + C + C + C + C + C + C + C + C + - C + + C + C + C + C + C + C +
10 2. PRINCIPIO DE EXCLUSIÓN DE DONNAN Cl - Na + Cl - Na + Cl - Na + Na + Cl - Cl - Na + Na + Na + Cl - Na + Cl - Na + Na + Na + Cl - Cl - Na + Na + Na + Cl - Na + El potencial electroquímico de una especie i en la disolución ha de ser igual al potencial electroquímico de esa especie en la membrana. s i m i
11 2. PRINCIPIO DE EXCLUSIÓN DE DONNAN El potencial electroquímico de una especie i se compone del potencial químico y del potencial eléctrico: Si no hay diferencias de presión entre la disolución y la membrana, el potencial químico viene dado por: Por tanto, en el equilibrio: Si el estado de referencia es el mismo en la disolución y en la membrana: Potencial de Donnan
12 2. PRINCIPIO DE EXCLUSIÓN DE DONNAN Cl - Na + Cl - Na + Cl - Na + Na + Cl - Cl - Na + Na + Na + Cl - Na + Cl - Na + Na + Na + Cl - Cl - Na + Na + Na + Cl - Na + El potencial de Donnan es el mismo para todos los componentes en la disolución:
13 2. PRINCIPIO DE EXCLUSIÓN DE DONNAN En la membrana y en la disolución se mantiene la electroneutralidad: Cl - Na + Cl - Na + Cl - Na + Na + Cl - Cl - Na + Na + Na + Cl - Na + Cl - Na + Na + Na + Cl - Cl - Na + Na + Na + Cl - Na + En la membrana. En la disolución.
14 2. PRINCIPIO DE EXCLUSIÓN DE DONNAN
15 3. NÚMEROS DE TRANSPORTE Determinación de propiedades de transporte en membranas de El transporte de iones se debe a tres contribuciones: Convección, Difusión y Migración. La densidad de corriente está relacionada con el flujo de iones a través de la ley de Faraday. El número de transporte se define como la fracción de corriente transportada por un determinado ión en ausencia de gradientes de concentración. t i i z u Ci u C 2 i i 2 zi i i RT Di z F j i 2 RTu i
16 3. NÚMEROS DE TRANSPORTE Determinación de propiedades de transporte en membranas de Permselectividad P M t j t 1 t j j
17 3. NÚMEROS DE TRANSPORTE. CRONOPOTENCIOMETRÍA Determinación de números de transporte. Cronopotenciometría. V 3 E m (V) V 2 I 3 I 2 I 1 V 1 t (s)
18 3. NÚMEROS DE TRANSPORTE. TRANSPRTE CRONOPOTENCIOMETRÍA Determinación de números de transporte. Cronopotenciometría. U m (V) a b 2 6 c t (s) d Transition time ( ) e 5 f a. Prácticamente vertical. Su altura es igual a la caída óhmica de potencial debido a la corriente impuesta. b. Electro-difusión. Disminución de la concentración en la disolución que se agota cerca de la membrana. c. Se hace importante la convección. El punto de inflexión existe sólo cuando la corriente aplicada es mayor que la límite. d. Estado estacionario. e. Caída óhmica de potencial sobre el sistema polarizado de la membrana en el momento en que se interrumpe la corriente aplicada. f. Relajación del sistema debido a la difusión.
19 3. NÚMEROS DE TRANSPORTE. CRONOPOTENCIOMETRÍA Transporte de materia durante medidas cronopotenciométricas. Segunda ley de Fick. Flujo de iones. En la membrana. En la disolución. En la superficie de la membrana.
20 3. NÚMEROS DE TRANSPORTE. CRONOPOTENCIOMETRÍA Concentración en la superficie de la membrana en función del tiempo. Ecuación de Sand. 0.8 U m (V) Transition time ( ) t (s)
21 3. NÚMEROS DE TRANSPORTE. CRONOPOTENCIOMETRÍA Determinación de números de transporte de diferentes iones.
22 3. NÚMEROS DE TRANSPORTE. CRONOPOTENCIOMETRÍA Efecto de la concentración.
23 3. NÚMEROS DE TRANSPORTE. CRONOPOTENCIOMETRÍA Determinación de la fracción conductora de la membrana.
24 3. NÚMEROS DE TRANSPORTE. CRONOPOTENCIOMETRÍA Efecto de las condiciones hidrodinámicas. Membrana Vertical con agitación Membrana Horizontal sin agitación
25 3. NÚMEROS DE TRANSPORTE. CRONOPOTENCIOMETRÍA Precipitación y disociación del agua. Precipitación de hidróxidos metálicos Disociación del agua. Comportamiento bipolar
26 4. DENSIDAD DE CORRIENTE LÍMITE Representa la máxima densidad de corriente que se puede aplicar. Es una consecuencia de la polarización por concentración. M En la capa límite el transporte es por difusión y migración. Ecuación de Nernst Plank: Compartimento de dilución Compartimento de concentración
27 4. DENSIDAD DE CORRIENTE LÍMITE M En la membrana el transporte es por migración. Relación entre el flujo de aniones y cationes en la membrana: Compartimento de dilución Compartimento de concentración Relación entre los coeficientes de difusión en la disolución:
28 4. DENSIDAD DE CORRIENTE LÍMITE En el estado estacionario, el transporte a través de la capa límite será igual al transporte por migración en la membrana: La densidad de corriente asociada al flujo de iones vale: Si los coeficientes de difusión y los números de transporte permanecen constantes:
29 4. DENSIDAD DE CORRIENTE LÍMITE Cuando la concentración en la superficie de la membrana vale cero: M Compartimento de dilución Compartimento de concentración i lim z j D F C (t j t j ) b
30 4. DENSIDAD DE CORRIENTE LÍMITE Consecuencias de superar la densidad de corriente límite Aumento de la resistencia eléctrica en las proximidades de la membrana. Aumenta el consumo de energía y disminuye la eficacia de corriente. Cambio del ph en las proximidades de la membrana. Se produce la disociación del agua, y los iones OH - pueden ser transferidos a través de las membranas aniónicas, mientras que los H + lo harán a través de las catiónicas.
31 4. DENSIDAD DE CORRIENTE LÍMITE. CURVAS DE POLARIZACIÓN Disociación del agua Convección gravitacional Electroconvección V 3 Región I Región II E m (V) V 2 I 3 I 2 I 1 I (ma) Región III V 1 t (s) E m (V) R Ilim l plateau
32 4. DENSIDAD DE CORRIENTE LÍMITE Efecto del electrolito. i lim z j D F C (t j t j ) b
33 4. DENSIDAD DE CORRIENTE LÍMITE Efecto del electrolito. i lim z j D F C (t j t j ) b
34 4. DENSIDAD DE CORRIENTE LÍMITE Efecto de la concentración. i lim z j D F C (t j t j ) b
35 4. DENSIDAD DE CORRIENTE LÍMITE Efecto de la concentración. i lim z j D F C (t j t j ) b
36 4. DENSIDAD DE CORRIENTE LÍMITE Efecto de la concentración sobre la densidad de corriente límite y la resistencia óhmica.
37 4. DENSIDAD DE CORRIENTE LÍMITE Disociación del agua.
38 4. DENSIDAD DE CORRIENTE LÍMITE Electroconvección.
39 4. DENSIDAD DE CORRIENTE LÍMITE Electroconvección M NiSO M NiSO 4 + CrO M
40 4. DENSIDAD DE CORRIENTE LÍMITE Longitud del plateau. otansporte por electroconvección de los iones Ni 2+ o Disminución de la longitud de plateau con la concentración de Ni 2+ o Transporte de H o Aumento de la longitud + por el de mecanismo de Grotthus plateau con la concentración de H +
41 4. DENSIDAD DE CORRIENTE LÍMITE Longitud del plateau.
CROMATOGRAFÍA IÓNICA Fundamentos de la técnica
 CROMATOGRAFÍA IÓNICA Fundamentos de la técnica QUÉ ES LA CROMATOGRAFÍA? CROMATOGRAFÍA IÓNICA Tanto FASE MÓVIL como FASE ESTACIONARIA son IÓNICAS INTERCAMBIADORES IÓNICOS Intercambiadores iónicos: Fases
CROMATOGRAFÍA IÓNICA Fundamentos de la técnica QUÉ ES LA CROMATOGRAFÍA? CROMATOGRAFÍA IÓNICA Tanto FASE MÓVIL como FASE ESTACIONARIA son IÓNICAS INTERCAMBIADORES IÓNICOS Intercambiadores iónicos: Fases
Tema 6. Equilibrios de precipitación
 Tema 6. Equilibrios de precipitación 1. Introducción. 2. Solubilidad y Constante de solubilidad. 3. Sales poco solubles. 4. Factores que afectan a la solubilidad. 5. Predicción de las reacciones de precipitación.
Tema 6. Equilibrios de precipitación 1. Introducción. 2. Solubilidad y Constante de solubilidad. 3. Sales poco solubles. 4. Factores que afectan a la solubilidad. 5. Predicción de las reacciones de precipitación.
COF SATCA 1 : Carrera:
 1. Datos Generales de la asignatura Nombre de la asignatura: Clave de la asignatura: SATCA 1 : Carrera: Electroquímica y cinética de la corrosión COF-1302 2-3-5 Ingeniería en Materiales 2. Presentación
1. Datos Generales de la asignatura Nombre de la asignatura: Clave de la asignatura: SATCA 1 : Carrera: Electroquímica y cinética de la corrosión COF-1302 2-3-5 Ingeniería en Materiales 2. Presentación
Conductividad en disoluciones electrolíticas.
 Conductividad en disoluciones electrolíticas. 1.- Introducción 2.- Conductores 3.- Definición de magnitudes 3.1- Conductividad específica 3.2 Conductividad molar " 4. Variación de la conductividad (, ")
Conductividad en disoluciones electrolíticas. 1.- Introducción 2.- Conductores 3.- Definición de magnitudes 3.1- Conductividad específica 3.2 Conductividad molar " 4. Variación de la conductividad (, ")
UNIDADES DE ESTUDIO Y SUS CONTENIDOS Unidad 1: PROPIEDADES DE LOS FLUIDOS PUROS.
 1. DATOS INFORMATIVOS ASIGNATURA: QUÌMICA-FÌSICA DEPARTAMENTO: CIENCIAS EXACTAS ELEMENTO DE COMPETENCIA: CÓDIGO: EXCT-22318 CARRERAS: PETROQUÌMICA NRC 4548 NIVEL: QUINTO ÁREA DEL CONOCIMIENTO: QUÌMICA
1. DATOS INFORMATIVOS ASIGNATURA: QUÌMICA-FÌSICA DEPARTAMENTO: CIENCIAS EXACTAS ELEMENTO DE COMPETENCIA: CÓDIGO: EXCT-22318 CARRERAS: PETROQUÌMICA NRC 4548 NIVEL: QUINTO ÁREA DEL CONOCIMIENTO: QUÌMICA
DENOMINACIÓN ASIGNATURA: FÍSICA II GRADO: INGENIERÍA BIOMÉDICA CURSO: 1º CUATRIMESTRE: 2º (*)
 DENOMINACIÓN ASIGNATURA: FÍSICA II GRADO: INGENIERÍA BIOMÉDICA CURSO: 1º CUATRIMESTRE: 2º CRONOGRAMA ASIGNATURA DESCRIPCIÓN DEL CONTENIDO DE LA SESIÓN SE- MA- NA SE- SIÓN 1 1 T1. La primera ley de la Termodinámica
DENOMINACIÓN ASIGNATURA: FÍSICA II GRADO: INGENIERÍA BIOMÉDICA CURSO: 1º CUATRIMESTRE: 2º CRONOGRAMA ASIGNATURA DESCRIPCIÓN DEL CONTENIDO DE LA SESIÓN SE- MA- NA SE- SIÓN 1 1 T1. La primera ley de la Termodinámica
Equilibrio Químico. CI4102 Ingeniería Ambiental Profesor Marcelo Olivares A.
 Equilibrio Químico CI4102 Ingeniería Ambiental Profesor Marcelo Olivares A. Introducción Las reacciones químicas que se ha considerado hasta este punto se denominan irreversibles debido a que ellas proceden
Equilibrio Químico CI4102 Ingeniería Ambiental Profesor Marcelo Olivares A. Introducción Las reacciones químicas que se ha considerado hasta este punto se denominan irreversibles debido a que ellas proceden
DATOS DE LA ASIGNATURA
 DATOS DE LA ASIGNATURA Denominación: TECNOLOGÍA ELECTROQUÍMICA Código: 57631 Clase: OPTATIVA Curso: 3º Carácter: CUATRIMESTRAL Cuatrimestre: 2º Créditos LRU: 4,5 Teóricos: 3 Prácticos: 1,5 Créditos ECTS:
DATOS DE LA ASIGNATURA Denominación: TECNOLOGÍA ELECTROQUÍMICA Código: 57631 Clase: OPTATIVA Curso: 3º Carácter: CUATRIMESTRAL Cuatrimestre: 2º Créditos LRU: 4,5 Teóricos: 3 Prácticos: 1,5 Créditos ECTS:
CONFERENCIA No. 1 Página 1 de 4. DE: Septiembre 7 del 2015 A : Septiembre 25 del 2015
 CONFERENCIA No. 1 Página 1 de 4 ÁREA: TEMA: PROFESOR: TIEMPO DE REALIZACIÓN: CIENCIAS NATURALES Y EDUCACIÓN GRADO: DÉCIMO AMBIENTAL - QUÍMICA Nomenclatura y reacciones de obtención de óxido, ácidos, bases
CONFERENCIA No. 1 Página 1 de 4 ÁREA: TEMA: PROFESOR: TIEMPO DE REALIZACIÓN: CIENCIAS NATURALES Y EDUCACIÓN GRADO: DÉCIMO AMBIENTAL - QUÍMICA Nomenclatura y reacciones de obtención de óxido, ácidos, bases
Nutrición Vegetal. Absorción de sales minerales
 Nutrición Vegetal Absorción de sales minerales Absorción - Es el proceso mediante el cual un ión o molécula ingresa a una célula o un cuerpo a través de una membrana. No intervienen fuerzas intermoleculares.
Nutrición Vegetal Absorción de sales minerales Absorción - Es el proceso mediante el cual un ión o molécula ingresa a una célula o un cuerpo a través de una membrana. No intervienen fuerzas intermoleculares.
QUIMICA UNIVERSIDAD DE BURGOS QUÍMICA GUÍA DOCENTE Denominación de la asignatura: QUIMICA. Titulación
 GUÍA DOCENTE 2010-2011 QUIMICA 1. Denominación de la asignatura: QUIMICA Titulación Ingeniería Electrónica Industrial y Automática Código 6400 2. Materia o módulo a la que pertenece la asignatura: Química
GUÍA DOCENTE 2010-2011 QUIMICA 1. Denominación de la asignatura: QUIMICA Titulación Ingeniería Electrónica Industrial y Automática Código 6400 2. Materia o módulo a la que pertenece la asignatura: Química
ESTUDIO DEL PROCESO DE TRANSFERENCIA MASA EN MEMBRANAS LÍQUIDAS SOPORTADAS
 ESTUDIO DEL PROCESO DE TRANSFERENCIA MASA EN MEMBRANAS LÍQUIDAS SOPORTADAS Mario Avila-Rodríguez Diana Fabiola Cholico González María del Pilar González Muñoz Mireya Edith Martínez Pérez José Antonio Reyes
ESTUDIO DEL PROCESO DE TRANSFERENCIA MASA EN MEMBRANAS LÍQUIDAS SOPORTADAS Mario Avila-Rodríguez Diana Fabiola Cholico González María del Pilar González Muñoz Mireya Edith Martínez Pérez José Antonio Reyes
15/03/2010. Definición:
 ph Definición: El ph es una medida de la acidez El ph es una medida de la acidez o alcalinidad de una sustancia. Es un valor numérico que expresa la concentración de iones de hidrógeno (H + ). El ph no
ph Definición: El ph es una medida de la acidez El ph es una medida de la acidez o alcalinidad de una sustancia. Es un valor numérico que expresa la concentración de iones de hidrógeno (H + ). El ph no
TÉCNICAS DE MUESTREO, ANÁLISIS E INTERPRETACIÓN DE DATOS. Ingeniería Ambiental
 TÉCNICAS DE MUESTREO, ANÁLISIS E INTERPRETACIÓN DE DATOS Ingeniería Ambiental Problema Elección del método analítico Toma de muestra Tratamiento de la muestra Proceso de medida Tratamiento de los datos
TÉCNICAS DE MUESTREO, ANÁLISIS E INTERPRETACIÓN DE DATOS Ingeniería Ambiental Problema Elección del método analítico Toma de muestra Tratamiento de la muestra Proceso de medida Tratamiento de los datos
GUÍA DIDACTICA CURSO QUÍMICA 2º BACHILLERATO. PROFESOR: Alicia Blanco Pozos
 GUÍA DIDACTICA QUÍMICA 2º BACHILLERATO CURSO 2016-17 PROFESOR: Alicia Blanco Pozos CONTENIDOS Los contenidos se organizan en 8 unidades didácticas distribuidos en 4 bloques: BLOQUE I UNIDAD 1. Estructura
GUÍA DIDACTICA QUÍMICA 2º BACHILLERATO CURSO 2016-17 PROFESOR: Alicia Blanco Pozos CONTENIDOS Los contenidos se organizan en 8 unidades didácticas distribuidos en 4 bloques: BLOQUE I UNIDAD 1. Estructura
Celdas Galvánicas y Electrolíticas
 Celdas Galvánicas y Electrolíticas Reacciones de óxido-reducción Reacciones en las cuales una o más de las sustancias intervinientes modifica su estado de oxidación. Znº (s) + Cu +2 (ac) Zn 2+ (ac) + Cuº
Celdas Galvánicas y Electrolíticas Reacciones de óxido-reducción Reacciones en las cuales una o más de las sustancias intervinientes modifica su estado de oxidación. Znº (s) + Cu +2 (ac) Zn 2+ (ac) + Cuº
QUIMICA UNIVERSIDAD DE BURGOS QUÍMICA GUÍA DOCENTE Denominación de la asignatura: QUIMICA. Titulación
 GUÍA DOCENTE 2012-2013 QUIMICA 1. Denominación de la asignatura: QUIMICA Titulación Ingeniería Electrónica Industrial y Automática Código 6400 2. Materia o módulo a la que pertenece la asignatura: Química
GUÍA DOCENTE 2012-2013 QUIMICA 1. Denominación de la asignatura: QUIMICA Titulación Ingeniería Electrónica Industrial y Automática Código 6400 2. Materia o módulo a la que pertenece la asignatura: Química
TEMA 2: Estructura Atómica
 TEMA 2: Estructura Atómica 2.1 Estructura atómica. Enlaces atómicos y propiedades. 2.2 Enlaces primarios: iónico, covalente y metálicos. Enlaces secundarios. 2.3 Los enlaces en metales, cerámicas y polímeros.
TEMA 2: Estructura Atómica 2.1 Estructura atómica. Enlaces atómicos y propiedades. 2.2 Enlaces primarios: iónico, covalente y metálicos. Enlaces secundarios. 2.3 Los enlaces en metales, cerámicas y polímeros.
CROMATOGRAFÍA LÍQUIDA DE ALTA RESOLUCIÓN
 CROMATOGRAFÍA LÍQUIDA DE ALTA RESOLUCIÓN Curso: Química Analítica II Loreto Ascar 2012 Esquema de las bases de la separación en cromatografía de: (a)absorción, (b) partición, (c) Intercambio iónico y (d)
CROMATOGRAFÍA LÍQUIDA DE ALTA RESOLUCIÓN Curso: Química Analítica II Loreto Ascar 2012 Esquema de las bases de la separación en cromatografía de: (a)absorción, (b) partición, (c) Intercambio iónico y (d)
Planificaciones Química Física. Docente responsable: RAZZITTE ADRIAN CESAR. 1 de 5
 Planificaciones 6316 - Química Física Docente responsable: RAZZITTE ADRIAN CESAR 1 de 5 OBJETIVOS Introducir al alumno en los conceptos bàsicos correspondientes a: sistemas iónicos y sus aplicaciones industriales.
Planificaciones 6316 - Química Física Docente responsable: RAZZITTE ADRIAN CESAR 1 de 5 OBJETIVOS Introducir al alumno en los conceptos bàsicos correspondientes a: sistemas iónicos y sus aplicaciones industriales.
PURIFICACIÓN DE PROTEÍNAS
 PURIFICACIÓN DE PROTEÍNAS ESQUEMA DE PURIFICACIÓN DE UNA PROTEÍNA tejido vegetal animal homogeneizar cultivo celular bacterias levaduras células mamíferos PREPARACIÓN EXTRACTO crudo fraccionamiento subcelular
PURIFICACIÓN DE PROTEÍNAS ESQUEMA DE PURIFICACIÓN DE UNA PROTEÍNA tejido vegetal animal homogeneizar cultivo celular bacterias levaduras células mamíferos PREPARACIÓN EXTRACTO crudo fraccionamiento subcelular
IES Atenea (S.S. de los Reyes) Departamento de Física y Química. PAU Química. Septiembre 2006 PRIMERA PARTE
 1 PAU Química. Septiembre 2006 PRIMERA PARTE Cuestión 1. La configuración electrónica del último nivel energético de un elemento es 4s 2 4p 3. De acuerdo con este dato: a) Deduzca la situación de dicho
1 PAU Química. Septiembre 2006 PRIMERA PARTE Cuestión 1. La configuración electrónica del último nivel energético de un elemento es 4s 2 4p 3. De acuerdo con este dato: a) Deduzca la situación de dicho
ELECTROQUÍMICA. 1. Conceptos de oxidación-reducción
 ELECTROQUÍMICA 1. Conceptos de oxidación-reducción Oxidación: transformación en la que una especie química pierde electrones o gana oxígeno. Reducción: transformación en la que una especie química gana
ELECTROQUÍMICA 1. Conceptos de oxidación-reducción Oxidación: transformación en la que una especie química pierde electrones o gana oxígeno. Reducción: transformación en la que una especie química gana
DIFUSIÓN UNIVERSIDAD TECNOLÓGICA DE PEREIRA TECNOLOGIA MECANICA
 DIFUSIÓN UNIVERSIDAD TECNOLÓGICA DE PEREIRA TECNOLOGIA MECANICA 1 CONTENIDO Concepto de difusión Mecanismos de difusión Difusión en régimen permanente y en régimen transitório Fatores que influeyen en
DIFUSIÓN UNIVERSIDAD TECNOLÓGICA DE PEREIRA TECNOLOGIA MECANICA 1 CONTENIDO Concepto de difusión Mecanismos de difusión Difusión en régimen permanente y en régimen transitório Fatores que influeyen en
Sevilla, 31 de mayo de El Rector, Miguel Ángel Castro Arroyo.
 página 145 3. Otras disposiciones Universidades Resolución de 31 de mayo de 2017, de la Universidad de Sevilla, por la que se publica la modificación del Plan de Estudios conducente a la obtención del
página 145 3. Otras disposiciones Universidades Resolución de 31 de mayo de 2017, de la Universidad de Sevilla, por la que se publica la modificación del Plan de Estudios conducente a la obtención del
Características y usos de los diagramas de Pourbaix
 Características y usos de los diagramas de Pourbaix Apellidos, nombre Muñoz Portero, María José (mjmunoz@iqn.upv.es) Departamento Centro Ingeniería Química y Nuclear Escuela Técnica Superior de Ingenieros
Características y usos de los diagramas de Pourbaix Apellidos, nombre Muñoz Portero, María José (mjmunoz@iqn.upv.es) Departamento Centro Ingeniería Química y Nuclear Escuela Técnica Superior de Ingenieros
Grado en Química Universidad de Alcalá Curso Académico 2016/2017 3º Curso Anual
 QUÍMICA FÍSICA (660013) Grado en Química Universidad de Alcalá Curso Académico 2016/2017 3º Curso Anual GUÍA DOCENTE Nombre de la asignatura: QUÍMICA FÍSICA Código: 660013 Titulación en la que se imparte:
QUÍMICA FÍSICA (660013) Grado en Química Universidad de Alcalá Curso Académico 2016/2017 3º Curso Anual GUÍA DOCENTE Nombre de la asignatura: QUÍMICA FÍSICA Código: 660013 Titulación en la que se imparte:
BOLETÍN OFICIAL DEL ESTADO UNIVERSIDADES
 Núm. 147 Miércoles 21 de junio de 2017 Sec. III. Pág. 51263 III. OTRAS DISPOSICIONES UNIVERSIDADES 7104 Resolución de 31 de mayo de 2017, de la Universidad de Sevilla, por la que se publica la modificación
Núm. 147 Miércoles 21 de junio de 2017 Sec. III. Pág. 51263 III. OTRAS DISPOSICIONES UNIVERSIDADES 7104 Resolución de 31 de mayo de 2017, de la Universidad de Sevilla, por la que se publica la modificación
Unidad 6: ELECTROQUIMICA
 Unidad 6: ELECTROQUIMICA REACCIONES DE OXIDACION-REDUCCION Las reacciones redox son aquellas en las cuales hay intercambio de electrones entre las sustancias que intervienen en la reacción. Oxidación:
Unidad 6: ELECTROQUIMICA REACCIONES DE OXIDACION-REDUCCION Las reacciones redox son aquellas en las cuales hay intercambio de electrones entre las sustancias que intervienen en la reacción. Oxidación:
INSTITUTO TECNOLÓGICO de Durango ELECTROQUÍMICA FISICOQUÍMICA 2. Dr. Carlos Francisco Cruz Fierro. Revisión Fisicoquímica 2.
 INSTITUTO TECNOLÓGICO de Durango ELECTROQUÍMICA FISICOQUÍMICA 2 Dr. Carlos Francisco Cruz Fierro Revisión 1 69156.17 7-ene-13 1 Electroquímica Relación entre la electricidad y la química Involucra la medición
INSTITUTO TECNOLÓGICO de Durango ELECTROQUÍMICA FISICOQUÍMICA 2 Dr. Carlos Francisco Cruz Fierro Revisión 1 69156.17 7-ene-13 1 Electroquímica Relación entre la electricidad y la química Involucra la medición
S.E.P. S.E.I.T DIRECCION GENERAL DE INSTITUTOS TECNOLOGICOS
 S.E.P. S.E.I.T DIRECCION GENERAL DE INSTITUTOS TECNOLOGICOS NOMBRE DE LA ASIGNATURA: QUIMICA ANALITICA II (4-2-10) NIVEL: LICENCIATURA. CARRERA: INGENIERIA BIOQUIMICA INGENIERIA QUIMICA CLAVE: ACC-9331
S.E.P. S.E.I.T DIRECCION GENERAL DE INSTITUTOS TECNOLOGICOS NOMBRE DE LA ASIGNATURA: QUIMICA ANALITICA II (4-2-10) NIVEL: LICENCIATURA. CARRERA: INGENIERIA BIOQUIMICA INGENIERIA QUIMICA CLAVE: ACC-9331
4. Un agente oxidante (2 correctas) A) Toma electrones de otra sustancia B) Da electrones a otra sustancia C) Se oxida D) Se reduce
 CUESTIONES. EQUILIBRIO OXIDO-REDUCCIÓN ---------------------------------------------------------------------------------------------------------- 1. Las reacciones químicas que implican transferencias
CUESTIONES. EQUILIBRIO OXIDO-REDUCCIÓN ---------------------------------------------------------------------------------------------------------- 1. Las reacciones químicas que implican transferencias
SUELO Fina capa de material fértil que recubre la superficie de la Tierra DIFERENCIACIÓN EN PROFUNDIDAD
 SUELO Fina capa de material fértil que recubre la superficie de la Tierra DIFERENCIACIÓN EN PROFUNDIDAD PROGRAMA DE TEORÍA I. INTRODUCCIÓN TEMA 1. Generalidades. La ciencia del suelo. Concepto. Evolución
SUELO Fina capa de material fértil que recubre la superficie de la Tierra DIFERENCIACIÓN EN PROFUNDIDAD PROGRAMA DE TEORÍA I. INTRODUCCIÓN TEMA 1. Generalidades. La ciencia del suelo. Concepto. Evolución
Operaciones Básicas en la Industria Química
 Unidad responsable: 240 - ETSEIB - Escuela Técnica Superior de Ingeniería Industrial de Barcelona Unidad que imparte: 713 - EQ - Departamento de Ingeniería Química Curso: Titulación: 2017 GRADO EN INGENIERÍA
Unidad responsable: 240 - ETSEIB - Escuela Técnica Superior de Ingeniería Industrial de Barcelona Unidad que imparte: 713 - EQ - Departamento de Ingeniería Química Curso: Titulación: 2017 GRADO EN INGENIERÍA
Ácidos, Bases y Electrolitos
 Ácidos, Bases y Electrolitos Semana 12 Licda. Lilian Judith Guzmán Melgar ACIDOS Y BASES ACIDOS Del latín Acidus= agrio Ejemplos Vinagre, jugo de limón. Tiene un sabor a agrio y pueden producir sensación
Ácidos, Bases y Electrolitos Semana 12 Licda. Lilian Judith Guzmán Melgar ACIDOS Y BASES ACIDOS Del latín Acidus= agrio Ejemplos Vinagre, jugo de limón. Tiene un sabor a agrio y pueden producir sensación
Horas semanales: 4 curso 4 trabajo individual. Fecha de actualización: Sept/2011
 Electroquímica Código del curso: XXXXX Tipo de curso: Curso Curso: Optativo Ciclo: Segundo semestre Duración total del curso: 128 hrs Horas semanales: 64 horas de teoría 64 horas trabajo individual Créditos:
Electroquímica Código del curso: XXXXX Tipo de curso: Curso Curso: Optativo Ciclo: Segundo semestre Duración total del curso: 128 hrs Horas semanales: 64 horas de teoría 64 horas trabajo individual Créditos:
PROBLEMAS RESUELTOS SELECTIVIDAD ANDALUCÍA 2013 QUÍMICA TEMA 6: EQUILIBRIOS ÁCIDO-BASE
 PROBLEMAS RESUELTOS SELECTIVIDAD ANDALUCÍA 201 QUÍMICA TEMA 6: EQUILIBRIOS ÁCIDO-BASE Junio, Ejercicio 5, Opción B Reserva 1, Ejercicio 6, Opción A Reserva 1, Ejercicio 4, Opción B Reserva 2, Ejercicio
PROBLEMAS RESUELTOS SELECTIVIDAD ANDALUCÍA 201 QUÍMICA TEMA 6: EQUILIBRIOS ÁCIDO-BASE Junio, Ejercicio 5, Opción B Reserva 1, Ejercicio 6, Opción A Reserva 1, Ejercicio 4, Opción B Reserva 2, Ejercicio
ELECTROOBTENCIÓN DE ZINC UTILIZANDO CELDA DE ELECTRODIALISIS REACTIVA
 UNIVERSIDAD DE SANTIAGO DE CHILE FACULTAD DE INGENIERIA DEPARTAMENTO DE INGENIERIA METALURGICA ELECTROOBTENCIÓN DE ZINC UTILIZANDO CELDA DE ELECTRODIALISIS REACTIVA Profesor Dr. GERARDO CIFUENTES MOLINA
UNIVERSIDAD DE SANTIAGO DE CHILE FACULTAD DE INGENIERIA DEPARTAMENTO DE INGENIERIA METALURGICA ELECTROOBTENCIÓN DE ZINC UTILIZANDO CELDA DE ELECTRODIALISIS REACTIVA Profesor Dr. GERARDO CIFUENTES MOLINA
TEMA 5 ENLACE QUIMICO. Propiedades de las sustancias iónicas, covalentes y metálicas. Prof: Noemy Quirós
 TEMA 5 ENLACE QUIMICO Propiedades de las sustancias iónicas, covalentes y metálicas 1 Prof: Noemy Quirós ESTADOS DE AGREGACIÓN A 298 K A 298 K, cuanto mayor es la atracción entre las partículas (átomos,
TEMA 5 ENLACE QUIMICO Propiedades de las sustancias iónicas, covalentes y metálicas 1 Prof: Noemy Quirós ESTADOS DE AGREGACIÓN A 298 K A 298 K, cuanto mayor es la atracción entre las partículas (átomos,
1.- DATOS DE LA ASIGNATURA. Nombre de la asignatura: Corrosión y degradación de Materiales. Carrera: Ingeniería en Materiales. Clave de la asignatura:
 1.- DATOS DE LA ASIGNATURA Nombre de la asignatura: Carrera: Clave de la asignatura: Horas teoría-horas práctica-créditos: Corrosión y degradación de Materiales Ingeniería en Materiales MAC 0506 4 2 10
1.- DATOS DE LA ASIGNATURA Nombre de la asignatura: Carrera: Clave de la asignatura: Horas teoría-horas práctica-créditos: Corrosión y degradación de Materiales Ingeniería en Materiales MAC 0506 4 2 10
MÁSTER UNIVERSITARIO EN INGENIERÍA QUÍMICA por la. Universidad de Castilla-La Mancha
 MÁSTER UNIVERSITARIO EN INGENIERÍA QUÍMICA por la Universidad de Castilla-La Mancha Paula Sánchez Paredes (CU, Coordinadora) Dpto. Ingeniería Química PASADO PRESENTE INGENIERO QUÍMICO (5 años) GRADUADO
MÁSTER UNIVERSITARIO EN INGENIERÍA QUÍMICA por la Universidad de Castilla-La Mancha Paula Sánchez Paredes (CU, Coordinadora) Dpto. Ingeniería Química PASADO PRESENTE INGENIERO QUÍMICO (5 años) GRADUADO
Nutrición Vegetal. Absorción de sales minerales
 Nutrición Vegetal Absorción de sales minerales Absorción - Adsorción Este proceso ayuda a la entrada de agua y minerales a las plantas. Algunas veces es un proceso endotérmico Este proceso ayuda a la imbibición
Nutrición Vegetal Absorción de sales minerales Absorción - Adsorción Este proceso ayuda a la entrada de agua y minerales a las plantas. Algunas veces es un proceso endotérmico Este proceso ayuda a la imbibición
UNIVERSIDAD RICARDO PALMA FACULTAD DE INGENIERIA ESCUELA ACADEMICO PROFESIONAL DE INGENIERIA INFORMATICA SÍLABO
 UNIVERSIDAD RICARDO PALMA FACULTAD DE INGENIERIA ESCUELA ACADEMICO PROFESIONAL DE INGENIERIA INFORMATICA SÍLABO 1. DATOS ADMINISTRATIVOS. Asignatura : QUÍMICA GENERAL Código : II0106 Area Académica : Química
UNIVERSIDAD RICARDO PALMA FACULTAD DE INGENIERIA ESCUELA ACADEMICO PROFESIONAL DE INGENIERIA INFORMATICA SÍLABO 1. DATOS ADMINISTRATIVOS. Asignatura : QUÍMICA GENERAL Código : II0106 Area Académica : Química
La membrana plasmática o citoplasmática es una estructura laminar que engloba a las células, define sus límites y contribuye a mantener el equilibrio
 Membranas celulares La membrana plasmática o citoplasmática es una estructura laminar que engloba a las células, define sus límites y contribuye a mantener el equilibrio entre el interior y el exterior
Membranas celulares La membrana plasmática o citoplasmática es una estructura laminar que engloba a las células, define sus límites y contribuye a mantener el equilibrio entre el interior y el exterior
INGENIERO INDUSTRIAL (CODIGO 05II)
 PRIMER CURSO (Sin docencia, sólo examen) INGENIERO INDUSTRIAL (CODIGO 05II) CÓD. ASIGNATURAS CRÉD TEÓRICAS PRÁCTICAS TIPO 1011 FÍSICA GENERAL I 6 4 2 Troncal 1º 1012 CÁLCULO I 6 3 3 Troncal 1º 1013 ÁLGEBRA
PRIMER CURSO (Sin docencia, sólo examen) INGENIERO INDUSTRIAL (CODIGO 05II) CÓD. ASIGNATURAS CRÉD TEÓRICAS PRÁCTICAS TIPO 1011 FÍSICA GENERAL I 6 4 2 Troncal 1º 1012 CÁLCULO I 6 3 3 Troncal 1º 1013 ÁLGEBRA
TRANSPORTE A TRAVÉS DE LA MEMBRANA CELULAR
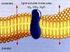 TRANSPORTE A TRAVÉS DE LA MEMBRANA CELULAR Introducción Compartimientos Acuosos separados por Barreras Biológicas Organelos selectivos, autocatalíticos, autoreproductivos, competitivos, adaptativos...
TRANSPORTE A TRAVÉS DE LA MEMBRANA CELULAR Introducción Compartimientos Acuosos separados por Barreras Biológicas Organelos selectivos, autocatalíticos, autoreproductivos, competitivos, adaptativos...
La electro-obtención de cobre es la recuperación del cobre como metal a partir de una solución en una celda electroquímica.
 ELECTRO-OBTENCIÓN DE COBRE La electro-obtención de cobre es la recuperación del cobre como metal a partir de una solución en una celda electroquímica. La electro-refinación de cobre es la purificación
ELECTRO-OBTENCIÓN DE COBRE La electro-obtención de cobre es la recuperación del cobre como metal a partir de una solución en una celda electroquímica. La electro-refinación de cobre es la purificación
Reacciones Ácido Base
 Reacciones Ácido Base Prof. Sergio Casas-Cordero E. sacce Contenido: (parte uno) 1. Definiciones 2. Equilibrio iónico del agua 3. Potencial de acidez; escala de ph 4. Fuerza de ácidos y bases 5. Medición
Reacciones Ácido Base Prof. Sergio Casas-Cordero E. sacce Contenido: (parte uno) 1. Definiciones 2. Equilibrio iónico del agua 3. Potencial de acidez; escala de ph 4. Fuerza de ácidos y bases 5. Medición
Reacciones redox (se profundiza en teóricos semana 3) Reacciones ácido-base (se profundiza en teóricos semanas 6 y 7)
 Dr. Hugo Cerecetto Prof. Titular de Química Temario 2) La reacción química: - Introducción. Clases principales de reacciones químicas - Reacciones de precipitación y reacciones ácido-base - Reacciones
Dr. Hugo Cerecetto Prof. Titular de Química Temario 2) La reacción química: - Introducción. Clases principales de reacciones químicas - Reacciones de precipitación y reacciones ácido-base - Reacciones
2º de Bachillerato EQUILIBRIOS DE SOLUBILIDAD
 º de Bachillerato EQUILIBRIOS DE SOLUBILIDAD Indice 1. Equilibrios heterogéneos.. Solubilidad. Reglas de solubilidad. 3. Reacciones de precipitación. 4. Producto de solubilidad. 5. Factores que modifican
º de Bachillerato EQUILIBRIOS DE SOLUBILIDAD Indice 1. Equilibrios heterogéneos.. Solubilidad. Reglas de solubilidad. 3. Reacciones de precipitación. 4. Producto de solubilidad. 5. Factores que modifican
Reacciones de precipitación Solubilidad y producto de solubilidad
 Reacciones de precipitación Recibe el nombre de precipitación la aparición de una fase sólida en el seno de un líquido, bien por adición de un reactivo que forme un producto insoluble con alguno de los
Reacciones de precipitación Recibe el nombre de precipitación la aparición de una fase sólida en el seno de un líquido, bien por adición de un reactivo que forme un producto insoluble con alguno de los
MECANISMOS DISIPATIVOS Y SUS FUERZAS IMPULSORAS
 MECANISMOS DISIPATIVOS Y SUS FUERZAS IMPULSORAS Temas de Biofísica Mario Parisi Bibliografía Capítulo 3: Los Grandes Mecanismos Disipativos y sus Fuerzas Impulsoras Gradiente Variación de una cierta cantidad
MECANISMOS DISIPATIVOS Y SUS FUERZAS IMPULSORAS Temas de Biofísica Mario Parisi Bibliografía Capítulo 3: Los Grandes Mecanismos Disipativos y sus Fuerzas Impulsoras Gradiente Variación de una cierta cantidad
Oferta tecnológica: Nuevo método para evaluar la durabilidad de los hormigones mediante el uso de geles conductores
 Oferta tecnológica: Nuevo método para evaluar la durabilidad de los hormigones mediante el uso de geles conductores Oferta tecnológica: Nuevo método para evaluar la durabilidad de los hormigones mediante
Oferta tecnológica: Nuevo método para evaluar la durabilidad de los hormigones mediante el uso de geles conductores Oferta tecnológica: Nuevo método para evaluar la durabilidad de los hormigones mediante
Programa de la asignatura Curso: 2008 / 2009 TERMODINÁMICA QUÍMICA (1226)
 Programa de la asignatura Curso: 2008 / 2009 TERMODINÁMICA QUÍMICA (1226) PROFESORADO Profesor/es: RAFAEL TEODORO ALCALDE GARCIA - correo-e: ralcalde@ubu.es INDALECIO ANTONIO PEÑACOBA MAESTRE - correo-e:
Programa de la asignatura Curso: 2008 / 2009 TERMODINÁMICA QUÍMICA (1226) PROFESORADO Profesor/es: RAFAEL TEODORO ALCALDE GARCIA - correo-e: ralcalde@ubu.es INDALECIO ANTONIO PEÑACOBA MAESTRE - correo-e:
EQUILIBRIO IÓNICO EN SOLUCIONES ACUOSAS
 EQUILIBRIO IÓNICO EN SOLUCIONES ACUOSAS Equilibrio entre una sal sólida poco soluble y sus iones en solución Producto de solubilidad (Kps) Muchos compuestos (sales, hidróxidos) son levemente solubles en
EQUILIBRIO IÓNICO EN SOLUCIONES ACUOSAS Equilibrio entre una sal sólida poco soluble y sus iones en solución Producto de solubilidad (Kps) Muchos compuestos (sales, hidróxidos) son levemente solubles en
CONDUCTIVIDAD DE LAS DISOLUCIONES ELECTROLITICAS
 CONDUCTIVIDAD DE LAS DISOLUCIONES ELECTROLITICAS INTRODUCCION En los conductores metálicos, el transporte de la corriente eléctrica tiene lugar debido al movimiento de los electrones del metal bajo la
CONDUCTIVIDAD DE LAS DISOLUCIONES ELECTROLITICAS INTRODUCCION En los conductores metálicos, el transporte de la corriente eléctrica tiene lugar debido al movimiento de los electrones del metal bajo la
Transporte a través de la membrana celular. Departamento de Biofísica Facultad de Medicina
 Transporte a través de la membrana celular Departamento de Biofísica Facultad de Medicina Objetivos Analizar parte de las funciones de las membranas celulares. Estudiar el pasaje de sustancias a través
Transporte a través de la membrana celular Departamento de Biofísica Facultad de Medicina Objetivos Analizar parte de las funciones de las membranas celulares. Estudiar el pasaje de sustancias a través
Fuerzas intermoleculares y líquidos y sólidos
 Fuerzas intermoleculares y líquidos y sólidos Capítulo 11 Copyright The McGraw-Hill Companies, Inc. Permission required for reproduction or display. Una fase es la parte homógenea de un sistema en contacto
Fuerzas intermoleculares y líquidos y sólidos Capítulo 11 Copyright The McGraw-Hill Companies, Inc. Permission required for reproduction or display. Una fase es la parte homógenea de un sistema en contacto
ÍNDICE CAPÍTULO 1: INTRODUCCIÓN A LA METODOLOGÍA EN QUÍMICA ANALÍTICA... 9 CAPÍTULO 2: EVALUACIÓN DE LOS DATOS ANALÍTICOS... 25
 ÍNDICE CAPÍTULO 1: INTRODUCCIÓN A LA METODOLOGÍA EN QUÍMICA ANALÍTICA... 9 1.1. CONCEPTO Y FINALIDAD DE LA QUÍMICA ANALÍTICA... 9 1.2. LA PROPIEDAD ANALÍTICA... 11 1.3. EL PROCESO ANALÍTICO... 12 1.4.
ÍNDICE CAPÍTULO 1: INTRODUCCIÓN A LA METODOLOGÍA EN QUÍMICA ANALÍTICA... 9 1.1. CONCEPTO Y FINALIDAD DE LA QUÍMICA ANALÍTICA... 9 1.2. LA PROPIEDAD ANALÍTICA... 11 1.3. EL PROCESO ANALÍTICO... 12 1.4.
Facultad de Ciencias Forestales y Ambientales Escuela de Ingeniería Forestal Departamento Ordenación de Cuencas. Coloides del Suelo
 Facultad de Ciencias Forestales y Ambientales Escuela de Ingeniería Forestal Departamento Ordenación de Cuencas Coloides del Suelo Su Naturaleza y Significado Práctico Prof. Clifford Peña Guillén CONTENIDO
Facultad de Ciencias Forestales y Ambientales Escuela de Ingeniería Forestal Departamento Ordenación de Cuencas Coloides del Suelo Su Naturaleza y Significado Práctico Prof. Clifford Peña Guillén CONTENIDO
Elementos Alcalinos:
 Elementos Alcalinos: Litio (Li) Sodio (Na) Potasio (K) Rubidio (Rb) Cesio (Cs) Francio (Fr) Berilio (Be) Magnesio (Mg) Calcio (Ca) Estroncio (Sr) Bario (Ba) Radio (Ra) 1 Propiedades físicas de los elementos
Elementos Alcalinos: Litio (Li) Sodio (Na) Potasio (K) Rubidio (Rb) Cesio (Cs) Francio (Fr) Berilio (Be) Magnesio (Mg) Calcio (Ca) Estroncio (Sr) Bario (Ba) Radio (Ra) 1 Propiedades físicas de los elementos
Un sistema se encuentra en un estado de equilibrio químico cuando su composición no varía con el tiempo.
 Un sistema se encuentra en un estado de equilibrio químico cuando su composición no varía con el tiempo. N 2 g 3 H 2 g 2 NH 3 g 2 NH 3 g N 2 g 3 H 2 g concentración H 2 N 2 NH 3 concentración NH 3 H 2
Un sistema se encuentra en un estado de equilibrio químico cuando su composición no varía con el tiempo. N 2 g 3 H 2 g 2 NH 3 g 2 NH 3 g N 2 g 3 H 2 g concentración H 2 N 2 NH 3 concentración NH 3 H 2
Tema 8: Equilibrios de solubilidad y de formación de complejos
 Tema 8: Equilibrios de solubilidad y de formación de complejos Equilibrio de solubilidad: conceptos básicos. Producto de solubilidad: K s. Solubilidad. Efecto del ión común. Precipitación. Equilibrios
Tema 8: Equilibrios de solubilidad y de formación de complejos Equilibrio de solubilidad: conceptos básicos. Producto de solubilidad: K s. Solubilidad. Efecto del ión común. Precipitación. Equilibrios
Celda de combustible AFC casera
 Propuesta de construcción de pila de pila AFC casera: Se trata de conseguir producir la reacción electroquímica de manera económica y sencilla para obtener energía a partir de hidrógeno y oxígeno. Para
Propuesta de construcción de pila de pila AFC casera: Se trata de conseguir producir la reacción electroquímica de manera económica y sencilla para obtener energía a partir de hidrógeno y oxígeno. Para
PLANIFICACIÓN DOCENTE CURSO
 PLANIFICACIÓN DOCENTE CURSO 2008-2009 ASIGNATURA: Nombre oficial de la asignatura QUIMICA CURSO: # PRIMER CURSO CUATRIMESTRE: # PRIMERO CICLO: # PRIMERO CARÁCTER: Obligatoria, troncal, de libre elección,
PLANIFICACIÓN DOCENTE CURSO 2008-2009 ASIGNATURA: Nombre oficial de la asignatura QUIMICA CURSO: # PRIMER CURSO CUATRIMESTRE: # PRIMERO CICLO: # PRIMERO CARÁCTER: Obligatoria, troncal, de libre elección,
Reacciones de transferencia de protones Ácidos y bases
 Tema 6 Reacciones de transferencia de protones Ácidos y bases Probablemente no haya otro tipo de equilibrio tan importante con el de ácidos y bases B. M. Mahan y R. J. Myers Química. Curso Universitario
Tema 6 Reacciones de transferencia de protones Ácidos y bases Probablemente no haya otro tipo de equilibrio tan importante con el de ácidos y bases B. M. Mahan y R. J. Myers Química. Curso Universitario
ESTRUCTURA, VALORACIÓN Y CONTENIDOS DEL EXAMEN DE QUÍMICA DE LAS PRUEBAS DE ACCESO A LA UNIVERSIDAD POLITÉCNICA DE CARTAGENA PARA MAYORES DE 25 AÑOS.
 ESTRUCTURA, VALORACIÓN Y CONTENIDOS DEL EXAMEN DE QUÍMICA DE LAS PRUEBAS DE ACCESO A LA UNIVERSIDAD POLITÉCNICA DE CARTAGENA PARA MAYORES DE 25 AÑOS. ESTRUCTURA La prueba constará de cuatro bloques, existiendo
ESTRUCTURA, VALORACIÓN Y CONTENIDOS DEL EXAMEN DE QUÍMICA DE LAS PRUEBAS DE ACCESO A LA UNIVERSIDAD POLITÉCNICA DE CARTAGENA PARA MAYORES DE 25 AÑOS. ESTRUCTURA La prueba constará de cuatro bloques, existiendo
ASIGNATURA: FÍSICO QUÍMICA CÓDIGO: 5312 PÁG.: 1 DE: 6 HORAS TEORÍA PRACTICA TRABAJO SUPERV LABORATORIO SEMINARIO Nº EMISIÓN: PERIODO VIGENTE: 01/2009
 FACULTAD: INGENIERÍA ESCUELA: INGENIERÍA QUÍMICA DEPARTAMENTO: TERMODINÁMICA Y FENÓMENOS DE TRANSPORTE ASIGNATURA: FÍSICO QUÍMICA CÓDIGO: 5312 PÁG.: 1 DE: 6 REQUISITOS: TERMODINÁMICA DEL EQUILIBRIO (5311)
FACULTAD: INGENIERÍA ESCUELA: INGENIERÍA QUÍMICA DEPARTAMENTO: TERMODINÁMICA Y FENÓMENOS DE TRANSPORTE ASIGNATURA: FÍSICO QUÍMICA CÓDIGO: 5312 PÁG.: 1 DE: 6 REQUISITOS: TERMODINÁMICA DEL EQUILIBRIO (5311)
Tiempo (minutos) Temperatura (ºC)
 EXAMEN FINAL 3º ESO. FÍSICA Y QUÍMICA. 1.- Al calentar un cierto sólido se ha obtenido la siguiente tabla de datos: Tiempo (minutos) 0 2 4 6 10 12 16 18 20 Temperatura (ºC) -5 0 5 10 20 20 20 25 30 Representa
EXAMEN FINAL 3º ESO. FÍSICA Y QUÍMICA. 1.- Al calentar un cierto sólido se ha obtenido la siguiente tabla de datos: Tiempo (minutos) 0 2 4 6 10 12 16 18 20 Temperatura (ºC) -5 0 5 10 20 20 20 25 30 Representa
Reacciones redox espontáneas
 Celda galvánica o voltaica o electroquímica Pila galvánica o voltaica o electroquímica Cuba galvánica o voltaica o electroquímica Cada una de las partes se denomina: semicelda o semipila o electrodo Pila
Celda galvánica o voltaica o electroquímica Pila galvánica o voltaica o electroquímica Cuba galvánica o voltaica o electroquímica Cada una de las partes se denomina: semicelda o semipila o electrodo Pila
Tema 6: Reacciones químicas
 Tema 6: Reacciones químicas Tema 6: Reacciones químicas 1.- Procesos físicos y químicos 2.- Reacciones químicas 3.- Leyes de las reacciones químicas 4.- Ecuaciones químicas 5.- Cálculos con ecuaciones
Tema 6: Reacciones químicas Tema 6: Reacciones químicas 1.- Procesos físicos y químicos 2.- Reacciones químicas 3.- Leyes de las reacciones químicas 4.- Ecuaciones químicas 5.- Cálculos con ecuaciones
UNIVERSIDAD RICARDO PALMA FACULTAD DE INGENIERIA ESCUELA ACADEMICO PROFESIONAL DE INGENIERIA ELECTRONICA SILABO PLAN DE ESTUDIOS
 1. DATOS GENERALES. ASIGNATURA CODIGO CONDICION UNIVERSIDAD RICARDO PALMA FACULTAD DE INGENIERIA ESCUELA ACADEMICO PROFESIONAL DE INGENIERIA ELECTRONICA SILABO PLAN DE ESTUDIOS 2006-2 NIVEL : 1 CREDITOS
1. DATOS GENERALES. ASIGNATURA CODIGO CONDICION UNIVERSIDAD RICARDO PALMA FACULTAD DE INGENIERIA ESCUELA ACADEMICO PROFESIONAL DE INGENIERIA ELECTRONICA SILABO PLAN DE ESTUDIOS 2006-2 NIVEL : 1 CREDITOS
SGUICEL009QM11-A16V1. Ácido base I: conceptos y teorías
 SGUICEL009QM11-A16V1 Ácido base I: conceptos y teorías Ítem Alternativa Habilidad 1 B Reconocimiento 2 A Comprensión 3 E Reconocimiento 4 E Comprensión 5 E ASE 6 E Comprensión 7 D Comprensión 8 E Comprensión
SGUICEL009QM11-A16V1 Ácido base I: conceptos y teorías Ítem Alternativa Habilidad 1 B Reconocimiento 2 A Comprensión 3 E Reconocimiento 4 E Comprensión 5 E ASE 6 E Comprensión 7 D Comprensión 8 E Comprensión
Programa de la asignatura Curso: 2007 / 2008 INYECCIÓN DE PLÁSTICO (4992)
 Programa de la asignatura Curso: 2007 / 2008 INYECCIÓN DE PLÁSTICO (4992) PROFESORADO Profesor/es: JESÚS PELÁEZ VARA - correo-e: jpelaez@ubu.es FICHA TÉCNICA Titulación: MÁSTER EN COMPONENTES EN AUTOMOCIÓN
Programa de la asignatura Curso: 2007 / 2008 INYECCIÓN DE PLÁSTICO (4992) PROFESORADO Profesor/es: JESÚS PELÁEZ VARA - correo-e: jpelaez@ubu.es FICHA TÉCNICA Titulación: MÁSTER EN COMPONENTES EN AUTOMOCIÓN
Introducción histórica
 Introducción histórica Ácidos y bases se conocen desde la antigüedad. Robert Boyle (s. XVII) propiedades de los ácidos. Primera descripción sistemática de las Lavoisier (1743 1794) Primera teoría sobre
Introducción histórica Ácidos y bases se conocen desde la antigüedad. Robert Boyle (s. XVII) propiedades de los ácidos. Primera descripción sistemática de las Lavoisier (1743 1794) Primera teoría sobre
Aprendizajes esperados
 Disoluciones II Aprendizajes esperados Identificar diluciones. Identificar los factores que afectan la solubilidad. Definir propiedades coligativas. Pregunta oficial PSU Al bajar gradualmente la temperatura,
Disoluciones II Aprendizajes esperados Identificar diluciones. Identificar los factores que afectan la solubilidad. Definir propiedades coligativas. Pregunta oficial PSU Al bajar gradualmente la temperatura,
Conductores Iónicos. BLOQUE IV: CERAMICAS DE ALTAS PRESTACIONES Cerámicas Funcionales
 BLOQUE IV: CERAMICAS DE ALTAS PRESTACIONES Cerámicas Funcionales Conductores Iónicos Bibliografía: Solid State Chemistry: An introduction, L. Smart and E. Moore. 1992 (Cap. 3) Solid State Chemistry and
BLOQUE IV: CERAMICAS DE ALTAS PRESTACIONES Cerámicas Funcionales Conductores Iónicos Bibliografía: Solid State Chemistry: An introduction, L. Smart and E. Moore. 1992 (Cap. 3) Solid State Chemistry and
ÁCIDOS Y BASES: DEFINICIÓN Y DISOLUCIONES. CONCEPTO DE ph.
 UNIDAD 4 PROCESOS DE EQUILIBRIO ÁCIDOS Y BASES: DEFINICIÓN Y DISOLUCIONES. CONCEPTO DE ph. Un ácido es una sustancia que, al ser añadida al agua, produce iones hidrógeno (H + ) /hidronio (H 3 O + ). Una
UNIDAD 4 PROCESOS DE EQUILIBRIO ÁCIDOS Y BASES: DEFINICIÓN Y DISOLUCIONES. CONCEPTO DE ph. Un ácido es una sustancia que, al ser añadida al agua, produce iones hidrógeno (H + ) /hidronio (H 3 O + ). Una
El acumulador redox Fe/Cr : Factores esenciales en su desarrollo
 Workshop LIFE ZAESS Baterías de flujo redox El acumulador redox Fe/Cr : Factores esenciales en su desarrollo Prof. VICENTE MONTIEL LEGUEY Grupo de Electroquímica Aplicada y Electrocatálisis Instituto de
Workshop LIFE ZAESS Baterías de flujo redox El acumulador redox Fe/Cr : Factores esenciales en su desarrollo Prof. VICENTE MONTIEL LEGUEY Grupo de Electroquímica Aplicada y Electrocatálisis Instituto de
Formación académica: Ingeniero de Minas. Universidad de Oviedo.1993 Doctora Ingeniera de Minas. Universidad de Oviedo. 31/01/97
 Marta María Cabeza Simó DNI: 9386766 Y Universidad de Vigo Dep Ingeniería de los Materiales, Mecánica Aplicada y Constucción. Escuela Técnica Superior de Ingenieros Industriales Campus Universitario de
Marta María Cabeza Simó DNI: 9386766 Y Universidad de Vigo Dep Ingeniería de los Materiales, Mecánica Aplicada y Constucción. Escuela Técnica Superior de Ingenieros Industriales Campus Universitario de
ESTRUCTURA DEL ÁTOMO
 ESTRUCTURA DEL ÁTOMO BANDAS DE VALENCIA Y DE CONDUCCIÓN MECANISMOS DE CONDUCCIÓN EN UN SEMICONDUCTOR SEMICONDUCTORES *Semiconductor *Cristal de silicio *Enlaces covalentes. Banda de valencia *Semiconductor
ESTRUCTURA DEL ÁTOMO BANDAS DE VALENCIA Y DE CONDUCCIÓN MECANISMOS DE CONDUCCIÓN EN UN SEMICONDUCTOR SEMICONDUCTORES *Semiconductor *Cristal de silicio *Enlaces covalentes. Banda de valencia *Semiconductor
TEMA 7 ÁCIDOS Y BASES
 TEMA 7 ÁCIDOS Y BASES ÍNDICE 7.1. Concepto de ácido y base Teoría de Arrhenius Teoría de Brönsted-Lowry - Pares ácido-base conjugados 7.2. Fuerza relativa de los ácidos. Contantes y grado de disociación
TEMA 7 ÁCIDOS Y BASES ÍNDICE 7.1. Concepto de ácido y base Teoría de Arrhenius Teoría de Brönsted-Lowry - Pares ácido-base conjugados 7.2. Fuerza relativa de los ácidos. Contantes y grado de disociación
EEQ1 - Experimentación en Ingeniería Química I
 Unidad responsable: Unidad que imparte: Curso: Titulación: Créditos ECTS: 2016 205 - ESEIAAT - Escuela Superior de Ingenierías Industriales, Aeroespacial y Audiovisual de Terrassa 713 - EQ - Departamento
Unidad responsable: Unidad que imparte: Curso: Titulación: Créditos ECTS: 2016 205 - ESEIAAT - Escuela Superior de Ingenierías Industriales, Aeroespacial y Audiovisual de Terrassa 713 - EQ - Departamento
FÍSICA Y QUÍMICA 4º ESO. MCU. Características. Magnitudes angulares. Ley del movimiento.
 FÍSICA Y QUÍMICA 4º ESO Unidad 1. El movimiento Sistema de referencia. o Carácter relativo del movimiento. Conceptos básicos para describir el movimiento. o Trayectoria, posición, desplazamiento. o Clasificación
FÍSICA Y QUÍMICA 4º ESO Unidad 1. El movimiento Sistema de referencia. o Carácter relativo del movimiento. Conceptos básicos para describir el movimiento. o Trayectoria, posición, desplazamiento. o Clasificación
IES Atenea (S.S. de los Reyes) Departamento de Física y Química. PAU Química. Junio 2006 PRIMERA PARTE
 PAU Química. Junio 2006 PRIMERA PARTE Cuestión. Sabiendo que el boro es el primer elemento del grupo trece del Sistema Periódico, conteste razonadamente si las siguientes afirmaciones son verdaderas o
PAU Química. Junio 2006 PRIMERA PARTE Cuestión. Sabiendo que el boro es el primer elemento del grupo trece del Sistema Periódico, conteste razonadamente si las siguientes afirmaciones son verdaderas o
QUÍMICA BÁSICA. 4 horas a la semana 6 créditos. 2 horas teóricas y 2 horas de laboratorio
 QUÍMICA BÁSICA 4 horas a la semana 6 créditos 2 horas teóricas y 2 horas de laboratorio OBJETIVO: El alumno analizará los conceptos básicos de Química para identificar las propiedades de las sustancias
QUÍMICA BÁSICA 4 horas a la semana 6 créditos 2 horas teóricas y 2 horas de laboratorio OBJETIVO: El alumno analizará los conceptos básicos de Química para identificar las propiedades de las sustancias
cromatografía 03/07/2012 INTRODUCCIÓN Etapas de un análisis cuantitativo Curso: Química Analítica II Loreto Ascar 2012 Proceso Analítico
 cromatografía Curso: Química Analítica II Loreto Ascar 2012 INTRODUCCIÓN Cómo determinar un analito en una muestra problema? X Proceso Analítico Etapas de un análisis cuantitativo Elección del método Obtención
cromatografía Curso: Química Analítica II Loreto Ascar 2012 INTRODUCCIÓN Cómo determinar un analito en una muestra problema? X Proceso Analítico Etapas de un análisis cuantitativo Elección del método Obtención
Solidificación e Imperfecciones. en Sólidos
 Preguntas definitivas Capítulo 2 Solidificación e Imperfecciones en Sólidos Ciencia de Materiales 28 PREGUNTA 2.1 Cuándo suele presentar interés el uso de un metal en estado puro?. Justifícalo. Pon un
Preguntas definitivas Capítulo 2 Solidificación e Imperfecciones en Sólidos Ciencia de Materiales 28 PREGUNTA 2.1 Cuándo suele presentar interés el uso de un metal en estado puro?. Justifícalo. Pon un
ALMACENAMIENTO ELECTROQUÍMICO DE ENERGÍA. Margarita Miranda Hernández
 ALMACENAMIENTO ELECTROQUÍMICO DE ENERGÍA Margarita Miranda Hernández Coordinación de Superficies, Interfases y Materiales Compuestos Departamento de Materiales Solares INTRODUCCIÓN SISTEMAS PARA APROVECHAR
ALMACENAMIENTO ELECTROQUÍMICO DE ENERGÍA Margarita Miranda Hernández Coordinación de Superficies, Interfases y Materiales Compuestos Departamento de Materiales Solares INTRODUCCIÓN SISTEMAS PARA APROVECHAR
Un equilibrio heterogéneo muy especial: Equilibrio de Precipitación
 Un equilibrio heterogéneo muy especial: Equilibrio de Precipitación Los equilibrios heterogéneos son aquellos en los cuales los reactivos y productos se presentan en distintos estados de agregación (sólido,
Un equilibrio heterogéneo muy especial: Equilibrio de Precipitación Los equilibrios heterogéneos son aquellos en los cuales los reactivos y productos se presentan en distintos estados de agregación (sólido,
El resultado es el Sistema Periódico. -En el sistema periódico los elementos están colocados por orden creciente de su número atómico (Z).
 Tema 2. La Tabla periódica -Desde hace tiempo los químicos han intentado ordenar los elementos de forma que queden agrupados aquellos que tienen propiedades químicas similares El resultado es el Sistema
Tema 2. La Tabla periódica -Desde hace tiempo los químicos han intentado ordenar los elementos de forma que queden agrupados aquellos que tienen propiedades químicas similares El resultado es el Sistema
LABENGAMB - Laboratorio de Ingeniería Ambiental
 Unidad responsable: Unidad que imparte: Curso: Titulación: Créditos ECTS: 2015 250 - ETSECCPB - Escuela Técnica Superior de Ingenieros de Caminos, Canales y Puertos de Barcelona 713 - EQ - Departamento
Unidad responsable: Unidad que imparte: Curso: Titulación: Créditos ECTS: 2015 250 - ETSECCPB - Escuela Técnica Superior de Ingenieros de Caminos, Canales y Puertos de Barcelona 713 - EQ - Departamento
QUÍMICA Reactividad y equilibrio químico. Oxido - reducción. Tutora: Romina Saavedra
 QUÍMICA Reactividad y equilibrio químico Oxido - reducción Tutora: Romina Saavedra Balance de reacciones de óxido reducción Una reacción redox o de óxido reducción se caracteriza por la existencia de dos
QUÍMICA Reactividad y equilibrio químico Oxido - reducción Tutora: Romina Saavedra Balance de reacciones de óxido reducción Una reacción redox o de óxido reducción se caracteriza por la existencia de dos
CUESTIONARIOS FÍSICA 4º ESO
 DPTO FÍSICA QUÍMICA. IES POLITÉCNICO CARTAGENA CUESTIONARIOS FÍSICA º ESO UNIDADES 8 y 10 Átomos, elementos y compuestos. Las reacciones químicas Mª Teresa Gómez Ruiz 2010 HTTP://WWW. POLITECNICOCARTAGENA.
DPTO FÍSICA QUÍMICA. IES POLITÉCNICO CARTAGENA CUESTIONARIOS FÍSICA º ESO UNIDADES 8 y 10 Átomos, elementos y compuestos. Las reacciones químicas Mª Teresa Gómez Ruiz 2010 HTTP://WWW. POLITECNICOCARTAGENA.
MÁSTER UNIVERSITARIO EN ENERGÍAS RENOVABLES, PILAS DE COMBUSTIBLE E HIDRÓGENO UNIVERSIDAD INTERNACIONAL MENÉNDEZ PELAYO
 MÁSTER UNIVERSITARIO EN ENERGÍAS RENOVABLES, PILAS DE COMBUSTIBLE E HIDRÓGENO UNIVERSIDAD INTERNACIONAL MENÉNDEZ PELAYO Este documento puede utilizarse como documentación de referencia de esta asignatura
MÁSTER UNIVERSITARIO EN ENERGÍAS RENOVABLES, PILAS DE COMBUSTIBLE E HIDRÓGENO UNIVERSIDAD INTERNACIONAL MENÉNDEZ PELAYO Este documento puede utilizarse como documentación de referencia de esta asignatura
TEMA 7: CINÉTICA HETEROGÉNEA FLUIDO - SÓLIDO CQA-7/1
 TEMA 7: CINÉTICA HETEROGÉNEA FLUIDO - SÓLIDO CQA-7/1 PLANTEAMIENTO DEL MODELO CINÉTICO Reacciones heterogéneas fluido-sólido: numerosas y de gran importancia industrial: Se ponen en contacto un gas o un
TEMA 7: CINÉTICA HETEROGÉNEA FLUIDO - SÓLIDO CQA-7/1 PLANTEAMIENTO DEL MODELO CINÉTICO Reacciones heterogéneas fluido-sólido: numerosas y de gran importancia industrial: Se ponen en contacto un gas o un
Celdas galvánicas o voltaicas
 Celdas galvánicas o voltaicas Apellidos, nombre Departamento Centro Atienza Boronat, Mª Julia (matien@qim.upv.es) Herrero Villén, Mª Asunción (maherrero@qim.upv.es) Noguera Murray, Patricia (pnoguera@qim.upv.es)
Celdas galvánicas o voltaicas Apellidos, nombre Departamento Centro Atienza Boronat, Mª Julia (matien@qim.upv.es) Herrero Villén, Mª Asunción (maherrero@qim.upv.es) Noguera Murray, Patricia (pnoguera@qim.upv.es)
Curso interactivo de cromatografía de líquidos. Módulo 1 parte A. Dr. Juan Carlos Vázquez Lira Abril 2016
 Curso interactivo de cromatografía de líquidos Módulo 1 parte A Dr. Juan Carlos Vázquez Lira Abril 2016 Bases de la cromatografía CROMATOGRAFÍA Separación Determinación La cromatografía es una técnica
Curso interactivo de cromatografía de líquidos Módulo 1 parte A Dr. Juan Carlos Vázquez Lira Abril 2016 Bases de la cromatografía CROMATOGRAFÍA Separación Determinación La cromatografía es una técnica
MÉTODO DEL IÓN-ELECTRÓN
 MÉTODO DEL IÓNELECTRÓN Para entender este método se debe tener claro cómo se producen las disociaciones de ácidos, bases y sales (electrolitos). Los ÁCIDOS se disocian en H + y el anión negativo. H H +
MÉTODO DEL IÓNELECTRÓN Para entender este método se debe tener claro cómo se producen las disociaciones de ácidos, bases y sales (electrolitos). Los ÁCIDOS se disocian en H + y el anión negativo. H H +
1817: Döbreiner. Triadas de elementos con propiedades semejantes. 1865: Newlands. Ley de las octavas. Ordenó 55 elementos.
 Evolución histórica de la Tabla Periódica 1817: Döbreiner. Triadas de elementos con propiedades semejantes. 1865: Newlands. Ley de las octavas. Ordenó 55 elementos. 1869: Mendeleev y Meyer: las propiedades
Evolución histórica de la Tabla Periódica 1817: Döbreiner. Triadas de elementos con propiedades semejantes. 1865: Newlands. Ley de las octavas. Ordenó 55 elementos. 1869: Mendeleev y Meyer: las propiedades
