INCOMPATIBILIDADES QUÍMICAS Y CONDICIONES A EVITAR
|
|
|
- Pablo Suárez Ruiz
- hace 6 años
- Vistas:
Transcripción
1 Incompatibilidades sustancias peligrosas. 1 Incompatibilidades químicas y condiciones a evitar 1,1-Dicloroetano 1,1,1- Tricloroetano 1,2- Dicloroetano 1,2-Butanidiol 1,2-Dibromometano 1,2-Dicloroetileno 1,4-Dioxano INCOMPATIBILIDADES QUÍMICAS Y CONDICIONES A EVITAR Se descompone al calentar originando fosgeno y cloruro de hidrógeno. Reacciona con oxidantes fuertes, metales alcalinos y alcalinotérreos y polvos metálicos con riesgo de incendio o explosión. En contacto con bases fuertes forma acetaldehído (gas tóxico e inflamable). Bases fuertes, aluminio, oxidantes fuertes, Mg, Na, K, luz ultravioleta, calor, acetona, óxidos de nitrógeno, metales pulverulentos metales alcalinos y alcalinotérreos, aluminio o magnesio en polvo, amidas alcalinas, ácido nítrico. Oxidantes fuertes. Al, Mg, Na, Zn, K,Ca, agentes oxidantes, bases, amoníaco líquido. En contacto con superficies calientes se desprende bromuro de hidrógeno. En contacto con llamas y superficies calientes se forman gases y vapores tóxicos. Reacciona con oxidantes fuertes. Puede formar peróxidos explosivos. Puede explotar por calentamiento intenso o contacto con las llamas. Puede formar peróxidos explosivos. Reacciona vigorosamente con oxidantes y ácidos fuertes. Reacciona explosivamente con algunos catalizadores. 2- Amino fenol Ácidos fuertes y oxidantes fuertes. Acetaldehído Acetato de amilo Puede formar peróxidos explosivos en contacto con el aire. Reacciona con oxidantes. Puede polimerizar por influencia de ácidos, trazas metálicas y materiales alcalinos. Agentes oxidantes fuertes. Acetato de amonio Agentes oxidantes fuertes, ácidos fuertes. Acetato de etilo Acetato de isoamilo Acetato de metilo Acetato de n-butilo Acetato de propilo Calentamiento. Metales alcalinos, flúor, hidruros, oxidantes fuertes, agua con aire y luz. Luz ultravioleta, bases y ácidos, plásticos. Calentamiento. Sustancias inflamables. Aire, bases, oxidantes fuertes, agua, luz ultravioleta. Ataca muchos metales. Oxidantes fuertes. Materias oxidantes, ataca plásticos.
2 Incompatibilidades sustancias peligrosas. 2 Acetato de sodio Calentamiento por encima de 120 º. Nitratos. Ácidos fuertes.puede polimerizar por calentamiento intenso. Peligro de incendio y explosión por calentamiento o aumento de presión. Reacciona con flúor, oxidantes, cloro y bajo influencia de luz originando riesgo de incendio o explosión. Reacciona con plata, cobre, mercurio y sus sales formando acetiluros sensibles al choque. Calentamiento. Hidróxidos alcalinos, halógenos, hidrocarburos halogenados, halogenuros de halógeno, metales alcalinos, nitrosilos, metales, etanolamina, 1,1,1,-tricloroetano. Puede formar peróxidos explosivos en contacto con oxidantes fuertes como ácido acético, ácido nítrico, y peróxido de hidrógeno. Acetonitrilo Calentamiento originando cianuro de hidrógeno y óxidos de nitrógeno.. Sustancias oxidantes, complejos cianurados. Se descompone en contacto con ácidos, agua y vapor de agua produciendo vapor inflamable y humos tóxicos. Ácido acético (glacial) Calentamiento fuerte. Anhídridos/agua, aldehídos, alcoholes, halogenuros de halógeno, oxidantes fuertes, metales, hidróxidos alcalinos, halogenuros de no metales, etanolamina, bases fuertes. Reacciona con oxidantes como el trióxido de cromo o permanganato potásico. Ataca muchos metales formando hidrógeno. Ácido benzoico Flúor, oxígeno. Oxidantes. Ácido bórico Potasio Ácido cítrico Agentes oxidantes, reductores, bases, nitratos metálicos. Ácido clorhídrico Ácido cloroacético Ácido fluorhídrico Ácido fórmico Aluminio, aminas, carburos, hidruros, flúor, metales alcalinos, metales, KMNO, soluciones fuertes de hidróxidos alcalinos, halogenatos, ácidos sulfúrico concentrado, óxidos de semimetales, aldehídos, sulfuros, siliciuro de litio, éter vinilmetílico, etileno, oxidantes fuertes y aluminio. Ataca los metales formando hidrógeno. Por calentamiento libera gases tóxicos y corrosivos de cloruro de hidrógeno y fosgeno. Reacción con bases. Glicerol + ácido nítrico, hidróxido de amonio, hidróxido sódico, permanganato potásico. Calentamiento. Soluciones de hidróxidos alcalinos, aluminio, oxidantes fuertes, ácido sulfúrico, óxidos no metálicos, nitrocompuestos orgánicos, catalizadores metálicos, óxidos de fósforo, peróxido de hidrógeno. Ataca muchos metales en presencia de agua. Ataca muchos plásticos. Ácido L-ascórbico Calentamiento. Ácido láctico Ácido nítrico, ácido fluorhídrico.
3 Incompatibilidades sustancias peligrosas. 3 Ácido nítrico Ácido orto-fosfórico Ácido oxálico Ácido perclórico Ácido pícrico Ácido sulfúrico Ácido tánico Ácidos orgánicos Acrilamida Acrilatos Calentar. Inflamables orgánicos, compuestos oxidables, disolventes orgánicos, alcoholes, cetonas, aldehídos, anhídridos, aminas, anilinas, nitrilos, nitrocompuestos orgánicos, hidracina, acetiluros, metales y aleaciones metálicas, óxidos metálicos, metales alcalinos y alcalinotérreos, amoníaco, soluciones de hidróxidos alcalinos, ácidos, hidruros, halógenos, compuestos halogenados, óxidos no metálicos, halogenuros de n metales, hidruros de no metales, no metales, fósforos, nitruros, siliciuro de litio, peróxido de hidrógeno, metales en polvo, resinas de intercambio aniónicas. Calentamiento fuerte. bases, metales, óxidos metálicos, nitrometano, bases fuertes. En presencia de calor se descompone originando ácido fórmico y monóxido de carbono. Reacciona con oxidantes fuertes. Reacciona con algunos compuestos de plata formando oxalato de plata explosivo. Soluciones de hidróxidos alcalinos, amoníaco, halogenatos, oxidantes, metales alcalinos y agua/calor. Reacciona con compuestos de plata, mercurio e hipoclorito sódico Nitrilos, alcoholes, semimetales, óxidos de semimetales, sustancias inflamables, halogenuros de halógeno, éteres, metales, ácidos, anhídridos, halógenos, sulfóxidos, inflamables orgánicos, hidrocarburos halogenados, compuestos orgánicos, óxidos no metálicos, reductores, ácido nítrico, ácido sulfúrico concentrado, calor, hidrógeno, impurezas/polvo. Puede descomponerse con explosión por choque, fricción o sacudida. Puede estallar por calentamiento intenso. Formación de compuestos inestables al choque frente al contacto con cobre, plomo, mercurio y cinc. Reacción con oxidantes y agentes reductores. Calentamiento fuerte. agua, metales alcalinos y alcalinotérreos, compuestos alcalinos y alcalinotérreos, amoníaco, soluciones de hidróxidos alcalinos, ácidos, metales (origina hidrógeno), fósforo, halogenuros de halógeno, halogenatos, permanganatos, nitratos, carburos, sustancias inflamables, disolventes orgánicos, acetiluros, nitrilos nitrocompuestos orgánicos, anilinas, peróxidos, picratos, nitruros, cobre, acetaldehído,. Agentes fuertemente oxidantes, bases fuertes, sales de metales pesados, gelatina, albúmina, Ácido sulfúrico, bases, amonio, aminas alifáticas, alcanolaminas, aminas aromáticas. Por calentamiento intenso o influencia de la luz puede polimerizar violentamente. Al descomponerse por calor puede producir gases tóxicos y óxidos de nitrógeno. Reacción violenta con oxidantes. Ácido sulfúrico, ácido nítrico, aminas aromáticas, alcanolaminas.
4 Incompatibilidades sustancias peligrosas. 4 Acroleína Alcohol alílico Alcohol bencílico Alcohol butílico Alcohol isopropílico Alcohol metílico Puede formar peróxidos explosivos. Puede polimerizar con peligro de incendio o explosión. Por calentamiento se producen humos tóxicos. Reacciona con bases, ácidos, aminas, tiourea, sales metálicas, oxidantes con peligro de incendio y explosión. Por combustión origina monóxido de carbono. Por calentamiento se originan humos tóxicos. Reacciona con tetracloruro de carbono, ácido nítrico y ácido clorosulfónico con peligro de incendio y explosión. Oxidantes, halogenuros de no metales, ácido sulfúrico concentrado, iniciadores de la polimerización. Calor, sustancias oxidantes, peróxidos orgánicos, aluminio, trióxido de cromo. Calentamiento fuerte. Metales alcalinos y alcalinotérreos, aluminio, oxidantes, nitrocompuestos orgánicos. Halogenuros de ácido, metales alcalinos y alcalinotérreos, oxidantes, hidruros, dietilo de cinc, halógenos, hipoclorito de sodio. Se descompone por calentamiento intenso desprendiendo formaldehído y monóxido de carbono. Alcohol n-propílico Reacciona con oxidantes fuertes (percloratos y nitratos) Alcoholes y glicoles Ácido sulfúrico, ácido nítrico, bases, aminas alifáticas, isocianatos. Aldehídos Ácidos minerales no oxidantes, ácido sulfúrico, ácido nítrico, bases, amoníaco, aminas alifáticas, alcanolaminas, aminas aromáticas, ácidos fuertes, materias oxidantes. Amidas Ácido sulfúrico, ácido nítrico, amoníaco, isocianatos, fenoles, cresoles. Amoníaco Anhídridos orgánicos Anilina Azidas Benceno Soluciones de hidróxidos alcalinos, ácidos, halógenos y oxidantes. Se forman compuestos inestables frente al choque con óxidos de mercurio, plata y oro. Incompatible con ácidos. Ataca el cobre, aluminio y cinc y sus aleaciones. Ácidos minerales no oxidantes, ácido sulfúrico, ácido nítrico, bases, amoníaco, aminas alifáticas, aminas aromáticas. Oxidantes, halogenuros de semimetales, anhídrido acético, metales alcalinos y alcalinotérreos originando hidrógeno. nitrocompuestos orgánicos, benceno y derivados. Produce humos de amoniaco y vapores inflamables por calentamiento intenso. Reacción con ácidos fuertes, ozono y flúor. Explosivo en contacto con cobre, plomo, aluminio, ácido nítrico, cloruro de benzoilo. Calentamiento fuerte. Ácidos inorgánicos, azufre, halógenos, halogenuros de halógeno, oxidantes, hidrocarburos halogenados. Reacciona con percloratos, ozono y oxígeno líquido.
5 Incompatibilidades sustancias peligrosas. 5 Benzaldehído Calentamiento fuerte. Bases, metales alcalinos, aluminio, hierro, ácido perfórmico, fenoles, aire, oxígeno. Benzoato de metilo Oxidantes fuertes. Borohidruro de sodio Calor. Ácidos, agua, oxidantes, hidróxidos alcalinos. Bromuro de etidio Calentamiento fuerte. Material oxidante. Bromuro de metilo Por calentamiento se desprenden humos tóxicos. Incompatible con oxidantes fuertes, aluminio y caucho. Calcio hidróxido Ácidos, hidrógeno sulfuro, metales ligeros. Cetonas Ácido sulfúrico, ácido nítrico, aminas alifáticas, alcanolaminas. Cianuro de potasio Ácidos y bases fuertes, plata amoniacal, nitrito de sodio o potasio, cloratos, nitritos, oxidantes. La sustancia se descompone en contacto con agua, humedad, carbonatos alcalinos produciendo cianuro de hidrógeno. Ciclohexano Se pueden generar cargas electrostáticas por agitación- Ciclohexanona Clorato de potasio Cloro Clorobenceno Clorobromometano Cloruro de amonio Cloruro de etilo Calentamiento. Peróxido de hidrógeno, ácido nítrico, agentes oxidantes originando riesgo de incendio y explosión. Produce dióxido de cloro, cloro y oxígeno al calentar intensamente, o en contacto con sustancias orgánicas, agentes combustibles, ácido sulfúrico, polvos metálicos, alcoholes o sustancias con el grupo amonio. Reacciona con materiales orgánicos o combustibles, azufre, vapores inflamables, fósforo rojo, hidracina, hidroxilamina, cloruro de cinc, hiposulfito sódico, aminas, azúcares con ferricianuro, hidrazina, vapores inflamables. Reacciona con muchos compuestos orgánicos, amoníaco y partículas metálicas con peligro de incendio y explosión. Altas temperaturas. Metales alcalinos y alcalinotérreos, oxidantes, sulfóxidos. Reacciona violentamente con cloratos. Ataca el caucho. Al calentarse desprende, cloro, fosgeno, ácido clorhídrico, cloruro de hidrógeno. Reacciona con oxidantes, acero, aluminio, magnesio y cinc. Calentamiento fuerte. Hidróxidos alcalinos, cloro, cloratos, nitratos, nitritos, halogenuros de halógeno. Reacciona con ácidos fuertes, amoníaco. Al calentarse desprende cloruro de hidrógeno y fosgeno. Reacciona violentamente con oxidantes, metales alcalinos, calcio, magnesio, aluminio en polvo y cinc. Reacciona con el agua o vapor produciendo cloruro de hidrógeno.
6 Incompatibilidades sustancias peligrosas. 6 Cloruro de metilo La sustancia se descompone al arder en contacto con materias oxidantes, amidas, aminas, aluminio produciendo cloruro de hidrógeno y fosgeno. Cloruro de vinilo Puede formar peróxidos en circunstancias específicas iniciando una polimerización explosiva. También polimerizará por calentamiento intenso y por influencia del aire, luz, en contacto con un catalizador, oxidantes fuertes y metales como cobre o aluminio con peligro de incendio o explosión. Diacetona alcohol Oxidantes, alcoholes, aminas, dióxido de carbono. Diaminobencidina Diclorobenceno Diclorometano Dicloruro de cadmio Dicloruro de mercurio Calentamiento fuerte. Halogenatos, permanganatos, nitratos, oxidantes fuertes. Metales alcalinos y alcalinotérreos, hidrocarburos halogenados, aluminio, metales ligeros, agua. Por combustión produce fosgeno y cloruro de hidrógeno. Se descompone por ácidos produciendo humos altamente tóxicos. Metales alcalinos y alcalinotérreos, metales en polvo, óxidos de nitrógeno, alcoholatos, amidas alcalinas, ácido perclórico, nítrico, óxidos no metálicos, oxígenos, alcoholes, hidrocarburos aromáticos, agua / KMnO, hidrocarburos aromáticos/ácidos. Oxidantes fuertes, metanol, aluminio, ácido nítrico, bases fuertes. Se descompone por calentamiento intenso formando humos muy tóxicos de cadmio y cloro. Reacciona con oxidantes fuertes. Explosivo en contacto con fósforo, antimonio, arsénico, sales de plata, por calor o impacto. Dicromato de sodio Aminas. Dicromato potásico Inflamables orgánicos, anhídridos, hidracina y derivados, hidroxilamina, sulfuros/agua, reductores, ácido sulfúrico concentrado, glicerina, boro, hierro magnesio, metales en polvo. Dietilbenceno Dióxido de carbono. Dimetilsulfóxido Bromometano, ácido perclórico, materiales oxidantes. Dióxido de plomo Materiales reductores, aluminio en polvo, dióxido de azufre. Disulfuro de carbono EDTA Aminas aromáticas. Puede reaccionar por calentamiento intenso. En contacto con superficies calientes y con el aire puede producir gases tóxicos. Reacciona violentamente con oxidantes, azidas, sodio, potasio y cinc.. Calentamiento. Agentes oxidantes fuertes, bases fuertes y cobre. Niquel. Esteres Ácido sulfúrico, ácido nítrico.
7 Incompatibilidades sustancias peligrosas. 7 Alcohol etílico Calentamiento fuerte. metales alcalinos y alcalinotérreos, óxidos alcalinos, oxidantes fuertes. Etanolamina Calentamiento fuerte. Ácidos fuertes y oxidantes. Éter dietílico Éter diisopropílico Halógenos, halogenuros de halógeno, no metales, oxihalogenuros no metálicos, oxidantes fuertes, cromilo cloruro, nitratos, cloruros metálicos, ácidos metálicos, material orgánico, compuestos de azufre, cromatos. Calentamiento. Aldehídos, aminas, ácidos minerales, oxidantes, cinc. Puede formar peróxidos explosivos. Éteres Ácidos fuertes. Éteres de glicol Ácido sulfúrico, isocianatos. Etilen glicol Dióxido de carbono, agua pulverizada. Etilmetilcetona Oxidantes, cloroformo, hidróxidos alcalinos. Fenol Puede explotar por calentamiento intenso por encima de 78 ºC. Reacciona con oxidantes. Reacciona con formaldehído, hipoclorito de calcio, nitrito de sodio. Fenoles y cresoles Ácido sulfúrico, ácido nítrico, bases, aminas alifáticas, amoníaco. Fluoruro de sodio Ácidos. Formaldehído Fósforo (blanco) Calentamiento. Metales alcalinos, ácidos, óxidos de nitrógeno, peróxido de hidrógeno, oxidantes, ácido perfórmico, oxidantes fuertes (peróxido de hidrógeno), carbonato de magnesio, bases fuertes, fenol, urea. Se puede incendiar espontáneamente en contacto con el aire produciendo humos tóxicos. Reacciona violentamente con oxidantes, halógenos y azufre. Reacciona con bases fuertes produciendo fosfina. Furfural Glicerina La sustancia polimeriza bajo la influencia de ácidos o bases con peligro de incendio o explosión. Reacciona fuertemente con oxidantes. Reacción con aceite mineral. Forma acroleína en contacto con superficies calientes. Reacciona con oxidantes fuertes con riesgo de incendio y explosión. Glutaraldehído Iniciadores de la polimerización y materiales oxidantes Haluros de vinilo Ácido nítrico. Heptano Dióxido de carbono. Oxidantes fuertes. Ataca muchos plásticos. Hidrocarburos halogenados El dicloroetil éter es incompatible con el ácido sulfúrico, el tricloroetileno es incompatible con las bases, la etilendiamina no es compatible con el dicloruro de etileno.
8 Incompatibilidades sustancias peligrosas. 8 Hidrocarburos aromáticos Hidrocarburos no halogenados Ácido nítrico. Sustancias oxidantes, ácidos fuertes. Hidrógeno peróxido (>60%) Metales alcalinos y alcalinotérreos, sales alcalinas, hidróxidos alcalinos, metales, óxidos metálicos, sales metálicas, no metales, óxidos no metálicos, aldehídos, alcoholes, aminas, amoníaco, hidracina, hidruros, sustancias inflamables, éteres, ácidos, anhídridos, oxidantes, compuestos orgánicos, peróxidos, impurezas(polvo, disolventes orgánicos, nitrocompuestos orgánicos, latón, Pt, Ag, Cu, Cr, Fe, Zn, Pb, Mn. Hidroquinona Oxidantes fuertes, soluciones de hidróxidos alcalinos. Hidróxido de hidracina Hidróxido de potasio Hidróxido de sodio Hipoclorito de calcio Hipoclorito de sodio Dinitroclorobenceno, óxido de mercurio, sodio, calor. Reacciona violentamente con ácidos fuertes y con estaño, cinc, aluminio y plomo originando hidrógeno.metales, ácidos, alcoholes, dióxido de cloro, tetrahidrofurano. Metales, metales ligeros, ácidos, nitrilos, metales alcalinotérreos en polvo, compuestos de amonio, cianuros, magnesio, nitrocompuestos orgánicos, inflamables orgánicos, fenoles y compuestos oxidables. Junto con cinc, estaño, plomo y aluminio se puede formar hidrógeno. Calentamiento. Aminas, antraceno, carbón, etanol, glicerol, óxidos de hierro o manganeso, grasa o aceite, mercaptanos, nitrometano, material orgánico, sulfuros orgánicos, azufre. Puede explotar en contacto con tetracloruro de carbono. Aminas, calor, ácidos, metanol en presencia de ácidos, materiales orgánicos combustibles. Isobutilmetilcetona Calentamiento. Oxidantes. Puede formar peróxidos explosivos. Isocianatos Ácidos minerales no oxidantes, ácido sulfúrico, ácido nítrico, ácidos orgánicos, bases, amoníaco, aminas alifáticas, alcanolaminas, aminas aromáticas, amidas, alcoholes, glicoles. Isooctano Calentamiento. Oxidantes fuertes. Mercurio Amoníaco, óxido de etileno, oxidantes, nitratos, cloratos, ácido nítrico con etanol, acetiluros, metales alcalinos, azidas, aminas, halógenos, ácidos, halogenóxidos. Metacrilato de metilo Nitratos, oxidantes, peróxidos, bases fuertes. Metil etil cetona Oxidantes fuertes y ácidos inorgánicos con peligro de incendio. Reacciona con isopropanol, peróxido de hidrógeno / ác. Nítrico.
9 Incompatibilidades sustancias peligrosas. 9 Metilamina N, N-Dimetilformamida Calentamiento. Alcoholes, halógenos, hidrocarburos halogenados, óxidos de nitrógeno, dióxido de carbono, monóxido de carbono, óxido de etileno, hidruros de no metales, óxidos no metálicos, óxidos de semimetales, acetileno, Metales alcalinos, halógenos, halogenuros, reductores, trietilo de aluminio, nitratos, óxidos metálicos, oxidantes fuertes, hidrocarburos halogenados. Por combustión puede formar dimetilamina, óxidos de nitrógeno y monóxido de carbono. N- Amilo Acetato Calentamiento. Metales alcalinos, oxidantes. N-butilamina Reacciona con oxidantes fuertes y ácidos. N-Hexano Calentamiento. Oxidantes fuertes. N-Nonano Calentamiento fuerte. Oxidantes fuertes. N-Octano Oxidantes fuertes. Nitrato de amonio Nitrato de sodio Al calentar se puede producir combustión violenta o explosión. Se descompone por calentamiento intenso produciendo óxidos de nitrógeno. Reacciona con materiales combustibles y reductores. Se descompone al calentarla desprendiendo óxidos de nitrógeno y oxígeno. Reacciona con materiales combustibles y reductores. Materiales fácilmente oxidables, aluminio, óxido de aluminio, fibras orgánicas. Nitrilos Ácido sulfúrico. Nitrito de sodio Nitrobenceno Puede estallar por calentamiento intenso. Se descompone en contacto con ácidos débiles. Reacciona con materiales combustibles y reductores originando riesgo de incendio y explosión. Hidrazina, haluros de amonio, sales de amonio, tiocianatos, potasio cianato, ferricianuros, material combustible, cianuros metálicos, fenol, sodio disulfito, sodio tiosulfato, urea, madera. Reductores, soluciones de hidróxidos alcalinos, metales alcalinos, ácidos fuertes, peróxidos. Por calentamiento intenso puede ocasionar humos corrosivos conteniendo óxidos de nitrógeno. Nitrocompuestos Bases, amoníaco, aminas alifáticas, alcanolaminas, aminas aromáticas. Nitroetano Nitrometano Formación de compuestos inestables frente al choque por calentamiento rápido o en contacto con álcalis fuertes, ácidos o combinación de aminas y óxidos de metales pesados. Calentamiento. Hidróxidos alcalinos, amoníaco, halogenuros, hidrocarburos halogenados, haloganatos, compuestos orgánicos, oxidantes, aldehídos, anilinas, soluciones fuertes de hidróxidos alcalinos, ácidos. Con aminas forma compuestos sensibles al choque. Puede descomponerse con explosión por choque fricción o sacudida.
10 Incompatibilidades sustancias peligrosas. 10 Óxido de etileno Ozono Óxidos, cloruros, ácidos, bromometano, alcohol, amoníaco, hidróxidos alcalinos, óxidos de hierro, plata, mercurio, magnesio. Sodio metálico y sustancias combustibles. Puede formar peróxidos explosivos con alquenos. Reacciona con materiales combustibles y reductores. Reacciona con alquenos, compuestos aromáticos, éteres, bromo, compuestos de nitrógeno y caucho. Paraformaldehído Oxidantes, ácidos y bases fuertes. Pentaclorobenceno Ácidos o humos ácidos. Pentaclorofenol Percloroetileno Permanganato de potasio Piridina Plata Plata nitrato Sílica Gel Sulfato de bario Sulfato de mercurio Oxidantes fuertes, bases fuertes, cloruros ácidos, anhídridos ácidos. Se descompone al calentar por encima de los 200 ºC produciendo cloruro de hidrógeno, dioxinas y fenoles clorados. Aluminio, Dióxido de nitrógeno, hidróxido de sodio, oxidantes fuertes, ácido nítrico. Ácido acético, acetona, alcoholes con ácido nítrico, glicerol, ácido clorhídrico, ácido fluorhídrico, peróxido de hidrógeno, compuestos orgánicos oxigenados, etilen glicol, propano 1,2-diol, manitol, trietanolamina, acetaldehído, polipropileno, ácido sulfúrico, N,N-dimetilformamida, glicerina, azufre, ácido fluorhídrico, fósforo, compuestos de amonio. Oxidantes fuertes. Ácidos fuertes, flúor, halogenuros de halógeno, cromatos, pecromatos, óxidos de nitrógeno, sulfóxidos, anhídridos. Por combustión forma humos tóxicos (aminas). Al calentar intensamente se origina cianuro de hidrógeno. Con acetileno se forman compuestos inestables al choque. La plata dividida finamente en contacto con peróxidos de hidrógeno puede estallar. En contacto con amoníaco puede originar compuestos explosivos en seco. Reacciona con ácido nítrico diluido y ácido sulfúrico concentrado caliente. Amonio hidróxido, etanol, amonio, amonio con sodio carbonato o sodio hidróxido, bases, aluminio, carbón, carbonatos, cloruros, fosfatos, plásticos, tiocianatos, ácido tánico. Ácido fluorhídrico Fósforo. La reducción con aluminio produce reacción violenta. Forma humos tóxicos de óxidos de azufre por calentamiento intenso. Al calentar se pueden formar humos de óxidos de azufre y mercurio. Reacciona violentamente con cloruro de hidrógeno. Sulfato de plomo Potasio Sulfuro de hidrógeno Metales alcalinos, hidróxidos alcalinos, amoníaco, aminas, oxidantes fuertes, halogenuros e halógeno y halógenos.
11 Incompatibilidades sustancias peligrosas. 11 Tetracloroetileno Tetracloruro de carbono Tetrahidrofurano Tetróxido de osmio Metales alcalinos y alcalinotérreos, metales pulverulentos, hidróxidos alcalinos, oxígeno, óxidos de nitrógeno. Por contacto con superficies calientes se origina cloruro de hidrógeno, fosgeno y cloro. Se descompone en contacto con humedad produciendo ácido trocloroacético y cloruro de hidrógeno. Calentamiento fuerte. Metales alcalinos y alcalinotérreos, aluminio en polvo, amidas alcalinas, aire/oxígeno, halogenuros de aluminio, trietilo de aluminio, amidas alcalinas. Reacciona con algunos metales como Al, Ba, Mg, K, Na y también con F y otras sustancias originando peligro de incendio y explosión. Calentamiento fuerte. Oxidantes fuertes, potasio hidróxido, litio aluminio hidróxido, sodio hidróxido, sodio, aluminio, hidrógeno. Se pueden formar peróxidos explosivos. Calentamiento. Reacciona con combustibles y reductores. Forma compuestos inestables con bases. Reacciona con ácido clorhídrico originando cloro gaseoso tóxico. Timol Agentes oxidantes fuertes, bases fuertes. Tiosulfato de sodio Nitratos metálicos. Nitritos y peróxidos, ácidos. Tolueno Tribromometano Tricloroetileno Triclorometano Calentamiento fuerte. Ácido nítrico concentrado, ácido sulfúrico, oxidantes fuertes, cloratos, halogenuros de halógeno, azufre/calor, óxidos de nitrógeno, nitrocompuestos orgánicos. Acetona, hidróxido de potasio, aluminio en polvo, cinc, magnesio, cloroformo, éteres, bases. Por calentamiento desprende bromuro de hidrógeno. Reacciona con metales alcalinos. Epóxidos, potasio hidróxido, sodio hidróxido, oxidantes, meales alcalinos y alcalinotérreos, metales en polvo, amidas alcalinas, hidruros de semimetales, oxígeno, metales ligeros. En contacto con superficies calientes se forma fosgeno, cloruro de hidrógeno y cloro. En contacto con bases fuertes se descompone produciendo dicloroacetileno. Reacciona con Li, Mg, Ti, Ba y Na. Bases fuertes, aluminio, magnesio, sodio, potasio, acetona, litio, hidróxido sódico con metanol. En contacto con superficies calientes se producen humos tóxicos de fosgeno, cloro y cloruro de hidrógeno. Se descompone lentamente por la influencia de la luz y el aire. Trietanolamina Calentamiento en estado gaseoso. Ácidos, anhídridos, oxidantes. Trióxido de arsénico Calentamiento. Ácidos, agentes oxidantes, halógenos. Trióxido de cromo Vinil acetato Ácido acético, anilina, quinolina, alcohol, acetona, grasa, oxidantes, material orgánico. Ácidos minerales no oxidantes, ácido sulfúrico, ácido nítrico, amoníaco, aminas alifáticas, alcanolaminas.
12 Incompatibilidades sustancias peligrosas. 12 Xileno Yoduro potásico Materiales oxidantes. Ácido sulfúrico, ácido nítrico, azufre. Metales alcalinos, amoníaco, halogenuros de halógeno, flúor, peróxido de hidrógeno. Sustancias inflamables.
INCOMPATIBILIDADES QUÍMICAS Y CONDICIONES A EVITAR
 INCOMPATIBILIDADES QUÍMICAS Y CONDICIONES A EVITAR En algunas situaciones la mezcla de sustancias químicas puede ser peligrosa. La mejor manera de evitar esta situación consiste en separar las sustancias
INCOMPATIBILIDADES QUÍMICAS Y CONDICIONES A EVITAR En algunas situaciones la mezcla de sustancias químicas puede ser peligrosa. La mejor manera de evitar esta situación consiste en separar las sustancias
ANEXO II: TABLA DE INCOMPATIBILIDADES QUÍMICAS
 ANEXO II: TABLA DE INCOMPATIBILIDADES QUÍMICAS 1,1-Dicloroetano 1,1,1-Tricloroetano 1,2-Dicloroetano 1,2-Butadiol 1,2-Dibromometano 1,2-Dicloroetileno 1,4-Dioxano. 2-Amino fenol. Acetaldehído. Acetato
ANEXO II: TABLA DE INCOMPATIBILIDADES QUÍMICAS 1,1-Dicloroetano 1,1,1-Tricloroetano 1,2-Dicloroetano 1,2-Butadiol 1,2-Dibromometano 1,2-Dicloroetileno 1,4-Dioxano. 2-Amino fenol. Acetaldehído. Acetato
GUIA DE RESISTENCIAS QUIMICAS PARA TUBERIA DE POLIPROPILENO COPOLIMERO RANDOM (TUBOPLUS)
 GUIA DE RESISTENCIAS QUIMICAS PARA TUBERIA DE POLIPROPILENO COPOLIMERO RANDOM (TUBOPLUS) R = Alta resistencia RM = Resistencia media NR = No resiste Reactivo químico Concentración Temperatura 20º Temperatura
GUIA DE RESISTENCIAS QUIMICAS PARA TUBERIA DE POLIPROPILENO COPOLIMERO RANDOM (TUBOPLUS) R = Alta resistencia RM = Resistencia media NR = No resiste Reactivo químico Concentración Temperatura 20º Temperatura
RESISTENCIA QUÍMICA GEOMEMBRANA PEAD ALVATECH 5002
 ABREVIATURAS v Satisfactorio x Insatisfactorio! Limite de aplicación posible --- No comprobado RESISTENCIA QUÍMICA GEOMEMBRANA PEAD ALVATECH 5002 CONCENTRACIÓN sol. sat. = solución saturada acuosa, preparada
ABREVIATURAS v Satisfactorio x Insatisfactorio! Limite de aplicación posible --- No comprobado RESISTENCIA QUÍMICA GEOMEMBRANA PEAD ALVATECH 5002 CONCENTRACIÓN sol. sat. = solución saturada acuosa, preparada
Guía de Resistencia Química
 Guía de Resistencia Química 1 Índice de contenidos RESISTENCIA QUÍMICA DE LOS ELASTÓMEROS SBR, Cuacho Natural, Neopreno, NBR, EPDM, IIR, Hypalon, Silicona, Viton, Kalrez... 3 RESISTENCIA QUÍMICA DE MATERIALES
Guía de Resistencia Química 1 Índice de contenidos RESISTENCIA QUÍMICA DE LOS ELASTÓMEROS SBR, Cuacho Natural, Neopreno, NBR, EPDM, IIR, Hypalon, Silicona, Viton, Kalrez... 3 RESISTENCIA QUÍMICA DE MATERIALES
NUMA INDUSTRIAL, S.A.
 TABLA DE S QUIMICAS v Satisfactorio x Insatisfactorio! Limite de aplicación posible --- No comprobado CONCENTRACIÓN sol. sat. = solución saturada acuosa, preparada a 20º C sol. = solución acuosa con concentración
TABLA DE S QUIMICAS v Satisfactorio x Insatisfactorio! Limite de aplicación posible --- No comprobado CONCENTRACIÓN sol. sat. = solución saturada acuosa, preparada a 20º C sol. = solución acuosa con concentración
Guía de Resistencia Química para polietileno de alta densidad.
 Guía de Resistencia Química para polietileno de alta densidad. Nomenclatura Químico o disolvente Guía de resistencias químicas para polietileno de alta densidad S= Satisfactorio, si se recomienda emplear
Guía de Resistencia Química para polietileno de alta densidad. Nomenclatura Químico o disolvente Guía de resistencias químicas para polietileno de alta densidad S= Satisfactorio, si se recomienda emplear
ESTANDAR REFORZADO EXTRA REFORZADO. Concentración %vol
 DENSIDAD 1.00 a 1.20 1.21 a 1.50 1.51 a 1.90 ESTANDAR REFORZADO EXTRA REFORZADO Concentración Temperatura Empaque a utilizar Compuesto 21 C 60 C Aceite de alcanfor normal desc NR viton pp/pe Aceite de
DENSIDAD 1.00 a 1.20 1.21 a 1.50 1.51 a 1.90 ESTANDAR REFORZADO EXTRA REFORZADO Concentración Temperatura Empaque a utilizar Compuesto 21 C 60 C Aceite de alcanfor normal desc NR viton pp/pe Aceite de
Libretto venturi (versione espagnolo).qxd 06/07/2007 0:05 Página 1
 ibretto venturi (versione espagnolo).qxd 6/7/7 :5 Página a nueva serie de Inyectores V PUS está disponible en 3/4, y /2. Fue estudiada para aplicaciones donde haga falta mezclar aire o líquidos el la conducción
ibretto venturi (versione espagnolo).qxd 6/7/7 :5 Página a nueva serie de Inyectores V PUS está disponible en 3/4, y /2. Fue estudiada para aplicaciones donde haga falta mezclar aire o líquidos el la conducción
GRUPOS Y SUBGRUPOS GENÉRICOS DE RESIDUOS PELIGROSOS
 Página 1 de 10 1. RELACIÓN DE GRUPOS GENÉRICOS DE RESIDUOS PELIGROSOS...2 1.1. RELACIÓN DE SUBGRUPOS GENÉRICOS DE RESIDUOS PELIGROSOS... 3 2. CARACTERÍSTICAS DE LOS RESIDUOS PELIGROSOS... 4 Fecha de entrada
Página 1 de 10 1. RELACIÓN DE GRUPOS GENÉRICOS DE RESIDUOS PELIGROSOS...2 1.1. RELACIÓN DE SUBGRUPOS GENÉRICOS DE RESIDUOS PELIGROSOS... 3 2. CARACTERÍSTICAS DE LOS RESIDUOS PELIGROSOS... 4 Fecha de entrada
Resistencia química de DONSEN PPR
 Resistencia química de DONEN PPR Introducción a tabla en este documento reúne la información derivada de resultados de pruebas y de la experiencia de la resistencia química del polipropileno DONEN. Esta
Resistencia química de DONEN PPR Introducción a tabla en este documento reúne la información derivada de resultados de pruebas y de la experiencia de la resistencia química del polipropileno DONEN. Esta
POLIETILENO DE ALTA DENSIDAD (PEAD)
 TABLA DE RESISTENCIA QUÍMICA. POLIETILENO DE ALTA DENSIDAD (PEAD) Observación: Las informaciones expresadas en la siguiente tabla son a titulo informativo y por lo tanto sujetas a modificaciones, dependiendo
TABLA DE RESISTENCIA QUÍMICA. POLIETILENO DE ALTA DENSIDAD (PEAD) Observación: Las informaciones expresadas en la siguiente tabla son a titulo informativo y por lo tanto sujetas a modificaciones, dependiendo
INCOMPATIBILIDADES ENTRE PRODUCTOS QUÍMICOS
 CÓDIGO FNS/008 Fecha: Abril de 2009 Revisión: 02 Página: 1 de 6 Los productos que pueden reaccionar entre sí de forma violenta deben almacenarse conjuntamente, especialmente a partir de ciertas cantidades.
CÓDIGO FNS/008 Fecha: Abril de 2009 Revisión: 02 Página: 1 de 6 Los productos que pueden reaccionar entre sí de forma violenta deben almacenarse conjuntamente, especialmente a partir de ciertas cantidades.
REJILLAS Resistencia química
 REJILLAS Resistencia química Concentracion Rejilla ISO Rejilla Vinilester % Estándar Estándar AMBIENTE QUÍMICO Moldeada Moldeada Temp Temp Max. C Max. C ACEITE DE COCO Todas NR 71 ACEITE DE ECHADOR 100
REJILLAS Resistencia química Concentracion Rejilla ISO Rejilla Vinilester % Estándar Estándar AMBIENTE QUÍMICO Moldeada Moldeada Temp Temp Max. C Max. C ACEITE DE COCO Todas NR 71 ACEITE DE ECHADOR 100
ALMACENAMIENTO DE PRODUCTOS QUÍMICOS
 ALMACENAMIENTO DE PRODUCTOS QUÍMICOS El almacenamiento de sustancias químicas dentro de los laboratorios docentes y de investigación, presenta unas características particulares con relación a: - Nº de
ALMACENAMIENTO DE PRODUCTOS QUÍMICOS El almacenamiento de sustancias químicas dentro de los laboratorios docentes y de investigación, presenta unas características particulares con relación a: - Nº de
CONTENIDO INTRODUCCIÓN 6. 1. OBJETIVOS 8 1.1. Objetivo General 8 1.2. Objetivos Específicos 8
 Jairo 2 CONTENIDO INTRODUCCIÓN 6 1. OBJETIVOS 8 1.1. Objetivo General 8 1.2. Objetivos Específicos 8 2. ESTRATEGIAS DE ALMACENAMIENTO DE SUSTANCIAS QUIMICAS 9 3. AREAS DE ALMACENAMIENTO 11 3.1. Estantería
Jairo 2 CONTENIDO INTRODUCCIÓN 6 1. OBJETIVOS 8 1.1. Objetivo General 8 1.2. Objetivos Específicos 8 2. ESTRATEGIAS DE ALMACENAMIENTO DE SUSTANCIAS QUIMICAS 9 3. AREAS DE ALMACENAMIENTO 11 3.1. Estantería
Tabla de Compatibilidad Química A = Excelente. B = Bueno. C = Pobre. D = No Usar. * = No Información
 Aceite Crudo B B B A A * A A C A A A A Aceite de Alquitrán A A A A A D C A * A A A A Aceite de Castor A B B A A B A A A A A A A Aceite de Coco B C C B * A A A A A A A A Aceite de Grasa de Cerdo B C C B
Aceite Crudo B B B A A * A A C A A A A Aceite de Alquitrán A A A A A D C A * A A A A Aceite de Castor A B B A A B A A A A A A A Aceite de Coco B C C B * A A A A A A A A Aceite de Grasa de Cerdo B C C B
INSTITUTO CULTURAL TAMPICO COORDINACIÓN LABORATORIOS DE CIENCIAS
 REACTIVO GRADO DE REACTIVIDAD EXISTENCIA 1 Aceite de inmersión Tipo B para microscopia 0 180 ml 2 Acetato de magnesio 0 410 g 3 Acetato de sodio 0 880 g 4 Ácido Cítrico anhidro 0 45 g 5 Ácido oxálico 0
REACTIVO GRADO DE REACTIVIDAD EXISTENCIA 1 Aceite de inmersión Tipo B para microscopia 0 180 ml 2 Acetato de magnesio 0 410 g 3 Acetato de sodio 0 880 g 4 Ácido Cítrico anhidro 0 45 g 5 Ácido oxálico 0
LABORATORIO DE CIENCIAS BACHILLERATO INVENTARIO DE REACTIVOS CICLO ESCOLAR AGOSTO 2014
 REACTIVO GRADO DE REACTIVIDAD EXISTENCIA Junio 2014 1 Acetato de magnesio 0 450 g 2 Acetato de sodio 0 1110 g 3 Ácido Cítrico anhidro 0 50 g 4 Ácido oxálico 0 400 g 5 Ácido palmítico 0 101.5 g 6 Agar bacteriológico
REACTIVO GRADO DE REACTIVIDAD EXISTENCIA Junio 2014 1 Acetato de magnesio 0 450 g 2 Acetato de sodio 0 1110 g 3 Ácido Cítrico anhidro 0 50 g 4 Ácido oxálico 0 400 g 5 Ácido palmítico 0 101.5 g 6 Agar bacteriológico
ARIETE 25, RESISTENCIA QUIMICA
 ARIETE 25, REITENCIA QUIMICA En las tablas que presentamos a continuación se detalla información sobre la resistencia química del polipropileno (PP) a diversos fluidos. La información se basa en los valores
ARIETE 25, REITENCIA QUIMICA En las tablas que presentamos a continuación se detalla información sobre la resistencia química del polipropileno (PP) a diversos fluidos. La información se basa en los valores
Compuesto N. Stock N. tradicional N. sistemática. óxido de hierro (III) óxido férrico trióxido de dihierro
 Ejemplos de óxidos básicos FeO Fe 2 O 3 Cu 2 O CuO CaO PbO 2 óxido de hierro (II) óxido ferroso monóxido de hierro óxido de hierro (III) óxido férrico trióxido de dihierro óxido de cobre (I) óxido cuproso
Ejemplos de óxidos básicos FeO Fe 2 O 3 Cu 2 O CuO CaO PbO 2 óxido de hierro (II) óxido ferroso monóxido de hierro óxido de hierro (III) óxido férrico trióxido de dihierro óxido de cobre (I) óxido cuproso
LABORATORIOS DE CIENCIAS INVENTARIO DE REACTIVOS Ciclo escolar ACTUALIZACION FEBRERO 2014 BACHILLERATO
 REACTIVO EXISTENCIA GRADO DE REACTIVIDAD 1 Acetato de magnesio 450 g 0 2 Acetato de sodio 950 g 0 3 Ácido Cítrico anhidro 60 g 0 4 Ácido oxálico 400 g 0 5 Ácido palmítico 101.5 g 0 6 Agar bacteriológico
REACTIVO EXISTENCIA GRADO DE REACTIVIDAD 1 Acetato de magnesio 450 g 0 2 Acetato de sodio 950 g 0 3 Ácido Cítrico anhidro 60 g 0 4 Ácido oxálico 400 g 0 5 Ácido palmítico 101.5 g 0 6 Agar bacteriológico
LISTADOS NACIONALES DE SUSTANCIAS QUIMICAS PELIGROSAS
 LISTADOS NACIONALES DE SUSTANCIAS QUIMICAS PELIGROSAS Listado 1: Listado según la Guía de Respuesta en Caso de Emergencia GRE Listado 2: Listados Nacionales de Productos Químicos Prohibidos, Peligrosos
LISTADOS NACIONALES DE SUSTANCIAS QUIMICAS PELIGROSAS Listado 1: Listado según la Guía de Respuesta en Caso de Emergencia GRE Listado 2: Listados Nacionales de Productos Químicos Prohibidos, Peligrosos
LA PROTECCIÓN INDIVIDUAL FRENTE A LA EXPOSICIÓN POR INHALACIÓN DE SUSTANCIAS QUÍMICAS: EQUIPOS DE PROTECCIÓN INDIVIDUAL (EPI)
 LA PROTECCIÓN INDIVIDUAL FRENTE A LA EXPOSICIÓN POR INHALACIÓN DE SUSTANCIAS QUÍMICAS: EQUIPOS DE PROTECCIÓN INDIVIDUAL (EPI) La absorción de un contaminante químico por el organismo supone su incorporación
LA PROTECCIÓN INDIVIDUAL FRENTE A LA EXPOSICIÓN POR INHALACIÓN DE SUSTANCIAS QUÍMICAS: EQUIPOS DE PROTECCIÓN INDIVIDUAL (EPI) La absorción de un contaminante químico por el organismo supone su incorporación
NTP 479: Prevención del riesgo en el laboratorio químico: reactividad de los productos químicos (II)
 NTP 479: Prevención del riesgo en el laboratorio químico: reactividad de los productos químicos (II) Prévention du risque au laboratoire: Reactivité des produits chimiques (II) Risk prevention in the chemical
NTP 479: Prevención del riesgo en el laboratorio químico: reactividad de los productos químicos (II) Prévention du risque au laboratoire: Reactivité des produits chimiques (II) Risk prevention in the chemical
Formula y nombra los siguientes compuestos. Fórmula Nomenclatura sistemática Nomenclatura StocK Nomenclatura tradicional Ba O
 Co I3 Formula y nombra los siguientes compuestos Fórmula Nomenclatura sistemática Nomenclatura StocK Nomenclatura tradicional Ba O Cu2O Al2 O3 Na H Ca H2 Al H3 Au H Co H3 Fe H2 H F H Cl H2 S H2 Se Al2
Co I3 Formula y nombra los siguientes compuestos Fórmula Nomenclatura sistemática Nomenclatura StocK Nomenclatura tradicional Ba O Cu2O Al2 O3 Na H Ca H2 Al H3 Au H Co H3 Fe H2 H F H Cl H2 S H2 Se Al2
RESISTENCIA QUÍMICA (ASTM)
 1,1,1-Tricloroetano F (2) 1,5 hr P NR (3) G (1) ND E NR (3) NR (3) (4) >480 E 1,2-Diclorobenceno NA NA NA NA NA (4) >480 E 1,2-Dicloroetano NA NA NA NA NA (4) >480 E 1,2-Dicloroetileno NA NA NA NA NA (4)
1,1,1-Tricloroetano F (2) 1,5 hr P NR (3) G (1) ND E NR (3) NR (3) (4) >480 E 1,2-Diclorobenceno NA NA NA NA NA (4) >480 E 1,2-Dicloroetano NA NA NA NA NA (4) >480 E 1,2-Dicloroetileno NA NA NA NA NA (4)
Acido fórmico (100%) S S Acido fórmico (20%) S S Acido fórmico (30%) S S Acido fosfórico (0-30%) S S Acido fosfórico (30-90%) S S Acido fosfórico (más
 Aceite de canela N N Aceite de castor concentrado S S Aceite de hígado de bacalao S S Aceite de hoja de cedro N N Aceite de limón A N Aceite de linaza S S Aceite de madera de cedro N N Aceite de maíz S
Aceite de canela N N Aceite de castor concentrado S S Aceite de hígado de bacalao S S Aceite de hoja de cedro N N Aceite de limón A N Aceite de linaza S S Aceite de madera de cedro N N Aceite de maíz S
LISTA DE PRODUCTOS FERMONT
 CATALOGO PRODUCTO 08502 1.10-FENANTROLINA A.C.S 5 Gm 06685 2,2,4-TRIMETILPENTANO ACS 4 LT H6682 2,2,4-TRIMETILPENTANO HPLC 4 LT. 02541 2,4-DINITROFENILHIDRACINA 25 GRS 03641 AC. 5-SULFOSALICILICO A.C.S.
CATALOGO PRODUCTO 08502 1.10-FENANTROLINA A.C.S 5 Gm 06685 2,2,4-TRIMETILPENTANO ACS 4 LT H6682 2,2,4-TRIMETILPENTANO HPLC 4 LT. 02541 2,4-DINITROFENILHIDRACINA 25 GRS 03641 AC. 5-SULFOSALICILICO A.C.S.
REACCIONES DE QUÍMICA INORGÁNICA. RENDIMIENTO Y RIQUEZA.
 PROBLEMAS ESTEQUIOMETRÍA 1º BACH. REACCIONES DE QUÍMICA INORGÁNICA. RENDIMIENTO Y RIQUEZA. 1. El cloruro amónico con hidróxido de calcio produce al reaccionar cloruro de calcio, amoníaco y agua. Si el
PROBLEMAS ESTEQUIOMETRÍA 1º BACH. REACCIONES DE QUÍMICA INORGÁNICA. RENDIMIENTO Y RIQUEZA. 1. El cloruro amónico con hidróxido de calcio produce al reaccionar cloruro de calcio, amoníaco y agua. Si el
Los productos químicos como factores de riesgo
 Los productos químicos como factores de riesgo Las sustancias químicas peligrosas son aquéllas que pueden dañar directa o indirectamente a las personas, a los bienes o al medio ambiente. En función de
Los productos químicos como factores de riesgo Las sustancias químicas peligrosas son aquéllas que pueden dañar directa o indirectamente a las personas, a los bienes o al medio ambiente. En función de
REACTIVOS ANALITICOS
 REACTIVOS ANALITICOS ACEITE DE INMERSION Pro-análisis ACEITE DE RICINO clarificado R.Q. ACETONA Pro-análisis (ACS) ACETONA R.Q. ACETONITRILO Pro-análisis (ACS) ACIDO 3-INDOLBUTIRICO (Sal potasica) 99%
REACTIVOS ANALITICOS ACEITE DE INMERSION Pro-análisis ACEITE DE RICINO clarificado R.Q. ACETONA Pro-análisis (ACS) ACETONA R.Q. ACETONITRILO Pro-análisis (ACS) ACIDO 3-INDOLBUTIRICO (Sal potasica) 99%
APÉNDICE II DESECACIÓN Y AGENTES DESECANTES DESECACIÓN
 259 APÉNDICE II DESECACIÓN Y AGENTES DESECANTES DESECACIÓN La desecación se emplea para extraer la humedad de los líquidos, soluciones y sustancias sólidas. El grado de desecación de una sustancia depende
259 APÉNDICE II DESECACIÓN Y AGENTES DESECANTES DESECACIÓN La desecación se emplea para extraer la humedad de los líquidos, soluciones y sustancias sólidas. El grado de desecación de una sustancia depende
[ Para protección de los hombres y del medio ]
![[ Para protección de los hombres y del medio ] [ Para protección de los hombres y del medio ]](/thumbs/57/40849697.jpg) Medición de sustancias peligrosas - [ Para protección de los hombres y del medio ] con tubos detectores MSA -1- Tabla de Tubos Detectores A B Acetaldehido Formaldehido-0.1 5086-813 497649 5... 50 ppm Acetileno
Medición de sustancias peligrosas - [ Para protección de los hombres y del medio ] con tubos detectores MSA -1- Tabla de Tubos Detectores A B Acetaldehido Formaldehido-0.1 5086-813 497649 5... 50 ppm Acetileno
ACETONA SOLUCION 80 % REACTIVO ACIDO ACETICO 1 NORMAL o MOLAR O FRACCIONAL ACIDO ACETICO 2 a 6 NORMAL o MOLAR
 1 8000-125 ACETO CARMIN SOLUCION 8005-125 ACETO ORCEINA SOLUCION 8010-500 ACETONA SOLUCION 80 % REACTIVO 8015-1000 ACIDO ACETICO 1 NORMAL o MOLAR O FRACCIONAL 8020-1000 ACIDO ACETICO 2 a 6 NORMAL o MOLAR
1 8000-125 ACETO CARMIN SOLUCION 8005-125 ACETO ORCEINA SOLUCION 8010-500 ACETONA SOLUCION 80 % REACTIVO 8015-1000 ACIDO ACETICO 1 NORMAL o MOLAR O FRACCIONAL 8020-1000 ACIDO ACETICO 2 a 6 NORMAL o MOLAR
RESISTENCIA DEL POLIETILENO DE ALTA DENSIDAD (PEAD) A LOS AGENTES QUÍMICOS
 RESISTENCIA DEL POLIETILENO DE ALTA DENSIDAD (PEAD) A LOS AGENTES QUÍMICOS Los resultados que se facilitan a continuación se obtuvieron después de 55 días, en probetas de (50 x 25 x 1) mm. Signos Convencionales:
RESISTENCIA DEL POLIETILENO DE ALTA DENSIDAD (PEAD) A LOS AGENTES QUÍMICOS Los resultados que se facilitan a continuación se obtuvieron después de 55 días, en probetas de (50 x 25 x 1) mm. Signos Convencionales:
Instrucción para la gestión de residuos químicos
 Página 1 de 14 MODIFICACIONES REVISIÓN FECHA DESCRIPCIÓN A 03/04/08 Primera revisión RESPONSABLE REVISADO APROBADO Subdirector Infraestructura Pedro Manuel López Director Calidad Dr. Valdivieso Director
Página 1 de 14 MODIFICACIONES REVISIÓN FECHA DESCRIPCIÓN A 03/04/08 Primera revisión RESPONSABLE REVISADO APROBADO Subdirector Infraestructura Pedro Manuel López Director Calidad Dr. Valdivieso Director
ANEXO 23 DE LAS REGLAS DE CARACTER GENERAL EN MATERIA DE COMERCIO EXTERIOR PARA 2011
 1 ANEXO 23 DE LAS REGLAS DE CARACTER GENERAL EN MATERIA DE COMERCIO EXTERIOR PARA 2011 Mercancías peligrosas o que requieran instalaciones y/o equipos especiales para su muestreo. Descripción de la mercancía
1 ANEXO 23 DE LAS REGLAS DE CARACTER GENERAL EN MATERIA DE COMERCIO EXTERIOR PARA 2011 Mercancías peligrosas o que requieran instalaciones y/o equipos especiales para su muestreo. Descripción de la mercancía
OBJETIVOS ESPECÍFICOS
 ASIGNATURA: TOXICOLOGIA LABORAL CARRERA: LICENCIATURA EN SEGURIDAD E HIGIENE PLAN DE ESTUDIOS: ORD. N 446/11 CURSADO: SEGUNDO CUATRIMESTRE 2013 INICIACION: 12 AGOSTO FINALIZACION: 29 NOVIEMBRE CANTIDAD
ASIGNATURA: TOXICOLOGIA LABORAL CARRERA: LICENCIATURA EN SEGURIDAD E HIGIENE PLAN DE ESTUDIOS: ORD. N 446/11 CURSADO: SEGUNDO CUATRIMESTRE 2013 INICIACION: 12 AGOSTO FINALIZACION: 29 NOVIEMBRE CANTIDAD
Lista de Tubos Detectores MSA. Tubo detector aplicable
 Descripción Técnica Aplicaciones * Minería * Electricidad *Industria Química * Soldaduras * Construcción * Papel y Pulpa * Industria Nuclear * Gas y Petróleo * Materiales Peligrosos Características Principales
Descripción Técnica Aplicaciones * Minería * Electricidad *Industria Química * Soldaduras * Construcción * Papel y Pulpa * Industria Nuclear * Gas y Petróleo * Materiales Peligrosos Características Principales
Materia: FÍSICA Y QUÍMICA Curso
 ACTIVIDADES DE REFUERZO FÍSICA Y QUÍMICA 3º ESO. JUNIO 2015. 1.- Realizar las configuraciones electrónicas de todos los elementos de los tres primeros periodos de la tabla periódica. 2.- Razonar cuales
ACTIVIDADES DE REFUERZO FÍSICA Y QUÍMICA 3º ESO. JUNIO 2015. 1.- Realizar las configuraciones electrónicas de todos los elementos de los tres primeros periodos de la tabla periódica. 2.- Razonar cuales
Colegio Superior de Señoritas Tema: Formación de Compuestos Químicos Septiembre 2010 Prof.: NVM 8vo Nivel Departamento de Ciencias
 COMPUESTOS QUÍMICOS Y SU CLASIFICACIÓN El número de oxidación: representa la cantidad de electrones que puede ganar o perder un elemento. El hidrógeno tiene número de oxidación +1 y puede perder un electrón;
COMPUESTOS QUÍMICOS Y SU CLASIFICACIÓN El número de oxidación: representa la cantidad de electrones que puede ganar o perder un elemento. El hidrógeno tiene número de oxidación +1 y puede perder un electrón;
Línea de prendas confeccionadas con materia prima. Eptaform
 Pàgina 1 de 5 Línea de prendas confeccionadas con materia prima Escafandras con costuras recubiertas con cintas resistentes a las altas temperaturas en el exterior y en el interior ( Technology) cat. 3
Pàgina 1 de 5 Línea de prendas confeccionadas con materia prima Escafandras con costuras recubiertas con cintas resistentes a las altas temperaturas en el exterior y en el interior ( Technology) cat. 3
MANUAL DE GESTIÓN DE RESIDUOS PELIGROSOS DE LA UNIVERSIDAD DE MURCIA
 MANUAL DE GESTIÓN DE RESIDUOS PELIGROSOS DE LA UNIVERSIDAD DE MURCIA María Dolores Alcázar Fernández Sección Radioprotección y Residuos Servicio de Apoyo a la Investigación Vicerrectorado de Investigación
MANUAL DE GESTIÓN DE RESIDUOS PELIGROSOS DE LA UNIVERSIDAD DE MURCIA María Dolores Alcázar Fernández Sección Radioprotección y Residuos Servicio de Apoyo a la Investigación Vicerrectorado de Investigación
QUÍMICA INORGÁNICA. Elementos Símbolo Valencia Elemento Símbolo Valencia. Hidrógeno H Oxigeno O -2. Flúor F -1 Nitrógeno N
 QUÍMICA INORGÁNICA VALENCIAS NO METALES Elementos Símbolo Valencia Elemento Símbolo Valencia Hidrógeno H -1 +1 Oxigeno O -2 Flúor F -1 Nitrógeno N -3 +1+3+5 Cloro Cl -1 +1+3+5+7 Fósforo P -3 +1+3+5 Bromo
QUÍMICA INORGÁNICA VALENCIAS NO METALES Elementos Símbolo Valencia Elemento Símbolo Valencia Hidrógeno H -1 +1 Oxigeno O -2 Flúor F -1 Nitrógeno N -3 +1+3+5 Cloro Cl -1 +1+3+5+7 Fósforo P -3 +1+3+5 Bromo
VOLUMENES ATOMICO Y MOLECULAR EN EL PUNTO DE EBULLICION NORMAL
 VOLUMENES ATOMICO Y MOLECULAR EN EL PUNTO DE EBULLICION NORMAL Volumen atómico x 10 3 ( m 3 / kg átomo ) Volumen molecular x 10 3 ( m 3 / kg mol ) Bromo 27,0 Aire 29,9 Carbono 14,8 Br 2 53,2 Cloro 24,6
VOLUMENES ATOMICO Y MOLECULAR EN EL PUNTO DE EBULLICION NORMAL Volumen atómico x 10 3 ( m 3 / kg átomo ) Volumen molecular x 10 3 ( m 3 / kg mol ) Bromo 27,0 Aire 29,9 Carbono 14,8 Br 2 53,2 Cloro 24,6
REACTIVOS QUIMICA MEYER
 CATÁLOGO DESCRIPCIÓN PRESENTACIÓN PRECIO 8000-125 ACETO CARMIN SOLUCION 125 ml $207.00 8000-250 250 ml $375.00 8000-500 500 ml $680.00 8005-125 ACETO ORCEINA SOLUCION 125 ml $561.00 8005-250 250 ml $1,019.00
CATÁLOGO DESCRIPCIÓN PRESENTACIÓN PRECIO 8000-125 ACETO CARMIN SOLUCION 125 ml $207.00 8000-250 250 ml $375.00 8000-500 500 ml $680.00 8005-125 ACETO ORCEINA SOLUCION 125 ml $561.00 8005-250 250 ml $1,019.00
REACCIONES DE TRANSFERENCIA DE ELECTRONES, AJUSTE Y ESTEQUIOMETRÍA. 1-Nombra tres sustancias que sean oxidantes enérgicos Por qué?
 REACCIONES DE TRANSFERENCIA DE ELECTRONES, AJUSTE Y ESTEQUIOMETRÍA 1-Nombra tres sustancias que sean oxidantes enérgicos Por qué? 2- Nombra tres cuerpos que sean fuertes reductores por qué? 3- Qué se entiende
REACCIONES DE TRANSFERENCIA DE ELECTRONES, AJUSTE Y ESTEQUIOMETRÍA 1-Nombra tres sustancias que sean oxidantes enérgicos Por qué? 2- Nombra tres cuerpos que sean fuertes reductores por qué? 3- Qué se entiende
3ºESO-A PROFESORA LUCÍA ROMERO
 PLAN DE REFUERZO ÁREA PENDIENTE DE CIENCIAS NATURALES 3ºESO-A PROFESORA LUCÍA ROMERO BIOLOGÍA Y GEOLOGÍA: Resumen de cada tema del libro y las siguientes actividades: PRIMER TRIMESTRE: - Tema 1: La salud
PLAN DE REFUERZO ÁREA PENDIENTE DE CIENCIAS NATURALES 3ºESO-A PROFESORA LUCÍA ROMERO BIOLOGÍA Y GEOLOGÍA: Resumen de cada tema del libro y las siguientes actividades: PRIMER TRIMESTRE: - Tema 1: La salud
Detergencia Higiene LISTADO DE PRODUCTOS
 LISTADO DE PRODUCTOS ÁCIDOS INORGÁNICOS Y ÁCIDOS MINERALES Ácido bórico Ácido fosfórico 85% (vía térmica) Ácido clorhídrico (32%- 35%) Ácido nítrico (diluciones) Ácido clorhídrico (diluciones) Ácido nítrico
LISTADO DE PRODUCTOS ÁCIDOS INORGÁNICOS Y ÁCIDOS MINERALES Ácido bórico Ácido fosfórico 85% (vía térmica) Ácido clorhídrico (32%- 35%) Ácido nítrico (diluciones) Ácido clorhídrico (diluciones) Ácido nítrico
CNAE ACTIVIDADES POSIBLES CONTAMINANTES Extracción de crudos de petróleo y gas natural. Hidrocarburos alifáticos
 ANEXO 4: RELACIÓN ENTRE LAS ACTIVIDADES INDUSTRIALES POTENCIALMENTE CONTAMINANTES DEL SUELO, CLASIFICADAS POR CNAE, Y LOS CONTAMINANTES PROPIOS DE CADA ACTIVIDAD. A continuación se presenta a modo de Guía
ANEXO 4: RELACIÓN ENTRE LAS ACTIVIDADES INDUSTRIALES POTENCIALMENTE CONTAMINANTES DEL SUELO, CLASIFICADAS POR CNAE, Y LOS CONTAMINANTES PROPIOS DE CADA ACTIVIDAD. A continuación se presenta a modo de Guía
SISTEMA INTEGRAL DE INFORMACION UNIVERSITARIA MODULO DE FINANZAS Catálago de Bienes
 Página: 1 Tipo de Bien Clasf. Tipo de Subtipo de 2510000024 PRODUCTOS QUIMICOS BASICOS 2510000196 ACEITE 2510000197 ACEITE DE CLAVO 500 ML. 2510007166 ACEITE MINERAL 2510007343 GLICERINA 2510000198 ACETATO
Página: 1 Tipo de Bien Clasf. Tipo de Subtipo de 2510000024 PRODUCTOS QUIMICOS BASICOS 2510000196 ACEITE 2510000197 ACEITE DE CLAVO 500 ML. 2510007166 ACEITE MINERAL 2510007343 GLICERINA 2510000198 ACETATO
5) Cuando un metal y un no metal reaccionan el tiende a perder electrones y el tiende a ganar electrones.
 Enlaces y compuestos iónicos. Opción Múltiple. Revisión PSI Química Nombre Electrones de valencia Aniones y Cationes 1) Los Metales tienden a electrones y no metales tienden a electrones. A) ganar, ganar
Enlaces y compuestos iónicos. Opción Múltiple. Revisión PSI Química Nombre Electrones de valencia Aniones y Cationes 1) Los Metales tienden a electrones y no metales tienden a electrones. A) ganar, ganar
Indices de Corrosión
 AGENTE Varios Aceite de Lino Aceite de Soja Aceites Crudos Aceites Minerales o Vegetales Agua Clorada Saturada Agua de Bromo Agua de Mar / Agua Salada Anilina Concentrada Azufre, húmedo Azufre, seco Baño
AGENTE Varios Aceite de Lino Aceite de Soja Aceites Crudos Aceites Minerales o Vegetales Agua Clorada Saturada Agua de Bromo Agua de Mar / Agua Salada Anilina Concentrada Azufre, húmedo Azufre, seco Baño
PROBLEMAS DE ESTEQUIOMETRÍA DE 1º DE BACHILLERATO
 PROBLEMAS DE ESTEQUIOMETRÍA DE 1º DE BACHILLERATO COLECCIÓN PRIMERA. 1. La descomposición térmica del carbonato de calcio produce óxido de calcio y dióxido de carbono gas. Qué volumen de dióxido de carbono,
PROBLEMAS DE ESTEQUIOMETRÍA DE 1º DE BACHILLERATO COLECCIÓN PRIMERA. 1. La descomposición térmica del carbonato de calcio produce óxido de calcio y dióxido de carbono gas. Qué volumen de dióxido de carbono,
Desperdicios peligrosos
 Desperdicios peligrosos 1 1 2 California-Arizona Consortium, Programa de Salud Laboral, Universidad de California, Berkeley Contenido 1. Sustancias peligrosas 2. Desperdicios peligrosos inflamable corrosivo
Desperdicios peligrosos 1 1 2 California-Arizona Consortium, Programa de Salud Laboral, Universidad de California, Berkeley Contenido 1. Sustancias peligrosas 2. Desperdicios peligrosos inflamable corrosivo
Límite Permisible Ponderado. p.p.m. mg / m3 p.p.m. Acetato de n Butilo Acetato de Etilo Piel
 Artículo 66: Los límites permisibles ponderados y temporales para las concentraciones ambientales de las sustancias que se indican, serán los siguientes: Sustancia Límite Permisible Ponderado Límite Permisible
Artículo 66: Los límites permisibles ponderados y temporales para las concentraciones ambientales de las sustancias que se indican, serán los siguientes: Sustancia Límite Permisible Ponderado Límite Permisible
COMPUESTOS BINARIOS TRADICIONAL STOCK SISTEMÁTICA
 1 COMPUESTOS BINARIOS 2 3 Debe tenerse en cuenta que la valencia de los nometales en estos compuestos es siempre el menor (cuando puede tener varios). Así: F, CI, Br, I -1 S, Se, Te -2 N, P, As C, Si.
1 COMPUESTOS BINARIOS 2 3 Debe tenerse en cuenta que la valencia de los nometales en estos compuestos es siempre el menor (cuando puede tener varios). Así: F, CI, Br, I -1 S, Se, Te -2 N, P, As C, Si.
NORMA DE SEGURIDAD. REACTIVIDAD DE PRODUCTOS QUÍMICOS Edición: 1 Fecha: 24/11/10 ÍNDICE. 1. Introducción
 ÍNDICE 1. Introducción 2. Compuestos que reaccionan violentamente con el agua 3. Compuestos que reaccionan violentamente con el aire o el oxígeno 4. Incompatibilidades 5. Reacciones peligrosas con los
ÍNDICE 1. Introducción 2. Compuestos que reaccionan violentamente con el agua 3. Compuestos que reaccionan violentamente con el aire o el oxígeno 4. Incompatibilidades 5. Reacciones peligrosas con los
Lista de Precios 171 (01/02/17) No. de Edición 23
 CAT. CANTIDAD POR CAJA DESCRIPCIÓN CAPACIDAD PRECIO DE LISTA POR ENVASE 08501 1 1.10-FENANTROLINA A.C.S. 1 $320.00 08502 1 1.10-FENANTROLINA A.C.S. 5 $700.00 06685 4 2,2,4-TRIMETILPENTANO ACS 4000 $2,185.70
CAT. CANTIDAD POR CAJA DESCRIPCIÓN CAPACIDAD PRECIO DE LISTA POR ENVASE 08501 1 1.10-FENANTROLINA A.C.S. 1 $320.00 08502 1 1.10-FENANTROLINA A.C.S. 5 $700.00 06685 4 2,2,4-TRIMETILPENTANO ACS 4000 $2,185.70
FÍSICA Y QUÍMICA cuaderno de ejercicios
 FÍSICA Y QUÍMICA cuaderno de ejercicios FORMULACIÓN y nomenclatura 1.** Determinen si las siguientes afirmaciones se refieren a metales o a no metales. 1.1. Presentan un brillo característico. 1.2. Los
FÍSICA Y QUÍMICA cuaderno de ejercicios FORMULACIÓN y nomenclatura 1.** Determinen si las siguientes afirmaciones se refieren a metales o a no metales. 1.1. Presentan un brillo característico. 1.2. Los
ALMACENAMIENTO DE PRODUCTOS QUÍMICOS Y GESTIÓN DE RESIDUOS PELIGROSOS EN LA UNIVERSIDAD DE ALICANTE
 ALMACENAMIENTO DE PRODUCTOS QUÍMICOS Y GESTIÓN DE RESIDUOS PELIGROSOS EN LA UNIVERSIDAD DE ALICANTE J.A. Reyes-Labarta* #, S. Blazquez #, V. Montiel +# *Dpto. Ingeniería Química, Oficina EcoCampus de Gestión
ALMACENAMIENTO DE PRODUCTOS QUÍMICOS Y GESTIÓN DE RESIDUOS PELIGROSOS EN LA UNIVERSIDAD DE ALICANTE J.A. Reyes-Labarta* #, S. Blazquez #, V. Montiel +# *Dpto. Ingeniería Química, Oficina EcoCampus de Gestión
CLASIFICACIÓN DE LAS REACCIONES QUÍMICAS. 1. Combinación de dos elementos para formar un compuesto
 CLASIFICACIÓN DE LAS REACCIONES QUÍMICAS REACCIONES DE COMBINACIÓN Las reacciones en que dos o más sustancias se combinan para formar un compuesto se llaman reacciones de combinación. Incluyen 1) la combinación
CLASIFICACIÓN DE LAS REACCIONES QUÍMICAS REACCIONES DE COMBINACIÓN Las reacciones en que dos o más sustancias se combinan para formar un compuesto se llaman reacciones de combinación. Incluyen 1) la combinación
UNIDAD 1. La Química y su importancia. Materia y Substancia. Mezclas y compuestos. Clasificación de los fenómenos... 1
 ÍNDICE UNIDAD 1 La Química y su importancia. Materia y Substancia. Mezclas y compuestos. Clasificación de los fenómenos... 1 CAPÍTULO 1. La Química y su importancia... 1 Definiciones y subdivisiones de
ÍNDICE UNIDAD 1 La Química y su importancia. Materia y Substancia. Mezclas y compuestos. Clasificación de los fenómenos... 1 CAPÍTULO 1. La Química y su importancia... 1 Definiciones y subdivisiones de
INVENTARIO DE REACTIVOS Y SUSTANCIAS SEPTIEMBRE 2017
 REACTIVO GRADO DE REACTIVIDAD EXISTENCIA 1. 2-4 disocianato de tolueno 1 200 g 2. 2-6 Dicloro indofenol 0 40 g 3. Aceite 3 en 1 1 42 ml 4. Aceite de inmersión Tipo B para microscopia 0 166 ml 5. Aceite
REACTIVO GRADO DE REACTIVIDAD EXISTENCIA 1. 2-4 disocianato de tolueno 1 200 g 2. 2-6 Dicloro indofenol 0 40 g 3. Aceite 3 en 1 1 42 ml 4. Aceite de inmersión Tipo B para microscopia 0 166 ml 5. Aceite
REACCIONES DE TRANSFERENCIA DE ELECTRONES 2ºBACH
 1. Ajusta las siguientes reacciones redox, utilizando el método del ion electrón: a) HNO 3 + Cu Cu(NO 3 ) 2 + NO 2 + H 2 O b) K 2 Cr 2 O 7 +HI + HClO 4 Cr(ClO 4 ) 3 +I 2 +KClO 4 + H 2 O c) H 2 SO 4 + HI
1. Ajusta las siguientes reacciones redox, utilizando el método del ion electrón: a) HNO 3 + Cu Cu(NO 3 ) 2 + NO 2 + H 2 O b) K 2 Cr 2 O 7 +HI + HClO 4 Cr(ClO 4 ) 3 +I 2 +KClO 4 + H 2 O c) H 2 SO 4 + HI
Para la casa 12. Predice si los siguientes elementos producirán aniones, cationes o no producirán ninguno
 Enlaces y compuestos iónicos- Revisión- Problemas PSI Química Nombre Electrones de valencia 1. Cuántos electrones de valencia tiene el Oxígeno? 2. Cuántos electrones de valencia tiene el Litio? 3. Cuántos
Enlaces y compuestos iónicos- Revisión- Problemas PSI Química Nombre Electrones de valencia 1. Cuántos electrones de valencia tiene el Oxígeno? 2. Cuántos electrones de valencia tiene el Litio? 3. Cuántos
Dpto. de Seguridad y Salud Ocupacional Rectorado. Primer Piso, Of. 128 Tel: , Interno 126.
 TRATAMIENTO Y MINIMIZACIÓN DE RESIDUOS Introducción Todos los residuos químicos producidos en los laboratorios tienen como destino final su recuperación, transformación o eliminación. Los residuos obtenidos
TRATAMIENTO Y MINIMIZACIÓN DE RESIDUOS Introducción Todos los residuos químicos producidos en los laboratorios tienen como destino final su recuperación, transformación o eliminación. Los residuos obtenidos
Tabla 2: Propiedades físicas y mecánicas PEAD (Venelene 6100M) 1
 Propiedades físicas del Polietileno de Alta Densidad (Venelene 6100M): Es un material de aplicación típica en: tuberías para acueductos, gas, riego, drenajes, entre otros. Este material cumple con los
Propiedades físicas del Polietileno de Alta Densidad (Venelene 6100M): Es un material de aplicación típica en: tuberías para acueductos, gas, riego, drenajes, entre otros. Este material cumple con los
INSTRUCTIVO ALMACENAMIENTO DE QUÍMICOS CCT CÓRDOBA - SERVICIO DE HIGIENE Y SEGURIDAD Ing. Alejandro Herrero Ing. Juan Carlos Beletti
 INSTRUCTIVO ALMACENAMIENTO DE QUÍMICOS CCT CÓRDOBA - SERVICIO DE HIGIENE Y SEGURIDAD Ing. Alejandro Herrero Ing. Juan Carlos Beletti ALMACENAMIENTO DE PRODUCTOS QUÍMICOS 1. OBJETIVO GENERAL Disponer de
INSTRUCTIVO ALMACENAMIENTO DE QUÍMICOS CCT CÓRDOBA - SERVICIO DE HIGIENE Y SEGURIDAD Ing. Alejandro Herrero Ing. Juan Carlos Beletti ALMACENAMIENTO DE PRODUCTOS QUÍMICOS 1. OBJETIVO GENERAL Disponer de
UD 2 ENLACE QUÍMICO Y FUERZAS INTERMOLECULARES FORMULACIÓN Y NOMENCLATURA DE COMPUESTOS TERNARIOS
 FORMULACIÓN Y NOMENCLATURA DE COMPUESTOS TERNARIOS Ácidos oxoácidos o ternarios Se formulan añadiendo una molécula de agua a los óxidos no metálicos. Óxidos no metálicos Cl 2 O SO Cl 2 O 3 SO 2 N 2 O 3
FORMULACIÓN Y NOMENCLATURA DE COMPUESTOS TERNARIOS Ácidos oxoácidos o ternarios Se formulan añadiendo una molécula de agua a los óxidos no metálicos. Óxidos no metálicos Cl 2 O SO Cl 2 O 3 SO 2 N 2 O 3
DESCRIPCIÓN ASTM 1418 ISO/DIN 1629 Pág. SBR Caucho de Estireno Butadieno SBR SBR 6. NR Caucho Natural NR NR 6
 CALVOSEALING Plancha de de Caucho caucho Elastómero: CALVOSEALING ofrece una amplia gama de cauchos para su uso en juntas en la industria general. Disponemos de 10 tipos de elastómeros donde cada una de
CALVOSEALING Plancha de de Caucho caucho Elastómero: CALVOSEALING ofrece una amplia gama de cauchos para su uso en juntas en la industria general. Disponemos de 10 tipos de elastómeros donde cada una de
LISTA DE PRODUCTOS FAGA LAB
 CATALOGO PRODUCTO 1024-1 ACIDO TRICLOROACETICO 100 GR. 1471-250 FRASCO COLOR AMBAR 250 ML 2000-125 ACEITE DE INMERSION 125 ML. 2000-250 ACEITE DE INMERSION 250 ML. 2000-30 ACEITE DE INMERSION 30 ML. 2000-50
CATALOGO PRODUCTO 1024-1 ACIDO TRICLOROACETICO 100 GR. 1471-250 FRASCO COLOR AMBAR 250 ML 2000-125 ACEITE DE INMERSION 125 ML. 2000-250 ACEITE DE INMERSION 250 ML. 2000-30 ACEITE DE INMERSION 30 ML. 2000-50
3. Calcula la cantidad estequiométrica de hidrógeno molecular, en moles, necesaria para reaccionar con 5 moles de oxígeno en la síntesis del agua.
 CÁLCULOS ESTEQUIOMÉTRICOS BÁSICOS 1. Ajusta las siguientes reacciones químicas: C 3 H 6 (g) + O 2 (g) CO 2 (g) + H 2 O (g) N 2 (g) + H 2 (g) NH 3 (g) KClO 3 (aq) KCl (aq) + O 2 (g) H 2 O 2 (l) O 2 (g)
CÁLCULOS ESTEQUIOMÉTRICOS BÁSICOS 1. Ajusta las siguientes reacciones químicas: C 3 H 6 (g) + O 2 (g) CO 2 (g) + H 2 O (g) N 2 (g) + H 2 (g) NH 3 (g) KClO 3 (aq) KCl (aq) + O 2 (g) H 2 O 2 (l) O 2 (g)
Mayo del 2006 Elaborado por Legiscomex.com Página 1 de 17
 Insumos en canasta A 199 productos clasificados en el capítulo 28 del Arancel Armonizado de Colombia, que hace referencia a Productos químicos inorgánicos; compuestos inorgánicos u orgánicos de los metales
Insumos en canasta A 199 productos clasificados en el capítulo 28 del Arancel Armonizado de Colombia, que hace referencia a Productos químicos inorgánicos; compuestos inorgánicos u orgánicos de los metales
NOMENCLATURA DE ÁCIDOS Y BASES
 COLEGIO SAN ESTEBAN DIÁCONO Departamento de Ciencias Química IVº Electivo Prof. Juan Pastrián Lisboa NOMENCLATURA DE ÁCIDOS Y BASES Objetivo: - Reconocer y aplicar reglas de nomenclatura tradicional y
COLEGIO SAN ESTEBAN DIÁCONO Departamento de Ciencias Química IVº Electivo Prof. Juan Pastrián Lisboa NOMENCLATURA DE ÁCIDOS Y BASES Objetivo: - Reconocer y aplicar reglas de nomenclatura tradicional y
INCOMPATIBILIDAD I N C O M P A T I B L E S P R O D U C T O S BASES METALES SULFUROS CIANUROS ACIDOS OTROS ACIDOS ACIDOS FUERTES
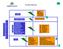 INCOMPATIBILIDAD ACIDOS BASES METALES SULFUROS CIANUROS ACIDOS FUERTES OTROS ACIDOS P R O D U C T O S I N C O M P A T I B L E S OXIDANTES CLORATOS CROMATOS DICROMATOS HALOGENOS NITRATOS PERCLORATOS PEROXIDOS
INCOMPATIBILIDAD ACIDOS BASES METALES SULFUROS CIANUROS ACIDOS FUERTES OTROS ACIDOS P R O D U C T O S I N C O M P A T I B L E S OXIDANTES CLORATOS CROMATOS DICROMATOS HALOGENOS NITRATOS PERCLORATOS PEROXIDOS
REACCIONES QUIMICAS TIPOS DE REACCIONES QUÍMICAS
 Universidad Católica Andrés Bello Facultad de Ingeniería Departamento de Química Prof. Ana M. Itriago REACCIONES QUIMICAS El estudio de las reacciones químicas es de vital importancia no solo como ciencia
Universidad Católica Andrés Bello Facultad de Ingeniería Departamento de Química Prof. Ana M. Itriago REACCIONES QUIMICAS El estudio de las reacciones químicas es de vital importancia no solo como ciencia
PROBLEMAS RESUELTOS SELECTIVIDAD ANDALUCÍA 2002 QUÍMICA TEMA 0: FORMULACIÓN
 PROBLEMAS RESUELTOS SELECTIVIDAD ANDALUCÍA 00 QUÍMICA TEMA 0: FORMULACIÓN Junio, Ejercicio 1, Opción A Junio, Ejercicio 1, Opción B Reserva 1, Ejercicio 1, Opción A Reserva 1, Ejercicio 1, Opción B Reserva,
PROBLEMAS RESUELTOS SELECTIVIDAD ANDALUCÍA 00 QUÍMICA TEMA 0: FORMULACIÓN Junio, Ejercicio 1, Opción A Junio, Ejercicio 1, Opción B Reserva 1, Ejercicio 1, Opción A Reserva 1, Ejercicio 1, Opción B Reserva,
METALES, NO METALES Y. B Si
 1 METALES, NO METALES Y B Si Ge As Sb Te At 2 3 4 COMPUESTOS INORGÁNICOS METALES ÓXIDOS METÁLICOS HIDRÓXIDOS HIDRUROS METÁLICOS NO METALES ÓXIDOS NO METÁLICOS OXIÁCIDOS HIDRUROS NO METÁLICOS SALES OXISALES
1 METALES, NO METALES Y B Si Ge As Sb Te At 2 3 4 COMPUESTOS INORGÁNICOS METALES ÓXIDOS METÁLICOS HIDRÓXIDOS HIDRUROS METÁLICOS NO METALES ÓXIDOS NO METÁLICOS OXIÁCIDOS HIDRUROS NO METÁLICOS SALES OXISALES
METALES, NO METALES Y. B Si
 1 METALES, NO METALES Y B Si Ge As Sb Te At 2 3 4 COMPUESTOS INORGÁNICOS METALES ÓXIDOS METÁLICOS HIDRÓXIDOS HIDRUROS METÁLICOS NO METALES ÓXIDOS NO METÁLICOS OXIÁCIDOS HIDRUROS NO METÁLICOS SALES OXISALES
1 METALES, NO METALES Y B Si Ge As Sb Te At 2 3 4 COMPUESTOS INORGÁNICOS METALES ÓXIDOS METÁLICOS HIDRÓXIDOS HIDRUROS METÁLICOS NO METALES ÓXIDOS NO METÁLICOS OXIÁCIDOS HIDRUROS NO METÁLICOS SALES OXISALES
U N IV E R S ID A D P O L IT É C N IC A D E M A D R ID. GC/Mercado Español BLOQUE 3- QUÍMICA DEL CARBÓN Y GAS.
 U N IV E R S ID A D P O L IT É C N IC A D E M A D R ID GC/Mercado Español BLOQUE 3- QUÍMICA DEL CARBÓN Y GAS. 1 El carbón es una roca orgánica heterogénea y compleja que no puede ser representada por una
U N IV E R S ID A D P O L IT É C N IC A D E M A D R ID GC/Mercado Español BLOQUE 3- QUÍMICA DEL CARBÓN Y GAS. 1 El carbón es una roca orgánica heterogénea y compleja que no puede ser representada por una
ACERO AL CARBONO BRONCE FUNDIDO HIERRO FUNDIDO HASTELLOY C 316 ACERO INOXIDABLE ALUMINIO TITANIO KYNAR LATÓN
 Cuadro de Resistencia Química El siguiente cuadro de resistencias químicas es provisto como una guía para ayudarlo a seleccionar los materiales para los componentes y las piezas del módulo de peso. La
Cuadro de Resistencia Química El siguiente cuadro de resistencias químicas es provisto como una guía para ayudarlo a seleccionar los materiales para los componentes y las piezas del módulo de peso. La
FORMULACIÓN Y NOMENCLATURA
 FORMULACIÓN Y NOMENCLATURA.- Formulación: Es la representación escrita de una molécula que se rige por unas normas universales establecidas por acuerdo de la comunidad científica..- Nomenclatura: Es el
FORMULACIÓN Y NOMENCLATURA.- Formulación: Es la representación escrita de una molécula que se rige por unas normas universales establecidas por acuerdo de la comunidad científica..- Nomenclatura: Es el
6. Análisis de Carreteras y Estaciones de Ferrocarril en el año 2009
 Estadística de las Emergencias de Accidentes en el Transporte de Mercancías Peligrosas Dirección General de Protección Civil y Emergencias 6. Análisis de Carreteras y Estaciones de Ferrocarril en el año
Estadística de las Emergencias de Accidentes en el Transporte de Mercancías Peligrosas Dirección General de Protección Civil y Emergencias 6. Análisis de Carreteras y Estaciones de Ferrocarril en el año
Septiembre Pregunta B1.- Ajuste las siguientes reacciones iónicas redox. Indique para cada caso el agente oxidante y el reductor.
 Modelo 2014. Pregunta 4A.- A 30 ml de una disolución de CuSO 4 0,1 M se le añade aluminio metálico en exceso. a) Escriba y ajuste las semirreacciones de reducción y oxidación e indique el comportamiento
Modelo 2014. Pregunta 4A.- A 30 ml de una disolución de CuSO 4 0,1 M se le añade aluminio metálico en exceso. a) Escriba y ajuste las semirreacciones de reducción y oxidación e indique el comportamiento
FORMULACIÓN QUÍMICA INORGÁNICA NÚMEROS DE OXIDACIÓN MÁS USUALES DE ALGUNOS ELEMENTOS METALES. Número de oxidación. + 1 Li, Na, K, Rb, Cs y Ag
 1 FORMULACIÓN QUÍMICA INORGÁNICA NÚMEROS DE OXIDACIÓN MÁS USUALES DE ALGUNOS ELEMENTOS METALES Número de oxidación Elementos + 1 Li, Na, K, Rb, Cs y Ag +2 Be, Mg, Ca, Sr, Ba ; Zn y Cd +3 B, Al +1, +2 Cu
1 FORMULACIÓN QUÍMICA INORGÁNICA NÚMEROS DE OXIDACIÓN MÁS USUALES DE ALGUNOS ELEMENTOS METALES Número de oxidación Elementos + 1 Li, Na, K, Rb, Cs y Ag +2 Be, Mg, Ca, Sr, Ba ; Zn y Cd +3 B, Al +1, +2 Cu
PROCEDIMIENTO DE GESTION DE RESIDUOS PARA LOS LABORATORIOS DOCENTES Y DE INVESTIGACIÓN.
 PROCEDIMIENTO DE GESTION DE RESIDUOS PARA LOS LABORATORIOS DOCENTES Y DE INVESTIGACIÓN. 1.- OBJETO El propósito del presente procedimiento es describir los pasos a seguir por todos los miembros de la comunidad
PROCEDIMIENTO DE GESTION DE RESIDUOS PARA LOS LABORATORIOS DOCENTES Y DE INVESTIGACIÓN. 1.- OBJETO El propósito del presente procedimiento es describir los pasos a seguir por todos los miembros de la comunidad
GRADO EN INGENIERÍA ELÉCTRICA. EXAMEN DE FEBRERO 2013
 GRADO EN INGENIERÍA ELÉCTRICA. EXAMEN DE FEBRERO 2013 GRUPO A Nombre: CUESTIONES 1) A) Indica, razonadamente, si las siguientes afirmaciones son verdaderas o falsas: a.1. Algunas reacciones exotérmicas
GRADO EN INGENIERÍA ELÉCTRICA. EXAMEN DE FEBRERO 2013 GRUPO A Nombre: CUESTIONES 1) A) Indica, razonadamente, si las siguientes afirmaciones son verdaderas o falsas: a.1. Algunas reacciones exotérmicas
FÍSICA Y QUÍMICA 4º DE ESO CURSO 16/ 17
 FÍSICA Y QUÍMICA 4º DE ESO CURSO 16/ 17 Alumno/a: 1. Completa la tabla, utilizando el SP: NOMBRE SÍMBOLO Z A P + e - N CARGA *catión *anión *carga 0 24 28 3+ 65 28 35 Cobre 63 29 0 33 75 36 18 16 2-29
FÍSICA Y QUÍMICA 4º DE ESO CURSO 16/ 17 Alumno/a: 1. Completa la tabla, utilizando el SP: NOMBRE SÍMBOLO Z A P + e - N CARGA *catión *anión *carga 0 24 28 3+ 65 28 35 Cobre 63 29 0 33 75 36 18 16 2-29
EVALUACIÓN FISICO-QUÍMICA DE LAS SUSTANCIAS y PREPARADOS QUÍMICOS
 JORNADAS TOXICOLOGÍA AMBIENTAL: SEGURIDAD QUÍMICA EVALUACIÓN FISICO-QUÍMICA DE LAS SUSTANCIAS y PREPARADOS QUÍMICOS EVALUACIÓN FISICO-QUÍMICA DE LAS SUSTANCIAS QUÍMICAS Las propiedades físico-químicas
JORNADAS TOXICOLOGÍA AMBIENTAL: SEGURIDAD QUÍMICA EVALUACIÓN FISICO-QUÍMICA DE LAS SUSTANCIAS y PREPARADOS QUÍMICOS EVALUACIÓN FISICO-QUÍMICA DE LAS SUSTANCIAS QUÍMICAS Las propiedades físico-químicas
QUÍMICA 2º BACHILLERATO
 REACCIONES DE TRANSFERENCIA DE ELECTRONES: Y ESTEQUIOMETRÍA 1.-/ Iguale por el método del ion-electrón la ecuación: Cu + HNO 3 Cu(NO 3 ) 2 + NO + H 2 O, correspondiente a la reacción del cobre con el ácido
REACCIONES DE TRANSFERENCIA DE ELECTRONES: Y ESTEQUIOMETRÍA 1.-/ Iguale por el método del ion-electrón la ecuación: Cu + HNO 3 Cu(NO 3 ) 2 + NO + H 2 O, correspondiente a la reacción del cobre con el ácido
Formulación Inorgánica Ejercicios (II)
 Ejercicios (II) EJERCICIOS DE FORMULACIÓN INORGÁNICA (II) COMPUESTOS BINARIOS DEL OXÍGENO 1.- Nombrar: Cl2O7 FeO N2O SO3 Cr2O3 Br2O P2O5 CO2 I2O5 2.- Formular: MnO2 Trióxido de dicromo Óxido de nitrógeno
Ejercicios (II) EJERCICIOS DE FORMULACIÓN INORGÁNICA (II) COMPUESTOS BINARIOS DEL OXÍGENO 1.- Nombrar: Cl2O7 FeO N2O SO3 Cr2O3 Br2O P2O5 CO2 I2O5 2.- Formular: MnO2 Trióxido de dicromo Óxido de nitrógeno
Tema 6 : Nomenclatura y formulación Química Inorgánica
 Tema 6 : Nomenclatura y formulación Química Inorgánica Esquema de trabajo: Introducción Compuestos Binarios 1. Combinaciones binarias del oxígeno: A. Oxidos B. Anhídridos 2. Combinaciones binarias del
Tema 6 : Nomenclatura y formulación Química Inorgánica Esquema de trabajo: Introducción Compuestos Binarios 1. Combinaciones binarias del oxígeno: A. Oxidos B. Anhídridos 2. Combinaciones binarias del
Química Orgánica Grupos funcionales con oxígeno o nitrógeno
 Química rgánica Grupos funcionales con oxígeno o nitrógeno IES La Magdalena. Avilés. Asturias La parte carbonada constituye el esqueleto fundamental de las moléculas orgánicas. En esta estructura básica
Química rgánica Grupos funcionales con oxígeno o nitrógeno IES La Magdalena. Avilés. Asturias La parte carbonada constituye el esqueleto fundamental de las moléculas orgánicas. En esta estructura básica
1 EJERCICIOS (Nomenclatura de Compuestos inorgánicos)
 1 EJERCICIOS (Nomenclatura de Compuestos inorgánicos) HCl Bromato de bario H 2 Te Hidróxido de manganeso (II) Yoduro de cobre (II) Ayala MnO 2 NO Hidruro de bario Óxido de férrico FeCl 3 Zn(OH) 2 Sulfato
1 EJERCICIOS (Nomenclatura de Compuestos inorgánicos) HCl Bromato de bario H 2 Te Hidróxido de manganeso (II) Yoduro de cobre (II) Ayala MnO 2 NO Hidruro de bario Óxido de férrico FeCl 3 Zn(OH) 2 Sulfato
11 Dióxido de carbono. 12 Trióxido de monoazufre. 13 Pentaóxido de difósforo. 14 Dióxido de monoselenio. 15 Dióxido de selenio. 16 Óxido de dimercurio
 1 FÍSICA Y QUÍMICA 3º ESO QUÍMICA - FORMULACIÓN Y SISTEMÁTICAMENTE LOS SIGUIENTES ÓXIDOS 1 Cu 2 O 2 Be O 3 I 2 O 5 4 CO 2 5 NiO 6 Ag 2 O 7 Li 2 O 8 N 2 O 3 9 CrO 10 Ni 2 O 3 11 Dióxido de carbono 12 Trióxido
1 FÍSICA Y QUÍMICA 3º ESO QUÍMICA - FORMULACIÓN Y SISTEMÁTICAMENTE LOS SIGUIENTES ÓXIDOS 1 Cu 2 O 2 Be O 3 I 2 O 5 4 CO 2 5 NiO 6 Ag 2 O 7 Li 2 O 8 N 2 O 3 9 CrO 10 Ni 2 O 3 11 Dióxido de carbono 12 Trióxido
DIRECCION NACIONAL DE ESTUPEFACIENTES
 ORGANIZACION DE LOS ESTADOS AMERICANOS COMISION INTERAMERICANA PARA EL CONTROL DEL ABUSO DE DROGAS CUADRAGESIMO SEGUNDO PERIODO ORDINARIO DE SESIONES Del 27 al 30 de noviembre de 2007 Santa Marta, Colombia
ORGANIZACION DE LOS ESTADOS AMERICANOS COMISION INTERAMERICANA PARA EL CONTROL DEL ABUSO DE DROGAS CUADRAGESIMO SEGUNDO PERIODO ORDINARIO DE SESIONES Del 27 al 30 de noviembre de 2007 Santa Marta, Colombia
LEYES PONDERALES Y LEYES DE LOS GASES
 LEYES PONDERALES Y LEYES DE LOS GASES En una cápsula de porcelana se colocan 2,15 gr de limaduras de hierro y se le agrega una cucharada de azufre suficiente como para que una vez que reaccionen quede
LEYES PONDERALES Y LEYES DE LOS GASES En una cápsula de porcelana se colocan 2,15 gr de limaduras de hierro y se le agrega una cucharada de azufre suficiente como para que una vez que reaccionen quede
Emisión de vapores en el proceso, trasvase, manipulaciones y/o almacenamiento. (Debido a la volatilidad de las sustancias)
 Recomendaciones básicas de seguridad y salud en el manejo de disolventes orgánicos y otras drogas peligrosas de uso común en el laboratorio de Polímeros Riesgos: Intoxicación aguda: mareos, dolor de cabeza,
Recomendaciones básicas de seguridad y salud en el manejo de disolventes orgánicos y otras drogas peligrosas de uso común en el laboratorio de Polímeros Riesgos: Intoxicación aguda: mareos, dolor de cabeza,
