10.4. COMPORTAMIENTO Y PROPIEDADES DE LOS CONTAMINANTES (I): INORGÁNICOS (NATURAL Y SALINIDAD)
|
|
|
- Eugenia Sosa Ortiz de Zárate
- hace 6 años
- Vistas:
Transcripción
1 Clase 10.4 Pág. 1 de COMPORTAMIENTO Y PROPIEDADES DE LOS CONTAMINANTES (I): INORGÁNICOS (NATURAL Y SALINIDAD) Introducción Los contaminantes de tipo mineral o inorgánicos son compuestos que en lo general, muestran una elevada persistencia en los suelos (del orden de hasta centenares de años en el caso de algunos metales) y en muchos de los casos, suelen ir acompañados por un incremento de la salinidad (o conductividad) del agua analizada. Además, debido a su relativamente baja reactividad a temperatura ambiente y condiciones de ph/eh aptos para el desarrollo biológico, son difíciles y costosos de eliminar. En el acuífero, la mayoría de dichos compuestos se mueven a velocidades similares a la del flujo de agua subterránea. Los más representativos de este grupo son los iones Cl, SO 4, NO 3, HCO 3 y Ca, Na, K, Fe, Mn Mg y los elementos del grupo de los "metales pesados", como el Pb, Zn, Cd, Hg, As, Cu, Ni, Co, Al o Cr Factores principales de control del comportamiento en medio acuoso La movilidad en la fase acuosa de estos compuestos viene condicionada por su capacidad de disolución, que puede ser muy elevada en determinados compuestos, como la mayoría de los cloruros y algunos sulfatos. Específicamente, en el caso de los metales pesados, el grado de disolución se cuantifica por su Kps o producto de solubilidad, que suele ser muy bajo si el elemento se transporta en compuestos inorgánicos. Los factores básicos que controlan el grado de disolución de estos contaminantes en el agua subterránea no hidrotermal son las variaciones de las condiciones REDOX y de ph de la ecuación de equilibrio en la que están implicados (Figura 10.5 y Figura 10.6). En general, a ph=7 y en medios oxidantes, los metales suelen fijarse al sedimento, permaneciendo fuera de la disolución y por tanto, no contaminando el agua. Un cambio a condiciones más reductoras manteniendo constante el ph (en ausencia de azufre), incrementa la disolución de dichos elementos (normalmente, en forma de óxidos o carbonatos) en el agua. La existencia de
2 Clase 10.4 Pág. 2 de 9 azufre suele provocar, por el contrario, la fijación de dichos metales en el sedimento en forma de sulfuros E M Volt p REDUCCIONES Reducción de O 2 Desnitrificación Oxido de Mn(IV) C => Mn (II) Reducción de NO 3 D B A Oxido de Fe(III) => Fe (II) Reducción de F Materia Orgánica 2- Reducción de SO 4 G Fermentación de CH 4 N 2 => NH 4 + Formación de H 2 L K J H E Oxidación de Mat. Org. M Sulfuros => SO 4 2- Ejemplos Combinación gº Ph = 7 Kcal/equiv. Respiración aeróbica Desnitrificación Reducción de nitratos Fermentación Reducción de sulfatos Fermentación de metano A+L B+L D+L F+L G+L H+L Fijación de N - J+L Oxidación de sulfuros A+M Nitrificación Oxidación del hierro Oxidación del Mn (II) A+O A+N A+P N Oxidación de Fe (II) O NH 4 + => NO 3 - P Oxidación de Mn (II) OXIDACIONES Q N 2 => NO 3 - R Formación de O p Kcal / equivalente Figura Secuencia de procesos importantes REDOX de origen bacteriológico a ph=7. (modificado de Stumm y Morgan, 1981).
3 Clase 10.4 Pág. 3 de 9 LLUVIA ÁCIDA HNO 3 / H 2 SO 4 / (NH 4 ) 2 SO 4 BIOMASA SUELO Ca 2+ Mg 2+ K + Na + NH 4 + AL 3+ ACIDIFICACIÓN H + SOLUCIÓN DEL SUELO H + AL 3+ Ca 2+ Na + Mg 2+ K + otros iones metálicos Zona Saturada Cl - NO 3 - SO 4 2- HCO 3 - AL 3+ Movilización del Aluminio METEORIZACIÓN AL 3+ H + METEORIZACIÓN LIXIVIACION Ca 2+ DE LOS Mg 2+ Ca 2+ CATIONES Otros minerales Mg 2+ DEL SUELO ARCILLA (ALUMINO SILICATO) ROCA MADRE Figura Efectos de una lluvia ácida en la variación de los componentes inorgánicos del suelo y su incorporación a la zona saturada del acuífero.
4 Clase 10.4 Pág. 4 de 9 Ejemplo 1) El cromo puede presentarse en el suelo y en el agua bajo la forma de CrIII o de CrVI, siendo considerado peligroso en concentraciones superiores a 50 ppb. En aguas oxigenadas, la tendencia a oxidar el CrIII a CrVI puede además ser acelerada por la existencia de otros óxidos, como el MnII, lo que provocará un mayor riesgo de contaminación de las aguas. Por el contrario, la existencia de pirita (FeS 2 ) susceptible de ser oxidada provocará la reducción de CrVI a CrIII, disminuyendo su movilidad en el agua. Las reacciones de complejación son, especialmente en el caso de la unión de metales con materia orgánica, uno de los campos actualmente de mayor investigación. En general, se puede apuntar que son procesos muy vinculados al ph y que el Kps se incrementa significativamente si el metal es incorporado a una molécula orgánica. Otro proceso implicado en la movilidad de los metales es la substitución isomórfica, donde átomos del metal ocupan puestos vacantes o substituyen iones de la estructura cristalina. Así, en los acuíferos con una cierta fracción arcillosa, es posible la substitución de Al III o de FeII o MgII por SiIV o Al III en la estructura de los silicatos. Otro ejemplo de la complejidad de comportamiento de los metales pesados se muestra en el siguiente caso real: Ejemplo 2) El plomo es un elemento que suele ser más móvil en suelos de masas forestales o en general, en suelos ricos en materia orgánica (con ph más variables y tendientes a ácidos), que en suelos agrícolas (más bajos en materia orgánica y con un ph más estable, normalmente cercano a 7), siempre que el agua de riego no incorpore plomo. Sin embargo, un cambio de usos de suelo, de agrícola a forestal puede modificar críticamente el valor de ph y movilizar compuestos de Pb hasta entonces inmóviles, que pueden contaminar un acuífero hasta entonces sin metales. También el medio sólido del acuífero puede verse afectado por diversos procesos. Los más significativos son los procesos de adsorción y los procesos relacionados con la formación de coloides Mecanismos naturales de degradación de la calidad del agua subterránea.
5 Clase 10.4 Pág. 5 de 9 Los procesos de degradación natural de la calidad del agua han sido, dentro del conjunto de procesos contaminantes, los que históricamente han recibido menor atención. Éstos no han sido estudiados de forma sistemática en España, ya que mayoritariamente se ha supuesto que no comportan más inconvenientes que un incremento en la salinidad. Sin embargo, la existencia de cada vez más estudios que verifican su importancia en la calidad final del agua y la relación entre la salud humana y el consumo de aguas salinas les está otorgando actualmente un interés creciente. Un resumen de las principales características del agua natural que pueden incidir en su calidad para consumo humano se muestran en la Tabla Característica o Compuesto Tipo de acuífero más vulnerable Normativa vigente valor guía (ppm del Compuesto) Valor tolerable para el consumo humano (ppm) Ac. Costeros, ac. Salinidad (Residuo confinados profundos, ac. Sólido. a 100ºC) evaporíticos Ac. costeros, rocas Cloruros evaporíticas, ac confinados profundos Sulfatos Ac. evaporíticos Hierro Ac. ambientes reductores, ac. deltaicos 0,05 0,2 Manganeso Ac. ambientes reductores, ac. deltaicos 0,02 0,05 Fluor Ac. Fisurados rocas ígneas-volcánicas 0 1,5 Arsénico Ac. cercanos a yacimientos minerales de As, ac. fisurados y metamórficos (Black Shales) 0 0,05 Tabla Principales características naturales del agua subterránea en función del tipo de acuífero y de la calidad considerada guía por la reglamentación y tolerable para la salud humana. Los procesos de contaminación natural se producen preferentemente en: - Acuíferos profundos, con tiempos de residencia del agua elevados. - Acuíferos situados en medios reductores.
6 Clase 10.4 Pág. 6 de 9 - Acuíferos costeros. - Acuíferos situados en zonas volcánicas. - Acuíferos que atraviesan masas mineralizadas. - Acuíferos que atraviesan series evaporíticas. Una de las formas más usuales de degradación natural del agua subterránea en España es la que se produce por el incremento de su concentración en cloruro, debido a la circulación a través de formaciones evaporíticas, de aguas salinas o de su mezcla con salmueras confinadas en el terreno, que se desplazan como consecuencia de la explotación. Del mismo modo, el paso del agua a través de dichas formaciones le permite incorporar grandes concentraciones de sulfato (Tabla 10.7). Otro de los tipos más extendidos de contaminación natural es la relacionada con la existencia de elevadas concentraciones de hierro y manganeso de origen natural, que generan graves problemas de incrustaciones en las captaciones y que dan color al agua. Existen también procesos de degradación natural provocada por elevadas concentraciones de flúor y CO 2, que han sido descritos en las Islas Canarias (Tabla 10.8) o en zonas de Cataluña y que suelen estar asociados a casos de fluorosis entre la población. Acuífero Descripción Contaminante Valor máximo medido Fuente Triásico de Niveles evaporitas Cl, SO 4 Desconocido PHBl (1) Baleares Gran Canaria Acuífero fisural CO 2 Bicarbonatos, PHCn (1) volcánico mg/l (máx) Hierro Acuífero fisural CO 2 Bicarbonatos, PHCn volcánico mg/l (máx) Tenerife Acuífero fisural CO 2 Bicarbonatos, PHCn volcánico mg/l (máx) Tenerife Acuífero fisural volcánico Flúor, F -: 9mg/L (máx) Aguas con tiempos de residencia muy elevados, 9 mg/l (máx) PHCn Tabla Ejemplos de contaminación natural citados en los proyectos de Planes de Cuenca Hidrográfica ( ). PHBI: Plan Hidrológico Islas Baleares, PHCn: Plan Hidrológico Nacional de Canarias. (1) PHBl: Plan Hidrológico Islas Baleares, PHCn: Plan Hidrológico de Canarias.
7 Clase 10.4 Pág. 7 de 9 También se producen contaminaciones por la existencia de compuestos presentes en el agua y que incorporan metales pesados en su estructura. Éstos están usualmente relacionados con la existencia de anomalías geoquímicas, indicios o yacimientos de sulfuros y arseniuros metálicos, a los que se les suele atribuir el origen de contaminaciones en abastecimientos locales, generalmente ubicados en España en los acuíferos paleozoicos o triásicos de la Península y Baleares. La peligrosidad de este tipo de elementos reside en su elevada toxicidad, incluso en muy bajas concentraciones. Un caso especialmente significativo lo constituye el arsénico, presente usualmente como sulfuro mixto de hierro y arsénico, que es fácilmente alterable en condiciones atmosféricas a compuestos más solubles. Ejemplo 3) El arsénico es uno de los elementos químicos que históricamente tiene más documentada su peligrosidad para la salud humana y uno de los que mayores extensiones ocupa en numerosos acuíferos de todo el mundo: India, China, Nepal, Bangla-Desh, Chile, Argentina, USA (Figura 10.7), etc. En forma natural, puede encontrarse bajo su forma elemental (arsénico nativo) o bajo la forma de sulfuros (rejalgar, oropimente), arseniatos mixtos de Fe-As hidratados (escorodita Fe-AsO 4.2H 2 0) u óxidos (Claudetita y arsenolita). Las formas oxidadas (Claudetita y arsenolita) son las más estables en la naturaleza y son el producto de la descomposición meteórica de sulfuros y arseniatos (Welch & Stoillenwerk, Ed, 2003). La adsorción es el mecanismo predominante que controla el transporte de arsénico en los sistemas acuíferos. Los principales compuestos adsorventes son los hidróxidos de hierro, aluminio y manganeso, así como los minerales de las arcillas. La extensión de los procesos de adsorción están controlados por la química del agua( ph, eh, especie de As disuelta y otros iones que puedan competir en las posibles reacciones). La existencia de fosfatos, sulfatos, carbonatos o sílice pueden provocar la disminución del grado de adsorción, y, por tanto, su incorporación en la fase acuosa.
8 Clase 10.4 Pág. 8 de 9 Figura Mapa de concentraciones de As en agua subterránea en USA. Fuente: USGS. Bajo iguales condiciones de ph el estado REDOX condiciona la especie de As predominante y su grado de adsorción en la matriz del acuífero. De este modo, en condiciones moderadamente reducidas, la fase predominante es el As 3+, lo que provoca que al aumentar el ph, aumente la capacidad de adsorción. Sin embargo, bajo condiciones oxidantes, la fase principal es el arseniato, y que, al aumentar el ph, provoca un descenso de dicha capacidad adsorvente. Como se deduce de lo anterior, la aparición de concentraciones elevadas de As en el agua subterránea depende, en ausencia de fuentes antrópicas, del tipo de sedimento o estructura sólida del acuífero. De todas formas, también pueden existir anomalías naturales de As relacionadas con aguas termales. La zonificación del arsénico natural en una determinada parte de una cuenca sedimentaria está en muchas ocasiones controlados por el flujo regional, a escala geológica, de la misma, y a la posibilidad de encontrar trampas geoquímicas que lo estabilicen en un determinado lugar.
9 Clase 10.4 Pág. 9 de 9 Otro grupo de contaminación natural, con unos condicionantes muy específicos y del cual no se dispone de datos publicados, son los indicios y yacimientos de minerales de uranio. Los procesos de tratamiento y remediación de este tipo de contaminación son costosos y no suelen dar efectos permanentes. Ello es debido a la propia naturaleza geológica de la litología potencialmente contaminante (y su disposición en estratos, diapiros, vetas o filones, procesos volcánicos, etc.), que normalmente llevan aportando dicho compuesto durante millones de años. En la mayoría de los casos se tiende a abandonar dicha fuente de agua (desarrollo de captaciones en otro acuífero, desvío del agua contaminada) o a la mezcla con otras fuentes de aguas menos mineralizadas. El tratamiento del agua suele mantenerse a medio o largo plazo sólo en el caso de ausencias de otro suministro.
TEMA 5. EQUILIBRIOS REDOX EN AGUAS NATURALES
 TEMA 5. EQUILIBRIOS REDOX EN AGUAS NATURALES 5.1 EQUILIBRIOS REDOX Y pe...2 5.1.1 Ec. de Nernst:...3 5.1.2 DIAGRAMAS DE EQUILIBRIOS REDOX EN AGUAS...5 5.2 DIAGRAMAS log C- pe...6 5.2.1 LÍMITES DE ESTABILIDAD
TEMA 5. EQUILIBRIOS REDOX EN AGUAS NATURALES 5.1 EQUILIBRIOS REDOX Y pe...2 5.1.1 Ec. de Nernst:...3 5.1.2 DIAGRAMAS DE EQUILIBRIOS REDOX EN AGUAS...5 5.2 DIAGRAMAS log C- pe...6 5.2.1 LÍMITES DE ESTABILIDAD
11. METALES PESADOS. Definición. Procedencia. Dinámica. Factores. Toxicidad. Fraccionamiento. 7 Estudio de casos
 11. METALES PESADOS 1 Definición 2 Procedencia 3 4 Dinámica Factores 5 Toxicidad 6 Fraccionamiento 7 Estudio de casos 1. Definición Densidad 5 gr/cm 3, o Nº atómico > 20 (excluidos alcalinos y alcalinotérreos)
11. METALES PESADOS 1 Definición 2 Procedencia 3 4 Dinámica Factores 5 Toxicidad 6 Fraccionamiento 7 Estudio de casos 1. Definición Densidad 5 gr/cm 3, o Nº atómico > 20 (excluidos alcalinos y alcalinotérreos)
GENERALIDADES. La molécula de agua. Propiedades. Química en Solución acuosa. Aguas ambientales-abundancia 1. Química en solución acuosa 2007
 GENERALIDADES Química en solución acuosa 2007 La molécula de agua Molécula de tipo AX 2 E 2 Angular Enlace O-H Alta energía Alta polaridad Capacidad para formar enlaces de hidrógeno Aguas ambientales-abundancia
GENERALIDADES Química en solución acuosa 2007 La molécula de agua Molécula de tipo AX 2 E 2 Angular Enlace O-H Alta energía Alta polaridad Capacidad para formar enlaces de hidrógeno Aguas ambientales-abundancia
CI61Q/CI71M PRINCIPIOS DE REMEDIACION Y RESTAURACION
 /CI71M PRINCIPIOS DE REMEDIACION Y RESTAURACION CLASE 3 FUENTES DE CONTAMINACION SEMESTRE PRIMAVERA 2009 UNIVERSIDAD DE CHILE FACULTAD DE CIENCIAS FÍSICAS Y MATEMÁTICAS DEPARTAMENTO DE INGENIERIA CIVIL
/CI71M PRINCIPIOS DE REMEDIACION Y RESTAURACION CLASE 3 FUENTES DE CONTAMINACION SEMESTRE PRIMAVERA 2009 UNIVERSIDAD DE CHILE FACULTAD DE CIENCIAS FÍSICAS Y MATEMÁTICAS DEPARTAMENTO DE INGENIERIA CIVIL
4. SÓLIDOS EN CONTACTO CON AGUAS NATURALES
 1 4. SÓLIDOS EN CONTACTO CON AGUAS NATURALES 4.1 INTRODUCCIÓN... 2 4.2 EQUILIBRIOS EN FASE SÓLIDA... 4 4.2.1. PRODUCTO DE SOLUBILIDAD... 5 4.2.2 EFECTO DEL IÓN COMÚN... 6 4.3 SOLUBILIDAD DE ÓXIDOS E HIDRÓXIDOS
1 4. SÓLIDOS EN CONTACTO CON AGUAS NATURALES 4.1 INTRODUCCIÓN... 2 4.2 EQUILIBRIOS EN FASE SÓLIDA... 4 4.2.1. PRODUCTO DE SOLUBILIDAD... 5 4.2.2 EFECTO DEL IÓN COMÚN... 6 4.3 SOLUBILIDAD DE ÓXIDOS E HIDRÓXIDOS
ACIDEZ DEL SUELO. Oscar Piedrahíta Junio 2009
 ACIDEZ DEL SUELO Oscar Piedrahíta Junio 2009 El ph del suelo es una medida de la acidez o de la alcalinidad de la solución del suelo ph = - log[h+] Los suelos minerales ácidos con ph inferiores a 5.2 contienen
ACIDEZ DEL SUELO Oscar Piedrahíta Junio 2009 El ph del suelo es una medida de la acidez o de la alcalinidad de la solución del suelo ph = - log[h+] Los suelos minerales ácidos con ph inferiores a 5.2 contienen
Equilibrios de solubilidad Problemas
 Equilibrios de solubilidad 16.39. Utilice BaSO 4 para describir la diferencia entre solubilidad, solubilidad molar y producto de solubilidad. 16.40. Por qué normalmente no se calculan los valores de K
Equilibrios de solubilidad 16.39. Utilice BaSO 4 para describir la diferencia entre solubilidad, solubilidad molar y producto de solubilidad. 16.40. Por qué normalmente no se calculan los valores de K
LAS AGUAS SUBTERRÁNEAS EN LA MINERÍA DÍA MUNDIAL DEL AGUA MAR 2015
 MAR 2015 LAS AGUAS SUBTERRÁNEAS EN LA MINERÍA Ing. Jose Luis Moreno Herrera Geología Ambiental y Riesgo Geológico INGEMMET jmoreno@ingemmet.gob.pe DÍA MUNDIAL DEL AGUA CONTENIDO I. II. III. IV. V. VI.
MAR 2015 LAS AGUAS SUBTERRÁNEAS EN LA MINERÍA Ing. Jose Luis Moreno Herrera Geología Ambiental y Riesgo Geológico INGEMMET jmoreno@ingemmet.gob.pe DÍA MUNDIAL DEL AGUA CONTENIDO I. II. III. IV. V. VI.
Suelos formados por viento (Loess)
 Suelos formados por viento (Loess) Procesos generales de formación de los suelos (continuación). Los elementos más facilmente lixiviables son las sales (carbonatos, cloruros, sulfatos, nitratos, bicarbonatos).
Suelos formados por viento (Loess) Procesos generales de formación de los suelos (continuación). Los elementos más facilmente lixiviables son las sales (carbonatos, cloruros, sulfatos, nitratos, bicarbonatos).
VÍDEOS EJERCICIOS OXIDACIÓN-REDUCCIÓN RESUELTOS: ENUNCIADOS
 VÍDEOS EJERCICIOS OXIDACIÓN-REDUCCIÓN RESUELTOS: ENUNCIADOS Ejercicio 1 Determinación del número de oxidación según las normas Determina el número de oxidación de los átomos de los siguientes compuestos:
VÍDEOS EJERCICIOS OXIDACIÓN-REDUCCIÓN RESUELTOS: ENUNCIADOS Ejercicio 1 Determinación del número de oxidación según las normas Determina el número de oxidación de los átomos de los siguientes compuestos:
MINISTERIO DE CIENCIA Y TECNOLOGÍA
 MINISTERIO DE CIENCIA Y TECNOLOGÍA CONVENIO DE COLABORACIÓN ENTRE EL INSTITUTO DE FOMENTO DE ANDALUCIA Y EL INSTITUTO GEOLÓGICO Y MINERO DE ESPAÑA PARA LA INVESTIGACIÓN Y DESARROLLO DE UN PROCESO Y SU
MINISTERIO DE CIENCIA Y TECNOLOGÍA CONVENIO DE COLABORACIÓN ENTRE EL INSTITUTO DE FOMENTO DE ANDALUCIA Y EL INSTITUTO GEOLÓGICO Y MINERO DE ESPAÑA PARA LA INVESTIGACIÓN Y DESARROLLO DE UN PROCESO Y SU
Ciencias del Mar. Meteorización de las Rocas. Oceanografía Química. Meteorización de las rocas
 Ciencias del Mar Meteorización de las Rocas Oceanografía Química Meteorización de las rocas La meteorización es el proceso de transformaciones físicas y químicas de las rocas parentales y minerales primarios
Ciencias del Mar Meteorización de las Rocas Oceanografía Química Meteorización de las rocas La meteorización es el proceso de transformaciones físicas y químicas de las rocas parentales y minerales primarios
9. CARTOGRAFÍA GEOQUÍMICA AMBIENTAL
 Página 123 de 148 9. CARTOGRAFÍA GEOQUÍMICA AMBIENTAL El sedimento, como muestra que representa una mezcla y un promedio de los materiales superficiales de la cuenca de drenaje, es susceptible de suministrar
Página 123 de 148 9. CARTOGRAFÍA GEOQUÍMICA AMBIENTAL El sedimento, como muestra que representa una mezcla y un promedio de los materiales superficiales de la cuenca de drenaje, es susceptible de suministrar
2º de Bachillerato EQUILIBRIOS DE SOLUBILIDAD
 º de Bachillerato EQUILIBRIOS DE SOLUBILIDAD Indice 1. Equilibrios heterogéneos.. Solubilidad. Reglas de solubilidad. 3. Reacciones de precipitación. 4. Producto de solubilidad. 5. Factores que modifican
º de Bachillerato EQUILIBRIOS DE SOLUBILIDAD Indice 1. Equilibrios heterogéneos.. Solubilidad. Reglas de solubilidad. 3. Reacciones de precipitación. 4. Producto de solubilidad. 5. Factores que modifican
9. Cuál es la solubilidad del sulfato de estroncio, SrSO 4? K ps = A) M B) M C) M D) 2.
 Equilibrio de precipitación ---------------------------------------------------------------------------------------------------------- 1. El producto de solubilidad de un sólido es: A) Una constante de
Equilibrio de precipitación ---------------------------------------------------------------------------------------------------------- 1. El producto de solubilidad de un sólido es: A) Una constante de
EJERCICIOS RESUELTOS DE REDOX
 EJERCICIOS RESUELTOS DE REDOX 1. Al hacer reaccionar cobre metálico con ácido nítrico diluido se obtiene monóxido de nitrógeno y nitrato de cobre (II). Plantee, iguale y complete la ecuación redox correspondiente,
EJERCICIOS RESUELTOS DE REDOX 1. Al hacer reaccionar cobre metálico con ácido nítrico diluido se obtiene monóxido de nitrógeno y nitrato de cobre (II). Plantee, iguale y complete la ecuación redox correspondiente,
TEMA 3. EQUILIBRIOS ACIDO BASE
 TEMA 3. EQUILIBRIOS ACIDO BASE 3.1 EQUILIBRIOS IÓNICOS...2 3.2 EQUILIBRIOS ACIDO BASE...3 3.3 PROCEDIMIENTOS GRÁFICOS PARA EL CÁLCULO DE EQUILIBRIOS...5 3.3.1 DIAGRAMA pc-ph...5 3.3.2 DIAGRAMA pc-ph para
TEMA 3. EQUILIBRIOS ACIDO BASE 3.1 EQUILIBRIOS IÓNICOS...2 3.2 EQUILIBRIOS ACIDO BASE...3 3.3 PROCEDIMIENTOS GRÁFICOS PARA EL CÁLCULO DE EQUILIBRIOS...5 3.3.1 DIAGRAMA pc-ph...5 3.3.2 DIAGRAMA pc-ph para
PROPIEDADES QUÍMICAS DEL SUELO
 PROPIEDADES QUÍMICAS DEL SUELO DEFINICIONES Ión: Átomos o moléculas que pierden o ganan electrones por lo cual adquieren una determinada carga; si ganan adquieren carga negativa: aniones (Cl -, NO 3- );
PROPIEDADES QUÍMICAS DEL SUELO DEFINICIONES Ión: Átomos o moléculas que pierden o ganan electrones por lo cual adquieren una determinada carga; si ganan adquieren carga negativa: aniones (Cl -, NO 3- );
Zonas Reactivas Anaeróbicas. Remediación in situ de agua subterránea contaminada con Cr VI. Aplicación en México
 Zonas Reactivas Anaeróbicas Remediación in situ de agua subterránea contaminada con Cr VI Aplicación en México Curso Soluciones a la Contaminación de Suelos y Acuíferos Ponente: Jerjes Pantoja Irys Fecha:
Zonas Reactivas Anaeróbicas Remediación in situ de agua subterránea contaminada con Cr VI Aplicación en México Curso Soluciones a la Contaminación de Suelos y Acuíferos Ponente: Jerjes Pantoja Irys Fecha:
4. Un agente oxidante (2 correctas) A) Toma electrones de otra sustancia B) Da electrones a otra sustancia C) Se oxida D) Se reduce
 CUESTIONES. EQUILIBRIO OXIDO-REDUCCIÓN ---------------------------------------------------------------------------------------------------------- 1. Las reacciones químicas que implican transferencias
CUESTIONES. EQUILIBRIO OXIDO-REDUCCIÓN ---------------------------------------------------------------------------------------------------------- 1. Las reacciones químicas que implican transferencias
Seminario de Química 2º Bachillerato LOGSE Unidad 0: Repaso Química 1º Bachillerato
 A) Composición Centesimal y Fórmulas químicas 1.- Determina la composición centesimal del Ca3(PO4)2. Datos: Masas atómicas (g/mol): Ca=40; P=31; O=16 S: Ca= 38,7%; P=20%; O=41,3% 2.- Determina la composición
A) Composición Centesimal y Fórmulas químicas 1.- Determina la composición centesimal del Ca3(PO4)2. Datos: Masas atómicas (g/mol): Ca=40; P=31; O=16 S: Ca= 38,7%; P=20%; O=41,3% 2.- Determina la composición
INTRODUCCION AL EQUILIBRIO PRECIPITACIÓN - SOLUBILIZACIÓN
 INTRODUCCION AL EQUILIBRIO PRECIPITACIÓN - SOLUBILIZACIÓN Lo básico que debes saber de Química General 14-1 LA SOLUBILIDAD DE ELECTROLITOS FUERTES POCO SOLUBLES Compuesto Solubilidad Electrolito NaCl BaSO
INTRODUCCION AL EQUILIBRIO PRECIPITACIÓN - SOLUBILIZACIÓN Lo básico que debes saber de Química General 14-1 LA SOLUBILIDAD DE ELECTROLITOS FUERTES POCO SOLUBLES Compuesto Solubilidad Electrolito NaCl BaSO
CHARLAS AMBIENTALES PARA LAS COMUNIDADES DEL VALLE ALTO DEL CHOAPA SUELO
 CHARLAS AMBIENTALES PARA LAS COMUNIDADES DEL VALLE ALTO DEL CHOAPA SUELO SUELO El suelo es un pequeño manto superficial de la corte terrestre que puede sostener la vida vegetal. Se origina de un proceso
CHARLAS AMBIENTALES PARA LAS COMUNIDADES DEL VALLE ALTO DEL CHOAPA SUELO SUELO El suelo es un pequeño manto superficial de la corte terrestre que puede sostener la vida vegetal. Se origina de un proceso
QUÍMICA 2º BACHILLERATO
 REACCIONES DE TRANSFERENCIA DE ELECTRONES: Y ESTEQUIOMETRÍA 1.-/ Iguale por el método del ion-electrón la ecuación: Cu + HNO 3 Cu(NO 3 ) 2 + NO + H 2 O, correspondiente a la reacción del cobre con el ácido
REACCIONES DE TRANSFERENCIA DE ELECTRONES: Y ESTEQUIOMETRÍA 1.-/ Iguale por el método del ion-electrón la ecuación: Cu + HNO 3 Cu(NO 3 ) 2 + NO + H 2 O, correspondiente a la reacción del cobre con el ácido
OXIDACIÓN-REDUCCIÓN. PAU-tipos de problemas
 OXIDACIÓN-REDUCCIÓN PAU-tipos de problemas Ajustar reacciones químicas de oxidación reducción por el método del ión-electrón y realizar cálculos estequiométricos (disoluciones, gases, sólidos, reactivos
OXIDACIÓN-REDUCCIÓN PAU-tipos de problemas Ajustar reacciones químicas de oxidación reducción por el método del ión-electrón y realizar cálculos estequiométricos (disoluciones, gases, sólidos, reactivos
Prof(a). María Angélica Sánchez Palacios
 Tema 5. Oxidación Reducción Prof(a). María Angélica Sánchez Palacios Los procesos electroquímicos consisten en reacciones de oxido-reducción en las cuales: - La energía liberada por una reacción espontánea,
Tema 5. Oxidación Reducción Prof(a). María Angélica Sánchez Palacios Los procesos electroquímicos consisten en reacciones de oxido-reducción en las cuales: - La energía liberada por una reacción espontánea,
Tema 5 Tratamientos térmicos EUETI Escola Universitaria de Enxeñería Técnica Industrial
 Tratamiento de Residuos Tema 5 Tratamientos térmicos EUETI Escola Universitaria de Enxeñería Técnica Industrial INCINERACIÓN DE RESIDUOS Definición: Es el procesamiento térmico de los residuos sólidos
Tratamiento de Residuos Tema 5 Tratamientos térmicos EUETI Escola Universitaria de Enxeñería Técnica Industrial INCINERACIÓN DE RESIDUOS Definición: Es el procesamiento térmico de los residuos sólidos
PAPEL DEL BIOCARBÓN (BIOCHAR) EN LA RECUPERACIÓN DE SUELOS CONTAMINADOS POR ELEMENTOS TRAZA
 PAPEL DEL BIOCARBÓN (BIOCHAR) EN LA RECUPERACIÓN DE SUELOS CONTAMINADOS POR ELEMENTOS TRAZA EDUARDO MORENO JIMÉNEZ DEPARTAMENTO DE QUÍMICA AGRÍCOLA Y BROMATOLOGÍA UNIVERSIDAD AUTÓNOMA DE MADRID, ESPAÑA
PAPEL DEL BIOCARBÓN (BIOCHAR) EN LA RECUPERACIÓN DE SUELOS CONTAMINADOS POR ELEMENTOS TRAZA EDUARDO MORENO JIMÉNEZ DEPARTAMENTO DE QUÍMICA AGRÍCOLA Y BROMATOLOGÍA UNIVERSIDAD AUTÓNOMA DE MADRID, ESPAÑA
Acidez de cationes y basicidad de oxoaniones
 Acidez de cationes y basicidad de oxoaniones Principles of descriptive inorganic chemistry Gary Wulfsberg La hidratación de un catión metálico: es una reacción ácidobase? M n+ (g) + nh 2 O(l) M n+ (ac)
Acidez de cationes y basicidad de oxoaniones Principles of descriptive inorganic chemistry Gary Wulfsberg La hidratación de un catión metálico: es una reacción ácidobase? M n+ (g) + nh 2 O(l) M n+ (ac)
Página 1
 TEMA 5. CINÉTICA QUÍMICA Y EQUILIBRIO QUÍMICO 6.2) A una hipotética reacción química A + B C le corresponde la siguiente ecuación de velocidad: v = k [A] [B]. Indique: a) El orden de la reacción respecto
TEMA 5. CINÉTICA QUÍMICA Y EQUILIBRIO QUÍMICO 6.2) A una hipotética reacción química A + B C le corresponde la siguiente ecuación de velocidad: v = k [A] [B]. Indique: a) El orden de la reacción respecto
1. Cuál(es) de los siguientes ejemplos corresponde(n) a una reacción redox? 2 MX 2 M + X 2
 Nº GUÍA PRÁCTICA Óxido reducción I: reacciones redox Ejercicios PSU 1. Cuál(es) de los siguientes ejemplos corresponde(n) a una reacción redox? I) xidación de metales II) Respiración celular III) Procesos
Nº GUÍA PRÁCTICA Óxido reducción I: reacciones redox Ejercicios PSU 1. Cuál(es) de los siguientes ejemplos corresponde(n) a una reacción redox? I) xidación de metales II) Respiración celular III) Procesos
SEMINARIOS (ÁCIDO-BASE Kps REDOX) QUÍMICA GENERAL II OTOÑO 2012
 SEMINARIOS (ÁCIDO-BASE Kps REDOX) QUÍMICA GENERAL II OTOÑO 2012 I. EQUILIBRIO ÁCIDO-BASE 1. Para las siguientes compuestos: NaCl, NaOH, HCl, CH 3 COOH, NH 3, FeCl 3, Na 2 CO 3, H 3 PO 4 : a) Clasifíquelos
SEMINARIOS (ÁCIDO-BASE Kps REDOX) QUÍMICA GENERAL II OTOÑO 2012 I. EQUILIBRIO ÁCIDO-BASE 1. Para las siguientes compuestos: NaCl, NaOH, HCl, CH 3 COOH, NH 3, FeCl 3, Na 2 CO 3, H 3 PO 4 : a) Clasifíquelos
QUÍMICA de 2º de BACHILLERATO ELECTROQUÍMICA
 QUÍMICA de 2º de BACHILLERATO ELECTROQUÍMICA CUESTIONES RESUELTAS QUE HAN SIDO PROPUESTAS EN LOS EXÁMENES DE LAS PRUEBAS DE ACCESO A ESTUDIOS UNIVERSITARIOS EN LA COMUNIDAD DE MADRID (1996 2010) VOLUMEN
QUÍMICA de 2º de BACHILLERATO ELECTROQUÍMICA CUESTIONES RESUELTAS QUE HAN SIDO PROPUESTAS EN LOS EXÁMENES DE LAS PRUEBAS DE ACCESO A ESTUDIOS UNIVERSITARIOS EN LA COMUNIDAD DE MADRID (1996 2010) VOLUMEN
OXIDACIÓN-REDUCCIÓN. PAU-tipos de problemas
 OXIDACIÓN-REDUCCIÓN PAU-tipos de problemas Ajustar reacciones químicas de oxidación reducción por el método del ión-electrón y realizar cálculos estequiométricos (disoluciones, gases, sólidos, reactivos
OXIDACIÓN-REDUCCIÓN PAU-tipos de problemas Ajustar reacciones químicas de oxidación reducción por el método del ión-electrón y realizar cálculos estequiométricos (disoluciones, gases, sólidos, reactivos
Septiembre Pregunta B1.- Ajuste las siguientes reacciones iónicas redox. Indique para cada caso el agente oxidante y el reductor.
 Modelo 2014. Pregunta 4A.- A 30 ml de una disolución de CuSO 4 0,1 M se le añade aluminio metálico en exceso. a) Escriba y ajuste las semirreacciones de reducción y oxidación e indique el comportamiento
Modelo 2014. Pregunta 4A.- A 30 ml de una disolución de CuSO 4 0,1 M se le añade aluminio metálico en exceso. a) Escriba y ajuste las semirreacciones de reducción y oxidación e indique el comportamiento
REACCIONES DE TRANSFERENCIA DE ELECTRONES 2ºBACH
 1. Ajusta las siguientes reacciones redox, utilizando el método del ion electrón: a) HNO 3 + Cu Cu(NO 3 ) 2 + NO 2 + H 2 O b) K 2 Cr 2 O 7 +HI + HClO 4 Cr(ClO 4 ) 3 +I 2 +KClO 4 + H 2 O c) H 2 SO 4 + HI
1. Ajusta las siguientes reacciones redox, utilizando el método del ion electrón: a) HNO 3 + Cu Cu(NO 3 ) 2 + NO 2 + H 2 O b) K 2 Cr 2 O 7 +HI + HClO 4 Cr(ClO 4 ) 3 +I 2 +KClO 4 + H 2 O c) H 2 SO 4 + HI
Unidad 3. Química de coordinación Capítulo 2 Hidrólisis de iones metálicos
 Unidad 3. Química de coordinación Capítulo 2 Hidrólisis de iones metálicos Sección 1. Complejos con el agua Centremos nuestra atención en los complejos que pueden encontrarse habitualmente en las disoluciones
Unidad 3. Química de coordinación Capítulo 2 Hidrólisis de iones metálicos Sección 1. Complejos con el agua Centremos nuestra atención en los complejos que pueden encontrarse habitualmente en las disoluciones
REACCIONES DE TRANSFERENCIA DE ELECTRONES 2ºBACH
 1. Ajusta las siguientes reacciones redox, utilizando el método del ion electrón: a) HNO 3 + Cu Cu(NO 3 ) 2 + NO 2 + H 2 O b) K 2 Cr 2 O 7 +HI + HClO 4 Cr(ClO 4 ) 3 +I 2 +KClO 4 + H 2 O c) H 2 SO 4 + HI
1. Ajusta las siguientes reacciones redox, utilizando el método del ion electrón: a) HNO 3 + Cu Cu(NO 3 ) 2 + NO 2 + H 2 O b) K 2 Cr 2 O 7 +HI + HClO 4 Cr(ClO 4 ) 3 +I 2 +KClO 4 + H 2 O c) H 2 SO 4 + HI
QUÍMICA I. TEMA 10 Equilibrio de solubilidad. Tecnólogo en Minería
 QUÍMICA I TEMA 10 Equilibrio de solubilidad Tecnólogo en Minería O b j e t i v o Examinar las propiedades físicas de las disoluciones y compararlas con las de sus componentes Disoluciones acuosas de sustancias
QUÍMICA I TEMA 10 Equilibrio de solubilidad Tecnólogo en Minería O b j e t i v o Examinar las propiedades físicas de las disoluciones y compararlas con las de sus componentes Disoluciones acuosas de sustancias
MODELO DE EXAMEN DE QUIMICA (25 AÑOS) INSTRUCCIONES PREGUNTAS
 MODELO DE EXAMEN DE QUIMICA (25 AÑOS) INSTRUCCIONES a. El examen de química consistirá en 30 preguntas de tipo test b. La duración del examen será de 1,5 horas. c. Sólo hay que elegir una respuesta por
MODELO DE EXAMEN DE QUIMICA (25 AÑOS) INSTRUCCIONES a. El examen de química consistirá en 30 preguntas de tipo test b. La duración del examen será de 1,5 horas. c. Sólo hay que elegir una respuesta por
FOTO 15. Mal estado de las componentes disueltos en el agua superficial y
 Los cuerpos de agua (ríos, lagos, lagunas, acuiferos, etc) que se constituyen como suministros naturales de agua no son puros en el sentido de que carecen de productos químicos disueltos como sucede con
Los cuerpos de agua (ríos, lagos, lagunas, acuiferos, etc) que se constituyen como suministros naturales de agua no son puros en el sentido de que carecen de productos químicos disueltos como sucede con
AJUSTE DE REACCIONES RÉDOX
 AJUSTE DE REACCIONES RÉDOX 1. Razona si son verdaderas o falsas las siguientes afirmaciones. En la reacción: a) Los cationes Ag + actúan como reductores. b) Los aniones NO 3 actúan como oxidantes. c) El
AJUSTE DE REACCIONES RÉDOX 1. Razona si son verdaderas o falsas las siguientes afirmaciones. En la reacción: a) Los cationes Ag + actúan como reductores. b) Los aniones NO 3 actúan como oxidantes. c) El
QUÍMICA PRE UNIVERSITARIA
 QUÍMICA PRE UNIVERSITARIA estás a punto de ingresar a la UNI REACCIONES QUÍMICAS QUÉ ES UNA REACCIÓN QUÍMICA? Son cambios que se producen en las sustancias debido a efectos termodinámicos como la presión
QUÍMICA PRE UNIVERSITARIA estás a punto de ingresar a la UNI REACCIONES QUÍMICAS QUÉ ES UNA REACCIÓN QUÍMICA? Son cambios que se producen en las sustancias debido a efectos termodinámicos como la presión
CLASIFICACIÓN DE LAS REACCIONES QUÍMICAS. 1. Combinación de dos elementos para formar un compuesto
 CLASIFICACIÓN DE LAS REACCIONES QUÍMICAS REACCIONES DE COMBINACIÓN Las reacciones en que dos o más sustancias se combinan para formar un compuesto se llaman reacciones de combinación. Incluyen 1) la combinación
CLASIFICACIÓN DE LAS REACCIONES QUÍMICAS REACCIONES DE COMBINACIÓN Las reacciones en que dos o más sustancias se combinan para formar un compuesto se llaman reacciones de combinación. Incluyen 1) la combinación
Tema 5. Oxidación Reducción. Prof(a). María Angélica Sánchez Palacios
 Tema 5. Oxidación Reducción Prof(a). María Angélica Sánchez Palacios Los procesos electroquímicos consisten en reacciones de oxido-reducción en las cuales: - La energía liberada por una reacción espontánea
Tema 5. Oxidación Reducción Prof(a). María Angélica Sánchez Palacios Los procesos electroquímicos consisten en reacciones de oxido-reducción en las cuales: - La energía liberada por una reacción espontánea
Hidrogeología. Tema 7 DE LAS AGUAS SUBTERRÁNEAS. Luis F. Rebollo. Luis F. Rebollo T7. CARACTERÍSTICAS AGUAS SUBTERÁNEAS
 Hidrogeología Tema 7 CARACTERÍSTICAS FÍSICOF SICO-QUÍMICAS DE LAS AGUAS SUBTERRÁNEAS 1 T7. CARACTERÍSTICAS FÍSICO-QUÍMICAS DE LAS AGUAS SUBTERÁNEAS 1. Características físicof de las aguas subterráneas.
Hidrogeología Tema 7 CARACTERÍSTICAS FÍSICOF SICO-QUÍMICAS DE LAS AGUAS SUBTERRÁNEAS 1 T7. CARACTERÍSTICAS FÍSICO-QUÍMICAS DE LAS AGUAS SUBTERÁNEAS 1. Características físicof de las aguas subterráneas.
QUÍMICA 2º BACHILLERATO
 1.-/ Para los compuestos poco solubles CuBr, Ba(IO 3 ) 2 y Fe(OH) 3 : a) Escriba la ecuación de equilibrio de solubilidad en agua. b) La expresión del producto de solubilidad. c) El valor de la solubilidad
1.-/ Para los compuestos poco solubles CuBr, Ba(IO 3 ) 2 y Fe(OH) 3 : a) Escriba la ecuación de equilibrio de solubilidad en agua. b) La expresión del producto de solubilidad. c) El valor de la solubilidad
TEMA 1. EL AGUA NATURAL
 TEMA 1. EL AGUA NATURAL 1.1.- EL AGUA. CARACTERÍSTICAS Y PROPIEDADES 1.1.1. Características del agua 1.2.2. Propiedad disolvente del agua 1.2. IMPURIFICACIÓN NATURAL DEL AGUA 1.3. FACTORES QUE INCIDEN
TEMA 1. EL AGUA NATURAL 1.1.- EL AGUA. CARACTERÍSTICAS Y PROPIEDADES 1.1.1. Características del agua 1.2.2. Propiedad disolvente del agua 1.2. IMPURIFICACIÓN NATURAL DEL AGUA 1.3. FACTORES QUE INCIDEN
Ejercicios 2 (Estequiometría) 3) Calcule la masa, en gramos, de 0,433 mol de nitrato de calcio. R: 71,1 g Ca(NO 3 ) 2
 Profesor Bernardo Leal Química El Mol y número de Avogadro: Ejercicios 2 (Estequiometría) 1) Calcule el número de moles de glucosa (C 6 H 12 O 6 ) que hay en 5,38 g de esta sustancia R: 0,03 mol C 6 H
Profesor Bernardo Leal Química El Mol y número de Avogadro: Ejercicios 2 (Estequiometría) 1) Calcule el número de moles de glucosa (C 6 H 12 O 6 ) que hay en 5,38 g de esta sustancia R: 0,03 mol C 6 H
LOS SUELOS CONTAMINADOS Y SU GESTIÓN. Master en Planificación Territorial y Gestión Ambiental UTEM - UB
 LOS SUELOS CONTAMINADOS Y SU GESTIÓN Master en Planificación Territorial y Gestión Ambiental UTEM - UB PROCESOS DE FORMACIÓN Físicos, químicos y biológicos Conducentes a la horizonación/haploidización
LOS SUELOS CONTAMINADOS Y SU GESTIÓN Master en Planificación Territorial y Gestión Ambiental UTEM - UB PROCESOS DE FORMACIÓN Físicos, químicos y biológicos Conducentes a la horizonación/haploidización
Química Básica del Agua
 Química Básica del Agua Índice de este módulo Soluciones iónicas Estructuras iónicas Terminología Índices de saturación S.D.I. TERMINOLOGÍA Ion Partícula cargada eléctricamente, positiva (catión) o negativa
Química Básica del Agua Índice de este módulo Soluciones iónicas Estructuras iónicas Terminología Índices de saturación S.D.I. TERMINOLOGÍA Ion Partícula cargada eléctricamente, positiva (catión) o negativa
APLICACIONES. 1. MEDIOAMBIENTE Determinación de metales y contaminantes en aguas continentales, potables, vertido, salmueras y aguas de mar
 APLICACIONES 1. MEDIOAMBIENTE Determinación de metales y contaminantes en aguas continentales, potables, vertido, salmueras y aguas de mar 2. ALIMENTACIÓN Y AGRICULTURA Determinación de metales y posibles
APLICACIONES 1. MEDIOAMBIENTE Determinación de metales y contaminantes en aguas continentales, potables, vertido, salmueras y aguas de mar 2. ALIMENTACIÓN Y AGRICULTURA Determinación de metales y posibles
Práctica 6: Recuperación de balsas ácidas.
 Práctica 6: Recuperación de balsas ácidas. Nombre de los alumnos: Primer Autor: Cañete Rioja, Elena Segundo Autor: Romero de Lucca Carrasco, Horacio Eduardo Tercer Autor: Sevilla Horrillo, Lucía de realización
Práctica 6: Recuperación de balsas ácidas. Nombre de los alumnos: Primer Autor: Cañete Rioja, Elena Segundo Autor: Romero de Lucca Carrasco, Horacio Eduardo Tercer Autor: Sevilla Horrillo, Lucía de realización
UBICACIÓN GEOGRÁFICA
 UBICACIÓN GEOGRÁFICA Minera Aurífera Retamas S.A. MARSA dedicada a la actividad minera subterránea, está ubicada en: Departamento: La Libertad. Provincia : Pataz. Distrito : Parcoy. Altitud : 2950 a 4200
UBICACIÓN GEOGRÁFICA Minera Aurífera Retamas S.A. MARSA dedicada a la actividad minera subterránea, está ubicada en: Departamento: La Libertad. Provincia : Pataz. Distrito : Parcoy. Altitud : 2950 a 4200
Betzy Escobedo Zamarripa. Cobaeh 2013-a
 Betzy Escobedo Zamarripa Cobaeh 2013-a Son procesos naturales que reciclan elementos en diferentes formas químicas desde el medio ambiente hacia los organismos, y luego a la inversa. Agua, carbón, oxígeno,
Betzy Escobedo Zamarripa Cobaeh 2013-a Son procesos naturales que reciclan elementos en diferentes formas químicas desde el medio ambiente hacia los organismos, y luego a la inversa. Agua, carbón, oxígeno,
LIMNOLOGÍA. LICENCIATURA EN GESTIÓN AMBIENTAL CURE/Facultad de Ciencias UdelaR
 LIMNOLOGÍA LICENCIATURA EN GESTIÓN AMBIENTAL CURE/Facultad de Ciencias UdelaR Ambiente/abiótico Maldonado, 2016 Estructura microscópica estratificación Molécula dipolar (atracciones intensas) Puentes de
LIMNOLOGÍA LICENCIATURA EN GESTIÓN AMBIENTAL CURE/Facultad de Ciencias UdelaR Ambiente/abiótico Maldonado, 2016 Estructura microscópica estratificación Molécula dipolar (atracciones intensas) Puentes de
Tema 6. Equilibrios de precipitación
 Tema 6. Equilibrios de precipitación 1. Introducción. 2. Solubilidad y Constante de solubilidad. 3. Sales poco solubles. 4. Factores que afectan a la solubilidad. 5. Predicción de las reacciones de precipitación.
Tema 6. Equilibrios de precipitación 1. Introducción. 2. Solubilidad y Constante de solubilidad. 3. Sales poco solubles. 4. Factores que afectan a la solubilidad. 5. Predicción de las reacciones de precipitación.
CHONPS Y LOS CICLOS BIOGEOQUIMICOS
 CHONPS Y LOS CICLOS BIOGEOQUIMICOS UNIVERSIDAD INTERAMERICANA DE PUERTO RICO RECINTO DE BAYAMÓN Math and Science Partnership for the 21st Century Elementary and Secondary School MSP-21 Phase IV PROFESORA
CHONPS Y LOS CICLOS BIOGEOQUIMICOS UNIVERSIDAD INTERAMERICANA DE PUERTO RICO RECINTO DE BAYAMÓN Math and Science Partnership for the 21st Century Elementary and Secondary School MSP-21 Phase IV PROFESORA
Ejercicios Estequiometria
 Ejercicios Estequiometria 1. Se hacen reaccionar 22,75 g de Zn que contiene un 7,25 % de impurezas con exceso de HCl. Calcula la masa de H 2 desprendida. HCl + Zn ZnCl 2 + H 2 2. Se calcinan en un horno
Ejercicios Estequiometria 1. Se hacen reaccionar 22,75 g de Zn que contiene un 7,25 % de impurezas con exceso de HCl. Calcula la masa de H 2 desprendida. HCl + Zn ZnCl 2 + H 2 2. Se calcinan en un horno
Colegio Superior de Señoritas Tema: Formación de Compuestos Químicos Septiembre 2010 Prof.: NVM 8vo Nivel Departamento de Ciencias
 COMPUESTOS QUÍMICOS Y SU CLASIFICACIÓN El número de oxidación: representa la cantidad de electrones que puede ganar o perder un elemento. El hidrógeno tiene número de oxidación +1 y puede perder un electrón;
COMPUESTOS QUÍMICOS Y SU CLASIFICACIÓN El número de oxidación: representa la cantidad de electrones que puede ganar o perder un elemento. El hidrógeno tiene número de oxidación +1 y puede perder un electrón;
LAS AGUAS RESIDUALES URBANAS
 LAS AGUAS RESIDUALES URBANAS Manhatan, New York Ciudadela del Machu Picchu, Perú Guayaquil, Ecuador Usos de las aguas residuales riego agrícola (cultivos y semilleros) riego de parques y jardines (campos
LAS AGUAS RESIDUALES URBANAS Manhatan, New York Ciudadela del Machu Picchu, Perú Guayaquil, Ecuador Usos de las aguas residuales riego agrícola (cultivos y semilleros) riego de parques y jardines (campos
El uso de fertilizantes sintéticos, los cultivos agrícolas y la quema de carbón y petróleo han duplicado el ritmo al cual el
 ( ) La diferencia de temperatura de las distintas fracciones ( ) La diferencia de densidad de los distintos hidrocarburos que forman las fracciones ( ) La solubilidad de cada una de las fracciones 5 El
( ) La diferencia de temperatura de las distintas fracciones ( ) La diferencia de densidad de los distintos hidrocarburos que forman las fracciones ( ) La solubilidad de cada una de las fracciones 5 El
PROCESOS DE FORMACION Y DISOLUCION DE SOLIDOS. Procesos básicos. Qca. en Solución Acuosa SOLIDO. Biomineralización. Erosión + Desgaste
 PROCESOS DE FORMACION Y DISOLUCION DE SOLIDOS Qca. en Solución Acuosa Procesos básicos SOLIDO Erosión + Desgaste Biomineralización ESPECIE EN SOLUCION Biomineralización Proceso de formación de un sólido
PROCESOS DE FORMACION Y DISOLUCION DE SOLIDOS Qca. en Solución Acuosa Procesos básicos SOLIDO Erosión + Desgaste Biomineralización ESPECIE EN SOLUCION Biomineralización Proceso de formación de un sólido
Problemas de electrolisis. Resueltos
 Problemas de electrolisis Resueltos Problemas 5,6 y 7 de la hoja de refuerzo Tambien estan al final de la hoja con enunciados de ejecicios PAU Serie refuerzo electroquímica 5 Se realiza la electrólisis
Problemas de electrolisis Resueltos Problemas 5,6 y 7 de la hoja de refuerzo Tambien estan al final de la hoja con enunciados de ejecicios PAU Serie refuerzo electroquímica 5 Se realiza la electrólisis
POSGRADO EN CIENCIAS DE LA TIERRA SEMESTRE EXAMEN DE QUIMICA No. EXAMEN:
 NOMBRE: POSGRADO EN CIENCIAS DE LA TIERRA EXAMEN DE QUIMICA No. EXAMEN: TUTOR: ORIENTACION: 1. Qué es el arsénico? a. Un metal b. Un metaloide c. Una tierra rara d. Un gas 2. Cuál es el ácido hipobromoso?:
NOMBRE: POSGRADO EN CIENCIAS DE LA TIERRA EXAMEN DE QUIMICA No. EXAMEN: TUTOR: ORIENTACION: 1. Qué es el arsénico? a. Un metal b. Un metaloide c. Una tierra rara d. Un gas 2. Cuál es el ácido hipobromoso?:
ATENDIENDO A LA ESTRUCTURA de las reacciones podemos clasificarlas en:
 REACCIONES QUÍMICAS ATENDIENDO A LA ESTRUCTURA de las reacciones podemos clasificarlas en: Reacciones de combinación o síntesis. En ellas se forman uno o varios compuestos a partir de elementos o compuestos.
REACCIONES QUÍMICAS ATENDIENDO A LA ESTRUCTURA de las reacciones podemos clasificarlas en: Reacciones de combinación o síntesis. En ellas se forman uno o varios compuestos a partir de elementos o compuestos.
OZONO O 3 INTEMPERISMO +H 2 O O 2 HNO 3 OH - +NO 2 O +SO 2 H 2 SO 4 VIENTOS LLUVIA ACIDA CO 2 CO 3 SULFATOS TERREMOTOS NITRATOS HUGO TORRENS
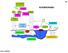 O 3 OZONO 1303 +H 2 O INTEMPERISMO O 2 +SO 2 OH - +NO 2 O HNO 3 H 2 SO 4 LLUVIA ACIDA CO 2 CO 3 2- VIENTOS SULFATOS NITRATOS TERREMOTOS HUGO TORRENS GRAN EXPLOSION 1304 1 H 1 4 He 2 FORMACION DE ESTRELLAS
O 3 OZONO 1303 +H 2 O INTEMPERISMO O 2 +SO 2 OH - +NO 2 O HNO 3 H 2 SO 4 LLUVIA ACIDA CO 2 CO 3 2- VIENTOS SULFATOS NITRATOS TERREMOTOS HUGO TORRENS GRAN EXPLOSION 1304 1 H 1 4 He 2 FORMACION DE ESTRELLAS
REACCIONES DE TRANSFERENCIA DE ELECTRONES, AJUSTE Y ESTEQUIOMETRÍA. 1-Nombra tres sustancias que sean oxidantes enérgicos Por qué?
 REACCIONES DE TRANSFERENCIA DE ELECTRONES, AJUSTE Y ESTEQUIOMETRÍA 1-Nombra tres sustancias que sean oxidantes enérgicos Por qué? 2- Nombra tres cuerpos que sean fuertes reductores por qué? 3- Qué se entiende
REACCIONES DE TRANSFERENCIA DE ELECTRONES, AJUSTE Y ESTEQUIOMETRÍA 1-Nombra tres sustancias que sean oxidantes enérgicos Por qué? 2- Nombra tres cuerpos que sean fuertes reductores por qué? 3- Qué se entiende
HUGO BONIFAZ. 13/03/2015 H Bonifaz
 MODELAMIENTO DEL FLUJO Y TRANSPORTE DE METALES PESADOS EN EL ACUÍFERO SUPERIOR DE LA ZONA URBANA DE LA PARROQUIA DE SAN CARLOS, PROVINCIA DE ORELLANA A TRAVÉS DE LA CARACTERIZACIÓN IN SITU DEL SUBSUELO
MODELAMIENTO DEL FLUJO Y TRANSPORTE DE METALES PESADOS EN EL ACUÍFERO SUPERIOR DE LA ZONA URBANA DE LA PARROQUIA DE SAN CARLOS, PROVINCIA DE ORELLANA A TRAVÉS DE LA CARACTERIZACIÓN IN SITU DEL SUBSUELO
EVALUACIÓN DE LA CALIDAD DEL AGUA EN LA ZONA COSTERA DE IXTAPA-ZIHUATANEJO
 UNIVERSIDAD AUTÓNOMA DE QUERÉTARO Centro de Estudios Académicos sobre Contaminación Ambiental FACULTAD DE QUÍMICA Laboratorio de Ciencias Ambientales EVALUACIÓN DE LA CALIDAD DEL AGUA EN LA ZONA COSTERA
UNIVERSIDAD AUTÓNOMA DE QUERÉTARO Centro de Estudios Académicos sobre Contaminación Ambiental FACULTAD DE QUÍMICA Laboratorio de Ciencias Ambientales EVALUACIÓN DE LA CALIDAD DEL AGUA EN LA ZONA COSTERA
BIODIGESTORES Una solución práctica para los desechos orgánicos con aporte de múltiples beneficios económicos.
 BIODIGESTORES Una solución práctica para los desechos orgánicos con aporte de múltiples beneficios económicos. Mediante equipos sencillos y de bajo costo se propone el tratamiento de los residuales orgánicos
BIODIGESTORES Una solución práctica para los desechos orgánicos con aporte de múltiples beneficios económicos. Mediante equipos sencillos y de bajo costo se propone el tratamiento de los residuales orgánicos
REACCIONES DE OXIDACIÓN-REDUCCIÓN
 10 REACCINES DE XIDACIÓN-REDUCCIÓN SLUCINES A LAS ACTIVIDADES PRPUESTAS EN EL INTERIR DE LA UNIDAD 1 Por qué en los procesos redox no puede existir una única semirreacción de oxidación o de reducción?
10 REACCINES DE XIDACIÓN-REDUCCIÓN SLUCINES A LAS ACTIVIDADES PRPUESTAS EN EL INTERIR DE LA UNIDAD 1 Por qué en los procesos redox no puede existir una única semirreacción de oxidación o de reducción?
ANEXO 1. Límites permisibles para descargas líquidas, Anexo A-2 del Reglamento en Materia de Contaminación Hídrica
 ANEXO 1 Límites permisibles para descargas líquidas, Anexo A-2 del Reglamento en Materia de Contaminación Hídrica Rev. 0 Pág. 1 de 5 PARÁMETROS APLICABLES A DESCARGA DE AGUAS RESIDUALES DE PRUEBAS HIDROSTÁTICAS
ANEXO 1 Límites permisibles para descargas líquidas, Anexo A-2 del Reglamento en Materia de Contaminación Hídrica Rev. 0 Pág. 1 de 5 PARÁMETROS APLICABLES A DESCARGA DE AGUAS RESIDUALES DE PRUEBAS HIDROSTÁTICAS
TRANSFERENCIA DE ELECTRONES AJUSTE DE REACCIONES REDOX
 TRANSFERENCIA DE ELECTRONES AJUSTE DE REACCIONES REDOX E1A.S2012 El dióxido de manganeso reacciona en medio hidróxido potásico con clorato de potasio para dar permanganato de potasio, cloruro de potasio
TRANSFERENCIA DE ELECTRONES AJUSTE DE REACCIONES REDOX E1A.S2012 El dióxido de manganeso reacciona en medio hidróxido potásico con clorato de potasio para dar permanganato de potasio, cloruro de potasio
CONCENTRACIONES Y SOLUCIONES
 Clase de problemas Nº 2 CONCENTRACIONES Y SOLUCIONES Introducción Las soluciones son mezclas homogéneas de componentes que no reaccionan entre si sino que se disuelven: Solución = Soluto + Solvente El
Clase de problemas Nº 2 CONCENTRACIONES Y SOLUCIONES Introducción Las soluciones son mezclas homogéneas de componentes que no reaccionan entre si sino que se disuelven: Solución = Soluto + Solvente El
Curso Hidrogeoquímica para Dummies
 Curso Hidrogeoquímica para Dummies Sesión 10 Componentes del Agua Subterránea www.gidahatari.com Cuando una especie iónica se encuentra en concentraciones superiores a 1mg/L se le denomina Especie Iónica
Curso Hidrogeoquímica para Dummies Sesión 10 Componentes del Agua Subterránea www.gidahatari.com Cuando una especie iónica se encuentra en concentraciones superiores a 1mg/L se le denomina Especie Iónica
Guía de ejercicios equilibrio químico
 Guía de ejercicios equilibrio químico Profesor Edwar Fuentes Química Analítica I Semestre primavera 2011 1.- Conociendo el valor de las constantes de equilibrio para las reacciones individuales, calcule
Guía de ejercicios equilibrio químico Profesor Edwar Fuentes Química Analítica I Semestre primavera 2011 1.- Conociendo el valor de las constantes de equilibrio para las reacciones individuales, calcule
Reacciones de transferencia de electrones
 DEPARTAMENTO DE FÍSICA Y QUÍMICA PROFESOR: LUIS RUIZ MARTÍN QUÍMICA 2º DE BACHILLERATO Actividades tema 8 Reacciones de transferencia de electrones Reacciones de oxidación-reducción 1.-Asigna el número
DEPARTAMENTO DE FÍSICA Y QUÍMICA PROFESOR: LUIS RUIZ MARTÍN QUÍMICA 2º DE BACHILLERATO Actividades tema 8 Reacciones de transferencia de electrones Reacciones de oxidación-reducción 1.-Asigna el número
PROSPECCIÓN GEOQUÍMICA. Tipo de muestras. Detalle y plan de muestreo 08/08/2014
 PROSPECCIÓN GEOQUÍMICA Definición: es la disciplina que emplea los principios de distribución y evolución de los elementos en los ciclos endógenos y exógenos para aplicarlos a la ubicación y exploración
PROSPECCIÓN GEOQUÍMICA Definición: es la disciplina que emplea los principios de distribución y evolución de los elementos en los ciclos endógenos y exógenos para aplicarlos a la ubicación y exploración
EL DRENAJE ÁCIDO DE MINA: CRITERIOS DE
 Segundo Curso sobre Soluciones a la Contaminación de Suelos y Acuíferos EL DRENAJE ÁCIDO DE MINA: CRITERIOS DE MANEJO PARA PREVENIR LA AFECTACIÓN DE ACUÍFEROS José Enrique Santos Jallath Departamento de
Segundo Curso sobre Soluciones a la Contaminación de Suelos y Acuíferos EL DRENAJE ÁCIDO DE MINA: CRITERIOS DE MANEJO PARA PREVENIR LA AFECTACIÓN DE ACUÍFEROS José Enrique Santos Jallath Departamento de
TRATAMIENTO DE AGUAS RESIDUALES SECTOR CERÁMICO. JORNADA DEMOSTRACIÓN PRÁCITCA DE TL s
 TRATAMIENTO DE AGUAS RESIDUALES SECTOR CERÁMICO JORNADA DEMOSTRACIÓN PRÁCITCA DE TL s ÍNDICE INTRODUCCIÓN CANON DE SANEAMIENTO CLASIFICACIÓN POR SUBSECTORES RESIDUALES INDUSTRIALES RESIDUALES SANITARIAS
TRATAMIENTO DE AGUAS RESIDUALES SECTOR CERÁMICO JORNADA DEMOSTRACIÓN PRÁCITCA DE TL s ÍNDICE INTRODUCCIÓN CANON DE SANEAMIENTO CLASIFICACIÓN POR SUBSECTORES RESIDUALES INDUSTRIALES RESIDUALES SANITARIAS
4.2. Una solución saturada de BaF 2 es 7, M, cuál es el producto de solubilidad del BaF 2?
 240 4.1. Escriba la expresión de la constante del producto de solubilidad para cada uno de los siguientes compuestos: (a) CdS; (b) CeF 3 ; (c) Fe 3 (AsO 4 ) 2 ; (d) Ce(OH) 4. 4.2. Una solución saturada
240 4.1. Escriba la expresión de la constante del producto de solubilidad para cada uno de los siguientes compuestos: (a) CdS; (b) CeF 3 ; (c) Fe 3 (AsO 4 ) 2 ; (d) Ce(OH) 4. 4.2. Una solución saturada
Gases disueltos en el agua. Oxígeno disuelto
 Gases disueltos en el agua Oxígeno disuelto Se adiciona libremente de la atmósfera Producto de la fotosíntesis 1 Importancia Respiración Regula el metabolismo dentro del cuerpo de agua Descomposición de
Gases disueltos en el agua Oxígeno disuelto Se adiciona libremente de la atmósfera Producto de la fotosíntesis 1 Importancia Respiración Regula el metabolismo dentro del cuerpo de agua Descomposición de
DISOLUCIÓN Y PRECIPITACIÓN DE SALES CAPITULO V. 5.1. Solubilidad 5.2. Disolución de compuestos poco solubles. 5.3. Precipitación Fraccionada
 CAPITULO V DISOLUCIÓN Y PRECIPITACIÓN DE SALES 5.1. Solubilidad 5.2. Disolución de compuestos poco solubles. 5.3. Precipitación Fraccionada El fenómeno de precipitación, así como el de disolución de precipitados
CAPITULO V DISOLUCIÓN Y PRECIPITACIÓN DE SALES 5.1. Solubilidad 5.2. Disolución de compuestos poco solubles. 5.3. Precipitación Fraccionada El fenómeno de precipitación, así como el de disolución de precipitados
ÁCIDOS Y BASES: DEFINICIÓN Y DISOLUCIONES. CONCEPTO DE ph.
 UNIDAD 4 PROCESOS DE EQUILIBRIO ÁCIDOS Y BASES: DEFINICIÓN Y DISOLUCIONES. CONCEPTO DE ph. Un ácido es una sustancia que, al ser añadida al agua, produce iones hidrógeno (H + ) /hidronio (H 3 O + ). Una
UNIDAD 4 PROCESOS DE EQUILIBRIO ÁCIDOS Y BASES: DEFINICIÓN Y DISOLUCIONES. CONCEPTO DE ph. Un ácido es una sustancia que, al ser añadida al agua, produce iones hidrógeno (H + ) /hidronio (H 3 O + ). Una
NOTA CALI/ORDEN/PRES ORTOGRAFÍA PUNTUACIÓN EXPRESIÓN NOTA FINAL
 1.- Formule o nombre los compuestos siguientes: a) Nitrito de escandio b) Peróxido de plata c) Ácido 2-hidroxiprop-2-enoico d) NH 4 H 2 PO 4 e) Y(CN) 3 f) C H 2 =CHCON(CH 3 ) 2 Res. a) Sc(NO 2 ) 3 ; b)
1.- Formule o nombre los compuestos siguientes: a) Nitrito de escandio b) Peróxido de plata c) Ácido 2-hidroxiprop-2-enoico d) NH 4 H 2 PO 4 e) Y(CN) 3 f) C H 2 =CHCON(CH 3 ) 2 Res. a) Sc(NO 2 ) 3 ; b)
Anexo E-1. Glosario de Términos
 Anexo E-1 Glosario de Términos Glosario de Términos de Suelos ACIDEZ CAMBIABLE: Es el porcentaje de la CIC de los cationes ácidos (aluminio más hidrógeno) retenidos en los coloides. AREAS MISCELANEAS:
Anexo E-1 Glosario de Términos Glosario de Términos de Suelos ACIDEZ CAMBIABLE: Es el porcentaje de la CIC de los cationes ácidos (aluminio más hidrógeno) retenidos en los coloides. AREAS MISCELANEAS:
Tema 7: Equilibrio en fase acuosa. Reacciones de precipitación
 Tema 7: Equilibrio en fase acuosa. Reacciones de precipitación 7.1 Introducción 7.2 El producto de solubilidad 7.3 Solubilidad y solubilidad molar 7.4 Reglas de solubilidad 7.5 Precipitación selectiva
Tema 7: Equilibrio en fase acuosa. Reacciones de precipitación 7.1 Introducción 7.2 El producto de solubilidad 7.3 Solubilidad y solubilidad molar 7.4 Reglas de solubilidad 7.5 Precipitación selectiva
QUÍMICA GENERAL E INORGÁNICA QUÍMICA GENERAL REACCIONES QUÍMICAS Y ESTEQUIOMETRÍA
 QUÍMICA GENERAL E INORGÁNICA QUÍMICA GENERAL REACCIONES QUÍMICAS Y ESTEQUIOMETRÍA 2016 Equipo docente: Profesora Titular: Dra. Graciela Valente Profesora Adjunta: Dra. Cecilia Medaura Jefes de Trabajos
QUÍMICA GENERAL E INORGÁNICA QUÍMICA GENERAL REACCIONES QUÍMICAS Y ESTEQUIOMETRÍA 2016 Equipo docente: Profesora Titular: Dra. Graciela Valente Profesora Adjunta: Dra. Cecilia Medaura Jefes de Trabajos
XXII OLIMPIADA DE QUÍMICA OLIMPIADA LOCAL 2009 Logroño 20 de Febrero
 XXII OLIMPIADA DE QUÍMICA OLIMPIADA LOCAL 2009 Logroño 20 de Febrero INSTRUCCIONES A. La duración de la prueba será de 2 horas. B. Conteste en la Hoja de Respuestas. C. Sólo hay una respuesta correcta
XXII OLIMPIADA DE QUÍMICA OLIMPIADA LOCAL 2009 Logroño 20 de Febrero INSTRUCCIONES A. La duración de la prueba será de 2 horas. B. Conteste en la Hoja de Respuestas. C. Sólo hay una respuesta correcta
Para los estudios de lixiviación se trabajó con un de mineral de gossan, molido a un 65% inferior a 40µm, cuya composición se da en la tabla 63.
 III. Resultados y discusión 21 III.7. TRATAMIENTO DE UN MINERAL DE ORO Como ejemplo de un mineral de oro oxidado, se trabajó con gossan procedente de la mina de Río Tinto (Huelva). Estudios de caracterización
III. Resultados y discusión 21 III.7. TRATAMIENTO DE UN MINERAL DE ORO Como ejemplo de un mineral de oro oxidado, se trabajó con gossan procedente de la mina de Río Tinto (Huelva). Estudios de caracterización
OPCIÓN A. S = 4 = 4, moles L 1.
 OPCIÓN A CUESTIÓN 1.- a) Razona con los correspondientes equilibrios en disolución acuosa si las siguientes especies tienen carácter ácido, básico o anfótero: ion hidrogenocarbonato, ion hidrogenosulfuro
OPCIÓN A CUESTIÓN 1.- a) Razona con los correspondientes equilibrios en disolución acuosa si las siguientes especies tienen carácter ácido, básico o anfótero: ion hidrogenocarbonato, ion hidrogenosulfuro
El hidróxido de magnesio es una sustancia ligeramente soluble en agua. El ph de una disolución saturada de dicho hidróxido es de 10,38.
 Calcula la solubilidad en g/l del fosfato de plomo (II) sabiendo que su producto de solubilidad es 1,5.10-32. Datos: Pb = 207,2; P = 31; O = 16. Sol: 1,37.10-11 g/l. Sabiendo que la solubilidad en g/l
Calcula la solubilidad en g/l del fosfato de plomo (II) sabiendo que su producto de solubilidad es 1,5.10-32. Datos: Pb = 207,2; P = 31; O = 16. Sol: 1,37.10-11 g/l. Sabiendo que la solubilidad en g/l
OBJETIVOS. b) Comprender las caracterizaciones de una mezcla compleja de iones en solución
 OBJETIVOS a) Comprender las marchas analíticas b) Comprender las caracterizaciones de una mezcla compleja de iones en solución c) Saber como tratar las muestras con reactivos que separen los iones en grupos,
OBJETIVOS a) Comprender las marchas analíticas b) Comprender las caracterizaciones de una mezcla compleja de iones en solución c) Saber como tratar las muestras con reactivos que separen los iones en grupos,
Índice de Calidad del Agua. María Soledad Novillo Bustos
 Índice de Calidad del Agua María Soledad Novillo Bustos ICA El Índice de Calidad del Agua indica el grado de contaminación del agua. Está expresado como porcentaje del agua pura. El agua altamente contaminada
Índice de Calidad del Agua María Soledad Novillo Bustos ICA El Índice de Calidad del Agua indica el grado de contaminación del agua. Está expresado como porcentaje del agua pura. El agua altamente contaminada
Física y Química 4º ESO: guía interactiva para la resolución de ejercicios
 REACCIONES QUÍMICAS Oxidación reducción. Pilas Física y Química º ESO: guía interactiva para la resolución de ejercicios I.E.S. Élaios Departamento de Física y Química EJERCICIO 1 Indica cuáles de las
REACCIONES QUÍMICAS Oxidación reducción. Pilas Física y Química º ESO: guía interactiva para la resolución de ejercicios I.E.S. Élaios Departamento de Física y Química EJERCICIO 1 Indica cuáles de las
TRABAJO PRÁCTICO N 9 ÓXIDO-REDUCCIÓN
 TRABAJO PRÁCTICO N 9 ÓXIDO-REDUCCIÓN Las reacciones químicas de óxido - reducción (reacciones redox) son aquellas en las cuales se produce una transferencia de electrones. Son las reacciones donde se producen
TRABAJO PRÁCTICO N 9 ÓXIDO-REDUCCIÓN Las reacciones químicas de óxido - reducción (reacciones redox) son aquellas en las cuales se produce una transferencia de electrones. Son las reacciones donde se producen
UTILIZACIÓN DE LODOS DE LA INDUSTRIA DEL MÁRMOL COMO ESTABILIZANTES DE METALES PESADOS EN SUELOS CONTAMINADOS
 UTILIZACIÓN DE LODOS DE LA INDUSTRIA DEL MÁRMOL COMO ESTABILIZANTES DE METALES PESADOS EN SUELOS CONTAMINADOS Jorge Marimón Santos Grupo de Investigación de Contaminación de Suelos Universidad de Murcia.
UTILIZACIÓN DE LODOS DE LA INDUSTRIA DEL MÁRMOL COMO ESTABILIZANTES DE METALES PESADOS EN SUELOS CONTAMINADOS Jorge Marimón Santos Grupo de Investigación de Contaminación de Suelos Universidad de Murcia.
IES Atenea (S.S. de los Reyes) Departamento de Física y Química. PAU Química. Septiembre 2006 PRIMERA PARTE
 1 PAU Química. Septiembre 2006 PRIMERA PARTE Cuestión 1. La configuración electrónica del último nivel energético de un elemento es 4s 2 4p 3. De acuerdo con este dato: a) Deduzca la situación de dicho
1 PAU Química. Septiembre 2006 PRIMERA PARTE Cuestión 1. La configuración electrónica del último nivel energético de un elemento es 4s 2 4p 3. De acuerdo con este dato: a) Deduzca la situación de dicho
UNIVERSIDADES PÚBLICAS DE LA COMUNIDAD DE MADRID PRUEBA DE ACCESO A LAS ENSEÑANZAS UNIVERSITARIAS OFICIALES DE GRADO
 UNIVERSIDADES PÚBLICAS DE LA COMUNIDAD DE MADRID PRUEBA DE ACCESO A LAS ENSEÑANZAS UNIVERSITARIAS OFICIALES DE GRADO MATERIA: QUÍMICA Curso 2009-2010 INSTRUCCIONES Y CRITERIOS GENERALES DE CALIFICACIÓN
UNIVERSIDADES PÚBLICAS DE LA COMUNIDAD DE MADRID PRUEBA DE ACCESO A LAS ENSEÑANZAS UNIVERSITARIAS OFICIALES DE GRADO MATERIA: QUÍMICA Curso 2009-2010 INSTRUCCIONES Y CRITERIOS GENERALES DE CALIFICACIÓN
