RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO
|
|
|
- Ángel Toro Segura
- hace 8 años
- Vistas:
Transcripción
1 RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1. NOMBRE DEL MEDICAMENTO Xomolix 2,5 mg/ml solución inyectable 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada mililitro de la solución contiene 2,5 mg de droperidol. Excipientes: sodio, < 23 mg por ml. Para consultar la lista completa de excipientes, ver sección FORMA FARMACÉUTICA Solución inyectable. Solución transparente e incolora, con ausencia de partículas visibles. El ph de la solución de droperidol inyectable es 3,0 3,8 y tiene una osmolaridad de aproximadamente 300 miliosmol/ kg de agua. 4. DATOS CLÍNICOS 4.1 Indicaciones terapéuticas Prevención y tratamiento de nauseas y vómitos post-operatorios en adultos y, de segunda línea, en niños y adolescentes. Prevención de nauseas y vómitos inducidos por los derivados de la morfina, durante la analgesia controlada por el paciente (PCA), en adultos. Hay que tomar ciertas precauciones al administrar droperidol: ver secciones 4.2, 4.3 y Posología y forma de administración Para uso intravenoso. Prevención y tratamiento de nauseas y vómitos post-operatorios (PONV). Adultos: 0,625 mg a 1,25 mg (0,25 a 0,5 ml). Ancianos: 0,625 mg (0,25 ml) Insuficiencia renal/hepática: 0,625 mg (0,25 ml) Niños (mayores de 2 años) y adolescentes: 20 a 50 microgramos/kg (hasta un máximo de 1,25 mg). Niños (menores de 2 años): no recomendado Se recomienda administrar droperidol 30 minutos antes de la hora en la que se espera que finalice la cirugía. Se puede repetir la dosis cada 6 horas según sea necesario. CORREO ELECTRÓNICO Sugerencias_ft@aemps.es C/ CAMPEZO, 1 EDIFICIO MADRID
2 La dosis se debe adaptar a cada caso individual. Los factores a tener en cuenta para ello incluyen la edad, el peso corporal, la medicación concomitante, tipo de anestesia y procedimiento quirúrgico. Prevención de nauseas y vómitos inducidos por derivados de la morfina durante la analgesia controlada por el paciente (PCA) en el postoperatorio. Adultos: de 15 a 50 microgramos de droperidol por cada mg de morfina, hasta una dosis máxima diaria de 5 mg de droperidol. Ancianos, y pacientes con insuficiencia renal y hepática: no hay datos disponibles en PCA. Niños (con edad superior a los 2 años) y adolescentes: no indicado en PCA. Una oximetría de pulso continua se deberá llevar a cabo en pacientes con sospecha o con riesgo identificado de arritmia ventricular y se deberá continuar durante 30 minutos tras la administración intravenosa. Para instrucciones sobre la disolución del producto antes de la administración, ver sección 6.6. Ver también secciones 4.3, 4.4 y Contraindicaciones El droperidol está contraindicado en pacientes con: Hipersensibilidad al droperidol o a alguno de los excipientes; Hipersensibilidad a las butirofenonas; Conocimiento o sospecha de prolongación del intervalo QT (QTc de > 450 ms en mujeres y > 440 ms en hombres). Esto incluye pacientes con prolongación congénita del intervalo QT, pacientes que tengan historia familiar de prolongación congénita del QT y aquellos tratados con medicamentos que se conozca que prolongan el intervalo QT (ver sección 4.5); Hipokalemia, hipomagnesemia; Bradicardia (< 55 latidos por minuto); Tratamiento concomitante que provoque bradicardia; Feocromocitoma; Estados comatosos; Enfermedad de Parkinson; Depresión severa. 4.4 Advertencias y precauciones especiales para su utilización Sistema Nervioso Central El droperidol puede aumentar la depresión del SNC producida por otros medicamentos depresores del SNC. Cualquier paciente sujeto a anestesia y recibiendo medicamentos depresores del SNC potentes o que muestren síntomas de depresión del SNC deberían ser estrictamente monitorizados. El uso concomitante de metoclopramida y otros neurolépticos puede llevar a un aumento de los síntomas extrapiramidales y debe ser evitado. (ver sección 4.5). Debe utilizarse con cuidado en pacientes con epilepsia (o con antecedentes de epilepsia) y en condiciones que predispongan a la epilepsia o a las convulsiones.
3 Cardiovascular Se ha observado hipotensión leve a moderada y, ocasionalmente, taquicardia (refleja) tras la administración de droperidol. Esta reacción generalmente remite espontáneamente. Sin embargo, si persistiese la hipotensión, se debe considerar la posibilidad de la presentación de un estado hipovolémico en cuyo caso deberá considerarse una adecuada reposición de líquidos. Los pacientes que tengan, o que se sospeche que puedan tener, los siguientes factores de riesgo de arritmia cardiaca deberán ser evaluados cuidadosamente antes de administrarles droperidol: Historia previa de enfermedad cardiaca importante incluyendo arritmia ventricular grave, bloqueo auriculo-ventricular de segundo o tercer grado, disfunción del nodo sinusal, insuficiencia cardiaca congestiva, cardiopatía isquémica e hipertrofia ventricular izquierda; Historia familiar de muerte súbita; Insuficiencia renal (particularmente con diálisis crónica); Enfermedad pulmonar obstructiva crónica significativa e insuficiencia respiratoria; Factores de riesgo de alteraciones electrolíticas, como sería el caso de pacientes que toman laxantes, glucocorticoides, diuréticos que inducen pérdida de potasio, asociada a la administración de insulina en casos agudos, o en pacientes con vómitos o diarrea prolongados. En los pacientes con riesgo de arritmia cardiaca se deben tener controlados los niveles de electrolitos y de creatinina sérica y se debe excluir la presencia de prolongación del intervalo QT antes de la administración de droperidol. Una oximetría de pulso continua se deberá llevar a cabo en pacientes con sospecha o con riesgo identificado de arritmia ventricular y se deberá continuar durante 30 minutos tras la administración intravenosa General Para prevenir la prolongación del intervalo QT, es necesario tener cuidado cuando los pacientes estén tomando medicamentos que puedan causar desequilibrio electrolítico (hipokalemia y/o hipomagnesemia), como por ejemplo diuréticos que inducen pérdida de potasio, laxantes y glucocorticoides. Las sustancias inhibidoras de la actividad de las isoenzimas del citocromo P450 (CYP) CYP1A2, CYP3A4 o ambas, pueden disminuir el grado de metabolización del droperidol y prolongar su acción farmacológica. Por eso se recomienda tener cuidado al administrar droperidol junto con inhibidores potentes de CYP1A2 y CYP3A4 (ver sección 4.5). Los pacientes que tengan, o se sospeche que puedan tener, historia de alcoholismo o que hayan consumido recientemente grandes cantidades de alcohol deben ser examinados minuciosamente antes de la administración de droperidol. En caso de hipertermia inexplicable, es esencial interrumpir el tratamiento, ya que puede ser señal de uno de los síntomas de síndrome neuroléptico maligno notificado con el uso de neurolépticos. La dosis debe reducirse en ancianos y en aquellos con insuficiencia renal y/o hepática (ver sección 4.2). Este medicamento contiene menos de 1 mmol de sodio (23 mg) por 1 ml, esto es, esencialmente exento de sodio. 4.5 Interacción con otros otras formas de interacción Contraindicado su uso concomitante Los medicamentos que se conozca que prolongan el intervalo QTc no deben administrarse
4 simultáneamente con droperidol. Ejemplos incluyen algunos antiarrítmicos, tales como los de Clase IA (por ejemplo quinidina, disopiramida, procainamida) y los de Clase III (por ejemplo amiodarona, sotalol); antibióticos macrólidos (por ejemplo azitromicina, eritromicina, claritromicina), antibióticos del grupo de las fluoroquinolonas (por ejemplo esparfloxacino); ciertos antihistamínicos (por ejemplo astemizol, terfenadina); antidepresivos tricíclicos (por ejemplo amitriptilina); ciertos antidepresivos tetracíclicos (por ejemplo maprotilina); ciertos medicamentos antipsicóticos (por ejemplo amisulpirida, clorpromazina, haloperidol, melperona, fenotiazinas, pimozida, sulpiride, sertindol, tiaprida); inhibidores de la recaptación de serotonina (por ejemplo fluoxetina, sertralina, fluvoxamina); agentes antimaláricos (por ejemplo quinina, cloroquina, halofantrina); cisaprida, pentamidina, tracrolimus, tamoxifeno, y vincamina. El uso concomitante de medicamentos que inducen síntomas extrapiramidales, por ejemplo metoclopramida y otros neurolépicos, puede llevar a un aumento en la incidencia de estos síntomas y por consiguiente debe ser evitado. Debe evitarse el consumo de bebidas alcohólicas. Se recomienda precaución para su uso concomitante Para prevenir la prolongación del intervalo QT, es necesario tener cuidado cuando los pacientes estén tomando medicamentos que puedan inducir un desequilibrio electrolítico (Hipokalemia y/o hipomagnasemia) por ejemplo diuréticos ahorradores de potasio, laxantes y glucocorticoides. El droperidol puede potenciar la acción de los sedantes (barbitúricos, benzodiazepinas, derivados de la morfina). Lo mismo aplica a los agentes antihipertensivos, ya que puede provocar hipotensión ortostática. Al igual que otros sedantes, el droperidol puede potenciar la depresión respiratoria causada por los opioides. Debido a que el droperidol bloquea los receptores de dopamina, puede inhibir la acción de los agonistas de la dopamina, tales como la bromocriptina, el lisuride y la L-dopa. Las sustancias inhibidoras de la actividad de las isoenzimas del citocromo P450 (CYP) CYP1A2, CYP3A4 o ambas pueden disminuir el grado de metabolización del droperidol y prolongar su acción farmacológica. Por eso, se recomienda tener cuidado al administrar droperidol junto con inhibidores de CYP1A2 (por ejemplo ciprofloxacino, ticlopidina), inhibidores de CYP3A4 (por ejemplo diltiazem, eritromicina, fluconazol, indinavir, itraconazol, ketoconazol, nefazodona, nelfinavir, ritonavir, saquinavir, verapamilo) o ambos (por ejemplo cimetidina, mibefradilo). 4.6 Embarazo y lactancia Embarazo En un estudio prospectivo, 80 pacientes que sufrían hiperemesis gravídica recibieron dosis altas de droperidol (media de 1 mg/h en un periodo de 50 h) para controlar las náuseas y vómitos. La edad gestacional al nacer, peso medio al nacer, incidencia de partos prematuros, e incidencia de corta edad gestacional son comparables al del grupo utilizado como control histórico. Otro estudio, en el que 28 pacientes recibieron 1 mg de droperidol cada hora durante 40 horas de media, no mostró diferencias estadísticamente significativas entre el grupo de tratamiento y los grupos de control histórico en la incidencia de abortos espontáneos, abortos de elección, puntuaciones en la escala de Apgar, edad gestacional al nacer y peso al nacer. No se ha visto que el droperidol sea teratogénico en ratas. Los estudios en animales son insuficientes para determinar las reacciones en el embarazo y desarrollo embrional/fetal, parto y desarrollo postnatal.
5 En niños recién nacidos de madres bajo tratamiento continuado y con altas dosis de neurolépticos, se han descrito alteraciones neurológicas temporales de naturaleza extrapiramidal. En la práctica, como medida preventiva, es preferible no administrar droperidol durante el embarazo. En la fase final del embarazo, si fuese necesaria su administración, se recomienda un control de las funciones neurológicas del recién nacido. Lactancia Es sabido que los neurolépticos del tipo butirofenona se excretan en la leche materna; el tratamiento con droperidol debe limitarse a una única administración. No se recomienda la administración repetida de este medicamento. 4.7 Efectos sobre la capacidad para conducir y utilizar máquinas La influencia de droperidol sobre la capacidad para conducir y utilizar máquinas es importante. Los pacientes no deben conducir ni manejar máquinas durante las 24 horas siguientes a la administración de droperidol. 4.8 Reacciones adversas Las reacciones adveras notificadas con mayor frecuencia durante la experiencia clínica fueron casos de somnolencia y sedación. Además se han notificado con menor frecuencia casos de hipotensión, arritmias cardíacas, síndrome neuroléptico maligno (SNM) y síntomas asociados con el SNM, trastornos de movimientos, tales como discinesias, además de casos de ansiedad o agitación. Clasificación de órganos del sistema Trastornos de la sangre y del sistema linfático Frecuentes ( 1/100, < 1/10 ) Poco frecuentes ( 1/1.000, < 1/100 ) Raras ( 1/10.000, < 1/1.000) Muy raras (< 1/10.000) Discrasias sanguíneas Frecuencia no conocida (no puede estimarse a partir de los datos disponibles) Trastornos del sistema inmunológico Reacción anafiláctica; Edema angioneurótico; Hipersensibilidad Trastornos del metabolismo y de la nutrición Trastornos psiquiátricos Ansiedad; Agitación/acatisi a Estados de confusión; Agitación Disforia Secreción inapropiada de la hormona antidiurética Alucinaciones
6 Trastornos del sistema nervioso Somnolencia Distonía; Crisis oculógiras Alteracione s extrapiramidales; Convulsion es; Temblor Crisis epilépticas; Enfermedad de Parkinson; Hiperactividad psicomotora; Coma Trastornos cardíacos Trastornos vasculares Hipotensión Taquicardia; Mareos Arritmias cardíacas, incluyendo arritmias ventriculares Paro cardíaco Torsade de pointes; Prolongación electrocardiográfi ca del intervalo QT Síncope Trastornos respiratorios, torácicos y mediastínicos Broncoespasmo; Laringoespasmo Trastornos de la piel y del tejido subcutáneo Erupción cutánea Trastornos generales y alteraciones en el lugar de administración Síndrome neuroléptico maligno (SNM) Muerte súbita Ocasionalmente, se han notificado síntomas potencialmente asociados con el SNM por ejemplo cambios en la temperatura corporal, rigidez y fiebre. Se ha observado alteración en el estado mental con confusión o agitación y alteraciones de la conciencia. La inestabilidad autonómica se puede manifestar como taquicardia, fluctuaciones de la presión arterial, transpiración excesiva/salivación y temblores. En casos extremos, el SNM puede conducir al coma o a trastornos renales y/o hepato-biliares Casos aislados de amenorrea, galactorrea, ginecomastia, hiperprolactinemia y oligomenorrea se han asociado con la exposición prolongada en indicaciones psiquiátricas. 4.9 Sobredosis Síntomas Las manifestaciones de la sobredosis con droperidol constituyen una extensión de sus acciones farmacológicas. Los síntomas de una sobredosis accidental son la indiferencia psíquica con una transición hasta el sueño, a veces asociados a un descenso de la tensión arterial. En dosis mayores o en pacientes sensibles, pueden tener lugar desórdenes extrapiramidales (salivación, movimientos anormales, a veces rigidez muscular). Pueden ocurrir convulsiones en dosis tóxicas. Raras veces se han notificado casos de prolongación del intervalo QT, arritmia ventricular y muerte súbita. Tratamiento No se conoce un antídoto específico. Sin embargo, cuando ocurren reacciones extrapiramidales, se debe administrar un anticolinérgico.
7 Los pacientes con sobredosis de droperidol deben ser estrechamente monitorizados para controlar que no existan signos de prolongación del intervalo QT. Factores que predisponen a las torsades de pointes, por ejemplo alteraciones electrolíticas (especialmente hipokalemia o hipomagnesemia) y bradicardia deben ser tenidos en cuenta. La hipotensión pronunciada se debe tratar estimulando el volumen circulatorio y tomando otras medidas apropiadas. Se deben mantener las vías respiratorias despejadas y una oxigenación adecuada; puede ser necesaria una vía respiratoria orofaríngea o un tubo endotraqueal. Si se requiere, el paciente debe ser observado cuidadosamente 24 horas o más; se deben mantener el calor corporal y un adecuado aporte de líquidos. 5. PROPIEDADES FARMACÓLOGICAS 5.1 Propiedades farmacodinámicas Grupo farmacoterapéutico: Derivados de la butirofenona, Código ATC: N05AD08 El droperidol es una butirofenona neuroléptica. Su perfil farmacológico se caracteriza principalmente por efectos bloqueante dopaminérgico y α - adrenolítico débil. El droperidol carece de actividad 1 anticolinérgica y antihistamínica. La acción inhibidora del droperidol sobre los receptores dopaminérgicos en la zona gatillo quimiorreceptora en el área postrema, proporciona un potente efecto antiemético, especialmente útil para la prevención y el tratamiento de náuseas y vómitos post-operatorios y/o inducidos por analgésicos opioides. A una dosis de 0,15 mg/kg, el droperidol induce una caída en la tensión arterial media (TAM) debido a una disminución del gasto cardíaco en una primera fase, y posteriormente a causa de una disminución en la pre-carga. Estos cambios ocurren independientemente a cualquier alteración en la contractilidad miocárdica o resistencia vascular. El droperidol no afecta la contractilidad miocárdica o el ritmo cardíaco, por consiguiente no causa efecto inotrópico negativo. Su efecto bloqueante α - adrenérgico débil puede 1 causar una hipotensión moderada y una disminución en la resistencia vascular periférica y puede reducir la presión arterial pulmonar (particularmente si se encuentra anormalmente elevada). También puede reducir la incidencia de la arritmia inducida por epinefrina, pero no previene otras formas de arritmia cardíaca. El droperidol produce un efecto antiarrítmico en particular a una dosis de 0,2 mg/kg por medio de un efecto en la contractilidad miocárdica (prolongación del período refractario) y una disminución en la presión sanguínea. Dos estudios (uno controlado con placebo y uno comparativo controlado con tratamiento activo) llevados a cabo en el contexto de la anestesia general y diseñados para identificar mejor los cambios del QTc asociados con el tratamiento de náuseas y vómitos post-operatorios por medio de pequeñas dosis de droperidol (0,625 y 1,25 mg intravenosos y 0,75 mg intravenosos respectivamente) identificaron una prolongación del intervalo QT de 3-6 min. trás la administración de 0,625 y 1,25 mg de droperidol (respectivamente 15 ± 40 y 22 ± 41 ms), pero estos cambios no difirieron significativamente si se comparan con aquellos observados con la solución salina (12 ± 35 ms). No se observaron diferencias estadísticamente significativas entre los grupos de droperidol y solución salina en el número de pacientes con una prolongación QTc mayor al 10% con respecto al valor basal. No hubo evidencia de prolongación de QTc inducida por droperidol después de la cirugía. No se notificaron latidos cardíacos ectópicos en los registros electrocardiográficos de 12 derivaciones durante el período periperatorio. El estudio comparativo con tratamiento activo con 0,75 mg de droperidol
8 intravenoso identificó una prolongación significativa del intervalo QTc (máximo de 17 ± 9 ms a los dos minutos de haberse inyectado droperidol cuando se lo comparó con la medición de QTc previa al tratamiento) con el intervalo QTc significativamente menor después del minuto Propiedades farmacocinéticas El efecto de una única dosis intravenosa comienza a los 2-3 minutos de su administración. Los efectos tranquilizantes y sedantes tienden a perdurar de 2 a 4 horas, aunque el estado de alerta puede verse afectado hasta 12 horas. Distribución Después de la administración intravenosa, las concentraciones en plasma disminuyen rápidamente durante los primeros 15 minutos. La unión a proteínas plasmáticas se encuentra entre 85-90%. El volumen de distribución es de aproximadamente 1,5 l/kg. Metabolismo El droperidol es extensamente metabolizado en el hígado y sufre oxidación, desalquilación, desmetilación e hidroxilación por las isoenzimas 1A2 y 3A4 del citocromo P450 y en menor medida por el 2C19. Los metabolitos carecen de actividad neuroléptica. Eliminación La eliminación ocurre principalmente a través del metabolismo; el 75% se elimina por medio de los riñones. Sólo el 1% de la sustancia activa se elimina en forma inalterada con la orina, y el 11% con las heces. El aclaramiento plasmático es del 0,8 (0,4 1,8) l/min. La semivida de eliminación (t ) es de 134 ½ß ± 13 min. 5.3 Datos preclínicos sobre seguridad Los datos de los estudios no-clínicos no muestran riesgos especiales para los seres humanos según los estudios convencionales de toxicidad a dosis repetidas, potencial carcinogénico y toxicidad para la reproducción. El droperidol no resultó ser mutagénico in vitro en un Test de Ames utilizando 5 variedades bacterianas y resultó negativo in vivo por inducción de micronúcleos en la médula espinal de rata, después de una inyección intravenosa. En una prueba in vitro haciendo uso de células L5178Y de linfoma de ratón, no se evidenció actividad mutagénica significativa en ninguno de los dos ensayos independientes sin activación metabólica (-S9), pero se observó un resultado positivo biológicamente significativo en el segundo ensayo con S9. Dentro de esta clase de componentes se han observado resultados conflictivos en estudios informados (haloperidol) y no es posible especificar si el resultado positivo de la mutación genética en el ensayo reciente in vitro llevado a cabo en el linfoma de ratón con droperidol, podría representar un efecto de clase. Los estudios electrofisiológicos de droperidol in vitro e in vivo indican riesgo de prolongación del intervalo QT en humanos. En humanos, el pico de concentración plasmática de droperidol libre estimado arriba, es aproximadamente entre 4 veces mayor y 25 veces menor que las concentraciones de droperidol que afectan a las variables examinadas en los diferentes sistemas de test in vitro e in vivo, utilizados para evaluar el impacto de este fármaco sobre la repolarización cardíaca. Los niveles plasmáticos disminuyen cerca de un orden de magnitud después de los primeros veinte minutos tras la administración. 6. DATOS FARMACÉUTICOS 6.1 Lista de excipientes
9 Manitol Ácido tartárico Hidróxido de sodio (para ajustar el ph) Agua para preparaciones inyectables 6.2 Incompatibilidades Incompatible con los barbitúricos. Este medicamento no debe mezclarse con otros excepto con los mencionados en el epígrafe Periodo de validez Cerrado: 3 años Después de la primera apertura: Para su uso inmediato Después de la dilución: Se ha demostrado la compatibilidad de droperidol con sulfato de morfina en cloruro de sodio al 0,9% (14 días a temperatura ambiente) en jeringuillas de plástico. Desde un punto de vista microbiológico, el producto diluido debe ser utilizado inmediatamente. Si no se utiliza inmediatamente, el tiempo y las condiciones en las que se haya guardado, una vez abierto, antes de ser utilizado, son responsabilidad del usuario y, normalmente, no deben superar las 24 horas a temperatura entre 2 y 8 ºC, a no ser que la disolución se haya conservado en condiciones asépticas validadas y controladas. 6.4 Precauciones especiales de conservación Conservar en el embalaje original. 6.5 Naturaleza y contenido del envase Ampollas de vidrio ámbar tipo I que contienen 1 ml de solución inyectable, en paquetes de 5 y 10 ampollas. Puede que solamente estén comercializados algunos tamaños de envases. 6.6 Precauciones especiales de eliminación y otras manipulaciones Sólo para uso individual. La solución que no se utilice se debe descartar La solución debe inspeccionarse visualmente antes de ser utilizada. Sólo se deben utilizar soluciones transparentes e incoloras, libres de partículas visibles. Para utilizar en la PCA: Extraiga droperidol y morfina con una jeringa y llegue al volumen deseado con 0,9% de cloruro sódico para inyección. La eliminación del medicamento no utilizado y de todos los materiales que hayan estado en contacto con él, se realizará de acuerdo a la normativa local. 7. TITULAR DE LA AUTORIZACIÓN DE COMERCIALIZACIÓN ProStrakan Ltd Galabank Business Park Galashiels TD1 1QH
10 Reino Unido Tel. +44 (0) Fax. +44 (0) Representante local: ProStrakan Farmacéutica, S.L.U. Avda. de Burgos, 17 1ª planta Madrid España 8. NÚMERO(S) DE AUTORIZACIÓN DE COMERCIALIZACIÓN 9. FECHA DE LA PRIMERA AUTORIZACIÓN/RENOVACIÓN DE LA AUTORIZACIÓN Junio FECHA DE REVISIÓN DEL TEXTO
FICHA TÉCNICA. Población pediátrica Niños (2 a 11 años) y adolescentes (12 a 18 años): 10 a 50 microgramos/kg (hasta un máximo de 1,25 mg).
 FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Xomolix 2,5 mg/ml solución inyectable 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada mililitro de la solución contiene 2,5 mg de droperidol. Excipientes: sodio,
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Xomolix 2,5 mg/ml solución inyectable 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada mililitro de la solución contiene 2,5 mg de droperidol. Excipientes: sodio,
RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO
 RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1. NOMBRE DEL MEDICAMENTO Xomolix 2,5 mg/ml solución inyectable 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada mililitro de la solución contiene 2,5 mg de droperidol.
RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1. NOMBRE DEL MEDICAMENTO Xomolix 2,5 mg/ml solución inyectable 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada mililitro de la solución contiene 2,5 mg de droperidol.
FICHA TÉCNICA. Población pediátrica Niños (2 a 11 años) y adolescentes (12 a 18 años): 10 a 50 microgramos/kg (hasta un máximo de 1,25 mg).
 FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Xomolix 2,5 mg/ml solución inyectable 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada mililitro de la solución contiene 2,5 mg de droperidol. Excipientes: sodio,
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Xomolix 2,5 mg/ml solución inyectable 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada mililitro de la solución contiene 2,5 mg de droperidol. Excipientes: sodio,
FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO
 FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1. NOMBRE DEL MEDICAMENTO Lactulosa Level 667,5 mg/ml solución oral 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA 1 mililitro de solución oral contiene
FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1. NOMBRE DEL MEDICAMENTO Lactulosa Level 667,5 mg/ml solución oral 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA 1 mililitro de solución oral contiene
Documento Local del Producto
 1 Documento Local del Producto Título del Documento de Producto: Alprazolam Fecha de CDS que reemplaza: 14 de octubre de 2013 Fecha Efectiva: 12 de diciembre de 2013 Versión CDS: 8.0 1. NOMBRE DEL MEDICAMENTO
1 Documento Local del Producto Título del Documento de Producto: Alprazolam Fecha de CDS que reemplaza: 14 de octubre de 2013 Fecha Efectiva: 12 de diciembre de 2013 Versión CDS: 8.0 1. NOMBRE DEL MEDICAMENTO
RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO
 RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1. NOMBRE DEL MEDICAMENTO Mupirocina ISDIN 20 mg/g pomada 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada gramo de pomada contiene 20 mg de mupirocina. Para consultar
RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1. NOMBRE DEL MEDICAMENTO Mupirocina ISDIN 20 mg/g pomada 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada gramo de pomada contiene 20 mg de mupirocina. Para consultar
PROSPECTO. NOVARTIS FARMACEUTICA, S.A. Ronda Santa Maria, 158. Barbera del Valles 08210 (Barcelona) España
 PROSPECTO Lea todo el prospecto detenidamente antes de que a usted o a su hijo le sea administrado Lioresal por vía intratecal, ya que contiene información importante. Conserve este prospecto. Puede tener
PROSPECTO Lea todo el prospecto detenidamente antes de que a usted o a su hijo le sea administrado Lioresal por vía intratecal, ya que contiene información importante. Conserve este prospecto. Puede tener
PROYECTO DE PROSPECTO. ORAP Forte PIMOZIDA. Comprimidos 4 mg. Venta bajo receta archivada Industria Portuguesa
 PROYECTO DE PROSPECTO ORAP Forte PIMOZIDA Comprimidos 4 mg Venta bajo receta archivada Lista IV Industria Portuguesa FÓRMULA CUALI-CUANTITATIVA: Cada comprimido contiene: Pimozida 4,00 mg Excipientes:
PROYECTO DE PROSPECTO ORAP Forte PIMOZIDA Comprimidos 4 mg Venta bajo receta archivada Lista IV Industria Portuguesa FÓRMULA CUALI-CUANTITATIVA: Cada comprimido contiene: Pimozida 4,00 mg Excipientes:
ARIPIPRAZOL En adolescentes contrastorno Bipolar I
 ARIPIPRAZOL En adolescentes contrastorno Bipolar I Información para profesionales sanitarios Preguntas frecuentes Disponible en la web de la AEMPS www.aemps.gob.es Información sobre prevención de riesgos
ARIPIPRAZOL En adolescentes contrastorno Bipolar I Información para profesionales sanitarios Preguntas frecuentes Disponible en la web de la AEMPS www.aemps.gob.es Información sobre prevención de riesgos
FICHA TÉCNICA. HIDROCLORURO DE FENILEFRINA GENFARMA 10 mg/ml, Solución inyectable.
 FICHA TÉCNICA NOMBRE DEL MEDICAMENTO HIDROCLORURO DE FENILEFRINA GENFARMA 10 mg/ml, Solución inyectable. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada ml contiene: Fenilefrina (D.O.E.) hidrocloruro 10 mg.
FICHA TÉCNICA NOMBRE DEL MEDICAMENTO HIDROCLORURO DE FENILEFRINA GENFARMA 10 mg/ml, Solución inyectable. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada ml contiene: Fenilefrina (D.O.E.) hidrocloruro 10 mg.
PROSPECTO: INFORMACIÓN PARA EL USUARIO. Xomolix 2,5 mg/ml solución inyectable Droperidol
 PROSPECTO: INFORMACIÓN PARA EL USUARIO Xomolix 2,5 mg/ml solución inyectable Droperidol Lea todo el prospecto detenidamente antes de empezar a usar este medicamento, porque contiene información importante
PROSPECTO: INFORMACIÓN PARA EL USUARIO Xomolix 2,5 mg/ml solución inyectable Droperidol Lea todo el prospecto detenidamente antes de empezar a usar este medicamento, porque contiene información importante
Pacientes de edad avanzada: debe considerarse la conveniencia de ampliar el intervalo de dosificación (Ver Propiedades Famacocinéticas).
 FT290191-B+2 1. NOMBRE DEL MEDICAMENTO DARVON 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Dextropropoxifeno (D.C.I.) napsilato 100 mg. 3. FORMA FARMACÉUTICA Cápsulas para administración por vía oral. 4.
FT290191-B+2 1. NOMBRE DEL MEDICAMENTO DARVON 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Dextropropoxifeno (D.C.I.) napsilato 100 mg. 3. FORMA FARMACÉUTICA Cápsulas para administración por vía oral. 4.
FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO
 FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1. NOMBRE DEL MEDICAMENTO Ginkokán 40 mg comprimidos Extracto de Ginkgo biloba EGb 761 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada comprimido
FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1. NOMBRE DEL MEDICAMENTO Ginkokán 40 mg comprimidos Extracto de Ginkgo biloba EGb 761 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada comprimido
Antihiperkalémico - Antihipermagnesémico. Composición. Cada 10 ml de solución contiene: Gluconato de Calcio 1.0 g. Excipientes:
 Antihiperkalémico - Antihipermagnesémico. Composición Cada 10 ml de solución contiene: Gluconato de Calcio 1.0 g Excipientes: 1 / 21 Sacarato de calcio agua para inyectables c.s. Proporciona: Calcio 0.465
Antihiperkalémico - Antihipermagnesémico. Composición Cada 10 ml de solución contiene: Gluconato de Calcio 1.0 g Excipientes: 1 / 21 Sacarato de calcio agua para inyectables c.s. Proporciona: Calcio 0.465
THIPENTHAL. TIOPENTAL SÓDICO 1 g INYECTABLE. VENTA BAJO RECETA ARCHIVADA (Lista III) FÓRMULA CUALI Y CUANTITATIVA. Cada frasco ampolla contiene:
 THIPENTHAL TIOPENTALSÓDICO1g INYECTABLE VENTABAJORECETAARCHIVADA(ListaIII) FÓRMULACUALIYCUANTITATIVA Cadafrascoampollacontiene: Tiopentalsódicoestéril 1g ACCIÓNTERAPÉUTICA: Anestésicogeneral,barbitúrico.CódigoATC:N01AF03.
THIPENTHAL TIOPENTALSÓDICO1g INYECTABLE VENTABAJORECETAARCHIVADA(ListaIII) FÓRMULACUALIYCUANTITATIVA Cadafrascoampollacontiene: Tiopentalsódicoestéril 1g ACCIÓNTERAPÉUTICA: Anestésicogeneral,barbitúrico.CódigoATC:N01AF03.
Escrito por Dra. Cristina Gisbert Garzón Lunes 17 de Febrero de :00 - Ultima actualización Miércoles 12 de Febrero de :18
 La muerte súbita cardíaca es una de las causas más comunes de muerte cardiovascular en los países desarrollados. En su mayor parte, se producen por una arritmia ventricular aguda, precedida de alteraciones
La muerte súbita cardíaca es una de las causas más comunes de muerte cardiovascular en los países desarrollados. En su mayor parte, se producen por una arritmia ventricular aguda, precedida de alteraciones
Prospecto: información para el usuario. Memantina Cinfa 10 mg comprimidos recubiertos con película EFG Memantina hidrocloruro
 Prospecto: información para el usuario Memantina Cinfa 10 mg comprimidos recubiertos con película EFG Memantina hidrocloruro Lea todo el prospecto detenidamente antes de empezar a tomar este medicamento,
Prospecto: información para el usuario Memantina Cinfa 10 mg comprimidos recubiertos con película EFG Memantina hidrocloruro Lea todo el prospecto detenidamente antes de empezar a tomar este medicamento,
ETIQUETA- PROSPECTO. CALZIUM 240/60/60 mg/ml, solución para perfusión para caballos, bovino, ovino, caprino y porcino. [ES, PT]
![ETIQUETA- PROSPECTO. CALZIUM 240/60/60 mg/ml, solución para perfusión para caballos, bovino, ovino, caprino y porcino. [ES, PT] ETIQUETA- PROSPECTO. CALZIUM 240/60/60 mg/ml, solución para perfusión para caballos, bovino, ovino, caprino y porcino. [ES, PT]](/thumbs/86/93088441.jpg) ETIQUETA- PROSPECTO CALZIUM 240/60/60 mg/ml, solución para perfusión para caballos, bovino, ovino, caprino y porcino. [ES, PT] 1. NOMBRE O RAZÓN SOCIAL Y DOMICILIO O SEDE SOCIAL DEL TITULAR DE LA AUTORIZACIÓN
ETIQUETA- PROSPECTO CALZIUM 240/60/60 mg/ml, solución para perfusión para caballos, bovino, ovino, caprino y porcino. [ES, PT] 1. NOMBRE O RAZÓN SOCIAL Y DOMICILIO O SEDE SOCIAL DEL TITULAR DE LA AUTORIZACIÓN
MEDICAMENTOS, PROLONGACIÓN DEL INTERVALO QT TEMAS CANDENTES 23 DE ABRIL DE 2013
 MEDICAMENTOS, PROLONGACIÓN DEL INTERVALO QT TEMAS CANDENTES 23 DE ABRIL DE 2013 PROLONGACIÓN DEL INTERVALO QT 2013 2012 2011 2011 2011 2004 2003 1999 1997 AZITROMICINA ONDANSETRON DOMPERIDONA ESCITALOPRAM
MEDICAMENTOS, PROLONGACIÓN DEL INTERVALO QT TEMAS CANDENTES 23 DE ABRIL DE 2013 PROLONGACIÓN DEL INTERVALO QT 2013 2012 2011 2011 2011 2004 2003 1999 1997 AZITROMICINA ONDANSETRON DOMPERIDONA ESCITALOPRAM
ORAP Forte PIMOZIDA. Comprimidos
 ORAP Forte PIMOZIDA Comprimidos Industria Portuguesa Venta bajo receta archivada Lista IV FÓRMULA CUALI-CUANTITATIVA: Orap forte Cada comprimido de 4 mg contiene: Pimozida 4,00 mg Excipientes: Fosfato
ORAP Forte PIMOZIDA Comprimidos Industria Portuguesa Venta bajo receta archivada Lista IV FÓRMULA CUALI-CUANTITATIVA: Orap forte Cada comprimido de 4 mg contiene: Pimozida 4,00 mg Excipientes: Fosfato
RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO. TORBUGESIC VET 10 mg/ml SOLUCIÓN INYECTABLE PARA CABALLOS PERROS Y GATOS
 RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1. DENOMINACIÓN DEL MEDICAMENTO VETERINARIO TORBUGESIC VET 10 mg/ml SOLUCIÓN INYECTABLE PARA CABALLOS PERROS Y GATOS 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA
RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1. DENOMINACIÓN DEL MEDICAMENTO VETERINARIO TORBUGESIC VET 10 mg/ml SOLUCIÓN INYECTABLE PARA CABALLOS PERROS Y GATOS 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA
ALPRAZOLAM 0,25 mg Tabletas
 ALPRAZOLAM 0,25 mg Tabletas Alprazolam 0,25 mg Tabletas Composición: Cada tableta contiene: Alprazolam 0,25 mg Excipientes c.s.p. Acción farmacológica Actúa como depresor del sistema nervioso central
ALPRAZOLAM 0,25 mg Tabletas Alprazolam 0,25 mg Tabletas Composición: Cada tableta contiene: Alprazolam 0,25 mg Excipientes c.s.p. Acción farmacológica Actúa como depresor del sistema nervioso central
SIMETICONA 100 mg- CLORDIAZEPÓXIDO (CLORHIDRATO) 5 mg- METOCLOPRAMIDA (CLORHIDRATO) 5mg CAPSULAS
 SIMETICONA 100 mg- CLORDIAZEPÓXIDO (CLORHIDRATO) 5 mg- METOCLOPRAMIDA (CLORHIDRATO) 5mg CAPSULAS Lea cuidadosamente este folleto antes de la administración de este medicamento. Contiene información importante
SIMETICONA 100 mg- CLORDIAZEPÓXIDO (CLORHIDRATO) 5 mg- METOCLOPRAMIDA (CLORHIDRATO) 5mg CAPSULAS Lea cuidadosamente este folleto antes de la administración de este medicamento. Contiene información importante
FICHA TÉCNICA. La cantidad de principios activos presentes en 1 ml de ADDAMEL es de:
 FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO ADDAMEL concentrado para solución para perfusión 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA 1 ml de ADDAMEL contiene: Principio activo Cantidad Cloruro de cromo,
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO ADDAMEL concentrado para solución para perfusión 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA 1 ml de ADDAMEL contiene: Principio activo Cantidad Cloruro de cromo,
FICHA TECNICA. TRAMADOL NORMON está indicado en el tratamiento del dolor, de intensidad moderada a severa.
 FICHA TECNICA 1. NOMBRE DEL MEDICAMENTO TRAMADOL NORMON 50 mg Cápsulas EFG 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada cápsula de TRAMADOL NORMON 50 mg contiene: Tramadol (D.C.I.) hidrocloruro... 50
FICHA TECNICA 1. NOMBRE DEL MEDICAMENTO TRAMADOL NORMON 50 mg Cápsulas EFG 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada cápsula de TRAMADOL NORMON 50 mg contiene: Tramadol (D.C.I.) hidrocloruro... 50
FICHA DE INFORMACIÓN AL PACIENTE: TERFENADINA
 FICHA DE INFORMACIÓN AL PACIENTE: TERFENADINA 1.- QUÉ ES Y PARA QUE SE UTILIZA 1.1 Acción: Antialérgico 1.2 Cómo actúa este fármaco: Inhibe la unión de la histamina a su receptor impidiéndose así, que
FICHA DE INFORMACIÓN AL PACIENTE: TERFENADINA 1.- QUÉ ES Y PARA QUE SE UTILIZA 1.1 Acción: Antialérgico 1.2 Cómo actúa este fármaco: Inhibe la unión de la histamina a su receptor impidiéndose así, que
RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO. REVERTOR 5 mg/ml SOLUCIÓN INYECTABLE PARA PERROS Y GATOS
 RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1. DENOMINACIÓN DEL MEDICAMENTO VETERINARIO REVERTOR 5 mg/ml SOLUCIÓN INYECTABLE PARA PERROS Y GATOS 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA 1 ml de solución
RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1. DENOMINACIÓN DEL MEDICAMENTO VETERINARIO REVERTOR 5 mg/ml SOLUCIÓN INYECTABLE PARA PERROS Y GATOS 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA 1 ml de solución
TEPAVIL Comprimidos Sulpirida
 Lea todo el prospecto detenidamente antes de empezar a tomar el medicamento. Conserve este prospecto. Puede tener que volver a leerlo. Si tiene alguna duda, consulte a su médico o farmacéutico. Este medicamento
Lea todo el prospecto detenidamente antes de empezar a tomar el medicamento. Conserve este prospecto. Puede tener que volver a leerlo. Si tiene alguna duda, consulte a su médico o farmacéutico. Este medicamento
CENAVUL Suspensión inyectable
 Camí Pedra Estela s/n 43205 Reus Telf. 977 75 72 73 Fax. 977 75 13 98 www.cenavisa.com E-mail: cenavisa@cenavisa.com FICHA TÉCNICA: CENAVUL Suspensión inyectable Reg. nº: 2145 ESP FICHA TÉCNICA (RESUMEN
Camí Pedra Estela s/n 43205 Reus Telf. 977 75 72 73 Fax. 977 75 13 98 www.cenavisa.com E-mail: cenavisa@cenavisa.com FICHA TÉCNICA: CENAVUL Suspensión inyectable Reg. nº: 2145 ESP FICHA TÉCNICA (RESUMEN
HIDROCLORURO DE EFEDRINA GENFARMA. 10 mg/ml, Solución inyectable
 HIDROCLORURO DE EFEDRINA GENFARMA 10 mg/ml, Solución inyectable Lea todo el prospecto detenidamente antes de empezar a usar el medicamento. - Conserve este prospecto ya que puede tener que volver a leerlo.
HIDROCLORURO DE EFEDRINA GENFARMA 10 mg/ml, Solución inyectable Lea todo el prospecto detenidamente antes de empezar a usar el medicamento. - Conserve este prospecto ya que puede tener que volver a leerlo.
FICHA TÉCNICA O RESUMEN DE LAS CARACTERISTICAS DEL PRODUCTO
 FICHA TÉCNICA O RESUMEN DE LAS CARACTERISTICAS DEL PRODUCTO 1. NOMBRE DEL MEDICAMENTO FormulaTus 7,33 mg Pastillas para chupar sabor miel 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada pastilla para chupar
FICHA TÉCNICA O RESUMEN DE LAS CARACTERISTICAS DEL PRODUCTO 1. NOMBRE DEL MEDICAMENTO FormulaTus 7,33 mg Pastillas para chupar sabor miel 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada pastilla para chupar
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO. GHRH 50 microgramos polvo y disolvente para solución inyectable. 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA
 FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO GHRH 50 microgramos polvo y disolvente para solución inyectable. 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA 1 ampolla de GHRH contiene 66,7 microgramos de somatorelina
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO GHRH 50 microgramos polvo y disolvente para solución inyectable. 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA 1 ampolla de GHRH contiene 66,7 microgramos de somatorelina
Resumen de las características del producto. 1 ml. Para consultar la lista completa de excipientes, ver sección 6.1.
 Resumen de las características del producto 1. NOMBRE DEL MEDICAMENTO Agua para preparaciones inyectables B.Braun Disolvente para uso parenteral 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Principio Activo
Resumen de las características del producto 1. NOMBRE DEL MEDICAMENTO Agua para preparaciones inyectables B.Braun Disolvente para uso parenteral 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Principio Activo
FICHA TÉCNICA 1. DENOMINACIÓN DEL MEDICAMENTO RIAMET
 FICHA TÉCNICA 1. DENOMINACIÓN DEL MEDICAMENTO RIAMET 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada comprimido contiene 20 mg de arteméter y 120 mg de lumefantrina. Excipientes, ver apartado 6.1. 3. FORMA
FICHA TÉCNICA 1. DENOMINACIÓN DEL MEDICAMENTO RIAMET 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada comprimido contiene 20 mg de arteméter y 120 mg de lumefantrina. Excipientes, ver apartado 6.1. 3. FORMA
4.2 Indicaciones de uso, especificando las especies de destino
 DEPARTAMENTO DE MEDICAMENTOS VETERINARIOS 1. DENOMINACIÓN DEL MEDICAMENTO VETERINARIO TIPAFAR 5 mg/ml Solución inyectable para perros y gatos 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada ml de solución
DEPARTAMENTO DE MEDICAMENTOS VETERINARIOS 1. DENOMINACIÓN DEL MEDICAMENTO VETERINARIO TIPAFAR 5 mg/ml Solución inyectable para perros y gatos 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada ml de solución
PROSPECTO RAPIFEN ALFENTANIL CLORHIDRATO
 PROSPECTO RAPIFEN ALFENTANIL CLORHIDRATO Industria Belga Venta bajo receta FORMULA CUALITATIVA Y CUANTITATIVA Cada mililitro contiene alfentanil clorhidrato 0,544 mg, equivalente a 0,500 mg de alfentanil.
PROSPECTO RAPIFEN ALFENTANIL CLORHIDRATO Industria Belga Venta bajo receta FORMULA CUALITATIVA Y CUANTITATIVA Cada mililitro contiene alfentanil clorhidrato 0,544 mg, equivalente a 0,500 mg de alfentanil.
Oxicodona. . Agonista puro opioide de los receptores mu, Kappa y delta, con efecto analgésico, ansiolítico y sedante.
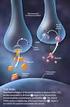 Oxicodona 1. Grupo Farmacoterapéutico:. Agonista puro opioide de los receptores mu, Kappa y delta, con efecto analgésico, ansiolítico y sedante. 2.- Formas farmacéuticas registradas:. Comprimidos de 10mg
Oxicodona 1. Grupo Farmacoterapéutico:. Agonista puro opioide de los receptores mu, Kappa y delta, con efecto analgésico, ansiolítico y sedante. 2.- Formas farmacéuticas registradas:. Comprimidos de 10mg
FICHA TÉCNICA ECHINACIN MADAUS solución oral Echinacea purpurea
 FICHA TÉCNICA ECHINACIN MADAUS solución oral Echinacea purpurea 1. NOMBRE DEL MEDICAMENTO ECHINACIN MADAUS solución oral Echinacea purpurea 2. COMPOSICION CUALITATIVA Y CUANTITATIVA Cada ml contiene: Jugo
FICHA TÉCNICA ECHINACIN MADAUS solución oral Echinacea purpurea 1. NOMBRE DEL MEDICAMENTO ECHINACIN MADAUS solución oral Echinacea purpurea 2. COMPOSICION CUALITATIVA Y CUANTITATIVA Cada ml contiene: Jugo
RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO
 RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1. DENOMINACIÓN DEL MEDICAMENTO VETERINARIO EMEPRID 5 mg/ml SOLUCIÓN INYECTABLE PARA PERROS Y GATOS 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada ml contiene:
RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1. DENOMINACIÓN DEL MEDICAMENTO VETERINARIO EMEPRID 5 mg/ml SOLUCIÓN INYECTABLE PARA PERROS Y GATOS 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada ml contiene:
FICHA TÉCNICA (RESUMEN DE CARACTERÍSTICAS DEL PRODUCTO)
 FICHA TÉCNICA (RESUMEN DE CARACTERÍSTICAS DEL PRODUCTO) 1. DENOMINACIÓN DEL MEDICAMENTO VETERINARIO EMEDOG 1 mg/ml solución inyectable para perros 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA 1 ml de solución
FICHA TÉCNICA (RESUMEN DE CARACTERÍSTICAS DEL PRODUCTO) 1. DENOMINACIÓN DEL MEDICAMENTO VETERINARIO EMEDOG 1 mg/ml solución inyectable para perros 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA 1 ml de solución
Composición Cada 100 ml de solución oftálmica de liberación prolongada contiene:
 CARTENS 1% y 2% Clorhidrato de Carteolol Solución Oftálmica de Liberación Prolongada Industria Argentina Venta bajo receta Composición Cada 100 ml de solución oftálmica de liberación prolongada contiene:
CARTENS 1% y 2% Clorhidrato de Carteolol Solución Oftálmica de Liberación Prolongada Industria Argentina Venta bajo receta Composición Cada 100 ml de solución oftálmica de liberación prolongada contiene:
I. DENOMINACION DISTINTIVA ERGEX DENOMINACION GENERICA. Ranitidina/Cisaprida. FORMA FARMACEUTICA Y FORMULACION
 I. DENOMINACION DISTINTIVA ERGEX II. DENOMINACION GENERICA Ranitidina/Cisaprida. III. FORMA FARMACEUTICA Y FORMULACION Suspensión. Cada 100 ml contienen: Ranitidina...1.5 g Cisaprida...0.1 g Vehículo cbp.
I. DENOMINACION DISTINTIVA ERGEX II. DENOMINACION GENERICA Ranitidina/Cisaprida. III. FORMA FARMACEUTICA Y FORMULACION Suspensión. Cada 100 ml contienen: Ranitidina...1.5 g Cisaprida...0.1 g Vehículo cbp.
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO. Passiflorine solución oral. 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA
 FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Passiflorine solución oral. 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada ml contiene: 100 mg de extracto líquido de partes aéreas de Passiflora incarnata L, (pasiflora)
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Passiflorine solución oral. 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada ml contiene: 100 mg de extracto líquido de partes aéreas de Passiflora incarnata L, (pasiflora)
RESUMEN DE LAS CARACTERISTICAS DEL PRODUCTO
 RESUMEN DE LAS CARACTERISTICAS DEL PRODUCTO 1. DENOMINACIÓN DEL MEDICAMENTO VETERINARIO Ancesol 10 mg/ml solución inyectable para bovino 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA 1 ml contiene: Sustancia
RESUMEN DE LAS CARACTERISTICAS DEL PRODUCTO 1. DENOMINACIÓN DEL MEDICAMENTO VETERINARIO Ancesol 10 mg/ml solución inyectable para bovino 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA 1 ml contiene: Sustancia
FICHA TECNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO
 FICHA TECNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1. NOMBRE DEL MEDICAMENTO Sinogan 25 mg comprimidos recubiertos con película Sinogan 100 mg comprimidos recubiertos con película 2. COMPOSICIÓN
FICHA TECNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1. NOMBRE DEL MEDICAMENTO Sinogan 25 mg comprimidos recubiertos con película Sinogan 100 mg comprimidos recubiertos con película 2. COMPOSICIÓN
FICHA TECNICA. Granisetrón Teva 1 mg/1 ml Concentrado para solución para perfusión EFG
 FICHA TECNICA 1. NOMBRE DEL MEDICAMENTO Granisetrón Teva 1 mg/1 ml Concentrado para solución para perfusión EFG 2. COMPOSICION CUALITATIVA Y CUANTITATIVA Cada 1 ml de concentrado contiene 1 mg de granisetrón
FICHA TECNICA 1. NOMBRE DEL MEDICAMENTO Granisetrón Teva 1 mg/1 ml Concentrado para solución para perfusión EFG 2. COMPOSICION CUALITATIVA Y CUANTITATIVA Cada 1 ml de concentrado contiene 1 mg de granisetrón
FICHA TÉCNICA. Hipersensibilidad al principio activo o a alguno de los excipientes incluidos en la sección 6.1.
 FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Oculotect 50 mg/ml colirio en solución en envase unidosis 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Un ml contiene 50 mg de povidona K25. Para consultar la lista
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Oculotect 50 mg/ml colirio en solución en envase unidosis 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Un ml contiene 50 mg de povidona K25. Para consultar la lista
SODIOFOLIN 50 mg/ml solución para inyección o perfusión intravenosa
 L e a t o d o e l p r o s p e c t o d e t e n i d a m e n t e a n t e s d e e m p e z a r En este prospecto 1. Qué es Sodiofolin 50 mg/ml solución para inyección o perfusión intravenosa y para qué se utiliza
L e a t o d o e l p r o s p e c t o d e t e n i d a m e n t e a n t e s d e e m p e z a r En este prospecto 1. Qué es Sodiofolin 50 mg/ml solución para inyección o perfusión intravenosa y para qué se utiliza
FICHA TÉCNICA. No se requieren ajustes en la dosificación en ancianos o en pacientes con insuficiencia renal.
 FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Loratadina ratiopharm 10 mg comprimidos EFG 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada comprimido contiene 10 mg de loratadina. Excipientes: Cada comprimido
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Loratadina ratiopharm 10 mg comprimidos EFG 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada comprimido contiene 10 mg de loratadina. Excipientes: Cada comprimido
RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO. Granisetrón Actavis 1 mg/ml concentrado para solución inyectable o para perfusión EFG
 RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1. NOMBRE DEL MEDICAMENTO Granisetrón Actavis 1 mg/ml concentrado para solución inyectable o para perfusión EFG 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA 1 ml
RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1. NOMBRE DEL MEDICAMENTO Granisetrón Actavis 1 mg/ml concentrado para solución inyectable o para perfusión EFG 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA 1 ml
FICHA TÉCNICA. No se requieren ajustes en la dosificación en ancianos o en pacientes con insuficiencia renal.
 FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Loratadina ratiopharm 10 mg comprimidos EFG 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada comprimido contiene 10 mg de loratadina. Excipientes con efecto conocido:
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Loratadina ratiopharm 10 mg comprimidos EFG 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada comprimido contiene 10 mg de loratadina. Excipientes con efecto conocido:
Vernakalant. Conversión rápida a ritmo sinusal de la fibrilación auricular de inicio reciente en adultos:
 Vernakalant Nuevo fármaco antiarrítmico con un mecanismo de acción único, aurículoselectivo para la cardioversión de FA de inicio reciente en pacientes adultos Uso exclusivamente intravenoso Vernakalant
Vernakalant Nuevo fármaco antiarrítmico con un mecanismo de acción único, aurículoselectivo para la cardioversión de FA de inicio reciente en pacientes adultos Uso exclusivamente intravenoso Vernakalant
PROSPECTO: INFORMACIÓN PARA EL USUARIO. flutamida cinfa 250 mg comprimidos EFG flutamida
 PROSPECTO: INFORMACIÓN PARA EL USUARIO flutamida cinfa 250 mg comprimidos EFG flutamida Lea todo el prospecto detenidamente antes de empezar a tomar el medicamento. - Conserve este prospecto, ya que puede
PROSPECTO: INFORMACIÓN PARA EL USUARIO flutamida cinfa 250 mg comprimidos EFG flutamida Lea todo el prospecto detenidamente antes de empezar a tomar el medicamento. - Conserve este prospecto, ya que puede
PROSPECTO. REVERSE 5 mg/ml Solución inyectable para perros y gatos
 PROSPECTO REVERSE 5 mg/ml Solución inyectable para perros y gatos 1. NOMBRE O RAZÓN SOCIAL Y DOMICILIO O SEDE SOCIAL DEL TITULAR DE LA AUTORIZACIÓN DE COMERCIALIZACIÓN Y DEL FABRICANTE RESPONSABLE DE LA
PROSPECTO REVERSE 5 mg/ml Solución inyectable para perros y gatos 1. NOMBRE O RAZÓN SOCIAL Y DOMICILIO O SEDE SOCIAL DEL TITULAR DE LA AUTORIZACIÓN DE COMERCIALIZACIÓN Y DEL FABRICANTE RESPONSABLE DE LA
Agua para preparaciones inyectables Meinsol, disolvente para uso parenteral. Agua para preparaciones inyectables 1 g por 1 ml. ph entre 4,5 y 7,0.
 1. NOMBRE DEL MEDICAMENTO Agua para preparaciones inyectables Meinsol, disolvente para uso parenteral 2. COMPOSICION CUALITATIVA Y CUANTITATIVA Agua para preparaciones inyectables 1 g por 1 ml. ph entre
1. NOMBRE DEL MEDICAMENTO Agua para preparaciones inyectables Meinsol, disolvente para uso parenteral 2. COMPOSICION CUALITATIVA Y CUANTITATIVA Agua para preparaciones inyectables 1 g por 1 ml. ph entre
FICHA TÉCNICA. Agua para preparaciones inyectables Meinsol, disolvente para uso parenteral
 FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Agua para preparaciones inyectables Meinsol, disolvente para uso parenteral 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Agua para preparaciones inyectables 1 g por
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Agua para preparaciones inyectables Meinsol, disolvente para uso parenteral 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Agua para preparaciones inyectables 1 g por
FICHA TÉCNICA. CORVERT 87 microgramos/ml, solución para perfusión intravenosa.
 FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO CORVERT 87 microgramos/ml, solución para perfusión intravenosa. 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Fumarato de ibutilida (DCI) 0,1 mg/ml, correspondiente
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO CORVERT 87 microgramos/ml, solución para perfusión intravenosa. 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Fumarato de ibutilida (DCI) 0,1 mg/ml, correspondiente
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO. Tusheel películas bucodispersables 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA
 FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Tusheel películas bucodispersables 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada película bucodispersable contiene 16 mg de extracto (como extracto seco) de hoja
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Tusheel películas bucodispersables 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada película bucodispersable contiene 16 mg de extracto (como extracto seco) de hoja
FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO
 FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1. NOMBRE DEL MEDICAMENTO Cleboril Pediátrico 62,5 microgramos/ml Gotas orales en solución 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada ml
FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1. NOMBRE DEL MEDICAMENTO Cleboril Pediátrico 62,5 microgramos/ml Gotas orales en solución 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada ml
FICHA TECNICA 1. NOMBRE DEL MEDICAMENTO 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA 3. FORMA FARMACÉUTICA 4. DATOS CLÍNICOS
 FICHA TECNICA 1. NOMBRE DEL MEDICAMENTO Otilonio Qualigen 40 mg comprimidos recubiertos con película EFG 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada comprimido contiene 40 mg de otilonio bromuro. Para
FICHA TECNICA 1. NOMBRE DEL MEDICAMENTO Otilonio Qualigen 40 mg comprimidos recubiertos con película EFG 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada comprimido contiene 40 mg de otilonio bromuro. Para
LABORATORIOS NORMON, S.A. AMBROXOL NORMON 15 mg/5 ml Jarabe EFG
 1. NOMBRE DEL MEDICAMENTO 2. COMPOSICION CUALITATIVA Y CUANTITATIVA Cada 5 ml de jarabe contienen: AMBROXOL (D.C.I.) hidrocloruro 15 mg Excipientes, ver apartado 6.1. 3. FORMA FARMACEUTICA Jarabe. 4. DATOS
1. NOMBRE DEL MEDICAMENTO 2. COMPOSICION CUALITATIVA Y CUANTITATIVA Cada 5 ml de jarabe contienen: AMBROXOL (D.C.I.) hidrocloruro 15 mg Excipientes, ver apartado 6.1. 3. FORMA FARMACEUTICA Jarabe. 4. DATOS
RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO
 RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1. DENOMINACIÓN DEL MEDICAMENTO VETERINARIO GESTAVET-PROST 75 mcg /ml SOLUCIÓN INYECTABLE. 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada ml contiene: Sustancia
RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1. DENOMINACIÓN DEL MEDICAMENTO VETERINARIO GESTAVET-PROST 75 mcg /ml SOLUCIÓN INYECTABLE. 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada ml contiene: Sustancia
RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1. DENOMINACIÓN DEL MEDICAMENTO VETERINARIO
 RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1. DENOMINACIÓN DEL MEDICAMENTO VETERINARIO REVAZOL 5 mg/ml para gatos y perros. 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada ml contiene: Sustancia activa:
RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1. DENOMINACIÓN DEL MEDICAMENTO VETERINARIO REVAZOL 5 mg/ml para gatos y perros. 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada ml contiene: Sustancia activa:
FICHA TÉCNICA (RESUMEN DE CARACTERÍSTICAS DEL PRODUCTO)
 DEPARTAMENTO DE MEDICAMENTOS VETERINARIOS FICHA TÉCNICA (RESUMEN DE CARACTERÍSTICAS DEL PRODUCTO) 1. DENOMINACIÓN DEL MEDICAMENTO VETERINARIO PRIVAPROL 50 mg/ml suspensión inyectable para perras 2. COMPOSICIÓN
DEPARTAMENTO DE MEDICAMENTOS VETERINARIOS FICHA TÉCNICA (RESUMEN DE CARACTERÍSTICAS DEL PRODUCTO) 1. DENOMINACIÓN DEL MEDICAMENTO VETERINARIO PRIVAPROL 50 mg/ml suspensión inyectable para perras 2. COMPOSICIÓN
FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO
 DEPARTAMENTO DE MEDICAMENTOS VETERINARIOS FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1. DENOMINACIÓN DEL MEDICAMENTO VETERINARIO REVERSE 5 mg/ml Solución inyectable para perros y gatos
DEPARTAMENTO DE MEDICAMENTOS VETERINARIOS FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1. DENOMINACIÓN DEL MEDICAMENTO VETERINARIO REVERSE 5 mg/ml Solución inyectable para perros y gatos
RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO. SEDASTOP 5 mg/ml SOLUCION INYECTABLE PARA GATOS Y PERROS
 RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1. DENOMINACIÓN DEL MEDICAMENTO VETERINARIO SEDASTOP 5 mg/ml SOLUCION INYECTABLE PARA GATOS Y PERROS 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA 1 ml de solución
RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1. DENOMINACIÓN DEL MEDICAMENTO VETERINARIO SEDASTOP 5 mg/ml SOLUCION INYECTABLE PARA GATOS Y PERROS 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA 1 ml de solución
FICHA TÉCNICA. Naloxona Kern Pharma 0,4 mg/ml solución inyectable y para perfusión
 FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Naloxona Kern Pharma 0,4 mg/ml solución inyectable y para perfusión 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada ampolla de 1 ml contiene 0,4 mg de hidrocloruro
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Naloxona Kern Pharma 0,4 mg/ml solución inyectable y para perfusión 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada ampolla de 1 ml contiene 0,4 mg de hidrocloruro
FICHA TÉCNICA. Cada ampolla de 1 ml contiene 0,4 mg de hidrocloruro de naloxona (como hidrocloruro de naloxona dihidrato).
 FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Naloxona B. Braun 0,4 mg/ml solución inyectable o para perfusión 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada ampolla de 1 ml contiene 0,4 mg de hidrocloruro de
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Naloxona B. Braun 0,4 mg/ml solución inyectable o para perfusión 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada ampolla de 1 ml contiene 0,4 mg de hidrocloruro de
Tratamiento sintomático de procesos alérgicos tales como: Rinitis o conjuntivitis alérgica, urticaria crónica, dermatitis alérgica.
 RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1. NOMBRE DEL MEDICAMENTO ASTEMIZOL RATIOPHARM 10 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada cápsula contiene: Astemizol (D.C.I.)... 10 mg Excipientes: véase
RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1. NOMBRE DEL MEDICAMENTO ASTEMIZOL RATIOPHARM 10 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada cápsula contiene: Astemizol (D.C.I.)... 10 mg Excipientes: véase
Prospecto: información para el usuario. Primperan 10 mg/2 ml solución inyectable Metoclopramida hidrocloruro
 Prospecto: información para el usuario Primperan 10 mg/2 ml solución inyectable Metoclopramida hidrocloruro Lea todo el prospecto detenidamente antes de empezar a usar este medicamento, porque contiene
Prospecto: información para el usuario Primperan 10 mg/2 ml solución inyectable Metoclopramida hidrocloruro Lea todo el prospecto detenidamente antes de empezar a usar este medicamento, porque contiene
Cloruro de Calcio Braun 100mg/ml Solución inyectable
 PROSPECTO: INFORMACIÓN PARA EL USUARIO Cloruro de Calcio Braun 100mg/ml Solución inyectable Lea todo el prospecto detenidamente antes de empezar a usar el medicamento - Conserve este prospecto, ya que
PROSPECTO: INFORMACIÓN PARA EL USUARIO Cloruro de Calcio Braun 100mg/ml Solución inyectable Lea todo el prospecto detenidamente antes de empezar a usar el medicamento - Conserve este prospecto, ya que
FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO. Sedastop 5 mg/ml solución inyectable para gatos y perros
 FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1. DENOMINACIÓN DEL MEDICAMENTO VETERINARIO Sedastop 5 mg/ml solución inyectable para gatos y perros 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA
FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1. DENOMINACIÓN DEL MEDICAMENTO VETERINARIO Sedastop 5 mg/ml solución inyectable para gatos y perros 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA
FICHA TÉCNICA. Primperan 10 mg/2 ml solución inyectable
 FICHA TÉCNICA Primperan 10 mg/2 ml solución inyectable 1. NOMBRE DEL MEDICAMENTO Primperan 10 mg/2 ml solución inyectable 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada ampolla de 2 ml contiene 10 mg de
FICHA TÉCNICA Primperan 10 mg/2 ml solución inyectable 1. NOMBRE DEL MEDICAMENTO Primperan 10 mg/2 ml solución inyectable 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada ampolla de 2 ml contiene 10 mg de
FICHA TÉCNICA. ORAP Pimozida ( D. C. I. )
 FICHA TÉCNICA ORAP Pimozida ( D. C. I. ) 1. - DENOMINACIÓN DE LOS MEDICAMENTOS ORAP 1 mg, comprimidos ORAP FUERTE 4 mg, comprimidos 2. - COMPOSICIÓN CUALITATIVA Y CUANTITATIVA ORAP1 mg, comprimidos Cada
FICHA TÉCNICA ORAP Pimozida ( D. C. I. ) 1. - DENOMINACIÓN DE LOS MEDICAMENTOS ORAP 1 mg, comprimidos ORAP FUERTE 4 mg, comprimidos 2. - COMPOSICIÓN CUALITATIVA Y CUANTITATIVA ORAP1 mg, comprimidos Cada
Prospecto: información para el usuario. Primperan 100 mg/5 ml solución inyectable Metoclopramida hidrocloruro
 Prospecto: información para el usuario Primperan 100 mg/5 ml solución inyectable Metoclopramida hidrocloruro Lea todo el prospecto detenidamente antes de empezar a tomar el medicamento, porque contiene
Prospecto: información para el usuario Primperan 100 mg/5 ml solución inyectable Metoclopramida hidrocloruro Lea todo el prospecto detenidamente antes de empezar a tomar el medicamento, porque contiene
ANEXO III RESUMENES DE LAS CARACTERÍSTICAS DEL PRODUCTO
 ANEXO III RESUMENES DE LAS CARACTERÍSTICAS DEL PRODUCTO CPMP/24844/02 1 EMEA 2002 RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO SUSPENSIÓN ORAL PARA NIÑOS CPMP/24844/02 2 EMEA 2002 1. NOMBRE DEL MEDICAMENTO
ANEXO III RESUMENES DE LAS CARACTERÍSTICAS DEL PRODUCTO CPMP/24844/02 1 EMEA 2002 RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO SUSPENSIÓN ORAL PARA NIÑOS CPMP/24844/02 2 EMEA 2002 1. NOMBRE DEL MEDICAMENTO
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO. FormulaTus 1,33 mg/ml jarabe sabor miel 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA.
 FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO FormulaTus 1,33 mg/ml jarabe sabor miel 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada ml contiene: Dextrometorfano, hidrobromuro (equivalente a 1,024 mg de dextrometorfano)
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO FormulaTus 1,33 mg/ml jarabe sabor miel 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada ml contiene: Dextrometorfano, hidrobromuro (equivalente a 1,024 mg de dextrometorfano)
FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO
 FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1 DENOMINACIÓN DEL MEDICAMENTO VETERINARIO Torphasol 10 mg/ml solución inyectable para caballos 2 COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada
FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1 DENOMINACIÓN DEL MEDICAMENTO VETERINARIO Torphasol 10 mg/ml solución inyectable para caballos 2 COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada
PROSPECTO PARA EL FABRICANTE LIBERADOR DEL LOTE FARMA MEDITERRANIA, S.L. PROSPECTO PARA: ANTIDORM 5 mg/ml Solución inyectable para perros y gatos
 PROSPECTO PARA EL FABRICANTE LIBERADOR DEL LOTE FARMA MEDITERRANIA, S.L. PROSPECTO PARA: ANTIDORM 5 mg/ml Solución inyectable para perros y gatos 1. NOMBRE O RAZÓN SOCIAL Y DOMICILIO O SEDE SOCIAL DEL
PROSPECTO PARA EL FABRICANTE LIBERADOR DEL LOTE FARMA MEDITERRANIA, S.L. PROSPECTO PARA: ANTIDORM 5 mg/ml Solución inyectable para perros y gatos 1. NOMBRE O RAZÓN SOCIAL Y DOMICILIO O SEDE SOCIAL DEL
Hiperfosfatemia, hiperpotasemia. Urolitiasis por fosfatos amónico o magnésico.
 PROSPECTO FOSFATO DIPOTÁSICO 1M FRESENIUS KABI, solución inyectable COMPOSICIÓN: Fosfato dipotásico Agua para inyección c.s.p. 1742 mg 10 ml FORMA FARMACÉUTICA Y CONTENIDO DEL ENVASE: Solución inyectable.
PROSPECTO FOSFATO DIPOTÁSICO 1M FRESENIUS KABI, solución inyectable COMPOSICIÓN: Fosfato dipotásico Agua para inyección c.s.p. 1742 mg 10 ml FORMA FARMACÉUTICA Y CONTENIDO DEL ENVASE: Solución inyectable.
FICHA TÉCNICA. La ranura sirve únicamente para fraccionar y facilitar la deglución pero no para dividir en dosis iguales.
 FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO LORATADINA KORHISPANA 10 mg comprimidos EFG 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada comprimido contiene 10 mg de loratadina. Excipientes: Lactosa, 75,50 mg.
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO LORATADINA KORHISPANA 10 mg comprimidos EFG 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada comprimido contiene 10 mg de loratadina. Excipientes: Lactosa, 75,50 mg.
FICHA TÉCNICA. LORATADINA KERN PHARMA está indicado para el tratamiento sintomático de rinitis alérgica y urticaria idiopática crónica.
 FICHA TÉCNICA 1. DENOMINACIÓN DEL MEDICAMENTO LORATADINA KERN PHARMA 10 mg comprimidos EFG 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada comprimido contiene 10 mg de loratadina. Lista de excipientes,
FICHA TÉCNICA 1. DENOMINACIÓN DEL MEDICAMENTO LORATADINA KERN PHARMA 10 mg comprimidos EFG 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada comprimido contiene 10 mg de loratadina. Lista de excipientes,
FICHA TÉCNICA O RESUMEN DE LAS CARACTERISTÍCAS DEL PRODUCTO 1. NOMBRE DEL MEDICAMENTO
 FICHA TÉCNICA O RESUMEN DE LAS CARACTERISTÍCAS DEL PRODUCTO 1. NOMBRE DEL MEDICAMENTO Supliven concentrado para solución para perfusión 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Supliven contiene: Principio
FICHA TÉCNICA O RESUMEN DE LAS CARACTERISTÍCAS DEL PRODUCTO 1. NOMBRE DEL MEDICAMENTO Supliven concentrado para solución para perfusión 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Supliven contiene: Principio
SINALERG Levocetirizina 2.5 mg / 5 ml Jarabe
 SINALERG Levocetirizina 2.5 mg / 5 ml Jarabe SINALERG (LEVOCETIRIZINA 2.5 mg/5 ml) Jarabe Antihistamínico COMPOSICIÓN Cada 100 ml contiene: Levocetirizina diclorhidrato... 0.05 g Excipientes c.s.p. INDICACIONES
SINALERG Levocetirizina 2.5 mg / 5 ml Jarabe SINALERG (LEVOCETIRIZINA 2.5 mg/5 ml) Jarabe Antihistamínico COMPOSICIÓN Cada 100 ml contiene: Levocetirizina diclorhidrato... 0.05 g Excipientes c.s.p. INDICACIONES
